ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к новым соединениям для лечения импотенции. В частности, настоящее изобретение относится к новым соединениям для лечения импотенции, способу их получения и к их применению.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Силденафил представляет собой селективный ингибитор фосфодиэстеразы, химическое название которого 1-[[4-этокси-3-(6,7-дигидро-1-метил-7-оксо-3-пропил-1Н-пиразоло[4,3-d]пиримидин-5-ил)фенилсульфонил]]-4-метилпиперазин. Данное соединение и способ его получения, а также его применение для лечения сердечно-сосудистых заболеваний, раскрыто в CN1057464А, в CN1124926A описано применение данного соединения для получения лекарственного препарата, которое может быть использовано для лечения нарушений эрекции у самцов животных. CN1168376A описывает новый способ получения силденафила. CN1246478A описывает другой способ получения силденафила. Несмотря на то что силденафил является весьма эффективным средством для лечения мужской эректильной дисфункции, токсичность и побочное действие данного соединения высоки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение предусматривает новый селективный ингибитор фосфодиэстеразы, т.е. соединение формулы (I) и его фармацевтически приемлемые соли или его стереоизомеры. Такое соединение имеет структуру формулы (I):
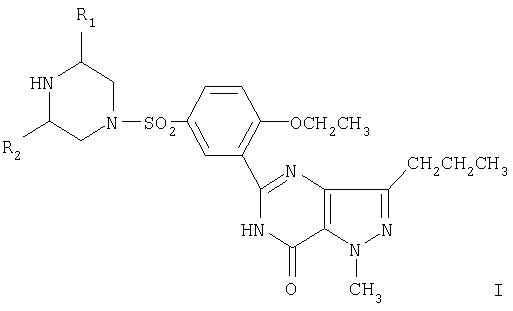
где R1 и R2 могут быть одинаковыми или различными и независимо представлять C1-6алкил, предпочтительно метил, более предпочтительно, как R1, так и R2, оба находятся в цис-форме пиперазинового кольца, при этом оба представляют метил.
Другой целью настоящего изобретения является разработка способа получения соединения формулы (I).
Существует несколько новых промежуточных соединений, которые могут быть использованы в способе синтеза в соответствии с настоящим изобретением. Поэтому следующей целью данного изобретения является разработка промежуточных соединений для получения соединений формулы (I).
Еще одной целью данного изобретения является разработка фармацевтической композиции, включающей соединение формулы (I) в качестве активного компонента.
Другой целью данного изобретения является применение соединений формулы (I) для получения лекарственного препарата, предназначенного для лечения импотенции.
В соответствии с настоящим изобретением пиперазиновое кольцо соединений формулы (I) имеет две замещенные группы R1 и R2, и два асимметричных атома углерода на пиперазиновом кольце соединений (I). R1 и R2 могут быть в цис- или транс-форме пиперазинового кольца. Поэтому соединения формулы (I) представлены в виде различных стереоизомеров. Данные изомеры и их фармацевтически приемлемые соли входят в объем соединений в соответствии с настоящим изобретением.
Соединение в соответствии с настоящим изобретением предпочтительно представляет собой соединение формулы (I), в котором R1 и R2 находятся в цис-форме, наиболее предпочтительно соединение, в котором как R1, так и R2 представляют метил в цис-форме. Оно имеет следующее химическое название: 5-[[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)фенил]]-1-метил-3-н-пропил-7,6-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-он, т.е. соединение формулы (I'):

Соединение формулы (I) в соответствии с настоящим изобретением не только эффективно для лечения импотенции, такой как эректильная дисфункция, но также отличается длительной терапевтической эффективностью и более низкой токсичностью.
Далее способ получения соединения формулы (I) описан на примере соединения формулы (I').
Способ синтеза соединений формулы (I') в соответствии с настоящим изобретением представлен на следующей схеме:
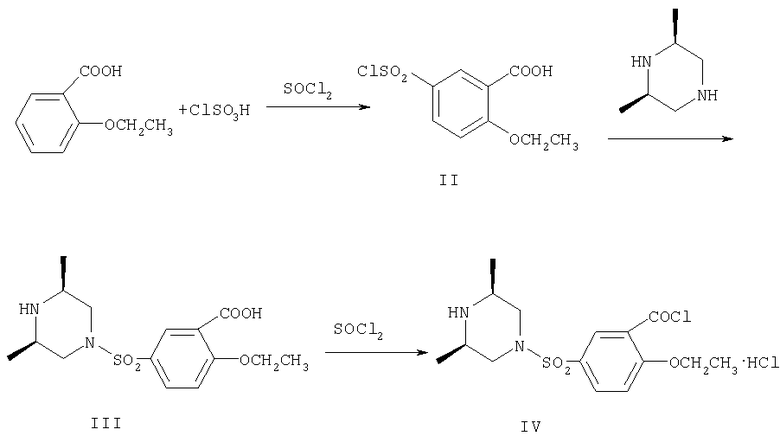
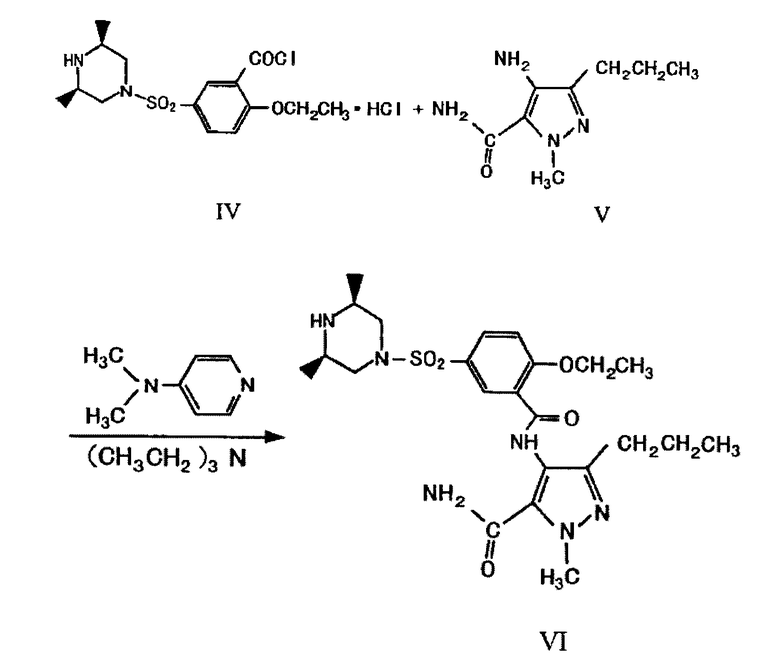
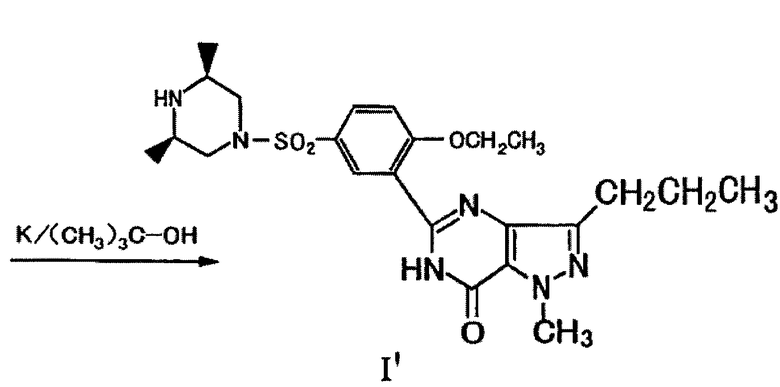
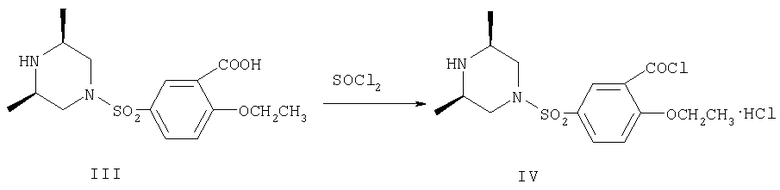
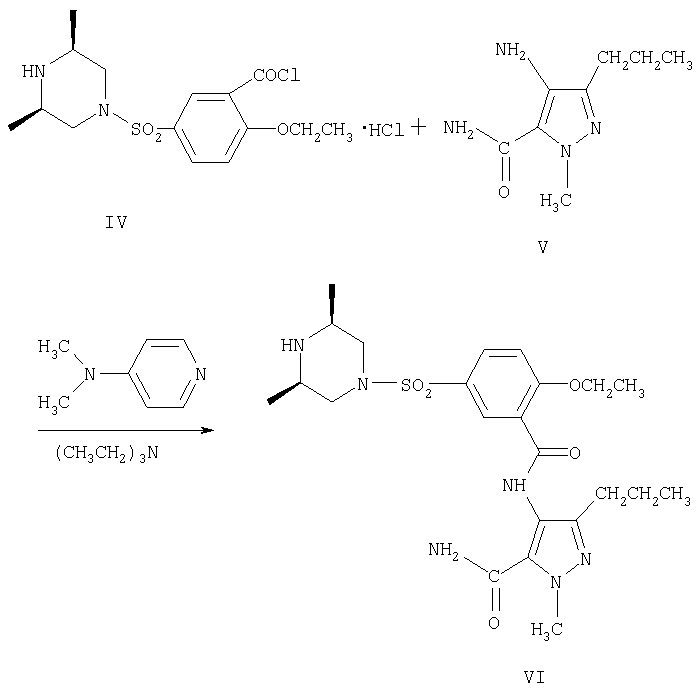
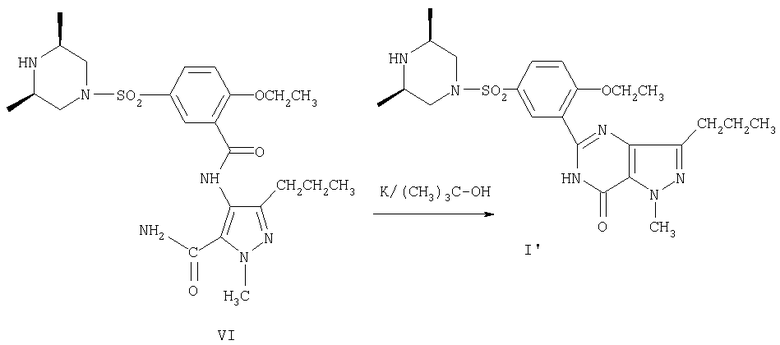
Соединение формулы (I') получают следующим образом: в результате взаимодействия 2-этоксибензойной кислоты в качестве исходного материала с хлорсульфоновой кислотой в присутствии дихлорида сульфоксида получают 5-хлорсульфонил-2-этоксибензойную кислоту (соединение II); в результате взаимодействия соединения (II) с цис-2,6-диметилпиперазином (см. Zhongguo Yiyao Gongye Zazhi, 1997, vol.28(11), pages 524˜525) получают 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензойную кислоту (соединение III); в результате ацилирования соединения (III), представляющего собой новое соединение, получают 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензоилхлорид (соединение IV); в результате взаимодействия соединения IV с соединением V (см. способ синтеза соединения формулы (IX) в CN1246478A) в присутствии 4-диметиламинопиридина и триэтиламина получают 4-[[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензамидо]]-1-метил-3-н-пропилпиразол-5-карбоксамид (соединение VI), который является новым соединением; в результате циклизации соединения VI в присутствии трет-бутоксида калия получают 5-[[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)фенил]]-1-метил-3-н-пропил-7,6-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-он (соединение I').
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Далее способ получения соединений формулы (I') в соответствии с настоящим изобретением и их фармацевтически приемлемых солей описан с помощью примеров. Следует отметить, что примеры способов получения приведены только с целью иллюстрации, а не ограничения настоящего изобретения. Любые модификации способов получения в соответствии с данным изобретением в рамках настоящего изобретения подпадают под объем данного изобретения.
Пример 1. Получение 5-хлорсульфонил-2-этоксибензойной кислоты (II)
В 250-миллилитровой трехгорлой колбе к ледяной смеси дихлорида сульфоксида (22 мл, 0,30 моль) и хлорсульфоновой кислоты (82,6 мл, 1,24 моль) по каплям при перемешивании добавляют 2-этоксибензойную кислоту (50 г, 0,30 моль). Во время добавления температуру реакционной смеси поддерживают на уровне ниже 25°С. Полученную смесь перемешивают при комнатной температуре в течение 18 часов, а затем выливают в ледяную воду при перемешивании, при этом появляется белый осадок. Реакционную смесь перемешивают в течение еще 1 часа, фильтруют, промывают водой и сушат в вакууме, получая 64,4 г сырого продукта в виде белого твердого вещества (II) (выход 81%), т.пл. 108-110°С. Сырой продукт используют непосредственно на следующей стадии без какой-либо очистки.
Пример 2. Получение 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензойной кислоты (III)
В 250-миллилитровую трехгорлую колбу при перемешивании добавляют 52,6 г (0,23 моль) цис-2,6-диметилпиперазина к суспензии соединения (II) (53 г, 0,20 моль) в воде (170 мл) при температуре около 10°С, одновременно поддерживая температуру реакционной смеси ниже 20°С. Затем реакционную смесь перемешивают при температуре 10°С в течение еще 2 часов. Осадок отфильтровывают, промывают ледяной водой, сушат, подвергают дефлегмации в ацетоне в течение часа и очищают, получая 48 г соединения (III) (выход 70%) в виде белых кристаллов, т.пл. 260,5-273,0°С (разл.). 1Н ЯМР (ДМСО), δ: 7,72-7,75 (2Н, Н-4 и Н-6 на бензольном кольце), 7,26-7,28 (1Н, Н-3 на бензольном кольце), 4,12-4,17 (2Н, -СН2- на -ОСН2СН3), 3,5-3,53 (2Н, -СН2- на пиперазиновом кольце), 2,89-2,92 (2Н, -СН- на пиперазиновом кольце), 1,80-1,86 (2Н, -СН2- на пиперазиновом кольце), 1,31-1,34 (3Н, -СН3 на -ОСН2СН3), 1,0-1,04 (6Н, -СН3 на пиперазиновом кольце).
Пример 3. Получение 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензоилхлорида (IV)
Соединение (III) (34,2 г, 0,1 моль) и дихлорид сульфоксида (73,0 мл, 0,5 моль) помещают в 250-миллилитровую трехгорлую колбу и полученную смесь нагревают с обратным холодильником в течение 3 часов. Затем непрореагировавший дихлорид сульфоксида выпаривают в вакууме. К остатку добавляют этилацетат и перемешивают. Остаток фильтруют, промывают этилацетатом и сушат в вакууме, получая 29,4 г (74%) соединения (IV) в виде желтого твердого вещества, т.пл. 206,0-209,5°С. 1Н ЯМР (D2О), δ: 8,0 (1Н, Н-6 на бензоле), 7,74-7,76 (1Н, Н-4 на бензоле), 7,14-7,16 (1Н, Н-3 на бензоле), 4,08-4,11 (2Н, -СН2- на -ОСН2СН3), 3,74-3,77 (2Н, -СН2- на пиперазиновом кольце), 3,32 (2Н, -СН- на пиперазиновом кольце), 2,19-2,25 (2Н, -СН2- на пиперазиновом кольце), 1,24-1,27 (3Н, -СН3 на -ОСН2СН3), 1,09-1,10 (6Н, -СН3 на пиперазиновом кольце).
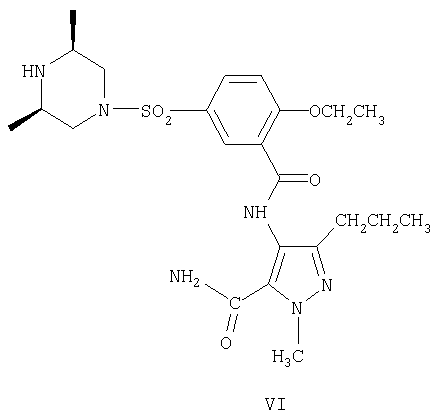
Пример 4. Получение 4-[-2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензамидо]-1-метил-3-н-пропилпиразол-5-карбоксамид (VI)
В 500-миллилитровую трехгорлую колбу последовательно помещают 125 мл метиленхлорида, 9,1 г (0,05 моль) 1-метил-4-амино-3-н-пропилпиразол-5-формамид (V), 0,06 г (0,0005 моль) 4-диметиламинопиридина и 10,1 г (0,1 моль) триэтиламина, а затем смесь охлаждают до температуры ниже 10°С. В смесь по каплям добавляют раствор соединения (IV) (25,80 г, 0,065 моль) в метиленхлориде (125 мл), а затем перемешивают при указанной температуре в течение 2 часов. Растворитель выпаривают, после чего к остатку добавляют воду. Твердое вещество отфильтровывают и промывают этилацетатом, получая 19,2 г соединения (VI) в виде серо-белого твердого вещества, т.пл. 197-198,5°С (выход 76%). 1Н ЯМР (CDCl3), δ: 8,62 (1Н, Н-6 на бензольном кольце), 7,90-7,92 (1Н, Н-4 на бензольном кольце), 7,90 (1Н, -СО-NH-), 7,17-7,27 (1Н, Н-3 на бензольном кольце), 5,73 (1Н, -NH - на пиперазиновом кольце), 4,37-4,41 (2H, -OCH2CH3), 4,06 (3H, N-CH3), 3,63-3,66 (2Н, -СН2- на пиперазиновом кольце), 3,0 (2Н, -СН- на пиперазиновом кольце), 2,52-2,56 (2H, -CH2CH2CH3), 1,84-1,90 (2H, -CH2- на пиперазиновом кольце), 1,65-1,69 (2Н, -СН2СН2СН3), 1,58-1,63 (3Н, -ОСН2СН3), 1,03-1,05 (6Н, -СН3 на пиперазиновом кольце), 0,94-0,97 (3Н, -СН2СН2СН3).
Пример 5. Получение 5-[[-2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)фенил]]-1-метил-3-н-пропил-7,6-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-она (I')
В 250-миллилитровую трехгорлую колбу помещают 1,8 г (0,046 моль) металлического калия и 96 мл сухого трет-бутилового спирта, а затем к смеси добавляют 19 г (0,0387 моль) соединения (IV). Смесь нагревают с обратным холодильником при перемешивании в течение 8 часов, а затем охлаждают до комнатной температуры. Добавляют 96 мл воды и рН доводят до 7,0, добавляя 0,5 моль/л соляной кислоты и получая осадок, после чего отстаивают смесь в течение часа при температуре ниже 10°С. Остаток фильтруют, промывают ледяной водой и сушат, получая 17,0 г соединения (I') (выход 93%) в виде белых кристаллов, т.пл. 202,2-203,2°С. 1Н ЯМР (MeOD), δ: 8,15 (1Н, Н-6 на бензольном кольце), 7,90-7,93 (1Н, Н-4 бензольное кольцо), 7,36-7,38 (1Н, Н-3 на бензольном кольце), 4,32 (2Н, -ОСН2СН3), 4,23 (3Н, NCH3), 3,75-3,78 (2Н, -СН2- на пиперазиновом кольце), 3,10 (2Н, -СН- на пиперазиновом кольце), 2,86-2,89 (2H, -CH2CH2CH3), 2,04-2,10 (2H, -CH2- на пиперазиновом кольце), 1,80-1,84 (2Н, -СН2СН2СН3), 1,45-1,48 (3Н, -ОСН2СН3), 1,14-1,17 (6Н, -СН3 на пиперазиновом кольце), 0,97-1,01 (3Н, -СН2СН2СН3). При необходимости соединение формулы (I') может быть превращено в его фармацевтически приемлемые соли известным способом.
Авторы данного изобретения обнаружили, что соединение в соответствии с настоящим изобретением весьма эффективно для лечения заболеваний, связанных с мужской эректильной дисфункцией, имеет более низкую токсичность и побочное действие. Конкретные результаты тестов на фармакодинамику и токсичность суммированы следующим образом.
Пример 6. Тест на фармакодинамику
Тест 1. Тест на эрекцию пениса в результате применения соединения формулы (I) у крыс с удаленными яичками.
Результаты показывают, что латентный период эрекции пениса в результате электрического раздражения (10 В) может быть существенно сокращен (Р<0,05 и P<0,01) у крыс после введения соединения формулы (I') в количестве 24 мг/кг и 12 мг/кг соответственно. Такой же результат получают после введения другого соединения, силденафила (P<0,01).
Тест 2. Действие соединения формулы (I') на половую функцию у мышей с удаленными яичками.
Результат а. Данный результат показывает, что латентный период, за который мышь-самец ловит мышь-самку, может быть существенно сокращен (Р<0,05 и P<0,01) после введения соединения формулы (I') в количестве 24 мг/кг и 12 мг/кг соответственно.
Результат b. Данный результат показывает, что период пребывания мыши-самца на мыши-самке (время полового акта) может быть существенно увеличен (Р<0,05 и P<0,01) после введения мыши-самцу соединения формулы (I') в количестве 24 мг/кг и 12 мг/кг соответственно.
Пример 7. Тест на токсичность
В результате применения способа Блисса (Bliss) было установлено, что полулетальная доза (LD50) составляет 901,5 мг/кг при пероральном введении мышам соединения формулы (I') через желудочный зонд. Доверительный предел 95% составляет 772,5-1052,1 мг/кг.
В соответствии с "Chinese Journal of Clinical Pharmacology and Therapeutics", 1999, 4(3), 237-240, LD50 такого соединения, как силденафил, составляет 625 мг/кг при пероральном введении разовой дозы мыши-самцу, а доверительный предел 95% составляет 50-672 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ПИРРОЛПИРИМИДИНОНА, СПОСОБ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2001 |
|
RU2263676C2 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ 5-[2-ЭТОКСИ-5-(4-МЕТИЛПИПЕРАЗИН-1-ИЛСУЛЬФОНИЛ)ФЕНИЛ]-1 МЕТИЛ-3-Н-ПРОПИЛ-1,6-ДИГИДРО-7H-ПИРАЗОЛ [4,3-D] ПИРИМИДИН-7-ОНА | 2003 |
|
RU2239637C1 |
| ПИРАЗОЛОПИРИМИДИНОНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ФОСФОДИЭСТЕРАЗЫ ЦИКЛИЧЕСКОГО ГУАНОЗИН-3',5'-МОНОФОСФАТА | 1992 |
|
RU2114113C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛОПИРИМИДИНОВЫХ СОЕДИНЕНИЙ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1991 |
|
RU2047617C1 |
| ПИРАЗОЛОПИРИМИДИНОНОВЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1991 |
|
RU2114114C1 |
| НОВЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ СЕКСУАЛЬНЫХ РАССТРОЙСТВ | 2005 |
|
RU2445095C2 |
| ЗАМЕЩЕННЫЙ 2-АМИНОПИРИДИН В КАЧЕСТВЕ ИНГИБИТОРА ПРОТЕИНКИНАЗЫ | 2014 |
|
RU2671212C2 |
| МОЛЕКУЛЫ-ИНГИБИТОРЫ БЕЛКА УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОТЕАЗЫ 7 | 2022 |
|
RU2814272C1 |
| ПРОИЗВОДНЫЕ 2,4,5-ТРИФЕНИЛИМИДАЗОЛИНА КАК ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ МЕЖДУ БЕЛКАМИ P53 И MDM2, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ПРОТИВОРАКОВЫХ СРЕДСТВ | 2006 |
|
RU2442779C2 |
| НОВЫЕ 1,2-БИС-СУЛЬФОНАМИДНЫЕ ПРОИЗВОДНЫЕ КАК МОДУЛЯТОРЫ ХЕМОКИНОВОГО РЕЦЕПТОРА | 2011 |
|
RU2654213C9 |
Настоящее изобретение относится к новым соединениям формулы (I), где R1 и R2 могут быть одинаковыми или различными и независимо представлять C1-6 алкил, которые являются селективными ингибиторами фосфодиэстеразы, их фармацевтически приемлемым солям или стереоизомерам. Настоящее изобретение также предусматривает способ получения предпочтительного соединения: 5-[[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)фенил]]-1-метил-3-н-пропил-7,6-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-она. Кроме того, предлагается новое промежуточное соединение, используемое в способе синтеза этого соединения. Соединения формулы (I) в соответствии с настоящим изобретением не только весьма эффективны для лечения заболеваний, связанных с импотенцией, таких как мужская эректильная дисфункция, но также отличаются такими признаками, как длительная терапевтическая эффективность и более низкая токсичность. Кроме того, объектами изобретения являются фармацевтическая композиция для лечения импотенции и применение соединения формулы (I) для получения лекарственного препарата, предназначенного для лечения заболеваний, связанных с импотенцией. 5 н. и 3 з.п. ф-лы.
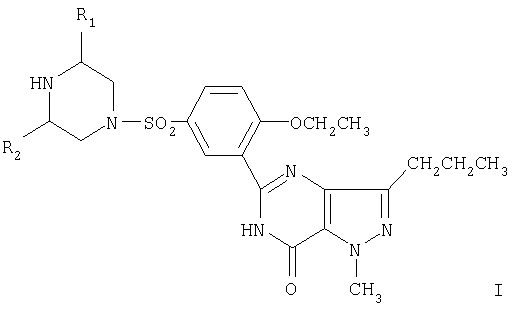
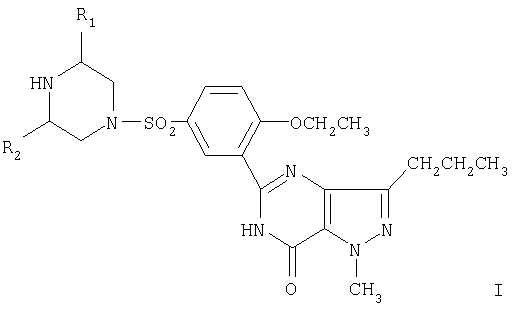
где R1 и R2 могут быть одинаковыми или различными и независимо представлять С1-6алкил.

а. взаимодействие 2-этоксибензойной кислоты в качестве исходного материала с хлорсульфоновой кислотой в присутствии дихлорида сульфоксида с получением 5-хлорсульфонил-2-этоксибензойной кислоты (соединение II);
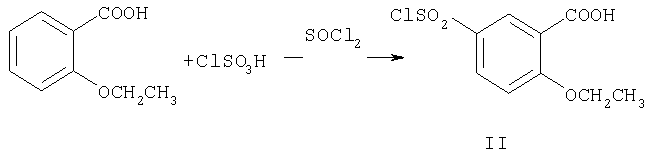
b. взаимодействие соединения (II) с цис-2,6-диметилпиперазином с получением 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензойной кислоты (соединение III);
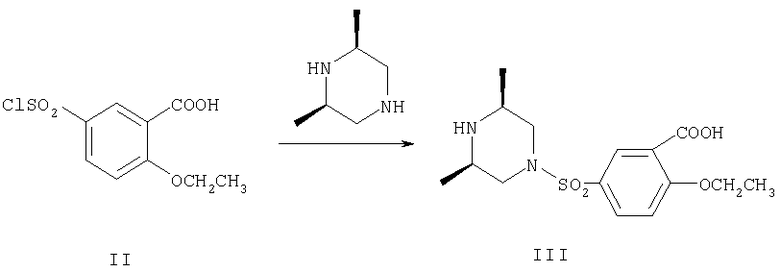
с. ацилирование соединения (III) с получением 2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензоилхлорида (IV);
d. взаимодействие соединения (IV) с соединением (V) в присутствии 4-диметиламинопиридина и триэтиламина с получением 4-[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)бензамидо]-1-метил-3-н-пропилпиразол-5-карбоксамида (соединение VI);
е. циклизацию соединения (VI) в присутствии трет-бутоксида калия с получением 5-[[2-этокси-5-(цис-2,6-диметилпиперазин-4-илсульфонил)фенил]]-1-метил-3-н-пропил-7,6-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-она (I').
Приоритеты:
| ПИРАЗОЛПИРИМИДИНОНЫ ДЛЯ ЛЕЧЕНИЯ ИМПОТЕНЦИИ | 1994 |
|
RU2130776C1 |
| ПИРАЗОЛОПИРИМИДИНОНОВЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1991 |
|
RU2114114C1 |
| Способ окускования флюоритовогоКОНцЕНТРАТА | 1979 |
|
SU812845A1 |
Авторы
Даты
2006-07-10—Публикация
2002-06-21—Подача