Область изобретения
Настоящее изобретение относится к удобному и экономичному способу получения дипептида без применения сложного способа синтеза и, более конкретно, оно относится к гену пептидообразующего фермента, пептидообразующему ферменту и способу получения дипептида с использованием фермента.
Предшествующий уровень техники
Дипептиды используются в области фармацевтических препаратов и функциональных продуктов питания, а также в других различных областях. Например, L-аланил-L-глутамин используется в качестве компонента не содержащей сыворотки среды и применяется в качестве инфузионных компонентов, поскольку он обладает большей стабильностью и более высокой растворимостью, чем L-глутамин.
Химические способы синтеза, которые обычно известны как способы получения дипептидов, необязательно являются простыми. Известные примеры таких способов включают способ, в котором используется N-бензилоксикарбонилаланин (далее "Z-аланин") и защищенный L-глутамин (смотри Bull. Chem. Soc. Jpn., 34, 739 (1961), Bull. Chem. Soc. Jpn., 35, 1966 (1962)), способ, в котором используется Z-аланин и защищенный метиловый эфир L-γ-глутаминовой кислоты (Bull. Chem. Soc. Jpn., 37, 200 (1964)), способ, в котором используется эфир Z-аланина и незащищенная глутаминовая кислота (Выложенная публикация заявки на патент Японии No. H1-96194), и способ, в котором в качестве исходного вещества используется 2-замещенный пропионилгалогенид и в качестве промежуточного продукта синтезируют производное N-(2-замещенный)пропионилглутамина (Выложенная публикация заявки на патент Японии No. H6-234715).
Однако во всех таких способах требуется введение и удаление защитной группы или синтез промежуточного соединения, так что такие способы получения не являются достаточно удовлетворительными с точки зрения промышленного производства. Известные примеры типичных способов получения дипептидов с использованием ферментов включают реакцию конденсации с использованием N-защищенного, C-незащищенного карбоксильного компонента и N-незащищенного, C-защищенного аминного компонента (реакция 1), и реакцию замещения с использованием N-защищенного, C-защищенного карбоксильного компонента и N-незащищенного, C-защищенного аминного компонента (реакция 2). Примером реакции 1 является способ получения метилового эфира Z-аспартилфенилаланина из Z-аспарагиновой кислоты и метилового эфира фенилаланина (Выложенная публикация заявки на патент Японии No. S53-92729), тогда как примером реакции 2 является способ получения ацетилфенилаланиллейцинамида из этилового эфира ацетилфенилаланина и лейцинамида (Biochemical J., 163, 531 (1977)). Имеется весьма ограниченное число примеров научных публикаций, в которых описываются способы с использованием N-незащищенных, C-защищенных карбоксильных компонентов. Пример реакции замещения с использованием N-незащищенного, C-защищенного карбоксильного компонента и N-незащищенного, C-защищенного аминного компонента (реакция 3) описан в патенте WO 90/01555, и примером такой реакции является способ получения амида аргиниллейцина из этилового эфира аргинина и амида лейцина. Пример реакции замещения с использованием N-незащищенного, C-защищенного карбоксильного компонента и N-незащищенного, C-незащищенного аминного компонента (реакция 4) описан в патенте EP 278787A, и примером такой реакции является способ получения тирозилаланина из этилового эфира тирозина и аланина. Естественно, к числу способов, которые могут служить в качестве наименее дорогих, относятся те, которые попадают в диапазон реакции 4, когда число защитных групп в используемых компонентах является минимальным.
Однако фермент, использованный в примере предшествующего уровня техники для реакции 4 (Patent EP 278787A), представляет собой относительно дорогой препарат карбоксипептидазы, полученный из плесневых грибов и растений, и получаемые дипептиды содержали аминокислоты с относительно высокой степенью гидрофобности. Для реакции 4 отсутствуют известные способы, в которых используются ферменты бактериального или дрожжевого происхождения, и не известен способ получения аланилглутамина или аланиласпарагина высокой гидрофильности. При таких обстоятельствах существует необходимость разработки способа получения таких пептидов в промышленном масштабе и при низкой стоимости.
С другой стороны, пролиниминопептидаза представляет собой фермент, который катализирует реакцию, в результате которой N-концевой пролин отщепляется от пептида, содержащего на своем N-конце пролин, и известно, что данный фермент существует во многих видах организмов. Например, известно, что он существует в высших животных, таких как морские свинки (мозг) (J. Biol. Chem., 258, 6147-6154 (1983)), крысы (мозг и почки) (Eur. J. Biochem., 190, 509-515 (1990)), в высших растениях, например, в абрикосовых косточках (J. Biochem., 92, 413-421 (1982)), ротовой полости спирохет, таких как Trichoderma denticola (Infect. Immun., 64, 702-708 (1996), нитевидных грибах, таких как Penicillium species (выложенная публикация заявки на патент Японии No. H1-215288), Basidiomycetes, таких как грибы шитаки (выложенная публикация заявки на патент Японии No. S58-36387), Actinomycetes, таких как Streptomyces plicatus (Biochem. Biophys. Res. Commun., 184, 1250-1255 (1992), и бактериях, таких как Corynebacterium variabilis (J. Appl. Microbiol., 90, 449-456 (2001)).
Кроме того, сообщалось о клонировании и последовательности оснований генов пролиниминопептидаз Arthrobacter nicotiana (FEMS Microbiol. Lett., 78, 191-197 (1999)), Escherichia coli (публикация выложенной заявки на патент Японии No. H2-113887), Flavobacterium meningosepticum (Arch. Biochem. Biophys., 336, 35-41 (1996)), Hafnia alvei (J. Biochem., 119, 468-474 (1996)), Lactobacillus delbrueckii (Microbiology, 140, 527-535 (1994)), Bacillus coagulans (J. Bacteriol., 174, 7919-1925 (1994)), Aeromonas sobria (J. Biochem., 116, 818-825 (1994)), Xanthomonas campestris (публикация выложенной заявки на патент Японии No. H9-121860), Neisseria gonorrhoeae (Mol. Microbiol., 9, 1203-1211 (1993)), Propionibacterium freundenreichii (Appl. Environ. Microbiol., 64, 4736-4742 (1998)), Serratia marcescens (J. Biochem., 122, 601-605 (1997)) и Thermoplasma acidophilum (FEBS Lett., 398, 101-105 (1996)).
Кроме того, в результате анализа полных геномов микроорганизмов недавно было сообщено о последовательностях оснований, которые как прогнозируется, кодируют пролиниминопептидазу в многочисленных видах организмов. Например, опубликована последовательность оснований полного генома Pseudomonasaeruginosa (Nature, 406, 959 (2000)), и в нем была выявлена последовательность оснований, которая, как предполагается, кодирует пролиниминопептидазу.
С другой стороны, было установлено, что дипептид, содержащий пролин, образуется, когда эфир L-пролина или DL-пролина и альфа-аминокислота взаимодействуют в присутствии пролиниминопептидазы (Выложенная публикация заявки на патент Японии No. H3-13391). Однако хотя пролиниминопептидаза представляет собой фермент, который катализирует реакцию с отщеплением N-концевого пролина от пептида, содержащего на своем N-конце пролин, и, естественно, можно было бы рассматривать получение пролиламинокислоты из эфира пролина и аминокислоты, синтез пептида из аминокислоты и эфира аминокислоты, отличающейся от пролина, с использованием пролиниминопептидазы совершенно не известен. Конечно, синтез L-аланил-L-глутамина из гидрохлорида этилового эфира L-аланина и L-глутамина также ранее не был известен. Кроме того, хотя частичная последовательность оснований пролиниминопептидазы Pseudomonas putida штамма ATCC 12633 описана (AF032970), какого-то ни было исследования ее активности, включая ее выявление, не проводилось.
Описание изобретения
Целью настоящего изобретения является разработка способа получения дипептида промышленно выгодным и простым путем с использованием дешевого исходного материала и источника фермента, который можно дешево восполнять (такого как микробная культура, клетки микроорганизмов или обработанный продукт клеток микроорганизмов).
В результате интенсивного научного исследования с вышеуказанной целью авторы настоящего изобретения установили, что пролиниминопептидаза обладает способностью продуцировать пептид из эфира L-аминокислоты и L-аминокислоты. Кроме того, авторы настоящего изобретения также клонировали и экспрессировали ген данного фермента и четко продемонстрировали широкую субстратную специфичность фермента в отношении продуцирования пептида с использованием очищенных рекомбинантных ферментов, что привело к осуществлению настоящего изобретения.
Настоящее изобретение является таким, как описано ниже.
[1] Белок (A) или (B):
(A) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 5 списка последовательностей,
(B) белок, состоящий из аминокислотной последовательности, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 5 списка последовательностей, и обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[2] Белок (C) или (D):
(C) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 15 списка последовательностей,
(D) белок, состоящий из аминокислотной последовательности, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 15 списка последовательностей, и обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[3] Белок (E) или (F):
(E) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 17 списка последовательностей,
(F) белок, состоящий из аминокислотной последовательности, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 17 списка последовательностей, и обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[4] ДНК (a) или (b):
(a) ДНК с последовательностью оснований, состоящей из оснований с номерами 57-1295 в последовательности оснований, представленной в SEQ ID NO: 4 списка последовательностей,
(b) ДНК, которая гибридизуется в жестких условиях с ДНК с последовательностью оснований, состоящей из оснований с номерами 57-1295 в последовательности оснований, представленной в SEQ ID NO: 4 списка последовательностей, и кодирует белок, обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[5] ДНК (c) или (d):
(c) ДНК с последовательностью оснований, состоящей из оснований с номерами 486-1496 в последовательности оснований, представленной в SEQ ID NO: 14 списка последовательностей,
(d) ДНК, которая гибридизуется в жестких условиях с ДНК с последовательностью оснований, состоящей из оснований с номерами 486-1496 в последовательности оснований, представленной в SEQ ID NO: 14 списка последовательностей, и кодирует белок, обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[6] ДНК (e) или (f):
(e) ДНК с последовательностью оснований, состоящей из оснований с номерами 311-1279 в последовательности оснований, представленной в SEQ ID NO: 16 списка последовательностей,
(f) ДНК, которая гибридизуется в жестких условиях с ДНК с последовательностью оснований, состоящей из оснований с номерами 311-1279 в последовательности оснований, представленной в SEQ ID NO: 16 списка последовательностей, и кодирует белок, обладающий продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
[7] ДНК по любому из вышеуказанных пунктов [4] - [6], где жесткие условия представляют собой условия, при которых промывку проводят при 60°C и концентрации соли, эквивалентной 1 × SSC и 0,1% SDS.
[8] Рекомбинантная ДНК, включающая введенную в нее ДНК по любому из вышеуказанных пунктов [4] - [7].
[9] Трансформированная клетка, включающая введенную в нее ДНК по любому из вышеуказанных пунктов [4] - [7] таким образом, что ДНК способна экспрессировать кодируемый ею белок.
[10] Способ получения образующего дипептид фермента, включающий культивирование трансформированных клеток по пункту [9] в среде и накопление белка, обладающего продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью в среде и/или в трансформированных клетках.
[11] Способ получения дипептида, включающий получение дипептида из эфира L-аминокислоты и L-аминокислоты с использованием белка, обладающего продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью, который продуцируется в трансформированных клетках по пункту [9] выше.
[12] Способ получения дипептида по вышеуказанному пункту [11], где эфир L-аминокислоты представляет собой один или несколько представителей, выбранных из группы, состоящей из эфира L-аланина, эфира глицина, эфира L-валина, эфира L-изолейцина, эфира L-метионина, эфира L-фенилаланина, эфира L-серина, эфира L-треонина, эфира L-глутамина, эфира L-тирозина, эфира L-аргинина, α-эфира L-аспарагиновой кислоты, β-эфира L-аспарагиновой кислоты, эфира L-лейцина, эфира L-аспарагина, эфира L-лизина, α,β-диметилового эфира L-аспарагиновой кислоты и γ-эфира L-глутамина.
[13] Способ получения дипептида по указанному выше пункту [11] или [12], где L-аминокислота представляет собой один или несколько представителей, выбранных из группы, состоящей из L-глутамина, L-аспарагина, глицина, L-аланина, L-лейцина, L-метионина, L-пролина, L-фенилаланина, L-триптофана, L-серина, L-треонина, L-тирозина, L-лизина, L-аргинина, L-гистидина и L-глутаминовой кислоты.
[14] Способ получения дипептида, включающий предоставление белку, обладающему пролиниминопептидазной активностью, возможности реагировать с эфиром L-аминокислоты и L-аминокислотой с образованием дипептида.
[15] Способ получения дипептида по вышеуказанному пункту [14], где белок, обладающий пролиниминопептидазной активностью, происходит из микроорганизма, принадлежащего к роду Corynebacterium, Pseudomonas или Bacillus.
[16] Способ получения дипептида по вышеуказанному пункту [14], где белок, обладающий пролиниминопептидазной активностью, происходит из любого из Corynebacterium glutamicum, Pseudomonas putida или Bacillus coagulans.
[17] Способ получения дипептида по любому из вышеуказанных пунктов [14]-[16], где эфир L-аминокислоты представляет собой один или несколько представителей, выбранных из группы, состоящей из эфира L-аланина, эфира глицина, эфира L-валина, эфира L-изолейцина, эфира L-метионина, эфира L-фенилаланина, эфира L-серина, эфира L-треонина, эфира L-глутамина, эфира L-тирозина, эфира L-аргинина, α-эфира L-аспарагиновой кислоты, β-эфира L-аспарагиновой кислоты, эфира L-лейцина, эфира L-аспарагина, эфира L-лизина, α,β-диметилового эфира L-аспарагиновой кислоты и γ-эфира L-глутамина.
[18] Способ получения дипептида по любому из пунктов [14]- [17] выше, где L-аминокислота представляет собой один или несколько представителей, выбранных из группы, состоящей из L-глутамина, L-аспарагина, глицина, L-аланина, L-лейцина, L-метионина, L-пролина, L-фенилаланина, L-триптофана, L-серина, L-треонина, L-тирозина, L-лизина, L-аргинина, L-гистидина и L-глутаминовой кислоты.
[19] Способ получения дипептида, включающий получение дипептида из эфира аминокислоты и аминокислоты с использованием культуры микроорганизма, принадлежащего к роду Corynebacterium, Pseudomonas или Bacillus и обладающего способностью продуцировать дипептид из эфира аминокислоты и аминокислоты, клеток микроорганизмов, выделенных из культуры, или обработанного продукта микроорганизма.
[20] Способ получения дипептида по вышеуказанному пункту [19], где эфир L-аминокислоты представляет собой один или несколько представителей, выбранных из группы, состоящей из эфира L-аланина, эфира глицина, эфира L-валина, эфира L-изолейцина, эфира L-метионина, эфира L-фенилаланина, эфира L-серина, эфира L-треонина, эфира L-глутамина, эфира L-тирозина, эфира L-аргинина, α-эфира L-аспарагиновой кислоты, β-эфира L-аспарагиновой кислоты, эфира L-лейцина, эфира L-аспарагина, эфира L-лизина, α,β-диметилового эфира L-аспарагиновой кислоты и γ-эфира L-глутамина.
[21] Способ получения дипептида по вышеуказанному пункту [19], где L-аминокислота представляет собой один или несколько представителей, выбранных из группы, состоящей из L-глутамина, L-аспарагина, глицина, L-аланина, L-лейцина, L-метионина, L-пролина, L-фенилаланина, L-триптофана, L-серина, L-треонина, L-тирозина, L-лизина, L-аргинина, L-гистидина и L-глутаминовой кислоты.
Другие цели, отличительные особенности и преимущества настоящего изобретения более конкретно указаны или станут очевидными из следующего подробного описания изобретения.
Краткое описание чертежа
Чертеж представляет собой график, иллюстрирующий дипептид-продуцирующую активность при добавлении ингибитора.
Наилучший способ осуществления изобретения
Настоящее изобретение относится к новому белку, обладающему продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью, ДНК, кодирующей данный белок, и способу получения дипептида с их использованием. Реакция, по которой происходит образование дипептида в способе получения дипептида по настоящему изобретению, показана далее на реакционной схеме. Как иллюстрируют следующие химические формулы, термин «дипептид», как он использован в данном описании, относится к пептидному полимеру, имеющему одну дипептидную связь.
R1-CH(NH2)-COOR+H2N-CH(COOH)-R2→R1-CH(NH2)-CONH-CH(COOH)-R2+ROH
(где R представляет собой замещенную или незамещенную углеводородную цепь, R1 представляет собой боковую цепь эфира аминокислоты и R2 представляет собой боковую цепь аминокислоты.)
Эфиры аминокислот представляют собой соединения, которые имеют невысокую стоимость. Способ по настоящему изобретению, в котором исходные вещества в виде эфира аминокислоты и незащищенной аминокислоты взаимодействуют в водном растворе с использованием бактерий, дрожжей и так далее в качестве источника фермента, представляет собой новый способ получения дипептида и дает возможность дешево получать дипептиды, полезные для использования в фармацевтических препаратах и функциональных продуктах питания.
Далее настоящее изобретение будет описано подробно в следующем порядке:
[I] Микроорганизмы, обладающие способность продуцировать дипептиды из эфиров L-аминокислот и L-аминокислот
[II] Выделение ДНК, кодирующей белок, обладающий продуцирующей пептид активностью
[III] Свойства продуцирующего пептид фермента
[IV] Способ получения дипептида
[I] Микроорганизмы, обладающие способностью продуцировать дипептиды из эфиров L-аминокислот и L-аминокислот
Микроорганизмы, обладающие способностью продуцировать дипептиды из эфиров L-аминокислот и L-аминокислот, можно использовать без каких-либо особых ограничений в качестве микроорганизма, используемого по настоящему изобретению. Примеры микроорганизмов, обладающих способностью продуцировать дипептиды из эфиров L-аминокислот и L-аминокислот, включают виды Bacillus, виды Corynebacterium и виды Pseudomonas, конкретные примеры которых указаны ниже.
Bacillus subtilis ATCC 6633
Bacillus coagulans EK01 (J. Bacteriol. 174, 7919-7925 (1992))
Corynebacterium glutamicum ATCC 13286
Pseudomonas putida AJ-2402 FERM BP-8101
Pseudomonas putida ATCC 12633
Pseudomonas putida AJ-2048 FERM BP-8123
Перечисленные выше штаммы микроорганизмов, которые указаны под ATCC номерами, депонированы в Американской коллекции типовых культур (P.O. Box 1549, Manassas, VA 20110), и субкультуры могут быть предоставлены при ссылке на каждый номер.
Перечисленные выше штаммы микроорганизмов, которые указаны под FERM номерами, депонированы в независимой административной корпорации, Международный депозитарий патентных организмов Национального института передовой промышленной науки и технологии (International Patent Organism Depositary of the National Institute for Advanced Industrial Science and Technology) (Chuo Dai-6, 1-1 Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Япония), и им были присвоены депозитные номера. Штамму Pseudomonas putida AJ-2402, который был депонирован в независимой административной корпорации, Международный депозитарий патентных организмов Национального института передовой промышленной науки и технологии, 1 октября 2001, присвоен депозитный номер FERM P-18544, контроль данного штамма позднее был передан на международное депонирование 1 июля 2002, и ему был присвоен депозитный номер FERM BP-8101. Отметим, что FERM BP-8101 (AJ-2402) был идентифицирован как указанный выше Pseudomonas putida на основании последующего классификационного эксперимента. Кроме того, штамм AJ-2048 Pseudomonas putida был депонирован в независимой административной корпорации, Международный депозитарий патентных организмов Национального института передовой промышленной науки и технологии 22 июля 2002, и ему был присвоен депозитный номер FERM BP-8123.
Штамм FERM BP-8101 Pseudomonas putida представляет собой подвижную аконидальныю палочку, которая была идентифицирована как бактерия, принадлежащая к роду Pseudomonas на основании таких свойств, как принадлежность к грамотрицательной палочке (0,7 до 0,8 × 1,5 до 2,0 микрометров (мкм)), которая не образует спор, является подвижной, образует круглые блестящие колонии кремового цвета с полностью гладкой или волнистой границей, растет при 30°C и является каталаза-положительной, оксидаза-положительной и отрицательной по OF-тесту (глюкоза). Более того, он был идентифицирован как Pseudomonas putida на основании таких физиологических свойств, как то, что он является отрицательным в отношении нитратного восстановления, отрицательным в отношении продуцирования индола, отрицательным в отношении кислотного продуцирования из глюкозы, аргининдигидролаза-положительным, уреаза-отрицательным, отрицательным в отношении эскулинового гидролиза, отрицательным в отношении желатинового гидролиза, β-галактозидаза-отрицательным, положительным в отношении ассимиляции глюкозы, отрицательным в отношении ассимиляции L-арабинозы, положительным в отношении ассимиляции D-маннозы, положительным в отношении ассимиляции D-маннита, отрицательным в отношении ассимиляции N-ацетил-D-глюкозамина, отрицательным в отношении ассимиляции мальтозы, положительным в отношении ассимиляции глюконата калия, положительным в отношении ассимиляции н-каприновой кислоты, отрицательным в отношении ассимиляции адипиновой кислоты, положительным в отношении ассимиляции dl-яблочной кислоты, положительным в отношении ассимиляции цитрата натрия, положительным в отношении ассимиляции фенилацетата, оксидаза-положительным, положительным в отношении продуцирования флуорохрома на агаровой среде King's B, положительным в отношении продуцирования левана из сахарозы и слабо ассимилирующим сорбит.
В качестве данных микроорганизмов можно использовать дикие штаммы или мутантные штаммы, а также можно использовать рекомбинантные штаммы и тому подобные, полученные слиянием клеток, генетическими манипуляциями или другими генетическими способами.
Для получения клеток данных микроорганизмов микроорганизмы можно культивировать и выращивать в подходящей среде. Не имеется особенного ограничения для среды, используемой в этих целях до тех пор, пока она позволяет микроорганизмам расти. Данная среда может представлять собой обычную среду, содержащую обычные источники углерода, источники азота, источники фосфора, источники серы, неорганические ионы и органические источники питания при необходимости.
Например, можно использовать любой источник углерода до тех пор, пока вышеуказанные микроорганизмы могут его использовать, и конкретные примеры такого источника, который можно использовать, включают сахара, такие как глюкоза, фруктоза, мальтоза и амилоза, спирты, такие как сорбит, этанол и глицерин, органические кислоты, такие как фумаровая кислота, лимонная кислота, уксусная кислота и пропионовая кислота и их соли, углеводороды, такие как парафин, и их смеси.
Примеры источников азота, которые могут использоваться, включают соли аммония неорганических кислот, такие как сульфат аммония и хлорид аммония, соли аммония органических кислот, такие как фумарат аммония и цитрат аммония, нитраты, такие как нитрат натрия и нитрат калия, органические азотсодержащие соединения, такие как пептоны, дрожжевой экстракт, мясной экстракт и кукурузный крепкий солод, а также их смеси.
Кроме того, источники питания, используемые в обычных средах, такие как неорганические соли, редкие металлы и витамины, также можно смешивать подходящим образом и использовать.
Не имеется особенного ограничения к условиям культивирования и культивирование можно проводить, например, в течение примерно от 12 до 48 часов при контролировании подходящим образом рН и температуры в диапазоне рН от 5 до 8 и диапазоне температуры от 15 до 40°C в аэробных условиях.
[II] Выделение ДНК, кодирующей белок, обладающей активностью продуцирующего пептид фермента
[II-1] Выделение ДНК
Авторы настоящего изобретения выделили и определили последовательность ДНК по настоящему изобретению, которая кодирует белок, обладающий синтезирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью. ДНК с последовательностью оснований, состоящей из оснований с номерами 57-1295 в последовательности, представленной в SEQ ID NO: 4 списка последовательностей, была выделена из штамма ATCC 13286 Corynebacterium glutamicum. Кроме того, ДНК с последовательностью оснований, состоящей из оснований с номерами 486-1496 в последовательности, представленной в SEQ ID NO: 14 списка последовательностей, была выделена из штамма ATCC 12633 Pseudomonas putida. Помимо этого, ДНК с последовательностью оснований, состоящей из оснований с номерами 311-1279 в последовательности, представленной в SEQ ID NO: 16 списка последовательностей, была выделена из штамма FERM BP-8123 Pseudomonas putida. Отметим, что в настоящем описании выражения «последовательность оснований, представленная в SEQ ID NO: 4», «последовательность оснований, представленная в SEQ ID NO: 14» и «последовательность оснований, представленная в SEQ ID NO: 16» относятся к CDS частям, если специально не указано другого.
Показан пример выделения ДНК. Во-первых, первоначально определяют аминокислотную последовательность очищенного продуцирующего пептид фермента. Аминокислотная последовательность может быть определена с использованием способа Эдмана (Edman) (смотри Edman, P., Acta Chem. Scand., 4, 227 (1950)). Кроме того, аминокислотная последовательность также может быть определена с использованием секвенатора, производимого Applied Biosystems. Аминокислотную последовательность определяют для N-концевого участка или примерно от 10 до 30 остатков пептида, полученного обработкой лизилэндопептидазой и так далее для очищенного пептидообразующего фермента; и на основании определенной аминокислотной последовательности может быть выведена последовательность оснований ДНК, которая ее кодирует. Для выведения последовательности оснований ДНК используются универсальные кодоны.
Затем синтезируют молекулу ДНК из примерно 30 пар оснований на основании выведенной последовательности оснований. Способ синтеза молекулы ДНК описан в Tetrahedron Letters, 22, 1859 (1981). Кроме того, молекула ДНК может быть синтезирована с использованием секвенатора, производимого Applied Biosystems. Затем ДНК, которая кодирует пептидообразующий фермент, может быть амплифицирована из хромосомной ДНК с помощью метода ПЦР при использовании молекулы ДНК в качестве праймера. Однако поскольку ДНК, которая была амплифицирована с использованием метода ПЦР, не содержит полноразмерную ДНК, которая кодирует пептидообразующий фермент, полноразмерную ДНК, кодирующую пептидообразующий фермент, выделяют из библиотеки хромосомных генов клеток различных микроорганизмов, таких как Corynebacterium glutamicum, Pseudomonas putida или Bacillus subtilis, с использованием ДНК, амплифицированной методом ПЦР, в качестве зонда.
Альтернативно, в том случае, когда известна часть последовательности оснований гена, полноразмерная ДНК, которая кодирует пептидообразующий фермент, может быть выделена из библиотеки хромосомных генов с использованием в качестве зонда ДНК, которая имеет известную последовательность.
Кроме того, в том случае, когда последовательность оснований гена гомологична известной последовательности, полноразмерная ДНК, которая кодирует пептидообразующий фермент, может быть выделена из библиотеки хромосомных генов с использованием в качестве зонда ДНК, которая имеет известную последовательность.
Методика метода ПЦР описана, например, White, T.J. et al., Trends Genet., 5, 185 (1989). Способ получения хромосомной ДНК так же, как и способ выделения целевой молекулы ДНК из библиотеки генов с использованием молекулы ДНК в качестве зонда, описаны в Molecular Cloning, 2nd edition, Cold Spring Harbor Press (1989).
Способ определения последовательности оснований выделенной ДНК, которая кодирует пептидообразующий фермент, описана в A Practical Guide to Molecular Cloning, John Wiley & Sons, Inc. (1985). Кроме того, последовательность оснований также может быть определена с использованием ДНК-секвенатора (Applied Biosystems). ДНК, которые кодируют пептидообразующие ферменты, выделенные таким образом из штамма ATCC 13286 Corynebacterium glutamicum, штамма ATCC 12633 Pseudomonas putida и штамма FERM BP-8123 Pseudomonas putida, представлены в последовательностях SEQ ID NO: 4, 14 и 16 соответственно.
ДНК, которые можно использовать в настоящем изобретении, представляют собой не только ДНК, определенные последовательностями SEQ ID NO: 4, 14 и 16. Например, в случае ДНК SEQ ID NO: 4, выделенной из штамма ATCC 13286 Corynebacterium glutamicum ниже, даже та ДНК, которая была получена внесением искусственной мутации в ДНК, которая кодирует пептидообразующий фермент и может быть выделена из хромосомной ДНК штамма ATCC 13286 Corynebacterium glutamicum, также представляет собой ДНК по настоящему изобретению, если она кодирует пептидообразующий фермент. Часто используемым способом для искусственного мутирования ДНК является способ сайт-направленного мутагенеза, описанный в Methods in Enzymol., 154 (1987).
Кроме того, ДНК, имеющая последовательность оснований, которая гибридизуется в жестких условиях с полинуклеотидом, имеющим последовательность оснований, комплементарную последовательности оснований, представленной в SEQ ID NO: 4 списка последовательностей, и кодирующая белок, обладающий пептидообразующей активностью, также может быть использована в качестве ДНК по настоящему изобретению.
Кроме того ДНК, по существу идентичная ДНК по настоящему изобретению, также может быть получена выделением ДНК, которая гибридизуется в жестких условиях с зондом, полученным на основе ДНК, состоящей из CDS, представленной в SEQ ID NO: 4 списка последовательностей, и кодирует белок, обладающий активностью пептидообразующего фермента. Зонд может быть получен в соответствии с разработанными способами на основе, например, последовательности оснований, представленной в SEQ ID NO: 4 списка последовательностей. Дополнительно, способ, в котором целевую ДНК выделяют с использованием зонда и отбора ДНК, которая гибридизуется с ним, также может быть осуществлен в соответствии с разработанными способами. Например, ДНК-зонд может быть получен амплификацией последовательности оснований, клонированной в плазмидном или фаговом векторе, и экстрагированием последовательности оснований, желаемой для использования в качестве зонда, путем расщепления с помощью фермента рестрикции. Положение, в котором последовательность расщепляют, может быть отрегулировано в соответствии с ДНК-мишенью.
Термин «жесткие условия», используемый в данном описании, относится к условиям, при которых образуется так называемый специфический гибрид, тогда как неспецифические гибриды не образуются. Хотя трудно четко определить данные условия, примеры таких условий включают условия, при которых ДНК, имеющая высокую степень гомологии, такая как ДНК, имеющая 50% гомологии или более, предпочтительно 80% или более, и более предпочтительно 90% или более, гибридизуется, тогда как ДНК, имеющая низкую степень гомологии, не гибридизуется; или условия, при которых ДНК гибридизуется при 60°C и концентрации соли, эквивалентной 1×SSC и 0,1% SDS, которые представляют собой условия промывки при стандартной гибридизации по Саузерну, предпочтительно при 60°C и концентрации соли, эквивалентной 0,1×SSC и 0,1% SDS, и более предпочтительно при 65°С и концентрации соли, эквивалентной 0,1×SSC и 0,1% SDS. Активность пептидообразующего фермента является такой, как объяснялось ранее. Однако в случае последовательности оснований, которая гибридизуется в жестких условиях с последовательностью оснований, комплементарной последовательности оснований, представленной в SEQ ID NO: 4 списка последовательностей, предпочтительно сохраняется 10% или более и предпочтительно 50% или более ферментативной активности белка, имеющего аминокислотную последовательность, представленную в SEQ ID NO: 4 списка последовательностей при условиях 50°C и pH 8.
Более того, белок, по существу идентичный пептидообразующему ферменту, кодированному ДНК, представленной в SEQ ID NO: 4 списка последовательностей, также можно использовать в настоящем изобретении. Таким образом, ДНК, которая кодирует «белок, имеющий аминокислотную последовательность, включающую замещение, удаление, вставку, добавление или перестановку местами одной или множества аминокислот в аминокислотной последовательности, представленной SEQ ID NO: 5 списка последовательностей, и обладающий катализирующей реакцию активностью пептидообразующего фермента, который продуцирует дипептид из эфира L-аминокислоты и L-аминокислоты», также может использоваться в настоящем изобретении. Термин «множество» относится к такому диапазону аминокислотных остатков, которое существенно не затрагивает трехмерную структуру белка или активность пептидообразующего фермента, и более конкретно имеет величину от 2 до 50, предпочтительно от 2 до 30 и более предпочтительно от 2 до 10. В дополнение, активность пептидообразующего фермента является такой, как объяснено ранее. Однако в случае аминокислотной последовательности, включающей замещение, удаление, вставку, добавление или перестановку местами одного или множества аминокислотных остатков в аминокислотной последовательности, представленной SEQ ID NO: 5 списка последовательностей, предпочтительно сохраняется 10% или более, и предпочтительно 50% или более ферментативной активности белка, имеющего аминокислотную последовательность, представленную в SEQ ID NO: 5 списка последовательностей, при условиях 50°C и pH 8.
Как описано выше, в дополнение к ДНК, выделенной из штамма ATCC 13286 Corynebacteriumglutamicum, ДНК, выделенной из штаммаATCC 12633 Pseudomonasputida, и ДНК, выделенной из штамма FERM BP-8123 Pseudomonasputida, ДНК, по существу идентичные данным ДНК, также рассматриваются как ДНК по настоящему изобретению. А именно, примеры ДНК, предусмотренные по настоящему изобретению, представляют собой следующее:
(i) ДНК, состоящая из CDS, представленной в SEQ ID NO: 4, 14 или 16 списка последовательностей;
(ii) ДНК, которая гибридизуется в жестких условиях с полинуклеотидом, состоящим из последовательности оснований, комплементарной CDS, представленной в SEQ ID NO: 4, 16 или 18 списка последовательностей, и кодирует белок, обладающий активностью пептидообразующего фермента для катализа реакции, в которой дипептид образуется из эфира L-аминокислоты и L-аминокислоты.
(iii) ДНК, которая кодирует белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 5, 15 или 17 списка последовательностей; и
(iv) ДНК, которая кодирует белок, имеющий аминокислотную последовательность, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 5, 15 или 17 списка последовательностей, и обладающий активностью пептидообразующего фермента для катализа реакции, в которой дипептид образуется из эфира L-аминокислоты и L-аминокислоты.
[II-2] Получение трансформанта
Далее будет описано получение трансформанта, который экспрессирует белок, обладающий пептидообразующей ферментативной активностью. Известно множество примеров получения ферментов, физиологически активных веществ и других полезных белков с использованием технологии рекомбинантной ДНК, и применение технологии рекомбинантной ДНК позволяет получать в большом количестве полезные белки, присутствующие в природе только в следовых количествах.
Предпочтительные примеры трансформантов, которые можно использовать в способе по настоящему изобретению, включают трансформанты, способные экспрессировать указанные далее белки (AA), (BB), (CC) или им подобные:
(AA) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 5, 15 или 17 списка последовательностей;
(BB) белок, имеющий аминокислотную последовательность, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 5, 15 или 17 списка последовательностей, и обладающий активностью пептидообразующего фермента для катализа реакции, в которой дипептид образуется из эфира L-аминокислоты и L-аминокислоты; или
(CC) белок, кодируемый ДНК, которая гибридизуется в жестких условиях с полинуклеотидом, состоящим из последовательности оснований, комплементарной последовательности оснований, представленной в SEQ ID NO: 4, 16 или 18 списка последовательностей, или зондом, полученным на основе последовательности оснований SEQ ID NO: 4, 16 или 18, и кодирует белок, обладающий активностью пептидообразующего фермента для катализа реакции, в которой дипептид образуется из эфира L-аминокислоты и L-аминокислоты.
Для получения трансформантов, которые экспрессируют белок, обладающий пептидообразующей активностью вышеуказанных (AA) - (CC), ДНК по (i), (ii), (iii) или (iv), указанная выше в разделе [II-1], может быть введена в клетки-хозяева. А именно, ДНК по (i), (ii), (iii) или (iv) вводят в рекомбинантную ДНК, и более конкретно в вектор экспрессии, способный экспрессироваться в клетках-хозяевах, с последующим введением данного вектора экспрессии в клетки-хозяева.
Кроме того, варианты, подобные указанному выше в (BB), получают модификацией последовательности оснований, так что замещают, удаляют, вставляют или добавляют аминокислоту в конкретном сайте гена фермента, например, методом сайт-направленного мутагенеза. Дополнительно, указанная выше модифицированная ДНК также может быть получена обычной мутагенной обработкой. Примеры мутагенной обработки включают способ, в котором ДНК, кодирующую фермент настоящего изобретения, обрабатывают in vitro гидроксиламином и так далее, и способ, в котором Escherichia coli, содержащую ДНК, кодирующую фермент настоящего изобретения, обрабатывают ультрафиолетовым облучением или N-метил-N'-нитро-N-нитрозогуанидином (NTG), азотистой кислотой или другим мутагеном, обычно используемым для искусственного мутагенеза.
В случае производства белка в большом количестве с использованием технологии рекомбинантной ДНК предпочтительным способом осуществления настоящего изобретения является способ конъюгации белка в трансформанте, который продуцирует белок, с образованием тела включения белка. Преимущества такого способа экспрессии и продуцирования включают защиту целевого белка от расщепления протеазами, присутствующими в клетках микроорганизмов, и простую очистку целевого белка разрушением клеток микроорганизмов с последующим центрифугированием.
Полученные таким образом тела включения белка солюбилизируют с помощью денатуирующего белок агента и затем преобразовывают в правильно уложенный, физиологически активный белок после процедуры регенерации активности, состоящей в первую очередь из удаления денатурирующего агента. Этому имеется множество примеров, включая регенерацию активности интерлейкина-2 человека (Выложенная публикация заявки на патент Японии No. S61-257931) и так далее.
Для получения активного белка из тел включения белка необходимо провести ряд операций, включая солюбилизацию и регенерацию активности, и способ является более сложным, чем в случае непосредственного продуцирования активного белка. Однако в случае продуцирования в клетках микроорганизмов большого количества белка, который оказывает нежелательное влияние на рост микроорганизмов, такое действие можно подавить путем аккумулирования белка в виде тел включения белка, которые являются неактивными в клетках микроорганизмов.
Примеры способов продуцирования целевого белка в большом количестве в виде тел включения включают способ, в котором целевой белок экспрессируют сам по себе под контролем мощного промотора, и способ, в котором целевой белок экспрессируют в виде слитого белка вместе с белком, о высокой экспрессии которого уже известно.
Кроме того, эффективным является расположение последовательности узнавания для узнавания рестрикционной протеазы в подходящем сайте для отщепления целевого белка после экспрессии в виде белка слияния.
В случае производства белка в большом количестве с использованием технологии рекомбинантной ДНК примеры клеток-хозяев, которые могут использоваться, включают бактериальные клетки, клетки Actinomyces, дрожжевые клетки, клетки плесневых грибов, клетки растений и клетки животных; обычно используют клетки кишечных бактерий, таких как Escherichia coli, при этом предпочтительно используются Escherichia coli. Это связано с тем, что имеется множество доступных сведений, касающихся способов получения белка в большом количестве с использованием Escherichia coli. Далее будет описан один вариант способа получения пептидообразующегося фермента с использованием трансформированных Escherichia coli.
Промоторы, обычно используемые при продуцировании гетерогенного белка в Escherichia coli, можно использовать в качестве промотора для экспрессирования ДНК, кодирующей пептидообразующий фермент, примеры которых включают сильные промоторы, такие как Т7-промотор, lac-промотор, trp-промотор, trc-промотор, tac-промотор, PR-промотор и PL-промотор лямбда-фага.
Для получения пептидообразующего фермента в виде тел включения слитого белка, ген, который кодирует другой белок, предпочтительно гидрофильный пептид, лигируют «слева» или «справа» от гена пептидообразующего фермента для получения гена слитого белка. Ген, который таким образом кодирует другой белок, может представлять собой любой ген, который увеличивает количество аккумулированного слитого белка и повышает растворимость слитого белка после стадий денатурирования и регенерирования. Кандидаты представляют собой, например, T7-ген 10, ген β-галактозидазы, ген редуктазы дегидрофолевой кислоты, ген γ-интерферона, ген интерлейкина-2 и ген прохимозина.
При лигировании данных генов с геном, кодирующим пептидообразующий фермент, рамки считывания кодонов делают совместимыми друг с другом. Их можно лигировать в подходящем сайте рестриктазы или можно использовать синтетическую ДНК с подходящей последовательностью.
Кроме того, для повышения продуцируемого количества является предпочтительным в некоторых случаях лигировать терминатор, который представляет собой терминирующую транскрипцию последовательность «правее» гена слитого белка. Примеры такого терминатора включают T7-терминатор, фаговый fd-терминатор, T4-терминатор, терминатор гена устойчивости к тетрациклину и терминатор гена trpA Escherichia coli.
В качестве вектора для введения в Escherichia coli гена, который кодирует пептидообразующий фермент или слитый белок, состоящий из пептидообразующего фермента и другого белка, являются предпочтительными так называемые векторы многокопийного типа, примеры которых включают плазмиды, имеющие репликатор, полученный из ColE1, такие как плазмида pUC, плазмида pBR322 или их производные. Термин «производное», как он использован в данном описании, относится к тем плазмидам, которые были подвергнуты модификации плазмиды путем замещения основания, удаления, вставки, добавления или изменения порядка оснований. Следует отметить, что упоминаемая в данном описании модификация включает модификацию в результате мутагенной обработки с использованием мутагена или УФ-облучения, или спонтанную мутацию. Более конкретно, примеры векторов, которые можно использовать, включают pUC19, pUC18, pBR322, pHSG299, pHSG298, pHSG399, pHSG398, RSF1010, pMW119, pMW118, pMW219 и pMW218. Помимо этого также можно использовать ДНК-фаги или ДНК-транспозоны.
Дополнительно, вектор предпочтительно имеет маркер, такой как ген устойчивости к ампициллину, для отбора трансформанта. Векторы экспрессии, имеющие сильные промоторы, являются коммерчески доступными для применения в качестве таких плазмид (такие как вектор pUC (производимый Takara Shuzo), вектор pPROK (производимый Clontech) и pKK233-2 (производимый Clontech) и другие).
Рекомбинантную ДНК получают лигированием фрагмента ДНК, включающего в указанном порядке промотор, ген, кодирующий пептидообразующий фермент, или слитый белок, состоящий из пептидообразующего фермента и другого белка, и, в зависимости от случая, терминатор, с ДНК вектора.
Когда Escherichia coli трансформируют с использованием рекомбинантной ДНК и полученную Escherichia coli культивируют, экспрессируется и продуцируется пептидообразующий фермент или слитый белок, состоящий из пептидообразующего фермента и другого белка. Хотя можно использовать штамм трансформированного хозяина, который обычно используется при экспрессии гетерогенного гена, штамм JM109 Escherichia coli является предпочтительным. Способы проведения трансформации и способы отбора трансформантов описаны в Molecular Cloning, 2nd Edition, Cold Spring Harbor Press (1989) и других публикациях.
В случае экспрессирования белка в виде слитого белка, слитый белок может быть получен таким образом, что пептидообразующий фермент может быть отщеплен с использованием рестрикционной протеазы, которая распознает последовательность, не присутствующую в пептидообразующем ферменте в виде последовательности распознавания, например, фактор Ха свертывания крови или калликреин.
Среда, обычно используемая для культивирования Escherichia coli, такая как среда с касаминокислотами М9 или среда LB, может использоваться в качестве среды для продуцирования. Кроме того, условия культивирования и условия индукции продуцирования выбирают подходящим образом в соответствии с маркером используемого вектора, промотором, типом микроорганизма-хозяина и так далее.
Следующий способ можно использовать для выделения пептидообразующего фермента или слитого белка, состоящего из пептидообразующего фермента и другого белка. Если пептидообразующий фермент или его слитый белок находятся в клетках микроорганизмов в солюбилизированном состоянии, то клетки микроорганизмов извлекают и затем разрушают или лизируют так, что они могут использоваться в качестве раствора неочищенного фермента. Кроме того, пептидообразующий фермент или его слитый белок при необходимости могут быть очищены перед применением обычными способами, такими как осаждение, фильтрование или колоночная хроматография. В таком случае также можно использовать способ очистки с применением антитела к пептидообразующему ферменту или его гибридному белку.
В том случае, когда образуются тела включения белка, данные тела включения солюбилизируют с помощью денатурирующего агента. Хотя их можно солюбилизировать вместе с белком клеток микроорганизмов, при рассмотрении следующей процедуры очистки тела включения предпочтительно выделяют и затем солюбилизируют. Для выделения тел включения клеток микроорганизмов можно использовать обычные известные способы. Например, тела включения могут быть выделены путем разрушения микробных клеток с последующим центрифугированием. Примеры денатурирующих агентов, способных солюбилизировать тела включения, включают гидрохлорид гуанидина (например, 6 M, pH от 5 до 8) и мочевину (например, 8 M).
Обладающий активностью белок регенерируют удалением таких денатурирующих агентов диализом. В качестве раствора для диализа, используемого при диализе, следует использовать Tris-HCl буферный раствор или фосфатный буферный раствор и тому подобные, в концентрации, например, от 20 мМ до 0,5 мМ, тогда как рН может составлять, например, от 5 до 8.
Концентрация белка во время стадии регенерации предпочтительно поддерживается на уровне примерно 500 мкг/мл или менее. Температура диализа предпочтительно составляет 5°C или ниже для ингибирования спонтанного образования поперечной связи в молекуле регенерированного пептидообразующего фермента. Кроме того, для удаления денатурирующих агентов в дополнение к диализу можно использовать разбавление или ультрафильтрацию, и можно ожидать, что ферментативная активность будет восстанавливаться вне зависимости от того, какой денатурирующий агент использовался.
В случае использования ДНК, указанной в SEQ ID NO: 4 списка последовательностей для ДНК, которая кодирует пептидообразующий фермент, продуцируется пептидообразующий фермент, который имеет аминокислотную последовательность, представленную в SEQ ID NO: 5. Кроме того, в случае использования ДНК, указанной в SEQ ID NO: 14 списка последовательностей в качестве ДНК, которая кодирует пептидообразующий фермент, продуцируется пептидообразующий фермент, который имеет аминокислотную последовательность, представленную в SEQ ID NO: 15. Кроме того, в случае использования ДНК, указанной в SEQ ID NO: 16 списка последовательностей в качестве ДНК, которая кодирует пептидообразующий фермент, продуцируется пептидообразующий фермент, который имеет аминокислотную последовательность, представленную в SEQ ID NO: 17.
Следует отметить, что методики генной инженерии можно осуществлять в соответствии со способами, описанными в литературе, например, Molecular Cloning, 2nd edition, Cold Spring Harbor Press (1989).
[III] Свойства пептидообразующего фермента
Далее приведены свойства пептидообразующего фермента, очищенного из штамма ATCC 13286 Corynebacterium glutamicum в качестве примера вышеуказанных микроорганизмов.
Взяв в качестве примера использование эфира L-аланина и L-глутамина в качестве исходных веществ (субстратов), данный пептидообразующий фермент обладает активностью продуцирования L-аланил-L-глутамина с использованием эфира L-аланина и L-глутамина в качестве субстратов. Дополнительно, взяв в качестве примера использование эфира L-аланина и L-аспарагина в качестве исходных веществ, данный пептидообразующий фермент обладает активностью продуцирования L-аланил-L-аспарагина с использованием эфира L-аланина и L-аспарагина в качестве субстратов.
Что касается действия фермента, взяв в качестве примера использование эфира L-аланина и L-аспарагина или L-глутамина в качестве исходных веществ, данный пептидообразующий фермент продуцирует одну молекулу L-аланил-L-глутамина и одну молекулу спирта из одной молекулы эфира L-аланина и одной молекулы L-глутамина, и продуцирует одну молекулу L-аланил-L-аспарагина и одну молекулу спирта из одной молекулы эфира L-аланина и одной молекулы аспарагина.
Оптимальное значение рН располагается в области 6,0-10,0, а оптимальная температура находится в области от 30 до 50°C. Рассчитано, что молекулярная масса субъединицы составляет от 42000 до 46000, как определено с помощью электрофореза в SDS-полиакриламидном геле.
[IV] Способ получения дипептида
В способе получения дипептида по настоящему изобретению дипептид получают из эфира L-аминокислоты и L-аминокислоты с использованием фермента или ферментсодержащего вещества, обладающего способностью синтезировать дипептид, и, более конкретно, дипептид получают из эфира L-аминокислоты и L-аминокислоты с использованием пептидообразующего фермента, полученного из культуры микроорганизмов, клеток микроорганизмов, выделенных из культуры, или продукта обработанных клеток микроорганизма, обладающего способностью продуцировать дипептид из эфира L-аминокислоты и L-аминокислоты. Следует отметить, что белок, обладающий пролиниминопептидазной активностью, полученный из указанных выше микроорганизмов или микроорганизмов, перечисленных в таблице 1, также можно использовать, поскольку они обладают продуцирующей дипептид из эфира L-аминокислоты и L-аминокислоты активностью.
Пептидообразующий фермент, продуцируемый вышеуказанными микроорганизмами, обладает активностью продуцирования дипептида при использовании в качестве субстратов эфира L-аминокислоты и L-аминокислоты.
В качестве способа, в соответствии с которым пептидообразующему ферменту, продуцируемому вышеуказанными микроорганизмами, дают возможность взаимодействовать с эфиром L-аминокислоты и L-аминокислотой, субстраты могут быть непосредственно добавлены в культуральную жидкость при культивировании вышеуказанных микроорганизмов, или клетки микроорганизмов могут быть отделены от микробной культуры центрифугированием и так далее, с последующим ресуспендированием в буфере, непосредственно или после промывки, а затем к ним добавляют эфир L-аминокислоты и L-аминокислоту и дают им возможность взаимодействовать. Альтернативно, можно использовать микробные клетки, которые иммобилизованы известными способами с использованием полиакриламидного геля, каррагена или геля из альгиновой кислоты.
Кроме того, разрушенные клетки микроорганизмов, обработанные ацетоном клетки микроорганизмов или лиофилизированные клетки микроорганизмов могут быть использованы в качестве продукта обработанных клеток микроорганизмов. Для разрушения клеток микроорганизмов можно использовать такие способы, как разрушение ультразвуком, разрушение с использованием пресса Френча или разрушение с помощью стеклянных шариков, тогда как в случае, когда проводят лизис клеток микроорганизмов, используют способы с применением лизозима яичного белка, обработки пептидазой или их подходящей комбинации.
Кроме того, пептидообразующий фермент может быть выделен из продукта обработанных клеток микроорганизмов и использован в виде раствора неочищенного фермента, или фермент может быть очищен перед применением при необходимости. Для очистки фермента, получаемого из культуры, можно использовать обычные способы очистки ферментов. Более конкретно, клетки микроорганизмов собирают центрифугированием и так далее, клетки затем разрушают механическими способами, такими как ультразвуковая обработка, стеклянные шарики или диноизмельчитель, и твердые материалы, такие как клеточные фрагменты, удаляют центрифугированием для получения неочищенного фермента с последующей очисткой вышеуказанного пептидообразующего фермента путем проведения фракционирования с использованием ультрацентрифугирования, высаливания, осаждения органическими растворителями, ионообменной хроматографии, адсорбционной хроматографии, гель-фильтрации, гидрофобной хроматографии и так далее.
Следует отметить, что «пептидообразующий фермент, полученный из микроорганизма», включает не только фермент, полученный из продукта обработанных клеток микроорганизма с помощью упомянутой выше стадии очистки, но также и фермент, получаемый так называемыми методами генной инженерии, в которых ген фермента экспрессируют в гетерогенном или гомогенном хозяине.
А именно, в случае фракции, обладающей активностью продуцирования дипептида из эфира L-аминокислоты и L-аминокислоты, можно использовать фермент целиком или ферментсодержащий материал. В данном описании термин «ферментсодержащий материал» относится к материалу, который содержит фермент и включает специфические формы, такие как культура микроорганизмов, которые продуцируют фермент, клетки микроорганизмов, отделенные от культуры, и продукты обработанных клеток микроорганизмов. Термин «культура микроорганизмов» относится к культуре, которую получают при культивировании микроорганизмов, и более конкретно, относится к смеси клеток микроорганизма, среде, используемой для культивирования микроорганизмов, и веществам, продуцируемым культивируемыми микроорганизмами. Кроме того, клетки микроорганизма могут быть отмыты и использованы в виде отмытых клеток микроорганизма. Продукт обработанных клеток микроорганизма включает клетки, которые были разрушены, лизированы или лиофилизированы и, кроме того, неочищенный фермент, выделенный обработкой клеток и так далее, а также очищенный фермент, полученный при его очистке. Частично очищенные ферменты и так далее, полученные различными способами очистки, также могут использоваться в качестве очищенных ферментов, или можно использовать иммобилизованный фермент, который иммобилизован путем ковалентного связывания, адсорбции или методами захвата. Кроме того, поскольку некоторые микроорганизмы подвергаются частичному лизированию уже во время культивирования в зависимости от используемых микроорганизмов, в таких случаях также можно использовать культуральный супернатант в качестве ферментсодержащего материала.
Следует отметить, что при использовании культуры, культивированных клеток микроорганизмов, отмытых клеток микроорганизмов или обработанных микробных клеток, в которых клетки были разрушены или лизированы, имеется множество случаев, когда в материале присутствует фермент, который не принимает участия в образовании пептидов, а напротив разрушает продуцированный пептид, и среди таких случаев имеются случаи, когда предпочтительным является добавление ингибитора металлофермента, такого как ингибитор металлопротеазы, например, этилендиаминотетрауксусная кислота (EDTA). Добавляемое количество находится в диапазоне от 0,1 мМ до 100 мМ, и предпочтительно составляет от 1 мМ до 50 мМ.
Используемое количество фермента или ферментсодержащего материала может быть достаточным, если оно представляет собой количество, при котором проявляется целевое действие (эффективное количество). Такое эффективное количество легко может быть определено с помощью простого предварительного эксперимента, проводимого обычным специалистом в данной области, например, при использовании отмытых клеток используемое количество составляет от 1 до 500 г/л реакционной смеси.
Можно использовать любой эфир L-аминокислоты при условии, что он вместе с L-аминокислотой может образовывать дипептид в соответствии с субстратной специфичностью пептидообразующего фермента, и примеры таких эфиров включают метиловые эфиры, этиловые эфиры, н-пропиловые эфиры, изопропиловые эфиры, н-бутиловые эфиры, изобутиловые эфиры и трет-бутиловые эфиры L-аминокислот. Кроме того, можно использовать не только эфиры L-аминокислот, соответствующие встречающимся в природе аминокислотам, но и эфиры L-аминокислот, соответствующие не существующим в природе аминокислотам или их производным. Примеры эфиров L-аминокислот, которые предпочтительно можно использовать в настоящем изобретении, включают эфир L-аланина, эфир глицина, эфир L-валина, эфир L-изолейцина, эфир L-метионина, эфир L-фенилаланина, эфир L-серина, эфир L-треонина, эфир L-глутамина, эфир L-тирозина, эфир L-аргинина, α-эфир L-аспарагиновой кислоты, β-эфир L-аспарагиновой кислоты, эфир L-лейцина, эфир L-аспарагина, эфир L-лизина, α,β-диметиловый эфир L-аспарагиновой кислоты и γ-эфир L-глутамина.
Не имеется особенного ограничения для L-аминокислоты и можно использовать любую L-аминокислоту, если она дает дипептид с эфиром L-аминокислоты в соответствии с субстратной специфичностью пептидообразующего фермента. Примеры L-аминокислот, которые предпочтительно можно использовать в настоящем изобретении, включают L-глутамин, L-аспарагин, глицин, L-аланин, L-лейцин, L-метионин, L-пролин, L-фенилаланин, L-триптофан, L-серин, L-треонин, L-тирозин, L-лизин, L-аргинин, L-гистидин и L-глутаминовую кислоту, где L-глутамин и L-аспарагин являются особенно предпочтительными.
Концентрация каждого из эфира L-аминокислоты и L-аминокислоты, используемых в качестве исходных соединений, составляет от 1 мМ до 10 M, и предпочтительно составляет от 0,05 M до 2 M. Однако есть случаи, в которых предпочтительно добавление эквимолярного количества или больше L-аминокислоты относительно количества эфира L-аминокислоты. Кроме того, в том случае, когда высокая концентрация субстрата ингибирует реакцию, субстраты можно вносить последовательно после разбавления до концентрации, которая не оказывает на реакцию ингибирующее действие.
Температура реакции составляет от 3 до 70°C, и предпочтительно от 5 до 50°C, тогда как рН реакции составляет от 2 до 12, и предпочтительно от 3 до 11. При проведении реакции таким образом в течение от примерно 2 до 48 часов дипептид продуцируется и накапливается в реакционной смеси. Затем полученный дипептид может быть выделен с помощью обычных способов и при необходимости очищен.
Примеры
Далее настоящее изобретение будет подробно описано со ссылкой на приведенные ниже примеры. Однако настоящее изобретение не ограничивается данными примерами. Следует отметить, что в примерах количественное определение L-аланина, L-аланил-L-глутамина или L-аланил-L-аспарагина проводили методом высокоэффективной жидкостной хроматографии (колонка: Inertsil ODS-2 (GL Science), элюат: водный фосфатный раствор (pH 2,2, 5,0 мМ 1-октансульфоната натрия/метанол = 100/15), скорость потока: 1,0 мл/мин, детектирование: 210 нм).
Пример 1
Влияние добавления EDTA на продуцирование L-аланил-L-глутамина
50 мл среды (pH 7,0), содержащей 5 г глюкозы, 5 г сульфата аммония, 1 г первичного кислого фосфата калия, 3 г вторичного кислого фосфата калия, 0,5 г сульфата магния, 10 г дрожжевого экстракта и 10 г пептона на литр, переносили в колбу Сакагуши (Sakaguchi) емкостью 500 мл и стерилизовали в течение 15 минут при 115°C. Одну петлю микроорганизмов штамма FERM BP-8101 Pseudomonas putida, которые культивировали в течение 24 часов при 30°C на косяке из агаровой среды, имеющей тот же состав (агар: 20 г/л, рН 7,0), инокулировали в вышеуказанную среду и культивировали при встряхивании в течение 17 часов при 30°C и 120 движений/минуту. После завершения культивирования клетки микроорганизмов отделяли центрифугированием и суспендировали в 100 мМ боратном буфере (pH 9,0) до плотности 100 г сырых клеток/л. 1 мл каждой клеточной суспензии добавляли соответственно к 1 мл 100 мМ боратного буфера (pH 9,0), содержащего 200 мМ гидрохлорида этилового эфира L-аланина и 400 мМ L-глутамина без EDTA или дополнительно содержащего 20 мМ EDTA (раствор субстрата), с получением конечного объема 2 мл и последующим проведением реакции в течение 1 часа при 30°C. В результате 4,9 mM L-аланил-L-глутамина было получено в части без добавления EDTA и 10,1 мМ в части с добавлением EDTA.
Следует отметить, что в данной реакционной системе при условиях, где 1 мл 100 мМ боратного буфера (pH 9,0) добавляли вместо клеточной суспензии к 1 мл раствора субстрата (не содержащая клеток серия), и при условиях, где 1 мл 100 мМ боратного буфера, не содержащего EDTA или содержащего 20 мМ EDTA, но не содержащего гидрохлорида этилового эфира L-аланина и глутамина, добавляли к суспензии клеток (не содержащая субстрата серия), продуцирование L-аланил-L-глутамина не наблюдалось ни в одном из случаев.
Пример 2
Применение эфира аминокислоты в качестве субстрата
1 мл клеточной суспензии сырых клеток (100 г/л) штамма FERM BP-8101 Pseudomonas putida, полученной таким же образом, как описано в примере 1, соответственно добавляли к 1 мл 100 мМ боратного буфера (pH 9,0), содержащего 20 мМ EDTA и перечисленные гидрохлориды эфиров L-аланина в концентрации 200 мМ и L-глутамин в концентрации 400 мМ, с получением конечного объема 2 мл и последующим проведением реакции в течение 1 часа при 30°C. В результате при использовании гидрохлорида метилового эфира L-аланина и L-глутамина в качестве субстратов было получено 14,9 мМ L-аланил-L-глутамина, при использовании гидрохлорида этилового эфира L-аланина и L-глутамина в качестве субстратов было получено 11,4 мМ L-аланил-L-глутамина, и при использовании гидрохлорида трет-бутилового эфира L-аланина и L-глутамина в качестве субстратов было получено 0,5 мМ L-аланил-L-глутамина.
Пример 3
Применение L-аминокислоты в качестве субстрата
1 мл клеточной суспензии сырых клеток (100 г/л) штамма FERM BP-8101 Pseudomonas putida, полученной таким же образом, как описано в примере 1,добавляли соответственно к 1 мл 100 мМ боратного буфера (pH 9,0), содержащего 20 мМ EDTA, перечисленные далее гидрохлориды эфиров L-аланина в концентрации 200 мМ и L-глутамин или L-аспарагин в концентрации 400 мМ, с получением конечного объема 2 мл и последующим проведением реакции в течение 1 часа при 30°C. В результате при использовании гидрохлорида метилового эфира L-аланина и L-глутамина в качестве субстратов было получено 12,7 мМ L-аланил-L-глутамина и 4,8 мМ L-аланил-L-аспарагина было получено при использовании в качестве субстратов гидрохлорида метилового эфира L-аланина и L-аспарагина.
Пример 4
Продуцирование микроорганизмами L-аланил-L-глутамина
50 мл среды (pH 7,0), содержащей 5 г глюкозы, 5 г сульфата аммония, 1 г первичного кислого фосфата калия, 3 г вторичного кислого фосфата калия, 0,5 г сульфата магния, 10 г дрожжевого экстракта и 10 г пептона на 1 л, переносили в 500 мл колбу Сакагуши и стерилизовали в течение 15 минут при 115°C. Одну петлю каждой из бактерий, представленных в таблице 1, которые культивировали в течение 24 часов при 30°C на косяке из агаровой среды (агар: 2 г/л, рН 7,0), содержащей 5 г глюкозы, 10 г дрожжевого экстракта, 10 г пептона и 5 г NaCl, инокулировали в вышеуказанную среду и культивировали при встряхивании в течение 17 часов при 30°C и 120 движений/минуту. После завершения культивирования клетки микроорганизмов отделяли центрифугированием и суспендировали в 0,1 М боратном буфере (pH 9,0), содержащем 10 мМ EDTA, из расчета 100 г сырых микробных клеток/л. К 0,1 мл данных суспензий микробных клеток соответственно добавляли 0,1 мл 100 мМ боратного буфера (pH 9,0), содержащего 10 мМ EDTA, 200 мМ гидрохлорида метилового эфира L-аланина и 400 мМ L-глутамина, с получением конечного объема 0,2 мл и последующим проведением реакции в течение 2 часов при 25°C. Продуцированные за это время количества (мМ) L-аланил-L-глутамина (Ala-Gln) показаны в таблице 1.
Corynebacterium glutamicum ATCC 13286
Pseudomonas putida FERM BP-8101
7,2
14,8
Пример 5
Влияние температуры на продуцирование L-аланил-L-глутамина
1 мл суспензии клеток штамма FERM BP-8101 Pseudomonas putida (100 г/л), полученной в соответствии со способом культивирования микроорганизмов примера 4, соответственно добавляли к 1 мл 100 мМ боратного буфера (pH 9,0), содержащего 10 мМ EDTA, 200 мМ гидрохлорида метилового эфира L-аланина и 400 мМ L-глутамина, с получением конечного объема 2 мл и последующим проведением реакции в течение 1 часа при температуре 20°C, 30°C и 40°C соответственно. Полученные результаты представлены в таблице 2. В случае штамма FERM BP-8101 Pseudomonas putida наиболее высокое значение для продуцирования L-аланил-L-глутамина (Ala-Gln) было продемонстрировано при температуре 40°C.
Пример 6
Очистка пептидообразующего фермента из штамма ATCC 13286 Corynebacterium glutamicum и продуцирование L-аланил-L-глутамина с использованием очищенного фермента
500 мл среды, содержащей 5 г глицерина, 5 г дрожжевого экстракта, 5 г пептона, 5 г хлорида натрия и 5 г гидрохлорида амида L-аланина на 1 л, переносили в колбу Сакагуши объемом 5 л и стерилизовали в течение 20 минут при 120°C. Культуральную жидкость штамма ATCC 13286 Corynebacterium glutamicum, культивированного в течение 20 часов в среде с таким же составом, как описано выше, инокулировали в среду из расчета 5% (об/об) и культивировали в течение 20 часов при 30°C и 120 движений/минуту. Клетки микроорганизмов собирали из 8 л такой культуральной жидкости центрифугированием. Последующую процедуру проводили на льду или при 4°C. После промывания клеток микроорганизмов 50 мМ калий-фосфатным буфером (pH 7,0) клетки подвергали разрушению в течение примерно 10 минут с использованием стеклянных шариков, имеющих диаметр 0,1 миллиметр. Стеклянные шарики и суспензию разрушенных клеток затем разделяли, и фрагменты разрушенных клеток удаляли центрифугированием в течение 30 минут при 20000×g для получения не содержащего клеток экстракта. Кроме того, нерастворимую фракцию удаляли ультрацентрифугированием в течение 60 минут при 200000×g для получения растворимой фракции в виде супернатанта (надосадочной жидкости). Затем к полученной в результате растворимой фракции добавляли сульфат аммония до 60%-ного насыщения с последующим выделением осадка центрифугированием в течение 30 минут при 20000×g. Полученный в результате осадок растворяли в небольшом объеме 50 мМ калий-фосфатного буфера (pH 7,0) и затем подвергали диализу против 50 мМ калий-фосфатного буфера (pH 7,0). Затем данный раствор фермента наносили на ВЭ колонку с Q-сефарозой (Q-Sepharose), предварительно уравновешенную 50 мМ калий-фосфатным буфером (pH 7,0), и фермент элюировали линейным градиентом концентрации - 50 мМ калий-фосфатным буфером (pH 7,0), содержащим от 0 до 1,0 М хлорида натрия. Собирали активную фракцию и наносили на 200 пг колонку Superdex, предварительно уравновешенную 50 мМ калий-фосфатным буфером (pH 7,0), и затем фермент элюировали тем же буфером. Собирали активную фракцию и подвергали ее диализу против 20 мМ калий-фосфатного буфера (pH 7,0), содержащего 0,5 М сульфата аммония, и затем наносили на ВЭ колонку с фенил-сефарозой (Phenyl-Sepharose), предварительно уравновешенную 20 мМ калий-фосфатным буфером (рН 7,0), содержащим 0,5 М сульфата аммония. Затем фермент элюировали линейным градиентом концентрации - 20 мМ калий-фосфатным буфером (pH 7,0), содержащим от 0,5 до 0 М сульфата аммония. Собирали активную фракцию и подвергали диализу протиа 50 мМ калий-фосфатного буфера (pH 7,0), а затем наносили на колонку MonoQ, предварительно уравновешенную 50 мМ калий-фосфатным буфером (pH 7,0), после чего фермент элюировали линейным градиентом концентрации - 50 мМ калий-фосфатным буфером (pH 7,0), содержащим от 0 до 1,0 М хлорида натрия. Очищенный пептидообразующий фермент был очищен до однородности по данным электрофореза.
Специфическая активность очищенного фермента составляла 9,841 Е/мг, и специфическая активность очищенного пептидообразующего фермента увеличивалась примерно в 246 раз в результате прохождения через такие стадии очистки. Кроме того, в результате применения для молекулярной массы очищенного ферментативного стандарта в SDS-полиакриламидном электрофорезе обнаруживали однородную полосу в положении, рассчитанном как представляющее молекулярную массу от 42000 до 46000. Измерения титра фермента проводили так, как описано ниже. 200 мкМ Tris-HCl буфера (pH 9,0), 50 мкМ амида L-аланина и подходящее количество раствора фермента добавляли до конечного объема 1 мл, смешивали и после этого оставляли взаимодействовать на 60 минут при 30°C, для остановки реакции добавляли 4 мл водной фосфорной кислоты (pH 2,1). Количество полученного аланина оценивали с использованием высокоэффективной жидкостной хроматографии, и количество фермента, которое приводило к 1 мкМ L-аланина за 1 минуту, принимали за 1 единицу.
Данный очищенный фермент затем добавляли к боратному буферу (pH 9,0), содержащему EDTA, гидрохлорид метилового эфира L-аланина и L-глутамин (или L-аспарагин), смешивали до общего объема 1 мл (для конечных концентраций, количество добавленного фермента составляло 2 единицы активности разложения амида аланина, концентрация EDTA составляла 10 мМ, концентрация гидрохлорида метилового эфира L-аланина составляла 100 мМ и концентрация L-глутамина (или L-аспарагина) составляла 200 мМ, боратного буфера - 100 мМ) и оставляли взаимодействовать на 4 часа при 30°C. (Следует отметить, что число единиц активности фермента не указывает на активность продуцирования, касающуюся продуцирования L-аланил-L-глутамина из метилового эфира L-аланина и L-глутамина, и просто указывает на активность разложения амида L-аланина.) Количество L-аланил-L-глутамина, полученное за это время, составило 50,2 мМ, тогда как полученное количество L-аланил-L-аспарагина составило 49,8 мМ.
Пример 7
Выделение гена пептидообразующего фермента из штамма ATCC 13286 Corynebacterium glutamicum и экспрессия в Escherichia coli
Далее будет описано выделение гена пептидообразующего фермента из штамма ATCC 13286 Corynebacterium glutamicum и его экспрессия в Escherichia coli (Escherichia coli). В качестве хозяина использовали Escherichia coli JM109, и pUC18 использовали в качестве вектора как для выделения, так и для экспрессии гена.
1. Получение ПЦР-праймера на основе определенной аминокислотной последовательности
Смешанные праймеры, указанные в SEQ ID NO: 2 и SEQ ID NO: 3 соответственно, получали на основе N-концевой аминокислотной последовательности пептидообразующего фермента, полученного из штамма ATCC 13286 Corynebacterium glutamicum (SEQ ID NO:1), полученного в примере 1.
2. Накопление микроорганизма
Микроорганизмы штамма ATCC 13286 Corynebacterium glutamicum высевали и культивировалив течение 24 часов при 30°C на CM2Gly-агаровой среде (0,5 г/дл глицерина, 1,0 г/дл дрожжевого экстракта, 1,0 г/дл пептона, 0,5 г/дл NaCl, 2 г/дл агара, pH 7,0). Затем одну петлю клеток инокулировали в колбу Сакагуши емкостью 500 мл, содержащую 50 мл жидкой среды CM2Gly с последующим культивированием при встряхивании в течение 16 часов при 30°C в аэробных условиях.
3. Получение хромосомной ДНК из клеток микроорганизмов
50 мл культуральной среды центрифугировали (12000 оборотов в минуту, 4°C, 15 минут) для сбора клеток микроорганизмов. Данные клетки микроорганизмов затем суспендировали в 10 мл 50 мМ Tris-HCl буфера (pH 8,0), содержащего 20 мМ EDTA, с последующим выделением клеток микроорганизмов центрифугированием. Клетки микроорганизмов опять суспендировали 10 мл 50 мМ Tris-HCl буфера (pH 8,0), содержащего 20 мМ EDTA. Кроме того, после добавления к этой суспензии 0,5 мл 20 мг/мл раствора лизозима и 1 мл 10% раствора SDS (додецилсульфат натрия) смесь инкубировали в течение 20 минут при 55°C. Данную проинкубированную смесь затем депротеинизировали добавлением эквимолярного количества фенола, насыщенного 10 мМ Tris-HCl буфером (рН 8,0), содержащим 1 мМ EDTA. К отделенному водному слою добавляли эквимолярное количество 2-пропанола для осаждения ДНК с последующим выделением осажденной ДНК. После растворения осажденной ДНК в 0,5 мл 50 мМ Tris-HCl буфера (pH 8,0), содержащего 20 мМ EDTA, добавляли 5 мкл 10 мг/мл РНКазы и 5 мкл 10 мг/мл протеинкиназы K и оставляли взаимодействовать в течение 2 часов при 55°C. После завершения реакции раствор депротеинизировали добавлением равного объема фенола, насыщенного 10 мМ Tris-HCl буфером (рН 8,0), содержащим 1 мм EDTA. Кроме того, к отделенному водному слою добавляли равный объем смеси в соотношении 24:1 хлороформ/изоамиловый спирт с последующим перемешиванием и отделением водного слоя. После того как данную процедуру осуществляли два раза, к полученному в результате водному слою добавляли 3М раствор ацетата натрия (рН 5,2) для получения конечной концентрации 0,4М, с последующим добавлением 2 объемов этанола. Полученную в виде осадка ДНК выделяли и после промывки 70% этанолом сушили и растворяли в 1 мл 10 мМ Tris-HCl буфера (pH 8,0), содержащего 1 мМ EDTA.
4. Получение ДНК-фрагмента, содержащего частичный ген пептидообразующего фермента, кассетной ПЦР.
Набор для клонирования TaKaRa LA PCR in vitro (производимый Takara Shuzo) использовали для выделения и амплификации молекул ДНК, содержащих ген (aah), кодирующий пептидообразующий фермент с использованием кассетного ПЦР-способа. Если не указано другого, эксперимент проводили на основе способа, описанного в руководстве. В кассетном ПЦР-способе при использовании праймера 1 (1-й ПЦР, SEQ ID NO: 2) и праймера 2 (2-й ПЦР, SEQ ID NO: 3) в качестве праймеров полосу в приблизительно 0,5 тысяч пар нуклеотидов (фрагмент 1) амплифицировали с помощью Eco RI-кассеты. В результате определения последовательности оснований данного фрагмента было подтверждено, что фрагмент 1 является частью aah.
5. Клонирование гена пептидообразующего фермента из библиотеки генов
Затем для получения полноразмерного aah первоначально проводили гибридизацию по Саузерну с использованием фрагмента 1 в качестве зонда.
ДНК-фрагмент, который служил в качестве зонда, растворяли с получением концентрации примерно 50 нг/мкл, и зонд метили инкубированием 16 мкл данного раствора ДНК в течение 24 часов при 37°C в соответствии с протоколом с использованием DIG High Prime (Boehringer Mannheim).
1 мкг хромосомной ДНК полностью расщепляли с использованием комбинации различных ферментов рестрикции и затем подвергали электрофорезу на 0,8% агарозном геле. Затем полученное блоттировали на положительно заряженные нейлоновые мембраны (Boehringer Mannheim, положительно заряженные нейлоновые мембраны). Гибридизацию по Саузерну проводили в соответствии со следующим разработанным способом. Гибридизацию проводили с использованием DIG Easy Hyb (Boehringer Mannheim) и после гибридизации в течение 30 минут при 50°C добавляли зонд с последующей гибридизацией в течение 18 часов при 50°C. Обнаружение проводили с использованием набора для обнаружения DIG Nucleotide Detection Kit (Boehringer Mannheim).
В результате была обнаружена полоса примерно в положении 7 тысяч пар оснований (т.п.о.) в продукте расщепления BglII. Фрагмент размером 7 т.п.н. собирали и лигировали с pUC18 для получения библиотеки (120 штаммов) в Escherichia coli JM109. Затем проводили гибридизацию колоний в соответствии со следующим разработанным способом. Колонии переносили на найловые мембраны для гибридизации колоний и бляшек (Boehringer Mannheim) с последующим щелочным денатурированием, нейтрализаций и иммобилизационной обработкой. Гибридизацию проводили с использованием DIG Easy Hyb. Фильтр погружали в буфер и предварительно гибридизировали в течение 30 минут при 42°C. Впоследствии добавляли вышеуказанный меченый зонд с последующей гибридизацией в течение 18 часов при 42°C. После промывки SSC-буфером был отобран один положительный клон с использованием набора для нуклеотидного обнаружения DIG Nucleotide Detection Kit.
6. Последовательность оснований гена пептидообразующего фермента, полученного из штамма ATCC 13286 Corynebacterium glutamicum
Плазмиды, удерживаемые отобранным трансформантом, получали в соответствии со способом, описанным в Molecular Cloning, 2nd edition, Cold Spring Harbor Press (1989), и определяли последовательность оснований в окрестности последовательности, которая гибридизовалась с зондом. Присутствовала открытая рамка считывания (ORF), которая кодирует белок, содержащий 30 остатков N-концевой аминокислотной последовательности пептидообразующего фермента, и подтверждали, что она является геном aah, который кодирует пептидообразующий фермент. Последовательность оснований полноразмерного гена пептидообразующего фермента показана в SEQ ID NO: 4 списка последовательностей. Полученная ORF проявляет 57,6% гомологичность последовательности оснований с известной пролиниминопептидазой, полученной из бактерий видов Propionibacterium. Следует отметить, что цифровое значение гомологичности представляет собой значение, полученное с помощью Genetyx (ниже то же самое применяется для данного примера).
7. Экспрессия гена пептидообразующего фермента в Escherichia coli
Плазмиду pUCAAH, содержащую aah ниже lac-промотора pUC18, конструировали для экспрессии aah в Escherichia coli. Фрагменты, амплифицированные с помощью ПЦР с использованием хромосомной ДНК штамма ATCC 13286 Corynebacterium glutamicum в качестве матрицы и олигонуклеотидов, показанных в таблице 3 в качестве праймеров, обрабатывали SacI и SmaI, и после лигирования с расщепленной SacI и SmaI pUC18 использовали для трансформации Escherichia coli JM109. Штаммы, имеющие целевую плазмиду, отбирали из ампициллин-устойчивых штаммов и сконструированную плазмиду экспрессии обозначили как pUCAAH.
Праймеры, использованные для конструирования вектора экспрессии пептидообразующего фермента
SacI SEQ ID NO: 6
SmaI SEQ ID NO: 7
Трансформант, экспрессирующий пептидообразующий фермент, - Escherichia coli, содержащую pUCAAH, предварительно культивировали в течение 16 часов при 37°C в среде LB, содержащей 0,1 мг/мл ампициллина. 1 мл такого предварительно прокультивированного бульона высевали в колбу Сакагуши емкостью 500 мл, содержащую 50 мл среды LB, с последующим окончательным культивированием при 37°C. Через 2 часа от начала культивирования добавляли изопропил-1-тио-β-D-галактопиранозид (IPTG) до конечной концентрации 1 мМ с последующим дополнительным культивированием в течение 3 часов.
После завершения культивирования микроорганизмы собирали и промывали, суспендировали в 10 мл 20 мМ фосфатного буфера (pH 8,0) и затем подвергали ультразвуковому разрушению в течение 30 минут при 180 Вт. Собирали раствор и центрифугировали в течение 10 минут при 12000g×10 минут, и полученный супернатант использовали в качестве не содержащего клеток экстракта.
Пример 8
Измерение активности пептидообразующего фермента
1. Активность фермента, полученного из штамма ATCC 13286 Corynebacterium glutamicum
После завершения культивирования описанным выше способом получали не содержащий клеток экстракт и измеряли активность пептидообразующего фермента с использованием его в качестве источника фермента. Измерение пептидообразующей ферментативной активности проводили инкубированием реакционной смеси, содержащей 100 мМ гидрохлорида метилового эфира L-аланина, 150 мМ L-глутамина, 100 мМ боратного буфера (pH 9,0), 10 мМ EDTA и раствора фермента, в течение 60 минут при 30°C, с последующей остановкой реакции добавлением 4-кратного объема фосфорной кислоты (pH 1,5). Количество L-аланил-L-глутамина определяли с помощью ВЭЖХ. Для выражения ферментативной активности в единицах за 1 единицу (Е) принимали ферментативную активность, дающую 1 мкмоль L-аланил-L-глутамина в 1 минуту при данных условиях.
Условия ВЭЖХ, использованные для проведения анализа, были следующими:
Колонка: Inertsil ODS-2
Подвижная фаза: (водный раствор фосфорной кислоты (pH 2,1)), 2,5 мМ 1-октансульфонат натрия/метанол = 10/1
Температура колонки: 40°C
Скорость потока: 1,0 мл/минута
Обнаружение: УФ 210 нанометров
В результате, в случае введения pUC18 AAH была выявлена активность 0,54 Е/мг синтеза L-аланил-L-глутамина из гидрохлорида метилового эфира L-аланина, что подтверждает, что клонированный aah-ген экспрессировался в Escherichia coli. Следует отметить, что активности не обнаруживалось при введении в качестве контроля только pUC18.
2. Экспрессия гена His-Tag пептидообразующего фермента в Escherichia coli
Конструировали плазмиду pQEAAH, которая экспрессирует ген пептидообразующего фермента в виде His-Tag-белка, находящийся ниже lac-промотора pUC18, для экспрессии aah в Escherichia coli. Фрагменты, амплифицированные с помощью ПЦР с использованием хромосомной ДНК штамма ATCC 13286 Corynebacterium glutamicum в качестве матрицы и олигонуклеотидов, показанных в таблице 4, в качестве праймеров, обрабатывали SacI и SmaI, и после лигирования с расщепленной SacI и SmaI плазмидой pQE-30 (Qiagen) использовали для трансформации Escherichia coli JM109. Штаммы, содержащие целевую плазмиду, отбирали из ампициллин-устойчивых штаммов, и сконструированную плазмиду экспрессии обозначили pQEAAH.
Праймеры, использованные для конструирования вектора экспрессии His-Tag-пептидообразующего фермента
SacI SEQ ID NO: 8
SmaI SEQ ID NO: 7
Когда активность трансформанта, экспрессирующего пептидообразующий фермент, - Escherichia coli, содержащей pQEAAH, измеряли с использованием такого же способа, как в примере 8, было установлено, что он проявляет пептидообразующую ферментативную активность, составляющую 5,28 Е/мг.
3. Получение очищенного His-Tag-фермента
Клетки микроорганизмов из 150 мл культурального бульона Escherichia coli JM109, содержащей pQEAAH, разрушали с использованием вышеуказанного способа и His-Tag-гидролазу амида L-аланина очищали с использованием His Trap набора (производимого Amersham Pharmacia Biotech) в соответствии с протоколом, прилагаемым к набору. Получали 24 мг белка, который мигрировал в виде единственной полосы при SDS-PAGE, и специфическая активность синтеза L-аланил-L-глутамина из гидрохлорида метилового эфира L-аланина составляла 148,3 Е/мг и 50,7% из расчета на гидрохлорид метилового эфира L-аланина.
4. Исследование субстратной специфичности с использованием очищенного His-Tag-фермента
Синтез пептидов, отличающихся от L-аланил-L-глутамина, с помощью полученного пептидобразующего фермента исследовали использованием очищенного His-Tag-фермента.
(1) Пептидный синтез из метилового эфира L-аланина и других L-аминокислот
Реакцию синтеза осуществляли инкубированием реакционной смеси, содержащей 100 мМ гидрохлорида метилового эфира L-аланина, 150 мМ исследуемой аминокислоты, 100 мМ боратного буфера (pH 9,0), 10 мМ EDTA и раствора фермента (0,05 Е/мл), в течение 3 часов при 25°C с последующим определением количества полученных пептидов с помощью ВЭЖХ. В результате при использовании в качестве другой аминокислоты L-аспарагина было получено 22,34 мМ L-аланил-L-аспарагина, при использовании глицина было получено 5,66 мМ L-аланил-глицина, при использовании L-аланина было получено 10,63 мМ L-аланил-L-аланина, при использовании L-лейцина было получено 13,73 мМ L-аланил-L-лейцина, при использовании L-метионина было получено 48,80 мМ L-аланил-L-метионина, при использовании L-пролина получено 1,02 мМ L-аланил-L-пролина, при использовании L-фенилаланина было получено 16,13 мМ L-аланил-L-фенилаланина, при использовании L-триптофана было получено 15,31 мМ L-аланил-L-триптофана, при использовании L-серина было получено 26,14 мМ L-аланил-L-серина, при использовании L-треонина было получено 24,23 мМ L-аланил-L-треонина, при использовании L-тирозина было получено 0,96 мМ L-аланил-L-тирозина, при использовании L-лизина было получено 7,91 мМ L-аланил-L-лизина, при использовании L-аргинина было получено 24,87 мМ L-аланил-L-аргинина, при использовании L-гистидина было получено 23,16 мМ L-аланил-L-гистидина, при использовании L-глутаминовой кислоты было получено 1,11 мМ L-аланил-L-глутаминовой кислоты.
(2) Пептидный синтез из метиловых эфиров других L-аминокислот и L-глутамина
Реакции проводили с использованием метиловых эфиров аминокислот, отличающихся от метилового эфира L-аланина.
Реакцию синтеза проводили инкубированием реакционной смеси, содержащей 100 мМ тестируемого метилового эфира аминоксилоты, 150 мМ L-глутамина, 100 мМ боратного буфера (pH 9,0), 10 мМ EDTA и фермента (0,05 Е/мл), в течение 3 часов при 25°C с последующим определением количества полученных пептидов с использованием ВЭЖХ. В результате при использовании в качестве метилового эфира L-аминокислоты метилового эфира глицина было получено 52,19 мМ глицил-L-глутамина, при использовании метилового эфира L-валина было получено 5,94 мМ L-валил-L-глутамина, при использовании метилового эфира L-изолейцина было получено 0,59 мМ L-изолейцил-L-глутамина, при использовании метилового эфира L-метионина было получено 4,31 мМ L-метионил-L-глутамина, при использовании метилового эфира L-фенилаланина было получено 3,67 мМ L-фенилаланил-L-глутамина, при использовании метилового эфира L-серина было получено 40,44 мМ L-серил-L-глутамина, при использовании метилового эфира L-треонина было получено 3,85 мМ L-треонил-L-глутамина, при использовании метилового эфира L-глутамина было получено 0,23 мМ L-глутаминил-L-глутамина, при использовании метилового эфира L-тирозина было получено 1,24 мМ L-тирозил-L-глутамина, при использовании метилового эфира L-аргинина было получено 6,52 мМ L-аргинила-L-глутамина и при использовании α-метилового эфира L-аспарагиновой кислоты было получено 8,22 мМ L-аспартил-α-L-глутамина. Кроме того, также подтверждено, что пептиды, состоящие из соответствующих аминокислот и L-глутамина, продуцируются при использовании в качестве метилового эфира аминокислоты метилового эфира L-лейцина, метилового эфира L-аспарагина, метилового эфира L-лизина, β-метилового эфира L-аспарагиновой кислоты, α,β-диметилового эфира L-аспарагиновой кислоты или γметилового эфира L-глутаминовой кислоты (определение количества не проводили, поскольку стандартные препараты были недоступны).
(3) Измерение активности пролиниминопептидазы (pepI)
Реакцию проводили при 30°C с использованием реакционной смеси состава: 50 мМ боратного буфера (pH 9,0), 5 мМ EDTA, 1 мМ пролин-2-нафтиламида (пролин-pNA). Скорость высвобождения нафтиламида измеряли по увеличению оптического поглощения при 405 нанометрах (нм) (ε=9,83). Активность, являющуюся результатом высвобождения 1 мкМ нафтиламида в 1 минуту, принимали за 1 единицу.
Пролиниминопептидазная активность очищенного фермента составила 5,83 × 103 Е/мг.
Пример 9
Выделение гена пролиниминопептидазы (pepI) из штамма ATCC 12633 Pseudomonas putida и экспрессия в Escherichia coli
1. Получение частичного фрагмента гена пролиниминопептидазы (pepI).
ДНК выделяли из культивированных клеток штамма ATCC 12633 Pseudomonas putida таким же способом, как описано в разделе 3 примера 7.
С другой стороны, синтетические ДНК олигомеры (SEQ ID NO: 10: GGC GGA TCC GGT GCT CAA AGC GCA A и SEQ ID NO: 11: GGC GGA TC AGG TCG CCG CGT TCT TC) были получены на основе частичной последовательности оснований (AF032970) пролиниминопептидазы штамма ATCC 12633 Pseudomonas putida, опубликованной в Генном банке (Genbank), и частичный фрагмент гена был амплифицирован с помощью ПЦР с TaKaRa LA (производимого Takara Shuzo) с использованием их в качестве праймеров.
2. Клонирование полноразмерного гена пролиниминопептидазы из библиотеки генов.
Для получения гена пролиниминопептидазы полной длины (pepI) штамма ATCC 12633 Pseudomonas putida, первоначально проводили Саузерн-гибридизацию таким же образом, как описано в части 5 примера 7 с использованием частичного фрагмента в качестве зонда. В результате была выявлена полоса примерно в положении 2,8 т.п.н. (тысяч пар нуклеотидов) в XhoI-расщепленном продукте. Затем такой фрагмент области в 2,8 т.п.н. собирали и лигировали с SalI-расщепленной pUC18 для получения библиотеки (100 штаммов) Escherichia coli JM109. Затем проводили гибридизацию колоний таким же образом, как описано в примере, и выбрали один положительный клон.
3. Последовательность оснований гена пролиниминопептидазы штамма ATCC 12633 Pseudomonas putida
Плазмиды, которые содержались в отобранных трансформантах, получали в соответствии со способом, описанным в Molecular Cloning, 2nd edition, Cold Spring Harbor Press (1989), и определяли последовательность оснований той части, где происходила гибридизация с зондом, и поблизости от нее. Присутствовала открытая рамка считывания (ORF), которая кодировала белок, состоящий из 337 аминокислот, и это подтверждало, что был получен данный ген полной длины. Последовательность оснований полного гена пролиниминопептидазы показана в SEQ ID NO: 14 списка последовательностей.
Следует отметить, что полученная ORF проявляла 46,3%-ную гомологию по последовательности оснований с известной пролиниминопептидазой, полученной из бактерии видов Corynebacterium, и проявляла 82,4%-ную гомологию с пролиниминопептидазой Pseudomonas putida PA01.
4. Экспрессия гена пролиниминопептидазы в Escherichia coli
Конструировали плазмиду pUCPPPEPI, содержащую ген пролиниминопептидазы (pepI) lac-промотора pUC18, для экспрессирования pepI в Escherichia coli. Фрагменты, амплифицированные с помощью ПЦР с использованием хромосомной ДНК в качестве матрицы и олигонуклеотидов, представленных в последовательностях SEQ ID NO: 9 и 11 (SEQ ID NO: 9: GGC GGA TCC GGT GCT CAA AGC GCA A; SEQ ID NO: 11: CAC GCG CTG CAG CAA ACC CCT CAT), в качестве праймеров, обрабатывали и после лигирования с расщепленными продуктами pUC18 использовали для трансформации Escherichia coli JM109. Штаммы, содержащие целевые плазмиды, отбирали из ампициллин-устойчивых штаммов, и сконструированную плазмиду экспрессии обозначили как pUCPPPEPI.
Трансформант Escherichia coli, имеющий pUCPPPEPI, предварительно культивировали в течение 16 часов при 37°C в среде LB, содержащей 0,1 мг/мл ампициллина. 1 мл культурального бульона, полученного после предварительного культивирования, инокулировали в 500 мл колбу Сакагуши (Sakaguchi), содержащую 50 мл среды LB, с последующим основным культивированием при 37°C. Через два часа после начала культивирования добавляли изопропил-1-тио-β-D-галактопиранозид (IPTG) до конечной концентрации 1 мМ с последующим дополнительным культивированием в течение 3 часов.
После завершения культивирования микроорганизмы собирали и промывали, суспендировали в 10 мл 20 мМ фосфатного буфера (pH 8,0), а затем подвергали ультразвуковому разрушению в течение 30 минут при 180 Вт. Раствор собирали и центрифугировали при 12000 g×10 минут и полученный в результате супернатант использовали в качестве не содержащего клеток экстракта. В результате активность пролиниминопептидазы (1,21 × 103 Е/мг) обнаруживали только в том случае, когда был введен pUCPPPEPI, и в конечном результате это подтверждало то, что клонированный ген pepI экспрессировался в Escherichia coli.
Пример 10
Синтез L-аланил-L-глутамина с использованием пролиниминопептидазы штамма ATCC 12633 Pseudomonas putida
1. Выявление L-аланил-L-глутамин-образующей активности в штамме ATCC 12633 Pseudomonas putida
Штамм ATCC 12633 Pseudomonas putida культивировали в течение ночи при 30°C в жидкой среде L для получения клеток микроорганизмов. Полученные клетки микроорганизмов суспендировали в 0,1 М боратном буфере (рН 9,0), 10 мМ EDTA, и полученную суспензию использовали в качестве ферментативной жидкости. Следует отметить, что определение L-аланил-L-глутамин-образующей активности проводили в соответствии со способом измерения ферментативной активности, описанным ниже. Ферментативную реакцию проводили при 30°C в реакционной смеси, состоящей из боратного буфера (pH 9,0) при конечной концентрации 0,1 M, EDTA в концентрации 10 мМ, гидрохлорида метилового эфира L-аланина в концентрации 100 мМ и L-глутамина - 150 мМ, и количество L-аланил-L-глутамина, продуцированное во время прохождения реакции определяли методом ВЭЖХ. Активность, которая приводила к 1 мкМ L-аланил-L-глутамина в 1 минуту принимали за 1 единицу.
Была выявлена L-аланил-L-глутамин-образующая активность, составляющая 0,051 единицу на 1 мл культуральной жидкости.
2. Синтез L-аланил-L-глутамина Escherichia coli, экспрессирующей пролиниминопептидазу
L-аланил-L-глутамин-образующую активность измеряли с использованием вышеуказанного экстракта, не содержащего клеток. В результате при введении pUCPPPEPI была выявлена L-аланил-L-глутамин-образующая активность, составлявшая 7,88 Е/мг, и это подтверждало, что клонированный ген pepI представлял собой ген L-аланил-L-глутамин-образующего фермента. Максимальное накопление L-аланил-L-глутамина составляло 25 мМ.
Пример 11
Выделение гена пролиниминопептидазы (pepI) из штамма FERM ВР-8123 Pseudomonas putida и экспрессия в Escherichia coli
1. Получение части гена пролиниминопептидазы (pepI)
ДНК выделяли из культивированных клеток (50 мл культуры) штамма FERM BP-8123 Pseudomonas putida с использованием того же способа, как в примере 1, для получения пролиниминопептидазы (pepI) из штамма FERM BP-8123 Pseudomonas putida.
С другой стороны, первоначально проводили гибридизацию по Саузерну таким же образом, как описано в разделе 5 примера 9 с использованием частичного фрагмента гена pepI штамма ATCC 12633 Pseudomonas putida, амплифицированного в примере 9 в качестве зонда. В результате определяли полосу примерно в положении 6,5 т.п.о. в PstI-расщепленном продукте.
Данный фрагмент области 6,5 т.п.о. собирали и лигировали с PstI-расщепленной pUC18 для получения библиотеки (200 штаммов) с использованием Escherichia coli JM109. Проводили гибридизацию колоний таким же образом, как описано в примере, и отобрали два положительных клона.
2. Последовательность оснований гена пролиниминопептидазы штамма FERM BP-8123 Pseudomonas putida
Получали плазмиды, удерживаемые отобранными трансформантами, в соответствии со способом, описанным в Molecular Cloning, 2nd edition, Cold Spring Harbor Press (1989), и определяли последовательность оснований в положении, где проходила гибридизация с зондом, и поблизости от него. Присутствовала открытая рамка считывания (ORF), которая кодирует белок, состоящий из 323 аминокислот, так что было подтверждено, что достигнута полная длина данного гена. Последовательность оснований полного гена пролиниминопептидазы показана в SEQ ID NO: 16 списка последовательностей. Полученная ORF проявляла гомологичность в 83% по последовательности оснований и гомологичность, составлявшую 85%, по аминокислотной последовательности с пролиниминопептидазой штамма ATCC 12633 Pseudomonas putida.
3. Экспрессия гена пролиниминопептидазы в Escherichia coli
Конструировали плазмиду, содержащую ген pepI ниже lac-промотора pUC18, для экспрессирования pepI гена в Escherichia coli. Фрагменты, амплифицированные с помощью ПЦР с использованием хромосомной ДНК в качестве матрицы и олигонуклеотидов, представленных в последовательностях SEQ ID NO: 12 и 13 (SEQ ID NO: 12: CCC GAA TTC TTA CGG AGC GCG CAA TG; SEQ ID NO: 13: CGG GGA TCC CTT CAT GCT TCT TCA GG), в качестве праймеров, обрабатывали и после лигирования с расщепленными продуктами pUC18 использовали для трансформации Escherichia coli JM109. Штаммы, содержащие целевые плазмиды, отбирали из ампициллин-устойчивых штаммов, и сконструированную плазмиду экспрессии обозначили как pUCPGPEPI.
Трансформант Escherichia coli, содержащий pUCPGPEPI, использовали для получения не содержащего клеток экстракта таким же способом, как описано в примере 8, и, когда измеряли активность пролиниминопептидазы, активность была обнаружена (3,48 × 101 Е/мг), что подтверждало то, что клонированный pepI-ген экспрессировался в Escherichia coli.
Пример 12
Синтез L-аланил-L-глутамина с помощью пролиниминопептидазы штамма FERM BP-8123 Pseudomonas putida
1. Выявление L-аланил-L-глутамин-образующей активности в штамме FERM BP-8123 Pseudomonas putida
Ферментативную активность измеряли, культивируя штамм FERM BP-8123 Pseudomonas putida таким же образом, как описано в примере 10. Была выявлена L-аланил-L-глутамин-образующая активность, составляющая 0,054 единицы на 1 мл культуральной жидкости.
2. Выявление L-аланил-L-глутамин-образующей ферментативной активности
L-аланил-L-глутамин-образующую активность измеряли с использованием не содержащего клеток экстракта трансформанта Escherichia coli, сохраняющего pUCPGPEPI. В результате L-аланил-L-глутамин-образующая активность, составляющая 0,470 Е/мг, была выявлена в случае введения pUCPGPEPI, так что это подтверждало то, что клонированный pepI-ген представлял собой ген L-аланил-L-глутамин-образующего фермента. Максимальное накопление L-аланил-L-глутамина составило 30 мМ.
Пример 13
Синтез L-аланил-L-глутамина с использованием фермента, обладающего пролиниминопептидазной активностью, полученного из штамма EK01 Bacillus coagulans
L-аланил-L-глутамин-образующую активность измеряли в соответствии со способом, описанным в примере 10, с использованием очищенного фермента (3.93 × 105 Е/мг) из штамма EK01 Bacillus coagulans, коммерчески доступного от Toyobo Co., Ltd. В результате была обнаружена активность, составлявшая 52 Е/мг, так что это подтвердило тот факт, что пролиниминопептидаза представляет собой фермент, обладающий L-аланил-L-глутамин-образующей активностью. Максимальное накопление L-аланил-L-глутамина составило 18 мМ.
Пример 14
Влияние ингибиторов на активность полученного фермента
Исследовали влияние ингибиторов на полученную пролиниминопептидазу. Ферментативную реакцию проводили в течение 30 минут при 30°C в реакционной смеси, состоящей из 0,1 M боратного буфера (pH 9,0), 10 мМ EDTA, 100 мМ гидрохлорида метилового эфира L-аланина, 150 мМ L-глутамина и 1 мМ ингибитора, с последующим измерением синтеза L-аланил-L-глутамина. Ферментативная активность практически полностью ингибировалась, когда NEM (N-этилмалеимид) добавляли в концентрации 1 мМ к штамму EK01 Bacillus coagulans, штамму ATCC 12633 Pseudomonas putida иштаммуFERM BP-8123 Pseudomonas putida. Кроме того, активности в определенной степени снижались после добавления IAA (иодацетоамида) в концентрации 1 мМ. С другой стороны, добавление PMSF (фенилметилсульфонилфторид) в концентрации 1 мМ не оказывало действия на ферментативную активность. Добавление каких-либо ингибиторов не влияло на активность, исследованную для штамма ATCC 13286 Corynebacterium glutamicum.
[Не содержащий текста список последовательностей]
SEQ ID NO: 1: N-концевая аминокислотная последовательность пептидообразующего фермента, полученного из Corynebacterium glutamicum
SEQ ID NO: 2: ПЦР праймер
SEQ ID NO: 3: ПЦР праймер
SEQ ID NO: 4: Кодирующая последовательность пептидообразующего фермента, полученного из Corynebacterium glutamicum
SEQ ID NO: 5: Аминокислотная последовательность пептидообразующего фермента, полученного из Corynebacterium glutamicum
SEQ ID NO: 6: Праймер
SEQ ID NO: 7: Праймер
SEQ ID NO: 8: Праймер
SEQ ID NO: 9: Праймер
SEQ ID NO: 10: Праймер
SEQ ID NO: 11: Праймер
SEQ ID NO: 12: Праймер
SEQ ID NO: 13: Праймер
SEQ ID NO: 14: Кодирующая последовательность пептидообразующего фермента, полученного из Pseudomonas putida ATCC 12633
SEQ ID NO: 15: Аминокислотная последовательность пептидообразующего фермента, полученного из Pseudomonas putida ATCC 12633
SEQ ID NO: 16: Кодирующая последовательность пептидообразующего фермента, полученного из Pseudomonas putida FERM BP-8123
SEQ ID NO: 17: Аминокислотная последовательность пептидообразующего фермента, полученного из Pseudomonas putida FERM BP-8123
Хотя для полного и ясного раскрытия изобретение было описано с приведением конкретного варианта осуществления, прилагаемую формулу изобретения подобным образом ограничивать не следует, а следует рассматривать как воплощение всех модификаций и альтернативных конструкций, которые могут быть осуществлены специалистом в данной области и которые в достаточной степени попадают под основные указания, приведенные выше в данном описании.
Промышленная применимость
В соответствии со способом получения дипептида по настоящему изобретению дипептид может быть получен с использованием эфира L-аминокислоты и L-аминокислоты, которые могут быть получены с низкой стоимостью, без использования сложного метода синтеза, что позволяет снизить стоимость производства дипептидов, используемых в качестве фармацевтических препаратов, функциональных продуктов питания и так далее. Кроме того, в соответствии со способом получения дипептида по настоящему изобретению могут быть получены различные типы дипептидов при использовании различных типов эфиров L-аминокислот и L-аминокислот в качестве исходных материалов.






















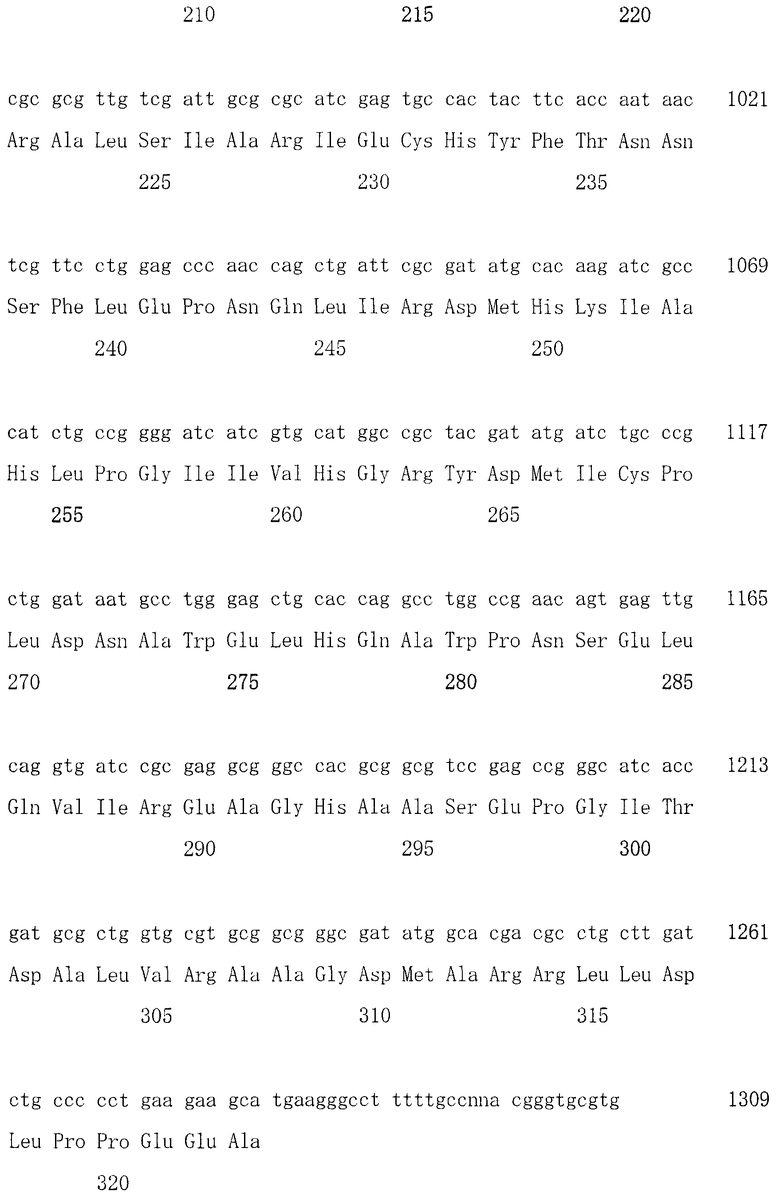



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИПЕПТИДА (ВАРИАНТЫ) | 2005 |
|
RU2316596C2 |
| НОВЫЙ ГЕН ПЕПТИДОБРАЗУЮЩЕГО ФЕРМЕНТА | 2003 |
|
RU2296798C2 |
| ДНК, КОДИРУЮЩАЯ ДИПЕПТИД-СИНТЕЗИРУЮЩИЙ ФЕРМЕНТ (ВАРИАНТЫ), БАКТЕРИЯ РОДА Escherichia И СПОСОБ ПОЛУЧЕНИЯ ДИПЕПТИДОВ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2013 |
|
RU2560980C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-АЛАНИЛ-L-ГЛУТАМИНА | 2002 |
|
RU2279440C2 |
| НОВЫЙ ФЕРМЕНТ, ОБРАЗУЮЩИЙ ПЕПТИД, МИКРООРГАНИЗМ, ПРОДУЦИРУЮЩИЙ ДАННЫЙ ФЕРМЕНТ, И СПОСОБ СИНТЕЗА ДИПЕПТИДА С ИХ ПРИМЕНЕНИЕМ | 2003 |
|
RU2300565C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТЫ | 2008 |
|
RU2515044C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-L-АСПАРТИЛ-L-ФЕНИЛАЛАНИН-БЕТА-ЭФИРА И СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-L-АСПАРТИЛ-L-ФЕНИЛАЛАНИН-АЛЬФА-МЕТИЛОВОГО ЭФИРА | 2004 |
|
RU2312149C2 |
| НОВАЯ ЛИЗИНДЕКАРБОКСИЛАЗА И СПОСОБ ПОЛУЧЕНИЯ КАДАВЕРИНА С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2016 |
|
RU2699516C2 |
| СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТЫ | 2003 |
|
RU2307165C2 |
| СПОСОБ ПРОДУКЦИИ 2-АМИНО-3-МЕТИЛ-4-КЕТОПЕНТАНОАТА | 2007 |
|
RU2392323C2 |
Изобретение относится к биотехнологии. Дипептид получают из эфира L-аминокислоты и L-аминокислоты с использованием белка, обладающего ферментативной активностью продуцирования дипептида из эфира L-аминокислоты и L-аминокислоты, в том числе пролиниминопептидазной активностью. При этом указанный белок получают культивированием трансформированной бактериальной клетки. Заявленное изобретение позволяет упростить и удешевить процесс получения дипептидов. 8 н. и 3 з.п. ф-лы, 1 ил., 4 табл.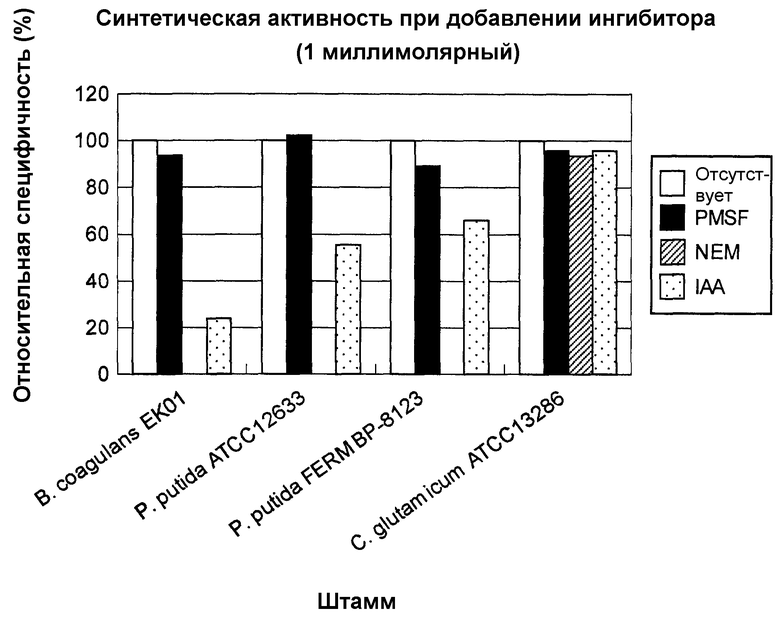
(C) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 15 списка последовательностей,
(D) белок, состоящий из аминокислотной последовательности, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 15 списка последовательностей, где указанное множество принимает значения от 2 до 50, и обладающий 50%-ной или более ферментативной активностью продуцирования дипептида из эфира L-аминокислоты и L-аминокислоты, в сравнении с соответствующей ферментативной активностью белка (С).
(Е) белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 17 списка последовательностей,
(F) белок, состоящий из аминокислотной последовательности, которая включает замещение, удаление, вставку, добавление или перестановку одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 17 списка последовательностей, где указанное множество принимает значения от 2 до 50, и обладающий 50%-ной или более ферментативной активностью продуцирования дипептида из эфира L-аминокислоты и L-аминокислоты, в сравнении с соответствующей ферментативной активностью белка (Е).
(c) ДНК с последовательностью оснований, состоящей из оснований с номерами 486-1496 в последовательности оснований, представленной в SEQ ID NO: 14 списка последовательностей,
(d) ДНК, которая гибридизуется в жестких условиях с ДНК с последовательностью оснований, комплементарной последовательности оснований, состоящей из оснований с номерами 486-1496 в последовательности оснований, представленной в SEQ ID NO: 14 списка последовательностей.
(e) ДНК с последовательностью оснований, состоящей из оснований с номерами 311-1279 в последовательности оснований, представленной в SEQ ID NO: 16 списка последовательностей,
(f) ДНК, которая гибридизуется в жестких условиях с ДНК с последовательностью оснований, комплементарной последовательности оснований, состоящей из оснований с номерами 311-1279 в последовательности оснований, представленной в SEQ ID NO: 16 списка последовательностей.
| ЭЛЕКТРОГИДРАВЛИЧЕСКАЯ ТРАМБОВКА | 1983 |
|
SU1108790A1 |
| WO 9426882, 24.11.1994 | |||
| ДИПЕПТИДИЛАМИНОПЕПТИДАЗА И СПОСОБ ФЕРМЕНТАТИВНОГО ОТЩЕПЛЕНИЯ N-КОНЦЕВЫХ ДИПЕПТИДОВ MET-TYR, MET-ARG ИЛИ MET-ASP ОТ ПОЛИПЕПТИДНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ | 1993 |
|
RU2096455C1 |
Авторы
Даты
2006-07-20—Публикация
2002-07-26—Подача