Настоящее изобретение относится к выбранным содержащим глицидильные или карбонильные функциональные группы N-алкокси-4,4-диоксиполиалкилпиперидиновым соединениям, обладающим ациклическим или циклическим кеталевым строением, к способной полимеризоваться композиции, включающей а) по меньшей мере один этиленовоненасыщенный мономер и б) содержащее глицидильную или карбонильную функциональную группу N-алкокси-4,4-диоксиполиалкилпиперидиннитроксидное инициаторное соединение. Другими объектами настоящего изобретения являются способ полимеризации этиленовоненасыщенных мономеров и применение содержащих глицидильные или карбонильные функциональные группы N-алкокси-4,4-диоксиполиалкилпиперидиннитроксидных инициаторов для радикальной полимеризации.
Соединения по настоящему изобретению обеспечивают получение полимерных смолистых продуктов, обладающих низкой полидисперсностью, и протекание процесса полимеризации с хорошей эффективностью превращения мономера в полимер. В частности, настоящее изобретение относится к стабильным опосредованным свободными радикалами процессам полимеризации, в ходе проведения которых получают гомополимеры, статистические сополимеры, блок-сополимеры, мультиблок-сополимеры, привитые сополимеры и т.п., при повышенных скоростях полимеризации и более высоких степенях превращения мономера в полимер.
В патенте US 4581429, выданном 8 апреля 1986 г. на имя Solomon и др., описан способ свободнорадикальной полимеризации, который обеспечивает регулирование роста полимерных цепей с получением короткоцепочечных или олигомерных гомополимеров и сополимеров, включая блок- и привитые сополимеры. При осуществлении этого способа используют инициатор, отвечающей формуле (неполной) R'R"N-O-X, где Х обозначает свободнорадикальный материал, способный полимеризовать ненасыщенные мономеры. Реакции, как правило, характеризуются низкими скоростями превращения. Конкретно упомянутые радикальные группы R'R"N-O• дериватизируют из 1,1,3,3 тетраэтилизоиндолина, 1,1,3,3 тетрапропилизоиндолина, 2,2,6,6 тетраметилпиперидина, 2,2,5,5 тетраметилпирролидина или дитрет-бутиламина. Однако предлагаемые соединения не удовлетворяют всем требованиям. Так, в частности, полимеризация акрилатов протекает недостаточно быстро и/или степень превращения мономера в полимер оказывается не настолько высокой, как это необходимо.
Инициаторы радикальной полимеризации, процессы полимеризации и полимерные продукты по настоящему изобретению содержат дополнительную глицидильную или карбонильную группу, которая может быть использована для дальнейших реакций. Получаемые смолы можно использовать для многих целей.
Во время реакции радикальной полимеризации глицидильная или алкилкарбонильная группа предлагаемых инициаторов остается по существу неизменной. Следовательно, инициаторы радикальной полимеризации по настоящему изобретению предоставляют на второй стадии (после завершения или обрыва цепи при радикальной полимеризации) возможность для взаимодействия глицидильной группы олигомеров или полимеров с нуклеофилами, такими как спирты, меркаптаны, амины, металлорганические соединения или т.п., изменяя тем самым свойства олигомеров или полимеров.
Глицидильная группа инициаторов способна также вступать во взаимодействие на первой стадии, например, вследствие анионной полимеризации в присутствии, например, дициандиамида, бутиллития или другого сильного основания, что приводит к образованию олигомерных/полимерных инициаторов радикальной полимеризации.
S.Kobatake и др. в Macromolecules 1997, 30, 4238-4242 и в WO 97/36894 описана анионная полимеризация бутадиена в присутствии соединения (а), которое в боковой цепи содержит глицидильную группу. Это соединение действует как агент, обрывающий цепь в процессе анионной полимеризации бутадиена.

Образовавшаяся макромолекула может быть в дальнейшем использована в качестве макроинициатора для радикальной полимеризации и получения блок-сополимеров, содержащих полибутадиеновый сегмент. Типичные сополимеры, которые могут быть получены, представляют собой акрилонитрил-бутадиен-стирольные (АБС) сополимеры.
По настоящему изобретению предлагаются инициаторы для радикальной полимеризации, которые содержат глицидильную или алкилкарбонильную группу, связанную с фенильной группой. Эти инициаторы демонстрируют высокую реакционную способность, хорошие скорости полимеризации и хорошие степени превращения мономера в полимер.
Оставшаяся глицидильная или карбонильная группа проявляет высокую реакционную способность в отношении нуклеофилов и при необходимости может быть легко превращена в другие химические группы.
Соединения по настоящему изобретению могут быть также использованы в качестве обрывающих цепь агентов в процессе анионной полимеризации, например, бутадиена, как изложено в WO 97/36894. С помощью предлагаемых соединений обрыв цепи при анионной полимеризации, например, бутадиена осуществляют быстро и полностью.
Содержащие глицидильные или карбонильные функциональные группы алкоксиамины, включающие тетраметилпиперидиновую группу, и их применение в качестве функционализованных инициаторов радикальной полимеризации/регуляторов уже описаны в WO 99/46261. Предлагаемые соединения отличаются от тех, которые представлены в WO 99/46261, тем, что в 4-м положении пиперидинового остатка они обладают кеталевым строением. В литературе, посвященной данной области техники, такие соединения и их применение в качестве инициаторов полимеризации/регуляторов не были описаны ни как конкретные соединения, ни в общем.
Было установлено, что среди 2,2,6,6-тетраалкилпиперидинов, описанных в литературе, посвященной данной области техники, особую ценность представляют те, которые являются производными 2,2,6,6-тетраметилпиперидина, 2,2-диэтил-6,6-диметилпиперидина и 2,6-диэтил-2,3,6-триметилпиперидина, которые в 4-м положении замещены двумя атомами кислорода с образованием ациклической или циклической кеталевой структуры.
Кеталевая структура в 4-м положении гарантирует высокую термостойкость, которая имеет важное значение для хранения, особенно при повышенных температурах. Кеталевая структура термически значительно более стабильна в сравнении со структурой соответствующего 4-оксосоединения.
Такие соединения проявляют неизменную инициирующую/регулирующую активность даже после хранения при повышенных температурах, которые создают, например, в ходе проведения обычных испытаний на стабильность.
Другой проблемой, связанной с опосредованной нитроксилом или нитроксиловым эфиром свободнорадикальной полимеризацией, является появление заметной окраски у полученного полимера. Соединения по настоящему изобретению, которые обладают кеталевой структурой в 4-м положении, придают полимеру менее интенсивную окраску в сравнении с другими, известными в данной области техники соединениями аналогичного строения.
Пространственное затруднение, обусловленное двумя диэтильными группами вместо двух метильных групп, приводит к еще более оптимизированному балансу в смысле стабильности соединений, инициирующей активности, и контроля за полимеризацией.
При такой конкретной картине замещения во 2-м и 6-м положениях пиперидинового кольца обеспечивается возможность достижения за короткое время высоких степеней превращения мономера в полимер и низких показателей полидисперсности, которые обычно составляют меньше 2. Высоких степеней превращения мономера в полимер добиваются даже с акрилатами, такими как этил- и бутилакрилат. Температура, необходимая для достижения за короткое время высокой степени превращения, может быть, например, такой низкой, как 120°С.
По настоящему изобретению предлагаются соединения, которые могут быть использованы в качестве инициаторов/регуляторов для регулирования радикальной полимеризации, которые дополнительно содержат высокореакционноспособную функциональную группу, позволяющую полимеру участвовать в аналогичных реакциях или останавливающую анионную полимеризацию, благодаря чему регулирование их инициирующей/регулирующей эффективности возможно регулированием пространственного затруднения при атоме азота и благодаря чему обеспечиваются превосходная стабильность при хранении и исключается окрашивание конечного полимера или ему сообщается лишь слабая окраска.
Соединения по настоящему изобретению являются новыми и, следовательно, одним объектом настоящего изобретения является соединение формулы Ia, IIa или IIIa



где
D обозначает группу  или группу C(O)-R13;
или группу C(O)-R13;
R13 обозначает фенил или С1-С18алкил;
m обозначает 1, 2 или 3;
n обозначает 1 или 2;
если n обозначает 1,
Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил, С3-С12алкинил, С5-С8циклоалкил, фенил, нафтил, С7-С9фенилалкил или
Y и Y' совместно образуют одну из следующих двухвалентных групп:
-C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, о-фенилен, 1,2-циклогексилиден, -СН2-СН=СН-СН2- или
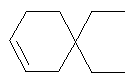 где
где
R1 обозначает водородный атом, С1-С12алкил, СООН, СОО-(С1-С12)алкил или CH2OR4;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил, СООН или СОО-(С1-С12)алкил;
R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный ацильный остаток, дериватизированный из алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 18 углеродных атомов;
если n обозначает 2,
Y и Y' совместно образуют одну из следующих четырехвалентных групп



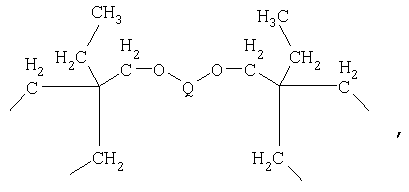
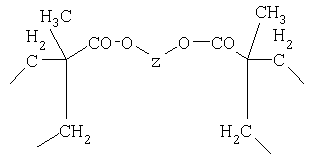 где
где
Q обозначает бисацильный остаток, который дериватизируют из С2-С12дикарбоновой кислоты, или С1-С12алкилен;
Z обозначает С1-С12алкилен;
R12 каждый независимо друг от друга обозначает Н или СН3.
С1-С18алкил может быть линейным или разветвленным. Примерами служат метил, этил, пропил, изопропил, бутил, 2-бутил, изобутил, трет-бутил, пентил, 2-пентил, гексил, гептил, октил, 2-этилгексил, трет-октил, нонил, децил, ундецил, додецил, гептадецил или октадецил.
Алкенил, содержащий от 3 до 12 углеродных атомов, представляет собой разветвленный или неразветвленный радикал, например пропенил, 2-бутенил, 3-бутенил, изобутенил, н-2,4-пентадиенил, 3-метил-2-бутенил, н-2-октенил, н-2-додеценил, изододеценил.
Алкинил, содержащий от 3 до 12 углеродных атомов, представляет собой разветвленный или неразветвленный радикал, например пропинил (-CH2-C≡CH), 2-бутинил, 3-бутинил, н-2-октинил или н-2-додецинил.
Примерами алкокси являются метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, пентокси, изопентокси, гексокси, гептокси и октокси.
С7-С9фенилалкил представляет собой, например, бензил, α-метилбензил, α, α-диметилбензил или 2-фенилэтил, предпочтителен бензил.
С1-С12алкилен представляет собой разветвленный или неразветвленный радикал, например метилен, этилен, пропилен, триметилен, тетраметилен, пентаметилен, гексаметилен, гептаметилен, октаметилен, декаметилен или додекаметилен.
С5-С8циклоалкил представляет собой, например, циклопентил, циклогексил, циклогептил, метилциклопентил или циклооктил.
Примерами монокарбоновой кислоты, содержащей до 18 углеродных атомов, являются муравьиная кислота, уксусная кислота, пропионовая кислота, изомеры валериановой кислоты, метилэтилуксусная кислота, триметилуксусная кислота, капроновая кислота, лауриновая кислота и стеариновая кислота. Примерами ненасыщенных алифатических кислот служат акриловая кислота, метакриловая кислота, кротоновая кислота, линолевая кислота и олеиновая кислота.
Типичными примерами циклоалифатических карбоновых кислот являются циклогексанкарбоновая кислота и циклопентанкарбоновая кислота.
Примерами ароматических карбоновых кислот служат бензойная кислота, салициловая кислота и коричная кислота.
Примерами дикарбоновых кислот являются щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота, себациновая кислота, фумаровая кислота, малеиновая кислота, фталевая кислота, изофталевая кислота, терефталевая кислота.
Предпочтительным является соединение, у которого в формулах Ia, IIa и IIIa D обозначает группу 
Особенно предпочтительно соединение формулы Ia IIa или IIIa, где D обозначает группу 
m обозначает 1;
n обозначает 1;
Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил, фенил или бензил; или
Y и Y' совместно образуют одну из следующих двухвалентных групп:
-C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, -СН2-СН=СН-СН2- или; где
R1 обозначает водородный атом, С1-С12алкил, СОО-(С1-С12)алкил или CH2OR4;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил или СОО-(С1-С12)алкил;
R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный ацильный остаток, дериватизированный из алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 12 углеродных атомов, и
один из R12 обозначает водородный атом, а другой обозначает метил.
Более предпочтительным является соединение формулы Ia, II или IIIa, где D обозначает группу 
m обозначает 1;
n обозначает 1;
Y и Y' совместно образуют одну из двухвалентных групп -CH2-C(R1)(R2)-СН(R3)-, где
R1 обозначает водородный атом, метил или этил;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил или СОО-(С1-С12)алкил и
один из R12 обозначает водородный атом, а другой обозначает метил.
Особенно предпочтительно соединение формулы IIIa.
Конкретные предпочтительные соединения перечислены в таблицах 1, 2 и 3.





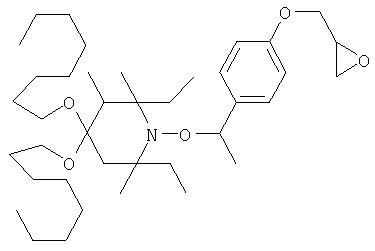
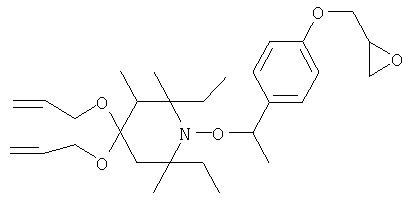






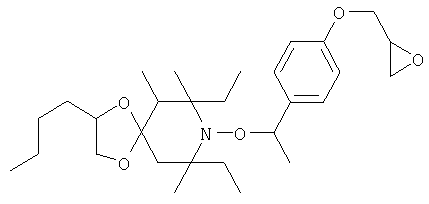
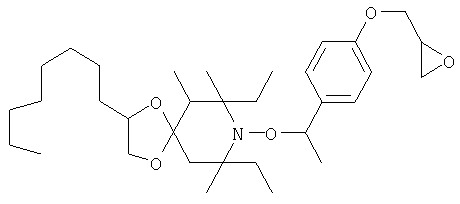



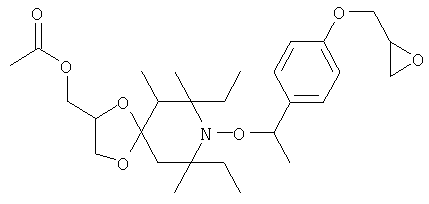






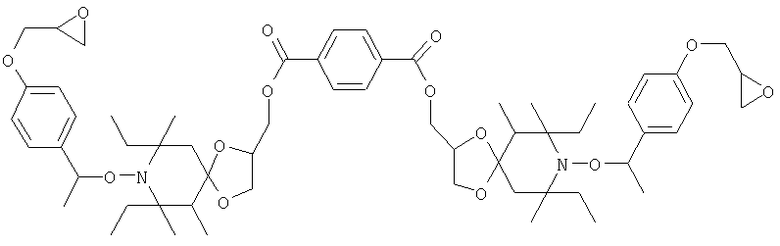
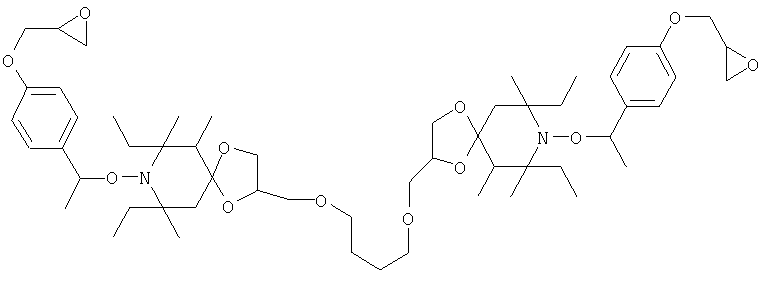
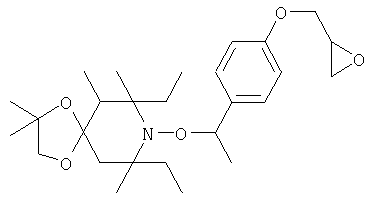



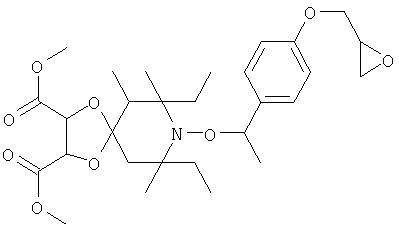



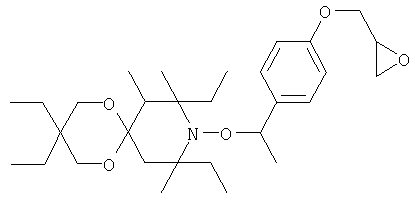
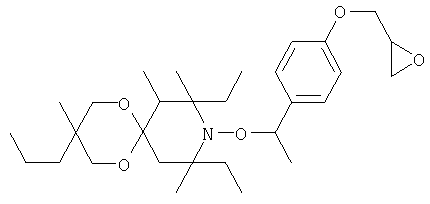













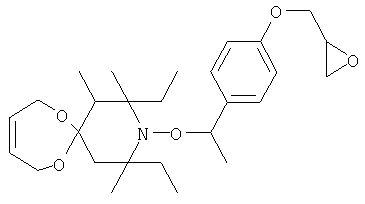
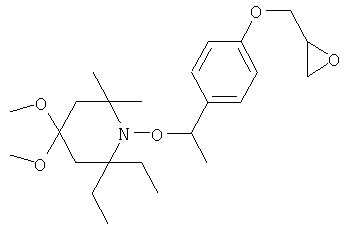



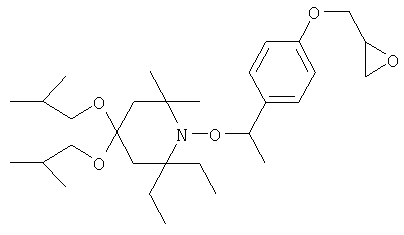


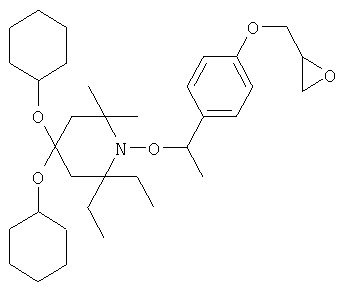






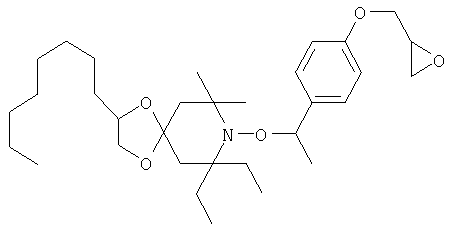



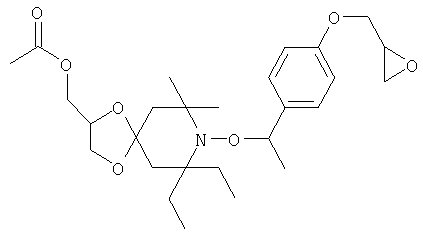





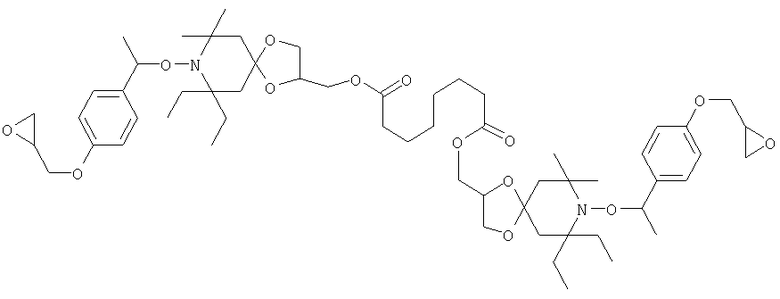







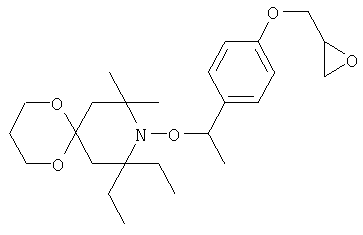
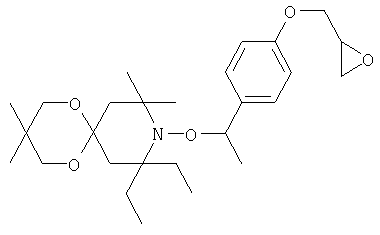
















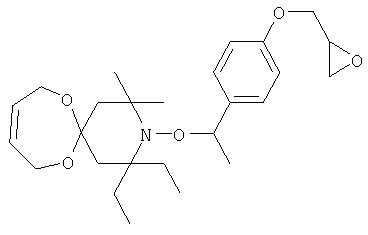
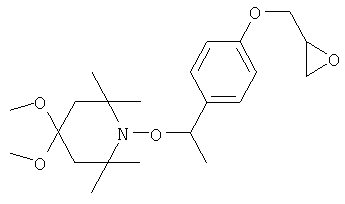















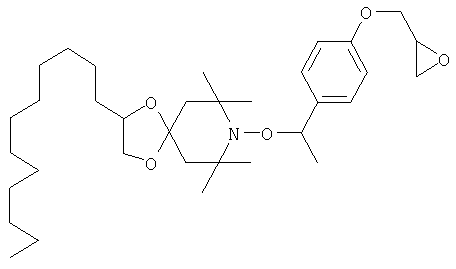





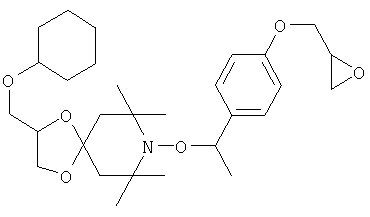
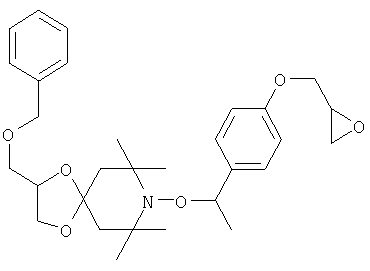
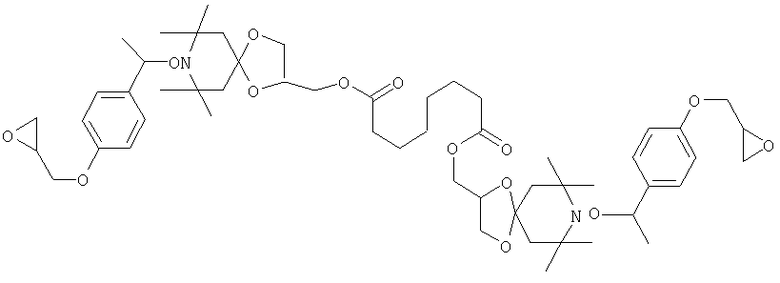
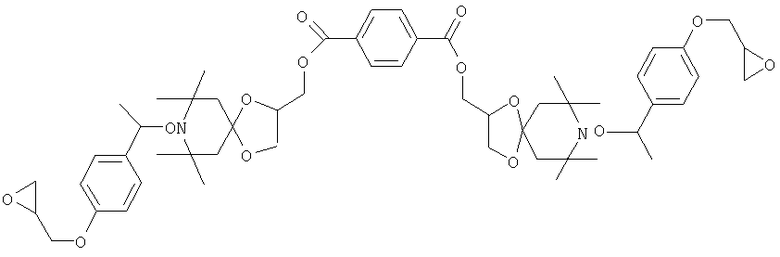
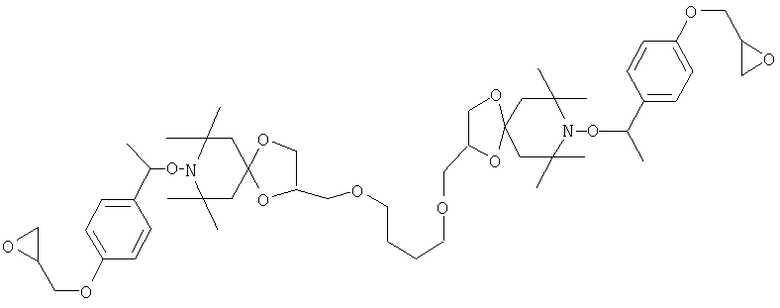

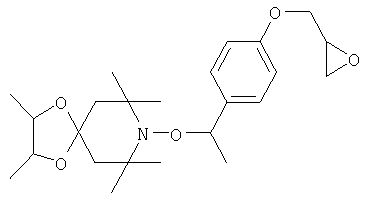



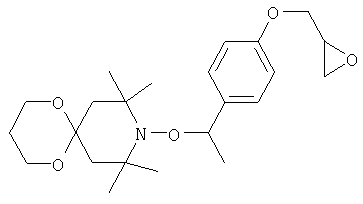
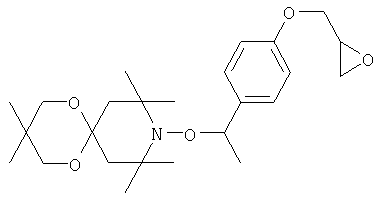


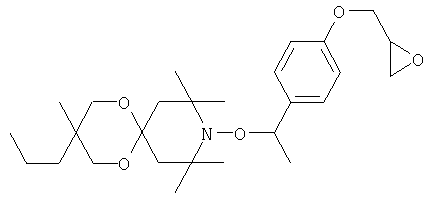








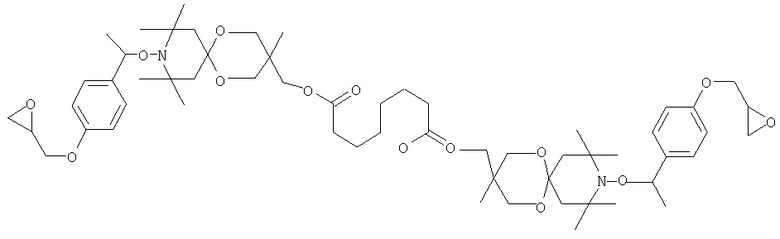




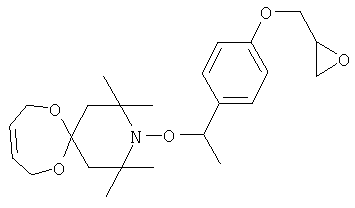



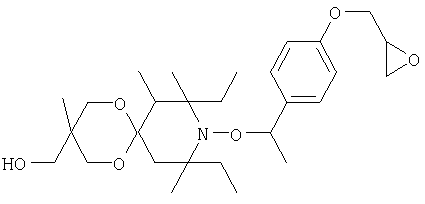


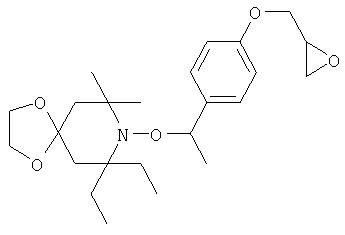
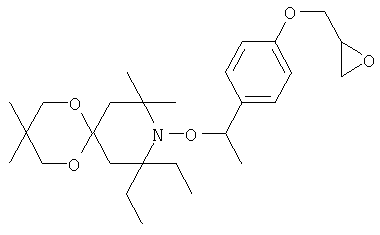
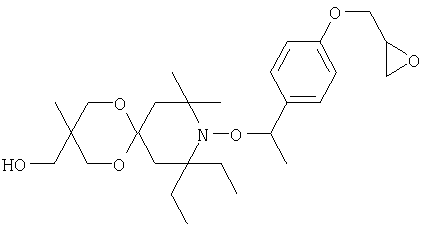





Другим объектом изобретения является способная полимеризоваться композиция, включающая
а) по меньшей мере один этиленовоненасыщенный мономер или олигомер и
б) соединение формулы Ia, IIa или IIIa

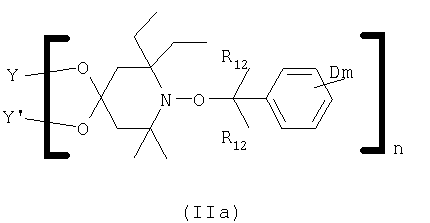

где D обозначает группу  или группу C(O)-R13;
или группу C(O)-R13;
R13 обозначает фенил или С1-С18алкил;
m обозначает 1, 2 или 3;
n обозначает 1 или 2;
если n обозначает 1,
Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил, С3-С12алкинил, С5-С8циклоалкил, фенил, нафтил, С7-С9фенилалкил или
Y и Y' совместно образуют одну из следующих двухвалентных групп:
-C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, о-фенилен, 1,2-циклогексилиден, -СН2-СН=СН-СН2- или  ,
,
где R1 обозначает водородный атом, С1-С12алкил, СООН, СОО-(С1-С12)алкил или CH2OR4;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил, СООН или СОО-(С1-С12)алкил;
R4 обозначает водородный атом, С1-С18алкил, бензил или одновалентный ацильный остаток, дериватизированный из алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 18 углеродных атомов;
если n обозначает 2,
Y и Y' совместно образуют одну из следующих четырехвалентных групп




 где
где
Q обозначает бисацильный остаток, который дериватизируют из С2-С12дикарбоновой кислоты, или С1-С12алкилен;
Z обозначает С1-С12алкилен;
R12 каждый независимо друг от друга обозначает Н или СН3.
Выше уже приведены определения и предпочтения в отношении этих соединений. Их также применяют для приготовления предлагаемой композиции.
Мономеры, приемлемые для применения при выполнении настоящего изобретения, могут быть водорастворимыми или нерастворимыми в воде. Водорастворимые мономеры, как правило, содержат соль карбоксильной группы. Нерастворимые в воде мономеры, как правило, не содержат кислотных и фенольных групп.
Типичными атомами металлов являются атомы Na, К или Li.
Типичные моноэтиленовоненасыщенные мономеры, не содержащие карбоксильных и фенольных групп, которые приемлемы для выполнения настоящего изобретения, включают алифатические эфиры акриловой и метакриловой кислот, такие как метилакрилат, этилакрилат, бутилакрилат, метилметакрилат, этилметакрилат, бутилметакрилат и изобутилметакрилат; гидроксиалифатические сложные эфиры акриловой и метакриловой кислот, такие как гидроксиэтилакрилат, гидроксипропилакрилат, гидроксиэтилметакрилат и гидроксипропилметакрилат; акриламид, метакриламид, N-третичный бутилакриламид, N-метилакриламид, N,N-диметилакриламид; акрилонитрил, метакрилонитрил, аллиловый спирт, диметиламиноэтилакрилат, диметиламиноэтилметакрилат, фосфоэтилметакрилат, N-винилпирролидон, N-винилформамид, N-винилимидазол, винилацетат, сопряженные диены, такие как бутадиен или изопрен, стирол, соли стиролсульфоновой кислоты, соли винилсульфоновой кислоты и соли 2-акриламидо-2-метилпропансульфоновой кислоты и акрилоилхлорид.
Предпочтительные этиленовоненасыщенные мономеры или олигомеры выбирают из группы, включающей стирол, замещенный стирол, сопряженные диены, акролеин, винилацетат, ангидриды (алкил)акриловых кислот, соли (алкил)акриловых кислот, (алкил)акриловые эфиры или (алкил)акриламиды.
Особенно предпочтительными этиленовоненасыщенными мономерами являются стирол, α-метилстирол, п-метилстирол, бутадиен, метилакрилат, этилакрилат, пропилакрилат, н-бутилакрилат, трет-бутилакрилат и акрилонитрил.
В наиболее предпочтительной композиции этиленовоненасыщенный мономер представляет собой стирол.
Предпочтительными акрилатами являются метилакрилат, этилакрилат, бутилакрилат, изобутилакрилат, трет-бутилакрилат, гидроксиэтилакрилат, гидроксипропилакрилат, диметиламиноэтилакрилат, глицидилакрилаты, метил(мет)акрилат, этил(мет)акрилат, бутил(мет)акрилат, гидроксиэтил(мет)акрилат, гидроксипропил(мет)акрилат, диметиламиноэтил(мет)акрилат, глицидил(мет)акрилаты, акрилонитрил, акриламид и метакриламид.
Примеры С8-С16этиленовоненасыщенных фенольных производных, которые также могут быть использованы в качестве сомономеров, включают 4-гидроксистирол, 4-гидрокси-α-метилстирол, 2,6-дитрет-бутил-4-винилфенол.
Другой класс карбоновокислотных мономеров, приемлемых для применения в качестве сомономеров при выполнении настоящего изобретения, составляют соли щелочных металлов и аммония С4-С6этиленовоненасыщенных дикарбоновых кислот. Приемлемые примеры включают малеиновую кислоту, малеиновый ангидрид, итаконовую кислоту, мезаконовую кислоту, фумаровую кислоту и цитраконовую кислоту. Предпочтительным моноэтиленовоненасыщенным дикарбоновокислотным мономером (мономерами) является малеиновый ангидрид (и итаконовая кислота).
Кислотные мономеры, приемлемые для применения при выполнении настоящего изобретения, находятся в форме солей щелочных металлов или аммониевых солей этих кислот.
Способная полимеризоваться композиция по настоящему изобретению может дополнительно включать растворитель, выбранный из группы, включающей воду, спирты, сложные эфиры, простые эфиры, кетоны, амиды, сульфоксиды, углеводороды и галоидированные углеводороды.
Объектом изобретения являются также способ свободнорадикальной полимеризации и полученные таким путем полимеры, причем осуществление этого способа позволяет устранить множество проблем и недостатков вышеупомянутых известных в данной области техники способов.
В предпочтительном варианте инициаторное соединение содержится в количестве от 0,01 до 20 мольных %, более предпочтительно в количестве от 0,01 до 10 мольных % и наиболее предпочтительный в количестве от 0,05 до 10 мольных % в пересчете на мономер или мономерную смесь.
Когда используют мономерные смеси, количества в мольных процентах рассчитывают по средней молекулярной массе смеси.
Другим объектом настоящего изобретения является способ получения олигомера, соолигомера, полимера или сополимера (блок- или статистического) свободнорадикальной полимеризацией по меньшей мере одного этиленовоненасыщенного мономера или олигомера, который включает (со)полимеризацию мономера или мономеров/олигомеров в присутствии инициаторного соединения формулы Ia, IIa или IIIa в реакционных условиях, способных вызвать разрыв связи O-С с образованием двух свободных радикалов, причем радикал  способен инициировать полимеризацию.
способен инициировать полимеризацию.
В предпочтительном варианте такой разрыв связи O-С осуществляют нагреванием, и он происходит при температуре в пределах 50 и 160°С.
Предпочтительные инициаторы и этиленовоненасыщенные мономеры уже упомянуты выше.
Предпочтительная полидисперсность (ПД) полимеров, получаемых по настоящему изобретению, находится в пределах 1,0 и 2,0, более предпочтительно в пределах 1,1 и 1,8 и наиболее предпочтительно в пределах 1,1 и 1,6.
Такой процесс можно проводить в среде органического растворителя или в водной среде, или в смесях органических растворителей и воды. При этом могут присутствовать дополнительные сорастворители или поверхностно-активные вещества, такие как гликоли или аммониевые соли жирных кислот. Другие приемлемые сорастворители представлены в настоящем описании ниже.
В предпочтительных процессах растворители используют в минимально возможных количествах. В предпочтительном варианте в реакционной смеси используют больше 30 мас.% мономера и инициатора, особенно предпочтительно больше 50%, а наиболее предпочтительно больше 80%.
Если используют органические растворители, приемлемые растворители или смеси растворителей, как правило, представляют собой чистые алканы (гексан, гептан, октан, изооктан), углеводороды (бензол, толуол, ксилол), галоидированные углеводороды (хлорбензол), алканолы (метанол, этанол, этиленгликоль, этиленгликольмонометиловый эфир), сложные эфиры (этилацетат, пропил-, бутил- или гексилацетат) и простые эфиры (диэтиловый эфир, дибутиловый эфир, этиленгликольдиметиловый эфир) или их смеси.
Реакции полимеризации в водной среде можно дополнять смешивающимся с водой или гидрофильным сорастворителем с целью еще большей гарантии того, что реакционная смесь останется гомогенной, однофазной в течение всего процесса превращения мономера. Можно использовать любой водорастворимый или смешивающийся с водой сорастворитель, лишь бы водная растворительная среда оказалась эффективной в создании растворительной системы, которая препятствует выпадению осадка или фазовому разделению реагентов или полимерных продуктов до тех пор, пока не завершатся все реакции полимеризации. Типичные сорастворители, которые можно использовать при выполнении настоящего изобретения, могут быть выбраны из группы, включающей алифатические спирты, гликоли, простые эфиры, гликолевые эфиры, пирролидины, N-алкилпирролидиноны, N-алкилпирролидоны, полиэтиленгликоли, полипропиленгликоли, амиды, карбоновые кислоты и их соли, сложные эфиры, органосульфиды, сульфоксиды, сульфоны, производные спиртов, производные неполных эфиров многоатомных спиртов, такие как бутилкарбитол и целлозольв, аминоспирты, кетоны и т.п., а также их производные и их смеси. Конкретные примеры включают метанол, этанол, пропанол, диоксан, этиленгликоль, пропиленгликоль, диэтиленгликоль, глицерин, дипропиленгликоль, тетрагидрофуран и другие водорастворимые или смешивающиеся с водой материалы и их смеси. Когда в качестве водной реакционной среды выбирают смеси воды и водорастворимых или смешивающихся с водой органических жидкостей, массовое соотношение между водой и сорастворителем, как правило, находится в интервале от примерно 100:0 до примерно 10:90.
Когда используют мономерные смеси или мономерные/олигомерные смеси, количества в мольных процентах рассчитывают в пересчете на среднюю молекулярную массу смеси.
Гидрофильные мономеры, полимеры и сополимеры по настоящему изобретению можно отделять друг от друга или выделять из полимеризационной реакционной смеси, например, варьированием рН реакционной среды и по другим хорошо известным, обычным методам разделения.
Температура полимеризации может находиться в интервале от примерно 50 до примерно 180°С, предпочтительно от примерно 80 до примерно 150°С. При температурах выше примерно 180°С скорость регулируемого превращения мономера в полимер уменьшается и образуются неопределенные и нежелательные побочные продукты, подобные обусловленному термическим действием полимеру, или может происходить деструкция регулятора полимеризации. Часто эти побочные продукты изменяют окраску полимерной смеси и для их удаления может потребоваться стадия очистки или они могут оказаться не поддающимися обработке.
Следовательно, высокая реакционная способность предлагаемых инициаторов, которые уже активны при относительно низких температурах, обуславливает сокращенное время реакции. Получаемые полимеры обычно бесцветны, и в большинстве случаев их можно использовать без какой-либо дополнительной стадии очистки. Это является важным преимуществом, если рассматривать в промышленном масштабе.
После завершения стадии полимеризации полученный (со)полимер выделяют. Стадию выделения предлагаемого способа осуществляют по известным методам, например отгонкой непрореагировавшего мономера или осаждением в подходящем осадителе, отфильтровыванием осажденного полимера и последующими промывкой и сушкой полимера.
Более того, блок-сополимеры по настоящему изобретению, в которых блоки чередуются между звеньями полярных мономеров и неполярных мономеров, можно использовать для многих целей в качестве амфифильных поверхностно-активных веществ или диспергаторов для получения высокогомогенных полимерных смесей.
(Со)полимеры по настоящему изобретению могут обладать среднечисленной молекулярной массой от 1000 до 400000 г/моль, предпочтительно от 2000 до 250000 г/моль, а более предпочтительно от 2000 до 200000 г/моль. Когда их получают в массе, среднечисленная молекулярная масса может достигать 500000 (при таких же минимальных массах, как указанные выше). Среднечисленную молекулярную массу можно определить эксклюзионной (молекулярно-ситовой) хроматографией (ЭСХ), гельпроникающей хроматографией (ГПХ), масс-спектрометрией с лазерной десорбцией/ионизацией с использованием вспомогательной матрицы (МС-ЛДИВМ) или, если инициатор несет группу, которую можно легко отличить от мономерной, то ЯМР-спектроскопией или по другим обычным методам.
Таким образом, объем настоящего изобретения охватывает также синтез новых блок-, мультиблок-, звездообразных, градиентных, статистических, сверхразветвленных и дендритных сополимеров, а также привитых сополимеров.
Полимеры, получаемые по настоящему изобретению, можно использовать, например, в следующих целях:
изготовление клеев, моющих средств, диспергаторов, эмульгаторов, поверхностно-активных веществ, пеногасителей, средств, усиливающих адгезию, замедлителей коррозии, индексных присадок, смазок, модификаторов реологических свойств, модифицирующих добавок, повышающих ударную прочность, сгустителей, сшивающих агентов, обработка бумаги, обработка воды, изготовление материалов для электроники, художественных красок, материалов покрытий, фотография, изготовление печатных красок, материалов для получения изображений, суперабсорбентов, косметических средств, средств ухода за волосами, консервантов, биоцидных материалов или добавок для улучшения свойств асфальта, кожи, текстильных материалов, керамики и дерева.
Поскольку описываемая полимеризация представляет собой "живую" полимеризацию, ее можно начинать и останавливать практически по желанию. Более того, полимерный продукт сохраняет функциональную алкоксиаминовую группу, что позволяет продолжать полимеризацию в уже существующем материале. Таким образом, в одном варианте выполнения настоящего изобретения, после того как на начальной стадии полимеризации израсходован первый мономер, в дальнейшем можно добавлять второй мономер с получением на растущей полимерной цепи на второй стадии полимеризации второго блока. Следовательно, существует возможность для проведения дополнительных процессов полимеризации с тем же или другим мономером (мономерами) и получения мультиблок-сополимеров.
Более того, поскольку эта полимеризация является радикальной, блоки можно получать, по существу, в любом порядке. Нет необходимости ограничиваться получением блок-сополимеров, когда последовательные стадии полимеризации должны протекать от по меньшей мере стабилизированного полимерного промежуточного продукта до наиболее стабилизированного полимерного промежуточного продукта, в частности, как в случае, когда проводят ионную полимеризацию. Таким образом, существует возможность для получения мультиблок-сополимера, когда вначале получают полиакрилонитрильный или поли(мет)акрилатный блок, затем к нему присоединяют стирольный или бутадиеновый блок и т.д.
Более того, необходимость в какой-либо связывающей группе, которая соединяет разные блоки данного блок-сополимера, отсутствует. Для получения последовательности блоков можно просто последовательно добавлять мономеры.
Благодаря осуществлению настоящего изобретения становится доступным множество специально спроектированных полимеров и сополимеров, таких как звездообразные и привитые (со)полимеры, как это представлено, помимо прочих работ, C.J.Hawker в Angew. Chemie, 1995, 107, cc.1623-1627, дендримеры, как они представлены в работе K.Matyaszewski и др. в Macromolecules 1996, том 29, №12, сс.4167-4171, привитые (со)полимеры, как они представлены в работе C.J.Hawker и др. в Macromol. Chem. Phys. 198, 155-166 (1997), статистические сополимеры, описанные в работе C.J.Hawker в Macromolecules 1996, 29, 2686-2688, и диблок- и триблок-сополимеры, как они описаны N.A.Listigovers в Macromolecules 1996, 29, 8992-8993.
Тем не менее, другими объектами изобретения являются полимер или олигомер, содержащий по меньшей мере одну инициаторную группу
 и по меньшей мере одну оксиаминогруппу формулы Ib, IIb или IIIb
и по меньшей мере одну оксиаминогруппу формулы Ib, IIb или IIIb


 где Y и Y'
где Y и Y'
имеют указанные выше значения, который может быть получен по вышеописанному способу; и применение соединения формулы Ia, IIa или IIIa для полимеризации этиленовоненасыщенных мономеров.
Объектом изобретения является также применение соединения формулы Ia, IIa или IIIa для обрыва цепи при анионной полимеризации диенового или винилового мономера.
Когда эти соединения используют для такого обрыва цепи при реакции, их обычно вводят в эквимолярном количестве или в избытке относительно инициирующего основания, такого как, например, втор-бутиллитий.
Процесс получения соединений по настоящему изобретению проводят в соответствии с известными реакционными стадиями. Осуществление общего метода получения соединений формулы Ia, IIa и IIIa начинается с 4-оксосоединения Ха или XIa, которые описаны в GB 2335190, или с соединения XIIa, которое является известным соединением, описанным, например, в DE 2352127.



Эти исходные соединения вводят в реакцию, например, с приемлемыми одноатомными спиртами, диолами или четырехатомными спиртами с получением промежуточных продуктов формулы Xb, XIb или XIIb, где Y, Y' и n имеют указанные выше значения. Такие реакции ацетализации в данной области техники известны хорошо, а наиболее известны соответствующие соединения. Такая реакция описана, например, в US 3790525, US 3899464, US 4007158 и US 4105626.
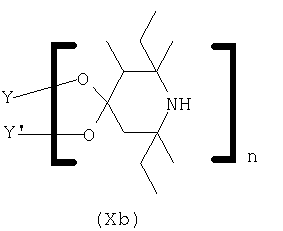


Соединения формул Xb, XIb и XIIb окисляют в соответствии со стандартными методами до соответствующих нитроксидов формул Хс, XIc и XIIc, как, например, изложено в GB 2335190 или WO 99/46261.
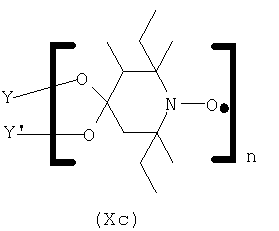


Затем проводят реакцию нитроксидов с соединением формулы
 в которой R12 и m имеют указанные выше значения, с получением соединения формулы Ia, IIa или IIIa.
в которой R12 и m имеют указанные выше значения, с получением соединения формулы Ia, IIa или IIIa.
Эта реакция сочетания также описана, например, в GB 2335190 или в WO 99/46261. В предпочтительном варианте реакцию сочетания проводят в присутствии соли Cu(II) в соответствии со способом, описанным в международной заявке № РСТ/ЕР 01/05668.
По другому варианту можно проводить реакцию нитроксидов формулы Хс, XIc или XIIc с соединением формулы 
Продукты взаимодействия в дальнейшем гидролизуют до образования соединения формулы Xd, XId или XIId.



Эти соединения являются новыми и, следовательно, также составляют объект настоящего изобретения. Приведенные выше определения и предпочтения применимы также для соединений формулы Xd, XId и XIId.
Можно проводить реакцию соединений формулы Xd, XId и XIId с эпихлоргидрином, в результате чего получают соединения, отвечающие формуле Ia, IIa или IIIa.
Изобретение иллюстрируют следующие примеры.
Получение промежуточного продукта, отвечающего формуле XIId.
Получение 4-[1-(3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илокси)этил]фенилового эфира уксусной кислоты

Смесь 25,6 г 3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксила (получен в соответствии с ЕР-А1 574666) и 82,1 г 4-этилфенилового эфира уксусной кислоты с перемешиванием нагревают до 50°С и добавляют 0,68 мл этанольного раствора, содержащего 0,13 г хлорида меди (II). Температуру повышают до 65°С и по каплям добавляют 19,4 г водного раствора бутилгидропероксида в воде (70%-ный). Реакционную смесь оставляют для дальнейшей реакции в течение 22 ч с выдержкой при температуре от 65 до 70°С, после чего охлаждают до комнатной температуры. Избыток трет-бутилгидропероксида удаляют, добавляя по каплям 4 мл водного раствора пиросульфита натрия (20%-ный). В реакционную смесь добавляют 50 мл этилового эфира уксусной кислоты и органическую и водную фазы разделяют. Органическую фазу промывают насыщенным раствором NaCl. После сушки сульфатом натрия и выпаривания растворителя в виде масла получают продукт, из которого дистилляцией (100°С/0,025 мбара) удаляют избыток 4-этилфенилового эфира уксусной кислоты. Остаток растворяют в метаноле/гексане (4/1 по объему) при нагревании до температуры кипения. После охлаждения до 0°С осадок отфильтровывают. После перекристаллизации из ацетона получают белые кристаллы, обладающие температурой плавления от 124 до 125°С.
Получение 4-[1-(3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илокси)этил]фенола

Смесь 8 г 4-[1-(3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илокси)этил]фенилового эфира уксусной кислоты и 3,9 г карбоната калия в 60 мл метанола в течение одного часа перемешивают при комнатной температуре. Смесь охлаждают до 0°С и нейтрализуют добавлением 60 мл 0,5 М соляной кислоты. Белую суспензию разбавляют водой (60 мл) и фильтруют через воронку Бюхнера. Остаток промывают водой и сушат в вакуумном сушильном шкафу при 50°С. Получают белое твердое вещество, температура плавления которого составляет от 133 до 134°С.
Получение соединений, отвечающих формулам Ia, IIa и IIIa
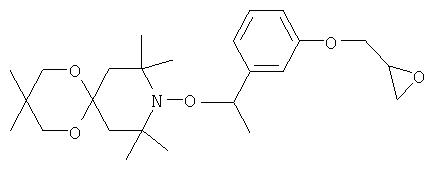
Пример А1: получение 7,7,9,9-тетраметил-8-[1-(4-оксиранилметоксифенил)этокси]-1,4-диокса-8-азаспиро[4.5]декана

Смесь 50 г 7,7,9,9-тетраметил-1,4-диокса-8-азаспиро[4.5]декан-8-оксила (получен в соответствии с ЕР-А1 574666) и 124,75 г 2-(4-этилфеноксиметил)оксирана с перемешиванием нагревают до 60°С и добавляют раствор 0,32 г хлорида меди (II) в 1,6 мл этанола. По каплям добавляют 45 г водного раствора бутилгидропероксида в воде (70%-ный). Реакционную смесь оставляют для дальнейшей реакции в течение 16 ч при 60°С, после чего охлаждают до комнатной температуры. Избыток третбутилгидропероксида удаляют, добавляя по каплям 15 мл водного раствора пиросульфита натрия. В реакционную смесь добавляют 100 мл этилового эфира уксусной кислоты и органическую и водную фазы разделяют. Органическую фазу дважды промывают 200 мл насыщенного раствора NaCl. После сушки сульфатом натрия и выпаривания растворителя в виде масла получают продукт, из которого дистилляцией (100°С/0,005 мбара) удаляют избыток 2-(4-этилфеноксиметил)оксирана. Остаток растворяют в гексане и отфильтровывают через слой оксида алюминия и вновь выпаривают растворитель. После перекристаллизации из гексана получают белые кристаллы, температура плавления которых составляет от 73,5 до 74,2°С.
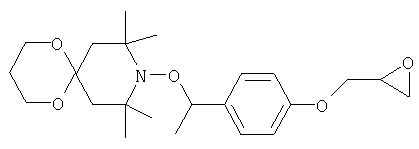
Пример А2: получение 3,3,8,8,10,10-гексаметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекана

Указанное в заглавии соединение получают аналогично примеру А1 из 3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксила (получен в соответствии с ЕР-А1 574666). Выделяют белые кристаллы.
Элементный анализ: рассч.: 69,25% С; 9,07% Н; 3,23% N; обнаруж.: 68,86% С; 9,05% Н; 3,18% N.
В соответствии с примером А1, исходя из соответствующего нитроксида, получают следующие соединения.

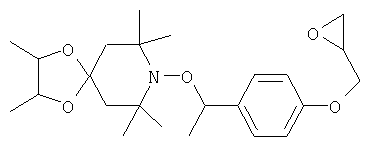


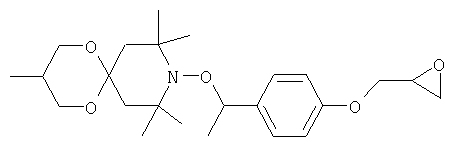
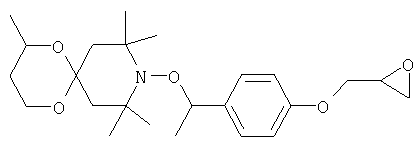




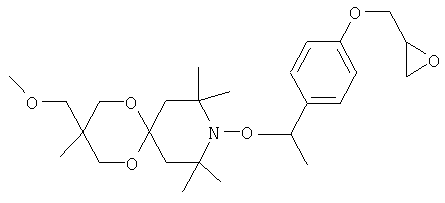



Пример А18: {4-[1-(3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илокси)этил]фенил)фенилметанон
Смесь 50 г 3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксила (CAS 98254-32-1) и 41 г (4-этилфенил)фенилметанона (получение ацилированием по Фриделю-Крафтсу 4-этилбензола бензоилхлоридом) нагревают до 60°С и добавляют раствор 0,26 г хлорида меди (II) в 1,3 мл этанола. По каплям добавляют 53,7 г 70%-ного водного раствора трет-бутилгидропероксида в воде. Реакционную смесь оставляют для дальнейшей реакции в течение 28 ч, после чего охлаждают до комнатной температуры. Далее избыток трет-бутилгидропероксида удаляют, добавляя по каплям водный раствор пиросульфита натрия. В реакционную смесь добавляют 100 мл этилацетата и органическую фазу отделяют от водной фазы. Органическую фазу дважды промывают 200 мл воды и растворитель выпаривают. Остаток очищают хроматографией на силикагеле с использованием гексана/этилацетата (7:3 по объему) в качестве элюента. После перекристаллизации из пентана/этанола (5:3 по объему) получают белые кристаллы соединения формулы
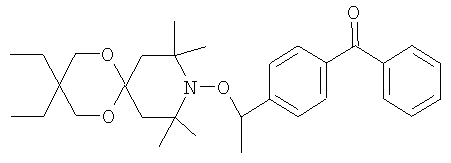
температура плавления которого составляет от 104 до 117°С.
1H-ЯМР (300 МГц; δ в част./млн; CDCl3): 0,7 (s широкий, 3 Н); 0,94 (s широкий, 6 Н); 1,18 (s широкий, 3 Н); 1,33 (s широкий, 6 Н); 1,51-1,53 (d, 3 Н); 1,4-1,65 (m, 2 Н); 2-2,25 (m, 2 Н); 3,46 (s широкий, 4 Н); 4,84-4,91 (q, 1 Н); 7,4-7,9 (ароматический Н, 9 Н).
Пример А19: 8,8-диэтил-3,3,10,10-тетраметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекан
В перемешиваемую смесь 25,6 г 8,8-диэтил-3,3,10,10-тетраметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксила и 80,2 г 2-(4-этилфеноксиметил)оксирана при 50°С добавляют раствор 0,12 г хлорида меди (II) в 0,6 мл этанола. Температуру реакционной смеси повышают до 70°С и по каплям добавляют 11,6 г 70%-ного водного раствора трет-бутилгидропероксида в воде. Реакционную смесь оставляют для дальнейшей реакции в течение 6 ч при 70°С, после чего охлаждают до комнатной температуры. Избыток трет-бутилгидропероксида удаляют добавлением по каплям 2 мл водного раствора пиросульфита натрия. В реакционную смесь добавляют 50 мл этилацетата и 50 мл 10%-ного водного раствора хлорида натрия. Смесь фильтруют через броунмиллерит и отделяют органическую фазу. Органическую фазу три раза промывают 10%-ным водным раствором хлорида натрия (100 мл) и сушат над сульфатом натрия. После выпаривания растворителя в виде масла получают продукт, из которого дистилляцией (80°С/0,025 мбара) удаляют избыток 2-(4-этилфеноксиметил)оксирана. Получают высоковязкий остаток, который при стоянии при комнатной температуре кристаллизуется. После двукратной перекристаллизации из метанола получают белые кристаллы соединения Формулы 
температура плавления которого составляет от 82 до 85°С.
В соответствии с получением 8,8-диэтил-3,3,10,10-тетраметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекана аналогичным образом синтезируют следующие соединения.


Пример А22: 8,10-диэтил-3,3,7,8,10-пентаметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекан
В перемешиваемую смесь 59,7 г 8,10-диэтил-3,3,7,8,10-пентаметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксила и 178,2 г 2-(4-этилфеноксиметил)оксирана при примерно 60°С добавляют раствор 0,27 г хлорида меди (II) в 1,35 мл этанола. Затем по каплям добавляют 38,7 г 70%-ного водного раствора трет-бутилгидропероксида в воде. Начинается экзотермическая реакция, и температуру поддерживают на уровне 70°С. Реакционную смесь оставляют для дальнейшей реакции в течение 24 ч при 70°С, после чего охлаждают до комнатной температуры. Реакционную смесь разбавляют 100 мл этилацетата. Избыток трет-бутилгидропероксида удаляют добавлением по каплям при температуре ниже 20°С 70 мл водного раствора пиросульфита натрия. Органическую фазу отделяют, дважды промывают 10%-ным водным раствором хлорида натрия (100 мл) и сушат над сульфатом натрия. После выпаривания растворителя в виде масла получают продукт, из которого дистилляцией (80°С/0,025 мбара) удаляют избыток 2-(4-этилфеноксиметил)оксирана. Получают высоковязкую смолу, которую растворяют в 20 мл метанола и охлаждают до примерно -18°С. Осаждаются белые кристаллы, которые собирают фильтрованием и температура плавления которых составляет от 141 до 147°С. Полученное соединение отвечает следующей структурной формуле
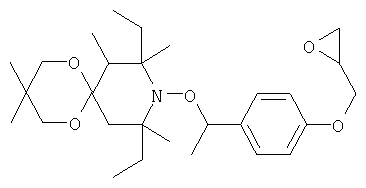
В соответствии с получением 8,10-диэтил-3,3,7,8,10-пентаметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекана аналогичным образом синтезируют следующие соединения.

Эксперименты с полимеризацией стирола
Пример Б1:
Перед применением стирол перегоняют под пониженным давлением. В сухой продуваемой аргоном трубке Шленка в 50 мл стирола растворяют нитроксиловый эфир в количествах, указанных в таблице 1. Этот раствор дегазируют в три последовательных цикла замораживания-оттаивания, а затем продувают аргоном. Затем перемешанный раствор помещают на масляную баню и полимеризуют при указанной температуре в течение 6 ч. После полимеризации остаточный мономер удаляют под вакуумом при 60°С, а полимер сушат при 60°С под вакуумом до тех пор, пока не добиваются постоянства массы.
Молекулярную массу и значения молекулярно-массового распределения определяют эксклюзионной (молекулярно-ситовой) хроматографией (ЭСХ) в жидкостном хроматографе HP 1090 (программное обеспечение: winGPC/Polymer Standard Services, Майнц, Германия) с использованием ТГФ в качестве элюента и сочетания колонок, калиброванных с помощью полистирольных стандартов с узким молекулярно-массовым распределением (Polymer Laboratories). Результаты представлены в таблице 1.
NOR примера А2
В соответствии с общим описанием примера Б1 проводят дополнительные процессы полимеризации стирола с получением следующих результатов.
Пример Б2
NOR примера А1

Пример Б3
NOR примера А6
Пример Б4
NOR примера А5
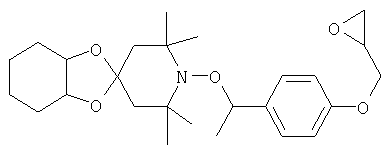
Пример Б5
NOR примера А4
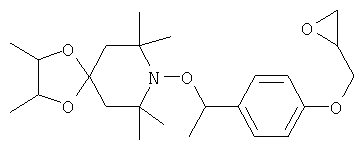
Пример Б6
NOR примера А9

Полимеризация н-BuA
Пример Б7
Перед применением н-бутилакрилат перегоняют под пониженным давлением. В сухой продуваемой аргоном трубке Шленка в 62,5 мл н-бутилакрилата растворяют нитроксиловый эфир в количествах, указанных в таблице 7. Этот раствор дегазируют в три последовательных цикла замораживания-оттаивания, а затем продувают аргоном. Затем перемешанный раствор помещают на масляную баню и полимеризуют при температуре 130°С в течение 6 ч. После полимеризации остаточный мономер удаляют под вакуумом при 30°С, а полимер сушат при 30°С под вакуумом до тех пор, пока не добиваются постоянства массы.
Молекулярную массу и значения молекулярно-массового распределения определяют эксклюзионной (молекулярно-ситовой) хроматографией (ЭСХ) в жидкостном хроматографе HP 1090 (программное обеспечение: winGPC/Polymer Standard Services, Майнц, Германия) с использованием ТГФ в качестве элюента и сочетания колонок, калиброванных с помощью полистирольных стандартов с узким молекулярно-массовым распределением (Polymer Laboratories). Результаты представлены в таблице 7.
Пример Б8: анионная полимеризация изопрена и обрыв цепи соединением примера А2
К 10,2 г (0,15 моль) изопрена, растворенного в 50 мл сухого толуола, в высушенной ампуле с тефлоновым краном, снабженной магнитной мешалкой, в атмосфере сухого аргона добавляют 3,34×10 моля втор-бутиллития (раствор концентрацией 1,3 моль/л в циклогексане, фирма Fluka) и перемешивают при комнатной температуре в течение 18 ч, предоставляя возможность для полимеризации. В дальнейшем посредством шприца отбирают образец полученного форполимера, его сушат при комнатной температуре под вакуумом и направляют на ГПХ. К оставшемуся слегка желтому раствору полиизопрена посредством шприца медленно добавляют расчетное количество соединения примера А2 (1,2- и 1,5-кратный молярный избыток относительно исходного молярного количества используемого втор-бутиллития) (растворенного в толуоле и дегазированного). Смесь оставляют для дальнейшей реакции при комнатной температуре в течение еще 6 ч. После этого реакцию обрыва цепи гасят, добавляя несколько миллилитров дегазированного метанола. Под вакуумом удаляют летучие вещества и полученный полиизопрен выделяют в виде слегка желтого каучука после сушки при комнатной температуре под вакуумом до тех пор, пока не достигают постоянства массы. Молекулярные массы определяют ГПХ в приборе HP 1090, оборудованном рефрактометрическим (ППр) и DAAD детектором (настроенным на длину волны 254 нм), с использованием ТГФ в качестве элюента (1 мл/мин) и ПС стандартов для калибровки.
Повторное инициирование полиизопрена стиролом после обрыва цепи (агентом обрыва цепи является соединение примера А2)
В высушенной продутой аргоном трубке Шленка, снабженной приспособлением для впуска аргона и магнитной мешалкой, 5 г вышеуказанных образцов 1 и 2 растворяют с использованием для каждого по 25 г свежеперегнанного стирола. Растворы дегазируют двумя последовательными циклами замораживания-оттаивания и помещают на масляную баню при 120°С, обеспечивая возможность полимеризации. По прошествии 6 ч остаточный мономер удаляют под вакуумом, а полученный полимер сушат под вакуумом при 70°С до тех пор, пока не достигают постоянства массы. Молекулярные массы определяют так, как изложено выше.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФУНКЦИОНАЛИЗИРОВАННЫЕ ТОНКОПЛЕНОЧНЫЕ ПОЛИАМИДНЫЕ МЕМБРАНЫ | 2009 |
|
RU2519377C9 |
| СПОСОБ УМЕНЬШЕНИЯ МОЛЕКУЛЯРНОЙ МАССЫ ПОЛИПРОПИЛЕНА | 2001 |
|
RU2298563C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ЦИАНОЕНОНА КАК МОДУЛЯТОРЫ KEAP1 | 2021 |
|
RU2822828C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗОТИАЗИНОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2006 |
|
RU2395508C1 |
| КОМПОЗИЦИЯ ДЛЯ ИЗДЕЛИЙ И ПОКРЫТИЙ | 2002 |
|
RU2286361C2 |
| СМЕСИ СТАБИЛИЗАТОРОВ ДЛЯ ПОЛИОЛЕФИНОВ | 2001 |
|
RU2263688C2 |
| СТАБИЛИЗИРУЮЩИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЗАМЕЩЕННЫЕ ХРОМАНОВЫЕ СОЕДИНЕНИЯ, И СПОСОБЫ ПРИМЕНЕНИЯ | 2013 |
|
RU2662823C2 |
| 1,2-БИС-АДДУКТЫ СТАБИЛЬНЫХ НИТРОКСИДОВ С ЗАМЕЩЕННЫМИ ЭТИЛЕНАМИ И СТАБИЛИЗИРОВАННЫЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2187502C2 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2742578C2 |
| ТЕХНОЛОГИЧЕСКИЕ ДОБАВКИ И ИХ ПРИМЕНЕНИЯ В РОТАЦИОННОМ ФОРМОВАНИИ | 2011 |
|
RU2597918C2 |
Изобретение относится к выбранным содержащим глицидильные или карбонильные функциональные группы N-алкокси-4,4-диоксиполиалкилпиперидиновым соединениям, обладающим ациклическим или циклическим кеталевым строением. Описываются соединения формул Ia, IIa или IIIa



где
D обозначает группу  ; m обозначает 1; n обозначает 1; Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил, фенил или бензил, или Y и Y' совместно образуют одну из следующих двухвалентных групп: -C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, -CH2-CH=CH-CH2-; где R1 обозначает водородный атом, С1-С12алкил, СОО-(С1-С12)алкил или CH2OR4; R2 и R3 каждый независимо обозначает водородный атом, метил, этил, или СОО-(С1-С12)алкил; R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный ацильный остаток алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 12 углеродных атомов; и один R12 обозначает Н, а другой СН3. Также описываются способная полимеризоваться композиция, способ получения олигомера, соолигомера, полимера или сополимера, полимер, применение соединения формулы Ia, IIa или IIIa для полимеризации этиленовоненасыщенных мономеров, применение соединения формулы Ia, IIa или IIIa для обрыва цепи анионной полимеризации диенового или винилового мономера, соединения формул Xd, XId и XIId. Технический результат - соединения по настоящему изобретению обеспечивают получение полимерных смолистых продуктов, обладающих низкой полидисперсностью, и протекание процесса полимеризации с хорошей эффективностью превращения мономера в полимер. 7 н. и 8 з.п. ф-лы, 7 табл.
; m обозначает 1; n обозначает 1; Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил, фенил или бензил, или Y и Y' совместно образуют одну из следующих двухвалентных групп: -C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, -CH2-CH=CH-CH2-; где R1 обозначает водородный атом, С1-С12алкил, СОО-(С1-С12)алкил или CH2OR4; R2 и R3 каждый независимо обозначает водородный атом, метил, этил, или СОО-(С1-С12)алкил; R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный ацильный остаток алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 12 углеродных атомов; и один R12 обозначает Н, а другой СН3. Также описываются способная полимеризоваться композиция, способ получения олигомера, соолигомера, полимера или сополимера, полимер, применение соединения формулы Ia, IIa или IIIa для полимеризации этиленовоненасыщенных мономеров, применение соединения формулы Ia, IIa или IIIa для обрыва цепи анионной полимеризации диенового или винилового мономера, соединения формул Xd, XId и XIId. Технический результат - соединения по настоящему изобретению обеспечивают получение полимерных смолистых продуктов, обладающих низкой полидисперсностью, и протекание процесса полимеризации с хорошей эффективностью превращения мономера в полимер. 7 н. и 8 з.п. ф-лы, 7 табл.



где D обозначает группу  ;
;
m обозначает 1;
n обозначает 1;
Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил,
фенил или бензил, или
Y и Y' совместно образуют одну из следующих двухвалентных групп:
-C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, -CH2-CH=CH-CH2-;
где R1 обозначает водородный атом, С1-С12алкил, СОО-(С1-С12)алкил или CH2OR4;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил, или СОО-(С1-С12)алкил;
R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный
ацильный остаток алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 12 углеродных атомов;
один R12 обозначает Н, а другой СН3.
где D обозначает группу  ;
;
m обозначает 1;
n обозначает 1;
Y и Y' совместно образуют одну двухвалентную группу:
-CH2-C(R1)(R2)-СН)(R3)-;
где R1 обозначает водородный атом, метил или этил;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил или СОО-(С1-С12)алкил;
и один из R12 обозначает водородный атом, а другой обозначает метил.
7,9-диэтил-6,7,9-триметил-8-[1-(4-оксиранилметоксифенил)этокси]-1,4-диокса-8-азаспиро[4.5]декан;
8,10-диэтил-3,3,7,8,10-пентаметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекан;
{8,10-диэтил-3,7,8,10-тетраметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундец-3-ил}метанол;
{3,8,10-триэтил-7,8,10-триметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундец-3-ил)метанол;
4,4-дибутокси-2,2-диэтил-6,6-диметил-1-[1-(4-оксиранилметоксифенил)этокси]пиперидин;
7,7-диэтил-9,9-диметил-8-[1-(4-оксиранилметоксифенил)этокси]-1,4-диокса-8-азаспиро[4.5]декан;
8,8-диэтил-3,3,10,10-тетраметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекан;
{8,8-диэтил-3,10,10-триметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундец-3-ил}метанол;
{3,8,8-триэтил-10,10-диметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундец-3-ил}метанол;
4,4-дибутокси-2,2,6,6-тетраметил-1-[1-(4-оксиранилметоксифенил)этокси]пиперидин;
7,7,9,9-тетраметил-8-[1-(4-оксиранилметоксифенил)этокси]-1,4-диокса-8-азаспиро[4.5]декан или
3,3,8,8,10,10-гексаметил-9-[1-(4-оксиранилметоксифенил)этокси]-1,5-диокса-9-азаспиро[5.5]ундекан.
а) по меньшей мере один этиленово-ненасыщенный мономер или олигомер и
б) соединение формулы Ia, IIa или IIIa



где D обозначает группу  ;
;
m обозначает 1;
n обозначает 1;
если n обозначает 1,
Y и Y' каждый независимо обозначает С1-С12алкил, С3-С12алкенил,
фенил или бензил, или
Y и Y' совместно образуют одну из следующих двухвалентных групп:
-C(R1)(R2)-CH(R3)-, -CH(R1)-CH2-C(R2)(R3)-, -CH(R2)-CH2-C(R1)(R3)-, -CH2-C(R1)(R2)-CH(R3)-, -CH2-CH=CH-CH2-;
где R1 обозначает водородный атом, С1-С12алкил, СОО-(С1-С12)алкил или OH2OR4;
R2 и R3 каждый независимо обозначает водородный атом, метил, этил или СОО-(С1-С12)алкил;
R4 обозначает водородный атом, С1-С12алкил, бензил или одновалентный ацильный остаток алифатической, циклоалифатической или ароматической монокарбоновой кислоты, содержащей до 12 углеродных атомов;
один R12 обозначает Н, а другой СН3.
 причем радикал способен инициировать полимеризацию.
причем радикал способен инициировать полимеризацию. и по меньшей мере одну оксиаминогруппу формулы Ib, IIb или IIIb
и по меньшей мере одну оксиаминогруппу формулы Ib, IIb или IIIb


где n, Y и Y' имеют значения, указанные в п.1, который может быть получен согласно способу по п.10.



где Y, Y', R12 и n имеют значения, указанные в п.1.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| ЭТИЛЕНОВО-НЕНАСЫЩЕННЫЕ ПОЛИМЕРИЗУЮЩИЕСЯ МОНОМЕРЫ НА ОСНОВЕ ПРОИЗВОДНОГО ПИПЕРИДИНА | 1992 |
|
RU2086540C1 |
Авторы
Даты
2006-08-10—Публикация
2001-11-12—Подача