Изобретение относится к области медицины, а именно к криохирургии, и может найти применение при хирургическом лечении ранений поджелудочной железы.
Известен способ лечения ран поджелудочной железы путем тампонирования места ранения и подведения дренажа к ране железы (см. книгу Лубенский Ю.М., Нихинсон Р.А., Гульман М.И. Повреждения поджелудочной железы. - Красноярск: Издательство Красноярского университета, 1983, 157 с.) и способ лечения данного вида травм поджелудочной железы путем использования различных пластических материалов (сальник, синтетические и биологические клеи, пленки) для герметизации раны железы (см. Методика операций при травмах поджелудочной железы. Метод. рекомендации. - Л.: Изд-во Ленинградского НИИ СП им. И.И.Джанелидзе, 1985, 8 с.).
Основными недостатками известных способов являются частое развитие осложнений в послеоперационном периоде, длительное нахождение больного в стационаре, высокие показатели летальности, а также высокая стоимость метода с использованием пластических материалов.
Эти недостатки обусловлены тем, что:
- в большинстве случаев осложнения (панкреонекроз, формирование панкреатических свищей, кист, ферментативный перитонит, парапанкреатит) формируются ввиду агрессивных свойств панкреатического сока;
- длительное пребывание больного в стационаре обусловлено частым развитием послеоперационных осложнений и необходимостью, в некоторых случаях, выполнения повторных хирургических вмешательств;
- высокий процент летальных исходов обусловлен развитием тяжелых осложнений в послеоперационном периоде.
- необходимость использования специальных пластических материалов ведет к значительному увеличению затрат на лечение категории больных с ранениями поджелудочной железы.
Известен также способ разрушения биологических тканей, включающий воздействие холодом, при этом одновременно дополнительно воздействуют вибрацией с частотой 50 Гц и амплитудой 0,8-1,5 нм (см. А.С. СССР №1827194, МПК А 61 В 17/36, опубл. 15.07.93. Бюл. №26).
Основными недостатками приведенного способа являются развитие сахарного диабета, большое число осложнений, высокая себестоимость метода.
Эти недостатки обусловлены тем, что:
- не учитывается разность критических температур для различных тканей, что приводит к гибели, как экзо-, так и эндокринной ткани железы,
- воздействие холодом одновременно с вибрацией увеличивает повреждающее действие низких температур, что приводит к выраженной деструкции не только тканей железы, но и окружающих органов,
- для осуществления метода необходимо наличие дорогостоящей аппаратуры;
Известен, принятый за прототип, способ деструкции биологической ткани путем последовательного многократного замораживания и отогрева патологически измененного участка, заключающийся в последовательном многократном замораживании и отогреве патологически измененной ткани, осуществляемым только на границе со здоровой тканью до температуры фазового превращения лед - жидкость без отогрева всего замороженного участка (см. А.С. СССР №1553087, МПК А 61 В 17/36, опубл. 30.03.90. Бюл. №12).
Основными недостатками этого способа являются развитие эндокринной недостаточности поджелудочной железы, высокая частота развития осложнений, большая себестоимость метода.
Данные недостатки обусловлены тем, что:
- не учитывается разность критических температур для различных тканей, что приводит к гибели как экзо-, так и эндокринной ткани, что в свою очередь приводит к развитию эндокринной недостаточности железы;
- многократное замораживание и отогрев тканей увеличивает повреждающее действие низких температур, что приводит к более выраженной деструкции не только тканей железы, но и окружающих органов;
- высокая себестоимость метода обусловлена необходимостью наличия дорогостоящей аппаратуры.
Техническим результатом заявляемого изобретения является снижение себестоимости операции, снижение числа послеоперационных осложнений и летальности, а также сокращение времени пребывания больного в стационаре.
Поставленный технический результат достигается тем, что в известном способе лечения ран поджелудочной железы, включающем воздействие холодом, согласно изобретению первоначально проводили обработку операционного поля, после чего выполняли верхне-срединную лапаротомию, затем воздействовали на переднюю поверхность поджелудочной железы 1 вдоль оси х-х раны 3 холодом, используя в качестве хладагента жидкий азот, при этом с помощью криоаппликатора производили последовательно один или более циклов криовоздействия в зависимости от размеров раны поджелудочной железы и проводили полную криогенную деструкцию участка ткани поджелудочной железы, причем процесс упомянутой полной криогенной деструкции проводили, по меньшей мере, два раза, после чего лапаротомную рану ушивали, а сальниковую сумку дренировали, при этом, одно криовоздействие проводили в течение 3-5 минут, каждое криовоздействие проводили на расстоянии между точками воздействия криоаппликатора, равном 26-28 мм (а), на расстоянии от стенки 3 двенадцатиперстной кишки до криоаппликатора, равном 20,5-21,5 мм (в), время наполнения рабочей части криоаппликатора при погружении в хладагент составляло 1-3 сек, кроме того, лапаротомную рану ушивали наглухо, сальниковую сумку дренировали силиконовой трубкой через контрапертуру в правом подреберье.
Между отличительными признаками и достигнутым техническим результатом существует следующая причинно-следственная связь.
В отличие от аналогов и прототипа в предлагаемом изобретении сокращается число послеоперационных осложнений, поскольку, в подавляющем большинстве случаев, осложнения после ушивания, тампонирования или использования различных пластических материалов (панкреатические свищи, кисты, ферментативный перитонит, парапанкреатит, панкреонекроз) формируются ввиду высокой агрессивности панкреатического сока. При воздействии низкими температурами одновременно с вибрацией или многократном замораживании и отогреве тканей не учитывается разность критических температур для различных тканей, что приводит к гибели как экзо-, так и эндокринной ткани железы, а также воздействие низкими температурами одновременно с вибрацией или многократное замораживание и отогрев тканей увеличивает повреждающее действие низких температур, что приводит к более выраженной деструкции не только тканей поджелудочной железы, но и соседних органов. В предлагаемом же способе криодеструкция экзокринной паренхимы (исключается воздействие агрессивного панкреатического сока) и сохранение эндокринной части (не развивается сахарный диабет) обеспечивается оригинальной методикой криовоздействия, а именно воздействием на поджелудочную железу холодом, используя в качестве хладагента жидкий азот, с помощью криоаппликатора на передней поверхности поджелудочной железы 1 вдоль оси х-х раны 3 производили последовательно один или более упомянутых выше циклов криовоздействия, в зависимости от размеров раны поджелудочной железы, проводя полную криогенную деструкцию участка ткани поджелудочной железы, и специально разработанными параметрами криовоздействия, а именно то, что одно криовоздействие проводили в течение 3-5 минут, каждое криовоздействие проводили на расстоянии между точками воздействия криоаппликатора, равном 26-28 мм (а), на расстоянии от стенки 2 двенадцатиперстной кишки до криоаппликатора, равном 20,5-21,5 мм (в), при этом время наполнения рабочей части криоаппликатора при погружении в хладагент составляло 1-3 сек. Значительное сокращение послеоперационных осложнений позволяет снизить затраты на лечение данной категории больных и одновременно длительность пребывания больного в стационаре, обусловленного, в объектах-аналогах и прототипе, развитием тяжелых послеоперационных осложнений, необходимостью в некоторых случаях производить повторные операции ввиду частого развития послеоперационных осложнений (при ушивании, тампонировании, применении пластических материалов, воздействии низкими температурами одновременно с вибрацией или многократном замораживании и отогреве тканей). Кроме того, в предложенном способе исключена необходимость в специальных пластических материалах, использование которых для герметизации раны железы ведет к значительному увеличению затрат на лечение данной категории больных. Воздействие низкими температурами одновременно с вибрацией или многократное замораживание и отогрев тканей также значительно увеличивает себестоимость операции вследствие необходимости наличия специальной аппаратуры, что ведет к повышению себестоимости лечения больных с данным видом травмы, а в предлагаемом способе это исключено, т.е. при использовании предлагаемого способа частота осложнений значительно снижается, больные меньше находятся в стационаре, нет необходимости в специальной дорогостоящей технике. Кроме того, низкий процент послеоперационных осложнений, вследствие исключения действия агрессивного панкреатического сока на окружающие ткани, сохранения эндокринной функции, сокращает сроки пребывания больных в стационаре и позволяет снизить процент летальности.
По имеющимся у заявителя сведениям, совокупность существенных признаков заявляемого изобретения «Способ лечения ран поджелудочной железы» не известна из уровня техники, что позволяет сделать вывод о соответствии заявляемого изобретения критерию "новизна".
По мнению заявителя, сущность заявляемого изобретения «Способ лечения ран поджелудочной железы» не следует главным образом из известного уровня техники, так как из него не выявляется вышеуказанное влияние на достигаемый технический результат - новое свойство объекта - совокупности признаков, которые отличают от прототипа заявляемое изобретение, что позволяет сделать вывод о его соответствии критерию "изобретательский уровень".
Совокупность существенных признаков, характеризующих сущность изобретения «Способ лечения ран поджелудочной железы», может быть многократно использована в стационарах любого уровня технической оснащенности, что позволяет сделать вывод о его соответствии критерию «промышленная применимость».
Сущность заявляемого изобретения поясняется примером конкретного выполнения и схемой криовоздействия при ранении поджелудочной железы без повреждения Вирсунгова протока.
Способ лечения ран поджелудочной железы осуществляли следующим образом.
В условиях операционной под наркозом после предварительной обработки операционного поля выполняли верхне-срединную лапаротомию. После чего криоаппликатор погружали в сосуд Дюара с жидким азотом (хладагент) непосредственно перед манипуляцией, время наполнения рабочей части криоаппликатора при погружении его в хладагент составило две секунды (1-3 секунды). После этого на переднюю поверхность поджелудочной железы 1 устанавливали криоаппликатор таким образом, чтобы рабочая поверхность его плотно прилегала к поверхности органа. Расстояние (а) между точками воздействия криоаппликатора составляло двадцать семь мм (26-28 мм), а стенка 2 двенадцатиперстной кишки располагалась на расстоянии (b) от криодеструктора, которое равнялось двадцати одному мм (20,5-21,5 мм). Затем производили последовательно вдоль оси х-х раны 3 необходимое количество циклов воздействия в зависимости от размеров раны поджелудочной железы (одно погружение криоаппликатора в резервуар с хладагентом и один контакт рабочей поверхности с поверхностью поджелудочной железы составляют один цикл воздействия). Экспозиция одного криовоздействия при осуществлении способа составила четыре минуты (3-5 минут). Согласно данным Э.И.Канделя, учитывая высокую резистентность стенки крупных сосудов к низкой температуре, возможно безопасное произведение криодеструкции тканей в непосредственной близости к этим сосудам (см. книгу Кандель Э.И. Криохирургия. М.: Медицина, 1974. - 303 с.). Полная криогенная деструкция участка ткани поджелудочной железы осуществлялась путем одного или последовательного многократного проведения описанного цикла в зависимости от размеров раны. Время криовоздействия регистрировали секундомером. После криодеструкции и раны поджелудочной железы ушивали наглухо лапаротомную рану и дренировали сальниковую сумку силиконовой трубкой через контрапертуру в правом подреберье.
В послеоперационном периоде проводилось динамическое наблюдение за состоянием больного. С целью контроля функции поджелудочной железы в послеоперационном периоде производили также забор крови для проведения общего анализа крови и биохимического анализа (билирубин, амилаза, сахар, АЛТ, ACT, кальций).
Экспериментально установлено, что именно заявляемые параметры криовоздействия на ткань поджелудочной железы при ранении поджелудочной железы способствуют решению поставленных перед изобретением задач, т.е. созданию эффективного, достаточно простого способа лечения ран поджелудочной железы.
Применение заявляемого изобретения позволило снизить себестоимость операций, снизить число послеоперационных осложнений и летальность, а также сократить время пребывания больного в стационаре.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ПОЛНОГО ПОПЕРЕЧНОГО РАЗРЫВА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2003 |
|
RU2261055C2 |
| СПОСОБ ГИПОТЕРМИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 1994 |
|
RU2110219C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРАВМЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2007 |
|
RU2358658C2 |
| СПОСОБ ЛЕЧЕНИЯ ПАНКРЕОНЕКРОЗА | 2000 |
|
RU2188045C2 |
| СПОСОБ ЛЕЧЕНИЯ КИСТОЗНЫХ ДОБРОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2015 |
|
RU2599875C1 |
| СПОСОБ ЛОКАЛЬНОЙ ДЕСТРУКЦИИ ПЕРВИЧНЫХ И МЕТАСТАТИЧЕСКИХ НОВООБРАЗОВАНИЙ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ И ЗАБРЮШИННОГО ПРОСТРАНСТВА С ЛАПАРОСКОПИЧЕСКИМ ДОСТУПОМ | 2021 |
|
RU2770279C1 |
| ЛАПАРОСКОПИЧЕСКИЙ СПОСОБ УДАЛЕНИЯ ЛОЖНЫХ И ИСТИННЫХ КИСТ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ | 2014 |
|
RU2547778C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПАНКРЕАТИТА | 2009 |
|
RU2421158C1 |
| СПОСОБ ПРОФИЛАКТИКИ ГНОЙНЫХ ОСЛОЖНЕНИЙ ПРИ ИЗОЛИРОВАННОЙ РЕЗЕКЦИИ ГОЛОВКИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2454942C1 |
| СПОСОБ ОБРАБОТКИ ПУНКЦИОННО-ДРЕНАЖНОГО КАНАЛА У БОЛЬНЫХ С ПАРАЗИТАРНЫМ ПОРАЖЕНИЕМ ПЕЧЕНИ ПОСЛЕ ДРЕНИРОВАНИЯ ПОЛОСТИ РАСПАДА | 2023 |
|
RU2811279C1 |
Изобретение относится к медицине, а именно к хирургии в лечении поджелудочной железы. Сущность: после верхне-срединной лапаротомии осуществляют воздействие жидким азотом на переднюю поверхность поджелудочной железы вдоль раны, криовоздействие проводят на расстоянии от стенки двенадцатиперстной кишки до криоаппликатора, равном 26-28 мм, одно воздействие проводят в течение 3-5 минут, лапаротомную рану ушивают наглухо, сальниковую сумку дренируют силиконовой трубкой через контрапертуру в правом подреберье, что исключает воздействие панкреатического сока на ткань железы, сохраняет эндокринную функцию железы. 1 ил.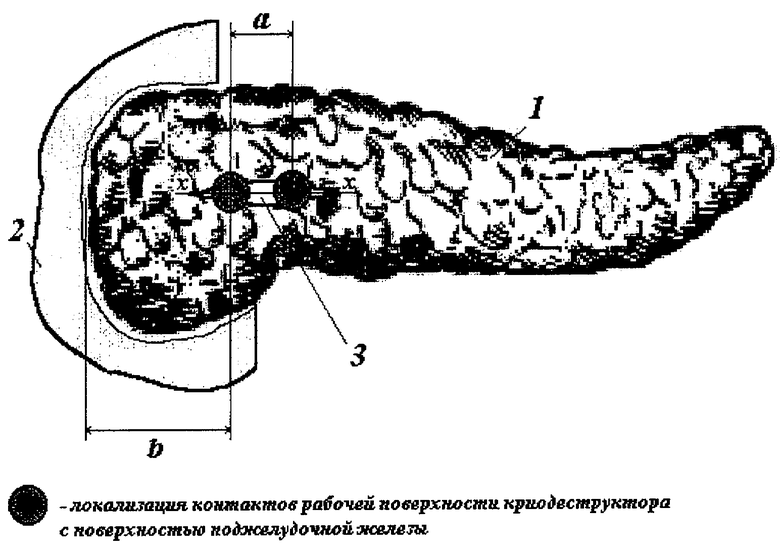
Способ лечения ран поджелудочной железы, включающий дренирование сальниковой сумки, ушивание лапаротомной раны, отличающийся тем, что после верхне-срединной лапаротомии осуществляют воздействие жидким азотом на переднюю поверхность поджелудочной железы вдоль раны, криовоздействие проводят на расстоянии от стенки двенадцатиперстной кишки до криоаппликатора, равном 26-28 мм, одно воздействие проводят в течение 3-5 мин, лапаротомную рану ушивают наглухо, сальниковую сумку дренируют силиконовой трубкой через контрапертуру в правом подреберье.
| СПОСОБ ЛЕЧЕНИЯ ТРАВМЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 1998 |
|
RU2166288C2 |
| Способ деструкции биологической ткани | 1983 |
|
SU1553087A1 |
| Способ лечения острого деструктивного панкреатита | 1981 |
|
SU1113096A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ДЕСТРУКТИВНЫХ ФОРМ ПАНКРЕАТИТА | 1994 |
|
RU2123806C1 |
| Способ криохирургического лечения | 1980 |
|
SU997671A1 |
| Способ лечения панкреатита | 1984 |
|
SU1344332A1 |
| Клиническая хирургия | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| Клиническая хирургия | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| ВАШЕТКО Р.В | |||
| Острый панкреатит и травмы поджелудочной железы | |||
| Питер, 2000, с.95-107, 192-222, 227-295. | |||
Авторы
Даты
2006-09-10—Публикация
2004-02-24—Подача