Данное изобретение относится к нуклеотидным последовательностям, которые участвуют в увеличении или уменьшение скорости овуляции у млекопитающих.
В частности, изобретение, в общем, касается новых мутаций в гене, который участвует в увеличении скорости овуляции у гетерозиготных особей женского пола млекопитающих; указанные мутации вызывают стерильность гомозиготных особей женского пола млекопитающих. Знание мутантной генной последовательности можно использовать в тесте по идентификации гетерозиготных или гомозиготных млекопитающих женского и мужского пола, несущих мутантный ген. Указанные сведения о биологической функции гена и его мутациях можно также использовать для того, чтобы увеличить или уменьшить скорость овуляции у особей женского пола млекопитающих, или для того, чтобы индуцировать стерильность или пониженную плодовитость млекопитающих женского пола.
ПРЕДПОСЫЛКА ИЗОБРЕТЕНИЯ
Все ссылки, включая любые патенты или патентные заявки, цитированные в данном описании, включены здесь в виде ссылки. Не делается допущения, что любая ссылка составляет предшествующий уровень техники. При обсуждении ссылок констатируется то, о чем утверждают их авторы, и заявители сохраняют право высказать сомнение в точности и релевантности цитированных документов. Будет совершенно понятно, что хотя здесь приведены ссылки на ряд публикаций предшествующего уровня техники, данное упоминание не является признанием того, что любой из указанных документов составляет часть основных общепринятых знаний в данной области в Новой Зеландии или какой-либо другой стране.
Ген высокой плодовитости Inverdale (FecXI) является основным геном плодовитости у овец, который впервые идентифицировали в отаре Ромни (Inverdale), состоящем из потомков овцы Ромни (А281), все из которых единообразно имели высокий по численности приплод. Исследования по расщеплению генов показали, что ген несет Х-хромосома (Davis et al., 1991). Одна копия гена у гетерозиготных овец I+ увеличивает скорость овуляции примерно на одну дополнительную яйцеклетку, и численность приплода примерно на 0,6 ягнят на окот овцы. Однако гомозиготные овцы II, несущие две копии гена, имеют небольшие нефункциональные яичники и являются бесплодными (Davis et al., 1992). Исследования эмбрионов овец I+ и II показали, что развитие яичников является нормальным примерно до 100 дня эмбриональной жизни: развитие эмбриональных клеток, формирование фолликулов яичника и самые ранние стадии роста фолликулов являются нормальными. Однако у эмбрионов II после 100 дня эмбриональной жизни нарушается развитие фолликулов после первичной стадии роста, и не обнаруживаются нормальные вторичные фолликулы (Smith et al., 1997). Между тем, как ооциты у животных II увеличиваются в диаметре (>40 мкм), нет данных о пролиферации зернистых клеток, в отличие от пролиферации, которая наблюдалась бы в норме (Braw-Tal et al., 1993; McNatty et al., 1995a; Smith et al., 1997). Таким образом, наличие инфантильных нефункциональных яичников у эмбрионов, новорожденных и взрослых животных II является следствием блокирования развития фолликулов после первичной стадии роста.
Также показано, что вторая плодовитая отара Ромни (Hanna, 1995), для которой известно родство с отарой Inverdale, несет Х-сцепленную мутацию с фенотипом, подобным Inverdale. Подтверждение того, что животные Hanna несли мутацию (FecXH) в гене Inverdale, получили, когда при скрещивании барана носителя Inverdale с овцами носительницами Hanna получили гомозиготных стерильных самок (Davis et al., 1995). Указанную линию Hanna содержали в Invermay в виде отдельной группы бок о бок с исходной линией Inverdale.
В качестве части поиска гена, ответственного за признак Inverdale, авторы изобретения сконструировали карту генетического сцепления Х-хромосомы овцы (Galloway et al., 1996), и локализовали ген Inverdale в районе 10 сМ, фланкированном минисателлитными маркерами (Galloway et al., 1999). Локализация гена в Х-хромосоме овец сузила поиск кандидатов на те гены, которые картированы в других Х-хромосомах млекопитающих, поскольку, почти без исключения, гены, присутствующие в Х-хромосоме одного млекопитающего, также присутствуют в Х-хромосомах других видов млекопитающих (Ohno, 1973).
Наследование гена Inverdale по Х-хромосоме предоставляет удобный способ получения плодовитых овец - носителей одной копии Inverdale, поскольку все дочери барана носителя Inverdale будут наследовать ген. Специалист по разведению баранов использует генетический маркер для того, чтобы идентифицировать баранов-носителей для продажи, а коммерческие специалисты по разведению покупают этих баранов, чтобы получить плодовитых овец, которых затем спаривают с конечным производителем с получением потомства для забоя. Показано, что коммерческое использование гена Inverdale является высоко прибыльным в существующей системе конечного спаривания с добавленной стоимостью, равной 1760$ на одного купленного барана Inverdale, по сравнению с обычным бараном (Amer et al., 1998). Для получения элитных баранов-производителей, несущих ген, необходимо различать не носителей (самок ++ или самцов +Y) и носителей одной копии (самок I+ или самцов IY).
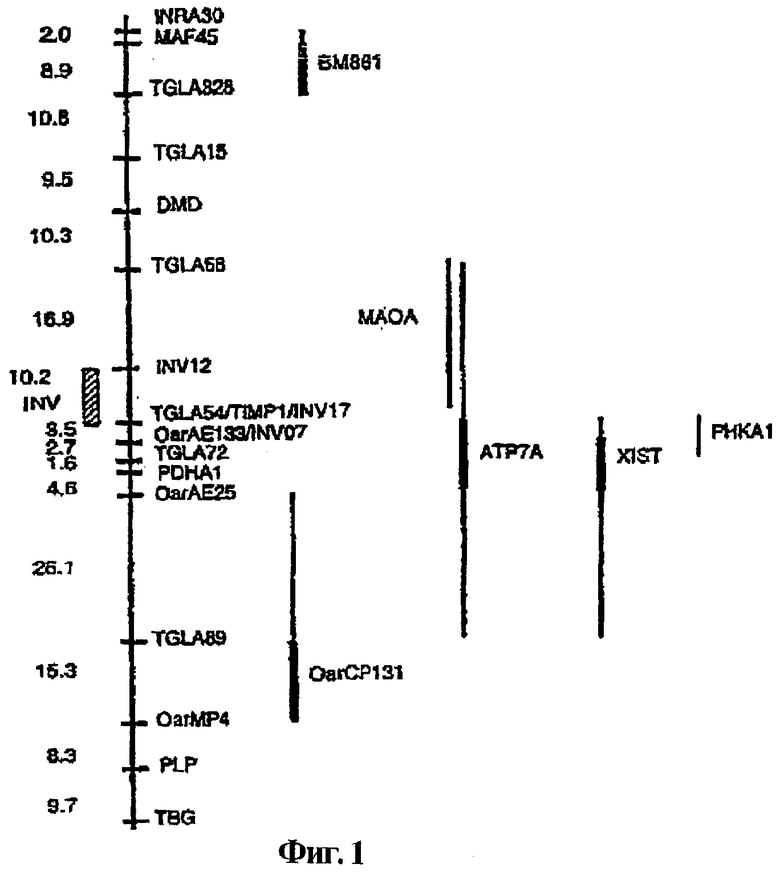
Тест с генетическим маркером разработали на основе наследования фланкирующих минисателлитных маркеров вокруг гена (т.е. тест на гаплотип) (Galloway et al., 1999); он показан на фигуре 1. Однако в данном тесте можно только идентифицировать тех животных, которые унаследовали гаплотип Inverdale от известного носителя, и не является точным на 100%, так как в тесте не выявляется ген Inverdale как таковой. Гаплотип из того же самого района Х-хромосомы овцы родословной Hanna, которая несет неродственный вариант Inverdale, отличался от гаплотипа, наблюдаемого в потомстве А281.
В 1996 году показали, что фактор роста и дифференцировки 9 (GDF-9), член суперсемейства трансформирующего фактора роста бета (TGF-β), специфично экспрессируется в ооците взрослой мыши, где он необходим для фолликулогенеза (Dong et al., 1996). Матричная РНК GDF-9 синтезируется только в ооците, начиная со стадии примордиального/первичного однослойного фолликула вплоть до периода после овуляции, и самки мышей, нокаутированных по GDF-9, стерильны вследствие блокирования развития фолликулов на этой стадии первичного однослойного фолликула. Животные, гомозиготные по гену Inverdale, стерильны с фенотипом, подобным фенотипу мыши, нокаутированной по GDF-9 (McNatty et al., 1995b). Затем GDF-9 картировали на хромосоме 5 овцы, и поэтому ген не может быть ответственным за фенотип Inverdale (Sadighi et al., 1998).
Второй родственный член семейства, GDF-9B, также называемый ВМР15, идентифицировали в яичниках мыши и человека, и обнаружили, что он совместно экспрессируется с GDF-9 (Laitinen et al., 1998; Dube et al., 1998). ВМР15 картировали у мышей на Х-хромосоме, вблизи Fsc1 (Dube et al., 1998). Fsc1 (компонент фиброзной оболочки) также известен как Akap4 (белок 4 якоря киназы А), который был картирован на Х-хромосоме мыши на расстоянии 1,6 сМ от центромеры (база данных генома мыши (MGD), октябрь 1999) и в полосе р11,2 Х-хромосомы человека (Dube et al., 1998). Предварительные исследования овцы Inverdale (генотипов ++, I+ и II) с использованием молекулярного зонда, который не делает различий между генотипами, показывают, что мРНК GDF-9B экспрессируется в ооцитах первичных, но не примордиальных фолликулов, и что экспрессия указанной мРНК в яичнике ограничена ооцитами (Galloway et al., 2000).
Члены суперсемейства TGF-β имеют сходные структуры генов. Район, кодирующий GDF-9B, находится в пределах двух экзонов, разделенных интроном длиной 4,2 т.п.н (человек) и 3,5 т.п.н. (мышь) (Dube et al., 1998). У людей полноразмерная кодирующая последовательность из 1176 п.н. продуцирует препропептид из 392 аминокислот, из которых первые 17 аминокислот соответствуют секреторному сигналу. Полноразмерный препропептид человека и мыши содержит сайт процессинга для протеолитического расщепления с высвобождением зрелого активного С-концевого пептида из 125 аминокислот и N-концевого продукта пропептида (Laitinen et al., 1998; Dube et al., 1998). Последовательность интрона находится в домене пропептида, так что полный зрелый кодирующий район обнаруживается в экзоне 2.
Последовательность гена ВМР15 (GDF-9B) человека дикого типа описана в патентах США 5728679 и 5635372. Белок дикого типа описан как пригодный для лечения дефектов кости и хряща и/или других соединительных тканей, и в заживлении ран и репарации тканей.
Авторы изобретения в настоящее время идентифицировали мутантную форму гена GDF-9B овцы у овец, экспрессирующих фенотип Inverdale или Hanna, и впервые обнаружили, что данная мутантная форма GDF-9B ответственна за повышенную овуляцию, наблюдаемую у данных овец, и за стерильность, наблюдаемую у гомозиготных овец.
Данное изобретение, в общем, направлено на мутантную последовательность и соответствующий кодируемый белок.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Таким образом, в первом аспекте данное изобретение относится к выделенной мутантной молекуле нуклеиновой кислоты GDF-9B, содержащей нуклеотидную последовательность, выбранную из группы, состоящей из:
а) SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5 или SEQ ID NO:7;
b) последовательности, способной гибридизоваться в жестких условиях с молекулой(ами) по (а);
с) последовательности, которая является функциональным вариантом или фрагментом молекулы(ул), определенной в (а);
d) последовательности, комплементарной молекуле(ам), определенной в (а), (b) или (с); и
e) антисмысловой последовательности, соответствующей любой из молекул(ы) по (а) - (d).
Молекула нуклеиновой кислоты может представлять собой молекулу РНК, кРНК, геномной ДНК или кДНК и может быть одно- или двуцепочечной. Молекула нуклеиновой кислоты также необязательно может включать одно или более синтетических неприродных или измененных нуклеотидных оснований, или их комбинацию.
Данное изобретение, кроме того, относится к способу идентификации млекопитающего, который несет мутантную молекулу нуклеиновой кислоты GDF-9B, при этом указанный способ включает следующие стадии:
(i) получение образца ткани или крови от млекопитающего;
(ii) выделение ДНК из образца;
(iii) необязательно выделение ДНК GDF-9B из ДНК, полученной на стадии (i);
(iv) необязательно исследование ДНК с помощью зонда, комплементарного мутантной ДНК GDF-9B согласно изобретению;
(v) необязательно амплификацию количества мутантной ДНК GDF-9B и
(vi) определение того, несет ли последовательность ДНК GDF-9B, полученная на стадии (ii), мутацию, связанную со стерильностью или с увеличением или снижением овуляции.
Предпочтительно стадию амплификации (v) можно выполнить любым традиционным способом, таким как полимеразная цепная реакция или лигазная цепная реакция.
Согласно еще одному аспекту данное изобретение относится к генетическому маркеру для связанной с ДНК селекции в отношении повышенной овуляции или стерильности у млекопитающего, содержащему молекулу нуклеиновой кислоты, которая специфично гибридизуется с нуклеотидной последовательностью согласно первому аспекту изобретения, или с геномной ДНК, включающей или связанной с мутантной молекулой нуклеиновой кислоты GDF-9B.
Млекопитающее может быть мужского или женского пола и может быть человеком, или домашним, проживающим вместе с человеком, зоопарковым или диким млекопитающим. Предпочтительно млекопитающее выбрано из людей, овец, крупного рогатого скота, коз, оленей, лошадей, верблюдов, опоссумов, свиней, мышей, крыс, ласок, кроликов, зайцев, хорьков, кошек и собак.
В следующем аспекте данное изобретение относится к выделенному полипептиду, кодируемому молекулой нуклеиновой кислоты, имеющей последовательность, представленную выше в (а)-(d). Предпочтительно полипептид имеет аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6 и SEQ ID NO:8, или ее функциональный вариант или фрагмент.
Еще в одном аспекте изобретение относится к выделенному полипептиду, имеющему аминокислотную последовательность, включающую SEQ ID NO:10, или его функциональному варианту или фрагменту.
В дополнительном аспекте изобретение относится к выделенной молекуле нуклеиновой кислоты, имеющей нуклеотидную последовательность, включающую SEQ I NO:9, или ее функциональному фрагменту или варианту.
В еще одном аспекте изобретение относится к выделенной молекуле нуклеиновой кислоты, которая кодирует полипептид, по существу такой, как описано выше.
В следующем аспекте изобретение относится к способу модулирования скорости овуляции у млекопитающего женского пола, при этом указанный способ включает стадию введения указанному млекопитающему эффективного количества мутантного полипептида GDF-9B, полипептида GDF-9B дикого типа или функционального фрагмента или варианта каждого из них.
Изобретение также относится к способу увеличения скорости овуляции у млекопитающего женского пола, который не несет мутантной молекулы нуклеиновой кислоты GDF-9B, включающему стадию введения указанному млекопитающему эффективного количества мутантного полипептида GDF-9B или его функционального варианта или фрагмента.
Кроме того, изобретение также относится к способу увеличения скорости овуляции у стерильной особи женского пола млекопитающего, которая несет две копии мутантной молекулы нуклеиновой кислоты GDF-9B, включающему стадию введения указанному млекопитающему эффективного количества полипептида GDF-9B дикого типа.
В еще одном аспекте изобретение относится к способу увеличения или уменьшения скорости овуляции или индукции стерильности у особи женского пола млекопитающего, включающему стадию введения эффективного количества агента, выбранного из группы, состоящей из:
а) эффективно иммунизирующего количества полипептида GDF-9B дикого или мутантного типа, или его функционального фрагмента или варианта;
b) антисмысловой молекулы нуклеиновой кислоты, направленной против ДНК, кодирующей полипептид GDF-9B дикого или мутантного типа или его функциональный фрагмент или вариант;
с) лиганда, который связывается с или является антигеном к полипептиду GDF-9B дикого или мутантного типа, или его функциональному фрагменту или варианту;
чтобы таким образом ингибировать биологическую активность полипептида GDF-9B мутантного или дикого типа.
В еще одном аспекте изобретение относится к композиции, содержащей эффективное количество мутантного полипептида GDF-9B или его функционального фрагмента или варианта, вместе с фармацевтически или ветеринарно приемлемым носителем или разбавителем.
В еще одном аспекте изобретение относится к композиции, содержащей эффективное количество агента, выбранного из группы, состоящей из:
а) мутантного полипептида GDF-9B согласно изобретению;
b) полипептида GDF-9B дикого типа согласно изобретению;
с) антисмысловой молекулы нуклеиновой кислоты, направленной против полипептида GDF-9B дикого или мутантного типа согласно изобретению;
d) лиганда, который связывается с или является антигеном к полипептиду GDF-9B дикого или мутантного типа согласно изобретению;
вместе с фармацевтически или ветеринарно приемлемым носителем или разбавителем.
Согласно еще одному аспекту изобретение относится к конструкции или вектору, содержащему молекулу нуклеиновой кислоты по существу такую, как описано выше.
Данное изобретение также относится к клетке-хозяину, трансформированной вектором или конструкцией, содержащей молекулу нуклеиновой кислоты согласно изобретению.
Согласно следующему аспекту изобретение относится к выделенной молекуле нуклеиновой кислоты, содержащей нуклеотидную последовательность, выбранную из группы, состоящей из SEQ ID NO:12 или SEQ ID NO:14, или ее функционально активному фрагменту или варианту.
Изобретение также относится к выделенному полипептиду, содержащему аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:13 и SEQ ID NO:15.
В еще одном аспекте изобретение относится к выделенному функционально активному варианту полипептида, который представлен в SEQ ID NO:11.
Согласно следующему аспекту данного изобретения представлена выделенная молекула нуклеиновой кислоты, содержащая последовательность нуклеиновой кислоты, которая представлена в SEQ ID NO:16.
Данное изобретение также относится к выделенному полипептиду, содержащему аминокислотную последовательность, которая представлена в SEQ ID NO:17.
Изобретение также охватывает способ уменьшения скорости овуляции или индукции стерильности у опоссума, который включает стадию введения эффективного количества полипептида, имеющего аминокислотную последовательность, которая представлена в SEQ ID NO:17, или его функционального варианта или фрагмента.
Несмотря на то, что изобретение в общих чертах определено выше, специалистам в данной области будет понятно, что оно этим не ограничено, и что изобретение также включает предпочтительные варианты, которые приведены ниже в виде примеров.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
В частности, предпочтительные аспекты изобретения будут описаны в связи с сопровождающими чертежами, где:
На фигуре 1 показана карта генетического сцепления Х-хромосомы овцы. Генетические расстояния даны в сантиморганах (сМ) по Kosamabi. Ген Inverdale картирован в районе, указанном заштрихованным столбиком.
На фигуре 2а показана нуклеотидная последовательность экзона 2 GDF-9B овцы Inverdale. Положение замены нуклеотида Т на А в Inverdale (на расстоянии 92 нуклеотидов от сайта процессинга) указано жирным шрифтом. Триплетный кодон, затронутый данной заменой, подчеркнут. Сайт процессинга для протеолитического отщепления пропептида от зрелого фрагмента и стоп-кодон TGA обведены рамкой. Кодирующая последовательность зрелого пептида находится между двумя рамками.
На фигуре 2b показана нуклеотидная последовательность экзона 2 GDF-9B у овец Hanna. Положение замены нуклеотида C на T в Hanna (на расстоянии 67 нуклеотидов от сайта процессинга) указано жирным шрифтом. Триплетный кодон, затронутый данной заменой, подчеркнут. Сайт процессинга для протеолитического отщепления пропептида от зрелого фрагмента и стоп-кодон TGA обведены рамкой. Кодирующая последовательность зрелого пептида находится между двумя рамками.
На фигуре 2с показана нуклеотидная последовательность 394-599 п.н. фигуры 2а.
На фигуре 2d показана нуклеотидная последовательность 394-599 п.н. фигуры 2b.
На фигуре 2e показана нуклеотидная последовательность 472-486 п.н. фигуры 2а.
На фигуре 2f показана нуклеотидная последовательность 448-462 п.н. фигуры 2b.
На фигуре 3а показана выведенная аминокислотная последовательность белка GDF-9B Inverdale, кодируемого нуклеотидной последовательностью, изображенной на фигуре 2а. Зрелый GDF-9B показан обычным шрифтом, а часть пропептида показана курсивом. Аминокислота (аспарагиновая кислота, D), получаемая заменой основания в Inverdale, отмечена жирным шрифтом.
На фигуре 3b показана выведенная аминокислотная последовательность укороченного белка GDF-9B Hanna, кодируемого нуклеотидной последовательностью, изображенной на фигуре 2b. Зрелый пептид GDF-9B показан обычным шрифтом, а часть пропептида показана курсивом. Аминокислота дикого типа (глутамин, Q) превращается в стоп-кодон (END) у мутанта Hanna.
На фигуре 4 показано сравнение выведенной аминокислотной последовательности GDF-9B овцы с белком человека и мыши. Номера в скобках выше линии указывают положения аминокислот зрелого пептида. Незаштрихованный треугольник показывает положение полиморфизма по Leu, а темный треугольник показывает положение единственного интрона. Предполагаемый сайт процессинга RRAR и консервативные цистеины заштрихованы серым. Положения мутаций FecXI и FecXH в положениях аминокислот 23 и 31 указаны жирным шрифтом.
На фигуре 5 показана хроматограмма последовательности GDF-9B овец Inverdale, Hanna и дикого типа, показывающая район, где происходят мутации.
На фигуре 6 показано сопоставление мутантного района предсказанного белка FecXI с членами суперсемейства TGFβ других видов.
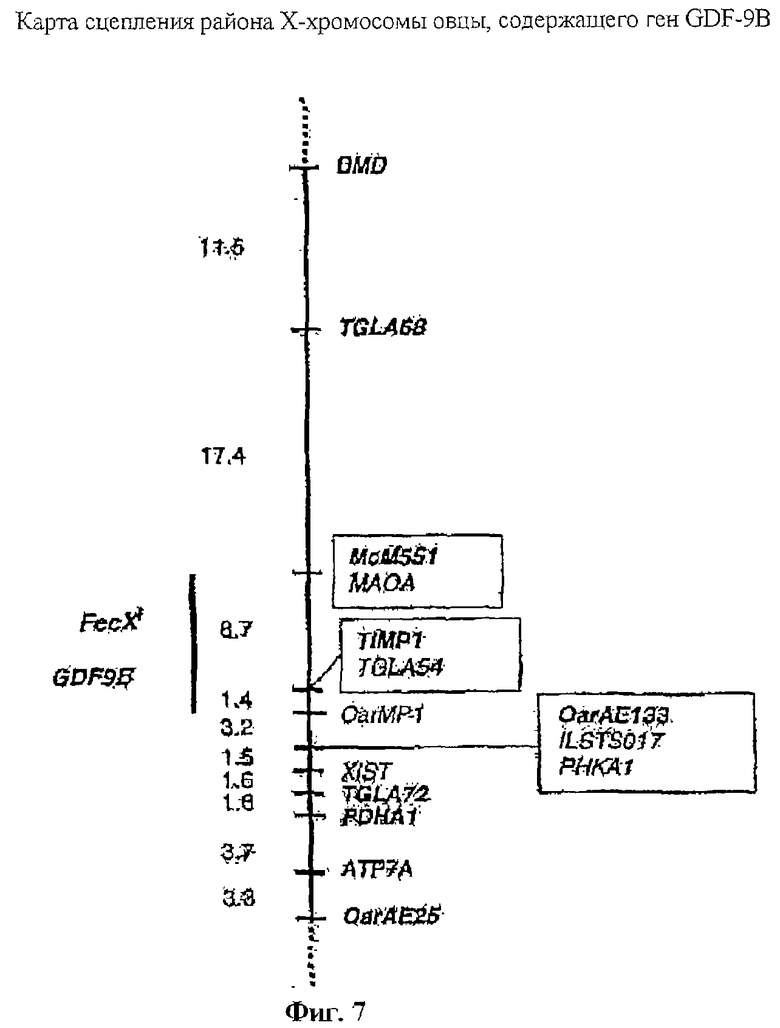
На фигуре 7 показана карта сцепления района Х-хромосомы овцы, содержащего ген GDF9-B.
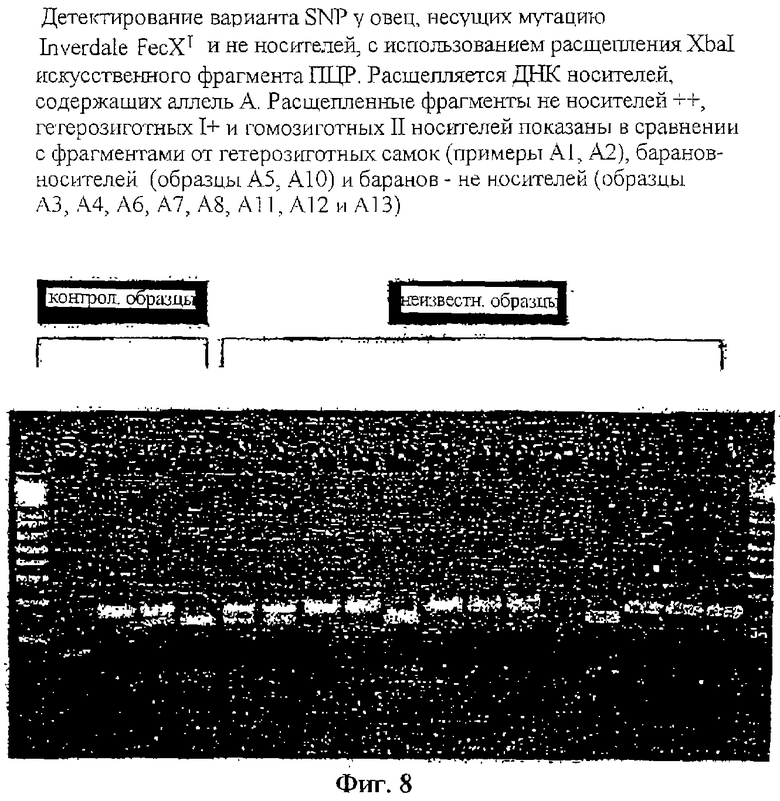
На фигуре 8 показаны результаты анализа выявления варианта SNP у овец, несущих мутацию FecXI Inverdale, и не носителей, с использованием расщепления XbaI искусственного фрагмента ПЦР. Расщепляются ДНК носителей, содержащих аллель А. Расщепленные фрагменты не носителей ++, гетерозиготных I+ и гомозиготных II носителей показаны в сравнении с фрагментами от гетерозиготных самок (образцы А1, А2), баранов-носителей (образцы А5, А10) и баранов - не носителей (образцы А3, А4, А6, А7, А8, А11, А12 и А13).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Впервые показано, что мутации в гене GDF-9B у овец Inverdale и Hanna ответственны за повышение скорости овуляции у гетерозиготных животных и за стерильность у гомозиготных животных.
В целях описания будет вполне понятно, что слово «включающий» означает «содержащий, но не ограниченный этим», и что слово «включает» имеет соответствующее значение.
Термин «выделенный» означает в значительной степени отделенный или очищенный от загрязняющих последовательностей в клетке или организме, из которого нуклеиновая кислота происходит в естественных условиях, и включает нуклеиновые кислоты, очищенные стандартными способами очистки, а также нуклеиновые кислоты, полученные посредством рекомбинантной технологии, включая способ ПЦР, и нуклеиновые кислоты, которые были синтезированы. Предпочтительно молекулу нуклеиновой кислоты выделяют из геномной ДНК овцы, экспрессирующей фенотип Inverdale или Hanna.
Термин «модулирование овуляции» означает увеличение или уменьшение скорости овуляции по сравнению со скоростью, наблюдаемой у интактного млекопитающего.
Термин «лиганд» относится к любой молекуле, которая может связываться с другой молекулой, такой как полипептид или пептид, и следует считать, что термин включает в себя, но не ограничен этим, антитела и молекулы фагового дисплея.
Зонд и праймеры, используемые в данном способе, также составляют часть изобретения. Указанные зонды и праймеры могут содержать фрагмент молекулы нуклеиновой кислоты согласно изобретению, способной гибридизоваться в жестких условиях с последовательностью мутантного гена GDF-9B. Такие зонды и праймеры также применимы в исследовании структуры и функции мутантного гена и для получения гомологов гена не от овец, а от других млекопитающих, экспрессирующих фенотип Inverdale или Hanna.
Зонды или праймеры нуклеиновой кислоты можно получить на основе нуклеиновых кислот согласно данному изобретению. «Зонд» содержит выделенную нуклеиновую кислоту, связанную с регистрируемой меткой или репортерной молекулой. Обычные метки включают радиоактивные изотопы, лиганды, хемилюминесцентные или флуоресцентные агенты и ферменты.
«Фрагмент» нуклеиновой кислоты является частью нуклеиновой кислоты, которая короче, чем полная длина, и содержит, по меньшей мере, минимальную последовательность, способную специфически гибридизоваться с молекулой нуклеиновой кислоты согласно изобретению, или с комплементарной ей последовательностью в жестких условиях, которые определены ниже. «Фрагмент» полипептида представляет собой часть полипептида, которая короче, чем полная длина, но которая продолжает сохранять биологическую функцию либо увеличения, либо уменьшения скорости овуляции у млекопитающего, или вызывает стерильность у млекопитающего. Следовательно, фрагмент согласно изобретению обладает, по меньшей мере, одной из биологических активностей нуклеиновой кислоты или полипептида согласно изобретению.
«Праймеры» представляют собой короткие нуклеиновые кислоты, предпочтительно олигонуклеотиды ДНК длиной 15 нуклеотидов или более, которые отжигаются с комплементарной цепью ДНК-мишени путем гибридизации нуклеиновых кислот, образуя гибрид между праймером и цепью ДНК-мишени, затем удлиняются вдоль цепи ДНК-мишени полимеразой, предпочтительно ДНК-полимеразой. Пары праймеров можно использовать для амплификации последовательности нуклеиновой кислоты, например полимеразной цепной реакцией (ПЦР) или другими способами амплификации нуклеиновых кислот, хорошо известными в данной области. Пары праймеров ПЦР можно получить из последовательности нуклеиновой кислоты согласно данному изобретению, например, используя компьютерные программы, предназначенные для этой цели, такие как Primer (версия 0,5© 1991, Whitehead Institute for Biomedical Research, Cambridge, MA).
Способы получения и применения зондов и праймеров описаны, например, в Sambrook et al. Molecular Cloning: A Laboratory Manual, 2nd ed, vol.1-3, ed Sambrook et al., Cold Spring Harbour Laboratory Press, Cold Spring Harbour, NY, 1989.
Зонды и праймеры могут быть свободными в растворе или ковалентно или нековалентно связанными с твердой подложкой стандартными способами.
«Жесткие условия» для амплификации последовательности нуклеиновой кислоты-мишени (например, посредством ПЦР) с использованием конкретной пары праймеров для амплификации представляют собой условия, которые позволяют паре праймеров гибридизоваться только с последовательностью нуклеиновой кислоты-мишени, с которой связался бы праймер, имеющий соответствующую последовательность дикого типа (или ее комплемент).
На гибридизацию нуклеиновых кислот влияют такие условия, как концентрация соли, температура или органические растворители, наряду с составом оснований, длиной комплементарных цепей и количеством ошибочных спариваний нуклеотидных оснований между гибридизующимися нуклеиновыми кислотами, что будет хорошо понятно специалистам в данной области.
В том случае, когда термин «специфичный для (последовательности-мишени)» относится к зонду или праймеру, он свидетельствует о том, что зонд или праймер в жестких условиях гибридизуется только с последовательностью-мишенью в данном образце, содержащем последовательность-мишень.
В одном варианте изобретение относится к генетическому маркеру для основанной на ДНК селекции животных в отношении повышенной овуляции или стерильности у овец, коз, крупного рогатого скота, оленей, мышей, крыс или других коммерчески важных млекопитающих. Изобретение относится к приспособлениям для использования молекулы нуклеиновой кислоты, содержащей последовательность, полученную из мутантной последовательности ДНК GDF-9B или геномной ДНК, которая связана с мутантным геном GDF-9B, чтобы идентифицировать варианты последовательности у отдельных животных, которые связаны с повышенной овуляцией или стерильностью у этого животного. Хотя указанные варианты необязательно непосредственно могут вызывать характерный признак повышенной овуляции или стерильности, они будут достаточно близко связанными с ним, чтобы предсказать наличие характерного признака. Способы, посредством которых идентифицируют указанные варианты последовательности, известны в данной области и включают, но не ограничены этим, полиморфизм длин рестрикционных фрагментов (RFLP), AFLP, прямое секвенирование ДНК в мутантном гене GDF-9B или связанной с ним ДНК, или идентификацию и характеристику варьирующего количества тандемных повторов (VNTR) или полиморфизм микросателлитов (ди- или тринуклеотидные повторы), выявление и характеристику однонуклеотидного полиморфизма (SNP).
Полипептид можно получить в результате экспрессии подходящего вектора, содержащего молекулу нуклеиновой кислоты согласно изобретению или ее функциональный вариант или фрагмент, в подходящей клетке-хозяине, что должно быть понятно специалисту в данной области.
Клонирующий вектор можно выбрать в соответствии с используемым хозяином или клеткой-хозяином. Пригодные векторы, как правило, имеют следующие характеристики:
(а) способность к саморепликации;
(b) обладание единственной мишенью для любой конкретной рестрикционной эндонуклеазы; и
(с) желательно несут гены для легко селектируемых маркеров, таких как устойчивость к антибиотикам.
Два основных типа векторов, обладающих такими характеристиками, представляют собой плазмиды и бактериальные вирусы (бактериофаги или фаги). Предпочтительные в настоящее время векторы могут включать следующие векторы: pUC, pBlueScript, pGEM, PGEX, pBK-CMV, ZAP лямбда, GEM лямбда и серию pSP. Однако указанный список не следует рассматривать как ограничивающий рамки данного изобретения.
Молекулы ДНК согласно изобретению можно экспрессировать, помещая их в функциональной связи с подходящими регуляторными последовательностями в реплицирующемся экспрессирующем векторе. Регуляторные последовательности наряду с прочими могут включать точки начала репликации, промотор, энхансер и последовательности терминации транскрипции. Выбор регуляторной последовательности, которую необходимо включить в экспрессирующий вектор, зависит от типа хозяина или клетки-хозяина, предназначенного для того, чтобы использовать его для экспрессии ДНК.
Как правило, пригодными хозяевами являются прокариотические, дрожжевые клетки и клетки млекопитающих. Также в термин «хозяева» включены плазмидные векторы. Подходящие прокариотические хозяева включают E.coli, виды Bacillus и различные виды Pseudomonas. Обычно используемые промоторы, такие как промоторные системы β-лактамазы (пенициллазы) и лактозы (lac), хорошо известны в данной области. Можно использовать любую доступную промоторную систему, совместимую с выбранным хозяином. Векторы, используемые для дрожжей, также доступны и хорошо известны. Подходящим примером является 2-микронная плазмида с началом репликации.
Подобным образом векторы для применения в клетках млекопитающих также хорошо известны. Такие векторы включают хорошо известные производные SV-40, аденовируса, последовательностей ДНК, полученных из ретровируса, вирусов простого герпеса и векторы, полученные в результате комбинации плазмидной и фаговой ДНК.
В данной области известны другие эукариотические экспрессирующие векторы (например, P.J.Southern and P. Berg, J. Mol. Appl. Genet. I, 327-341 (1982); S. Subramani et al., Mol. Cell. Biol. I, 854-864 (1981); R J. Kaufmann and P.A.Sharp, «Amplification and Expression of Sequences Cotransfected with a Modular Dihydrofolate Reducase Complementary DNA Gene, J. Mol. Biol. 159, 601-621 (1982); R J. Kaufmann and P.A.Sharp, Mol. Cell. Biol. 159, 601-664 (1982); S.I.Scahill et al., «Expressions and Characterisation of the Product of a Human Immune Interferon DNA Gene in Chinese Hamster Ovary Cells,» Proc. Natl. Acad. Sci. USA. 80, 4654-4659 (1983); G. Urlaub and L.A.Chasin, Proc. Natl. Acad. Sci. USA. 77, 4216-4220, (1980).
Применимые в данном изобретении экспрессирующие векторы содержат, по меньшей мере, одну последовательность регуляции экспрессии, которая функционально связана с последовательностью ДНК или фрагментом, который необходимо экспрессировать. Регуляторная последовательность встроена в вектор для того, чтобы контролировать и регулировать экспрессию клонированной последовательности ДНК. Примерами пригодных последовательностей регуляции экспрессии является система lac, система trp, система tac, система trc, основные районы оператора и промотора фага лямбда, гликолитические промоторы кислой фосфатазы дрожжей, например, Pho5, промоторы синхронизирующих факторов альфа дрожжей и промоторы, полученные из вируса полиомы, аденовируса, ретровируса и вируса обезьян, например ранний и поздний промоторы SV40, и другие последовательности, которые контролируют экспрессию генов прокариотических и эукариотических клеток, и их вирусов, или их комбинации.
В конструкции вектора также предпочтительно иметь возможность отличать вектор, включающий чужеродную ДНК, от немодифицированных векторов посредством удобного и быстрого анализа. Репортерные системы, используемые в таких анализах, включают репортерные гены и другие детектируемые метки, которые дают измеряемые изменения цвета, устойчивость к антибиотикам и тому подобное. В одном предпочтительном векторе используют репортерный ген β-галактозидазы, и этот ген детектируется благодаря клонам, проявляющим синий фенотип на чашках с X-гал. Это облегчает селекцию. В одном варианте ген β-галактозидазы можно заменить геном, кодирующим полиэдрин; и указанный ген детектируется благодаря клонам, проявляющим белый фенотип при окрашивании с помощью X-гал. Указанная селекция на основе сине-белого окрашивания может служить в качестве маркера, применимого для детектирования рекомбинантных векторов.
После селекции векторы можно выделить из культуры, используя стандартные способы, такие как экстракция замораживанием-оттаиванием, с последующей очисткой.
Для экспрессии векторы, содержащие ДНК согласно изобретению и регуляторные сигналы, встраивают или вводят посредством трансфекции в хозяина или клетку-хозяина. Некоторые пригодные экспрессирующие клетки-хозяева включают хорошо известные прокариотические и эукариотические клетки. Некоторые подходящие прокариотические хозяева включают, например, E.coli, такие как E.coli SG-936, E.coli HB 101, E.coli W3110, E.coli X1776, E.coli X2282, E.coli DHT и E.coli MR01, Pseudomonas, Bacillus, такие как Bacillus subtilis, и Streptomyces. Подходящие эукариотические клетки включают дрожжи и другие грибы, клетки насекомых, клетки животных, такие как клетки COS и клетки CHO, клетки человека в культуре ткани.
В зависимости от используемого хозяина трансформацию выполняют согласно стандартным способам, подходящим для таких клеток. Для прокариот или других клеток, которые содержат прочные клеточные стенки, можно применять способ обработки кальцием (Cohen, S N Proceedings, National Academy of Science, USA 69 2110 (1972)). Для клеток млекопитающих, не имеющих таких клеточных стенок, предпочтителен способ осаждения фосфатом кальция Graeme and Van Der Eb, Virology 52: 546 (1978). Трансформации дрожжей осуществляют согласно способу Van Solingen et al. J. Bact. 130: 946 (1977) и Hsiao et al. Proceedings, National Academy of Science, 76: 3829 (1979).
После трансформации выбранного хозяина соответствующим вектором можно продуцировать кодируемый полипептид или пептид часто в форме слитого белка посредством культивирования клеток-хозяев. Полипептид или пептид согласно изобретению можно детектировать посредством быстрого анализа, как указано выше. Затем полипептид или пептид извлекают и очищают как это необходимо. Извлечения и очистки можно достичь, используя любой из способов, известных в данной области, например, абсорбцией на анионообменной смоле и элюированием. Указанный способ продуцирования полипептида или пептида согласно изобретению составляет следующий аспект данного изобретения.
Клетки-хозяева, трансформированные векторами согласно изобретению, также образуют следующий аспект изобретения.
Кроме того, в предпочтительных вариантах также можно использовать нуклеотиды и пептиды, обладающие значительной идентичностью с нуклеотидными и аминокислотными последовательностями согласно изобретению. В данном описании «значительная идентичность» означает, что две последовательности при оптимальном сопоставлении, таком как с помощью программ GAP или BESTFIT (нуклеотиды и пептиды), используя оценку пробелов по умолчанию, или оцениваемые с помощью компьютерного алгоритма BLASTP (пептиды) или BLASTX (нуклеотиды), проявляют идентичность, по меньшей мере, 60%, предпочтительно 75% и наиболее предпочтительно 90-95% последовательностей.
Предпочтительно положения остатков, которые не являются идентичными, отличаются консервативными аминокислотными заменами. Например, замены аминокислот, имеющих сходные химические свойства, такие как заряд или полярность, не должны влиять на свойства белка. Примеры включают замены аспарагина на глутамин или аспарагиновой кислоты на глутаминовую кислоту.
Термин «вариант» в используемом здесь смысле включает молекулы нуклеиновой кислоты и полипептиды и пептиды, имеющие «значительную идентичность» с последовательностями согласно изобретению. Вариант может быть результатом модификации нативной нуклеотидной или аминокислотной последовательности такими модификациями, как инсерции, замены или делеции одного или более нуклеотидов или аминокислот, или может представлять собой вариант природного происхождения. Термин «вариант» также включает гомологичные последовательности, которые гибридизуются с последовательностями согласно изобретению в стандартных условиях гибридизации, такими как 2 × SSC при 65°С, или предпочтительно в жестких условиях гибридизации, такими как 6 × SSC при 55°С, при условии, что вариант способен модулировать скорость овуляции у млекопитающих женского пола. В тех случаях, когда желателен такой вариант, нуклеотидную последовательность нативной ДНК изменяют соответствующим образом. Указанное изменение можно осуществить посредством синтеза ДНК или посредством модификации нативной ДНК, например, сайт-специфичным или кассетным мутагенезом. Предпочтительно в тех случаях, когда необходимы модификации последовательностей частей кДНК или геномной ДНК, применяют сайт-специфичный направляемый праймером мутагенез, используя стандартные в данной области способы.
Термин «белок или полипептид» относится к белку, кодируемому молекулой нуклеиновой кислоты согласно изобретению, включая фрагменты, мутации и гомологи, имеющие такую же биологическую активность, т.е. активность в модулировании овуляции. Белок или полипептид согласно изобретению можно выделить из природного источника, получить посредством экспрессии рекомбинантной молекулы нуклеиновой кислоты или синтезировать химическим путем.
В следующем аспекте изобретение относится к применению мутантного полипептида GDF-9B, который имеет аминокислотную последовательность, представленную на фигуре 3а или 3b, или его варианта или фрагмента, по существу обладающего его активностью, в способе модулирования скорости овуляции у млекопитающего.
Способ может включать введение указанному млекопитающему эффективного количества GDF-9B мутантного или дикого типа, или его антитела или антигена, или его варианта.
Предпочтительно модулирование скорости овуляции включает индуцирование стерильности у млекопитающего женского пола посредством введения лиганда или антигена мутантного GDF-9B, чтобы снизить уровень эндогенного мутантного GDF-9B.
В дополнительном аспекте данное изобретение относится к лиганду, который связывается с полипептидом согласно изобретению. В большинстве случаев лигандом является антитело. Следует понимать, что термин «антитело» охватывает фрагменты или аналоги антител, которые сохраняют способность связываться с полипептидом согласно изобретению, включая, но не ограничивая этим, Fv, F(ab)2-фрагменты, молекулы ScFv и тому подобное. Антитело может быть поликлональным или моноклональным, но предпочтительно является моноклональным. В некоторых вариантах лигандом может быть молекула фагового дисплея.
Согласно следующему аспекту представлена композиция, содержащая, по меньшей мере, полипептид согласно изобретению и фармацевтически или ветеринарно приемлемый носитель или разбавитель. Конечно, в композицию можно включить более одного полипептида согласно изобретению.
Согласно еще одному аспекту данного изобретения представлен набор для идентификации млекопитающих мужского и женского пола, которые несут единственную копию (гетерозиготы) и/или особей женского пола, несущих две копии (гомозиготы) мутантной молекулы нуклеиновой кислоты GDF-9B согласно изобретению, включающий в себя:
- пару праймеров для амплификации соответствующего района GDF-9B и необязательно один или более следующих компонентов;
- солевой буферный раствор для амплификации, такой как ПЦР-амплификация;
- смеси дезоксинуклеотидов;
- термостабильный фермент ДНК-полимеразу;
- контрольную ДНК вида, который подвергают тестированию;
- соответствующие стандарты;
- соответствующую систему детекрирования, которая может содержать один из праймеров в каждой паре, меченный флуоресцентно или другим способом, меченый зонд для детекрирования продукта и
- инструкции и протоколы для амплификации и последующего детекрирования продуктов амплификации и интерпретации результатов.
Изобретение также относится к набору для детекрирования циркулирующего мутантного белка GDF-9B у млекопитающего. Такой набор может содержать стандартный набор для формата ELISA или иммуноферментного анализа, известный специалистам в данной области; например, набор может содержать специфическое антитело, направленное к мутантному белку GDF-9B, и стандартные компоненты амплификации вторичного антитела для усиления сигнала. Антитела можно конъюгировать с флуоресцентной или радиоактивной или хемилюминесцентной меткой, или можно метить второе антитело. Также можно добавлять соответствующие растворы, контроли, буферы, инструкции и протоколы.
Теперь изобретение будет описано подробно только посредством обращения к следующим неограничивающим примерам и чертежам.
Животные
Животные, тестируемые в данном исследовании, были из племенных отар AgResearch Inverdale, находящихся в Invermay Agricultural Centre и Woodlands Research Station, и из коммерческих отар Arnold Gray, Orawia, Southland (Gray and Davis, 1995). Все животные носители Inverdale были потомками исходной овцы Inverdale (A281), у которой впервые выявили ген Inverdale.
Оценки фенотипа
Статус носителя у овец определяли лапароскопией, чтобы идентифицировать стерильных овец II, или скорость овуляции, чтобы отличить носителей I+ от не носителей ++.
Статус носителя у баранов также определяли на основе скорости овуляции у их дочерей. После обнаружения бесплодных яичников у овец II, использовали быстрый способ тестирования потомства баранов путем спаривания каждого барана с семью-десятью овцами I+ и проведением лапароскопии у дочерей в возрасте 6 месяцев. Любое полученное в результате стерильное потомство II подтверждает, что производитель является носителем. Цель состояла в том, чтобы получить пять дочерей от каждого барана, так как вероятность того, что баран IY не имеет дочерей с полосковидными яичниками в примере с пятью дочерьми, составляет только 0,031 (Davis et al., 1994).
Очистка и секвенирование ДНК
ДНК очищали из лейкоцитов, присутствующих в объеме от 5 до 10 мл цельной крови от каждого животного (Montgomery and Sise, 1990). Секвенирование всех субклонов и продуктов ПЦР выполняла коммерческая сервисная служба, управляемая University of Otago Centre for Gene Research (автоматический секвенатор ABI 373).
Маркеры ДНК
Микросателлитные (динуклеотидные повторы) маркеры, которые амплифицировали ДНК овец, разрабатывали в AgResearch Molecular Biology Unit, как описано ранее (Galloway et al., 1996), или брали из литературы по генетическому картированию крупного рогатого скота и овец. Новые маркеры картировали на Х-хромосоме овец, как описано ранее (Galloway et al., 1996).
ПЦР-амплификация и рестрикционное расщепление продуктов гена GDF-9B овец
Использовали стандартные условия амплификации геномной ДНК посредством полимеразной цепной реакции (ПЦР). Праймеры разрабатывали на основе последовательностей человека и мыши (Galloway et al., 2000), и показано, что они успешно амплифицируют фрагменты гена из ДНК овец. Продукты ПЦР, содержащие мутации одиночных нуклеотидов, расщепляли коммерчески доступными рестриктазами SpeI, BsrSI и/или XbaI, используя стандартные условия, рекомендованные производителем. Продукты ПЦР и продукты фрагментов рестрикции идентифицировали посредством разделения электрофорезом в 2-3% агарозных гелях вместе с коммерчески доступными маркерами размера ДНК.
Способы секвенирования и детектирования мутаций
Авторы изобретения секвенировали ген GDF-9B овец во всех трех генотипах (Inverdale FecXI, Hanna FecXH и FecX+ дикого типа) из фрагментов ПЦР (Galloway et al., 2000), и секвенирование проводили в секвенаторе ABI 373. Авторы подтвердили замены единичных оснований секвенированием геномной ДНК, охватывающей полный кодирующий район, по меньшей мере, от шести животных, несущих каждый аллель (FecXI, FecXH и FecX+). Помимо замен оснований FecXH или FecXI (фигуры 2a и 2b) выявили только одно другое изменение в гене GDF-9B овец, а именно делецию одного кодона Leu (CTT) в L10 или L11 в сигнальной последовательности у некоторых животных (см. фигуры 4 и 5). Делеция Leu не связана ни с аллелем FecXH, ни с аллелем FecXI и, как оказалось, связана с породой. Замена С→Т FecXH приводит к потере сайта рестрикции BsrSI (actg/gn) и приобретению сайта SpeI (a/ctagt). Авторы подтвердили указанную замену основания, показав, что SpeI расщепляет продукт ПЦР длиной 541 п.н., охватывающий данный район, на два фрагмента длиной 476 и 65 п.н. у самок FecXH/FecXH и самцов FecXH/Y, но не у FecXI и животных дикого типа. У овец, несущих копию каждого аллеля (FecXI/FecXH), идентифицировали все три фрагмента (541, 476 и 65 п.н.). Подобным образом фрагменты, расщепляемые BsrSI, имели место в случае животных FecXI и животных дикого типа, но не для носителей FecXH. В продукте ПЦР длиной 154 п.н. ДНК носителей FecXI (получаемом с праймерами:
№12 (GAAGTAACCAGTGTTCCCTCCACCCTTTTCT) и
№13 (CATGATTGGGAGAATTGAGACC)) создавался искусственный сайт рестрикции XbaI. XbaI (t/ctaga) расщепляла продукты ПЦР, получаемые для самок FecXI/FecXI и самцов FecXI/Y, несущих аллель А (tctaga), но не продукты ПЦР в случае дикого типа или FecXH, несущие аллель T (tctagt). Таким образом, XbaI расщепляла продукт ПЦР длиной 154 п.н. до фрагмента длиной 124 п.н. удалением 30-нуклеотидного праймера №12 только у носителей FecXI. Все рестрикционные расщепления выполняли в аликвотах продуктов ПЦР, как указано производителями, и фрагменты разделяли в 3% агарозных гелях FMC Metaphor.
Способы картирования сцепления
Авторы сконструировали карту генетического сцепления Х-хромосомы овец посредством многоточечного анализа с использованием CRIMAP, как описано ранее (Galloway et al., 1996), и картировали дополнительные маркеры MAOA, McM551, OarMP1 и TIMP1 (Galloway et al., 2000). FecXI и GDF-9B картировали в семьях с Inverdale в карте сцепления, получаемых при спаривании девяти самцов-носителей (FecXI/Y) с самками дикого типа, с получением во втором поколении потомства из 62 гетерозиготных самок FecXI/FecX+. 62 полученные самки при спаривании с 10 самцами FecXI/Y дали потомство из 96 гомозиготных FecXI/FecXI или гетерозиготных FecXI/FecX+ самок. Авторы определяли статус носителей Inverdale лапароскопией, чтобы идентифицировать стерильных самок FecXI/FecXI, и тестированием потомства и лапароскопией потомства женского пола, чтобы идентифицировать самцов FecXI/Y. Происхождение подтверждали с помощью генетических маркеров, и все отобранные в третьем поколении самки FecXI/FecX+ были полными сибсами стерильных самок FecXI/FecXI. В первом поколении не было собрано ДНК от самок дикого типа. Авторы картировали GDF-9B на основе мутации T→A в кодирующем районе гена.
РЕЗУЛЬТАТЫ
Результаты секвенирования
Секвенировали фрагменты ПЦР, кодирующие полный зрелый пептид, из геномной ДНК Inverdale и Hanna. Секвенированный район также содержал большую часть пропептида в экзоне 2 (от 70 оснований с 3'-стороны интрон/экзонной границы человек/мышь до 30 оснований после стоп-кодона tga). Последовательность из двух указанных линий овец сравнивали с последовательностью GDF-9B овец дикого типа. На основе данных о последовательностях выявили две отдельные замены единичного основания в зрелом пептиде GDF-9B, одна расщепляющаяся в родословной Inverdale и одна в родословной Hanna (фигура 2).
У животных Hanna нуклеотид C в положении на расстоянии 67 нуклеотидов от сайта процессинга зрелого пептида заменен на Т. Это превращает кодон CAG (кодирующий аминокислоту глутамин (G)) в кодон TAG (кодирующий терминацию) и обуславливает образование укороченного зрелого белка (фигура 3b).
У животных Inverdale нуклеотид T в положении нуклеотидов 92 позднее сайта процессинга зрелого пептида превратился в А, превращая кодон GTC (аминокислота валин (V)) в GAC (аминокислота аспарагиновая кислота (D)) (фигура 3a).
Подтверждение единичных замен оснований
Указанные единичные замены оснований подтвердили секвенированием, по меньшей мере, 6 животных, несущих каждый генотип (Inverdale, Hanna и не носители дикого типа). Для каждого животного секвенирование проводили, по меньшей мере, один раз (таблица 1). В указанной подгруппе животных не выявлены замены ни Inverdale, ни Hanna у животных дикого типа, не наблюдали замены Inverdale у животных Hanna и наоборот.
Таблица 1
Идентификация единичных замен оснований у животных Inverdale и Hanna посредством секвенирования.
Животные имеют известный фенотип из хорошо охарактеризованных родословных (+ = аллель дикого типа, I = аллель Inverdale, H = аллель Hanna, Y = Y-хромосома). Цифрами указано количество раз встречаемости независимой последовательности у того животного, у которого идентифицировано соответствующее изменение последовательности.
Исследование с рестриктазами показало, что замена основания Hanna обуславливает сайт расщепления рестриктазой SpeI (a/ctagt) и удаляет сайт BsrSI (actg/gn) вокруг данной замены. Указанные сайты расщепления подтвердили, показав, что фермент SpeI способен расщеплять фрагмент ПЦР длиной 541 п.н., охватывающий этот район, на фрагменты длиной 476 п.н. и 65 п.н. у животных HY и HH, но не у животных IY и +Y. У овец, несущих по одной копии каждого из двух генов Inverdale и Hanna (HI), идентифицированы оба фрагмента длиной 541 п.н. и 476 п.н.
Подобным образом показано, что BsrS1 расщепляет фрагменты животных IY и +Y, но не HY, а у овец HI обнаружена смесь обеих полос.
Вокруг сайта замены основания Inverdale не создаются и не удаляются сайты расщепления ферментами, поэтому создан искусственный праймер RFLP, который вводит сайт расщепления Xba1 (t/ctaga) в продукт ПЦР, созданный на основе аллеля Inverdale, но не аллеля дикого типа. Продукт ПЦР, содержащий введенный сайт Xba1, получают только тогда, когда присутствует мутация А Inverdale, и его нет у животных Hanna или животных дикого типа. В данном случае продукт ПЦР расщепляется Xba1 с удалением 30 оснований, приводя к изменению длины конечного продукта.
Цепь ДНК Inverdale..TTTCAAGACAGCTT..
Окончание 30-нуклеотидного ПЦР-праймера - tttct
обуславливает получение сайта разрезания Xba1 tctaga в конечном продукте ПЦР.
При использовании данного способа фрагменты ПЦР 2 HY, 1 HH, 2 +Y и 3 ++ животных не расщеплялись Xba1, тогда как фрагменты от 36 животных II и 12 IY расщеплялись. У одного животного HI и 47 животных I+ выявлена смесь расщепленных и нерасщепленных фрагментов, как и ожидалось для гетерозигот.
Секвенирование и детектирование мутации
Авторы секвенировали последовательности гена GDF-9B овцы из кДНК и геномной ДНК, используя праймеры, сконструированные на основе последовательностей человека, мыши и овцы (Galloway et al., 2000). Ген овцы сходен с генами человека, мыши и крысы (Laitinen et al., 1998; Dube et al., 1998; Aaltonen et al., 1999; Jaatinen et al., 1999), и при этом обладает свойствами гена, типичными для других представителей суперсемейства TGFβ. Полноразмерная последовательность из 1179 п.н. кодирует препропептид из 393 аминокислот (фигура 4), охватывающий два экзона, разделенных интроном длиной примерно 5,4 т.п.н. Рассчитанный сигнальный пептид длиной 25 аминокислот предшествует прорайону из 244 аминокислот и предполагаемому С-концевому району зрелого пептида из 125 аминокислот после сайта расщепления протеазой RRAR. Кодирующий район овцы на 82,9% гомологичен району человека и на 78,8% району мыши и на 78,4% району крысы на уровне нуклеотидов.
Авторы также секвенировали геномную ДНК у носителей Inverdale (FecXI) и Hanna (FecXH) (фигура 5). Единственная транзиция С→T в положении нуклеотидов 67 кодирующего района зрелого пептида у носителей FecXH вводит преждевременный стоп-кодон вместо глутаминовой кислоты (Q) в аминокислотном остатке 23 (остаток 291 непроцессированного белка). Преждевременное прерывание зрелого пептида у носителей FecXH в таком раннем положении, по-видимому, приводит к полной потере функции GDF-9B. Отдельная единичная транзиция Т→А происходит у носителей FecXI в нуклеотидном положении 92 зрелого пептида. Мутация заменяет валин (V) аспарагиновой кислотой (D) в остатке 31 (остаток 299 непроцессированного белка). Мутация FecXI представляет собой неконсервативную замену в высоко консервативном районе белка. Все другие представители суперсемейства FGFβ из широкого круга видов содержат в этом положении только консервативные гидрофобные аминокислоты валин, изолейцин или лейцин (фигура 6).
Картирование GDF-9B у овец
Для того чтобы локализовать FecXI, авторы создали карту генетического сцепления Х-хромосомы овцы (Galloway et al., 1996), и авторы картировали локус FecXI между фланкирующими маркерами на расстоянии 10 сМ от центра Х-хромосомы овцы (фигура 7). Связь группы сцепления с фенотипом Inverdale наблюдали в семье из 177 животных, имеющей структуру, состоящую из трех поколений, с максимумом информативных мейозов у особей женского пола, равном 96. Картирование сцепления показало, что FecXI картировался в районе, содержащем TIMP1 и MAOA (синтенично области Xp11.2-11.4 человека), но не в районе, содержащем PHKA1, XIST и ATP7A (Xq13 человека). Точка разрыва вблизи OarMP1 у овец, по-видимому, разделяет указанные две группы генов, относящиеся к отдельным синтеничным группам в Х-хромосомах человека и мыши. GDF-9B картируется в Xp11.2 человека и в синтеничной области Х-хромосомы мыши (Dube et al., 1998; Aaltonen et al., 1999). Авторы картировали GDF-9B овец в таком же интервале в 10 сМ как и FecXI в родословной, в которой они картировали Inverdale, и не обнаружили рекомбинантов между фенотипом FecXI и BMP15 ни в одном из 78 коинформативных мейозов у особей женского пола, показанных в таблице 2.
Анализ сцепления в двух точках CRIMAP c фенотипом FecXI в родословной, картированной по Inverdale.
Не выявлено значимых различий в последовательностях между кодирующей ДНК TIMP1 овец дикого типа и FecXI, и при идентификации следующих рекомбинантов среди дополнительных носителей FecXI TIMP1 исключен из кандидатов на FecXI.
Применение выделенного полипептида и антитела для того, чтобы манипулировать овуляцией
Полученный из E.coli зрелый белок GDF-9B, содержащий последовательность дикого типа, представленную в SEQ ID NO:10, химическим способом конъюгировали с белком гемоцианина слизня (KLH), и данный антиген в полном адъюванте Фрейнда (FCA) подкожно (п/к) инъецировали 10 овцам Ромни-марш в анэструсе (0,4 мг/овцу). Другим 9 овцам Ромни-марш в анэструсе инъецировали только KLH (п/к) в FCA, служащий в качестве контроля (0,4 мг/овцу). После этого всем животным с месячными интервалами инъецировали бустер-антиген (0,2 мг/овцу KLH-GDF9B или 0,2 мг/овцу KLH) в масляном адъюванте, содержащем спан и твин. По мере того, как овцы вступали в сезон размножения, некоторые через 3-4 месяца после начала иммунизаций, животных, проявляющих эструсное поведение, что детектировали с помощью вазэктомированного барана с меченым поводком, подвергали процедуре лапароскопии, чтобы визуализировать количество corpora lutea (т.е. мест овуляции) на поверхности яичников. Семь из 10 животных, обработанных KLH-GDF-9B, и все 9 животных, обработанных KLH, проявляли эструсное поведение. Средние скорости овуляции у овец, иммунизированных KLH-GDF9B и KLH, которые проявляли эструсную активность, показаны в таблице 3.
Животные, обработанные KLH-GDF-9B, показали высоко значимое увеличение скорости овуляции по сравнению с контрольными животными, обработанными KLH (p<0,001) ANOVA.
+ Доказательство того, что повышенная скорость овуляции у животных, обработанных KLH-GDF-9B, которые проявляли эструс, связана с гуморальным ответом на GDF-9B, показано в таблице 4.
Уровни антител измеряли способом ELISA после разведения плазмы овец 1:5000. Способ ELISA включал покрытие 96-луночного планшета 100 нг/лунку полноразмерными GDF-9B, экспрессированным в E.coli, и инкубацию с 100 мкл разведенной плазмы овец и 100 мкл буфера для анализа, после соответствующей блокирующей обработки и последующих промывок. После инкубации с плазмой овец и нескольких промывок добавляли кроличье антиовечье антитело, конъюгированное с HRP, на 1 час при 37°С. Затем лунки промывали и проявляли с помощью о-фенилендиамина плюс перекись водорода, проявление останавливали серной кислотой.
В отдельном исследовании для того, чтобы показать, что функциональный вариант GDF-9B овец будет влиять на развитие фолликулов яичника, 10 самок мышей внутрибрюшинно (в/б) иммунизировали зрелым белком GDF-9B овец, полученным из E. coli (0,2 мг) в FCA (0,22 мл), а других 10 самок мышей иммунизировали альфа-лактальбумином коров (0,2 мг) в FCA (0,22 мл, в/б), служащим в качестве контроля. Затем с интервалами в 2 недели проводили 3 бустер-инъекции соответствующих антигенов (0,1 мг при первой бустер-иммунизации и 0,05 мг при второй и третьей бустер-иммунизации) в смеси спан/твин/масло, и животных забивали через 1 неделю после последней бустер-иммунизации. После этого яичники фиксировали в водном фиксаторе Боуина и обрабатывали для морфометрического анализа. Суммарное количество растущих преантральных и антральных фолликулов в яичнике определяли с использованием способа систематического случайного отбора образцов. Данные суммированы в таблице 5.
Количество преантральных фолликулов у животных, обработанных GDF9B, значимо ниже, чем количество у мышей, обработанных бычьим α-лактальбумином, p<0,005 (ANOVA). Не было значимых различий между группами обработки в отношении количества антральных фолликулов.
Доказательством того, что различия в количестве преантральных фолликулов связано с гуморальным ответом на GDF-9B, является следующее. Средний от предельных уровень антител в сыворотке мышей, разведенной 1:50000, после повторной иммунизации составлял 2,18 (1,28-2,90), тогда как у всех мышей, иммунизированных α-лактальбумином, ответа не было (т.е., <0,1). Значения для антител, представленные в виде оптической плотности при 490 нм, измеряли способом ELISA.
В следующем исследовании авторы индуцировали стерильность у животных-реципиентов введением антигена, соответствующего последовательности пептида GDF-9B овец. Чтобы добиться стерильности, 15-мерную аминокислотную последовательность пептида, соответствующую варианту зрелого района GDF-9B овец мутантного или дикого типа, синтезировали с С-концевым цистеином для конъюгации с гемоцианином слизня (KLH), чтобы создать антиген. Пептидная последовательность, которую использовали авторы, представляла собой следующее: SEVPGPSREHDGPESC. В данном исследовании 10 овцам Ромни-марш в анэструсе инъецировали 0,4 мг/овцу пептидного антигена KLH-GDF-9B в полном адъюванте Фрейнда, и 9 овцам Ромни-марш в анэструсе инъецировали 0,4 мг/овцу антигена KLH, в качестве контрольной группы. Затем с месячными интервалами 6 раз проводили бустер-иммунизацию животных дополнительным антигеном (0,2 мг/овцу в каждом случае) в смеси спан/твин/масло (п/к), и эструсную активность регестрировали 2-3 раза еженедельно, используя вазэктомированных баранов. Скорость овуляции, оцениваемую лапараскопически, определяли примерно за 1 неделю до последней бустер-обработки.
Все 9 овец, обработанных KLH, проявляли регулярную цикличную эструсную активность, тогда как только 1 из 10 животных, обработанных пептидом KLH-GDF-9B, проявляло эструсную активность. Средняя геометрическая (и 95% доверительные интервалы) скорости овуляции у контрольных животных, обработанных KLH, составляла 1,5 (1,1; 1,9), тогда как у 9 животных, обработанных пептидом KLH-GDF-9B, которые не проявляли эструсной активности, скорость овуляции была равна нулю. У одного животного, обработанного пептидом KLH-GDF-9B, проявляющего эструсную активность, скорость овуляции составляла 5. Полученные данные четко показывают, что стерильность можно индуцировать введением антитела или мутантного антигена GDF-9B или его варианта.
Доказательство, подтверждающее утверждение о том, что индукция овуляции у 9 животных, обработанных пептидом KLH-GDF-9B (16-мер) (т.е. 15-мер + С-концевой цистеин), представленным в SEQ ID NO:11, которые не проявляли эструса, связана с гуморальным ответом на GDF-9B, показано в таблице 6.
Уровни антител измеряли способом ELISA, который в общих чертах описан для таблицы 4.
Взятые вместе полученные результаты свидетельствуют о том, что полученная в результате введения антигена GDF-9B продукция антител у реципиентных животных может приводить к измененной активности фолликулов яичника и таким образом вызывать модуляцию скорости овуляции.
ДНК-тест на мутации
Варианты последовательностей в гене GDF-9B можно определить разными способами, хорошо известными специалистам в данной области, которые специально предназначены для того, чтобы идентифицировать различия между аллелями гена. В частности, указанные способы можно использовать для того, чтобы идентифицировать однонуклеотидный полиморфизм (SNP) Inverdale (FecXI) и Hanna (FecXH), а именно транзиция C→T имеет место у носителей FecXH, а транзиция T→A имеет место у носителей FecXI, но такие способы также можно применять по отношению к другим аллелям данного гена, которые могут присутствовать у других млекопитающих. Образцы можно получать либо из ДНК, либо непосредственно из пунктатов цельной крови, нанесенной пятнами непосредственно на бумагу FTA®, или из фолликулов волос или шерсти.
Один из таких способов включает использование рестриктаз для расщепления ДНК, специфичной в одном аллеле, но не в другом, или для расщепления фрагмента ПЦР, содержащего праймер, который был сконструирован так, чтобы он содержал сайт расщепления в комбинации с одним или с другим аллелем.
Результатом замены С→Т в FecXH является потеря сайта рестрикции BsrSI (actg/gn) и приобретение сайта SpeI (a/ctagt). Авторы подтвердили указанную замену основания, показав, что SpeI расщепляет продукт ПЦР длиной 541 п.н., охватывающий указанный район, на фрагменты длиной 476 и 65 п.н. у самок FecXH/FecXH и самцов FecXH/Y, но не у FecXI и животных дикого типа. У овец, несущих копию каждого из аллелей (FecXI/FecXH), идентифицированы все три фрагмента (541, 476 и 65 п.н.). Подобным образом BsrSI расщепляла фрагменты в случае FecXI и животных дикого типа, но не носителей FecXH.
В продукте ПЦР длиной 154 п.н. ДНК носителей FecXI (получаемом с праймерами:
№12 (GAAGTAACCAGTGTTCCCTCCACCCTTTTCT) и
№13 (CATGATTGGGAGAATTGAGACC)) создавался искусственный сайт рестрикции XbaI. XbaI (t/ctaga) расщепляла продукты ПЦР, получаемые для самок FecXI/FecXI и самцов FecXI/Y, несущих аллель А (tctaga), но не продукты ПЦР в случае дикого типа или FecXH, несущие аллель T (tctagt). Таким образом, XbaI расщепляла продукт ПЦР длиной 154 п.н. до фрагмента длиной 124 п.н. удалением 30-нуклеотидного праймера №12 только у носителей FecXI, фигура 8.
Продукты выявляли электрофорезом в 3% агарозных гелях FMC Metaphor, содержащих этидий, и визуализировали в ультрафиолетовом свете.
Другой способ детектирования SNP включает использование флуоресцентно меченых праймеров вместе со способом искусственного RFLP, описанным выше, и визуализацию продуктов в устройстве для секвенирования, таком как ABI377.
Другие способы детектирования SNP включают использование либо способа распознавания аллелей Taqman®, либо набора для удлинения праймеров SnaPshot ddNTP (здесь приведена вставка из подробного описания производителей). В способе распознавания аллелей Taqman применяют технологию зондов, в которой используют 5'-3'-нуклеазную активность ДНК-полимеразы AmpliTaq Gold ®, чтобы обеспечить прямое детектирование продукта ПЦР благодаря высвобождению флуоресцентного репортера в результате ПЦР. В анализе распознавания аллелей используют два зонда, по одному зонду для каждого аллеля, при этом каждый зонд содержит особый репортерный краситель. Система SnaPshot основана на удлинении с использованием одного дидезоксинуклеотида (флуоресцентно меченного) немеченого олигонуклеотидного праймера для выявления однонуклеотидного полиморфизма (SNP). В другом способе выявления SNP применяют масс-спектрометрию, при этом район вокруг SNP или мутации амплифицируют посредством ПЦР, и олигонуклеотидный праймер удлиняют вдоль SNP или мутации в присутствии дидезоксинуклеотидов. Варианты SNP выявляют на основе различия по массе.
Специалисту в данной области будет понятно, что несмотря на то, что изобретение описано с некоторыми подробностями в целях ясности и понимания, можно провести различные модификации и изменения описанных здесь вариантов и способов, не выходя за рамки концепции изобретения, приведенной в данном описании и прилагаемой формуле изобретения.
Цитированные здесь ссылки приведены в списке на следующих страницах и включены здесь в виде ссылки.
СПИСОК ЛИТЕРАТУРЫ.
Aaltonen, J., Laitinen, M.P., Vuojolainen, K., Jaatinen. R., Horelli-Kuitunen, N., Seppa, L., Louhio, H., Tuuri, Т., Sjoberg, J., Butzow, R., Hovata, O., Dale, L. and Ritvos, O. (1999) Human growth differentiation factor 9 (GDF-9) and its novel homolog GDF-9b are expressed in oocytes during early folliculogenesis. J.Clin Endocrinol Metab 84: 2744-2750.
Amer, P.R., McEwan, J.C., Dodds, K.G. and Davis, G.H. 1998: Cost benefit analysis of commercial use of the Inverdale prolificacy gene in sheep. Proceedings of the New Zealand Society of Animal Production 58: 157-160.
Braw-Tal, R., McNatty, K.P., Smith, P., Heath, D.A., Hudson, N.L., Phillips, D.J., McLeod, B.J. and David, G.H. 1993: The ovaries of ewes homozygous for the X-linked Inverdale gene (FecX1) are devoid of secondary and tertiary follicles but contain many abnormal structures. Biology of Reproduction 49: 895-907.
Davis, G.H., McEwan, J.C., Fenneasy, P.F., Dodds, K.G. and Farquhar, P.A. 1991: Evidence for the presence of a major gene influencing ovulation rate on the X-chromosome of sheep. Biology of Reproduction 44: 620-624.
Davis, G.H., McEwan, J.C., Fennessy, P.F., Dodds, K.G., McNatty, K.P. and O, W-S. 1992: Infertility due to bilateral ovarian hypoplasia in sheep homozygous (FecXI FecX1) for the Inverdale prolificacy gene located on the X-chromosome. Biology of Reproduction 46: 636-640.
Davis, G.H., Bruce, G.D. and Reid, P.J. 1994: Breeding implications of the streak ovary condition in homozygous (FecXI FecX1) Inverdale sheep. Proceedings of the 5th World Congress on Genetics Applied to Livestock Production. 19:249-252.
Davis, G.H., McEwan, J.C., Fennessy, P.F., Dodds, K.G. 1995: Discovery of the Inverdale gene (FecX). Proceedings of the New Zealand Society of Animal Production 55:289-290.
Dong J., Albertini D.F., Nishimori K., Rajendra Kumar Т., Lu N. & Matzuk M.M. 1996: Growth differentiation factor-9 is required during early ovarian folliculogenesis. Nature 383:531-535.
Dube, J.L., Wang, P., Elvin. J., Lyons, KM., Celeste. A.J. and matzuk, M.M. 1998: The bone morphogenic protein 15 gene is X-linked and expressed m oocytes. Molecular Endocrinology 12:1809-1817.
Galloway, S.M., Hanrahan, V., Dodds, K.G., Potts, M.D., Crawford, A.M. and Hill, D.F. 1996: A linkage map of the ovine X chromosome. Genome Research 6:667-677.
Galloway, S.M., Cambridge, L.M., Henry, H.H., van Stijn, T.C. and Davis, G.H. 1999; A genetic test to identify carriers of the ovine Inverdale fecundity gene. Proceedings of the New Zealand Society of Animal Production 59:114-116.
Galloway, S.M., McNatty, K.P., Cambridge, L.M., Laitinen. M.P.E., Juengel. J.L., Jokiranta, T.S., McLaren. R.J., Luiro, K., Dodds, K.G., Montgomery, G.W., Beattie, A.E., Davis, G.H., and Ritvos, O. (2000) Mutations in an oocyte-derived growth factor gene (BMP 15) cause increased ovulation rate and infertility in a dosage-sensitive manner. Nature Genetics 25:279-283.
Gray, A.J. and Davis, G.H. Commercial performance of sheep carrying the Inverdale gene (FecX). Proceedings of the New Zealand Society of Animal Pioduction 55:294-295.
Hanna, M.M. 1995: Living witn the Inverdale gene (FecX) in a Romney flock. Proceedings of the New Zealand Society of Animal Production 55:296-297.
Jaatinen, R., Laitinen, M.P., Vuojolainen, K., Aaltonen, J., Louhio, H., Heikinheimo, K., Lehtonen, E. and Ritvos, O. (1999) Localisation of growth differentiation factor-9 (Gdf-9) mRNA and protein in rat ovaries and cDNA cloning of rat GDF-9 and its novel homolog GDF-9B.Mol Cell Endocrinol 156:189-193.
Laitinen, M, Vuojolainen, K., Jaatinen, R., Ketola. L., Aaltonen, J., Lehtonen, E., Heikinheimo. M. and Ritvos, O. 1998: A novel growth differentiation factor-9 (GDF-9) related factor is co-expressed with GDF-9 in mouse oocytes during folliculogenesis. Mechanisms of Development 78:135-140.
McNatty, K.P., Smith, P., Hudson, N.L., Heath, DA., Tisdall, D.J., O, W-S., Braw-Tal, R. 1995: Development of the sheep ovary during foetal and early neonatal life and the effect of fecundity genes. Journal of Reproduction and Fertility, Supplement 49:123-135.
McNatty, K.P., Smith, P., Hudson, N.L., Lun, S., Heath, D., Sbackell, G and Corrigan, K. 1995: Ovarian characteristics in Inverdale ewes heterozygous (I+) and homozygous (II) for the Inverdale gene (FecX). Proceedings of the New Zealand Society of Animal Production 55: 301-303.
Montgomery, G.W. and Sise, J.A. 1990: Extraction of DNA from sheep white blood cells. New Zealand Journal of Agricultural Research 33:437-441.
Mouse Genome Database (MGD), Mouse Genome Informatics, The Jackson Laboratory, Bar Harbor, Maine (October 1999).
World Wide Web (URL: http://www.informatics.iax.org/).
Ohno, S. 1973: Ancient linkage groups and frozen accidents. Nature 244:259-262.
Sadighi. M., Montgomery, G.W., Bodensteiner, K.J., and Galloway, S.M. 1998; The growth differentiation factor-9 maps to sheep chromosome 5. Proceedings of the 26tfa International Conference on Animal Genetics, Auckland, New Zealand, abstract C020.
Smith, P., O, W-S., Corrigan. K.A., Smith, Т., Lundy, Т., David, G.H. and McNatty, K.P. 1997: Ovarian morphology and endocrine characteristics of female sheep foetuses that are heterozygous or homozygous for the Inverdale prolificacy gene (FecX1). Biology of Reproduction 57; 1183-1192.



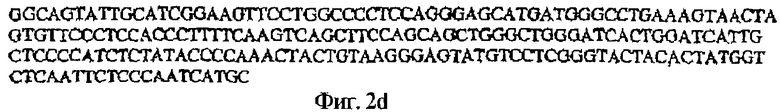
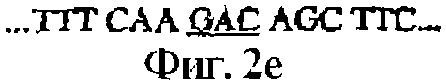
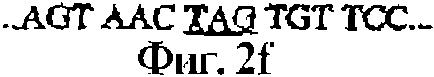

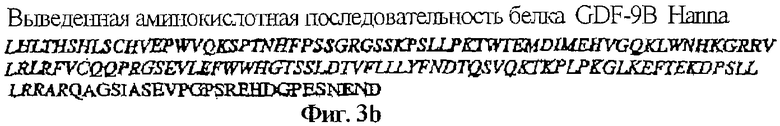



Изобретение относится к нуклеотидной последовательности, участвующей в увеличении или уменьшении скорости овуляции у млекопитающих, а именно GDF-9B. Предложена мутированная молекула GDF-9B которая используется для модулирования скорости овуляции у млекопитающего женского пола. Предложены также различные способы модулирования скорости овуляции, а также композиции для осуществления таких способов. Изобретение может быть использовано для индуцирования стерильности или пониженной плодовитости млекопитающих женского пола. 12 н. и 18 з.п. ф-лы, 14 ил., 6 табл.
a) SEQ ID NO:1, SEQ ID NO:3, SEQ ID NO:5 или SEQ ID NO:7;
b) последовательности, способной гибридизоваться в жестких условиях с молекулой, определенной в (а);
c) последовательности, которая является функциональным вариантом или фрагментом молекулы, определенной в (а);
d) последовательности, кодирующей полипептид, выбранный из группы, состоящей из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6 или SEQ ID NO:8;
e) SEQ ID NO:9;
f) SEQ ID NO:12 или SEQ ID NO:14, и
g) SEQ ID NO 16 и
h) последовательности, которая является функциональным вариантом или фрагментом молекулы, определенной в (d)-(f).
a) SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:13, SEQ ID NO:15, SEQ ID NO:17, или
b) функционального варианта или фрагмента последовательности, определенной в (а).
(i) получение образца ткани или крови млекопитающего;
(ii) выделение ДНК из образца; и необязательно
(iii) выделение ДНК GDF-9B из ДНК, полученной на стадии (i);
(iv) зондирование указанной ДНК зондом, комплементарным мутированной ДНК GDF-9B по п.1;
(v) амплификация количества мутированной ДНК GDF-9B; и/или
(vi) определение того, несет ли последовательность ДНК GDF-9B, полученная на стадии (ii), мутацию, связанную со стерильностью или с повышенной или пониженной овуляцией.
а) эффективного иммунизирующего количества полипептида GDF-9B дикого или мутированного типа, включающего аминокислотную последовательность по п.11;
b) антисмысловой молекулы нуклеиновой кислоты, направленной против нуклеиновой кислоты, кодирующей полипептид GDF-9B дикого или мутированного типа, включающий аминокислотную последовательность по п.11;
c) лиганда, который связывается с или является антигеном к полипептиду GDF-9B дикого или мутированного типа, включающему аминокислотную последовательность по п.11,
тем самым ингибируя биологическую активность полипептида GDF-9B мутированного или дикого типа.
a) полипептида, включающего аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8 или ее функционального варианта или фрагмента;
b) полипептида GDF-9B дикого или мутированного типа, включающего аминокислотную последовательность по п.11;
c) антисмысловой молекулы нуклеиновой кислоты, направленной против полипептида, определенного в (b);
d) лиганда, который связывается с или является антигеном к полипептиду, определенному в (b),
и фармацевтически или ветеринарно приемлемый носитель или разбавитель.
a) пару праймеров по п.8 для амплификации соответствующего участка GDF-9B;
и необязательно один или более из следующих компонентов:
b) буферный раствор для амплификации ДНК;
c) смесь дезоксинуклеотидов;
d) средства для амплификации ДНК;
e) контрольная ДНК тестируемого вида;
f) соответствующие стандарты; и
g) система детектирования.
| AALTONEN J | |||
| et al., «Human growth differentiation factor 9 (GDF-9) and its novel homolog GDF-9B are expressed in oocytes during early folliculogenesis», J Clin Endocrinol Metab | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
Авторы
Даты
2006-09-20—Публикация
2001-05-04—Подача