ИСПРАШИВАНИЕ ПРИОРИТЕТА
По настоящей заявке испрашивается приоритет даты подачи предварительной заявки на патент США 61/429,390, поданной 3 января 2011 года, "ГЕН И ВАРИАЦИИ, СВЯЗАННЫЕ С ФЕНОТИПОМ BM1, МОЛЕКУЛЯРНЫЕ МАРКЕРЫ, И ИХ ПРИМЕНЕНИЕ".
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее описание относится к фенотипу кукурузы brown midrib (bm). В конкретных вариантах осуществления, настоящее описание относится к определенным измененным генам CAD2 в кукурузе, которые вносят вклад в фенотип bm1 в некоторых сортах кукурузы, к молекулам нуклеиновой кислоты, включающим измененный ген CAD2, и/или белковым продуктам, получаемым в результате трансляции таких молекул нуклеиновых кислот.
УРОВЕНЬ ТЕХНИКИ
Лигнины являются универсальными компонентами растений, которые образуют поперечные связи с такими углеводами, как гемицеллюлозы в клеточной стенке. Лигнин и целлюлоза являются двумя преобладающими компонентами клеточной стенки растений. Клеточная стенка растения обеспечивает естественный барьер от внеклеточной среды. Многие исследования продемонстрировали, что одна из реакций растений на биотические стрессы (например, инфекцию, вызванную патогенным микроорганизмом) или абиотические стрессы (например, засуху, механический стресс и т.д.) состоит из укрепления клеточной стенки растения, в особенности посредством увеличения содержания лигнина в клеточной стенке растения. Многие сельскохозяйственные или промышленные применения связаны с целевыми растительными продуктами (например, продуктами, используемыми в производстве бумаги, производстве силоса и производстве энергии, например в форме биотоплива), выходы которых непосредственно связаны с содержанием и/или составом лигнина в клеточной стенке растения.
Лигниновые полимеры ограничивают перевариваемость волокна в растении кукурузы. Лигниновые полимеры снижают перевариваемость волокна у жвачных, причем степень лигнификации может быть обратно пропорциональна перевариваемости кормовой культуры (Cherney et al. (1991) Adv. Agron. 46:157-98). Модуляция содержания и состава лигнина может требоваться для повышения перевариваемости фуража. Модуляция лигнинового состава также может быть необходима, например, для укрепления клеточных стенок растения и, таким образом, повышения устойчивости к стрессам, или, наоборот, для уменьшения прочности клеточных стенок растения с целью облегчения извлечения целлюлозы или других химических соединений (Baucher et al. (1998) Plant Mol. Biol. 39:437-47).
Впрочем, довольно сложно узнать, как изменить путь биосинтеза лигнина и спрогнозировать, каковы будут последствия модификаций. Это, по меньшей мере, частично, обусловлено тем, что путь биосинтеза лигнина является сложным метаболическим путем, включающим большое количество ферментативных реакций. См., например, Dixon et al. (2001) Phytochemistry 57(7):1069-84. Возможные механизмы, с помощью которых метаболический путь может быть изменен физиологически, например, для компенсации изменения, вводимого модификацией в метаболическом пути, не известны.
Лигнин представляет собой нерастворимый полимер из 3 мономеров-спиртов или монолигнолов: п-кумариловый спирт (H субъединицы), конифериловый спирт (G субъединицы) и синапиловый спирт (S субъединицы), которые образуются в фенилпропаноидном пути (Neish (1968) Constitution and Biosynthesis of Lignin, eds. New York, Springer Verlag 1-43). Каждый тип субъединицы может образовывать различные связи с другими субъединицами и, таким образом, формировать лигнин. Другие связи также могут образовываться с другими париетальными соединениями (например, полисахаридами и белками), что приводит к формированию сложной трехмерной сети.
Этапы в сложном пути синтеза лигнина включают гидроксилирование, O-метилирование ароматических колец и конверсию карбоксила боковой цепи в спиртовую функциональную группу. Текущая гипотеза относительно монолигнольного пути биосинтеза включает последовательные реакции гидроксилирования и O-метилирование на различных уровнях окисления боковых цепей в метаболической сети, приводящие в результате к формированию S и G субъединиц. Ферменты сети включают 3-O-метилтрансферазу кофейной кислоты (COMT); гидроксициннамат:кофермент А лигазы (4CL); цитохром P450-зависимые ферулат-5-гидроксилазы (F5H); и некоторые изоформы циннамоил-КоА-редуктазы (CCR) и циннамилалкогольдегидрогеназы (CAD).
В течение нескольких лет предпринимались попытки модифицировать содержание и состав лигнинов растений посредством повышения или понижения экспрессии одного или нескольких генов пути биосинтеза лигнина (Anterola and Lewis (2002) Phytochemistry 61:221-94). Несмотря на то, что предлагали различные стратегии, повышение или понижение экспрессии одного или более ферментов в пути биосинтеза лигнина не всегда дает надежные и предсказуемые результаты.
Другая стратегия состоит в использовании, в схемах отбора, мутантов целевого гена в пути биосинтеза лигнина. Растения, содержащие мутацию brown midrib (bmr), демонстрируют измененный лигниновый состав и перевариваемость. В кукурузе были идентифицированы по меньшей мере четыре независимых мутации brown midrib (Kuc et al. (1968) Phytochemistry 7:1435-6). Все указанные мутации, которые называются "bm1, bm2, bm3 и bm4", демонстрируют пониженное содержание лигнинов по сравнению с контрольной кукурузой. Растения кукурузы brown midrib отличаются коричневой пигментацией средней жилки листа на стадии V4-V6 и светло-коричневой окраской паренхимы после выбрасывания султанов. Одной из описанных bmr мутаций является мутация со вставкой в ферменте COMT (bm3).
Зрелые растения кукурузы bm1 имеют уменьшенное на 10-20% содержание лигнина, небольшое уменьшение количества сложных эфиров феруловой кислоты и существенно сниженное содержание (~40%) сложных эфиров п-кумаровой и феруловой кислоты (Provan et al. (1997) J. Agric. Food 73:133-42; Barriére et al. (2004) Comptes Rendus Biologie 327:847-60). Частота п-гидроксифениловых, гваяциловых и сирингиловых мономеров тиоацидолиза аналогична в растениях bm1 и растениях дикого типа, показывая, что мутация bm1 не оказывает существенного влияния только на один тип лигниновой субъединицы (Guillaumie et al. (2007) Planta 226 (1):235-50). Лигнины растений bm1, по-видимому, действительно существенно обогащены углерод-углеродными межсубъединичными связями (Halpin et al. (1998) Plant J. 14 (5):545-53; Barriére et al. (2004), выше), при этом лигнины bm1 имеют существенное включение кониферилового альдегида и, в меньшей степени, синапового альдегида (Kim et al. (2002) J. Biol. Chem. 277:47412-9).
Важные в сельскохозяйственном отношении применения кукурузы включают силос. Силос представляет собой ферментированный фураж высокой влажности, который можно использовать в качестве корма для жвачных. Его заквашивают и сохраняют в процессе, называемом силосованием, и обычно приготавливают из кукурузы или других кормовых культур, включая сорго или другие зерновые злаки, используя всю зеленую массу растений. Силосную массу обычно дают на корм молочному скоту, тогда как силос в брикетах обычно используют для мясного скота, овец и лошадей. Так как силос проходит процесс ферментации, энергия используется ферментативными бактериями для продукции летучих жирных кислот, таких как ацетат, пропионат, лактат и бутират, которые консервируют фураж. Результат состоит в том, что силос имеет более низкую энергетическую ценность, чем исходный фураж, поскольку ферментативные бактерии используют некоторые углеводы для синтеза летучих жирных кислот. Кукурузный силос является распространенным кормом для жвачных животных, потому что он обладает высокой энергетической ценностью и усвояемостью и легко приспособлен к механизации от полевой культуры до момента кормления. Кукурузный силос обычно имеет цвет от коричневатого до темно-зеленого и легкий, приятный запах.
Пониженное содержание лигнина в кукурузе brown midrib (кукурузе bm) приводит к получению силоса с более усвояемыми волокнами по сравнению с обычной кукурузой, и демонстрирует повышенную степень превращения в биотопливо. Кормление дойных коров силосом из кукурузы bmr, как было показано, увеличивает потребление сухого вещества (DMI) и выход молока (Grant et al. (1995) J. Dairy Sci. 78:1970-80; Oba and Allen (2000) J. Dairy Sci. 83:1333-41; Oba and Allen (1999) J. Dairy Sci. 82:135-42). Однако силос из кукурузы bmr уменьшал средний ежедневный прирост веса и эффективность кормления (G:F) у коров мясных пород, по сравнению с кукурузным силосом из обычного сорта кукурузы (Tjardes et al. (2000) J. Anim. Sci. 78:2957-65). Гибридные линии кукурузы brown midrib, как также часто обнаруживали, являлись низкоурожайными. Гибридную кукурузу brown midrib также обычно связывали с полеганием кормовых растений и недостаточной стойкостью к полеганию.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящей заявке описаны молекулы нуклеиновых кислот, включающие мутантный ген CAD2, который вносит вклад в фенотип bm1 кукурузы. Также описаны молекулярные маркеры, которые связаны или присутствуют в мутантном гене CAD2 кукурузы. Неожиданно, сложный путь биосинтеза лигнина подвергается очевидному изменению в присутствии мутантного гена CAD2, в результате чего растения, содержащие мутантный ген CAD2, имеют более низкие уровни лигнина по сравнению с уровнями лигнина, обнаруживаемыми в растениях дикого типа. Исследование мутантных генов CAD2 и идентификация маркеров, связанных с мутантными генами CAD2, может существенно облегчить создание и введение фенотипов с пониженным содержанием лигнина в зародышевую плазму растения. В некоторых вариантах осуществления, маркеры, которые связаны или присутствуют в мутантном гене CAD2 кукурузы или в последовательности мутантного гена CAD2 кукурузы непосредственно, могут применяться для введения мутантного гена CAD2 кукурузы в другие организмы, например растения, дрожжи и прокариоты.
В конкретных вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может включать нуклеотидную последовательность, кодирующую усеченный белок CAD2. Например, мутантный ген CAD2, включающий мутацию со вставкой в экзоне (например, экзоне 3) или интроне (например, интроне 1) гена CAD2, может вводить преждевременный стоп-кодон, что приводит к синтезу более короткого продукта гена. В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может включать встречающуюся в природе мутацию в одной или более линиях кукурузы. В некоторых вариантах осуществления, мутантный ген CAD2 клонирован из известного сорта кукурузы bmr, например 515Dbm1. В других вариантах осуществления, мутантный ген CAD2 клонирован из ранее неизвестного сорта кукурузы bmr, например, DASbm1. При экспрессии в растении, мутантный ген CAD2 согласно настоящему описанию может обеспечивать некоторый фенотип растения, например, с пониженными уровнями РНК CAD2 в тканях растения и/или с пониженным содержанием лигнина в тканях растения.
Также в настоящей заявке описаны способы применения молекулярных маркеров на основе нуклеиновой кислоты, которые связаны с или присутствуют в мутантном гене CAD2 кукурузы согласно настоящему описанию, в качестве неограничивающего примера: для идентификации растений, имеющих фенотип, характеризуемый пониженным содержанием лигнина; для введения мутантного гена CAD2 кукурузы в генотипы новых растений (например, посредством скрещивания с помощью маркеров или генетической трансформации); для различения генов CAD2 дикого типа и определенных мутантных генов CAD2 согласно настоящему описанию; и для получения растений и семян растений из кроссов первого растения, включающего молекулярные маркеры на основе нуклеиновой кислоты, которые связаны с или присутствуют в мутантном гене CAD2 кукурузы согласно настоящему описанию, и второго растения, необязательно несущего мутантный ген CAD2 кукурузы. В некоторых вариантах осуществления, мутантный ген CAD2 кукурузы введен с помощью генно-инженерных манипуляций в виды растений, отличные от кукурузы.
Кроме того, описаны средства для получения генетически модифицированного растения (например, кукурузы), включающего мутантный ген CAD2 кукурузы, а также средства для идентификации растений (например, кукурузы), несущих мутантный ген CAD2 кукурузы. Средство для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы, является маркером, который связан с или присутствует в мутантном гене CAD2 кукурузы согласно настоящему описанию. Средство для идентификации растений, несущих мутантный ген CAD2 кукурузы, является зондом, который специфично гибридизуется с маркером, связанным с или присутствующим в мутантном гене CAD2 кукурузы согласно настоящему описанию.
Раскрыты способы увеличения количества мяса у животного, откармливаемого силосом, например, путем увеличения отношения прироста веса к массе потребляемого корма (G:F) в случае кукурузного силоса. В некоторых вариантах осуществления, способ увеличения количества мяса у животного, откармливаемого силосом, может включать в себя получение растительного материала, полученного из кукурузы, включающей мутантный ген CAD2 кукурузы согласно настоящему описанию, применение растительного материала для производства кукурузного силоса, и включение кукурузного силоса в конечный рацион для откорма жвачного. Таким образом, мясо и мясные продукты, произведенные из животного, откормленного на конечном рационе согласно настоящему описанию или согласно способу, который также представлен в настоящем описании.
Предыдущие и другие признаки станут более ясны из последующего подробного описания некоторых вариантов осуществления, которые следуют далее со ссылкой на сопровождающие фигуры.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 включает диаграмму, на которой показаны относительные длины и положения семи перекрывающихся ПЦР-фрагментов 515Dbm1 CAD2. Фиг.1 также включает диаграмму, на которой показаны относительные длины и положения тринадцати перекрывающихся ПЦР-фрагментов DASbm1 CAD2.
Фиг.2 включает диаграмму, на которой показаны геномная структура вставки в DASbm1 CAD2. Показаны только два первых эндогенных экзона CAD2.
Фиг.3 включает выравнивание геномных последовательностей ZmCAD2 с использованием последовательности B73 из общедоступного образца AC230031. Идентифицированы 15 SNP и 8 вставок/делеций, а также вставка транспозона в DASbm1. AC-вставка присутствует только в мутанте 515Dbm1 в экзоне 3. Экзоны показаны заглавным шрифтом. Интроны и промоторная область показаны строчным шрифтом.
Фиг.4 включает выравнивание предсказанных кДНК последовательностей ZmCAD2, включая кДНК последовательности, амплифицированные с использованием пары праймеров CVF/CVR с DASbm1, 515Dbm1 и дикого типа 6XN442 (подчеркнута). DASbm1 содержит вставку размером 409 п.н.
Фиг.5 включает выравнивание предсказанных последовательностей белка ZmCAD2, при этом показано, что CAD2 из 515Dbm1 содержит только 147 аминокислот из-за наличия AC вставки, которая вызывает сдвиг рамки считывания и вводит преждевременный стоп-кодон. CAD2 из DASbm1 содержит только 48 аминокислот, по сравнению с 367 аминокислотами в CAD2 из 6XB442. Области идентичности выделены полужирным шрифтом. Аминокислотная последовательность B73 CAD2 идентична аминокислотной последовательности 6XN422 CAD2 и поэтому не показана.
Фиг.6 включает данные, показывающие относительные уровни экспрессии РНК CAD2 в средних жилках и листьях кукурузы дикого типа, 515Dbm1 и DASbm1. Данные нормализованы по уровню РНК в средней жилке листьев кукурузы дикого типа 6XN442. Данные представляют собой среднее значение для 3 растений, и планки погрешностей указывают стандартное отклонение.
Фиг.7 включает данные, показывающие относительные количества общего лигнина в кукурузе дикого типа, 515Dbm1 и DASbm1. Данные представляют собой среднее значение для 3 растений, при этом с каждого растения получали по пять образцов из листьев и из междоузлий. Планки погрешностей указывают стандартное отклонение, и P-значения получали с использованием t-критерия Стьюдента.
Фиг.8 включает диаграмму системы анализа KASPar с последовательностями праймеров и матриц. Показаны последовательности матриц 515Dbm1 (SEQ ID NO:45) и 6XN442 (SEQ ID NO:46).
Фиг.9 включает данные, показывающие определение аллеля bm1 с помощью анализа KASPar. Необработанные данные по интенсивности флуоресценции от планшет-ридера анализировали с использованием системы KBioscience Laboratory Information Management System (KLIMS). График, на котором показаны значения RFU FAM, нанесенные в зависимости от RFU от VIC, также был получен при использовании KLIMS. Определение генотипа выполняли на основе разделения кластеров, как показано в изображении кластеров.
Фиг.10 включает данные, показывающие TaqMan определение аллелей CAD2. Аллельную дискриминацию вычисляли при использовании программы для амплификатора iCycler с оптической системой, при этом относительные единицы флуоресценции (RFU) VIC показаны на оси Y, а RFU FAM показаны на оси X.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Последовательности нуклеиновых кислот, перечисленные в сопровождающем списке последовательностей, показаны с использованием стандартных буквенных сокращений для нуклеотидных оснований, как определено в 37 C.F.R. § 1.822. Показана только одна цепь каждой последовательности нуклеиновой кислоты, но при этом следует понимать, что комплементарная цепь включена посредством любой отсылки к показанной цепи. В сопровождающем списке последовательностей:
В SEQ ID NO: 1 показана геномная последовательность 515Dbm1 CAD2 размером 5924 п.н.
В SEQ ID NO: 2 показана предсказанная кДНК последовательность 515Dbm1 CAD21512 размером п.н.
В SEQ ID NO: 3 показана предсказанная последовательность усеченного белка 515Dbm1 CAD2 размером 147 аминокислот.
В SEQ ID NO: 4 показана геномная последовательность 6XN442 CAD2 размером 5898 п.н.
В SEQ ID NO: 5 показана предсказанная кДНК последовательность 6XN442 CAD2 размером 1510 п.н.
В SEQ ID NO: 6 показана предсказанная последовательность белка 6XN442 CAD2 размером 367 аминокислот.
В SEQ ID NO: 7 показана геномная последовательность B73 CAD2 размером 5916 п.н.
В SEQ ID NO: 8 показана предсказанная кДНК последовательность B73 CAD2 размером 1510 п.н.
В SEQ ID NO: 9-22 показаны прямые и обратные праймеры, используемые для амплификации семи перекрывающихся фрагментов CAD2, а также мутанта 515Dbm1 и кукурузы дикого типа 6XN442.
В SEQ ID NO: 23 показана геномная последовательность DASbm1 CAD2 размером 9360 п.н.
В SEQ ID NO: 24 показана неполная кДНК последовательность DASbm1 CAD2, амплифицированная с использованием пары праймеров CVF/CVR.
В SEQ ID NO: 25 показана предсказанная последовательность усеченного белка DASbm1 CAD2 размером 48 аминокислот.
В SEQ ID NO: 26-34 показаны прямые и обратные праймеры, используемые для амплификации неполных фрагментов CAD2 из мутанта DASbm1.
В SEQ ID NO: 35 и 36 показаны прямой и обратный праймеры, используемые для амплификации неполного кДНК фрагмента CAD2.
В SEQ ID NO: 37-39 показаны прямые и обратный праймеры, используемые для амплификации неполных фрагментов CAD2 из мутанта DASbm1.
В SEQ ID NO: 40 показана вставка транспозона длиной 3444 п.н. в DASbm1 CAD2.
В SEQ ID NO: 41 показана дуплицированная последовательность длиной 11 п.н. во вставке транспозона DASbm1 из первого интрона CAD2: TACTGATATCT.
В SEQ ID NO: 42-44 показаны праймеры, используемые в анализе KASPar™ для дифференцирования аллеля 515Dbm1 от других аллелей bm1 и CAD2 дикого типа.
В SEQ ID NO: 45 и 46 показаны последовательности матриц, с которыми праймеры отжигаются в анализе KASPar. SEQ ID NO: 45 представляет собой геномную последовательность из 515Dbm1. SEQ ID NO: 46 представляет собой геномную последовательность из 6XN442.
В SEQ ID NO: 47 показан зонд, специфичный к мутанту DASbm1.
В SEQ ID NO: 48 показан зонд, специфичный к аллелю CAD2 дикого типа.
В SEQ ID NO: 49-51 показаны праймеры, используемые в анализе KASPar™ для дифференцирования аллелей DASbm1 и CAD2 дикого типа.
В SEQ ID NO: 52 показан зонд, специфичный к мутанту 515Dbm1.
В SEQ ID NO: 53 показан зонд, специфичный к аллелю CAD2 дикого типа.
В SEQ ID NO: 54 и 55 показаны праймеры, используемые в анализе KASPar™ для дифференцирования аллелей 515Dbm1 и CAD2 дикого типа.
В SEQ ID NO: 56-61 показаны праймеры и зонды, используемые для кПЦР-ОТ CAD2 и контролей.
В SEQ ID NO: 62 показана нуклеотидная последовательность первого экзона CAD2.
В SEQ ID NO: 63 показана нуклеотидная последовательность второго экзона CAD2.
В SEQ ID NO: 64 показана нуклеотидная последовательность третьего экзона CAD2.
СПОСОБ(Ы) ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
I. Краткий обзор нескольких вариантов осуществления
Мутант bm1 включает неописанную ранее мутацию, которая колокализована с локусом CAD (Halpin et al. (1998), выше; Guillaumie et al. (2007), выше). В настоящей заявке описана идентификация специфических мутаций в кодирующей последовательности CAD2 Zea mays, которые вносят вклад в bm1 фенотип. Некоторые варианты осуществления включают мутантный ген CAD2, клонированный из общедоступной линии кукурузы bm1, 515Dbm1, который содержит AC вставку в 3-ем экзоне, что приводит к образованию усеченного белка CAD2. Некоторые варианты осуществления включают мутантный ген CAD2, клонированный из недавно обнаруженной линии кукурузы bmr, DASbm1, который содержит вставку транспозона, которая приводит к особому усеченному белку CAD2. Растения DASbm1 имеют значительно более низкие уровни экспрессии РНК CAD2, чем растения дикого типа, а также демонстрируют пониженное содержание лигнина. Также описано создание, проверка и применение высокоэффективных маркеров, связанных с каждой конкретной мутацией.
Молекулярная основа фенотипа bm1 не известна настолько, насколько известна, например, bm3. Halpin с сотр. (1998), см. выше, показали, что активности CAD, уровни белка и транскрипта, были значительно снижены в генотипах bm1, и ген CAD, позднее идентифицированный как CAD2, был картирован близко сцепленным с локусом bm1. Поскольку некоторое количество белка и мРНК CAD можно обнаружить в мутантных растениях, авторы предположили, что bm1 не была нулевой мутацией CAD2, а вместо этого влияла на его экспрессию посредством регуляторных элементов (Halpin et al. (1998), выше). Последующие исследования экспрессии генов с использованием микрочипов показали, что большое количество генов, помимо только CAD2, характеризовались пониженной экспрессией в растениях bm1 (Guillaumie et al. (2007), выше). Такое множество генов с пониженной экспрессией включали много генов пути биосинтеза лигнина и факторов транскрипции, что приводило к дальнейшему предположению, что возможно один из факторов транскрипции был ключевым геном для bm1.
Позднее было показано, что нонсенс-мутации в гене сорго SbCAD2 являлись ключевым механизмом в случае bmr мутанта сорго, bmr6, в некоторых сортах (Saballos et al. (2009) Genetics 181:783-95; Sattler et al. (2009) Plant Physiology 150:584-95). Нонсенс-мутация содержит замену C на T, которая создает преждевременный стоп-кодон и приводит к усеченному белку SbCAD2, который не имеет NADPH-связывающего и C-концевого каталитического доменов. Id.
Ввиду вышеизложенного, была поставлена под сомнение общепринятая теории, что bm1 фенотип связан с мутацией в факторе транскрипции или регуляторном элементе гена, и было проведено исследование с целью определить, могла ли мутация в CAD2 кукурузы давать фенотип bm1. Тщательная проверка генетической/физической карты кукурузы в области локусов bm1 и CAD2 показала, что CAD2 кукурузы расположен очень близко к центромере на хромосоме 5. Такая близость представляет существенное затруднение для генного картирования высокого разрешения вследствие известной супрессии рекомбинации вблизи центромерных областей. Поэтому, успех традиционных методов картирования генов был по меньшей мере непредсказуем, если не полностью маловероятен, и был разработан основанный на ПЦР метод клонирования гена-кандидата для идентификации каких-либо определенных мутаций в ZmCAD2, которые могли быть ответственны за bm1 фенотип в рассматриваемых сортах кукурузы.
Таким образом, в некоторых вариантах осуществления, идентификация определенных мутантов CAD2 может быть выполнена с применением основанного на ПЦР метода клонирования. В некоторых вариантах осуществления, CAD2 Zea mays может быть клонирован как из bm1, так и из зародышевой плазмы дикого типа, с целью идентификации определенной мутации в CAD2 из зародышевой плазмы bm1. В конкретных вариантах осуществления, в зародышевой плазме bm1 идентифицирована мутация со вставкой динуклеотида AC, приводящая к сдвигу рамки считывания. В других вариантах осуществления, в зародышевой плазме bm1 идентифицирована вставка транспозона длиной 3444 пары оснований в первом интроне CAD2. Конкретный мутантный ген CAD2, приводящий к bm1 фенотипу в кукурузе, описанный в настоящей заявке, включает вставку динуклеотида AC в третьем экзоне гена CAD2, клонированного из сорта bm1, 515Dbm1.
Другой мутантный ген CAD2, приводящий к bm1 фенотипу в кукурузе, описанный настоящей заявке, включает вставку транспозона в гене CAD2 нового сорта bm1, DASbm1. Идентифицированная вставка имеет длину 3444 пары оснований и расщеплена на три экзона (409 пар оснований), которые формируют химерную мРНК с CAD2. Химерная мРНК вызывает сдвиг рамки считывания и вводит преждевременный стоп-кодон в кодирующей области, что приводит к усеченному белку CAD2 размером лишь 48 аминокислот. Указанный усеченный белок не имеет NADPH-связывающего и C-концевого каталитического доменов, и поэтому наиболее вероятно нефункционален, даже если он продуцируется в клетке.
Растения DASbm1, как и 515Dbm1, имеют значительно сниженные уровни РНК CAD2 и пониженное содержание общего лигнина. Как было определено, CAD2 является ключевым геном в фенотипе кукурузы bm1 в таких природных мутантах и обеспечивает молекулярную основу для наблюдаемого фенотипа bmr. С учетом вставки транспозона в DASbm1 и AC вставки в 515Dbm1, высокопроизводительные анализы KASPar и TaqMan для обнаружения указанных конкретных аллелей CAD2 и их дифференцирования от аллелей дикого типа были определены и оценены. Данные анализы могут применяться для идентификации зародышевой плазмы bm1, для ускорения интрогрессии признака bm1, а также для облегчения молекулярной селекции растений, обеспечивающих, например, получение силоса с улучшенной перевариваемостью и/или повышенный выход этанола для получения биотоплива. Последовательности модифицированного гена CAD2 могут применяться для введения фенотипа bm1 в новые генотипы кукурузы или другие культуры, например, сорго и просо, с использованием трансгенных методов. Фенотип bm1 и другие bmr фенотипы также могут применяться в качестве маркеров визуальной селекции для трансгенов в сочетании с технологией EXZACT Precision Technology (Dow AgroSciences).
Высокоэффективные ПЦР-маркеры могут применяться, среди прочего: для идентификации в организме мутации CAD2, которая вносит вклад в фенотип bm1 в кукурузе; для введения в организм (например, растение) мутации CAD2, которая вносит вклад в фенотип bm1 в кукурузе; и для облегчения селекции кукурузы bm1 с использованием маркеров. Таким образом, также описано создание, проверка и применение конкретных высокоэффективных ПЦР-маркеров на основе определенных мутаций в CAD2 (например, мутация со сдвигом рамки считывания и вставка транспозона).
II. Сокращения
III. Термины
Бэккроссинг или обратное скрещивание: методы обратного скрещивания могут использоваться для введения последовательности нуклеиновой кислоты в растения. Метод обратного скрещивания широко использовался в течение многих десятилетий для введения новых признаков в растения (Jensen, N., Ed. Plant Breeding Methodology, John Wiley & Sons, Inc., 1988). В типичной методике обратного скрещивания исходный целевой сорт (рекуррентный родитель) скрещивают со вторым сортом (нерекуррентным родителем), несущим целевой ген, который нужно передать. Полученное потомство от этого кросса затем снова скрещивают с рекуррентным родителем и повторяют процесс до тех пор, пока не будет получено растение, обладающее по существу всеми требуемыми морфологическими и физиологическими характеристиками рекуррентного растения, в дополнение к переданному гену от нерекуррентного родителя.
Растение кукурузы: Используемый в настоящем описании термин "растение кукурузы" относится к растению вида Zea mays (кукуруза сахарная или маис).
Кукуруза BM: Используемый в настоящем описании термин "кукуруза BM" (или "кукуруза BMR") относится к сортам кукурузы, которые содержат мутацию brown midrib. Сорта кукурузы BM обычно демонстрируют красновато-коричневую пигментацию средней жилки листа. Кукуруза BM также обычно характеризуется более низким содержанием лигнина, более высокой перевариваемостью волокна и более высоким накоплением сухого вещества. Неограничивающие примеры сортов кукурузы BM включают сорта кукурузы bm1; например, 515Dbm1.
Фенотип bm1: Используемый в настоящем описании термин "фенотип bm1" может относиться к профилю измененного содержания и/или состава лигнина, который наблюдался в кукурузе bm1. В качестве неограничивающего примера, фенотип bm1 может быть охарактеризован одной или более следующими особенностями: содержание лигнина, которое снижено на 10-20% по сравнению с содержанием лигнина в растении дикого типа тех же видов (Guillaumie et al. (2007), выше); пониженное содержание сложных эфиров феруловой кислоты (Id.); пониженное содержание простых эфиров феруловой кислоты (Id.); уменьшенное содержание сложных эфиров п-кумаровой кислоты (Marita et al. (2003) J. Agric. Food Chem. 51:1313-21); повышенные уровни альдегидов (Id).; обогащение лигнинов углерод-углеродными межсубъединичными связями (Halpin et al. (1998), выше; Barriére et al. (2004), выше); а также существенное включение в лигнины кониферилового альдегида и/или синапового альдегида (Kim et al. (2002), выше; и Barriére et al. (2004), выше).
Сухое вещество: Используемый в настоящем описании термин "сухое вещество" относится к любому корму, включая фураж.
Система SNP генотипирования на основе конкурентной аллель-специфической ПЦР (KASPar™) KBiosciences: KASPar™ представляет собой коммерческую гомогенную флуоресцентную систему для определения SNP генотипов (KBiosciences Ltd., Hoddesdon, UK). Анализ KASPar™ включает SNP-специфичную "аналитическую смесь", которая содержит три немеченых праймера, и "реакционную смесь", которая содержит все остальные необходимые компоненты, например, универсальную флуоресцентную репортерную систему. В дополнение к указанным смесям, пользователь обеспечивает, среди прочего, FRET-совместимый планшет-ридер, микротитровальный планшет(ы) и образцы ДНК, которые содержат приблизительно 5 нг/л ДНК.
Типовой анализ KASPar™ включает следующие этапы: подбор аллель-специфичных праймеров (например, с использованием PrimerPicker™, который является бесплатным сервисом, доступным через Интернет на веб-сайте KBiosciences); приготовление реакционной смеси, включающей аллель-специфичные праймеры; добавление реакционной смеси к образцам ДНК в микротитровальном планшете; амплификацию; сканирование планшета на флуоресцентном планшет-ридере; и построение кривых и оценку флуресцентных данных. Данные для каждого образца наносят вместе на 2-мерный график, где оси X и Y соответствуют значениям флуоресценции FAM и VIC. Образцы, имеющие один и тот же SNP генотип, объединяют в кластер на графике (то есть A/A; A/a и a/a). Дополнительную техническую информацию о системе KASPar, включая руководство по решению часто встречаемых проблем, можно получить от KBiosciences Ltd. (например, из руководства KASPar SNP Genotyping System Reagent Manual).
Сцепленный, сильно сцепленный и очень сильно сцепленный: Используемое в настоящем описании сцепление между генами или маркерами может относиться к такому явлению, когда гены или маркеры на хромосоме показывают измеряемую вероятность совместного переноса в индивидуальные организмы в следующем поколении. Чем ближе друг к другу расположены два гена или маркера, тем ближе к (1) становится данная вероятность. Таким образом, термин "сцепленный" может относиться к одному или более генам или маркерам, которые передаются вместе с геном с вероятностью больше 0,5 (что ожидается из независимого распределения, когда маркеры/гены расположены на различных хромосомах). Когда присутствие гена вносит вклад в фенотип индивидуального организма, можно сказать, что маркеры, которые сцеплены с геном, связаны с фенотипом. Таким образом, термин "сцепленный" может относиться к взаимосвязи между маркером и геном или между маркером и фенотипом.
Поскольку близость двух генов или маркеров на хромосоме непосредственно связана с вероятностью того, что гены или маркеры будут вместе передаваться индивидуальным организмам в следующем поколении, термин "сцепленный" также может относиться в настоящем описании к одному или более генам или маркерам, которые расположены в пределах приблизительно 2,0 мпн друг от друга на одной и той же хромосоме кукурузы. Таким образом, два "сцепленных" гена или маркера могут быть разделены приблизительно на 2,1 мпн; 2,00 мпн; приблизительно на 1,95 мпн; приблизительно на 1,90 мпн; приблизительно на 1,85 мпн; приблизительно на 1,80 мпн; приблизительно на 1,75 мпн; приблизительно на 1,70 мпн; приблизительно на 1,65 мпн; приблизительно на 1,60 мпн; приблизительно на 1,55 мпн; приблизительно на 1,50 мпн; приблизительно на 1,45 мпн; приблизительно на 1,40 мпн; приблизительно на 1,35 мпн; приблизительно на 1,30 мпн; приблизительно на 1,25 мпн; приблизительно на 1,20 мпн; приблизительно на 1,15 мпн; приблизительно на 1,10 мпн; приблизительно на 1,05 мпн; приблизительно на 1,00 мпн; приблизительно на 0,95 мпн; приблизительно на 0,90 мпн; приблизительно на 0,85 мпн; приблизительно на 0,80 мпн; приблизительно на 0,75 мпн; приблизительно на 0,70 мпн; приблизительно на 0,65 мпн; приблизительно на 0,60 мпн; приблизительно на 0,55 мпн; приблизительно на 0,50 мпн; приблизительно на 0,45 мпн; приблизительно на 0,40 мпн; приблизительно на 0,35 мпн; приблизительно на 0,30 мпн; приблизительно на 0,25 мпн; приблизительно на 0,20 мпн; приблизительно на 0,15 мпн; приблизительно на 0,10 мпн; приблизительно на 0,05 мпн; приблизительно на 0,025 мпн и приблизительно на 0,01 мпн. Конкретные примеры маркеров, которые могут быть "сцеплены" с фенотипом bm1 в кукурузе, включают нуклеотидные последовательности на хромосоме 5L генома кукурузы.
Используемый в настоящем описании термин "сильно сцепленный" может относиться к одному или более генам или маркерам, которые расположены в пределах приблизительно 0,5 мпн друг от друга на одной и той же хромосоме кукурузы. Таким образом, два "сильно сцепленных" гена или маркера могут быть разделены приблизительно на 0,6 мпн; приблизительно на 0,55 мпн; 0,5 мпн; приблизительно на 0,45 мпн; приблизительно на 0,4 мпн; приблизительно на 0,35 мпн; приблизительно на 0,3 мпн; приблизительно на 0,25 мпн; приблизительно на 0,2 мпн; приблизительно на 0,15 мпн; приблизительно на 0,1 мпн и приблизительно на 0,05 мпн. Конкретные примеры маркеров, которые могут быть "сильно сцеплены" с фенотипом bm1 в кукурузе, включают нуклеотидные последовательности вблизи или в локусе CAD2 генома кукурузы.
Используемый в настоящем описании термин "очень сильно сцепленный" может относиться к одному или более генам или маркерам, которые расположены в пределах приблизительно 100 тпн друг от друга на одной и той же хромосоме кукурузы. Таким образом, два "очень сильно сцепленных" гена или маркера могут быть разделены приблизительно на 125 тпн; приблизительно на 120 тпн; приблизительно на 115 тпн; приблизительно на 110 тпн; приблизительно на 105 тпн; 100 тпн; приблизительно на 95 тпн; приблизительно на 90 тпн; приблизительно на 85 тпн; приблизительно на 80 тпн; приблизительно на 75 тпн; приблизительно на 70 тпн; приблизительно на 65 тпн; приблизительно на 60 тпн; приблизительно на 55 тпн; приблизительно на 50 тпн; приблизительно на 45 тпн; приблизительно на 40 тпн; приблизительно на 35 тпн; приблизительно на 30 тпн; приблизительно на 25 тпн; приблизительно на 20 тпн; приблизительно на 15 тпн; приблизительно на 10 тпн; приблизительно на 5 тпн и приблизительно на 1 тпн. Конкретные примеры маркеров, которые "очень сильно сцеплены" с фенотипом bm1 в кукурузе, включают нуклеотидные последовательности в интронах и экзонах гена CAD2.
С учетом вышеизложенного, необходимо понимать, что маркеры, сцепленные с конкретным геном или фенотипом, включают такие маркеры, которые сильно сцеплены, а также маркеры, которые очень сильно сцеплены, с геном или фенотипом. Сцепленные, сильно сцепленные и очень сильно сцепленные генетические маркеры фенотипа bm1 могут быть полезными в программах селекции с применением маркеров для идентификации сортов кукурузы, имеющих сниженное содержание лигнина и повышенную перевариваемость, и для введения указанных признаков в другие сорта кукурузы.
Локус: Используемый в настоящем описании термин "локус" относится к положению в геноме, которое соответствует измеримой характеристике (например, признаку). Локус SNP определяют с помощью зонда, который гибридизуется с ДНК, содержащейся в локусе.
Маркер: Используемый в настоящем описании маркер относится к гену или нуклеотидной последовательности, которая может применяться для идентификации растений, несущих определенный аллель. Маркер может быть описан как вариация в данном геномном локусе. Генетический маркер может быть короткой последовательностью ДНК, такой как последовательность, окружающая одиночную замену пары оснований (однонуклеотидный полиморфизм или "SNP"), или длинной последовательностью ДНК, например, минисателлитной/простой повторяющейся последовательностью ("SSR"). "Маркерный аллель" относится к варианту маркера, который присутствует в конкретном индивидуальном организме.
Термин маркер, используемый в настоящем описании, может относиться к клонированному сегменту хромосомной ДНК кукурузы (например, к нуклеотидным последовательностям вблизи или в пределах локуса CAD2 генома кукурузы), и может также, дополнительно или альтернативно, относиться к молекуле ДНК, которая комплементарна клонированному сегменту хромосомной ДНК кукурузы (например, к ДНК, которая комплементарна нуклеотидной последовательности вблизи или в пределах локуса CAD2 генома кукурузы). Конкретные примеры маркеров bm1 в кукурузе включают, без ограничения, последовательности нуклеиновых кислот, включающие нуклеотид 66 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 284 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 415 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 443 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 735 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 760 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 1345 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 1408 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 1585 из гена CAD2; последовательности нуклеиновой кислоты, включающие любой из нуклеотидов 1627-1640 и/или 1642-1648 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 2252 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 2269 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 2786 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 2966 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3205 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3719 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3783 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3798 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3800 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 3994 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 4141 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 4338 из гена CAD2; последовательности нуклеиновых кислот, включающие нуклеотид 4583 из гена CAD2; и последовательности нуклеиновых кислот, включающие нуклеотид 5403 из гена CAD2. Перечисленные выше маркеры идентифицированы положением нуклеотида в сорте кукурузы дикого типа, B73.
В некоторых вариантах осуществления, присутствие маркера в растении может быть обнаружено с помощью зонда на основе нуклеиновой кислоты. Зонд может быть молекулой ДНК или молекулой РНК. РНК зонды можно синтезировать способами, известными в уровне техники, например, при использовании матричной молекулы ДНК. Зонд может содержать полную нуклеотидную последовательность маркера или ее часть, а также дополнительную, примыкающую (смежную) нуклеотидную последовательность из генома растения. Такой зонд называется в настоящем описании "смежным зондом". Дополнительная, примыкающая нуклеотидная последовательность расположена "слева" или "справа" от исходного маркера в зависимости от того, находится ли смежная нуклеотидная последовательность относительно хромосомы растения на 5’ или 3’ стороне исходного маркера, как обычно понимается. Как известно средним специалистам в данной области, процесс получения дополнительной, смежной нуклеотидной последовательности для включения в маркер можно повторять почти до бесконечности (с ограничением только длиной хромосомы), идентифицируя таким образом дополнительные маркеры на хромосоме. Все вышеописанные маркеры могут применяться в некоторых вариантах осуществления настоящего изобретения.
Последовательность олигонуклеотидного зонда может быть получена с помощью синтеза или при клонировании. Подходящие клонирующие векторы известны специалистам в данной области. Олигонуклеотидный зонд может быть меченым или нет. Существует целый ряд методов для введения меток в молекулы нуклеиновых кислот, включая, в качестве неограничивающего примера: введение радиоизотопной метки посредством ник-трансляции; случайное праймирование; наращивание 3’-концов терминальной дезокситрансферазой; или подобное, где применяемые нуклеотиды метят, например, радиоактивным 32P. Другие метки, которые могут использоваться, включают, в качестве неограничивающего примера: флуорофоры (например, FAM и VIC); ферменты; субстраты ферментов; кофакторы ферментов; ингибиторы ферментов и т.п. В альтернативе, применение метки, которая дает детектируемый сигнал, отдельно или в сочетании с другими активными агентами, можно заменить лигандами, с которыми связываются рецепторы, где рецепторы содержат метки (например, вышеуказанные метки), обеспечивая детектируемые сигналы, либо самостоятельно, либо в сочетании с другими реагентами. См., например, Leary et al. (1983) Proc. Natl. Acad. Sci. USA 80:4045-9.
Зонд может содержать нуклеотидную последовательность, которая не является смежной с последовательностью исходного маркера; данный зонд называется в настоящем описании "несмежным зондом". Последовательность несмежного зонда расположена достаточно близко к последовательности исходного маркера на геноме, так, что несмежный зонд генетически сцеплен с тем же геном или признаком (например, bm1/сниженное содержание лигнина). Например, в некоторых вариантах осуществления, несмежный зонд расположен в пределах 500 тпн; 450 тпн; 400 тпн; 350 тпн; 300 тпн; 250 тпн; 200 тпн; 150 тпн; 125 тпн; 100 тпн; 0,9 тпн; 0,8 тпн; 0,7 тпн; 0,6 тпн; 0,5 тпн; 0,4 тпн; 0,3 тпн; 0,2 тпн; или 0,1 тпн исходного маркера на геноме кукурузы.
Зонд может быть точной копией маркера, который нужно детектировать. Зонд также может быть молекулой нуклеиновой кислоты, включающей или состоящей из нуклеотидной последовательности, которая по существу идентична клонированному сегменту хромосомной ДНК рассматриваемого организма (например, кукурузы). Используемый в настоящем описании термин "по существу идентичный" может относиться к нуклеотидным последовательностям, которые являются идентичными больше чем на 85%. Например, по существу идентичная нуклеотидная последовательность может быть на 85,5%; 86%; 87%; 88%; 89%; 90%; 91%; 92%; 93%; 94%; 95%; 96%; 97%; 98%; 99% или 99,5% идентична референсной последовательности.
Зонд также может быть молекулой нуклеиновой кислоты, которая способна к "специфичной гибридизации" или является "специфично комплементарной" с точной копией детектируемого маркера ("ДНК-мишенью"). "Специфично гибридизуемый" и "специфично комплементарный" являются терминами, которые указывают на достаточную степень комплементарности, при которой происходит устойчивое и специфичное связывание между молекулой нуклеиновой кислоты и ДНК-мишенью. Молекула нуклеиновой кислоты не должна быть обязательно на 100% комплементарной со своей последовательностью-мишенью, чтобы она могла специфично гибридизоваться с ней. Молекула нуклеиновой кислоты является специфично гибридизуемой, когда существует достаточная степень комплементарности, позволяющая избежать неспецифичного связывания нуклеиновой кислоты с нецелевыми последовательностями при условиях, когда требуется специфичное связывание, например, при строгих условиях гибридизации.
Условия гибридизации, приводящие к определенным степеням строгости, изменятся в зависимости от природы выбранного метода гибридизации, а также состава и длины гибридизуемых последовательностей нуклеиновой кислоты. Как правило, строгость гибридизации определяет температура гибридизации и ионная сила (в особенности концентрация Na+ и/или Mg++) гибридизационного буфера, хотя на строгость также влияет продолжительность промывки. Вычисления относительно условий гибридизации, требуемых для достижения определенных степеней строгости, известны средним специалистам в данной области, и описаны, например, в Sambrook et al. (ed.) Molecular Cloning: A Laboratory Manual, 2nd ed., vol. 1-3, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989, главы 9 и 11; а также в Hames and Higgins (eds.) Nucleic Acid Hybridization, IRL Press, Oxford, 1985. Дополнительную подробную инструкцию и руководство касательно гибридизации нуклеиновых кислот можно найти, например, в Tijssen, "Overview of principles of hybridization and the strategy of nucleic acid probe assays", в Laboratory Techniques in Biochemistry and Molecular Biology-Hybridization with Nucleic Acid Probes, часть I, глава 2, Elsevier, NY, 1993; и в Ausubel et al., Eds., Current Protocols in Molecular Biology, глава 2, Greene Publishing and Wiley-Interscience, NY, 1995.
Используемые в настоящем описании "строгие условия" охватывают условия, при которых гибридизация произойдет только в том случае, если между гибридизуемой молекулой и ДНК-мишенью будет присутствовать менее 50% некомплементарных оснований. "Строгие условия" включают также определенные уровни строгости. Таким образом, используемые в настоящем описании условия "умеренной строгости" являются такими условиями, при которых молекулы с более чем 50% некомплементарных оснований в последовательности, не будут гибридизоваться; условия "высокой строгости" являются условиями, при которых не будут гибридизоваться последовательности с более чем 20% некомплементарных оснований; и условия "очень высокой строгости" являются условиями, при которых не будут гибридизоваться последовательности с более чем 10% некомплементарных оснований.
В конкретных вариантах осуществления, строгие условия могут включать гибридизацию при 60°C в мастер-миксе TaqMan® для генотипирования (Applied Biosystems, Foster City, CA, # 4371355), разведенном согласно инструкциям производителя.
Ниже представлены репрезентативные, неограничивающие условия гибридизации.
Очень высокая строгость (обнаруживает последовательности, которые обладают по меньшей мере 90% идентичностью последовательности): гибридизация в 5xSSC буфере при 65°C в течение 16 часов; двухкратная промывка в 2xSSC буфере при комнатной температуре в течение 15 минут каждая; и двухкратная промывка в 0,5xSSC буфере при 65°C в течение 20 минут каждая.
Высокая строгость (обнаруживает последовательности, которые обладают по меньшей мере 80% идентичностью последовательности): гибридизация в 5х-6xSSC буфере при 65-70°C в течение 16-20 часов; двухкратная промывка в 2xSSC буфере при комнатной температуре в течение 5-20 минут каждая; и двухкратная промывка в 1xSSC буфере при 55-70°C в течение 30 минут каждая.
Умеренная строгость (обнаруживает последовательности, которые обладают по меньшей мере 50% идентичностью последовательности): гибридизация в 6xSSC буфере при температуре от комнатной до 55°C в течение 16-20 часов; промывка, по меньшей мере двухкратная, в 2х-3xSSC буфере при температуре от комнатной до 55°C в течение 20-30 минут каждая.
Что касается всех описанных выше зондов, зонд может включать дополнительные последовательности нуклеиновых кислот, например, промоторы; сигналы транскрипции и/или векторные последовательности. Любой из описанных выше зондов может применяться для дополнительного определения маркеров, которые сильно сцеплены с геном, вовлеченным в фенотип bm (например, bm1), при этом маркеры, идентифицированные таким образом, могут быть эквивалентны примерным маркерам, указанным в настоящем описании, и, таким образом, включены в объем изобретения.
Селекция с использованием маркеров: используемый в настоящем описании термин "селекция с использованием маркеров" может относиться к методу селекции непосредственно по одному или более сложным признакам (например, bm1/пониженное содержание лигнина). В сложившейся практике, растениеводы-селекционеры пытаются идентифицировать легко обнаруживаемые признаки, такие как цвет цветов, вид семенной оболочки или изоферментные варианты, которые связаны с сельскохозяйственным важным признаком. Затем селекционеры отслеживают сельскохозяйственный признак в расщепляющихся, селекционных популяциях, прослеживая сегрегацию легко обнаруживаемого признака. Впрочем, очень немногие из таких отношений сцепления доступны для применения в селекции растений.
Селекция с использованием маркеров обеспечивает быстрый и рентабельный процесс улучшения сортов растений. Некоторые примеры применения селекции с использованием маркеров включают применение изоферментных маркеров. См., например, Tanksley and Orton, eds. (1983) Isozymes in Plant Breeding and Genetics, Amsterdam: Elsevier. Одним из примеров является изоферментный маркер, связанный с геном устойчивости к нематодам в томате. Устойчивость регулирует ген, обозначенный Mi, который расположен на хромосоме 6 томата и очень сильно сцеплен с Aps1, изоферментом кислой фосфатазы. Применение изоферментного маркера Aps1 для косвенного отбора гена Mi обеспечило преимущества, состоящие в том, что сегрегация в популяции может быть четко определена с помощью стандартных электрофоретических методов; изоферментный маркер может быть оценен в тканях рассады, что устраняет необходимость в выращивании растений до зрелого состояния; и кодоминантность аллелей изоферментных маркеров позволяет установить различия между гомозиготами и гетерозиготами. См. Rick (1983), в Tanksley and Orton, выше.
Мясо: используемый в настоящем описании термин "мясо" относится к ткани животных, используемой, например, в качестве пищи. Термин "мясо" обычно относится к скелетной мышце и связанному жиру, но может также относиться к немышечным органам, включая легкие, печень, кожу, головной мозг, костный мозг, почки, яички, кишечник и т.д.
Нерастворимое в нейтральном детергенте волокно: используемый в настоящем описании термин "нерастворимое в нейтральном детергенте волокно" (NDF) относится к показателю содержания медленно перевариваемого материала в широком спектре кормов. Уровни NDF в фураже повышаются по мере созревания растений. Средние уровни NDF в травяном силосе могут составлять приблизительно 55 процентов от сухого веса (550 г/кг сухого веса). Содержание NDF в полном рационе может находиться в пределах 35-50% от сухого веса. Рацион с менее чем 32 процентами NDF может вызывать проблемы, связанные с ацидозом. Диеты, которые содержат больше 50 процентов NDF, могут иметь ограниченную пищевую ценность.
Молекула нуклеиновой кислоты: используемый в настоящем описании термин "молекула нуклеиновой кислоты" может относиться к полимерной форме нуклеотидов, которая может включать как смысловые, так и антисмысловые цепи РНК, кДНК, геномной ДНК, а также их синтетические формы и смешанные полимеры. Нуклеотид может относиться к рибонуклеотиду, дезоксирибонуклеотиду или модифицированной форме любого типа нуклеотида. "Молекула нуклеиновой кислоты", используемая в настоящем описании, синонимична "нуклеиновой кислоте" и "полинуклеотиду". Молекула нуклеиновой кислоты обычно имеет длину по меньшей мере 10 оснований, если не определено иное. Термин включает одно- и двунитевые формы ДНК. Молекула нуклеиновой кислоты может включать природные и/или модифицированные нуклеотиды, соединенные природными и/или неприродными нуклеотидными связями.
Молекулы нуклеиновых кислот могут быть модифицированы химически или биохимически, или могут содержать неприродные или дериватизированные нуклеотидные основания, как будет очевидно специалистам в данной области. Такие модификации включают, например, метки, метилирование, замену одного или большего количества природных нуклеотидов аналогом, межнуклеотидные модификации (например, незаряженные связи: например, метилфосфонаты, сложные фосфотриэфиры, фосфорамидаты, карбаматы и т.д.; заряженные связи: например, фосфоротиоаты, фосфородитиоаты и т.д.; боковые группы: например, пептиды; интеркаляторы: например, акридин, псорален и т.д.; хелатирующие агенты; алкилирующие агенты; и модифицированные связи: например, альфа-аномерные нуклеиновые кислоты и т.д.). Термин "молекула нуклеиновой кислоты" также включает в себя любую топологическую конформацию, включая однонитевые, двунитевые, частично дуплексные, триплексные, шпилечные, кольцевые и запертые конформации.
Идентичность последовательности: термин "идентичность последовательности" или "идентичность" используется в настоящем описании в контексте двух последовательностей нуклеиновых кислот или полипептидов и может относиться к остаткам в двух последовательностях, которые являются одинаковыми при выравнивании с максимальным соответствием в указанном окне сравнения.
Используемый в настоящем описании термин "процент идентичности последовательности" может относиться к значению, определяемому при сравнении двух оптимально выровненных последовательностей (например, последовательностей нуклеиновых кислот и аминокислотных последовательностей) в окне сравнения, где часть последовательности в окне сравнения может включать дополнения или делеции (то есть пропуски) по сравнению с референсной последовательностью (которая не включает дополнений или делеций), для оптимального выравнивания двух указанных последовательностей. Процент вычисляют, определяя в обеих последовательностях число положений, в которых присутствует идентичный нуклеотидный или аминокислотный остаток, получая число не совпавших положений, деля число не совпавших положений на общее количество положений в окне сравнения, и умножая результат на 100, получая процент идентичности последовательности.
Методы выравнивания последовательностей для сравнения известны в уровне техники. Различные программы и алгоритмы выравнивания описаны, например, в Smith and Waterman (1981) Adv. Appl. Math. 2:482; Needleman and Wunsch (1970) J. Mol. Biol. 48:443; Pearson and Lipman (1988) Proc. Natl. Acad. Sci. U.S.A. 85:2444; Higgins and Sharp (1988) Gene 73:237-44; Higgins and Sharp (1989) CABIOS 5:151-3; Corpet et al. (1988) Nucleic Acids Res. 16:10881-90; Huang et al. (1992) Comp. Appl. Biosci. 8:155-65; Pearson et al. (1994) Methods Mol. Biol. 24:307-31; Tatiana et al. (1999) FEMS Microbiol. Lett. 174:247-50. Подробное описание методов выравнивания последовательностей и вычисления гомологии можно найти, например, в Altschul et al. (1990) J. Mol. Biol. 215:403-10.
Программа BLAST (Basic Local Alignment Search Tool) (BLAST™; Altschul et al. (1990)) Национального центра биотехнологической информации США (NCBI) доступна из нескольких источников, включая Национальный центр биотехнологической информации (Bethesda, MD), и в Интернете, для использования совместно с несколькими программами анализа последовательности. Описание того, как определять идентичность последовательности с использованием данной программы, доступно в Интернете в разделе "help" BLAST™. Для сравнений последовательностей нуклеиновых кислот может применяться функция программы BLAST™ (Blastn) "Blast 2 sequences" с использованием матрицы BLOSUM62 с установленными параметрами по умолчанию. Последовательности нуклеиновых кислот с еще большим подобием с референсными последовательностями будут показывать возрастающий процент идентичности при оценке данным методом.
Однонуклеотидный полиморфизм: используемый в настоящем описании термин "однонуклеотидный полиморфизм" (SNP) может относиться к вариации последовательности ДНК, появляющейся, когда одиночный нуклеотид в геноме (или другой общей последовательности) отличается между представителями вида или в парных хромосомах индивидуального организма. В пределах популяции, SNP могут быть соотнесены с частотой минорного аллеля, которая является самой низкой частотой аллеля в локусе, которая наблюдается в конкретной популяции. Это просто наименьшая из двух аллельных частот для однонуклеотидных полиморфизмов. Различные популяции, как ожидается, будут демонстрировать, по меньшей мере, немного отличающиеся аллельные частоты. Конкретные популяции могут демонстрировать значительно отличающиеся аллельные частоты. В некоторых примерах, маркеры, связанные с bm1 фенотипом, являются SNP маркерами.
SNP могут находиться в пределах кодирующих последовательностей генов, некодирующих областей генов или в межгенных областях между генами. SNP в кодирующей последовательности могут, не обязательно, изменять аминокислотную последовательность синтезируемого белка вследствие вырожденности генетического кода. SNP, при котором обе формы приводят к синтезу одной и той же полипептидной последовательности, называют "синонимичным" (иногда называют молчащей мутацией). Если образуется другая полипептидная последовательность, их называют "несинонимичными". Несинонимичное изменение может быть либо миссенс или нонсенс, где миссенс-изменение приводит к другой аминокислоте, а нонсенс-изменение приводит к преждевременному стоп-кодону. SNP, которые не находятся в кодирующих белок областях, могут все же оказывать влияние на сплайсинг гена, связывание факторов транскрипции или последовательность некодирующей РНК. SNP обычно биаллельны и, таким образом, легко выявляются при анализе у растений и животных (Sachidanandam (2001) Nature 409:928-33).
Силос: используемый в настоящем описании термин "силос" относится к определенному типу сохраняемого фуража. Как правило, силос производят из растений (например, растений кукурузы) в процессе, названном силосованием. В ходе данного процесса, растения или части растений подвергаются анаэробному брожению, вызываемому местными микроорганизмами (например, одним или несколькими штаммами молочнокислых бактерий, например, Lactobacillus spec.), превращающими сахара в кислоты, и с поглощением кислорода, присутствующего в растительном материале, при этом устранение кислорода сохраняет фураж в сочетании с вырабатываемыми бактериями летучими жирными кислотами, такими как ацетат, пропионат, лактат и бутират. Силос широко используется для откорма молочных и мясных пород животных, таких как молочный скот и мясной скот.
Термин "производство силоса" описывает процесс получения силоса, подходящего для откорма мясных пород животных. Как правило, силос производят из растений, например, растений кукурузы, путем измельчения собранной растительной биомассы силосоуборочным комбайном.
Источник волокна: используемый в настоящем описании термин "источник волокна" относится к материалу, получаемому из растительного или микробного источника, который содержит пищевые волокна. Практические, но не ограничивающие, примеры источников волокон включают шелуху семян после производства сельскохозяйственных продуктов, таких как соевые бобы, или от зерновых культур, таких как рис, пшеница, кукуруза, ячмень; стебли таких зерновых культур (солому); растительное/на растительной основе сырье для получения мыла, кукурузную солому, которая обычно включает стебли, шелуху и листья от собранных растений кукурузы; фракции переработанных компонентов сельскохозяйственных продуктов, обогащенные волокном, например, кукурузный глютеновый корм; лиственный материал из любого растительного источника и высушенная барда, с сухими растворимыми веществами или без них. Таким образом, в конкретных примерах, источник волокна может включать, например, смеси следующего: люцерну, продукты ячменя (например, солому), свекловичный жом, соевую шелуху, просо, кукурузное волокно, соевое волокно, оболочки какао-бобов, сердцевину кукурузных початков, кукурузную шелуху, кукурузную солому, пшеничную солому, чешую пшеницы, рисовую солому, льняную шелуху, соевую муку, кукурузную муку, зародыши пшеницы, зародыши кукурузы, кустарники и травы. В целях ясности в настоящем описании, высушенная барда (с или без растворимых веществ), и барда (с или без растворимых веществ) содержат волокно, но не считаются "источниками волокна". Высушенная барда (с или без растворимых веществ) и барда (с или без растворимых веществ) считаются "побочными продуктами переработки кукурузы", как изложено ниже.
Побочный продукт переработки кукурузы: используемый в настоящем описании термин "побочный продукт переработки кукурузы" относится к продуктам, которые остаются после влажного размола или сухого размола кукурузы. Неограничивающие примеры побочных продуктов переработки кукурузы включают кукурузный глютен, барду, барду с растворимыми веществами, высушенную барду, высушенную барду с растворимыми веществами, концентрированные растворимые вещества из барды, отруби, модифицированную барду, модифицированную барду с растворимыми веществами.
Добавка: используемый в настоящем описании термин "добавка" относится к любому компоненту, включаемому в кормовую смесь для увеличения пищевой ценности кормовой смеси. Обычно используемые добавки включают белок (например, соевую муку или мочевину), минеральные вещества (например, костную муку), высококалорийные добавки (например, животный жир) и витамины.
Признак или фенотип: термины "признак" и "фенотип" используются в настоящем описании попеременно. В рамках настоящего описания наибольший интерес представляет признак bm1/сниженное содержание лигнина.
IV. Ген и вариации гена, ассоциированные с фенотипом bm1, и их применения
В настоящем описании предложены новые мутантные гены CAD2, которые вносят вклад в фенотип bm1 в кукурузе. Растения (например, кукуруза), которые включают мутантный ген CAD2, описанный в настоящей заявке, могут иметь клеточные стенки, уровни лигнина в которых ниже, чем уровни лигнина, обнаруживаемые в растениях дикого типа того же вида. В некоторых вариантах осуществления молекула нуклеиновой кислоты, включающая мутантный ген CAD2 согласно настоящему описанию, может быть введена в организм, например, для содействия в создании фенотипов с уменьшенным содержанием лигнина. В конкретных вариантах осуществления, организм может быть растением (например, кукурузой). Впрочем, молекула нуклеиновой кислоты, включающая мутантный ген CAD2 согласно настоящему описанию, может быть введена в организм, который не является растением, например, в дрожжи или прокариоты. В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может применяться для идентификации растений, включающих мутантный ген CAD2, или растений, которые могут иметь bm1 или другой фенотип с уменьшенным содержанием лигнина. Например, последовательность мутантного гена CAD2 согласно настоящему описанию может применяться для создания зондов, которые позволяют обнаружить присутствие мутантного гена CAD2 в растении или в образце, полученном из растения. В конкретных примерах предложен зонд на основе нуклеиновой кислоты, который гибридизуется с нуклеотидной последовательностью мутантного гена CAD2, но не с определенным геном CAD2 дикого типа.
В некоторых вариантах осуществления изобретение также включает такие молекулы нуклеиновых кислот, которые включают последовательность, которая по существу идентична мутантному гену CAD2 согласно настоящему описанию, где указанная последовательность может содержать, или не содержать, вставку динуклеотида AC и/или вставку транспозона, как описано в настоящей заявке. Например, в некоторых вариантах осуществления молекула нуклеиновой кислоты может включать последовательность, которая по меньшей мере на приблизительно 85% идентична мутантному гену CAD2 согласно настоящему описанию. Таким образом, молекула нуклеиновой кислоты может включать последовательность, которая по существу идентична мутантному гену CAD2 согласно настоящему описанию, а именно на 86%; 87%; 88%; 89%; 90%; 91%; 92%; 93%; 94%; 95%; 96%; 97%; 98%; 99% или 99,5% идентична мутантному гену CAD2 согласно настоящему описанию. Такие молекулы нуклеиновых кислот, которые по существу идентичны мутантному гену CAD2 согласно настоящему описанию, могут быть с легкостью идентифицированы и выделены, например, из любых полных или частичных геномов, с легкостью доступных специалистам в данной области для различных организмов.
Некоторые варианты осуществления также включают функциональные варианты мутантного гена CAD2 согласно настоящему описанию. Функциональные варианты мутантного гена CAD2 согласно настоящему описанию могут включать, например, мутантный ген CAD2 согласно настоящему описанию, включающий одну или более нуклеотидных замен, делеций или вставок, где функциональный вариант вносит вклад в bm1 или другой фенотип с уменьшенным содержанием лигнина, что можно измерить с помощью стандартных методов, известных средним специалистам в данной области. Например, функциональный вариант мутантного гена CAD2 согласно настоящему описанию может включать вставку динуклеотида AC и/или вставку транспозона, как описано в настоящей заявке. Способность конкретного варианта мутантного гена CAD2 согласно настоящему описанию уменьшать содержание лигнина или вносить вклад в фенотип bm1, может быть определено посредством стандартного введения мутации или фрагмента в растение, с последующим обычным наблюдением растения на наличие уменьшенного содержания лигнина или других характеристик фенотипа bm1. Функциональные варианты мутантного гена CAD2 согласно настоящему описанию могут быть созданы с помощью сайт-направленного мутагенеза, индуцированной мутации, или они могут существовать в виде аллельных вариантов (полиморфизмов, например, SNP).
Таким образом, в некоторых вариантах осуществления, функциональные варианты мутантного гена CAD2 согласно настоящему описанию могут включать дополнительные мутации гена CAD2, фрагменты меньшего размера, чем последовательность мутантного гена CAD2 согласно настоящему описанию, и/или химерные белки, которые включают мутантный ген CAD2 согласно настоящему описанию, где функциональные варианты сохраняют свойства мутантного гена CAD2. Такие мутации и фрагменты, как поэтому полагают, включены в объем изобретения. Средний специалист в данной области может с легкостью определить, сохраняют ли дополнительная мутация или фрагмент мутантного гена CAD2 согласно настоящему описанию свойства мутантного гена CAD2.
В некоторых вариантах осуществления, способность вводить в растение и обнаруживать в растении мутантный ген CAD2 согласно настоящему описанию может облегчать селекцию с использованием маркеров и отбор растений, содержащих мутантный ген CAD2, где указанные растения также могут с вероятностью иметь bm1 или другой фенотип с уменьшенным содержанием лигнина. В конкретных примерах, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение (например, с помощью генетической трансформации или традиционных методов селекции, таких как скрещивание), и включающие мутантный ген CAD2 растения могут быть затем отобраны при использовании зонда, который позволяет обнаружить присутствие мутантного гена CAD2 в растении. Растения, в которые был введен мутантный ген CAD2 согласно настоящему описанию, могут быть скрещены с растениями, которые могут также содержать, или не содержать, мутантный ген CAD2, и затем потомство может быть отобрано при использовании зонда, который позволяет обнаружить присутствие мутантного гена CAD2 согласно настоящему описанию в растении. Последующие кроссы могут быть проведены с целью получить растение с требуемым генотипом.
В случае, когда последовательность нуклеиновой кислоты (например, мутантный ген CAD2 согласно настоящему описанию) "вводят" в организм, такой как растение, метод или методика, используемые для введения молекулы нуклеиновой кислоты, включающей конкретную последовательность, не являются существенными для изобретения, и это может осуществляться с помощью любого метода или методики, известных специалистам в данной области. Например, молекула нуклеиновой кислоты может быть введена прямыми методами трансформации, такими как агробактериальная трансформация растительной ткани; бомбардировка микрочастицами; электропорация и т.д. В альтернативе, молекула нуклеиновой кислоты может быть введена путем скрещивания растения, содержащего конкретную нуклеотидную последовательность, с другим растением, при этом указанная нуклеотидная последовательность будет включена в геном потомства. Такие методы селекции известны квалифицированному специалисту. Методы селекции с использованием маркеров, раскрытые в настоящем описании, могут существенно облегчать введение мутантного гена CAD2 согласно настоящему описанию с помощью таких скрещиваний.
В вариантах осуществления, в которых мутантный ген CAD2 согласно настоящему описанию вводят в организм, может быть предпочтительно, чтобы мутантный ген CAD2 вводили так, чтобы мутантный ген CAD2 был функционально связан с одной или более регуляторными последовательностями, например, введение производят при использовании плазмиды, включающей мутантный ген CAD2 согласно настоящему описанию, функционально связанный с необходимыми регуляторными последовательностями. Регуляторные последовательности, применяемые в экспрессии гетерологичных последовательностей нуклеиновых кислот, известны в уроне техники и включают, в качестве неограничивающего примера: промоторы (например, конститутивные промоторы; тканеспецифические промоторы и промоторы, специфичные для стадии развития); терминационные последовательности; энхансерные последовательности; последовательности субклеточного таргетинга; стабилизирующие или лидерные последовательности и интроны.
Мутантный ген CAD2 согласно настоящему описанию может быть введен в организм с одним или более маркерными генами, функционально связанными с регуляторным элементом (например, промотором), которые позволяют выделять трансформированные клетки, содержащие маркер, либо посредством отрицательной селекции (то есть при ингибировании роста клеток, которые не содержат селективный маркерный ген), либо посредством положительной селекции (то есть с помощью скрининга продукта, кодируемого генетическим маркером). Множество селективных маркерных генов для трансформации известны в области трансформации и включают, например, гены, кодирующие ферменты, которые метаболически детоксифицируют селективный химический агент, который может быть антибиотиком или гербицидом, или гены, кодирующие измененную мишень, которая может быть нечувствительна к ингибитору. Несколько методов положительной селекции также известны в уровне техники. Примеры маркерных генов, подходящих для применения в клетках растений, могут включать, в качестве неограничивающего примера: ген неомицинфосфотрансферазы II (nptII) (Fraley et al. (1983) Proc. Natl. Acad. Sci. USA 80:4803); ген гигромицинфосфотрансферазы (Vanden Elzen et al. (1985) Plant Mol. Biol. 5); гентамицинацетилатрансферазу, стрептомицинфосфотрансферазу, аминогликозид-3’-аденилтрансферазу и детерминанту устойчивости к блеомицину (см., например, Hayford et al. (1988) Plant Physiol. 86:1216; Jones et al. (1987) Mol. Gen. Genet. 210:86); Svab et al. (1990) Plant Mol. Biol. 14:197; и Hille et al. (1986) Plant Mol. Biol. 7:171); селективные маркерные гены, которые придают устойчивость к гербицидам, таким как глифосат, глифосинат или бромоксинил (см., например, Comai et al. (1985) Nature 317:741-744; Gordon-Kamm et al. (1990) Plant Cell 2:603-618; и Stalker et al. (1988) Science 242:419-423); мышиную дигидрофолатредуктазу (Eichholtz et al. (1987) Somatic Cell Mol. Genet. 13:67); растительную 5-енолпирувилшикимат-3-фосфатсинтазу (Shah et al. (1986) Science 233:478); растительную ацетолактатсинтазу (Charest et al. (1990) Plant Cell Rep. 8:643).
Другой класс маркерных генов, подходящих для трансформации растений, применяет скрининг предполагаемо трансформированных клеток растения, а не прямую генетическую селекцию трансформированных клеток на устойчивость к токсичному веществу, такому как антибиотик. Такие гены особенно полезны при количественном определении или визуализации пространственного профиля экспрессии гена в определенных тканях, и часто упоминаются как "репортерные гены", поскольку они могут быть слиты с геном или регуляторной последовательностью гена для исследования экспрессии генов. Обычно используемые для скрининга трансформированных клеток гены включают β-глюкуронидазу (GUS), β-галактозидазу, люциферазу и хлорамфениколацетилтрансферазу. См., например, Jefferson (1987) Plant Mol. Biol. Rep. 5:387; Teeri et al. (1989) EMBO J. 8:343; Koncz et al. (1987) Proc. Natl. Acad. Sci U.S.A. 84:131; и DeBlock et al. (1984) EMBO J. 3:1681.
Недавно стали доступными методы in vivo визуализации активности GUS, которые не требуют разрушения ткани растения (Molecular Probes publication 2908, Imagene Green.TM., p. 1-4, 1993; и Naleway et al. (1991) J. Cell Biol. 115:151a). Кроме того, гены, кодирующие флуоресцентные белки (например, GFP, EGFP, EBFP, ECFP и YFP), использовались в качестве маркеров экспрессии генов в прокариотических и эукариотических клетках. См. Chalfie et al. (1994) Science 263:802. Флуоресцентные белки и мутации флуоресцентных белков могут использоваться в качестве маркеров, пригодных для скрининга.
В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию и/или фрагменты или сегменты мутантного гена CAD2 согласно настоящему описанию могут применяться для идентификации гомологичных последовательностей мутантного гена CAD2 из организмов помимо кукурузы (например, с помощью сравнения последовательностей). Последовательности из организмов помимо кукурузы, которые гомологичны мутантному гену CAD2 согласно настоящему описанию, могут быть идентифицированы и выделены в соответствии с известными методами, например, на основе их гомологии последовательности с мутантным геном CAD2 согласно настоящему описанию.
Таким образом, в некоторых вариантах осуществления, вся или часть кодирующей последовательности из мутантного гена CAD2 согласно настоящему описанию может применяться в качестве зонда, который специфично гибридизуется с другими последовательностями, присутствующими в популяции клонированных фрагментов геномной ДНК (то есть в геномной библиотеке) из организма, в соответствии со стандартными методами. Таким образом, в некоторых вариантах осуществления, изобретение включает такие нуклеотидные последовательности, которые специфично гибридизуются с мутантным геном CAD2 согласно настоящему описанию.
В других вариантах осуществления, последовательности из организмов помимо кукурузы, которые гомологичны мутантному гену CAD2 согласно настоящему описанию, могут быть идентифицированы и выделены с помощью сравнения последовательностей. Например, может быть проведен поиск по полному или частичному отсеквенированному геному организма согласно стандартным методам с последовательностью мутантного гена CAD2 согласно настоящему описанию с целью идентификации генов в геноме организма, которые обладают высокой степенью идентичности последовательности с мутантным геном CAD2 и поэтому могут являться гомологами мутантного гена CAD2.
Например, весь или часть мутантного гена CAD2 согласно настоящему описанию может применяться в качестве "референсной последовательности". Как правило, последовательности нуклеиновых кислот (например, клонированные или фрагменты геномной ДНК из геномной библиотеки), которые сравнивают с референсной последовательностью, включают "окно сравнения", которое представляет собой определенный непрерывный сегмент последовательности нуклеиновой кислоты. Окно сравнения может включать дополнения или делеции (то есть пропуски) по сравнению с референсной последовательностью (которая не включает дополнений или делеций) при оптимальном выравнивании двух указанных последовательностей. Окно сравнения обычно имеет длину по меньшей мере 20 последовательных нуклеотидов, но может иметь длину 30, 40, 50, 100 или 200 нуклеотидов, или больше. Для предотвращения высокого подобия референсной последовательности из-за включения делеций в окне сравнения полинуклеотидной последовательности, может быть введен "штраф за пропуски", вычитаемый из числа совпадений нуклеотидов.
Методы выравнивания последовательностей для сравнения хорошо известны в уровне техники. Определение процента идентичности последовательностей между любыми двумя последовательностями может быть выполнено при использовании доступных математических алгоритмов. Неограничивающими примерами таких математических алгоритмов является алгоритм Майерса и Миллера (Myers and Miller (1988), CABIOS 4:11-7); алгоритм локального выравнивания Смита (Smith et al. (1981) Adv. Appl. Math. 2:482); алгоритм глобального выравнивания Нидлмэна и Вунша (Needleman and Wunsch (1970), J. Mol. Biol. 48:443-53); метод поиска локального выравнивания Пирсона и Липмана (Pearson and Lipman (1988), Proc. Natl. Acad. Sci. USA 85:2444-8); алгоритм Карлина и Альтшуля (Karlin and Altschul (1990), Proc. Natl. Acad. Sci. USA 87:2264, а также Karlin and Altschul (1993) Proc. Natl. Acad. Sci. USA 90:5873-7).
Средний специалист в данной области может выполнить указанные математические алгоритмы на компьютере для сравнения последовательностей с целью определения идентичности последовательностей или для поиска в базе данных, включающей множество последовательностей (например, база данных геномов организмов), согласно общей идентичности последовательностей с референсной последовательностью. Такие процедуры включают, без ограничения, CLUSTAL в программе PC/Gene (Intelligenetics, Mountain View, CA); и программу ALIGN, а также GAP, BESTFIT, BLAST, FASTA и TFASTA в пакете программ GCG Wisconsin Genetics Software Package, v. 10 (Accelrys Inc., San Diego, CA). Выравнивания последовательностей с использованием указанных программ могут быть выполнены при использовании их параметров по умолчанию. В альтернативе, может требоваться изменить параметры по умолчанию в некоторых поисках (например, изменить значения штрафа за пропуски). Выбор конкретного компьютерного исполнения математических алгоритмов для вычисления идентичности последовательности и выбора значений параметров для использования в выбранном алгоритме производится по усмотрению специалиста в данной области.
В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее дополнительный требуемый ген (например, мутантный ген или минорный аллель) или фенотип путем скрещивания. В альтернативе, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее дополнительный требуемый ген или фенотип, например, с помощью генетической трансформации. В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее мутацию в одном или более дополнительных генах, участвующих в биосинтезе или метаболизме лигнина. В качестве неограничивающего примера, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее мутацию, например, в другом гене CAD; в COMT; 4CL; F5H; ZmCAD1 EgCAD1-типа; SAD; гене хоризматмутазы; PAL; HCT; OMT; гене цитохром P450; SAMS3; CCR; DFR; гене хальконсинтазы; гене лакказы; гене пероксидазы; гене ALDH (например, одном из шести генов ALDH кукурузы, описанных в Skibbe et al. (2002) Plant Mol. Biol. 48:751-64); AGO; гене фактора транскрипции MYB (например, ZmMYB38; и APL кукурузы); гене фактора транскрипции LIM; гене фактора bZIP кукурузы; гене MADS-бокса (например, ZmZAG5); гене MP; гене ABC-переносчика; гене β-глюкозидазы; гене S-глутатионтрансферазы (например, ZmGST17); нодулин MtN21-подобном гене; ортологичном гене PINOID; гистидинкиназе (например, ZmHK1, ZmHK2, и ZmHK3); и/или ортологичном гене COV1. В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее один или более требуемых признаков, которые не участвуют в биосинтезе или метаболизме лигнина, с получением растения как с bm1 или другим фенотипом с пониженным содержанием лигнина, так и с одним или более требуемыми признаками, которые не участвуют в биосинтезе или метаболизме лигнина.
Предполагается, что растения указанного и других вариантов осуществления, которые содержат множество мутантных генов в путях биосинтеза или метаболизма лигнина, будут демонстрировать новые полезные фенотипы, например, дополнительные фенотипы bm и/или другие лигниновые фенотипы. См., например, Marita et al. (2003), выше. Например, было отмечено, что объединение признака bm1 с признаком bm3 приводит к дополнительному увеличению перевариваемости силоса и весьма существенному повышению выхода сбраживаемых сахаров при гидролизе биомассы без предварительной обработки.
В некоторых вариантах осуществления применяются средства для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы и/или средства для идентификации растений, несущих мутантный ген CAD2 кукурузы. В некоторых примерах, средство для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы, может быть маркером, который расположен в мутантном гене CAD2 кукурузы согласно настоящему описанию. В некоторых примерах, средство для идентификации растений, несущих мутантный ген CAD2 кукурузы, может быть зондом, который специфично гибридизуется с маркером, который расположен в мутантном гене CAD2 кукурузы согласно настоящему описанию. Мутантные гены CAD2 согласно настоящему описанию (применительно к средству для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы, и к средству для идентификации растений, несущих мутантный ген CAD2 кукурузы) являются такими мутантными генами CAD2, которые вносят вклад в фенотип bm1 либо в инбредной линии маиса 515Dbm1, либо в линии DASbm1. Указанные мутантные гены CAD2 характеризуются либо мутацией со сдвигом рамки считывания в третьем экзоне гена CAD2, которая приводит к усеченному белку CAD2, либо вставкой транспозона длиной 3444 пары оснований в первом интроне гена CAD2, которая приводит к усеченному белку CAD2. Таким образом, в некоторых вариантах осуществления, мутантный ген CAD2 может включать в себя первый экзон геномной последовательности гена ZmCAD2 и/или второй экзон геномной последовательности гена ZmCAD2, но может не включать всю или часть третьего экзона геномной последовательности гена ZmCAD2.
Мутантные гены CAD2, раскрытые в настоящей заявке, отличаются от ранее описанных мутаций CAD2, которые могут быть вовлечены в фенотипы bmr. Например, мутантный ген CAD2 согласно настоящему описанию может иметь одну или более следующих особенностей: вставку динуклеотида в экзоне гена ZmCAD2 (например, экзоне 3); мутацию, приводящую к сдвигу рамки считывания; вставку транспозона в интроне гена ZmCAD2, которая приводит к усеченному белку; мутацию, приводящую к усеченному ферменту ZmCAD2; мутацию, приводящую к инактивации (например, при удалении) NADPH-связывающего и/или C-концевого каталитического домена(ов) ZmCAD2; мутацию, которая вносит вклад в фенотип bm1 в инбредной линии кукурузы 515Dbm1; и мутацию, которая вносит вклад в фенотип bm1 в инбредной линии кукурузы DASbm1. Напротив, ранее описанные природные мутантные гены CAD2 характеризуются наличием вставки транспозона в первом интроне гена (заявка на патент США 2010/0203196 A1); сниженной экспрессией полноразмерного белка CAD (Halpin et al. (1998), выше); точечной мутацией, приводящей к усечению фермента Sorghum bicolor CAD2 (Saballos et al. (2009), выше; Sattler et al. (2009)), выше; точечной мутацией в кофактор-связывающем сайте S. bicolor CAD2 (Id).; нарушением вторичной структуры вне активного сайта в S. bicolor CAD2 (Id).; и 2 п.н. вставкой аденозинов в ген Pinus taeda L. CAD, которая приводит к усеченному ферменту (патент США 6,921,643).
V. Молекулярные маркеры, сцепленные с геном, и вариации гена, связанные с фенотипом bm1, и их применения
Предложены молекулярные маркеры, которые сцеплены (например, сильно сцеплены) с мутантным геном CAD2 согласно настоящему описанию. Молекулярный маркер, связанный с мутантным геном CAD2 согласно настоящему описанию, может быть частично описан своим положением в конкретной области на хромосоме 5L кукурузы. Молекулярные маркеры, которые связаны с мутантным геном CAD2 согласно настоящему описанию, могут включать в себя SNP маркеры, которые расположены в мутантном гене CAD2 или присутствуют рядом с ним. Например, в некоторых вариантах осуществления, G/A SNP, расположенный в нуклеотидном положении 5410 в гене CAD2 линии bm1 кукурузы, 515Dbm1, и в нуклеотидном положении 8903 в линии bm1 кукурузы, DASbm1 (или эквивалентный ему маркер), может быть молекулярным маркером, который связан с мутантным геном CAD2 согласно настоящему описанию. В некоторых вариантах осуществления, G/A SNP, расположенный в нуклеотидном положении 5410 в гене CAD2 линии bm1 кукурузы, 515Dbm1, может быть молекулярным маркером, который сцеплен с мутантным геном CAD2 согласно настоящему описанию.
Дополнительные маркеры могут быть идентифицированы, например, при определении частоты рекомбинации между дополнительным маркером и мутацией CAD2 согласно настоящему описанию, или молекулярным маркером, который сцеплен с мутантным геном CAD2 согласно настоящему описанию (например, G/A SNP, расположенным в нуклеотидном положении 5410 в линии bm1 кукурузы, 515Dbm1). В таких определениях может применяться усовершенствованный метод ортогональных контрастов, основанный на методе Мазера (Mather (1931), The Measurement of Linkage in Heredity, Methuen & Co., London), с последующей оценкой по критерию максимальной вероятности для определения частоты рекомбинации (Allard (1956) Hilgardia 24:235-78). Если значение частоты рекомбинации меньше или равно 0,10 (то есть, 10%) в организме (например, кукурузе), то дополнительный маркер, как предполагают, сцеплен с мутантным геном CAD2, и эквивалентен конкретному референсному маркеру в целях применения в способах, раскрытых в настоящей заявке.
Способы применения молекулярных маркеров на основе нуклеиновой кислоты, которые сцеплены с, или присутствует в мутантном гене CAD2 согласно настоящему описанию, для идентификации растения с bm1 или другим фенотипом с пониженным содержанием лигнина, могут приводить к экономической выгоде для селекционеров растений, поскольку такие способы могут устранить необходимость в скрещивании растений, включающих мутантный ген CAD2, с другими линиями растений, и затем определять фенотип потомства кросса.
Средством для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы, является маркер, который сцеплен с мутантным геном CAD2 согласно настоящему описанию. Таким образом, средство для получения генетически модифицированного растения, включающего мутантный ген CAD2 кукурузы, включает последовательности нуклеиновых кислот из растений кукурузы, при этом обнаружение любых таких последовательностей нуклеиновой кислоты обеспечивает, по меньшей мере, сильный признак того, что растение, включающее последовательность нуклеиновой кислоты, включает мутантный ген CAD2 согласно настоящему описанию.
Средством для идентификации растений, несущих мутантный ген CAD2 кукурузы, является зонд, который специфично гибридизуется с маркером, который связан с, или присутствует в мутантном гене CAD2 кукурузы согласно настоящему описанию. Специфичная гибридизация нуклеиновых кислот является детектируемым сигналом, при этом зонд на основе нуклеиновой кислоты, который специфично гибридизуется с маркером, который сцеплен с, или присутствует в мутантном гене CAD2 кукурузы согласно настоящему описанию, предоставляет, таким образом, детектируемый сигнал при добавлении к образцу, полученному из растения, несущего мутантный ген CAD2 согласно настоящему описанию.
В некоторых вариантах осуществления, сцепленные маркеры, фланкирующие мутантный ген CAD2 согласно настоящему описанию в геноме организма, могут применяться для переноса сегмента(ов) донорной родительской ДНК, который точно содержит мутантный ген CAD2. В некоторых вариантах осуществления, способ применения сцепленных маркеров, фланкирующих мутантный ген CAD2 согласно настоящему описанию, для переноса сегмента(ов) донорной родительской ДНК, который точно содержит мутантный ген CAD2, может включать анализ геномной ДНК двух исходных растений с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2; половое скрещивание двух генотипов родительских растений с получением популяции потомства и анализ данного потомства на присутствие маркеров, связанных с мутантным геном CAD2; обратное скрещивание потомства, содержащего маркеры, сцепленные с мутантным геном CAD2, с донорным генотипом, с получением первой популяции обратного скрещивания, и затем продолжение программы обратного скрещивания до получения конечного потомства, которое включает любой требуемый признак(и), проявляемый родительским генотипом и мутантным геном CAD2. В конкретных вариантах осуществления, индивидуальный потомок, получаемый в каждом кроссе и этапе обратного скрещивания, отбирают с помощью анализа сцепленных маркеров в каждом поколении. В некоторых вариантах осуществления, анализ геномной ДНК двух указанных исходных растений с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2, показывает, что одно из исходных растений содержит меньшее количество сцепленных маркеров, с которыми зонды специфично гибридизуются, или не содержит ни одного из сцепленных маркеров, с которыми специфично гибридизуются зонды.
В некоторых вариантах осуществления, маркеры, которые сцеплены с, или присутствует в мутантном гене CAD2 согласно настоящему описанию, или последовательность мутантного гена CAD2 непосредственно, могут применяться для введения мутантного гена CAD2 согласно настоящему описанию в растение кукурузы с помощью генетической трансформации. В конкретных вариантах осуществления, маркеры, без ограничения, включают в себя G/A SNP, расположенный в нуклеотидном положении 5410 линии bm1 кукурузы, 515Dbm1, и в нуклеотидном положении 8903 линии bm1 кукурузы, DASbm1, или эквивалентный им маркер. В некоторых вариантах осуществления, способ введения мутантного гена CAD2 согласно настоящему описанию в растение кукурузы с помощью генетической рекомбинации может включать анализ геномной ДНК растения (например, растения кукурузы) с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2 или с мутантным геном CAD2 непосредственно, для идентификации мутантного гена CAD2 в растении; выделение сегмента геномной ДНК растения, включающего мутантный ген CAD2, например, посредством экстракции геномной ДНК и расщепления геномной ДНК одним или более ферментами, эндонуклеазами рестрикции; необязательно, амплификацию выделенного сегмента ДНК; введение выделенного сегмента ДНК в клетку или ткань хозяйского растения кукурузы; и анализ ДНК хозяйского растения кукурузы с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2, или с мутантным геном CAD2 непосредственно, для идентификации мутантного гена CAD2 в хозяйском растении кукурузы. В конкретных вариантах осуществления, выделенный сегмент ДНК может быть введен в хозяйское растение кукурузы так, что он стабильно интегрируется в геном хозяйского растения кукурузы.
В некоторых вариантах осуществления, маркеры, которые сцеплены с, или присутствуют в мутантном гене CAD2 согласно настоящему описанию, или последовательность мутантного гена CAD2 непосредственно, могут применяться для введения мутантного гена CAD2 согласно настоящему описанию в другие организмы, например, растения. В конкретных вариантах осуществления, маркеры включают в себя, без ограничения, G/A SNP, расположенный в нуклеотидном положении 5410 линии bm1 кукурузы, 515Dbm1, и в нуклеотидном положении 8903 линии bm1 кукурузы, DASbm1, или эквивалентный им маркер. В некоторых вариантах осуществления, способ введения мутантного гена CAD2 согласно настоящему описанию в организм, отличный от кукурузы (например, сою, люцерну, пшеницу, рапс, рис и сорго), может включать анализ геномной ДНК растения, отличного от растения кукурузы, с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2 согласно настоящему описанию, или с мутантным геном CAD2 непосредственно, для идентификации мутантного гена CAD2 в растении; выделение сегмента геномной ДНК растения, включающего мутантный ген CAD2, например, путем экстракции геномной ДНК и расщепления геномной ДНК одним или несколькими ферментами, эндонуклеазами рестрикции; необязательно, амплификацию выделенного сегмента ДНК; введение выделенного сегмента ДНК в организм, отличный от кукурузы; и анализ ДНК организма, отличного от кукурузы, с применением зондов, которые способны к специфичной гибридизации с маркерами, сцепленными с мутантным геном CAD2 согласно настоящему описанию, или с мутантным геном CAD2 непосредственно, для идентификации мутантного гена CAD2 в организме. В конкретных вариантах осуществления, выделенный сегмент ДНК может быть введен в организм так, что он стабильно интегрируется в геном организма.
В некоторых вариантах осуществления, маркеры, которые сцеплены с, или присутствуют в мутантном гене CAD2 согласно настоящему описанию, или последовательность мутантного гена CAD2 непосредственно, могут применяться для идентификации растения с bm1 или другим фенотипом с уменьшенным содержанием лигнина. В конкретных вариантах осуществления, растение является растением кукурузы. В некоторых вариантах осуществления, молекулы нуклеиновых кислот (например, геномная ДНК или мРНК) могут быть выделены из растения. Затем выделенные молекулы нуклеиновых кислот можно подвергнуть контакту с одним или более зондами, которые способны к специфичной гибридизации с маркерам, сцепленным с мутантным геном CAD2 согласно настоящему описанию, или с мутантным геном CAD2 непосредственно. Специфичная гибридизация одного или большего количества зондов с выделенными молекулами нуклеиновой кислоты указывает на присутствие bm1 или другого фенотипа с уменьшенным содержанием лигнина в растении.
Подбор праймеров и скрининг сцепления.
Олигонуклеотидные зонды (например, праймеры) могут быть подобраны для специфичного обнаружения маркеров, которые физически расположены в, вблизи или между CAD2, которые сцеплены с мутацией bm1. Как правило, может быть создан олигонуклеотидный зонд, который специфично гибридизуется только с одним аллелем маркера. В некоторых вариантах осуществления, для обнаружения маркера bm1 создают два олигонуклеотидных зонда, которые специфично гибридизуются с аллелем bm1, с которым специфично не гибридизуется другой зонд, а другой зонд специфично гибридизуется с аллелем CAD2 дикого типа (или другим аллелем bm1), с которым специфично не гибридизуется другой зонд. Как будет ясно специалистам в данной области, длина или состав олигонуклеотидных зондов для конкретного маркера могут быть различными согласно установленным принципам, при этом зонд должен сохранять специфичность к одному аллелю маркера.
В некоторых вариантах осуществления, олигонуклеотидные зонды могут быть праймерами. В определенных вариантах осуществления, могут быть подобраны праймеры для обнаружения маркеров в анализе генотипирования KASPar™. В конкретных вариантах осуществления, могут быть подобраны праймеры для обнаружения маркеров, сцепленных с фенотипом bm1 в кукурузе, при помощи анализа генотипирования KASPar™. В этом и других вариантах осуществления, система обнаружения может обеспечивать высокую производительность и удобный формат для генотипирования индивидуальных организмов в картируемой популяции, что может значительно облегчать идентификацию организмов, несущих конкретный ген или признак, а также может существенно облегчать проведение или выполнение программы селекции с использованием маркеров.
В определенных вариантах осуществления, олигонуклеотидными зондами могут быть праймеры, созданные для обнаружения маркеров в анализе генотипирования TaqMan®. В данном методе используются специфичные праймеры для амплификации области ДНК, содержащей маркер, близко сцепленный с мутацией bm1, а также флуоресцентно меченые зонды, специфичные к маркеру. Зонд, который специфично гибридизуется с аллелем bm1, может быть помечен флуоресцентным красителем, таким как FAM, тогда как зонд, который специфично гибридизуется с аллелем CAD2 дикого типа (или другим аллелем bm1) может быть помечен другим флуоресцентным красителем, таким как VIC. Данные анализируют на присутствие или отсутствие сигнала флуоресцентного красителя. Система обнаружения может обеспечивать высокую производительность и удобный формат, например мультиплексирование для генотипирования индивидуальных организмов в картируемой популяции, что может существенно облегчать идентификацию организмов, несущих конкретный ген или признак, а также может существенно облегчать проведение или выполнение программы селекции с использованием маркеров.
Таким образом, также в настоящей заявке описан геноспецифический TaqMan® ПЦР-анализ по конечной точке, обычно применяемый для анализа зиготности кукурузы bm1 или предполагаемой bm1 кукурузы. В конкретных вариантах осуществления, геноспецифический TaqMan® ПЦР-анализ по конечной точке может применяться для анализа зиготности кукурузы по мутации bm1.
Праймеры и зонды для применения в геноспецифическом TaqMan® ПЦР-анализе по конечной точке могут быть созданы на основе известной мутации в целевом гене. Например, праймеры и зонды для bm1-специфичного анализа могут быть созданы на основе вставки длиной 3444 п.н. в первом интроне гена CAD2. В биплексных реакциях, в которых олигонуклеотиды, специфичные к мутации (например, bm1), и непрерванный ген дикого типа (например, CAD2) используются в одном и том же анализе, специфичные олигонуклеотиды обеспечивают селективную амплификацию последовательности из мутированного гена и/или из гена дикого типа, который присутствует в образце геномной ДНК.
В некоторых вариантах осуществления, в bm1-специфичном анализе амплифицируют фрагмент, который является уникальным в отношении нуклеотидной последовательности длиной 3444 п.н., которая была встроена в геномный ген CAD2 дикого типа. В некоторых вариантах осуществления, в анализе, специфичном к гену CAD2 дикого типа, амплифицируют фрагмент гена CAD2, который включает сайт соединения, по которому была встроена нуклеотидная последовательность длиной 3444 п.н. в ген CAD2 дикого типа. В определенных вариантах осуществления, мишень-специфичный зонд гибридизуется в условиях высокой строгости с целевой последовательности в образце геномной ДНК между двумя ПЦР-праймерами.
Мишень-специфичные олигонуклеотиды могут быть помечены, например, флуоресцентными красителями (например, FAM, VIC и MGBNFQ), что может позволить выполнять быстрое количественное определение мишень-специфичного флуоресцентного сигнала. Продукты ПЦР могут быть измерены после заданного числа циклов, например, когда реакция находится в ранней экспоненциальной фазе. Образцы отрицательного контроля могут включать геномную ДНК из любого сорта кукурузы, например, без мутации bm1. Образцы положительного контроля могут включать геномную ДНК из сорта кукурузы с мутацией BMR, такой как мутация bm1 со вставкой в гене CAD2. Контрольные гемизиготные образцы могут включать любую геномную ДНК из сорта кукурузы, в отношении которого изначально известно, что он является гемизиготным по мутации bm1; или гемизиготный образец может включать равные пропорции ДНК отрицательного контроля и ДНК из сорта кукурузы, в отношении которого изначально известно, что он является гомозиготным по мутации bm1.
ДНК может быть выделена (например, экстрагирована и очищена) из ткани растения кукурузы методами, известными специалистам в данной области. Коммерческие наборы для выделения ДНК поставляются, например, компанией Qiagen, Inc. В некоторых вариантах осуществления, диски листьев конкретного растения выбивают и переносят в пробирки для сбора. Выбойку можно очищать после взятия каждого образца 70%-ым спиртом, промывать водой и сушить. Буферы для экстракции ДНК могут быть приготовлены согласно рекомендациям производителя. Затем ДНК может быть выделена с использованием набора согласно инструкциям производителя. Наконец, концентрация выделенной ДНК может быть определена при использовании, например, набора Quant-iT™ PicoGreen® Quantfication Kit (Invitrogen, Carlsbad, CA) и спектрофотометра, или любой другой подходящей методики.
После того как праймеры, зонды и образец(ы) геномной ДНК были получены или сделаны доступными иным способом, можно провести реакцию ПЦР для идентификации целевых последовательностей нуклеиновых кислот (например, последовательностей, специфичных мутации BMR) в образце(ах) геномной ДНК. В конкретных вариантах осуществления, приготавливают индивидуальные реакционные ПЦР-смеси, которые содержат все компоненты реакции, кроме образца(ов) геномной ДНК. Для биплексной реакции, включающей праймеры и геноспецифичные зонды к мутанту bm1 и CAD2 кукурузы дикого типа, реакционная смесь может включать фермент, реакционный буфер, прямой и обратный праймеры к мутации bm1, прямой и обратный праймеры к гену CAD2 дикого типа, геноспецифичный зонд к bm1 мутации, геноспецифичный зонд к гену CAD2 и воду. В некоторых системах ПЦР-анализа (например, в TaqMan® ПЦР-анализе), фермент и буфер могут присутствовать в одном компоненте набора (например, в мастер-миксе для генотипирования TaqMan®; Applied Biosystems, Foster City, CA, кат. # 4371355).
После того, как реакционная смесь была иным способом приготовлена, может быть добавлен образец(ы) геномной ДНК и начата реакция. В образце не требуется нормализовать количества геномной ДНК. Впрочем, квалифицированный специалист может достигнуть наилучших результатов при использовании образцов геномной ДНК с относительно равными концентрациями.
В некоторых вариантах осуществления, ПЦР-анализ (например, ПЦР-анализ TaqMan®) может быть подготовлен с подходящими контролями. Например, реакция в многолуночном планшете может быть выполнена с контрольными лунками, включающими: (1) отрицательный контроль(и) с реактивами, но без образца ДНК; (2) гомозиготный положительный контроль(и), включающий геномную ДНК кукурузы bm1; и (3) гемизиготный положительный контроль(и), как описано выше. Затем ДНК амплифицируют с помощью ПЦР при подходящих условиях циклов. Например, в некоторых вариантах осуществления, при использовании системы GenAmp® PCR System 9700, может присутствовать один цикл денатурации при 95°C в течение 15 минут, с 30 последующими циклами денатурации (92°C в течение 15 секунд) и отжига/достройки (60°C в течение 60 секунд). Специалистам в данной области известно, что условия циклов ПЦР могут быть различными и приниматься по усмотрению специалиста-практика, и на основе полученных сопоставимых результатов.
ПЦР-анализ (например, TaqMan® ПЦР-анализ по конечной точке) может использоваться для анализа генотипа и/или зиготности BMR кукурузы или предполагаемой BMR кукурузы. В некоторых вариантах осуществления, геноспецифичный олигонуклеотидный зонд может быть помечен репортером (например, флуоресцентной молекулой). Для анализа с использованием флуориметрического детектирования, продукты реакции ПЦР могут быть проанализированы в спектрофлуориметре (например, Tecan GENios™; Männedorf, Switzerland) при использовании параметров настройки длины волны возбуждения и эмиссии, подходящих для обнаружения зонда(ов). Например, флуоресцентный краситель FAM может быть измерен при длине волны возбуждения 485 нм и длине волны эмиссии 535 нм. В альтернативе, флуоресцентный краситель VIC может быть измерен при длине волны возбуждения 525 нм и длине волны эмиссии 560 нм.
После завершения реакции ПЦР и детектирования зонда, могут быть созданы таблица и график распределения с использованием, например, любого подходящего графического компьютерного программного обеспечения. Результаты, полученные с ДНК дикого типа, гемизиготной и гомозиготной ДНК подобного генотипического фона могут служить в качестве отрицательного и положительного контролей. В расщепляющейся популяции могут быть получены три кластера точек данных, что позволяет визуально определить, к какому из расщепляющихся кластеров относится результат образца. В альтернативе, программное обеспечение для анализа данных может использоваться в целях вычисления вероятности того, что результат образца относится к каждому расщепляющемуся кластеру, при этом наиболее вероятный кластер служит назначением образца. После выполнения визуального определения, граница каждого кластера может быть условной, например, когда четко видимы три кластера точек данных.
Необработанные данные интенсивности флуоресценции могут также быть проанализированы непосредственно в планшет-ридере с использованием подходящего пакета программ для анализа, такого как KLIMS™ (KBioscience laboratory information management system). Можно построить график, на одной оси которого откладывают относительные единицы флуоресценции (RFU) сигнала флуоресценции, генерируемого зондом, специфичным к мутантному аллелю, а на другой оси - RFU сигнала флуоресценции, генерируемого зондом, специфичным к аллелю дикого типа. Определения зиготности затем могут быть выполнены на основе разделения кластеров при графическом представлении данных.
Образцы, которые не содержат мутантной геномной ДНК (например, мутации BMR), могут давать только показания флуоресценции ПЦР-продукта дикого типа. Образцы, содержащие гемизиготную или гомозиготную мутантную геномную ДНК, могут давать RFU показания для мутант-специфичного зонда, которые превышают показания для отрицательного фонового контроля. Если образец не дает никаких адекватных результатов, геномная ДНК в образце, возможно, не обладает достаточным качеством и/или не содержится в достаточном количестве, и необходимо выполнить получение новой ДНК и/или новую реакцию ПЦР. Предпочтительно, образец отрицательного контроля, не содержащий образца ДНК, показывает очень низкое детектирование геноспецифичного зонда(ов). Также предпочтительно, что известные гомозиготные контроли показывают только высокое детектирование мутантной ДНК или ДНК дикого типа в контроле, и что известные гемизиготные контроли показывают высокое детектирование ДНК дикого типа и мутантной ДНК.
Метод ПЦР и определение генотипа и/или зиготности могут быть выполнены в "тестовом режиме" со всеми подходящими контролями перед скринингом образцов. Дополнительная оптимизация методов может потребоваться для компонентов, которые могут различаться при каждом применении (например, метод получения геномной ДНК, Taq ДНК-полимераза, олигонуклеотиды, лабораторное оборудование и т.д.). Условия ПЦР и тепловых циклов могут быть установлены с обеспечением амплификации как мутантной последовательности, так и последовательности дикого типа в известной геномной ДНК-матрице с приемлемыми уровнями детектирования зонда (например, приемлемыми значениями RFU для флуоресцентно меченых олигонуклеотидных зондов).
VI. Организмы, имеющие сниженную активность CAD2, и их применения
A. Организмы, имеющие сниженную активность CAD2
В некоторых вариантах осуществления настоящего изобретения также предложен организм, включающий молекулу нуклеиновой кислоты, включающую мутантный ген CAD2 согласно настоящему описанию, последовательность нуклеиновой кислоты, которая способна к специфичной гибридизации с мутантным геном CAD2 согласно настоящему описанию, или функциональный вариант мутантного гена CAD2 согласно настоящему описанию. Подходящий организм может быть любым подходящим растением, дрожжами или бактерией. В качестве неограничивающего примера, растение, включающее вышеуказанные последовательности, может быть растением сельскохозяйственного значения, например, без ограничения: кукурузой; соей; люцерной; пшеницей; рапсом; рисом; сорго; свеклой; различными овощами, включая огурец, помидор, перец и т.д.; различными деревьями, включая яблоню, грушу, персик, вишню, красное дерево, сосну, дуб и т.д.; и различными декоративными растениями. В конкретных вариантах осуществления, организм может быть растением, которое применяется для производства силоса.
Клетки растения, включающие мутантный ген CAD2 согласно настоящему описанию, последовательность нуклеиновой кислоты, которая способна к специфичной гибридизации с мутантным геном CAD2 согласно настоящему описанию, или функциональный вариант мутантного гена CAD2 согласно настоящему описанию, можно культивировать и поддерживать в качестве клеток в культуре ткани растения, или же определенные растительные гормоны, известные в уровне техники, могут быть добавлены в культуральную среду, вызывая таким образом дифференцировку клеток в культуре тканей растения и формирование растения нового сорта, которое может демонстрировать bm1 или другой фенотип с уменьшенным содержанием лигнина. Такие способы культивирования растений, применяемые в данном и других вариантах осуществления, являются стандартными и известны из уровня техники.
В некоторых вариантах осуществления изобретения предложен вирус (например, бактериофаг или вирус растения), включающий мутантный ген CAD2 согласно настоящему описанию, последовательность нуклеиновой кислоты, которая способна к специфичной гибридизации с мутантным геном CAD2 согласно настоящему описанию, или функциональный вариант мутантного гена CAD2 согласно настоящему описанию.
B. Силос, получаемый из растений, имеющих сниженную активность CAD2
В настоящей заявке раскрыты способы увеличения количества мяса у животного, откармливаемого силосом, в которых применяется силос, полученный из сортов растений, демонстрирующих сниженное содержание лигнина, повышения ежедневного прироста веса и эффективности корма по сравнению с обычным кукурузным силосом в конечном рационе. Такой силос может эффективно заменить зерно кукурузы в конечном рационе мясных пород домашних быков. В некоторых вариантах осуществления, способ включает получение силоса, произведенного из сорта растения, включающего мутантный ген CAD2 согласно настоящему описанию, откорм животного силосом, произведенным из сорта растения, включающего мутантный ген CAD2 согласно настоящему описанию, и производство мяса или мясных продуктов из указанного животного. В данном и других вариантах осуществления, откармливаемое силосом животное может быть жвачным. В конкретных вариантах осуществления, откармливаемое силосом животное может быть любым животным, откармливаемым силосом, например, крупным рогатым скотом, овцой, свиньей, лошадями, козами, бизоном, яками, индийским буйволом и оленем.
В некоторых вариантах осуществления, способы, предложенные для увеличения количества мяса у откармливаемого силосом животного, дополнительно включают действие, выбранное из группы, состоящей из: помещения силоса в контейнер, предназначенный для транспортировки, и связывание с силосом указания, которое способно давать конечному пользователю инструкции относительного того, как давать силос животному. Таким образом, предложены наборы, включающие силос, которые позволяют конечному пользователю увеличивать количество мяса у откармливаемого силосом животного.
Также раскрыты конечные рационы мясных пород домашних быков, которые включают силос из кукурузы, включающей мутантный ген CAD2 согласно настоящему описанию. Также раскрыты мясо и мясные продукты, изготовленные из животного, которое откармливали таким силосом.
Производство силоса из растений (например, кукурузы), имеющих сниженную активность CAD2
В процессе силосования, клетки растения остаются живыми и метаболически активными, при этом продолжающийся в клетках растения метаболизм и микроорганизмы в спрессованном силосе вызывают выделение диоксида углерода и тепла при использовании воздуха, захваченного в засилосованном растительном материале. Анаэробные метаболические условия развиваются по мере роста в силосе уровня диоксида углерода. Требуемые бактерии начинают процесс брожения, когда дыхание растения останавливается. Если присутствует слишком много воздуха, или если диоксид углерода улетучивается, анаэробные условия могут не развиваться. В таком случае дыхание может продолжаться, а дышащие клетки растения могут использовать слишком много сахара и углеводов. Это может приводить к израсходованию питательных веществ, требуемых нужным бактериям для сохранения растительного материала в виде силоса, и может приводить к получению силоса плохого качества. Чтобы избежать такого нежелательного эффекта, может быть важна упаковка и закрывание силоса сразу после наполнения.
Как только дыхание растительных клеток прекращается, бактерии, которые питаются доступными крахмалами и моносахаридами в засилосованной кукурузе, вырабатывают уксусную и молочную кислоты. Чтобы стимулировать рост необходимых бактерий, силос может содержать небольшое количество воздуха, иметь температуру 80-100°F (~27-38°C), и содержать крахмалы и сахара для питания. Ферментация может продолжаться до тех пор, пока кислотность силоса не станет достаточно высокой, чтобы рост бактерий остановился. В некоторых примерах, требуемая степень кислотности приблизительно соответствует pH 4,2. Указанная степень кислотности может устанавливаться в течение 3 недель после заполнения силосохранилища.
Если влажность фуража слишком высокая, может произойти выход жидкости. Выход жидкости включает в себя слив вод (избыточной влаги из силоса и пульпы) из силоса, которые обычно проникают в окружающую среду как серьезный загрязнитель. В результате выхода жидкости, нужные компоненты (например, соединения азота, такие как белок; и минеральные вещества) силоса могут быть потеряны. Выход жидкости обычно достигает своего пика приблизительно на четвертый день после загрузки силосохранилища. Поэтому, чтобы избежать, например, потери требуемых компонентов силоса из силоса, содержание влаги в фураже, поступающем в силосохранилище, может быть выбрано так, чтобы оно было достаточно низким, чтобы уменьшить или предотвратить потерю при выходе жидкости. Впрочем, силос, который является слишком сухим, может не уплотняться надлежащим образом, и может также демонстрировать высокую потерю нужных компонентов из силоса вследствие избыточной ферментации и гниения.
Растения могут быть засилосованы при содержании сухого вещества приблизительно 30-40%, чтобы обеспечить оптимальный процесс брожения и минимизировать потери в процессе брожения. Чтобы достичь содержания сухого вещества приблизительно 30-40%, растительный материал может потребоваться высушить в поле после скашивания и перед измельчением, например, силосоуборочным комбайном. При приготовлении силоса, зерно можно собирать вместе с остальной частью растения. Для повышения доступности питательных веществ в силосе для усвоения в кишечном тракте откармливаемого силосом животного, может быть желательно расплющить зерно в ходе процесса измельчения.
Собранный растительный материал (например, материал растения кукурузы) может быть помещен в силосохранилище. Неограничивающие примеры силосохранилищ, которые могут применяться для приготовления силоса, включает: силосный бункер, силосную куча, бетонную сборную силосную башню или силосную башню. Растительный материал уплотняют в силосохранилище, чтобы удалить из растительного материала воздух и обеспечить анаэробное брожение. Может потребоваться герметично закрыть силосохранилище пластиковой силосной пленкой, в зависимости от типа используемого силосохранилища. Использование пластикового покрытия на траншейном силосохранилище, силосной яме или силосной башне большого диаметра может существенно сократить потери корма. Как правило, покрытие применяют сразу после загрузки последней партии растительного материала в силосохранилище, при этом пластиковые покрытия утяжеляют грузом, чтобы прочно удерживать их на поверхности силоса. В альтернативе, растительный материал может быть подготовлен к ферментации в ходе загрузки силосохранилища при брикетировании растительного материала и обертывания брикетов силосной пленкой для герметичности. В траншейных или бункерных силосохранилищах может быть желательно делать насыпь или уклон на фураже. Это может облегчать стекание дождевой воды из силосохранилища.
Добавки необязательно могут быть добавлены к растительному материалу для улучшения ферментации. Примеры добавок в растительный материал, которые могут потребоваться в определенных применениях, включают микробные добавки, такие как Lactobacillus spp., и другие прививочные материалы; кислоты, такие как пропионовую кислоту, уксусную кислоту или муравьиную кислоту; или сахар. Как будет очевидно специалистам в данной области, также могут использоваться другие методы производства силоса помимо конкретно описанных в настоящей заявке.
Одно из преимуществ производства силоса состоит в том, что процесс может не оказывать никакого влияния на состав, количество или доступность пищевых веществ, содержащихся в растительном материале, используемом для производства силоса. Напротив, цели самого процесса состоят в сохранении качества растительного материала в том виде, в котором он находился до его использования с целью производства силоса, а также в сохранении положительных свойств растительного материала в течение длительного периода времени. Таким образом, растительный материал может использоваться в качестве фуража намного позже того, как растительный материал был собран.
Кукуруза может быть собрана на силос после достижения восковой спелости початков, но перед тем как листья высохнут до коричневого цвета. На этой стадии роста початок может накопить большую часть своей потенциальной питательной ценности, но при этом также может быть небольшая потеря листьев и стеблей. Таким образом, количество и качество кукурузного силоса могут быть на пике, когда растительный материал собирают в течение данной стадии. Зерна в початках обычно становятся хорошо вдавленными, когда початки имеют 32-35% влажность. С течением времени, после того, как зерна стали хорошо вдавленными, кормовая ценность растительного материала может уменьшаться, тогда как полевые потери могут расти. Кукуруза, собранная для силоса на молочной стадии (зерно кукурузы выделяет белую жидкость при вскрытии) или на молочно-восковой стадии (зерно кукурузы начинает приобретать рыхлую консистенцию наподобие теста) может приводить к меньшему количеству питательных веществ с акра, чем если бы ее собрали позднее. Растительный материал из кукурузы также может неправильно ферментироваться в силосохранилище, если его собрать слишком рано.
Зрелость обычно относится ко времени, когда початок накопил почти весь свой потенциал накопления сухого вещества. Температуры в течение роста могут влиять на степень зрелости кукурузы, особенно во время осени. Например, полный потенциал накопления сухого вещества початков может быть не достигнут, если температура воздуха слишком низкая и/или стоит облачная погода. Силос из кукурузы, который собран поздно и имеет коричневые и мертвые листья и стебли, может давать силос удовлетворительного качества, но полное производство с акра может резко снизиться. С существенными полевыми потерями сталкивались, когда силос собирали поздней осенью или в начале зимы. Кроме того, уменьшение количества сухого вещества, хранящегося в силосохранилище, можно обнаружить в случае силоса, который срезали поздно.
Кукуруза, которая была повреждена, например, при засухе, высоких температурах, увядании, морозе или граде, может быть сохранена для силоса. Впрочем, качество такого сохраненного силоса может быть не таким высоким, как у силоса, полученного из неповрежденной кукурузы, которая достигла восковой стадии. Кормовая ценность силоса может зависеть как от состояния развития кукурузы, так и от того, как кукурузу обрабатывали после ее повреждения. Обычные наблюдаемые показатели силоса из незрелой кукурузы включают: более высокую влажность; другой процесс ферментации, нежели у зрелой кукурузы; кислый запах и повышенный слабительный эффект. Кукуруза, которое подвергалась воздействию мороза, обычно имеет низкое содержание каротина. Она быстро высыхает и теряет листья. Таким образом, может потребоваться добавить воду к кукурузе, которая замерзла и стала слишком сухой. Также может потребоваться добавить воду к кукурузе после засухи.
В случае незрелой кукурузы, которая была повреждена воздействием очень высоких температур, может быть желательным не подвергать ее силосованию сразу. Незрелая, поврежденная высокой температурой кукуруза может не дать початки, но если отложить ее сбор, может последовать небольшой дополнительный рост стебля. Дополнительный рост стебля приведет к получению дополнительного корма. Если кукурузу собирают на силос слишком рано после сильного повреждения растений высокой температурой, стебель может иметь слишком высокую влажность, чтобы можно было получить высококачественный силос. Кукуруза, собранная слишком рано после сильного теплового повреждения, которая имеет слишком высокую влажность, также может потерять питательные вещества при выходе жидкости.
Возможные проблемы, связанные с силосом, приготовленным из поврежденной кукурузы, включают ее недостаточную энергетическую ценность из-за неполного формирования зерна и неправильной ферментации, вызванной избыточной сухостью поврежденного растения. Как известно специалистам в данной области, указанные проблемы могут быть исправлены, по меньшей мере частично, при добавлении дополнительного источника энергии и добавлении влаги, соответственно.
Силос из кукурузы может быть измельчен в частицы, которые имеют длину ½”-3/4” (1,3-1,9 см). Частицы такого размера могут уплотняться более сильно, и дополнительно могут быть более подходящими для откармливаемых силосом животных. Очень мелко нарезанный силос, который имеет длину меньше 1/2”, может быть сделан с помощью вторичного измельчителя. Использование очень мелко нарезанного силоса увеличивает количество сухого вещества, которое можно сохранить, например, в силосохранилище. Впрочем, очень мелко нарезанный силос может быть менее пригоден для животного, откармливаемого таким силосом.
Если силос слишком сухой, может потребоваться добавить воды, например, создав воздухонепроницаемые условия. Как правило, 3,79 литра воды можно добавить в 0,9 метрических тонны силоса для требуемого повышения влагосодержания на 1 процент. Следует понимать, что может потребоваться больше или меньше воды, и значения могут быть взяты в процессе загрузки силосохранилища, чтобы гарантировать добавление достаточного, но не слишком большого, количества воды. Воду можно добавлять по мере заполнения силосохранилища. Если воду добавить после заполнения силосохранилища, он может просочиться вниз по стенкам силосохранилища и поэтому не проникнуть в силосную массу. Такая утечка может вызвать вымывание питательных веществ из силоса и может нарушить воздухонепроницаемость, и привести к неправильной ферментации.
Высококачественный силос может быть сделан без добавления добавок или консервантов. Однако добавки могут быть добавлены в силос для повышения одной или нескольких характеристик силоса. Например, патока и зерно могут быть добавлены в кукурузный фураж во время загрузки силосохранилища.
В случае крупнотоннажного силосохранилища и высокоскоростных методов заполнения, в силосохранилищах требуется контролировать распределение и плотность силоса. Ненадлежащее распределение и плотность могут вызвать повышенный выход влаги, плохую ферментацию и/или потери емкости хранилища. Половина объема цилиндрического силосохранилища находится на внешнем крае силосохранилища. Например, для цилиндрического силосохранилища диаметром 14’ (4,3 м), половина его объема находится за пределами 2’ его диаметра. Если материал в этой внешней области уплотнен слишком свободно, вместимость силосохранилища может значительно уменьшиться. Таким образом, силосные башни могут быть оборудованы распределителем, который облегчает надлежащее распределение и уплотнение силоса.
Потеря питательных веществ происходит во всем силосе в течение процесса силосования из-за присутствия живых микроорганизмов, которые выполняют процесс ферментации. Величина пищевой ценности, потерянная в процессе силосования, зависит, среди прочего, от удаления воздуха при заполнении и от предотвращения потери диоксида углерода. Диоксид углерода необходим для прекращения дыхания засилосованных клеток растения и предотвращения потерь жидкости, нежелательного брожения и/или порчи из-за обнажения поверхности растительного материала. Поэтому правильные методы силосования обычно приводят к более высококачественному силосу с максимальным содержанием питательных веществ.
Силос из растений (например, кукурузы), имеющих пониженную активность CAD2, в конечном рационе
Силос из растений, имеющих пониженную активность CAD2, имеет сниженное содержание лигнина по сравнению с растениями дикого типа того же вида, и может быть нарезан на более длинные частицы, чем обычный силос, независимо от того, обработан он или нет. Перевариваемость NDF силоса bm1 может быть выше, чем у обычного силоса. Состав свежеприготовленного силоса не обязательно отражает состав корма, который съест откармливаемое силосом животное. Таким образом, ферментируемые образцы могут быть проанализированы по истечении некоторого периода времени в силосохранилище. Например, образцы могут быть проанализированы по меньшей мере через две недели, или по меньшей мере через два месяца, в силосохранилище.
После того, как силос из растений, имеющих пониженную активность CAD2, готов, и при этом было определено, что силос готов для потребления животным, силос может быть включен в конечный рацион, который дают животному, которое будет использоваться для производства мяса или мясного продукта. В некоторых примерах, конечный рацион, включающий силос, может не содержать зерно кукурузы, например, сухую плющенную кукурузу или размолотую кукурузу. Типичные конечные рационы включают по меньшей мере приблизительно 11% белка, приблизительно 60 МКал чистой энергии, приблизительно 0,5% кальция, приблизительно 0,35% фосфора и приблизительно 0,6% калия. В некоторых примерах, преимущество состоит в том, что конечный рацион демонстрирует более высокую кормовую эффективность (G:F). В конкретных примерах, конечный рацион, который не включает зерно кукурузы, может приводить к среднему ежедневному приросту веса у животного, откармливаемого конечным рационом, который сопоставим со средним ежедневным приростом веса, получаемым с применением обычных конечных рационов, в которых в качестве источника энергии используется зерно кукурузы.
В некоторых примерах, конечный рацион производят с применением силоса из растений (например, кукурузы), включающих мутантный ген CAD2 согласно настоящему описанию, где конечный рацион включает приблизительно от 15% до приблизительно 30% силоса. Таким образом, конечный рацион может включать, например, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32% или 33% силоса. В конкретных примерах, конечный рацион производят с применением силоса из кукурузы bm1. В некоторых примерах производят конечный рацион, включающий по меньшей мере один источник волокна. Таким образом, конечный рацион может включать, например, один, два, три, четыре или больше четырех источников волокна. В некоторых примерах производят конечный рацион, включающий по меньшей мере один продукт переработки кукурузы. Таким образом, конечный рацион может включать, например, один, два, три, четыре или больше четырех продуктов переработки кукурузы. В некоторых примерах производят конечный рацион, включающий меньше 60% сухого вещества. В других примерах конечный рацион включает меньше 55% сухого вещества. В некоторых определенных примерах конечный рацион включает меньше 50% сухого вещества. Таким образом, конечный рацион может включать, например, 59%, 58%, 57%, 56%, 55%, 54%, 53%, 52%, 51%, 50%, 49%, 48%, 47%, 46%, 45%, 44%, 43%, 42%, 41% или 40% сухого вещества.
C. Сочетание мутантного гена CAD2 и одного или более дополнительных признаков
В некоторых вариантах осуществления, мутантный ген CAD2 согласно настоящему описанию может быть введен в растение, включающее один или более требуемых признаков, с целью получения растения как с bm1 или другим фенотипом с уменьшенным содержанием лигнина, так и с одним или более требуемыми признаками. Процесс введения мутантного гена CAD2 согласно настоящему описанию в растение, включающее один или более требуемых признаков (либо введение в существующую линию растений, либо введение мутантного гена CAD2 в растение одновременно с дополнительной молекулой нуклеиновой кислоты, которая обеспечивает требуемый признак), указано в настоящем описании как "сочетание". В некоторых примерах, при сочетании мутантного гена CAD2 с одним или более требуемыми признаками, bm1 или другой фенотип с уменьшенным содержанием лигнина можно скомбинировать с одним или более требуемыми признаками. Например, сочетание признака bm1 с признаком bm3 может приводить к дополнительному повышению перевариваемости силоса и существенному повышению выхода сбраживаемых сахаров в гидролизе биомассы без предварительной обработки.
Примеры признаков, которые могут быть предпочтительными для комбинирования с bm1 или другим фенотипом с уменьшенным содержанием лигнина, включают, без ограничения: цитоплазматическую мужскую стерильность; гены устойчивости к болезни растения (см., например, Jones et al. (1994) Science 266:789 (ген Cf-9 устойчивости томата к Cladosporium fulvum); Martin et al. (1993) Science 262:1432 (ген Pto устойчивости томата к Pseudomonas syringae); и Mindrinos et al. (1994) Cell 78:1089 (ген RSP2 устойчивости к Pseudomonas syringae)); ген, придающий устойчивость к вредителю; белок Bacillus thuringiensis, его производное или синтетический полипептид, моделируемый на его основе (см., например, Geiser et al. (1986) Gene 48:109 (ген δ-эндотоксина Bt; молекулы ДНК, кодирующие гены δ-эндотоксина могут приобретены в Американской коллекции типовых культур (ATCC, Manassas, VA), например, под регистрационными номерами ATCC 40098, 67136, 31995 и 31998)); лектин (см., например, Van Damme et al. (1994) Plant Molec. Biol. 24:25 (гены манноза-связывающих лектинов Clivia miniata)); витамин-связывающий белок, например, авидин (см. международную публикацию PCT US93/06487 (применение авидина и гомологов авидина в качестве ларвицидов против насекомых-вредителей)); ингибитор фермента; протеазу или ингибитор протеиназ (см., например, Abe et al. (1987) J. Biol. Chem. 262:16793 (ингибитор цистеинпротеиназы риса); Huub et al. (1993) Plant Molec. Biol. 21:985 (ингибитор протеиназы-I табака; и патент США 5,494,813); ингибитор амилазы (см. Sumitani et al. (1993) Biosci. Biotech. Biochem. 57:1243 (ингибитор альфа-амилазы Streptomyces nitrosporeus)); гормон или феромон насекомого, например, экдистероид или ювенильный гормон, их вариант, миметик на их основе, или их антагонист или агонист (см., например, Hammock et al. (1990) Nature 344:458 (инактиватор ювенильного гормона)); инсектоспецифический пептид или нейропептид, который нарушает физиологию поражаемого вредителя (см., например, Regan (1994) J. Biol. Chem. 269:9 (рецептор диуретического гормона насекомых); Pratt et al. (1989) Biochem. Biophys. Res. Comm. 163:1243 (аллостатин из Diploptera puntata); патент США 5,266,317 (инсектоспецифические паралитические нейротоксины)); инсектоспецифичный яд, вырабатываемый в природе змеей, осой или любым другим организмом (см., например, Pang et al. (1992) Gene 116:165 (инсектотоксичный пептид скорпиона)); фермент, ответственный за гипернакопление монотерпена, сесквитерпена, стероида, гидроксамовой кислоты, фенилпропаноидного производного или другой небелковой молекулы с инсектицидной активностью; фермент, участвующий в модификации, включая посттрансляционную модификацию, биологически активной молекулы, например, гликолитического фермента; протеолитический фермент; липолитический фермент; нуклеазу; циклазу; трансаминазу; эстеразу; гидролазу; фосфатазу; киназу; фосфорилазу; полимеразу; эластазу; хитиназу или глюканазу, природную или синтетическую (см., международную публикацию PCT WO 93/02197 (ген каллазы); молекулы ДНК, которые содержат кодирующие хитиназу последовательности (например, из ATCC, под регистрационными номерами 39637 и 67152); Kramer et al. (1993) Insect Biochem. Molec. Biol. 23:691 (хитиназа табачного бражника); и Kawalleck et al. (1993) Plant Molec. Biol. 21:673 (ген ubi4-2 полиубиквитина петрушки); молекулу, которая стимулирует трансдукцию сигнала (см., например, Botella et al. (1994) Plant Molec. Biol. 24:757 (кальмодулин); и Griess et al. (1994) Plant Physiol. 104:1467 (кальмодулин кукурузы); пептид гидрофобного момента (см., например, международную публикацию PCT WO 95/16776 (производные пептида тахиплезина, которые ингибируют грибковые патогены растений); и международная публикация PCT WO 95/18855 (синтетические антибактериальные пептиды, которые придают устойчивость к заболеванию)); мембранную пермеазу, каналообразователь или блокатор каналов (см. Jaynes et al. (1993) Plant Sci 89:43 (аналог литического пептида цекропина-β, придающий трансгенным растениям устойчивость к Pseudomonas solanacearum); вирусно-инвазивный белок или получаемый из него комплексный токсин (см. Beachy et al. (1990) Ann. rev. Phytopathol. 28:451 (опосредованная белками оболочки устойчивость против вируса мозаики люцерны, вируса мозаики огурца, вируса полосатости табака, вируса-X картофеля, вируса-Y картофеля, вируса гравировки табака, вируса погремковости табака и вируса табачной мозаики)); инсектоспецифичное антитело или иммунотоксин, получаемый из него (см. Taylor et al., Abstract #497, Seventh Int’l Symposium on Molecular Plant-Microbe Interactions (Edinburgh, Scotland) (1994) (энзиматическая инактивация посредством получения фрагментов одноцепочечных антител); вирусоспецифическое антитело (см. например, Tavladoraki et al. (1993) Nature 366:469 (гены рекомбинантного антитела для защиты от атаки вируса)); ингибирующий развитие белок, продуцируемый в природе патогеном или паразитом (см. Lamb et al. (1992) Bio/Technology 10:1436 (грибковые эндо-α-1,4-D-полигалактуроназы способствуют грибковой колонизации и высвобождение питательных веществ растения под действием гомо-α-1,4-D-полигалактуроназы, солюбилизирующей растительную клеточную стенку; Toubart et al. (1992) Plant J. 2:367 (белок, ингибирующий эндополигалактуроназу)); и ингибирующий развитие белок, продуцируемый в природе растением (см. Logemann et al. (1992) Bio/Technology 10:305 (ген инактивации рибосом ячменя обеспечивает повышенную устойчивость к грибковому заболеванию)).
Дополнительные примеры признаков, которые могут быть предпочтительными для комбинирования с bm1 или другим фенотипом с уменьшенным содержанием лигнина, включают, без ограничения, гены, которые придают устойчивость к гербициду (Lee et al. (1988) EMBO J. 7:1241 (мутантный фермент ALS); Miki et al. (1990) Theor. Theor. Appl. Genet. 80:449 (мутантный фермент AHAS); патенты США 4,940,835 и 6,248,876 (мутантные гены 5-енолпирувилшикимат-3-фосфатсинтазы (EPSP), обеспечивающие устойчивость к глифосату); патент США 4769061 и регистрационный номер ATCC 39256 (гены aroA); гены глифосатацетилтрансферазы (устойчивость к глифосату); другие фосфоновые соединения из видов Streptomyces, включая Streptomyces hygroscopicus и Streptomyces viridichromogenes), такие как описанные в европейской заявке 0 242 246 и DeGreef et al. (1989) Bio/Technology 7:61 (гены глюфосинатфосфинотрицинацетилтрансферазы (PAT), обеспечивающие устойчивость к глифосату); пиридинокси- или феноксипропионовые кислоты и циклогексоны (устойчивость к глифосату); европейской заявке 0 333 033 и патенте США 4,975,374 (гены глутаминсинтазы, обеспечивающие устойчивость к гербицидам, таким как L-фосфинотрицин); Marshall et al. (1992) Theor. Appl. Genet. 83:435 (гены Acc1-S1, Acc1-S2 и Acc1-S3, обеспечивающие устойчивость к феноксипропионовым кислотам и циклогексонам, такие как сетоксидим и галоксифоп); WO 2005012515 (гены GAT, обеспечивающие устойчивость к глифосату); WO 2005107437 (гены, придающие устойчивость к 2,4-D, фоп и пиридилоксиауксиновым гербицидам); и гербицид, который ингибирует фотосинтез, такой как триазин (гены psbA и gs+) или бензонитрил (ген нитрилазы) (см., например, Przibila et al. (1991) Plant Cell 3:169 (мутантные гены psbA); нуклеотидные последовательности генов нитрилазы, раскрытые в патенте США 4,810,648, и молекулы ДНК, содержащие указанные гены, доступны под рег. номерами ATCC 53435, 67441 и 67442; а также Hayes et al. (1992) Biochem. J. 285:173 (глутатион-S-трансфераза)).
Дополнительные примеры признаков, которые могут быть предпочтительными для комбинирования с bm1 или другим фенотипом с уменьшенным содержанием лигнина, включают, без ограничения, гены, которые придают или вносят вклад в признак с дополнительными свойствами, например, модифицированный метаболизм жирных кислот (см., например, Knultzon et al. (1992) Proc. Natl. Acad. Sci. U.S.A. 89:2624 (антисмысловой ген стеарил-ACP-десатуразы для повышения содержания стеариновой кислоты в растении)); уменьшенное содержание фитата (см., например, Van Hartingsveldt et al. (1993) Gene 127:87 (ген фитазы Aspergillus niger усиливает расщепление фитата, добавляя большее количество свободного фосфата в трансформированное растение); и Raboy et al. (1990) Maydica 35:383 (клонирование и повторное включение ДНК, ассоциированной с аллелем, ответственным за мутантные формы кукурузы, содержащие низкие уровни фитиновой кислоты)); и модифицированный углеводный состав, получаемый, например, при трансформации растения геном, кодирующим фермент, который изменяет профиль разветвления крахмала (см., например, Shiroza et al. (1988) J. Bacteol. 170:810 (мутантный ген фруктозилтрансферазы Streptococcus); Steinmetz et al. (1985) Mol. Gen. Genet. 20:220 (ген левансахаразы); Pen et al. (1992) Bio/Technology 10:292 (α-амилаза); Elliot et al. (1993) Plant Molec. Biol. 21:515 (гены инвертазы томата); Sogaard et al. (1993) J. Biol. Chem. 268:22480 (ген α-амилазы ячменя); и Fisher et.al. (1993) Plant Physiol. 102:1045 (разветвляющий крахмал фермент II эндосперма кукурузы)).
D. Другие применения растения, имеющего пониженную активность CAD2
Многие сельскохозяйственные или промышленные применения помимо производства силоса касаются целевых растительных продуктов, выходы которых непосредственно связаны с содержанием и/или составом лигнина в стенке растительной клетки. Примеры таких продуктов и применений включают без ограничения: продукты, применяемые в производстве бумаги и производстве энергии, например, в форме биотоплива. Растения, включающие мутантный ген CAD2 согласно настоящему описанию, могут иметь bm1 или другой фенотип с уменьшенным содержанием лигнина. Как сумеют оценить специалисты в данной области, могут ожидать, что растительные продукты, полученные из таких растений, будут иметь характеристики, отличающие их от растения дикого типа того же вида, где такие отличающие характеристики могут быть предпочтительными. Таким образом, любое применение растения, включающего мутантный ген CAD2 согласно настоящему описанию, которое обладает преимуществом ожидаемого bm1 или другого фенотипа с уменьшенным содержанием лигнина в растении, включено в рамки настоящего описания.
Следующие примеры представлены для пояснения некоторых конкретных признаков и/или вариантов осуществления изобретения. Примеры не следует рассматривать в качестве ограничения настоящего описания конкретными представленными признаками или вариантами осуществления.
ПРИМЕРЫ
Пример 1: Клонирование и секвенирование генов CAD2 из двух линий bm1
Использовали образцы листа кукурузы из инбредных линий 515Dbm1 (bm1 мутант), 6XN442 (дикий тип) и DASbm1. DASbm1 представляет собой новый, природный bmr мутант, обнаруженный в генетическом окружении CV5123/GR8207. Исходное поколение F1, из которого происходила мутация DASbm1, было создано в селекционном блоке летом 2003 года при использовании GR8207 в качестве мужского растения и его скрещивания с женским CV5123. Данный кросс самоопыляли в зимнем питомнике 2003 года, и початки F2 затем доращивали, получив семена F2. Популяцию F2 высевали летом 2004 года, и 60 самоопыленных початков отбирали для дальнейшей селекции в тестировании зерен. Указанные 60 початков отправляли в зимний питомник в 2004 году для самоопыления с целью создания дальнейшей селекции початков S2. Затем початки S2 высевали в 2006 году в летнем питомнике.
Открытие bmr мутанта сделали при осмотре инбредных линий в питомнике. Идентифицировали ряд, показывающий явный фенотип BMR. Данный ряд был получен из початка 31, взятого из 60 початков, отобранных из популяции CV5123/GR8207-B, и показал очень высокое подобие по структуре растения с другими 59 отобранными початками, за исключением наличия признака BMR. Первоначально было невозможно определить, являлся ли мутант bm3, bm1 или другой мутацией. Затем растения S2 самоопыляли, а семена собирали и сохраняли. Летом 2007 года, семена S3 высевали, при этом все растения все еще показывали признак BMR. Растения S3 самоопыляли, получив початки S4, и линию отмечали, как представляющую потенциальный интерес для производства силоса. Летом 2008 года тестовые кроссы получали с известными инбредными линиями bm1 и bm3 для определения фона bmr мутанта. Летом 2009 года семена тестовых кроссов проращивали в тесте потомства и определяли, что мутация была новой bm1 мутацией, поскольку все растения в тесте потомства с инбредной линией bm1 экспрессировали признак BMR, тогда как все растения в потомстве bm3 не показывали признак BMR. Затем отбирали образцы ткани листьев из CV5123/GR8207 NIL, инбредной линии 515Dbm1, а также гетерозиготные и нулевые растения из различных генетических окружений, и подвергали молекулярному генетическому анализу, включая работу маркеров, для определения точной природы bmr мутанта DASbm1.
Образцы листьев кукурузы растирали в тонкий порошок при использовании Genogrinder 2000 (SPEX CertiPrep, Metuchen, NJ). ДНК выделяли согласно стандартной методике выделения ДНК с использованием 2,5% CTAB (цетилтриметиламмонийбромида). Перед ПЦР, образцы ДНК анализировали количественно с использованием набора Quant-it PicoGreen Quantification Kit (Invitrogen, Carlsbad, CA) согласно инструкциям производителя.
Геномную последовательность CAD2 из инбредной линии кукурузы, маиса B73, получали из Genbank (регистрационный номер в Genbank AC230031). Данная последовательность имела длину приблизительно 5,9 тпн и включала промотор протяженностью 1,7 тпн, четыре экзона, три интрона и короткий терминатор. Праймеры подбирали на основе последовательности B73, и реакцию ПЦР проводили, используя систему ABI GeneAmp PCR System 9700 (Applied Biosystems, Foster City, CA). Реакционные смеси содержали 2,5 единицы полимеразы TaKaRa LA Taq (Takara Bio Inc., Shiga, Japan), 400 нМ dNTP, 200 нМ прямого и обратного праймеров, и 30 нг геномной ДНК. Использовали следующую программу ПЦР: ПЦР начиналась с этапа денатурации продолжительностью 2 минуты при 94°C; с последующими 30 циклами при 94°C в течение 45 секунд, 55°C в течение 45 секунд и 72°C в течение 2 минут. Продукты ПЦР визуализировали в 2% агарозном геле E-Gel® и затем выделяли с использованием набора PURELINK™ ДЛЯ быстрого выделения из геля (Invitrogen, Carlsbad, CA). Очищенные продукты ПЦР затем отправляли в Eurofins MWG Operon (Huntsville, AL) для прямого секвенирования. Последовательности анализировали с использованием Sequencher 4.8 (Ann Arbor, MI). Мутации идентифицировали путем сравнения последовательностей CAD2, амплифицированных из bmr мутантов и 6XN442, с последовательностью, приведенной для маиса B73.
Из-за присутствия трех довольно больших интронов и некоторых необычных особенностей последовательности (например, простого TA повтора длиной 82 п.н. в интроне 3), первоначальные попытки амплифицировать ген CAD2 в виде одного фрагмента длиной 5,9 тпн не были успешными. Поэтому создали набор праймеров для вложенной ПЦР (см. Таблицу 1), которые использовали для успешной амплификации семи перекрывающихся фрагментов CAD2 из 515Dbm1 и линии дикого типа (Фиг.1). Полноразмерные последовательности CAD2 из 515Dbm1 и линии дикого типа собирали из семи полученных фрагментов. Последовательности геномной, предсказанной кДНК и белков для 515Dbm1 и 4XN442 приведены в SEQ ID NO: 1-6.
AATGCACGATGTCAACTCTCTTGCCTATAA
AATTTTCTCATGAAAACGCTGAAACTGC
TGAGCACAAACGGTTAACACAC
ATTGTATCAGTTCACGGTGGTG
CACACCAACCACAATAATAAGCTAATACTC
AACGATCACCCCGACGCCTACC
CCACCGTGAACTGATACAATAACAATAAAG
ACACTGCATGCAAGATAACGCTGAAAATAA
TGCAACAAGAAGATCTGGTCAT
TCATACCGTACTTTCCACATCAA
TTTTGCGAGAAGTGGACGAGATAAGGT
AATGTTGTTGGAGGTAGGTGGTGTGGTTT
C1-R14
GAGAAATGAGGATAACTTTCTCCATCGTT
CTATAGACGAGACAGAAGGGAACGGATTTG
Сравнение 515Dbm1 мутанта CAD2 с мутантом дикого типа (6XN442) и bm1 (B73) показало присутствие 15 SNP и восьми вставок/делеций. Большинство указанных изменений было расположено в промоторной области или в интронах, за исключением вставки динуклеотида AC (нуклеотид 3994-3995 в 515Dbm1), расположенной в экзоне 3 мутанта bm1, и SNP G/A (нуклеотид 5410 в 515Dbm1), расположенного в 4-ом экзоне (см. Фиг.3 и 4). Вставка AC в 515Dbm1 вызывает сдвиг рамки считывания и вводит преждевременный стоп-кодон через 52 п.н. после вставки, что приводит к намного более короткому белку CAD2 (147 аминокислот для 515Dbm1 CAD2 в сравнении с 367 аминокислотами для CAD2 дикого типа (Фиг.4). Усеченный белок CAD2 в 515Dbm1, наиболее вероятно, нефункционален, даже если он и продуцируется, поскольку он не имеет NADPH-связывающего и C-концевого каталитического доменов.
Те же семь пар праймеров, показанных в Таблице 1, использовали в попытке амплификации перекрывающихся фрагментов CAD2 из DASbm1, и 6 пар амплифицировали ожидаемые фрагменты. Однако с помощью пары F5/R5 не удалось амплифицировать ожидаемый 3327 п.н. фрагмент, или даже какие-то специфичные продукты ПЦР, даже после многократных попыток. Поэтому создали дополнительные праймеры для вложенной ПЦР (см. Таблицу 2), которые использовали для успешной амплификации 5’-концовых 2757 п.н. отсутствующего 3327 п.н. фрагмента. Впрочем, амплифицировать 3’-конец (приблизительно 570 п.н.) с использованием многих пар праймеров и условий ПЦР не удалось. За исключением недостающего пропуска длиной 570 п.н., амплифицированная геномная 5346 п.н. последовательность CAD2 из DASbm1 идентична последовательности из B73. Возникло подозрение, что это была область, которая содержала молекулярные изменения для фенотипа BMR.
AATGCACGATGTCAACTCTCTTGCCTATAA
TGGGTTGAGAAATTGGGTAAGTGC
TGCCCGGTCCAATCTTTCTTA
CGTCTTTCGAGGAGGTCTAC
CGTTTGGTATCGTCCGAGTTGTGT
GCCGGGTAGTGCGATCTTTCTGG
AGATCATGCTGGAAAGGTAGTAGG
TGATCGAAAATATGCCCCAAGTC
ACGCGCCTCCTCCAGTAGTTCTCC
CAAGTTCACACGCTGCTGGGTCTG
Создали праймеры, охватывающие предсказанный экзон 1 и экзон 3 (CVF: GTCCGAGAGGAAGGTGGTC (SEQ ID NO: 35) и CVR: GGCCGTCCATCAGTGTAGA (SEQ ID NO: 36)), которые затем использовали для амплификации кДНК фрагмента CAD2 из DASbm1, 515Dbm1 и 6XN442. Как ожидалось, фрагмент 375 п.н. был амплифицирован с 515Dbm1 и 6XN442. С другой стороны, ПЦР-продукт из DASbm1, как обнаружили, был значительно длиннее. Результаты секвенирования показали, что кДНК CAD2 из DASbm1 содержала дополнительную вставку 409 п.н. между эндогенными экзоном 1 и экзоном 2 (Фиг.4). Поиск BLAST в сравнении с геномом B73 позволил предположить, что 409 п.н. вставка кДНК в DASbm1, наиболее вероятно, является результатом РНК сплайсинга из части предполагаемого транспозона/повторного гена (GRMZM2G017736), расположенного на хромосоме 1, который содержит несколько интронов.
На основе 409 п.н. вставки кДНК, наблюдаемой в DASbm1 и его вероятном геномном источнике, были созданы дополнительные ПЦР-праймеры (см. Таблицу 3), которые использовали для амплификации химерной геномной области CAD2 из DASbm1 (Фиг.1). Результаты секвенирования показали, что геномная вставка имеет длину 3444 п.н., а полноразмерный геномный CAD2, амплифицированный из DASbm1,-9360 п.н. Выравнивание геномного CAD2 из DASbm1, B73, 515Dbm1 и 6XN442 показано на Фиг.3. За исключением вставки 3444 п.н., остальная последовательность CAD2 из DASbm1 идентична последовательности CAD2 из B73. Вставка транспозона 3444 п.н. в DASbm1 приведена в SEQ ID NO: 40.
TATGGGTACTGCTCCTGCAC
CCTTGCAGCAGAACCACTG
AGAATATCATTAGCAGCCAGA
AATTTTCTCATGAAAACGCTGAAACTGC
Геномная природа вставки в DASbm1.
Как показано на Фиг.2, участок вставки в DASbm1 расположен в эндогенном интроне 1 CAD2. Более тщательное исследование последовательности 3444 п.н. вставки показало, что последние 11 оснований, с последовательностью TACTGATATCT (SEQ ID NO:41), являлись прямым повтором 11 п.н. последовательности из интрона 1 CAD2, расположенной непосредственно перед вставкой (Фиг.2). Такие прямые повторы указывают, что вставка, вероятно, обусловлена активностью ДНК транспозона.
Результаты поиска в BLAST с использованием 3433 п.н. вставки (без прямого 11 п.н. повтора) в сравнении с геномными последовательностями B73 выявили многочисленные гомологичные совпадения на различных хромосомах, что указывало на повторы в последовательности. Однако, только один хит на хромосоме 1 (маис B73 RefGen_v1, нуклеотидные положения 148086176-148089850) был на 100% идентичен по всей длине, за исключением отсутствующего 242 п.н. пропуска во вставке DASbm1 (Фиг.4). Другие хиты идентичны менее чем на 100% и соответствуют только части вставки. Так как CAD2 расположен на хромосоме 5, вставка в DASbm1, наиболее вероятно, вырезана из ее исходного местоположения на хромосоме 1 и повторно вставлена в CAD2 посредством активности транспозона. Отсутствующий 242 п.н. пропуск может отражать различие между геномами B73 и DASbm1 (CV5123/GR8207), или он может быть обусловлен делецией при транспозиции.
Предсказанный ген (GRMZM2G017736) расположен в последовательности 3433 п.н. вставки и явно транскрибируется в нормальных растениях кукурузы, так как довольно много соответствующих полноразмерных EST (например, EU976746 и EU976335) обнаружены в базе данных. Предсказанная ORF в GRMZM2G017736 кодирует малый белок размером 167 аминокислот, который показывает высокие степени гомологии со многими hAT (сокр. от hobo из Drosophila, Ac из кукурузы и Tam3 из львиного зева) из семейства транспозаз, которые обычно являются большими белками. Поскольку усеченный белок размером 167 аминокислот не имеет ДНК-связывающего домена BED с цинковыми пальцами (Pfam02892), обычно присутствующего у полноразмерных транспозаз, фрагмент длиной 3433 п.н., более вероятно, является Ds элементом, который требует присутствия Ac элемента в другом месте для транспозиции.
После введения в CAD2 локус на хромосоме 5, вставка и CAD2 формируют химерный ген. Вставка расщеплена на 3 экзона 409 п.н. и формирует химерную мРНК с эндогенными экзонами CAD2 (Фиг.2 и 4). Первый 1158 п.н. фрагмент вставки соединен с 5’концом 927 п.н. первого интрона CAD2 в виде химерного интрона, полная предсказанная ORF GRMZM2G017736 соединена в виде части 1204 п.н. интрона, и последний 463 п.н. фрагмент вставки соединен с 3’ концом 231 п.н. первого интрона CAD2 в виде химерного интрона (Фиг.2).
Вставка транспозона вводит преждевременный стоп-кодон в DASbm1 CAD2
Как описано выше, вставка транспозона в DASbm1 создает химерный ген, который транскрибируется в виде химерной мРНК с дополнительными 409 п.н. между эндогенными экзоном 1 и экзоном 2 CAD2 (Фиг.4). Указанная дополнительная 409 п.н. последовательность, как было предсказано, создает сдвиг рамки считывания и вводит преждевременный стоп-кодон, что приводит к намного более короткому белку CAD2 размером только 48 аминокислот (в сравнении с 367 аминокислотами для белка дикого типа) (Фиг.5). Аналогично усеченному белку CAD2 515Dbm1, 48 аминокислот DASbm1 CAD2, наиболее вероятно, нефункциональны, даже если он продуцируется, потому что он не имеет NADPH-связывающего и C-концевого каталитического доменов.
Пример 2: Высокопроизводительный анализ CAD2 на основе аллель-специфичной ПЦР и проверка
Анализ KASPar™ был разработан на основе вставки AC в экзоне 3 515Dbm1 ZmCAD2 для отличения мутантного аллеля от аллеля дикого типа. Тридцать две инбредные линии дикого типа, без мутации bm1, а также расщепляющиеся популяции, содержащие мутацию bm1, тестировали согласно методике, полученной от производителя (KBioSciences, Hoddesdon, Hertfordshire, UK).
На основе последовательностей, окружающих вставку AC, создали три олига (SEQ ID NO:42 (AC_R1): TCAGTCTCAAGAACTCACTTCTGG, SEQ ID NO:43 (AC_A1): GAAGGTGACCAAGTTCATGCTACTGATGGACGGCCCACA и SEQ ID NO:44 (AC_A2): GAAGGTCGGAGTCAACGGATTACTGATGGACGGCCCACG) для высокопроизводительного маркерного анализа KASPar™, который может применяться для дифференцирования аллеля CAD2 515Dbm1 от других аллелей bm1 и CAD2 дикого типа (Фиг.8).
Анализ KASPar™ сначала проверяли с использованием выборки из 32 инбредных линий дикого типа и мутантной линии bm1, 515Dbm1. Данный анализ показал, что другие линии кроме bm1 не содержали вставку AC. Затем анализ проверяли в расщепляющихся популяциях линий кукурузы bm1, которые обладали одним из трех генотипов: гомозиготный дикий тип; гомозиготный bm1 (содержащий 515Dbm1 вставку AC); и гетерозиготный (Фиг.9). Маркер KASPar обнаружил bm1 вставку AC в гомозиготной bm1 и гетерозиготной популяциях. Кроме того, данный высокопроизводительный анализ различал гомозиготную bm1 популяцию, гетерозиготную популяцию и гомозиготную популяцию дикого типа друг от друга. Таким образом, маркеры такого типа, как указанные, могут применяться для быстрого выполнения точной идентификации зиготности для генотипа bm1 в растениях, подозреваемых на присутствие bm1 из 515Dbm1. Данный анализ может поэтому применяться для идентификации зародышевой плазмы bm1, ускоренной интрогрессии признака bm1 и молекулярной селекции с использованием bm1, для улучшения перевариваемости силоса или увеличения выхода этанола.
Также разработали новые TaqMan™ анализы для различения аллелей DASbm1, 515Dbm1 и CAD2 дикого типа. Праймеры и зонды, которые применялись для DASbm1 и 515Dbm1, перечислены в Таблице 4 и Таблице 5, соответственно. Поскольку DASbm1 содержит большую вставку транспозона, отдельные прямые праймеры для DASbm1 (DASbm1_F) и дикого типа (Wt CAD2_F) подбирали так, чтобы соответствующие ПЦР продукты амплифицировались в стандартных условиях TaqMan™ анализа. На основе вставки транспозона в DASbm1, вставки AC в 515Dbm1 и последовательности CAD2 дикого типа, праймеры и зонды для TaqMan™ анализа создавали при использовании Primer Express 3.0. Праймеры и меченые зонды с двумя метками - FAM или VIC, и красителями Minor Grove Binding Non Fluorescence Quencher™ I (MGBNFQ) - были синтезированы в Applied Biosystems (Foster City, CA). Олиги растворяли в 1×Трис-ЭДТА до 100 µM. Мастер-микс для TaqMan™ генотипирования (Applied Biosystems, Foster City, CA, кат. #4371355) использовали для всех реакциях ПЦР. Реакции ПЦР в реальном времени в объеме 25 µл подготавливали при использовании 96-луночного планшета на оптической системе iCycler™ (BioRad, Hercules, CA), начиная с 15 минут денатурации при 95°C, согласно рекомендациям, с последующими 50 циклами при 92°C в течение 15 секунд и 60°C в течение 1 минуты. Сигналы флуоресценции регистрировали в конце каждого цикла.
и дикого типа
Результаты анализов аллельной дискриминации с использованием праймеров, представленных в Таблицах 4 и 5, показаны на Фиг.10. Поскольку данные анализы и KASPar™ маркеры основаны непосредственно на мутациях bm1 в CAD2, они обеспечат более точное генотипирование, чем доступные косвенные маркеры bm1.
Пример 3: Характеристики кукурузы bm1, содержащей мутации с усечением CAD2
Поскольку DASbm1 представляет собой новую мутацию bm1, о DASbm1 ничего не известно, за исключением того, что она имеет фенотип BMR. Решили исследовать уровни экспрессии РНК и содержание лигнина в растениях DASbm1, и сравнить их с таковыми в 515Dbm1 и растениях дикого типа (6XN442). Ожидалось, что растения 515Dbm1 и DASbm1 имели значительно сниженную активность CAD вследствие мутаций в генах CAD2 двух указанных линий кукурузы, которые в свою очередь привели к введению преждевременного стоп-кодона CAD2. Кроме того, выдвинули предположение, что растения 515Dbm1 и DASbm1 имели сниженные уровни CAD2 транскрипта.
Растения DASbm1, 515Dbm1 и 6XN442 выращивали в теплице. Ткани листьев собирали с растений четырехнедельного возраста и отделяли ткани средней жилки. Образцы измельчали в тонкий порошок в жидком азоте и экстрагировали с использованием набора Qiagen’s RNeasy™ plant mini kit. Набор SuperScript™ III One-Step RT-PCR kit производства Invitrogen и iCycler™ (BioRad) использовали для количественной ПЦР-ОТ для определения уровней экспрессии РНК. CAD2-специфичные олиги создавали на основе четвертого экзона CAD2, и инвертазу кукурузы использовали в качестве контроля для вычисления Delta-Delta Ct.
Для сравнения уровней экспрессии РНК CAD2, на основе четвертого экзона CAD2 и инвертазы кукурузы создавали следующие праймеры/зонды для количественной ПЦР-ОТ (Таблица 6).
Как показано на Фиг.6, растения bm1 имеют намного более высокий уровень экспрессии CAD2, чем остальные ткани листьев, независимо от исходной мутации. Различия были следующими: 4,1, 8,0 и 3,4 раз для 6XN442, 515Dbm1 и DASbm1, соответственно. Линии DASbm1 и 515Dbm1 имеют значительно более слабую экспрессию CAD2, со средним снижением 91% в средней жилке и 89% в листе для DASbm1, и 87% в средней жилке и 93% в листе для 515Dbm1. Впрочем, между двумя bm1 мутантами нет никакого существенного различия (Фиг.6). Такие результаты согласуются с данными, приведенными в литературе для кукурузы bm1 (Halpin et al. (1998), выше), а также для мутанта сорго, bmr6 (Saballos et al. (2009), выше). Снижение экспрессии РНК вероятно происходит главным образом из-за деградации РНК, опосредованной нонсенс-мутациями, которые приводят к продукции преждевременно терминированных белков CAD2 в мутантах 515Dbm1 и DASbm1, механизму, ранее наблюдаемому в растениях и других видах (Conti and Izaurralde (2005) Curr Opin Cell Biol. 17:316-25).
Для сравнения относительного содержания лигнина в мутантных растениях и растениях дикого типа, растертые листья и междоузлия подвергали Фурье-ИК спектроскопическому анализу.
Фурье-ИК измерения выполняли с использованием спектрометра Bruker Vertex (Bruker Optics Inc, 19 Fortune Drive, Manning Park, Billerica MA 01821), с приставкой нарушенного полного внутреннего отражения (НПВО) Miracle с алмазным кристаллом (Pike Technologies, Madison, WI). Спектрометр оборудован детектором на основе дейтерированного триглицинсульфата (ДТГС), работающим при разрешениях 4 см−1 и скорости сканирования 0,32 см/с. Двести пятьдесят шесть интерферограмм были добавлены перед преобразованием Фурье. Инструменту позволяли произвести продувку в течение 5 мин газообразным азотом (сорта 1) перед регистрацией спектров для минимизации влияния атмосферного диоксида углерода и паров воды. Приставка НПВО MIRacle содержит алмазный кристалл однократного отражения для применения в Фурье-ИК спектрометре. Глубина проникновения инфракрасного луча составляет 1,46 микрона. Главное преимущество данной приставки состоит в том, что она допускает анализ образцов меньшего объема по сравнению с приставкой многократного НПВО горизонтального типа (HATR).
Листья (7-ой и 8-ой, 9-ый и 10-ый) и междоузлия (1-ое и 2-ое, 7-ое и 8-ое, 9-ое и 10-ое) собирали с выращенных в теплице растений кукурузы сразу после выметывания пестичных столбиков, лиофилизировали и растирали в тонкие порошки. Небольшую часть образцов помещали непосредственно на алмазный кристалл НПВО для получения данных. Спектры регистрировали в области отпечатков пальцев с 800-1800 см-1. Получали однолучевые спектры всех образцов, и спектральные данные представлены как отношение фонового спектра воздуха в оптических единицах. После каждого измерения, кристалл НПВО тщательно очищали и высушивали, и его спектр проверяли, чтобы убедиться, что на поверхности кристалла не остались остатки образца от предыдущей регистрации. Все спектры корректировали по базовой линии и нормализовали по площади для устранения артефактов.
Содержание лигнина в образцах прямо пропорционально относительному оптическому поглощению Фурье-ИК. Как ожидается, снижение экспрессии РНК CAD2 в обоих мутантах приводит к существенному уменьшенному содержания лигнина (Фиг.7). В среднем, снижение общего содержания лигнина составляло приблизительно 24% в DASbm1 (P=0,03) и 30% в 515Dbm1 (P=0,006) по сравнению с диким типом 6XN442. Между двумя мутантами bm1 не было никакого значимого различия (P=0,4).
Мутации bm1 в кукурузе проявляются в красновато-коричневой пигментации средней жилки листа, связанной со значительно сниженным содержанием лигнина и измененным составом лигнина. Данный фенотип наблюдается с V6 и до более поздних стадий в только что развившихся листьях и других тканях. Были идентифицированы молекулярные основы двух независимых мутантов bm1 (DASbm1 и 515Dbm1). На основе определенных мутаций также разработали высокопроизводительный ПЦР анализ для обнаружения различных аллелей. Предшествующие результаты демонстрируют, что ZmCAD2 является ключевым геном для мутации bm1 в 515Dbm1 и DASbm1, и обеспечивает молекулярную основу для наблюдаемого фенотипа. Поскольку мутации bmr достаточно распространены среди многих видов однодольных, вышеописанные мутации и маркеры также могут применяться в других зерновых культурах; например, сорго обыкновенное, сахарном тростнике, просо, рисе, а также в видах, применяемых в биоэнергетике, таких как просо.
Пример 4: Brown midrib 1 (bm1) в качестве визуального селективного маркера для трансгенов
Технология EXZACT Precision Technology представляет собой генно-инженерную технологию на основе цинковых пальцев, которая, как было показано, способна точно связывать любую последовательность ДНК и точно модифицировать геном посредством прерывания, редактирования или введения генов. На основе технологии EXZACT Precision Technology и недавних открытий bm1, могут быть внедрены два альтернативных метода создания визуального селективного маркера, позволяющего отличать трансгенные растения от их нулевых сегрегантов. Визуальный маркер позволит селекционерам и ученым в полевых условиях быстро идентифицировать трансгенные организмы в расщепляющейся популяции (например, T1) и сравнивать их с нулями без подробной молекулярной работы, а также ускорит процесс конвейерного скрининга трансгенов. Высокопроизводительные анализы также доступны и могут применяться для подтверждения визуального наблюдения, в случае необходимости.
В первом репрезентативном методе, мутантная кукуруза bm1 (DASbm1 или 515Dbm1) может применяться в качестве целевой зародышевой плазмы для трансформации. Посредством молекулярной селекции мутация bm1 может быть введена в текущую трансформируемую зародышевую плазму (B104) с применением маркеров на основе CAD2. Wt CAD2 и целевой ген (GOI) в одной конструкции направляются в эндогенный мутантный локус cad2 с помощью EXZACT Precision Technology. Поскольку мутация bm1 является рецессивной, растения, гомозиготные по GOI-WtCAD2 или гетерозиготные, имеют нормальную пигментацию, тогда как нулевые сегреганты имеют фенотип brown midrib. Это также работает и без EXZACT Precision Technology, но сайт вставки трансгена в геном является случайным. Альтернативный вариант осуществления включает конструирование одного или более белков с цинковыми пальцами, которые удаляют вставку транспозона в DASbm1 или вставку AC в 515Dbm1 в эндогенном мутантном локусе cad2 и в то же время вводят GOI в соседний локус (чтобы предотвратить существенную сегрегацию GOI и bm1 маркера). Это устраняет потребность в Wt CAD2 в трансгенной конструкции.
Во втором репрезентативном методе, растения Wt используются в качестве целевой зародышевой плазмы для трансформации. GOI можно направить в эндогенный Wt CAD2 локус с помощью EXZACT Precision Technology. Сайт вставки может быть таким же, как вставка транспозона в DASbm1, вставка AC в 515Dbm1 или любое положение в локусе CAD2, которое приводит к нефункциональному белку (функциональные домены CAD2 известны). В данном случае, растения, гомозиготные по трансгену, имеют фенотип brown midrib, тогда как гетерозиготы и нули имеют нормальную пигментацию. Brown midrib и ассоциированные фенотипы являются полезными, при этом технология EXZACT Precision Technology может применяться для направления в локусы BM1 (CAD2) и/или BM3 (O-метилтрансфераза кофейной кислоты).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ СПЕЦИФИЧЕСКИХ МАРКЕРОВ ГЕНА КОРИЧНЕВОЙ СРЕДНЕЙ ЖИЛКИ 3 (BROWN MIDRIB-3) У КУКУРУЗЫ ДЛЯ ИНТРОГРЕССИИ ПРИЗНАКОВ | 2011 |
|
RU2593958C2 |
| ГЕН-СПЕЦИФИЧЕСКИЙ АНАЛИЗ НА FLUORY2 В МАИСЕ ДЛЯ ИНТРОГРЕССИИ МУЧНИСТОГО ПРИЗНАКА (FL2) | 2013 |
|
RU2661110C2 |
| ОПТИМАЛЬНЫЕ ЛОКУСЫ СОИ | 2014 |
|
RU2719150C2 |
| КАНОЛА HO/LL С УСТОЙЧИВОСТЬЮ К ЗАБОЛЕВАНИЮ КИЛОЙ КРЕСТОЦВЕТНЫХ | 2012 |
|
RU2618846C2 |
| КАНОЛА HO/LL С УСТОЙЧИВОСТЬЮ К ЗАБОЛЕВАНИЮ КИЛОЙ КРЕСТОЦВЕТНЫХ | 2012 |
|
RU2711934C2 |
| ГЕН-ВОССТАНОВИТЕЛЬ RF4 ДЛЯ ЦИТОПЛАЗМАТИЧЕСКОЙ МУЖСКОЙ СТЕРИЛЬНОСТИ (CMS) C-ТИПА КУКУРУЗЫ, МОЛЕКУЛЯРНЫЕ МАРКЕРЫ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2603005C2 |
| ФУНКЦИОНАЛЬНЫЕ ЛОКУСЫ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ ДЛЯ САЙТА-МИШЕНИ СВЯЗЫВАЮЩИЕСЯ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656158C2 |
| БЫСТРЫЙ НАПРАВЛЕННЫЙ АНАЛИЗ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР ДЛЯ ОПРЕДЕЛЕНИЯ ДОНОРНОЙ ВСТАВКИ | 2014 |
|
RU2668819C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЗИГОТНОСТИ ГЕНА FAD3 В КАНОЛЕ | 2012 |
|
RU2630998C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ И СПОСОБЫ ПОЛУЧЕНИЯ СЕМЯН, ИМЕЮЩИХ В ЗАРОДЫШЕ ПОЛНЫЙ ДИПЛОИДНЫЙ ГЕНОМ, КОМПЛЕМЕНТАРНЫЙ МАТЕРИНСКОМУ | 2006 |
|
RU2438297C2 |

































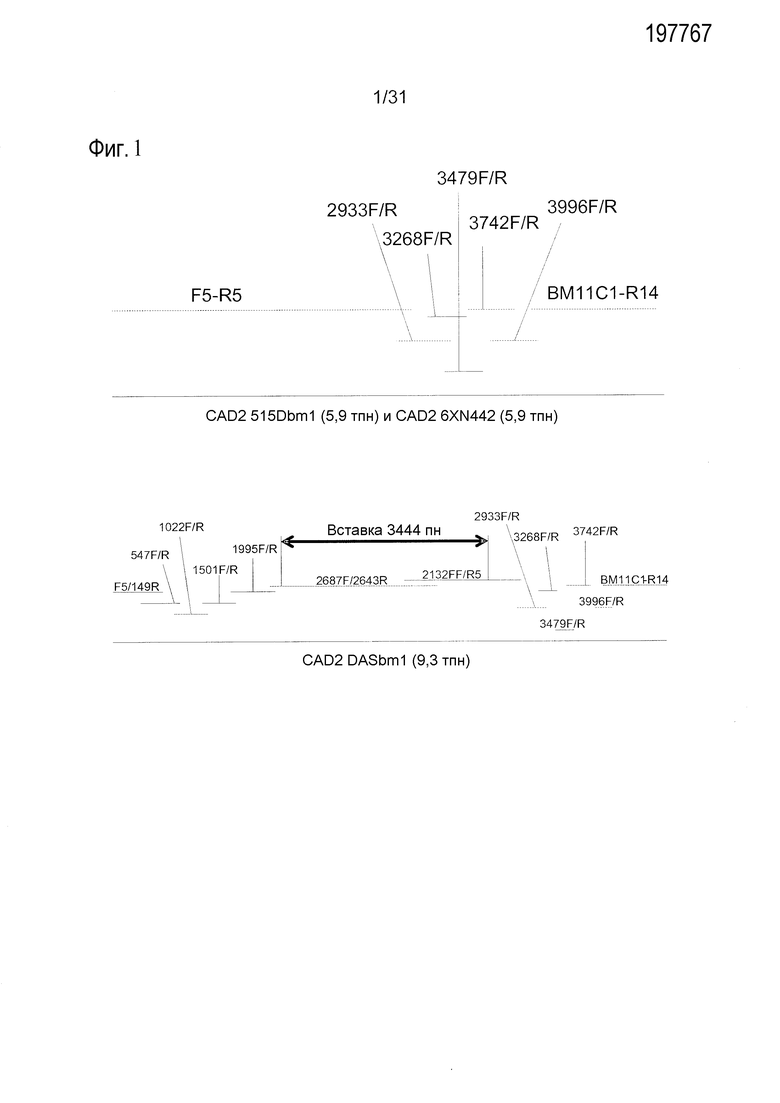
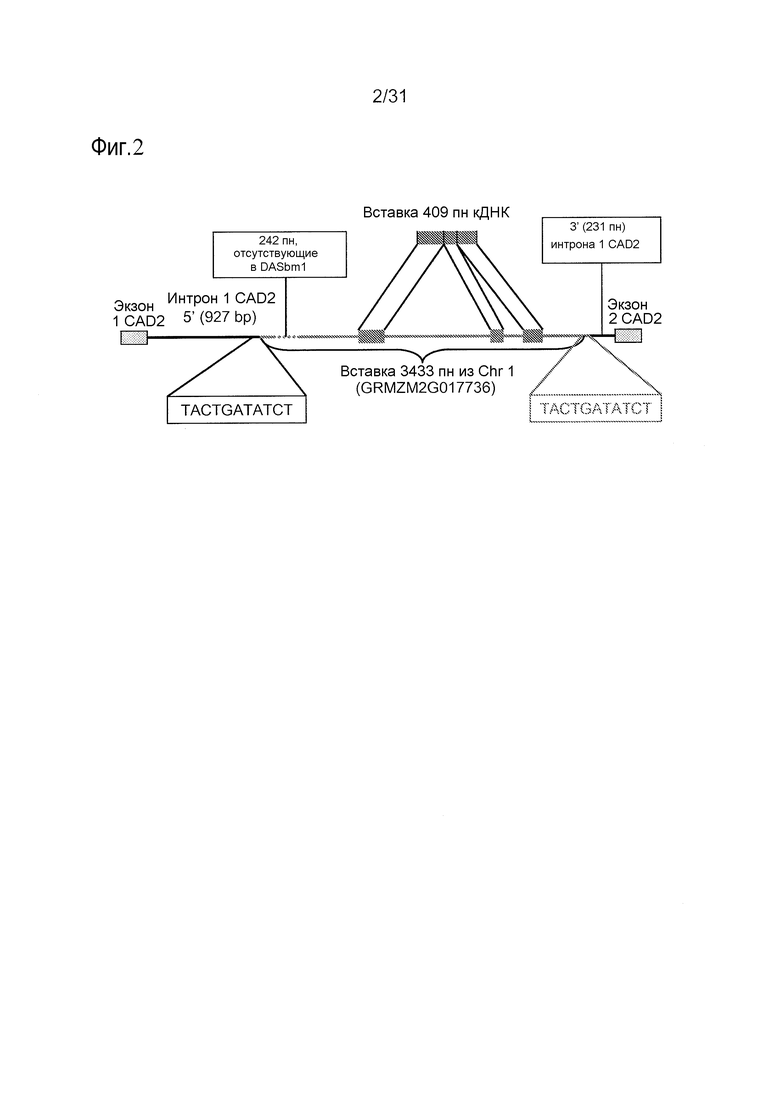
























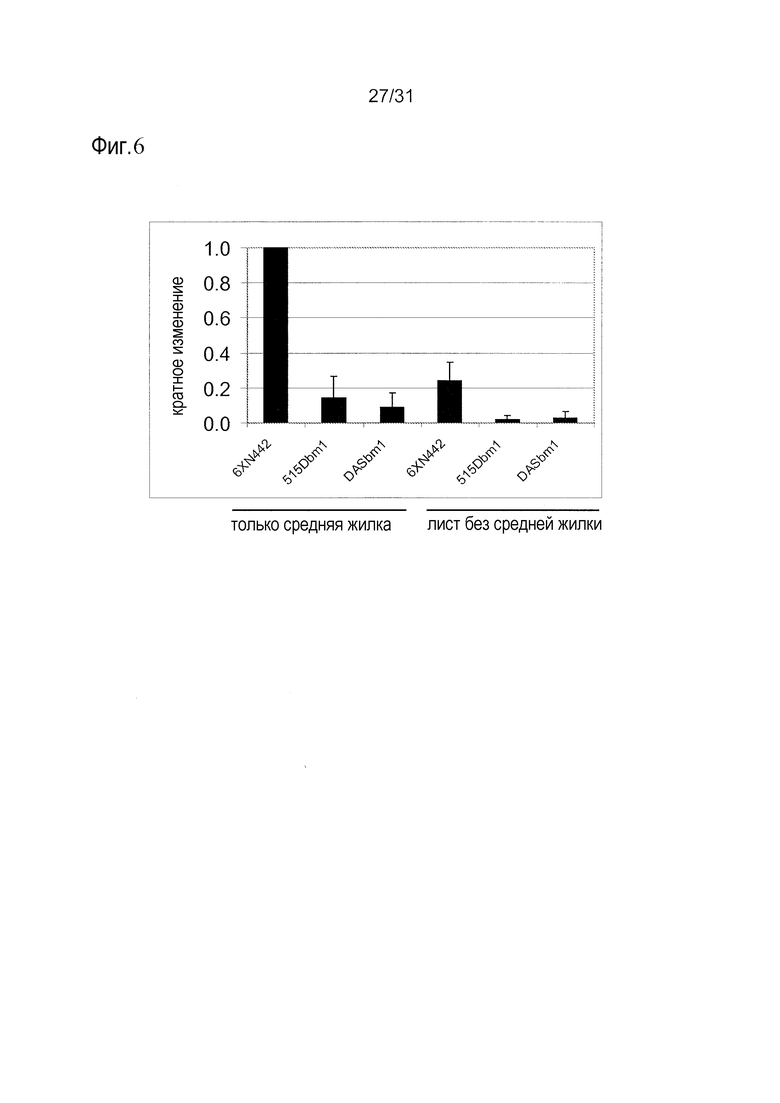


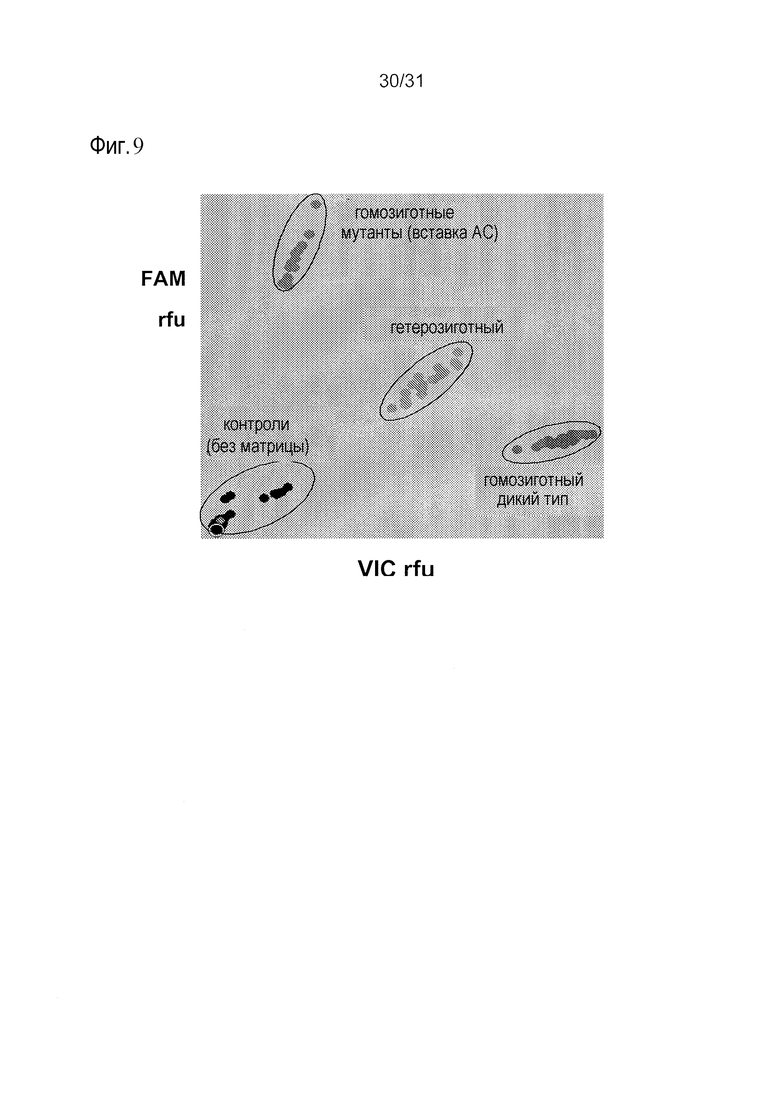

Изобретение относится к области биохимии, в частности к трансгенному растению, имеющему сниженное количество лигнина по сравнению с диким растением того же вида, где растение включает полинуклеотид, кодирующий мутантный белок циннамилалкогольдегидрогеназы 2 (CAD2), а также к способу его идентификации. Также раскрыт способ получения генетически сконструированного растения с фенотипом коричневой жилки, включающий введение в растение нуклеотидной последовательности, кодирующей мутантный белок CAD2, способ откорма животного, питающегося силосом, включающий откорм животного силосом на основе кукурузы, имеющей сниженное количество лигнина, а также способ введения в растение гена мутантного белка CAD2 кукурузы. Изобретение также относится к конечному рациону для мясных пород домашних быков, включающему силос на основе кукурузы, имеющей сниженное количество лигнина. Изобретение позволяет эффективно получать трансгенное растение, имеющее сниженное количество лигнина по сравнению с диким растением того же вида. 7 н. и 15 з.п. ф-лы, 10 ил., 6 табл., 4 пр.
1. Трансгенное растение, имеющее сниженное количество лигнина по сравнению с диким растением того же вида, где растение включает полинуклеотид, кодирующий мутантный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный белок CAD2 представляет собой усеченный белок CAD2, не имеющий NADPH-связывающего и C-концевого каталитического доменов, и где белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25.
2. Растение по п. 1, где растением является Zea mays.
3. Способ идентификации растения, включающего мутантный ген циннамилалкогольдегидрогеназы 2 (CAD2), где способ включает:
скрининг молекул нуклеиновых кислот, выделенных из растений, относительно полинуклеотида, кодирующего мутантный усеченный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный усеченный белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25.
4. Способ по п. 3, где скрининг осуществляется с помощью полимеразной цепной реакции с использованием по меньшей мере двух праймеров, выбранных из группы, состоящей из SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 52, SEQ ID NO: 54, SEQ ID NO: 55, SEQ ID NO: 47, SEQ ID NO: 49 и SEQ ID NO: 50.
5. Растение по п. 1, где растение имеет фенотип коричневой пигментации средней жилки.
6. Растение по п. 2, где растение Zea mays обладает фенотипом коричневой пигментации средней жилки (bm1 фенотип).
7. Способ по п. 3, где выделенными молекулами нуклеиновых кислот являются геномные молекулы ДНК из растений кукурузы F1, полученных путем скрещивания растения кукурузы, имеющего фенотип bm1, с растением кукурузы, не имеющим фенотипа bm1, с получением растений кукурузы F1; где идентифицированное растение кукурузы F1 имеет фенотип (bm1) коричневой пигментации средней жилки.
8. Способ получения генетически сконструированного растения с фенотипом коричневой жилки, включающий введение в растение нуклеотидной последовательности, кодирующей мутантный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный белок CAD2 представляет собой усеченный белок CAD2, не имеющий NADPH-связывающего и С-концевого каталитического доменов, и где белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25.
9. Способ по п. 8, где растением является Zea mays.
10. Способ по п. 9, где нуклеотидную последовательность вводят в растение Zea mays путем скрещивания с Zea mays растения для получения растения F1 поколения, включающего нуклеотидную последовательность.
11. Способ по п. 8, где нуклеотидную последовательность вводят в растение с помощью генетической трансформации.
12. Способ по п. 11, где нуклеотидная последовательность стабильно интегрирована в геном растения.
13. Способ по п. 12, где растением является Zea mays.
14. Способ откорма животного, питающегося силосом, включающий:
откорм животного силосом на основе кукурузы, имеющей сниженное количество лигнина по сравнению с растением кукурузы дикого типа, где силос содержит нуклеотидную последовательность, кодирующую мутантный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный белок CAD2 представляет собой усеченный белок CAD2, не имеющий NADPH-связывающего и С-концевого каталитического доменов, и где белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25.
15. Способ по п. 14, где животное, питающееся силосом, является жвачным.
16. Способ по п. 15, где животное, питающееся силосом, является коровой.
17. Способ по п. 14, где силос, произведенный из растения кукурузы по п. 6, составляет более 15% сухого вещества в рационе животного.
18. Способ по п. 17, где силос, произведенный из растения кукурузы по п. 6, составляет по меньшей мере приблизительно 25% сухого вещества в рационе животного.
19. Конечный рацион для мясных пород домашних быков, включающий силос на основе кукурузы, имеющей сниженное количество лигнина по сравнению с растением кукурузы дикого типа, где силос содержит нуклеотидную последовательность, кодирующую мутантный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный белок CAD2 представляет собой усеченный белок CAD2, не имеющий NADPH-связывающего и С-концевого каталитического доменов, и где белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25.
20. Способ введения в растение мутантного белка циннамилалкогольдегидрогеназы 2 (CAD2) кукурузы, где способ включает:
(a) осуществление анализа геномной ДНК первого растения и геномной ДНК второго растения относительно полинуклеотида, кодирующего мутантный усеченный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный усеченный белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25;
(b) проведение полового скрещивания первого и второго растения с получением популяции-потомка;
(c) осуществление анализа популяции-потомка на присутствие полинуклеотида, кодирующего мутантный усеченный белок CAD2;
(d) осуществление обратного скрещивания представителя популяции-потомка, который содержит полинуклеотид, кодирующий мутантный усеченный белок CAD2, с первым или вторым растением для получения следующего поколения популяции;
(e) выявление присутствия у представителя следующего поколения популяции желаемого признака от первого или второго растения и полинуклеотида, кодирующего мутантный усеченный белок CAD2; и
(f) в случае отсутствия у представителя следующего поколения популяции желаемого признака от первого или второго растения и полинуклеотида, кодирующего мутантный усеченный белок CAD2, повторение стадий (d) и (е) до выявления у представителя желаемых признаков от первого или второго растения и полинуклеотида, кодирующего мутантный усеченный белок CAD2.
21. Способ по п. 20, где представителя популяции-потомка каждого поколения, полученного на каждой стадии скрещивания и обратного скрещивания, анализируют относительно присутствия полинуклеотида, кодирующего мутантный усеченный белок CAD2.
22. Способ введения в организм-хозяин гена мутантного белка циннамилалкогольдегидрогеназы 2 (CAD2) кукурузы путем генетической трансформации, где способ включает:
осуществление анализа геномной ДНК растения кукурузы для выявления в растении кукурузы мутантного CAD2 гена, кодирующего мутантный усеченный белок циннамилалкогольдегидрогеназы 2 (CAD2), где мутантный усеченный белок CAD2 имеет аминокислотную последовательность SEQ ID NO: 3 или SEQ ID NO: 25;
выделение мутантного CAD2 гена из геномной ДНК растения кукурузы;
введение мутантного CAD2 гена в организм-хозяин и
осуществление анализа ДНК организма-хозяина для выявления в организме-хозяине мутантного CAD2 гена, кодирующего мутантный усеченный белок циннамилалкогольдегидрогеназы 2 (CAD2).
| WO2006076423 A2, 20.07.2006 | |||
| US2007209085 A1, 06.09.2007 | |||
| HALPIN C | |||
| et al., Brown-midrib maize (bm1)--a mutation affecting the cinnamyl alcohol dehydrogenase gene, Plant J., 1998, Vol.14, N.5, pp.545-553 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ РАСТЕНИЙ КУКУРУЗЫ | 2007 |
|
RU2351120C1 |
Авторы
Даты
2017-04-28—Публикация
2012-01-03—Подача