ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к бактериальным патогенам. Более конкретно, изобретение частично относится к секретируемым белкам бактериальных патогенов и способам их применения.
УРОВЕНЬ ТЕХНИКИ
Escherichia coli представляет собой исключительно изменчивый организм. В дополнение к тому, что она является представителем нормальной кишечной флоры, штаммы E. coli могут также вызывать инфекции мочевого пузыря, менингит и диарею. Вызывающие диарею E. coli включают, по меньшей мере, пять типов E. coli, которые вызывают различные симптомы, варьирующие от холероподобной диареи до острого колита. Каждый тип вызывающих диарею E. coli обладает конкретным набором факторов вирулентности, включая адгезины, инвазины и/или токсины, которые отвечают за индукцию конкретного типа диареи.
Энтеропатогенная E. coli (EPEC) представляет собой преобладающую причину детской диареи во всем мире. Заболевание EPEC характеризуется водянистой диареей различной тяжести, с рвотой и лихорадкой, часто сопровождающимися потерей жидкости. В дополнение к отдельным вспышкам в дневных медицинских и детских учреждениях в развивающихся странах EPEC представляет серьезную угрозу здоровью младенцев (<6 месяцев). По всему миру EPEC представляет собой ведущую причину опосредованной бактериями диареи у младенцев, и, по оценкам, EPEC является причиной гибели нескольких сотен тысяч детей в год.
Энтерогеморрагическая E. coli, также называемая продуцирующей шигатоксин E. coli (STEC) или продуцирующей веротоксин E. coli (VTEC), вызывает более тяжелую диарею, чем EPEC (энтероколит) и примерно в 10% случаев данное заболевание прогрессирует в заболевание почек - гемолитико-уремический синдром (HUS), который зачастую является фатальным. EHEC O157:H7 представляет собой наиболее распространенный серотип в Канаде и Соединенных Штатах, и ассоциирован с загрязнением пищи и воды (3). Другие серотипы EHEC также вызывают значительные проблемы в Азии, Европе и Южной Америке, и, в меньшей степени, в Северной Америке. EHEC колонизирует крупный рогатый скот и вызывает повреждения A/E, но не вызывает заболевание у взрослых животных, и вместо этого микроорганизмы выбрасываются в окружающую среду. Однако это вызывает серьезные проблемы здравоохранения, поскольку для инфицирования людей достаточно относительно небольшого количества EHEC.
В отличие от диареи другого происхождения, вызываемой E. coli, например, вызываемых E. coli, образующими энтеротоксины, диарея, вызванная EHEC и EPEC, не опосредована токсином. Вместо этого, EPEC и EHEC связываются с поверхностью кишечника (EPEC с тонким кишечником, EHEC с толстым кишечником) и вызывают характерный гистологический очаг повреждения, называемый очагом прикрепления и сглаживания (A/E) (8).
Очаги A/E отмечаются растворением поверхности ресничного эпителия кишечника и потерей эпителиальных микроворсинок (сглаживание) в участках прикрепления бактерий. Связавшись, бактерии остаются на чашевидных выступах или ложах. В основе данного ложа в эпителиальной клетке лежат некоторые компоненты цитоскелета, включая актин и ассоциированные с актином цитоскелетные белки. Образование очагов A/E и богатых актином лож под прикрепленными бактериями является гистопатологическим признаком A/E патогенов (1, 2).
Данная патология может имитироваться на культивируемых клетках in vitro, и образование лож может наблюдаться путем флуоресцентного окрашивания актина (2, 11). Образование A/E-очагов может быть ответственным за разрушение ресничного слоя и микроворсинок, секреции жидкости и диареи.
EPEC и EHEC принадлежат к семейству A/E-патогенов, включая несколько EPEC-подобных животных патогенов, которые вызывают заболевания у кроликов (REPEC), свиней (PEPEC) и мышей (Citrobacter rodentium). Данные патогены содержат островки патогенности (PAI), которые кодируют специализированные системы секреции и секретируемые факторы вирулентности, критичные в плане развития заболевания. Гены, требуемые для образования A/E-очагов, как полагают, кластеризованы вместе в один хромосомный островок патогенности, известный как локус сглаживания энтероцитов (LEE), которые включают регуляторные элементы, систему секреции III типа (TTSS), секретируемые эффекторные белки и связанные с ними шапероны (4-8).
LEE содержит 41 ген, что делает его одним из наиболее сложных PAI. Основная функция LEE TTSS представляет собой доставку эффекторов в клетки-хозяина, где они нарушают функции клеток-хозяев и опосредуют заболевание (9, 10, 34). Идентифицировано пять кодируемых LEE эффекторов (Tir, EspG, EspF, Map и EspH) (35-40). Tir (перемещаемый рецептор интимина) перемещается в клетки-хозяина, где он связывается с цитоскелетными и сигнальными белками хозяина и инициирует полимеризацию актина в участке прикрепления бактерии (31, 44), что приводит к образованию ложеобразных актиновых структур, лежащих под прикрепленными бактериями, которые непосредственно взаимодействуют с внеклеточной петлей Tir посредством белка внешней мембраны бактерии интимина. CesT играет роль в качестве шаперона для стабильности и секреции Tir (18, 19).
В А/Е-патогенах охарактеризованы четыре других кодируемых в LEE TTSS-перемещаемых эффектора: EspH усиливает удлинение актиновых лож (40); EspF играет роль в разъединении плотных контактов между кишечными эпителиальными клетками (38); EspG родственен связанному с микротрубочками Shigella эффектору VirA (36, 55); и Map локализован в митохондриях (37), но также играет роль в динамике актина (48). Ler (кодируемый в LEE регулятор) является единственным идентифицированным кодируемым в LEE регулятором.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Изобретение, в частности, основано на идентификации нескольких новых общих секретируемых белков A/E-патогенов.
В одном аспекте изобретение относится к композициям, включающим полипептид или его фрагмент, или его вариант, или надосадочную жидкость культуры клеток, включающую такой полипептид, где по существу чистый полипептид включает аминокислотную последовательность, по существу идентичную последовательности любой одной или нескольким из SEQ ID NO: 22-43, 59, или 73-84, или их фрагментам, или вариантам. Изобретение также относится к композициям, включающим молекулу нуклеиновой кислоты, где молекула нуклеиновой кислоты содержит нуклеотидную последовательность, по существу идентичную любой одной или нескольким последовательностям из SEQ ID NO: 1-21 или 60-72; и к композициям, включающим нуклеотидную последовательность, кодирующую полипептид, по существу идентичный любой одной или нескольких последовательностей из SEQ ID NO: 22-43, или их фрагментам. Композиции могут дополнительно включать физиологически приемлемый носитель, или дополнительно включать адъювант. Композиции могут также включать полипептид или молекулу нуклеиновой кислоты, такую как EspA, EspB, EspD, EspP, Tir, шигатоксин 1, шигатоксин 2, или интимин. Полипептиды или молекулы нуклеиновой кислоты могут быть по существу чистыми.
В альтернативных аспектах изобретение также относится к бактериям или к их препаратам, где бактерия включает мутацию в гене, таком как nleA, nleB, nleC, nleD, nleE, nleF, nleG, nleH, или в их гомологе, или включает мутацию в бактериальном геноме в нуклеотидной последовательности, которая является по существу идентичной в отношении SEQ ID NO: 1-21 или 60-72. В некоторых вариантах осуществления бактерия может представлять собой A/E-патоген, например энтерогеморрагическую E. coli (EHEC; например, EHEC О157:H7 или EHEC О157:NM), энтеропатогенную E. coli (EPEC; например, EPEC О127:H6) или Citrobacter rodentium. В некоторых вариантах осуществления мутация может ослаблять вирулентность или может происходить в нуклеотидной последовательности в геноме A/E-патогена, которая по существу идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-21 или 60-72. Бактерия может предоставляться в виде композиции, в комбинации с адъювантом. В некоторых вариантах осуществления бактерия может быть живой. В некоторых вариантах осуществления бактерия может быть убитой. Способ введения может быть пероральным или парентеральным.
В альтернативных вариантах изобретение также относится к способу выявления A/E-патогена в образце путем предоставления образца; и выявления нуклеотидной последовательности, по существу идентичной последовательности, выбранной из SEQ ID NO: 1-21 или 60-72, или ее фрагменту, или варианту; нуклеотидной последовательности, кодирующей полипептидную последовательность, по существу идентичную последовательности, выбранной из SEQ ID NO: 22-43, 59, или 73-84, или полипептида, включающего аминокислотную последовательность, по существу идентичную последовательности, выбранной из SEQ ID NO: 22-43, 59 или 73-84, или ее фрагменту, или варианту, где присутствие нуклеотидной последовательности или аминокислотной последовательности указывает на присутствие A/E-патогена в образце (например, в яйце, фекалиях, крови или кишечнике). Выявление может включать в себя контакт нуклеотидной последовательности с зондом или праймером, по существу идентичным последовательности, выбранной из группы, состоящей из SEQ ID NO: 1-21 или 60-72, или нуклеотидной последовательности, кодирующей полипептидную последовательность, по существу идентичную последовательности, выбранной из группы, состоящей из SEQ ID NO: 22-43, 59, или 73-84, или их части, или может включать в себя контакт аминокислотной последовательности с антителом, которое специфически связывается с последовательностью, выбранной из группы, состоящей из SEQ ID NO: 22-43, 59, или 73-84, или его фрагментом, или вариантом.
В альтернативных вариантах изобретение также относится к способам индукции иммунного ответа против A/E-патогена или его компонента, или для снижения колонизации A/E-патогеном или выделения A/E-патогена из животного (например, человека; жвачного, такого как овцы, козы, крупный рогатый скот, и т.д.; или любого другого животного, такого как свиньи, кролики, домашняя птица (например, утки, куры, индейки) и т.д.), путем идентификации животного, инфицированного A/E-патогеном или имеющего риск инфицирования им; и введения животному эффективного количества композиции, включающей полипептид, содержащий аминокислотную последовательность, по существу идентичную последовательности любой одной или нескольких SEQ ID NO: 22-43, 59, или 73-84; нуклеотидную последовательность, кодирующую полипептидную последовательность, по существу идентичную последовательности, выбранной из SEQ ID NO: 22-43, 59, или 73-84; молекулу нуклеиновой кислоты, включающую нуклеотидную последовательность, по существу идентичную последовательности любой одной или нескольких из SEQ ID NO: 1-21 или 60-72; или надосадочную жидкость клеточной культуры, содержащую такие полипептиды, что, таким образом, вызывает иммунный ответ или снижает колонизацию A/E-патогеном или выделение A/E-патогена из животного.
В альтернативных аспектах изобретение также относится к способу ослабления вирулентности A/E-патогена, путем предоставления A/E-патогена; и мутации гена, такого как nleS, nleB, nleC, nleD, nleE, nleF, nleG, или nleH, или их гомолога в A/E-патогене, или мутации одной или нескольких нуклеотидных последовательностей в геноме A/E-патогена, где нуклеотидная последовательность выбрана из SEQ ID NO: 1-21 или 60-72, с ослаблением за счет этого вирулентности.
В альтернативных аспектах изобретение также относится к способу скрининга соединения, которое ослабляет вирулентность A/E-патогена, путем предоставления системы (например, клетки, например, клетки EHEC, EPEC или C. rodentium, экспериментального животного или системы in vitro), включающей: полипептид, содержащий аминокислотную последовательность, по существу идентичную последовательности любой одной или нескольких из SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту; нуклеотидную последовательность, кодирующую полипептидную последовательность, по существу идентичную последовательности, выбранной из SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту; или молекулу нуклеиновой кислоты, включающую нуклеотидную последовательность, по существу идентичную любой одной или нескольких последовательностей из SEQ ID NO: 1-21, или 60-72, или их варианту, или фрагменту; предоставления тестируемого соединения; и определения того, модулирует ли тестируемое соединение экспрессию, секрецию или биологическую активность полипептида или молекулы нуклеиновой кислоты, где изменение, например снижение экспрессии, секреции, или биологической активности полипептида или молекулы нуклеиновой кислоты, указывает на соединение, которое ослабляет вирулентность A/E-патогена.
В альтернативных вариантах изобретение также относится к способу продукции фактора вирулентности A/E-патогена путем предоставления рекомбинантной клетки, включающей полипептид, содержащий аминокислотную последовательность, по существу идентичную любой из SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту; нуклеотидную последовательность, кодирующую полипептидную последовательность, по существу, идентичную последовательности, выбранной из группы, состоящей из SEQ ID NO: 22-43, 59, или 73-84, или их фрагмента, или варианта; или молекулу нуклеиновой кислоты, включающей нуклеотидную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагменту, или варианту; выращивания рекомбинантной клетки в условиях, которые обеспечивают экспрессию и/или секрецию полипептида, и, необязательно, выделения полипептида. В некоторых вариантах осуществления полипептид может секретироваться из клетки.
В альтернативных вариантах изобретение также относится к способу лечения или профилактики инфекции, вызываемой A/E-патогеном, путем идентификации млекопитающего, имеющего инфекцию, вызванную A/E-патогеном или имеющего риск такой инфекции; и введения млекопитающему эффективного количества соединения, которое ослабляет вирулентность A/E-патогена, где соединение ингибирует экспрессию или секрецию полипептида, включающего аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту. В некоторых вариантах осуществления соединение может представлять собой антисмысловую молекулу нуклеиновой кислоты, комплементарную в отношении нуклеотидной последовательности, по существу идентичной любой из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагменту, или варианту, или может представлять собой siРНК.
В альтернативных вариантах изобретение также относится к рекомбинантному полипептиду, включающему аминокислотную последовательность, по существу идентичную последовательности SEQ ID NO: 22-43, 59, или 73-84, или к выделенной молекуле нуклеиновой кислоты, включающей нуклеотидную последовательность, по существу идентичную последовательности SEQ ID NO: 1-21 или 60-72; и/или к вектору, включающему такие нуклеотидные последовательности; и/или к клетке-хозяину (например, к A/E-патогену, такому как энтерогеморрагическая E. coli (EHEC), энтеропатогенная E. coli (EPEC) или Citrobacter rodentium), включающей такие векторы. Вектор может иметь способность интегрироваться в геном A/E-патогена или может не обладать такой способностью.
В альтернативных аспектах изобретение также относится к применению композиций, бактерий, полипептидов, или молекул нуклеиновой кислоты по изобретению, для получения лекарственного средства для индукции иммунного ответа против A/E-патогена, или его компонента, или для снижения выделения, или колонизации A/E-патогена у животного.
В альтернативных аспектах изобретение также относится к наборам, включающим реагент для выявления в образце A/E-патогена и вкладыш в упаковку с инструкциями для выявления в образце A/E-патогена. Реагент может включать в себя зонд, или праймер-зонд, или праймер, по существу идентичный в отношении: нуклеотидной последовательности, выбранной из группы, состоящей из одной или нескольких из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагмента, или варианта, или нуклеотидной последовательности, кодирующей полипептид, по существу идентичный одной или нескольким последовательностям SEQ ID NO: 22-43, 59, 73-84, или их фрагменту, или варианту, или антитело, которое специфически связывается с последовательностью, выбранной из группы, состоящей из одной или нескольких последовательностей из SEQ ID NO: 22-43, 59, 73-84, или их фрагмента, или варианта.
«A/E-патоген» представляет собой патоген, например патогенную бактерию E. coli, который может связываться с поверхностями кишечника животного, например млекопитающего, например крупного рогатого скота, овец, коз, свиней, кроликов, собак, кошек, и т.д., или видов птиц, например кур, уток, индеек, и т.д., и вызывать появление характерного гистологического очага повреждения, называемого очагом прикрепления и сглаживания (A/E) (8). В целом, инфекция, вызванная A/E-патогеном, может приводить к диарее, энтероколиту, заболеванию почек (например, к гемолитико-уремическому синдрому).
Однако инфекция, вызываемая A/E-патогеном, не обязательно проявляется в симптомах заболевания; млекопитающее-хозяин, инфицированное A/E-патогеном, может являться носителем патогена и оставаться здоровым и не больным. Таким образом, млекопитающие, инфицированные A/E-патогеном или имеющие риск такого инфицирования, включают животных, например сельскохозяйственных животных, таких как домашняя птица, например кур, индеек, уток, или жвачные, например крупный рогатый скот, овцы, козы, и т.д., или других сельскохозяйственных животных, например свиней, у которых не проявляются симптомы заболевания, а также включают людей, чувствительных к тяжелому кишечному заболеванию в результате инфекции, вызываемой A/E-патогеном.
Неограничивающие примеры A/E-патогенов включают энтерогеморрагическую E. coli (EHEC) (также известную как продуцирующая шигатоксин E. coli (STEC) или продуцирующая веротоксин E. coli (VTEC)), например серотипы EHEC 0157 (например, EHEC0157:H7, геномная последовательность которой описана в инвентарных номерах AE005594, AE005595, AP002566, AE 005174, NC_002695 или NC_002655) или 0158, 05, 08, 018, 026, 045, 048, 052, 055, 075, 076, 078, 084, 91, 0103, 0104, 0111, 0113, 0114, 0116, 0118, 0119, 0121, 0125, 028, 0145, 0146, 0163, 0165; энтеропатогенную E. coli (EPEC); а также патогенную E. coli, инфицирующую мышей (например, Citrobacter rodentium); свиней; овец; собак; и других млекопитающих.
Многие штаммы A/E-патогенов коммерчески доступны, например, посредством American Type Culture Collection (ATCC), Manassus, Виргиния, США. A/E-патогены могут также выделяться из инфицированных субъектов, например, непосредственным высеванием на сорбитный агар MacConkey, дополненный цефиксимом и теллуритом, или путем иммуномагнитного обогащения с последующим высеванием на ту же среду (72, 107, 108).
«Белок», «пептид» или «полипептид» представляет собой любую цепь из двух или нескольких аминокислот, включающих встречающие в природе или неприродные аминокислоты или аналоги аминокислот, вне зависимости от посттрансляционных модификаций (например, гликозилирования или фосфорилирования). «Аминокислотная последовательность», «полипептид», «пептид» или «белок» по изобретению могут включать пептиды или белки, которые имеют аномальные связи, перекрестные связи или концевое кэпирование, непептидные связи или альтернативные модифицирующие группы. Такие модифицированные пептиды также входят в объем изобретения. Термин «модифицирующие агенты», как подразумевается, включает структуры, непосредственно присоединенные к пептидной структуре (например, ковалентным присоединением), а также те, которые непрямым образом присоединены к пептидной структуре (например, путем стабильной нековалентной ассоциации или путем ковалентного присоединения к дополнительным аминокислотным остаткам, или их миметики, аналоги или производные, которые могут фланкировать центральную пептидную структуру). Например, модифицирующая группа может присоединяться к N-концу или к С-концу пептидной структуры или к области пептида или пептидомиметика, фланкирующего центральный домен.
Альтернативно, модифицирующая группа может присоединяться к боковой цепи, по меньшей мере, одного аминокислотного остатка пептидной структуры или к области пептида или пептидомиметика, фланкирующего центральный домен (например, через эпсилон-аминогруппу остатка(-ов) лизина, через карбоксигруппу остатка(-ов) аспарагиновой кислоты или остатка(-ов) глутаминовой кислоты, через гидроксигруппу остатка(-ов) тирозина, остатка(-ов) серина или остатка(-ов) треонина или другой подходящей реакционноспособной группы боковой цепи аминокислоты). Модифицирующие группы, ковалентно связанные с пептидной структурой, могут присоединяться посредством и с использованием способов, хорошо известных в данной области, для связывания химических структур, включающих, например, связи амида, алкиламино, карбамата или мочевины.
Термины «нуклеиновая кислота» или «молекула нуклеиновой кислоты» охватывают РНК (плюс- и минус-цепи) и ДНК, включающую кДНК, геномную ДНК, и синтетическую (например, химически синтезированную) ДНК. Нуклеиновая кислота может быть двухцепочечной или одноцепочечной. Когда нуклеиновая кислота одноцепочечная, она может являться смысловой цепью или антисмысловой цепью. Молекула нуклеиновой кислоты может представлять собой любую цепь из двух или большего числа ковалентно связанных нуклеотидов, включая встречающиеся в природе или неприродные нуклеотиды, или аналоги или производные нуклеотидов. «РНК» означает последовательность двух или большего числа ковалентно связанных, встречающихся в природе или модифицированных рибонуклеотидов. Одним из примеров модифицированной РНК, включенной в данный термин, является фосфотиоатная РНК. Под «ДНК» подразумевается последовательность двух или большего числа ковалентно связанных, встречающихся в природе или модифицированных рибонуклеотидов. Под «кДНК» подразумевается комплементарная или копийная ДНК, продуцированная с РНК-матрицы под действием РНК-зависимой ДНК-полимеразы (обратной транскриптазы). «Клон кДНК» означает дуплексную последовательность ДНК, комплементарную интересующей молекуле РНК, которая включена в клонирующий вектор. Под «комплементарностью» подразумевается, что две нуклеиновые кислоты, например ДНК или РНК, содержат достаточное число нуклеотидов, которые способны образовывать пары оснований Уотсона-Крика, образуют область двухцепочечности двух нуклеиновых кислот. Таким образом, аденин в одной цепи ДНК или РНК образует пару с тимином в противоположной комплементарной цепи ДНК или с урацилом в противолежащей комплементарной цепи РНК. Следует понимать, что каждый нуклеотид в молекуле нуклеиновой кислоты не обязательно должен образовывать точную пару оснований Уотсона-Крика с нуклеотидом в противолежащей комплементарной цепи с образованием дуплекса. Молекула нуклеиновой кислоты «комплементарна» в отношении другой молекулы нуклеиновой кислоты, если она гибридизуется, в условиях высокой жесткости, со второй молекулой нуклеиновой кислоты.
Используемый здесь термин «надосадочная жидкость клеточной культуры» в основном относится к надосадочной жидкости, полученной в результате культивирования бактерии или другого организма (например, дрожжей) или клетки (например, клетки насекомых), которая способна секретировать один или несколько полипептидов, включающих аминокислотную последовательность, по существу, идентичную любой из последовательностей SEQ ID NO: 22-43, 59, 73-84, или их фрагменту, или варианту, или их иммуногенной части, в клеточную культуральную среду. В некоторых вариантах осуществления надосадочная жидкость культуры клеток является по существу чистой, т.е., по существу, лишенной бактериальных клеток или лизата таких клеток.
В некоторых вариантах осуществления надосадочная жидкость клеточной культуры также может содержать один или несколько из полипептидов EspA, EspB, EspD, Tir, интимина, шигатоксина 1 или 2, или EspP, или их фрагментов, или агрегатов.
Бактерия может представлять собой A/E-патоген, например EHEC, EPEC или Citrobacter rodentium, которая, в некоторых вариантах осуществления может модифицироваться или мутироваться, или преимущественно экспрессировать или секретировать описанные здесь белки, или может представлять собой некоторую другую бактерию, например непатогенную бактерию, например непатогенную E. coli, такую как HB101, или не-A/E-патоген, который был модифицирован или мутирован, например, рекомбинантным или другим способом, так что он стал секретировать один или несколько описанных здесь белков, например полипептид, включающий аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, 59, 73-84, или их фрагменту, или варианту, или его иммуногенную часть, в клеточную культуральную среду. В некоторых вариантах осуществления бактерия не является EHEC или EPEC.
В некоторых вариантах осуществления, в которых бактерия является A/E-патогеном, она также может нести дальнейшую модификацию, которая ослабляет ее способность экспрессировать или секретировать полипептид (например, EspA, EspB, EspD, Tir, интимин, шигатоксин 1 или 2, или EspP), который в норме будет секретировать его в отсутствие модификации. В некоторых вариантах осуществления другой организм (например, дрожжи) или клетка (например, клетка насекомого) модифицированы или мутированы, например, рекомбинантным или другим способом, так что они секретируют один или несколько описанных здесь белков, например полипептид, включающий аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, или ее иммуногенной части, в клеточную культуральную среду.
Соединение является «по существу чистым» или «выделенным», когда оно отделено от компонентов, которые сопутствуют ему в природе. Обычно соединение является по существу чистым, когда оно составляет, по меньшей мере, 10%, 20%, 30%, 40%, 50%, или 60%, или, более обычно, по меньшей мере, 70%, 75%, 80%, 85%, 90%, 95% или 99% по массе от всего материала образца.
Таким образом, полипептид, который химически синтезирован или продуцирован рекомбинантной технологией, в основном по существу лишен ассоциированных с ним в природе компонентов. Полипептид также в основном является, по существу чистым, если он отделен от ассоциированных с ним в природе компонентов физическими методами, такими как центрифугирование, преципитация, колоночная хроматография, гель-электрофорез, ВЭЖХ, и т.д.
Молекула нуклеиновой кислоты, в основном, является по существу чистой или «выделенной», когда она не является непосредственно слитой (т.е. ковалентно связанной) с кодирующей последовательностью, к которой она обычно прилегает в имеющемся в природе геноме организма, из которого происходит ДНК по изобретению. Поэтому «выделенный» ген или молекула нуклеиновой кислоты, как подразумевается, означает ген или молекулу нуклеиновой кислоты, которая не фланкирована молекулами нуклеиновой кислоты, которые обычно (в природе) фланкируют ген или молекулу нуклеиновой кислоты (как в геномных последовательностях), и/или полностью или частично очищена от других транскрибируемых последовательностей (например, в библиотеке кДНК или РНК). Например, выделенная нуклеиновая кислота по изобретению может быть по существу выделена от комплексной клеточной среды, в которой он присутствует в природе. В некоторых случаях выделенный материал образует часть композиции (например, неочищенный экстракт содержит другие вещества), буферной системы или смеси реагентов.
В других обстоятельствах материал может очищаться до достаточной гомогенности, что, например, определяется путем электрофореза в полиакриламидном геле (PAGE) или колоночной хроматографии, такой как ВЭЖХ. Поэтому данный термин включает в себя, например, рекомбинантную нуклеиновую кислоту, введенную в вектор, такой как автономно реплицирующаяся плазмида или вирус; или в геномную ДНК прокариота или эукариота, или ту, которая существует в отдельной молекуле (например, фрагменте кДНК или геномной ДНК, продуцированной путем ПЦР или обработки рестрикционной эндонуклеазой), независимо от других последовательностей. Она также включает рекомбинантную нуклеиновую кислоту, которая является частью гибридного гена, кодирующего дополнительных полипептидных последовательностей. Предпочтительно, выделенная нуклеиновая кислота включает в себя, по меньшей мере, примерно 50, 80 или 90 процентов (на основе молярного соотношения) всех присутствующих видов макромолекул. Таким образом, выделенный ген или молекула нуклеиновой кислоты может включать ген или молекулу нуклеиновой кислоты, которая синтезирована химически или рекомбинантными способами. Рекомбинантные ДНК, содержащиеся в векторе, включены в используемое здесь определение «выделенный». Также выделенные молекулы нуклеиновой кислоты включают молекулы рекомбинантной ДНК в гетерологичных клетках-хозяевах, а также частично или по существу очищенные молекулы ДНК в растворе. Полученные in vivo и in vitro РНК-транскрипты молекул ДНК по настоящему изобретению также относятся к «выделенным» молекулам нуклеиновой кислоты. Такие выделенные молекулы нуклеиновой кислоты могут использоваться в производстве кодируемого полипептида, в качестве зонда для выделения гомологичных последовательностей (например, из других видов млекопитающих), для картирования гена (например, путем гибридизации in situ с хромосомами), или для выявления экспрессии гена в ткани (например, в человеческой ткани, такой как периферическая кровь), например, путем анализа нозерн-блоттингом.
По существу чистое соединение может быть получено, например, экстракцией из природного источника; экспрессией рекомбинантной молекулы нуклеиновой кислоты, кодирующей полипептидное соединение; или путем химического синтеза. Чистота может измеряться с использованием любого подходящего способа, такого как колоночная хроматография, гель-электрофорез, ВЭЖХ, и т.д.
По существу чистый препарат клетки, например бактериальной клетки, представляет собой препарат клетки, в которой контаминирующие клетки, которые не имеют требуемого мутантного генотипа, или не экспрессируют или не секретируют требуемый полипептид в подходящих количествах, составляют менее 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% общего количества клеток в препарате.
Различные гены и последовательности нуклеиновой кислоты по изобретению может представлять собой рекомбинантные последовательности. Термин «рекомбинантный» означает, что нечто подлежало рекомбинации, так что при ссылке на конструкцию нуклеиновой кислоты термин относится к молекуле, которая составлена последовательностями нуклеиновой кислоты, которые объединены вместе или продуцированы посредством способов молекулярной биологии. При ссылке термина «рекомбинантный» на белок или полипептидную молекулу данный термин означает, что белковая или полипептидная молекула экспрессирована с использованием рекомбинантной конструкции нуклеиновой кислоты, созданной посредством способов молекулярной биологии. При ссылке термина «рекомбинантный» на генетическую композицию данный термин относится к гамете или к потомству с новыми комбинациями аллелей, которые не присутствовали в исходных геномах. Конструкции рекомбинантной нуклеиновой кислоты могут включать нуклеотидную последовательность, которая лигирована с последовательностью нуклеиновой кислоты, с которой она не лигирована в природе или с которой она лигирована в природе в другом положении, или данная нуклеиновая кислота подвергается манипуляциям, приводящим к такому лигированию. Поэтому ссылка на конструкцию нуклеиновой кислоты как на «рекомбинантную» указывает на то, что молекула нуклеиновой кислоты подвергалась манипуляциям с использованием генной инженерии, т.е. за счет человеческого вмешательства.
Рекомбинантные конструкции нуклеиновой кислоты могут, например, вводиться в клетку-хозяина путем трансформации. Такие рекомбинантные конструкции нуклеиновой кислоты могут включать последовательности, происходящие из одного вида клеток-хозяев или из различных видов клеток-хозяев, которые могут выделяться и повторно вводиться в клетки вида хозяина. Последовательности рекомбинантных конструкций нуклеиновой кислоты могут становиться интегрированными в геном клетки-хозяина, в результате исходной трансформации клеток-хозяев, или в результате последующих событий рекомбинации и/или репарации.
Используемый здесь термин «гетерологичный» в отношении нуклеиновой кислоты или белка представляет собой молекулу, с которой манипулировали за счет человеческого вмешательства, так что она локализуется в месте, отличном от места, в котором она находится в природе. Например, последовательность нуклеиновой кислоты из одного вида может вводиться в геном другого вида, или последовательность нуклеиновой кислоты из одного геномного локуса может перемещаться в другой геномный или внехромосомный локус того же вида. Гетерологичный белок включает, например, белок, экспрессированный с гетерологичной кодирующей последовательности или белок, экспрессированный с рекомбинантного гена в клетке, которая в природе не экспрессирует данный белок.
«По существу идентичная» последовательность представляет собой аминокислотную или нуклеотидную последовательность, которая отличается от последовательности сравнения только одной или несколькими консервативными заменами, описанными выше, или одной или несколькими неконсервативными заменами, делециями или вставками, расположенными в тех положениях последовательности, которые не отменяют биологической функции аминокислотной молекулы или молекулы нуклеиновой кислоты. Такая последовательность может характеризоваться идентичностью, составляющей любое целое число от 10% до 99%, или, более конкретно, по меньшей мере, от 10%, 20%, 30%, 40%, 50%, 55% или 60%, или, по меньшей мере, 65%, 75%, 80%, 85%, 90%, или 95%, или, как минимум 96%, 97%, 98%, или 99%, в отношении аминокислотной последовательности или последовательности нуклеотидов, использованной для сравнения, с применением, например, программы Align (96) или FASTA. Для полипептидов длина последовательностей сравнения может составлять, по меньшей мере, 2, 5, 10, или 15 аминокислот, или, по меньшей мере, 20, 25, или 30 аминокислот. В альтернативных вариантах осуществления длина последовательностей сравнения может составлять, по меньшей мере, 35, 40, или 50 аминокислот, или свыше 60, 80, или 100 аминокислот. Для молекул нуклеиновой кислоты длина последовательностей сравнения может составлять, по меньшей мере, 5, 10, 15, 20, или 25 нуклеотидов, или, по меньшей мере, 30, 40, или 50 нуклеотидов. В альтернативных вариантах осуществления длина последовательностей сравнения может составлять, по меньшей мере, 60, 70, 80, или 90 нуклеотидов, или свыше 100, 200, или 500 нуклеотидов. Идентичность по последовательности может легко измеряться с использованием программного обеспечения для анализа последовательности (например, пакета программного обеспечения Sequence Analysis Software Package от Genetics Computer Group, University of Wisconsin Biotechnology Center, 1710 University Avenue, Madison, Wis. 53705, или программного обеспечения BLAST, доступного от National Library of Medicine, или как описано здесь).
Примеры подходящего программного обеспечения включают в себя программы Pile-up и PrettyBox. Такое программное обеспечение ищет сходные последовательности путем оценки гомологии различных замен, делеций и других модификаций.
Альтернативно или дополнительно, две последовательности нуклеиновой кислоты могут быть «по существу идентичными», если они гибридизуются в условиях высокой жесткости. В некоторых вариантах осуществления условия высокой жесткости представляют собой, например, условия, которые обеспечивают гибридизацию, сравнимую с гибридизацией, которая происходит с использованием ДНК-зонда, по меньшей мере, 500 нуклеотидов в длину, в буфере, содержащем 0,5M NaHPO4, pH 7,2, 7% SDS, 1 мМ EDTA и 1% BSA (фракция V), при температуре 65ºC, или в буфере, содержащем 48% формамида, 4,8× SSC, 0,2M Tris-Cl, pH 7,6, 1× раствор Denhardt, 10% декстран-сульфат, и 0,1% SDS, при температуре 42°C. (Это обычные жесткие условия для нозерн- или саузерн-гибридизации.) Гибридизации можно проводить в течение периода примерно от 20 до 30 минут, или примерно от 2 до 6 часов, или примерно от 10 до 15 часов, или свыше 24 часов или более. Условия гибридизации высокой жесткости обеспечивают успех многих способов, рутинно выполняемых молекулярными биологами, например ПЦР высокой жесткости, секвенирования ДНК, анализа одноцепочечного конформационного полиморфизма, и гибридизации in situ. В отличие от нозерн- и саузерн-гибридизации, данные способы рутинно выполняются с относительно короткими зондами (например, обычно 16 нуклеотидов или длиннее для ПЦР или секвенирования и примерно 40 нуклеотидов или более для гибридизации in situ). Условия высокой жесткости, используемые в данных способах, хорошо известны специалистам в области молекулярной биологии (61).
По существу идентичная последовательность может, например, представлять собой аминокислотную последовательность, которая является по существу идентичной любой из последовательностей SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту, или нуклеотидную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагменту, или варианту. В некоторых вариантах осуществления по существу идентичная последовательность может, например, представлять собой нуклеотидную последовательность, комплементарную любой из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагменту, или варианту, или последовательность, гибридизующуюся с ними. В некоторых вариантах осуществления по существу идентичная последовательность может быть получена из A/E-патогена.
«Зонд» или «праймер» представляет собой одноцепочечную молекулу ДНК или РНК с определенной последовательностью, которая может образовывать пару со второй молекулой ДНК или РНК, которая содержит комплементарную последовательность (мишень). Стабильность полученной в результате гибридной молекулы зависит от степени образования пар оснований, которое происходит, и подлежит влиянию параметров, таких как степень комплементарности между зондом и целевой молекулой, и степени жесткости условий гибридизации. Степень жесткости гибридизации подлежит влиянию параметров, таких как температура, концентрация соли и концентрация органических молекул, таких как формамид, и определяется способами, известными специалистам в данной области. Зонды или праймеры, специфичные в отношении описанных здесь последовательностей нуклеиновой кислоты или их частей, могут варьировать по длине на число нуклеотидов, равное любому целому числу, по меньшей мере, от 8 нуклеотидов до числа свыше 500 нуклеотидов, включая любое значение между ними, в зависимости от цели и условий применения зонда или праймера. Например, зонд или праймер может составлять, по меньшей мере, 8, 10, 15, 20 или 25 нуклеотидов в длину, или может составлять, по меньшей мере, 30, 40, 50 или 60 нуклеотидов в длину, или может составлять свыше 100, 200, 500 или 1000 нуклеотидов в длину. Зонды или праймеры, специфичные в отношении описанных здесь молекул нуклеиновой кислоты, может характеризоваться идентичностью, равной любому целому числу примерно от 10% до 99% или, в более общем плане, по меньшей мере, 10%, 20%, 30%, 40%, 50%, 55% или 60% или, по меньшей мере, 65%, 75%, 80%, 85%, 90%, или 95%, или как минимум 96%, 97%, 98%, или 99% в отношении описанных здесь последовательностей нуклеиновой кислоты, которая определена с использованием, например, программы Align (96).
Зонды или праймеры могут быть радиоактивно или нерадиоактивно меченными, с возможностью детектирования посредством способов, которые известны специалистам в данной области. Зонды или праймеры могут использоваться в способах, задействующих гибридизацию нуклеиновой кислоты, например, при секвенировании нуклеиновой кислоты, амплификации нуклеиновой кислоты путем полимеразной цепной реакции, анализе одноцепочечного конформационного полиморфизма (SSCP), анализе полиформизма длин рестрикционных фрагментов, саузерн-гибридизации, нозерн-гибридизации, гибридизации in situ, анализа сдвига электрофоретической подвижности (EMSA) и других способов, которые известны специалистам в данной области. Зонды или праймеры могут происходить из геномной ДНК или кДНК, например, путем амплификации, или из клонированных сегментов ДНК, или могут быть химически синтезированы.
«Мутация» включает какое-либо изменение последовательности ДНК, т.е. генома организма, по сравнению с родительским штаммом. Изменение может возникать спонтанно или за счет воздействия на организм мутагенного стимула, например мутагенного химиката, энергии, излучения, рекомбинантных способов, конъюгации или любых других способов, применяемых для изменения ДНК. Мутация может включать изменение в любой из описанных здесь нуклеотидных последовательностей или может включать изменение в нуклеотидной последовательности, кодирующей любой из описанных здесь полипептидов.
Мутация может «ослаблять вирулентность», если в результате мутации уровень вирулентности мутантной клетки снижается, по меньшей мере, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%, при сравнении с родительскими штаммами. Снижение вирулентности также может измеряться снижением, по меньшей мере, на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%, экспрессии полипептида, например полипептида, включающего аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, 59 или 73-84, или их фрагменту, или варианту, в мутантном штамме по сравнению с родительским штаммом. Вирулентность A/E-патогена может измеряться, как описано здесь, или, как известно в данной области. Снижение вирулентности может также измеряться изменением, по меньшей мере, на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%, биологической активности полипептида, например полипептида, включающего аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту, или варианту.
«Модулирование» или «модулирует» означает изменение, за счет повышения или снижения. Повышение или снижение может являться изменением на любое целое число от 10% до 90% или на любое целое число от 30% до 60% или может представлять собой свыше 100%, по сравнению с контролем, или образцом, или соединением сравнения.
«Тестируемое соединение» представляет собой любое встречающееся в природе химическое соединение или соединение искусственного происхождения. Неограничивающие примеры тестируемых соединений могут включать пептиды, полипептиды, синтетические органические молекулы, встречающиеся в природе органические молекулы и молекулы нуклеиновой кислоты. Тестируемое соединение может «конкурировать» с известным соединением, таким как любой из полипептидов или молекул нуклеиновой кислоты, описанных здесь, например, препятствуя вирулентности или препятствуя любой биологической реакции, индуцируемой известным соединением.
В общем тестируемое соединением может характеризоваться любым значением степени модулирования от 10% до 200% или свыше 500%, по сравнению с контрольным соединением. Например, тестируемое соединение может характеризоваться, по меньшей мере, любым положительным или отрицательным целым числом от 10% до 200% модулирования, или, по меньшей мере, любым положительным или отрицательным целым числом от 30% до 150% модулирования, или, по меньшей мере, любым положительным или отрицательным целым числом от 60% до 100% модулирования, или, по меньшей мере, любым положительным или отрицательным целым числом свыше 100% модулирования. Соединение, которое представляет собой отрицательный модулятор, в общем снижает модулирование относительно известного соединения, в то время как соединение, которое представляет собой позитивный модулятор, в общем, повышает модулирование относительно известного соединения.
«Вектор» представляет собой молекулу ДНК, происходящую, например, из плазмиды, бактериофага, или вируса млекопитающего или насекомого, или искусственной хромосомы, в которую может встраиваться молекула нуклеиновой кислоты, например, нуклеотидная последовательность, по существу идентичная любой из последовательностей SEQ ID NO: 1-21, или 60-72, или их фрагменту, или варианту. Вектор может содержать один или несколько уникальных сайтов рестрикции и может быть способен к автономной репликации в определенном хозяине, таким образом, что клонированная последовательность воспроизводится. Вектор может представлять собой экспрессирующий ДНК-вектор, т.е. любой автономный элемент, способный направлять синтез рекомбинантного полипептида, и таким образом может использоваться для экспрессии полипептида, например, полипептида, включающего аминокислотную последовательность, по существу идентичную любой из последовательностей SEQ ID NO: 22-43, 59 или 73-84, или их фрагменту, или варианту, в клетке-хозяине. Экспрессирующие ДНК-векторы включают бактериальные плазмиды и фаги, плазмиды и вирусы млекопитающих и насекомых. Вектор может быть способным интегрироваться в геном клетки-хозяина, так что любая модификация, вводимая в геном клетки-хозяина посредством вектора становится частью генома клетки-хозяина. Вектор может быть неспособным интегрироваться в геном клетки-хозяина, поэтому оставаться в виде автономно реплицирующейся единицы, такой как плазмида.
Антитело «специфически связывается» с антигеном, когда оно распознает и связывает антиген, например полипептид, включающий аминокислотную последовательность, по существу, идентичную любой из последовательностей SEQ ID NO: 22-43, 59, или 73-84, или их фрагменту или варианту, но, по существу, не распознает и не связывает другие молекулы в образце. Такое антитело характеризуется, например, сродством в отношении антигена, которое, по меньшей мере, в 10, 100, 1000 или 10000 раз выше сродства антитела в отношении другой молекулы сравнения в образце.
«Образец» может представлять собой любой орган, ткань, клетку или клеточный экстракт, выделенный из субъекта, например образец, выделенный из животного, инфицированного A/E-патогеном, или из животного, которому ввели один или несколько полипептидов или нуклеиновых кислот по изобретению, или их иммуногенных фрагментов. Например, неограничивающие примеры образца могут включать ткань (например, из биопсии или аутопсии), клетки, кровь, сыворотку, молоко, мочу, кал, слюну, экскременты, яйца, культуру клеток млекопитающих или культуральную среду, или любой другой образец, или любой экстракт данных материалов, полученный от пациента (человека или животного), тестируемого субъекта или экспериментального животного. Неограничивающие примеры образца могут также включать продукты, продуцируемые в клеточной культуры нормальными или трансформированными клетками (например, путем технологии рекомбинантной ДНК или моноклональных антител). «Образец» может также представлять собой клетку или клеточную линию, созданную в экспериментальных условиях, которые не выделены непосредственно из субъекта. Образец также может быть лишенным клеток, искусственно полученным или синтезированным.
Образец может анализироваться для выявления гена, генома, полипептида, молекулы нуклеиновой кислоты, происходящей из A/E-патогена, или для выявления мутации в гене, происходящем из A/E-патогена или для выявления уровней экспрессии гена или полипептида, происходящего из A/E-патогена, или для определения биологической функции гена или полипептида, происходящего из A/E-патогена, с использованием способов, известных в данной области и/или описанных здесь. Например, такие способы, как секвенирование, анализ одноцепочечного конформационного полиморфизма (SSCP) или анализ длин рестрикционных фрагментов (RFLP) продуктов ПЦР, происходящих из образца, может использоваться для выявления мутации в гене; ELISA или вестерн-блоттинг может использоваться для измерения уровней полипептида или сродства антител; нозерн-блоттинг может использоваться для измерения уровней мРНК, или ПЦР может использоваться для измерения уровня молекулы нуклеиновой кислоты.
«Иммунный ответ» включает в качестве неограничивающих примеров одну или несколько следующих реакций млекопитающего: индукцию антител, В-клеток, Т-клеток (включая хелперные T-клетки, супрессорные Т-клетки, цитотоксические Т-клетки, γδ-T-клетки), специфично направленных на антиген(-ы) в композиции или вакцине, после введения композиции или вакцины. Таким образом, иммунный ответ на композицию или вакцину включает развитие в млекопитающем-хозяине клеточного или опосредованного антителами ответа на интересующую композицию или вакцину. В целом, данный иммунный ответ будет приводить к предотвращению или снижению инфекции, вызываемой A/E-патогеном; к устойчивости кишечника к колонизации A/E-патогеном; или к снижению выделения A/E-патогена.
«Иммуногенный фрагмент» полипептида или нуклеиновой кислоты относится к аминокислотной последовательности или к последовательности нуклеиновой кислоты, которая вызывает иммунный ответ. Таким образом, иммуногенный фрагмент может включать в себя без ограничений, любую часть любой из описанных здесь последовательностей, или последовательность, по существу, идентичную ей, которая включает один или несколько эпитопов (участок, распознаваемый специфичной клеткой иммунной системы, такой как T-клетка или В-клетка). Например, иммуногенный фрагмент может включать в себя без ограничений пептиды любой длины от 6 до 60 или свыше 60 аминокислот, например пептиды любой длины от 10 до 20 аминокислот или от 20 до 40 аминокислот, происходящие из любой из описанных здесь последовательностей. Такие фрагменты могут идентифицироваться с использованием стандартных способов, известных специалистам в данной области, например способов картирования эпитопов, или графиков антигенности или гидрофобности, с использованием, например, программы Omiga version 1.0 от Oxford Molecular Group (см., например, патент США № 4708871) (76, 77, 81, 92, 73).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1A-F показаны нуклеотидные и аминокислотные последовательности NleA из C. rodentium, EPEC и EHEC (SEQ ID NO: 1-3 и 22-24).
На фиг. 2A-J показаны нуклеотидные и аминокислотные последовательности NleB и NleB2 из C. rodentium, EPEC и EHEC (SEQ ID NO: 4-7 и 25-29 & 60).
На фиг. 3A-F показаны нуклеотидные и аминокислотные последовательности NleC из C. rodentium, EPEC и EHEC (SEQ ID NO: 8-10 и 30-32).
На фиг. 4A-F показаны нуклеотидные и аминокислотные последовательности NleD из C. rodentium, EPEC и EHEC (SEQ ID NO: 11-13 и 33-35).
На фиг. 5A-H показаны нуклеотидные и аминокислотные последовательности NleE из C. rodentium, EPEC и EHEC (SEQ ID NO: 14-17 и 36-39).
На фиг. 6A-H показаны нуклеотидные и аминокислотные последовательности NleF из C. rodentium, EPEC и EHEC (SEQ ID NO: 18-21 и 40-43).
На фиг.7 показано выравнивание аминокислотной последовательности 7 C. rodentium Orfl1/GrlA (SEQ ID NO: 56) с положительным регулятором трансляции CaiF (SEQ ID NO: 57) и с предсказанной аминокислотной последовательностью неохарактеризованного белка Salmonella (SEQ ID NO: 58). Подчеркнут предсказанный мотив спираль-поворот-спираль, характерный для ДНК-связывающих белков. Идентичные аминокислотные последовательности показаны *, в то время как консервативные изменения показаны +.
На фиг.8 показана комплементация C. rodentium Δorf11 посредством orf11 из C. rodentium (pCRorf11), EHEC (pEHorf11) или EPEC (pEPorf11) и комплементация двойного мутанта C. rodentium Δler-Δorf11 посредством C. rodentium ler или orf11.
Фиг.9 представляет собой схематичную диаграмму, на которой показано относительное расположение O-островков, содержащих 6 впервые идентифицированных эффекторных генов генома EHEC О157:H7. Также показанное расположение генов шигатоксина (stx), LEE, и inv-spa TTSS. Отмечается ассоциация многих из данных генов с профагами (CP-933 и BP-933).
На фиг. 10A-B показан протеомный анализ секретируемых белков EHEC. A. Одномерный гель SDS-PAGE общих секретируемых белков из EHEC дикого типа (wt) и мутанта секреции III типа (escN-). Миграция маркеров молекулярной массы (в кДа) показана слева от геля. B. Двумерный гель общих секретируемых белков из EHEC дикого типа. Миграция маркеров молекулярной массы (в кДа) показана слева, и примерные значения pI показаны вверху геля. Белковые пятна, анализированные путем масс-спектроскопии (см. таблицу I), обведены кружком и пронумерованы.
На фиг. 11A-C показана геномная организация, распределение и консервативность NleA. A. Графическое представление области, окружающей nleA в геноме EHEC. Направление транскрипции каждой ORF отмечено стрелкой. Аннотация ORF модифицирована из (3). NleA выделен жирным шрифтом. B. Анализ путем саузерн-блота геномной ДНК из EPEC, EHEC, REPEC, Citrobacter rodentium (Citro.) и непатогенного штамма E. coli HB101. Каждый образец геномной ДНК расщепляли BamHI (дорожки 1, 4, 7, 10, 13), EcoRI (дорожки 2, 5, 8, 11, 14), и PstI (дорожки 3, 6, 9, 12, 15). C. Множественное выравнивание белковой последовательности NleA из EHEC, профага интимин-позитивного, не относящегося к О157 штамма EHEC (О84:H4), EPEC и Citrobacter rodentium. Идентичные остатки представлены точками (.), аминокислоты, отсутствующие в конкретной последовательности, представлены тире (-). Два гидрофобных участка, которые могут представлять собой предполагаемые трансмембранные домены, выделены жирным шрифтом в последовательности EHEC.
На фиг.12 показан вестерн-блот-анализ секретируемых белков (левые дорожки) и бактериальных сгустков (правые дорожки) дикого типа (wt) EHEC и мутанта секреции III типа (escN-), экспрессирующего pNleA-HA и нетрансформированных контролей. Блоты зондировали посредством HA(A.), анти-DnaK (B.), анти-Tir (C.).
На фиг. 13A-B показана секреция III типа и транслокация в ΔnleA EHEC. A. Гель SDS-PAGE общих секретируемых белков из EHEC дикого типа (wt) и мутанта ΔnleA. Миграция маркеров молекулярной массы (в кДа) показан слева от геля. B. Вестерн-блот-анализ секретируемых белков из EHEC дикого типа (wt) и мутанта ΔnleA с антисывороткой ΔNleA. Миграция маркеров молекулярной массы (в кДа) показана слева от геля.
На фиг. 14A-B показан вестерн-блот-анализ фракций инфицированных клеток-хозяев. A. Клетки HeLa инфицировали EHEC дикого типа (wt) или escN- EHEC, экспрессирующую меченную HA NleA и подвергали субклеточному фракционированию путем дифференциального центрифугирования. Анализированные фракции представляли собой: бактерии, неразрушенные клетки и цитоскелет (осадок, полученный с низкой скоростью), цитозоль клетки-хозяина (цитозоль хозяина) и мембраны клеток-хозяев (мембраны хозяина). Фракции анализировали путем вестерн-блота с использованием анти-HA, анти-DnaK, антител против кальнексина и антител против тубулина. B. Выделяли фракции мембран из клеток, инфицированных EHEC дикого типа, экспрессирующей меченный HA NleA. Затем мембранные фракции экстрагировали на льду при высокой концентрации соли (1M NaCl), высоком pH (pH 11,4), нейтральном pH и изотонической соли (контроль) или нейтральном pH и изотонической соли, содержащей 1% triton x100 (Triton X100), и повторно центрифугировали с получением растворимых (S) и нерастворимых фракций мембран (P). Данные фракции подвергали вестерн-блот-анализу посредством антител против HA (верхняя панель), антител против кальнексина (средняя панель) и антител против кальретикулина (нижняя панель).
На фиг. 15A-D показаны исследования вирулентности Citrobacter rodentium на мышах. A. Вестерн-блот общих бактериальных экстрактов из C. rodentium дикого типа (wt) и мутанта ΔnleA, тестируемых антисывороткой против NleA. Миграция маркеров молекулярной массы (в кДа) показана слева от геля. B. Графики выживания для мышей C3H/HeJ, инфицированных C. rodentium дикого типа (черные квадраты), ΔnleA C. rodentium (незакрашенные кружки), и мышей, ранее инфицированных мутантом ΔnleA и впоследствии стимулированных C. rodentium дикого типа (вертикальные полосы). Мышей подвергали мониторингу ежесуточно в течение курса инфекции, и когда мышь начинала погибать, ее немедленно фиксировали. Показан процентная доля мышей от исходного числа мышей в каждой группе, которые были жизнеспособны на каждые сутки. C. Титры C. rodentium из кишечника инфицированных швейцарских мышей NIH. Мышей инфицировали C. rodentium дикого типа (черные кружки) или штаммом ΔnleA (незакрашенные кружки) и фиксировали на 10 сутки после инфицирования. Ткань кишечника и сгустки фекалий гомогенизировали и высевали на агар MacConkey для определения общей нагрузки C. rodentium в кишечнике мыши на время фиксации. Каждая мышь в эксперименте представляет единичную точку. Среднее в каждой группе указано на графике горизонтальными полосками. D. Массы кишечника и селезенки инфицированных швейцарских мышей NIH. Мышей инфицировали C. rodentium дикого типа (черные кружки и треугольники) или штаммом ΔnleA (незакрашенные квадраты и треугольники) и фиксировали на 10 сутки после инфицирования. Кишки (квадраты) и селезенки (треугольники) рассекали и взвешивали. Каждая мышь в эксперименте была представлена одной точкой. Среднее в каждой группы указано на графике горизонтальными полосами.
На фиг. 16A-B показаны нуклеотидные и аминокислотные последовательности гомолога NleG из EHEC (SEQ ID NO: 61 и 73).
На фиг. 17A-B показаны нуклеотидные и аминокислотные последовательности NleH1 из EHEC (SEQ ID NO: 62 и 74).
На фиг. 18A-B показаны нуклеотидные и аминокислотные последовательности NleH2 из EHEC (SEQ ID NO: 63 и 75).
На фиг. 19A-B показаны нуклеотидные и аминокислотные последовательности Z2076 из EHEC (SEQ ID NO: 64 и 76).
На фиг. 20A-B показаны нуклеотидные и аминокислотные последовательности Z2149 из EHEC (SEQ ID NO: 65 и 77).
На фиг. 21A-B показаны нуклеотидные и аминокислотные последовательности Z2150 из EHEC (SEQ ID NO: 66 и 78).
На фиг. 22A-B показаны нуклеотидные и аминокислотные последовательности Z2151 из EHEC (SEQ ID NO: 67 и 79).
На фиг. 23A-B показаны нуклеотидные и аминокислотные последовательности Z2337 из EHEC (SEQ ID NO: 68 и 80).
На фиг. 24A-B показаны нуклеотидные и аминокислотные последовательности Z2338 из EHEC (SEQ ID NO: 69 и 81).
На фиг. 25A-B показаны нуклеотидные и аминокислотные последовательности Z2339 из EHEC (SEQ ID NO: 70 и 82).
На фиг. 26A-B показаны нуклеотидные и аминокислотные последовательности Z2560 из EHEC (SEQ ID NO: 71 и 83).
На фиг. 27A-B показаны нуклеотидные и аминокислотные последовательности Z2976 из EHEC (SEQ ID NO: 72 и 84).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы изобретения идентифицировали несколько новых секретируемых белков A/E патогенов (таблица 2) с использованием позитивного регулятора LEE (глобальный регулятор активатора LEE, или GrlA), который может применяться для значительного повышения секреции, и позволил авторам провести функциональный скрининг на предмет белков, секретируемых посредством кодируемого LEE TTSS с использованием подхода, основанного на протеомике. Данные новые белки, названные Nle (не кодируемый LEE эффектор) от A до H, присутствуют в содержащих LEE патогенах, и отсутствуют в непатогенных штаммах E. coli, и в не имеющих LEE патогенах кодируются снаружи от LEE посредством 3 PAI, которые присутствуют в A/E-патогенах, и эволюционируют совместно с LEE (3,8). Идентификация данных белков в некоторых случаях обеспечивала придание функции ORF с ранее неизвестной функцией. Типовой белок NleA (p54) представляет собой эффектор III типа в A/E-патогенах, включая C. rodentium, EPEC и EHEC, и играет критическую роль в вирулентности. NleA кодируется в ассоциированном с фагом островке патогенности в геноме EHEC, отдельном от LEE. Кодируемый в LEE- TTSS направляет транслокацию NleA в клетки-хозяина, где он локализуется в аппарате Гольджи. nleA присутствует в содержащих LEE патогенах и отсутствует в непатогенных штаммах E. coli и в не содержащих LEE патогенах.
В некоторых вариантах осуществления изобретения данные полипептиды и нуклеиновые кислоты, кодирующие данные полипептиды или их части, могут использоваться в качестве вакцин, терапевтических средств, диагностических средств, или инструментов для скрининга лекарственных средств против инфекций, вызываемых A/E-патогенами, или в качестве реагентов.
Полипептиды и тестируемые соединения
Соединения по изобретению включают, без ограничений, полипептиды и молекулы нуклеиновой кислоты, описанные, например, в SEQ ID NO: 1-56, 59-84, и их фрагменты, аналоги и варианты. Соединения по изобретению также включают продукты генов orf11/grlA, nleA, nleB, nleB2, nleC, nleD, nleE, nleF, nleG, nleH (nle Н1 и/или nle H2) или их гомологи.
Соединения по изобретению также включают полипептиды и молекулы нуклеиновой кислоты, описанные, например, в геномной последовательности EHEC (например, AE005174) под номерами Z0985 (NleB2), Z0986 (NleC), Z0990 (NleD), Z6020 (NleF), Z6024 (NleA), Z4328 (NleB), Z4329 (NleE), Z6025 (гомолог NleG), Z6021(NleH1), Z0989 (NleH2), Z2076, Z2149, Z2150, Z2151, Z2337, Z2338, Z2339, Z2560, Z2976 или L0043 (Orf11/GrlA) (инвентарный № AF071034) и их фрагменты, аналоги и варианты.
Соединения могут быть получены, например, заменой, делецией или вставкой аминокислотного остатка в любое положение описанного здесь полипептида, другими консервативными аминокислотными остатками, т.е. остатками, имеющими сходные физические, биологические или химические свойства, и путем скрининга, например, на способность соединения усиливать вирулентность. В некоторых вариантах осуществления изобретения соединения по изобретению включают антитела, которые специфически связываются с описанными здесь полипептидами, например с SEQ ID NO: 22-43, 59 или 73-84.
В данной области хорошо известно, что некоторые модификации и изменения могут быть сделаны в структуре полипептида без существенного изменения биологической функции такого пептида с получением биологически эквивалентного полипептида. В одном из аспектов изобретения полипептиды по настоящему изобретению также расширены до биологически эквивалентных пептидов или «вариантов», которые отличаются от части последовательности полипептидов по настоящему изобретению консервативными аминокислотными заменами, или отличаются неконсервативными заменами, которые не изменяют биологической функции, например вирулентности. Применяемый здесь термин «консервативная аминокислотная замена» относится к замене одной аминокислоты на другую в данном положении пептида, причем замена может быть проведена без существенной потери соответствующей функции. При проведении таких замен подобные аминокислоты могут замещаться на основе относительного сходства заместителей боковых цепей, например, их размера, заряда, гидрофобности, гидрофильности и тому подобного, и такие замены могут анализироваться на предмет их влияния на функцию пептида путем рутинного тестирования.
Применяемый здесь термин «аминокислоты» означает те L-аминокислоты, которые обычно находятся во встречающихся в природе белках, D-аминокислоты и такие аминокислоты при их модификации. В соответствии с этим, аминокислоты по изобретению могут включать, например: 2-аминоадипиновую кислоту; 3-аминоадипиновую кислоту; бета-аланин; бета-аминопропионовую кислоту; 2-аминомасляную кислоту; 4-аминомасляную кислоту; пиперидиновую кислоту; 6-аминокапроновую кислоту; 2-аминогептановую кислоту; 2-аминоизомасляную кислоту; 3-аминоизомасляную кислоту; 2-аминопимелиновую кислоту; 2,4-диаминомасляную кислоту; десмозин; 2,2'-диаминопимелиновую кислоту; 2,3-диаминопропионовую кислоту; N-этилглицин; N-этиласпарагин; гидроксилизин; алло-гидроксилизин; 3-гидроксипролин; 4-гидроксипролин; изодесмозин; алло-изолейцин; N-метилглицин; саркозин; N-метилизолейцин; 6-N-метиллизин; N-метилвалин; норвалин; норлейцин; и орнитин.
В некоторых вариантах осуществления могут проводиться консервативные аминокислотные замены, в которых аминокислотный остаток замещен на другой, имеющий сходный уровень гидрофобности (например, в пределах значения плюс или минус 2,0, или плюс или минус 1,5, или плюс или минус 1,0, или плюс или минус 0,5), где следующей может быть аминокислота, имеющая индекс гидропатичности примерно -1,6, например Tyr (-1,3) или Pro (-1,6), а аминокислотным остаткам назначены следующие индексы (как подробно описано в патенте США № 4554101, включенном в данное описание в качестве ссылки): Arg (+3,0); Lys (+3,0); Asp (+3,0); Glu (+3,0); Ser (+0,3); Asn (+0,2); Gln (+0,2); Gly (0); Pro (-0,5); Thr (-0,4); Ala (-0,5); His (-0,5); Cys (-1,0); Met (-1,3); Val (-1,5); Leu (-1,8); Ile (-1,8); Tyr (-2,3); Phe (-2,5) и Trp (-3,4).
В альтернативных вариантах осуществления могут проводиться консервативные аминокислотные замены, в которых аминокислотный остаток замещен на другой, имеющий сходный гидропатический индекс (например, в пределах значения плюс или минус 2,0, или плюс или минус 1,5, или плюс или минус 1,0, или плюс или минус 0,5). В таких вариантах осуществления каждому аминокислотному остатку может назначаться гидропатический индекс на основе характеристик гидрофобности и заряда, следующим образом: Ile (+4,5); Val (+4,2); Leu (+3,8); Phe (+2,8); Cys (+2,5); Met (+1,9); Ala (+1,8); Gly (-0,4); Thr (-0,7); Ser (-0,8); Trp (-0,9); Tyr (-1,3); Pro (-1,6); His (-3,2); Glu (-3,5); Gln (-3,5); Asp (-3,5); Asn (-3,5); Lys (-3,9); и Arg (-4,5).
В альтернативных вариантах могут проводиться консервативные аминокислотные замены с использованием общедоступных семейств матриц сходства (60, 70, 102, 103, 94, 104, 86). Матрица PAM основана на коэффициентах, полученных из эволюционной модели, в то время как матрица Blosum использует коэффициенты, происходящие из высококонсервативных блоков при выравнивании. Коэффициент сходства выше нуля в матрицах PAM или Blosum может использоваться для получения консервативных аминокислотных замен.
В альтернативных вариантах осуществления могут быть сделаны консервативные аминокислотные замены, в которых аминокислотный остаток замещается другим того же класса, где аминокислоты подразделяются на классы неполярных, кислых, основных и нейтральных, следующим образом: неполярные Ala, Val, Leu, Ile, Phe, Trp, Pro, Met; кислые Asp, Glu; основные Lys, Arg, His; нейтральные Gly, Ser, Thr, Cys, Asn, Gln, Tyr.
Консервативные аминокислотные замены могут включать в себя замену L-аминокислоты соответствующей D-аминокислотой, консервативной D-аминокислотой, или встречающейся в природе не кодируемой генетически формой аминокислоты, а также консервативной заменой L-аминокислоты. Встречающаяся в природе некодируемые в геноме аминокислоты включают бета-аланин, 3-аминопропионовую кислоту, 2,3-диаминопропионовую кислоту, альфа-аминоизомасляную кислоту, 4-аминомасляную кислоту, N-метилглицин (саркозин), гидроксипролин, орнитин, цитруллин, трет-бутилаланин, трет-бутилглицин, N-метилизолейцин, фенилглицин, циклогексилаланин, норлейцин, норвалин, 2-нафтилаланин, пиридилаланин, 3-бензотиенилаланин, 4-хлорфенилаланин, 2-фторфенилаланин, 3-фторфенилаланин, 4-фторфенилаланин, пеницилламин, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, бета-2-тиенилаланин, метионинсульфоксид, гомоаргинин, N-ацетиллизин, 2-аминомасляную кислоту, 2-аминомасляную кислоту, 2,4-диаминомасляную кислоту, п-аминофенилаланин, N-метилвалин, гомоцистеин, гомосерин, цистеиновую кислоту, эпсилон-аминогексановую кислоту, дельта-аминовалериановую кислоту или 2,3-диаминомасляную кислоту.
В альтернативных вариантах осуществления консервативные аминокислотные замены включают замены, основанные на соображениях гидрофильности или гидрофобности, размера или объема, или заряда. Аминокислоты могут в общем характеризоваться гидрофобностью или гидрофильностью, в первую очередь, в зависимости от боковой цепи аминокислоты. Гидрофобная аминокислота характеризуется гидрофобностью выше нуля, а гидрофильная аминокислота характеризуется гидрофильностью ниже нуля, основываясь на нормализованной консенсусной шкале гидрофобности Eisenberg et al. (71). Кодируемые генами гидрофобные аминокислоты включают в себя Gly, Ala, Phe, Val, Leu, Ile, Pro, Met и Trp, и кодируемые генами гидрофильные аминокислоты включают в себя Thr, His, Glu, Gln, Asp, Arg, Ser и Lys. Не кодируемые генами гидрофобные аминокислоты включают трет-бутилаланин, тогда как не кодируемые генами гидрофильные аминокислоты включают цитруллин и гомоцистеин.
Гидрофобные и гидрофильные аминокислоты могут далее подразделяться на основе характеристик их боковых цепей. Например, ароматическая аминокислота представляет собой гидрофобную аминокислоту с боковой цепью, содержащей, по меньшей мере, одно ароматическое или гетероароматическое кольцо, которое может содержать один или несколько заместителей, таких как -OH, -SH, -CN, -F, -Cl, -Br, -I, -NO2, -NO, -NH2, -NHR, -NRR, -C(O)R, -C(O)OH, -C(O)OR, -C(O)NH2, -C(O)NHR, -C(O)NRR, и т.д., где R независимо представляет собой (C1-C6)-алкил, замещенный (C1-C6)-алкил, (C1-C6)-алкенил, замещенный (C1-C6)-алкенил, (C1-C6)-алкинил, замещенный (C1-C6)-алкинил, (C5-C20)-арил, замещенный (C5-C20)-арил, (C6-C26)-алкиларил, замещенный (C6-C26)-алкиларил, 5-20-членный гетероарил, замещенный 5-20-членный гетероарил, 6-26-членный алкилгетероарил, или замещенный 6-26-членный алкилгетероарил. Кодируемые генами ароматические аминокислоты включают Phe, Tyr, и Trp, в то время как не кодируемые генами аминокислоты включают фенилглицин, 2-нафтилаланин, бета-2-тиенилаланин, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, 4-хлорфенилаланин, 2-фторфенилаланин, 3-фторфенилаланин, и 4-фторфенилаланин.
Неполярная аминокислота представляет собой гидрофобную аминокислоту с боковой цепью, которая не изменена при физиологическом pH и которая имеет связи, в которых пары электронов, общие для двух атомов, в равной степени удерживаются каждым из двух атомов (т.е. боковые цепи неполярны). Кодируемые генами неполярные аминокислоты включают Gly, Leu, Val, Ile, Ala и Met, в то время как не кодируемые генами неполярные аминокислоты включают циклогексилаланин. Неполярные аминокислоты могут далее подразделяться таким образом, что будут включать алифатические аминокислоты, которые представляют собой гидрофобные аминокислоты, имеющие алифатическую углеводородную боковую цепь. Кодируемые генами алифатические аминокислоты включают в себя Ala, Leu, Val и Ile, тогда как не кодируемые генами алифатические аминокислоты включают норлейцин.
Полярная аминокислота представляет собой гидрофильную аминокислоту с боковой цепью, которая не заряжена при физиологическом pH, но которая имеет одну связь, в которой пара электронов, общая для двух атомов, удерживается ближе к одному из атомов. Кодируемые генами полярные аминокислоты включают Ser, Thr, Asn и Gln, тогда как не кодируемые генами полярные аминокислоты включают цитруллин, N-ацетиллизин и метионинсульфоксид.
Кислая аминокислота представляет собой гидрофильную аминокислоту со значением pKa боковой цепи менее 7. Кислые аминокислоты обычно имеют отрицательно заряженные боковые цепи при физиологическом рН вследствие потери иона водорода. Кислые аминокислоты, кодируемые генами, включают Asp и Glu. Основная аминокислота представляет собой гидрофильную аминокислоту со значением pKa боковой цепи выше 7. Основные аминокислоты обычно имеют положительно заряженные боковые цепи при физиологическом рН вследствие ассоциации с ионом гидрония. Основные аминокислоты, кодируемые генами, включают Arg, Lys и His, тогда как не кодируемые генами основные аминокислоты включают нециклическую аминокислоту орнитин, 2,3-диаминопропионовую кислоту, 2,4-диаминомасляную кислоту и гомоаргинин.
Специалисту в данной области понятно, что указанные выше классификации не абсолютны и что аминокислота может классифицироваться более чем в одну категорию. Кроме того, аминокислоты могут классифицироваться на основе их известного поведения и/или характерных химических, физических или биологических свойств, на основе конкретных тестов или по сравнению с ранее идентифицированными аминокислотами. Аминокислоты могут включать бифункциональные радикалы, имеющие подобные аминокислотам боковые цепи.
Консервативные замены также могут включать замену химически дериватизированного радикала на недериватизированный остаток, например, путем реакции функциональной боковой группы аминокислоты. Таким образом, данные замены могут включать соединения, свободные аминогруппы которых дериватизированы с образованием гидрохлоридов амина, п-толуолсульфонильных групп, карбобензоксигрупп, трет-бутилоксикарбонильных групп, хлорацетильных групп или формильных групп. Сходным образом, свободные карбоксильные группы могут дериватизироваться с образованием солей, сложных эфиров метила и этила или других типов сложных эфиров или гидразидов, и боковые цепи могут дериватизироваться с образованием О-ацил- или О-алкилпроизводных свободных гидроксильных групп или N-im-бензилгистидина для азота имидазола гистидина. Пептидные аналоги также включают аминокислоты, которые были химически изменены, например, путем метилирования, амидирования C-концевой аминокислоты алкиламином, таким как этаноламин или этилендиамин, или ацилирования или метилирования боковой цепи аминокислоты (например, ацилирование эпсилон-аминогруппы лизина). Пептидные аналоги также могут включать замену амидной связи пептида замещенным амидом (например, группами формулы -C(O)-NR, где R представляет собой (C1-C6)-алкил, (C1-C6)-алкенил, (С1-C6)-алкинил, замещенный (C1-C6)-алкил, замещенный (C1-C6)-алкенил, или замещенный (C1-C6)-алкинил) или изостерамидной связи (например, -CH2NH-, -CH2S, -CH2CH2-, -CH=CH- (цис и транс), -C(O)CH2-, -CH(OH)CH2-, или -CH2SO-).
Соединения могут быть ковалентно связаны, например, полимеризацией или конъюгацией, с образованием гомополимеров или гетерополимеров. Могут использоваться спейсеры и линкеры, обычно состоящие из малых нейтральных молекул, таких как аминокислоты, которые незаряжены в физиологических условиях. Связи могут достигаться несколькими путями. Например, остатки цистеина могут добавляться к концам пептидов, и множественные пептиды могут ковалентно связываться путем контролируемого окисления. Альтернативно, могут использоваться гетеробифункциональные средства, такие как образующие дисульфид/амид агенты или тиоэфир/амид агенты. Соединение также может связываться с другим соединением, которое, например, может модулировать иммунный ответ. Соединение также может быть напряженным, например, за счет наличия циклических частей.
Пептиды или пептидные аналоги могут синтезироваться стандартными химическими способами, например путем автоматического синтеза с использованием раствора или методологии твердофазного синтеза. Автоматические пептидные синтезаторы являются коммерчески доступными, и в них используются способы, хорошо известные в данной области. Пептиды или пептидные аналоги могут также быть получены с использованием рекомбинантной ДНК-технологии с использованием стандартных способов, таких как описаны, например, в Sambrook, et al. (110) или Ausubel et al. (111). В общем, соединения-кандидаты идентифицированы в больших библиотеках природных продуктов или синтетических (или полусинтетических) экстрактах или химических библиотеках способами, известными в данной области. Специалисты в области обнаружения и разработки лекарственных средств понимают, что конкретный источник тестируемых экстрактов или соединения не является критичным в отношении способа(-ов) по изобретению. В соответствии с этим по существу любое количество химических экстрактов или соединений могут подвергаться скринингу с использованием описанных здесь типовых способов. Примеры таких экстрактов или соединений включают в себя, в качестве неограничивающих примеров, основанные на растениях, грибах, прокариотах или животных экстракты, бульоны ферментации и синтетические соединения, а также модификацию существующих соединений. Многие способы также доступны для случайного или направленного синтеза (например, полусинтеза или полного синтеза) любого числа химических соединений, включая в качестве неограничивающих примеров соединения на основе сахаров, липидов, пептидов и нуклеиновых кислот. Коммерчески доступны синтетические библиотеки соединений. Альтернативно, коммерчески доступны библиотеки природных соединений в виде бактериальных, грибных, растительных или животных экстрактов из ряда источников, включая Biotics (Sussex, Великобритания), Xenova (Slough, Великобритания), Harbor Branch Oceanographic Institute (Ft. Pierce, Флорида, США), и PharmaMar, Массачусетс, США. Кроме того, натуральные и синтетически продуцированные библиотеки, например полипептиды патогена A/E, продуцируются, если требуется, способом, известным в данной области, например стандартными способами экстракции и фракционирования. Более того, если требуется, любая библиотека или соединение легко модифицируется с использованием стандартных химических, физических или биохимических способов.
Когда обнаруживают, что грубый экстракт модулирует вирулентность, необходимо дальнейшее фракционирование позитивного экстракта-кандидата для выделения химических составляющих, ответственных за наблюдаемый эффект. Так, целью процесса экстракции, фракционирования и очистки является тщательная характеристика и идентификация химической сущности в неочищенном экстракте, обладающем свойствами по модулированию вирулентности. Те же анализы, что описаны здесь для детекции видов активности в смесях соединений, могут использоваться для очистки активного компонента и для тестирования его производных. Способы фракционирования и очистки таких гетерогенных экстрактов известны в данной области. Если требуется, соединения, которые, как показано, могут использоваться в качестве лекарственных средств, химически модифицируют способами, известными в данной области. Соединения, идентифицированные как обладающие терапевтической, профилактической, диагностической или иной ценностью, могут впоследствии анализироваться с использованием Citrobacter или модели инфекции, вызываемой A/E-патогеном на крупном рогатом скоте, или любой другой модели инфекции, вызываемой A/E-патогеном на животных.
Вакцины
«Вакцины» являются соединениями, включающими в себя материалы, которые вызывают требуемый иммунный ответ. Вакцина может выделять, активировать или использовать память В- и Т-клеток иммунной системы для, например, включения механизмов удаления из организма инфекционных агентов, таких как А/Е патогены или их компоненты. В некоторых вариантах осуществления вакцина включает соответствующий носитель, такой как адъювант, который является агентом, действующим неспецифическим способом для повышения иммунного ответа на специфичный антиген или на группу антигенов, вызывая уменьшение количества антигена при назначении любой дозы вакцины или уменьшение частоты введения вакцины, необходимой для получения требуемого иммунного ответа. Требуемый иммунный ответ может включать полную или частичную защиту от заражения (присутствует в экскрементах инфицированного животного, например млекопитающего) или образования колоний (присутствует в кишечнике инфицированного животного, например млекопитающего) А/Е патогеном. Например, требуемый иммунный ответ может включать любую степень, от 10% до 100%, например 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% защиты от заражения или образования колоний А/Е патогеном вакцинированного животного в сравнении с невакцинированным животным.
Вакцины, относящиеся к изобретению, могут включать в себя полипептиды и нуклеиновые кислоты, описанные здесь, или их иммуногенные фрагменты, и могут назначаться с использованием любой известной или описанной здесь формы введения. В некоторых вариантах осуществления изобретения вакцина может включать в себя живой А/Е патоген, мертвый А/Е патоген или их компоненты. Живой А/Е патоген, который может быть назначен в форме пероральной вакцины, может содержать невосстановимое генетическое повреждение, снижающее вирулентность А/Е патогена, но не его способность вызывать иммунный ответ. Живая вакцина может быть способна заселять кишечник вакцинированного животного, например, млекопитающего.
В некоторых вариантах осуществления, полипептиды и молекулы нуклеиновых кислот, описанные здесь, или их иммуногенные фрагменты, или мутировавшие бактерии (например, ослабленные бактерии), описанные здесь, могут вводиться птицам, например, цыплятам, уткам, индейкам и др., чтобы вызвать иммунный ответ, например, повышение уровня антител, у птиц. Яйца или их продукты, полученные от таких птиц, проявляющие иммунный ответ против полипептидов и молекул нуклеиновых кислот, описанных здесь, или против их иммуногенных фрагментов, могут быть назначены животным, например, человеку, крупному и мелкому рогатому скоту, овцам и др., чтобы вызвать иммунный ответ на полипептиды и молекулы нуклеиновых кислот, описанные здесь, или их иммуногенные фрагменты, у животных. Способы повышения уровня антител у птиц и применения таких антител описаны, например, в патенте США 5750113, выданном Cook 12 мая 1998 года; в патенте США 6730822, выданном Ivarie, et al. 4 мая 2004 года; и публикациях 113-117, приводимых здесь.
Вакцины, относящиеся к изобретению, могут быть в дальнейшем дополнены добавлением рекомбинантных или очищенных антигенов, таких как EspA, EspB, EspD, EspP, Tir, шигатоксин 1 или 2 и/или интимин, с использованием известных стандартных способов. Например, получение и использование рекомбинантных белков ЕНЕС О157:Н7, таких как EspA, Tir, EspB и интимин, было описано (публикация PCT № WO 99/24576; 51).
Клеточная культура
А/Е патогены могут выращиваться в соответствии с любыми известными или описанными здесь способами. Например, А/Е патогены могут сначала выращиваться на среде Luria-Bertani (LB) в течение примерно от 8 до 48 часов или примерно от 12 до 24 часов и затем разводиться примерно от 1:5 до 1:100, например 1:67, или примерно от 1:5 до 1:25, или примерно 1:10, в минимальной среде М-9, дополненной 20-100 мМ NaHCO2 или NaHCO3, или примерно 30-50 мМ, или примерно 44 мМ NaHCO2 или NaHCO3; 4-20 мМ MgSO4, или примерно 5-10 мМ; или примерно от 0,8 мМ до 8 мМ MgSO4, от 0,1 до 1,5% глюкозы, или примерно от 0,2% до 1%, или примерно 0,4% глюкозы и от 0,05 до 0,5% казаминовых кислот, или примерно от 0,07 до 0,2%, или примерно 0,1% казаминовых кислот. Культуры в основном поддерживаются при примерно 37ºС, возможно в 2-10% СО2 или примерно в 5% СО2, и выращиваются до оптической плотности примерно 600 нм от 0,7 до 0,8. Целые клетки затем удаляются любым пригодным способом, например микрофильтрацией или центрифугированием, и супернатант может быть концентрирован, например, в 10-1000 раз или более, например в 100 раз, с использованием диализа, ультрафильтрации или подобных способов. Общий белок легко определяется с использованием хорошо известных в науке способов.
Супернатанты клеточных культур могут быть получены с использованием культур любых А/Е патогенов, включая дикий тип или мутантные А/Е патогены, например, ЕНЕС, как описано здесь или известно научным специалистам. В общем, А/Е патоген культивируется в пригодной среде, в условиях, способствующих секреции антигена типа III (патенты США № 6136554 и 6165743) (51, 74).
Изолирование и идентификация дополнительных генов
На основе нуклеотидных или аминокислотных последовательностей, описанных здесь, например в SEQ ID NO: 1-56 или 59-84, изолирование и идентификация дополнительных генов становятся возможными с использованием стандартных способов. Любой А/Е патоген может служить источником таких генов.
В некоторых вариантах осуществления, последовательности нуклеиновых кислот, описанные здесь, могут быть использованы для создания проб и праймеров, включая вырожденные олигонуклеотидные пробы или праймеры, на основе последовательности любой цепи ДНК. Пробы и праймеры могут быть использованы в дальнейшем для поиска в геномных или кДНК библиотеках генов других А/Е патогенов, с применением стандартных способов амплификации и гибридизации.
В некоторых вариантах осуществления, аминокислотные последовательности, описанные здесь, могут быть использованы для получения антител или других реагентов, которые применяются для поиска полипептидов А/Е патогенов, которые связываются с этими антителами.
В некоторых вариантах осуществления, связывающиеся партнеры могут быть идентифицированы путем мечения полипептидов по изобретению (например, таких в значительной степени схожих с SEQ ID NO: 22-43, 59 или 73-84) эпитопной последовательностью (например, FLAG или 2HA) и введения их в клетку-хозяина, как путем трансфекции с подходящим вектором, содержащим последовательность нуклеиновых кислот, кодирующую полипептид по изобретению, так и путем эндогенного введения бактерий типа III с последующей иммунопреципитацией и идентификацией связывающихся партнеров.
Клетки HeLa могут быть инфицированы штаммами, экспрессирующими белки слияния FLAG или 2НА, с последующим лизисом и иммунопреципитацией с анти-FLAG или анти-2НА антителами. Связывающиеся партнеры могут быть идентифицированы с помощью масс-спектрометрии. Если полипептид по изобретению не образуется в достаточных количествах, такой способ может не произвести нужного объема меченого белка для идентификации его партнера. Как часть дополнительного способа, каждый полипептид по изобретению может быть клонирован в вектор трансфицирования млекопитающих, слитый, например, с 2НА, GFP и/или с FLAG. После трансфицирования клетки HeLa могут быть лизированы и меченый полипептид иммунопреципитирован. Связывающийся партнер может быть идентифицирован с помощью SDS PAGE и последующей масс-спектрометрии.
В некоторых вариантах осуществления, полипептид по изобретению может быть помечен, получен в больших количествах и использован в аффинных колонках и в иммунопреципитации для идентификации и/или подтверждения идентифицированных соединений-мишеней. Белки, меченные FLAG, НА и/или His, могут быть использованы на таких аффинных колонках для извлечения из клеточных экстрактов факторов клетки-хозяина, и преобладающий фактор может быть подтвержден стандартными анализами связывания, кривыми насыщения и другими методами, описанными здесь или известными специалистам в этой области.
В некоторых вариантах осуществления бактериальная двухгибридная система может быть использована для изучения белок-белковых взаимодействий. Последовательности нуклеиновых кислот, описанные здесь, или последовательности, в значительной степени схожие с ними, могут быть клонированы в плазмиду приманки рВТ двухгибридной системы, и коммерчески доступная библиотека из 5×106 независимых клонов селезенки мыши может быть использована как библиотека-мишень для приманок. Потенциальные преобладающие факторы могут быть в дальнейшем характеризованы путем восстановления плазмид и их возвращения к первоначальному состоянию для уменьшения ложноположительных результатов от вариантов приманки клона и клонов-приманок библиотеки, которые активируют репортерные гены независимо от клонированной приманки. Воспроизводимые преобладающие факторы могут быть изучены, в дальнейшем, как здесь описано.
В некоторых вариантах осуществления, А/Е патогенный штамм, экспрессирующий GrlA, например штамм ЕНЕС О157, экспрессирующий клонированный GrlA, может быть использован для протеомного анализа секретируемых А/Е протеомов типа III, с применением, например, 2D гелевого анализа супернатантов. Кроме того, полный А/Е патоген (например, основанные на ЕНЕС биочипы) может применяться для определения того, какие гены регулируются GrlA. Вирулентность определяют способами, описанными здесь, или известными специалистам в этой области.
После идентификации кодирующих последовательностей, они могут быть изолированы с использованием стандартных способов клонирования и введены в любой подходящий вектор или репликон для, например, получения полипептидов. Такие векторы и репликоны включают, без ограничения, бактериофаг Х (E. coli), pBR322 (E. coli), pACYC177 (E. coli), pKT230 (грамотрицательная бактерия), pGV1 106 (грамотрицательная бактерия), pLAFR1 (грамотрицательная бактерия), pME290 (не-E. coli грамотрицательная бактерия), pHv14 (E. coli и Bacillus subtilis), pBD9 (Bacillus), pIJ61 (Стрептомицеты), pUC6 (Стрептомицеты), YIp5 (Сахаромицеты), YCp19 (Сахаромицеты) или вирус коровьей папилломы (клетки млекопитающего).
В целом, полипептиды по изобретению могут быть получены в любой приемлемой клетке-хозяине, измененной или трансфицированной подходящим вектором (69). Способ изменения или трансфицирования и выбор экспрессирующего носителя будут зависеть от выбранной системы хозяина. Могут применяться разнообразные экспрессирующие системы, и выбор строго определенной клетки-хозяина некритичен для изобретения. Например, полипептид, в соответствии с изобретением, может быть получен в прокариотической клетке-хозяине (например, E. coli) или в эукариотической клетке-хозяине (например, Saccharomyces cerevisiae, клетках насекомых, например, клетках Sf21, или в клетках млекопитающих, например клетках NIH 3T3, HeLa или COS). Эти клетки доступны из различных источников (например, the American Type Culture Collection, Manassus, VA). Бактериальные экспрессирующие системы для получения полипептидов включают E. coli рЕТ экспрессирующую систему (Novagen, Inc., Madison, Wis.) и pGEX экспрессирующую систему (Pharmacia).
Анализы
Соединения-кандидаты, включая полипептиды, молекулы нуклеиновых кислот и малые молекулы, могут быть выявлены и оценены с использованием различных способов, описанных здесь или известных научным специалистам. Соединения, уменьшающие уровень экспрессии любых полипептидов или молекул нуклеиновых кислот по изобретению могут быть использованы, например, как лекарства против А/Е патогенной инфекции.
Скрининговые анализы могут сопровождаться, например, измерением экспрессии гена стандартным нозерн-блот-анализом, с использованием любого подходящего фрагмента нуклеиновой кислоты, в соответствии с изобретением, как гибридизационной пробы, где уровень экспрессии гена в присутствии соединения-кандидата сравнивают с уровнем экспрессии гена в отсутствии соединения-кандидата. С другой стороны, или дополнительно, эффект соединения-кандидата может быть определен по уровню экспрессии или секреции полипептида, с использованием, например, иммунопреципитации или приемов вестерн-блота.
Другие анализы могут быть проведены следующим образом.
Подтверждение секреции и транслокации типа III в клетках-хозяевах
Для определения, какое из соединений-кандидатов нуждается в TTSS для секреции, каждый ген или порция генов могут быть присоединены к С-концу FLAG, и супернатанты собирают с WT и TTSS мутантов, например, WT EHEC и изогенного мутанта escN типа III, как описано здесь или известно науке. Другой способ определения секреции включает исследование супернатантов на снижение продуктов секреции в мутантных штаммах, или повышение антител к белку, с использованием вестерн-анализа супернатантов WT и типа III. Для подтверждения того, что ни один из интересующих белков не является компонентом TTSS, супернатанты от каждого из соединений-кандидатов, росших в условиях, индуцирующих тип III, могут быть исследованы на секрецию типа III. LEE TTSS секретирует два класса белков: транслоконы (EspA, B и D), которые связаны с поверхностью бактериальной клетки, и эффекторы, которые перемещаются непосредственно в клетку-хозяина. Соединения-кандидаты изучают для определения, являются они эффекторами или транслокаторами. Например, FLAG-меченные предполагаемые эффекторы в ЕНЕС или других А/Е патогенах могут быть использованы для инфицирования культивируемых эпителиальных HeLa клеток и исследованы с помощью иммунофлюоресцентной микроскопии после окрашивания с анти-FLAG антителами. Такая визуализация обычно показывает проникновение бактерий в клетку-хозяина и часто выявляет, какая органелла является мишенью эффектора (например, мембрана - для Tir, комплекс Гольджи - для NleA). Антитела к различным клеточным структурам могут быть использованы таким образом для подтверждения локализации. В дополнение к визуализации, инфицированные HeLa клетки могут быть фракционированы на цитозоль, нерастворимый, и мембранные фракции, с использованием известных способов фракционирования (30), и с помощью вестерн-анализа, производимого с применением анти-FLAG антител, определяют, какая клеточная фракция является мишенью эффектора. В качестве контроля клетки инфицируют меченым эффектором, экспрессируемым в TTSS-дефектном штамме. Если мишенью является мембранная фракция, обработка высшей солью или щелочной рН может быть использована для определения, является ли это интегральным белком мембраны. Если соединение-кандидат экспрессируется на низком уровне и определение перемещения способом иммунофлюоресценции затруднено, может быть применено генетическое слияние с аденилатциклазой, ферментом, для активности которого необходим цитоплазматический кофактор млекопитающих (кальмодулин) (87).
Эффекты на формирование ложа и усвоение
Учитывая, что накопление актина и образование ложа являются отличительными признаками А/Е патогенов, соединения-кандидаты выявляют по накоплению актина и образованию ложа, например, в культивируемых эпителиальных HeLa клетках.
Инвазия ЕРЕС и ЕНЕС является другим фенотипом клеточной культуры, который легко определяется и свидетельствует о взаимодействии культивируемыми эпителиальными клетками и способности изменять цитоскелет клетки-хозяина (кроме мутантов типа III и штаммов, дефицитных по Tir и интимину). Уровни инвазии различных соединений-кандидатов могут сравниваться в мутантных А/Е патогенах WT и типа III, например, WT и TTSS мутантных ЕНЕС в клетках HeLa, с использованием гентамицинового защитного анализа.
Кроме того, определяют способность соединений-кандидатов блокировать фагоцитоз культивируемых макрофагов, так как ЕРЕС и ЕНЕС подавляют фагоцитоз культивируемых макрофагов через ингибирование активности PI 3-киназы клетки-хозяина тип III-зависимым образом (Celli, J., M. Oliver and B.B. Finlay. 2001. Enteropathogenic Escherichia coli mediates antiphagocytosis through the inhibition of PI 3-kinase-dependent pathways. Embo J 20: 1245-58). Если какие-либо соединения-кандидаты не способны подавлять фагоцитоз, может быть проведен дополнительный анализ ингибирования PI 3-киназы.
Эффекты на поляризованные эпителиальные монослои
Состояние межклеточных взаимодействий играет ключевую роль в развитии диареи. Помимо образования ложа, А/Е патогены вызывают и другие LEE типа III-эффекты на поляризованные эпителиальные клетки, включая утрату микроворсинок (сглаживание микроворсинок) и снижение трансмонослойного электрического сопротивления, критерия плотности взаимодействия. Используя поляризованные кишечные монослои клеток Сасо-2 человека, может быть применена сканирующая электронная микроскопия высокого разрешения монослоев, инфицированных А/Е патогеном WT (например, WT ЕНЕС), TTSS мутантный А/Е патоген, например, ЕНЕС escN и любое из соединений-кандидатов. Монослои инфицируют различное число раз, отмывают и изучают на SEM, используя стандартные способы (66), и выявляют снижение электрического сопротивления после инфицирования поляризованных клеток Сасо-2.
Эффекты на врожденный иммунитет и воспаление
Легко выявляемой чертой патогенов является способность подавлять врожденные иммунные и воспалительные ответы. Подобные эффекты описаны для А/Е патогенов, таких как ЕНЕС и ЕРЕС, и данное исследование может быть использовано для изучения соединений-кандидатов в штаммах WT и TTSS мутантных А/Е патогенов. Например, ЕНЕС вызывает подавление NF-kβ, приводящее к угнетению некоторых цитокинов, таких как Il-8, Il-6 и Il-1α в клетках HeLa (80), и этот процесс требует LEE TTSS. Соединения-кандидаты исследуют на подавление этих факторов вслед за, например, инфицированием клеток HeLa, используя стандартные способы, такие как RT-ПЦР (ПЦР в реальном времени) и коммерчески доступные анализы ELISA.
Функциональные исследования на основе информации о локализации
В дополнение к изучению фенотипа, соединения-кандидаты исследуют в зависимости от их локализации в клетке-хозяине. Например, если соединение-кандидат локализуется в комплексе Гольджи, оно может быть изучено для определения наличия отрицательного влияния на функционирование комплекса Гольджи, включая биохимические исследования гликозилирования и функциональные исследования комплекса Гольджи на дрожжевых грибах, экспрессирующих соединение-кандидат. Если соединение-кандидат локализуется в митохондриях, применяют исследования апоптоза и других митохондриальных функций. Если мишенью соединения-кандидата является эндоплазматический ретикулум, изучают синтез и секрецию белков. Если мишенью является ядро, проводят транскрипционные исследования.
Роль вирулентности
Конкурентные индексы (CI) широко используются для определения роли минорных вирулентных факторов, а также принадлежности двух вирулентных факторов к одному вирулентному «пути» (63). Кратко, два штамма с разной устойчивостью к антибиотикам совместно вводят животному и, после достаточного времени инкубации, бактерии выделяют и определяют соотношение двух штаммов. Индекс 1 означает равную вирулентность. Если идентифицированные соединения влияют на вирулентность, их CI, в сравнении с WT, могут быть определены. Также CI используют для определения, к какому вирулентному пути принадлежат соединения-кандидаты. Например, CI могут быть получены при сравнении мутантов двух вирулентных факторов, в дополнение к сравнению каждого из них с WT. При сравнении одиночных мутантов с двойным мутантом, соотношение CI, равное 1 означает, что они принадлежат к одному общему вирулентному пути, тогда как соотношение, отличающееся от 1, означает, что они принадлежат к разным вирулентным «путям».
Микроскопические исследования
Микроскопические способы используют для характеристики заболевания, вызванного А/Е патогеном, включая трансмиссионную электронную микроскопию (ТЕМ) и сканирующую электронную микроскопию (SEM) для изучения лимфоидных фолликулов в бляшках Пейера дистальной части подвздошной кишки кроликов, инфицированных REPEC, для подтверждения формирования А/Е повреждений (63), конфокальную микроскопию для наблюдения поступления в мышиные ворсинки, и гистологический анализ болезненного процесса в инфицированных мышах.
Эти способы используют для изучения соединений-кандидатов на приемлемых животных моделях, например мышах, инфицированных различными штаммами цитробактера, несущими мутации в последовательностях кандидата. Для каждого соединения-кандидата может быть предпринято комплексное исследование для отслеживания прогрессирования (или его отсутствия) заболевания в этой системе. Кроме того, определяют уровень колонизации этими мутантами поверхности кишечника. Применяют инфицирование животных штаммами, мечеными антибиотиками, после чего изымают ткань кишечника. Ткань гомогенизируют и подсчитывают количество бактерий на селективных счетных пластинках.
Основной особенностью А/Е патогена, например цитробактерной инфекции, является выраженное воспаление. Клеточные признаки воспаления исследуют с помощью конфокальной микроскопии у различных мутантов соединений-кандидатов. Путем мечения тканей антителами или лектинами, с последующей конфокальной микроскопией, выявляют клетки воспаления, мобилизованные к месту инфицирования мутантами, в сравнении с родительским штаммом. Антитела к некоторым факторам врожденного ответа доступны и могут также быть использованы для анализа мутантных фенотипов в ходе инфекции путем изучения факторов врожденного ответа и клеток, таких как макрофаги, нейтрофилы, продукции iNOS, дендритные клетки и др.
Гистологические исследования
Могут проводиться гистологические исследования окрашенных тканей. Например, окрашенные гематоксилином или эозином срезы подвздошной кишки кроликов, инфицированных REPEC, и штаммы с делециями соединений-кандидатов изучают для сравнения воспаления и повреждения тканей и характеристики А/Е патогенных инфекций (58). Подобное же окрашивание проводят на мышах со штаммами цитробактера, дефицитными по соединениям-кандидатам. Доступны некоторые другие гистологические красители, с помощью которых можно определить воспаление, связанное с цитробактером и изогенными мутантами, включая Гимза и Толуидин синий О (для общей морфологии), Шифф-йодная кислота (окрашивает карбогидраты, позволяя выявить кишечный слизистый слой и бокаловидные клетки), Грам, хлорацетатэстераза (окрашивает клетки воспаления) и Реакция каспаз (для апоптоза). Иммуногистохимия позволяет использовать антитела, направленные против антигенов бактериальных клеток и клеток млекопитающих.
Антитела
Соединения по изобретению могут быть использованы для получения антител к полипептидам по изобретению, с применением стандартных способов получения (45) или способов, известных специалистам в этой области.
Например, кодирующую последовательность для полипептида по изобретению очищают до степени, необходимой для иммунизации кролика. С целью минимизировать возможные проблемы, связанные с низкой аффинностью или специфичностью антисыворотки, создают две или три полипептидные конструкции для каждого протеина, и каждая конструкция вводится, по меньшей мере, двум кроликам. Количество антисыворотки может нарастать в серии инъекций, предпочтительно включающей, по меньшей мере, три ревакцинирующих инъекции. Первичную иммунизацию проводят с полным адъювантом Фрейнда, а последующие иммунизации - с неполным адъювантом Фрейнда. Титры антител отслеживают с помощью вестерн-блота и иммунопреципитационных анализов, используя очищенный белок. Специфичность антисыворотки определяют с использованием панели неродственных белков. Альтернативно или дополнительно, пептиды, связанные с относительно уникальными иммуногенными участками полипептида по изобретению, могут быть получены и сцеплены с гемоцианином лимфы улитки (KLH) через включенный С-терминальный лизин. Антисыворотку к каждому из этих пептидов аффинно очищают на пептидах, конъюгированных с BSA, и проверяют специфичность с помощью ELISA и вестерн-блота, с использованием пептидных конъюгатов, и с помощью вестерн-блота и иммунопреципитации.
Альтернативно, моноклональные антитела, которые специфически связывают любой из полипептидов по изобретению, получают в соответствии со стандартным гибридомным способом (91, 90, 89, 78). Полученные моноклональные антитела также проверяют на специфичность распознавания с помощью вестерн-блота или иммунопреципитации. Антитела, которые специфически связывают полипептид по изобретению, признаются применимыми; такие антитела могут быть использованы, например, в иммунологическом анализе. Альтернативно, моноклональные антитела получают с использованием полипептида по изобретению, описанному выше, и библиотеки фагового дисплея (112).
В некоторых вариантах осуществления, антитела получают с использованием фрагментов полипептидов, предположительно обладающих иммуногенными свойствами, исходя из таких критериев, как высокая частота заряженных остатков. Антитела специально разрабатывают с расчетом на минимизацию побочного иммунного ответа реципиента с использованием, например, химерных антител, содержащих антиген-связывающий домен от одного вида и Fc-фрагмент от другого вида, или с использованием антител, полученных от гибридомы соответствующего вида.
В некоторых вариантах осуществления, антитела против любого из полипептидов, описанных здесь, используют для лечения или профилактики А/Е патогенной инфекции.
Животные модели
Соединения могут быть быстро изучены на различных животных моделях А/Е патогенной инфекции.
Цитробактерная мышиная инфекционная модель является моделью заболевания, встречающейся в естественных условиях, а модель ЕНЕС-выделяющей инфекции взрослых коров - моделью естественного носительства, не проявляющегося болезнью (скот не заболевает, хотя ЕНЕС не является частью нормальной флоры). Для цитробактерной модели, вирулентность мутантов изучают на мышах, как описано здесь. Нокаут(КО)/мутантных мышей используют для изучения роли кандидатных последовательностей в инфекции. Получены несколько линий КО мышей, включая определение роли iNOS (20), Т- и В-клеток (106), Tlr-4 и установление степени восприимчивости реципиента (54), так же, как Nck.
Для коровьей модели, ЕНЕС мутанты изучают на годовалых животных (см., например, публикация PCT № WO 02/053181). Кратко, 108 CFU мутанта или WT О157 вводят животному через ротожелудочную интубацию. В течение 14 дней после введения фекальные выделения отслеживают на селективных счетных пластинках, и колонии исследуются с помощью многоканальной ПЦР, уровня выделений, гистологического и микроскопического анализов перианальной области, где концентрируется ЕНЕС (97). Другая модель представляет собой петли кишечника коровы, в которые вводят ЕНЕС и несколько раз изучают гистологически и морфологически, а также подсчитывают количество адгезированных бактерий с помощью счетной пластинки.
Естественную кроличью инфекционную модель инфекции RDEC-1 проводят следующим образом: после культивирования в течение ночи, бактериальную культуру собирают центрифугированием и растворяют в одном мл фосфатного буфера. Новозеландским белым кроликам (весом от 1,0 до 1,6 кг), после голодания в течение ночи, вводят в желудок через орально-гастральный зонд 5 мл 2,5% стерильного натрия бикарбоната и 1 мл RDEC-1 или кандидатной последовательности мутантных штаммов (2:-5×1010). Такую же дозу бактерий вводят каждому кролику на следующий день. Каждого кролика ежедневно взвешивают и собирают выделяемые с фекалиями бактерии с помощью ректальных тампонов и из каловых катышков. Ректальные тампоны раскатывают по половине поверхности чашек MacConkey, содержащих налидиксовую кислоту. Пять каловых катышков или такое же количество жидких каловых масс собирают от каждого кролика и растворяют в 3 мл фосфатного буфера и 0,1 мл каждой каловой суспензии наносят на чашки MacConkey, содержащие налидиксовую кислоту. Рост колоний, устойчивых к налидиксовой кислоте, подсчитывают следующим образом: 0, нет роста; 1, редко расположенные колонии; 2, плотно расположенные колонии; 3, сплошной рост колоний. Ткани выделяют немедленно после усыпления внутривенной инъекцией кетамина и передозировки фенобарбитала натрия. Степень бактериальной колонизации тканей кишечника измеряли следующим образом: на сегмент кишечника (10 см), кроме слепой кишки, накладывают двойные лигатуры на проксимальном и дистальном концах, перерезают между двойными лигатурами, затем промывают 10 мл ледяного фосфатного буфера. Один грамм вязкого содержимого слепой кишки добавляют к 9 мл фосфатного буфера. Полученную суспензию разводят и наносят на чашки MacConkey, содержащие налидиксовую кислоту. Образцы ткани выделяют с помощью 9 мм зажима, трижды промывают фосфатным буфером, добавляют к 2 мл ледяного фосфатного буфера и гомогенизируют в гомогенизаторе, затем последовательно разведенные образцы наносят на чашки MacConkey. Число бактерий, адгезированных на квадратном сантиметре каждой ткани, подсчитывают следующим образом:
CFU/см2=число бактерий/чашка×фактор разведения×2 мл/-0,452
Лечение и диагностика
Полипептиды и молекулы нуклеиновых кислот, описанные здесь, могут быть использованы как лекарства, например, для получения вакцин или лекарственных соединений, или создания А/Е патогенов с ослабленной вирулентностью. Такие А/Е патогены могут быть получены, как описано здесь, например, путем создания праймеров на основе последовательностей нуклеиновых кислот, описанных здесь, и с использованием способа аллельного обмена на основе sacB (29). Полипептиды и молекулы нуклеиновых кислот могут быть использованы по отдельности или в комбинации друг с другом или с другими подходящими молекулами, такими как EspA, EspB, EspC, EspD, EspP, Tir, шигатоксин 1, шигатоксин 2 или молекулы интимина.
В некоторых вариантах осуществления, молекулы нуклеиновых кислот, описанные здесь, могут быть использованы в антисмысловых способах. Под «антисмысловой», как упоминается здесь в отношении нуклеиновых кислот, подразумевается последовательность нуклеиновых кислот, комплементарная к кодирующей цепи молекул нуклеиновых кислот, например гену, такому как nleA, nleB, nleC, nleD, nleE или nleF, или комплементарная к нуклеотидной последовательности, значительно схожей с последовательностью любой из SEQ ID NO: 1-21, или 60-72, или ее фрагменту, или варианту. В некоторых вариантах осуществления, антисмысловая молекула нуклеиновой кислоты способна снизить уровень полипептида, кодируемого комплементарным геном, когда они оба экспрессируются в клетке. В некоторых вариантах осуществления, уровень полипептида снижается в степени, равной любому целому числу от, по меньшей мере, 10% до, по меньшей мере, 25%, или в степени, равной любому целому числу от, по меньшей мере, 25% до, по меньшей мере, 50%, или в степени, равной любому целому числу от, по меньшей мере, 50% до, по меньшей мере, 75%, или в степени, равной любому целому числу от, по меньшей мере, 75% до 100%, в сравнении с уровнем полипептида в клетке, экспрессирующей только ген, а не комплементарную антисмысловую молекулу нуклеиновой кислоты.
В некоторых вариантах осуществления, экспрессию гена или интересующего кодирующего или некодирующего участка можно подавить или предотвратить с использованием способа интерференции РНК (PHKi), разновидности пост-транскрипционного генного сайленсинга. PHKi используют для создания функционального «нокаута», то есть системы, в которой экспрессия гена или интересующего кодирующего или некодирующего участка снижена, проявляясь в общем снижении количества кодируемого продукта. Таким образом, PHKi применяют для мечения представляющей интерес нуклеиновой кислоты или ее фрагмента или варианта, чтобы, в свою очередь, снизить ее экспрессию и уровень активности продукта, который ей кодируется. Такая система применяется для функциональных исследований продукта, а также для лечения А/Е патогенных инфекций. PHKi описана, например, в опубликованном патенте США 20020173478 (Gewirtz; опубликован 21 ноября 2002 года) и 20020132788 (Lewis et al., опубликован 7 ноября 2002 года) (79, 67). Реагенты и наборы для работы с PHKi коммерчески доступны, например, в Ambion Inc. (Austin, Техас, США) и New England Biolabs Inc. (Beverly, Массачусетс, США).
Предполагается, что в некоторых системах исходным агентом для PHKi является молекула dsРНК, связанная с нуклеиновой кислотой-мишенью. Затем, предполагается, dsРНК расщепляется на короткие интерферирующие молекулы РНК (siРНК) длиной 21-23 нуклеотида (дуплексы 19-21 н.п., каждый с двумя «липкими» нуклеотидами на 3'-конце). Фермент, предположительно осуществляющий эту первую стадию расщепления, был назван «Dicer» и классифицирован как член РНКаз III семейства dsРНК-специфичных рибонуклеаз. С другой стороны, на PHKi возможно воздействовать через введение непосредственно в клетку, или образование в клетке, при введении в клетку подходящего предшественника (например, вектора и т.д.), таких siРНК или siРНК-подобных молекул. siРНК может затем связываться с другими внутриклеточными компонентами для формирования РНК-индуцированного комплекса сайленсинга (RISC). Образовавшийся RISC затем связывается с представляющим интерес транскриптом через спаривание оснований между компонентом своей siРНК и транскриптом-мишенью, по принципу гомологичности, приводя к расщеплению транскрипта-мишени на расстоянии примерно 12 нуклеотидов от 3'-конца siРНК. Таким образом, мРНК-мишень расщепляется, и уровень кодируемого ей белкового продукта снижается.
Воздействие на PHKi возможно через введение в клетку подходящих siРНК или siРНК-подобных молекул, синтезированных in vitro. Воздействовать на PHKi можно, например, с использованием химически синтезированной РНК (64), для чего подходящие молекулы РНК химически синтезируют, применяя известные способы. С другой стороны, используют подходящие векторы экспрессии для транскрибирования такой РНК как in vitro, так и in vivo. Транскрипцию in vitro смысловых и антисмысловых цепей (кодированных последовательностями, представленными на том же векторе или на отдельных векторах) проводят с использованием, например, Т7 РНК полимеразы, в таком случае вектор включает подходящую кодирующую последовательность, функционально связанную с Т7 промотером. Транскрибированная in vitro РНК может, в некоторых вариантах осуществления, быть обработана (например, с использованием РНКазы III E. coli) in vitro до размеров, приемлемых для PHKi. Смысловые и антисмысловые транскрипты объединяют для образования РНК дуплекса, который вводят в представляющую интерес клетку-мишень. Используют и другие векторы, которые экспрессируют РНК малой шпильки (shРНК), которые вводят в siРНК-подобные молекулы. В науке известны различные способы, основанные на применении векторов (65, 93, 95, 98, 99, 105, 109). Также известны различные способы введения таких векторов в клетки как in vitro, так и in vivo (например, генная терапия).
В целом, в осуществлении, экспрессия полипептида, включающего последовательность аминокислот, существенно схожую с последовательностью любой из SEQ ID NO: 22-43, может быть подавлена путем введения в клетку или образования в клетке siРНК или siРНК-подобной молекулы, соответствующей молекуле нуклеиновой кислоты, кодирующей полипептид или ее фрагменту, или гомологичной нуклеиновой кислоте. В различных вариантах осуществления, такой способ предполагает прямое введение siРНК или siРНК-подобной молекулы в клетку или использование векторных способов, описанных выше. В осуществлении, siРНК или siРНК-подобная молекула имеют длину менее 30 нуклеотидов. В дальнейших вариантах осуществления, siРНК или siРНК-подобная молекула имеют длину около 21-23 нуклеотидов. В осуществлении, siРНК или siРНК-подобная молекула включают в себя дуплексы 19-21 н.п., каждый с двумя «липкими» нуклеотидами на 3'-конце. В осуществлении, siРНК или siРНК-подобная молекула существенно схожа с нуклеиновой кислотой, кодирующей полипептид, или его фрагмент, или вариант (или фрагмент варианта). Такой вариант способен кодировать белок, имеющий активность полипептида, кодированного SEQ ID NO: 22-43. В осуществлении, смысловая цепь siРНК или siРНК-подобной молекулы существенно схожи с SEQ ID NO: 1-21 или ее фрагментом (РНК, имеющие U вместо Т остатка последовательности ДНК).
В некоторых вариантах осуществления, повышенный уровень антител против полипептидов по изобретению используют как лечение А/Е патогенной инфекции.
В некоторых вариантах осуществления, полипептид или молекулы нуклеиновой кислоты используют для определения присутствия в образце А/Е патогена. Молекулы нуклеиновой кислоты используют для создания проб или праймеров, способных, например, гибридизироваться с ДНК А/Е патогена в образце, или используют для амплификации ДНК А/Е патогена в образце, применяя, например, способ полимеразной цепной реакции. Полипептиды используют, например, для получения антител, специфически связывающихся с полипептидом, экспрессируемом А/Е патогеном. Такие пробы или праймеры могут быть определимо помечены. Под «определимо помечены» имеются в виду любые способы мечения и идентификации присутствия молекулы, например, олигонуклеотидной пробы или праймера, гена или его фрагмента, или молекулы сДНК. Способы определимого мечения молекул хорошо известны в науке и включают, без ограничений, радиоактивное мечение (например, изотопом, таким как 32P или 35S) и нерадиоактивное мечение, такое как ферментативное мечение (например, с использованием пероксидазы хрена или алкалинфосфатазы), хемолюминесцентное мечение, флюоресцентное мечение (например, с использованием, флюоресцеина), биолюминесцентное мечение или определение лиганда, связанного с пробой, с помощью антител. Также этот термин включает молекулы, определимо помеченные непрямым способом, например молекулы, связанные с первым агентом (таким, как биотин), который, в свою очередь, связан со вторым агентом, который может быть обнаружен или проанализирован (таким, как стрептавидин, меченый флюоресцеином). Метки также включают дигоксигенин, люциферазы и экворин.
Фармацевтические и ветеринарные соединения, дозировки и назначение
Здесь описаны соединения, включающие полипептид и молекулы нуклеиновой кислоты, а также соединения, идентифицируемые с использованием способов по изобретению. В соответствии с изобретением, соединения могут применяться отдельно или в комбинации с другими соединениями (например, молекулами нуклеиновой кислоты, малыми молекулами, полипептидами, пептидами или аналогами пептидов), в присутствии липосом, адъюванта или любого фармацевтически приемлемого носителя, в форме, пригодной для назначения млекопитающим, например человеку, крупному рогатому скоту, овцам и т.д. При необходимости, лечение соединением в соответствии с изобретением можно комбинировать с более традиционными и привычными способами лечения А/Е патогенной инфекции.
Общепринятая фармацевтическая практика может быть применена для разработки приемлемых прописей и составов для назначения соединений больным, инфицированным А/Е патогеном. Любой принятый путь введения может быть использован, например парентеральный, внутривенный, подкожный, внутримышечный, интракраниальный, внутриглазничный, офтальмический, внутрижелудочковый, внутрикапсулярный, интраспинальный, интрацистернальный, интраперитонеальный, интраназальный, аэрозольный или оральное введение. Прописи могут быть в форме жидких растворов или суспензий; таблеток или капсул; порошков, носовых капель или аэрозолей.
Способы приготовления прописей хорошо известны в науке (57). Прописи для парентерального введения могут содержать, например, инертный наполнитель, стерильную воду или соль, полиалкиленгликоли, такие как полиэтиленгликоль, масла растительного происхождения или гидрогенизированные нафталины. Биосовместимый, биоразлагаемый лактидный полимер, лактид/гликолидный сополимер или полиоксиэтилен-полиоксипропиленовые сополимеры используют для контроля высвобождения соединения. Другие потенциально применимые первичные системы доставки модулирующих соединений включают этилен-винилацетатные сополимерные частицы, осмотические помпы, имплантируемые инфузионные системы и липосомы. Прописи для ингаляции могут содержать инертный наполнитель, например лактозу, или могут быть с содержанием водных растворов, например полиоксиэтилен-9-лаурила эфира, гликохолата и дезоксихолата, или могут быть масляными растворами для назначения в форме носовых капель или геля. Для лечебных или профилактических целей соединения назначаются индивидууму в количествах, достаточных для прекращения или замедления А/Е патогенной инфекции.
«Эффективное количество» соединения, в соответствии с изобретением, включает терапевтически эффективное количество или профилактически эффективное количество. «Терапевтически эффективным количеством» является количество, эффективное, в дозах и необходимом периоде времени, для достижения требуемого терапевтического результата, такого как уменьшение колонизации А/Е патогеном или выделения А/Е патогена. Терапевтически эффективное количество соединения может различаться в зависимости от ряда факторов, таких как стадия заболевания, возраст, пол, вес субъекта и способности соединения вызывать требуемый ответ у субъекта. Режимы дозирования устанавливают так, чтобы вызвать оптимальный лечебный ответ. Терапевтически эффективное количество также таково, что любой токсический или побочный эффект соединения перевешивается положительными терапевтическими эффектами. «Профилактически эффективным количеством» является количество, эффективное, в дозах и необходимом периоде времени, для достижения требуемого профилактического результата, такого как предотвращение колонизации А/Е патогеном. Как правило, профилактическая доза применяется у субъектов перед началом или на ранних стадиях заболевания, так что профилактически эффективное количество может быть меньше, чем терапевтически эффективное количество. Предпочтительный уровень для терапевтически и профилактически эффективного количества соединения может быть равен любому целому числу от 0,1 нМ до 0,1 М, от 0,1 нМ до 0,05 М, от 0,05 нМ до 15 мкМ или от 0,01 нМ до 10 мкМ.
Следует заметить, что величина дозировки может меняться при улучшении состояния больного. Для каждого конкретного субъекта устанавливают специальные режимы дозирования на время, в соответствии с его индивидуальной потребностью и профессиональным опытом специалиста, назначающего соединение или контролирующего назначение соединения. Величины дозировок, приведенные здесь, являются примерными и не ограничивают дозировок, которые могут быть выбраны практикующими врачами. Количество активного соединения в препарате может различаться в соответствии с рядом факторов, таких как стадия заболевания, возраст, пол, вес индивидуума. Режимы дозирования устанавливают так, чтобы вызвать оптимальный лечебный ответ. Например, может быть назначено единственное введение, может быть назначено несколько доз, вводимых дробно в течение определенного промежутка времени или доза может быть пропорционально уменьшена или увеличена, исходя из особенностей терапевтической ситуации. Желательным является такое составление единицы дозирования исходного препарата, которое облегчило бы его назначение и унифицировало прием.
В случае прописи вакцины, может быть разработано эффективное количество соединения по изобретению, в отдельности или в комбинации с другими соединениями, и с одним или более иммунологическим адъювантом, для вызова иммунного ответа. Адъюванты, в соответствии с изобретением, могут включать в себя эмульгаторы, мурамил дипептиды, авридин, водные адъюванты, такие как гидроксид алюминия, адъюванты, основанные на хитозане, сапонины, масла, Амфиген®, LPS, экстракты клеточной стенки бактерий, бактериальную ДНК, бактериальные комплексы, синтетические олигонуклеотиды и комбинации этого (100). Адъювант может включать экстракт клеточной стенки Mycobacterium phlei (M. phlei) (MCWE) (патент США № 4744984), ДНК M. Phlei (M-DNA), или комплекс микобактериальной клеточной стенки (МСС). Эмульгаторы включают в себя натуральные или синтетические эмульгирующие агенты. Синтетические эмульгирующие агенты включают в себя анионные агенты (например, калий, натрий и аммонийные соли лауриновой и олеиновой кислот, кальциевые, магниевые и алюминиевые соли жирных кислот, например металлосодержащие мыла, и органические сульфонаты, такие как натрия лаурил сульфат), катионные агенты (например, цетилтриметиламмония бромид), неионные агенты (например, глицериновые сложные эфиры, такие как глицерина моностеарат, полиоксиэтиленгликоля сложные эфиры и простые эфиры, и эфиры сорбитановых жирных кислот, такие как сорбитанмонопальмитат и его полиоксиэтиленовые производные, например, полиоксиэтилена сорбитанмонопальмитат). Натуральные эмульгирующие агенты включают в себя акацию, желатин, лецитин и холестерин. Другие приемлемые адъюванты включают в себя масло, такое как отдельно взятое масло, смесь масел, эмульсию масло-в-воде (например, EMULSIGENTM, EMULSIGEN PLUSTM, или VSA3), или эмульсию не-масло-в-воде (например, масляную эмульсию, эмульсию вода-в-масле или эмульсию вода-в-масле-в-воде). Масло может быть минеральным маслом, растительным маслом или животным маслом. Приемлемые животные масла включают в себя, например, масло печени трески, масло палтуса, масло американской сельди, масло хоплостета или масло печени акулы, все они коммерчески доступны. Приемлемые растительные масла включают в себя, без ограничений, масло канолы, миндальное масло, хлопковое масло, кукурузное масло, оливковое масло, арахисовое масло, сафлоровое масло, масло кунжута или соевое масло. С другой стороны, различные алифатические азотистые основания могут быть использованы как адъюванты в прописи вакцины. Например, известные иммунологические адъюванты включают в себя амины, четвертичные соединения аммония, гуанидины, бензамидины и соединения тиоурония (75). Специфичные адъювантные соединения включают в себя диметилдиоктадециламмония бромид (DDA) (патент США № 5951988) (88, 59, 85, 68, 84, 82, 83) и N,N-диоктадецил-N,N-бис(2-гидроксиэтил)пропандиамин («авридин») (патент США № 4310550, патент США № 5151267) (62). Адъювант, в соответствии с изобретением, может, например, включать в себя минеральное масло и диметилдиоктадециламмония бромид.
Вакцинные препараты могут быть получены с использованием стандартных способов, включающих в себя, но не ограниченных этим, смешивание, обработку ультразвуком и микрофлюидизацию. Адъювант может составлять примерно от 10 до 50% (об/об) от вакцины, или примерно от 20 до 40% (об/об), или примерно от 20 до 30% или 35% (об/об), или любое значение в этих границах. Соединение также может быть связано с несущей молекулой, такой как бычий сывороточный альбумин или гемоцианин лимфы улитки, для повышения иммуногенности.
В целом, соединения по изобретению должны применяться, не вызывая существенного токсичного эффекта. Токсичность соединения по изобретению определяют с использованием стандартных способов, например путем тестирования на клеточных культурах или экспериментальных животных и определения терапевтического индекса, то есть соотношения между LD50 (летальная доза для 50% популяции) и LD100 (летальная доза для 100% популяции). В некоторых обстоятельствах, однако, таких как некоторые условия заболевания, может быть необходимо назначение существенно более высоких доз соединений.
Следующие примеры предназначены для иллюстрации осуществлений по изобретению и не должны истолковываться как ограничения сферы применения по изобретению.
Пример 1
Создание мутантов
Используют следующие бактериальные штаммы: EHEC O157:H7 штамм 86//24 (32), EHEC EDL933 (изолят дикого типа E. coli O127:H7; 3), EHEC escN-(47), дикий тип EPEC E2348/69 (изолят дикого типа E. coli O127:H6; 50), C. rodentium DBS100 (ATCC 51459; 53), REPEC 0103:K-:H2 85/150 (52), E. coli HB101.
Используют следующие плазмиды:
Для ПЦР и обратной ПЦР обычно использовали амплификационную систему проверочного считывания ELONGASE (GIBCO BRL/Life Technologies) для снижения уровня ошибок ПЦР. Продукты ПЦР клонировали с использованием TOPO TA Cloning Kit от Invitrogen, или с pCR2.1-TOPO, или с pCRII-TOPO. Последовательность ДНК определяли с использованием Taq Dye-терминаторного способа и автоматического 373А ДНК секвенатора (Applied Biosystems). Для рутинного клонирования, трансформации и инфекции бактерии выращивали в агаре Luria-Bertani (LB) или в бульоне LB с добавлением соответствующих антибиотиков, при 37ºС. Применяли различные антибиотики в следующих концентрациях: ампициллин 100 мкг/мл, карбенициллин 100 мкг/мл, канамицин 50 мкг/мл и хлорамфеникол 30 мкг/мл. Рост на среде Eagle в модификации Dullbecco (DMEM) использовали для вызывания экспрессии гена LEE и секреции белка типа III.
sacB-основанный аллельный обмен (14) и систему лямбда Red рекомбиназы (17) использовали для создания мутантов. В целом, 75% или более внутреннего содержания каждого гена удаляли для уверенности в том, что функция гена нарушена. Ген ler был мутирован с помощью лямбда red рекомбиназного способа, гены ler, orf11/grlA и cesT были мутированы способом sacB-основанного аллельного обмена. Двойной мутант ler/orf11 также был создан с использованием sacB-основанного способа. Создание мутантов tir и escD было описано ранее (20, 56). Мутанты были мутантами с делецией внутри рамки считывания, с введением ферментного сайта рестрикции (или Nhe I, или Bam HI, или Sal I) в место делеции, как описано ниже:
Эти мутанты были верифицированы с помощью реакций ПЦР. Комплементарность тестировали для Δtir, Δler, и Δorf11 мутантов путем введения соответствующего гена в плазмиду. Все эти гены могут быть комплементарны, подтверждая, что мутации, созданные обоими способами аллельного обмена не оказывают отрицательного влияния на функцию нижележащих генов и являются, таким образом, неполярными.
Для создания EHEC-pNleA-HA, кодирующий участок nleA амплифицировали с использованием амплификационной системы проверочного считывания ELONGASE (Invitrogen) и следующих праймеров: Z6024F: 5'AGATCTGAAGGAGATATTATGAACATTCAACCGACCATAC (SEQ ID NO: 44); Z6024R: 5'CTCGAGGACTCTTGTTTCTTCGATTATATCAAAG (SEQ ID NO: 45). Продукты ПЦР клонировали с использованием TOPO TA Cloning Kit (Invitrogen) и последовательность ДНК верифицировали с использованием Taq Dye-терминаторного способа и автоматического 373А ДНК секвенатора (Applied Biosystems). Затем продукт субклонировали в pCRespG-2HA/BglII, pACYC-производную плазмиду, сконструированную для управления экспрессией белка от C. rodentium EspG промотора и для добавления двух молекул гемагглютинина (НА) к С-концу экспрессируемого белка. Конструкции плазмиды были затем введены в дикий тип ЕНЕС и ЕНЕС escN- с помощью электропорации.
Мутант с делецией в nleA штамма ЕНЕС, устойчивого к налидиксовой кислоте, создали sacB-основанным аллельным обменом (29). Два фрагмента ДНК, которые фланкируют nleA амплифицировали способом ПЦР с использованием хромосомной ДНК ЕНЕС как матрицы.
Фрагмент А амплифицировали способом ПЦР с использованием праймера NT10 5'CCGGTACCTCTAACCATTGACGCACTCG (SEQ ID NO: 46) и праймера NT11 5'AACCTGCAGAACTAGGTATCTCTAATGCC (SEQ ID NO: 47) для создания продукта с 1,3 т.н.п.
Фрагмент В амплифицировали с использованием праймера NT12 5'AACCTGCAGCTGACTATCCTCGTATATGG (SEQ ID NO: 48) и праймера NT13 5'CCGAGCTCAGGTAATGAGACTGTCAGC (SEQ ID NO: 49) для создания продукта с 1,3 т.н.п.
Фрагменты А и В затем инкубировали в течение 1 часа с PstI и затем фермент инактивировали нагреванием до 65ºС в течение 20 минут. Приблизительно 50 нг каждого обработанного фрагмента связывали Т4 ДНК лигазой в течение 1 часа при комнатной температуре. Реакцию связывания разводили 1/10 и 1 мкл добавляли в ПЦР с использованием праймеров NT10 и NT13. Полученный в результате ПЦР продукт с 2,3 т.н.п. затем инкубировали с SacI и KpnI, связывали с соответствующими участками pRE112 (14) и трансформировали в DH5αλpir для создания pNT225. pNT225 трансформировали в конъюгативный штамм SM10λpir, который служил в качестве донорского штамма в конъюгации с диким типом ЕНЕС. Устойчивые к налидиксовой кислоте и хлорамфениколу экзоконъюгаты отбирали на LB агаре. Затем экзоконъюгаты помещали на LB агар, содержащий 5% (об/об) сахарозы, без NaCl. Полученные в результате колонии затем исследовали на чувствительность к хлорамфениколу, после чего идентифицировали с помощью ПЦР изоляты с делецией nleA и утраченными последовательностями плазмиды. Мутантов с делецией nleA затем изолировали и использовали в дальнейшей работе. Мутант C. rodentium создали с использованием ПЦР и применяли для создания, в pRE118 (14), вектора-«самоубийцы», несущего внутреннюю делецию nleA.
Использовали следующие праймеры: dellF: 5'GGTACCACCACACAGAATAATC (SEQ ID NO: 50); dellR: 5'CGCTAGCCTATATACTGCTGTTGGTT (SEQ ID NO: 51); del2F: 5'GCTAGCTGACAGGCAACTCTTGGACTGG (SEQ ID NO: 52); del2R: 5'GAGCTCAACATAATTTGATGGATTATGAT (SEQ ID NO: 53). Полученную в результате плазмиду вводили в C. rodentium с помощью электропорации для создания антибиотикоустойчивого меродиплоидного штамма. Отсутствие плазмидных последовательностей после второго эпизода рекомбинации отбирали, как описано выше. Антибиотикочувствительные, сахарозоустойчивые колонии верифицировали на наличие соответствующей рекомбинации с помощью ПЦР, применяя праймеры, фланкирующие участки делеции. Отсутствие NleA подтверждали с помощью вестерн-блота полных клеточных лизатов с поликлональной анти-NleA-антисывороткой.
Изучение общих и секретируемых белков/протеомика
Секретируемые белки получали, как описано ранее (51).
Штаммы C. rodentium выращивали в течение ночи при постоянном встряхивании в 4 мл бульона Luria (LB) при 37ºС. Культуры пересевали 1 к 50 в 4 мл среды Игла в модификации Дульбекко (DMEM), которую предварительно инкубировали в течение ночи в инкубаторе культуры ткани (при 5% СО2), и выращивали без встряхивания в течение 6 часов в том же инкубаторе для вызывания экспрессии гена LEE. Культуры центрифугировали дважды при 13000 об/мин в течение 10 мин. Для удаления бактерий и супернатант преципитировали 10% трихлоруксусной кислотой (ТСА) для концентрирования белков, секретированных в культуральную среду. Бактериальный осадок растворяли в 2X SDS-PAGE буфере и принимали за общий бактериальный белок. Секретированные белки, преципитированные из супернатанта, также растворяли в 2X SDS-PAGE буфере, а оставшуюся ТСА нейтрализовывали 1 мкл насыщенного Tris. Объемы буфера, использованные для ресуспендирования бактериального осадка и секретированных белков, нормализовывали до OD600 культур для обеспечения равного содержания в образцах. Секретированные белки анализировали в 12% или 17% SDS-PAGE и окрашивали 0,1% Coomassi Blue G250. Для вестерн-блота-анализа общие и секретированные белки разделяли в SDS-PAGE и переносили на нитроцеллюлозную мембрану (Bio-Rad). Использовали крысиные поликлональные антитела против His-меченного Tir цитробактера и мышиные моноклональные антитела против EPEC EspB. Затем применяли стандартные протоколы вестерн-блота ECL (Amersham Life Science).
Дикие типы ЕНЕС и ЕНЕС CVD451 выращивали в течение ночи на среде LB. Затем культуры разбавляли 1:100 в минимальной среде М-9 с добавлением 44 мМ NaHCO3, 8 мМ MgSO4, 0,4% глюкозы и 0,1% казаминовых кислот и растили без встряхивания при 37ºС в 5% СО2 до OD600 от 0,6 до 0,8.
Секретированные белки собирали центрифугированием культур при 8000g в течение 30 минут, отделяя супернатанты от осадков. Супернатанты фильтровали через фильтры с размером пор 0,45 микрон и определяли концентрацию белка с помощью анализа BCA (Sigma). Белки готовили для электрофореза путем преципитации с 1/9 объемом 100% ледяной ТСА, на льду, в течение от 45 до 120 мин, после чего центрифугировали при 17600g, в течение 30 мин. Осадки промывали в холодном 100% ацетоне и растворяли в 1Х laemmli буфере (для 1-мерных SDS-PAGE гелей) или в буфере для приготовлении образца для 2D гелей (8 М мочевины, 2 М тиомочевины, 4% CHAPS, 20 мМ Tris, 0,002% бромофенола синего). Для 2D гелей предварительно добавляли DDT до 6 мг/мл и IPG буфер (рН 3-10: Amersham Biosciences) до 0,5%. 18 см Immobiline Dry Strips (pH3-10: Amersham) регидратировали в образце в течение ночи при 20ºС. Затем образцы концентрировали при 15ºС до 65000 Vh. После концентрирования стрипы уравновешивали в ЕВ+10 мг/мл DTT в течение 15 минут и затем в ЕВ+25 мг/мл иодоацетамида в течение 15 минут (ЕВ - это 50 мМ Tris, 6 M мочевины, 30% глицерина, 2% SDS, рН 8,8). Уравновешенные стрипы наносили на верхнюю часть SDS-PAGE гелей большого формата (12% или 14% акриламида) с использованием 0,5% раствора агарозы в SDS-PAGE буфере+0,002% бромофенола синего, и гели подвергали электрофорезу, пока краситель не выйдет за пределы геля.
Гели окрашивали Sypro Ruby согласно инструкциям производителей (BioRad) и визуализировали на светостоле UV или с помощью MS/MS на масс-спектрометре LCQ Deca с ионной ловушкой (Thermo Finnigan), оснащенном системой жидкостной хроматографии с нанопотоком (LC Packings-Dionex). Из гелей, визуализированных на светостоле UV, интересующие пятна выделяли вручную. Внутригелевое расщепление белков проводили на Investigator ProGest Robot (Genomic Solutions, Ann Arbor, MI), как описано (23). Образцы с высоким содержанием белка анализировали с помощью LC-MS системы, состоящей из системы жидкостной хроматографии с нанопотоком, оснащенной FAMOS Autosampler (LC Packings-Dionex, San Francisco, CA), и масс-спектрометра LCQ Deca с ионной ловушкой (Thermo Finnigan, San Jose, CA) (24).
Колонки с обратной фазой PicoFrit Columns PFC7515-PP18-5 (New Objective, Woburn, MA, USA) использовали для разделения пептидов и эффлюент с колонки распыляли непосредственно в масс-спектрометре. Использовали скорость потока 200 нл/мин, и общее время детекции одного образца было равно 45 мин.
Образцы с низким содержанием белка анализировали на масс-спектрометре API QSTAR Pulsar Hybryd MS/MS (Applied Biosystems/MDS SCIEX, Concord, Canada) (12), оснащенном Nanospray Ion Source (Proxeon, Odense, Denmark). Перед анализом образцы очищали и концентрировали на ZipTips (Millipore, Billerica, MA). API QSTAR Pulsar также использовали для сиквенса пептидов de novo.
Спектры исследовали по базе данных NCBI (Bethesda, MD) с помощью поисковых систем Mascot (Matrixscience) или Sonar (Proteometrics Canada Ltd.).
Конструкция транскрипционных слияний cat и анализ CAT
ПЦР фрагменты, несущие промоторы и все вышележащие регуляторные элементы ler (LEE1) и tir (LEE5) цитробактера расщепляли с помощью Bam HI Hind III и клонировали в плазмиду pKK232-8, содержащую лишенный промоторов ген cat. Здесь показаны позиции, занимаемые клонированными фрагментами. Активность САТ, определяемую этими слияниями в различных штаммах цитробактера, определяли, как описано выше (21, 22). Образцы отбирали в различные промежутки времени из бактериальных культур, росших на DMEM, как описано выше.
Анализ последовательностей и способы биоинформатики
Анализ последовательностей ДНК и белков и поиск гомологии с помощью BLASTN, TBLASTN и BLASTP проводили с использованием программ, доступных на вебсайте NCBI (http://www.ncbi.nih.org/). Использовали базы данных с сайтов NCBI, Sanger Genome Centre (http://www.sanger.ac.uk/Projects/Microbes) и SwissProt (http://www.expasy.org/sprot/). Позиции LEE PAI, так же как и профагов, в геноме ЕНЕС были получены из данных, созданных программой IslandPath (http://www.pathogenomics.sfu.ca/islandpath/) (13).
Саузерн-блот анализ
Образцы геномной ДНК для саузерн-блот анализа готовили с использованием набора DNeasy Tissue (Qiagen). Пробы готовили путем расщепления pNleA-HA ферментами SalI и BglII для получения фрагментов с 500 н.п., которые метили с использованием набора BrightStar Psoralen-Biotin Nonisotopic Labeling (Ambion).
Пять микрограмм каждого образца геномной ДНК полностью расщепляли в 25 единицах BamHI, EcoRI и PstI в течение ночи. Образцы разводили в 1% агарозном геле с помощью электрофореза и перемещали на найлоновую мембрану BrightStar-Plus (Ambion) путем пассивной, слабощелочной нисходящей элюции. ДНК перекрестно связывали с мембраной облучением мембраны УФ светом в течение 2 мин, после чего высушивали 30 мин при 80ºС.
Мембрану прегибридизировали промыванием в 10 мл ультрачувствительного гибридизационного буфера ULTRAhyb (Ambion) при 42ºС в течение 30 мин. Десять микролитров полученной пробы затем добавляли к прегибридизированной мембране в буфере и пробу гибридизировали к мембране при 42ºС в течение ночи. Мембрану промывали 2 раза по 5 мин в моющем буфере пониженной жесткости (Ambion) и 2 раза по 15 мин в моющем буфере повышенной жесткости (Ambion) при комнатной температуре. Гибридизированную пробу изучали с помощью набора BrightStar BioDetect Nonisotopic Detection (Ambion), после чего фотографировали на пленку Kodak.
Создание анти-NleA антисыворотки
Кодирующий участок nleA амплифицировали из геномной ДНК ЕНЕС и клонировали в his-меченный вектор экспрессии (рЕТ28а, Novagen), используя следующие праймеры: 5'TTCCATATGAACATTCAACCGACC (SEQ ID NO: 54) и 5'GGAATTCAATAATAGCTGCCATCC (SEQ ID NO: 55). Эту плазмиду вводили в BL21 (λDE3), выращивали до оптической плотности 600 (А600) от 0,8 и индуцировали с помощью 0,5 мМ IPTG при 20ºС в течение 16 часов. Белок, меченный His, очищали на колонке Ni-NTA, согласно инструкциям производителя (Qiagen). Фракции, содержащие NleA, объединяли и добавляли тромбин (500:1), белок диализировали в течение ночи против 20 мМ tris рН 8,2, 50 мМ NaCl. На следующий день белок помещали на колонку monoQ FPLC с использованием линейного градиента от 50 до 500 мМ NaCl. Фракции, содержащие NleA, объединяли. После этой стадии чистота белка была >90%. Очищенный белок использовали для иммунизации двух крыс Sprague Dawley мужского пола, 300 мкг/крыса, с применением полного адъюванта Фрейнда (Sigma), и полученную антисыворотку аффинно очищали с использованием активированного геля с иммуноафинной поддержкой Affi-Gel 15, согласно инструкциям производителя (BioRad). Для иммунофлюоресцентных экспериментов антисыворотку затем очищали абсорбцией против ацетонсодержащих порошков, полученных из клеток HeLa и из ЕНЕС NleA, как описано в (45). Специфичность антисыворотки подтверждали анализом вестерн-блота клеточных экстрактов из дикого типа ЕНЕС и ЕНЕС NleA.
Иммуноблот-анализ
Образцы для анализа путем вестерн-блота разделяли путем SDS-PAGE (от 9% до 12% полиакриламид). Белки переносили на нитроцеллюлозу и блокировали иммуноблот в 5% растворе обезжиренного сухого молока (NFDM) в TBS, рН 7,2, содержащем 0,1% Tween 20 (TBST), в течение ночи при 4ºС, и затем инкубировали с первичными антителами в 1% NFDM TBST в течение 1 ч при комнатной температуре (RT). Мембраны промывали 6 раз в TBST и затем инкубировали с 1:5000 раствором конъюгированных с пероксидазой хрена козьих анти-мышиных (H+L) антител (Jackson ImmunoResearch Laboratories Inc.) в течение 1 ч при RT. Затем мембраны промывали, как описано выше. Комплексы антиген-антитело визуализировали улучшенным набором хемолюминесцентного определения (Amersham), после чего фотографировали на пленку Kodak (Perkin Elmer). Использовали следующие первичные антитела: анти-НА.11 (Covance), DnaK (Stressgen), анти-EHEC Tir, анти-NleA (данное исследование), анти-кальнексин (Stressgen), анти-кальретикулин (Affinity Bioreagents), анти-тубулин (Sigma).
Иммунофлюоресценция
Клетки HeLa выращивали на стеклянном покрытии в 24-луночных плашках для клеточных культур и инфицировали в течение 6 часов 1 мкл (ЕНЕС) выдержанной в течение ночи культуры с OD ~0,4. Через 6 часов после инфицирования клетки промывали 3 раза в PBS, содержащем Са2+ и Mg2+, и фиксировали в 2,5% параформальдегиде в PBS в течение 15 мин при комнатной температуре. Клетки делали проницаемыми в 0,1% сапонине в PBS, блокировали в 5% козьей сыворотке или 5% BSA в PBS+0,1% сапонина и инкубировали со следующими первичными антителами, разведенными в блокирующем растворе в течение 1 часа при комнатной температуре: анти-EHEC Tir, 1:1000; анти-E.coli О157 (Difco), 1:200; аффинно-очищенные крысиные поликлональные анти-NleA (данное исследование), 1:100; анти-маннозидаза II (любезно предоставленная Dr. Marilyn Farquhar, UCSD), 1:1000. После 3 промываний в PBS/сапонине, клетки инкубировали во вторичных антителах (Alexa-488 или -568-конъюгированные анти-мышиные, кролика, крысы (Molecular Probes) 1:400), в течение 30 мин при комнатной температуре, промывали 3 раза в PBS/сапонине и один раз в PBS и помещали на стеклянные пластинки с использованием mowiol+DABCO. Для визуализации полимеризованного актина, к вторичным антителам добавляли Alexa-488-конъюгированный фаллоидин (Molecular Probes) в соотношении 1:100. При обнаружении клетки инкубировали с 5 мкг/мл брефелдином A (Boehringer Mannheim) в течение 30 минут перед фиксацией. Изображения получали с использованием микроскопа Zeiss Axioskop, оснащенного цифровой камерой Empix DVC1300, и анализировали с использованием программного обеспечения визуализации Northern Eclipse, или микроскопа BioRad Radiance Plus confocal, с использованием программного обеспечения Lasersharp.
Фракционирование инфицированных реципиентных клеток
Для каждого образца две одинаковые 100 мм чашки с культурой клеток HeLa инфицировали диким типом EHEC-pNleA-HA или EHECescN-pNleA-HA, с использованием исходной MOI 1:10. Через 6 часов после инфицирования клетки отмывали три раза ледяным PBS и подвергали биохимическому фракционированию, как описано ранее (30, 49). Кратко, клетки ресуспендировали в 300 мкл гомогенизационного буфера (3 мМ имидазола, 250 мМ сахарозы, 0,5 мМ EDTA, рН 7,4) с добавлением коктейля ингибиторов протеаз COMPLETE (Roche), и механически разрушали пропусканием через иглу 22 размера. Гомогенат центрифугировали на низкой скорости (3000g) в течение 15 минут при 4ºС для осаждения неразрашенных клеток, бактерий, ядер и компонентов клеточного скелета (низкоскоростной осадок). Супернатант подвергали высокоскоростному ультрацентрифугированию (41000g) в течение 20 минут при 4ºС в роторе TLS55 центрифуги TL100 (Beckman) для отделения мембран реципиентных клеток (осадок) от цитоплазмы (супернатант). Осадки ресуспендировали в 300 мкл 1Х Laemmli буфере, а супернатант добавляли к 1Х Laemmli буферу с использованием 5Х маточного раствора. Равные объемы всех фракций разделяли путем SDS-PAGE (9% полиакриламид), переносили на нитроцеллюлозу и анализировали способом вестерн-блота.
Для экстракционных исследований мембран, связанных с NleA, две 100 мм чашки с культурой инфицированных клеток HeLa фракционировали, как описано выше для каждого условия экстракции. Высокоскоростные осадки (фракция мембран реципиента) ресуспендировали в 300 мкл одного из следующих экстракционных буферов: (i) 10 мМ Tris, 5 мМ MgCl2, pH 7 M NaHCO3, 5 мМ MgCl2, pH 11,4; (iv) 10 мМ Tris, 5 мМ MgCl2, 1% Triton X-100, pH 7,4. Экстракцию проводили на льду путем пипетирования образцов вверх и вниз каждые 5 минут в течение 30 минут, и образцы рецентрифугировали при 100000g в течение 30 минут. Осадок (нерастворимая фракция) ресуспендировали в 300 мкл Laemmli буфера, а супенатант (растворимая фракция) преципитировали в 10% трихлоруксусной кислоте на льду в течение 30 минут, отмывали в 100% ацетоне и ресуспендировали в 300 мкл Laemmli буфера. Равные объемы разделяли путем SDS-PAGE (9% полиакриламид), переносили на нитроцеллюлозу и анализировали способом вестерн-блота.
Анализ инфицирования мышей C. rodentium
Пятинедельных мышей C3H/HeJ (Jackson Laboratory) и аутбредных швейцарских мышей NIH (Harlan Sprague-Dawley) выращивали в виварии Университета Британской Колумбии в строгом соответствии с правилами, установленными Комитетом защиты животных Университета Британской Колумбии и Канадским советом по использованию лабораторных животных. Дикий тип C. rodentium и мутанты с делецией nleA выращивали на LB бульоне в течение ночи при постоянном встряхивании при 200 об/мин и 100 мкл культур использовали для инфицирования мышей через пищеварительный тракт. Инфекционный агент титровали последовательными разведениями и посевами и рассчитывали до количества 4×108 КОЕ/мышь для обеих групп. Для инфицирования высокочувствительных C3H/HeJ мышей C. rodentium, выживание инфицированных мышей определяли ежедневно в течение курса инфицирования. Для оценки гиперплазии толстого кишечника, первые 4 см дистальной толстой кишки, начиная с анального отверстия, отбирали и взвешивали после удаления всех фекальных масс. Для оценки бактериальной колонизации, ткани толстой кишки и фекальные массы гомогенизировали в PBS, с использованием Polytron Tissue Homogenizer, и последовательно разводили перед посадкой на агар MacConkey (Difco Laboratories). Ткань толстой кишки и фекальные массы объединяли для определения общего бактериального обсеменения толстой кишки мыши к моменту усыпления. Агар MacConkey является селективным для грамотрицательных бактерий, на котором C. rodentium образует колонии с высокой степенью отличия и характерными чертами морфологии, нетипичными для E. coli (26). Для гистологического анализа последние 0,5 см толстой кишки инфицированной мыши фиксировали в 10% нейтральном буферном формалине, выдерживали, разрезали на фрагменты по 3 мкм и окрашивали гематоксилином и эозином. Гистологический анализ проводили в Лаборатории морфологических работ отделения патологии и медицинской лаборатории университета Британской Колумбии.
Пример 2
Анализ регуляции экспрессии гена LEE
Чтобы выяснить, какие гены в LEE регулируют экспрессию гена LEE у C. rodentium, анализировали LEE мутантов на экспрессию EspB и Tir, которые кодируются оперонами LEE4 и LEE5 (Tir) соответственно. Общие клеточные лизаты бактерий, выращенных на DMEM, анализировали способом вестерн-блота с анти-Tir и анти-EspB сыворотками. Эти результаты подтвердили важную роль Ler в экспрессии LEE, так как Tir и EspB не вырабатывались в Δler. Как и ожидалось, Δtir и ΔespB не вырабатывали Tir и EspB соответственно. Tir не визуализировали в ΔcesT, в соответствии с ролью CesT, как шаперона для стабильности и секреции Tir (18, 19). К удивлению, другой LEE-кодируемый белок, Orfl1, также был необходим для экспрессии Tir и EspB. Экспрессия Tir и EspB в Δorfl1 соответствовала плазмиде, несущей только Citrobacter orfl1 (фиг.8). Ген orfl1 широко представлен в А/Е патогенах, и как ЕНЕС, так и ЕРЕС orfl1 комплементарны Citrobacter Δorfl1 (фиг.8), показывая, что Orfl1 функционально эквивалентен в положительной регуляции экспрессии гена LEE в А/Е патогенах.
Анализ последовательностей показывает, что Orfl1/GrlA демонстрирует 23% идентичности CaiF, транскрипционному активатору оперонов cai и fix Enterobacteriaceae (15) и 37% идентичности полученной аминокислотной последовательности нехарактеризованного продукта Salmonella, кодируемого геном, находящимся ниже края оперона std (16) (фиг.7). На фигуре этот гомолог Salmonella показан как SGH (Salmonella GrlA гомолог). Все три белка содержат предсказанную helix-turn-helix мотивную характеристику ДНК связывающих белков.
Для определения иерархии Orfl1 и Ler в регуляции экспрессии гена LEE, создали двойного мутанта ler и orfl1 в C. rodentium. Тогда как экспрессия Tir и EspB в Δler Δorfl1 может быть частично восстановлена экспрессией Ler в транс-положении, подобная экспрессия Orfl1 не имеет такого эффекта (фиг.8), позволяя предположить, что Orfl1 действует выше Ler в каскаде регуляции. Расширенный анализ праймеров подтверждает эту регуляторную иерархию, показывая, что промотор Citobacter ler подобен ЕРЕС ler и его экспрессия снижена в Δorfl1.
Роль Orfl1 в регуляции экспрессии ler была в дальнейшем продемонстрирована при наблюдении активностей транскрипционных слияний между регуляторными участками оперонов LEE1 (Ler) (pLEE1-CAT) или LEE5 (Tir)(pLEE5-CAT) и репортерным ген cat в штаммах Citrobacter WT, Δler и Δorfl1, выращенных на модифицированной среде Дульбекко (DMEM) в течение 6 часов. Активность слияния LEE1-cat уменьшалась в Δorfl1, а активность слияния LEE5-cat выраженно снижалась как в Δler, так и в Δorfl1. Эти результаты показывают, что Orfl1 является новым положительным регулятором экспрессии Ler, который существенно способствует экспрессии других оперонов LEE. Так как Orfl1 действует выше, чем Ler, в каскаде регуляции, он был назван GrlA (для общего регулятора LEE-активатора).
Пример 3
Идентификация эффекторов, секретируемых LEE-кодируемым TTSS
А/Е патогены секретируют некоторые белки в тканевую культуру или минимальную среду, но секретируемые белки являются в основном транслокаторами EspA, EspB и EspD. Секретируемые белки концентрировали преципитацией с ТСА из супернатанта бактериальных культур, выращенных на DMEM, и анализировали с использованием 12% SDS-PAGE, после чего окрашивали Куммасси Синим. C. rodentium, несущий плазмиду, содержащую orfl1/grlA, секретировал, по меньшей мере, на 300% больше EspA, EspB и EspD, чем штамм WT.
Для выявления эффекторов, кодированных LEE цитробактера, метили различные LEE-кодируемые белки, не вовлеченные в TTS и адгезию клеток-реципиентов, двойным гемаглютининовым (2Н) эпитопом на углеродном конце и анализировали их секрецию в WT и мутантных C. rodentium. Только Tir, EspG, EspF, EspH и Мар секретировались LEE-кодируемым TTSS в C. rodentium, позволяя предположить, что LEE кодирует только 5 эффекторов. Ранее невыявленный белок с молекулярной массой 54 кДа (р54) был легко определен окрашиванием Куммасси в мутанте, который также имел высокий уровень секреции Tir, позволяя предположить, что он представляет собой новый мнимый эффектор, кодируемый вне LEE.
Для идентификации р54 и определения, действительно ли дополнительные эффекторы кодируются вне LEE в C. rodentium, воспользовались способностью GrlA увеличивать экспрессию гена LEE и/или секрецию типа III и ввели плазмиду grlA в мутанты, которые секретируют эффекторы, но не транслокаторы. Сверх-экспрессия GrlA значительно увеличивает (более чем на 400%) секрецию Tir в этих мутантах, при отсутствии секреции транслокаторов. Наблюдали, по меньшей мере, 6 дополнительных секретируемых белков, что означает, что LEE-кодируемый TTSS секретирует несколько дополнительных белков, не кодируемых LEE.
Для идентификации этих белков секретируемые белки анализировали с использованием 2-D гелей. Так как для некоторых из LEE-кодируемых эффекторов (EspF, EspH и Мар) были предсказаны щелочные значения pI, с EspF, имеющим максимальный pI 11,00, секретируемые белки были сначала сфокусированы на Immobiline Dry Strips с кислотным (рН 3-10) и щелочным (рН 6-11) градиентами, а затем разделены в 12% и 14% SDS-PAGE соответственно. Гели окрашивали Sypro Ruby, выбранные белковые пятна извлекали вручную и анализировали с использованием масс-спектрометрии и построения белков de novo.
Этот анализ подтвердил, что LEE-кодируемые Tir, EspF, EspG, EspH и Мар были секретированы типом III (Таблица 2).
В дополнение к пяти LEE-кодируемым эффекторам, идентифицировали семь не-LEE-кодируемых секретируемых белка, возможно, являющихся эффекторами. Эти секретируемые белки, кодируемые вне LEE, были соответственно обозначены как NleA (p54), NleB, NleC, NleD, NleE, NleF и NleG (QQENAPSS(I/L)QTR; SEQ ID NO: 59) (для не-LEE-кодируемых эффекторов), чтобы отличить их от LEE-кодируемых секретируемых белков/эффекторов (Esp) (таблица 2). Среди семи идентифицированных белков только NleG был уникален для C. rodentium, а остальные 6 белков имели постоянно присутствующие гомологи в EHEC О157 (таблица 2). EHEC гомологи кодируются генами, объединенными в трех отдельных районах генома, при этом каждый район кодирует, по меньшей мере, два белка, демонстрирующих гомологию к секретируемым белкам C. rodentium (таблица 2). Гены Z6024 и Z6020, кодирующие гомологи NleA и NleF, расположены в EHEC O-районе 71, связанном с профагом CP-933P. Сходным образом, гены Z4328 и Z4329, кодирующие гомологи NleB и NleE, расположены в EHEC O-районе 122, а гены, кодирующие гомологи NleC и NleD (Z0986 и Z0990), расположены в O-районе 36 (таблица 2, Фиг.9). Кроме того, Z4328 (O-район 122) имеет сильную гомологию с Z0985, геном, расположенным после Z0986 в O-районе 36.
Гомологи всех шести новых EHEC эффекторных генов также представлены и сходно организованы в EHEC, последовательность генома которого определена (http://www.sanger.ac.uk/Projects/Microbes/). Кроме Z6024, демонстрирующего 89% нуклеотидной идентичности гену EHEC, остальные 5 генов EHEC показывают более чем 95% идентичность их гомологам в EHEC. Более того, некоторые из этих эффекторов также постоянно присутствуют в других патогенных бактериях. NleD/Z0990 имеет сходство с эффектором типа III HopPtoH томата P.syringae pv. (41, 42). NleE/Z4329 имеет значительную гомологию с RorfD EPEC кролика (REPEC) и Orf212 S. flexneri (8, 33), тогда как NleB/Z4328 имеет значительную гомологию с RorfE REPEC и двумя гипотетическими белками S.typhimurium. Гены для Z4328 и Z4329 смежно расположены в EHEC, сходно с расположением генов rorfD и rorfE в REPEC (8). Однако rorfD и rorfE расположены после LEE в REPEC, тогда как их аналоги в ЕНЕС находятся в районе (O-район 122), отдаленном от LEE. O-район 122 ЕНЕС, несущий Z4328 и Z4329, также содержит гены, кодирующие два цитотоксина, так же, как и гомолог PagC, важный Pho/PhoQ-регулируемый вирулентный фактор S. enterica (3, 43). Три O-района в ЕНЕС, которые кодируют новые эффекторы, имеют динуклеотидное смещение и низкое GC% содержание, отличительные особенности PAI (9). Кроме того, они либо ассоциированы с профагом, либо фланкированы мобильными инсерционными последовательностями, и не представлены в геноме не-патогенной E. coli (3), позволяя предположить горизонтальный перенос этих генов. В целом, это позволяет предположить важное значение этих районов и вновь идентифицированных эффекторов Citrobacter и ЕНЕС в вирулентности. Это также показывает, что, хотя они отличаются друг от друга, соответствующие патогены поддерживают удивительно постоянный набор PAI, несмотря на различающиеся локализации PAI в бактериальных хромосомах.
Пример 4
Идентификация NleA
Хотя тип III-секреция считается, как правило, контакт-зависимой (46), определенные условия культуры in vitro могут побудить ЕНЕС секретировать эффекторы типа III в экстрацеллюлярную среду в процессе роста в жидкой культуре (28, 51). Супернатанты культуры готовили из дикого типа ЕНЕС (wt) и тип III-секретирующего мутанта (escN-), выращенного в условиях, индуцирующих тип III-секрецию. Анализ секретированных белков с использованием SDS-PAGE выявил один избыточный белок с большой молекулярной массой, общий для секретированных белков как образцов дикого типа, так и escN-, и несколько других избыточных белков, уникальных для образца дикого типа (Фиг.10А). Секретированные белки разделяли 2-мерным электрофорезом и избыточные выделенные белковые пятна извлекали из геля и анализировали масс-спектрометрически (Фиг.10В, Таблица 1).
(кДа)
(кДа)
Пятно № 1, которое присутствовало в супернатантах культур как дикого типа, так и escN- идентифицировали как EspP, плазмид-кодируемый белок ЕНЕС, который секретируется по аутотранспортному механизму, независимому от секреции типа III (25). Четыре основных пятна (№ 2, 3, 4, 5) были уникальны для супернатантов дикого типа. Три из этих пятен идентифицировали как известные секретируемые белки типа III, кодируемые LEE: Tir (пятно № 2), EspB (пятно № 4) и EspA (пятно № 5) (фиг.10В, таблица 1). Пятно № 3 идентифицировали как белок с предсказанной молекулярной массой 48 кДа, кодируемый открытой рамкой считывания генома ЕНЕС, но вне LEE (фиг.10С). Этот белок назвали NleA, для не-LEE-кодируемого эффектора А.
Пример 5
Характеристика локуса, содержащего nleA
Ген nleA расположен в О-районе: районе генома ЕНЕС, отсутствующего в геноме непатогенного штамма К-12 E. coli (3). Район между последним геном, постоянно присутствующим в остове К12 E. coli (YciE), и генами, кодирующими структурные белки фага, содержит несколько фрагментов мнимой транспосазы и один фрагмент мнимой рекомбиназы (фиг.11А). Анализ этого района с помощью Islandpath, программы, созданной для идентификации PAI (13), показывает, что все ORF этого района имеют динуклеотидные смещения и содержание GC, отличные от показателей генома ЕНЕС. 10 ORF этого района имеют содержание GC, по меньшей мере, на 1 стандартное отклонение ниже показателей генома ЕНЕС, тогда как 2 из 6 ORF имеют содержание GC, по меньшей мере, на 1 стандартное отклонение выше показателей генома ЕНЕС. Взятые вместе, эти результаты позволяют предположить, что nleA расположен в PAI, содержащем горизонтально-перемещенные гены. Несколько других ORF этого района имеют свойства, позволяющие предположить их роль в вирулентности, включая мнимый шаперон (Z2565) и два белка, сходных с тип III-секретируемыми белками других патогенов (Z6021, Z6020).
Для дальнейшего исследования природы и распространенности гена nleA получали пробы nleA и использовали саузерн-блот на панели геномной ДНК других А/Е патогенов и непатогенного штамма E. coli. Как показано на фиг.11В, ген nleA был представлен во всех исследованных А/Е патогенах, но отсутствовал в непатогенной E. coli. Анализ в процессе геномной последовательности ЕРЕС выявил, что nleA находится в непосредственной близости от места инсерции фага в геноме ЕРЕС. nleA также присутствует в профаге интимин-позитивного, не-О157 ЕНЕС штамма, О84:Н4, но отсутствует в непатогенных штаммах E. coli, уропатогенной E. coli, которые не содержат LEE. nleA также отсутствует в других TTSS-содержащих патогенах, таких как Salmonella и Shigella. Таким образом, nleA представляется специфичным компонентом А/Е патогенов. Многочисленные исследования последовательностей гена nleA из C. rodentium, ЕРЕС, ЕНЕС и О84:Н4 выявили высокую степень устойчивости данной последовательности в этих четырех А/Е патогенах (фиг.11С).
Пример 6
NleA секретируется системой секреции LEE-кодируемого типа III
ЕНЕС и ЕРЕС эффекторы LEE-кодируемого TTSS, описанные в настоящее время, кодируются в LEE, в непосредственной близости к генам, кодирующим секрецию самого аппарата. Для определения, зависима ли секреция NleA от LEE-кодируемого TTSS, эпитоп-меченную версию NleA экспрессировали из плазмиды в дикий тип ЕНЕС и escN-штамм, которые являются дефицитными по секреции типа III (47). Как показано на фиг.12А, хотя НА-меченный NleA экспрессировали до одинакового уровня в диком типе ЕНЕС и escN-ЕНЕС, белок секретировался в экстрацеллюлярную среду только бактериями NleA-НА-трансформированного дикого типа. DnaK, несекретируемый бактериальный белок, использовали в качестве контроля отсутствия несекретируемых белков в образцах, секретирующих белок (фиг.12В). Tir секретировался неизмененным и NleA-НА-трансформированным штаммами дикого типа, но не секретировался escN-штаммом (фиг.12С), подтверждая ожидавшиеся TTSS фенотипы. Сходные результаты были получены для экспрессии эпитоп-меченного NleA в диком типе ЕРЕС и нескольких тип III-секретирующих мутантах ЕРЕС, что показывает, что NleA также может секретироваться ЕРЕС TTSS.
Пример 7
NleA транслоцируется в реципиентные клетки
При выращивании ЕНЕС в условиях, индуцирующих секрецию типа III, два типа белков секретируются в экстрацеллюлярную среду. Для определения, является ли NleA транслокатором или транслоцированным эффектором, мы исследовали секрецию и транслокацию типа III в отсутствие NleA путем создания мутантного штамма с делецией. Анализировали профили секретируемых белков штамма дикого типа и ΔnleA мутантного ЕНЕС штамма. Образец дикого типа содержал избыточный белок с молекулярной массой примерно 50 кДа, который отсутствовал среди белков, секретированных ΔnleA (фиг.13А). Анализ вестерн-блота с антисывороткой против NleA продемонстрировал, что 50 кДа NleA был представлен среди белков, секретированных диким типом и отсутствовал в образце ΔnleA (фиг.13В). Однако, за исключением присутствия или отсутствия NleA, профили секретируемых белков штаммов дикого типа и ΔnleA были идентичными (фиг.13А). Таким образом, NleA не требуется для секреции других тип III-секретируемых эффекторов. Для определения, является ли NleA необходимым для транслокации других тип III эффекторов в клетки реципиента, клетки HeLa инфицировали диким типом ЕНЕС и ЕНЕС ΔnleA и наблюдали транслокацию и функционирование Tir с использованием иммунофлюоресцентного окрашивания инфицированных клеток. Формирование ложа диким типом ЕНЕС и мутантом ΔnleA изучали, подвергая инфицированные клетки иммунофлюоресценции с анти-ЕНЕС и анти-Tir антителами и наблюдая филаменты актина с использованием фаллоидина. Результаты показали, что ЕНЕС ΔnleA адгезировались к клеткам HeLa на одинаковом уровне с диким типом ЕНЕС. Иммунофлюоресцентное окрашивание показало, что Tir был транслоцирован в реципиентные клетки и сосредоточен под инфекционными бактериями, как в штамме дикого типа, так и в штамме ΔnleA ЕНЕС. Для подтверждения функциональной транслокации Tir инфицированные клетки окрашивали флюоресцентным фаллоидином для визуализации полимеризованного актина, вовлеченного в формирование ложа под адгезированными бактериями. В клетках, инфицированных как диким типом, так и ΔnleA ЕНЕС, актиновые ложа были свидетельством того, что транслокация и функционирование других эффекторов типа III могут происходить в отсутствие NleA. Эти результаты также показывают, что NleA не требуется для формирования ложа.
Так как NleA не играет роли в секреции или транслокации других эффекторов, исследовали, транслокацируется ли сам NleA. Клетки HeLa инфицировали в течение 6 часов диким типом или escN-ЕНЕС, экспрессирующими НА-меченный NleA и подвергали субклеточному фракционированию и анализу вестерн-блота с анти-НА антителами. Как показано на фиг.14А, NleA транслоцируется в реципиентные клетки, где связывается с мембранной фракцией реципиентных клеток. Транслокация NleA не наблюдалась в процессе инфицирования клеток тип III секретирующим мутантом, экспрессирующим НА-меченный NleA, что означает, что транслокация NleA и связывание с мембраной реципиента являются TTSS-зависимыми. Анализ вестерн-блота фракций с антителами к белкам, специфичным для каждой фракции, подтвердил отсутствие перекрестной контаминации фракций. Кальнексин, интегральный мембранный белок реципиентных клеток, отсутствовал в цитоплазматической фракции, а тубулин, цитоплазматический белок реципиентных клеток, отсутствовал в мембранной фракции реципиентных клеток. DnaK, несекретируемый бактериальный белок, присутствовал только в низкоскоростном осадке, демонстрируя отсутствие бактериальной контаминации мембран реципиента и цитозольных фракций. NleA и DnaK отсутствовали в низкоскоростном осадке в тип III мутант-инфицированных клетках, в связи с зависимостью типа III от адгезии ЕНЕС. Для подтверждения неожиданного отсутствия NleA тип III мутант-инфицированных образцах, в связи с зависимостью типа III от адгезии ЕНЕС, проводили сходные эксперименты, экспрессируя и вводя NleA-НА с помощью дикого типа и тип III мутанта ЕРЕС, так как адгезия ЕРЕС к клеткам HeLa не зависит от тип III секреции. NleA присутствовал в мембранной фракции клеток, инфицированных диким типом, но не штаммом тип III мутанта ЕРЕС. И NleA, и DnaK присутствовали в низкоскоростных осадочных фракциях клеток, инфицированных диким типом и тип III мутантом ЕРЕС.
Для изучения природы связывания NleA с мембранами реципиентных клеток мембранные фракции инфицированных реципиентных клеток, содержащие НА-меченный NleA, экстрагировали на льду, при определенных условиях, и рецентрифугировали для получения растворимых и нерастворимых мембранных фракций (фиг.14В). Эти фракции были подвергнуты анализу вестерн-блота с анти-НА антителами для определения НА-меченного NleA. Обработкой высшей солью (1М NaCl) или щелочным рН (0,2 мМ Na2CO3, рН 11,4) удаляли белки, которые периферийно связаны с мембранами электростатическими или гидрофильными взаимодействиями соответственно. Связь NleA с мембранами реципиентных клеток выдерживала разрушение такой обработкой (фиг.14В, верхняя панель), так же, как и кальнексин, интегральный мембранный белок (фиг.14В, средняя панель). Напротив, значительное количество кальретикулина, периферийного мембранного белка, была удалена из мембранной фракции в процессе обработки, как высшей солью, так и щелочным рН (фиг.14В, нижняя панель). Обработка мембранных фракций неионным детергентом Triton X-100, который растворяет интегральные мембранные белки, такие как кальнексин (фиг.14В, средняя панель), почти полностью растворила NleA, в результате чего НА-меченный NleA белок перешел из нерастворимой фракции в растворимую (фиг.14В, верхняя панель). Эти результаты показывают, что NleA транслоцируется в реципиентные клетки, где ведет себя как интегральный мембранный белок. Действительно, анализ последовательности белка NleA несколькими программами предсказания трансмембранных доменов предсказал один или два мнимых трансмембранных домена в этой последовательности (фиг.11С).
Пример 8
NleA локализуется в комплексе Гольджи реципиента
Затем определяли субклеточную локализацию NleA в реципиентных клетках. Клетки HeLa инфицировали диким типом ЕНЕС или ЕНЕС ΔnleA и подвергали иммунофлюоресценции с антителами против NleA и маннозидазы II. Некоторые образцы обрабатывали брефелдином А в течение 30 минут перед фиксацией. Проводили двухцветное слоистое окрашивание NleA и маннозидазы II. Клетки HeLa трансфицировали экспрессирующей конструкцией, кодирующей белок слияния GFP-NleA, и подвергали иммунофлюоресценции с антителами против маннозидазы II.
Иммунофлюоресцентное окрашивание клеток HeLa, инфицированных диким типом ЕНЕС, с использованием анти-NleA антител, приводило к образованию перинуклеарных частиц красителя, которые отсутствовали в клетках, инфицированных ЕНЕС ΔnleA или в не инфицированных клетках. Эти частицы не были похожи на окрашивание, получаемое с маркерами для поздних эндосом, лизосом, ER, митохондрий или ядер. Однако очень похожие частицы красителя наблюдались, когда клетки докрашивали с анти-NleA и антителами к маркерам комплекса Гольджи, включая маннозидазу II, где два белка были локализованы рядом. Для подтверждения локализации NleA в комплексе Гольджи инфицированные клетки инкубировали с брефелдином А, грибковым метаболитом, разрушающим структуру комплекса Гольджи (27), перед фиксацией и иммунофлюоресценцией. Обработка брефелдином А вызывала диффузию окрашивания маннозидазы II и NleA, как и ожидалось для белков, локализованных в комплексе Гольджи. Солокализацию NleA наблюдали с несколькими другими маркерами для комплекса Гольджи, а также наблюдали локализацию в комплексе Гольджи в экспериментах, исследовавших эпитоп-меченный NleA, окрашенный антителами к метке, связывавшими как НА, так и FLAG эпитопные метки. Для определения, требует ли локализация NleA в комплексе Гольджи других бактериальных факторов или является собственным свойством NleA, клетки трансфицировали экспрессирующей конструкцией, кодирующей белок слияния GFP-NleA. Трансфицированный NleA GFP также располагается в комплексе Гольджи, где перекрывается с окрашиванием маннозидазы II.
Таким образом, наши результаты показывают, что NleA локализуется в комплексе Гольджи. Наблюдение, что трансфицированный белок слияния GFP-NleA локализуется в комплексе Гольджи, позволяет предположить, что белок NleA содержит информацию, нацеленную на комплекс Гольджи, и не нуждается в других бактериальных факторах для его достижения. NleA, введенный в бактерии, также локализуется в комплексе Гольджи.
Пример 9
NleA необходим для вирулентности
Высокая степень устойчивости последовательности NleA в А/Е патогенах (фиг.11С) позволяет предположить, что NleA играет схожую роль в инфекции. C. rodentium является естественным патогеном у мышей (53) и используется как модельная система для изучения А/Е патогенеза. Для чувствительных линий инфекция C. rodentium является фатальной и, как правило, вызывает смерть инфицированных мышей между 6 и 10 днем заражения (54). Более устойчивые линии мышей не умирают от инфекции C. rodentium, но подвергаются колонизации с развитием кишечного воспаления и гиперплазии толстого кишечника (54).
Для определения роли NleA в вирулентности создали штамм C. rodentium с делецией nleA и подтвердили отсутствие NleA с помощью вестерн-блота общих бактериальных экстрактов с NleA антисывороткой (фиг.16А). Мышей инфицировали равными количествами бактерий дикого типа или ΔnleA через желудочный зонд. У мышей C3H-HeJ, чувствительных к C. rodentium, NleA был абсолютно необходим для вирулентности. Все мыши C3H-HeJ, инфицированные диким типом C. rodentium, умерли между 6 и 10 днем заражения (n=9), тогда как все ΔnleA-инфицированные мыши (n=13) показали некоторые легкие симптомы заболевания, такие как жидкий стул, но по-прежнему прибавляли в весе, были активны в продолжение инфекции и все выжили (фиг.16В). Более того, ΔnleA-инфицированные мыши были устойчивы к последующему заражению диким типом C. rodentium (n=5, фиг.16В). Таким образом, хотя штамм ΔnleA не является патогенным для чувствительных мышей, он взаимодействует с реципиентом в достаточной мере для стимуляции защитного иммунитета.
В отличие от мышей C3H-HeJ, инфекция C. rodentium не является летальной для аутбредных швейцарских мышей NIH. У этих мышей колонизация C. rodentium толстой кишки ведет к воспалению кишечника, гиперплазии толстого кишечника и слабым симптомам диареи. Швейцарских мышей NIH инфицировали диким типом C. rodentium или штаммом ΔnleA и усыпляли на 10 день заражения. Мыши, инфицированные штаммом ΔnleA, имели в толстом кишечнике на 10 день, в среднем, титр C. rodentium в 20 раз ниже (фиг.16С).
Гистологический анализ толстого кишечника инфицированных швейцарских мышей NIH проводили путем инфицирования мышей диким типом C. rodentium или штаммом ΔnleA и усыпления на 10 день заражения. Последние 0,5 см толстой кишки инфицированных мышей фиксировали в 10% нейтральном буферном формалине, обрабатывали, делали срезы по 3 мкм и окрашивали гематоксилином и эозином. Тканевые срезы всех мышей изучали и фотографировали с использованием объективов 5Х и 63Х. Результаты показывают, что в гистологических анализах биопсий, взятых из анального края инфицированных мышей, обнаружено большое количество бактерий в тканях, инфицированных диким типом, и незначительное число бактерий в образцах, инфицированных ΔnleA. Все животные, инфицированные диким типом C. rodentium, демонстрировали патологические знаки гиперплазии толстого кишечника, тогда как мыши, инфицированные ΔnleA, не имели признаков гиперплазии. Образцы, инфицированные диким типом, демонстрировали выраженное воспаление и гиперплазию, до степени, когда исчезал просвет кишечника и внешний мышечный слой был визуально растянут для вмещения увеличенного объема эпителия. Напротив, ΔnleA-инфицированные образцы демонстрировали относительно нормальную гистологию. Относительная выраженность кишечного воспаления и гиперплазии также проявлялась в различии веса толстого кишечника, ко времени усыпления, в двух группах мышей (фиг.16D). Мыши, инфицированные диким типом, имели также увеличенную селезенку, по сравнению с ΔnleA-инфицированными мышами, что проявлялось в увеличении веса селезенки.
Таким образом, продемонстрировали выраженное воздействие NleA на вирулентность на мышиной модели заболевания. У чувствительных мышей присутствие функционирующего NleA в C. rodentium ведет к летальной инфекции в течение 10 дней. Мыши, инфицированные штаммом, дефицитным по NleA, показывают незначительные симптомы и обязательно выживают после инфекции. У более устойчивых мышиных линий, где инфекция C. rodentium не является летальной, NleA необходим для развития гиперплазии толстого кишечника, и на 10 день инфекции меньшее количество бактерий с ΔnleA мутантом присутствует в кишечнике реципиента. Эти исследования показывают явное участие NleA в вирулентности C. rodentium. Эти результаты ЕНЕС инфицирования клеток HeLa продемонстрировали, что in vitro NleA не снижает адгезию бактерий на реципиентных клетках или транслокацию других эффекторов, позволяя предположить, что NleA может действовать на уровне затруднения процесса выведения у клетки-реципиента, а не увеличения бактериальной адгезии. Более того, устойчивость ΔnleA-инфицированных мышей к последующему заражению диким типом C. rodentium доказывает, что колонизации штаммом nle мутанта и его взаимодействия с реципиентом достаточно для стимуляции иммунитета реципиента. Это отличает его от тип III-мутантов C. rodentium, которые не колонизируют реципиента и не создают защиты от последующего заражения. Таким образом, nleA мутантные штаммы могут использоваться как ослабленные штаммы вакцины.













Другие варианты осуществления
Хотя здесь описаны различные варианты осуществления, многие адаптации и модификации могут быть сделаны в пределах объема изобретения в соответствии с общими знаниями специалистов в данной области. Такие модификации включают в себя замены известных эквивалентов любого аспекта изобретения для достижения того же результата, по существу, тем же путем.
Применяемые здесь инвентарные номера относятся к инвентарным номерам многих баз данных, включая GenBank, European Molecular Biology Laboratory (EMBL), DNA Database of Japan (DDBJ) или Genome Sequence Data Base (GSDB), для нуклеотидных последовательностей, и включая Protein Information Resource (PIR), SWISSPROT, Protein Research Foundation (PRF) и Protein Data Bank (PDB) (последовательности для разрешенных структур), а также к результатам трансляции из аннотированых кодирующих областей в GenBank, EMBL, DDBJ или RefSeq, для полипептидных последовательностей. Численные интервалы включают числа, определяющие интервал. В спецификации слово «включающий» применяется в качестве неограниченного термина, по существу эквивалентного выражению «включающий в качестве неограничивающих примеров», и выражение «включает» имеет соответствующее значение. Цитирование приведенных здесь ссылок не подразумевает допущения, что такие ссылки представляют собой предшествующий по отношению к настоящему изобретению уровень техники.
Все публикации включены в данное описание в качестве ссылки так, как если бы каждая отдельная публикация была конкретно и отдельно указана как включенная в данное описание в качестве ссылки и была бы полностью приведена в данном описании. Изобретение относится ко всем вариантам осуществления и вариациям, по существу описанным здесь и выше, со ссылкой на примеры и чертежи.


























































































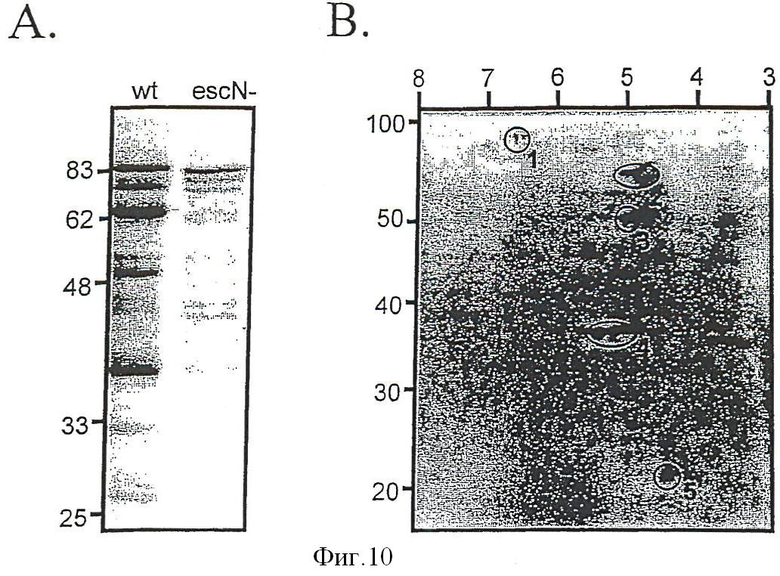
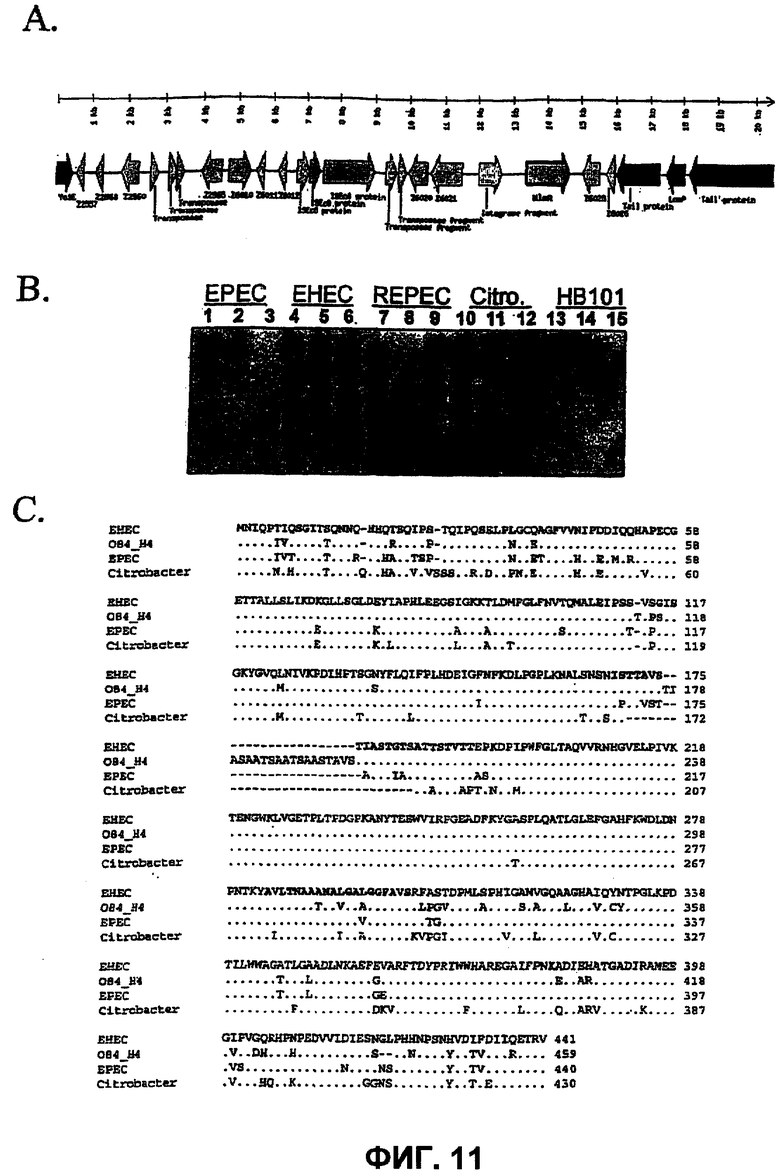
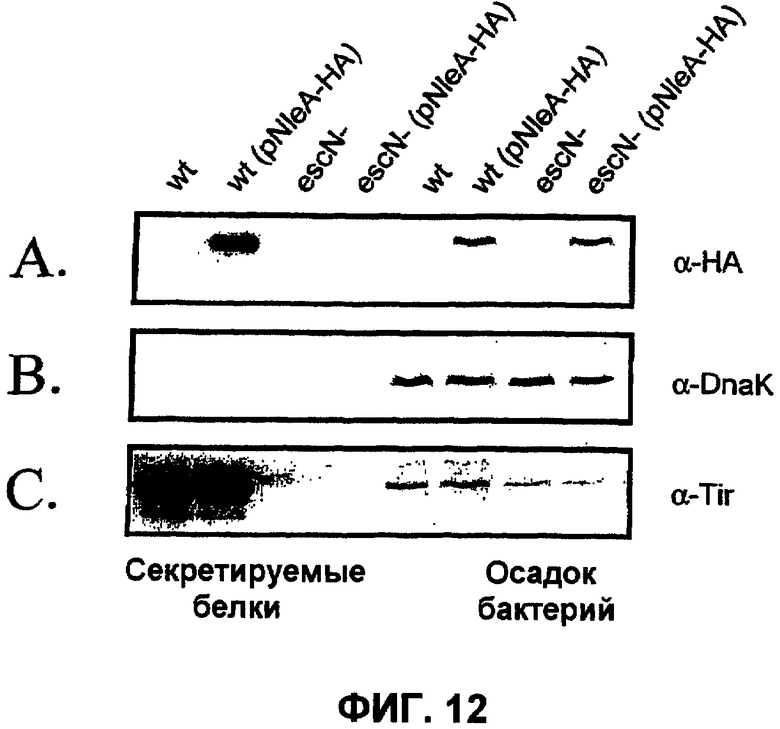
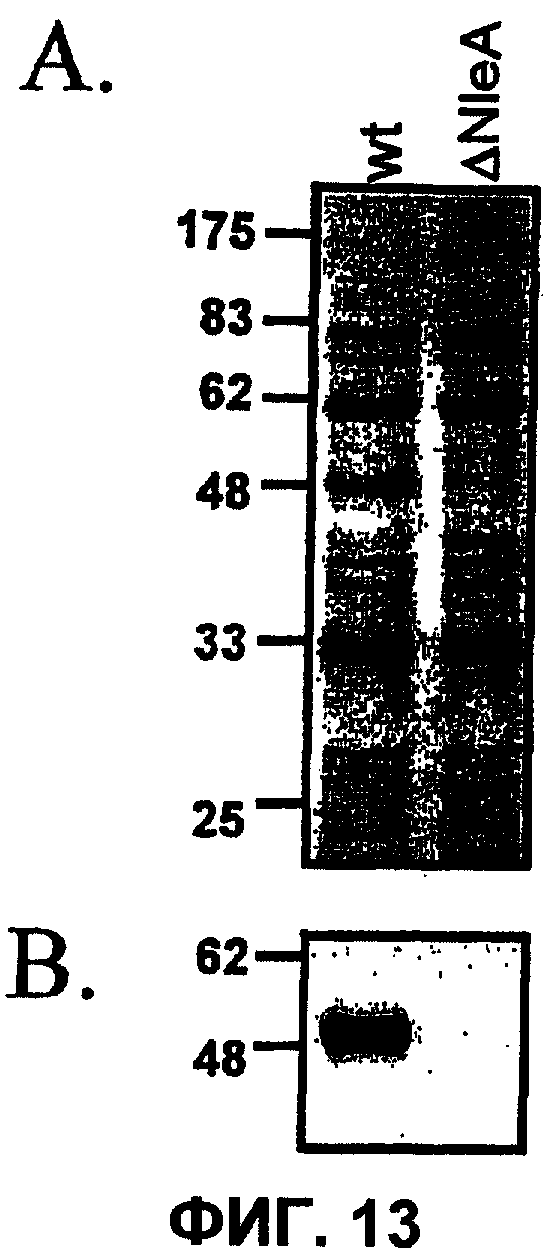

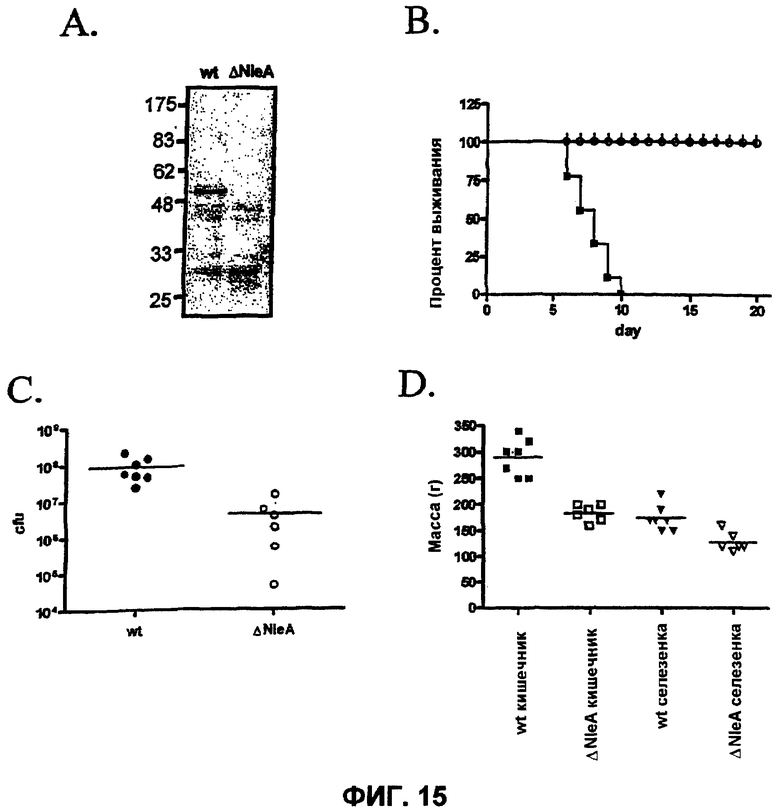






















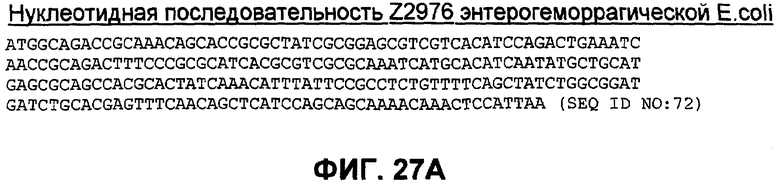

Изобретение относится к области биохимии. Представлены варианты рекомбинантных вирулентных полипептидов и кодирующие их молекулы нуклеиновых кислот с последовательностями, раскрытыми в описании, используемые для получения вакцинной композиции против А/Е-патогена. Описана композиция вакцины для индукции против А/Е-патогена у животных, содержащая указанный полипептид; указанную молекулу нуклеиновой кислоты; супернатант клеточной культуры, содержащий указанный полипептид; и/или бактерию или ее препарат, имеющей мутацию в своем геноме в указанной молекуле нуклеиновой кислоты, приводящую к ослаблению вирулентности, или имеющей делецию гена nleA, в сочетании с физиологически приемлемым носителем. Предложен способ ослабления вирулентности А/Е-патогена, включающий делетирование гена nleA в А/Е-патогене или делетирование одной или более указанных нуклеиновых кислот в геноме А/Е-патогена. Изобретение позволяет получить вакцину против А/Е-патогена. 4 н. и 20 з.п. ф-лы, 2 табл., 27 ил., 9 пр.
1. Композиция вакцины для индукции иммунного ответа против А/Е-патогена у животных, содержащая:
a) полипептид, который содержит аминокислотную последовательность, по существу идентичную последовательности SEQ ID NO:22-24, или ее иммуногенный фрагмент, и/или
b) молекулу нуклеиновой кислоты, кодирующую полипептид, который содержит аминокислотную последовательность, по существу идентичную последовательности SEQ ID NO:22-24, или ее иммуногенный фрагмент, и/или
c) молекулу нуклеиновой кислоты, которая содержит нуклеотидную последовательность, по существу идентичную последовательности SEQ ID NO:1-3, или ее иммуногенный фрагмент, и/или
d) супернатант клеточной культуры, который содержит рекомбинантный полипептид, содержащий аминокислотную последовательность, по существу идентичную последовательности SEQ ID NO:22-24, или ее иммуногенный фрагмент, и/или
e) бактерию или ее препарат, причем бактерия содержит мутацию в бактериальном геноме в нуклеотидной последовательности, которая по существу идентична SEQ ID NO:1-3, и причем мутация приводит к ослаблению вирулентности; и/или
f) бактерию или ее препарат, причем бактерия содержит делецию в гене, по существу идентичном nleA, причем делеция приводит к ослаблению вирулентности,
в сочетании с физиологически приемлемым носителем.
2. Композиция по п.1, в которой полипептид составляет 20% клеточного белка, присутствующего в композиции, содержащей супернатант клеточной культуры.
3. Композиция по п.1, дополнительно содержащая EspA, EspB, EspD, EspP, Tir, шигатоксин 1, шигатоксин 2 или полипептид интимин.
4. Композиция по п.1, в которой бактерия представляет собой энтерогеморрагическую E.coli (EHEC), энтеропатогенную E.coli (EPEC) или Citrobacter rodentium.
5. Композиция по п.4, в которой ЕНЕС представляет собой ЕНЕС О157:Н7 или ЕНЕС O157:NM; или ЕРЕС представляет собой ЕРЕС О127:Н6.
6. Композиция по п.1, в которой бактерия является живой и составлена в рецептуру для перорального введения.
7. Композиция по п.1, в которой бактерия является убитой и составлена в рецептуру для парентерального введения.
8. Композиция по п.1, дополнительно содержащая адъювант.
9. Композиция по п.8, в которой адъювант представляет собой эмульсию «масло-в-воде» или эмульсию, не представляющую собой «масло-в-воде».
10. Композиция по п.9, в которой эмульсия «масло-в-воде» представляет собой EMULSIGEN™ или EMULSIGEN PLUS™.
11. Композиция по п.8, в которой адъювант представляет собой минеральное масло или диметилдиоктадециламмония бромид или содержит и минеральное масло, и диметилдиоктадециламмония бромид.
12. Композиция по п.8, в которой адъювант включает один или более агентов, выбранных из группы, состоящей из эмульгирующего средства, мурамилдипептида, средства на водной основе, средства, основанного на хитозане, сапонина, масла, липополисахарида, экстракта бактериальной клеточной стенки, бактериальной ДНК, бактериального комплекса, синтетического олигонуклеотида и алифатического азотистого основания.
13. Композиция по п.12, в которой масло представляет собой Amphigen®.
14. Композиция по п.8, в которой адъювант включает экстракт клеточной стенки микобактерии, ДНК микобактерии или комплекс клеточной стенки микобактерии.
15. Композиция по п.8, в которой адъювант присутствует в композиции в концентрации от 20% до 40% (об./об.).
16. Способ ослабления вирулентности А/Е-патогена, включающий делетирование гена nleA в А/Е-патогене или делетирование одной или более нуклеотидных последовательностей в геноме А/Е-патогена, в котором нуклеотидная последовательность выбрана из SEQ ID NO:1-3.
17. Рекомбинантный вирулентный полипептид для получения композиции по п.1, содержащий аминокислотную последовательность, по существу идентичную последовательностям SEQ ID NO:22-24.
18. Выделенная молекула нуклеиновой кислоты для получения композиции по п.1, кодирующая вирулентный полипептид, содержащая нуклеотидную последовательность, по существу идентичную последовательностям SEQ ID NO:1-3.
19. Выделенная молекула нуклеиновой кислоты по п.18, встроенная в вектор.
20. Выделенная молекула нуклеиновой кислоты по п.19, где указанный вектор встроен в клетку-хозяина.
21. Композиция по п.1, где животное представляет собой жвачное животное.
22. Композиция по п.21, где жвачное животное представляет собой корову или овцу.
23. Композиция по п.1, где аминокислотная последовательность по меньшей мере на 75% идентична последовательности SEQ ID NO:22-24.
24. Композиция по п.1, где нуклеотидная последовательность гибридизуется в условиях высокой жесткости с последовательностью SEQ ID NO:1-3.
| US 6365723 В1, 02.04.2002 | |||
| DATABASE: UniProtKB/TrEMBL, Q8XAJ5, 01.03.2002 | |||
| ВАКЦИНА ПРОТИВ ЭШЕРИХИОЗА ЖИВОТНЫХ | 1993 |
|
RU2043771C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИННОЙ КОМПОЗИЦИИ ПРОТИВ КИШЕЧНОЙ ИНФЕКЦИИ | 1992 |
|
RU2127121C1 |
Авторы
Даты
2012-10-27—Публикация
2004-10-29—Подача