Изобретение относится к фармацевтически активным стероидным соединениям, фармацевтическим композициям, включающим эти соединения, применению этих соединений для получения фармацевтической композиции, пригодной для регуляции репродукции, особенно мейоза, к применению для получения контрацептива или в качестве профертильного препарата, к способу регуляции репродукции, например мейоза, способу усовершенствования возможности присущей овоцитам способности развиваться в млекопитающее, а также к способам получения новых стероидных соединений.
Мейоз является уникальным и завершающим событием эмбриональных клеток, на котором основано половое воспроизведение. Мейоз включает два мейотических деления. В ходе первого деления происходит обмен между материнскими и отцовскими генами до разделения пар хромосом в дочерних клетках. Они содержат только половину числа (1n) хромосом и удвоенную ДНК 2с. Второе мейотическое деление проходит без синтеза ДНК. Поэтому это деление приводит к образованию гаплоидных зародышевых клеток только с ДНК 1с.
Мейотические события схожи в мужской и женской зародышевых клетках, но временной режим и процессы дифференцировки, которые приводят к женским эмбриональным клеткам и сперматозоидам, отличаются основательно. Все женские зародышевые клетки входят в профазу первого мейотического деления в ранний период жизни, часто до рождения, но все они позже останавливаются в виде овоцитов в профазе (диктиатное состояние) до тех пор, пока после периода половой зрелости не произойдет овуляция. Таким образом, начиная с раннего периода жизни, женщина имеет запас овоцитов, которые расходуются пока запас не исчерпан. Мейоз у женщин не завершается до тех пор, пока не произойдет оплодотворение, и приводит только к одной зародышевой клетке и двум абортивным полоцитам на зародышевую клетку. В противоположность этому, только некоторые мужские зародышевые клетки входят в мейоз после наступления полового созревания и покидают популяцию зародышевых клеток в течение всей жизни. Однажды инициированный, мейоз в мужской клетке проходит без значительной задержки и дает четыре сперматозоида.
Совсем мало известно о механизмах, которые контролируют инициацию мейоза у мужчины и у женщины. Новые исследования указывают на то, что находящиеся в фолликуле пурины, гипоксантин и аденозин могут быть ответственны за остановку мейоза в овоците [S.M.Downs и др., Dev. Biol., 82, 454-458 (1985); J.J. Epplg. и др., Dev. Biol., 119. 313-321 (1986); S.M.Downs, Mol. Reprod. Dev., 35, 82-94 (1993)]. Присутствие способного диффундировать вещества, регулирующего мейоз, впервые описано Byskov и др. на культуре эмбриональных мышиных гонад [A.G.Byskov и др., Dev. Biol., 52, 193-200 (1976)]. Активирующее мейоз вещество (MAS) секретируется эмбриональным мышиным яичником, в котором происходит мейоз, а предотвращающее мейоз вещество (MPS) выделяется из морфологически дифференцированного яичка с покоящимися клетками, не входящими в мейоз. Было высказано предположение о том, что относительные концентрации MAS и MPS регулируют начало, остановку и возобновление мейоза в мужских и женских зародышевых клетках [A.G.Byskov и др. в: The Physiology of Reproduction (ред. Е.Knobil и J.D.Neill), Raven Press, New York (1994)]. Ясно, что если мейоз может быть регулируемым, то воспроизведение может быть контролируемым. В недавней статье [A.G.Byskov et al., Nature, 374, 559-562 (1995)] описано выделение некоторых стеринов, которые активируют мейоз овоцитов из бычьих яичек и из человеческой фолликулярной жидкости [T-MAS (стерин, активирующий мейоз в яичках) и FF-MAS (стерин, активирующий мейоз в фолликулярной жидкости):4,4-диметил-5α-холеста-8,14,24-триен-3β-ол].
Было также продемонстрировано, что микромолярные концентрации синтетического FF-MAS способны индуцировать возобновление мейоза дозозависимым способом в овоцитах крысы, который остановлен ингибитором фосфодиэстеразы IBMX (3-изобутил-1-метилксантином) [С.Hegele-Hartung и др., Biol. Reprod., 64, 418-424 (2001)]. Было показано, что данный эффект может наблюдаться, когда множественные экранированные овоциты (СЕО) и обнаженные овоциты (DO) культивируют in vitro в присутствии FF-MAS.
Дополнительные вещества, которые регулируют мейоз, описаны в WO 96/00235 A1, WO 96/27658 A1, WO 97/00884 A1, WO 98/28323 A1, WO 98/52965 A1, WO 99/58549 A1 и WO 00/68245 A1.
В заявке WO 98/52965 A1 описаны активирующие мейоз производные 20-аралкил-5α-прегнана.
В заявке WO 00/68245 A1 раскрыты стероидные производные, которые способны подавлять мейоз, так что эти соединения применимы в качестве контрацептивов у женщин и мужчин. Эти соединения являются прежде всего ненасыщенными производными холестана, отличающимися тем, что 3β-атом водорода связан с С14-атомом углерода холестанового скелета.
В заявке WO 96/00235 A1 описаны индуцирующие мейоз стерины, известные как промежуточные вещества в биосинтезе холестерина, а также некоторые структурно родственные синтетические стерины. Было найдено, что эти вещества регулируют мейоз. Подобно холестерину, данные стерины содержат боковую цепочку при С17 скелета стерина и дополнительно к этому, по меньшей мере, одну двойную связь Δ7, Δ8 или Δ8(14).
В заявке WO 96/27658 A1 раскрыт способ стимуляции мейоза зародышевой клетки, который включает введение в клетку in vivo, ex vivo или in vitro эффективного количества соединения, которое вызывает накопление эндогенного активирующего мейоз вещества до уровня, при котором индуцируется мейоз. Раскрывается, что такими соединениями, которые вызывают накопление активирующего мейоз вещества, являются амфотерицин В, аминогуанидин, 3α,5α,6β-тригидроксихолестан, мелатонин, 6-хлормелатонин и 5-метокситриптамин, а также другие производные и их агонисты. Сообщается также, что среди прочих активирующими мейоз веществами являются 5α-холестан-3β-ол, D-гомохолеста-8,14-диен-3β-ол и 22,25-диазахолестерин, 25-аза-24,25-дигидроланостерин, 24,25-иминоланостерин, 23- и 24-азахолестерин, а также производные 25-азахолестанола.
В заявках WO 97/00884 A1 и WO 98/28323 A1 описаны вещества, которые могут быть использованы для стимуляции мейоза in vitro, in vivo или ex vivo. Следовательно, раскрываемые соединения являются агонистами существующих в природе активаторов мейоза и поэтому могут применяться в лечении бесплодия, которое объясняется недостаточной стимуляцией, мейоза у мужчин и женщин. В этом документе раскрыты также некоторые соединения, которые могут быть антагонистами существующих в природе активаторов мейоза, так что эти соединения могут быть пригодны для применения в качестве контрацептивов. Раскрываемые среди прочих соединения включают 5α-холест-8-ен-3β-олы и 5α-холест-8,14-диен-3β-олы, которые, в частности, могут содержать аминогруппу в боковой цепи, связанной с С17 холестеринового скелета, причем аминогруппа присоединена к стериновому скелету через С4-спейсер. С аминогруппой связаны (С1-С4)алкил или (С3-С6)циклоалкил.
Дополнительно в заявке WO 99/58549 A1 раскрыты производные стерина, которые эффективны в регуляции мейоза. Описывается, что данные соединения обладают свойством ослаблять бесплодие особей мужского и женского пола, особенно человека. Производными стерина, эффективными в качестве регулирующих веществ, среди прочих являются (20R)-20-метил-23-диметиламино-5α-прегна-8,14-диен-3β-ол, (20R)-20-метил-23-диметиламино-5α-прегна-5,7-диен-3β-ол, 4,4-диметил-24-фенил-амино-5α-хола-8,14-диен-3β-ол, 4,4-диметил-24-(N,N-диметиламино)-24-циано-5α-холеста-8,14-диен-3β-оли, кроме того, множество производных стеринов с амидами кислот в положении 24, имеющих одну двойную связь или несколько двойных связей в стериновом скелете.
Ненасыщенные производные стерина, имеющие аминогруппу в боковой цепи при С17, описаны также J.J.Sheets и L.E.Vickery, "Active Site-directed Inhibitors of Cytochrome P-450scc", J. Biol. Chem., том 258 (19), 1983, стр.11446-11452, в отношении воздействия этих стеринов на расщепляющий боковую цепь бычьего аденокортикального холестерина цитохром Р-450 (P-450scc). В данном документе среди прочих соединений раскрыты 22-амино-23,24-биснорхол-5-ен-3β-ол и 23-амино-24-норхол-5-ен-3β-ол.
Дополнительные ненасыщенные производные, имеющие аминогруппу в боковой цепи при С17, описаны А.Т.Mangla и W.D.Nes: "Sterol C-methyl Transferase from Prototheca wickerhamii. Mechanism, Sterol Specificity and Inhibition", Bioorg. and Med. Chem. (2000), 8 (5), 925-936. В данном документе раскрыт, в частности, 32-азазимостерин.
При использовании описанных ранее регулирующих мейоз компонентов было обнаружено, что возобновление мейоза происходит в обнаженных овоцитах in vitro. Однако эти соединения имели только пограничную эффективность при стимуляции мейоза в овоцитах, окруженных зернистыми клетками яичника (СЕО - множественными экранированными овоцитами). Раскрытие приведенных выше документов включено путем цитирования.
Одна цель по настоящему изобретению состоит в нахождении веществ, которые применимы для регуляции воспроизведения, в особенности мейоза, у особей женского и мужского пола, главным образом, у млекопитающих и, более конкретно, у человека.
Другая цель по настоящему изобретению состоит в обеспечении фармацевтической композиции, включающей новые вещества.
Другая предпочтительная цель по настоящему изобретению состоит в обеспечении применения новых веществ при получении фармацевтической композиции, пригодной для регуляции воспроизведения, особенно мейоза.
Другая предпочтительная цель по настоящему изобретению состоит в обеспечении нового способа регуляции воспроизведения, например, мейоза.
Дополнительная цель по настоящему изобретению состоит в обеспечении способа лечения человеческого бесплодия.
Дополнительная цель по настоящему изобретению состоит в усовершенствовании созревания человеческих овоцитов.
Еще одна цель по настоящему изобретению состоит в улучшении синхронности созревания ядерных, цитоплазматических и/или мембранных овоцитов.
Еще одна цель по настоящему изобретению состоит в совершенствовании скорости имплантации овоцитов при созревании у человека и оплодотворении in vitro.
Еще одна дополнительная цель по настоящему изобретению состоит в уменьшении случаев появления человеческих предэмбрионов с хромосомными аномалиями (анэуплодия).
Еще одна дополнительная цель по настоящему изобретению состоит в повышении скорости расщепления человеческих предэмбрионов.
Еще одна дополнительная цель по настоящему изобретению состоит в улучшении качества человеческих предэмбрионов.
Другая цель по настоящему изобретению состоит в обеспечении способа получения новых веществ.
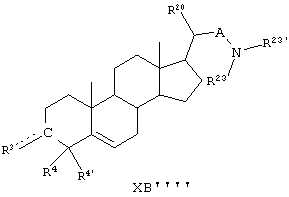
В соответствии с настоящим изобретением стероидные соединения общей формулы Х могут быть с пользой применены в регуляции воспроизведения, например, мейоза у млекопитающих, например у мужских и женских особей, и, в частности, у человека:

где в фрагменте

каждая связь между С5 и С6, между С6 и С7, между С7 и С8, между С8 и С9, между С8 и С14 и между С14 и С15 означает независимо одинарную связь или двойную связь, причем, по меньшей мере, одна из этих связей является двойной связью, и
где каждый атом углерода С5, С6, С7, С8, С9, С14 и С15 связан с соседним атомом углерода одинарной связью или, самое большее, одной двойной связью и где между всеми другими атомами углерода стероидного скелета имеются одинарные связи, и
С3R3 означает
а) С3=O или
б) С3H-OR3', где R3' выбирают из группы, включающей водород, незамещенный или замещенный, линейный или разветвленный (С1-С10)алкил и С3(O)-R3", присоединенный к части СН-O через С(O)-группу, где
R3" выбирают из группы, включающей
i) замещенный или незамещенный, линейный или разветвленный (С1-С10)алкил,
ii) замещенный или незамещенный, линейный или разветвленный (C1-С10)фторалкил,
iii) незамещенный или замещенный (С6-С10)арил,
iv) незамещенный или замещенный (C5-С10)гетероарил,
v) незамещенный или замещенный, линейный или разветвленный (C1-С10)алкилокси и
vi) незамещенный или замещенный, линейный или разветвленный (C1-С10)алкиламино или
в) С3H-SO2-R3" или С3=NOR3", где R3" имеет такие же значения, как выше, или
г) С3H-O-R3''', где R3''' означает незамещенный или замещенный, линейный или разветвленный (С2-С10)алкилен и образует циклический простой эфир как с атомом углерода стероидного скелета, так и атомом кислорода, или
д) циклическую структуру с атомом С3, в которой R3' означает незамещенный или замещенный, линейный или разветвленный (С2-С10)алкилен, или
е) С3Н-Hal, где Hal означает F, Cl, Br or I, и
R4, R4' и R20 выбирают независимо из группы, включающей водород и незамещенный или замещенный, линейный или разветвленный (С1-С4)алкил, и
R23 и R23' выбирают независимо из группы, включающей:
а) водород,
б) незамещенный или замещенный, линейный или разветвленный (C1-С8)алкил,
в) незамещенный или замещенный, линейный или разветвленный (С2-С8)алкенил,
г) незамещенный или замещенный, линейный или разветвленный (C1-С8)алкил, причем, по меньшей мере, один из углеродных атомов алкила замещен любым из атомов кислорода, азота и серы,
д) незамещенный или замещенный, линейный или разветвленный (С2-С8)алкенил, причем, по меньшей мере, один из углеродных атомов алкенила замещен любым из атомов кислорода, азота и серы, и
е) незамещенный или замещенный, линейный или разветвленный (С6-С10)арил, или
R23 и R23' образуют вместе
а) незамещенный или замещенный, линейный или разветвленный (С2-С7)алкилен, особенно (С5-С7)группу или
б) незамещенный или замещенный, линейный или разветвленный (С2-С7)алкилен, особенно (С5-С7)группу, где, по меньшей мере, один из алкиленовых атомов углерода заменен кислородом, азотом или серой, и
А означает метиленовую или этиленовую группу, причем группа является незамещенным или замещенным метиленом или этиленом; в предпочтительном варианте воплощения изобретения А означает метилен или этилен,
при условии отказа от прав на следующие соединения: (20R)-20-метил-23-диметиламино-5α-прегна-8,14-диен-3β-ол и (20R)-20-метил-23-диметиламино-5α-прегна-5,7-диен-3β-ол, 23-азазимостерин, 22-амино-23,24-биснорхол-5-ен-3β-ол, 23-амино-24-норхол-5-ен-3β-ол.
Предпочтительно изобретение относится к стероидным соединениям, в которых, по меньшей мере, одна двойная связь присутствует в стероидном скелете между атомами углерода С6, С7, С8, С9, С14 и С15 соответственно. В одном дополнительном варианте воплощения по настоящему изобретению двойная связь может находиться между С5 и С6 вдобавок, по меньшей мере, к одной двойной связи между С6, С7, С8, С9, С14 и С15 соответственно. Особенно предпочтительно, когда в стероиде двойные связи сопряжены друг с другом, если стероидный скелет содержит больше одной двойной связи.
Все указания на Сn-алкил, Сn-фторалкил, Сn-алкилокси, Сn-алкиламино, Сn-циклоалкил, Сn-алкилен, Сn-алкенил, Сn-арил, Сn-гетероарил и тому подобное относятся к радикалам с n атомами углерода в остатке, причем число n атомов углерода включает все углеродные атомы в боковых цепях, например, разветвленных радикалов. Если в контексте не описано иначе, алкильная, алкокси, алкиленовая или ацильная группы содержат 1-10 атомов углерода, включая углеродные атомы боковой цепи, если эти группы являются разветвленными; алкенильная или алкинильная группа содержит 2-10 углеродных атомов, включая углеродные атомы боковой цепи, если эти группы являются разветвленными; кроме того, циклоалкил содержит 4-7 углеродных атомов; арил содержит 6-10 углеродных атомов; и гетероциклическое кольцо или гетероарил содержит 6-10 кольцевых атомов. Кроме того, арил означает также алкиларил; гетероарил означает также алкилгетероарил; и циклоалкил означает также алкилциклоалкил.
Новые стероидные соединения имеют несколько хиральных центров, так что эти соединения существуют в нескольких изомерных формах. Все эти изомерные формы охватываются объемом по настоящему изобретению, если в контексте не описано иначе.
Стероидное соединение со следующей общей формулой является предпочтительным:

Особенно производные Δ5-прегнена, производные Δ8,14-прегнадиена, производные Δ8-прегнена и производные Δ5,7-прегнадиена применимы в качестве фармацевтически активных стероидных соединений для регуляции воспроизведения, например, мейоза, т.е. соединения, имеющие следующие общие формулы:



Неожиданно было найдено, что соединения по настоящему изобретению обладают сильным стимулирующим мейоз эффектом в овоцитах, особенно в СЕО, хотя эти соединения структурно сильно отличаются от стерина FF-MAS. В этом отношении соединения по данному изобретению превосходят это ранее описанное вещество, регулирующее мейоз [например: A.G.Byskov и др., Nature, 374. 559-562 (1995)]. Предпочтительными соединениями общей формулы Х являются такие соединения, которые вызывают разрушение эмбриональных везикул, по меньшей мере, на 40%, предпочтительно, по меньшей мере, на 60% и особенно, по меньшей мере, на 80% при исследовании в пробе с овоцитами, как описано в примере 23.
Соединения по настоящему изобретению превосходят ранее описанные соединения и по второму аспекту: в то время как FF-MAS не способен вызвать созревание в культуральной системе фолликул, соединения по настоящему изобретению обладают способностью активировать мейоз в данных условиях.
По этой причине новые стероидные соединения могут быть использованы, например, для применения in vivo, а также для применения поп in vivo, которое, в частности, включает применение in vitro. Стероидные соединения особенно пригодны для оплодотворения in vitro и in vivo млекопитающих, в особенности человека.
Исключительные свойства новых соединений могут быть приписаны аминогруппе в боковой цепи, связанной с атомом углерода С17 в стероидном скелете через (С2-С3)алкиленовый спейсер (включая группу С20-R20).
Особенно предпочтительными являются соединения, в которых часть С3R3 означает СН-ОН, в частности, 3β-гидроксирадикал, связанный с атомом С3 стероидного скелета. Часть может также означать CH-O-C(O)-R3" (=CH-O-R3', где R3' означает C(O)-R3"), где R3" имеет приведенные выше значения. В частности, R3" может быть эфирным радикалом монокарбоновой кислоты, дикарбоновой кислоты или неорганической кислоты, или какой-либо другой кислоты, связанным с атомом С3 стероидного скелета. В частности, для R3, означающего эфирный радикал дикарбоновой кислоты, R3" может быть (СН2)n-СОООН, где n означает 1, 2, 3, 4, 5 или 6. Эфирный радикал может быть также образован из неорганической кислоты, такой как фосфорная кислота, серная кислота и сульфаминовая кислота, кроме того, из монокарбоновой кислоты, такой как уксусная кислота, пропионовая кислота, н-бутановая кислота, триметилуксусная кислота, бензойная кислота, никотиновая кислота и изоникотиновая кислота. В частности, эфирный радикал может быть образован из дикарбоновой кислоты, такой как янтарная кислота и глутаровая кислота.
Дополнительные стероидные соединения по настоящему изобретению могут также включать производные, в которых C-O-R3 означает циклический эфир, включающий атом С3 стероидного скелета.
Заместитель R3 может также образовать циклическую кольцевую структуру вместе с атомом С3, причем R3 означает незамещенный или замещенный, линейный или разветвленный (С2-С10)алкилен. Например, группа С3R3 может означать циклопропиленовый, циклобутиленовый, циклопентиленовый или циклогексиленовый радикал. Она может также обозначать ненасыщенную циклическую кольцевую структуру, такую как циклопропенилен, циклобутенилен, циклопентенилен и циклогексенилен. Кольцевая структура может быть также замещена любым галоидом, гидроксигруппой, алкоксигруппой, арилоксигруппой и тому подобным.
Вещества по настоящему изобретению с пользой могут быть также соединениями, в которых R3" выбирают из группы, включающей фторметил, арил, гетероарил и (СН2)nСООН, где n означает 1, 2, 3, 4, 5 или 6, особенно соединениями, в которых R3' (=C(O)-R3") означает ацетил, пропионил, пивалоил, бутаноил, бензоил, никотинил, изоникотинил, гемиглутароил, бутилкарбамоил, фенилкарбамоил, этоксикарбонил и трет.-бутоксикарбонил. В особо предпочтительном стероидном соединении R3' может быть гемисукциноилом.
Кроме того, в новых стероидных соединениях R4 и R4' означают независимо предпочтительно водород или линейную либо разветвленную (С1-С4)алкильную группу, т.е. метил, этил, пропил, бутил и особенно метил.
Кроме того, R4 и R4' независимо могут быть также (С1-С4)алкилом, замещенным галоидом, гидрокси, алкокси или арилокси.
R20 означает предпочтительно водород или линейный либо разветвленный (С1-С4)алкил, т.е. метил, этил, пропил и бутил. R20 означает, главным образом, метил.
R23 и R23' независимо могут быть, в частности, водородом или (C1-С8)алкильной группой, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет.-бутил, н-пентил, изопентил, трет.-пентил, неопентил, кроме того, гексил, циклогексил и тому подобное. Затем R23 и R23' независимо могут быть также (С2-С6)алкенильной группой, т.е. ненасыщенной алкильной группой, например, винильной, аллильной, изопропенильной и фенильной, затем (С6-С10)арильной, такой как фенил и 1-нафтил, эта группа, включая также алкиларил, связывается через арильную часть или через алкильную часть с атомом азота, например, бензил и толил. R23 и R23' могут быть предпочтительно алкилом или алкенилом, замещаемыми, по меньшей мере, одним радикалом, выбранным из группы, включающей линейный или разветвленный (С1-С4)алкил и (С1-С4)алкокси. Фенильный и 1-нафтильный радикал могут быть также замещены галоидом, (С1-С4)алкокси, гидрокси или (С1-С4)алкилом, включая производные фторалкокси и фторалкила. Затем R23 и R23' независимо могут быть в дальнейшем, например, 4-гидроксифенилом, 4-метоксифенилом, 2,4,6-триметилфенилом, 2,4-дихлорфенилом, 4-фторфенилом, 4-трифторметилфенилом и 2-пентафторэтилфенилом.
Кроме того, R23 и R23' независимо могут также означать алкил и алкенил, причем, по меньшей мере, один из алкильных и алкенильных углеродных атомов соответственно замещен любым из атомов кислорода, азота и серы, например, метоксиметилен, метоксиэтилен, метоксипропилен, этоксипропилен и тому подобное.
R23 и R23' вместе могут также образовать гетероциклическую кольцевую структуру, связанную с боковой цепью через атом азота в боковой цепи, причем атом азота связан с углеродным атомом С стероидного скелета через спейсерную группу А. Гетероциклическая кольцевая структура, образованная N(R23)(R23'), может быть, в частности, выбрана из группы, включающей пиперидин-1-ильную, морфолин-4-ильную, пиперазин-1-ильную, пирролидин-1-ильную, пиррол-1-ильную, индол-1-ильную, пиразол-1-ильную, имидазол-1-ильную, тиазолидин-1-ильную и оксазолидин-3-ильную кольцевые структуры и их производные. Особенно предпочтительными гетероциклическими кольцевыми структурами являются насыщенные радикалы, а именно пиперидин-1-ил, морфолин-4-ил, пиперазин-1-ил и пирролидин-1-ил. Гетероциклические кольцевые структуры могут быть замещены гидрокси, карбокси, амино, алкиламино, диалкиламино, алкилом, алкенилом, алкинилом, циклоалкилом, циклоалкенилом, алкилцикло алкилом, арилом, алкиларилом, алкокси, алкилциклоалкилокси, алкилоксициклоалкилом, алкиларилокси, алкилоксиарилом, галоидом и ацилом, где алкил, алкенил, алкинил, циклоалкил, арил, алкокси и ацил содержат такое количество атомов углерода, как указано выше. Гетероциклическая кольцевая структура может быть также замещена гетероциклическими радикалами, такими, как гетероциклические кольцевые структуры, с которыми они могут быть связаны, и вдобавок к ним в качестве дополнительных радикалов, например, пиридинил, хинолинил, изохинолинил, пиридазинил, пиримидинил, пиразинил, хиноксалинил, тиазолил и оксазолил, включая, кроме того, все другие изомеры данных радикалов, например, пиридин- 2-ил, пиридин-3-ил и пиридин-4-ил. Далее, если N(R23)(R23') означает гетероциклическую кольцевую структуру, то эта кольцевая структура может также содержать в кольце оксогруппу.
Если N(R23)(R23') означает пиперазин-1-ил, то эта часть может быть, в частности, замещена пиридин-2-илом, пиридин-3-илом и пиридин-4-илом, чтобы предпочтительно образовать соответствующие группы N(R23)(R23'), в которых остаток пиперазин-1-ила замещен в пара-положении, например, 4-(пиридин-3-ил)пиперазин-1-ил.
Группа N(R23)(R23') может быть также любой из части

связанной с С20 в боковой цепи стероидного скелета через атом азота данной части, где Z означает О, S, N-R24, N-C(O)-R24, где R24 означает алкил, алкенил, алкинил, арил, число атомов углерода которых определено выше. Кроме того, R24 может быть гетероциклической кольцевой структурой, в которой число кольцевых атомов такое, как определено выше.
Атом азота группы N(R23)(R23') не связан непосредственно с атомом С20, а связан с ним через А, который означает незамещенную или замещенную метиленовую или этиленовую спейсерную группу, такую, как, например (незамещенный) метилен и (незамещенный) этилен и, кроме того, изопропилен, трет.-бутилен и тому подобное. Предпочтительно А означает метилен и этилен.
Особенно предпочтительными являются соединения, в которых R3 означает гидрокси или гемисукцинатную группу, где R4, R4' и R20 означают каждый метил и где гетероциклическая кольцевая структура N(R23)(R23'), включая атом азота аминогруппы, является незамещенным или замещенным морфолин-4-илом, пиперидин-1-илом, пиперазин-1-илом или пирролидин-1-илом. Группа N(R23)(R23') означает, в частности, 3-гидроксипиперидин-1-ил, 4-гидроксипиперидин-1-ил, 3-кетопиперидин-1-ил, 4-кето пиперидин-1-ил, 4-диметиламинопиперидин-1-ил, 3,3-диметилпиперидин-1-ил, 4,4-диметилпиперидин-1-ил, 3-карбоксипиперидин-1-ил, 4-карбоксипиперидин, 4-фенилпиперидин-1-ил, 4-бензоилпиперидин-1-ил, 4-(пиперидин-1-ил)пиперидин-1-ил, 4-метилпиперазин-1-ил, 4-ацетилпиперазин-1-ил, 4-фенилпиперазин-1-ил, 4-бензилпиперазин-1-ил, 4-бензоилпиперазин-1-ил, 4-(пиридин-2-ил)пиперазин-1-ил, 4-(пиридин-4-ил)пиперазин-1-ил, 4-(пиримидин-2-ил)пиперазин-1-ил.
Атомы водорода могут быть соединены со всеми другими углеродными атомами стероидного соединения, т.е. с С1, С2, С6, С7, С8, С9, С11, С12, С14, С15 и С16.
Предпочтительно фармацевтически приемлемыми соединениями по настоящему изобретению являются соли стероидных соединений общей формулы X. Примеры данных солей приведены в Journal of Pharmaceutical Science, 66, 2 и послед. (1977), которые тем самым включены путем цитирования. Примеры таких солей включают соли органических кислот, таких как муравьиная кислота, фумаровая кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, молочная кислота, виноградная кислота, щавелевая кислота, янтарная кислота, яблочная кислота, винная кислота, лимонная кислота, бензойная кислота, салициловая кислота, метансульфоновая кислота и тому подобное. Соответствующие неорганические кислоты для образования фармацевтически приемлемых солей включают хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, фосфорную кислоту и тому подобное.
Следующие соединения по настоящему изобретению особенно предпочтительны:
1) (20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
2) (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5β-прегна-8,14-диен-3β-ол
3) (20S)-20-[(4,4-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
4) (20S)-20-[(4-метилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
5) (20S)-20-[(4-фенилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
6) (20S)-20-[(морфолин-4-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
7) (20S)-20-[(4-(пиримидин-2-ил)пиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
8) (20S)-20-[(пирролидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
9) гемисукцинат (20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ола
10) (20S)-20-[N-(3-метоксипропил)аминометил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
11) (20S)-20-аминометил-4,4-диметил-5α-прегна-8,14-диен-3β-ол
12) (20S)-20-[N-ди-(2-метоксиэтил)аминометил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
13) (20S)-20-[N-(2,2-диметилэтилен)аминометил]-4,4-диметил-5β-прегна-8,14-диен-3β-ол
14) (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ол
15) (20S)-20-[(4-(пиридин-2-ил)пиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
16) (20S)-20-[(4-фенилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
17) (20S)-20-[(4-метилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
18) (20S)-20-[(N-диметиламино)этил]-4,4-диметйл-5α-прегна-8,14-диен-3β-ол
19) (20S)-20-[(морфолин-4-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
20) (20S)-20-[(пирролидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
21) (20S)-20-[(пиперидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
22) (20S)-20-[(4-фенилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
23) (20S)-20-[(пиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
24) (20S)-20-[(морфолин-4-ил)метил]-5α-прегна-5-ен-3β-ол
25) (20S)-20-[(пирролидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
26) (20S)-20-[(4-карбоксиэтилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
27) (20S)-20-[(3-гидроксипиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
28) (20S)-20-[(4-бензоилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
29) (20S)-20-[(4-(пиперидин-1-ил)пиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
30) (20S)-20-[(4-тиоморфолинил)метил]-5α-прегна-5-ен-3β-ол
31) (20S)-20-[(4-диметиламинопиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
32) (20S)-20-[(4-кето пиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
33) (20S)-20-[(3-кетопиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
34) (20S)-20-[(4-карбоксилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
35) (20S)-20-[(3-карбоксилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
36) (20S)-20-[(4-гидроксипиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
37) (20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
38) (20S)-20-[(4,4-диметилпиперидин-1-ил)метил]-5α-прегна-5α-ен-3β-ол
39) (20S)-20-[(4-пиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
40) (20S)-20-[(4-фенилпиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
41) (20S)-20-[(4-метилпиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
42) (20S)-20-[(4-бензилпиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
43) (20S)-20-[(4-ацетилпиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
44) (20S)-20-[(4-бензоилпиперазин-1-ил)метил]-5α-прегна-5-ен-3β-ол
45) (20S)-20-[{4-(2-пиридил)пиперазин-1-ил}метил]-5α-прегна-5-ен-3β-ол
46) (20S)-20-[{4-(3-пиридил)пиперазин-1-ил}метил]-5α-прегна-5-ен-3β-ол
47) (20S)-20-[{4-(4-пиридил)пиперазин-1-ил}метил]-5α-прегна-5-ен-3β-ол
48) (20S)-20-[{4-(2-пиримидил)пиперазин-1-ил}метил]-5α-прегна-5-ен-3β-ол
49) (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-Δ8(14)1-ен-3β-ол
Структурные формулы данных стероидных соединений показаны на фиг.1А-1К.
Дополнительной целью по настоящему изобретению являются фармацевтические композиции, включающие, по меньшей мере, одно стероидное соединение общей формулы Х и, по меньшей мере, один фармацевтически приемлемый наполнитель, хорошо известный в данной области, например, по меньшей мере, один носитель, разбавитель, усилитель поглощения, консервант, буфер, агент для поддержания осмотического давления и реологических свойств лекарственного средства, если это будет жидкость, поверхностно-активный агент, растворитель, дезинтегратор для таблеток, микрокапсулы, заполнитель, скользящая добавка, краситель, ароматизатор и другие ингредиенты. Эти вещества обычно используются в данной области техники. Стероидные соединения по изобретению предпочтительно включают в фармацевтические композиции в эффективном количестве.
Примерами твердых носителей являются карбонат магния, стеарат магния, декстрин, лактоза, сахар, тальк, желатин, пектин, крахмал, силикагель, трагакант, метилцеллюлоза, карбоксиметилцеллюлоза в натриевой форме, низкоплавкий воск и масло какао.
Жидкие композиции включают стерильные растворы, суспензии и эмульсии, которые могут быть введены перорально, назальным путем или в качестве мази. Такие жидкие композиции могут быть также применимы для инъекции или для использования в связи с применением ex vivo или in vivo. Для перорального введения жидкость может содержать фармацевтически приемлемое масло и/или липофильное вещество, поверхностно-активный агент и/или растворитель, который смешивается с водой. В этой связи делается ссылка на заявку WO 97/21440 А1, которая тем самым включена путем цитирования.
Жидкие композиции могут также содержать и другие ингредиенты, которые обычно используют в данной области, некоторые из которых упомянуты в перечне выше. Кроме того, композиция для трансдермального введения соединения по настоящему изобретению может быть предусмотрена в форме пластыря. Композиция для назального введения может быть предусмотрена в форме назального распылителя в жидкой или порошкообразной форме.
Для того чтобы увеличить биодоступность стероидных соединений, данные соединения могут быть также разработаны в виде циклодекстриновых клатратов. С этой целью соединения смешивают с α-, β- или γ-циклодекстрином или его производными.
Кремы, мази, лосьоны и другие жидкости, вводимые наружно, должны быть в таком состоянии, чтобы стероидные соединения по настоящему изобретению могли быть доставлены в достаточном количестве пациенту, нуждающемуся в регуляции мейоза. С этой целью лекарственное средство содержит наполнители для регуляции его реологических свойств, поверхностно-активные вещества, консерванты, растворители,
разбавители, вещества для усиления способности проникновения через кожу, кроме того, ароматизаторы и защищающие кожу вещества, такие как кондиционеры и регуляторы влажности.
Лекарственное средство может также содержать дополнительные активные агенты, чтобы усилить или регулировать эффективность стероидных соединений или получить другие требуемые эффекты лекарственного средства.
Для парентерального введения стероидные соединения могут быть растворены или суспендированы в фармацевтически приемлемом разбавителе. Очень часто используют масла в комбинации с растворителями, поверхностно-активными агентами, суспензионными или эмульсионными агентами, например оливковое масло, масло земляного ореха, касторовое масло и тому подобное. Для получения инъецируемого лекарственного средства может быть использован любой жидкий носитель. Эти жидкости часто содержат также агенты для регуляции их вязкости, а также агенты для регуляции изотонических свойств жидкости.
Стероидное соединение по настоящему изобретению, кроме того, может быть введено в виде инъецируемой депо-формы или в виде имплантата, который может, например, быть введен подкожно, так что становится возможным замедленное высвобождение стероидных соединений. С этой целью могут использоваться различные технические приемы, например, введение депо-форм, которые включают мембрану, содержащую активное соединение, или медленно растворяющиеся депо-формы. Имплантаты могут содержать, например, биологически деградируемые полимеры или синтетические силиконы в качестве инертного материала.
Доза применяемого стероидного соединения будет определяться врачом и зависеть среди прочего от конкретного используемого стероидного соединения, пути введения и цели применения. Обычно композиции по настоящему изобретению получают путем введения в тесный контакт активного соединения с жидкостью или вспомогательными ингредиентами и затем, если необходимо, формированием продукта в требуемую композицию.
Обычно не более чем 3000 мг, предпочтительно не более чем 350 мг и в некоторых предпочтительных случаях не более чем 30 мг стероидного соединения в сутки вводят млекопитающим, например человеку.
Настоящее изобретение относится также к применению стероидных соединений общей формулы Х для получения композиции, применимой для регуляции воспроизведения, например, мейоза. Предпочтительно данная композиция применима в качестве лекарственного средства.
Настоящее изобретение относится далее к применению новых стероидных соединений общей формулы Х для получения контрацептивного или профертильного препарата.
Настоящее изобретение относится далее к применению стероидного соединения общей формулы Х для применения non-in-vivo.
Настоящее изобретение относится также к способу регуляции воспроизведения, например, мейоза, включающему введение субъекту, нуждающемуся в такой регуляции, эффективного количества, по меньшей мере, одного стероидного соединения общей формулы X.
Кроме того, настоящее изобретение относится к способу совершенствования способности овоцитов развиваться в млекопитающем, включающему контакт овоцита, взятого у млекопитающего, со стероидным соединением общей формулы X.
Регуляция воспроизведения, например, мейоза, используется в контексте, чтобы показать, что соединения по настоящему изобретению особенно пригодны для стимуляции воспроизведения, например, мейоза у млекопитающих, особенно у человека, овоцитов, так что данные соединения, которые являются агонистическими аналогами природных активаторов мейоза, могут применяться в лечении бесплодия, возникающего из-за недостаточной стимуляции мейоза у женщин и мужчин.
Путем введения композиций, содержащих соединение по настоящему изобретению, может быть любой путь, который эффективно транспортирует активное стероидное соединение к участку его действия.
Так, когда стероидные соединения должны вводиться млекопитающему, они обычно обеспечиваются в форме фармацевтической композиции, которая включает, по крайней мере, одно стероидное соединение по настоящему изобретению в сочетании с фармацевтически приемлемым носителем. Для перорального применения такие композиции являются предпочтительными в форме таблеток или капсул.
Настоящее изобретение относится также к способу получения стероидных соединений общей формулы X, где R4 и R4' означают незамещенный или замещенный, линейный или разветвленный (С1-С4)алкил, а не водород.
Упомянутые выше стероидные соединения могут быть синтезированы аналогично получению известных соединений. Следовательно, синтез стероидных соединений формулы Х может следовать общепринятым синтетическим методикам, описанным в обширной литературе по стеринам и стероидам. Следующая литература может быть использована в качестве основного источника для синтеза: L.F.Fieser и М.Fieser: Steroids, Reinhold Publishing Corporation, N.Y., 1959; Rood's Chemistry of Carbon Compounds (ред. S.Coffrey): Elsevier Publishing Company, 1971; и особенно Dictionary of Steroids (ред. R.A.Hill, D.N.Kirk, H.L.J.Makin и G.M.Murphy), Chapman и Hall, тем самым данная литература включена путем цитирования. Последний источник содержит обширный перечень ссылок на оригинальные статьи, охватывая период до 1990 года.
В частности, стероидные соединения могут быть синтезированы, например, в соответствии с общим способом, включающим следующие этапы:
(а) исходя из (20S)-20-гидроксиметилпрегна-4-ен-3-она,
(б) введение двух алкильных групп в положение 4 алкилированием,
(в) восстановление кетогруппы в гидроксигруппу,
(г) введение двойной связи Δ7 бромированием/дегидробромированием,
(д) изомеризация диена Δ5,7 в диен Δ8,14 нагреванием в присутствии кислоты,
(е) окисление 17-гидроксигруппы в альдегидную группу и
(ж) восстановительное аминирование альдегидной группы.
Соответствующая схема синтеза этого первого синтетического способа приведена на фиг.2. Согласно схеме сначала гидроксильную группу в боковой цепи (20S)-20-гидроксиметилпрегна-4-ен-3-она 1 защищают в виде силилового эфира, например, в виде триизопропилсилилового (TIPS) эфира, получая соединение 2. Для того, чтобы получить соединение 3, две метильные группы вводят в положение 4 стероидного скелета посредством алкилирования с йодистым метилом в присутствии такого основания, как трет.-бутилат калия. На следующем этапе 3-кетогруппу восстанавливают обычным восстанавливающим агентом, таким как алюмогидрид лития или боргидрид натрия. Образующийся спирт 4 затем защищают, превращая, например, в ацетат (соединение 5). Впоследствии вводят вторую двойную связь с помощью последовательности реакций бромирования-дегидробромирования. Образующуюся Δ5,7-диеновую систему в соединении 6 затем изомеризуют в Δ8,14-диеновую систему посредством нагревания в присутствии хлористоводородной кислоты, чтобы получить соединение 7. На данном этапе, катализируемом кислотой, обе гидроксильные группы деблокируются, и может быть получен диол 7. Мягкое избирательное окисление триацетоксиперйодинаном по Десс-Мартину гидроксильной группы в боковой цепи приводит к альдегиду 8, который служит в качестве основного промежуточного соединения для введения различных аминов в боковую цепь посредством восстановительного аминирования. С этой целью могут применяться различные восстанавливающие агенты, как боргидрид натрия или трис(ацетокси)боргидрид натрия. В результате получают стероидные соединения 9 по настоящему изобретению.
По способу получения стероидных соединений по настоящему изобретению получаются новые соединения, а именно (20S-4,4-диметил-20-гидроксиметил-5α-прегна-8,14-диен-3β-ол и (20S)-4,4-диметил-5α-прегна-8,14-диен-3β-ол-20-карбальдегид. Следовательно, настоящее изобретение относится также и к данным промежуточным соединениям.
Альтернативно стероидные соединения могут быть также синтезированы следующим способом:
(а) исходя из (20S)-20-триметилпрегна-8,14-диен-3β,21-диола, в частности, из (20S)-4,4,20-триметилпрегна-8,14-диен-3β,21-диола,
(б) нуклеофильное замещение при С21, преимущественно с толуолсульфоновой кислотой,
(в) замещение нуклеофильной группы (тозилата) при С21 цианидом с образованием новой углерод-углеродной связи при С21,
(г) восстановление полученного нитрила с образованием альдегида,
(д) восстановительное аминирование нитрила с образованием различных аминов.
Соответствующая схема синтеза этого второго синтетического способа приведена на фиг.3. Тозилируют п-толуолсульфохлоридом (20S)-4,4,20-триметилпрегна-8,14-3β,21-диол 1 по боковой цепи. Затем тозилат 2 замещают цианидом в качестве строительного блока С1. После этого образующийся нитрил 3 восстанавливают диизобутилалюминийгидридом с образованием альдегида 4. Альдегид 4 затем взаимодействует с амином по реакции восстановительного аминирования в присутствии трис(ацетокси)боргидрида натрия. Образующийся конечный продукт 5 может быть очищен стандартной колоночной хроматографией или ВЭЖХ.
Примеры приведены для более подробного описания настоящего изобретения.
Пример 1: (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 2)
(a) (20S)-20-[((Триизопропилсилил)окси)метил]прегна-4-ен-3-он
К раствору 30 г (20S)-20-[(гидроксиметил]прегна-4-ен-3-она и 13,5 г имидазола в 300 мл дихлорметана при комнатной температуре прибавляли по каплям 26 мл триизопропилсилилхлорида. Реакционную смесь перемешивали в течение 20 ч при той же температуре и затем выливали в воду. Водный слой экстрагировали этилацетатом. Органические слои объединяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении, получая 45,4 г неочищенного (20S)-20-[((триизопропилсилил)окси)метил]прегна-4-ен-3-она в виде коричневого масла, которое использовали без дальнейшей очистки.
МС [химическая ионизация с образованием положительных ионов (CI+)]: 487 (М+Н).
(б) (20S)-4,4-Диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3-он
Раствор 45,4 г неочищенного (20S)-20-[((триизопропилсилил)окси)метил]прегна-4-ен-3-она в 320 мл тетрагидрофурана прибавляли к раствору 42,3 г трет.-бутилата калия в 950 мл трет.-бутанола при температуре 50°С. Смесь перемешивали в течение 10 мин при той же температуре. Затем прибавляли 50 мл йодистого метила и продолжали перемешивание в течение 1 ч. Реакционную смесь выливали в воду и экстрагировали этилацетатом. Органические слои объединяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 27,3 г (20S-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5-ен-3-она в виде бледно-желтого твердого вещества.
MC(CI+): 515(M+H).
(в) (20S)-4,4-Диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3β-ол
К раствору 27,3 г (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3-она в 500 мл тетрагидрофурана осторожно небольшими порциями прибавляли 1,24 г алюмогидрида лития при комнатной температуре. Реакционную смесь перемешивали в течение 1 ч, затем охлаждали до 0°С. Прибавляли последовательно 2,5 мл воды, 2,5 мл 0,1 н. раствора гидроксида натрия и 7,5 мл воды. Смесь фильтровали через целит. Фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 18,2 г (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3β-ола в виде бледно-желтого твердого вещества.
МС(CI+):517(М+Н).
(г) Ацетат (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил)прегна-5-ен-3β-ола
К раствору 18,2 г (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]-прегна-5-ен-3β-ола в 175 мл пиридина прибавляли 6,24 мл уксусного ангидрида при комнатной температуре. Реакционную смесь перемешивали в течение 20 ч и затем выливали в смесь лед/хлористоводородная кислота. Полученную смесь экстрагировали этилацетатом. Органические слои объединяли, промывали насыщенным солевым раствором, сушили над сульфатом натрия и концентрировали при пониженном давлении, получая 16, 2 г ацетата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5-ен-3β-ола в виде белого твердого вещества, которое использовали без дальнейшей очистки.
МС (CI+): 559 (М+Н).
(д) Ацетат (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5,7-диен-3β-ола
К раствору 16,2 г ацетата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5-ен-3β-ола в смеси 100 мл бензола и 100 мл гексана прибавляли порциями 4,93 г 1,3-дибром-5,5-диметилгидантоина при 70°С. Через 30 мин смесь охлаждали до 0°С и фильтровали. Фильтрат упаривали в вакууме.
К полученной смеси прибавляли 160 мл толуола и 7,8 мл 2,4,6-триметилпиридина. Смесь нагревали при кипении в течение 2,5 ч. После охлаждения реакционную смесь промывали 1 н. хлористоводородной кислотой, насыщенным раствором бикарбоната натрия и насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и упаривали в вакууме. Остаток очищали колоночной хроматографией, получая 12,5 г ацетата (20S)-4,4-диметил-20-[((триизопропилсилил)-окси)метил]прегна-5,7-диен-3β-ола в виде белого твердого вещества.
МС (CI+): 557 (М+Н).
(e) (20S)-4,4,20-Триметилпрегна-8,14-диен-3β,21-диол
Смесь 16,1 г ацетата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]-прегна-5,7-диен-3β-ола, 210 мл этанола, 28 мл бензола и 28 мл концентрированной хлористоводородной кислоты нагревали при кипении в течение 6 ч. После охлаждения смесь выливали в насыщенный раствор бикарбоната натрия, экстрагировали этилацетатом и промывали насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток перекристаллизовывали из дихлорметана и метанола, получая 4,48 г (20S)-4,4,20-триметилпрегна-8,14-диен-3β,21-диола.
МС [ионизация с электрораспылением с образованием положительных ионов (EI+)]: 358 (М).
(ж) (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль
К раствору 1 г (20S)-4,4,20-триметилпрегна-8,14-диен-3β,21-диола в 10 мл дихлорметана прибавляли при комнатной температуре 5,4 мл 0,5 М раствора триацетоксиперйодинана для окисления по Дессу-Мартину. Смесь перемешивали в течение 1 ч, выливали в насыщенный раствор бикарбоната натрия, экстрагировали этилацетатом и промывали насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 230 мг (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аля в виде белого твердого вещества.
МС (ES+): 356 (М).
(з) (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
Прибавляли 38 мг трис(ацетокси)боргидрида натрия к раствору 42 мг (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аля и 10 мкл пиперидина в 3 мл тетрагидрофурана при комнатной температуре. Смесь перемешивали в течение 2 ч, выливали в насыщенный раствор бикарбоната натрия, экстрагировали этилацетатом и промывали насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 15 мг (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ола в виде белого твердого вещества.
МС (EI+): 425 (М).
Пример 2: (20S)-20-[(3.3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль 3,3-диметилпиперидином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 453 (М).
Пример 3: (20S)-20-[(4-фенилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 5)
Обрабатывали (20S)-3р-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль N-фенилпиперазином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-[(4-фенилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 502 (М).
Пример 4: (20S)-20-[(морфолин-4-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 6)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль морфолином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-[(морфолин-4-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 427 (М).
Пример 5: (20S)-20-[(4-(пиримидин-2-ил)пиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 7)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль N-(пиримидин-2-ил)пиперазином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-[(4-(пиримидин-2-ил)пиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 504 (М).
Пример 6: (20S)-20-[(пирролидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 8)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль пирролидином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-[(пирролидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 411 (М).
Пример 7: (20S)-20-N-(3-метоксипропил)аминометил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол(соединение № 10)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-аль 3-метоксипропиламином и трис(ацетокси)боргидридом натрия, как описано в примере 1з. Выделяли (20S)-20-N-(3-метоксипропил)аминометил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 429 (М).
Пример 8: (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ол (соединение № 14)
(a) Бензоат (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3β-ола
Прибавляли 34,4 мл бензоилхлорида к раствору 70 г неочищенного (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5-ен-3β-ола (пример 1в) (не очищенный хроматографией) в 670 мл пиридина при 0-3°С. Реакционную смесь перемешивали в течение 2 ч при комнатной температуре и выливали на смесь льда с водой. Осадок отделяли фильтрованием, промывали водой и перекристаллизовывали из ацетона, получая 42 г бензоата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5-ен-3β-ола.
1НЯМР (CDCl3, δ): 8,05 (2Н, d); 7,56 (1Н, t); 7,45 (2Н, t); 5,60 (1Н, t); 4,74 (1H, m); 3,68 (1H, dd); 3,36 (1H, m).
(б) Бензоат (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5,7-диен-3β-ола
Обрабатывали 42 г бензоата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5,7-диен-3β-ола с 13,7 г 1,3-дибром-5,5-диметилгидантоина и 18 мл 2,4,6-триметилпиридина, как описано в примере 1д, получая (без очистки колоночной хроматографией) 41,9 г бензоата (20S)-4,4-диметил-20-[((триизопропилсилил)окси)-метил]прегна-5,7-диен-3β-ола.
1Н-ЯМР (CDCl3, δ): 8,05 (2Н, d); 7,57 (1Н, t); 7,45 (2H,t); 5,95 (1H, d); 5,56 (1H, m); 4,85 (1H, m); 3,7 (1H, dd); 3,39 (1H, m).
(в) 3-Бензоат (20S)-4,4,20-триметилпрегна-5,7-диен-3β,21-диола
Прибавляли 2 г размолотых молекулярных сит (4А) и 1,27 г гидрата тетрабутиламмоийфторида к раствору 2,0 г (20S)-4,4-диметил-20-[((триизопропилсилил)окси)метил]прегна-5,7-диен-3β-ола в 50 мл тетрагидрофурана. Смесь перемешивали в течение ночи при комнатной температуре, концентрировали при пониженном давлении и очищали колоночной хроматографией, получая 1,17 г 3-бензоата (20S)-4,4,20-триметилпрегна-5,7-диен-3β,21-диола.
1H-ЯМР (CDCl3, δ): 8,06 (2Н, d); 7,56 (1H, t); 7,45 (2Н, t); 5,94 (1H, d); 5,56 (1H, m); 4,85 (1H, m); 3,66 (1H, m); 3,41 (1H, m).
(г) Бензоат (20S)-4,4-диметил-20-[((толуол-4-сульфонил)окси)метил]прегна-5,7-диен-3β-ола
Раствор 0,573 г толуол-4-сульфонилхлорида в 4 мл пиридина прибавляли по каплям к раствору 0,926 г 3-бензоата (20S)-4,4,20-триметилпрегна-5,7-диен-3β,21-диола в 15 мл пиридина при охлаждении в бане со льдом. Реакционную смесь перемешивали в течение 1 ч при 0-3°С и в течение ночи при комнатной температуре. Реакционную смесь выливали в смесь льда с водой и экстрагировали этилацетатом. Органические слои объединяли, промывали 1 н. хлористоводородной кислотой, насыщенным раствором бикарбоната натрия и насыщенным солевым раствором. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении, получая 1,0 г бензоата (20S)-4,4-диметил-20-[((толуол-4-сульфонил)окси)-метил]прегна-5,7-диен-3β-ола, который в дальнейшем мог быть очищен кристаллизацией из метанола.
1Н-ЯМР (CDCl3, δ): 8,05 (2Н, d); 7,8 (1Н, d); 7,56 (1H, t); 7,45 (2H, t); 7,34 (2Н, d); 5,94 (1Н, d); 5,55 (1H, m); 4,85 (1H, m); 4,0 (1H, dd); 3,81 (1H, m); 2,45 (3H, s).
(д) Бензоат (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ола
Прибавляли 0,625 мл пиперидина к раствору 0,154 г бензоата (205)-4,4-диметил-20-[((толуол-4-сульфонил)окси)метил]прегна-5,7-диен-3β-ола в 3 мл N,N-диметилформамида. Реакционную смесь перемешивали в течение 48 ч при комнатной температуре и концентрировали при пониженном давлении. Остаток растворяли в дихлорметане и трижды промывали водой. Органический слой сушили над сульфатом натрия, фильтровали и упаривали в вакууме.
Остаток (125 мг) кристаллизовали из метанола, получая 45 мг бензоата (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ола.
1H-ЯМР (CDCl3, δ): 8,05 (2H, d); 7,57 (1H, t); 7,46 (2H, t); 5,94 (1H, d); 5,56 (1H, m); 4,88 (1H, t); 2,43 (2H, m).
(е) (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ол
Раствор 45 мг бензоата (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ола в 2,5 мл тетрагидрофурана прибавляли к суспензии 45 мг алюмогидррида лития в 2 мл тетрагидрофурана. После перемешивания в течение 2 ч при комнатной температуре прибавляли 3 мл насыщенного раствора сульфата натрия и 5 мл 1 н. раствора гидроксида натрия. Смесь трижды экстрагировали 10 мл дихлорметана. Органические слои объединяли, промывали 1 н. раствором гидроксида натрия и водой, сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток (35 мг) очищали колоночной хроматографией, получая 22 мг (20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-5,7-диен-3β-ола.
1H-ЯМР (CDCl3, δ): 5,93 (1H, d); 5,53 (1H, m); 3,4 (1H, t); 2,42 (2H, m); 1,22 (3H, s); 1,13 (3H, s); 1,02 (3H, d); 0,98 (3H, s); 0,6 (3H, s).
Пример 9: (20S)-20-[(4-(пиридин-2-ил)пиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 15)
(a) (20S)-4,4,20-Триметил-21-тозилоксипрегна-8,14-диен-3β-ол
Прибавляли 4,7 г тозилхлорида небольшими порциями к раствору 4,5 г (20S)-4,4,20-триметилпрегна-8,14-диен-3β,21-диола в 91 мл пиридина при комнатной температуре. Смесь перемешивали в течение 3 ч при комнатной температуре и затем концентрировали при пониженном давлении. Остаток растворяли в этилацетате, промывали водой и раствором хлористого натрия. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 3,2 г (20S)-4,4,20-триметил-21-тозилоксипрегна-8,14-диен-3β-ола в виде белого твердого вещества.
МС (EI+): 512 (М).
б) (20S)-3β-Гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбонитрил
Прибавляли 1,7 г цианистого калия к раствору 4,7 г (20S)-4,4,20-триметил-21-тозилоксипрегна-8,14-диен-3β-ола в 90 мл ДМСО при комнатной температуре. Смесь перемешивали в течение 2 ч при 90°С, выливали в воду, экстрагировали этилацетатом и промывали водой. Органический слой сушили сульфатом натрия, фильтровали и концентрировали при пониженном давлении, получая 2,8 г (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбонитрила в виде белого твердого вещества, которое использовали без дальнейшей очистки.
МС (EI+): 367 (М).
(в) (20S)-3β-Гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид
Прибавляли 16 мл диизобутилалюминийгидрида (20% в толуоле) по каплям к раствору 920 мг (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбонитрила в 60 мл толуола при температуре -72°С. Смесь перемешивали в течение 2 ч при той же температуре, выливали в раствор 2 н. серной кислоты, экстрагировали этилацетатом, промывали 2 н. серной кислотой и затем промывали полунасыщенным раствором хлористого натрия. Органический слой сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении, получая 750 мг (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегида в виде белого твердого вещества, которое использовали без дальнейшей очистки.
МС (EI+): 370 (М).
(г) (20S)-20-[(4-(Пиридин-2-ил)пиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол
Прибавляли 107 мг трис(ацетокси)боргидрида натрия к раствору 125 мг (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегида и 82,6 мг N-(2-пиридил)-пиперазина в 2 мл тетрагидрофурана при комнатной температуре. Смесь перемешивали в течение 20 ч, выливали в воду и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией, получая 84 мг (20S)-20-[(4-(пиридин-2-ил)пиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ола в виде белого твердого вещества.
МС(EI+): 517(М).
Пример 10: (20S)-20-[(4-фенилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение №16)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид N-фенилпиперазином и трис(ацетокси)боргидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(4-фенилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС(EI+): 516 (М).
Пример 11: (20S)-20-[(4-метилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 17)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид 1-метилпиперазином и трис(ацетокси)бор гидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(4-метилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 454 (М).
Пример 12: (20S)-20-[(N,N-диметиламино)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 18)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид N,N-диметиламином и трис(ацетокси)боргидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(N,N-диметиламино)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 399 (М).
Пример 13: (20S)-20-[(морфолин-4-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 19)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид морфолином и трис(ацетокси)боргидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(морфолин-4-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 441 (М).
Пример 14: (20S)-20-[(пирролидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 20)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид пирролидином и трис(ацетокси)боргидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(пирролидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 425 (М).
Пример 15: (20S)-20-[(пиперидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол (соединение № 21)
Обрабатывали (20S)-3β-гидрокси-4,4,20-триметилпрегна-8,14-диен-21-карбальдегид пиперидином и трис(ацетокси) бор гидридом натрия, как описано в примере 9г. Выделяли (20S)-20-[(пиперидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол в виде белого твердого вещества.
МС (EI+): 439 (М).
Пример 16: (20S)-20-[(4-фенилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение № 22)
(а) Метиловый эфир 3β-трет.-бутилдиметилсилилоксибиснорхоленовой кислоты
Перемешивали 3β-гидроксибиснорхоленовую кислоту (10 г), бикарбонат калия (12 г), йодистый метил (10 мл) и диметилформамид в течение 3 суток при комнатной температуре и выливали в воду (1,5 мл). Белый осадок отделяли фильтрованием. Прибавляли диэтиловый эфир к белому осадку, и нерастворимый материал отфильтровывали. Концентрация эфирной фазы в вакууме дала неочищенный силиловый эфир, который растворяли в диметилформамиде (400 мл). Прибавляли трет.-бутилдиметилсилилхлорид (6 г) и имидазол (6 г), и смесь концентрировали в вакууме и очищали флэш-хроматографией, получая 5,3 г метилового эфира 3β-трет.-бутилдиметилсилилоксибиснорхоленовой кислоты.
(б) 3β-трет.-Бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-ол
Прибавляли 2,2 экв. диизобутилалюминийгидрида (2 М) в толуоле к метиловому эфиру 3β-трет.-бутилдиметилсилилоксибиснорхоленовой кислоты, и реакционную смесь перемешивали при комнатной температуре. Реакционную смесь прибавляли к воде, экстрагировали, используя диэтиловый эфир, концентрировали в вакууме и очищали флэш-хроматографией, получая 3,3 г 3β-трет.-бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-ола.
(в) 3β-трет.-Бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-аль
Раствор Десс-Мартина (триацетоксиперйодинана) (1,9 г в 30 мл дихлорметана) прибавляли к 1,6 г 3β-трет.-бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-ола в дихлорметане (30 мл), и реакционную смесь перемешивали в течение 24 ч, затем выливали в диэтиловый эфир и экстрагировали 1 н. гидроксидом натрия. Органический слой сушили сульфатом магния и концентрировали в вакууме, получая 1,6 г 3β-трет.-бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-аля.
(г) 3β-трет.-Бутилдиметилсилилокси-(20S)-20-[(4-фенилпиперидин-1-ил)метил]-5α-прегна-5-ен
Прибавляли 4-фенилпиперидин (0,16 г) к 0,26 г 3β-трет.-бутилдиметил-силилокси-(20S)-20-метил-5α-прегна-5-ен-21-аля в ТГФ (20 мл) с последующим прибавлением трис(ацетокси)боргидрида натрия (0,38 г). Через 5 ч реакционную смесь выливали в насыщенный раствор бикарбоната натрия, экстрагировали этилацетатом, сушили и концентрировали в вакууме. Флэш-хроматография дала 76 мг 3β-7-трет.-бутилдиметилсилилокси-(20S)-20-[(4-фенилпиперидин-1-ил)метил]-5α-прегна-5-ена.
(д) (20S)-20-[(4-Фенилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол
Прибавляли 6 н. хлористоводородную кислоту (0,2 мл) к смеси 100 мг 3β-трет.-бутилдиметилсилилокси-(20S)-20-[(4-фенилпиперидин-1-ил)метил]-5α-прегна-5-ена в 10 мл этанола, и смесь перемешивали в течение 4 дней при комнатной температуре. Прибавляли дихлорметан, и органическую фазу промывали раствором бикарбоната натрия, сушили над сульфатом магния и концентрировали при пониженном давлении, получая заглавное соединение.
МС (EI+): 478 (М).
Примеры 17-22:
Воспроизводили этапы (г) и (д) из примера 16 на 3β-трет.-бутилдиметилсилилокси-(20S)-20-метил-5α-прегна-5-ен-21-але, получая следующие примеры соединений.
Пример 17: (20S)-20-[(пиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение № 23)
Используя пиперидин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 400 (М).
Пример 18: (20S)-20-[(морфолин-4-ил)метил]-5α-прегна-5-ен-3β-ол (со единение № 24)
Используя морфолин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 402 (М).
Пример 19: (20S)-20-[(пирролидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение № 25)
Используя пирролидин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 386 (М).
Пример 20: (20S)-20-[(4-карбоксиэтилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение № 26)
Используя 4-карбоксиэтилпиперидин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 472 (М).
Пример 21: (20S)-20-[(3-гидроксипиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение №27)
Используя 3-гидроксипиперидин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 416(М).
Пример 22: (20S)-20-[(4-бензоилпиперидин-1-ил)метил]-5α-прегна-5-ен-3β-ол (соединение № 28)
Используя 4-бензоилпиперидин на этапе восстановительного аминирования (г) с последующим деблокированием этапа (д), получали заглавное соединение.
МС (EI+): 504 (М).
Пример 23: исследование активирующих мейоз веществ в анализе мышиных овоцитов
Животные
Овоциты получали от незрелых самок мышей (C57BI/6J×DBA/2J F1-гибриды, Bomholtgaard, Denmark) весом 13-16 г, которые содержались при контролируемых освещении и температуре. Мыши получали внутрибрюшинную инъекцию 0,2 мл гонадотропинов [содержащую 10 международных единиц (ME) сывороточного гонадотропина жеребой кобылы (PMSG), Sigma Cat. No. G-4877)] и через 48 ч животных забивали путем смещения шейных позвонков.
Сбор и культивирование овоцитов
Яичники вскрывали и овоциты выделяли в Нх-среде (смотри ниже) под стереомикроскопом путем ручного разрыва фолликул, используя пару игл 27 размера. Сферические множественные экранированные овоциты (СЕО), обладающие интактным зародышевым пузырьком (GV), помещали в минимальную эссенциальную среду в модификации α (α-МЕМ без рибонуклеозидов, Gibco BRL, Cat. No. 22561) с добавлением 3 мМ гипоксантина (Нх) (Sigma Cat. No. Н-9377), 8 мг/мл человеческого сывороточного альбумина (HAS, State Serum Institute, Denmark), 0,23 мМ пирувата (Sigma, Cat. No. S-8636), 2 мМ глутамина (Flow Cat. No. 16-801), 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина (Flow Cat. No. 16-700) Данную среду обозначили Нх-среда.
Овоциты промывали три раза в Нх-среде и культивировали в 4-ячеечных многолуночных планшетах (Nunclon, Denmark), в которых каждая ячейка содержала 0,4 мл Нх-среды и приблизительно 25 овоцитов. Один контроль (т.е. приблизительно 25 овоцитов, культивированных в Нх-среде без добавления исследуемого соединения) всегда проводили одновременно с анализируемыми культурами, которые были приготовлены с различными концентрациями исследуемых соединений. Культуры функционировали при 37°С и влажности 100% в атмосфере с 5% углекислого газа. Время культивирования составило 22 ч.
Исследование овоцитов
Овоциты останавливали в мейозе и характеризовали с помощью интактных ядер с выпуклыми ядрышками, известными как зародышевые пузырьки (GV). При повторной инициации мейоза ядрышки и ядерные оболочки исчезают, и это характеризуется с помощью расщепления GV, которое в таком случае называют расщеплением зародышевых пузырьков (GVB). Несколькими часами позже овоцит завершает восстановленное деление и выявляется первое, так называемое, полярное тельце (РВ).
В конце культурального периода число овоцитов с зародышевым пузырьком (GV) или расщеплением зародышевых пузырьков (GVB) и овоцитов с полярным тельцем (РВ) подсчитывали, используя стереомикроском или инвертированный микроскоп с дифференциальным интерференционным контрастным оборудованием. В анализируемых культурах рассчитывали процент овоцитов с GVB от общего числа овоцитов и процент овоцитов с РВ от общего числа овоцитов и сравнивали с данными контрольной культуры.
активация мейоза в множественных экранированных мышиных экранированных овоцитах
GV означает зародышевый пузырек
GVB означает расщепление зародышевого пузырька
РВ означает полярное тельце
n означает число овоцитов
Пример 24: исследование активирующих мейоз веществ в культуральной системе мышиных фолликул
Животные
Фолликулы получали от незрелых 19-21-дневных самок мышей (C57B1/6J×CBA/J), которые содержались при контролируемых освещении и температуре.
Сбор сыворотки и культивирование фолликул
Животным давали эфирный наркоз и собирали кровь путем удаления глаз. После свертывания кровь центрифугировали в течение 15 мин при 4000g, собирали сыворотку и хранили при -20° до использования. Яичники удаляли и помещали в среду Лейбовица L-15 (Gibco Cat. No. 41300) с добавлением глутамина 1 ммоль/л, BSA 3 мг/мл, человеческого трансферрина (без железа) 5 мкг/мл, инсулина 5 мкг/мл (степень чистоты - реагенты для культур, Sigma, St. Louis, МО) при 37°С.
Преантральные фолликулы диаметром 170-190 мкм выделяли механически с двумя иглами 27 размера, присоединенными к шприцу на 1 мл. Их помещали в 4-ячеечные культуральные планшеты (Nunclon, Denmark) и после этого трижды промывали минимальной эссенциальной средой в модификации α (α-МЕМ, Gibco Cat. No. 11900) с добавлением глутамина 2 ммоль/л, трансферрина 10 мкг/мл, инсулина 10 мкг/мл и BSA 3 мг/мл.
Фолликулы 170-190 мкм нормального морфологического вида, т.е. центральный сферический овоцит, высокая плотность гранулоцитов и оболочечный слой, окружающий фолликул полностью, отбирали и по отдельности культивировали в 96-ячеечном культуральном планшете (Nunclon, Denmark) с введениями 40 мкл культуральной среды α-МЕМ с добавлением незрелой мышиной сыворотки 50 мкл/мл, инсулина 5 мкг/мл, глутамина 2 ммоля/л, человеческого трансферрина 10 мкг/мл и 0,2 международных единицы фолликулостимулирующего гормона (FSH) (Gonal F, Serono, Solna, Sweden). Без какого-либо масляного покрытия фолликулы культивировали в увлажненном термостате, наполненном воздухом с 5% CO2 при 37°С.
Начало культивирования было определено как день 0. Культуральную среду меняли каждый день. Диаметр фолликул измеряли каждый день, используя 100-кратное увеличение и калиброванный микрометр. Кроме того, выживаемость фолликул контролировали путем оценки деградации (потемнения фолликула) и разрыва (потери овоцита). Время культивирования составило 4 дня.
В день 2 и 3 культивирования исследуемое соединение или пузырек с объемом 1,72 мкл прибавляли в культуральную среду. Исследуемое соединение растворяли в этаноле (пузырек).
Исследование фолликул
Овоциты останавливали в мейозе и характеризовали с помощью интактных ядер с выпуклыми ядрышками, известными как зародышевые пузырьки (GV). При повторной инициации мейоза ядрышки и ядерные оболочки исчезают, и это характеризуется с помощью расщепления GV, которое в таком случае называют расщеплением зародышевых пузырьков (GVB).
В день 4, в конце культурального периода фолликулы контролировали на возобновление мейоза. Число фолликул, имеющих овоциты с зародышевым пузырьком (GV) или расщеплением зародышевых пузырьков (GVB), подсчитывали, используя стереомикроскоп или инвертированный микроскоп с дифференциальным интерференционным контрастным оборудованием. В анализируемых культурах рассчитывали процент фолликул с GVB от общего числа фолликул и сравнивали с контрольной культурой пузырьков.
активация созревания овоцитов в системе культуры мышиных фолликул
GVB означает овоциты с расщеплением зародышевых пузырьков
n означает число фолликул
Пример 25: лечение бесплодия с применением агониста MAS in vitro
Яйцеклетки извлекали с помощью направляемой ультразвуком трансвагинальной аспирации из яичника или стимулированной гормоном, или не стимулированной гормоном женщины-пациента.
Гормональная стимуляция могла проходить по протоколу оплодотворения in vitro (IVF) стандартной продолжительности, включающему понижающую регуляцию антагонистом гонадотропина, например, спреем для носа синарелла, затем через 14 дней ежедневную инъекцию фолликулостимулирующего гормона (FSH) (Gonal-F, подкожно) 150 МЕ/день. За 36 ч до сбора яйцеклеток пациенту давали человеческий хорионический гонадотропин (hCG) (10000 ME подкожно), чтобы вызвать окончательное созревание фолликула и овоцита.
Соединение прибавляли в культуральную среду в концентрации 3 мкМ и давали взаимодействовать с половой клеткой до оплодотворения или для опосредования, или для улучшения процедуры мейотического созревания. Овоциты оплодотворяли in vitro, культивировали in vitro и возвращали в матку пациентки обычно на день 3 после сбора овоцитов. Пациентке давали прогетерон (кринон в виде вагинального геля, 1 доза в день) и/или эстрадиол (валерат эстрадиола, 2 мг/день), чтобы улучшить имплантацию и придать матке большую восприимчивость.
Соединение, добавленное в культуральную среду, значительно улучшало качество созревания овоцитов, что привело к более высоким показателям оплодотворения, более интенсивному развитию перед имплантацией, более высоким показателям имплантации и в конечном итоге к более высокому показателю рожденных здоровыми человеческих младенцев.
Пример 26: лечение женского бесплодия с применением агониста MAS in vivo
Соединение вводили пациентке перорально дважды в день в дозе 10 мг/кг с момента окончательного созревания овоцитов, вызванного инъекцией hCG (10000 ME человеческого хорионического гонадотропина, подкожно). Человеческий хорионический гонадотропин мог быть введен в течение нормального цикла. Цикл мог быть индуцирован синдромом отмены прогестерона, вводимого минимум 10 дней перед отменой, чтобы вызвать кровотечение и циклическую активность у пациентки с аменореей или синдромом поликистозных яичников. Или hCG мог быть введен в качестве интегрированной части гормональной стимуляции нормальной продолжительности по протоколу IVF (используя понижающую регуляцию антагонистом гонадотропина, например, спреем для носа синарелла, затем через 14 дней путем ежедневной инъекции фолликулостимулирующего гормона 150-225 МЕ/день).
Пациентка получала лечение или в качестве дополнения к обычной терапии IVF с отбором яйцеклеток, IVF и переносом эмбриона, или альтернативно было применено лечение в комбинации с оплодотворением яйцеклетки, используя осеменение или естественные половые сношения.
Лечение повысило уровень агонистов MAS в сыворотке пациентки непосредственно перед овуляцией, тем самым было получено улучшенное качество созревания овоцитов. Качество подвергшейся овуляции яйцеклетки было улучшено путем индукции мейоза ежедневно вводимым соединением, которое привело к более высоким показателям оплодотворения, более интенсивному развитию перед имплантацией, более высоким показателям имплантации и в конечном итоге к более высокому показателю рожденных здоровыми человеческих младенцев.
Пример 27: лечение мужского бесплодия с применением агониста MAS in vivo
Соединение вводили перорально пациенту мужского пола дважды в день в дозе 10 мг/кг последовательно в течение, по меньшей мере, 60 (шестидесяти) дней.
Лечение повышало уровень агониста MAS в сыворотке пациента, что положительно стимулировало ход мейоза в яичке и, следовательно, с течением времени показатели качества спермы. Показатели качества спермы (число сперматозоидов, морфология, прогрессирующая подвижность и т.д.) по отдельности или вместе совершенствовали ведение к улучшенной фертильности спермы упомянутого пациента.
Это выражалось в том, что можно было избежать оплодотворения путем интрацитоплазматической инъекции спермы (ICSI) и добиться оплодотворения только путем IVF или в другом примере, что оплодотворение IVF/ICSI отменялось, и можно было добиться оплодотворения путем осеменения или естественного оплодотворения яйцеклетки.
Пример 28: терапевтическая схема женской контрацепции, использующая агонист MAS и раннее созревание овоцитов
Соединение вводили перорально пациентке дважды в день в дозе 50 мг/кг каждый день на протяжении всего нормального цикла. Пациентка получала терапию или в качестве добавления к обычному лечению по протоколу IVF с отбором яйцеклеток, IVF и переносом эмбриона, или альтернативно терапию проводили в комбинации с оплодотворением, достигнутым путем осеменения или естественных половых сношений.
Терапия повышала уровень агонистов MAS в сыворотке пациентки задолго до того, как происходила овуляция и опосредовала созревание овоцитов задолго до овуляции. В результате овуляции возникающие перезрелые овоциты больше не были жизнеспособными или способными к оплодотворению. Нормальный менструальный цикл не подвергся воздействию, не изменились также нормальный уровень и динамика стероидных гормонов.
Пример 29: терапевтическая схема женской контрацепции, использующая антагонист MAS, блокирующий ход мейоза в яичниках
Соединение вводили перорально пациентке дважды в день в дозе 50 мг/кг каждый день на протяжении всего нормального цикла.
Терапия повышала в сыворотке пациентки уровень агонистов MAS, которые эффективно ингибировали прохождение естественного созревания овоцитов. Этап овуляции проходил нормально, и цикловая активность оставалась неизмененной. Однако во время овуляции мейоз останавливался, и поэтому происходил выход незрелых и неоплодотворяемых овоцитов. Нормальные уровни и динамика стероидных гормонов оставались незатронутыми, так же как оставались незатронутыми естественная цикловая активность и месячная менструация.
Пример 30: терапевтическая схема мужской контрацепции, использующая антагонист MAS. блокирующий ход мейоза в яичке
Соединение вводили перорально пациенту мужского пола дважды в день в дозе 50 мг/кг последовательно в течение, самое меньшее, 60 (шестидесяти) дней. Прохождение сперматогенеза у мужчины занимает приблизительно 60-65 дней.
Терапия индуцировала у подвергшегося обработке субъекта уровень антагонистов MAS в сыворотке, который эффективно подавлял естественный ход мейоза и дифференциацию, которая вела к образованию оплодотворяющих зрелых сперматозоидов в яичке субъекта. Ход сперматогенеза подавлялся, и образовывались и выделялись исключительно не оплодотворяющие сперматозоиды. Однако эндокринология яичка не затрагивалась, и нормальный уровень и динамика стероидных гормонов оставались неизмененными.
ниже приведена таблица, в которой дана информация о физико-химических свойствах некоторых полученных соединений.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТИОМОРФОЛИНОВЫЕ ПРОИЗВОДНЫЕ СТЕРОИДОВ, ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ РЕГУЛИРУЮЩИХ МЕЙОЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ И СПОСОБ ПОЛУЧЕНИЯ ЭТИХ СОЕДИНЕНИЙ | 2004 |
|
RU2349597C2 |
| СТЕРОИДЫ, СПОСОБ РЕГУЛИРОВАНИЯ МЕЙОЗА | 1996 |
|
RU2182909C2 |
| ПРИМЕНЕНИЕ СОЕДИНЕНИЙ СТЕРИНА ДЛЯ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, РЕГУЛИРУЮЩЕГО МЕЙОЗ, И СПОСОБ РЕГУЛЯЦИИ МЕЙОЗА | 1995 |
|
RU2194510C2 |
| СТИМУЛЯЦИЯ МЕЙОЗА | 1996 |
|
RU2188006C2 |
| КОМПОЗИЦИЯ ДЛЯ ОПЛОДОТВОРЕНИЯ IN VITRO | 2000 |
|
RU2263516C2 |
| НОВЫЕ СТЕРОИДНЫЕ СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ В ВОДЕ И УСТОЙЧИВОСТЬЮ К МЕТАБОЛИЗМУ, И СПОСОБЫ ИХ ПРИГОТОВЛЕНИЯ | 2007 |
|
RU2458065C2 |
| СПОСОБ КАРБОНИЛИРОВАНИЯ | 2001 |
|
RU2323926C2 |
| ПРОИЗВОДНЫЕ АНДРОСТАНА, ЗАМЕЩЕННЫЕ ПО 16-ПОЛОЖЕНИЮ ЧЕТВЕРТИЧНОЙ АММОНИЕВОЙ ГРУППОЙ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2124021C1 |
| СОЕДИНЕНИЯ, НАБОР, АНДРОГЕННАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2242479C2 |
| ПРОИЗВОДНЫЕ 22-ТИАВИТАМИНА D, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ, СОЕДИНЕНИЯ | 1995 |
|
RU2142941C1 |
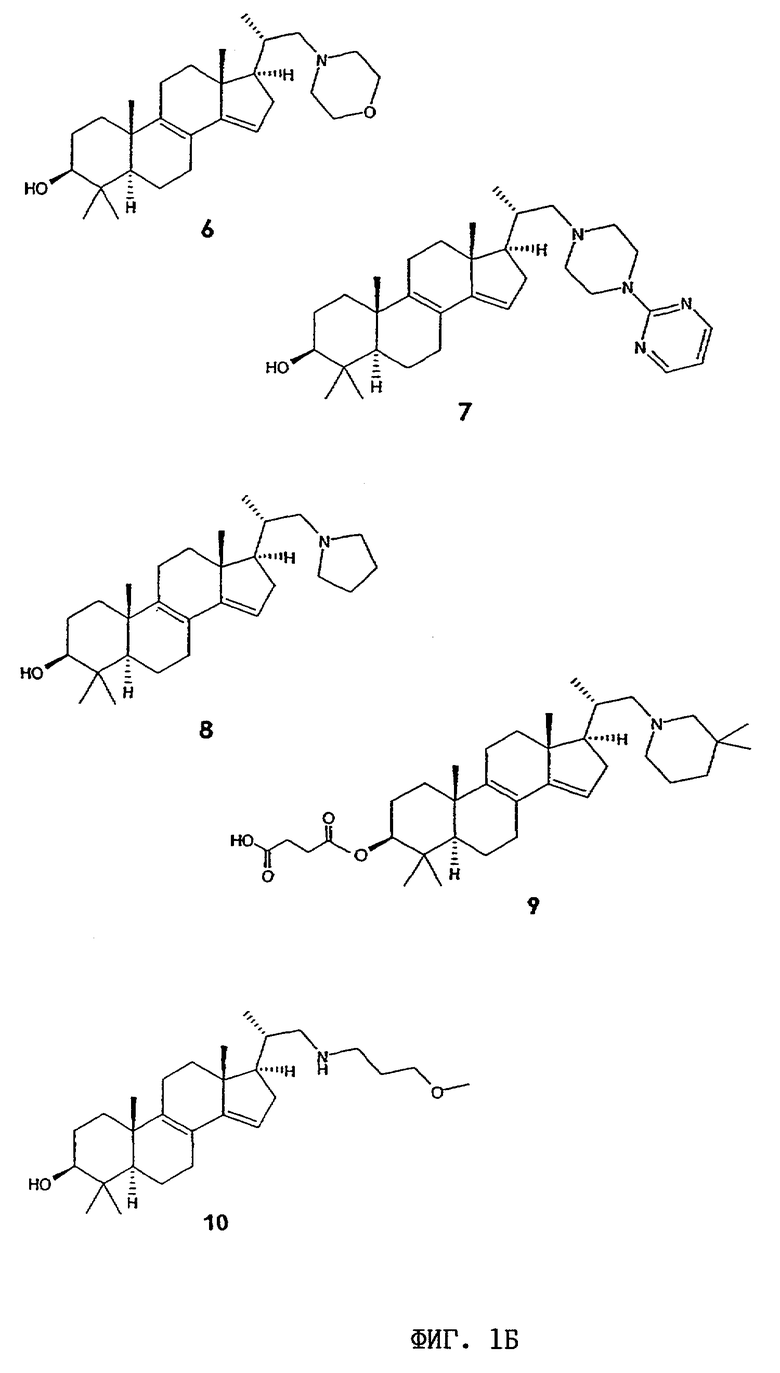
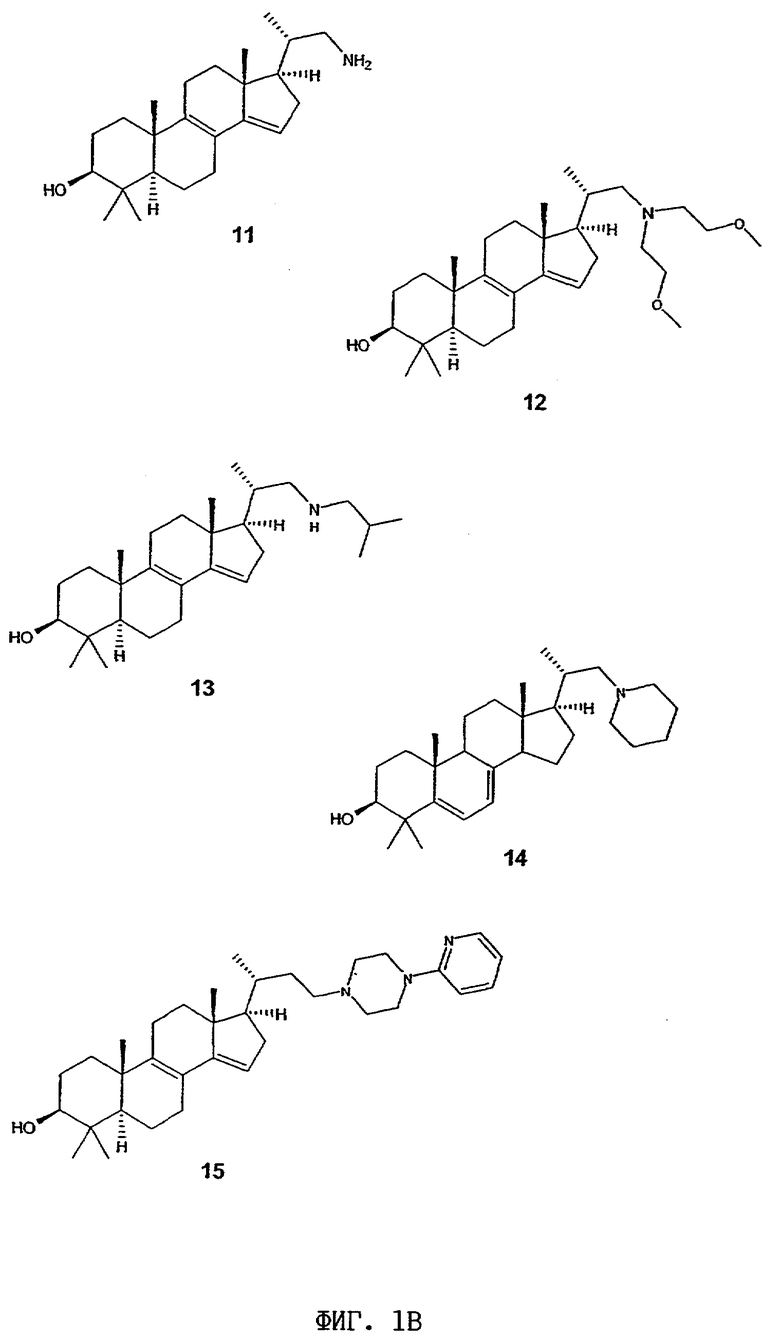
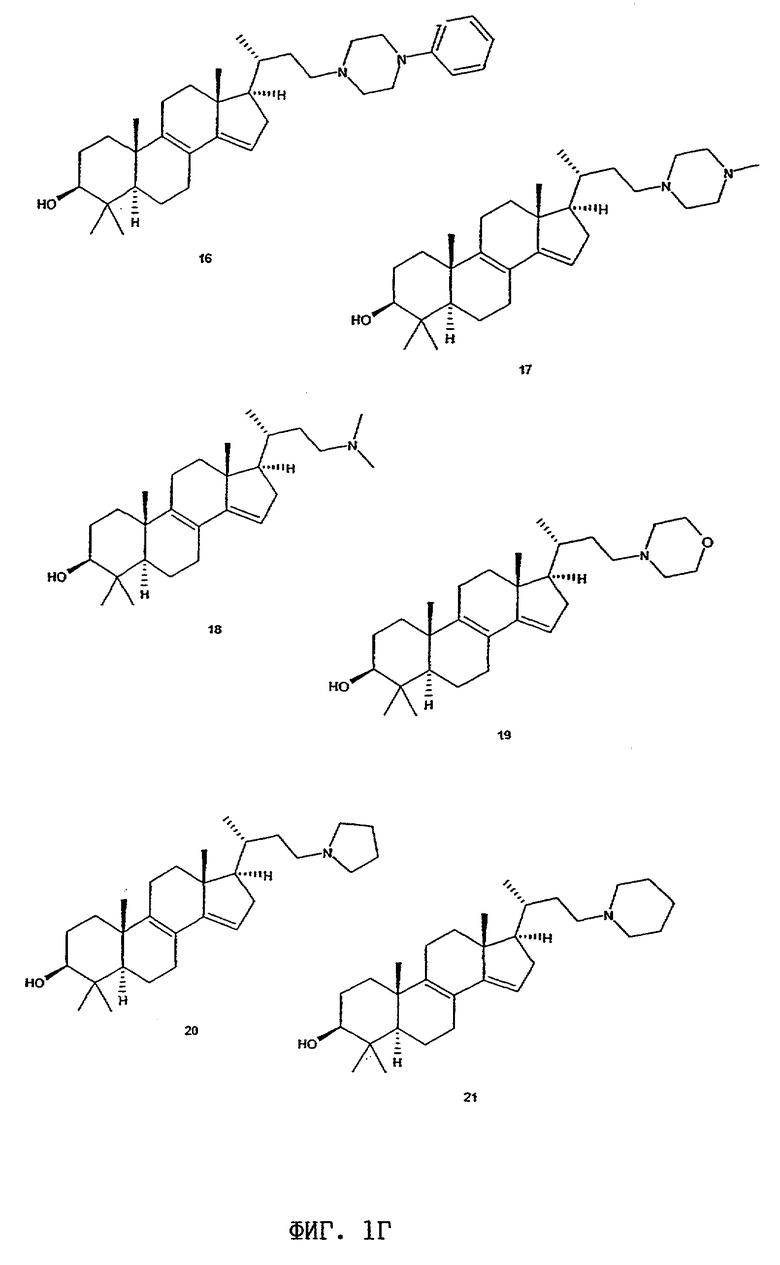
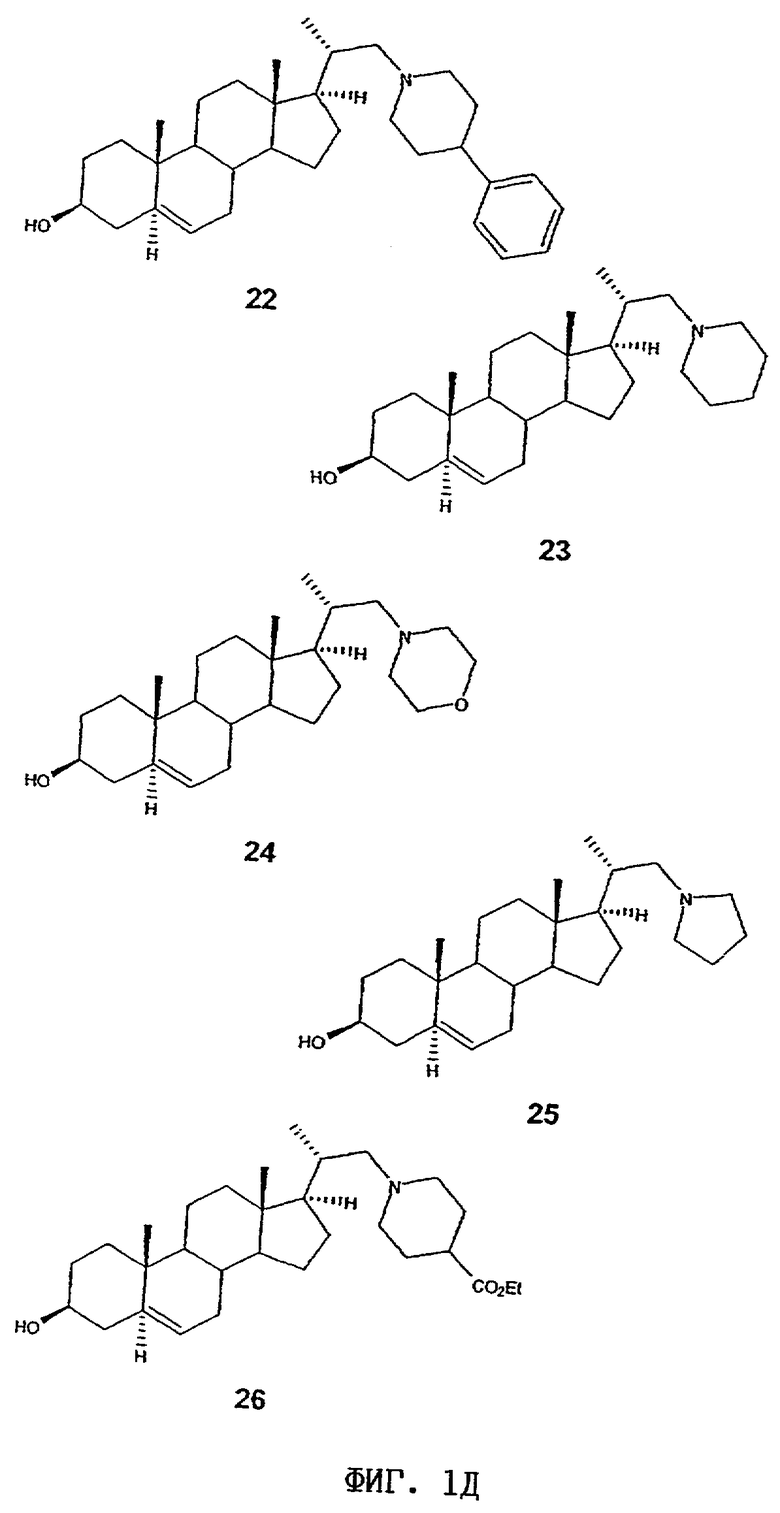
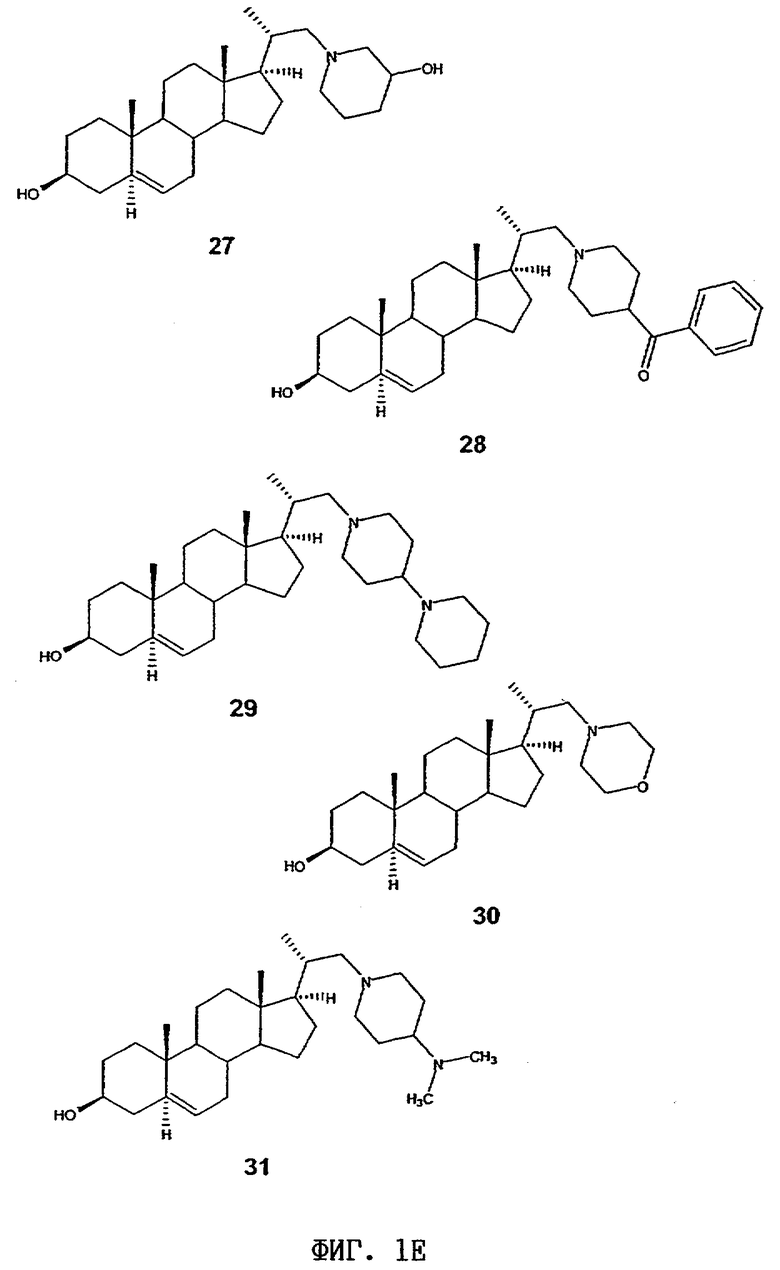

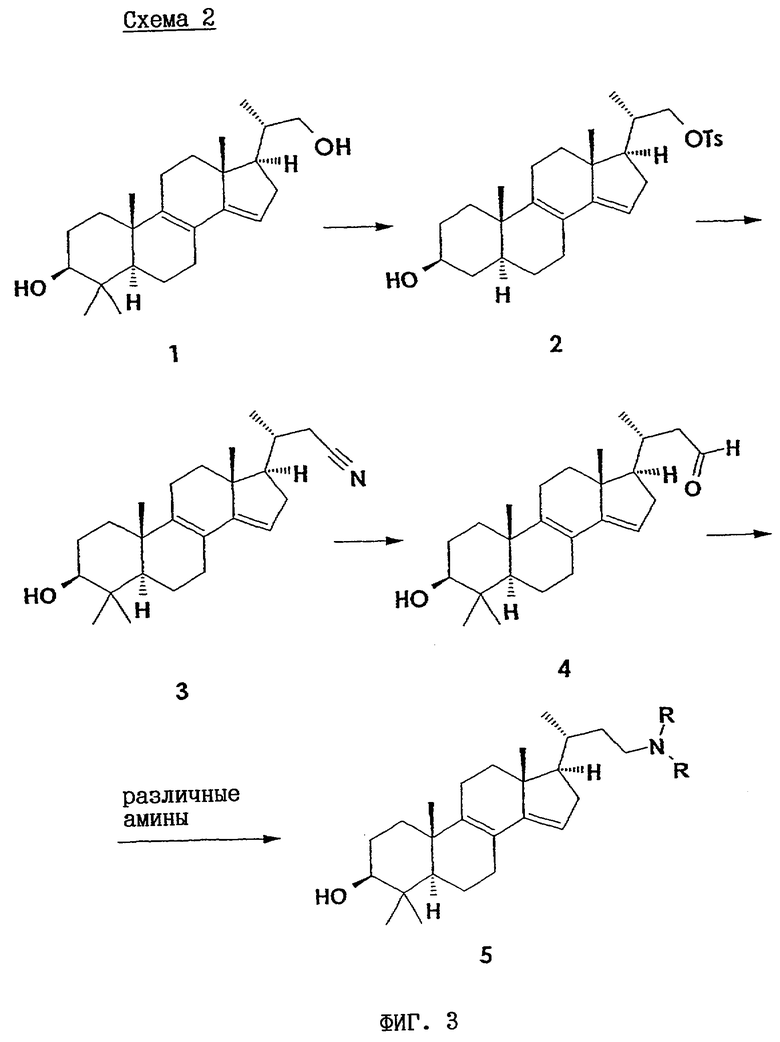
Изобретение относится к стероидным соединениям общей формулы X, где в фрагменте ХА:

каждая связь между С6 и С7, между С7 и С8, между С8 и С9, между С8 и С14 и между С14 и С15 одинарная или двойная связь при условии, что каждый атом С6, С7, С8, С9, С14 и С15 связан с каждым соседним атомом С одинарной связью или одной двойной связью, CR3-СНОН, А - метилен или этилен, R4 и R4 - C1-C4алкил, Н, R20 - С1-С4алкил, R23 и R23' - вместе - пиперидин-1-ил, морфолин-4-ил, пирролидин-1-ил, пиперазинил, возможно замещенные ОН, бензолом, пиридином, пиримидином, фенилом, алкоксикарбонилом, или R23-H, a R23' - замещенный алкил, которые могут быть с пользой применены для стимуляции мейоза в овоцитах человека, причем стероид специфически отличается тем, что атом азота аминогруппы связан с С17 стероидного скелета с помощью спейсера А.

8 н. и 8 з.п. ф-лы, 12 ил., 3 табл.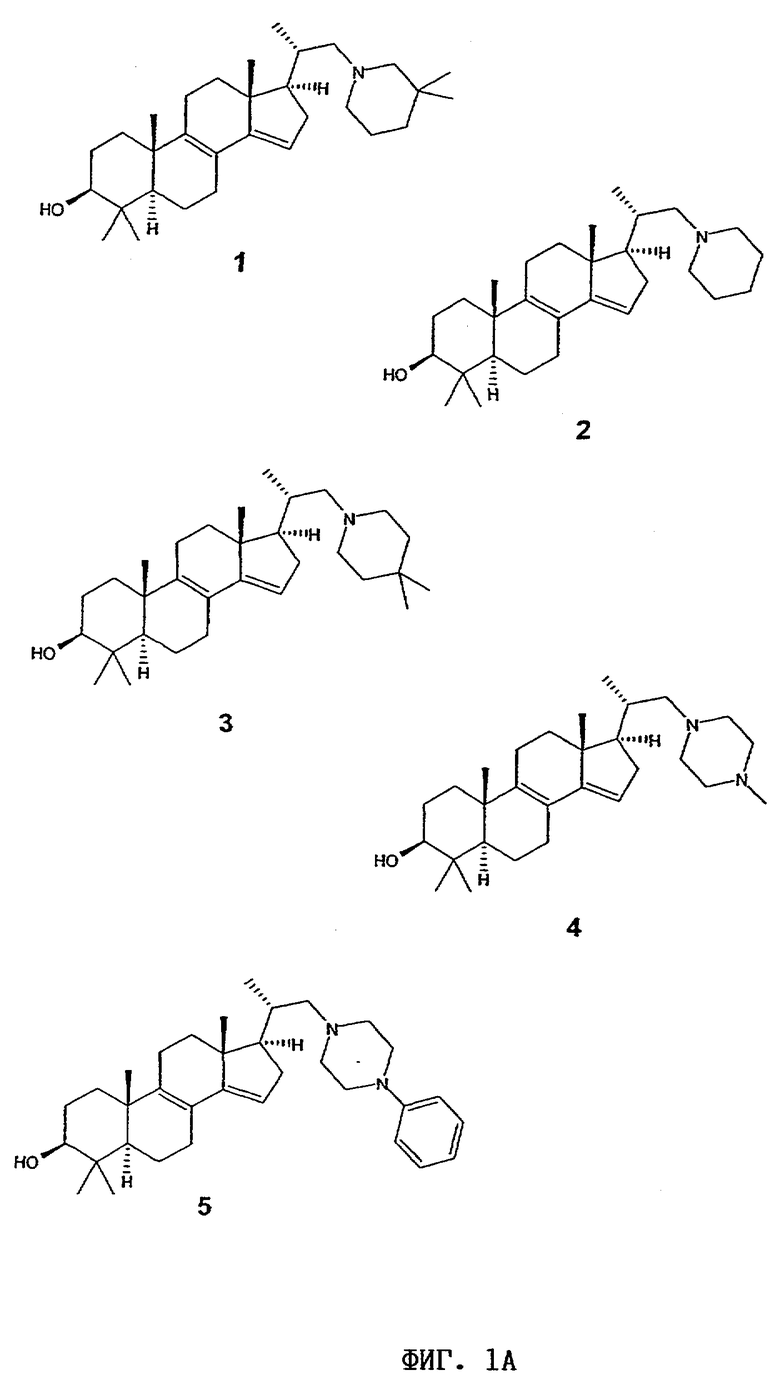
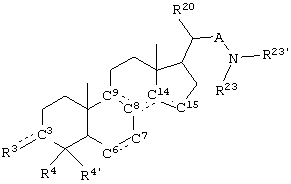
где в фрагменте
ХА:

каждая связь между С6 и С7, между С7 и С8, между С8 и С9, между С8 и С14 и между С14 и С15 означает независимо одинарную связь или двойную связь при условии, что каждый атом углерода С6, С7, С8, С9, С14 и С15 связан с каждым соседним атомом углерода одинарной связью или, самое большее, одной двойной связью;
CR3 означает СН-ОН;
А - метиленовый или этиленовый спейсер;
R4 и R4' - С1-С4алкил, водороды;
R20 - С1-C4алкил;
R23 и R23' вместе образуют пиперидин-1-ил, морфолин-4-ил, пирролидин-1-ил, пиперазинил, возможно замещенные гидроксигруппой, бензолом, пиридином, пиримидином, фенилом, алкоксикарбонилом
или R23 означает водород, а R23' - замещенный алкил.

(20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4,4-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4-метилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4-фенилпиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(морфолин-4-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4-(пиримидин-2-ил)пиперазин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(пирролидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
гемисукцинат(20S)-20-[(3,3-диметилпиперидин-1-ил)метил]-4,4-диметил-5α-прегна-8,14-диен-3β-ола,
(20S)-20-[(4-(пиридин-2-ил)пиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4-фенилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(4-метилпиперазин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(морфолин-4-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(пирролидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол,
(20S)-20-[(пиперидин-1-ил)этил]-4,4-диметил-5α-прегна-8,14-диен-3β-ол.
(20S)-20-[(пиперидин-1-ил)метил]-4,4-диметил-прегна-5,7-диен-3β-ол,
(20S)-20-[(4-фенилпиперидин-1-ил)метил]-прегна-5-ен-3β-ол,
(20S)-20-[(пиперидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(морфолин-4-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(пирролидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(4-карбоксиэтилпиперидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(3-гидроксипиперидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(4-бензоилпиперидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(4-гидроксипиперидин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(4,4-диметилпиперидин-1-ил)метил]прегна-5α-ен-3β-ол,
(20S)-20-[(4-пиперазин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[(4-фенилпиперазин-1-ил)метил]прегна-5-ен-3β-ол,
(20S)-20-[{4-(2-пиридил)пиперазин-1-ил}метил]прегна-5-ен-3β-ол,
(20S)-20-[{4-(3-пиридил)пиперазин-1-ил}метил]прегна-5-ен-3β-ол,
(20S)-20-[{4-(4-пиридил)пиперазин-1-ил}метил]прегна-5-ен-3β-ол,
(20S)-20-[{4-(2-пиримидил)пиперазин-1-ил}метил]прегна-5-ен-3β-ол.
(а) исходя из (20S)-20-метилпрегна-8,14-диен-3β,21-диола,
(б) замещение путем нуклеофильной атаки по С21,
(в) замещение нуклеофильной группы при С21 цианидом с образованием новой углерод-углеродной связи при С21,
(г) восстановление полученного нитрила с образованием альдегида,
(д) восстановительное аминирование нитрила с образованием различных аминов.
(а) исходя из (20S)-20-гидроксиметилпрегна-4-ен-3-она,
(б) введение путем алкилирования двух алкильных групп в положение 4,
(в) восстановление кетогруппы в гидроксигруппу,
(г) введение двойной связи Δ7 путем бромирования/дегидробромирования,
(д) изомеризация диена Δ5,7 в диен Δ8,14 нагреванием в присутствии кислоты,
(е) окисление 17-гидроксигруппы в альдегидную группу и
(ж) восстановительное аминирование альдегидной группы.
(20S)-4,4-диметил-20-гидроксиметил-5α-прегна-8,14-диен-3β-ол и
(20S)-4,4-диметил-5α-прегна-8,14-диен-3β-ол-20-карбальдегид.
| WO 9627658, А, 12.09.1996 | |||
| WO 9958549, А, 18.11.1999 | |||
| US 3419661, А, 31.12.1968 | |||
| DE 1930473, А, 17.12.1970. |
Авторы
Даты
2006-12-20—Публикация
2002-03-20—Подача