Область, к которой относится изобретение
Настоящее изобретение относится к области медицины, в частности к новым составам вакцинных антигенов. Технической задачей настоящего изобретения является разработка новых вакцинных составов, сведение к минимуму числа компонентов, способных индуцировать усиленный и разнообразный иммунный ответ посредством их взаимодействия. Кроме того, разработка комбинированных вакцинных составов является подходом для усиления иммунного ответа, индуцированного в отношении совместно введенных антигенов.
Предшествующий уровень техники
Существуют некоторые препятствия для получения эффективной вакцины против HCV. Поскльку он является РНК-вирусом, HCV может быстро мутировать при адаптации к окружающей среде. Это вносит свой вклад в большое многообразие последовательностей многочисленных вирусных изолятов, идентифицированных в мире. Наибольшая гетерогенность концентрируется в гипервариабельной области I белка Е2 HCV, где был описан возможный нейтрализующий эпитоп. Несмотря на существование активного иммунного ответа, HCV вызывает персистирующую инфекцию (Lechmann et al., Semin Liver Dis 2000, 20, 211-226). Не существует ни экспериментальной модели на животных, ни культуральных систем in vitro для эффективной репликации данного вируса и исследований относительно наличия нейтрализующих антител. Не были определены иммунологические структуры, ассоциированные с прогрессированием заболевания или с защитой. Возможно, что для разрешения инфекционного процесса необходимы сильные, мультиспецифичные и продолжительные как гуморальные, так и клеточные иммунные реакции (Lechmann et al., Semin Liver Dis 2000, 20, 211-226).
Для разработки вакцины против HCV было использовано несколько подходов. Наиболее широко апробированы рекомбинантные белки, синтетические пептиды, вирусоподобные частицы, ДНК вакцины и живые вирусные векторы.
Разработка вакцин, основанных на белковых субъединицах, являлась одной из первых стратегий, апробированной для HCV, поскольку антитела, направленные к поверхностным белкам, могут обеспечивать защиту от некоторых флавивирусов. Некоторые варианты, основанные на структурных антигенах HCV, достигли ограниченной защиты против данного вируса в экспериментальной модели на животных. Так дело обстоит с шимпанзе, иммунизированными E1-E2 гетеродимерами. Вакцинировали семь шимпанзе, пять были защищены, и у двух развилось заболевание, проходящее без лечения (Choo et al., PROC NATL ACAD SCI USES 1994, 91, 1294-1298). Эта защита коррелировала с наличием антител (АТ), обладающих способностью ингибировать связывание Е2 с клетками человека (Rosa et al., PROC NATL ACAD SCI USES 1996, 93, 1759-1763).
Рекомбинантный белок E1 из изолята генотипа 1 b был очищен в виде гомодимеров самоассоциирующихся в частицы диаметром 9 нм, приблизительно (Maertens et al., Records Gastroenterol Belg 2000, 63, 203). Два шимпанзе, хронически инфицированные HCV, получали 9 доз по 50 мкг рекомбинантного белка E1. Вакцинация улучшила гистологию печени и обусловила исчезновение вирусных антигенов в печени. Вакцинация рекомбинантным белком Е1 также снижает уровни аланинаминотрансферазы (АЛТ). Хотя во время лечения уровни вирусной РНК в сыворотке не изменились, после лечения усилилось воспаление ткани печени и повысились уровни вирусных антигенов. Наблюдали связь между высокими уровнями антител к Е1 и положительной динамикой заболевания (Maertens et al., Records Gastroenterol Belg 2000, 63, 203).
В частности, образование вирусоподобных частиц из рекомбинантных белков и их использование в качестве вакцин является очень привлекательным, поскольку эти структуры зачастую имитируют вирусные характеристики. Этот вид частиц, полученный из клеток насекомых, инфицированных рекомбинантным бакуловирусом, содержащим последовательность структурных антигенов HCV, обладал способностью генерировать как гуморальную, так и клеточную иммунную реакцию на эти антигены (Baumert et al., Gastroenterology 1999, 117, 1397-407; Lechmann et al., Hepatology 1999, 30, 423-429). Несмотря на ободряющие результаты, полученные с вакцинами, основанными на белковых субъединицах, иммунная реакция, индуцированная этими вариантами, является, главным образом, гуморальной, кратковременной и изолированно-специфичной.
С другой стороны, при разработке рекомбинантных вакцин против HCV были апробированы различные рекомбинантные вирусные векторы. В частности, в качестве кандидатов интерес представляют рекомбинантные аденовирусные векторы благодаря их тропизму к ткани печени, их способности индуцировать как гуморальный, так и клеточный иммунитет и пригодности для пероральной или системной доставки. Аденовирусы, содержащие последовательность ДНК, кодирующую структурные белки HCV, индуцируют антительный ответ против каждого из этих белков (Makimura et al., Vaccine 1996, 14, 28-36). Более того, после иммунизации мышей рекомбинантными аденовирусами для С и Е1, против этих антигенов определяется специфический ЦТЛ ответ (Bruna-Romero et al., Hepatology 1997, 25, 470-477). Несмотря на то, что данные результаты были ободряющими, недавние проблемы при использовании рекомбинантных аденовирусов в генной терапии вызвали сомнения в их использовании у людей. Другие рекомбинантные вирусы, подобные вирусу коровьей оспы, и оспы домашней птицы, содержащие различные гены HCV, индуцировали сильный ЦТЛ и Т-хелперный иммунные ответы у мышей (Shirai et al., J Virol 1994, 68, 3334-3342; Large et al., J Immunol 1999, 162, 931-938). Однако эти рекомбинантные вирусы, также как и другие варианты альфа вируса, подобные вирусу леса Семлики, подвергаются действию проблем регулирования и интересов безопасности, связанных с их применением.
Идентификация нескольких эпитопов для CD4+ и CD8+ T клеток в полипротеине HCV, которые могли бы иметь важное значение для ликвидации вируса, говорит в пользу исследования синтетических пептидов в качестве кандидатных вакцин против этого патогена. Различные пептиды, липидизированные или нет, содержащие эпитопы C, NS4 и NS5, индуцировали сильный CTL ответ у мышей (Shirai et al., J Infect Dis 1996, 173, 24-31; Hiranuma et al., J Gene Virol 1999, 80, 187-193; Oseroff et al., Vaccine 1998, 16, 823-833).
Другая стратегия, используемая для разработки вакцины против HCV, основана на возможности образовывать антитела против линейных эпитопов. Эта альтернанива была апробирована по существу для генерирования антител против HVR-I HCV, с некоторыми ободряющими результатами у кроликов и шимпанзе (Esumi et al., Arch Virol 1999, 144, 973-980; Shang et al., Virology 1999, 258, 396-405). Псевдовиды являются основной проблемой отбора HVR-I в качестве мишени для вакцины против HCV.
Основным препятствием для пептидных вакцин является то, что эти пептиды без эпитопов для хелперных Т-клеток могут быть недостаточно иммуногенны. Более того, эффективность вакцины зачастую основана на индукции специфического иммунного ответа против широкого ряда различных антигенов. Данные ограничения являются важными недостатками этой стратегии.
ДНК иммунизация является одной из последних стратегий в разработке вакцин. ДНК вакцина состоит из очищенной плазмиды, содержащей последовательность, кодирующую интересующий антиген, под контролем фукциональной единицы транскрипции в эукариотических клетках. После инъекции данной плазмиды в мышцу или кожу данная плазмида поглощается клетками-хозяевами и данный антиген экспрессируется внутриклеточно. Данная экспрессия закодированных антигенов в клетках-хозяевах является главным преимуществом этой методики, поскольку сходна с естественными вирусными инфекциями. Другим перимуществом ДНК вакцинации является простота манипулирования ДНК, вместе со стабильностью ДНК, что делает возможной относительно дешевую массовую продукцию ДНК.
Иммунный ответ, индуцированный этим типом вакцин, может быть видоизменен под действием ко-иммунизации молекулами или генами, кодирующими ко-стимуляторные молекулы, подобные цитокинам. Данные генетические конструкции могут быть модифицированы вставками или делециями трансмембранных доменов, сигнальными последовательностями секреции или остатками других типов, влияющих на внутриклеточный транспорт и процессинг данного антигена.
В частности, ДНК иммунизация была значительно изучена при разработке вакцин против HCV. Были созданы различные векторы экспрессии, кодирующие полные или усеченные варианты капсидного белка HCV (Lagging et al., J Virol 1995, 69, 5859-5863; Chen et al., Vaccine Res 1995, 4, 135-144). Другие конструкции также включают в себя 5' нетранслируемую область HCV 5' (Tokushige et al., Hepatology 1996, 24, 14-20). Были апробированы плазмиды, экспрессирующие слитые варианты к поверхностному антигену вируса гепатита B (HBV) или другим антигенам оболочки HBV (Major et al., J VIROL 1995, 69, 5798-5805). Иммунизация данными плазмидами, главным образом, индуцировала определенную ЦТЛ и лимфоцитпролиферативную реакцию.
Белки оболочки HCV также представляют интерес для этого вида технологии. В случае HCV E2 кажется, что гуморальная реакция, главным образом, направлена на HVR-1 (Lee et al., Mol Cells 1998, 8, 444-451). Иммунизация плазмидами, экспрессирующими внутриклеточные или секретируемые варианты E1 и E2 белков, воспроизвела сходную иммунную реакцию (Lee et al., J VIROL 1998, 72, 8430-8436). Заражение бицистронными плазмидами, экспрессирующими GM-CSF и E1 или E2 белки HCV, усиливает и гуморальный и клеточный иммунный ответ. В последнее время бицистронные плазмиды, экспрессирующие белки Е1 и Е2, использовали для исследования влияния гетеродимерной структуры между данными белками in vivo на иммунный ответ, индуцированный после ДНК иммунизации. При образовании гетеродимеров не было получено антительного ответа против Е1 и Е2 белков HCV. В резком отличии от этого, после иммунизации плазмидами, экспрессирующими усеченные варианты Е1 и Е2, были получены высокие уровни титров антител, направленных и к линейным и к конформационным эпитопам. Следовательно, кажется необходимым избегать гетеродимерных структур для получения сильного антительного ответа в тех случаях, когда апробируют конструкции, включающие в себя данные антигены (Fournillier et al., J VIROL 1999, 73, 497-504).
По этой технологии также были апробированы неструктурные белки. Были получены хорошие результаты при включении в вектор области, кодирующей С-концевой домен белка NS3, что дает возможность одновременной и независимой экспрессии этого домена и IL-2 (Papa et al., Res Virol 1998, 149, 315-319). Под действием этой стратегии иммунизации белки NS4 и NS5 также генерируют антительный и ЦТЛ ответы (Encke et al., J IMMUNOL 1998, 161, 4917-4923). В последнее время использование конструкции, кодирующей GM-CSF и неструктурные белки вириона (NS3, NS4 и NS5), индуцировало сильный антительный ответ и потенцированную лимфопролиферативную реакцию против каждого неструктурного белка (Cho et al., Vaccine 1999, 17, 1136-1144).
В общих чертах для различных ДНК конструкций сообщалось об эффективной экспрессии различных антигенов HCV, а также о генерации анти-HCV антител на уровнях, начиная от 1:100 и до 1:100000 в соответствии с комбинацией в исследовании (Inchauspe et al., Vaccine 1997, 15, 853-856). Дополнительно было показано развитие специфической ЦТЛ лимфоцитпролиферативной реакции (Inchauspe et al., DNA AND CELL BIOLOGY 1997, 16, 185-195). Однако требуются усилия для улучшения этой методики для воспроизведения сильного и гуморального, и клеточного ответа против различных белков HCV. Таким образом, было апробировано несколько вариантов, таких как липосомы (Gramzinski et al., Mol Medicine 1998, 4, 109-118) и сапонин QS-21 (Sasaki et to the., J Virol 1998, 72, 4931-4939) для усиления иммунного ответа, индуцированного после ДНК вакцинации. При ДНК иммунизации в качестве биологических адъювантов также были изучены дендритные клетки. Дендритные клетки (ДК), полученные из клеток генетически модифицированого костного мозга мыши для экспрессии опухолевых антигенов с использованием вирусных векторов (Specht et al., J Exp Med 1997, 186, 1213-1221; Brossart et al., J Immunol 1997, 158, 3270-3276; Song et al., J Exp Med 1997, 186, 1247-1256) или РНК (Boczkowski et to the., J Exp Med 1996, 184, 465-472), продемонстрировали способность стимулировать Т клеточный ответ, специфичный в отношении опухолевых антигенов и клеточно опосредованный профилактический иммунитет против опухолей у мышей.
В настоящее время усовершенствование векторов для ДНК иммунизации, включающее в себя вставку CpG мотивов для усиления иммунного ответа против экспрессированных антигенов (Hasan et al., J Immunol Meth 1999, 229,1-22), и системы доставки ДНК, является ключевым для преодоления ограничений этой технологии.
Благодаря признакам, которые описывают HCV инфекцию, и из-за отсутствия четкого определения в отношении иммунологических параметров, коррелирующих с защитой от этого патогена, возможно, что эффективная вакцина против HCV потребует мультиспецифического подхода, стимулирующего несколько аспектов иммунного ответа. Решение этой проблемы возможно заключается в комбинировании отдельных методик иммунизации, исследованных к настоящему времени. В частности, были апробированы схемы иммунизации, которые объединяют первую дозу с ДНК вакциной и ревакцинирующую дозу с рекомбинантными белками или вирусными векторами (Hu et al., Vaccine 1999, 17, 3160-3170; Pancholi et al., J Infect Dis 2000, 182, 18-27), несмотря на положительные результаты требовались дополнительные исследования для доказательства могут ли реально стратегии первой активной иммунизации индуцировать протективный иммунитет против HCV.
Дополнительно для модели гепатита В была апробирована вакцинная композиция, содержащая комплекс, образованный поверхностным антигеном вируса гепатита В, антителом, специфичным к данному антигену и ДНК вакциной, экспрессирующей данный антиген (Wen et al., US6221664, 1998). Этот состав давал возможность антигенной презентации различными способами и быстрой индукции иммунного ответа, который в результате лучше относительно иммунного ответа, вызванного отдельными вариантами.
В настоящем изобретении описан вакцинный состав, содержащий в качестве компонентов только белковый антиген и плазмиду, экспрессирующую один или несколько белков, по меньшей мере один из которых действует как адъювант другого. В частности, апробированы капсидный антиген вируса гепатита С или В и плазмида, экспрессирующая единичные или полипротеиновые варианты белка Е1 HCV. В противоположность композициям, описанным ранее для модели гепатита В, присутствие антител в данном составе не требуется для того, чтобы вызвать активацию иммунного ответа, следовательно, требуется уменьшение количества компонентов. Кроме того, наибольшая гибкость в вакцинной композиции также дает возможность генерировать одновременно сильный иммунный ответ против различных антигенов.
Подробное описание изобретения
Настоящее изобретение относится к композиции и способам профилактической или терапевтической иммунизации против HCV и HBV, а также к их комбинации. Это первое сообщение о вакцинном составе, содержащем в качестве компонентов: (а) ДНК, экспрессирующую вариант белка, включающий в себя области Е1 антигена оболочки HCV и (b) белковый антиген HCV или HBV, в соответствующих пропорциях. Новизна настоящего изобретения показана адъювантным действием по меньшей мере одного компонента на иммунную реакцию, вызываемую на другой компонент. Антигены, кодируемые генетическими конструкциями и экспрессируемые клетками-хозяевами, а также белковые антигены, включенные в вакцинный состав, являются интересными объектами для формирования иммунного ответа против HCV и HBV. Таким образом, иммунный ответ может быть направлен против широкого спектра важных антигенов.
Данный вакцинный состав включает в себя ДНК, усиливающую иммунный ответ на белковый антиген, смешанную с ним; это действие является зависимым от экспрессии одного или нескольких белков, кодируемых данной ДНК, у иммунизируемого хозяина. ДНК получают из бактериального штамма и очищают в соответствии с принятыми методиками (Horn et al., H Gene Ther 1995, 6, 565-573).
Данный вакцинный состав в предпочтительном варианте осуществления включает в себя по меньшей мере одну из следующих плазмид: pIDKE1S, pIDKE2 и pAEC-ME, ДНК последовательности которых, кодирующие экспрессируемые белковые варианты, идентифицированы последовательностями с номерами 2-4, соответственно.
Плазмида pIDKE1S экспрессировала белок, содержащий аминокислоты от 176 до 363 HCV E1 (Sec. Id. No. 2). С другой стороны, плазмида pIDKE2 экспрессировала белок, включающий первые 650 аминокислот вирусного полипротеина (C, E1 и часть E2) (Sec. Id. No.3). Плазмида pAEC-ME экспрессирует химерный белок, содержащий В и Т клеточные эпитопы различных антигенов HCV (Sec. Id. No. 4). В этих плазмидах кодирующая последовательность для вирусных антигенов была получена из кДНК HCV кубинского изолята (Morales et al., 1998, WO 98/25960). Плазмиды pAEC-ME, pIDKE1S и pIDKE2 содержат кодирующие последовательности для антигенов HCV, вставленных в множественный клонирующий сайт pAEC-K6 плазмиды (Herrera et al., Biochem Biophys Res Commun. 2000, 279, 548-551). Плазмиды, включенные в настоящее изобретение имеют регуляторные элементы, способные управлять антигенной экспрессией в клетках человека. Данные регуляторные элементы включают в себя функциональную единицу транскрипции у млекопитающих, интегрированную, например, промотором цитомегаловируса человека и сигналом полиаденилирования обезьяньего вируса 40. Данные плазмиды также содержат репликатор у бактерий и маркер селекции на устойчивость к канамицину.
Белковый компонент этого состава может быть растворимым вирусным антигеном, способным образовывать частицы, с чистотой выше 90%. В предпочтительных вариантах осуществления, компонентами этого вакцинного состава являются капсидные антигены HCV и HBV, усиливающие иммунный ответ, вызванный против белков, экспрессируемых ДНК, смешанной с ними.
Настоящее изобретение также рассматривает методику смешивания ДНК с антигеном. Указанную смесь готовят путем добавления компонентов, ДНК и антигена, растворенных в соответствующем буфере. В предпочтительных вариантах осуществления этот состав может быть приготовлен путем объединения обоих компонентов, растворенных в фосфатно-солевом растворе, в пропорции 10/1 (масс/масс). Указанную смесь инкубируют по меньшей мере 2 часа при температуре от 26°C до 30°C, взбалтывая перед введением пациентам. Данный состав может быть введен внутримышечно, подкожно, интраперитонеально, подслизисто, внутривенно, сублингвально, или другим путем. Иммунизация может быть проведена с помощью шприца, генной пушки, спреев или других способов доставки. Каждый пациент получает дозу начиная от 0,001 и до 10 мг каждого компонента в объеме, определяемом видом животного и используемой методикой иммунизации.
В случае вакцинных составов, содержащих в качестве компонентов ДНК, смешанную с белковым антигеном, может быть получен лучший продукт по сравнению с каждым отдельным компонентом вследствие:
возможности вызывать сильный и разнообразный как гуморальный, так и клеточный иммунный ответ, направленный на более широкий ряд эпитопов;
токсическое действие, вызываемое введением адъюванта может быть устранено, поскольку антиген 2 одновременно является адъювантом;
возможности использования указанных составов в качестве основы для комбинированных вакцин.
Технологический процесс получения вакцинного состава не требует адсорбирования антигена.
В случае, когда речь идет о составах, содержащих ДНК, экспрессирующую вариант белка, который содержит области белка Е1 HCV, капсидного белка HCV, может быть получен лучший продукт по сравнению с каждым отдельным компонентом вследствие:
возможности вызывать сильный и разнообразный как гуморальный, так и клеточный иммунный ответ, направленный на более широкий ряд эпитопов;
токсическое действие, вызываемое введением адъюванта может быть устранено, поскольку антиген 2 одновременно является адъювантом;
возможности использования ДНК плюс капсид в качестве основы для комбинированных или мультивалентных вакцин.
С другой стороны, иммунизация ДНК, экспрессирующей вариант белка, который содержит области белка Е1 HCV, увеличила иммуногенность белковых антигенов HBV, присутствующих в данном составе. В частности, смесь с HBsAg или HBcAg, дает лучшие результаты, чем результаты, полученные с этими антигенами вследствие того, что:
a) уровни IgG, индуцированного против HbsAg, выше уровней, полученных при вакцинации HBsAg с гидроксидом алюминия;
b) создает возможную комбинированную вакцину HBV-HCV;
c) в процессе составления не требуется адсорбции антигена.
Описание фигур
Фиг.1. Схематическое представление плазмид pAEC-ME, pIDKE1S и pIDKE2.
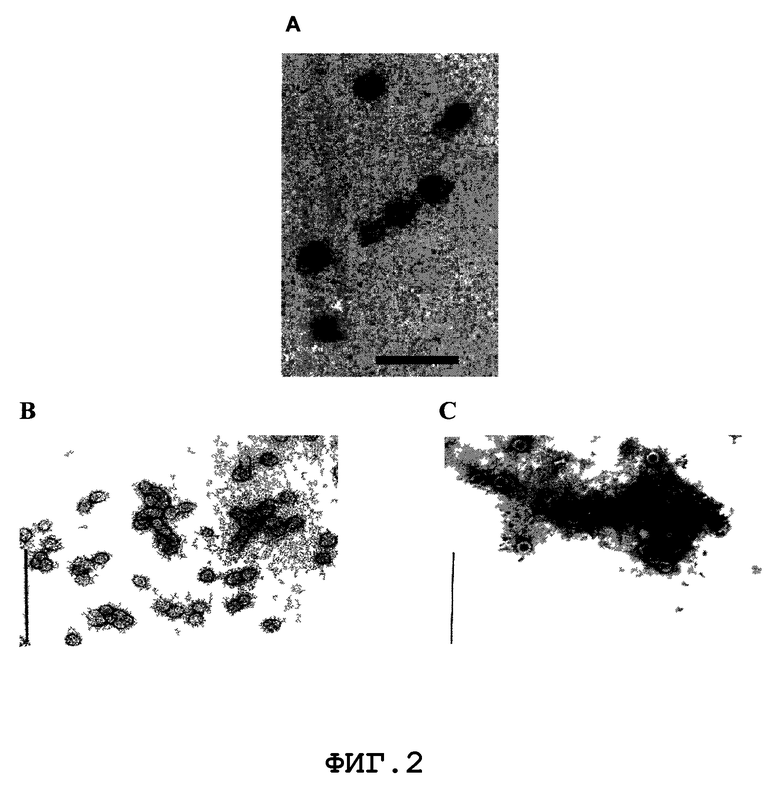
Фиг.2. Электронная микроскопия частиц капсида вируса гепатита С (A), поверхностного антигена вируса гепатита В (B) и капсида вируса гепатита В (C).
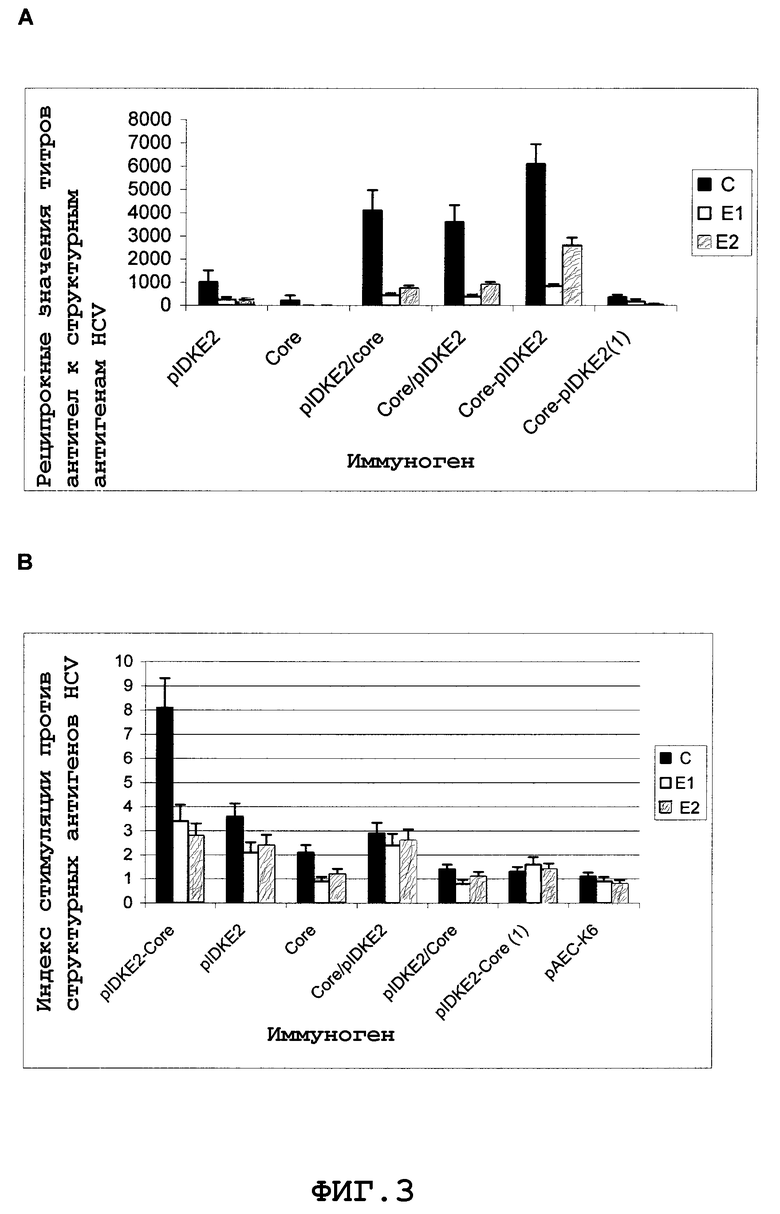
Фиг.3. Схема иммунизации плазмидой pIDKE2 и Капсидным белком. Животных иммунизировали внутримышечно 50 мкг ДНК и 5 мкг белка.
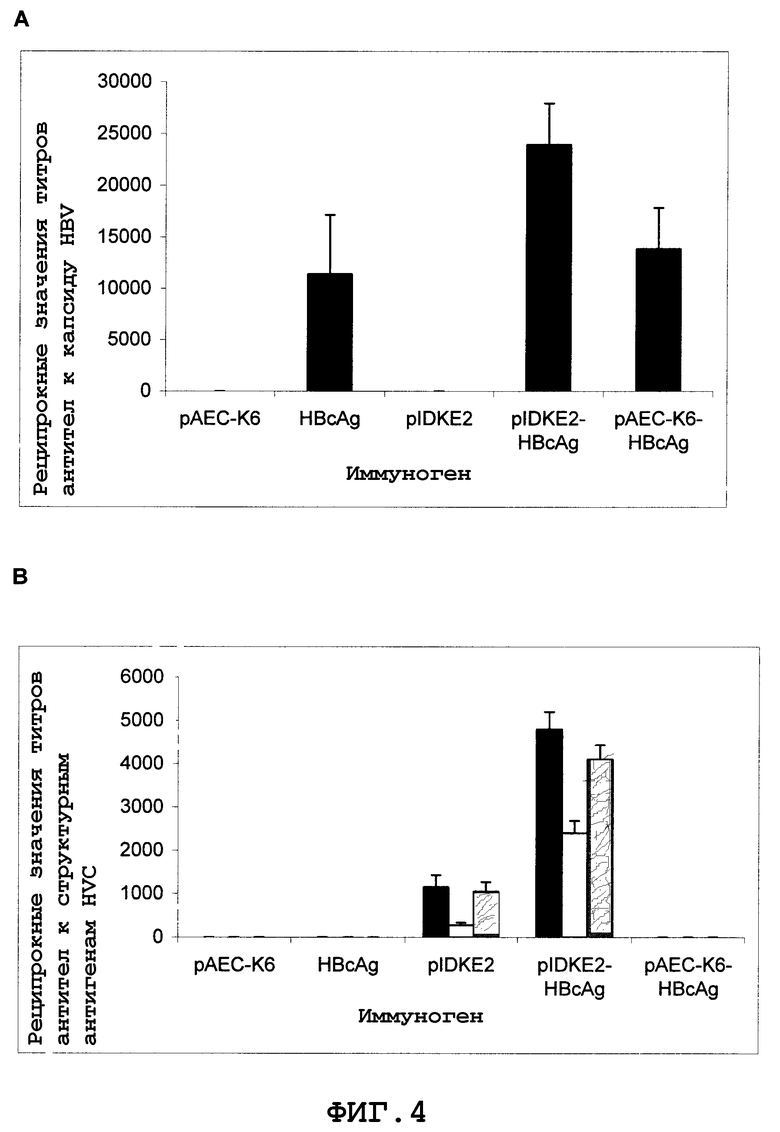
Фиг.4. Схема иммунизации различными плазмидами и белком HBcAg. Животных иммунизировали внутримышечно 50 мкг ДНК и 5 мкг белка.
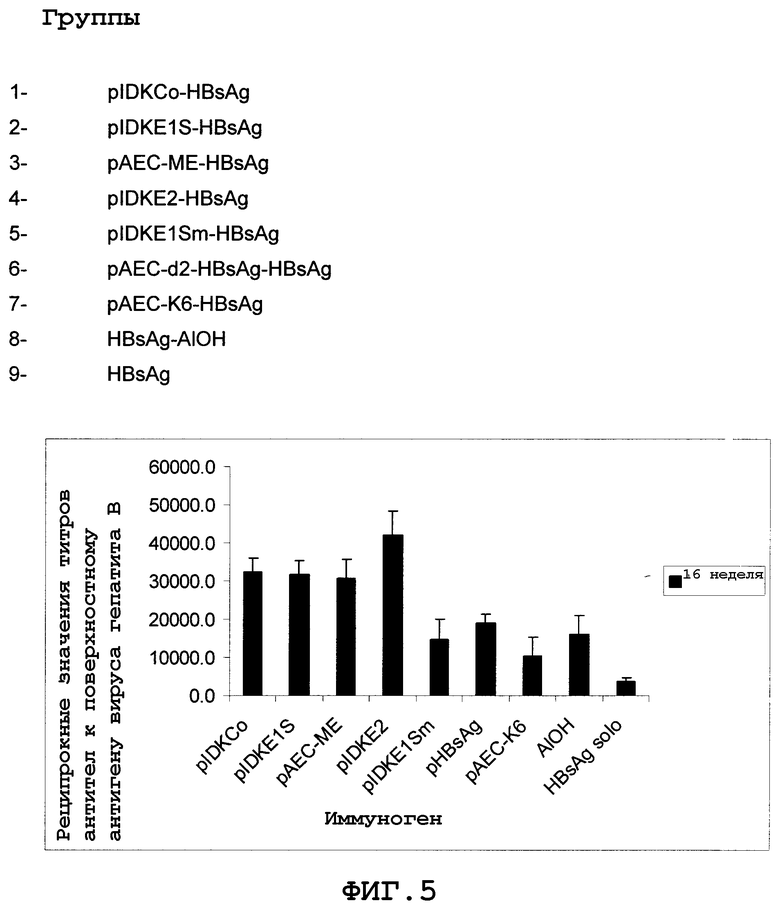
Фиг.5. Схема иммунизации различными плазмидами и белком HBsAg. Животных иммунизировали внутримышечно 50 мкг ДНК и 5 мкг белка.
Примеры
Пример 1: Иммуногенность составов, содержащих в качестве компонентов ДНК, экспрессирующую полипротеин Капсид-E1-E2 HCV, и белковый антиген капсида HCV
С целью демонстрации усиления иммунного ответа, вызываемого против структурных антигенов HCV после введения смеси плазмиды pIDKE2 (Фиг.1) с рекомбинантными частицами капсида HCV (Фиг.2A), иммунизировали внутримышечно группы по 10 самок мышей BALB/c в возрасте 8 недель. Схема включала в себя 2 иммунизации в дни 0 и 21 за исключением одной из групп, в которой изучали действие однократной дозы. Образцы крови брали через 14 недель после первой иммунизации. Иммуногены вводили в фосфатно-солевом буферном растворе (PBS). Группу 1 иммунизировали 50 мкг pIDKE2 плазмиды (Фиг.1, данная плазмида содержит последовательность, кодирующую первые 650 аминокислот вирусного полипротеина, Sec. Id. No.3). Группу 2 иммунизировали 5 мкг Капсидного белка (содержащим первые 173 аминокислоты капсидного белка HCV). Группа 3 получила в первой дозе 5 мкг Капсидного белка и во второй дозе 50 мкг pIDKE2 (Core/pIDKE2). Группу 4 иммунизировали в условиях, подобных иммунизации группы 3, но в обратном порядке (pIDKE2/Core). Группу 5 иммунизировали смесью 50 мкг pIDKE2 и 5 мкг Капсидного белка в дни 0 и 21 (Core-pIDKE2). Группу 6 иммунизировали таким же образом, как группу 5, но только в день 0 (Core-pIDKE2 (1)). Дополнительно, седьмую группу, отрицательный контроль, иммунизировали 50 мкг плазмиды pAEC-K6 (плазмида не содержит последовательности, кодирующие антигены HCV).
Антительный ответ определяли с помощью ELISA для обнаружения антительного ответа против структурных белков HCV. Для анализа результатов использовали критерий Стьюдента, статистические расхождения принимали при p < 0,05.
Фиг.3 показывает, что возможно усиление иммунного ответа на структурные антигены HCV путем введения двух доз смеси pIDKE2 с Капсидным белком по отношению к отдельным компонентам. Этот состав (в двух дозах) индуцировал титры антител против Е1 и Е2 белков оболочки HCV статистически выше тех, что получены в остальных группах (Фиг.3A). Эти титры антител были также статистически выше уровней антител против капсидного белка HCV, образованных под действием смеси pIDKE2-Core, вводимой в единичной дозе (Фиг.3A). Вакцинация смесью в единичной дозе всегда вызывала более низкие уровни антител среди иммунизируемых групп.
Оценка лимфопролиферативной реакции против структурных антигенов HCV (Фиг.3B) показала значительно лучшую реакцию против капсида в группе животных, иммунизированных pIDKE2-core в 2 дозах, по сравнению с остальными группами. Эти результаты показаны в виде индекса стимуляции клеток селезенки, полученных от иммунизированных животных. Индекс стимуляции определяли с помощью поглощения (H3) тимидина. Можно сделать вывод о том, что иммунизация смесью pIDKE2 и Капсидного белка вызывает синергическую стимуляцию иммунного ответа, индуцированного против структурных антигенов HCV.
Пример 2: Иммуногенность составов, содержащих в качестве компонентов ДНК, экспрессирующую полипротеин Капсид-E1-E2 HCV, и белковый антиген капсида HBV
С целью исследования поведения иммунной реакции, вызванной смесью плазмиды pIDKE2 с белковыми антигенами других патогенов, группы по 10 самок мышей BALB/c в возрасте 8 недель вакцинировали внутримышечно смесью вышеуказанной плазмиды с рекомбинантными частицами капсида HBV (HBcAg, Фиг.2C). Схема включала в себя 2 вакцинации в дни 0 и 21. Образцы крови брали на 9 и 19 неделях после первой иммунизации. Иммуногены готовили в фосфатно-солевом буферном растворе (PBS). Плазмиды вводили в дозе 50 мкг и капсидный белок HBV в дозе 5 мкг. Группу 1 вакцинировали плазмидой pAEC-K6 (отрицательный контроль). Группе 2 вводили белок HBcAg. Группу 3 вакцинировали pIDKE2. Группы 4 и 5 вакцинировали смесью HBcAg с плазмидами pIDKE2 и pAEC-K6, соответственно. Для статистического анализа использовали критерий Стьюдента, достоверное различие принимали при p < 0,05.
Фиг.4 показывает антительный ответ, индуцированный у мышей на 19 неделе после первой иммунизиции. Фиг.4A показывает, что смесь плазмиды pIDKE2 с HBcAg индуцировала титры антител к HBcAg, статистически более высокие, чем наблюдалось у других вакцинированных животных. Не было установлено статистически достоверных различий между группами, иммунизированными одним HBcAg или смесью с pAEC-K6. Следовательно, можно сделать вывод о том, что плазмида pIDKE2 усиливает иммунную реакцию против HBcAg.
С другой стороны Фиг.4B показывает, что смесь плазмиды pIDKE2 с HBcAg индуцирует титры антител к структурным антигенам HCV выше титров, образующихся у животных, иммунизированных одной pIDKE2. Следовательно, HBcAg также обладает способностью усиливать иммунный ответ, индуцированный против структурных антигенов HCV, вызванный после введения pIDKE2.
Пример 3: Иммуногенность составов, содержащих в качестве компонентов плазмиды, экспрессирующие варианты HCV и HBV, вариант белка поверхностного антигена HBV
С целью демонстрации усиления иммунного ответа, вызванного против других белковых антигенов, наблюдаемого после совместного введения с плазмидой pIDKE2, и для изучения других плазмид со сходными адъювантными свойствами, группы по 10 самок мышей BALB/c в возрасте 8 недель внутримышечно вакцинировали смесью плазмиды с рекомбинантными частицами HBsAg (Фиг.2B). Схема включала в себя 3 вакцинации в дни 0, 21 и 50. Образцы крови брали на 16 неделе после первой иммунизации. Все иммуногены готовили в фосфатно-солевом буферном растворе (PBS), за исключением группы, составленной с гидроксидом алюминия. Группу 1 вакцинировали смесью 50 мкг плазмиды pIDKCo, содержащей последовательность, кодирующую первые 176 аминокислот капсидного белка HCV (Duecas-Carrera et al., Vaccine 2000;19(7):992-997), и 5 мкг HBsAg (pIDKCo-HBsAg). Группы со 2 по 7 вакцинировали смесями ДНК и HBsAg в тех же количествах, но с использованием следующих плазмид: группа 2 (pIDKE1S-HBsAg), плазмида pIDKE1S (Фиг.1, содержащая последовательность, кодирующую аминокислоты 176-363 полипротеина HCV, Sec. Id. No.2); группа 3 (pAEC-ME-HBsAg), плазмида pAEC-ME (Фиг.1, содержащая последовательность, кодирующую белок, включающий в себя различные эпитопы антигенов HCV, Sec. Id. No.4); группа 4 (pIDKE2-HBsAg), плазмида pIDKE2 (Фиг.1), содержащая последовательность, кодирующую аминокислоты 1-650 полипротеина HCV, Sec. Id. No.3; группа 5 (pIDKE1Sm-HBsAg), плазмида pIDKE1Sm, идентичная плазмиде pIDKE1S за исключением того, что содержит 2 нуклеотидные вставки в области, кодирующей E1 HCV, что изменяет открытую рамку считывания и препятствует экспрессии данного белка (Sec. Id. No.5); группа 6 (pAEC-d2-HBsAg-HBsAg), плазмида pAEC-d2-HBsAg содержит последовательность, кодирующую HBV HBsAg (Musacchio et al., Biochem Bioph Res Commun 2001, 282, 442-446); группа 7 (pAEC-K6-HBsAg), плазмида pAEC-K6 (отрицательный контроль, не содержит кодирующей последовательности под контролем единицы транскрипции). Наконец, группы 8 и 9 вакцинировали 5 мкг HbsAg, приготовленного в гидроксиде алюминия или в чистом виде, соответственно. Для статистического анализа результатов использовали критерий Стьюдента, достоверное различие принимали при p < 0,05.
Фиг.5 показывает титры антител, вырабатываемые к HBsAg, 16 недель после первой иммунизации. Уровни антител, индуцированных только HBsAg в PBS, были статистически ниже уровней остальных апробированных вариантов кроме смеси, образованной HBsAg и pAEC-K6. С другой стороны, смеси HBsAg с плазмидами pIDKCo, pIDKE1S, pAEC-ME и pIDKE2 индуцировали титры антител к HBsAg статистически выше тех, которые вызывались иммунизацией HBsAg, приготовленного в гидроксиде алюминия или в смеси с pAEC-K6. Иммунизация HBsAg, приготовленным с гидроксидом алюминия или в смеси с pAEC-K6, pIDKE1Sm и pAEC-d2-HBsAg, индуцировала сходные уровни титров антител к HBsAg. Можно сделать вывод о том, что экспрессия в клетках-хозяевах вариантов белка, содержащих аминокислотные области Е1 антигена HCV, от введенных плазмид усиливает иммунный ответ, сформировавшийся против белковых антигенов в смеси с ДНК конструкцией.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННАЯ КОМПОЗИЦИЯ ПРОТИВ ВИРУСА ГЕПАТИТА С | 2005 |
|
RU2351363C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ТЕРАПЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2004 |
|
RU2362586C2 |
| ХИМЕРНЫЕ АНТИГЕНЫ ДЛЯ ВАКЦИНЫ ПРОТИВ ВИРУСА ГЕПАТИТА С | 2013 |
|
RU2639504C2 |
| РЕКОМБИНАНТНЫЕ ВЕКТОРЫ НА ОСНОВЕ "ЖИВОГО" ВИРУСА ОСПЫ ДОМАШНЕЙ ПТИЦЫ И ИХ ПРИМЕНЕНИЕ В ФАРМАЦЕВТИЧЕСКИХ КОМПОЗИЦИЯХ ПРОТИВ ВИРУСА ГЕПАТИТА С | 2005 |
|
RU2353651C2 |
| СРЕДСТВА И СПОСОБЫ ЛЕЧЕНИЯ ВИРУСА ГЕПАТИТА B | 2017 |
|
RU2740802C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕННЫХ АГРЕГАТОВ И ИХ ПРИМЕНЕНИЕ В ПРЕПАРАТАХ | 2001 |
|
RU2266754C2 |
| ПОЛИНУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ, КОДИРУЮЩАЯ СКОНСТРУИРОВАННЫЙ БЕЛОК ПЕРТАКТИН, ВЕКТОР, ВКЛЮЧАЮЩИЙ ТАКУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ, И ВАКЦИННЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ БЕЛОК ПЕРТАКТИНА ИЛИ ВЕКТОР | 2008 |
|
RU2499046C2 |
| РЕКОМБИНАНТНЫЙ МОДИФИЦИРОВАННЫЙ ВИРУС ВАКЦИНЫ АНКАРА, СПОСОБНЫЙ ЭКСПРЕССИРОВАТЬ СТРУКТУРНЫЕ АНТИГЕНЫ ВИРУСА ГЕПАТИТА С | 2002 |
|
RU2270860C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pUC8HBc-preS1, КОДИРУЮЩАЯ ГЕН БЕЛКА КОРОВОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В, ВКЛЮЧАЮЩИЙ ЭПИТОП pre-S1 РАЙОНА ПОВЕРХНОСТНОГО БЕЛКА ВИРУСА ГЕПАТИТА В (27-37 А.О.), И ШТАММ БАКТЕРИЙ Escherichia coli - ПРОДУЦЕНТ ГИБРИДНОГО БЕЛКА HBc-preS1 | 2005 |
|
RU2295570C2 |
| АГЕНТЫ И СПОСОБЫ, ОСНОВАННЫЕ НА ПРИМЕНЕНИИ ДОМЕНА EDA ФИБРОНЕКТИНА | 2006 |
|
RU2430738C2 |
Изобретение относится к области биотехнологии и медицины. Предложен вакцинный состав для лечения и профилактики инфекции вируса гепатита С и/или гепатита В. Состав содержит ДНК, которая экспрессирует вариант белка, содержащий области Е1 антигена вируса гепатита С, и капсидный белок вируса гепатита С или В. При этом, один из компонентов состава действует как адъювант другого. Изобретение может быть использовано в медицине. 1 н. и 6 з.п. ф-лы, 5 ил.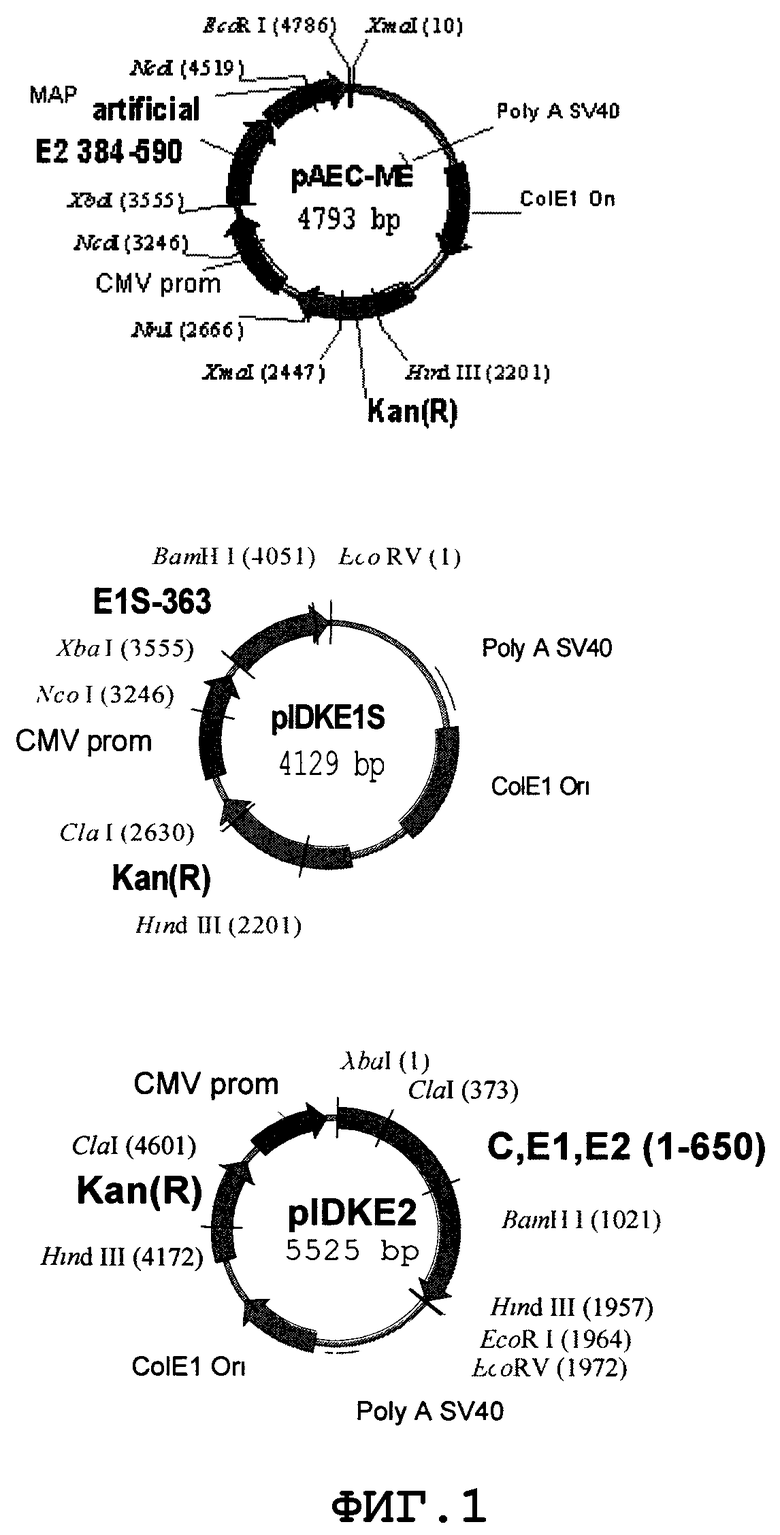
| ЕР 0913157, 06.05.1999 | |||
| Поршень | 1982 |
|
SU1043399A2 |
| WO 9825960, 18.06.1998. | |||
Авторы
Даты
2007-02-27—Публикация
2002-07-12—Подача