Изобретение относится к области органической химии - синтезу гетероциклических соединений - непредельных производных индола, представляющих интерес для получения новых аналогов противоопухолевых препаратов.
Изобретение относится к разработке способа получения 4-[1-(толил-4-сульфонил)-1Н-индолил-2]-бут-3-ен-2-онов общей формулы I, которые могут быть использованы в синтезе аналогов препаратов ряда эллиптицина, проявляющих противоопухолевую активность [Arasambattu К. Mohanakrisnan, Panayencheri С. Srinivasan. J.Org.Chem. 1995, 60, 1939-1946].

Ia R=ОСН3, R1=Ph; Iб R=ОСН3, R1=4-Br-Ph; Iв R=ОСН3, R1=СН3; Iг R=ОСН3, R1=4-СН3-Ph; Iд R=ОСН3, R1=С2Н5; Ie R=ОСН3, R1=Н; Iж R=-O-CH2-CH2-O-, R1=СН3.
В литературе описаны различные подходы к синтезу непредельных производных индолов, в которых исходные соединения уже содержат готовый индольный фрагмент. Так, при взаимодействии силилиндолов с Pd(OAc)2 и винилкетоном получают 2-(1-алкенил)индолы [Cacchi S; Marinelli F. Tetrahedron Lett., 1986, 27, 6397]. 3-Индолилпропеналь может быть синтезирован по реакции Вильсмеера-Хаака из (N,N-диметиламино)акролеина [Kathawala, F.G. World Pat., 1984, 02131]. Для синтеза непредельных производные индолов используют реакцию Виттига: при взаимодействии индолил-3-аля с 1-(трифенилфосфоранилиден)-2-пропаноном в ТГФ образуется к 1'-[1-(фенилсульфонил)-2-метилиндол-3-ил]бутен-3'-он [Arasambattu К. Mohanakrisnan, Panayencheri С. Srinivasan. J.Org.Chem. 1995, 60, 1939-1946].
Существенным недостатком всех описанных методов является необходимость применения исходных соединений, содержащих готовый индольный фрагмент, которые, зачастую, могут быть труднодоступными.
Известен синтез непредельного производного индола - 3-(5-метилфур-2-ил)-2-(3-оксобутен-1-ил)индола, в котором в качестве исходного соединения использовано производное бензилфурана - 2-нитрофенил-бис(5-метилфур-2-ил)метан [Butin A.V., Abaev V.T., Stroganova T.A., Gutnov V.T. Molecules, 1997, 2, 62-68]. Производное индола с выходом 57% было получено в результате восстановления бис(5-метилфур-2-ил)-2-нитрофенилметана хлористым оловом в присутствии HCl или (СН3)3SiCl.
Основным недостатком этого метода является невозможность использования в качестве исходных соединений производных бензилфурана, содержащих в бензольном кольце донорные заместители в пара-положении к нитрогруппе, и, как следствие, невозможность получения индолов с донорными группами в бензольном кольце индола.
Наиболее близким из известных способов получения функционализированных насыщенных кетонов индольного ряда на основе бензилфуранов является синтез 2-оксобутилиндолов из 2-N-тозиламинобензилфуранов [патент РФ №2176243. Способ получения производных индола // Бутин А.В., Строганова Т.А., Лодина И.В., Крапивин Г.Д.]. Производные индола, содержащие 3-оксобутильный фрагмент в положении 2 индольного цикла, были получены при кипячении 2-тозиламинобензилфуранов в насыщенном растворе газообразного хлороводорода в этаноле в течение 10 минут
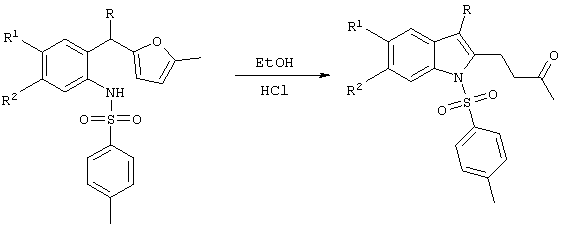
В основе этого метода лежит реакция раскрытия фуранового цикла и одновременное замыкание индольного ядра, протекающее под действие кислотных катализаторов.
Для синтеза непредельных индольных кетонов подобные условия ранее не использовались.
Нами предлагается принципиально новый метод получения непредельных производных индола, основанный на реакции раскрытия и рециклизации фуранового кольца 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фуранов, которые легко получаются при алкилировании N-тозилфурфуриламина соответствующими фенилметанолами.

Задача изобретения - разработка нового способа получения непредельных производных индола I с 3-оксобутенильным фрагментом в положении 2 индольного цикла, позволяющего варьировать заместители как в бензольном кольце, так и в положении 3 индольного фрагмента; снижение осмоления реакционной массы и увеличение выхода целевых продуктов.
Поставленная задача достигается тем, что способ получения 4-[1-(толил-4-сульфонил)-1Н-индолил-2]-бут-3-ен-2-онов (I), включающий образование непредельных производных индолов в результате рециклизации фуранового кольца промежуточно образующихся производных 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фурана, осуществляют при кипячении N-[2-(гидроксифенилметил)арил]-4-метилбензолсульфамидов и N-фуран-2-илметил-4-метилбензолсульфамида в уксусной кислоте с добавлением фосфорной кислоты в качестве катализатора в течение 11 часов. Соотношение фенилметанол : фосфорная кислота составляет 0,01 моль : 3 мл.
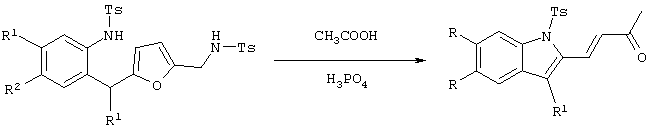
Полученный технический результат позволяет расширить ряд производных индолов.
Особенностью предлагаемого способа получения является последовательное протекание реакции алкилирования тозилфурфуриламина соответствующими бензгидролами и последующей рециклизации образующихся 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фуранов при кипячении в уксусной кислоте в присутствии фосфорной кислоты, что позволяет избежать выделения и очистки промежуточно образующихся 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фуранов.
Выбор 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фуранов в качестве исходных соединений позволяет в отличие от метода, описанного в патенте [патент РФ №2176243 Способ получения производных индола // Бутин А.В., Строганова Т.А., Лодина И.В., Крапивин Г.Д. //], провести реакцию по иному механизму, включающему отрыв тозиламида от образующихся 5-[о-(тозиламино)бензил]-2-(тозиламинометил)фуранов, перенос положительного заряда по системе сопряжения и последующую рециклизацию фуранового цикла. Полученные продукты реакции представляют собой непредельные производные индола - 4-[1-(толил-4-сульфорил)-1Н-индолил-2]-бут-3-ен-2-оны.
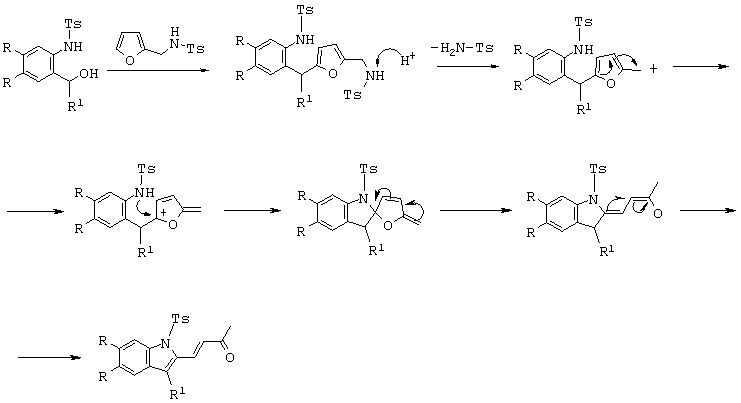
Использование системы ледяная уксусная кислота (растворитель)/фосфорная кислота (катализатор) позволяет гладко провести последовательность реакций алкилирования и рециклизации.
С целью сокращения длительности конверсии исходных веществ и рециклизации промежуточно образующегося бензилфурана, снижения степени осмоления фурановых субстратов и увеличения выхода целевых продуктов целесообразно проводить реакцию при кипячении до полной конверсии исходных веществ. Проведение реакции при кипячении в течение 11 часов (табл.1, п.4) позволяет наряду с уменьшением общей продолжительности процесса повысить выход конечного продукта за счет снижения осмоления реакционной массы.
Таким образом, совокупность существенных признаков, изложенных в формуле изобретения, позволяет достичь желаемого технического результата.
Индивидуальность и строение синтезированных соединений I подтверждены данными ПМР-спектроскопии и элементного анализа.
Примеры осуществления заявляемого способа получения 4-[1-(толил-4-сульфорил)-1Н-индолил-2]-бут-3-ен-2-онов I.
Пример 1.
4-[5,6-Диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-он
Смесь 4,13 г (0,01 моль) N-[2-(гидроксифенилметил)-4,5-диметоксифенил]-4-метилбензолсульфамида, 3,012 г (0,012 моль) N-фуран-2-илметил-4-метилбензолсульфамида, 30 мл уксусной кислоты и 3 мл фосфорной кислоты кипятят с обратным холодильником в течение 10 мин. Реакционную смесь выдерживают при комнатной температуре в течение 48 часов до полной конверсии исходных веществ (ТСХ контроль). Затем раствор выливают в 500 мл воды и нейтрализуют NaHCO3. Выпавший осадок отфильтровывают и очищают методом колоночной хроматографии (адсорбент силикагель (фракция 50/160), элюент ацетон-хлористый метилен-гексан 5:3:20)), получая 1,135 г (24%) соединения Ia (в расчете на исходный бензгидрол).
Тпл.=172-173°С.
Найдено для C27H25NO5S, %:
Вычислено: С 68.19; Н 5.30; N 2.95
ПМР спектр (200 MHz, CDCl3): 2.29 (3Н, s, СН3); 2.36 (3Н, s, СН3); 3.77 (3Н, s, ОСН3); 4.05 (3Н, s, ОСН3); 6.01 (1Н, ∂, J=16.5 Hz=CH); 6.62 (1Н, s, НInd); 7.17 (2H, ∂, J=8.2 Hz, HTs); 7.19-7.26 (2H, m, НPh); 7.40-7.47 (3Н, m, НPh); 7.55 (2H, ∂, J=8.2 Hz, НTs); 7.86 (1Н, s, HInd); 8.09 (1H, ∂, J=16.5 Hz=CH).
Пример 2.
4-[5,6-Диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-он
Смесь 4,13 г (0,01 моль) N-[2-(гидроксифенилметил)-4,5-диметоксифенил]-4-метилбензолсульфамида, 3,012 г (0,012 моль) N-фуран-2-илметил-4-метилбензолсульфамида, 30 мл уксусной кислоты и 3 мл фосфорной кислоты кипятят с обратным холодильником в течение 1 ч. Реакционную смесь выдерживают при комнатной температуре в течение 24 часов. Затем раствор выливают в 500 мл воды и нейтрализуют NaHCO3. Выпавший осадок отфильтровывают и очищают методом колоночной хроматографии (адсорбент силикагель (фракция 50/160), элюент ацетон-хлористый метилен-гексан 5:3:20)), получая 1,324 г (28%) соединения Ia (в расчете на исходный бензгидрол).
Пример 3.
4-[5,6-Диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-он
Смесь 4,13 г (0,01 моль) N-[2-(гидроксифенилметил)-4,5-диметоксифенил]-4-метилбензолсульфамида, 3,012 г (0,012 моль) N-фуран-2-илметил-4-метилбензолсульфамида, 30 мл уксусной кислоты и 3 мл фосфорной кислоты кипятят с обратным холодильником в течение 5 часов. Реакционную смесь выдерживают при комнатной температуре в течение 14 часов. Затем раствор выливают в 500 мл воды и нейтрализуют NaHCO3. Выпавший осадок отфильтровывают и очищают методом колоночной хроматографии (адсорбент силикагель (фракция 50/160), элюент ацетон-хлористый метилен-гексан 5:3:20)), получая 1,527 г (32%) соединения Ia (в расчете на исходный бензгидрол).
Пример 4.
4-[5,6-Диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-он
Смесь 4,13 г (0,01 моль) N-[2-(гидроксифенилметил)-4,5-диметоксифенил]-4-метилбензолсульфамида, 3,012 г (0,012 моль) N-фуран-2-илметил-4-метилбензолсульфамида, 30 мл уксусной кислоты и 3 мл фосфорной кислоты кипятят с обратным холодильником в течение 11 часов. Затем раствор выливают в 500 мл воды и нейтрализуют NaHCO3. Выпавший осадок отфильтровывают и очищают методом колоночной хроматографии (адсорбент силикагель (фракция 50/160), элюент ацетон-хлористый метилен-гексан 5:3:20)), получая 1,817 г (38%) соединения Ia (в расчете на исходный бензгидрол).
Пример 5.
4-[5,6-Диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-он
Смесь 4,13 г (0,01 моль) N-[2-(гидроксифенилметил)-4,5-диметоксифенил]-4-метилбензолсульфамида, 3,012 г (0,012 моль) N-фуран-2-илметил-4-метилбензолсульфамида, 30 мл уксусной кислоты и 3 мл фосфорной кислоты кипятят с обратным холодильником в течение 20 часов. Затем раствор выливают в 500 мл воды и нейтрализуют NaHCO3. Выпавший осадок отфильтровывают и очищают методом колоночной хроматографии (адсорбент силикагель (фракция 50/160), элюент ацетон-хлористый метилен-гексан 5:3:20)), получая 1,638 г (34,5%) соединения Ia (в расчете на исходный бензгидрол).
В таблице 1 приведены данные о влиянии продолжительности нагрева на выход 4-[5,6-диметокси-3-фенил-1-(толил-4-сульфонил)-1Н-индол-2-ил]-бут-3-ен-2-она (Ia) (примеры 1-5).
Как видно из таблицы 1, большие выходы целевого продукта достигаются при более длительном кипячении исходных веществ в уксусной кислоте в присутствии фосфорной кислоты. В то же время увеличение продолжительности кипячения более 11 часов нецелесообразно, поскольку при этом наблюдается снижение выхода в результате частичного осмоления реакционной смеси (табл.1, п.5).
Данные таблицы 1 свидетельствуют, что для получения 4-[1-(толил-4-сульфорил)-1Н-индолил-2]-бут-3-ен-2-онов (I) оптимальным является проведение реакции при кипячении реагентов в уксусной кислоте с добавлением фосфорной кислоты в качестве катализатора в течение 11 часов.
Заявляемым способом получен ряд 4-[1-(толил-4-сульфонил)-1Н-индолил-2]-бут-3-ен-2-онов (Iб-ж), выходы, температуры плавления и спектральные характеристики которых приведены в таблице 2.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-{1-[(4-МЕТИЛФЕНИЛ)СУЛЬФОНИЛ]-1Н-ИНДОЛ-2-ИЛ}БУТ-3-ЕН-2-ОНА | 2012 |
|
RU2488581C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ (Е)-4-(ИНДОЛ-2-ИЛ)ПРОП-2-ЕН-1-ОНА | 2016 |
|
RU2633999C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-(2-АЦИЛВИНИЛ)ИНДОЛОВ | 2014 |
|
RU2570421C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-(1Н-ИНДОЛ-3-ИЛ)-БУТ-3-ЕН-2-ОНА | 2009 |
|
RU2409564C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ N-АЦЕТИЛ-4-ГИДРОКСИ-2-МЕТИЛ-5-(5-МЕТИЛФУР-2-ИЛ)-1Н-БЕНЗО[g]ИНДОЛА | 2008 |
|
RU2368611C9 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 11Н-ИНДОЛО [2,3-c]ХИНОЛИНА | 2010 |
|
RU2439071C1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 4-АМИНОЦИКЛОГЕКСАНА | 2009 |
|
RU2501790C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АРИЛ(ГЕТАРИЛ)-1Н-ИНДОЛОВ | 2010 |
|
RU2439056C1 |
| 1,3-ДИЗАМЕЩЕННЫЕ 4-МЕТИЛ-1Н-ПИРРОЛ-2-КАРБОКСАМИДЫ И ИХ ПРИМЕНЕНИЕ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2007 |
|
RU2463294C2 |
| ПРОИЗВОДНЫЕ АЗАИНДОЛА-ИНДОЛА, СПОСОБЫ ИХ ИЗГОТОВЛЕНИЯ И ИСПОЛЬЗОВАНИЯ | 2008 |
|
RU2486184C2 |
Изобретение относится к способу получения новых соединений формулы I

где a R означает ОСН3, R1 означает Ph; б R означает ОСН3, R1 означает 4-Br-Ph; в R означает ОСН3, R1 означает СН3; г R означает ОСН3, R1 означает 4-СН3-Ph; д R означает ОСН3, R1 означает С2Н5; е R означает ОСН3, R1 означает Н; ж R означает -O-СН2-СН2-O-, R1 означает СН3; заключается в том, что бензгидрол формулы II

где R и R1 приведены выше, подвергают взаимодействию с N-фуран-2-ил-метил-4-метилбензолсульфонамидом формулы
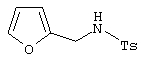
в уксусной кислоте при кипячении в течение 0,2-20 ч в присутствии фосфорной кислоты в качестве катализатора, где на 0,01 моль бензгидрола формулы II вводят 3 мл фосфорной кислоты. Соединения I могут быть использованы для получения новых аналогов противоопухолевых препаратов. 2 табл.
Способ получения 4-[1-(толил-4-сульфонил)-1Н-индолил-2]-бут-3-ен-2-онов общей формулы I

где a R означает ОСН3, R1 означает Ph; б R означает ОСН3, R1 означает 4-Br-Ph; в R означает ОСН3, R1 означает СН3; г R означает ОСН3, R1 означает 4-СН3-Ph; д R означает ОСН3, R1 означает C2H3; e R означает OCH3, R1 означает H; ж R означает -O-CH2-CH2-O-, R1 означает CH3,
заключающийся в том, что бензгидрол формулы II
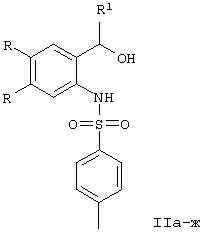
где R и R1 приведены выше,
подвергают взаимодействию с N-фуран-2-ил-метил-4-метилбензолсульфонамидом формулы
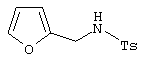
в уксусной кислоте при кипячении в течение 0,2-20 ч в присутствии фосфорной кислоты в качестве катализатора, где на 0,01 моль бензгидрола формулы II вводят 3 мл фосфорной кислоты.
| J.Org.Chem | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИНДОЛА | 2000 |
|
RU2176243C2 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
Авторы
Даты
2007-02-27—Публикация
2005-04-04—Подача