Область изобретения
Настоящее изобретение касается оксазиновых соединений. В частности, изобретение касается оксазиновых соединений и способов их производства, указанные соединения полезны в качестве фотохромных соединений.
Обоснование изобретения
Различные классы фотохромных соединений были синтезированы и предложены к применению в областях, где обратимые изменения цвета или затемнение вызываются действием солнечного света. Например, спирооксазин и соединения хромена известны как обладающие превосходной усталостной прочностью. Кроме того, известны фотохромные 2,2-дизамещенные соединения [2H-1,4]-нафтоксазина, такие как соединения, описанные в патенте США № 5801243. Такие соединения обладают большей усталостной прочностью, чем соединения хромена, но невыгодны по причине того, что способы их получения крайне ограничены. Таким образом, существует потребность в дополнительных фотохромных оксазиновых соединениях, позволяющих преодолеть недостатки известных соединений.
Описание изобретения и предпочтительные варианты выполнения
Настоящее изобретение касается оксазиновых соединений, имеющих ароматический заместитель в положении 2 оксазиновой группы, а также способов синтеза таких соединений.
По одному из вариантов выполнения настоящее изобретение касается соединения, включающего в себя как часть, состоящего по существу из соединения и состоящего полностью из соединения формулы I:
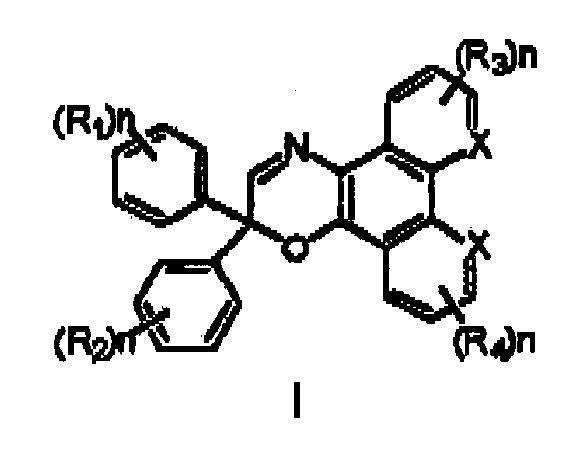
где X означает азот илиуглерод; R1, R2, R3 и R4 являются идентичными или различными и каждый независимо может означать водород, гидрокси, галоген, бензил, формил, трифторметил, нитро, циано, арил, арил(C1-С4)алкил, арилокси, цикло(C3-С6)алкил, (C1-18)алкокси, галоген(C1-С6)алкокси, (C1-С4)алкоксикарбонил или гетероциклический азотсодержащий заместитель с 5 или 6 атомами в цикле, такой как, не в порядке ограничения, пирролидино, пиперидино и морфолино; и n равно 1 или 2. Когда n равно 1, существует один заместитель в фенильной группе или пиридиновой группе и R1 и R2 могут находиться в орто-, мета- или пара- положении фенильного кольца.
В предпочтительном варианте выполнения X означает углерод или азот; каждый из R1, R2, R3 и R4 независимо означает водород, гидрокси, фтор, хлор, бром, бензил, формил, трифторметил, нитро, циано, арил, арил(C1-С4)алкил, арилокси, цикло(C3-С6)алкил, (C1-4)алкокси, (C1-С4)алкоксикарбонил или гетероциклический азотсодержащий заместитель с 5 или 6 атомами в цикле, такой как, не в порядке ограничения, пирролидино, пиперидино и морфолино; и n равно 1 или 2. Более предпочтительно, X означает углерод или азот, каждый из R1, R2, R3 и R4 означает водород, фтор, хлор, метил, метокси, этокси, метоксикарбонил, этоксикарбонил, пиперидино, морфолино или пирролидино; и n равно 1 или 2.
В более предпочтительном варианте выполнения изобретение касается соединения, которое означает 2,2-дифенилфенантро(9,10)-2H-[1,4]-оксазин, 2-(4-метоксифенил)-2-фенилфенантро(9,10)-2H-[1,4]-оксазин, 2-(4-фторфенил)-2-(4-метоксифенил)фенантро(9,10)-2H-[1,4]-оксазин или 2,2'-бис-(4-метоксифенил)фенантро(9,10)-2H-[1,4]-оксазин.
Соединение формулы I может быть получено по схемам реакций А-E. При всех взаимодействиях R1, R2 и "n" принимают вышеуказанные значения. Бензофеноны, представленные ниже формулой IV, выпускаются промышленно либо могут быть получены по реакции Фриделя-Крафтса с использованием бензоилхлорида формулы II и бензола формулы III. Реакция Фриделя-Крафтса описана в George A, Olah, "Friedel-Crafts and Related Reactions" (Vol.3, 1964).
Согласно схеме реакций A соединения формул II и III растворяют в дихлорметане и подвергают взаимодействию в присутствии кислоты Льюиса, включающей, но не в порядке ограничения, хлорид алюминия, с образованием соответствующего замещенного бензофенона.
Схема реакций A

Дизамещенная акриловая кислота, представленная формулой VI, может быть получена по альтернативным схемам реакций, представленным на схемах реакций B и C. По схеме реакций B бензофенон подвергают взаимодействию с ацетонитрилом в присутствии избыточного количества гидроксида натрия с образованием 2,2-дизамещенного акрилонитрила формулы V, указанный способ описан в J. Org. Chem., 44 (25), 4640-4649 (1979). Затем гидролизом гидроксидом натрия в этиленгликоле с последующим подкислением может быть получена дизамещенная акриловая кислота.
Альтернативно, по схеме реакций C, реакция Хорнера-Эммонса, описанная в Tetrahedron, 52 (31), 10455-10472 (1996), может быть осуществлена исходя из бензофенона. Полученный этиловый эфир 3,3-дизамещенной акриловой кислоты формулы VII может быть гидролизован с образованием дизамещенной акриловой кислоты, представленной формулой VI. R1, R2 и "n" принимают вышеуказанные значения.
Схема реакций B

Схема реакций С

Согласно схеме реакций D 3,3-дизамещенную акриловую кислоту обрабатывают тионилхлоридом, с последующим взаимодействием с азидом натрия, что приводит к образованию 3,3-дизамещенного бут-2-еноилазида формулы VIII. При нагревании в неполярном растворителе, включающем, но не в качестве ограничения, бензол или толуол, 3,3-дизамещенный бут-2-еноилазид перегруппировывается с образованием изоцианата формулы IX.
Схема реакций D

Решающая стадия синтеза фотохромных оксазинов формулы I представлена схемой реакций Е, где изоцианатное производное формулы IX подвергают взаимодействию с симметричным хиноном, включающим, но не в порядке ограничения, замещенный или незамещенный фенантрен-9,10-дион и замещенный или незамещенный 1,10-фенантролин-5,6-дион формулы X, в присутствии каталитического количества трифениларсеноксида в подходящем органическом растворителе в мягких условиях в течение времени, достаточного для завершения взаимодействия, обычно приблизительно от 2 до 10 часов. Органические растворители, которые могут быть использованы, включают, но не в порядке ограничения, бензол, диоксан, тетрагидрофуран ("ТГФ"), толуол и тому подобное, и их комбинации. Температуры реакции варьируются и обычно находятся в пределах приблизительно от 40°С до 120°С. В предпочтительном варианте выполнения используют растворитель, такой как бензол или толуол, и взаимодействие осуществляют приблизительно при 50-110°С в течение 1-15 ч. Более предпочтительно растворитель означает толуол или бензол и взаимодействие осуществляют приблизительно при 60-80°С в течение 2-4 ч.
Схема реакций Е

Альтернативно, фотохромные оксазиновые соединения по настоящему изобретению могут быть получены, как показано на схемах реакций F и G. R1, R2 и "n" принимают вышеуказанные значения. Согласно реакционной схеме F бензофенон формулы IV превращают в 1,1-дизамещенный эпоксид формулы XI обработкой иодидом триметилсульфоксония и трет-бутилатом калия в диметилсульфоксиде ("ДМСО"). Такое взаимодействие описано в Org. Chem., 62 (19), 6547-6561 (1997). Обработка замещенного эпоксида азидом натрия в N,N-диметиформамиде ("ДМФА") в присутствии хлорида лития приводит к образованию замещенного 2-азидо-1,1-дизамещенного этилена формулы XII.
Согласно методике, описанной в J. Org. Chem., 33 (6), 2411-2416 (1968), дегидратация 2-азидо-1,1-дизамещенного этилена при обработке тионилхлоридом в пиридине приводит к 2-азидо-1,1-дизамещенному этилену формулы XIII. Последующая реакция Штаудингера, осуществляемая обработкой 2-азидо-1,1-дизамещенного этилена трифенилфосфином, приводит к образованию илида, представленного формулой XIV.
Нагревание илида с симметричным хиноном формулы X в любом подходящем растворителе в течение достаточного для завершения взаимодействия времени дает требуемый оксазин формулы I. Используемым органическим растворителем может являться, но не в порядке ограничения, бензол, диоксан, тетрагидрофуран, толуол и тому подобное, и их комбинации. Температура реакции варьируется и обычно находится в пределах приблизительно от 60°С до 120°С, и время реакции составляет примерно от 2 до 24 ч. В предпочтительном варианте выполнения используемым растворителем является бензол или толуол, и взаимодействие осуществляют приблизительно при 70-100°С в течение 5-15 ч.
Схема реакций F
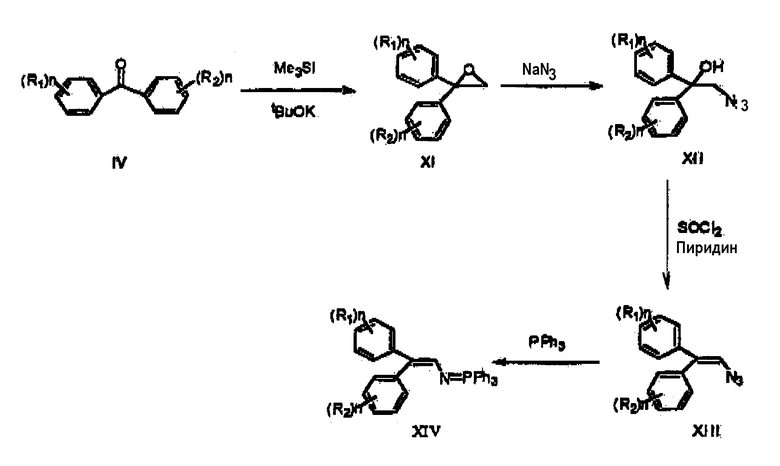
Схема реакций G

Оксазины по изобретению можно использовать в любых областях, где органические фотохромные вещества обычно находят применение, включая, но не в порядке ограничения, офтальмологические линзы, окна, остекление автомобиля, полимерные пленки и тому подобное. Оксазины по изобретению могут быть использованы в органическом растворителе или в органической полимерной основе. Органическим растворителем может быть любой подходящий растворитель, включающий, но не в порядке ограничения, бензол, толуол, метилэтилкетон, ацетон, этанол, метанол, тетрагидрофуран, диоксан, этилацетат, этиленгликоль, ксилол, циклогексан, N-метилпирролидон и тому подобное, и их комбинации. Полимерной основой может быть прозрачный полимер, такой как полиметакрилат, полистирол, поликарбонат и ацетат целлюлозы. Количество используемого оксазина подбирается таким, чтобы материал органической основы, на который фотохромное соединение наносят или в который соединения включают, имел требуемый результирующий цвет, например, по существу нейтральный цвет при активации под действием нефильтрованного солнечного света. Количество фотохрома, используемого в растворе или полимерной матрице, зависит от степени требуемого затемнения и обычно составляет приблизительно от 0,001 до 20 мас.% от массы основного полимера.
Далее изобретение поясняется путем рассмотрения следующих нелимитирующих примеров.
Пример 1
Стадия 1
В трехгорлую колбу объемом 100 мл загружают твердый KOH (3,30 г, 0,05 моль) и 25 мл ацетонитрила в атмосфере аргона, после чего содержимое нагревают до температуры кипения с обратным холодильником. Бензофенон (9,1 г, 0,05 моль) в 20 мл ацетонитрила добавляют при перемешивании. После 8 ч нагревания до температуры кипения с обратным холодильником горячий реакционный раствор выливают на 100 г колотого льда и экстрагируют дихлорметаном (3Ч15 мл). Объединенные органические экстракты промывают водой, сушат над безводным сульфатом натрия и фильтруют. Растворитель удаляют, остаток очищают флэш-хроматографией на силикагеле (смесь диэтиловый эфир-гексан 1:5 в качестве элюента), получают 7,9 г бесцветного масла (выход: 77%). 1H ЯМР свидетельствует о том, что продукт имеет структуру, отвечающую 3,3-дифенилакрилонитрилу. 1H ЯМР (CDCl3): δ 5,75 (с, 1Н), 7,27-7,50 (м, 10Н).
Стадия 2
3,3-Дифенилакрилонитрил (5,76 г, 2,81 ммоль), полученный на стадии 1, и гидроксид натрия (11,2 г, 280 ммоль) нагревают до температуры кипения с обратным холодильником в смеси из 180 мл этиленгликоля и 1 мл воды в течение 3 дней. Реакционную смесь охлаждают и разбавляют 100 мл воды, подкисляют 5M хлористоводородной кислотой до pH<1, фильтруют при разрежении и тщательно промывают водой. Твердые вещества в виде пасты растворяют в этилацетате и промывают разбавленной хлористоводородной кислотой. Органический слой отделяют и водный слой экстрагируют дважды этилацетатом. Объединенный этилацетатный раствор сушат над безводным сульфатом натрия и фильтруют. Растворитель удаляют в вакууме до достижения общего объема порядка 40 мл. Раствор фильтруют через короткую колонку с силикагелем и промывают этилацетатом. После удаления растворителя в вакууме остаток растирают с небольшим объемом смеси гексан-этилацетат (4:1), перекристаллизовывают из смеси этилацетат/гексан. Получают (выход: 84,8%) бесцветные кристаллы (5,34 г). 1H ЯМР свидетельствует о том, что продукт имеет структуру, отвечающую 3,3-дифенилакриловой кислоте.
1H ЯМР (CDCl3): δ 6,38 (с, 1Н), 7,24-7,35 (м, 1Н), 7,40-7,46 (м, 3Н).
Стадия 3
Суспензию акриловой кислоты (225 мг, 1 ммоль) в безводном бензоле (4 мл) нагревают до температуры кипения с обратным холодильником с избытком тионилхлорида (0,20 мл) в течение двух часов. Удаление растворителя и избыточного тионилхлорида при пониженном давлении дает требуемый хлорангидрид 3,3-ифенилакриловой кислоты. Ацилхлорид в безводном ТГФ (2,5 мл) охлаждают до 0°C и обрабатывают раствором азида натрия (130 мг, 2 ммоль) в воде (2 мл). Смесь перемешивают при 0°C в течение 2 ч, прежде чем добавить воду (10 мл). Смесь экстрагируют диэтиловым эфиром (2Ч10 мл) и сушат безводным сульфатом натрия.
Удаление растворителя при пониженном давлении дает желтое масло (200 мг), которое нагревают до 80°C в течение ночи вместе с 9,10-фенантренхинолином (146 мг, 0,7 ммоль) и трифениларсеноксидом (16 мг) в безводном толуоле (12 мл). После очистки хроматографией (силикагель, смесь дихлорметан-гексан 2:1 в качестве элюента) и перекристаллизации из смеси дихлорметан-гексан получают 203 мг требуемого фотохромного оксазина в виде белых (слегка бледно-желтых) кристаллов (выход: 52,7%).
Пример 2
Иодид триметилсульфоксония (1,12 Г, 5 ммоль) и трет-бутилат калия (0,59 г, 5 ммоль) перемешивают в ДМСО (10 мл) при комнатной температуре в течение 10 мин. Добавляют бензофенон (0,77 г, 4,2 ммоль) и смесь перемешивают при 40°C в течение 24 ч, после чего указанную смесь охлаждают, добавляют колотый лед и воду и экстрагируют диэтиловым эфиром (3Ч15 мл). Объединенные эфирные растворы промывают водой, сушат над безводным сульфатом магния и фильтруют. Растворитель удаляют и получают бледно-желтое масло, содержащее главным образом 1,1-ифенилоксиран, которое используют непосредственно на стадии 2 без очистки.
1H ЯМР (CDCl3): δ 3,29 (с, 2Н), 7,30-7,40 (м, 10Н).
Стадия 2
Масло, полученное на стадии 1, вместе с азидом натрия (0,36 г, 5,5 ммоль) и хлоридом лития (0,32 г, 7,5 ммоль) в ДМФА (20 мл) перемешивают при 80°C в атмосфере азота в течение 24 ч, охлаждают, добавляют воду (20 мл) и смесь экстрагируют диэтиловым эфиром (3Ч20 мл). Объединенные эфирные растворы промывают водой, сушат над безводным сульфатом магния и фильтруют. После удаления растворителя в вакууме остаток очищают хроматографией на силикагеле (смесь дихлорметан-гексан 1:2 в качестве элюента). Получают бесцветное масло (0,64 г). Инфракрасный спектр указывает на сильное поглощение при 2100 см-1.
1H ЯМР (CDCl3): δ 2,91 (с, 2H), 4,02 (с, 2H), 7,27-7,45 (м, 10Н).
13С ЯМР (CDCl3): δ 60,4, 78,2, 126,3, 127,8, 128,5, 143,8.
Стадия 3
2-Азидо-1,1-дифенилметанол, полученный на стадии 2 (160 мг, 0,67 ммоль), тионилхлорид (0,2 мл) и пиридин (2 мл) нагревают до температуры кипения с обратным холодильником в течение 2 ч. После охлаждения в реакционную смесь осторожно добавляют воду (10 мл) при охлаждении смесью лед-вода и экстрагируют диэтиловым эфиром (3Ч5 мл). Объединенные эфирные растворы промывают 4М хлористоводородной кислотой, водой и насыщенным раствором соли, сушат над безводным сульфатом магния и фильтруют. После удаления растворителя получают желтое масло (120 мг). Инфракрасный спектр указывает на сильное поглощение при 2097 см-1. 1H ЯМР свидетельствует о том, что полученный продукт является весьма чистым 2-азидо-1,1-дифенилэтиленом.
1H ЯМР (CDCl3): δ 6,69 (с, 1Н), 7,18-7,42 (м, 10Н).
Стадия 4
К 2-азидо-1,1-дифенилэтилену, полученному на стадии 3, в безводном толуоле (5 мл) добавляют трифенилфосфин (157 мг, 0,6 ммоль) при комнатной температуре в атмосфере азота. После перемешивания в течение 0,5 ч добавляют 9,10-фенантрен-9,10-дион (104 мг, 0,5 ммоль). Смесь нагревают до 80°С в течение ночи. Фотохромный продукт получают хроматографией на силикагеле (дихлорметан-гексан 1:1 в качестве элюента) и перекристаллизацией из смеси дихлорметан-гексан в виде бледно-желтых кристаллов (45 мг).
1H ЯМР (CDCl3): δ 7,24-7,29 (м, 6H), 7,46-7,70 (м, 8H), 8,12 (с, 1H), 8,43-8,52 (м, 1H), 8,53-8,62 (м, 3H).
13С ЯМР (CDCl3): δ 79,5, 122,5, 122,7, 122,8, 123,0, 125,1, 126,9, 126,9, 127,1, 127,3, 127,6, 128,4, 128,6, 129,8, 131,3, 128,0, 141,4, 155,7.
Пример 3
Стадия 1
К перемешиваемой суспензии гидрида натрия (95%, 0,507 г, 20 ммоль) в ТГФ (15 мл) добавляют 2-3 мл раствора триэтилфосфоноацетата (4,48 г, 20 ммоль) в ТГФ (20 мл). Для инициирования реакции добавляют каплю этанола, затем оставшуюся часть триэтилфосфоноацетатного раствора добавляют по каплям за 40 мин при охлаждении смесью лед-вода. После перемешивания в течение 15 мин реакционную смесь переносят в капельную воронку и добавляют по каплям к кипящему раствору 4-метоксибензофенона (4,38 г, 20 ммоль) в ТГФ (20 мл). После нагревания до температуры кипения с обратным холодильником в течение 24 ч большую часть растворителя удаляют. К охлажденному остатку добавляют насыщенный водный раствор хлорида натрия (20 мл) и экстрагируют дихлорметаном. Удаление дихлорметана дает бледно-желтое масло (5,42 г), содержащее главным образом этиловый эфир (E)- и (Z)-3-п-метоксифенил-3-фенилакриловой кислоты, как установлено 1H ЯМР, которое используют непосредственно на стадии 2 без дополнительной очистки.
Стадия 2
Масло, полученное на стадии 1, гидролизуют в растворе KOH (5,07 г, метанол (30 мл)) при нагревании до температуры кипения с обратным холодильником в течение 1 ч. Охлажденную реакционную смесь выливают в смесь лед-вода, подкисляют разбавленной хлористоводородной кислотой до рН<1 и экстрагируют этилацетатом (3Ч20 мл). Объединенный органический раствор сушат над безводным раствором сульфата натрия, растворитель удаляют, остаток перекристаллизовывают из смеси этилацетат/гексан и получают белый твердый продукт. Маточный раствор подвергают хроматографии и перекристаллизации. Всего получают 3,826 г требуемого продукта в виде белого твердого вещества и выделяют 0,677 г непрореагировавшего кетона (выход: 75,3%). 1H ЯМР свидетельствует о том, что выделенный продукт является смесью (E)- и (Z)-3-п-метоксифенил-3-фенилакриловой кислоты.
Стадия 3
Повторяют методику для стадии 3 примера 1 за тем исключением, что используют 3-п-метоксифенил-3-фенилакриловую кислоту (254,5 мг, 1 ммоль) вместо 3,3-дифенилакриловой кислоты для взаимодействия с 9,10-фенантренхиноном (44 мг, 0,21 ммоль) и трифениларсеноксидом (5 мг). Обработка дает 23,5 мг требуемого фотохромного оксазина в виде желтых кристаллов (выход: 5,66%).
1H ЯМР (CDCl3): δ 3,74 (с, 3H), 6,84 (д, 2H, J=8,7 Гц), 7,29-7,42 (м, 5H), 7,50-7,60 (м, 3Н), 7,61-7,66 (м, 3Н), 8,07 (с, 1Н), 8,42-8,62 (м, 4Н).
13С ЯМР (CDCl3): δ 55,2, 79,4, 114,0, 122,5, 122,7, 122,8, 122,8, 122,9, 125,1, 125,2, 126,8 126,9, 127,0, 127,5, 128,3, 128,6, 129,8, 131,2, 133,3, 138,0, 141,6, 155,9, 159,7.
Пример 4
Стадия 1
К смеси анизола (11,9 г, 0,11 моль) и п-фторбензоилхлорида (97%, 16,34 г, 0,1 моль) в дихлорметане (50 мл) добавляют хлорид алюминия (14,67 г, 0,11 моль), небольшими порциями, при перемешивании и охлаждении смесью лед-вода. После добавления реакционную смесь перемешивают при комнатной температуре в течение 1 часа, выливают в смесь из колотого льда (400 г) и хлористоводородной кислоты (20 мл) и перемешивают до исчезновения оранжевой окраски. Смесь экстрагируют дихлорметаном, сушат над сульфатом натрия, пропускают через короткую колонку с силикагелем и промывают дихлорметаном. Растворитель удаляют, остаток перекристаллизовывают из смеси дихлорметан-гексан, получают 21,96 г бесцветных кристаллов (выход: 95,4%). 1H ЯМР свидетельствует о том, что продукт имеет структуру, отвечающую п-фторфенил-п-метоксифенилкетону.
1H ЯМР (CDCl3): δ 3,89 (с, 3Н), 6,97 (д, 2H, J=8,7 Гц), 7,13 (дд, 2H, J=8,7 Гц), 7,76-7,84 (м, 4H).
Стадия 2
Повторяют методику для стадии 1 примера 1 за тем исключением, что используют п-фторфенил-п-метоксифенилкетон (4,60 г, 20 ммоль) вместо бензофенона, и время реакции равно 48 часам. Образующееся масло содержит в основном этиловый эфир (E)- и (Z)-3-п-метоксифенил-3-п-метоксифенилакриловой кислоты, который используют на стадии 3 без дополнительной очистки.
Стадия 3
Масло, полученное на стадии 2, гидролизуют в смеси KOH (5,2 г) и метанола (30 мл) в течение 80 минут и растворитель удаляют в вакууме. Добавляют воду (30 мл), смесь фильтруют при разрежении и промывают водой. Фильтрат экстрагируют диэтиловым эфиром (15 мл) и водный слой отделяют и подкисляют 4М хлористоводородной кислотой до рН<1. Твердый продукт отфильтровывают и перекристаллизовывают из смеси дихлорметан/гексан, получают 4,8 г белых кристаллов (выход: 88,1%). 1H ЯМР свидетельствует о том, что продукт имеет структуру, отвечающую смеси (E)- и (Z)-3-п-фторфенил-п-метоксифенилакриловой кислоты.
Стадия 4
Повторяют методику для стадии 3 примера 1 за тем исключением, что используют 3-п-фторфенил-п-метоксифенилакриловую кислоту (272,5 мг, 1 ммоль) вместо 3,3-ифенилакриловой кислоты для взаимодействия с 9,10-енантренхиноном (60 мг, 28,8 ммоль) и трифениларсеноксидом (5 мг). Обработка дает 75 мг требуемого фотохромного оксазина в виде желтых кристаллов (выход: 17,3%).
1H ЯМР (CDCl3): δ 3,74 (с, 3Н), 6,85 (м, 2Н), 7,04 (м, 2Н), 7,38 (м, 2H), 7,46-7,60 (м, 3Н), 7,62-7,70 (м, 3Н), 8,02 (с, 1Н), 8,43-8,47 (м, 1Н), 8,54-8,63 (м, 3Н).
13С ЯМР (CDCl3): δ 55,2, 79,0, 114,0, 115,3, 115,6, 115,6, 122,6, 122,7, 122,8, 125,0, 125,0, 125,1, 126,8, 127,3, 127,6, 128,4, 128,8, 128,9, 129,5, 131,1, 132,8, 137,2, 137,7, 155,4, 159,6, 164,1.
Пример 5
Стадия 1
К перемешиваемой суспензии гидрида натрия (0,48 г, 20 ммоль) в ТГФ (20 мл) добавляют по каплям раствор триэтилфосфоноацетата (4,48 г, 20 ммоль) в безводном ТГФ (25 мл) в атмосфере азота и при охлаждении на бане со смесью лед-вода. Спустя 40 мин раствор переносят в капельную воронку и добавляют по каплям к кипящему раствору бис(п-метоксифенил)кетона в безводном ТГФ (20 мл) за 20 мин. Реакционную смесь нагревают до температуры кипения с обратным холодильником в течение 48 ч и затем гидролизуют насыщенным раствором хлорида натрия (40 мл). Водную фазу экстрагируют диэтиловым эфиром (3Ч70 мл). Объединенные органические экстракты сушат, фильтруют и концентрируют, получая остаток, который очищают хроматографией, элюируя смесью метиленхлорид/гексан (1:2). Получают (выход: 67,8%) бесцветное масло (4,23 г). 1H ЯМР свидетельствует о том, что выделенный продукт имеет структуру, отвечающую этиловому эфиру 3,3-бис(п-метоксифенил)акриловой кислоты.
1H ЯМР (CDCl3): δ 1,16 (т, 3Н, J=7,1 Гц), 3,81 (с, 3Н), 3,84 (с, 3Н), 4,07 (кв, 2Н, J=7,1 Гц), 6,22 (с, 1Н), 6,84 (д, 2Н, J=9,1 Гц), 6,90 (д, 2Н, J=9,1 Гц), 7,15 (д, 2Н, J=9,1 Гц), 7,24 (д, 2Н, J=9,1 Гц).
Стадия 2
Этиловый эфир 3,3-бис(п-метоксифенил)акриловой кислоты (4,23 г, 13,5 ммоль), полученный на стадии 1, гидролизуют в 22 мл метанола в присутствии гидроксида калия (3,7 г, 66 ммоль) в течение 1 часа при нагревании до температуры кипения с обратным холодильником. Охлажденную реакционную смесь выливают в смесь лед-вода (50 мл), подкисляют разбавленной хлористоводородной кислотой до рН<1. Полученный твердый продукт фильтруют, промывают водой и перекристаллизовывают из смеси этилацетат/гексан. Получают (выход: 93,78%) белое твердое вещество (3,6 г). 1H ЯМР свидетельствует о том, что продукт имеет структуру, отвечающую 3,3-бис(п-метоксифенил)акриловой кислоте.
1H ЯМР (CDCl3): δ 3,82 (с, 3Н), 3,85 (с, 3Н), 6,22 (с, 1Н), 6,85 (д, 2Н, J=9,0 Гц), 6,91 (д, 2Н, J=8,7 Гц), 7,17 (д, 2Н, J=8,7 Гц), 7,24 (д, 2Н, J=8,7 Гц).
Стадия 3
Повторяют методику для стадии 3 примера 1 за тем исключением, что используют 3,3-бис(п-метоксифенил)акриловую кислоту (284,3 мг, 1 ммоль) вместо 3,3-дифенилакриловой кислоты для взаимодействия с 9,10-фенантренхиноном (43 мг, 0,2 ммоль) и трифениларсеноксидом (5 мг). Обработка дает 8 мг требуемого фотохромного оксазина в виде желтых кристаллов (выход: 1,8%).
1H ЯМР (CDCl3): δ 3,75 (с, 6Н), 6,85 (д, 2Н, J=8,7 Гц), 7,41 (д, 2Н, J=9,1 Гц), 7,52-7,60 (м, 1Н), 7,62-7,68 (м, 3Н), 8,03 (с, 1Н), 8,43-8,47 (м, 1Н), 8,54-8,63 (м, 3Н).
13С ЯМР (CDCl3): δ 55,2, 79,3, 113,0, 122,5, 122,7, 122,8, 122,9, 125,1, 126,8, 127,3, 127,5, 128,5, 129,8, 131,2, 133,5, 156,1, 159,7.
Пример 6
Оксазиновые соединения, полученные в примерах 1, 3, 4 и 5, растворяют в органическом растворителе, затем облучают УФ-светом при 365 нм в течение 15 с. Каждый из растворов приобретает интенсивное окрашивание и затем теряет окраску сразу после прекращения УФ-облучения. Максимальные поглощения в видимой области приведены ниже в таблице. Характерное поглощение имеет две полосы. Сильное поглощение около 450-490 нм зависит от структуры фотохрома и растворителя вместе с более слабым поглощением при длине волны, большей приблизительно на 100 нм.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФОТОХРОМНЫЕ ОКСАЗИНОВЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРОИЗВОДСТВА | 2002 |
|
RU2315042C2 |
| Замещенные 4-арил-гексагидро-7Н-имидазоло[1,5-b][1,2]оксазин-7-оны и способ их получения | 2018 |
|
RU2670097C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-5-ФТОР-3-ХЛОР-6-(ЗАМЕЩЕННЫХ)ПИКОЛИНАТОВ | 2013 |
|
RU2653855C2 |
| Способ получения (6R,7S,7aS)-6-((R)-1-(3,5-бис(трифторметил)фенил)этокси)-7-(4-фторфенил)гексагидро-3Н-пирролизин-3-она | 2022 |
|
RU2789599C1 |
| ПРОИЗВОДНЫЕ 2-ИМИНОПИРРОЛИДИНА | 2002 |
|
RU2270192C2 |
| НОВЫЕ АМИНОАЛКИЛБЕНЗОТИАЗЕПИНОВЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2679891C2 |
| СОЕДИНЕНИЯ С ГИДРОКСИКАРБОНИЛЬНЫМИ-ГАЛОГЕНАЛКИЛЬНЫМИ БОКОВЫМИ ЦЕПЯМИ | 2000 |
|
RU2247106C2 |
| СПОСОБ ПОЛУЧЕНИЯ НЕСИММЕТРИЧНЫХ 1,2-ДИТИЕНИЛЗАМЕЩЕННЫХ ЦИКЛОПЕНТЕНОВ | 2009 |
|
RU2421453C9 |
| НОВЫЕ 2',5'-ДИАРИЛСПИРО[ИНДОЛ-3,3'-ПИРРОЛИДИН]-2(1Н)-ОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2730287C1 |
| Способ получения замещенных 3-арилпирролов | 2024 |
|
RU2831117C1 |
Изобретение относится к химии фотохромных соединений, в частности, к способу получения оксазиновых фотохромных соединений. Описываются два варианта способа получения фотохромного соединения, один из которых заключается во взаимодействии изоцианатного производного формулы IX с симметричным хиноном таким, как замещенным или не замещенным 9,10-фенантрен-9,10-дионом или 9,10-1,10-фенантролин-5,6-дионом при нагревании, предпочтительно, при 40°-120°С в течение 2-24 ч в присутствии каталитического количества трифениларсеноксида. Другой способ заключается во взаимодействии азаилидного соединения формулы XIV с указанным симметричным хиноном при нагревании, предпочтительно, при 60°-120°С в течение 4-24 ч. Предложенные способы обеспечивают получение эффективных фотохромных соединений по упрощенной технологии. 2 н. и 4 з.п. ф-лы.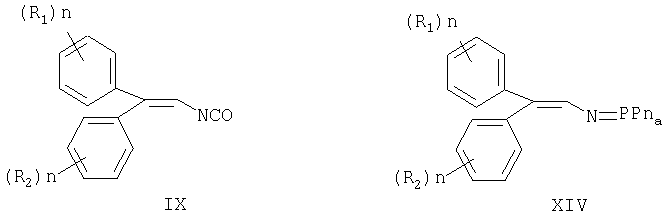

включающий стадию нагревания изоцианатного производного формулы

с симметричным хиноном формулы

где в каждой формуле Х означает азот или углерод; каждый из R1, R2, R3 и R4 независимо означает водород, гидрокси, галоген, бензил, формил, трифторметил, нитро, циано, арил, арил(С1-С4)алкил, арилокси, цикло(С3-С6)алкил, (C1-C18)алкокси, галоген(С1-С6)алкокси, (С1-С4)алкоксикарбонил или гетероциклический азотсодержащий заместитель с 5 или 6 атомами в цикле и n равно 1 или 2,
и где нагревание осуществляют в присутствии каталитического количества трифениларсеноксида.

включающий нагревание азаилидного соединения формулы XIV

с симметричным хиноном формулы

где в каждой формуле Х означает азот или углерод; каждый из R1, R2, R3 и R4 независимо означает водород, гидрокси, галоген, бензил, формил, трифторметил, нитро, циано, арил, арил(С1-С4)алкил, арилокси, цикло(С3-С6)алкил, (C1-C18)алкокси, галоген(С1-С6)алкокси, (С1-С4)алкоксикарбонил или гетероциклический азотсодержащий заместитель с 5 или 6 атомами в цикле и n равно 1 или 2.
| СОСУД ВЫСОКОГО ДАВЛЕНИЯ (ВАРИАНТЫ) | 2007 |
|
RU2338955C1 |
| 0 |
|
SU156372A1 | |
| 0 |
|
SU153690A1 | |
| RU 94032148 A1, 10.07.1996 | |||
| БЕНЗОКСАЗИНОВЫЕ ИЛИ ПИРИДООКСАЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, СПОСОБЫ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 1996 |
|
RU2191179C2 |
| Способ получения 2-дибутиламино-6-арил-1,3-оксазин-4-онов | 1981 |
|
SU950721A1 |
Авторы
Даты
2007-03-20—Публикация
2002-11-07—Подача