Настоящее изобретение относится к сложным эфирам целлобиозы, к содержащим их композициям и к их применению в качестве структурообразователей.
Многие композиции, предназначенные для топического нанесения на кожу, включая ряд композиций для различных частей тела, таких как лицо, десны, руки, конечности, ступни, торс, подмышки, грудь, гениталии, волосы и другие части тела, включают одно или несколько активных веществ, которые распределены в жидкости-носителе или иным образом поддерживаются ею. Хотя возможно, что во многих случаях такие композиции находятся в форме лосьонов, часто желательно, чтобы активный ингредиент таких композиций, будь то для медицинских или для косметических целей, оставался в основном локализованным в той области тела, на которую он был топически нанесен. Для этого, а также чтобы сделать возможным применение альтернативных раздаточных устройств для композиции, жидкость-носитель может быть загущена или структурирована путем, например, ввода для этой целей одного или нескольких веществ. Загущенные или структурированные композиции обычно принимают форму твердых косметических карандашей или мягких твердых веществ и кремов. В таких обстоятельствах материалы часто называют структурообразователями или гелеобразователями и могут иногда альтернативно называть загустителями, в зависимости от конечной формы композиции. Жидкий носитель может включать воду и/или смешивающуюся с водой органическую жидкость и, альтернативно, или дополнительно, не смешивающуюся с водой жидкость.
В принципе, выбор структурообразователей или загустителей имеет тенденцию варьироваться в соответствии с физической природой жидкости-носителя и в особенности от того, является ли она смешивающейся или не смешивающейся с водой. Настоящее изобретение относится в особенности к материалам, которые способны структурировать не смешивающуюся с водой жидкость, которая способна действовать сама по себе как носитель для активных ингредиентов или включает не смешивающуюся с водой жидкость в эмульсии или микроэмульсии.
Многие материалы были предложены для структурирования или загущения не смешивающейся с водой жидкой фазы композиций, предназначенных для топического нанесения человеку. Они включали воски, природные воски, такие как парафиновые воски или воски, обычно экстрагируемые из растений, такие как канделильский воск, или глицеридные воски, или полученные химической переработкой натуральных масел, например, гидрировании касторового масла, или полученные экстракцией из животного сырья, такие как пчелиный воск или спермацетовый воск, или их производные или синтетические варианты. Другие включают линейные спирты, например линейные спирты С18 или С20. Другие материалы являются полимерными, такими как полисилоксановые спирты, или полисилоксановые эластомеры или различные сополимеры полиамид/полисилоксан.
В последние годы 20-го века был найден ряд структурообразователей, которые авторы настоящего изобретения классифицируют как волокнообразующие. Они включают 12-гидроксистеариновую кислоту, различные амиды аминокислот, включающие, в частности, стеролы и сложные эфиры стеролов, включая, в частности, β-ситостерол и γ-оризонол, производные треитола, диамидные производные циклогексана и ацилированные производные целлобиозы. Каждый из различных структурообразователей имеет в большей или меньшей степени свои конкретные достоинства и свои характерные недостатки либо в абсолютных, либо в относительных величинах. Такие свойства могут включать способность вещества гелировать или иным образом структурировать жидкость-носитель, включая получаемые твердость, и стабильность, и сенсорные свойства, и внешний вид получаемой композиции, причем последнее очень важно для косметических композиций.
Один из наиболее предпочтительных классов структурообразователей включает ацилированную целлобиозу, как описано в находившейся на рассмотрении заявке РСТ № PCT/GB 00/01228, ныне опубликованной как WO 00/61079, в частности для структурирования не смешивающейся с водой жидкости в косметических композициях, включающих, в особенности, антиперспираторные и дезодорирующие композиции. Указанная заявка РСТ описывает различные преимущества структурообразователя из ацилированной целлобиозы и приводит примеры многих композиций, демонстрирующих такие преимущества. В указанной заявке РСТ указано, что целлобиоза может принимать или α- или β-конфигурацию, предпочтительно первую, и приведены различные предпочтительные варианты и для ряда ацильных заместителей ядра целлобиозы, и для химических составляющих заместителей. Описание альтернатив включало выбор алифатического ацильного заместителя, будь он линейным или разветвленным, и длину его цепи. Были приведены примеры ацилированных целлобиоз, в которых применялись идентичные ацильные заместители. Наиболее предпочтительной ацилированной целлобиозой, описанной здесь, является октанонаноат целлобиозы.
Продолжающиеся исследования свойств ацилированных целлобиозных материалов и композиций, структурированных с их использованием, показали, что вариации структурообразователей могут привести к изменениям различных свойств структурированных композиций, включая среди прочего термическую стабильность конечного структурированного материала, резистентность структурообразователя кристаллизации in situ, и прозрачность, и твердость композиции.
Было показано, что октанонаноат α-целлобиозы является весьма хорошим структурообразователем для не смешивающихся с водой жидкостей, включая силиконовые жидкости и не смешивающиеся с водой жидкие смягчающие вещества, применяемые во многих косметических композициях. Однако последние исследования ацилированных целлобиозных структурообразователей показали, что их термическая стабильность может быть улучшена и что длительное хранение может приводить к постепенному понижению прозрачности. Это должно быть ясно из исследований, связанных с кристаллизацией структурообразователя. Любой эффект приносит самоочевидные недостатки. Потеря структурной прочности во времени ограничивает время хранения продукта, а уменьшение визуальной прозрачности может быть воспринято покупателем как видимый сигнал того, что эффективность ухудшилась. Может потребоваться длительное время для того, чтобы продажные формы прошли по обычным каналам производства и дистрибьюции, и эти формы могут провести долгое время на полке покупателя до или во время применения, так что желательно найти пути улучшения или устранения любых отрицательных эффектов, которые могут так или иначе возникнуть во время хранения.
Следует, конечно, понимать, что при любых сделанных изменениях следует стремиться не принести в жертву какое-либо из других благоприятных свойств продуктов.
Однако многие композиции желательно являются пропускающими свет или прозрачными, и заданная твердость композиции остается важной характеристикой. Соответственно, при любом изменении, сделанном в рецептуре или сделанном альтернативном выборе из класса ацилированных целлобиозных материалов, следует стремиться минимизировать или даже преодолеть и обернуть вспять любые ухудшения других свойств структурообразователя, которые могут возникнуть при попытке улучшить одно из свойств. В качестве примера, при улучшении стабильности в отношении кристаллизации in situ может уменьшиться твердость. Могут быть рассмотрены смеси материалов, и тогда наблюдается некоторое изменение в поведении смеси структурообразователей по сравнению с их составляющими.
Задачей настоящего изобретения является создание ацилированной целлобиозы, которая демонстрирует привлекательное сочетание свойств, в особенности в качестве структурообразователя для не смешивающейся с водой жидкости.
Следует, однако, понимать, что, хотя материал по настоящему изобретению рассматривается, в частности, для применения в косметических композициях, его потенциальное использование намного шире, включая структурирование не смешивающейся с водой жидкости для приготовления крема, мягкого твердого вещества или карандаша для любых других целей. Они могут включать топические медикаменты, топически наносимые ветеринарные продукты или косметические средства для животных и воски или полировочные средства.
Настоящее изобретение относится к новому соединению, ацилированной целлобиозе, соответствующей общей формуле:
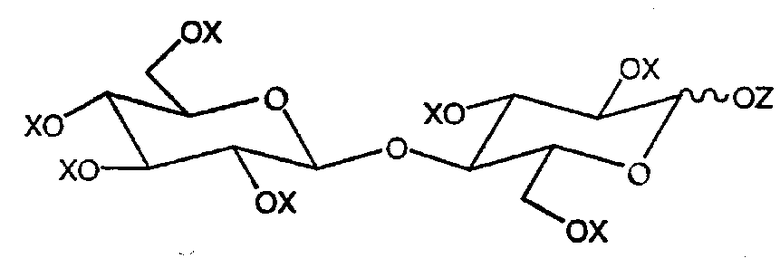
в которой X представляет ацильную группу (R-CO-) или H, Z представляет ацильную группу (R'-CO-) или H, и не более чем меньшая часть радикалов X + Z представляет H;
R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода, и
R' представляет радикал, отличный от R, который представляет собой:
(i) углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 1 до 31 атомов углерода, необязательно замещенный, или
(ii) ароматический углеводородный радикал, необязательно замещенный, или
(iii) циклоалифатический углеводород, необязательно замещенный.
Заместитель Z находится в аномерном положении.
Такой сложный эфир, в котором R отличается от R', иногда обозначают здесь как CHME.
Такие материалы, т.е. СНМЕ, проявляют превосходное сочетание свойств, делающее эти материалы особо пригодными для структурирования или загущения не смешивающихся с водой жидкостей, делая возможным их применение при производстве базовых гелей для косметических или медицинских активных веществ и, в частности, для прозрачных базовых гелей. Преимущества могут быть увеличены выбором замещения R' по аномерному углероду, которое отличается от замещения других алкильных групп R.
При сравнении, например, с применением различных целлобиозных октаэфиров, можно благоприятно видеть улучшение одного или нескольких из следующих свойств, а именно прозрачности, термической стабильности и устойчивости к кристаллизации in situ, в то же время без ухудшения твердости.
Согласно второму аспекту настоящего изобретения предложен способ получения ацилированной целлобиозы, описанной здесь выше, включающий стадию реакции ацилированной целлобиозы, имеющей общую формулу 2:
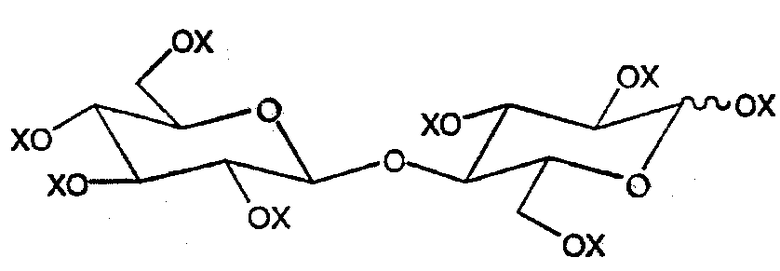
в которой X представляет ацильную группу (R-CO-) или H, причем Н представляет не более чем меньшую часть радикалов X, и R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода, с ацилирующим агентом, содержащим радикал R', как он описан здесь выше, предпочтительно по аномерному углероду целлобиозы.
Согласно настоящему способу проводят ацилирование гидроксильной группы аномерного атома углерода либо проводят переэтерифицию ацильной группы R-CO- у аномерного атома углерода.
Настоящее изобретение относится также к применению ацилированной целлобиозы, как она описана здесь выше, для загущения или структурирования не смешивающейся с водой жидкости с образованием в результате крема, мягкого твердого вещества или твердого вещества.
Настоящее изобретение, кроме того, относится к базовой композиции в форме крема, мягкого твердого вещества или твердого вещества, содержащей в качестве структурирующего агента или загустителя ацилированную целлобиозу, определенную выше.
Согласно настоящему изобретению базовая композиция дополнительно содержит активный косметический, медицинский или ветеринарный агент.
Подробное описание изобретения и предпочтительных осуществлений
Ацилированные соединения целлобиозы соответствуют формуле, показанной ниже:
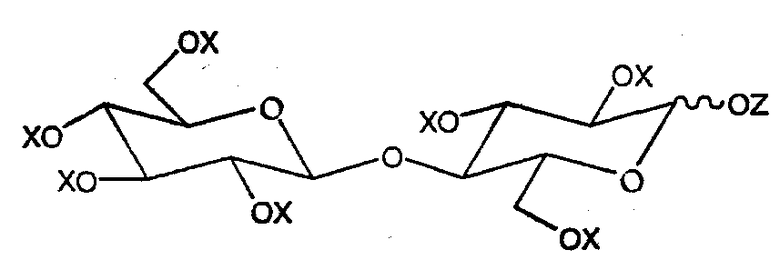
Когда X и Z представляют в данной формуле соответственно -COR и -COR', R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, который содержит от 5 до 31 атомов углерода, часто до 18 атомов углерода, предпочтительно от 7 до 12 атомов углерода и особо предпочтительно 8 или 9 атомов углерода. Предпочтительно радикалы R являются насыщенными и желательно линейными. Наиболее желательно, все группы R являются одинаковыми. Следует понимать, что на практике алкильный заместитель с заданной длиной цепи в ацилирующем агенте может содержать на уровне примеси изомеры и близкие гомологи. Например, если R номинально представляет октил, заместитель может включать в качестве примесей небольшие количества, обычно не более 5%, изооктильных и н-гептильных/н-нонильных групп.
В данной формуле R' представляет алифатический, ароматический или циклоалифатический радикал. R' может быть алкилом, алкарилом, арилом или аралкилом, необязательно замещенным. Предпочтительно, когда R' является неалифатическим, если R является алифатическим.
Радикал R', если он алифатический, может включать насыщенный или ненасыщенный углеводородный радикал с линейной или разветвленной цепью, содержащий от 1 до 31 атомов углерода, более желательно линейный и предпочтительно с числом атомов углерода от 2 до 22. Радикалы R и R' отличаются друг от друга, так что R' часто выбирают из радикалов, имеющих максимальную длину цепи в интервале до R-2 атомов углерода или от R+2 атомов углерода и обычно в интервалах от 1 до 6 и от 13 до 22 атомов углерода. Особенно предпочтительные алкильные радикалы R' включают метил, этил и пропил. Алкильные группы внутри R' могут быть, необязательно, фторированы или замещены арильной группой, такой, как будет определено здесь далее, или циклоалифатической группой, такой, как будут описаны здесь далее, или аминной, или амидной группой. Замещенный алифатический радикал R' желательно содержит не более 31 и предпочтительно не более 22 атомов углерода.
Если R' представляет или содержит ароматический радикал, в частности арильный радикал, подходящие примеры включают фенильный, нафтильный и бифенильный радикалы. Арильная группа может включать 1 или множество ядер, которые могут быть конденсированными или неконденсированными. Арильное кольцо или кольца в ней могут быть замещенными, например, алкильной или алкокси группой, содержащей до 20 атомов углерода, или галогенной группой, такой как фторгруппой, или нитрогруппой, или группой алкильного сложного эфира, алкиламина или алкиламида. Замещенный алкильный радикал R' желательно содержит не более 26 атомов углерода.
Если R' представляет циклоалифатический углеводородный радикал, подходящие примеры включают циклогексан и циклооктан. Циклоалифатическое кольцо может быть замещено, например, алкильной или алкоксигруппой, содержащей до 20 атомов углерода, или арильной группой, такой, как описана выше.
R' может включать алкильный, арильный, циклоалкильный, алкарильный, аралкильный или циклоалкиларильный радикал.
Ацилированные целлобиозные материалы согласно настоящему изобретению могут представлять или α-, или β-аномерные формы или их смеси. В ряде особо предпочтительных осуществлений, например, в тех, в которых R' является насыщенным углеводородным радикалом, таким как циклогексил или линейный алкил С4-С10, который отличается от радикала R, CHME является, по меньшей мере, на 60 мол.% в β-аномерной форме, предпочтительно, по меньшей мере, на 80 мол.%, и особо предпочтительно, по меньшей мере, на 90 мол.% СНМЕ находится в β-аномерной форме. В других предпочтительных осуществлениях, например, в тех, в которых R' включает ненасыщенный углеводородный радикал, такой как бензоил или 4-бифеноил, предпочтительно, по меньшей мере, 90 мол.% CHME находится в β-аномерной форме.
Предпочтительно ацилированная целлобиоза ацилирована суммарно более чем шестью и во многих случаях более чем семью ацильными заместителями R-CO- + R'-CO-, в среднем, и предпочтительно составляющими, по меньшей мере, 95 мол.% от общего ацилирования. На практике было найдено, что ацилирование часто происходит преимущественно по атомам углерода целлобиозы, отличным от ее аномерного атома углерода, так что первые атомы углерода имеют склонность быть полностью ацилированными, обычно представляя R-CO-, по меньшей мере, в шести из семи местоположений X, и, во многих случаях, представляя R-CO- во всех или почти всех семи местоположениях Х, тогда как аномерный атом углерода может быть и обычно является ацилированным в меньшей пропорции.
Желательно, чтобы аномерный углерод был ацилирован, по меньшей мере, на 50%, предпочтительно, по меньшей мере, на 60%, более предпочтительно был ацилирован, по меньшей мере, на 75%, и наиболее желательно, в сочетании с Х, представляющим на 100% или почти на 100% R-CO- (обычно, по меньшей мере, в 6 из семи местоположений и предпочтительно более чем 97%). Особо желательно применять СНМЕ, в котором имеется не только высокая степень ацилирования по аномерному углероду, но также одновременно высокая мольная доля эфира находится в β-аномерной форме; каждый из данных характерных признаков был подробно описан здесь выше.
Особо подходящий подкласс СНМЕ включает сложные эфиры, в которых: i) каждый заместитель R представляет линейный октильный радикал; ii) аномерное положение ацилировано в высокой степени и предпочтительно, по меньшей мере, на 75 мол.%; и iii) большая часть и, по меньшей мере, 80 мол.% СНМЕ находится в β-аномерной форме.
Когда рассматривается применение сложных эфиров целлобиозы в общем и сложных эфиров по изобретению, в частности, для приготовления полупрозрачных гелей не смешивающихся с водой жидкостей, таких как силиконовые жидкости или другие упомянутые здесь не смешивающиеся с водой жидкости, желательно выбирать такие материалы, которые имеют относительно высокую температуру растворения волокон (ТРВ). Благоприятно то, что многие из эфиров по данному изобретению имеют ТРВ, по меньшей мере, 48°С, и особо предпочтительными эфирами являются эфиры, имеющие ТРВ, по меньшей мере, 51°С, поскольку они проявляют тенденцию давать гели, имеющие более высокую стабильность при хранении.
Ацилированные целлобиозы по настоящему изобретению могут быть использованы как единственные или первичные структурообразователи или могут быть использованы как не основной или дополнительный структурообразователь в сочетании с одним или несколькими из классов структурообразователей, которые упомянуты здесь далее. В качестве примера, структурообразователи по изобретению могут быть использованы вместе с ацилированной целлобиозой, описанной в PCT/GB 00/01228, в которой аномерная ацильная групп является такой же, как, по меньшей мере, некоторые из других ацильных групп, т.е. R=R', такой как октанонаноат целлобиозы или предпочтительно октадеканоат.
Особенно предпочтительно применять ацилированные целлобиозы, идентифицированные здесь (СНМЕ), в которых все заместители R являются одинаковыми и представляют н-нонил или предпочтительно н-октил, и, по меньшей мере, 75% заместителей у аномерного углерода представляют R' (т.е., по меньшей мере, 75 мол.% замещения в аномерном положении) и представляют циклогексил, фенил, нафтил или метил и предпочтительно циклогексил. Такие особенно желательные СНМЕ материалы предпочтительно, по меньшей мере, на 80 мол.% находятся в β-аномерной форме.
Приготовление материалов
Один удобный и общий способ получения ацилированных целлобиоз по настоящему изобретению включает стадию переэтерификации соответствующей ацилированной целлобиозы, в которой ацильные заместители -COR и -COR' являются одинаковыми. Такой процесс на практике может быть двухстадийным, первая стадия которого включает получение октаэтерифицированной целлобиозы, например, описанным здесь ниже способом. Вторая стадия такого процесса включает реакцию октаэфира с ацилирующим агентом, содержащим радикал -COR', способный, если необходимо, заместить радикал -COR в присутствии сильного ацилирующего катализатора. Полученный продукт часто включает часть остаточных радикалов R-CO- у аномерного атома углерода.
Аналогичный способ включает ацилирование соответствующей частично ацилированной целлобиозы ацилирующим агентом, содержащим радикал -COR', где требуется в присутствии ацилирующего катализатора, чтобы аномерный углерод был частично или предпочтительно полностью или почти полностью замещен гидроксильной группой. Такой субстрат может быть получен, например, полным или частичным деацилированием октаэфира целлобиозы. Соответственно, смешанные эфирные соединения целлобиозы по изобретению могут быть получены в трехстадийном процессе, включающем стадии: во-первых, получения октаэфира, у которого ацильный заместитель -COR' у аномерного углерода является таким же, как и у других углеродов целлобиозы, R-CO-; во-вторых, удаления аномерного ацильного заместителя; и затем переацилирования по аномерному положению отличным ацильным заместителем.
По одному способу осуществления первой стадии, будь то двух- или трехстадийный процесс, указанный выше, целлобиозу (обычно D-(+)-целлобиозу) вводят в реакцию с мольным избытком, часто со значительным избытком, ацилирующего агента, такого как хлорангидрид кислоты, RCOCl, карбоновая кислота RCO2H или ангидрид кислоты (RCO)2O, и, если необходимо, катализатором ацилирования. Группы R являются такими, как описаны здесь выше. Например, если в качестве ацилирующего агента используют кислоту, катализатор может быть предпочтительно полученным из кислоты, имеющей низкую pKа, таким как ангидрид (R"CO)2O, часто в значительном мольном избытке. Группа R" желательно является полихлорированным или предпочтительно, полифторированным алкилом, таким как трифторметил. Ацилирующий агент, например карбоновую кислоту, предпочтительно используют в мольном отношении к целлобиозе в интервале от, по меньшей мере, 50:1 и особо предпочтительно от 60:1 до 100:1. Катализатор предпочтительно используют с кислотой при мольном отношении к целлобиозе, по меньшей мере, 20:1 и предпочтительно от 22:1 до 50:1. Ацилирование желательно проводить при повышенной температуре, такой как выше 70°С и особо предпочтительно, около 100°С в течение, по меньшей мере, 2 часов и особо предпочтительно от 3 до 10 часов. Полученный продукт является преимущественно или полностью ацилированным, т.е. можно сказать, что было ацилировано, по меньшей мере, 90% и часто, по меньшей мере, 95% способных к ацилированию гидроксильных групп целлобиозы.
На первой стадии целлобиозу (обычно D-(+)-целлобиозу) вводят в реакцию с мольным избытком, часто со значительным избытком, ацилирующего агента, такого как хлорангидрид кислоты, RCOCl, в растворе летучего хлоруглеводорода, такого как хлороформ, в присутствии избытка сильного основного катализатора, такого как пиридин, и наиболее предпочтительно в сухой инертной атмосфере. Предпочтительно ацилирующийагент используют в мольном отношении к целлобиозе в интервале от 12:1 до 24:1, в 1,5-3 раза выше стехиометрического количества для октаацилирования. Основный катализатор обычно применяют в мольномсоотношении к целлобиозе от 6:1 до 12:1. Стадию ацилирования желательно проводить при умеренно повышенной температуре, такой как от 40 до 75°С, и часто от 45 до 60°С. Ход реакции хорошо контролировать методом ЖХВР и/или протонной ЯМР и дать ей продолжаться до тех пор, пока гептаацилированная целлобиоза не будет больше обнаруживаться. Такой период реакции часто находится в интервале от10 до 30 часов. Продукт ацилирования может быть извлечен охлаждениемдо комнатной температуры и осаждением в метаноле. Данный метод особенно применим для получения сложных эфиров преимущественно в β-аномерной форме.
На второй стадии вышеупомянутого трехстадийного процесса ацилированную целлобиозу, полученную на первой стадии, т.е. преимущественно α- или β-аномерную форму или их смесь, частично деацилируют предпочтительно по аномерному углероду. Способ включает реакцию полностью ацилированной целлобиозы со смесью алифатической кислоты низкого молекулярного веса (C1-C4) и предпочтительно уксусной кислоты с алкилендиамином, таким как предпочтительно этилендиамин, при низкой концентрации в ТГФ (тетрагидрофуране), такой как от 4 до 15% от массы ацилированной целлобиозы. Кислота, используемая на второй стадии, имеет более высокое значение pKa, чем катализатор на первой стадии. При реакции предпочтительно применяют примерно эквимольное отношение кислоты к ацилированной целлобиозе, такое как в интервале от 0,9 до 1,2:1, и небольшой мольный избыток диамина к ацилированной целлобиозе, такой как от 1,6 до 2,5:1. Реакцию обычно можно проводить при комнатной температуре или близкой, например от 20° до 30°С, в течение продолжительного времени реакции, часто, по меньшей мере, 12 часов и предпочтительно от 24 до 60 часов, или при умеренно повышенной температуре, такой как до 45°С, в течение соответственно более короткого периода времени, такого, как выбранное в интервале от 5 до 10 часов. Полученное частично деацилированное вещество может быть извлечено экстракцией в галогеноалкановом растворителе, таком как дихлорметан, и промыто кислотой. После сушки его можно перекристаллизовать из смеси ТГФ/метанол. На третьей стадии частично ацилированную целлобиозу переацилируют. Переацилирование можно проводить, используя карбоновую кислоту, хлорангидрид кислоты или ангидрид кислоты.
По первому варианту третьей стадии целлобиоза реагирует с, по меньшей мере, эквимольным количеством хлорида кислоты формулы R'COCl, предпочтительно с небольшим мольным избытком от 1,1 до 1,5:1 в присутствии, по меньшей мере, эквимольного количества триэтиламина и предпочтительно с небольшим мольным избытком от 1,1 до 1,5:1. Реакцию желательно проводить при температуре кипения с обратным холодильником или в пределах 10°С от нее, предпочтительно в течение, по меньшей мере, 1 часа и предпочтительно от 2 до 4 часов. Желательно дать реакции продолжаться до тех пор, пока не будет достигнута, по меньшей мере, предварительно заданная степень ацилирования по аномерному углероду, такая как, по меньшей мере, 80% и часто, по меньшей мере, 90%. По данному первому варианту полученный СНМЕ находится преимущественно в β-аномерной форме, точное соотношение α- и β-форм зависит от ацилирующего заместителя и принятых условий процесса.
По второму варианту данной третьей стадии частично деацилированная целлобиоза реагирует со значительным избытком карбоновой кислоты формулы R'CO2H, таким как при мольном отношении, по меньшей мере, 50:1 и предпочтительно от 60 до 100:1 в присутствии значительного мольного избытка сильного кислотного катализатора, такого как катализатор, используемый на первой стадии, и предпочтительно при мольном отношении к целлобиозе, по меньшей мере, 20:1 и предпочтительно от 22:1 до 50:1. Реакцию предпочтительно ведут при повышенной температуре, такой как предпочтительно выше 90°С и более предпочтительно около 100°С. Время реакции составляет предпочтительно, по меньшей мере, 4 часа и более предпочтительно от 5 до 10 часов. Реакция желательно должна продолжаться до тех пор, пока не будет достигнута, по меньшей мере, предварительно заданная степень ацилирования по аномерному углероду, такая как, по меньшей мере, 80% и часто, по меньшей мере, 90%. По данному второму варианту полученный СНМЕ находится преимущественно в α-аномерной форме, точное соотношение α- и β-форм зависит от ацилирующего заместителя и принятых условий процесса.
По третьему варианту осуществления третьей стадии, частично деацилированная целлобиоза реагирует с ангидридом формулы (R'CO)2O. Реакцию обычно ведут в углеводородном растворителе, имеющем температуру кипения, по меньшей мере, 80°С, таком как толуол. При реакции обычно используют избыток ангидрида, предпочтительно при мольном отношении к целлобиозе, по меньшей мере, 2:1 и часто от 2,5 до 10:1.
Косметические композиции
Косметические композиции настоящего изобретения могут включать вспомогательные компоненты, в частности гелеобразователь. Количество гелеобразователя в косметических композициях согласно изобретению может быть выбрано в интервале от 0,1 до 20 мас.% и предпочтительно от 0,5 до 15 мас.% в комбинации с водонесмешиваемой жидкости.
Косметическая композиция может дополнительно содержать один или более активных агентов, выбранных из агентов для ухода за кожей, агентов личной гигиены, лекарственных средств, солнцезащитных средств или средств, способствующих загару, предпочтительный агент личной гигиены обладает антиперспирантной активностью.
Не смешивающаяся с водой жидкость
Не смешивающаяся с водой жидкость, которая во многих осуществлениях действует как носитель дисперсной твердой или жидкой фазы, обычно включает одно из веществ или смесь веществ, которые являются настолько гидрофобными, что не смешиваются с водой. В не смешивающуюся с водой жидкость могут быть включены некоторое количество гидрофильной жидкости в такой степени, чтобы она была растворимой или смешивающейся с не смешивающейся с водой жидкостью и давала общую смесь жидкости-носителя, которая была бы не смешивающейся с водой. Обычно желательно, чтобы такой носитель был жидким (в отсутствие структурообразователя) при температуре 15°С и выше. Она может иметь некоторую летучесть, но ее давление паров обычно должно быть ниже 4 кПа (30 мм рт.ст.) при 25°С так, чтобы вещество могло считаться маслом или смесью масел. Более конкретно, в некоторых осуществлениях желательно, чтобы, по меньшей мере, 80% мас.гидрофобного носителя состояло из веществ с давлением паров, не превышающим величину 4 кПа при 25°С.
Предпочтительно, например, для использования в косметических рецептурах, чтобы гидрофобное вещество-носитель включало летучий жидкий силикон, например жидкий полиорганосилоксан. Чтобы быть классифицированным как "летучий", такое вещество должно иметь измеримое давление пара при 20° или 25°С. Обычно давление паров летучего силикона лежит в интервале от 1 или 10 Па до 2 кПа при 25°С.
Летучий силикон желательно включать из-за того, что он придает "осушающее" ощущение нанесенной пленке после нанесения композиции на кожу.
Летучие полиорганосилоксаны могут быть линейными, или циклическими, или их смесью. Предпочтительные циклические силоксаны включают полидиметилсилоксаны и, в частности, те, которые содержат от 3 до 9 атомов кремния, предпочтительно не более 7 атомов кремния и наиболее предпочтительно от 4 до 6 атомов кремния, часто называемые иначе циклометиконами. Предпочтительные линейные силоксаны включают полидиметилсилоксаны, содержащие от 3 до 9 атомов кремния. Летучие силоксаны обычно сами по себе имеют вязкость ниже 10-5 м2/сек (10 сантистокс) и предпочтительно выше 10-7 м2/сек (0,1 сантистокс), линейные силоксаны обычно имеют вязкость ниже 5×10-6 м2/сек (5 сантистокс). Летучие силиконы могут также включать разветвленные линейные или циклические силоксаны, такие как вышеупомянутые линейные или циклические силоксаны, замещенные одним или несколькими подвешенными -O-Si(CH3)3 группами. Примеры доступных на рынке силиконовых масел включают масла, имеющие марки 344, 345, 244, 245 и 246 от Dow Corning Corporation; Silicon 7207 и Silicon 7158 от Union Carbide Corporation и SF1202 от General Electric.
Гидрофобный не смешивающийся с водой жидкий носитель, применяемый во многих композициях, может здесь альтернативно или дополнительно включать нелетучие силиконовые масла, которые включают полиалкилсилоксаны, полиалкиларилсилоксаны и полиэфиросилоксановые сополимеры. Они могут быть удачно выбраны из диметикона и сополиолов диметикона. Выбранные полиалкиларилсилоксаны включают полисилоксаны с короткой цепью, например три- или тетрасилоксаны, содержащие в среднем, по меньшей мере, одну фенильную группу на силоксановое звено, например тетрафенилтрисилоксаны. Доступные на рынке нелетучие силиконовые масла включают Dow Corning 556, серию Dow Corning 200 и DC704.
Не смешивающийся с водой жидкий носитель может содержать от 0 до 100 мас.% одного или нескольких жидких силиконов. Некоторые осуществления содержат жидкие силиконы в количестве, по меньшей мере, 10%, лучше, по меньшей мере, 15% от массы всей композиции. Если используют силиконовое масло, в некоторых осуществлениях летучий силикон предпочтительно составляет от 10 до 100 % от массы жидкости-носителя. Во многих случаях, если присутствует нелетучее силиконовое масло, его массовое отношение к летучему силиконовому маслу выбирают в интервале менее чем 3:1, такое как от 1:3 до 1:40, тогда как в некоторых других осуществлениях доля летучих силиконовых масел составляет от 0 до менее чем 10% так, что массовое отношение нелетучих к летучим силиконовым маслам больше чем 10:1, такое как от 15:1 до ∞:1. В других осуществлениях жидкие силиконы отсутствуют или присутствуют лишь в малых долях от не смешивающейся с водой фазы, таких как до 7 или 8 мас.%. Соответственно, для структурирования сложными эфирами СНМЕ по изобретению в качестве носителя может быть использован ряд смесей силиконовых масел и несиликоновых масел. Во многих из таких смесей применяют массовое соотношение силиконовых масел к несиликоновым маслам от 4:1 до 1:4. Выбор жидкости-носителя часто делают, принимая в расчет показатель преломления компонентов смеси жидкости-носителя и показатель преломления конкретного активного составляющего, такого как антиперспирант, или не смешивающейся с водой фазы.
Вместо жидких силиконов, а в некоторых осуществлениях в добавление к жидким силиконам могут быть использованы не содержащие силиконы гидрофобные жидкости. Не содержащие силиконы гидрофобные органические жидкости, которые могут быть введены, включают летучие или нелетучие жидкие алифатические углеводороды, такие как минеральные масла или гидрированный полиизобутен, часто выбранные так, чтобы они имели низкую вязкость. Дополнительными примерами жидких углеводородов являются полидецен, парафины и изопарафины с, по меньшей мере, 10 атомами углерода.
Другими гидрофобными носителями являются жидкие алифатические или ароматические сложные эфиры, но для некоторых применений, например для антиперспираторных композиций, они должны использоваться только как часть жидкого носителя, желательно не более 20%, и, возможно, менее 10% от массы не смешивающегося с водой жидкого носителя.
Подходящие алифатические сложные эфиры содержат, по меньшей мере, одну алкильную группу с длинной цепью, такие как эфиры, полученные из алканолов С1-С20, этерифицированных алкановой кислотой от С8 до С22 или алкандиоевой кислотой от С6 до С10. Алканольную и кислотную группы или их смеси предпочтительно выбирают так, чтобы каждая из них имела температуру плавления ниже 20°С. Такие сложные эфиры включают изопропилмиристат, лаурилмиристат, изопропилпальмитат, диизопропилдисебацинат и диизопропиладипинат.
Подходящие жидкие ароматические сложные эфиры, предпочтительно имеющие температуру плавления ниже 20°С, включают жирные алкилбензоаты. Примеры таких эфиров включают подходящие С9-С18 алкилбензоаты или их смеси.
Дополнительные примеры подходящих гидрофобных носителей включают жидкие алифатические простые эфиры, полученные из, по меньшей мере, одного жирного спирта, такие как производные миристиловые эфиры, например PPG-3 миристиловый эфир, или низшие алкиловые эфиры полигликолей, например С2-С4 алкильные простые эфиры PPG, такие как промышленные продукты, имеющие CFTA с номинальным обозначением PPG-14 бутиловый эфир.
Алифатические спирты, являющиеся твердыми при 20°С, такие как стеариловый спирт, предпочтительно отсутствуют или присутствуют в низких концентрациях, таких как менее 5% от массы всей композиции, поскольку они приводят к видимым белым отложениям при использовании композиции.
Однако могут применяться алифатические спирты, являющиеся жидкими при 20°С. Они включают спирты с разветвленной цепью с, по меньшей мере, 10 атомами углерода, такие как изостеариловый спирт и октилдодеканол.
Не содержащие силикон жидкости могут составлять от 0 до 100% несмешивающегося с водой жидкого носителя. Предпочтительно, чтобы присутствовало силиконовое масло и/или углеводородное масло и чтобы общее количество других жидких носителей предпочтительно составляло до 50 или 60%, например от 0 до 10% или от 10 до 20% от массы не смешивающейся с водой жидкости-носителя.
Особо предпочтительная комбинация не смешивающихся с водой жидкостей-носителей включает смесь силиконовой жидкости, такой как циклометикон, и углеводородной жидкости с массовым соотношением первой жидкости к последней от 3:2 до 1:10, необязательно в присутствии не смешивающейся с водой смягчающей жидкости.
Эмульсия
Многие композиции согласно настоящему изобретению содержат также более полярную дисперсную фазу. В таких композициях ацилированная целлобиоза по изобретению действует как структурообразователь в сплошной не смешивающейся с водой фазе. Дисперсная фаза может быть одной полярной жидкостью или, обычно, включает раствор активного ингредиента, такого как антиперспираторная соль.
Гидрофильная дисперсная фаза в эмульсии обычно включает в качестве растворителя воду и может включать одну или несколько водорастворимых или смешивающихся с водой жидкостей в добавление к воде или взамен ее. Долю гидрофильной жидкости-носителя, например воды, в дисперсной фазе эмульсии в соответствии с настоящим изобретением часто выбирают в интервале до 60% и предпочтительно от 10% до 40 или 50% от всей композиции.
Один класс водорастворимых или смешивающихся с водой жидкостей включает одноатомные спирты с короткой цепью, например, от С1 до С4 и в особенности этанол или изопропанол, которые могут придать композиции дезодорирующую способность. Следующий класс гидрофильных жидкостей включает диолы или полиолы, предпочтительно имеющие температуру плавления ниже 40°С или которые являются смешивающимися с водой. Примеры водорастворимых или смешивающихся с водой жидкостей с, по меньшей мере, одной свободной гидроксильной группой включают этиленгликоль, 1,2-пропиленгликоль, 1,3-бутиленгликоль, гексиленгликоль, диэтиленгликоль, дипропиленгликоль, 2-этоксиэтанол, монометиловый эфир диэтиленгликоля, монометиловый эфир триэтиленгликоля и сорбитол. Особо предпочтительными являются пропиленгликоль и глицерин.
В эмульсии дисперсная фаза, вероятно, составляет от 5 до 80 или 85% от массы композиции, предпочтительно от 5 до 50 или 65%, более предпочтительно от 25 или 35% до 50 или 65%, тогда как сплошная фаза со структурообразователем в ней обеспечивает оставшиеся по балансу от 15 или 35% до 95% от массы композиции. Преимущества могут возрасти, если объем внутренней фазы составляет меньшую часть эмульсии, такую как от примерно 30 до 45% по массе. Преимущества еще возрастают при объеме внутренней фазы от 45 до 65%. Композиции с высокой долей дисперсной фазы, т.е. с 65-85% дисперсной фазы, также могут быть предпочтительными. Они могут обеспечить хорошую твердость даже в тех случаях, когда концентрация структурообразователя - этерифицированного сахарида - может составлять лишь малый процент от всей композиции.
Эмульсионная композиция обычно должна включать один или несколько эмульгирующих сурфактантов, которые могут быть анионными, катионными, цвиттерионными и/или неионными поверхностно-активными веществами (ПАВ). Долю сурфактанта в композиции часто выбирают в интервале до 10% мас. и во многих случаях от 0,1 или 0,25 до 5% от массы композиции. Наиболее предпочтительным является количество от 0,1 или 0,25 до 2 или 3 мас.%, такое как 0,3, 0,4 или 0,5 мас.%, или количество между этими значениями. Неионные эмульгаторы часто классифицируют по величине ГЛБ. Желательно использовать эмульгатор или смесь эмульгаторов с общим значением ГЛБ в интервале от 2 до 10, предпочтительно от 3 до 8.
Может быть удобно использовать сочетание двух или нескольких эмульгаторов, которые имеют различные величины ГЛБ, выше и ниже желаемой величины. Применяя вместе два эмульгатора в нужном соотношении, легко достичь средневзвешенного значения ГЛБ, которое ускоряет образование эмульсии.
Многие подходящие эмульгаторы с высоким ГЛБ представляют собой неионные сложные или простые эфирные эмульгаторы, включающие полиоксиалкиленовую часть, особенно полиоксиэтиленовую часть, часто содержащую от примерно 2 до 80 и предпочтительно от 5 до 60 оксиэтиленовых единиц, и/или содержат полигидроксисоединение, такое как глицерин или сорбитол или другой альдитол в качестве гидрофильной части. Гидрофильная часть может содержать полиоксипропилен. Эмульгаторы дополнительно включают гидрофобную алкильную, алкенильную или аралкильную часть, обычно содержащую от примерно 8 до 50 атомов углерода и предпочтительно от 10 до 30 атомов углерода. Гидрофобная часть может быть либо линейной, либо разветвленной и часто является насыщенной, хотя может быть ненасыщенной и, необязательно, фторированной. Гидрофобная часть может включать смесь цепей разной длины, например, полученных из таллового, лярдового, пальмового масла, подсолнечного масла или масла соевых бобов. Такие неионные сурфактанты могут также быть получены из полигидроксисоединения, такого как глицерин, или сорбитол, или другие альдитолы. Примеры эмульгаторов включают цетеарет-10 до -25, цетет-10-25, стреарет-10-25 (т.е. спирты С16-С18, этоксилированные 10-25 этиленоксидными остатками) и ПЭГ-15-25 стеарат или дистеарат. Другие подходящие примеры включают моно-, ди- и триглицериды жирных кислот С10-С20. Дополнительные примеры включают простые эфиры жирных спиртов С18-С22 полиэтиленоксидов (от 8 до 12 единиц ЭО).
Примерами эмульгаторов, которые обычно имеют низкую величину ГЛБ, часто величину от 2 до 6, являются моно- или, возможно, диэфиры жирных кислот и многоатомных спиртов, таких как глицерин, сорбитол, эритрит или триметилолпропан. Жирноацильная часть часто представляет от С14 до С22 и во многих случаях является насыщенной, включая цетил, стеарил, арахидил и бегенил. Примеры включают моноглицериды пальмитиновой или стеариновой кислоты, моно- или диэфиры сорбитола с миристиновой, пальмитиновой или стеариновой кислотой и эфиры триметанолпропана со стеариновой кислотой.
Особо желательный класс эмульгаторов включает сополимеры диметикона, а именно модифицированные полиоксиалкиленом диметилполисилоксаны. Полиоксиалкиленовая группа часто представляет собой полиоксиэтилен (ПОЭ), или полиоксипропилен (ПОП), или сополимер ПОЭ и ПОП. Сополимеры часто оканчиваются алкильными группами от С1 до С12. Особо желательный пример данного класса доступен под торговым наименованием ABIL EM90 для использования в вышеуказанном интервале соотношений.
Подходящие эмульгаторы и соэмульгаторы широко доступны под многими торговыми марками и названиями, включающими Abil™, Arlacel™, Brij™, Cremophor™, Dehydrol™, Dehymuls™, Emerest™, Lameform™, Pluronic™, Prisorine™, Quest PGPR™, Span™, Tween™, SF1228, DC225C и Q2-5200.
Антиперспираторные активные агенты
Если композиция является антиперспираторной, она должна содержать антиперспираторно активный агент. Антиперспираторно активные агенты предпочтительно вводятся в количестве от 0,5 до 60%, более предпочтительно от 5 до 30 или 40% и наиболее предпочтительно от 5 или 10% до 30 или 35% от массы композиции.
Антиперспираторно активные агенты, используемые здесь, часто выбирают из солей с вяжущей активностью, включающих, в частности, соли алюминия, циркония и смешанные алюминий-циркониевые соли, включая и неорганические соли, и соли с органическими анионами, и комплексы. Предпочтительные вяжущие соли включают галогенидные и галогеногидратные соли, такие как хлоргидраты, алюминия, циркония и алюминия/циркония.
Галогеногидраты алюминия обычно определяются общей формулой Al2(OH)xQy•wH2O, в которой Q представляет хлор, бром или йод, x представляет переменную от 2 до 5, и (x+y)=6, тогда как wH2O представляет различное количество гидратаций (гидратов). Особо эффективные галогеногидратные соли алюминия, известные как активированные хлоргидраты алюминия, описаны в заявке EP-A-6739 (Unilever NV et al), содержание которой включено в качестве ссылки. Некоторые активированные соли не сохраняют свою повышенную активность в присутствии воды, но используются в практически безводных рецептурах, т.е. в композициях, которые не содержат различимую водную фазу.
Циркониевые активные агенты могут обычно быть представлены эмпирической общей формулой ZrO(OH)2n-nzBz•wH2O, в которой z является переменной величиной со значениями в интервале от 0,9 до 2,0, так, что величина (2n-nz) равна нулю или положительна, n представляет валентность B, и B выбирают из группы, состоящей из хлорида, других галогенидов, сульфамата, сульфата и их смесей. Возможная гидратация в переменной степени представлена выражением wH2O. Предпочтительно, чтобы В представляло хлорид, а переменная z лежала в интервале от 1,5 до 1,87. На практике такие циркониевые соли не применяют сами по себе, а используют как компонент комбинированных антиперспирантов на основе алюминия и циркония.
Вышеописанные соли алюминия и циркония могут содержать координационную и/или связанную воду в различных количествах и/или могут представлять полимерные вещества, смеси или комплексы. В частности, гидрокси соли циркония часто представляют собой ряд солей, имеющих различные количества гидроксигрупп.
Особенно предпочтительными может быть хлоргидрат цирконий-алюминия.
Могут быть применены антиперспираторные комплексы на основе вышеупомянутых вяжущих солей алюминия и/или циркония. В комплексах часто применяют соединение с карбоксилатной группой, и предпочтительно оно представляет собой аминокислоту. Примеры подходящих аминокислот включают dl-триптофан, dl-β-фенилаланин, dl-валин, dl-метионин и β-аланин и предпочтительно глицин, который имеет формулу CH3CH(NH2)CO2H.
Крайне желательно применять комплексы комбинации галогеногидратов алюминия и галогеногидратов циркония с аминокислотой, такой как глицин, которые описаны в US-A-3792068 (Luedders et al.). Некоторые из таких Al/Zr комплексов обычно называют в литературе ZAG. Активные агенты ZAG обычно содержат алюминий, цирконий и хлорид с соотношением Al/Zr в интервале от 2 до 10, предпочтительно от 2 до 6, и имеют соотношение Al/Cl от 2,1 до 0,9 и различное количество глицина. Активные агенты такого типа могут быть получены от Westwood, от Summit и от Reheis.
Другие активные агенты, которые могут использоваться, включают вяжущие соли титана, например те, которые описаны в GB 2299506A.
Доля твердой антиперспираторной соли в композиции обычно включает массу всей гидратационной воды и всего комплексообразующего агента, которые могут также присутствовать в твердом активном агенте. Однако, если активная соль находится в растворе, ее масса исключает любую присутствующую воду.
Если композиция находится в виде эмульсии, антиперспираторный активный агент должен быть растворен в дисперсной фазе. В таком случае антиперспираторный активный агент часто должен составлять от 3 до 60% от массы водной дисперсной фазы, предпочтительно от 10% или 20% до 55% или 60% от этой фазы.
Альтернативно, композиция может принимать вид суспензии, в которой антиперспираторный агент в форме частиц суспендирован в не смешивающемся с водой жидком носителе. Такая композиция, возможно, не будет иметь отдельной водной фазы и может условно называться "практически безводной", хотя следует понимать, что может присутствовать некоторое количество воды, связанной с антиперспираторным агентом или как небольшое количество растворенного вещества внутри не смешивающейся с водой жидкой фазы. В таких композициях размер частиц антиперспираторной соли часто попадает в интервал от 0,1 до 200 мкм при среднем размере частиц от 3 до 20 мкм. Может рассматриваться также и более крупный, и более мелкий средний размер частиц, как от 20 до 50 мкм или от 0,1 до 3 мкм.
Необязательные ингредиенты
Необязательные ингредиенты в композициях по данному изобретению могут включать дезодоранты, например, в концентрации до примерно 10 мас.%. Подходящие дезодорирующие агенты могут включать дезодорирующие эффективные концентрации антиперспираторных солей металлов, дезодорирующих отдушек и/или микробицидов, включая предпочтительно бактерициды, такие как хлорированные ароматические соединения, включающие производные бигуанидина, из которых вещества, известные как триклозан, например Igasan DP300™, Tricloban™ и хлоргексидин, заслуживают особого упоминания. Еще один класс включает соли бигуанидина, такие как соли, доступные под торговой маркой Cosmosil™.
Еще один класс антимикробных агентов, который может успешно использоваться здесь, включает хелаторы переходных металлов, такие как аминокислоты или их соли, которые имеют аффинность к железу(III) и предпочтительно константу связи с железом(III) больше 1010 или, для оптимальной характеристики, больше 1026. "Константа связи с железом(III)", о которой сказано выше, представляет константу абсолютной стабильности комплекса хелаторжелезо(III). Особенно предпочтительным хелатообразующим агентом является ДЭТАПУК (диэтилентриаминпентауксусная кислота) и ее соли. Такие антимикробные агенты подавляют возобновление роста микробов. Обычное количество их составляет от 0,35 до 2 мас.%.
Другие необязательные ингредиенты включают моющие агенты, часто присутствующие в количестве до 10 мас.%, для того, чтобы помочь удалить композицию с кожи или с одежды. Такие моющие агенты обычно представляют собой неионные поверхностно-активные вещества (ПАВ), такие как сложные или простые эфиры, содержащие алкильную группу от С8 до С12 и гидрофильную группу, которая может включать полиоксиалкиленовую группу (ПОЭ или ПОП) и/или полиол.
Данные композиции могут включать одно или несколько косметических вспомогательных веществ, обычно предназначенных для антиперспирантных твердых продуктов или мягких твердых продуктов. Такие косметические вспомогательные вещества могут включать агенты, улучшающие ощущение на коже, такие как тальк или тонко измельченный полиэтилен, например, в количестве до 10%, полезные для кожи агенты, такие как аллантоин или липиды, например, в количестве до 5%, красители, охлаждающие кожу агенты, отличные от уже упоминавшихся спиртов, такие как ментол и производные ментола, часто в количестве до 2%, где все проценты указаны на массу композиции. Обычно применяемым вспомогательным веществом является отдушка, которая обычно присутствует в концентрации от 0 до 4% и во многих рецептурах от 0,25 до 2% от массы композиции.
Следующим необязательным составляющим композиций является один или несколько вторичных структурообразователей, которые могут использоваться в добавление к этерифицированным сахаридам по настоящему изобретению. Количество таких вторичных структурообразователей в рецептуре часто составляет ноль и обычно не более 15% от композиции. Во многих осуществлениях оно обычно не больше количества первичного структурообразователя.
Используемые здесь вторичные структурообразователи могут быть неполимерными или полимерными. Могут быть включены твердые линейные жирные спирты, но они не являются предпочтительными. Неполимерные структурообразователи, иногда называемые гелеобразователями, могут быть выбраны из жирных кислот или их солей, таких как стеариновая кислота, или стеарат натрия, или 12-гидроксистеариновая кислота. Другие подходящие гелеобразователи могут включать дибензилиденальдитолы, например дибензилиденсорбитол. Следующие подходящие гелеобразователи могут включать ланостерол, избранные производные N-ациламинокислот, включая эфирные и амидные производные, такие как дибутиламид N-лаурилглютаминовой кислоты, каковые гелеобразователи могут быть рассмотрены в сочетании с 12-гидроксистеариновой кислотой или ее эфирными или амидными производными. Еще следующие гелеобразователи включают амидные производные двух- или трехосновных карбоновых кислот, такие как N,N'-диалкилсукцинамиды, например додецил-N,N'-дибутилсукцинамид.
Полимерные структурообразователи, которые могут быть применены, могут включать органополисилоксановые эластомеры, такие как продукты реакции полисилоксана с винильной группой на конце и сшивающего агента или поли(метилзамещенных) или поли(фенилзамещенных) силоксанов с алкил- или алкиленполиоксиалкиденовой группой на конце. В качестве структурообразователей для гидрофобных жидкостей описан также ряд полиамидов. Полимеры, содержащие и силоксановые, и образующие водородную связь группы, которые могут быть использованы в качестве вторичных структурообразователей, были описаны в WO 97/36572 и WO 99/06473. Если присутствует водная дисперсная фаза, для структурирования или загущения этой водной фазы могут быть использованы полиакриламиды, полиакрилаты или полиалкиленоксиды.
Наиболее предпочтительным вторичным структурообразователем является этерифицированная целлобиоза, как описано в PCT/GB 00/01228, описание которого включено здесь в качестве ссылки. Такой структурообразователь иногда называют здесь АСВ структурообразователем. Предпочтительно АСВ структурообразователь может быть представлен формулой
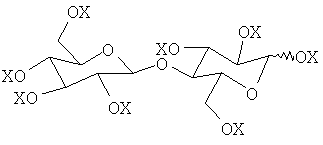
в которой Х представляет либо гидроксильную, либо ацильную группу R-CO-, где R таково, как определено выше. Более предпочтительно ацильная группа -COR составляет, по меньшей мере, 50% и предпочтительно, по меньшей мере, 75% от X. В таких АСП структурообразователях алкильная группа R представляет октил или нонил или, предпочтительно, может включать смеси групп R, имеющие на два атома углерода меньше или на два атома углерода больше, чем среднее от 8 до 9 атомов углерода. Заместитель -ОХ присутствует в целлобиозе у аномерного атома углерода. АСВ структурообразователь может быть получен в виде или α-, или β-аномера. Крайне желательно, чтобы доля α-аномера в АСВ структурообразователе была больше 50%, предпочтительно больше 80% и особо предпочтительно больше 90%.
Здесь может быть выгодно использован АСВ структурообразователь с первичным структурообразователем по изобретению (СНМЕ) в широком интервале концентраций, таком как при массовом соотношении к нему до 25:1 и во многих случаях до 15:1, и в тех же самых или других осуществлениях в интервале от 1:25 или иногда от 1:5 или от 1:1. Обычное массовое соотношение АСВ к СНМЕ составляет от 5:1 до 12:1. В некоторых особо предпочтительных рецептурах массовое соотношение АСВ к СНМЕ составляет от 65:35 до 85:15.
В ряде наиболее подходящих композиций АСВ выбирают из октадеканоатных эфиров целлобиозы, в особенности тех из них, у которых, по меньшей мере, 80 мол.% например от 80 до 95 мол.%, составляет α-аномер. В некоторых из таких наиболее подходящих композиций и в различных других подходящих композициях СНМЕ эфир включает гептанодекаиоатный монобензоатный эфир целлобиозы и предпочтительно такой СНМЕ эфир, в котором, по меньшей мере, 90 мол.% β-аномера, как от 93 до 100 мол.% β-аномера.
Полупрозрачная/прозрачная композиция
Если композицию по данному изобретению составляют как эмульсию, возможно создать такую композицию, что эмульсия будет полупрозрачной или прозрачной. Для того чтобы достичь этого, показатели преломления не смешивающейся с водой сплошной фазы и полярной или водной дисперсной фазы должны быть подобраны друг к другу и значение показателя преломления, к которому они должны быть подобраны, должно примерно соответствовать показателю преломления структурообразователя.
Показатель преломления волокнистой сети структурообразователя может быть определен путем использования данного структурообразователя для гелеобразования ряда масел или масляных смесей с различным показателем преломления. Волокнистые сети ацилированной целлобиозы по изобретению (СНМЕ) имеют показатель преломления, который попадает в интервал между 1,45 и 1,51 при 22°С.
Для сплошной фазы описанные здесь не содержащие силиконы не смешивающиеся с водой жидкие масла обычно имеют показатель преломления в интервале от 1,43 до 1,49 при 22°С и могут быть использованы одни или в смеси для того, чтобы получить не содержащую силиконы жидкость-носитель с показателем преломления в этом интервале. Летучие силиконовые масла обычно имеют при 22°С показатель преломления немного ниже 1,40, а некоторые нелетучие силиконовые масла, например диметиконовые масла, аналогично имеют показатель преломления при 22оС около 1,41, но смеси жидкостей-носителей с показателями преломления в интервале от 1,41 до 1,46 могут быть получены смешением летучего или такого нелетучего силикона с другими маслами. Другие нелетучие силиконовые масла, содержащие арильные заместители, обычно имеют показатель преломления, по меньшей мере, 1,45, например от 1,45 до 1,48 при 22°С, масла с более высоким отношением фенильных заместителей к алкильным заместителям могут обеспечить более высокий показатель преломления, такой как от 1,49 до 1,56. Такие другие вышеупомянутые нелетучие силиконовые масла могут быть включены, если желательно получить смесь жидкости-носителя, имеющую желаемый показатель преломления.
Показатель преломления структурированной сплошной фазы обычно должен быть очень близок к показателю преломления жидкости-носителя (обычно смеси жидкостей-носителей), которая является ее главным компонентом.
Для дисперсной фазы один раствор антиперспираторно активной соли в воде обычно имеет показатель преломления ниже 1,425. Показатель преломления может быть повышен включением в водный раствор диола или полиола. Считают, что выгодно довести показатель преломления полярной дисперсной фазы до показателя преломления сетки структурообразователя со сплошной фазой. Кроме того, это может быть достигнуто без использования такого большого количества диола или полиола, которое может сделать композицию избыточно липкой.
Механические свойства и упаковка продукта
Композиции по данному изобретению являются стуктурированными жидкостями и могут быть по внешнему виду твердыми или мягкими. Даже мягкое твердое вещество имеет способность сохранять свою форму. Например, если его удалять через фильеру, не подвергая сдвигу, оно будет сохранять свою форму, по меньшей мере, 30 секунд, обычно дольше.
Композиция по данному изобретению обычно должна поступать на рынок в виде косметического изделия, включающего контейнер с некоторым количеством композиции в нем, причем контейнер имеет, по меньшей мере, одно отверстие для доставки композиции и устройство для движения композиции в контейнере по направлению к доставочному отверстию. Обычные контейнеры имеют форму гильзы с овальным поперечным сечением с доставочным отверстием (отверстиями) на одном конце гильзы.
Композиция по данному изобретению может быть достаточно жесткой, то есть нелегко деформируемой давлением руки, и она пригодна для применения в качестве косметического карандаша, в котором некоторое количество композиции в форме палочки помещено внутрь гильзы контейнера, имеющей открытый конец, из которого выдвигается для использования конечная часть палочки композиции. Противоположный конец гильзы закрыт.
Обычно контейнер должен включать крышку для его открытого конца и составляющую часть, которую иногда называют подъемником или поршнем, вставленную в гильзу и способную к относительному аксиальному движению вдоль нее. Палочку композиции помещают в гильзу между поршнем и открытым концом гильзы. Поршень используют для того, чтобы двигать палочку композиции вдоль гильзы. Поршень и палочка композиции могут двигаться аксиально вдоль гильзы давлением руки на нижний конец поршня, используя палец или стержень, вставленный внутрь гильзы. Другой возможностью является то, что стержень, присоединенный к поршню, выступает через прорезь или прорези в гильзе и используется для того, чтобы двигать поршень и палочку. Предпочтительно контейнер включает также транспортный механизм для движения поршня, включающий врезанный стержень, который входит аксиально в палочку через соответствующее прорезанное отверстие в поршне, и устройство, установленное на гильзе для вращения стержня. Обычно стержень вращают посредством маховичка, установленного на гильзе на ее закрытом конце, т.е. на конце, противоположном доставочному отверстию.
Если композиция по данному изобретению является более мягкой, но еще способна сохранять свою форму, она более пригодна для распределения через закрытый конец, а не через открытый конец, где закрытый конец имеет одно или несколько отверстий, через которые композиция может выдавливаться из гильзы. Число и форма таких отверстий определяются по усмотрению разработчика упаковки.
Составляющие части таких контейнеров часто изготавливают из термопластичных материалов, например из полипропилена или полиэтилена. Описание подходящих контейнеров, некоторые из которых имеют дополнительные характерные признаки, можно найти в патентах США 4865231, 5000356 и 5573341.
После описания изобретения в общих чертах его конкретные осуществления будут описаны более полно только для примера.
Пример 1
В данном примере соединения гептанонаноатного эфира целлобиозы по настоящему изобретению, перечисленные ниже в табл.1, получали трехстадийным способом, две первые стадии которого были общими для всех вариантов, а третью стадию которого проводили одним из трех методов. Способ пояснен на примере гептанонаноатных эфиров целлобиозы. Другие ацилированные эфиры целлобиозы получали, заменяя нонановую кислоту такими же мольными количествами альтернативных ацилирующих агентов.
Стадия 1. Получение октанонаноата целлобиозы
Целлобиозу этерифицировали нонановой кислотой, получая полностью этерифицированный продукт в виде его α-аномера, следуя в основном методике, описанной Takada et al., Liquid Crystals, Volume 19, No 4, p. 441 (1995).
Использовали следующие материалы, полученные от Acros Organics - Fisher Scientific:
D-(+)-целлобиоза, 20 г, 0,058 моль;
Нонановая кислота, 591,6 г, 3,74 моль;
Трифторуксусный ангидрид, 297,6 г, 1,42 моль.
Нонановую кислоту загружали в 2-литровый сосуд с фланцами, снабженный устройством для перемешивания воздухом, водяным конденсатором и дополнительным вводом для трифторуксусного ангидрида. Полученную прозрачную смесь перемешивали и нагревали до 100°С, используя баню с силиконовым маслом и датчик температуры. Во время нагрева было замечено, что цвет реакционной смеси темнел и появлялся темно-коричневый оттенок. После того как смеси давали перемешиваться в течение одного часа при 100°С, к темному активированному раствору медленно добавляли целлобиозу через воронку для твердого порошка, и образовывалась темно-коричневая суспензия, которую за 10-20 минут вновь растворяли, образуя прозрачный черный раствор.
Реакционный сосуд затем выдерживали при 100°С в течение суммарно 6 часов, затем охлаждали до температуры окружающей среды в лаборатории. Далее содержимое колбы переносили в 2 л метанола, содержащего 10% деионизированной воды, в охлаждаемый льдом 5-литровый химический стакан. Из раствора немедленно выпадал беловатый твердый осадок, который отфильтровывали и собирали. Сырое твердое вещество перекристаллизовывали в общем 4 раза из раствора тетрагидрофуран/метанол, получая белый твердый продукт.
Продукт получали в количестве 31,5 г, что дает выход 37%. Он имел температуру плавления 110°С.
Стадия 2. Частичное деацилирование
Ледяную уксусную кислоту (2,04 г) медленно добавляли по каплям при перемешивании в раствор этилендиамина (4,09 г) в тетрагидрофуране (ТГФ, 850 см3). Образовывался белый осадок, который сохранялся во время реакции. Затем добавляли октанонаноат α-целлобиозы (50 г) и всю реакционную смесь перемешивали при комнатной температуре в течение 48 часов.
По окончании реакции содержимое колбы переносили в 2-литровую разделительную воронку, добавляли 350 см3 воды и смесь экстрагировали дихлорметаном (250 см3). Органический слой отбирали и далее промывали последовательно 350 см3 порциями (1) разбавленной HCl (0,1 М), (2) водного раствора бикарбоната натрия (1 М) и (3) воды.
Полученную органическую фазу извлекали, сушили над безводным сульфатом магния, фильтровали и удаляли остаточный растворитель в роторном испарителе. Получали слабо липкий беловатый твердый продукт-сырец. Затем его перекристаллизовывали из смеси ТГФ/метанол (50:300 см3). Во время хранения в течение ночи выпадал белый осадок, который отфильтровывали, сушили и собирали, получая 30,5 г белого свободно пересыпающегося твердого вещества в качестве промежуточного продукта (выход 68%).
Стадия 3
3А. Переацилирование ацилхлоридом
Этот путь пояснен на примере бензоатного эфира и является применимым ко всем эфирам при замене бензоилхлорида хлорангидридами других кислот.
В 3-горлую 500 см3 круглодонную колбу загружали гептанонаноат целлобиозы (5 г, 3,78×10-3 моль) вместе с 125 см3 толуола. Смесь тщательно перемешивали до получения прозрачного раствора. Далее к раствору медленно добавляли по каплям триэтиламин (0,479 г, 4,73×10-3 моль).
После этого в реакционную смесь через капельную воронку уравненного давления медленно и осторожно добавляли бензоилхлорид (0,665 г, 4,73×10-3 моль). Когда добавление реагентов завершалось, весь реакционный раствор нагревали и выдерживали в условиях кипения с обратным холодильником в целом в течение 2-3 часов. Затем нагревание прекращали и после охлаждения содержимое колбы фильтровали для удаления присутствующей твердой соли гидрохлорида триэтиламина. Получали прозрачную жидкость соломенного цвета. Затем весь растворитель удаляли в роторном испарителе, получая сырой продукт, гелеобразное вещество соломенной окраски. Сырой продукт кристаллизовали из ТГФ-МеОН (20 см3:120 см3). Полученный продукт, белое свободно пересыпающееся твердое вещество, отфильтровывали, собирали и сушили при 40-45°С. Выход составлял 3,5 г (65%).
3В. Переацилирование с применением кислоты/катализатора
Данный способ продемонстрирован на примере использования бензойной кислоты и может быть также применен для приготовления других сложных эфиров целлобиозы при замене бензойной кислоты другой подходящей кислотой.
В 2-горлую 250 см3 круглодонную колбу загружали бензойную кислоту (29,54 г, 0,24 моль) и трифторукусусный ангидрид (19,05 г, 0,091 моль). Смесь перемешивали и нагревали до 100°С и поддерживали при этой температуре в течение одного часа. В активированный раствор медленно вводили гептанонаноат целлобиозы (5 г, 3,8×10-3 моль) через воронку для ввода твердого вещества. После того как добавление завершалось, реакционную смесь выдерживали при 100°С при перемешивании в течение суммарно 6 часов. Затем реакционную колбу охлаждали до комнатной температуры. В колбу выливали охлажденный на льду метанольноводный раствор (400 см3 МеОН:40 см3 воды), в результате чего немедленно образовывался твердый осадок, осадок отфильтровывали и перекристаллизовывали из ТГФ-МеОН (20 см3:120 см3). Полученный продукт отфильтровывали, собирали и перекристаллизовывали вторично из ТГФ-МеОН для удаления следов кислоты. Конечный продукт, белое твердое вещество, отфильтровывали, собирали и сушили при 40-45°С. Выход составил 3,1 г (58%).
3С. Переацилирование с использованием ангидрида
Способ пояснен на примере использования уксусного ангидрида, и другие сложные эфиры целлобиозы могут быть получены при замене уксусного ангидрида соответствующим ангидридом.
В 3-горлую 500 см3 круглодонную колбу загружали гептанонаноат целлобиозы (5 г, 3,78×10-3 моль) и толуол (150 см3). Смесь перемешивали, получая желтый прозрачный раствор. Добавляли уксусный ангидрид (1,16 г, 1,13×10-2 моль) через капельную воронку с выравненным давлением. Когда его добавление завершалось, реакционную смесь нагревали до 120оС и кипятили с обратным холодильником в течение 6 часов. Смесь охлаждали до комнатной температуры и весь растворитель удаляли в роторном испарителе, получая сырое гелеобразное твердое вещество, которое отфильтровывали и перекристаллизовывали из ТГФ-МеОН (20 см3:120 см3), отфильтровывали и сушили при 40-45°С. Выход - 4,4 г (85%).
Перечисленные в табл.1 заместители находятся у аномерного атома углерода, и перечисленные % Y представляют долю аномерного ОН, который превращен в указанную ацильную группу.
Проценты А (α-аномер) и Y (степень ацилирования по аномерному углероду) могут быть определены методом протонной ЯМР-спектроскопии с использованием Bruker DRX 500 мГц ЯМР-спектрометра. Образцы вводились в растворителе 99,8 % атомных D-хлороформе (CDCl3), содержащем 0,03% тетраметилсилана (ТМС).
В полученных с использованием протонной ЯМР-спектроскопии спектрах ацилированной целлобиозы альфа- и бета-аномеры имеют различимые пики при различимых химических сдвигах. Положение пиков зависит также от того, был ли аномерный углерод замещен гидроксильной или ацильной группой. Дублет в низкой области обусловлен протоном аномерного углерода альфа-аномера (Jaxial-equa=3,8 Гц; 6,2 ч/млн), если аномерный углерод ацилирован, тогда как соответствующий дублет имеет химический сдвиг 5,36 ч/млн, если его заместителем является гидроксил. Соответственно, спектр включает набор дублетов в более высокой области, обусловленных протоном аномерного углерода бета-аномера (Jaxial-axial=7,9 Гц; 5,65 ч/млн), если аномерный углерод ацилирован, и c химическим сдвигом 4,82 ч/млн, если аномерный углерод замещен простым гидроксилом. Линейное сравнение площадей пиков позволяет определить относительное содержание двух аномеров.
Способность протонной ЯМР спектроскопии различать молекулы ацилированной целлобиозы, в которых аномерный углерод целлобиозы замещен гидроксильной или ацильной группой, может быть улучшена применением метода, по которому снимают спектр исходного образца, проводят реакцию гидроксильной группы образца с трихлорацетилизоцианатом (ТХАИ) и вновь снимают спектр образца. Химический сдвиг для альфа-молекулы с присоединенным ТХАИ составляет 6,33 ч/млн, а для бета-молекулы с присоединенным ТХАИ составляет 5,73 ч/млн. Путем сравнения площадей пиков спектра можно определить относительные содержания альфа плюс бета гидроксила, альфа-ацилированных и бета-ацилированных молекул.
Пример 2
В данном примере получали гептадеканоатные эфиры целлобиозы, аналогично описанным в примере 1, но применяя на стадии 1 декановую кислоту вместо нонановой кислоты. Результаты приведены ниже в табл.2.
Сравнительные вещества октанонаноат целлобиозы, октадеканоат целлобиозы и гептанонаноат целлобиозы, которые были применены в примерах 5-17, приведены в табл.3.
Пример 3
В данном примере готовили другие сложные эфиры, включающие гептанонаноат целлобиозы и различные сложноэфирные группы в аномерном положении. Способ включает вариации трехстадийного процесса, описанного выше в примере 1, причем принципиальные отличия будут здесь указаны.
На стадии 1 применяли основной катализатор, получая β-октанонаноат D-целлобиозы.
D-(+)-целлобиозу (ACROS; 99% ЖХВР; 67% β-аномера), нонаноилхлорид (83 г, 0,47 моль; 96 % ALDRICH (анализ: ГХ: 97,4% с остаточным 2-метилоктаноилхлорида); сухой хлороформ 99+% (бутыли Sure Seal™, реактивной квалификации, ALDRICH), сухой пиридин 99,8+% (бутыли Sure Seal™, реактивной квалификации, ALDRICH), тетрагидрофуран (FISHER, реактивной квалификации) и метанол (FISHER, реактивной квалификации) использовали в том виде, в каком их получали.
250-мл трехгорлая круглодонная колба была оборудована двойным поверхностным конденсатором, воронкой уравненного давления и устройством для перемешивания воздухом. Всю стеклянную установку предварительно сушили в течение ночи при 105°С.
Прозрачный слабо-желтый нонаноилхлорид (83,2 г, 0,47 моль) при 50°С и непрерывном перемешивании медленно (за время между 15 и 30 мин) добавляли по каплям к раствору целлобиозы (10 г, 0,029 моль) в сухом хлороформе (40 мл) и сухом пиридине (20 мл). Полученной гетерогенной слабо-желтой смеси давали реагировать при 50°С в инертной атмосфере и интенсивном перемешивании до тех пор, пока мониторинг методами протонной ЯМР и ЖХВР не показывал отсутствие гептазамещенной целлобиозы за период около 20 часов.
Гетерогенную слабо-желтую смесь охлаждали до комнатной температуры. Затем реакционную смесь выливали в метанол (1000 мл) и перемешивали в течение примерно 15 минут, получая осадок, который извлекали фильтрацией, промывали 50 мл свежего метанола и сушили в вакуумном сушильном шкафу (0,8 мбар, 80 Па) при 40-45°С в течение 5 часов. Было извлечено 39 г белого твердого вещества.
Белое твердое вещество трижды перекристаллизовывали из смеси тетрагидрофуран/метанол (75/200 мл), фильтровали, промывали 50 мл метанола и сушили в вакуумном сушильном шкафу в течение 5 часов при 40-45°С. Было получено 18 г (42%) белого твердого вещества.
На стадии 2 повторяли процесс стадии 2 примера 1, но в масштабе 1/5. Реакционную смесь выдерживали при 40°С в течение суммарно 7 часов. Выделенный кристаллический осадок сушили в вакуумном сушильном шкафу при 40°С в течение между 5 и 6 часами под давлением между 0,8 и 1,0 мбар (от 80 до 100 Па).
На стадии 3 повторяли процесс стадии 3А примера 1, за исключением того, что и триэтиламин, и ацилхлорид применяли в мольном отношении 2,5:1 к гептанононаноату целлобиозы. Выделенный кристаллический осадок сушили в вакуумном сушильном шкафу при 40°С в течение времени между 5 и 6 часами под давлением между 0,8 и 1,0 мбар.
Степень ацилирования и соотношение α- и β-аномеров определяли, как в примере 1, и результаты представлены в табл.4.
Пример 4
В данном примере различные образцы этерифицированной целлобиозы, полученные, как в примерах 1 или 2, выше, использовали для гелеобразования не смешивающихся с водой косметических жидкостей в соответствии с приведенной ниже методикой, по которой большое число гелей могло быть приготовлено одновременно.
Образцы испытывали в 96-луночном (8×12 рядов) стеклянном микротитрационном планшете. Каждая лунка имела объем около 1 мл. Примерно 0,01 или 0,02 г каждой этерифицированной целлобиозы помещали в 8 последовательных лунок в одном ряду таким образом, чтобы каждая лунка содержала приблизительно 5% или 10% эфира целлобиозы. Остальную часть объема каждой лунки заполняли косметической жидкостью добавлением приблизительно 0,2 г соответствующей жидкости в каждую ячейку. Сверху на планшет помещали стеклянную крышку. Планшет осторожно помещали в термостатически регулируемый сушильный шкаф с вспомогательным вентилятором при 150°С на 2,5 часа. Планшет вынимали из сушильного шкафа и давали ему остыть естественным путем до температуры окружающей среды в лаборатории. Содержимое лунок оценивали в конце периода охлаждения визуальным контролем и протыканием содержимого каждой лунки микрошпателем. Планшеты выдерживали при 18°С в течение 18 часов и оценивали содержимое, дополнительно выдерживали в течение 18 часов при 4°С и оценивали в третий раз. Полученные при испытаниях результаты суммированы в табл.5, в которой использованы следующие обозначения:
примера
масло
Из табл.5 можно видеть, что сложные эфиры СНМЕ наиболее пригодны для гелеобразования силиконовых масел, углеводородных масел, простых эфиров и жидких жирных спиртов.
Пример 5
В данном примере определяли температуру растворения волокна (ТРВ) по способу ДСК, описанному здесь далее, наблюдая момент растворения волокон во время подъема температуры. За ТРВ принимали пиковую температуру самого высокого пика.
Результаты приведены в табл.6, в которой описание аномерного состава указывает соотношение α : β и ацильный заместитель у аномерного углерода. В сравнительных образцах REF2 и REF3 ацильными заместителями у других семи центров целлобиозы являются нонаноильные радикалы.
(оС)
Из табл.6 могут быть сделаны два умозаключения. Во-первых, температура растворения волокон структурообразователя согласно настоящему изобретению выше, чем у известных структурообразователей, взятых для сравнения, указывая на то, что термическая стабильность (устойчивость к плавлению) геля, полученного с использованием структурообразователя по изобретению, выше.
Во-вторых, растворимость структурообразователей по изобретению при 25°С имеет склонность быть ниже, чем у сравнительных структурообразователей. Авторы обнаружили, что такая более низкая растворимость улучшает сопротивление структурообразователя кристаллизации во время хранения гелей.
Метод ДСК
Образцы геля (около 20 мл) запаивали в капсулах из нержавеющей стали для ДСК. В качестве физического стандарта использовали пустую капсулу из нержавеющей стали. Образцы подвергали испытаниям по следующей температурной программе.
Образец нагревали до 100°С и выдерживали при 100°С в течение 1 минуты для того, чтобы получить изотропный раствор. Затем образец охлаждали при 5 К/мин до -20°С. Образец выдерживали при -20°С в течение 1 минуты. Теперь образец представлял собой гель на дне капсулы с образцом, полученный воспроизводимым образом. Затем гель нагревали при 5 К/мин до 100°С. Были также получены данные для пустых чашек из нержавеющей стали в качестве и физических образцов, и стандарта. Эти холостые данные были позднее вычтены из данных для образца, чтобы устранить любую кривизну базовой линии.
Пример 6
Проверка стабильности
Готовили гели, используя 10% структурообразователь в смеси гидрированного полиизобутена (Panalene L14E): DC245 60:40. Гели в запаянных стеклянных пузырьках оставляли стоять в течение 18 часов при комнатной температуре, после чего их переносили в сушильный шкаф, термостатически поддерживающий 37°С. Образцы периодически проверяли на видимые глазом признаки роста кристаллов. Образец REF1 представлял октанонаноат. Результаты обобщены в табл.7.
- Большее количество и более крупные кристаллы после 6 час при 37°С.
- Кристаллы по всему гелю после 3 суток при 37°С.
- Мелкие кристаллы на поверхности после 8 суток при 37°С
- Мелкие игольчатые кристаллы по всему гелю после 9 суток при
37°С.
- Больше игольчатых кристаллов в объеме геля и масса кристаллов на поверхности после 13 суток при 37°С
- Большое количество кристаллов по всему гелю после 3 суток при 37°С
Табл.7 показывает, что структурообразователи по изобретению имеют заметное преимущество перед и REF1, и REF2 по резистентности к кристаллизации во время хранения.
Пример 7
Данный пример показывает определенные преимущества, которые можно получить, применяя часть структурообразователя согласно настоящему изобретению в сочетании со структурообразователем, приведенным в примерах или описании в PCT/GB 00/01228.
В данном примере гидрированный полидецен:DC245 60:40 подвергали гелеобразованию сочетанием 9% октанонаноата целлобиозы (87,5 % α, код REF2) и 1% описанного в заявке сложного эфира целлобиозы. Прозрачность и полупрозрачность образцов обобщены в табл.8, в которой %Т представляет % полупрозрачность с длиной волны 580 нм.
полупрозрачный 4
полупрозрачный 4
полупрозрачный 5
полупрозрачный 4
Из табл.8 можно видеть, что добавление структурообразователей по изобретению проявляет тенденцию образовывать гель, который визуально несколько лучше в том, что число баллов для него выше, чем при добавлении сравнительных структурообразователей. Это подтверждается данными по %Т, пропусканию света, которые аналогично показывают такое же и в большинстве случаев более высокое пропускание света.
Шкала визуальной оценки
Гель, содержащийся в кювете толщиной 1 см, помещали прямо на лист белой бумаги, в котором был напечатан черным 21 набор фигур. Фигуры систематически изменялись по размеру и толщине и были пронумерованы от -12 (самый крупный и самый толстый набор) через 0 до 8 (самый мелкий и самый тонкий набор). Баллом, присваиваемым каждому гелю, был самый большой номер набора, который мог быть ясно прочитан через гель. Чем больше номер, тем больше прозрачность.
Пропускание света
Просвечиваемость композиции можно измерить, помещая образец стандартизованной толщины в световой пучок спектрофотометра и замеряя пропускание как процент от света, пропущенного в отсутствие геля.
Такое испытание проводили, используя двухпучковый спектрофотометр. Образец композиции наливали горячим в 4,5 мл кювету из полиметилметакрилата (ПММА) и давали ему остыть до температуры окружающей среды 20-25°С. Такая кювета дает толщину композиции 1 см. Измерения проводили на 580 нм с идентичной, но пустой кюветой в сравнительном пучке спектрофотометра после выдержки образца в кювете в течение 14 часов. Пропускание, измеренное при любой температуре в интервале 20-25°С, является обычно адекватно точным, но если требовалась большая точность, то измерение проводили при 22°С.
Пример 8
В данном примере проводили оценку температуры растворения волокна, пропускания света и визуальной прозрачности для гептанонаноата моноциклогексаноата целлобиозы, изготовленного в соответствии с примером 1 или 3, используя методы, описанные в примерах 5 и 7. Гели готовили в смеси 60:40 (мас.) гидрированный полидецен:летучий силикон (Silkflo 364:DC245). Результаты обобщены в табл.9.
(оС)
Пример 9
В данном примере следовали методике примера 7, но применяли 9% REF4, к которому добавляли 1% его самого, или другого сравнительного материала, или материала по изобретению. Гели испытывали таким же образом, как в примере 7, и результаты приведены в табл.10.
Из табл.10 можно видеть, что добавление структурообразователей по изобретению проявляет тенденцию давать гель, который визуально намного лучше в том, что визуальная оценка для него выше, чем при добавлении сравнительных структурообразователей. Это подтверждается данными по %Т, пропусканию света, которые аналогично показывают намного более высокое пропускание света.
Пример 10
В данном примере гели получали, как в примере 9, но применяли различные массовые соотношения АСВ структурообразователя REF4 и эфира по изобретению, полученного в примере 2.6, при общем массовом содержании 10% в смеси 60:40 (мас.) гидрированный полидецен:летучий силикон (Silkflo 364NF:DC245). Результаты обобщены ниже в табл.11.
Из табл.11 можно видеть, что прозрачность гелей, включающих смесь эфира СНМЕ (по изобретению) и сравнительного продукта, превосходила прозрачность геля, в котором применяли только эфир по изобретению или сравнительный продукт REF4. Наилучшая прозрачность была достигнута, когда применяли избыточное соотношение структурообразующего эфира АСВ, в особенности при соотношении СНМЕ:АСВ в интервале от 35:65 до 15:85.
Пример 11
В данном примере повторяли пример 10, но применяли сравнительный эфир REF2 и эфир СНМЕ - продукт примеров 1.12 или 1.13. Результаты обобщены в табл.12.
Из табл.12 можно видеть, что даже в тех случаях, когда сравнительный (АВС) эфир дает полупрозрачный гель, можно подобрать такую комбинацию эфиров СНМЕ и АВС, которая дает улучшенную прозрачность, в особенности при массовом соотношении эфиров СНМЕ и АСВ в интервале от 35:65 до 15:85.
Пример 12
Гели готовили и испытывали в соответствии с методикой примера 6, как таковой или модифицированной с применением массового соотношения в 9% REF1 и 1% дополнительного структурообразователя, как указано в табл.13.
Большее количество и более крупные кристаллы после 6 час при 37°С; кристаллы по всему гелю после 3 суток при 37°С.
Намного большая кристаллизация на поверхности и кристаллы игольчатой формы в объеме геля после 6 суток при 37°С
Кристаллы по всему гелю после 9 суток при 37°С; больше кристаллов в всем геле после 13 суток при 37°С.
Табл.13 показывает, что имеется значительное улучшение стабильности как результат добавления доли структурообразователя по данному изобретению к структурообразователю по РСТ/GB 00/01228. Подобным же образом существует преимущество добавления продуктов по изобретению по сравнению с добавлением сравнительного продукта REF3 к структурообразователю по РСТ/GB 00/01228.
Пример 13
Повторяли процедуру испытаний примера 9, но в качестве структурообразователя использовали один АСВ структурообразователь REF2, к которому добавляли структурообразователь СНМЕ. Результаты обобщены в табл.14.
Мелкие кристаллы на поверхности после 8 суток при 37°С.
Мелкие игольчатые кристаллы во всем геле после 9 суток при 37°С.
Больше игольчатых кристаллов в объеме геля и кристаллической массы на поверхности после 13 суток при 37°С.
Немного игольчатых кристаллов в объеме геля после 12 суток при 37°С
Из табл. 14 можно видеть, что добавление структурообразователей по изобретению к сравнительному структурообразователю REF2 по РСТ/GB 00/01228 улучшает резистентность структурообразователя кристаллизации во время хранения.
Пример 14
Готовили антиперспираторный суспензионный карандаш, используя не смешивающуюся с водой жидкость или смесь не смешивающихся с водой жидкостей, антиперспираторный активный агент и этерифицированную целлобиозу. Методика была следующей.
Смесь жидкостей нагревали до температуры на 5-10°С выше температуры, при которой наблюдалось растворение этерифицированной целлобиозы в предварительном испытании. Во время этого нагрева жидкость осторожно перемешивали, используя миксер Сильверсона. Добавляли этерифицированную целлобиозу и давали ей раствориться. Далее, к данному раствору добавляли рассыпчатый антиперспираторный активный агент. Затем полученной смеси давали остыть (или нагреться, если необходимо), в то же время осторожно перемешивая ее до тех пор, пока она не достигала температуры на 5-10°С выше температуры гелеобразования. На этой стадии смесь выливали в гильзы для антиперспираторных карандашей и оставляли охлаждаться без дополнительного перемешивания до тех пор, пока композиция не отверждалась.
Полученные карандаши оценивали после 24 часов пребывания при температуре окружающей среды в лаборатории, отмечали внешний вид карандаша, пенетрометром определяли твердость и проводили испытания отложения и белизны полученного отложения, используя методики, описанные здесь ниже. Результаты обобщены в табл.15.
Материалами, примененными в композициях в данном и в последующих примерах, были следующие:
(гидратированный)
Из табл.15 можно видеть, что суспензионный карандаш с подходящей твердостью и слабовидимыми отложениями может быть изготовлен при использовании сочетания целлобиозного АСВ структурообразователя по PCT/GB 00/01228 и СНМЕ структурообразователя по изобретению.
Следующие суспензионные карандаши, имеющие приемлемую твердость и слабовидимые отложения, могут быть изготовлены при замене структурообразователя, полученного в примере 1.7, или объединенной массы REF1 плюс структурообразователь примера 1.1 в вышеприведенной рецептуре, или, аналогично, структурообразователя примеров 2.1-2.5 в сочетании с REF4 вместо REF1, структурообразователем, полученным в каждом из примеров от 1.1 до 1.6 или от 1.8 до 1.11.
Пример 15
В данном примере были изготовлены другие антиперспираторные карандаши по способу примера 14 для приготовления карандашей, содержащих различные жидкости-носители из СНМЕ эфиров, полученных в описанном ранее примере, одних или со сравнительным структурообразователем REF4, как представлено в табл.16. Твердость представляет твердость по пенетрометру, а отложение представляет измеренное отложение на черной шерсти спустя 24 часа.
Пример 16
В данном примере готовили эмульсионный карандаш смешением циклометикона с другими органическими жидкостями, включающими сополиол цетилдиметикона, который действует как эмульгатор (силиконовый сурфактант), и смесь нагревали при осторожном перемешивании до температуры на 5-10°С выше той температуры, при которой наблюдалось растворение структурообразователя. Затем добавляли этерифицированную целлобиозу и давали ей раствориться.
Дисперсной фазой (называемой также внутренней фазой) являлся алюминий-циркониевый активный агент, растворенный в воде или в смеси полиола и воды. Эту дисперсную фазу предварительно нагревали до такой же температуры, как у органического масла, содержащего этерифицированную целлобиозу, и медленно добавляли к нему в течение одной минуты при перемешивании миксером Сильверсона. После того как добавление завершилось, композицию перемешивали с высокой скоростью в течение пяти минут. Затем скорость перемешивания уменьшали на одну минуту дополнительно, после чего смесь выливали в гильзы для карандашей и давали остыть без перемешивания до температуры окружающей среды в лаборатории. Карандаши испытывали пенетрометром и на белизну отложения, в каждом случае по методикам испытаний, приведенным ранее. Результаты обобщены в табл.17.
Из табл.17 можно видеть, что эмульсионный карандаш, изготовленный в соответствии с примером 11, имеет приемлемую твердость и особенно малые видимые отложения и имеет высокую визуальную прозрачность.
Другие эмульсионные карандаши, имеющие приемлемую твердость и малые видимые отложения, были изготовлены при замене структурообразователя, изготовленного по примеру 1.10, структурообразователем, изготовленным в каждом из примеров от 1.1 до 1.9 или 1.11, или от 2.1 до 2.5, или заменой до 90% от массы структурообразователя на REF1, или REF2, или REF4, описанные здесь выше.
Пример 17
В данном примере по способу примера 16 были приготовлены другие эмульсионные карандаши, состав которых, округленный до первого знака после запятой, и свойства приведены в табл.18. Для многих из карандашей определяли также характеристики плавления и кристаллизационную стабильность, и результаты приведены в табл.20. Описание всех кристаллов, видимых при интенсивном источнике света, относится к указанному периоду, в течение которого карандаш был полупрозрачным.
Сравнительные композиции
Сравнительные композиции с дефицитом СНМЕ эфирного структурообразователя готовили таким же образом, как композиции примера 17. Их состав и некоторые из их свойств приведены в табл.19 и 20.
Мягкий и текучий при 50оС.
Полностью плавится при 55°С.
Полностью плавится при 55°С.
Полностью плавится при 53оС.
Полностью плавится при 55°С.
Полностью плавится при 56°С.
Немного жидкий на верхушке при 55°С, но сохраняет свою первоначальную форму.
Немного жидкий на верхушке при 55°С, но сохраняет свою первоначальную форму.
Мягкий и слабо текучий при 45°С.
Полностью плавится при 50°С.
Полностью плавится при 50оС.
Мягкий и текучий при 47°С.
Полностью плавится при 49°С.
Полностью плавится при 49°С.
Сравнение композиций примера 17 и сравнительного примера 17С показывает, что сравнительная композиция плавилась при более низкой температуре и становилась непрозрачной и пестрой во время периодов хранения, при которых композиции по изобретению еще оставались прозрачными, демонстрируя тем самым превосходную стабильность композиций по изобретению. Испытание кристаллизации не выявило максимального времени, в течение которого композиции по изобретению могут оставаться полупрозрачными, поскольку ни в одном случае оно не продолжалось до тех пор, когда карандаш по изобретению становился непрозрачным.
Определение свойств
i) Твердость карандаша по пенетрометру
Твердость и жесткость композиции, которая является прочным твердым веществом, может быть определена пенетрометрией. Если композиция является более мягким твердым веществом, это должно проявиться в существенном отсутствии какой-либо резистентности щупу пенетрометра.
Подходящей методикой является использование лабораторного пенетрометра PNF, оборудованного иглой Seta wax (масса 2,5 г), которая имеет конический угол на конце иглы 9°10"±15". Использовали образец композиции с плоской верхней поверхностью. Иглу опускают на поверхность композиции и затем проводят испытание твердости, позволяя игле с ее держателем упасть под силой суммарного веса (т.е. объединенного веса иглы и держателя) в 50 г за период времени пять секунд, после чего отмечают глубину пенетрации. Желательно проводить испытание в ряде точек каждого образца и усреднять результаты. При использовании испытания такого типа приемлемой для применения в распределительном контейнере с открытым концом является пенетрация при таком испытании менее чем 30 мм, например, в интервале от 2 до 30 мм. Предпочтительно пенетрация находится в интервале от 5 мм до 20 мм.
В конкретном протоколе для таких испытаний измерения для карандаша проводили в гильзе карандаша. Карандаш выдвигали так, чтобы он выходил с открытого конца гильзы, и затем обрезали его, оставляя плоскую однородную поверхность. Иглу осторожно опускали на поверхность карандаша и затем проводили определение пенетрационной твердости. Такой процесс проводили в шести различных точках на поверхности карандаша. Приведенное значение твердости является средним значением для 6 измерений.
ii) Отложение и белизна отложения
Другим испытанием свойств композиции являлось количество композиции, которое откладывалось на поверхности, когда композицией проводили по этой поверхности (представляя нанесение продукта карандаша на кожу человека). Для проведения такого испытания на отложение образец композиции с стандартизированными формой и размером вставляли в прибор, который проводил образцом по испытательной поверхности в стандартизированных условиях. Количество продукта, перенесенное на поверхность, определяли как увеличение массы подложки, на которую его наносили. Если требовалось, впоследствии можно было определить цвет, непрозрачность или прозрачность отложения.
При использованной процедуре для таких испытаний использовали прибор для нанесения отложений с карандаша на подложку в стандартизированных условиях и затем измеряли средний уровень белизны отложения, используя анализ изображений.
Использованной подложкой являлась полоса 12×28 см черной шерстяной ткани Worsted.
Подложки перед использованием взвешивали. Карандаши ранее не использовались, и поверхность верхнего купола была неизмененной.
Прибор включал плоское основание, на котором плоская подложка крепилась зажимами на каждом конце. Стойку, имевшую седло для вставки гильзы карандаша стандартного размера, устанавливали на консоли, которая двигалась горизонтально поперек подложки посредством пневматического поршня.
Каждый карандаш выдерживали при температуре окружающей лаборатории в течение ночи перед тем, как проводили измерение. Карандаш выдвигали из гильзы на заданную величину. Затем гильзу помещали в прибор и устанавливали пружину, чтобы карандаш воздействовал на подложки со стандартизированной силой. При работе прибора карандаш проходил поперек подложки восемь раз. Подложку осторожно удаляли со стенда и заново взвешивали.
Белизна отложений
Отложения от предыдущего испытания оценивали по их белизне спустя приблизительно 24 часа.
Это осуществляли, используя монохромную видеокамеру Sony XC77 с линзой Cosmicar с фокусным расстоянием 16 мм, установленную вертикально над черным столом, освещенным под большим углом с использованием флюоресцентных трубок для исключения образования теней. Аппаратуру вначале калибровали, используя в качестве стандарта серую карту, после чего флюоресцентные трубки поворачивали до тех пор, пока не получали стабильный выход света. Ткань с отложением на ней от предыдущего испытания помещали на стол и использовали камеру для получения изображения. Выбирали зону изображения отложения и анализировали, используя анализатор изображений Kontron IBAS. Прибор мысленно делил изображение на большой набор элементов и определял уровень серого цвета каждого элемента по шкале от 0 (черный) до 255 (белый). Рассчитывали среднюю интенсивность серости. Она являлась мерой белизны отложения, причем большие числа указывали на более белое отложение. Предполагалось, что более низкие числа указывают на прозрачное отложение, позволяющее видеть цвет подложки.
iii) Плавление карандаша
Испытуемый карандаш в его обычном контейнере с открытым концом помещали в камеру с постоянной температурой, которую поддерживали в течение цикла в 48 часов, чтобы дать возможность проявиться всем изменениям условий. Температуру поднимали с инкрементом 2°С или 5°С перед каждым последующим циклом. Карандаш обследовали в конце каждого цикла и определяли температуру, при которой становились заметными изменения внешнего вида.
iv) Кристаллизационная стабильность при 45°С
В испытании для определения стабильности структурированных эфиром антиперспираторных карандашей при повышенной температуре испытуемый карандаш помещали в камеру с постоянной температурой, которую поддерживали при 45°С. Карандаши осматривали каждую неделю, чтобы определить, остались ли они еще полупрозрачными или их внешний вид изменился. Карандаши освещали интенсивным светом и проводили визуальную проверку того, видны ли какие-либо кристаллы или домены. В нескольких случаях испытание карандашей останавливали, если они еще были полупрозрачными, когда сравнительный карандаш становился непрозрачным, или вскоре после этого.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИПЕРСПИРАНТНАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2242966C2 |
| КОСМЕТИЧЕСКИЕ КОМПОЗИЦИИ | 2000 |
|
RU2247553C2 |
| АЦИЛИРОВАННЫЕ ОРГАНИЧЕСКИЕ ОЛИГОМЕРЫ ГЛИЦЕРИНА | 2014 |
|
RU2658830C2 |
| КОМПОЗИЦИИ КОСМЕТИЧЕСКИХ КАРАНДАШЕЙ | 2004 |
|
RU2329784C2 |
| АНТИПЕРСПИРАНТНЫЕ ИЛИ ДЕЗОДОРИРУЮЩИЕ КОМПОЗИЦИИ | 2006 |
|
RU2424789C2 |
| СТАБИЛИЗИРОВАННЫЕ ПО ОТНОШЕНИЮ К ПРОТЕАЗАМ АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 2009 |
|
RU2571857C2 |
| АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 1995 |
|
RU2160118C2 |
| НОВЫЕ АЦИЛИРОВАННЫЕ ПСЕВДОДИПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1999 |
|
RU2223262C2 |
| КОМПОЗИЦИИ ДЛЯ МЕСТНОГО НАНЕСЕНИЯ, СОДЕРЖАЩИЕ N-АЦИЛ-ДИПЕПТИДНЫЕ ПРОИЗВОДНЫЕ И ГЛИКОЛЕВУЮ КИСЛОТУ | 2020 |
|
RU2822387C2 |
| АЦИЛИРОВАННЫЕ АМИНОАЛКИЛИМИДАЗОЛЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2152933C2 |
Изобретение относится к новой смеси ацилированной целлобиозы общей формулы (I), которая может быть использована для загущения или структурирования не смешивающейся с водой жидкости, к способу ее получения, к косметической композиции на ее основе, к применению косметической композиции для нанесения на кожу и к способу загущения или структурирования не смешивающейся с водой жидкости.
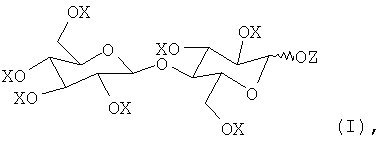
где Х представляет ацильную группу (R-CO-) или Н, Z представляет ацильную группу (R'-CO-) или Н, и, по меньшей мере, 50% радикалов Z ацилированы и в среднем более чем 6 радикалов X+Z ацилированы, где R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода, и R' представляет радикал, отличный от R и который представляет собой: (i) углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 1 до 31 атомов углерода, необязательно замещенный фтором, аминогруппой, амидогруппой, фенильной группой, нафтильной группой, бифенильной группой, циклогексильной или циклооктильной группой, или (ii) ароматический углеводородный радикал, содержащий не более 26 атомов углерода, включающий фенильную, нафтильную или бифенильную группу, необязательно замещенную алкильной или алкоксигруппой, содержащей до 20 атомов углерода, или галогеном, или нитрогруппой, или группой сложноалкильного эфира алкиламина или алкиламида, или (iii) циклоалифатический углеводород, включающий циклогексильную или циклооктильную группу, необязательно замещенный алкильной или алкоксигруппой, содержащей до 20 атомов углерода, или фенильной, нафтильной или бифенильной группой. 5 н. и 44 з. п. ф-лы, 20 табл.
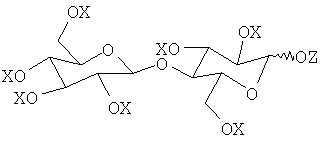
в которой Х представляет ацильную группу (R-CO-) или Н; Z представляет ацильную группу (R'-CO-) или Н, и, по меньшей мере, 50% радикалов Z ацилированы и в среднем более чем 6 радикалов X+Z ацилированы, где R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода, и
R' представляет радикал, отличный от R и который представляет собой:
(i) углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 1 до 31 атомов углерода, необязательно замещенный фтором, аминогруппой, амидогруппой, фенильной группой, нафтильной группой, бифенильной группой, циклогексильной или циклооктильной группой, или
(ii) ароматический углеводородный радикал, содержащий не более 26 атомов углерода, включающий фенильную, нафтильную или бифенильную группу, необязательно замещенную алкильной или алкоксигруппой, содержащей до 20 атомов углерода или галогеном, или нитрогруппой, или группой сложноалкильного эфира алкиламина или алкиламида, или
(iii) циклоалифатический углеводород, включающий циклогексильную или циклооктильную группу, необязательно замещенный алкильной или алкоксигруппой, содержащей до 20 атомов углерода, или фенильной, нафтильной или бифенильной группой, полученная взаимодействием частично деацилированной целлобиозы общей формулы 2
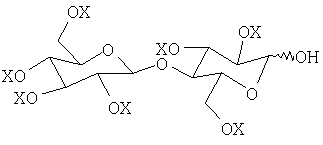
с избытком более молярного количества ацилирующего агента, включающего карбоновую кислоту, хлорангидрид карбоновой кислоты, ангидрид карбоновой кислоты, содержащего радикал R'-CO-, при повышенной температуре, по меньшей мере, 80°С, и, предпочтительно, при температуре 10°С или в интервале 10°С - температура кипения смеси, и, в случае необходимости, в присутствии катализатора, до тех пор, пока, по меньшей мере, 50% -ОН групп на аномерном атоме углерода целлобиозы будет ацилировано.

в которой Х представляет ацильную группу (R-CO-) или Н; Z представляет ацильную группу (R'-CO-) или Н, и, по меньшей мере, 50% радикалов Z ацилированы и в среднем более чем 6 радикалов X+Z ацилированы, где R представляет углеводородный радикал с насыщенной или ненасыщенной, линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода,
включающий стадию взаимодействия соответствующей частично деацилированной целлобиозы, имеющей общую формулу 2

в которой Х и R определены в п.1,
с избытком более молярного количества ацилирующего агента, содержащего радикал R'-CO-, где R' определен в п.1, при повышенной температуре, по меньшей мере, 80°С, и, предпочтительно, при температуре 10°С или в интервале 10°С - температура кипения смеси, и, в случае необходимости, в присутствии катализатора, до тех пор, пока, по меньшей мере, 50% -ОН групп на аномерном атоме углерода целлобиозы будет ацилировано.
на первой стадии путем взаимодействия целлобиозы с избытком более 8 моль ацилирующего агента, выбранного из хлорангидрида формулы RCOCl, или карбоновой кислоты формулы RCOOH, или ангидрида формулы (RCO)2O на 1 моль целлобиозы и
на второй стадии путем, по меньшей мере, частичного деацилирования продукта, полученного на первой стадии, по аномерному атому углерода целлобиозы путем взаимодействия продукта первой стадии при концентрации от 4 до 15 мас.% в тетрагидрофуране с, по меньшей мере, эквимолярным количеством C1-C4 алифатической кислоты и с небольшим молярным избытком, по меньшей мере, 1,6:1 алкилендиамина при температуре от 20 до 30°С.
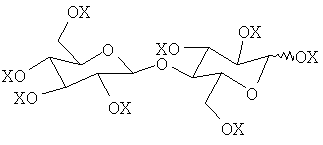
в которой, по крайней мере, 50% Х представляют ацильную группу (R-CO-) и остальные Х представляют Н и R представляет насыщенный или ненасыщенный углеводородный радикал с линейной или разветвленной цепью, содержащий от 5 до 31 атомов углерода.
| Способ получения поверхностно активного вещества | 1975 |
|
SU906383A3 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| N | |||
| IDE et al, Gelation of Fully Acylated Cellobiose in Alkane Solution, Bull | |||
| Chem | |||
| Soc | |||
| Jpn., 1995, vol.68, pp.3423-3428 | |||
| P | |||
| TERECH et al, Low Molecular Mass Gelators of Organic Liquids and the Properties of Their Gels | |||
| Chem | |||
| Rev., 1997, vol.97, pp.3133-3159. | |||
Авторы
Даты
2007-03-20—Публикация
2001-09-18—Подача