Изобретение относится к области химической технологии кремнийорганических соединений и может найти промышленное применение при получении модификаторов, в частности термостабилизаторов, различных полимеров. Более конкретно изобретение относится к новым функциональным металлосилоксанам и к способу их получения.
Использование металлов, в частности солей органических кислот, в качестве термостабилизирующих добавок к полимерным композициям, в частности к органосилоксановым полимерам, основано на их способности ингибировать цепные свободно-радикальные процессы, протекающие при термическом окислении, дезактивируя образующиеся свободные радикалы или промежуточные продукты окисления (патент США US 3142655, 1964 г.; авт. свид. СССР №369131, 1973 г.). Однако для эффективной термостабилизации полимеров необходимо решение ряда проблем, как, например, возможность гомогенного введения добавки, отсутствие ее летучести при высоких температурах, доведение диспергирования стабилизирующих добавок до нано-размеров, в том числе в резиновых смесях, и др.
Добавление органических солей ряда металлов к полимерным композициям в качестве термостабилизирующих добавок известно (см. например, патенты США US 4193885, 1980, US 4528313, 1985). В описаниях к патентам рассмотрен достаточно широкий спектр металлов. Однако плохая совместимость таких соединений и полимерных матриц и проблемы их диспергирования в полимере значительно понижает их эффективность и усложняет процесс введения добавок.
Известны термостойкие и частично функциональные металлосилоксановые соединения, полученные взаимодействием 1,4-триметилсилоксибензола и гидрооксида натрия, с последующим обменом натрия на алюминий, цинк и кальций (J. Chem. Soc., Dalton trans., 1999, p.4535-4540). Эти соединения обладают плохой растворимостью, содержат остатки воды и их структура не детерминирована.
Описано взаимодействие двухлористой меди и фенилсиланолов в присутствии гидроокиси натрия и металлического натрия, в результате которого получают фенилмедьнатрийсилоксан. Аналогично был получен и никельсодержащий металлосилоксан (Металлоорган. Химия, 1991, 4, 74; ДАН СССР, т.325, №6, 1992; Eur. J. Inorg. Chem. 2004, 1253-1261). Другие радикалы у атомов кремния, а также другие металлы не рассматривались. Полученные соединения не исследовались на предмет их термостабилизирующего влияния в полимерных смесях. Недостатками данного процесса является использование в процессе металлического натрия, а также содержание воды и спиртов в составе этих соединений усложняют их использование на следующих стадиях.
Наиболее близким по строению к заявляемым функциональным металлосилоксановым соединениям и к способу их получения является диэтоксиалюмоэтилсиликат, полученный взаимодействием диалкоксиалюминий бромида и калийокситриэтоксисилана (ЖОХ, 1995, т.65, вып.4, с.612-615). Полученное соединение содержит наряду с металлом и функциональные группы у атома кремния, позволяющие осуществлять дальнейшие превращения. Недостатком является отсутствие органических радикалов у атомов кремния, что делает данное соединение практически неорганическим и вводит ограничения по совместимости таких соединений и полимерных матриц. Кроме того, предложенный способ не является универсальным, он осуществлен только с участием алюминийсодержащих соединений, введение других металлов не изучалось. Использование синтезированного соединения в качестве термостабилизирующей добавки к полимерным композициям не описано.
Задачей заявляемого изобретения являлось получение нового технического результата, заключающегося в создании новых функциональных металлосилоксанов, обладающих набором свойств, необходимых для их эффективного использования в качестве термостабилизирующих добавок: содержать в своей структуре определенное количество атомов соответствующего металла, обладать хорошей растворимостью в органических растворителях и хорошей совместимостью с полимерной матрицей, содержать в своем составе функциональные группы, способные к взаимодействию с компонентами полимерной композиции, в состав которой они будут вводиться.
Кроме того, задачей изобретения являлась разработка нового способа получения заявленных функциональных металлосилоксанов в приемлемых условиях, дающих высокий выход продукта заданного строения и пригодного к применению и в промышленных условиях.
Задача решается тем, что получены металлосилоксаны общей формулы (I),

где М двух- или трехвалентный металл из ряда: Zr, Zn, Fe(II), Fe(III), Ce, Cu, Cr, Sm, Eu, а значение m соответствует валентности металла;
Alk означает заместитель CH3- или C2H5-;
R' означает заместитель CH3- или C6H5- или NH2(CH2)3-;
R" означает заместитель СН2=СН-;
n равно 0 или 1.
В частности, М может означать двухвалентный металл из ряда Zr, Zn, Fe(II), Cu, а n может быть 0 или 1.
В частности, М может означать трехвалентный металл из ряда Fe(III), Се, Cr, Sm, Eu. При этом n также может быть 0 или 1.
Как в случае двухвалентного металла, так и в случае трехвалентного металла Alk может означать CH3- или C2H5-, R' может означать CH3- или C6H5- или NH2(CH2)3-. В частности, в случаях, когда n равно 0, R" означает заместитель CH2=CH-.
Функциональные металлосилоксаны получены путем взаимодействия натрийокси(алкокси)органосилана общей формулы (II)
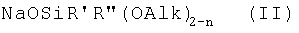
где R', R", Alk, n имеют вышеуказанные значения, с солями металлов общей формулы (III),
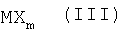 ,
,
где М и m имеют вышеуказанные значения,
а Х означает Cl или Br или CH3COO- по общей схеме:
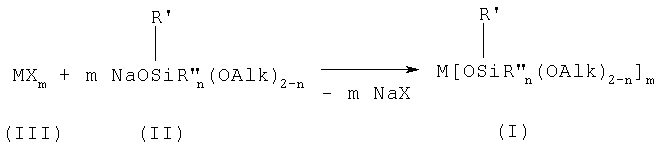
Функциональные металлосилоксаны предназначены для использования в качестве термостабилизирующих добавок в полимерных композициях.
В отличие от известного диэтоксиалюмоэтилсиликата заявленные функциональные металлосилоксаны содержат различные органические заместители у атомов кремния, а также различные атомы металлов. Это позволяет значительно улучшить совместимость таких соединений и полимерных композиций различных типов, включая лаки и жидкости, получать различные модификации этих соединений с использованием функциональных групп, а также варьированием типа металла улучшать их термостабилизирующее действие при введении в полимер.
Задача решается также тем, что разработан способ получения новых функциональных металлосилоксанов общей формулы (I), заключающийся в том, что осуществляют взаимодействие натрийокси(алкокси)органосилана общей формулы (II)
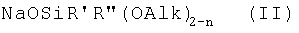
где R', R", Alk, n имеют вышеуказанные значения,
с солями металлов общей формулы (III),
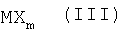 ,
,
где М и m имеют вышеуказанные значения,
а Х означает Cl или Br или CH3COO-.
Общая схема процесса может быть представлена следующим образом:
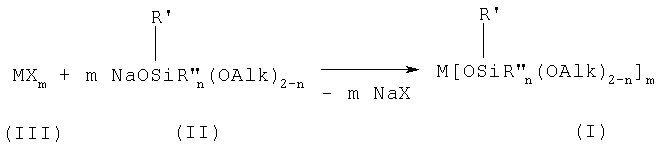
где R', R", Alk, n, X, M и m имеют вышеуказанные значения.
В частности процесс взаимодействия натрийокси(алкокси)органосилана с солью металла можно осуществлять одновременно с процессом образования натрийокси(алкокси)органосилана из гидроксида натрия и алкоксиорганосилана, выбранного из ряда алкоксиорганосиланов общей формулы (V),
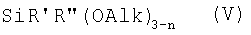 ,
,
где R', R", Alk, n имеют вышеуказанные значения.
В данном случае процесс осуществляют без выделения натрийокси(алкокси)органосилана и металлосилоксан получают в одну стадию по следующей общей схеме:
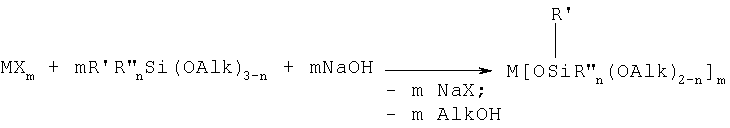
В обоих случаях процесс взаимодействия компонентов можно проводить в среде органического растворителя, выбранного из ряда эфиров: тетрагидрофуран, диоксан, дибутиловый эфир, диметиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля, или из ряда низших спиртов: метанол, этанол, пропанол. При этом взаимодействие исходных компонентов предпочтительно проводят при температуре в пределах от минус 5° до 50°С, при их стехиометрическом мольном соотношении и в течение времени, необходимого для полной конверсии соли металла.
В частности соль металла может быть выбрана из ряда солей металлов общей формулы (III), где М означает двухвалентный металл из ряда: Zr, Zn, Fe(II), Cu, или соль металла может быть выбрана из ряда солей металлов общей формулы (III), где М означает трехвалентный металл из ряда: Fe(III), Се, Cr, Sm, Eu.
В частности, в случае когда М равно двухвалентному металлу, общая схема процесса может быть представлена следующим образом:
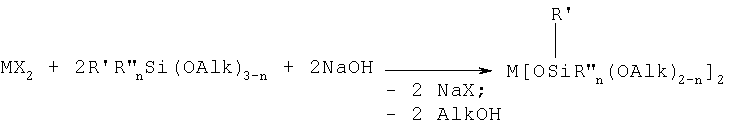
В данном случае, когда M равно Cu+2, при R' равно CH3-, R" равно CH2=CH-, n равно 0, реакция получения имеет следующий вид:
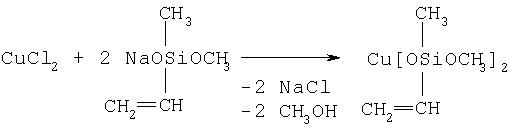
В частности, в случае когда М равно трехвалентному металлу, общая схема процесса может быть представлена следующим образом:
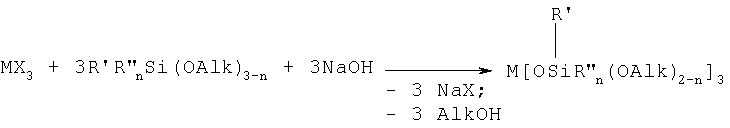
В случае, когда M равно Fe+3, R' равно CH3-; Alk равно C2H5-, n равно 0, процесс может быть представлен следующей схемой:
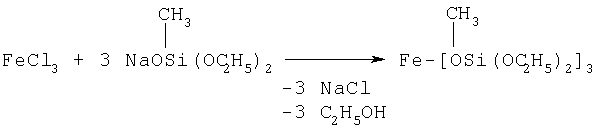
Полученное соединение имеет следующую структуру:
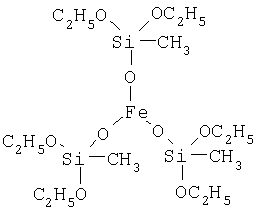
В частности, в качестве натрийокси(алкокси)органосилана можно использовать натрийоксиметилдиэтоксисилан, а в качестве соли металла - хлорид железа (III).
В частности, в качестве алкоксиорганосилана можно использовать метилвинилдиэтоксисилан или метилвинилдиэтоксисилан, а в качестве соли металла - хлорид железа (III) или хлорид циркония соответственно.
Полученные согласно заявленному способу функциональные металлосилоксаны предназначены для получения методом гидролитической поликонденсацией функциональных полиметаллосилоксанов статистического циклолинейного строения.
Структуру синтезированных соединений доказывали данными элементного анализа, ЯМР и ИК-спектроскопии, хроматографическими методами анализа.
По данным ГПХ синтезированные функциональные металлосилоксаны обладают мономодальным распределением по молекулярному весу (см. Фиг.1). По данным ГПХ, полученным с использованием линейных полистирольных стандартов, молекулярные массы металлосилоксанов соответствуют ˜200 (см. фиг.1).
Заявленные соединения имеют структуру, оптимальную для введения в состав силоксановых полимерных композиций, благодаря своей полимерной природе и наличию функциональных групп. В отличие от известных соединений (мономерных, плохо совместимых с полимерами, либо дорогостоящих полимерных и не обладающих функциональными группами) их использование позволяет проводить полимераналогичные превращения с целью дальнейшего улучшения совместимости с определенными полимерными композициями. Наличие в их структуре химически связанных атомов переходных металлов позволяет, в частности, использовать данные соединения как эффективные термостабилизирующие добавки.
Исследование термодеструкции самих функциональных металлосилоксанов показало, что их термо- и термоокислительная деструкция не сопровождается разрушением молекулярного скелета и образования осколков.
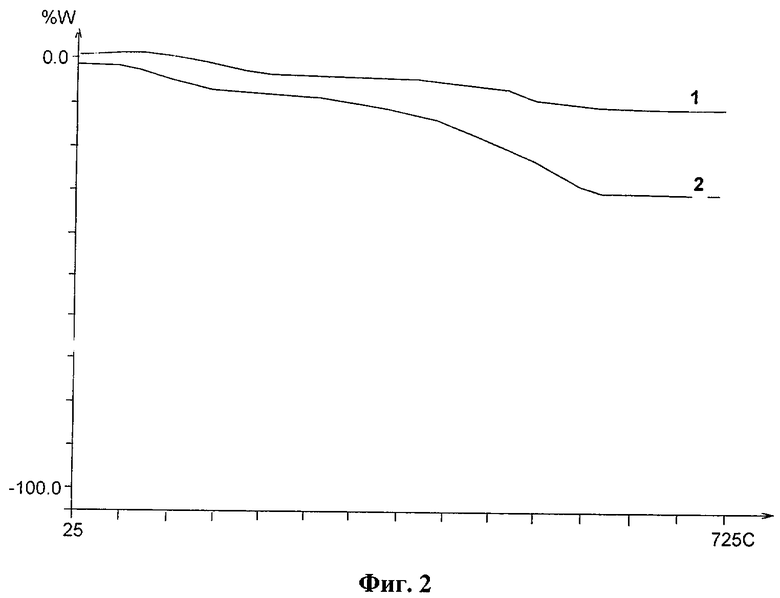
На Фиг.2 приведены кривые ТТА железовинилсилоксанового олигомера на воздухе и в инертной среде. Из приведенных данных видно, что потери массы начинаются довольно рано (следствие высокой концентрации концевых групп) - суммарные потери в аргоне меньше 10%, а на воздухе около 25%, что существенно меньше реальной органической составляющей металлосилоксана.
Исследование термостабилизации полимера в присутствии синтезированных металлосилоксановых добавок проводили методом ДТА (методика приведена после примеров). В качестве полимера термостабилизируемого полимера использовали метилсилсесквиоксановую смолу. Введение металлосилоксановых добавок в состав смолы осуществляли путем совместного растворения. Полученные результаты ДТА испытаний, приведенные в таблице, показывают, что активность полученных добавок в качестве термостабилизаторов высока. В качестве сравнительного примера в таблице приведены параметры для силсесквиокановой смолы без добавления металлосилоксанов.
Во всех случаях количество вводимой добавки составляло 2-3% в расчете на чистый металл. Как видно из приведенных данных, во всех случаях наблюдается эффект стабилизации, так, температура 10%-ных потерь при введение метилэтоксижелезосилоксана смещается на 90°С, а в случае аминопропилэтоксицерийсилоксана - более чем на 120°С в сторону высоких температур. Содержание коксового остатка не изменяется, однако положение максимума на кривой ДТА смещается в случае первой добавки почти на 180°С, а в случае церийсодержащего модификатора - на 140°С. Менее эффективным оказался аминопропилэтоксижелезосилоксан, но и в этом случае свойства композиции выше, чем в сравнительной системе.
Таким образом, первые серии испытаний подтвердили перспективность использования функциональных металлосилоксанов в качестве термостабилизаторов.
На Фиг.1 представлена ГПХ кривая железосодержащего метилдиэтоксисилоксана.
На Фиг.2 представлены кривые ТГА железометилвинилэтоксисилоксанасилоксана, где кривая 1 - нагрев в среде аргона, 2 - нагрев на воздухе (скорость нагрева 5°С/мин).
В таблице приведены данные ДТА метилсилсесквиоксановой смолы в присутствии металлосилоксанов как термостабилизирующих добавок по примерам 1, 3 и 7. Как сравнительный пример приведены данные ДТА чистой метилсилсесквиоксановой смолы.
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. Синтез железосодержащего этоксифункционального метилсилоксана.
К 4,45 г (0,0274 моль) хлорида железа (III) в 200 мл ТГФ прикапывают раствор (0,0822 моль) натрийоксиметилдиэтоксисилана в 70 мл ТГФ при температуре +5°С. Реакционную смесь перемешивают при 50°С 28 часов. Осадок хлористого натрия отфильтровывают, удаляют летучие в вакууме. Выход продукта 68%. По данным элементного анализа найдено: Fe 9,39%; Si 17,41%; С 36,28%; Н 8,02%. Вычислено: Fe 11,09%; Si 16,74%; С 35,8%; Н 7,75%.
Пример 2. Синтез самарийсодержащего этоксифункционального метилсилоксана:
Смешивают 7,036 г (0,0274 моль) хлорида самария, 14,64 г (0,0822 моля) метилтриэтоксисилана и 3,29 г (0,0822 моль) гидроксида натрия в 200 мл ТГФ, при температуре 0°С, в среде инертного газа. Реакционную смесь перемешивают 4 часа при комнатной температуре. Осадок хлористого натрия отфильтровывают, удаляют этиловый спирт и избыток метилтриэтоксисилана в вакууме масляного насоса. Выход продукта 79%. ГПХ: мономодальное распределение Мр=200 по полистирольным стандартам). По данным элементного анализа найдено: Sm 24,52%; Si 14,46%; С 43,03%; Н 6,99%. Вычислено: Sm 25,11%; Si 14,06%; С 42,19%; Н 6,53%.
Пример 3. Синтез церийсодержащего этоксифункционального метилсилоксана:
Синтез осуществляют по методике, описанной в примере 2, но вместо хлорида самария используют хлорид церия в эквимольном количестве, вместо ТГФ берут метанол. Выход продукта 73%. ГПХ: мономодальное распределение Мр=200 (по полистирольным стандартам). ЯМР-1Н спектр в CDCI3: δ=0,13 м.д. (м. 9Н, SiCH3), δ=1,21 м.д. (т.18 Н, CH2CH3), δ=3,79 м.д. (к. 12Н, OCH2).
Пример 4. Синтез цинксодержащего метоксифункционального фенилсилоксана:
Синтез осуществляют по методике, описанной в примере 2, но вместо хлорида самария используют хлорид цинка и вместо метилтриэтоксисилана используют фенилтриметоксисилан. Выход продукта 81%. ГПХ: мономодальное распределение Мр˜200 (по полистирольным стандартам). ЯМР-1Н спектр в CDCL3: δ=3,47 м.д. (м. 6Н, OCH3); δ=7,2 м.д. (м. 5Н, C6H5). Элементный анализ: найдено, %: Si 11,95; Zn 14,84; С 39,06; Н 4,87. Вычислено, %: Si 12,99; Zn 15,16; С 38,94; Н 5,09
Пример 5. Синтез железосодержащего этоксифункционального метилвинилсилоксана:
Синтез осуществляют по методике, описанной в примере 2, но вместо хлорида самария используют хлорид железа (III), вместо метилтриэтоксисилана используют метилвинилдиэтоксисилан, все в эквимольном количестве. Выход продукта 82,2%. ГПХ: мономодальное распределение Мр=200 (по полистирольным стандартам). ЯМР-1Н спектр в CDCl3: δ=0,15 м.д. (с. 9Н); δ=1,2 м.д. (м. 9Н); δ=3,71 м.д. (м. 6Н); δ=5,92 м.д. (м. 9Н). Элементный анализ: найдено, %: Si 22,68; Fe 13,39; С 29,76; Н 5,71. Вычислено, %: Si 18,75; Fe 12,46; С 40,06; Н 7,35.
Пример 6. Синтез цирконийсодержащего метоксифункционального силоксана:
Синтез осуществляют по методике, описанной в примере 2, но вместо хлорида самария используют хлорид циркония, вместо метилтриэтоксисилана используют метилвинилдиэтоксисилан, все в эквимольном количестве. Выход продукта 89,5%. ГПХ: мономодальное распределение Мр=200 (по полистирольным стандартам). ЯМР-1Н спектр в CDCl3: δ=0,15 м.д. (с. 9Н); δ=1,2 м.д. (м. 9Н); δ=3,71 м.д. (м. 6Н); δ=5,92 м.д. (м. 9Н). Элементный анализ: найдено, %: Si 17,66; Zr 27,79; С 14,66; Н 5,71. Вычислено, %: Si 17,20; Zr 28,04; С 14,76; Н 5,5.
Пример 7. Синтез железосодержащего γ-аминопропилдиэтоксисилоксана:
При перемешивании, в токе аргона, смешивают 1.62 г (0,010 моль) хлорида железа (III), 4,43 г (0,020 моль) γ-аминопропилтриэтоксисилана, 0,8 г (0,020 моль) гидроксида натрия в 50 мл метил-трет-бутилового эфира. Реакцию проводят 2 суток при комнатной температуре. Осадок хлористого натрия отфильтровывают, удаляют летучие соединения в вакууме масляного насоса. ГПХ: Мр˜200. ЯМР-1Н в CDCI3: δ=0,6 м.д. (м. 4Н, SiCH2), δ=0,84 м.д. (д. 4Н, NH2), δ=1,22 м.д. (м. 6Н, CH2CH3), δ=1,67 м.д. (ушир с. 4Н, CH2), δ=3,33 м.д. (к. 2Н, CH2NH2), δ=3,8 м.д. (м. 4Н, CH2O).
Пример 8. Синтез хромсодержащего метоксифункционального силоксана:
Синтез осуществляют по методике, описанной в примере 2, но вместо хлорида самария используют хлорид хрома, вместо метилтриэтоксисилана используют метилвинилдиэтоксисилан, все в эквимольном количестве. Выход продукта 75,3%. ГПХ: мономодальное распределение Мр=200 (по полистирольным стандартам). ЯМР-1Н спектр в CDCl3: δ=0,15 м.д. (с. 9Н); δ=1,2 м.д. (м. 9Н); δ=3,71 м.д. (м. 6Н); δ=5,92 м.д. (м. 9Н). Элементный анализ: найдено, %: Si 20,61; Cr 12,71; С 34,96; Н 6,71. Вычислено, %: Si 20,84; Cr 12,90; С 35,73; Н 6,70.
Пример 9. Синтез поли(медь)метилвинилсилоксана:
11,9 г (0,04 моль) медьсодержащего метоксифункционального метилвинилсилоксана Cu[OSiMeVinOMe]2 растворяют в 100 мл ТГФ и добавляют при перемешивании 0,08 мл (0,004 моль) воды, в соотношении 1 моль металлосилоксана / 0.05 моль H2O. Через 10 ч перемешивания при комнатной температуре удаляют в вакууме летучие компоненты. Выход продукта 73%. ГПХ: широкое мономодальное распределение Мр˜100000 (по полистирольным стандартам). ЯМР-1Н спектр в CDCl3: δ=0,15 м.д. (с. 3Н); δ=3,71 м.д. (м. 3Н); δ=5,92 м.д. (м. 3Н).
Методика испытания термостабилизирующего действия металлосилоксанов.
Смешивают раствор 0,7 г метилсилсесквиоксановой смолы в 6,5 мл метил-трет-бутилового эфира (МТБЭ) и раствор 0,14 г трис(диэтоксиметилсилокси)железа (или другого синтезированного металлосилоксана) в 2 мл МТБЭ (1,8% Fe к массе смолы). Полученный гомогенный раствор выдерживают на воздухе в тонком слое до высыхания растворителя. Полученную однородную прозрачную пленку нагревают в вакуумном шкафу при температуре 200°С в течение 2 часов. Анализируют полученный образец методом ДТА и сравнивают с данными ДТА метилсилсесквиоксановой смолы без добавок металлосилоксанов. Результаты ряда испытаний приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФУНКЦИОНАЛЬНЫЕ ПОЛИМЕТАЛЛОСИЛОКСАНЫ | 2005 |
|
RU2293746C1 |
| ФУНКЦИОНАЛЬНЫЕ МЕТАЛЛОСИЛОКСАНЫ, ПРОДУКТЫ ИХ ЧАСТИЧНОГО ГИДРОЛИЗА И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2649392C2 |
| МЕТАЛЛОСИЛОКСАНОВЫЕ ОЛИГОМЕРЫ В КАЧЕСТВЕ ОТВЕРДИТЕЛЕЙ ЭПОКСИДНЫХ СМОЛ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2641909C1 |
| ГРЕБНЕОБРАЗНЫЕ ПОЛИМЕТИЛСИЛОКСАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2440382C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОРГАНОСИЛОКСАНОВЫХ МОЛЕКУЛЯРНЫХ ЩЕТОК | 2021 |
|
RU2783679C1 |
| ПОЛИСИЛОКСАНОВЫЕ КОМПОЗИЦИИ И ЭЛАСТОМЕРНЫЕ МАТЕРИАЛЫ С ВЫСОКОЙ ДИЭЛЕКТРИЧЕСКОЙ ПРОНИЦАЕМОСТЬЮ НА ИХ ОСНОВЕ | 2020 |
|
RU2767650C1 |
| ПОЛИНАТРИЙОКСИОРГАНОСИЛОКСАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2293743C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНЫХ ПОЛИДИМЕТИЛСИЛОКСАНОВ С КОНЦЕВЫМИ ГИДРОКСИЛЬНЫМИ ГРУППАМИ ПОЛИКОНДЕНСАЦИЕЙ ДИМЕТИЛДИАЛКОКСИСИЛАНОВ В АКТИВНОЙ СРЕДЕ | 2010 |
|
RU2456308C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИНЕЙНОГО ПОЛИМЕТИЛФЕНИЛСИЛОКСАНА С КОНЦЕВЫМИ ГИДРОКСИЛЬНЫМИ ГРУППАМИ ПОЛИКОНДЕНСАЦИЕЙ МЕТИЛФЕНИЛДИАЛКОКСИСИЛАНА В АКТИВНОЙ СРЕДЕ | 2011 |
|
RU2456307C1 |
| КОМПОЗИЦИИ ДЛЯ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ МАТЕРИАЛОВ С ЭФФЕКТОМ САМОЗАЛЕЧИВАНИЯ | 2020 |
|
RU2766219C1 |
Изобретение относится к области синтеза кремнийорганических соединений и может найти применение при получении модификаторов различных полимеров и, в частности, термостабилизаторов. Описываются новые функциональные металлосилоксаны общей формулы (I),
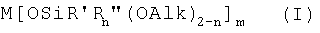 ,
,
где М означает двух- или трехвалентный металл из ряда: Zr, Zn, Fe(II), Fe(III), Ce, Cu, Cr, Sm, Eu, а значение m соответствует валентности металла; Alk означает заместитель CH3- или C6H5-; R' означает заместитель CH3- или C6H5- или NH2(CH2)3-; R" означает заместитель CH2=CH-; n равно 0 или 1, и способ получения функциональных металлосилоксанов, заключающийся в том, что осуществляют взаимодействие натрийокси(алкокси)органосилана, выбранного из ряда натрийокси(алкокси)органосиланов общей формулы (II)
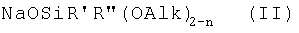 ,
,
где R', R", Alk, n имеют вышеуказанные значения, с солью металлов, выбранной из ряда солей металлов общей формулы (III), 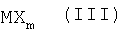 , где М, m имеют вышеуказанные значения, а Х означает Cl или Br или CH3COO-. Техническим результатом является улучшение совместимости получаемых соединений с полимерными композициями, а также варьирование типа металла позволяет улучшить их термостабилизирующие действия при введении в полимер. 2 н. и 22 з.п. ф-лы, 2 ил., 1 табл.
, где М, m имеют вышеуказанные значения, а Х означает Cl или Br или CH3COO-. Техническим результатом является улучшение совместимости получаемых соединений с полимерными композициями, а также варьирование типа металла позволяет улучшить их термостабилизирующие действия при введении в полимер. 2 н. и 22 з.п. ф-лы, 2 ил., 1 табл.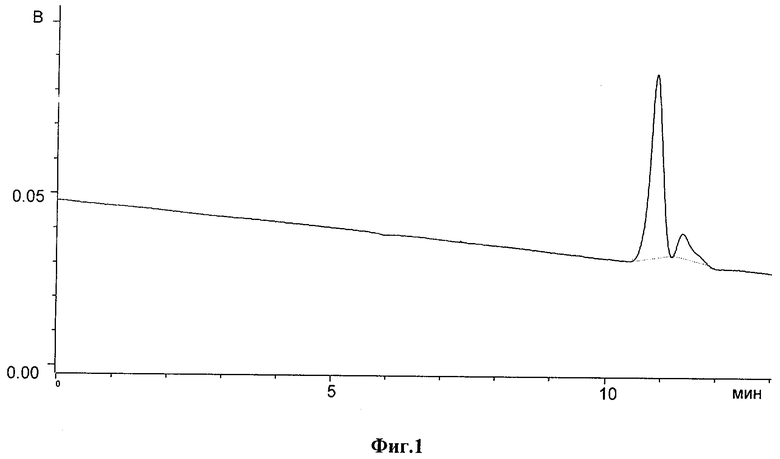
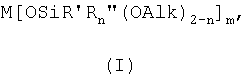
где М означает двух- или трехвалентный металл из ряда Zr, Zn, Fe(II), Fe(III), Ce, Cu, Cr, Sm, Eu, а значение m соответствует валентности металла;
Alk означает заместитель CH3- или C2H5-;
R' означает заместитель CH3- или C6H5- или NH2(CH2)3-;
R" означает заместитель СН2=СН-;
n равно 0 или 1.
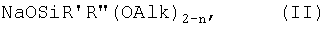
где R', R", Alk, n, M и m имеют вышеуказанные значения,
с солью металлов, выбранной из ряда солей металлов общей формулы (III)

где M, m имеют вышеуказанные значения; Х означает Cl или Br или CH2COO-.
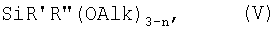
где R', R", Alk, n, имеют вышеуказанные значения.
| В.И.ЩЕРБАКОВ и др., Получение смешанных алкоксидов из алкоксипроизводных кремния и алюминия, ЖУРНАЛ ОБЩЕЙ ХИМИИ, 1995 | |||
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| US 6297302 А, 02.10.2001 | |||
| Металлокремнийорганические соединения как катализаторы хлорирования ароматических углеводородов | 1975 |
|
SU536185A1 |
Авторы
Даты
2007-04-10—Публикация
2005-12-29—Подача