Изобретение относится к области органической химии, точнее к способам получения органических соединений, содержащих в качестве гетероатомов фосфор в фосфорильной форме - N-дифенилфосфорил-N'-алкил(С6-С10)мочевин.
Изобретение может наиболее эффективно использоваться при получении экстрагентов для радиохимических производств, в том числе для выделения высокорадиоактивных элементов америция и европия. Упомянутые соединения позволяют сконцентрировать и удалять из технологических растворов наиболее радиоактивные отходы и тем самым снять сложившееся на радиохимических производствах напряжение экологического характера.
Известен способ получения N-дифенилфосфорил-N'-алкил(С3-С5)мочевин взаимодействием дифенилфосфорилизоцианата (синтезирован из циановокислого серебра и хлорангидрида дифенилфосфиновой кислоты) с соответствующими первичными аминами в растворе бензола [K.Utvary, E.Freundlinger, V.Gutmann "N-Diphenylphosphinyl-harnstoffe", Monatshefte fur Chemie, 97, №2, 348-360 (1966)]. Недостатком способа является использование для получения дифенилфосфорилизоцианата дорогостоящего циановокислого серебра.
Известен способ получения N-дифенилфосфорил-N'-алкил(С6-С10)мочевин, который выбран нами в качестве прототипа [В.П.Моргалюк, А.М.Сафиулина, И.Г.Тананаев, Е.И.Горюнов, И.Б.Горюнова, Г.Н.Молчанова, Т.В.Баулина, Э.Е.Нифантьев, Б.Ф.Мясоедов "N-Дифенилфосфорил-N'-алкилмочевины - новый тип экстрагентов для концентрирования актиноидов", Доклады АН, 403, №2, 201-204 (2005)]. Он включает в себя две индивидуальные стадии. Первая стадия представляет собой взаимодействие хлорангидрида дифенилфосфиновой кислоты с циановокислым натрием в присутствии каталитических количеств безводного хлорида магния в ацетонитриле при кипячении реакционной смеси (80-85°С) с последующим выделением образующегося дифенилфосфорилизоцианата перегонкой в вакууме, вторая стадия представляет собой взаимодействие полученного изоцианата с первичными алкил(С6-С10)аминами в растворе бензола при температуре 20-25°С с последующим выделением N-дифенилфосфорил-N'-алкилмочевин обычным способом.
Недостатком известного способа является то, что его первая стадия требует очистки полученного продукта высоковакуумной перегонкой, что затрудняет синтез в укрупненных масштабах. Кроме этого, исходное вещество первой стадии (хлорангидрид дифенилфосфиновой кислоты) является дорогим продуктом и в промышленном масштабе не производится.
Задача изобретения заключается в разработке нового способа получения N-дифенилфосфорил-N'-алкил(С6-С10)мочевин, который базируется на доступном сырье и является эффективным и технологичным.
Поставленная задача решается путем окисления дифенилхлорфосфина хлористым сульфурилом при температуре 20-25°С в среде четыреххлористого углерода, в результате чего образуется хлорангидрид дифенилфосфиновой кислоты, который подвергают взаимодействию с циановокислым натрием в растворе ацетонитрила в присутствии безводного хлористого магния в качестве катализатора при температуре 20-25°С с последующей реакцией присоединения образующегося дифенилфосфорилизоцианата к н-алкиламинам при температуре 20-25°С в среде растворителя, в качестве которого используется ацетонитрил.
Сущность изобретения состоит в том, что N-дифенилфосфорил-N'-алкил(С6-С10)мочевин получают по схеме с использованием в качестве исходного соединения дифенилхлорфосфина и с изменением совокупности действий в процессе синтеза.
Получение N-дифенилфосфорил-N'-алкил(С6-С10)мочевин протекает по следующей схеме:
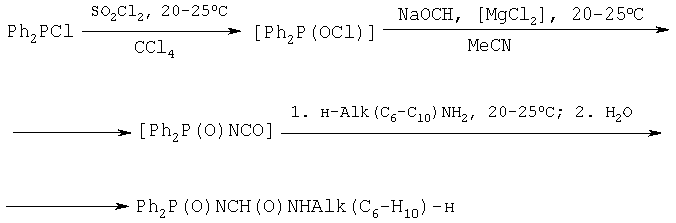
Сначала коммерчески доступный продукт - дифенилхлорфосфин, окисляют хлористым сульфурилом в четыреххлористом углероде при 20-25°С, что приводит к получению хлорангидрида дифенилфосфиновой кислоты; в последующем растворитель и другие летучие компоненты реакционной смеси удаляют в вакууме. Затем в тот же реактор последовательно добавляют растворитель - ацетонитрил, 2,5 мол.% безводного хлористого магния, являющегося катализатором, и циановокислый натрий; после часового перемешивания при комнатной температуре к реакционной массе, содержащей образовавшийся дифенилфосфорилизоцианат в растворе ацетонитрила, добавляют соответствующий первичный амин. После перемешивания в течение одного часа при комнатной температуре реакционную смесь разлагают водой, осадок целевой N-дифенилфосфорил-N'-алкил(С6-С10)мочевины отфильтровывают, промывают и сушат на воздухе.
Существенным отличием заявляемого способа от известного решения является то, что предварительно дифенилхлорфосфин окисляют хлористым сульфурилом при температуре 20-25°С в среде четыреххлористого углерода для получения исходного хлорангидрида дифенилфосфиновой кислоты, причем взаимодействие этого хлорангидрида с циановокислым натрием проводят при комнатной температуре (20-25°С), а в качестве растворителя при взаимодействии дифенилфосфорилизоцианата с н-алкиламинами используют ацетонитрил, в связи с чем заявляемое решение соответствует критерию новизны.
Конкретный способ получения N-дифенилфосфорил-N'-алкил(С6-С10)мочевин приведен в нижеследующих примерах.
Пример 1. N-дифенилфосфорил-N'-н-октилмочевина
В одногорлую грушевидную колбу, снабженную форштосом с капельной воронкой, подводом для аргона и жидкостным затвором, заполненным конц. серной кислотой, помещают раствор 7.28 г (0.033 моль) дифенилхлорфосфина в 15 мл абс. четыреххлористого углерода, при перемешивании на магнитной мешалке в атмосфере аргона при комнатной температуре в течение 1 часа 20 мин добавляют по каплям раствор 5.4 г (0.040 моль) свежеперегнанного хлористого сульфурила в 10 мл абс. четыреххлористого углерода, после прибавления раствора хлористого сульфурила смесь перемешивают еще 20 мин при этой температуре, растворитель и другие летучие компоненты реакционной смеси удаляют в вакууме водоструйного насоса (10-12 мм рт.ст.) (20 мин), а затем выдерживают в вакууме механического насоса (˜1 мм рт.ст.) (1 час). По данным спектра ЯМР 31Р остаток содержит 99.8% хлорангидрида дифенилфосфиновой кислоты. Остаток растворяют в 50 мл абс. ацетонитрила; к полученному раствору добавляют 0.080 г (0.840 ммоль) мелко растертого безводного хлористого магния, перемешивают на магнитной мешалке до полного растворения последнего (˜5 мин), прибавляют 4.29 г (0.066 моль) циановокислого натрия, смесь перемешивают на магнитной мешалке в течение 1 ч при комнатной температуре. По данным спектра ЯМР 31P реакционная смесь содержит 97.8% дифенилфосфорилизоцианата. К полученной суспензии добавляют 4.27 г (0.033 моль) н-октиламина, перемешивают на магнитной мешалке в течение 1 ч при комнатной температуре, добавляют 50 мл дистиллированной воды, перемешивают на магнитной мешалке в течение 1 ч при комнатной температуре и оставляют на ночь. Осадок отфильтровывают, промывают смесью 34 мл дистиллированной воды и 6 мл ацетонитрила, затем смесью 56 мл 1% соляной кислоты и 4 мл ацетонитрила, и затем дистиллированной водой (4 х 30 мл). Сушат на воздухе. Выход N-дифенилфосфорил-N'-н-октилмочевины 12.0 г (97.7%), т.пл. 155-156°С. Спектр ЯМР 1H (CDCl3, δ, м.д.): 0.85 т (3Н, СН3, 3JH-Н=6.7 Гц), 1.05-1.42 м [12 Н, (CH2)6], 3.06 д.т (2Н, CH2NH, 3JCH-H=6.7 Гц, 3JCH-H =6.0 Гц), 6.79 т (1Н, NHCH2, 3JH-Н=6.0 Гц), 7.33-7.46 м (4Н, m-С6Н5), 7.47-7.57 м (2Н, р-С6H5), 7.67-7.83 м (4Н, о-С6Н5), 7.96 д [1Н, NHP(O), 2JH-Р=11.0 Гц]. Спектр ЯМР 31Р{1Н}, (CDCl3, δ, м.д.): 24,31 с. Спектр ЯМР 13С{1Н}, (CDCl3, δ, м.д.): 13.97 с (СН3), 22.52 с (СН3СН2), 26.63 с (СН3СН2СН2), 29.08 с [СН3(СН2)2СН2], 29.13 с [СН3(СН2)3СН2], 29.60 с [СН3(СН2)4СН2], 31.68 с [СН3(СН2)5СН2], 40.03 с (CH2NH), 128.45 д [С2(6)НР, 2JC-Р=13.2 Гц], 131.31 д [С3(5)НР, 3JC-P=10.3 Гц], 131.31 д (С1P, 1JC-Р=128.4 Гц), 132.27 д (C4НР, 4JC-P=2.2 Гц), 155.98 с (С=O). Найдено, %: С 67.84, Н 7.87, N 7.41, Р 8.32. C21H29N2O2P. Вычислено, %: С 67.72, Н 7.85, N 7.52, Р 8.32.
Вещества-гомологи, полученные аналогичным способом, приведены в таблице (примеры 2-5).
В качестве исходных соединений использовались технический дифенилхлорфосфин (CAS Index [1079-66-9], фирма Acros, 95%), хлористый сульфурил (CAS Index [7791-25-5], фирма Acros, 98,5%), безводный хлористый магний (CAS Index [7786-30-3], фирма Aldrich, ≥98%), циановокислый натрий (CAS Index [917-61-3], фирма Aldrich, 96%), н-гексиламин (CAS Index [111-26-2], фирма Acros, 99%), н-гептиламин (CAS Index [111-68-2], фирма Acros, 99+%), н-октиламин (CAS Index [111-86-4], фирма Acros, 99+%), н-нониламин (CAS Index [112-20-9], фирма Acros, 98%), н-дециламин (CAS Index [2016-57-1], фирма Aldrich, ≥98%). В качестве растворителей использовали отечественные четыреххлористый углерод (ГОСТ 20288-74) и ацетонитрил [ТУ 6-09-3534-87 (1-4 изм.)].
Данное изобретение позволяет получать N-дифенилфосфорил-N'-алкил(С6-С10)мочевины с выходом (считая на дифенилхлорфосфин) не менее 91% (см. таблицу) и с высокой (не менее 98%) степенью чистоты. Весь процесс, включая синтез исходного хлорангидрида дифенилфосфиновой кислоты, проходит в одном реакторе ("one-pot" reaction). Все стадии проводятся при комнатной температуре, не требуют высоковакуумных перегонок промежуточных продуктов или других сложных процедур. Длительность процесса ˜ 6 часов, т.е. в 2-3 раза короче метода-прототипа. Все это, в совокупности, приводит к снижению энерго- и трудозатрат и, как следствие, к существенному уменьшению стоимости N-дифенилфосфорил-N'-алкил(С6-С10)мочевин, что, в свою очередь, сделает реальностью их практическое использование в качестве экстрагентов.
Выходы, константы и данные элементного анализа N-дифенилфосфорил-N'-алкил(С6-С10)мочевин Ph2P(O)NHC(O)NHAlk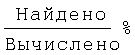
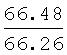
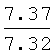
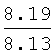
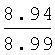
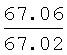
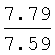
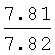
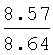
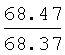
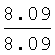
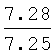
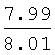
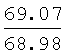
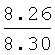
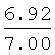
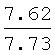
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ УРОВНЯ РАБОТОСПОСОБНОСТИ ЛАБОРАТОРНЫХ ЖИВОТНЫХ В ЭКСПЕРИМЕНТЕ | 2015 |
|
RU2601393C1 |
| СПОСОБ ПОЛУЧЕНИЯ (2RS)-2,5,7,8-ТЕТРАМЕТИЛ-2-[(4RS,8RS)-4,8,12-ТРИМЕТИЛТРИДЕЦИЛ]-ХРОМАН-6-ИЛ-N-[3-ОКСОЛУП-20(29)-ЕН-28-ОИЛ]-ГЛИЦИНАТА | 2008 |
|
RU2440366C2 |
| АМИДЫ АКРИЛОВОЙ И МЕТАКРИЛОВОЙ КИСЛОТ С N-АЛКИЛПИПЕРАЗИНО-ПИПЕРИДИНАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2617409C1 |
| БИС(2-ФЕНИЛПИРИДИНАТО-N,C){2-[2'-(4-АЛКИЛБЕНЗОЛСУЛЬФОНАМИДО)ФЕНИЛ]БЕНЗОКСАЗОЛАТО-N,N'}ИРИДИЯ(III) И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО НА ЕГО ОСНОВЕ | 2015 |
|
RU2602236C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ КОНДЕНСАЦИЕЙ АРОМАТИЧЕСКИХ АЛЬДЕГИДОВ С АЛЬФА-КЕТОКСИМАМИ С ОБРАЗОВАНИЕМ N-ОКСИДОВ И ПОСЛЕДУЮЩИМ ВЗАИМОДЕЙСТВИЕМ С АКТИВИРОВАННЫМИ ПРОИЗВОДНЫМИ КИСЛОТ | 2005 |
|
RU2402537C2 |
| N, N', N'-ТРИЗАМЕЩЕННЫЕ ИЗОСЕЛЕНОМОЧЕВИНЫ | 2010 |
|
RU2434852C1 |
| АМИДЫ АКРИЛОВОЙ И МЕТАКРИЛОВОЙ КИСЛОТ С ОЛИГОПИПЕРИДИНАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2617694C1 |
| N-ФЕНИЛАМИДНЫЕ И N-ПИРИДИЛАМИДНЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1998 |
|
RU2214409C2 |
| НОВЫЕ ОПТИЧЕСКИ АКТИВНЫЕ 4-ГИДРОКСИ-2-АЗА-9,10-АНТРАХИНОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2436775C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 2006 |
|
RU2456296C2 |
Изобретение относится к получению органических соединений, в частности к производным мочевины, которые могут быть использованы в технологии обработки радиоактивных отходов радиохимических производств. Способ осуществляют путем окисления дифенилхлорфосфина хлористым сульфурилом при температуре 20-25°С в среде четыреххлористого углерода. Образующийся хлорангидрид дифенилфосфиновой кислоты подвергают взаимодействию с циановокислым натрием в растворе ацетонитрила в присутствии безводного хлористого магния в качестве катализатора при температуре 20-25°С с последующей реакцией присоединения образующегося дифенилфосфорилизоцианата к н-алкиламинам при температуре 20-25°С в среде растворителя, в качестве которого используется ацетонитрил. Технический результат - упрощение способа с получением высокочистого продукта при снижении энергетических и экономических затрат. 1 табл.
Способ получения N-дифенилфосфорил-N'-алкил(С6-С10)мочевин путем взаимодействия хлорангидрида дифенилфосфиновой кислоты с циановокислым натрием в растворе ацетонитрила в присутствии хлористого магния в качестве катализатора с последующим взаимодействием полученного дифенилфосфорилизоцианата с н-алкиламинами при комнатной температуре в среде растворителя, отличающийся тем, что предварительно дифенилхлорфосфин окисляют хлористым сульфурилом при температуре 20-25°С в среде четыреххлористого углерода для получения исходного хлорангидрида дифенилфосфиновой кислоты, взаимодействие хлорангидрида дифенилфосфиновой кислоты с циановокислым натрием проводится при температуре 20-25°С, а в качестве растворителя при взаимодействии дифенилфосфорилизоцианата с н-алкиламинами используется ацетонитрил.
| МОРГАЛЮК В.П | |||
| и др., Доклады РАН, 2005, т.403, №2, с.201-204 | |||
| ГОРЮНОВ Е.И и др., Доклады РАН, т.399, №6, с.780-782 | |||
| US 3136801 А, 9.06.1964 | |||
| G.Tomaschewski, B.Breitfeld, J.Pract | |||
| Chem | |||
| Приспособление к индикатору для определения момента вспышки в двигателях | 1925 |
|
SU1969A1 |
Авторы
Даты
2007-04-10—Публикация
2006-01-30—Подача