Изобретение относится к новым соединениям в ряду хелатных комплексов иридия, а именно к бис(2-фенилпиридинато-N,C2′){2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолато-N,N′}иридия(III) общей формулы I,
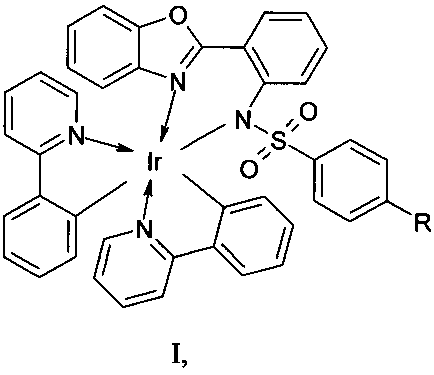
где R= алкил (C1-C6), проявляющему электролюминесцентные свойства, и электролюминесцентным устройствам (органическим светоизлучающим диодам, известных как ОСИД или OLED - Organic Light Emitting Diodes, - которые используются в качестве эффективных и высокоэкономичных твердотельных источников освещения нового поколения) с использованием в них вышеуказанного соединения в качестве активного люминесцентного слоя.
Известны электролюминесцентные устройства на основе хелатных комплексов иридия - замещенные по фенильному и пиридиновому кольцам трис(2-фенилпиридинато-N,C2′)иридия(III) (Jung S.-O., Kang Y., Kim H.-S., Kim Y.-H., Lee C.-L., Kim J.-J., Lee S.-K., Kwon S.-K. Effect of substitution of methyl groups on the luminescence performance of Ir(III) complexes: Preparation, structures, Electrochemistry, Photophysical properties and their applications in organic light emitting diodes (OLEDs) // Europ. Journ. of Inorg. Chem. 16 (2004), p. 3415-3423; Xu M.-L., Li T.-L., Li W.-L., Hong Z.-R., An Z.-W., Zhou Q. Optical and electroluminescent properties of a new Ir(III) complex- fac-tris[2,5-di(4-methoxyphenyl)pyridinato-C,N] iridium(III) // Thin Solid Films. 497 (2006), p. 239-242); Kwon S.-K., Kuppusamy Т., Kim S.-O., Youngjin K., Kim Y.-H. The Efficient Green Emitting Iridium(III) Complexes and Phosphorescent Organic Light Emitting Diode Characteristics, from “Organic Light Emitting Diode”, Marco Mazzeo (Ed.) (2010), ISBN: 978-953-307-140-4) и ацетилацетонаты замещенных бис(2-фенилпиридинато-N,C2′)иридия(III) (Liu Z.W., Bian Z.Q., Ming L., Ding F., Shen H.Y., Nie D.B., Huang C.H. Green and blue-green phosphorescent heteroleptic iridium complexes containing carbazole-functionalized β-diketonate for non-doped organic light-emitting diodes // Org. Electron. 9 (2008), p. 171-182), излучающие в синей и зеленой областях спектра.
Наиболее близким по выполнению является электролюминесцентное устройство на основе хелатного комплекса иридия - бис(2-фенилпиридинато-N,C2′)[2-(2′-гидроксифенил)-5-метилбензоксазолато-N,O2′]иридия (A), являющееся наиболее близким по структуре к заявляемому соединению.

Комплекс проявляет высокоэффективную фотолюминесценцию в зеленой области (λФЛ=525 нм). OLED устройство с конфигурацией ITO/CuPc (10 нм)/NPD (40 нм)/комплекс A:CBP (30 нм)/BAlq (10 нм)/ 1 (Alq3) (30 нм) LiF:Al (150 нм) излучает в зеленой области (λЭЛ=515 нм), обладает яркостью 4753 кД/м2 при напряжении 9,5 В, координаты CIE (x=0.28, y=0.52). (You Y., Seo J., Kim S.H., Kim K.S., Ahn Т.К., Kim D., Park S.Y. Highly Phosphorescent Iridium Complexes with Chromophoric 2-(2-Hydroxyphenyl)oxazole- Based Ancillary Ligands: Interligand Energy-Harvesting Phosphorescence // Inorg. Chem. 47 (5) (2008) p. 1476-1487).
В ряду бис(2-фенилпиридинато-N,C2′) бензоксазолатов иридия, не известны соединения, излучающие в желтой области спектра.
Техническим результатом изобретения являются новые соединения в ряду бис(2-фенилпиридинато-N,С2′) бензоксазолатов иридия, излучающие в желтой области спектра.
Технический результат достигается бис(2-фенилпиридинато-N,C2′){2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолато-N,N′}иридия(III) общей формулы I.
Способ их получения заключается во взаимодействии 2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолов (II) с тетракис(2-фенилпиридинато-N,C2′) (µ-дихлор) дииридием (III).

Техническим результатом изобретения является также электролюминесцентное устройство на основе хелатных комплексов - бис(2-фенилпиридинато-N,C2′) бензоксазолатов иридия в качестве активного люминесцентного слоя, излучающее в желтой области спектра.
Технический результат достигается электролюминесцентным устройством, включающим дырочный инжектирующий, дырочный транспортный, дырочный блокирующий, электронный транспортный, электронный инжектирующий слои и активный люминесцирующий слой на основе люминесцентного вещества, в качестве которого он содержит бис(2-фенилпиридинато-N,C2′){2-[2′-(4-алкилбензолсульфонамидо)фенил] бензоксазолато-N,N′}иридия(III) I.
Изобретение удовлетворяет критерию изобретательского уровня, так как используемый комплекс иридия формулы I не известен как электролюминесцентное вещество.
Ниже приведены примеры получения соединения и его применения.
Пример 1. Получение 2-(2′-тозиламинофенил)бензоксазола (II, R=CH3).
Синтез 2-(2′-тозиламинофенил)бензоксазола II осуществляют по методике [Чернова Н.И., Лосева М.В., Болотин Б.М., Нурмухаметов Р.Н., Рябокобылко Ю.С. Синтез и оптические свойства 5-замещенных 2-(2-тозиламинофенил)бензоксазолов. Химия гетероцикл. соедин. 1973. №4. С. 492-498].
К раствору 10.91 г (0.1 моль) о-аминофенола в 250 мл диоксана при перемешивании прибавляют 30.97 г (0.1 моль) хлорангидрида тозилантраниловой кислоты. Реакционную смесь охлаждают до комнатной температуры. Выделившееся масло через 30 мин превращается в кристаллический осадок, который отфильтровывают, промывают и кристаллизуют из метанола. Ацилированный о-аминофенол нагревают при 180-200°C. Образовавшуюся твердую массу охлаждают и очищают хроматографированием на окиси алюминия (элюент - хлороформ) и последующей перекристаллизацией из метанола. Получают 22.5 г чистого вещества. Т. пл. 165-166°C. Выход 64%.
Найдено, %: C 66.10; H 4.51; N 7.59; S 8.75. Для C20H16N2O3S вычислено, %: C 65.91; H 4.43; N 7.69; S 8.80.
1H ЯМР спектр, ДМСО-d6, δ, м.д.: 2.25 (с, 3H, CH3), 7.24-8.12 (м, 12H, CAr-H), 11.44 (уш. с, 1H, NH).
ИК спектр, (порошок), ν (см-1): 1615 ср., 1588 с., 1538 ср. (бензоксазольная система), 1340 с. (νas SO2), 1160 о.с. (νs SO2), 3433 (NH).
Пример 2. Получение тетракис(2-фенилпиридинато-N,C2′) (µ-дихлор) дииридия (III) (II).
Синтез осуществляют по методике [Tamayo А.В., Alleyne B.D., Djurovich P.I., Lamansky S., Tsyba I., Ho N.N., Bau R., Thompson M.E. Synthesis and Characterization of Facial and Meridional Tris-cyclometalated Iridium (III) Complexes // J. Am. Chem. Soc. 125 (2003) pp. 7377-7387).
К 27 мл смеси этилцеллозольва и воды (в объемном отношении 3:1) добавляют 352 мг (1.0 ммоль) тригидрата хлорида иридия и 372 мг (2.4 ммоль) 2-фенилпиридина. Смесь нагревают при перемешивании в атмосфере аргона при 110°C в течение 12 часов. Охлаждают, осадок ярко-желтого цвета отфильтровывают, промывают этанолом и гексаном, высушивают на воздухе. Выход 346 мг (63%). Соединение III без очистки используют для получения комплекса I.
Пример 3. Получение бис(2-фенилпиридинато-N,C2′)[2-(2′-тозиламинофенил)бензоксазолато-N,N′]иридия(III) (I, R=CH3).
Смесь 172 мг (0.16 ммоль) тетракис(2-фенилпиридинато-N,C2′) (µ-дихлор) дииридия (III) (III), 128 мг (0.35 ммоль) 2-(2′-тозиламинофенил)бензоксазола (II, R=CH3) и 170 мг (1.6 ммоль) карбоната натрия в 14 мл этилцеллозольва нагревают при перемешивании в атмосфере аргона при 140°C в течение 5 часов. Охлаждают, добавляют 70 мл этилацетата. Затем для извлечения этилцеллозольва обрабатывают 120 мл воды (3×40 мл). Этилацетат отгоняют, остаток обрабатывают 10 мл смеси этилацетат:гексан (2:3), нерастворившуюся часть отфильтровывают, промывают этой же смесью, высушивают. Очищают на хроматографической колонке (силикагель, элюент - хлористый метилен), собирая фракцию с Rf 0.1. Выход 182 мг (66%). После перекристаллизации из ацетонитрила оранжевые кристаллы с т.пл. >250°C.
Найдено, %: C 58.30; H 3.71; N 6.57. Для C42H31IrN4O3S вычислено, %: C 58.39; H 3.62; N 6.48.
ИК-спектр (в твердой фазе): 1608 ср, 1602 ср, 1583 ср, 1563 ср, 1476 с, 1454 ср, 1439 ср, 1426 ср, 1418 ср, 1351 сл, 1324 сл, 1298 с (νas SO2), 1285 ср, 1264 ср, 1231 с, 1187 ср, 1165 сл, 1134 с (νs SO2), 1085 с, 1063 ср, 1048 ср, 1030 ср, 1008 сл, 983 сл, 959 ср, 921 с, 895 сл, 864 сл, 824 ср, 807 ср, 791 ср, 753 с, 731 с, 712 ср, 689 ср, 669 сл, 649 с, 630 с, 585 ср, 558 с см-1.
1H ЯМР спектр, CDCl3, δ, м.д.: 2.21 (3H, с, CH3), 6.31 (1Н, д, J=7.8 Гц, CAr-H), 6.50 (1Н, д, J=7.5 Гц, CAr-H), 6.66 (2Н, т, J=7.0 Гц, CAr-H), 6.73-6.85 (8Н, м, CAr-H), 6.88 (2Н, д, J=8.1 Гц, CAr-H), 6.96-7.01 (1H, м, CAr-H), 7.18 (2H, т, J=7.8 Гц, CAr-H), 7.28 (2H, д, J=8.1 Гц, CAr-H), 7.50 (2H, д, J=8.1 Гц, CAr-H), 7.53-7.60 (3H, м, CAr-H), 7.66-7.73 (2H, м, CAr-Н), 7.84 (1H, д, J=8.1 Гц, CAr-H), 8.19 (1H, уш. с, CAr-H).
УФ-спектр: 405, 440, 475 нм (поглощение, ДМСО). Люминесценция 591 нм (ДМСО, λвозб=590 нм).
Пример 4. Электролюминесцентные свойства.
Использованные в работе вещества и ссылки на каталоги:
1. Phthalocyanine Copper complex (CuPc), ALDRICH, CAS 147-148.
2. 4,4′,4″-Tris(N-(2-naphthyl)-N-phenyl-amino)triphenylamine (2-TNATA) KINTEC, lot: KZ88BuOMEEO, sales@kintec.hk
3. Di-[4-(N,N-di-p-tolyl-amino)-phenyl]cyclohexane (TAPC), Luminescence Technology Corp, CAS: 58473-78-2.
4. 4,4′-Bis(carbazol-9-yl)biphenyl(СВР)), Luminescence Technology Corp, CAS: 58328-31-7
5. 2,9-Dimethyl-4,7-diphenyl-1,10-phenanhroline (BCP) KINTEC, lot: KZ86BUOHRYO, sales@kintec.hk
6. 4,7-Diphenyl-1,10-phenanthroline (Bphen) KINTEC, lot: KZ88BuOMEEO, sales@kintec.hk
7. LiF ALDRICH, CAS: 7789-24-4.
Для изготовления электролюминесцентного устройства /ЭЛУ/ со структурой ITO/CuPc/2-TNATA/ТАРС/комплекс I (R=СН3) : CBP/BCP/Bphen/LiF/Al используют стеклянную подложку с полупрозрачным слоем смешанного оксида индия и олова с сопротивлением 30-70 Ом/квадрат (дырочно-инжектирующий слой). На подложку методом испарения в вакууме последовательно наносят следующие слои: слой CuPc (дырочно-инжектирующий слой) толщиной 0.004 мкм, слой 2-TNATA (дырочно-транспортный слой) толщиной 0.020 мкм, слой ТАРС (дырочно-транспортный слой) толщиной 0.015 мкм, слой комплекса иридия I (R=CH3) в СВР толщиной 0.016 мкм, слой ВСР (дырочно-блокирующий слой) толщиной 0.006 мкм, слой Bphen (электронно-транспортный слой) толщиной 0.020 мкм и слой LiF (электронно-инжектирующий слой) толщиной 0.001 мкм. Затем также методом испарения в вакууме напыляют алюминиевый электрод (электронно-инжектирующий слой). Толщина металлического электрода порядка 0,1 мкм. Площадь светящейся поверхности 8.0 мм2. Полученное ЭЛУ обладает следующими параметрами: яркость 7500 кд/м2 достигается при напряжении 15 В и токе 120 мА (рис. 1. Вольт-амперные и Вольт-яркостные характеристики ЭЛУ с соединением I (R=CH3). ЭЛУ является источником, излучающим в желтой области спектра с максимумом электролюминесценции около 630 нм (рис. 2. Электролюминесценция ЭЛУ). Координаты цветности CIE (Commission internationale de l′eclairage) для ЭЛУ x=0.513, y=0.465 (рис. 3. Координаты цветности CIE для ЭЛУ).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 2009 |
|
RU2408648C1 |
| МНОГОСЛОЙНОЕ ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 2013 |
|
RU2532565C2 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 2013 |
|
RU2551675C2 |
| БИС{3-МЕТИЛ-1-ФЕНИЛ-4-[(ХИНОЛИН-3-ИМИНО)-МЕТИЛ]1-Н-ПИРАЗОЛ-5-ОНАТО}ЦИНКА(II) И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО НА ЕГО ОСНОВЕ | 2011 |
|
RU2470025C1 |
| БИС[2-(N-ТОЗИЛАМИНО)БЕНЗИЛИДЕН-4'-ДИМЕТИЛАМИНОФЕНИЛИМИНАТО]ЦИНКА(II) И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО НА ЕГО ОСНОВЕ | 2012 |
|
RU2518893C1 |
| [N,N'-БИС(2-ТОЗИЛАМИНОБЕНЗИЛИДЕН)ДИАМИНОДИПРОПИЛИМИНАТ]МЕТАЛЛА, ОБЛАДАЮЩИЙ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2562456C1 |
| Комплексы цинка 2-(N-тозиламинобензилиден)-2'-иминоалкилпиридинов, обладающие люминесцентной активностью | 2016 |
|
RU2616979C1 |
| ЦИНКОВЫЕ КОМПЛЕКСЫ 5-[2-ГИДРОКСИ(ТОЗИЛАМИНО)БЕНЗИЛИДЕНАМИНО]-2-(2-ТОЗИЛАМИНОФЕНИЛ)-1АЛКИЛБЕНЗИМИДАЗОЛОВ, ОБЛАДАЮЩИЕ ФОТОЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532904C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 1998 |
|
RU2140956C1 |
| ((2-(5,6-БИС(4-ФТОРФЕНИЛ)-1,2,4-ТРИАЗИН-3-ИЛ)ХИНОЛИН)БИС(2-ФЕНИЛПИРИДИН))ИРИДИЙ(III) ХЛОРИД - КЛЕТОЧНЫЙ ФЛУОРЕСЦЕНТНЫЙ КРАСИТЕЛЬ | 2024 |
|
RU2837462C1 |



Изобретение относится к новым соединениям в ряду хелатных комплексов иридия, а именно к бис(2-фенилпиридинато-N,С2′){2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолато-N,N′}иридия(III) формулы I

где R = алкил (С1-С6). Также предложено электролюминесцентное устройство. Соединение формулы I проявляет электролюминесцентные свойства и применяется в качестве активных люминесцентных слоев в электролюминесцентном устройстве, излучающем в желтой области спектра. 2 н.п. ф-лы, 3 ил., 4 пр.
1. Бис(2-фенилпиридинато-N,С2′){2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолато-N,N′}иридия(III) формулы I

где R = алкил (С1-С6).
2. Электролюминесцентное устройство, включающее дырочный инжектирующий, дырочный транспортный, дырочный блокирующий, электронный транспортный, электронный инжектирующий слои и активный люминесцирующий слой на основе люминесцентного вещества, в качестве которого он содержит бис(2-фенилпиридинато-N,С2′){2-[2′-(4-алкилбензолсульфонамидо)фенил]бензоксазолато-N,N′}иридия(III) формулы I

где R = алкил (С1-С6).
| YOU Y | |||
| et al, Highly Phosphorescent Iridium Complexes with Chromophoric 2-(2-Hydroxyphenyl)oxazole-Based AncillaryLigands: Interligand Energy-Harvesting Phosphorescence, Inorg | |||
| Chem., 2008, v | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Кювет для обработки кинолент | 1924 |
|
SU1476A1 |
| WO 2012148511 A1, 01.11.2012 | |||
| US 20120292600 A1, 22.11.2012 | |||
| JUNG S | |||
| et al, Effect of Substitution of Methyl Groups on the | |||
Авторы
Даты
2016-11-10—Публикация
2015-08-31—Подача