Изобретение предназначено для выявления физической зависимости и, в частности, для диагностики опийной наркомании. Набор реагентов «Нарко-ИФА-пептидный тест» предназначен для количественного иммуноферментного определения содержания пептидного фрагмента рекомбинантного мю-/дельта опиатного рецептора (МДОР) мозга человека в крови людей, употребляющих наркотические вещества. МДОР является пептидным компонентом сложного рецепторного белка синаптических мембран, появление которого в биологических жидкостях, в том числе крови, может приводить к патологическим изменениям в ЦНС. Увеличение концентрации МДОР коррелирует с наличием и предрасположенностью к опийной наркомании. Изобретение позволит эффективно выявлять опийную наркоманию.
Изобретение относится к биотехнологии, а именно к наборам реагентов для выявления состояния головного мозга млекопитающих, в частности для диагностики наркотической зависимости.
Заявляемый набор реагентов для выявления опийной наркомании, отличающийся тем, что выявляет физическую зависимость к наркотическим препаратам и группу риска, предназначен для скоростного анализа (10-30 мин) эндогенного пептида в концентрациях в 10 раз или 105 раз чувствительнее существующих аналогов.
Технический результат настоящего изобретения заключается в том, что диагностика опийной наркомании проводится путем количественного определения МДОР пептида, рекомбинантного компонента мю-/дельта нейрорецептора.
Сущность изобретения
Принцип работы диагностического набора реагентов Нарко-ИФА-пептидный тест состоит в количественном выявлении несвязанного в иммунный комплекс МДОР пептида фрагмента опиатных рецепторов мозга человека. Сорбция специфических куриных антител (IgY), полученных против синтетического пептида МДОР, на поверхности твердого носителя позволяет избирательно извлекать МДОР из плазмы (100 микролитров), отобранной у пациента из вены или пальца. Образовавшийся комплекс антитело-антиген выявляется с помощью меченных флуоресцеином антител человека против второго эпитопа МДОР. Иммуноферментная реакция измеряется по изменению флуоресценции, регистрируемой с помощью флуориметра вертикального сканирования при длине волны возбуждения 480 нм, и длине волны эмиссии 530 нм. Количество МДОР оценивается относительно калибровочной кривой зависимости волны эмиссии от известной концентрации калибратора, представляющего собой синтетический пептид МДОР.
Анти-МДОР куриные поликлональные антитела (IgY) и антитела человека, конъюгированные с флуоресцеином (золотом, пероксидазой), наносятся на твердый носитель (полистироловый иммунологический микропланшет, нитроцеллюлоза или нейлон) и инкубируются в течение 14-16 ч при +4°С для получения иммуносорбента. В ходе испытаний положительный, отрицательный контрольные образцы, 6 разведений калибратора и образцы плазмы пациентов и здоровых лиц наносили на иммуносорбент. В качестве положительного контрольного образца служит МДОР пептид, применяемый в концентрации 0,5 нг/мл. Отрицательным контрольным образцом служит МДОР пептид в концентрации 0,05 нг/мл. Калибратор представляет собой концентрированный образец МДОР пептида (концентрация 1,0 нг/мл), который наносится в лунки планшета-иммуносорбента параллельно с исследуемыми образцами в следующих концентрациях: 0; 0,05; 0,1; 0,25; 0,5; 1,0 нг/мл и используется при проведении контроля качества набора реагентов на заводе-изготовителе.
При использовании 96-луночного микропланшета, после нанесения образцов плазмы, иммуносорбент инкубировали 30 мин при температуре 37°С. Уровень связывания антител с МДОР-содержащим образцом определяли по результату иммунофлуоресцентной реакции в каждой лунке микропланшета на спектрофотометре вертикального сканирования (вариант сканирования планшеты со дна) при длине волны возбуждения 480 нм, и длине волны эмиссии 530 нм. Строили калибровочную кривую, откладывая по оси абсцисс концентрацию антител, по оси ординат - величину флуоресценции. Концентрацию МДОР пептида в пробах определяли по калибровочной кривой на основании величин флуоресценции. Концентрации отрицательного и положительного контрольных образцов должны соответствовать указанным выше значениям. Содержание МДОР пептида в крови здоровых лиц лежит в пределах 0,05-0,10 нг/мл. Содержание МДОР антител свыше 0,10 нг/мл обнаруживается в крови пациентов с опийной зависимостью.
Количественное содержание МДОР пептида в крови коррелирует с наличием или предрасположенностью к наркотической зависимости. Повышенные сверх нормы (0,10 нг/мл) концентрации МДОР пептида в крови свидетельствуют о нарушении функции опиатных нейрорецепторов под воздействием наркотических веществ, приводящее к физической зависимости от наркотиков. Достоверные стабильно повышенные концентрации МДОР пептида свидетельствуют о предрасположенности к физической зависимости, указывая на группу риска, например, у детей, матери которых потребляли наркотики во время беременности. Изменения концентрации МДОР пептида, и в том числе резкое его накопление в крови пациентов, служит критерием их функционального состояния.
Пример 1.
Реагенты для ИФА набора
Заявляемый набор реагентов «Нарко-ИФА-пептидный тест», количественный вариант, состоит из следующих компонентов:
- планшет 96-луночный полистироловый с иммобилизованными на внутренней поверхности лунок антителами против МДОР (куриные IgY),
- 10 X конъюгат IgG человека, меченных флуоресцеином - 1 уп. (200 мкл),
- положительный контрольный образец (МДОР пептид в концентрации 0,5 нг/мл), лиофилизированный, при разведении которого получается 1 мл раствора - 1 фл.;
- отрицательный контрольный образец (МДОР пептид в концентрации 0,05 нг/мл) лиофилизированный, при разведении которого получается 1 мл раствора - 1 фл.
- 10Х фосфатно-солевой буфер с Твин-20 - 1 уп. (100 мл);
- готовый к употреблению раствор тетраметилбензидин (ТМБ) - 1 уп. (15 мл).
Калибратор представляет собой концентрированный образец МДОР пептида (концентрация - 1,0 нг/мл), в набор не включается и применяется для контроля качества набора реагентов при его производстве.
Набор реагентов «Нарко-ИФА-пептидный тест» рассчитан на проведение анализа в дубликатах 45 исследуемых образцов плазмы и 2 образцов положительного и отрицательного контроля, 1 «бланк» образца. К каждому набору прилагается инструкция.
Специфический сорбент
Специфический сорбент готовили добавлением 100 мкл раствора немодифицированных или модифицированных (биотинилированные IgY) куриных иммуноглобулинов IgY (0,1-1 мкг/мл) в лунки планшетов высокой сорбции (пассивная адсорбция) или стрептавидиновые планшеты (ковалентное связывание) и инкубировали при комнатной температуре (20-25°С) в течение 1-14 часов. По окончании инкубации лунки планшетов промывали три раза по 5 мин фосфатным буфером, рН 7,4, сушили на открытом воздухе. Высушенные планшеты упаковывали под вакуумом в мешочки, изготовленные из плотной фольги, и хранили при комнатной температуре.
Пример 2.
Приготовление реагентов
Все разведения реагентов представлены для проведения анализа на 1 планшете.
Приготовление рабочего раствора фосфатно-солевого буфера с Твин-20 (РБ-Т).
В мерный стакан вместимостью 500 мл внесли 50 мл 10Х фосфатно-солевого буфера, добавили дистиллированную воду до метки 500 мл и тщательно перемешали, используя магнитную мешалку, избегая пенообразования. Полученный раствор РБ-Т можно хранить при температуре +2-8°С не более 7 дней.
Приготовление положительного и отрицательного контрольных образцов
В ампулу с положительным и отрицательным контрольным образцом внесли по 1,0 мл РБ-Т и тщательно перемешали до полного растворения, избегая пенообразования. Полученные растворы можно хранить при температуре +2-8°С не более 7 дней.
Приготовление калибратора
Приготовили 5 пробирок (емкость 5 мл) с маркировкой №№1-4 и в каждую внесли по 0,5 мл РБ-Т. В ампулу с калибратором внесли по 1,0 мл РБ-Т (1 нг/мл) и тщательно перемешали до полного растворения, избегая пенообразования. Отобрали 0,5 мл полученного раствора, внесли в пробирку №1 (0,5 нг/мл) и тщательно перемешали, затем отобрали 0,5 мл полученного раствора и внесли в пробирку №2 (0,25 нг/мл). Таким образом готовили 5 разведений калибратора от 0,05 нг/мл к 1,0 нг/мл. Приготовленные растворы калибратора не хранятся.
Приготовление раствора конъюгата
Из пробирки с конъюгатом отобрали 100 мкл раствора и внесли в стакан емкостью 30 мл, содержащий 10 мл РБ-Т, перемешали, избегая пенообразования.
Полученный раствор можно хранить при температуре +2-8°С не более 7 дней.
Приготовление анализируемых образцов сыворотки крови
Анализируемые образцы сыворотки крови перед определением следует развести в соотношении 1:50; в стеклянные или пластиковые пробирки внести по 20 мкл сыворотки крови, добавить 980 мкл РБ-Т и тщательно перемешать содержимое вращательными движениями. Разведенные образцы сыворотки крови можно хранить при температуре +2-8°С не более 7 дней.
Проведение анализа
Промыли лунки планшета следующим образом: внесли во все лунки планшета по 200 мкл РБ-Т и инкубировали планшет при постоянном встряхивании на шейкере в течение 5 мин при комнатной температуре. Содержимое лунок удалили стряхиванием, оставшуюся в лунках планшета жидкость удалили, постукивая перевернутым планшетом о ровную поверхность, покрытую фильтровальной бумагой. Повторили процедуру промывки лунок планшета еще 2 раза.
Внесли в лунки планшета по 100 мкл положительного контрольного образца, отрицательного контрольного образца, 5 проб калибратора и анализируемых образцов сыворотки крови в дубликатах. Инкубировать планшет при постоянном встряхивании на шейкере в течение 60 мин при комнатной температуре (+18-25°С).
По окончании инкубации удалить содержимое лунок стряхиванием. Промыть лунки планшета 3 раза так, как это указано выше; при каждом промывании лунок планшета необходимо его инкубировать на шейкере в течение 5 мин при комнатной температуре.
Внести во все лунки планшета по 100 мкл раствора коньюгата и инкубировать планшет при постоянном встряхивании на шейкере в течение 30 мин при комнатной температуре. После окончания инкубации удалить содержимое лунок встряхиванием. Промыть лунки планшета 3 раза так, как это указано выше; при каждом промывании лунок планшета необходимо его инкубировать на шейкере в течение 5 мин при комнатной температуре. Добавить по 100 мкл РБ-Т и немедленно измерить флуоресценцию в лунках планшета при длине волны возбуждения/испускания 488/530 нм. Рассчитать средние арифметические величины флуоресценции для каждого образца анализируемой сыворотки крови, положительного контрольного образца и отрицательного контрольного образца. Строили кривую зависимости концентрации калибратора от флуоресценции и определяли концентрацию неизвестного образца, откладывая по оси ординат величину флуоресценции.
Пример 3. Реагенты для полуколичественного набора
Антиген
Синтетический пептид МДОР, соответствующий последовательностям аминокислот консервативного цитоплазматического участка общего для мю- и дельта опиатных рецепторов, был получен методом твердофазного синтеза на NPS-400 полуавтоматическом синтезаторе (Neosystem Laboratory, Франция) с использованием метил-бутил-гидроацетилового основания и N-трет-бутоксикарбонил/бензиловой методики для первых двух аминокислот. Препаративная очистка пептида осуществлялась методом HPLC на DeltaPac Cig Column (Waters Chromatography, Milford, MA, США) в системе вода/ацетонитрил/0,015 М трифторуксусная кислота. Чистота пептида была определена аналитическим HPLC и варьировалась от 90 до 98%. Последовательность пептида были проверены анализом аминокислот после гидролиза пептида.
Антитепа
Получение, очистка и мечение поликлональных антител куринного белка (IgY)
МДОР пептид конъюгировали с гемоцианином (KLH, Aves Labs, США) и использовали для иммунизации несушек (возраст 25-50 недель). Внутримышечную иммунизацию (pectoral muscles) МДОР-KLH конъюгатом, иммульгированным с полным или неполным адъювантом Фрейнда (ПАФ) проводили каждые 2-3 недели. По окончании 4-ой инъекции собирали "иммунизированные" яйца несушек и выделяли из желтка IgY фракцию (Aves Labs, США), которую очищали иммуной хроматографией на колонке, содержащей МДОР-агарозу. Элюцию очищенных IgY проводили глициновым буфером, с рН 2,8. Пробу диализовали против физиологического раствора фосфатного буфера, концентрировали с использованием мембраны РМ-30 (Ami con, США).
Меченные красителем антитела IgY (Aves Labs, США) получали конъюгированием с коллоидным золотом. Поверхность стандартных частиц золота содержит отрицательно-заряженные ионы, которые свободно взаимодействуют с образованием ионной связи с позитивно-заряженными аминокислотными остатками пептида.
Выделение и мечение иммуноглобулинов человека (IgG)
Иммуноглобулины G, выделенные из сыворотки людей (Институт им. Пастера, С.-Петербург), в концентрации 10 мг/мл разводили 1:5 (объем:объем) фосфатным буфером и наносили на колонку, содержащую МДОР-агарозу. Элюировали пробу IgG с колонки в соответствии с описанным выше методом. Титр антител определяли методом иммуноферментного анализа, используя МДОР в качестве антигена. Чистоту полученного препарата IgG оценивали при помощи SDS-электрофореза в полиакриламидном геле.
Полученные IgG конъюгировали с флуоресцентным маркером (FITC) для получения меченых антител, используемых в количественном варианте «Нарко-ИФА-тесте» или метили с помощью пероксидазы хрена для использования в полуколичественном варианте скоростного теста в качестве фиксирующих антител.
Антитела козы против IgY
Антитела козы против IgY (Aves Labs, США) были конъюгированы с пероксидазой хрена для получения детекрирующих антител (Д).
Пример 4.
Конструкция и описание метода для полуколичественного набор реагентов
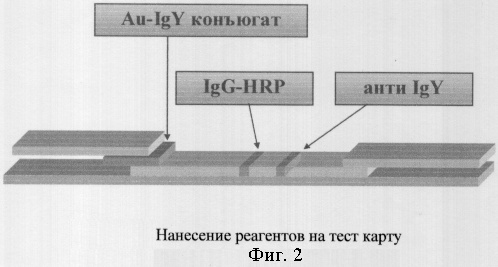
Тест-карта является основным компонентом набора «Нарко-ИФА-пептидный тест» (полуколичественный вариант), предназначенного для анализа свежеотобранной крови пациента (фиг.1). В состав тест-карты включаются фильтр, содержащий ЕДТА для отделения плазмы, нироцеллюлозная мембрана с нанесенными полосами: (1) меченных красителем IgY, (2) IgG-HRP (тест полоса) и (3) козьих антител против IgY (контрольная полоса, фиг.1, 2). Адсорбент представляет собой фильтр, содержащий блокирующий реагент. Тест карта помещается в пластиковый корпус с окном результата, в котором должны быть видны контрольная и тестовая полосы (фиг.2).
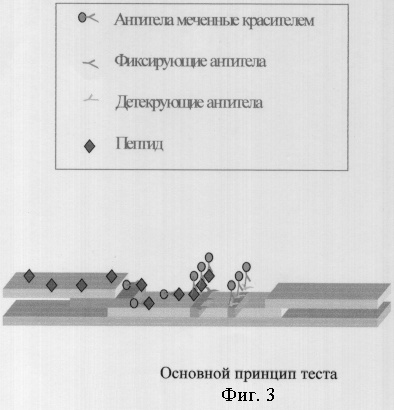
Принцип анализа основан на качественном твердофазном конкурентном иммуноферментном связывании антигена, содержащего разные иммунногенные епитопы, с двумя типами: фиксирующими и детектирующими антителами (фиг.3).
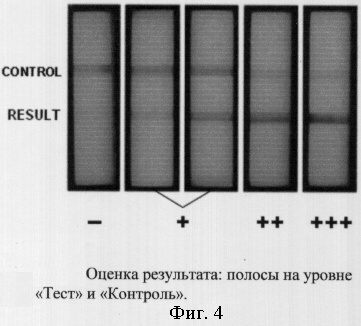
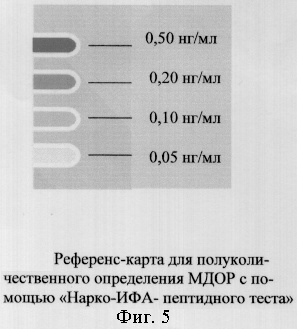
Реакция активируется при добавлении 3-х капель свежеотобранной крови (80-100 мкл) в окно для образца прибора (фиг.1). Пептид МДОР крови связывается с куриными иммуноглобулинами (IgY), меченными коллоидным золотом (фиг.3). Полученный комплекс AuIgY-МДОР продвигается вдоль нитроцеллюлозной мембраны к следующей зоне фиксирующих антител (Ф) - антител человека IgG, конъюгированных с пероксидазой хрена (HRP). Образовавшийся комплекс AuIgY-МДОР-IgG/HRP проявляется в виде красной полосы концентрированных частиц золота (фиг.4) в полосе теста (фиг.5). Интенсивность и скорость проявления полосы соответствует концентрации МДОР в крови (фиг.4). Непрореагировавшие с МДОР пептидом образца избыточные концентрации меченых AuIgY двигаются по мембране к контрольной зоне, расположенной на расстоянии от фиксирующей зоны и содержащей козьи антитела против IgY (1,5 мкг/карту), образовывая полосу контроля.
Результат (фиг.4) считается положительным при проявлении ярко-красной МДОР полосы в положении «Результат» (+++), красной МДОР полосы (-н-) и розовой МДОР полосы (+) или количественном варианте в соответствии с интенсивностью окраски на референс-карте (фиг.5). При проявлении только контрольной полосы результат считается отрицательным (-). При окончании срока годности полосы отсутствуют.
Предлагаемый полуколичественный вариант предназначен для скоростного анализа при осмотре пациента в кабинете врача для подтверждения предварительного диагноза. Для получения конкретного количественного результата образец плазмы должен быть проанализирован в клинической лаборатории с помощью количественного варианта «Нарко-ИФА-пептидного теста».
Пример 5.
Характеристика работы набора реагентов.
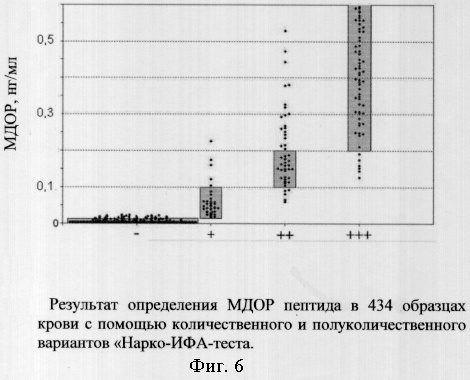
На фиг.6 представлены результаты тестирования 434 образцов крови, из которых 218 пациентов употребляли опийные наркотики. Концентрация МДОР пептида, определенная с помощью полу- и количественного «Нарко-ИФА-теста», варьировалась в широком диапазоне от <0,05 до ˜0,60 нг/мл. Значения МДОР пептида распределялись следующим образом: 227 образцов показали концентрацию МДОР≤0,05 нг/мл и 207 образцов в пределах от 0,1 до 0,60 нг/мл. Определение основных характеристик тестов показали чувствительность выявления заболевания 93% и специфичность выявления здоровых лиц 98%. Фальш-положительный ответ определен в 4 случаях и фальш-отрицательный ответ - в 15 случаях.
Заявляемые наборы реагентов «Нарко-ИФА - пептидный тест» позволяют быстро (10-30 мин) и эффективно провести диагностику физической зависимости к опиатам одновременно у значительного числа пациентов. Полуколичественный «Нарко-ИФА- пептидный тест» дает возможность профилактического обследования широких слоев населения с целью выявления группы риска по заболеванию.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ОПИЙНОЙ НАРКОМАНИИ | 2001 |
|
RU2193199C1 |
| ПРОГНОЗИРОВАНИЕ ТЕЧЕНИЯ И ИСХОДА КОМЫ И ПОСТКОМАТОЗНЫХ БЕССОЗНАТЕЛЬНЫХ СОСТОЯНИЙ (В ТОМ ЧИСЛЕ ВЕГЕТАТИВНЫХ) С ПОМОЩЬЮ ГЕМОТЕСТОВ | 2016 |
|
RU2648515C1 |
| ДИАГНОСТИЧЕСКИЙ НАБОР РЕАГЕНТОВ "CIS-ТЕСТ" ДЛЯ ВЫЯВЛЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ ГОЛОВНОГО МОЗГА МЛЕКОПИТАЮЩИХ | 1998 |
|
RU2146826C1 |
| НАБОР "ПА-ТЕСТ" ДЛЯ ДИАГНОСТИКИ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1995 |
|
RU2112243C1 |
| ДИАГНОСТИЧЕСКИЙ НАБОР РЕАГЕНТОВ ДЛЯ ВЫЯВЛЕНИЯ ХРОНИЧЕСКИХ ПАТОЛОГИЙ МОЗГА ИШЕМИЧЕСКОГО ГЕНЕЗА | 2017 |
|
RU2668534C1 |
| СПОСОБ ДИАГНОСТИКИ ОСТРОЙ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ | 1996 |
|
RU2123704C1 |
| БИОМАРКЕРЫ ИШЕМИИ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНЫХ НЕВРОЛОГИЧЕСКИХ ПОСЛЕДСТВИЙ ХИРУРГИЧЕСКОЙ ОПЕРАЦИИ | 2006 |
|
RU2435165C2 |
| НАБОР РЕАГЕНТОВ ДЛЯ ИММУНОФЕРМЕНТНОГО ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ЭНДОГЕННЫМ БИОРЕГУЛЯТОРАМ В СЫВОРОТКЕ КРОВИ ДЛЯ ВЫЯВЛЕНИЯ ЗАБОЛЕВАНИЙ ЗАВИСИМОСТИ | 2011 |
|
RU2495433C2 |
| СПОСОБ ДИАГНОСТИКИ РИСКА РАЗВИТИЯ СОМАТО-АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ ПРИ ПРИМЕНЕНИИ СПЕЦИАЛИЗИРОВАННЫХ ПРОДУКТОВ ДЕТСКОГО ПИТАНИЯ (СПДП) С ПОМОЩЬЮ ТЕСТ-СИСТЕМЫ | 2006 |
|
RU2327166C2 |
| ТЕСТ-СИСТЕМА ИММУНОФЕРМЕНТНАЯ ДЛЯ ОПРЕДЕЛЕНИЯ КОКЛЮШНЫХ АНТИТЕЛ В СЫВОРОТКАХ КРОВИ ЧЕЛОВЕКА И ЖИВОТНЫХ | 2015 |
|
RU2582959C1 |
Изобретение относится к средствам диагностики, а именно к набору реагентов для выявления состояния головного мозга млекопитающих, в частности для диагностики наркотической зависимости. Сущность изобретения включает набор реагентов «Нарко-ИФА-пептидный тест», содержащий антитела к двум эпитопам (МДОР) пептидного фрагмента рекомбинантного опиатного мю-/дельта рецептора: куриные IgY, полученные против синтетического МДОР-пептида, иммобилизованные на твердом полимерном носителе, поликлональные IgG человека, содержащие МДОР-антитела, иммобилизованные на полимерном носителе и реагенты для определения присутствия МДОР-пептида: коньюгированные с флуоресцеином, коллоидным золотом или пероксидазой хрена поликлональные IgG человека, содержащие МДОР-антитела, и коньюгированные с флуоресцеином, коллоидным золотом или пероксидазой хрена козьи антитела, полученные против куриных IgY. Преимущество изобретения заключается в повышении чувствительности способа. 9 з.п. ф-лы, 6 ил.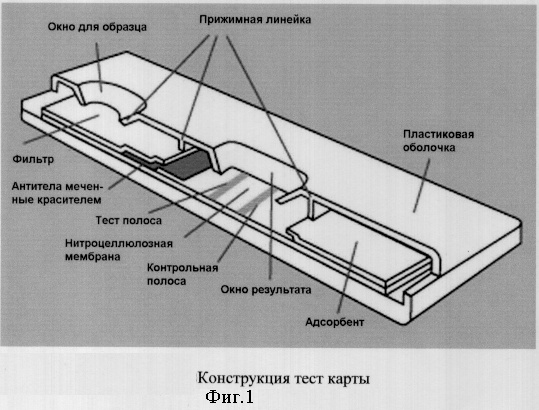
и реагенты для определения присутствия МДОР-пептида: коньюгированные с флуоресцеином, коллоидным золотом или пероксидазой хрена поликлональные IgG человека, содержащие МДОР-антитела;
коньюгированные с флуоресцеином, коллоидным золотом или пероксидазой хрена козьи антитела, полученные против куриных IgY.
| ТЕСТ-СИСТЕМА ДЛЯ ВЫЯВЛЕНИЯ ОПИЙНОЙ НАРКОМАНИИ | 2001 |
|
RU2193199C1 |
| US 6855807 A, 15.02.2005 | |||
| US 6432652 A, 13.08.2002 | |||
| US 6337207 А, 08.01.2002. | |||
Авторы
Даты
2007-04-20—Публикация
2005-03-02—Подача