По данной заявке испрошен приоритет на основании предварительной заявки на патент США № 60/326032, поданной 28 сентября 2001 г., которая полностью включена сюда в качестве ссылки, в соответствии с положениями §119 35 Свода законов США.
Область изобретения
Данное изобретение относится в общем к способам и устройствам для получения везикул, включая мицеллы, и в частности липосомы, экструзией растворов, включающих материалы, способные формировать везикулы, через сетчатую мембрану под высоким давлением.
Предпосылки изобретения
Использование липосом для доставки лекарственных препаратов было предложено для расширения номенклатуры лекарственных препаратов, в частности тех, которые вводят парентерально. Липосомы могут обеспечить контролируемое высвобождение из «депо» введенного лекарственного препарата в течение длительного периода времени и ослабление побочных эффектов лекарственного препарата ограничением концентрации свободного лекарственного препарата в потоке крови. Липосомы могут также изменить тканевое распределение и захват лекарственных препаратов терапевтически благоприятным образом и могут увеличить удобство лечения благодаря возможности менее частого введения лекарственных препаратов. Данные эффекты можно усилить прикреплением лигандов, которые нацеливают липосомы на определенные типы клеток или тканей внутри организма. Обзор липосомных систем доставки лекарственных препаратов проведен в публикации Poznansky et al., 1984, Pharmacol. Rev. 36:277-336.
В целом, оптимальный размер диаметра липосом для использования при парентеральном введении находится в диапазоне приблизительно от 70 до 300 и вплоть до приблизительно 400 нм. Липосомы в данном диапазоне размеров можно стерилизовать путем пропускания через обычные пористые фильтры, имеющие избирательность размера частиц приблизительно 200 нм. Данный диапазон размеров липосом также способствует биологическому распределению в определенных органах-мишенях, таких как печень, селезенка и костный мозг, и дает более равномерные и прогнозируемые скорости высвобождения лекарственных препаратов и стабильность их уровня в потоке крови. Липосомы, размеры которых менее чем приблизительно 400 нм, также проявляют меньшую тенденцию к агрегации при хранении и, таким образом, в целом безопаснее и менее токсичны при парентеральном применении, чем липосомы более крупного размера.
Были предложены разнообразные методики получения липосом, включая, например, способы обработки ультразвуком, экструзии, гомогенизации при высоком давлении, микрофлюидизации, детергентного диализа, вызванного кальцием слияния мелких липосомных везикул, и инфузии простого эфира (см., например, патент США № 4186183; патент США № 4217344; патент США № 4261975; патент США № 4485054; патент США № 4774085; патент США № 4946787; патент США № 6139871; Публикация РСТ WO 91/17424, Deamer et al., 1976, Biochim. Biophys. Acta, 443:629-34; Fraley, et al., 1979, Proc. Natl. Acad. Sci. USA, 76:3348-52; Hope, et al., 1985, Biochim. Biophys. Acta, 812:55-65; Mayer, et al., Biochim. Biophys. Acta, 858:161-68; Williams, et al., 1988, Proc. Natl. Acad. Sci. USA, 85:242-46 и Szoka, et al., 1980, Biochim. Biophys. Acta, 601:559-71). Обычно указанные способы обеспечивают получение липосом, которые являются гетеродисперсными и преимущественно имеют размер более чем около 1 мкм. Данные исходные гетеродисперсные суспензии можно уменьшить в размере и распределении размера с использованием ряда известных способов. Одним из способов изменения размера, который подходит для крупномасштабного производства, является гомогенизация. При этом исходный препарат гетеродисперсных липосом прокачивают под высоким давлением через камеру с малым отверстием или реакционную камеру. Суспензию обычно подвергают циклической обработке прогонкой через реакционную камеру до тех пор, пока не будет достигнут желательный средний размер липосомных частиц. Ограничение данного способа состоит в том, что распределение размера липосом обычно достаточно широкое и изменчивое, особенно в диапазоне размера среднего диаметра липосом 100 нм, в зависимости от числа циклов гомогенизации и внутренней температуры. Также обработанная жидкость может собирать металлические и масляные примеси из насоса гомогенизатора и может, кроме того, загрязняться остаточными химическими реагентами, используемыми для стерилизации уплотнителей насоса.
Обработка ультразвуком или ультразвуковое облучение представляет собой еще один способ, который используют для уменьшения размеров липосом. Данную методику используют главным образом для получения мелких однослойных везикул (SUV) в диапазоне размеров от 25 до 80 нм. Однако узкого распределения размеров липосом можно достичь лишь при размерах липосом приблизительно 50 нм, т.е. после того, как липосомы были уменьшены до их самых маленьких размеров. Данные очень мелкие липосомы имеют ограниченную способность переноса или загрузки лекарственных препаратов и менее благоприятные свойства биологического распределения, чем свойства при диапазоне размеров от 100 до 400 нм, как отмечено ниже. Возможности обработки данным способом также достаточно ограничены, поскольку требуется долговременная обработка ультразвуком относительно небольших объемов. Генерирование тепла во время обработки ультразвуком может также привести к перекисному повреждению липидов, и с ультразвуковых зондов сходят титановые частицы, которые потенциально достаточно токсичны in vivo.
Третий общий способ изменения размера основан на экструзии липосом через мембрану с однородным размером пор, изготовленную из поликарбоната или другого аналогичного материала (см. Szoka, et al., 1978, Proc. Natl. Acad. Sci. USA, 75:4194-8). Данная процедура имеет преимущества перед указанными выше способами гомогенизации и обработки ультразвуком в том, что имеется разнообразие размеров пор мембраны для продукции липосом при различных выбранных диапазонах размеров, и кроме того, распределение размеров липосом можно сделать достаточно узким, в частности, циклической обработкой материала пропусканием несколько раз через фильтр с выбранным размером пор. Известны публикации о ряде методик экструзии липосом. Например, в патенте США № 4927637 описан способ экструзии липидов через нейлон с извитыми каналами, TUFFRYN® (Pall Corp., East Hills NY), мембрану из полисульфона, полипропилена или волокнистой стали под низким давлением (например, 250 фунтов/кв. дюйм). В патенте США № 5008050 речь идет о способе экструзии липосом через поликарбонатный фильтр под давлением от 100 до 700 фунтов/кв. дюйм или более. В патенте США № 4737323 речь идет о способе производства липосом экструзией суспензии липидов через керамическую мембрану под давлением от 200 до 250 фунтов/кв. дюйм.
Однако способы экструзии через мембрану имеют несколько недостатков при крупномасштабной обработке. Во-первых, поры в мембране имеют тенденцию к засорению, в частности, при обработке концентрированных суспензий и/или когда размеры липосом существенно больше, чем размеры пор мембраны. Большинство устройств экструзии в промышленном масштабе не обеспечивает возможность промывки обратной струей для очистки мембран. Замена засоренной мембраны свежей мембраной открывает устройство для экструзии воздействию окружающей среды и создает риск загрязнения продукта даже если мембрану подвергают промывке обратной струей. Мембраны нельзя подвергать паровой стерилизации на месте с высокой степенью надежности ввиду присущей им хрупкости. Независимо от того, какой способ используют для преодоления засорения или загрязнения мембраны, он удлиняет и удорожает процесс экструзии.
Недостатки доступных в настоящее время способов экструзии липосом особенно остры, когда осуществляют экструзию определенных типов липидов. Липидные двухслойные структуры приобретают кристаллическую фазу ниже температуры Tc', гелевую фазу при температурах от Tc' до Tc и жидкокристаллическое состояние выше температуры Tc (см. Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71). Может быть особенно трудно проводить экструзию через поликарбонатные мембраны липидов с температурой Tc больше, чем приблизительно комнатная температура. Величина Tc для конкретного липида зависит от ряда факторов, включая длину и степень насыщения углеводородной цепи липида. Липиды с более длинными, более насыщенными углеводородными цепями имеют тенденцию к более высоким величинам Tc (и имеют тенденцию к более трудной экструзии через поликарбонатные мембраны), чем липиды с более короткими, менее насыщенными углеводородными цепями. Липиды также может быть трудно подвергать экструзии ввиду наличия примесей в исходном материале, например загрязнения смолами, которые представляют собой побочный продукт процесса изготовления. Липиды, которые трудно подвергать экструзии, также имеют более медленные скорости потока и легче загрязняют или засоряют мембраны, чем другие липиды. Как объяснено выше, засоренные или загрязненные мембраны необходимо очистить или заменить, что увеличивает время и затраты на производство и возможность загрязнения.
Таким образом, существует необходимость в более быстрых и экономически эффективных способах и устройствах для экструзии липидов, в частности липидов, которые трудно подвергнуть экструзии, со сниженной частотой засорения или загрязнения мембран и со сниженной вероятностью загрязнения продукта.
Сущность изобретения
Данное изобретение относится к способам и устройствам, которые, в частности, можно использовать для изготовления везикул, включая мицеллы, и в частности липосомы, и к фармацевтическим продуктам, содержащим везикулы, мицеллы или липосомы. Конкретнее, было обнаружено, что экструзия липидов через сетчатую мембрану (мембраны) под высоким давлением приводит к значительно увеличенным скоростям потока, в то же самое время продуцируя везикулы желательного размера и ламеллярности. Сетчатые мембраны, как будет описано подробно ниже, представляют собой мембраны, которые имеют поры, чьи каналы через мембрану в среднем представляют собой по существу прямые линии. Способы и устройства настоящего изобретения можно, в частности, использовать для производства везикул желательного размера и ламеллярности из липидов, которые трудно подвергнуть экструзии с использованием обычных методик.
Кроме того, было обнаружено, что экструзия липидного препарата через мембраны PORETICSTM (Osmonics, Minnetonka MN) приводит к значительно увеличенным скоростям потока по сравнению с экструзией через другие имеющиеся в продаже мембраны.
Кроме того, было обнаружено, что использование гидрофильной мембраны в соответствии с изобретением и высокого давления экструзии приводит к уменьшению размера везикул, которые продуцируются экструзией.
Способы и устройства изобретения можно использовать относительно беспроблемным образом при сниженном засорении или загрязнении мембран, при высоких объемах выхода и при крупномасштабной работе. Таким образом, способы и устройства изобретения хорошо подходят для использования при производстве липосом.
В одном аспекте изобретение обеспечивает способ изготовления липосом, включающий экструзию водной суспензии липидов через гидрофильную мембрану, в частности сетчатую мембрану (мембраны), под высоким давлением. Изобретение обеспечивает способ получения суспензии липосом с равномерным распределением размеров. То есть липосомы, созданные способом изобретения, проявляют небольшую изменчивость распределения среднего размера. Кроме того, изобретение обеспечивает способ получения суспензии липосом любой формы, например суспензию липосом можно лиофилизировать для получения порошка.
В другом аспекте изобретение обеспечивает способ получения суспензии липосом, включающий экструзию под высоким давлением водной суспензии липидов через сетчатую мембрану с расположенными под углом порами. Сетчатые мембраны с расположенными под углом порами, как будет подробно описано ниже, представляют собой сетчатые мембраны, в которых углы, образованные порами относительно плоскости лицевой стороны мембраны, составляют менее чем приблизительно 90°.
В другом аспекте изобретение обеспечивает способ получения суспензии липосом, включающий экструзию под высоким давлением водной суспензии липидов через гидрофильную мембрану с расположенными под углом порами.
В другом аспекте изобретение обеспечивает устройство для экструзии водной суспензии липидов под высоким давлением, включающее гидрофильную сетчатую мембрану (мембраны) в опорном кассетном держателе.
При осуществлении способов изобретения производят экструзию суспензии липидов через гидрофильную сетчатую мембрану под высоким давлением. Полученные в результате липосомы имеют средний диаметр приблизительно от 50 до 400 нм и стандартное распределение размера приблизительно 50 нм в зависимости от количества используемых мембран, количества циклов пропускания липосом через мембраны, толщины мембран, давления экструзии, диаметра и плотности пор в мембранах, химического состава мембран, использования способа шагового понижения, типа используемого липида, использования смачивающего агента, присутствия агента, инкапсулированного в липосомы или ассоциированного с липосомами, и т.д., как будет подробно описано ниже. Способы изобретения позволяют регулировать размер и распределение размера полученных липосом.
Суспензию можно пропускать через мембрану множество раз, каждый раз в одном и том же направлении через мембрану. Альтернативно, направление потока через мембрану можно менять на противоположное в течение одного или нескольких прохождений через мембрану. То есть суспензию можно пропускать через мембрану в направлении снаружи вовнутрь для поддержания мембраны в незакупоренном состоянии, обеспечивая возможность высокопроизводительной обработки даже для концентрированной суспензии липосом.
Желательного размера липосом можно достичь с использованием способа «пошагового понижения». То есть суспензию липидов пропускают через мембраны с уменьшающимся размером диаметра пор серией циклов пропускания через мембраны для получения липосом все более уменьшающегося среднего диаметра.
Данные и другие аспекты и признаки настоящего изобретения станут полнее очевидными при прочтении следующего подробного описания изобретения в сочетании с сопутствующими чертежами.
Краткое описание чертежей
Фиг.1 представляет объем экструзии как функцию времени для двух различных коммерчески доступных мембран (поликарбонатные, подвергнутые образующему каналы пор протравливанию мембраны (PCTE) с диаметром пор 0,1 мкм от компаний Osmonics ("O") и Whatman ("W")) при давлении 400 и 800 фунтов/кв. дюйм.
Фиг.2 представляет собой группу графиков, которые сравнивают экструзию через одиночную мембрану PCTE с одиночной полиэфирной, подвергнутой образующему каналы пор протравливанию мембраной (PETE), причем обе мембраны имеют диаметры пор 0,1 мкм. Фиг.2А представляет собой график, представляющий размер частиц как функцию количества прохождений. Фиг.2В представляет собой график, представляющий скорость потока как функцию количества прохождений.
Фиг.3А представляет собой график, сравнивающий полученный экструзией объем в зависимости от времени для экструзии 20% l-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолина (POPC) через мембраны PCTE и PETE со средним диаметром пор 0,1 мкм при давлении 400 фунтов/кв. дюйм. Фиг.3В представляет собой график, сравнивающий полученный экструзией объем в зависимости от времени для экструзии 20% POPC через мембраны PCTE и PETE со средним диаметром пор 0,1 мкм при давлении 800 фунтов/кв. дюйм.
Фиг.4 представляет собой серию графиков, описывающих влияние размера стопки мембран на экструзию РОРС с использованием PETE мембран со средним диаметром пор 0,1 мкм, сложенных стопкой из 1, 2, 5 и 10 штук, при давлении 800 фунтов/кв. дюйм. Фиг.4А представляет собой график, показывающий средний размер частиц крупной однослойной везикулы (LUV) как функцию количества прохождений. Фиг.4В представляет собой график, показывающий скорость потока как функцию количества прохождений. Фиг.4С представляет собой график, показывающий связь между размером стопки мембран и количеством прохождений, необходимых для достижения среднего размера частиц приблизительно 120 нм.
Фиг.5 представляет собой серию графиков, описывающих влияние давления на экструзию РОРС с использованием стопки из 5 мембран из PETE с диаметром пор 0,1 мкм при величинах давления экструзии 400, 600 и 800 фунтов/кв. дюйм. Фиг.5А представляет собой график, показывающий размер частиц как функцию количество прохождений. Фиг.5В представляет собой график, показывающий скорость потока как функцию количества прохождений. Фиг.5С представляет собой график связи между давлением экструзии и количеством прохождений, необходимым для получения частиц со средним размером приблизительно 120 нм.
Фиг.6 представляет максимальный объем экструзии как функцию давления экструзии для мембран PORETICSТМ из PCTE и PETE с размером пор 0,1 мкм формы Osmonics и мембран NUCLEPORETM из PCTE фирмы Whatman c таким же размером пор перед загрязнением или засорением мембран.
Подробное описание изобретения
В одном аспекте изобретение обеспечивает простой и быстрый способ получения везикул желаемого размера путем экструзии препарата липидов через гидрофильную сетчатую мембрану под высоким давлением. Препарат липидов можно подвергнуть экструзии через мембрану один раз или более одного раза, множеством «прохождений» для получения везикул желаемого размера. При использовании многократных прохождений направление потока суспензии через мембрану можно сменить на обратное в течение одного или нескольких прохождений. Препарат липидов можно также подвергнуть экструзии через множество «уложенных стопкой» мембран для уменьшения количества прохождений, требуемых для достижения частиц желательного размера. Альтернативно, препарат липидов можно пропустить внутри одного и того же канала через последовательно расположенные мембраны, которые уложены стопкой, или не уложены стопкой, или через комбинацию уложенных стопкой и не уложенных стопкой мембран при их последовательном расположении.
В другом аспекте настоящее изобретение обеспечивает устройство для получения липосом диаметром от около 50 до около 400 нм экструзией водной суспензии липидов через гидрофильную сетчатую мембрану под высоким давлением.
Важным признаком способов и устройств настоящего изобретения является использование высокого давления для принудительного прохождения водной суспензии липидов через мембрану. Было обнаружено, что использование величин давления, значительно превышающих минимальное давление, требуемое для экструзии, обеспечивает неожиданно хорошие результаты при достижении получения липосом желательного среднего диаметра и во избежание проблем, связанных с засорением или загрязнением мембраны. Использование высокого давления особенно благоприятно для экструзии липидов, которые трудно подвергнуть экструзии с использованием обычных способов. Как показано в примерах, чем больше используемое давление, тем реже происходит засорение и загрязнение. Нет видимого верхнего предела данной взаимосвязи. Используемое давление ограничено только прочностью используемого устройства для экструзии, опор мембраны и самих мембран. При минимуме используемое давление должно быть больше чем приблизительно 400 фунтов/кв. дюйм. Предпочтительно, используют давление более чем приблизительно 800 фунтов/кв. дюйм. Предпочтительнее, используют давление более чем приблизительно 1000 фунтов/кв. дюйм. Еще предпочтительнее, используют давление, превышающее приблизительно 1500 фунтов/кв. дюйм. Еще предпочтительнее, используют давление, превышающее приблизительно 5000 фунтов/кв. дюйм. Наиболее предпочтительно, используют давление, превышающее приблизительно 8000 фунтов/кв. дюйм.
Используемые здесь термины «липосома», «везикула» и «липосомная везикула» следует понимать как определяющие структуры, которые имеют содержащие липиды мембраны, заключающие водную внутреннюю среду. При отсутствии других указаний структуры могут также иметь одну или несколько липидных мембран, хотя обычно липосомы имеют только одну мембрану. Такие липосомы, имеющие одиночный слой, именуются здесь «однослойными». Однослойные липосомы можно классифицировать как маленькие однослойные везикулы (SUV), большие однослойные везикулы (LUV) или гигантские однослойные везикулы (GUV) (см. Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71 на стр. 70). SUV обычно определяют как липосомы, в которых эффекты кривизны важны для их свойств. При использовании данного определения размер липосомы, который можно охарактеризовать как SUV, зависит от липида или жидкостей, которые она включает. В целом, для мягкой двухслойной структуры верхний предел для SUV составляет приблизительно 50 нм, в то время как для механически очень когезионных двухслойных структур верхний предел может находиться в диапазоне от около 80 до около 100 нм. GUV обычно определяют как липосомы с диаметром более чем приблизительно 1 мкм. Специалисту в данной области будет понятно, что границы между данными классами везикул не резко определены и что имеется существенное перекрытие между ними по их граничным значениям.
В одном варианте воплощения липосомы изобретения могут представлять собой содержащие липиды мембраны, содержащие водную внутреннюю среду, причем водная внутренняя среда содержит лекарственное соединение. В другом варианте воплощения липосомы могут не содержать лекарственный препарат в водной внутренней среде, но представляют собой содержащую липиды мембрану, включающую внутреннюю среду. Такие не содержащие лекарственный препарат липосомы можно использовать для удаления холестерина из потока крови и лечения или предотвращения атеросклероза.
Используемые здесь термины «связанное с липосомой» или «связывание с липосомой» указывают на то, что обсуждаемое соединение ковалентно или не ковалентно связано с поверхностью липосомы или полностью или частично содержится во внутренней среде липосомы.
Термины «фармацевтически активное соединение» и «лекарственный препарат» предназначены указывать на синтетическое соединение, пригодное для терапевтического применения без ассоциированных носителей, адъювантов, активаторов или кофакторов. Липосомы изобретения могут содержать лекарственный препарат в водной внутренней среде. В определенных вариантах воплощения липосомы могут не содержать лекарственный препарат во внутренней среде, и в таких вариантах воплощения сами липосомы могут представлять собой лекарственные препараты или фармацевтически активные соединения. Данные «пустые» липосомы можно использовать для удаления холестерина из орагнизма и лечения или предотвращения атеросклероза.
«Сетчатые мембраны» представляют собой мембраны, которые имеют поры, чьи каналы через мембрану в среднем представляют по существу прямые линии. Сетчатые мембраны могут иметь поры, которые перпендикулярны плоскости мембраны, и/или поры, расположенные под углом. Мембраны «с порами, расположенными под углом» представляют собой сетчатые мембраны, в которых углы, образованные порами относительно плоскости лицевой стороны мембраны, составляют менее чем приблизительно 90°. «Рифовая длина» поры представляет собой длину поры, измеренную от одной поверхности мембраны до другой. Так, пора, которая перпендикулярна плоскости мембраны, имеет рифовую длину, которая равна толщине мембраны. Поры с меньшими углами пор имеют большие величины рифовой длины.
Для определенной капельки на твердой поверхности «угол контакта» представляет собой измерение угла, образованного между поверхностью твердого вещества и касательной линией к радиусу капельки от точки контакта с твердым веществом. Угол контакта связан с поверхностным натяжением уравнением Янга, посредством которого можно рассчитать поведение специфических взаимодействий между жидкостью и твердым веществом. Угол контакта, равный нулю, приводит к смачиванию, в то время как угол от 0 до 90° приводит к распространению капли (вследствие молекулярного притяжения). Углы более чем 90° указывают на то, что жидкость имеет тенденцию образовывать маленькую каплю или удаляться с твердой поверхности. Таким образом, чем меньше угол контакта между поверхностью и капелькой воды, тем более гидрофильной является поверхность (см., например, Morgan, et al., 1983, Physical Pharmacy: Physical Chemical Principles in the Pharmaceutical Sciences, Lea & Febiger Publishers, Philadelphia; Gennaro, et al., 1990, Remington's Pharmaceutical Sciences, 18th edition, Mack Publishing Company, Easton, Pennsylvania).
«Трудные липиды» представляют собой липиды, которые относительно трудно подвергнуть экструзии с использованием обычных методик, потому что они имеют тенденцию засорять или загрязнять мембрану для экструзии. Напротив, «легкие липиды» представляют собой липиды, которые относительно легко подвергнуть экструзии с использованием обычных методик. Обычно липиды, имеющие температуру перехода (Тс) бульшую, чем комнатная температура, трудно подвергнуть экструзии, в то время как липиды, имеющие Тс около комнатной температуры или ниже, легко подвергнуть экструзии. Несколько трудных липидов имеют температуры перехода ниже комнатной температуры, например l-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолин (POPC). Ряд различных факторов может влиять на то, трудно ли подвергнуть экструзии конкретный липид. Самым важным фактором является жесткость ацильной цепи липида. Липиды, имеющие более жесткие ацильные цепи, например липиды, включающие мононенасыщенную ацильную цепь, имеют тенденцию труднее подвергаться экструзии с использованием обычных способов и устройств. Примеси в липидном препарате, например смолы, внедренные во время процесса изготовления липида, также могут сделать липид труднее экструдируемым. Кроме того, примеси могут воздействовать на конформацию липидов в растворе или на способность липида деформироваться через поры мембран. Данные проблемы можно преодолеть, если используют мембраны с большей площадью поверхности или большей пористостью, например мембраны Whatman ANOPORETM.Трудными липидами могут также быть липиды, ассоциированные с лекарственными препаратами, заряженные липиды и липиды с белками. Некоторые липиды, которые легко экструдируются в лабораторном масштабе, может быть трудно экструдировать в более крупном масштабе производства. Примеры липидов, которые трудно экструдировать, включают, но не ограничиваются ими, РОРС, дипальмитоилфосфатидилхолин, дипальмитоилфосфатидилглицерин и дистеароилфосфатидилэтаноламин. Примеры легких липидов включают, но не ограничиваются ими, фосфатидилхолин яичного желтка (ЕРС), яичный фосфатидилглицерин и диолеилфосфатидилхолин.
Мембраны
Мембрана, которую можно использовать для осуществления настоящего изобретения, представляет собой гидрофильную сетчатую мембрану. Гидрофильная сетчатая мембрана, которую можно использовать для осуществления заявляемого изобретения, можно изготовить из любого гидрофильного материала. Мембрану можно изготовить из одного гидрофильного материала или из более чем одного гидрофильного материала, или из смеси гидрофильных и негидрофильных материалов. В предпочтительном варианте воплощения мембрана изготовлена из естественно гидрофильного материала. В другом предпочтительном варианте воплощения мембрана изготовлена из материала, который сделан гидрофильным во время изготовления мембраны, например полиэфира. В предпочтительном варианте воплощения гидрофильные сетчатые мембраны, которые можно использовать для осуществления настоящего изобретения, имеют угол контакта поверхности с водой менее чем 120 градусов, предпочтительно, менее чем 70 градусов, предпочтительнее, менее чем 50 градусов, наиболее предпочтительно, 40 градусов или менее. В другом предпочтительном варианте воплощения гидрофильные сетчатые мембраны, которые можно использовать для осуществления заявляемого изобретения, имеют поверхностное натяжение перед протравливанием около 41 дин/см или более, предпочтительно, 42 дин/см или более, а наиболее предпочтительно, 43 дин/см или более. Конкретные гидрофильные мембраны, которые можно использовать для осуществления настоящего изобретения, включают, но не ограничиваются ими, полиэтилентерефталат (полиэфир), оксид алюминия, полиакрилонитрил, ацетат целлюлозы, смешанный сложный эфир целлюлозы, стекло, полиэфирсульфон, полисульфон и полигексаметиленадипамид (нейлон). Следует отметить, что было определено, что полиэфир представляет собой в настоящее время самую подходящую из коммерчески доступных мембран для использования в способах и устройствах изобретения.
Мембраны, изготовленные из более гидрофобных материалов, также можно использовать при условии, что они модифицированы для проявления более гидрофильных свойств. Способы увеличения гидрофильности мембран хорошо известны в данной области и включают, но не ограничиваются ими, обработку мембраны поверхностно-активным агентом, покрытие мембраны смачивающим агентом или нанесение тонкой пленки другого полимера или мономерной системы для образования новой поверхности посредством формирования композита, например поливинилпиролидина (PVP), химической прививки к мембране активной группы (мономера) низкой молекулярной массы, формирования мембраны из комбинации двух или более полимеров и модификации плазмы (см., например, Matrin, et al., 1983, Physical Pharmacy: Physical Chemical Principles in the Pharmaceutical Sciences, Lea & Febiger Publishers, Philadelphia; Gennaro, et al., 1990, Remington's Pharmaceutical Sciences, 18th edition, Mack Publishing Company, Easton, Pennsylvania).
В другом предпочтительном варианте воплощения сетчатая мембрана, которую можно использовать для осуществления настоящего изобретения, изготовлена из TEFLON® (Du Pont, Wilmington, DE). В более предпочтительном варианте воплощения мембрана состоит из или состоит по существу из TEFLON®. В другом более предпочтительном варианте воплощения мембрана включает TEFLON® и одно или несколько других веществ.
Сетчатые мембраны имеют «прямые сквозные» каналы (именуемые также порами капиллярного типа). То есть канал поры проявляет или описывает по существу прямую линию через мембрану. Если данная линия перпендикулярна или проходит под прямым углом к плоскости поверхности мембраны, то она имеет угол пор 90°. Мембраны с наклонными порами имеют поры под углом меньше, чем 90°.
Сетчатые мембраны, изготовленные с использованием любого способа, можно использовать в способах и устройствах настоящего изобретения. Сетчатые мембраны обычно изготавливаются при двухэтапной процедуре образующего каналы пор протравливания (см., например, Wagner, 2001, Membrane Filtration Handbook: Practical Tips and Hints, 2nd Edition, Printed by Osmonics, Inc., Minnetonka, MN). На первом этапе мембрану подвергают действию ионизирующего излучения. Данное излучение образует следы повреждения, которые беспорядочно распределены по поверхности мембраны. Следы повреждения протравливают в поры сквозь мембраны погружением мембраны в протравливающий раствор, например концентрированный щелочной раствор, такой как гидроксид натрия. Угол, под которым заряженные частицы ударяют и проходят через мембраны на первом этапе, определяет угол пор полученного в результате канала. Таким образом, можно изготовить фильтр с желательным средним углом пор регулированием угла, под которым заряженные частицы ударяют мембрану.
Процесс протравливания может воздействовать на гидрофильность мембраны. Для многих типов мембран, включая поликарбонатные и полиэфирные мембраны, погружение в ванну протравливания увеличивает гидрофильность мембран. Некоторые мембраны, такие как полиэфирные мембраны, становятся более гидрофильными быстрее, чем другие мембраны, такие как поликарбонатные мембраны, обработанные в аналогичных условиях протравливания (см., например, Kroschwitz, 1990, Concise Encyclopedia of Polymer Science and Engineering, Wiley, New York, 363-67, 558-60; Domininghaus, 1993, Plastics for Engineers: Material, Properies, Applications, Hanser Publishers, New York, Chapter 14; Zeronian, et al., 1990, J. Appl. Polym. Sci. 41:527-34; Gillberg, et al., 1981, J. Appl. Polym. Sci. 26:2023-51).
Было обнаружено, что экструзия через мембраны Osmonics PORETICSTM приводит к значительно увеличенным скоростям потока по сравнению с экструзией через другие коммерчески доступные мембраны, и что указанное различие особенно велико, когда продавливаемый через мембрану липид представляет собой трудный липид. Без ограничения определенной теорией необходимо отметить, что на скорость потока и размер частиц липосом влияет ряд факторов, включая, но не ограничиваясь ими, диаметр пор, плотность пор, средний угол пор, диапазон углов пор, толщина мембраны и материал, использованный для изготовления или покрытия мембраны, как описано здесь. Свойства полиэфира, поликарбоната и других мембран обсуждаются, например, в публикациях Kroschwitz, 1990, Concise Encyclopedia of Polymer Science and Engineering, Wiley, New York; Domininghaus, 1993, Plastics for Engineers: Material, Properties, Applications, Hanser Publishers, New York; Zeronian, et al., 1990, J. Appl. Polym. Sci. 41:527-34 и Gillberg, et al., 1981, J. Appl. Polym. Sci. 26:2023-51.
В предпочтительном варианте воплощения мембраны представляют собой мембраны с расположенными под углом порами. В более предпочтительном варианте воплощения мембрана имеет средний угол относительно плоскости поверхности мембраны (т.е. средний угол пор) менее чем около 56°. В наиболее предпочтительном варианте воплощения средний угол пор составляет около 45°. В другом предпочтительном варианте воплощения средний угол пор составляет около 90° для минимизации рифовой длины поры до того же расстояния, что и толщина мембраны.
Коммерчески доступные полиэфирные мембраны, подходящие для использования в настоящем изобретении, включают, но не ограничиваются ими, PETE мембраны NUCLEPORETM, каталожные № 188607, 188107, 188606, 188106, 188605, 188105 и 188604 (Whatman), PETE мембраны CYCLOPORETM, каталожные № 7061-2504, 7061-4704, 7061-2502, 7061-4702, 7061-2501 и 7061-4701 (Whatman) и PETE мембраны PORETICSTM, каталожные № T01CP02500, T04CP04700, T02CP02500, T02CP04700, T01CP02500 и T01CP04700 (Osmonics).
Мембрану любой толщины можно использовать в способах и устройствах настоящего изобретения. Специалисту в данной области будет понятно, что более толстая мембрана продуцирует меньшие везикулы и обеспечивает более медленную скорость потока по сравнению с более тонкой мембраной при прочих аналогичных условиях. Верхний предел размера толщины мембраны, которую можно использовать в способах и устройствах настоящего изобретения, определяется прочностью используемого устройства для экструзии. Нижний предел размера толщины мембраны, которую можно использовать в способах и устройствах настоящего изобретения, определяется хрупкостью мембраны и ее способностью выдерживать давление экструзии. В предпочтительном варианте воплощения толщина мембраны составляет от около 3 до около 50 мкм. В более предпочтительном варианте воплощения толщина мембраны составляет от около 3 до около 20 мкм. В наиболее предпочтительном варианте воплощения толщина мембраны составляет от около 3 до около 12 мкм.
В способах и устройствах настоящего изобретения можно использовать мембрану любого размера и формы. Размер и форма мембраны ограничивается только прочностью устройства для экструзии. В целом, чем больше площадь поверхности мембраны, тем больше скорость потока через мембрану. Мембрану любого желаемого размера и формы можно вырезать из большего листа мембраны. Мембрана может быть, например, круглой, квадратной или прямоугольной с площадью поверхности от около 1 до около 3 м2. В предпочтительном варианте воплощения мембрана является круглой и имеет диаметр приблизительно 25 мм. В другом предпочтительном варианте воплощения мембрана является круглой и имеет диаметр приблизительно 47 мм. В другом предпочтительном варианте воплощения мембрана является круглой и имеет диаметр приблизительно 90 мм. В другом предпочтительном варианте воплощения мембрана является круглой и имеет диаметр приблизительно 142 мм. В еще одном предпочтительном варианте воплощения мембрана является круглой и имеет диаметр приблизительно 293 мм.
В способах и устройствах настоящего изобретения можно использовать мембрану любой топологии, ограниченной только прочностью используемого устройства для экструзии. Специалисту в данной области известно, как манипулировать топологией мембраны для увеличения площади поверхности мембраны, которая находится в контакте с препаратом, который подлежит экструзии, и что это снижает засорение или загрязнение мембраны. В предпочтительном варианте воплощения мембрана является плоской. В другом предпочтительном варианте воплощения мембрана является гофрированной.
В способах и устройствах настоящего изобретения можно использовать мембрану с любым средним диаметром пор. При прочих аналогичных условиях мембрана с большим средним диаметром пор производит большие везикулы и обеспечит большую скорость потока, чем мембрана с меньшим средним диаметром пор. В предпочтительном варианте воплощения мембрана имеет средний диаметр пор, который приблизительно равен диаметру везикул, которые предстоит получить. В другом предпочтительном варианте воплощения средний диаметр пор составляет от около 50 до около 400 нм. В более предпочтительном варианте воплощения средний диаметр пор составляет от около 75 до около 200 нм. В еще более предпочтительном варианте воплощения средний диаметр пор составляет от около 100 до около 125 нм. В наиболее предпочтительном варианте воплощения средний диаметр пор составляет около 100 нм.
В способах и устройствах настоящего изобретения можно использовать мембрану с любой плотностью пор. При прочих аналогичных условиях мембрана с большей плотностью пор будет иметь меньшее засорение или загрязнение и большую скорость потока, чем мембрана с меньшей плотностью пор. Таким образом, в целом, предпочтительна большая плотность пор. Однако большие плотности пор связаны с несколькими недостатками. Во-первых, высокая плотность пор может уменьшить прочность на растяжение мембраны, таким образом, уменьшая ее способность выдерживать давление экструзии, которое на нее воздействует. Во-вторых, в мембране с беспорядочно распределенными порами количество перекрывающих пор увеличивается с увеличением плотности пор. Перекрывающие поры имеют диаметр пор больший, чем рассчитанный размер мембраны, следовательно, они могут вызвать увеличение среднего диаметра везикул, экструдируемых через мембрану. Следовательно, предпочтительна плотность пор, которая настолько высока, насколько можно достичь без нарушения прочности на растяжение мембраны или значительного увеличения среднего диаметра частиц везикул после экструзии через мембрану. Максимальная достижимая или желательная плотность пор также ограничена средним диаметром пор мембраны. Мембрана с большим средним диаметром пор имеет меньшую максимальную плотность пор, чем в остальном аналогичная мембрана с меньшим средним диаметром пор. В предпочтительном варианте воплощения плотность пор составляет приблизительно от 8·105 до 9·109 беспорядочно распределенных пор/см2. В более предпочтительном варианте воплощения плотность пор составляет приблизительно от 8·106 до 5·109 беспорядочно распределенных пор/см2. В наиболее предпочтительном варианте воплощения плотность пор составляет приблизительно от 1,5·107 до 2,6·109 беспорядочно распределенных пор/см2.
Больших диаметров пор можно достичь в мембране без значительного увеличения ее среднего диаметра пор использованием упорядоченного распределения пор. Можно создать сетчатую мембрану с упорядоченным расположением пор, в которой случаи перекрывающих друг друга пор по существу исключены даже при очень высоких значениях плотности пор. Таким образом, в предпочтительном варианте воплощения плотность пор составляет приблизительно от 8·105 до 9·109 беспорядочно распределенных пор/см2. В более предпочтительном варианте воплощения плотность пор составляет приблизительно от 8·106 до 5·109 беспорядочно распределенных пор/см2. В наиболее предпочтительном варианте воплощения плотность пор составляет приблизительно от 1,5·107 до 2,6·109 беспорядочно распределенных пор/см2.
Устройство для эффективного манипулирования и/или замены мембран во время процесса экструзии можно использовать со способами изобретения. Такое устройство может представлять собой опорный держатель, включающий, например, мембрану (мембраны) и опорное кольцо (кольца) для удерживания мембраны (мембран) в одной плоскости для предотвращения складывания или застревания. Устройство в виде опорного держателя может состоять из мембран с различным или одинаковым диаметром пор, расположенных в виде многослойной или уложенной стопкой конфигурации. Устройство изобретения может обеспечить легкость и удобство при работе с мембранами, например устройство можно легко удалить или заменить во время процесса экструзии, и его можно стерилизовать.
Способы изобретения
В соответствии со способами изобретения материал, способный сформировать везикулу, мицеллу или липосому, продавливают через сетчатую мембрану под высоким давлением для получения суспензии везикул, мицелл или липосом. Примеры материалов, подходящих для экструзии с использованием способов и устройств настоящего изобретения, обсуждаются ниже.
Способы и устройства настоящего изобретения на практике используют при высоком давлении экструзии. Экструзия, проводимая под более высоким давлением, будет иметь более высокую скорость потока, мембраны будут менее легко засоряться или загрязняться, что позволит мембране переносить большую степень загрязнения или засорения во время производства и обеспечит получение везикул меньшего размера, чем при прочих идентичных экструзиях, проводимых под более низким давлением. Давление, которое можно использовать, ограничивается только прочностью устройства для экструзии и используемой мембраной. В предпочтительном варианте воплощения используют давление более чем около 400 фунтов/кв. дюйм. В другом предпочтительном варианте воплощения используют давление более чем около 800 фунтов/кв. дюйм. В более предпочтительном варианте воплощения используют давление более чем около 1500 фунтов/кв. дюйм. В еще более предпочтительном варианте воплощения используют давление более чем около 5000 фунтов/кв. дюйм. В наиболее предпочтительном варианте воплощения в изобретении используют давление более чем около 8000 фунтов/кв. дюйм.
Настоящее изобретение можно осуществлять при любой температуре. В предпочтительном варианте воплощения экструзию проводят при регулируемой температуре. В более предпочтительном варианте воплощения регулируемая температура представляет собой постоянную температуру. В другом варианте воплощения постоянная температура приблизительно является комнатной температурой. В другом варианте воплощения постоянная температура равна Тс подвергаемого экструзии липида или больше нее. В другом варианте воплощения подвергаемая экструзии смесь включает множество липидов, а постоянная температура равна самой высокой Тс подвергаемых экструзии липидов или больше нее. В другом варианте воплощения постоянная температура составляет от около 15 до около 35°С. В более предпочтительном варианте воплощения постоянная температура составляет от около 20 до около 30°С. В более предпочтительном варианте воплощения постоянная температура составляет от около 23 до около 27°С. В наиболее предпочтительном варианте воплощения постоянная температура составляет около 25°С.
Способы и устройства настоящего изобретения можно использовать для изготовления везикул любого желательного среднего диаметра. В целом, выбирают мембрану, которая имеет средний диаметр пор, аналогичный желательному среднему диаметру везикул, как объяснено выше. Средний размер везикул можно уменьшить, например, экструзией полученных в результате экструзии везикул еще один или несколько дополнительных раз с использованием стопки мембран, с использованием более толстой мембраны, увеличивая давление экструзии или обрабатывая везикулы, как описано в настоящем описании. Размер везикул можно определить с использованием любой методики, известной в данной области. Например, квази-электрическое рассеивание света (QELS), также известное как динамическое рассеивание света (DLS), можно использовать, как описано в публикации Bloomfield, 1981, Ann. Rev. Biophys. Bioeng. 10:421-50. В предпочтительном варианте воплощения везикулы имеют средний диаметр приблизительно от 50 до 400 нм. В более предпочтительном варианте воплощения средний диаметр составляет приблизительно от 50 до 150 нм. В еще более предпочтительном варианте воплощения средний диаметр составляет приблизительно от 100 до 150 нм. В наиболее предпочтительном варианте воплощения средний диаметр составляет приблизительно 169±37 нм, 158±39,5 нм, 136±42 нм, 153,6±45,2 нм, 138,6±35,6 нм, 114,4±35,8 нм или 118,1±36,2 нм.
Способы и устройства настоящего изобретения можно использовать для изготовления везикул желательной ламеллярности. Однослойная везикула имеет одиночный слой мембраны. Многоламеллярная везикула (MLV) включает множество слоев мембраны (см. Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71). В предпочтительном варианте воплощения изобретения суспензию MLV экструдируют через мембрану с использованием способов или устройств настоящего изобретения для получения суспензии однослойных везикул желательного среднего диаметра. В другом предпочтительном варианте воплощения эмульсию экструдируют через мембрану с использованием способов или устройств настоящего изобретения.
Везикулы, полученные с использованием способов или устройств настоящего изобретения, можно дополнительно обработать с использованием любой методики обработки. В предпочтительном варианте воплощения средний диаметр везикул суспензии везикул, полученных с использованием способов и устройств настоящего изобретения, изменяют после того, как их получили в результате экструзии. В более предпочтительном варианте воплощения везикулы, полученные в результате экструзии, подвергают экструзии еще один или несколько раз. В еще более предпочтительном варианте воплощения дополнительную экструзию осуществляют с использованием способов и устройств настоящего изобретения. В наиболее предпочтительном варианте воплощения везикулы получают экструзией при многократных прохождениях с использованием процедуры «шагового понижения», т.е. при которой каждую последующую экструзию проводят через мембрану с меньшим средним диаметром пор. В другом более предпочтительном варианте воплощения суспензию пропускают через мембрану попеременно в направлениях вперед и назад для уменьшения количественной характеристики засорения или загрязнения мембраны.
В другом предпочтительном варианте воплощения средний диаметр полученных экструзией везикул дополнительно уменьшают обработкой ультразвуком. В другом предпочтительном варианте воплощения прерывистые циклы обработки ультразвуком перемежают оценкой QELS для управления эффективным синтезом везикул.
В другом предпочтительном варианте воплощения полученные экструзией везикулы обрабатывают для удаления загрязняющих материалов или примесей. В другом предпочтительном варианте воплощения подлежащая экструзии суспензия содержит вещество, которое предстоит включить в везикулы, и стадия обработки удаляет ту часть вещества, которая не была включена в везикулы. В более предпочтительном варианте воплощения вещество, которое предстоит включить в везикулы, представляет собой фармацевтически активное вещество, такое как мелкомолекулярный лекарственный препарат, белок, пептид, нуклеиновую кислоту или олигонуклеотид.
Способы и устройства настоящего изобретения можно практически осуществлять с использованием любого количества сложенных стопкой мембран. Специалисту в данной области понятно, что экструзия через большее число сложенных стопкой мембран будет иметь более низкую скорость потока и продуцировать везикулы, имеющие меньший средний диаметр, чем в остальном аналогичная экструзия через меньшее количество уложенных стопкой мембран. Количество мембран, которые можно использовать в стопке, ограничено только прочностью устройства для экструзии. В предпочтительном варианте воплощения стопка включает от 2 до 10 мембран. В наиболее предпочтительном варианте воплощения стопка включает от 2 до 5 мембран. В другом предпочтительном варианте воплощения мембраны в стопке отличаются, по меньшей мере, от одной из мембран в стопке. Различие может заключаться в любом свойстве, которое воздействует на экструзию. Различие может заключаться, например, в составе мембраны, покрытии, размере пор, плотности пор, угле пор, форме пор или размере мембраны, как описано здесь.
В другом предпочтительном варианте воплощения экструзию выполняют с использованием множества прохождений через мембрану или стопку мембран. Если при экструзии используют вариант воплощения с мембранами, уложенными стопкой, многократные прохождения могут не быть необходимыми для получения липосом желательного диаметра. В особенно предпочтительном варианте воплощения используют способ пошагового понижения. При способе пошагового понижения многократные прохождения суспензии производят через мембраны с уменьшающимся диаметром пор. В особенно предпочтительном варианте способа пошагового понижения первое прохождение проводят через мембрану с диаметром пор около 0,4 мкм, второе прохождение проводят через мембрану с диаметром пор около 0,2 мкм и, если необходимо, третье, четвертое, пятое и шестое прохождение производят через мембрану с диаметром пор около 0,1 мкм.
В другом предпочтительном варианте воплощения мембрану обрабатывают промывочным агентом перед экструзией. В другом предпочтительном варианте воплощения мембрану обрабатывают промывочным агентом после того, как было завершено, по меньшей мере, одно прохождение через мембрану, и перед тем, как было выполнено, по меньшей мере, еще одно прохождение через мембрану. Промывочный агент может представлять собой любое вещество или композицию, которая удаляет материал из засоренной или загрязненной поры мембраны или предотвращает засорение или загрязнение мембран или создание «эффекта отсеивания». В предпочтительном варианте воплощения промывочный агент включает органический спирт. В более предпочтительном варианте воплощения промывочный агент включает этанол.
Устройства для экструзии
Для воплощения способов и устройств заявляемого изобретения можно использовать любое устройство для экструзии, способное разместить в себе соответствующую мембрану и выдержать высокое давление экструзии. В предпочтительном варианте воплощения устройство для экструзии настоящего изобретения и устройства, которые можно использовать для осуществления способов настоящего изобретения, включают гидрофильную, расположенную под углом пору или гидрофильную сетчатую мембрану с расположенными под углом порами. В более предпочтительном варианте воплощения мембрана представляет собой полиэфирную мембрану, подвергнутую образующему каналы пор протравливанию (PETE). В другом более предпочтительном варианте воплощения устройство для экструзии дополнительно включает корпус и сосуд для сбора, причем корпус функционально прикреплен к первой стороне мембраны устойчивым к давлению и жидкости уплотнителем, а сосуд для сбора расположен для приема суспензии, полученной экструзией, после того как она выйдет со второй стороны мембраны. В еще одном более предпочтительном варианте воплощения устройство дополнительно включает опору мембраны или устройство. В другом более предпочтительном варианте воплощения устройство для экструзии имеет такую конфигурацию, что водную суспензию можно альтернативно подвергнуть экструзии через мембрану в направлении вперед и в обратную сторону. В другом предпочтительном варианте воплощения устройство для экструзии использует тангенциальный поток. Коммерчески доступные устройства, которые можно снабдить соответствующими мембранами и использовать в настоящем изобретении, включают, но не ограничиваются ими, THE MINI-EXTRUDERTM, каталожный № 610000 (AVANTI® Polar Lipids, Inc., Alabaster AL), см. Subbarao, et al., 1991, Biochim. Biophys. Acta, 1063:147-54, Liposome Extruder, Part № ER-1 (Eastern Scientific, Rockville MD), см. EMULSIFLEX®-C50 Extruder, каталожный № EFC50EX (Avestin, Inc., Ottowa, Ontario, Canada), см. LIPOSOFASTTM, (Avestin, Inc.), LIPEXTM Extruders (Northern Lipids Inc., Vancouver, British Columbia, Canada). Другие устройства для экструзии, которые можно использовать для осуществления настоящего изобретения, включают устройства, описанные в патентах США № 5948441, 5556580 и 6217899 В1.
Устройство для экструзии должно быть способно выдерживать высокие уровни давления экструзии. В качестве общего правила большие уровни давления приводят к улучшенной работе, например увеличенным скоростям потока, меньшему загрязнению и засорению мембраны и более быстрому уменьшению размера везикул, полученных в результате экструзии. Как минимум, устройство для экструзии должно быть способно выдерживать уровни давления более чем около 400 фунтов/кв. дюйм. В предпочтительном варианте воплощения устройство для экструзии должно быть способно выдерживать уровни давления более чем около 800 фунтов/кв. дюйм. В более предпочтительном варианте воплощения устройство для экструзии должно быть способно выдерживать уровни давления более чем около 1000 фунтов/кв. дюйм. В другом более предпочтительном варианте воплощения устройство для экструзии должно быть способно выдерживать уровни давления более чем около 1500 фунтов/кв. дюйм. В более предпочтительном варианте воплощения устройство для экструзии должно быть способно выдерживать уровни давления более чем около 5000 фунтов/кв. дюйм. В самом предпочтительном варианте воплощения устройство для экструзии должно быть способно выдерживать уровни давления более чем около 8000 фунтов/кв. дюйм.
Можно также использовать держатель или корпус опоры мембраны, которые оптимизируют доступную площадь поверхности при условии, что мембрана может выдержать давление экструзии, которому она подвергается. В предпочтительном варианте воплощения мембрана является гофрированной. В другом предпочтительном варианте воплощения в держателе или корпусе опоры мембраны используется трехмерное расположение мембраны. Изобретение, кроме того, обеспечивает способы и устройство для эффективного манипулирования с мембранами и/или замены мембран во время процесса экструзии. Коммерчески доступные поликарбонатные подвергнутые образующему каналы пор протравливанию (PCTE) и полиэфирные подвергнутые образующему каналы пор протравливанию (PETE) мембраны являются тонкими и статически заряженными. Указанные мембраны легко сгибаются и слипаются друг с другом, затрудняя манипулирование ими и их размещение в держателях мембран, используемых для экструзии. Это особенно очевидно, когда мембраны или держатели мембран влажные. Кроме того, PCTE, РЕТЕ и другие типы мембран очень нежные и требуют осторожного манипулирования. Для облегчения данной проблемы изобретение предоставляет способы и устройство для эффективного обеспечения возможности манипулирования и загрузки мембран в держатели путем использования держателя или корпуса опоры мембран. Опорный держатель мембран может представлять собой, например, кассетный опорный держатель.
Опорный держатель мембран в одном из вариантов воплощения может состоять из опорного кольца (колец), способных фиксировать мембрану или мембраны к периметру опорного кольца (колец) в одной плоскости для предотвращения складывания и прилипания при высоких давлениях. Устройство способно удерживать мембрану или мембраны в различных конфигурациях, например мембраны можно помещать в виде «многослойной» или уложенной стопкой конфигурации. Если в патрон помещают множество мембран, мембраны могут иметь одинаковый или различный диаметр пор. Устройство или патрон могут иметь разнообразие других признаков, например кассетный держатель можно предварительно загрузить мембранами, устройство можно стерилизовать и легко включить в автоматизированное устройство замены мембран.
Устройство кассетного держателя обеспечивает преимущества минимизации манипулирования мембранами и большей эффективности при загрузке мембран. Кроме того, устройство кассетного держателя обеспечивает общее повышение эффективности при производстве, например засоренную или загрязненную мембрану можно заменить в то время, как поток продукта отклоняется в новое устройство кассетного держателя, пока происходит замена засоренного или загрязненного устройства кассетного держателя.
Липиды
Способы и устройства настоящего изобретения можно использовать для экструзии везикул, мицелл или липосом из любого подходящего вещества. В предпочтительном варианте воплощения способы и устройства настоящего изобретения можно использовать для получения липосом из липида или комбинации липидов. Можно использовать любой липид или комбинацию липидов. В предпочтительном варианте воплощения полученный экструзией липид трудно подвергнуть экструзии с использованием обычных способов и устройств. В более предпочтительном варианте воплощения трудный липид имеет значение Тс большее, чем приблизительно комнатная температура. В другом предпочтительном варианте воплощения трудный липид включает жесткую ацильную цепь. В более предпочтительном варианте воплощения жесткая ацильная цепь представляет собой мононенасыщенную ацильную цепь. В другом предпочтительном варианте воплощения трудный липид включает примесь или загрязняющий материал. В более предпочтительном варианте воплощения примесь или загрязняющий материал представляет собой смолу или примесь, которая затрудняет экструзию липида. В более предпочтительном варианте воплощения примесь или загрязняющий материал представляет собой смолу, внедренную во время процесса изготовления. В другом предпочтительном варианте воплощения трудный липид ассоциирован с другой молекулой. В более предпочтительном варианте воплощения молекула представляет собой лекарственный препарат. В другом предпочтительном варианте воплощения молекула представляет собой белок. В другом предпочтительном варианте воплощения трудный липид представляет собой заряженный липид. В другом предпочтительном варианте воплощения трудный липид трудно подвергнуть экструзии в производственном масштабе. В особенно предпочтительном варианте воплощения трудный липид выбирают из группы, состоящей из l-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолина (POPC), дипальмитоилфосфатидилхолина, дипальмитоилфосфатидилглицерина и дистеароилфосфатидилэтаноламина.
В другом предпочтительном варианте воплощения липид представляет собой легкий липид. В более предпочтительном варианте воплощения легкий липид выбирают из группы, состоящей из фосфатидилхолина яичного желтка (ЕРС), яичного фосфатидилглицерина и диолеилфосфатидилхолина.
Другие фосфолипиды, подходящие для использования с настоящем изобретением, включают, но не ограничиваются ими, дилауроилфосфатидилхолин, дилауроилфосфатидилглицерин, олеоилпальмитоилфосфатидилхолин, связанные с гликолипидами фосфолипиды, фосфатидилхолин, фосфатидилглицерин, лецитин, β,γдипальмитоил-α-лецитин, сфингомиелин, фосфатидилсерин, фосфатидовую кислоту, хлорид N-(2,3-ди(9-(Z)-октадеценилокси))проп-1-ил-N,N,N-триметиламмония, фосфатидилэтаноламин, лизолецитин, лизофосфатидилэтаноламин, фосфатидилинозитол, цефалин, кардиолипин, цереброзиды, дицетилфосфат, диолеоилфосфатидилхолин, диолеоилфосфатидилглицерин, пальмитоилолеилфосфатидилхолин, дистеароилфосфатидилхолин, стеароилпальмитоилфосфатидилхолин, дипальмитоилфосфатидилэтаноламин, дистеароилфосфатидилэтаноламин, димирстоилфосфатидилсерин, диолеилфосфатидилхолин и им подобные.
В наиболее предпочтительном варианте воплощения липид представляет собой фосфатидилхолин или сфингомиелин.
Не содержащие фосфор липиды можно также использовать в липосомах композиций настоящего изобретения. Они включают, но не ограничиваются ими, холестерин, другие стерины, стеариламин, доцециламин, ацетилпальмитат и амиды жирных кислот.
Дополнительные липиды, подходящие для использования в липосомах настоящего изобретения, хорошо известны специалистам в данной области и приводятся в разнообразных хорошо известных источниках, например McCutcheon's Detergents and Emulsifiers and McCutcheon's Functional Materials, Allured Publishing Co., Ridgewood, N.J.
Липиды, используемые в способах и устройствах настоящего изобретения, включают химически модифицированные липиды. В предпочтительном варианте воплощения липид ковалентно прикреплен к модифицирующей группе. Модифицирующая группа может воздействовать на любое свойство или свойства липида. Например, модифицирующая группа может изменить температуру перехода липида, свойства ансамбля, свойства экструзии, свойства инкапсуляции, свойства направленности действия in vivo, свойства переработки in vivo, физиологические эффекты, стабильность или период полувыведения. В предпочтительном варианте воплощения модифицированный липид является связанным с полиэтиленгликолем (PEG-связанным). В другом предпочтительном варианте воплощения модифицированный липид представляет собой связанный с PEG фосфолипид.
В другом предпочтительном варианте воплощения в способах и устройствах настоящего изобретения можно использовать комбинации липидов. Например, в способах и устройствах настоящего изобретения можно использовать фосфолипид и липид, связанный с PEG.
Подлежащий экструзии препарат может также содержать другие типы молекул. Примеры других молекул или ионов, которые могут быть ассоциированы с липидами, включают, но не ограничиваются ими, холестерин или другие стероиды или производные стероидов, растворители, буферы, кислоты, основания, соли, металлы, хелатообразующие соединения, сахара, белки, нуклиновые кислоты и лекарственные препараты, как описаны ниже (см., например, Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71).
Для получения липосом, которые предстоит ввести индивидууму, в целом желательно, чтобы липосомы состояли из липидов, которые находятся в жидкокристаллическом состоянии при 37°С, часто при 35°С и даже при 32°С. Поскольку индивидуумы обычно имеют внутреннюю температуру приблизительно 37°С, липосомы, состоящие из липидов, которые являются жидкокристаллическими при 37°С, во время лечения обычно находятся в жидкокристаллическом состоянии.
Высшее качество сырьевых материалов используют в способах частично ввиду высоких уровней давления, которые применяют. Липиды сырьевого материала должны соответствовать определенным стандартам контроля качества перед использованием в процессе экструзии. Например, следует контролировать рН, размер порошка, форму высушенного порошка, размер смоченных частиц, осмоляльность, уровень кальция, уровень вещества в виде частиц, условия сушки и уровни добавок, остаточных материалов или примесей в результате процесса производства. Указанные показатели могут воздействовать на физические характеристики липидов в растворе или суспензии, затрудняя экструзию липидов. В частности, рН следует регулировать, и он должен быть соответствующим, уровни кальция должны быть низкими, и сырьевой материал должен хорошо сушиться и иметь хорошие визуальные характеристики.
Препарат липидов
Любой препарат, включающий одно или несколько веществ, которые можно подвергнуть экструзии для образования везикул, мицелл или липосом, можно использовать в способах и устройствах настоящего изобретения. В предпочтительном варианте воплощения используют препарат, включающий один или несколько липидов. В особенно предпочтительном варианте воплощения препарат представляет собой водную суспензию, включающую один или несколько липидов. Можно использовать любой способ приготовления такого препарата (см., например, Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71 на стр.88-91; Szoka, et al., 1980, Biochim. Biophys. Acta, 601:559-71). Указанные способы в целом включают приготовление водной суспензии липидов. В предпочтительном варианте воплощения липиды формируют многослойные везикулы (MLV) в суспензии. Суспензии MLV можно подвергать экструзии для получения везикул желательного размера и ламеллярности, например SUV или LUV. Обычно используют концентрацию липидов приблизительно от 5 до 50 мМ, хотя пригодны концентрации липидов, достигающие приблизительно 400 мг/мл или более. При использовании множества липидов липиды в целом сначала смешивают в органическом растворителе, таком как хлороформ, смесь хлороформа:метанола 3:1 (об./об.) или третичный бутанол. Липиды растворяют в растворителе, обычно при температуре от около 30 до около 50°С, затем быстро замораживают, например, инкубацией на бане с сухим льдом-этанолом или сухим льдом-ацетоном. Затем органический растворитель выпаривают и сухую липидную пленку, лепешку или порошок регидратируют в соответствующем водном растворе. Регидратацию обычно проводят при температуре большей, чем Тс липида с самой высокой Тс (при использовании более чем одного липида), в водном растворе, например дистиллированной воде, дистиллированной воде с буфером, солевом растворе или сахарном растворе или другом растворе растворенных неэлектролитов. Стадия гидратации предпочтительно длится дольше чем около 1 ч и сопровождается перемешиванием, хотя ее можно осуществить даже за несколько минут, в зависимости от липида. Диапазон размера MLV, сформированных во время процесса гидратации, в целом составляет от около 500 до около 10000 нм (10 мкм) или более. Обычно более энергичное перемешивание во время гидратации способствует формированию более мелких MLV. За гидратацией необязательно следует содержание смеси в покое в течение ночи, что может содействовать последующему формированию однослойных везикул. В предпочтительном способе получения водной суспензии липидов раствор липидов в хлороформе подвергают перемешиванию вихревой мешалкой, и растворитель удаляют в постоянном потоке N2. Образец сушат в высоком вакууме. Полученную сухую липидную пленку регидратируют в 150 мМ NaCl и 20 мМ [4-(2-гидроксиэтил)]пиперазинэтансульфоновой кислоты (Hepes, pH 7,4).
В другом предпочтительном варианте воплощения подлежащий экструзии препарат включает эмульсию одного или нескольких липидов. Эмульсию можно сформировать с использованием любой известной методики и механического устройства, такого как гомогенизатор, микрофлюидизатор, или миксера, такого как рото-статор (см., например, Martin, et al., 1983, Physical Pharmacy: Physical Chemical Principles in the Pharmaceutical Sciences, Lea & Febiger Publishers, Philadelphia; Gennaro, et al., 1990, Remington's Pharmaceutical Sciences, 18th edition, Mack Publishing Company, Easton, Pennsylvania). При получении липидов можно также использовать другие методики формирования липосом, для которых невозможно достичь желаемого конечного среднего диаметра везикул или узкого диапазона диаметров везикул внутри препарата липосом, включающие, но не ограничивающиеся ими, гомогенизацию, микрофлюидизацию, обработку ультразвуком, смешиванием с высоким усилием сдвига или экструзию через металлические фритты или керамические фильтры (см., например, New, 1990, Liposomes: A Practical Approach, Oxford University Press, New York, Chapter 2).
В другом предпочтительном варианте воплощения липосомы формируют в условиях высокой эффективности инкапсуляции. Предпочтителен способ обратной фазы выпаривания. Везикулы обратной фазы выпаривания (REV), сформированные данным способом, характеризуются (а) наличием одной или нескольких двухслойных структур, (b) эффективностью инкапсуляции обычно приблизительно 20-50% и (с) широким спектром размеров приблизительно от 500 до 20000 нм (20 мкм). Обзор указанных и других способов получения липосом см. в публикации Szoka, et al., 1980, Biochim. Biophys. Acta, 601:559-71.
Препарат, который предстоит подвергнуть экструзии, может включать любое вещество, которое желательно инкапсулировать или связать с везикулой, мицеллой или липосомой. В предпочтительном варианте воплощения вещество представляет собой холестерин или другой стероид или стероидное производное, растворитель, буфер, кислоту, основание, соль, металл, хелатообразующее соединение, сахар, белок, нуклеиновую кислоту или лекарственный препарат (см., например, Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71). В более предпочтительном варианте воплощения вещество представляет собой холестерин, полиэтиленгликоль, алкилсульфат, бромид аммония или альбумин. В другом более предпочтительном варианте воплощения вещество представляет собой лекарственный препарат. Липосомы можно использовать, например, для изменения тканевого распределения и захвата лекарственных препаратов терапевтически благоприятным образом и для увеличения удобства лечения путем обеспечения возможности менее частого введения лекарственного препарата (см., например, Poznansky et al., 1984, Pharmacol. Rev. 36:277-336). В еще более предпочтительном варианте воплощения лекарственный препарат представляет собой антигиперлипидемическое средство (см. The Physicians' Desk Reference (54th ed., 2000)). В еще более предпочтительном варианте воплощения антигиперлипидемическое средство представляет собой гидрохлорид колестипола, этил-2-(пара-хлорфенокси)-2-метилпропионат, гемфиброзил, фенофибрат, церивастатин натрий, флювастатин натрий, аторвастатин кальций, ловастатин, правастатин натрий, симвастатин или никотиновую кислоту (см. там же). В другом более предпочтительном варианте воплощения лекарственный препарат представляет собой антибиотик. В еще более предпочтительном варианте воплощения антибиотик представляет собой доксорубицин (см. там же на стр.508). В другом еще более предпочтительном варианте воплощения антибиотик представляет собой амфотерицин В (см. там же на стр.1653). В другом предпочтительном варианте воплощения противораковый лекарственный препарат представляет собой винкристин, митоксантрон или другие противораковые лекарственные препараты (см., например, Bally, et al., 1990, Biochim. Biophys. Acta 1023: 133-9; Sugarman, et al., 1992, Crit. Rev. Oncol. Hematol. 12:231-42, Kim, et al., 1993, Drugs 46:618-38; Lim, 1997, J. Pharmacol. Exp. Ther. 281:566-73; Fielding, 1991, Clin. Pharmokinet. 21:155-64).
Для липосом, которые предполагают применять in vivo, можно использовать водный буфер, включающий фармацевтически приемлемый носитель. Композиции могут содержать фармацевтически приемлемые вспомогательные вещества, которые требуются для приближения к физиологическим условиям, такие как регулирующие рН и буферные агенты, агенты, регулирующие тоничность, и им подобные, например ацетат натрия, лактат натрия, хлорид натрия, фосфат натрия, хлорид калия, хлорид кальция и т.д. В предпочтительном варианте воплощения используют водный буфер, который имеет приблизительно физиологическую осмоляльность (т.е. 290 мОсм/кг). Примеры таких буферов включают 0,9% солевой, 5% декстрозный и 10% сахарозный растворы. Можно использовать много других фармацевтически приемлемых носителей. Обычно в качестве фармацевтически приемлемого носителя используют физиологический солевой раствор. Другие подходящие носители включают, например, воду, воду с буфером, 0,4% солевой раствор, 0,3% глицин и им подобные, включающие гликопротеины для усиления стабильности, такие как альбумин, липопротеин, глобулин и т.д.
Препарат, который предстоит подвергнуть экструзии, также может содержать примеси или загрязняющие материалы, хотя в предпочтительном варианте воплощения данные вещества удаляют из водного раствора до, во время или после процесса экструзии.
Данные композиции можно стерилизовать обычными, хорошо известными методиками стерилизации. Полученные водные растворы можно упаковывать для использования или профильтровать в асептических условиях и лиофилизировать, причем лиофилизированный препарат объединяют со стерильным водным раствором перед введением.
Виды применения липосом
Везикулы, мицеллы и липосомы, созданные с использованием способов и устройств настоящего изобретения, можно использовать любым образом, которым можно применять везикулы, мицеллы и липосомы, созданные с использованием обычных методик. В предпочтительном варианте воплощения липосомы, созданные с использованием способов и устройств настоящего изобретения, используют для доставки лекарственного препарата или фармацевтически активного вещества пациенту (см., например, патенты США № 4769250, 4906477, 5736155, 6060080; Poznansky et al., 1984, Pharmacol. Rev. 36:277-336; Lim, 1997, J. Pharmacol. Exp. Ther. 281:566-73; Kim, et al., 1993, Drugs 46:618-38; Fielding, 1991, Clin. Pharmokinet. 21:155-64; Sugarman, et al., 1992, Crit. Rev. Oncol. Hematol. 12:231-42; Bally, et al., 1990, Biochim. Biophys. Acta 1023: 133-39). В более предпочтительном варианте воплощения липосома предпочтительно доставляет лекарственный препарат или фармацевтически активное вещество к ткани или типу клеток у индивидуума. В другом предпочтительном варианте воплощения липосомы инкапсулируют нуклеиновую кислоту (см. Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71). В особенно предпочтительном варианте воплощения нуклеиновая кислота представляет собой антисмысловую нуклеиновую кислоту, используемую для ингибирования экспрессии гена. В другом особенно предпочтительном варианте воплощения липосому, содержащую нуклеиновую кислоту, используют в последовательности операций генной терапии для лечения, например, генетического заболевания (такого как, например, кистозный фиброз, болезнь Гоше, серповидноклеточная анемия, талассемия, гемофилия или семейная гиперхолестеринемия), рака (например, усилением иммуногенности опухоли, усилением активности иммунных клеток, инсерцией суицидного гена в опухоль, инсерцией в опухоль гена-суппрессора опухоли, блокировкой экспресси гена, защитой стволовых клеток или инсерцией кодирующих токсины генов под контролем специфичного для опухоли промотера), инфекционного заболевания (такого как, например, синдром приобретенного иммунодефицита, гепатит или герпес), неврологического заболевания (такого как, например, болезнь Паркинсона, болезнь Альцгеймера или боковой амиотрофический склероз), сердечно-сосудистого заболевания (такого как, например, атеросклероз, рестеноз, тромбоз или ишемия сердца) или любого заболевания или состояния (такого как, например, артрит, астма, диабет, остеопороз и немощные состояния, связанные с пожилым возрастом) (см, Lasic, 1997, Liposomes in Gene Delivery, CRC Press LLC, Boca Raton 67-71 на стр.8-13).
В особенно предпочтительном варианте воплощения способы и устройства настоящего изобретения используют для изготовления липосом, которые можно использовать для лечения атеросклероза, как описано в патентах США № 5746223, 6367479, 6079416, 6080422, 5736157, 5948435, 5858400, 5843474, 6312719 и 6139871. Липосомы можно связать с белком или полипептидом для увеличения скорости переноса холестерина или способности липосомы нести холестерин. Особенно полезно связывание аполипопротеинов с липосомами. Аполипопротеин А1, аполипопротеин А2 и аполипопротеин Е или их фрагменты, производные, агонисты, аналоги или пептидные миметики будут в целом самыми полезными аполипопротеинами для связывания с липосомами (см., например, патенты № 6037323, 6004925 и 6046166). Данные аполипопротеины способствуют переносу холестерина и сложных холестериловых эфиров в печень для метаболизма. Лецитин-холестериновую ацилтрансферазу можно также использовать для метаболизирования свободного холестерина в сложные холестериловые эфиры. Липосомы могут быть связаны с молекулами аполипопротеина А1, аполипопротеина А2 и лецитин-холестериновой ацилтрансферазы или их фрагментами, производными, агонистами, аналогами или пептидными миметиками, отдельно или в любой комбинации и молярном соотношении.
В предпочтительном варианте воплощения липосомы для лечения пациента, осуществляемого в соответствии со способами и устройствами настоящего изобретения, присутствуют в физиологически приемлемом буфере, носителе или разбавителе. Концентрация липосом в буфере, носителе или разбавителе может варьироваться. В целом, концентрация составит приблизительно 20-300 мг/мл, обычно приблизительно 100-300 мг/мл, а наиболее часто, приблизительно 100-200 мг/мл. Специалисты в данной области могут изменять указанные концентрации для оптимизации лечения различными липосомальными компонентами или для конкретных пациентов. Например, концентрацию можно увеличить для снижения жидкостной нагрузки, связанной с лечением. Это может быть особенно желательно у пациентов, имеющих связанную с атеросклерозом застойную сердечную недостаточность или тяжелую гипертензию. Альтернативно, липосомы, составленные из раздражающих липидов, можно разбавить до низких концентраций для уменьшения воспаления в участке введения.
ПРИМЕРЫ
1. Экструзия 20% РОРС через поликарбонатные подвергнутые образующему каналы пор протравливанию мембраны с размером пор 0,1 мкм при давлении 600 фунтов/кв. дюйм
Следующий пример демонстрирует, что трудный липид может засорить или загрязнить мембрану для экструзии при использовании обычных способов и устройств, однако в этих случаях можно выгодно использовать промывающий агент.
2 г l-пальмитоил-2-олеоил-sn-глицеро-3-фосфохолина (POPC) (Genzyme, Cambridge MA, каталожный № LP-04-031) добавляли к 8 мл солевого раствора с фосфатным буфером (PBS) (140 мМ солевой раствор, 20 мМ фосфат, рН ˜7,4) в 50 мл конической пробирке и энергично встряхивали рукой в течение приблизительно 5 мин для образования однородной суспензии РОРС MLV в PBS с концентрацией 200 мг/мл. В экструдер LIPEXTM (Northern Lipids, Vancouver, British Columbia, Canada) емкостью 10 мл устанавливали стопку из 2 поликарбонатных подвергнутых образующему каналы пор протравливанию мембран (PCTE) NUCLEOPORETM c диаметром пор 0,1 мкм (Whatman, Ann Arbor, MI; каталожный № 110605) в соответствии с инструкциями изготовителя экструдера и промывали PBS. Суспензию POPC-PBS MLV пропускали через стопку мембран под давлением 600 фунтов/кв. дюйм. Общее время, требовавшееся для экструзии объема 10 мл, составило 17 мин 32 с. Была предпринята попытка второго пропускания через ту же мембрану, но она была прекращена через 25 мин. В то время только около 2,5 мл суспензии прошли через стопку мембран, указывая на то, что она засорилась или загрязнилась. Это было подтверждено путем добавления этанола в устройство и продолжением экструзии. 100% этанол добавляли в резервуар экструдера для доведения конечной концентрации этанола 10%. Приблизительно 0,8 мл 100% этанола добавляли в стакан, доводя концентрацию этанола в содержимом приблизительно до 10% перемешиванием в стакане вихревой мешалкой в течение 2 мин. Подача в экструдер давления 600 фунтов/кв. дюйм позволила продолжать экструзию, указывая на то, что фильтры засорились или загрязнились РОРС MLV.
2. Экструзия 20% РОРС через стопку из 2 PCTE мембран PORETICSTM и NUCLEPORETM под давлением 400 и 800 фунтов/кв. дюйм
Пример демонстрирует, что экструзия 20% суспензии POPC продолжается при значительно меньшем засорении или загрязнении при использовании PCTE мембран PORETICSTM (Osmonics, Minnetonka MN), чем PCTE мембран NUCLEOPORETM, и что различие работы указанных двух мембран увеличивается с увеличением давления.
Получали 20% суспензию POPC GENZYMETM и подвергали ее экструзии через экструдер LIPEXTM емкостью 10 мл, как описано в примере 1. В отдельных испытаниях экструдер был укомплектован стопкой из 2 PCTE мембран либо PORETICSTM, либо NUCLEOPORETM со средним размером пор 0,1 мкм (соответственно Osmonics, PORETICSTM, каталожный № К01СР02500 и Whatman NUCLEOPORETM, каталожный № 110605). В отдельных испытаниях экструзии проводили при 400 или 800 фунтах/кв. дюйм. Как показано на фиг.1, даже при 400 фунтах/кв. дюйм PCTE мембраны PORETICSTM засорялись или загрязнялись меньше, чем PCTE мембраны NUCLEOPORETM. Данное различие также наблюдается при давлении 800 фунтов/кв. дюйм.
3. Экструзия 20% POPC через полиэфирные, подвергнутые образующему каналы пор протравливанию мембраны (PETE)
Данный пример демонстрирует, что липид можно пропустить через гидрофильную мембрану для экструзии без засорения или загрязнения мембраны.
В отдельных испытаниях 10 мл суспензии POPC MLV в PBS с концентрацией 200 мг/мл (полученной как описано в примере 1) подвергали экструзии через полиэфирные, подвергнутые образующему каналы пор протравливанию мембраны (PETE), каталожные № Т04СР02500 (средний диаметр пор 0,4 мкм, диаметр мембран 25 мм), T02CP047FX (средний диаметр пор 0,2 мкм, диаметр мембран 47 мм (обрезанные вручную до диаметра 25 мм)) и Т01СР02500 (средний диаметр пор 0,1 мкм, диаметр мембран 25 мм). Результаты представлены в таблице 1. Свежую партию POPC MLV готовили для каждого испытания. Экструдер промывали солевым раствором в промежутке между каждым испытанием. Средний размер частиц полученной экструзией суспензии определяли QELS с использованием измерителя частиц 380 ZLS (Nicomp, Santa Barbara, CA) в соответствии с инструкциями изготовителя.
Данные результаты демонстрируют, что PETE мембраны не засоряются или загрязняются в условиях, когда PCTE мембраны засоряются или загрязняются. Кроме того, данные результаты демонстрируют, что размер частиц, полученных в результате экструзии липида, можно уменьшить увеличением давления экструзии.
4. Экструзия 20% ЕРС через стопку из 5 РЕТЕ мембран под высоким и низким давлением
Данный пример демонстрирует, что относительно легкий липид можно подвергнуть экструзии через гидрофильную мембрану.
20% раствор ЕРС готовили доведением 6 г LIPOID EPC® (Lipoid, Ludwigshafen, Germany), фосфатидилхолина из яичного желтка до общего объема 30 мл в солевом растворе (Abbott, Abbott Park, IL) в конической колбе емкостью 50 мл. Колбу встряхивали рукой в течение 5 мин до тех пор, пока раствор не становился визуально однородным. В экструдер LIPEXTM емкостью 10 мл устанавливали стопку из 5 PETE мембран PORETICSTM (каталожный № Т01СР02500) диаметром 25 мм со средним диаметром пор 0,1 мкм. В двух отдельных испытаниях 10 мл суспензии ЕРС 10 раз пропускали через фильтр или под давлением 400, или 800 фунтов/кв. дюйм. Экструдер очищали между испытаниями. Результаты данных испытаний показаны в таблице 2.
Таким образом, экструзия ЕРС под высоким давлением через РЕТЕ мембраны увеличивает скорости потока и уменьшает размер частиц.
5. Экструзия 20% РОРС через одиночную РСТЕ или РЕТЕ мембрану под давлением 800 фунтов/кв. дюйм
Данный пример демонстрирует, что экструзия через РЕТЕ мембрану дает бульшую скорость потока, чем экструзия через РСТЕ мембрану.
Получали 20% суспензию GENZYMETM POPC и подвергали ее экструзии через экструдер LIPEXTM емкостью 10 мл, как описано в примере 1. В отдельных испытаниях экструдер был оснащен либо одной РЕТЕ мембраной PORETICSTM со средним размером пор 0,1 мкм, либо одной РСТЕ мембраной PORETICSTM со средним размером пор 0,1 мкм (соответственно Osmonics, каталожные № Т01СР02500 и К01СР02500). Как показано на фиг.2, в данных условиях РСТЕ мембрана продуцирует частицы меньшего размера при меньшем количестве прохождений, чем РЕТЕ мембрана (фиг.2А). Однако экструзия через РЕТЕ мембрану происходила при скорости потока, которая была приблизительно в 3 раза выше, чем скорость потока, достигнутая при РСТЕ мембране (фиг.2В).
6. Экструзия 20% РОРС через стопку из 5 РЕТЕ мембран под давлением 600 фунтов/кв. дюйм
Данный пример демонстрирует, что суспензию трудного липида можно эффективно превратить в суспензию SUV экструзией через гидрофильную мембрану под умеренно высоким давлением.
20% суспензию GENZYMETM POPC готовили, как описано в примере 1. В экструдер LIPEXTM емкостью 10 мл устанавливали стопку из 5 РЕТЕ мембран PORETICSTM со средним размером пор 0,1 мкм (каталожный № Т01СР02500). Суспензию РОРС подвергали экструзии через мембраны при пяти прохождениях при давлении 600 фунтов/кв. дюйм. Результаты показаны в таблице 3.
7. Экструзия РОРС через стопку из 2 РСТЕ и РЕТЕ мембран при давлении 400 и 800 фунтов/кв. дюйм
Данный пример демонстрирует, что РЕТЕ мембраны засоряются или загрязняются гораздо труднее, чем РСТЕ мембраны с расположенными под углом порами при высоком давлении.
В некоторых из ранее проведенных экспериментов часть суспензии липида, подвергнутого экструзии, была утрачена после экструзии ввиду избыточной утечки газообразного азота при высоких скоростях из выпускной трубки сбора в конце экструзии, проводимой под высоким давлением. Данный утекающий газ часто вызывал сдувание выпускной трубки с основания экструдера, а также вызывал разбрызгивание полученного раствора из контейнера сбора. Для решения данной проблемы была установлена предохранительная трубка для предотвращения сдувания выпускной трубки сбора с основания экструдера. Предохранительная трубка представляла собой по существу отрезок трубки большего диаметра, чем диаметр ввинченной более тонкой выпускной трубки сбора. Предохранительная трубка обеспечивала дополнительное трение основной пластины о выпускную трубку сбора. Для дополнительной регулировки экструзии раствора устанавливали кольцевую стойку для ее действия в качестве направляющей, заставляющей трубку оставаться в правильной ориентации, причем полученная экструзией суспензия адекватно собиралась в сосуд для сбора. Указанные два дополнения к устройству добавили достаточный дополнительный контроль выпускной трубки сбора для предотвращения потери большей части продукта.
20% суспензию GENZYMETM POPC готовили, как описано в примере 1. В отдельных испытаниях в экструдер LIPEXTM емкостью 10 мл устанавливали стопку из 2 РЕТЕ мембран PORETICSTM (каталожный № Т01СР02500) или РСТЕ мембран (каталожный № К01СР02500) со средним размером пор 0,1 мкм. Для каждой из указанных установок суспензию РОРС подвергали экструзии через мембраны при давлении либо 400, либо 800 фунтов/кв. дюйм, и объем полученной экструзией суспензии, которую можно было обработать одним прохождением, измеряли как функцию времени. Результаты представлены на фиг.3. На фиг.3А показано, что при давлении 400 фунтов/кв. дюйм нет значимого различия между РЕТЕ и РСТЕ мембранами. На фиг.3В показано, что при высоком давлении конфигурация РЕТЕ мембраны может обработать значительно больший объем, чем конфигурация РСТЕ мембраны, до того как мембрана становится засоренной или загрязненной.
8. Экструзия 20% РОРС через стопку из 1, 2, 5 и 10 РЕТЕмембран
Следующий пример демонстрирует влияние количества мембран на эффективность получения POPC LUV.
20% суспензию GENZYMETM POPC готовили и подвергали экструзии через экструдер LIPEXTM емкостью 10 мл, как описано в примере 1. В отдельных испытаниях экструдер оснащали 1, 2, 5 или 10 РЕТЕ мембранами PORETICSTM (Osmonics Poretics, каталожный № Т01СР02500) со средним размером пор 0,1 мкм. Все эксперименты проводили при давлении 800 фунтов/кв. дюйм. Результаты показаны на фиг.4. На фиг.4А показана связь между количеством прохождений и средним диаметром частиц, полученных LUV. В целом, существует обратная корреляция между количеством мембран в стопке и количеством прохождений, требуемых для получения LUV желательного среднего диаметра. На фиг.4В показана связь между количеством прохождений и скоростью потока. Для каждого данного количества прохождений скорость потока обратно пропорциональна количеству фильтров в стопке. Как показано на фиг.4С, количество прохождений, требуемое для получения LUV среднего диаметра 120 нм, несколько меньше для стопки из 5 мембран (4 прохождения), чем для стопки из 10 мембран (5 прохождений).
9. Экструзия 20% РОРС через стопку из 5 РЕТЕ мембран при давлении 400, 600 и 800 фунтов/кв. дюйм
Данный пример демонстрирует влияние давления на эффективность получения POPC LUV.
Получали 20% суспензию GENZYMETM POPC и подвергали ее экструзии через экструдер LIPEXTM емкостью 10 мл, как описано в примере 1. Экструдер оснащали стопкой из 5 РЕТЕ мембран PORETICSTM (Osmonics PoreticsТМ, каталожный № Т01СР02500) со средним размером пор 0,1 мкм. В отдельных испытаниях экструзию проводили при давлении 400, 600 или 800 фунтов/кв. дюйм. Как показано на фиг.5А, получение частиц меньшего размера достигали после меньшего числа прохождений с использованием давления 600 или 800 фунтов/кв. дюйм по сравнению с давлением 400 фунтов/кв. дюйм. На фиг.5В показано, что скорость потока для данного прохождения была приблизительно вдвое больше при давлении 800 фунтов/кв. дюйм, чем при давлении 600 фунтов/кв. дюйм, а скорость потока при давлении 600 фунтов/кв. дюйм была приблизительно вдовое больше, чем скорость потока при давлении 400 фунтов/кв. дюйм. На фиг.5С показано, что для получения LUV со средним диаметром приблизительно 120 нм необходимо 8 прохождений при давлении 400 фунтов/кв. дюйм, 5 прохождений при давлении 600 фунтов/кв. дюйм и 4 прохождения при давлении 800 фунтов/кв. дюйм.
10. Экструзия GENZYMETM POPC через стопку из 2 РСТЕ и РЕТЕ мембран PORETICSTM и РСТЕ мембран NUCLEOPORETM при давлении 400-1500 фунтов/кв. дюйм
Данный пример демонстрирует, что увеличение давления экструзии через РЕТЕ мембрану вызывает неожиданно большое уменьшение загрязнения или засорения мембраны и, таким образом, неожиданно большое увеличение способности мембраны обрабатывать липид по сравнению с экструзией через РСТЕ мембрану. Данный пример, кроме того, демонстрирует, что нет видимого верхнего предела данного эффекта.
20% суспензию РОРС готовили, как описано выше. В отдельных испытаниях в экструдер LIPEXTM емкостью 10 мл устанавливали либо стопку из 2 РЕТЕ или РСТЕ мембран PORETICSTM, или РСТЕ мембран NUCLEOPORETM со средним размером пор 0,1 мкм (соответственно Osmonics PORETICSTM, каталожные № Т01СР02500, К01СР02500 и Whatman Nucleopore, каталожный № 110605). Для каждой из указанных установок суспензию РОРС подвергали экструзии через мембраны при давлении в диапазоне от 400 фунтов/кв. дюйм до 1500 фунтов/кв. дюйм. Массу подвергнутой экструзии суспензии РОРС измеряли как функцию времени, и рассчитывали максимальное количество суспензии, которую могла пропустить каждая мембрана при данном давлении. Данные расчеты наносили на график зависимости от давления экструзии, как показано на фиг.6. Для каждого использованного типа мембран максимальное количество суспензии, обработанное перед тем, как мембрана становилась полностью засоренной, линейно увеличивалось с увеличением давления экструзии. Нет видимого верхнего предела линейности данного увеличения. Наклон кривой графика каждой мембраны представляет собой показатель степени улучшения для мембраны по мере увеличения давления. Наклоны для нанесенных на графики результатов для РЕТЕ PORETICSTM, РСТЕ PORETICSTM и РСТЕ NUCLEOPORETM мембраны составили соответственно 0,051, 0,028 и 0,015.
11. Экструзия 20% POPC через стопку из 2 РЕТЕ мембран с пошаговым уменьшением размера пор при давлении до 5000 и 8000 фунтов/кв. дюйм
Данный пример демонстрирует, что использование более высоких уровней давления экструзии быстрее уменьшает размер частиц, и поэтому желаемый размер частиц достигается при меньшем количестве прохождений при экструзии. Пример аналогичен ситуации, описанной в примере 9 (фиг.5С), за исключением того, что в данном примере способ обработки экструзией с пошаговым понижением применяли в комбинации с более высокими уровнями давления экструзии, и материал пропускали через стопки из двойных мембран с уменьшающимися диаметрами размеров пор. Ввиду более высоких уровней давления экструзии, для достижения желательного размера частиц требуется меньшее количество прохождений экструзии, а следовательно, значительно уменьшается общее время обработки.
В отдельных испытаниях 20% суспензии РОРС получали гидратацией РОРС в солевом растворе с фосфатным буфером. Полученные растворы затем пропускали в виде дискретных прохождений через мембраны для экструзии при уровнях давления экструзии либо 5000, либо 8000 фунтов/кв. дюйм. Первое прохождение при экструзии осуществляли через стопку из 2 РЕТЕ мембран PORETICSTM с диаметром пор 0,4 мкм, второе прохождение осуществляли через стопку из 2 РЕТЕ мембран PORETICSTM с диаметром пор 0,2 мкм и остальные прохождения осуществляли через стопку из 2 РЕТЕ мембран PORETICSTM с диаметром пор 0,1 мкм. Измерения размера частиц проводили после каждого прохождения при экструзии. Данные в таблице 4 показывают, что количество прохождений, требовавшееся для достижения среднего диаметра размера частиц менее чем 140 нм, уменьшено вследствие более высоких уровней давления.
12. Экструзия 20% POPC через стопку из 2 мембран Whatman ANOPORETM при уровнях давления до 1500 фунтов/кв. дюйм
Данный пример демонстрирует, что использование более высоких уровней давления экструзии увеличивает объем экструзии и уменьшает засорение или загрязнение. В данном примере готовили 20% POPC и проводили ее экструзию через стопку из 2 неорганических мембран из оксида алюминия Whatman ANOPORETM при меняющихся уровнях давления. Больший объем материала мог течь через мембраны при более высоком давлении.
Были описаны различные варианты воплощения изобретения. Описания и примеры предназначены для иллюстрации изобретения, а не для его ограничения. Действительно, для специалистов в данной области будет очевидно, что можно внести модификации в различные описанные варианты воплощения изобретения без отхода от сущности изобретения или объема притязаний, определяемого прилагаемой формулой изобретения, представленной ниже.
Все приведенные в настоящем описании ссылки полностью включены в него в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСОВЕРШЕНСТВОВАННЫЕ ЛИПОСОМЫ И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2482837C2 |
| ВЫСУШЕННЫЕ ВОССТАНОВЛЕННЫЕ ВЕЗИКУЛЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2443412C2 |
| ВЫСОКОЭФФЕКТИВНАЯ ИНКАПСУЛЯЦИЯ ГИДРОФИЛЬНЫХ СОЕДИНЕНИЙ В УНИЛАМЕЛЛЯРНЫЕ ЛИПОСОМЫ | 2018 |
|
RU2788456C2 |
| ЛИПОСОМНЫЙ СОСТАВ И ЕГО ПОЛУЧЕНИЕ | 2013 |
|
RU2649805C2 |
| ЛИПОСОМНЫЙ СОСТАВ И ЕГО ПОЛУЧЕНИЕ | 2018 |
|
RU2728976C2 |
| НОВЫЕ КОМПОЗИЦИИ ЛИПОСОМ | 2006 |
|
RU2454229C2 |
| НАЦЕЛИВАЮЩИЕ АМИНОКИСЛОТНЫЕ ЛИПИДЫ | 2013 |
|
RU2654210C2 |
| СИСТЕМА ДОСТАВКИ ЛЕКАРСТВ ДЛЯ ГИДРОФОБНЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 2002 |
|
RU2279872C2 |
| ЗАМЕДЛЕННОЕ ВЫСВОБОЖДЕНИЕ ПРОТИВОИНФЕКЦИОННЫХ АГЕНТОВ | 2006 |
|
RU2438655C2 |
| УЛУЧШЕННЫЕ ЛИПОСОМАЛЬНЫЕ СОСТАВЫ ЛИПОФИЛЬНЫХ СОЕДИНЕНИЙ | 2011 |
|
RU2641605C2 |
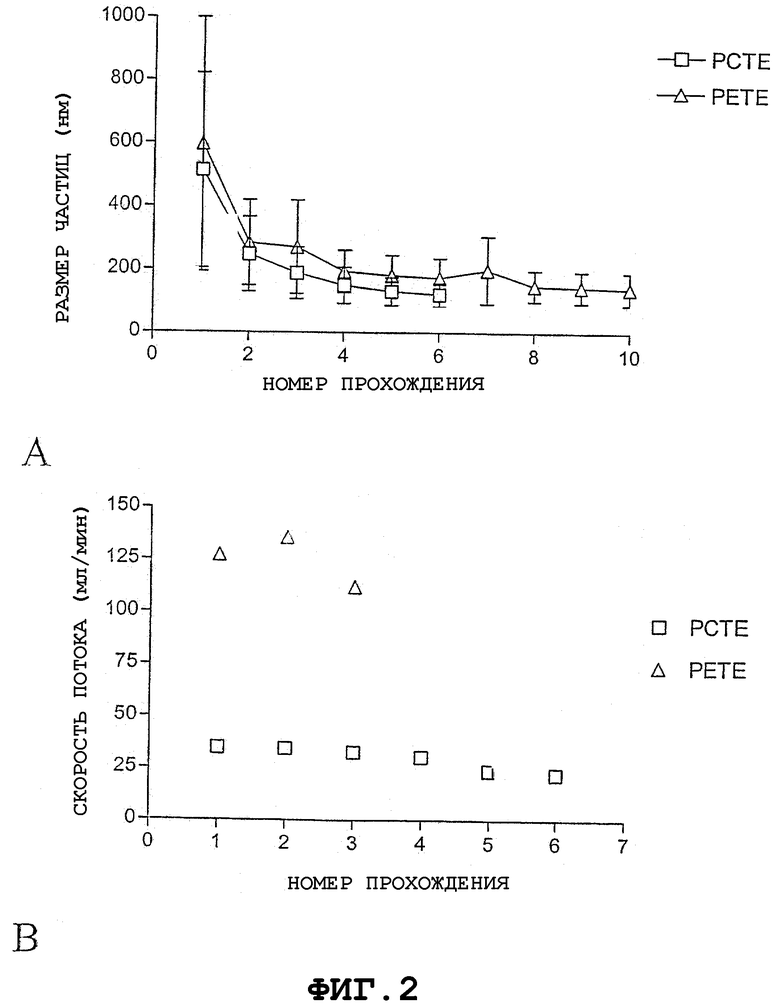
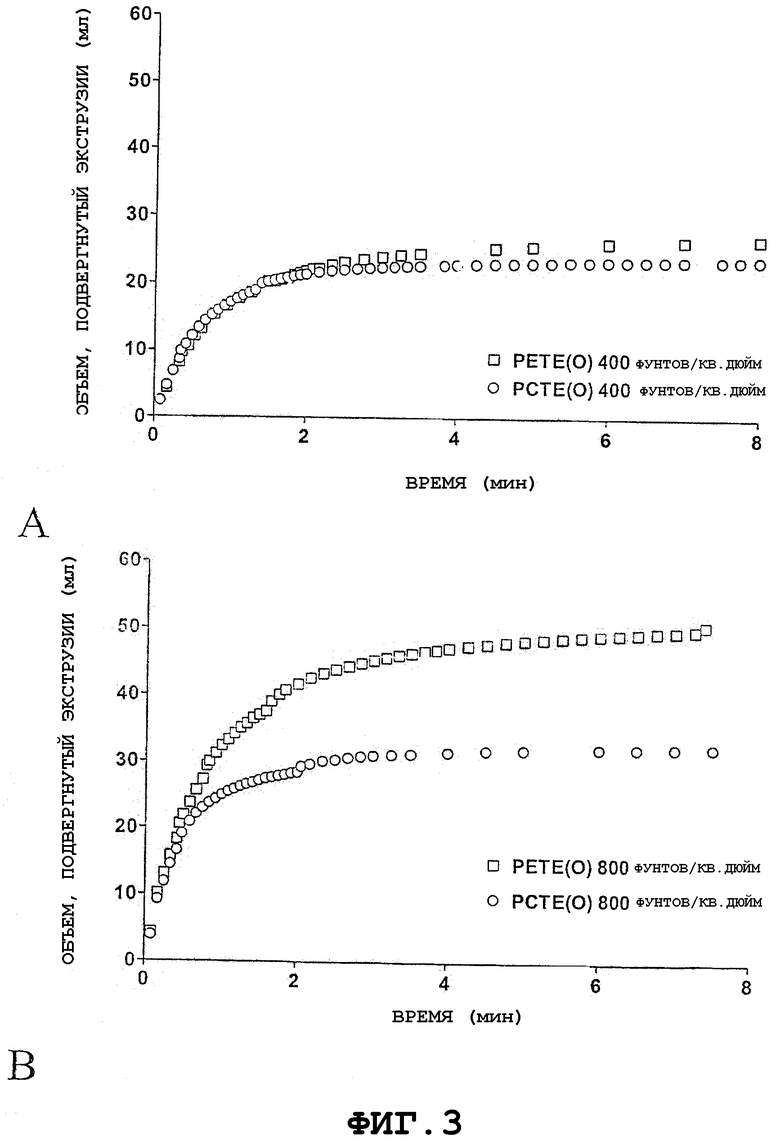
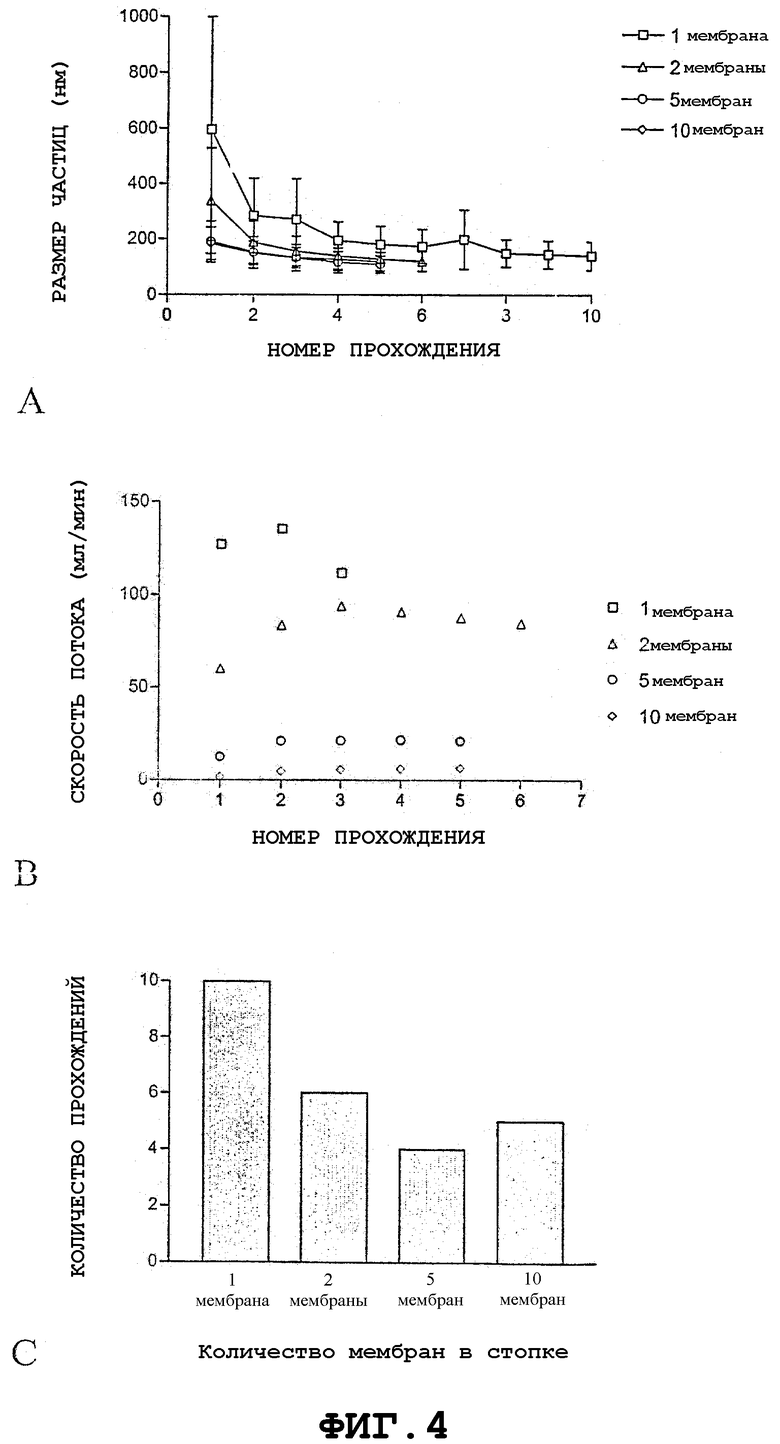
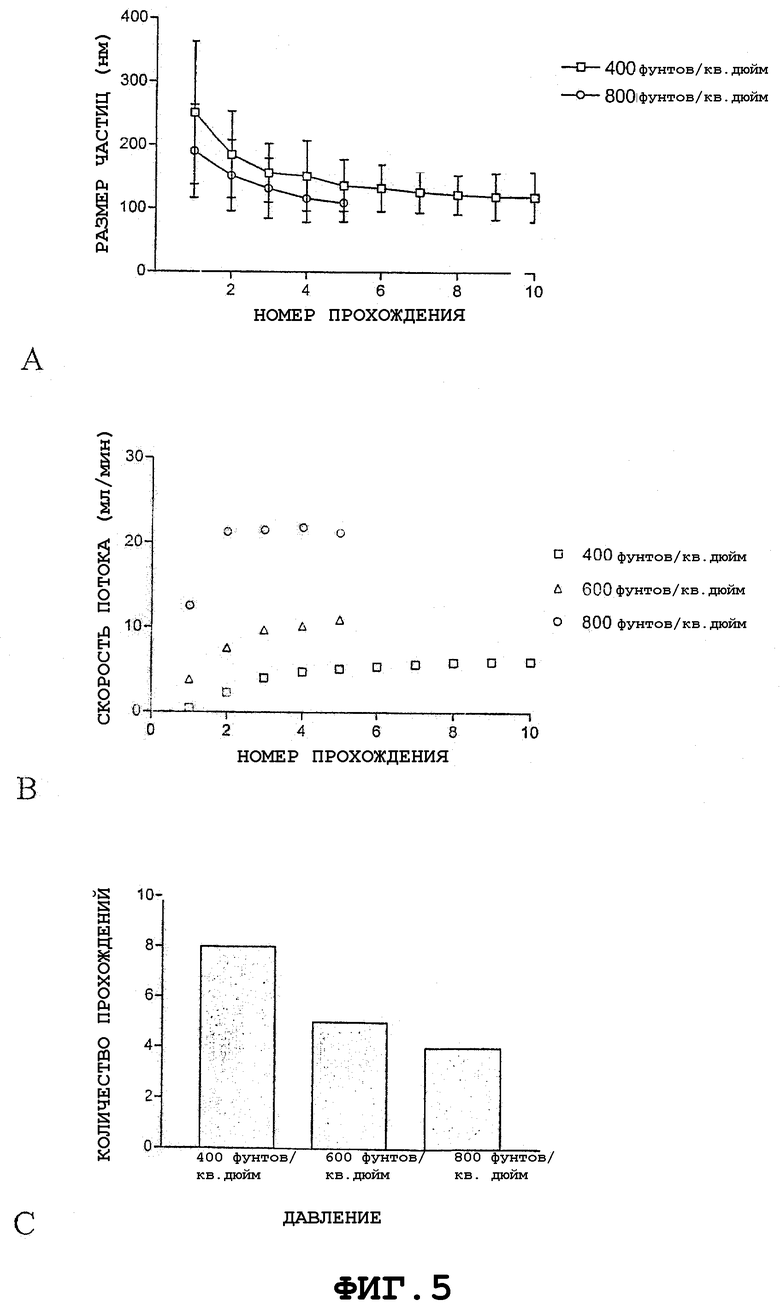
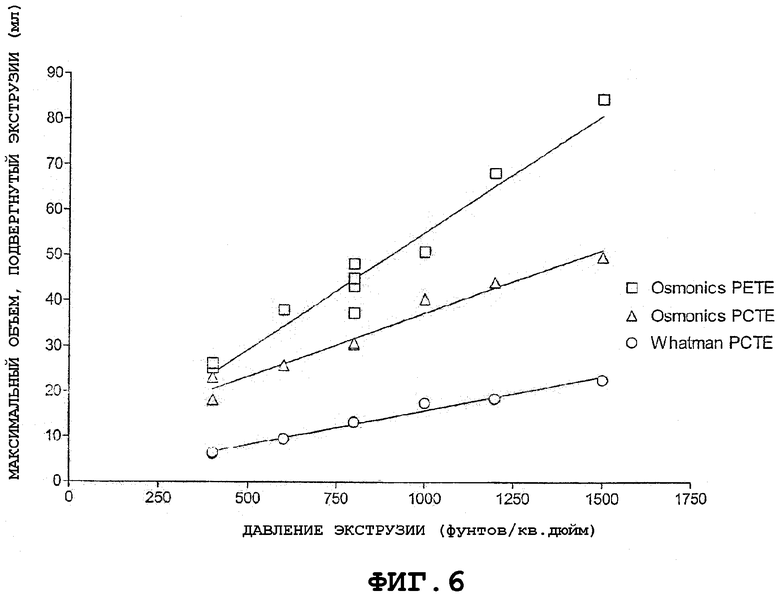
Изобретение относится к медицине, в частности к способу и устройству для получения везикул, включающих мицеллы, и в частности липосомы, экструзией растворов, включающих материалы, способные образовывать везикулы, через сетчатую мембрану под высоким давлением более 400 фунтов/кв. дюйм. Требуемый размер частиц менее 140 нм достигается значительно быстрее, что существенно снижает общие временные затраты на производство. 3 н. и 35 з.п. ф-лы, 5 табл., 6 ил.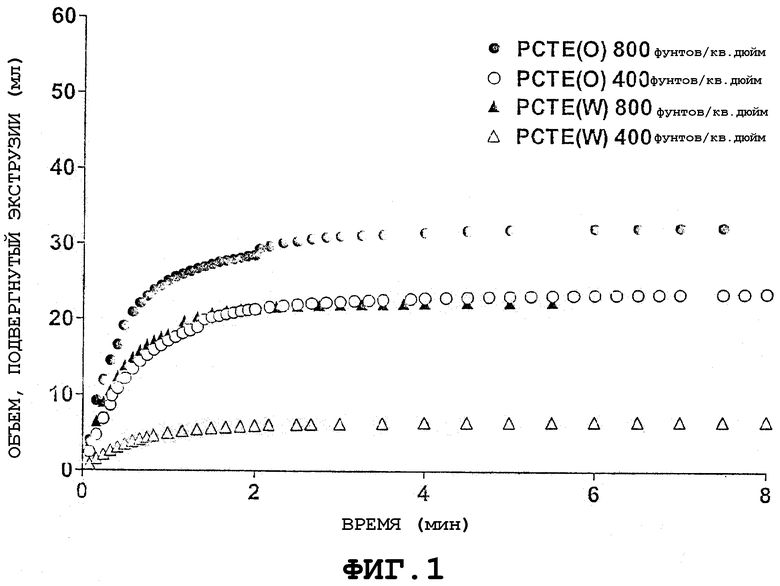
(a) экструзию смеси, содержащей липид, через гидрофильную сетчатую мембрану, имеющую поверхностное натяжение более 43 дин/см, под давлением более 400 фунтов/кв. дюйм; и
(b) выделение полученных везикул.
(a) экструзию смеси, содержащей липид, через полиэфирную сетчатую мембрану под давлением более 400 фунтов/кв. дюйм; и
(b) выделение полученных везикул.
| US 4927637 А, 22.05.1990 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМ | 1994 |
|
RU2071765C1 |
| RU 94027344 A1, 10.05.1996. | |||
Авторы
Даты
2007-04-27—Публикация
2002-09-27—Подача