Настоящее изобретение относится к новому способу получения тиофенолов и к их применению в качестве промежуточных продуктов при получении гербицидов изобензофуранонового типа.
В соответствии с работой Methoden der organischen Chemie (Houben-Weyl), том 9, 12 (1955), тиофенолы могут быть получены, например, диазотированием анилина и последующей реакцией полученной диазониевой соли с этилксантогенатом калия в основной спиртовой среде. В СЬеш.Вег. 10, 2959 (1968) говорится, что тиофенолы могут быть получены реакцией фенилдиазониевой соли с полисульфидом натрия. В соответствии с The Chemistry of the Thiol Group, часть 1, 220 (1974) и Chem.Ber. 120, 1161, вместо полисульфидов могут быть также использованы дисульфиды, и в качестве приемлемого реагента в Pestic. Sci. 1996, 47, 332 указан динатрийсульфид.
Было установлено, что получение тиофенолов может быть значительно улучшено, если в реакции соответствующих фенилдиазониевых солей вместо ксантогенатов, полисульфидов или сульфидов использовать элементарную серу.
Таким образом, объектом настоящего изобретения является способ получения тиофенолов формулы
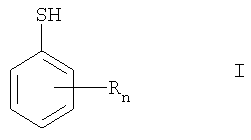
в которой n обозначает целое число от 1 до 5, а
R обозначает водородный атом, алкил, гидроксиалкил, алкиламино-,диалкиламино-, алкенил, алкинил, алкокси, алкилтио, фенил, нафтил, фенокси, фенилтио, атом галогена, гидроксил, меркапто-, карбоксил, сульфо-, гидроксиламиногруппу или гетероциклил, реакцией фенилдиазониевой соли формулы
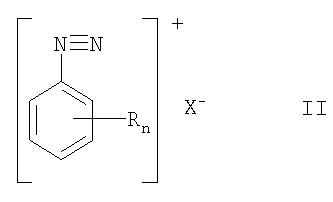
в которой n и R имеют указанные значения, а Х обозначает атом галогена или бисульфат, с серой при повышенной температуре в присутствии водного основания и выделением соединений формулы I.
У соединений формулы I в предпочтительном варианте n обозначает целое число от 1 до 3. Значение n преимущественно составляет 2. Было установлено, что эти соединения формулы I, которые содержат карбоксильную или сульфогруппу, или их соли особенно приемлемы и представляют особую ценность. Было показано, что соединение формулы I, которое, в частности, содержит карбоксильную группу в орто-положении и гидроксиалкильную группу, преимущественно группу СН3СН(ОН), в мета-положении (3-е положение), оказывается особенно эффективным. Фенилдиазониевая соль формулы II, соответствующая этому соединению, содержится в водном растворе в зависимом от рН гидролизном равновесии с соответствующей замкнутой лактоновой формой, с 7-меркапто-3-метил-3Н-изобензофуран-1-оном. Такое соединение можно с успехом применять при получении гербицидов изобензофуранонового типа.
В общем соединения формул I и II, которые содержат смежные относительно друг друга заместители, способные совместно образовывать (конденсированное) кольцо, например карбоксильную группу в орто-положении и гидроксиалкильную группу в мета-положении, находятся в водном растворе в зависимом от рН равновесии с соответствующей замкнутой формой, например с лактоновой формой, в частности формой 5-членного циклического лактона, например как 7-меркапто-3-метил-3Н-изобензофуран-1-он, который особенно легко образуется в кислотном растворе. Как правило, с увеличением размера кольца тенденция к образованию кольца уменьшается, 6- 7-членные кольца обычно образуются менее легко, чем 5-членное кольцо.
Таким образом, способ в соответствии с изобретением охватывает также получение тех замкнутых форм соединений формулы I, у которых два заместителя R образуют конденсированное кольцо.
Алкильные радикалы, упомянутые среди значений R, в предпочтительном варианте содержат от 1 до 4 углеродных атомов каждый и включают, например, метил, этил, пропил, бутил и их разветвленные изомеры. Предпочтительные алкокси-, алкилтио- и гидроксиалкильные радикалы дериватизируют из упомянутых алкильных радикалов. Алкенильные и алкинильные радикалы R в предпочтительном варианте содержат от 2 до 4 углеродных атомов каждый и включают, например, этенил, пропенил, этинил, пропинил, равно как и разветвленные изомеры этого последнего и пропенила, а также бутенил, бутинил и их разветвленные и диненасыщенные изомеры. Понятия гидроксил (-ОН), меркапто-(-SH), сульфогруппа (-SO3H) и карбоксил (-СО2Н) также в каждом случае включают их солевые формы, например соли щелочных металлов, щелочноземельных металлов и аммония. Термин "гетероциклил" понимают как охватывающий в предпочтительном варианте 4-8-членные насыщенные и ненасыщенные кольца, каждое из которых содержит по меньшей мере один гетероатом, выбранный из атомов азота, серы и кислорода. Их примеры включают пиридил, фуранил, тиофуранил, оксетанил, тиазинил, морфолинил,пиперазинил, пиридазинил, пиразинил, тиопиранил, пиразолил, пиримидинил, триазинил, изофуранил, пиранил, пиперидил, пиколинил, тиадиазолинил, тиетанил, триазолил, оксазоланил, тиоланил, азепинил, тиазолил, изотиазолил, имидазолил и пирролил.
В предпочтительном варианте серу используют в форме порошка. Предпочтение отдают применению от 1,2 до 5 молей, преимущественно от 1,5 до 3 молей серы на моль фенилдиазониевой соли.
Диазониевые соли получают по известному методу дозированием раствора нитрита натрия в кислый раствор соответствующего амина в воде при температуре примерно от -5°С до +5°С.
Выражение "повышенная температура" в предпочтительном варианте означает температурный диапазон от 20 до 100°С. Особенно выгодно проводить процесс в интервале от 30 до 80°С.
В предпочтительном варианте приемлемое водное основание представляет собой водный раствор гидроксида щелочного или щелочноземельного металла или аммония. Предпочтение отдают применению от 2,5 до 5 молей, преимущественно от 1,5 до 3 молей основания на моль диазониевого соединения. Если фенилдиазониевая соль формулы II уже содержит в качестве заместителей кислотные группы, в предпочтительном варианте для каждой кислотной группы требуется дополнительный моль основания.
Способ в соответствии с изобретением обладает основным преимуществом, состоящим в том, что его можно осуществлять в большом, промышленном масштабе. Способ заключается в том, что обычно в водное основание при повышенной температуре вводят серу и в него же дозируют диазониевую соль формулы II.
Способ в соответствии с изобретением можно осуществлять либо проведением непрерывного либо прерывистого процесса (не непрерывного, периодического процесса), причем предпочтение отдают прерывистому процессу. В предпочтительном варианте как прерывистые, так и непрерывные реакционные процессы проводят в сосуде с мешалкой или в каскаде сосудов с мешалками.
Было установлено, что для выделения тиолов добавлением сульфита натрия, бисульфита натрия или диоксида серы целесообразно избыток серы превращать в тиосульфат натрия. Далее реакционный раствор подкисляют, вследствие чего тиол отделяется и его можно выделить из водного раствора соли. Для дополнительный очистки можно отгонять фенилтиол.
Значения выхода выделенного тиола обычно составляют от 80 до 100%. Химический выход в реакционной смеси обычно превышает 95%.
Способ в соответствии с изобретением в сравнении со способами, известными в данной области техники, характеризуется следующими преимуществами:
его можно осуществлять в большом, промышленном масштабе,
реакционный процесс является простым, в особенности в сравнении с дисульфидным вариантом, в котором с целью подавить замену диазогруппы водородным атомом дисульфидный раствор и раствор диазосоединения необходимо дозировать в водное основание одновременно, при этом не образуются токсичные вспомогательные продукты, как это преимущественно происходит в случае ксантогенатного метода, при осуществлении которого во время обработки в молярных количествах образуются COS,
в сравнении с дисульфидным и полисульфидным вариантом реакция протекает очень селективно,
в результате продукты получают со значениями выхода плоть до 98%, его можно осуществлять в универсальном оборудовании.
Тиолы формулы I, полученные в соответствии с изобретением, используют, в частности, в качестве промежуточных продуктов при получении гербицидов изобензофуранонового типа, которые описаны, например, в US 5332717 и US 5428002.
Изобретение дополнительно проиллюстрировано в следующих примерах.
Пример 1. Получение 7-меркапто-3-метил-3Н-изобензофуран-1-она
В первом реакторе 203 г 2-амино-6-(1-гидроксиэтил)бензойной кислоты (натриевая соль) в форме 50%-ного водного раствора (1,0 моля) и 181 г 40%-ного водного раствора нитрита натрия (1,05 моля) одновременно вводят в 428 г соляной кислоты (32%). После завершения реакции избыток нитрита разрушают добавлением сульфаминовой кислоты.
Во втором реакторе 800 г гидроксида натрия в форме 30%-ного раствора и 71 г порошкообразной серы (2,20 моля) выдерживают при 60°С и перемешивают в течение 60 мин. В образовавшуюся смесь добавляют раствор диазониевой соли, приготовленный в первом реакторе, причем соответствующий тиол получают с выделением азота.
Для обработки в реакционную смесь добавляют 300 г толуола и 195 г бисульфита натрия (0,75 моля) в форме 40%-ного водного раствора. При температуре 80°С с использованием уксусной кислоты значение рН доводят до 8, в результате чего замыкается фталидное кольцо, а избыток серы превращают в тиосульфат. При 30°С вследствие дальнейшего понижения рН до 6 тиол высвобождают и растворяют в толуольной фазе. Толуольную фазу отделяют и добавляют в нее 5 г трифенилфосфина и 150 г воды. Осуществляют нагревание до примерно 30°С и значение рН доводят до 11, благодаря чему фенилтиол в форме его натриевой соли растворяется в водной фазе, из которой в форме водного раствора 7-меркапто-3-метил-3Н-изобензофуран-1-он может быть выделен в форме его натриевой соли с выходом 85% (в пересчете на 2-амино-6-(1-гидроксиэтил)бензойную кислоту).
Настоящее изобретение относится к способу получения 7-меркапто-3-метил-3Н-изобензофуран-1-она (I) взаимодействием фенилдиазониевой соли формулы
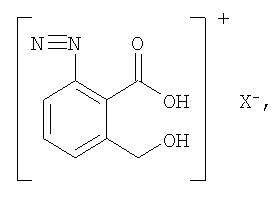
где Х - галоген или бисульфат с серой при повышенной температуре в присутствии водного основания. Продукт выделяют преимущественно в виде натриевой соли. Соединение I может быть использовано в качестве промежуточного продукта при получении гербицидов изобензофуранового типа. 1 н. и 1 з.п. ф-лы.
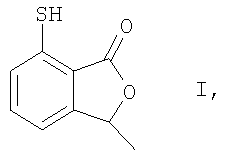
отличающийся тем, что фенилдиазониевую соль формулы
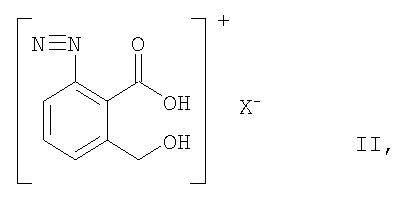
в которой Х обозначает атом галогена или бисульфат, подвергают взаимодействию с серой при повышенной температуре в присутствии водного основания и с последующим выделением целевого продукта.
| SU, 1222912, 30.03.1986 | |||
| DE, 433103, 20.08.1926. |
Авторы
Даты
2007-11-20—Публикация
2001-10-09—Подача