Изобретение относится к области медицины, в частности лечению онкологических заболеваний наружных органов человека.
Известен способ фотодинамической терапии (ФДТ) онкологических заболеваний, включающий введение фотосенсибилизатора и использование источника света, что обеспечивает фотохимическое индуцированное разрушение клеток [1]. В известном способе пациенту внутривенно вводят раствор фотосенсибилизатора, который концентрируется в опухоли. Затем фотосенсибилизатор возбуждают низкоинтенсивным лазерным излучением. В результате фотохимической реакции фотосенсибилизатора с окружающими опухоль молекулами кислорода образуется высокотоксичный для раковых клеток синглетный кислород.
Недостатком способа является низкая эффективность лечения, обусловленная тем, что поскольку раковые клетки растут быстрее, чем клетки, ответственные за образование новых кровеносных капилляров, то в зоне опухолевой ткани образуется дефицит молекул кислорода, который увеличивается во время сеанса ФДТ, это приводит к гипоксии в зоне облучения [2].
Ближайшим по техническому решению к предлагаемому способу, является двухцветная лазерная фотодинамическая терапия опухолей, основанная на введении фотосенсибилизатора в зону опухолевой ткани и одновременном воздействии лазерным излучением при двух различных длинах волн - прототип [3].
Причем, длины волн лазерного излучения подбираются таким образом, чтобы обеспечить одновременное воздействие на фотосенсибилизатор и оксигемоглобин крови. Использование второй длины волны излучения лазера вызывает фотодиссоциацию оксигемоглобина и, тем самым, способствует повышению локальной концентрации молекулярного кислорода в зоне облучения. Таким образом, дополнительная подпитка свободным молекулярным кислородом значительно улучшает терапевтический эффект способа ФДТ.
Существенным недостатком способа является невысокий его терапевтический эффект из-за низкого квантового выхода фотодиссоциации оксигемоглобина, который не превышает 10% [4].
Задачей изобретения является повышение эффективности способа фотодинамической терапии онкологических заболеваний. Поставленная задача решается следующим образом. В способе фотодинамической терапии онкологических заболеваний, основанном на введении фотосенсибилизатора в зону опухолевой ткани и одновременном воздействии лазерным излучением при двух длинах волн, температуру в зоне опухолевой ткани повышают до 42°-43°C и поддерживают ее в течение всего периода облучения.
Сущность предлагаемого изобретения поясняется чертежами, полученными авторами на основе экспериментальных исследований, где:
на фиг.1 изображена диаграмма изменения степени насыщения оксигемоглобином артериальной крови в кожном кровеносном сосуде во время воздействия на него лазерным излучением с λ=638 мкм при нормальной температуре тела 36°С;
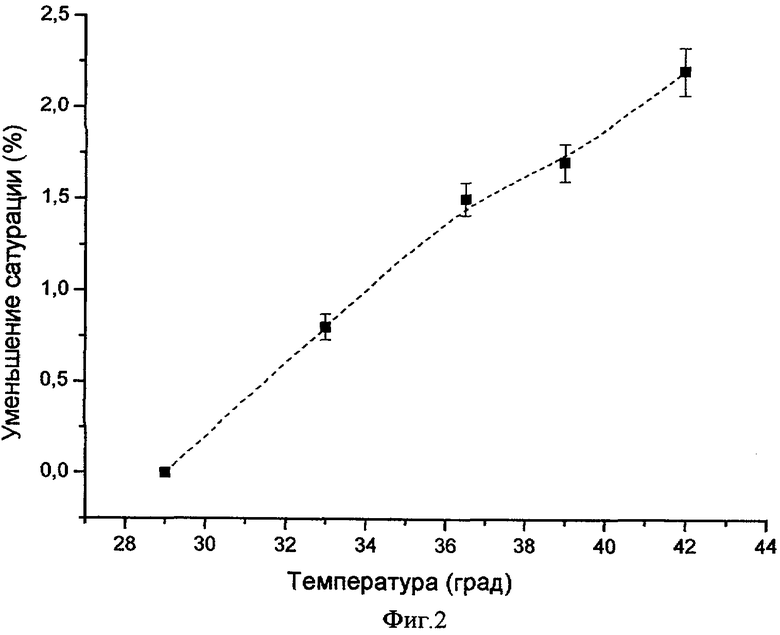
на фиг.2 изображена зависимость изменения величины насыщения артериальной крови оксигемоглобином от температуры в зоне воздействия лазерным излучением.
В основе возможности воздействия на величину локальной концентрации свободного молекулярного кислорода в зоне опухоли лежит использование явления зависимости квантового выхода фотодиссоциации оксигемоглобина крови in vivo от температуры, полученной авторами экспериментально.
Из диаграммы на фиг.1 видно, что при воздействии излучением лазера величина насыщения артериальной крови оксигемоглобином при температуре тела 36°С снижается на 1,3%. Это свидетельствует о высвобождении кислорода в зоне воздействия в результате фотодиссоциации оксигемоглобина с квантовым выходом фотодиссоциации оксигемоглобина ˜10%. Причем, высвобождение кислорода происходит одновременно с началом облучения и продолжается на протяжении всего периода воздействия лазерным излучением, что видно на фиг.1.
При увеличении температуры в зоне опухолевой ткани от 36°С до 42°С насыщение артериальной крови оксигемоглобином уменьшается, как это видно из фиг.2, от 1,3% до 2,4%, т.е. в 1,8 раз. Это свидетельствует о более значительном высвобождении молекулярного кислорода в крови в результате фотодиссоциации оксигемоглобина. При этом квантовый выход фотодиссоциации оксигемоглобина составляет ˜18%.
Как видно из фиг.2 при температуре порядка 29°С изменения в величине насыщения артериальной крови оксигемоглобином не наблюдается, а при повышении температуры она растет, достигая своей максимальной величины около 42°-43°С.
Таким образом, повышение температуры тела в зоне опухолевой ткани до 42°-43°С обеспечивает при воздействии на опухоль лазерным излучением увеличение локальной концентрации свободного молекулярного кислорода в 1,8 раз за счет увеличения квантового выхода фотодиссоциации оксигемоглобина в крови до 18-20%, что обеспечивает повышение эффективности способа фотодинамической терапии онкологических заболеваний, где молекулярный кислород является важным и обязательным компонентом фотодинамической реакции.
Источники информации
1. Pass HI. Photodynamic therapy in oncology: mechanism and clinical use. J Natl. Cancer Inst., vol.85, N6, (1993), p.443-456.
2. A.A.Стратонников, В.Б.Дощенов, А.Ю.Дуплик, В.И.Конов. Российский хим. журн., т.42, (1998), с.53-67.
3. Б.М.Джагаров, Э.А.Жаврид, Ю.П.Истомин, В.Н.Чалов. Двухцветная лазерная фотодинамическая терапия опухолей. Жур. прикл. спектр., т.68, (2001), с.151-153.
4. Б.М.Джагаров, B.C.Чирвонный, Г.П.Гуринович. Пикосекундная спектроскопия и фотохимия биомолекул, под ред. B.C.Летохова. М., (1987), с.180-212.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2438733C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ КАРБОКСИГЕМОГЛОБИНА КРОВИ | 2009 |
|
RU2408400C1 |
| СПОСОБ ЛОКАЛЬНОГО ПОВЫШЕНИЯ КОНЦЕНТРАЦИИ МОЛЕКУЛЯРНОГО КИСЛОРОДА В ДЕРМЕ КОЖНОЙ ТКАНИ | 2011 |
|
RU2484861C2 |
| УСТРОЙСТВО ДЛЯ СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ СОСТОЯНИЯ БИОЛОГИЧЕСКИХ ТКАНЕЙ В ПРОЦЕССЕ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ НА ОСНОВЕ ХЛОРИНА E6 | 2022 |
|
RU2807133C1 |
| СПОСОБ ПОВЫШЕНИЯ КОНЦЕНТРАЦИИ МОЛЕКУЛЯРНОГО КИСЛОРОДА В ДЕРМЕ КОЖНОЙ ТКАНИ | 2011 |
|
RU2484860C2 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2539367C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНЫХ ЭНЕРГЕТИЧЕСКИХ ПАРАМЕТРОВ ЛАЗЕРНО-ИНДУЦИРОВАННОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ДИСПЛАЗИИ И РАКА ШЕЙКИ МАТКИ | 2023 |
|
RU2815258C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННЫХ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2446842C2 |
| ФОТОСЕНСИБИЛИЗАТОР НА ОСНОВЕ КОМПЛЕКСА ХЛОРИНА Е6 И ЕВРОПИЯ | 2022 |
|
RU2797948C1 |
| Способ комбинированного лечения неоплазии мягких тканей | 2024 |
|
RU2839984C1 |
Изобретение относится к области медицины, онкологии, и может быть использовано в фотодинамической терапии онкологических заболеваний. Для этого вводят фотосенсибилизатор в зону опухолевой ткани. Затем на опухолевую ткань воздействуют лазерным излучением одновременно при двух длинах волн. Вторая длина волны выбирается так, чтобы обеспечить насыщение плазмы артериальной крови кислородом. При этом температуру в зоне опухолевой ткани повышают до 42°-43°С и поддерживают весь период облучения. Проведение такой терапии позволяет повысить концентрацию свободного кислорода и увеличить генерацию синглетного кислорода при фотодинамической реакции. 2 ил.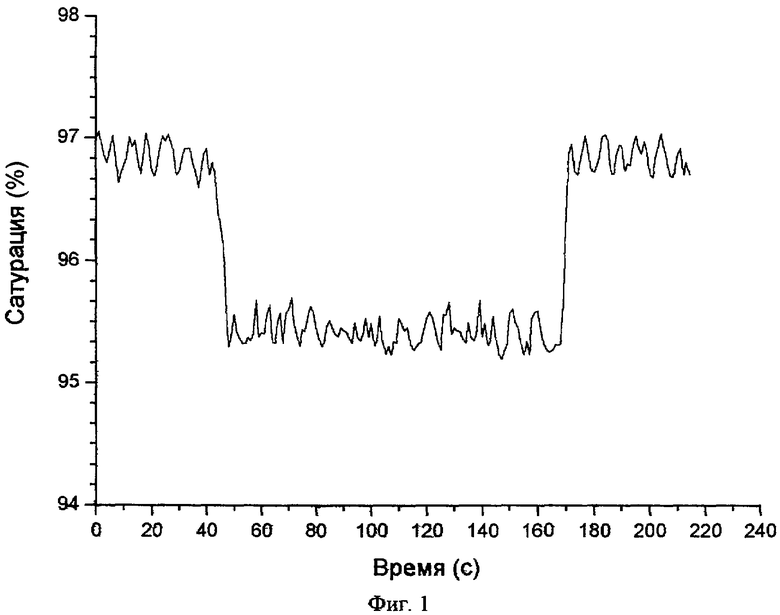
Способ фотодинамической терапии онкологических заболеваний, включающий введение фотосенсибилизатора в зону опухолевой ткани и воздействие на нее лазерным излучением одновременно при двух длинах волн, при этом вторая длина волны выбирается так, чтобы обеспечить насыщение плазмы артериальной крови кислородом, отличающийся тем, что температуру в зоне опухолевой ткани повышают до 42-43°С, поддерживая ее в течение всего периода облучения.
| СРЕДСТВО ДЛЯ ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ И НЕОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2219921C1 |
| JP 2003052816, 25.02.2003 | |||
| КАРАНДАШОВ В.И | |||
| Фототерапия (светолечение) | |||
| Руководство для врачей | |||
| - М., 2001, с.153-165, 330-343 | |||
| DJUGHERTY TJ | |||
| Photodynamic therapy for the treatment of cancer | |||
| // Conference on lasers and electro-optics technical digest | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Anhcim (California), 1984, p.214. | |||
Авторы
Даты
2007-12-20—Публикация
2006-01-16—Подача