Изобретение относится к области фармакологии и биотехнологии, и направлено на решение задачи усиления фотодинамического повреждения клеток-мишеней с помощью биологически активных соединений хлоринового ряда, и может быть использовано в клеточной и молекулярной биологии, в разработке методов, применимых в экспериментальной медицине и фармакологии в качестве высокоэффективного фотосенсибилизатора (ФС) для фотодинамической терапии (ФДТ) рака и других новообразований различного генезиса.
В настоящее время в клинической практике при ФДТ применяется целый ряд ФС, созданных на основе соединений различных химических классов. Однако наряду с ныне используемыми препаратами продолжаются активные поиски и исследования новых, более эффективных ФС. Так в течение последних двух десятилетий особый интерес в качестве ФС представляют производные природных хлорофиллов - хлорины. Установлено, что ФС хлоринового ряда быстро накапливаются в опухолевой ткани с высоким градиентом контрастности опухоль/здоровая ткань, обладают высокой фотодинамической активностью и терапевтической эффективностью. Кроме того, хлорины быстро выводятся из организма, что полностью решает проблему длительной кожной фототоксичности, являющейся основным недостатком почти всех применяющихся в клинике ФС.
Не смотря на все преимущества ФДТ, в ряде случаев ее использование связано с невозможностью создания достаточной концентрации фотосенсибилизатора в опухоли или невозможностью эффективной доставки лазерного излучения при некоторых локализациях злокачественных новообразований. Целый ряд нозологических форм первичной опухоли и ее метастазов недоступны для воздействия света, что ограничивает возможности применения ФДТ. Одним из решений данной проблемы считается создание фармакологических препаратов для ФДТ на основе комплексов органических фотосенсибилизаторов с наночастицами, которые помимо доставки фотосенсибилизатора в опухоль могут выполнять роль эффективного донора энергии фотовозбуждения.
Наиболее широко распространенным типом таких наночастиц на данный момент является использование коллоидных полупроводниковых квантовых точек. Так известен патент [Пат. WO2010151074, опубликован 19.05.2011] согласно которому предлагается для ФДТ использовать фотосенсибилизатор, представляющий собой квантовые точки, ковалентно связанные в комплекс с производными хлорина е6. В данном комплексе реализуется безызлучательный резонансный перенос энергии от квантовых точек к молекулам, производным хлорина, который приводит к сенсибилизации генерации ими синглетного кислорода. Формирование данных комплексов проводится в водных средах, в которых хлорин е6 склонен к образованию агрегатов, что в свою очередь приводит к значительному снижению эффективности активации молекул кислорода, а значит - к уменьшению эффекта ФДТ. Кроме того, для увеличения селективности накопления комплексов в опухоли предлагается использовать специальные молекулы, что говорит, по сути, о создании сложной, трехкомпонентной структуры, усложнение методов формирования и очистки которой приведут к резкому повышению себестоимости конечного лекарственного препарата на основе таких комплексов.
Еще одним аналогичным изобретением является [патент РФ 2629390, опубликован 04.07.2017], сущность, которого заключается в том, что формирование комплексов осуществляется в результате ковалентного связывания в комплекс хиральных полупроводниковых квантовых точек с молекулами хлорина е6 в мономерной форме в диметилсульфоксиде. После формирования комплексов происходит их очистка и концентрирование, затем полученный концентрированный раствор комплексов вводится в водный раствор. В результате облучения комплексов квантовых точек с молекулами хлорина е6 светом с длиной волны, которая эффективно ими поглощается, комплексы переходят в возбужденное состояние, в котором при взаимодействии с молекулами кислорода способны переводить их в активную синглетную форму. Основным недостатком данного способа является потенциально высокая токсичность квантовых точек CdSe/ZnS.
Кроме использования квантовых точек как доноров энергии фотовозбуждения, было предложено использовать в качестве источника видимого света нанолюминофор, который преобразует рентгеновское или гамма-излучение в видимый свет с необходимой для ФС длиной волны. Нанолюминофоры являются маломощными источниками света, поэтому они не вызывают нагревания и испарения тканей.
Одним из таких известных ФС является препарат, который наряду с фотосенсибилизатором включает коллоидный раствор нанолюминофора Ва3(PO4)2:Eu2+ [В. Бахметьев и др. Нанолюминофоры для рентгенофотодинамической терапии онкологических заболеваний / Наноиндустрия. 2013. №8. С. 46.]. Авторами данного изобретения разработана технология, позволяющая получать нанолюминофоры на основе ортофосфатов осаждением из водных растворов золь-гель-методом. Синтезирован ряд соединений с различными катионами, в частности, состава Ва3(PO4)2:Eu2+, обладающих наиболее высокой интенсивностью свечения при возбуждении жестким рентгеновским излучением с длинами волн 0,12-0,31 А, что соответствует излучению медицинских терапевтических установок. К недостаткам известного препарата относится необходимость использования жесткого рентгеновского излучения, которое оказывает пагубное влияние на здоровые клетки, кроме того, продуцируемый фотосенсибилизатором активный кислород неизбежно должен расходоваться помимо прямого назначения на окисление Eu2+ до более устойчивого состояния Eu3+, и, следовательно, эффективность фотосенсибилизатора будет снижаться.
Известен препарат для ФДТ, содержащий фотосенсибилизатор «Радахлорин» основу которого составляет смесь натриевых солей хлорина е6, хлорина р6 и пурпурина 5 и нанолюминофоры (NaGdF4:Eu3+), (YF3:Yb3+,Er3+) [В.В. Бахметьевт др. Нанолюминофоры на основе смешанных фторидов для фотодинамической терапии онкологических заболеваний / Известия СПбГТИ(ТУ). 2018. №42 С. 26-51]. Авторами показано, что люминофор NaGdF4:Eu3+ является наиболее подходящим для ФДТ с использованием рентгеновского излучения, а люминофор YF3:Yb3+,Er3+ - для ФДТ с использованием инфракрасного излучения. Исследована эффективность генерации активного кислорода препаратом, содержащим наноломинофор YF3:Yb3+,Er3+ и фотосенсибилизатор «Радахлорин», под воздействием инфракрасного лазера с длиной волны 980 нм. В частности, был приготовлен препарат на основе бидистиллированной воды, содержащий нанолюминофор YF3:Yb3+,Er3+ в концентрации 2,0 г/л и фотосенсибилизатор «Радахлорин» в концентрации 8,75 мг/л. В качестве стабилизатора коллоидного раствора использовался лаурилсульфат натрия. К недостаткам данного препарата относится низкая эффективность генерации активного кислорода, обусловленная тем, что люминофор и фотосенсибилизатор непосредственно не связаны между собой, что затрудняет передачу энергии от люминофора.
В качестве прототипа выбран [О.В. Шевченко и др. Молекулярные комплексы хлорина е6 и европия для радиофотодинамической терапии / Вестник ДВО РАН. 2020. №2. С. 103-107] фотосенсибилизатор и способ его получения представляющий собой мультимодальный комплекс на основе полиэтиленимина (PEI) с молекулярной массой 25 тыс. дальтон, который синтезировали поэтапным связыванием компонентов с аминогруппами. Для активации карбоксильных групп хлорина е6 (Е6), диэтилентриаминпентауксусной (DTPA) и фолиевой кислот (FA) использовали 1,2 М водорастворимого карбодиимида, 1,2 моль N-оксисукцинимида и 0,12 М 4-диметиламинопиридина в каждом случае. Фолиевую кислоту присоединяли для целевой доставки комплекса к раковым клеткам. В растворе полученное вещество состава PEI/E6/DTPA/FA (мольное соотношение 1:1:1:1) насыщали EuCl3 при рН 6,5. Данный препарат эффективно генерирует активные формы кислорода при воздействии гамма-излучением. Недостатком этого препарата является его положительный заряд, обусловленный свободными амино-группами и вызывающий неспецифическое ионное связывание с клетками.
Задачей изобретения является создание фотосенсибилизатора, содержащего в качестве люминофора соединение европия (3+) для фотодинамической терапии, на основе конъюгата хлорина е6 с европием, в котором европий выполняет роль эффективного донора энергии фотовозбуждения, обладающего селективностью накопления в опухоли, для усовершенствования метода фотодинамической терапии.
Технический результат заявляемого изобретения заключается в увеличении селективности накопления препарата в тканях злокачественных новообразований за счет подавления положительного заряда конъюгата, а, следовательно, увеличение эффективности фотосенсибилизатора и минимизация повреждения здоровых тканей.
Технический результат предлагаемого изобретения достигается созданием конъюгата на основе полиэтиленимина (PEI), содержащего европий (Eu3+), Хлорин е6 (Е6), диэтилентриаминпентауксусную кислоту (DTPA), фолиевую кислоту (FA) и лимонную кислоту (СА), связанные ковалентно с помощью 1-этил-3-(3-диметиламинопропил)карбодиимида (WSC), N-гидроксисукцинимида (NHS) и 4-диметиламинопиридина (DMAP) с адресной доставкой к раковым клеткам.
Поставленная задача решается следующим образом.
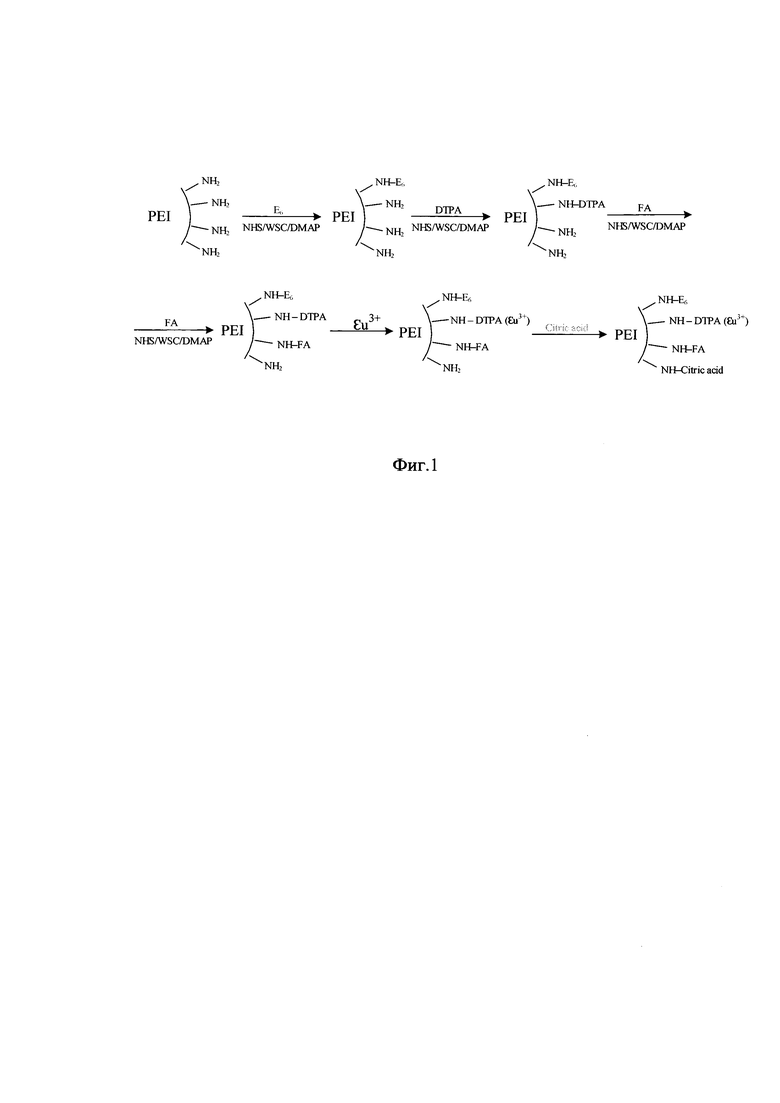
Для получения фотосенсибилизатора к раствору Хлорина е6 добавляют раствор водорастворимого карбодиимида, N-гидроксисукцинимида, 4-диметиламинопиридина в дистиллированной воде реакционную смесь перемешивают 30 минут на магнитной мешалке. Далее к полученному раствору добавляют раствор полиэтиленимина в дистиллированной воде. На следующем этапе к этому раствору добавляют натриевую соль диэтилентриаминпентауксусной кислоты в 0,01 М NaHCO3 с предварительной активацией WSC, NHS, DMAP в дистиллированной воде. На следующем этапе вносят фолиевую кислоту, карбоксильные группы которой активируют WSC, NHS и DMAP в дистиллированной воде, при перемешивании в течение 30 минут. К полученному раствору добавляют ЕuСl3. На завершающем этапе свободные аминогруппы ацилируют избытком лимонной кислоты, активированной WSC, NHS и DMAP в дистиллированной воды. Финальный препарат диализируют против дистиллированной воды и хранят при 4°С. Все операции проводят при защите от прямого света. В результате получают конъюгат PEI/E6/DTPA/FA/CA/Eu.
Так как все клетки заряжены отрицательно для усиления адресной доставки препарата раковым клеткам его положительный заряд, вызывающий неспецифическое ионное взаимодействие со свободными положительно заряженными группами полиэтиленимина, подавляется на последнем этапе получения конъюгата их ацилированием избытком лимонной кислоты.
Все активные элементы препарата, такие как Хлорин е6, фолиевая кислота, хелатор европия и лимонная кислота связаны ковалентными связями с полиэтиленимином. Полученный препарат представляет собой изотонический раствор темно-зеленого цвета.
Описанный синтез препарата, в результате которого формируется конъюгат, показан на схеме, представленной на Фиг. 1.
Возможность конкретного осуществления изобретения подтверждается следующим примером.
Для получения фотосенсибилизатора в раствор, содержащий 5,0 мг Хлорина е6, добавляют раствор 1,9 мг карбодиимида (1-этил-3-(3-диметиламинопропил)карбодиимид), 1,2 мг N-гидроксисукцинимида, 0,3 мг 4-диметиламинопиридина в 1 мл дистиллированной воды, реакционную смесь перемешивают 30 минут на магнитной мешалке. Далее к полученному раствору добавляют раствор 400 мг полиэтиленимина в 2 мл дистиллированной воды. На следующем этапе к этому раствору добавляют 1,7 мг натриевой соли диэтилентриаминпентауксусной кислоты в 0,01 М NaHCO3 с предварительной активацией раствором 1,1 мг WSC, 0,6 мг NHS, 0,1 мг DMAP в 1 мл дистиллированной воды. На следующем этапе при перемешивании в течение 30 минут вводят 1,5 мг фолиевой кислоты (ее карбоксильные группы активируют раствором 1,3 мг WSC, 0,8 мг NHS и 0,1 мг DMAP в 1 мл дистиллированной воды). К полученному раствору добавляют 65,8 мкмоль EuCl3. На завершающем этапе свободные аминогруппы ацилируют избытком лимонной кислоты (12 мг), активированной WSC, NHS и DMAP (10, 5 и 0,5 мг, соответственно) в 5 мл дистиллированной воды. Финальный препарат диализируют против дистиллированной воды (5 смен воды по 2 л каждые 4 часа) и хранят при 4 С°. Все операции проводят при защите от прямого света.
Интенсивность генерации активных форм кислорода (АФК) молекулярным конъюгатом PEI/E6/DTPA/FA/CA/Eu при облучении красным светом 645 нм в присутствии 2',7'-дихлордигидрофлуоресцеина, который является специфическим сенсором активных форм кислорода, в 5,1 раз превышала продукцию этой молекулы свободным хлорином е6 при 5-ти мин облучении.
Исследование фотоцитотоксичности проводили с помощью Резазурин-теста. Установлено, что уже по истечении суток после облучения наблюдается более активная гибель клеток в присутствии молекулярного конъюгата по сравнению с действием свободного Хлорина е6.
| название | год | авторы | номер документа |
|---|---|---|---|
| Радиолюминесцентный препарат на основе аддукта хлорина Е6 и европия для фотодинамической терапии глубоких опухолей | 2024 |
|
RU2838226C1 |
| ПРОИЗВОДНЫЕ ХЛОРОФИЛЛА α, МОДИФИЦИРОВАННЫЕ ФРАГМЕНТАМИ МИРИСТИНОВОЙ КИСЛОТЫ | 2018 |
|
RU2673888C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ИНАКТИВАЦИИ ГРАМОТРИЦАТЕЛЬНЫХ ПАТОГЕННЫХ МИКРООРГАНИЗМОВ | 2021 |
|
RU2781892C1 |
| Фотосенсибилизатор на основе карбоцианинового красителя для фотодинамической терапии опухолей | 2016 |
|
RU2638131C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИГЛИОМНОЙ АКТИВНОСТЬЮ, И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ГЛИОБЛАСТОМЫ | 2022 |
|
RU2794666C1 |
| Модифицированный фотосенсибилизатор на основе наночастиц селена и гидрофильного полимера | 2024 |
|
RU2835425C1 |
| Способ оптимизации фотодинамической терапии гнойных ран (варианты) | 2015 |
|
RU2609735C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2005 |
|
RU2323722C2 |
| ПОЛУГИДРАТ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА МЕЛАМИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2617778C1 |
| Способ фотодинамической терапии с интрадермальной фотосенсибилизацией | 2020 |
|
RU2750975C1 |
Изобретение относится к области фармакологии и биотехнологии, а именно к фотосенсибилизатору на основе хлорина е6, содержащему в качестве люминофора соединение европия. Фотосенсибилизатор получают путем формирования на полиэтиленимине конъюгата, содержащего европий(3+), хлорин е6, диэтилентриаминпентауксусную кислоту, фолиевую кислоту, связанные ковалентно с помощью водорастворимого 1-этил-3-(3-диметиламинопропил)карбодиимида (WSC), N-гидроксисукцинимида (NHS) и 4-диметиламинопиридина (DMAP). При этом конъюгат дополнительно содержит ковалентно связанную лимонную кислоту, что достигается путем ацилирования на завершающем этапе свободных аминогрупп избытком лимонной кислоты, активированной WSC, NHS и DMAP в дистиллированной воде. Технический результат заявляемого изобретения заключается в увеличении селективности накопления препарата в тканях злокачественных новообразований за счет подавления положительного заряда конъюгата, а следовательно увеличении эффективности фотосенсибилизатора и минимизации повреждения здоровых тканей. 1 ил., 1 пр.
Фотосенсибилизатор на основе Хлорина е6, содержащий в качестве люминофора соединение европия, получаемый путем формирования на полиэтиленимине конъюгата, содержащего европий(3+), Хлорин е6, диэтилентриаминпентауксусную кислоту, фолиевую кислоту, связанные ковалентно с помощью водорастворимого 1-этил-3-(3-диметиламинопропил)карбодиимида (WSC), N-гидроксисукцинимида (NHS) и 4-диметиламинопиридина (DMAP), отличающийся тем, что конъюгат дополнительно содержит ковалентно связанную лимонную кислоту, что достигается путем ацилирования на завершающем этапе свободных аминогрупп избытком лимонной кислоты, активированной WSC, NHS и DMAP в дистиллированной воде.
| ШЕВЧЕНКО О.В | |||
| и др | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Клапанный регулятор для паровозов | 1919 |
|
SU103A1 |
| YUAN WEIEN et al | |||
| Polymer-based nanocarriers for therapeutic nucleic acids delivery, Chapter 14, 2017, p | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОЙ БОКОВОЙ СТАБИЛИЗАЦИИ | 1921 |
|
SU445A1 |
| Автоматический сцепной прибор | 1921 |
|
SU449A1 |
| WEI C | |||
| et al | |||
| The one-step preparation of | |||
Авторы
Даты
2023-06-13—Публикация
2022-08-03—Подача