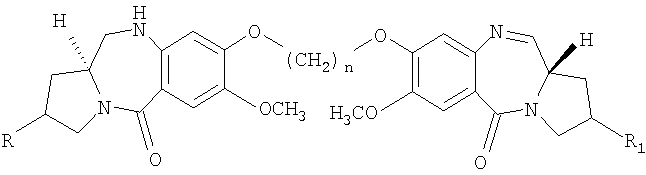
Настоящее изобретение относится к новым пирроло[2.1-c][1.4]бензодиазепинам, которые применимы как потенциальные противоопухолевые средства. Данное изобретение относится к способу получения новых пирроло[2.1-c][1.4]бензодиазепиновых соединений, применимых в качестве противоопухолевых средств. Более конкретно, изобретение относится к способу получения 7-метокси-8-{n-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]алкилокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она с различной длиной алифатической цепи и его 2-гидроксипроизводных, обладающих противораковой (противоопухолевой) активностью. Структурная формула новых пирроло[2.1-c][1.4]бензодиазепинов представляет собой формулу, указанную ниже:
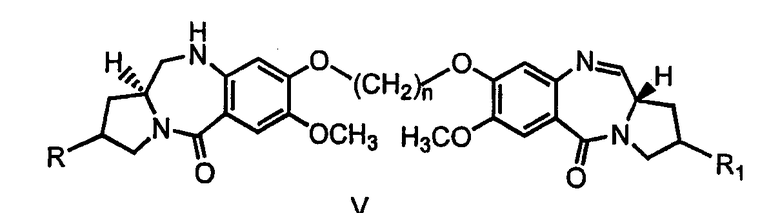
где R и R1 представляют собой Н и/или ОН; n принимает значения от 3 до 5.
В последние несколько лет появился растущий интерес к разработке новых пирроло[2.1-c][1.4]бензодиазепинов (PBDs). Данные антибиотики взаимодействуют ковалентно с ДНК c образованием N2-гуанинового аддукта, который находится внутри малой бороздки дуплексной ДНК за счет кислотно-лабильной аминальной связи с электрофильным имином в положении N10-C11 (Ссылки: Kunimoto, S.; Masuda, T.; Kanbayashi, N.; Hamada, M.; Naganawa, H.; Miyamoto, M.; Takeuchi, T. and Unezawa, H. J. Antibiot. 1980, 33, 665; Kohn, K.W. and Speous, C.L. J. Mol. Biol. 1970, 51, 551; Hurley, L.H., Gairpla, C. and Zmijewski, M. Biochem. Biophys. Act. 1977, 475, 521; Kaplan, D.J. and Hurley L.H. Biochemistry 1981, 20, 7572). Данные молекулы обладают правосторонним вращением, которое позволяет им следовать по кривизне малой бороздки В-формы двухцепочечной ДНК, включающей три пары оснований. Недавняя разработка посвящена связыванию двух PBD-единиц через их С8-положения с получением бифункциональных алкилирующих средств, способных сшивать ДНК (Ссылки: Thurston, D.E.; Bose, D.S.; Thomson, A.S.; Howard, P.W.; Leoni, A.; Croker, S.J.; Jenkins, T.C.; Neidle, S. and Hurley, L.H. J. Org. Chem. 1996, 61, 8141-8147). Недавно были синтезированы не сшитые смешанные имин-амидные PBD-димеры, которые обладают значительной ДНК-связывающей способностью и потенциальной противоопухолевой активностью (Kamal, A.; Laxman, N.; Ramesh, G.; Ramulu, P. and Srinivas, O. US Pat. No. 636233. dt 26-03-2002; Kamal, A.; Ramesh, G.; Laxman, N.; Ramulu, P.; Srinivas, O.; Neelima, K.; Kondapi, A.K.; Srinu, V.B.; Nagarajaram, H.M. J. Med. Chem. 2002, 45, 4679).
Природные пирроло[2.1-c][1.4]бензодиазепины принадлежат к группе противоопухолевых антибиотиков, производимых видами Streptomyces. В последнее время существует большой прогресс в области PBD-систем, так как они могут распознавать и связывать специфические последовательности в ДНК. Примеры природных PBS включают антрамицин, DC-81, томаймицин, сибиромицин и неотрамицин.
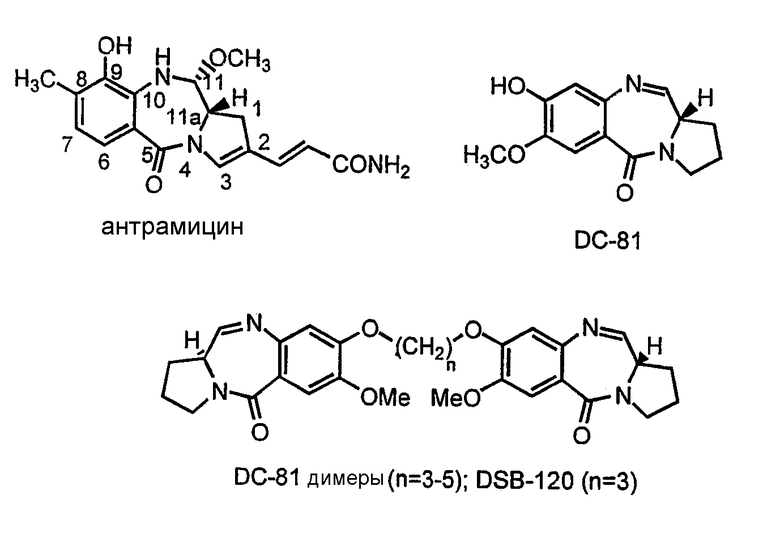
Однако клиническая эффективность данных антибиотиков снижена рядом ограничений, таких как слабая растворимость в воде, кардиотоксичность и метаболическая инактивация.
Соединения данного изобретения отличаются от представителей того же типа, С-8 связанных вторичных аминов, замещением фенольного водорода (11аS)-8-гидрокси-7-метокси-1,2,3,11а-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (DC-81).
Пирроло[2.1-c][1.4]бензодиазепин-5-оны представляют собой класс соединений, которые связываются с ДНК нековалентными взаимодействиями, такими как гидрофобные, Ван-дер-ваальсовы взаимодействия и водородная связь между заместителями кольца и ДНК, и также являются ответственными за влияние на селективность последовательного связывания.
Задачей настоящего изобретения является создание соединения и его производных, обладающих противоопухолевой активностью, т.е., противораковыми активностями.
Другой задачей настоящего изобретения являются новые пирроло[2.1-с][1.4]бензодиазепины, применимые в качестве противоопухолевых средств.
Задачей настоящего изобретения также является способ получения новых пирроло[2.1-с][1.4]бензодиазепинов, применимых в качестве противоопухолевых средств.
Также задачей данного изобретения является фармацевтическая композиция для лечения злокачественных и других опухолей.
Еще одной задачей данного изобретения является способ лечения пациентов, страдающих от рака или родственных заболеваний.
В соответствии с изложенным данное изобретение относится к новому пирроло[2.1-с][1.4]бензодиазепину формулы V, где R=H, ОН, R1=H, ОН и n принимает значения от 3 до 5, и способу его получения.
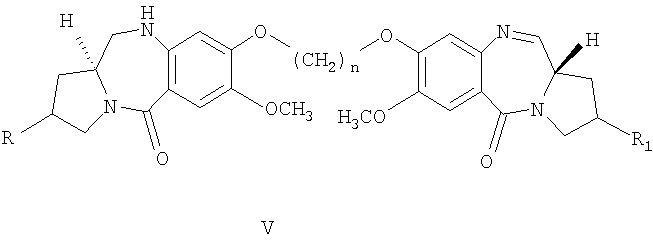
Один из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=R1=H и n=3.
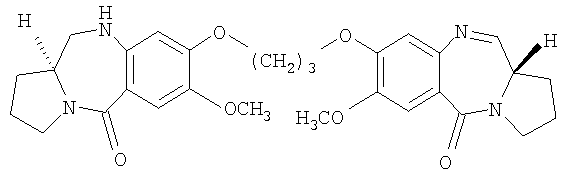
Один из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=R1=H и n=4.
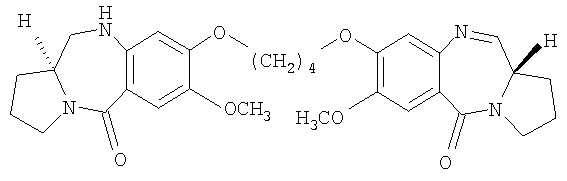
Еще один из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=R1=H и n=5.
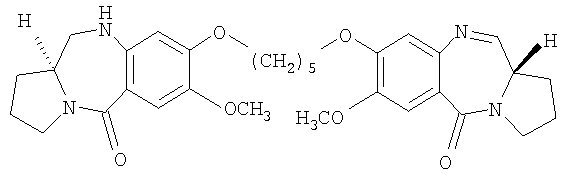
Еще другой из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=OH, R1=H и n=3.
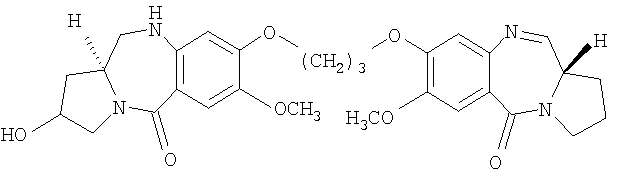
Другой из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=OH, R1=H и n=4.
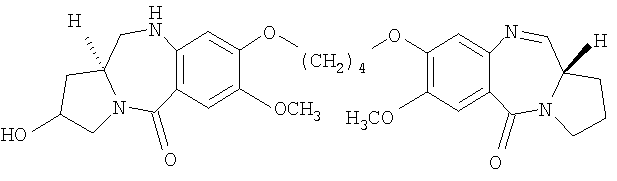
Еще другой из вариантов осуществления данного изобретения относится к пирролобензодиазепину структурной формулы, представленной ниже, где R=OH, R1=H и n=5.
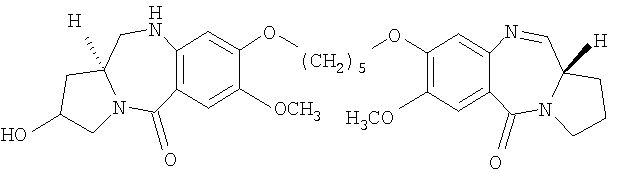
В другом варианте осуществления данное изобретение относится к пирролобензодиазепиновому соединению структурной формулы, представленной ниже, где R=H, R1=H и n=3.
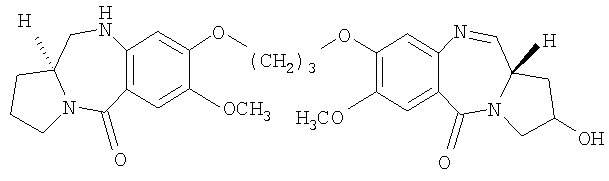
В другом варианте осуществления данное изобретение относится к пирролобензодиазепиновому соединению структурной формулы, представленной ниже, где R=H, R1=OH и n=4.
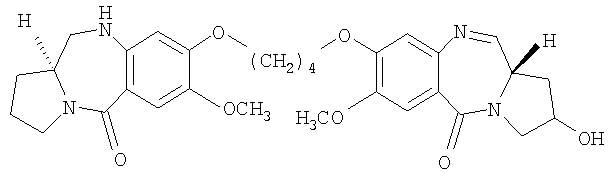
В другом варианте осуществления данное изобретение относится к пирролобензодиазепиновому соединению структурной формулы, представленной ниже, где R=H, R1=OH и n=5.
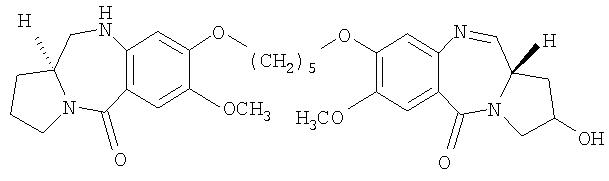
Другой вариант осуществления данного изобретения относится к активности пирроло[2.1-с][1.4]бензодиазепина формулы V против клеточных линий опухолей человека.
Еще другой вариант осуществления данного изобретения относится к ростингибирующей активности данных соединений в отношении различных типов клеток рака, такого как лейкемия, меланома, рак толстой кишки, яичника, простаты, CNS, молочной железы, немелкоклеточной карциномы легкого.
Еще один вариант осуществления данного изобретения относится к способу получения соединений, причем указанный способ включает стадии: а) взаимодействие соединения формулы (I)
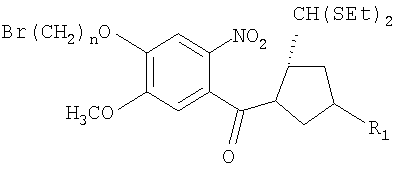
с соединением формулы (II)
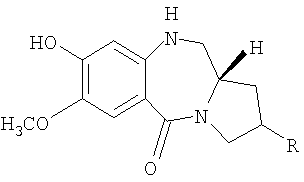
в присутствии слабого основания в апротонном органическом растворителе, смешивающемся с водой, при кипячении с обратным холодильником в течение периода от 16 до 48 ч,
с получением соединения формулы (III)
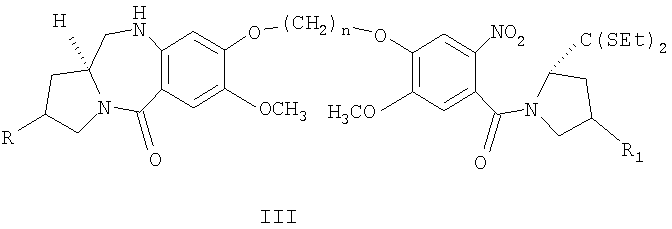
в) восстановление нитросоединения формулы (III) с помощью дигидрата хлорида олова(II) в галогенированном растворителе при кипячении с обратным холодильником в течение периода 0,5 ч-2 ч, с) установление рН реакционной смеси со стадии (в) до 8 с помощью щелочного бикарбонатного раствора,
d) экстрагирование раствора со стадии (с) этилацетатом, упаривание этилацетатного экстракта при пониженном давлении с получением неочищенного соединения формулы (IV)
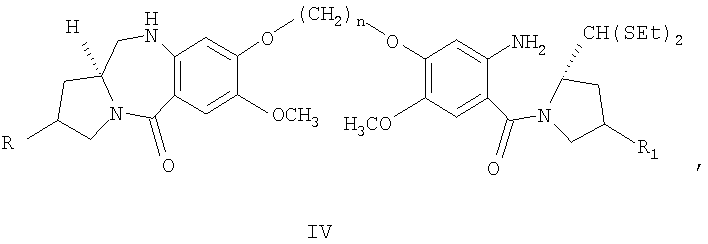
e) растворение соединения формулы (IV) в смеси ацетонитрил/Н2О при соотношении 4:1,15 мл, добавление хлорида ртути(II), карбоната кальция, перемешивание при комнатной температуре от 6 ч до 12 ч,
f) фильтрование и упаривание органического слоя при пониженном давлении с последующим разбавлением остатка в этилацетате,
g) добавление насыщенного раствора бикарбоната натрия к этилацетатному раствору со стадии (f) при комнатной температуре,
h) фильтрование полученного раствора со стадии (g) через слой броунмиллерита, упаривание фильтрата с получением соединения формулы V
 , и
, и
k) с последующей очисткой сырого соединения со стадии (h) на силикагеле в качестве адсорбента, используя в качестве элюента смесь метанол/этилацет при соотношении 2:8, с получением очищенного соединения формулы (V), в которой R и R1 принимают значения, определенные выше.
В еще другом варианте осуществления апротонный органический растворитель, применяемый на стадии (а), выбран из группы, включающей тетрагидрофуран, ацетон или диметилформамид.
В еще другом варианте осуществления слабое основание, используемое на стадии (а), выбрано из группы карбоната натрия, карбоната калия, карбоната лития, карбоната бария и карбоната цезия.
В еще другом варианте осуществления галогенированный растворитель, используемый на стадии (в), выбран из группы, включающей четыреххлористый углерод, хлороформ и дихлорметан, предпочтительно дихлорметан.
Еще другой вариант осуществления относится к процессу, где щелочной карбонатный раствор, используемый на стадии (с), выбран из растворов бикарбоната натрия, бикарбоната калия или бикарбоната лития.
Таким образом, данный способ относится к способу получения пирроло[2.1-с][1.4]бензодиазепинов формулы V, где R представляет собой Н, ОН, R1 представляет собой Н, ОН и n принимает значения от 3 до 5, который включает: взаимодействие диэтилтиоацеталя (25)-N-[4-(n-бромалкокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида, где R1 представляет собой Н, ОН и n принимает значения 3-5, соединений формулы I, со вторичным амином формулы II, где R представляет собой Н и ОН, в присутствии неорганических слабых оснований, подобных К2СО3, CsCO3 и ВаСО3, в присутствии апротонных смешивающихся с водой органических растворителей, подобных ацетону, ТГФ и ДМФА, кипячение с обратным холодильником в течение вплоть до 12-48 часов, выделение диэтилтиоацеталя (2S)-N-{4-[n-(7-метокси-(11aS)-1,2,3,10,11,11а-гексагидро-5H-пирроло[2.1-с][1.4]бензодиазепин-5-он-8-илокси)алкилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида, формулы III, где R представляет собой Н, ОН, R1 представляет собой Н, ОН и n принимает значения от 3 до 5, обычными способами, восстановление вышеуказанных нитросоединений формулы III с помощью SnCl2·2H2O в присутствии органического растворителя при температуре вплоть до кипячения с обратным холодильником, выделение диэтилтиоацеталя (25)-N-{4-[n-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5H-пирроло[2.1-с][1.4]бензодиазепин-5-он-8-илокси)алкокси]-5-метокси-2-амино-бензоил}пирролидин-2-карбоксальдегида формулы IV, где R представляет собой Н, ОН, R1 представляет собой Н, ОН и n принимает значения от 3 до 5, известными способами, взаимодействие вышеуказанного аминосоединения формулы IV с последующим снятием защитных групп традиционным способом с получением новых пирроло[2.1-с][1.4]бензодиазепинов формулы V, где R представляет собой Н, ОН, R1 представляет собой Н, ОН и n принимает значения от 3 до 5.
Еще один вариант осуществления данного изобретения относится к фармацевтической композиции, эффективной против клеточных линий опухолей человека, причем указанная композиция содержит эффективное количество производного пирроло[2.1-с][1.4]бензодиазепина формулы V, где R и R1 представляют собой Н и/или ОН; и n принимает значения от 3 до 5, вместе с фармацевтически приемлемыми добавками.
Композиция вводится млекопитающим, включая людей. Композиция вводится перорально, системно или любыми другими обычными способами. Фармацевтически приемлемые добавки выбраны из группы, включающей наполнители, разбавители, растворители, носители, лубриканты, связывающие средства и стабилизаторы.
В другом варианте осуществления данного изобретения указанная композиция ингибирует рост раковых клеток.
В другом варианте осуществления указанная композиция ингибирует рост клеток рака, такого как лейкемия, меланома, рак толстой кишки, яичника, простаты, CNS, молочной железы, немелкоклеточной карциномы легкого.
Предшественники, диэтилтиоацеталь (2S)-N-[4-(n-бромалкокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I получен способами, описанными в литературе (ссылка: Kamal, А.; Laxman, N; Ramesh, G.; Nileema, К.; Kondapi, А.К. Chem. Соттип.2001, 437), и 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-с][1.4]бензодиазепин-5-он формулы II получен по литературному способу (ссылка: Kamal, A.; Howard, P.W.; Reddy, B.S.N.; Reddy, B.S.P.; Thurston, D.E. Tetrahedron 1997, 53, 3223-3230).
Некоторые типичные соединения формулы V данного изобретения представлены ниже: 7-метокси-8-{3-[7-метокси-(11aS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-с][1.4]бензодиазепин-5-он-8-илокси]пропокси}-(11аS)-1,2,3,11а-тетрагидро-5Н-пирроло[2.1-с][1.4]бензодиазепин-5-он;
7-метокси-8-{4-[7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он;
7-метокси-8-{5-[7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пентилокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он;
7-метокси-8-{3-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пропокси}-(2R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он;
7-метокси-8-{4-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(2R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он;
7-метокси-8-{5-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пентилокси}-(2R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он.
Способ получения новых пирроло[2.1-c][1.4]бензодиазепинов раскрыт и заявлен заявителями в параллельной заявке, находящейся на рассмотрении.
Данные новые аналоги пирроло[2.1-c][1.4]бензодиазепинов, соединенные в положении С-8, проявили обещающую противораковую активность на различных клеточных линиях. Синтезированные молекулы со свойством к потенциальному последовательному селективному связыванию с ДНК имеют огромное биологическое значение. Данное свойство привело к конструированию и синтезу новых представителей, которые представлены на схеме 1, включающей:
1. Эфирное связывание в положении С-8 промежуточных продуктов DC-81 с вторичным амином.
2. Кипячение реакционной смеси с обратным холодильником в течение 24-48 ч.
3. Синтез противоопухолевых PBD-иминов со свойствами антибиотиков, соединенных в положении С-8.
4. Очистка продукта колоночной хроматографией с помощью различных растворителей подобных этилацетату, гексану и метанолу.
Следующие примеры приведены в качестве иллюстраций и не должны быть восприняты как средства ограничения объема изобретения.
Краткое описание сопровождающего чертежа
Чертеж представляет собой схематическую диаграмму получения соединения общей формулы V.
Пример 1
Раствор диэтилтиоацеталя (2S)-N-[4-(3-бромпропокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (521 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником в течение 48 ч. После завершения реакции, контролируемой ТСХ (TLC), EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc:гексан (8:2), получая чистый диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
1ЯМР (CDCl3) δ 1,35-1,45 (м, 6H), 1,70-2,45 (м,10Н), 2,72-2,90 (м, 4H), 3,20-3,28 (м, 3Н), 3,50-3,58 (м, 1H), 3,62-3,75 (м, 1H) 3,80-3,90 (м, 4H), 4,20 (т, 2H), 4,35 (т, 2H), 4,65-4,75 (м, 1H), 4,85 (д, 1H, J=4,28 Гц), 6,25 (с, 1H), 6,82 (с, 1H), 7,48 (с, 1H), 7,72 (с, 1H); МС (FAB), 689 [М+Н]+.
Диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (688 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2.2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником в течение 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (658 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{3-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пропокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
1H ЯМР (CDCl3) δ 1,65-2,45 (м, 10Н), 3,15-3,25 (м, 2H), 3,48-3,75 (м, 4H), 3,78-3,88 (м, 4H), 3,90 (с, 3H), 4,25-4,35 (м, 5H), 6,18 (с, 1H), 6,82 (с, 1H), 7,48 (с, 1H), 7,52 (с, 1Н), 7,65 (d, 1H, J=4,8 Гц); МС (FAB) 535 [М+H]+.
Пример 2
Раствор диэтилтиоацеталя (2S)-N-[4-(4-бромбутокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (535 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc:гексан (8:2), получая чистый диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
1H ЯМР (CDCl3) δ 1,35-1,45 (м, 6Н), 1,70-2,45 (м, 12H), 2,72-2,90 (м, 4H), 3,20-3,28 (м, 3Н), 3,50-3,58 (м, 1H), 3,62-3,75 (м, 1H) 3,80-3,90 (м, 4H), 4,20 (т, 2H), 4,35 (т, 2Н), 4,65-4,75 (м, 1H), 4,85 (d, 1H, J=4,28 Гц), 6,25 (с, 1H), 6,82 (с, 1H), 7,48 (с, 1H), 7,72 (с, 1H); МС (FAB) 703 [М+Н]+.
Диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида (702 мг, 1,0 ммоль) формулы III растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV (672 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{4-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
1ЯМР (CDCl3) δ 1,65-2,45 (м, 10H), 3,15-3,25 (м, 2H), 3,48-3,75 (м, 4H), 3,78-3,88 (м, 4H), 3,90 (с, 3H), 4,25-4,35 (м, 5H), 6,18 (с, 1H), 6,82 (с, 1H), 7,48 (с, 1H), 7,52 (с, 1H), 7,65 (d, 1H, J=4,8 Гц); МС (FAB) 549 [М+H]+.
Пример 3
Раствор диэтилтиоацеталя (2S)-N-[4-(5-бромпентилокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (549 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc:гексан (8:2), получая чистый диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
1H ЯМР (CDCl3) δ 1,30-1,40 (м, 6Н), 1,65-2,35 (м, 14H), 2,65-2,75 (м, 4H), 3,18-3,32 (м, 3Н), 3,45-3,75 (м, 2Н), 3,80-3,85 (с 4H), 3,85-4,0 (м, 5H), 4,65-4,72 (м, 1H), 4,85 (d, 1H, J=4,38 Гц), 6,0 (с, 1H), 6,78 (с, 1H), 7,52 (с, 1H), 7,65 (с, 1H); МС (FAB) 717 [M+H]+.
Диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (716 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (686 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток растворяли в EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{5-[7-метокси-(11aS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-с][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(11аS)-1,2,3,11а-тетрагидро-5H-пирроло[2.1-с][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
1H ЯМР (CDCl3) δ 1,20-2,45 (м, 14Н), 3,10-3,20 (м, 2Н), 3,20-3,28 (м, 1Н), 3,40-3,78 (м, 5Н), 3,80 (с, 3Н), 3,98 (с, 3Н), 4,10-4,22 (м, 4Н), 6,0 (с, 1Н), 7,02 (с, 1Н); 7,50 (с, 1Н), 7,55 (с, 1Н), 7,65 (g, 1Н, J=5,1 Гц); МС (FAB) 563 [М+Н]+.
Пример 4
Раствор диэтилтиоацеталя (2S)-N-[4-(3-бромпропокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (521 мг, 1 ммоль), 8-гидрокси-7-метокси-(2R}-гидрокси-(11aS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-с][1.4]бензодиазепин-5-она (264 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 24-48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (704 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[3-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[3-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (674 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{3-[7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пропокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (3:7).
Пример 5
Раствор диэтилтиоацеталя (2S)-N-[4-(4-бромбутокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (535 мг, 1 ммоль), 8-гидрокси-7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (264 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида (718 мг, 1,0 ммоль) формулы III растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[4-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[4-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV (688 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{4-[7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (3:7).
Пример 6
Раствор диэтилтиоацеталя (2S)-N-[4-(5-бромпентилокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (549 мг, 1 ммоль), 8-гидрокси-7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (264 мг, 1 ммоль) II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (732 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (2S)-N-{4-[5-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV.
Раствор диэтилтиоацеталя (2S)-N-{4-[5-(7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (702мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc:метанол) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{5-[7-метокси-(2R)-гидрокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пентилокси}-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (3:7).
Пример 7
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-[4-(3-бромпропокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (537 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (704 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2.2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-{4-[3-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пропокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (674 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{3-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пропокси}-(4R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
Пример 8
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-[4-(4-бромбутокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (551 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) формулы II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида (718 мг, 1,0 ммоль) формулы III растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2.2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV.
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-{4-[4-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)бутокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV (688 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{4-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]бутокси}-(4R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
Пример 9
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-[4-(5-бромпентилокси)-5-метокси-2-нитробензоил]пирролидин-2-карбоксальдегида формулы I (565 мг, 1 ммоль), 8-гидрокси-7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-она (248 мг, 1 ммоль) II и К2СО3 (414 мг, 3 ммоль) в сухом ацетоне (20 мл) кипятили с обратным холодильником 48 ч. После завершения реакции, контролируемой ТСХ, EtOAc, реакционную смесь выливали в воду и затем экстрагировали этилацетатом. Упаривание органического слоя приводило к неочищенному продукту, который затем очищали колоночной хроматографией на силикагеле при элюировании EtOAc, получая чистый диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III.
Диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-нитробензоил}пирролидин-2-карбоксальдегида III (732 мг, 1,0 ммоль) растворяли в дихлорметане (5 мл), метаноле (10 мл) и добавляли SnCl2·2H2O (1,124 г, 5,0 ммоль), смесь кипятили с обратным холодильником 1,5 ч. Затем рН реакционной смеси осторожно доводили до 8 с помощью насыщенного раствора NaHCO3 и смесь экстрагировали этилацетатом (3х20 мл). Объединенную органическую фазу сушили над Na2SO4 и упаривали в вакууме, получая неочищенный диэтилтиоацеталь (4R)-гидрокси-(2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида формулы IV.
Раствор диэтилтиоацеталя (4R)-гидрокси-(2S)-N-{4-[5-(7-метокси-(11аS)-1,2,3,10,11,11а-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси)пентилокси]-5-метокси-2-аминобензоил}пирролидин-2-карбоксальдегида IV (702 мг, 1 ммоль), HgCl2 (794 мг, 2,93 ммоль) и СаСО3 (300 мг, 3 ммоль) в СН3CN/H2O (4:1, 15 мл) перемешивали при комнатной температуре 12 ч с хроматографическим контролем (ТСХ, EtOAc) до полного исчезновения исходного продукта. Затем органический слой упаривали в вакууме и остаток разбавляли EtOAc. К содержимому при комнатной температуре медленно добавляли насыщенный раствор NaHCO3, смесь фильтровали через броунмиллерит и промывали этилацетатом. Фильтрат упаривали в вакууме, получая неочищенный 7-метокси-8-{5-[7-метокси-(11аS)-1,2,3,10,11,11a-гексагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он-8-илокси]пентилокси}-(4R)-гидрокси-(11aS)-1,2,3,11a-тетрагидро-5Н-пирроло[2.1-c][1.4]бензодиазепин-5-он формулы V, который затем очищали колоночной хроматографией на силикагеле при элюировании метанол:EtOAc (2:8).
Биологическая активность. Исследования биологической активности in vitro были проведены в Национальном институте рака США.
Цитотоксичность. Соединения Va и Vc оценивали in vitro на шестидесяти клетках опухолей человека, продуцируемых девятью типами рака (лейкемия, немелкоклеточная карцинома легкого, меланома, рак толстой кишки, CNS, яичника, простаты, почки и молочной железы). Для каждого соединения определяли кривые доза-ответ для каждой клеточной линии минимум при пяти концентрациях при 10-кратных разбавлениях. Использовали учет/запись непрерывного воздействия лекарственного средства в течение 48 ч и использовали сульфородамин В (SRB) белковый анализ для оценки жизнеспособности и роста клеток. Вычисляли концентрацию, вызывающую 50% ингибирования роста клеток (GI50), тотальное ингибирование роста клеток (TGI 0% роста) и 50% гибели клеток (LC50, -50% роста) по сравнению с контролем. Средние графические серединные значения log10TGI и log10LC50, а также log10GI50 для Va и Vc перечислены в таблице 1. Как видно из средней графической характеристики, соединение Vc проявляет интересный профиль активности и селективности на различных клеточных линиях. Средние графические серединные значения log10TGI и log10LC50 оказались подобными картине средних графических серединных значений log10GI50.
Средние графические серединные значения (MG-MID) Log10GI50 log10TGI и log10LC50 по цитотоксическим данным in vitro для соединений Va и Vc против клеточных линий опухолей человека.
Значения Log10LC50 (концентрация в моль/л, вызывающая 50% летальности) для соединений Va и Vc.
Каждый тип рака представляет собой в среднем от шести до восьми различных раковых клеточных линий. Противораковая активность для двух представленных соединений дана в таблице 2. Сравнение данных таблицы 2 показывает важность алканового мостика. При увеличении алканового мостика до 3-5 цитотоксическая активность умеренно уменьшалась. Мостик из 3 атомов углерода в соединении Va обеспечивает подходящую подгонку к структуре малой бороздки двойной спирали ДНК и приводит к слабому повышению активности в данных рядах соединений Va и Vc.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИМЕРЫ ПИРРОЛО [2, 1-c][1, 4] БЕНЗОДИАЗЕПИНА В КАЧЕСТВЕ ПРОТИВООПУХОЛЕВЫХ СРЕДСТВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2338747C2 |
| ПИРРОЛОПИРАЗИНОВЫЕ ИНГИБИТОРЫ КИНАЗЫ | 2012 |
|
RU2673064C2 |
| НОВЫЕ ИНГИБИТОРЫ ДИПЕПТИДИЛПЕПТИДАЗЫ IV, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2007 |
|
RU2443687C2 |
| БИЦИКЛИЧЕСКИЕ КЕТОНЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2797922C2 |
| КОНЪЮГАТ АНТИТЕЛО-ПРОИЗВОДНОЕ ПИРРОЛОБЕНЗОДИАЗЕПИНА | 2018 |
|
RU2820928C2 |
| PROTAC, ЦЕЛЕНАПРАВЛЕННО ВОЗДЕЙСТВУЮЩИЕ НА ТАУ-БЕЛОК, И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2017 |
|
RU2805523C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛО[1,5-a]ПИРИМИДИНА И ТИЕНО[3,2-b]ПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ IRAK-4 | 2011 |
|
RU2604062C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗОПИРИДИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ HDM2 | 2013 |
|
RU2690663C2 |
| Бициклические конденсированные гетероарильные или арильные соединения в качестве модуляторов IRAK4 | 2016 |
|
RU2684324C1 |
| ПРОИЗВОДНЫЕ БЕНЗОКСАЗЕПИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СТИМУЛЯТОРОВ РЕЦЕПТОРА АМРА | 2002 |
|
RU2279434C2 |
Описываются новые пирроло [2.1-с] [1.4] бензодиазепины общей формулы V,
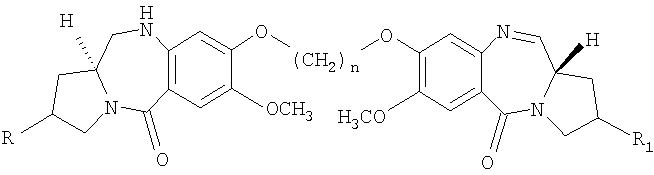
где R и R1 представляют собой Н и/или ОН; и n принимает значения от 3 до 5, способ получения данных соединений и фармацевтическая композиция на их основе. Новые соединения являются ингибиторами роста раковых клеток и могут использоваться в медицине. 3 н. и 18 з.п. ф-лы, 2 табл., 1 ил.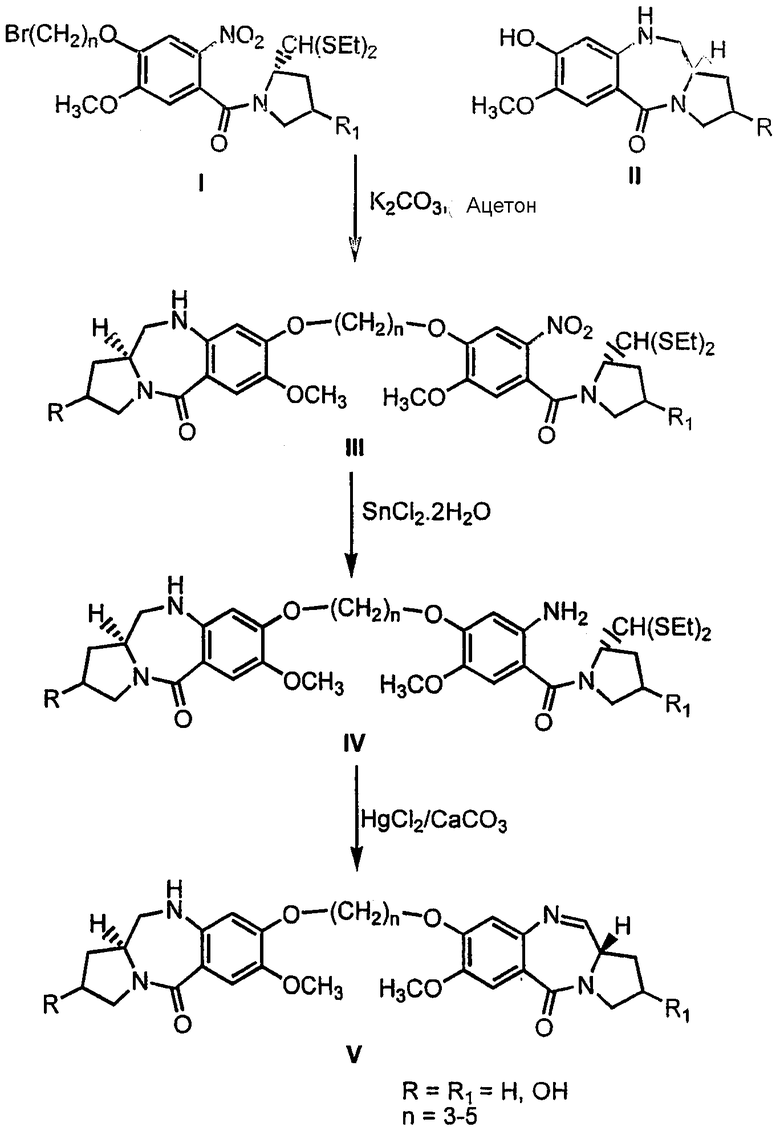
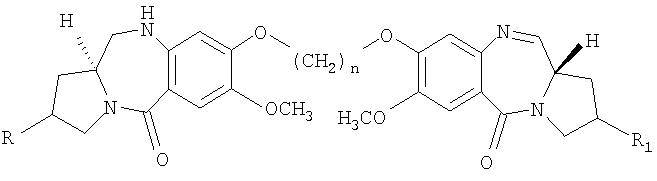
где R и R1 представляют собой Н и/или ОН; n принимает значения от 3 до 5.
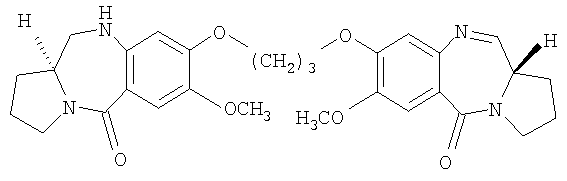
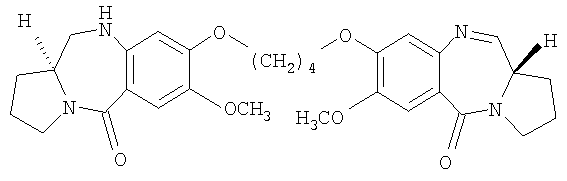
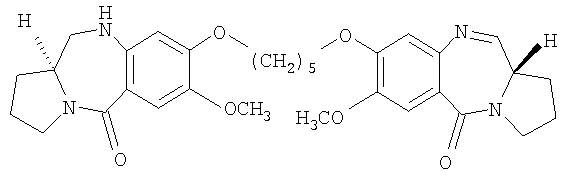
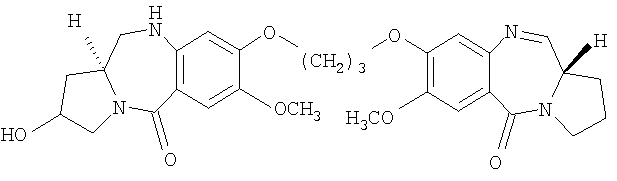
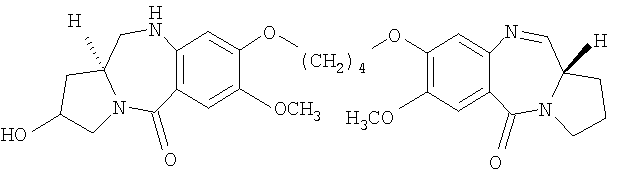
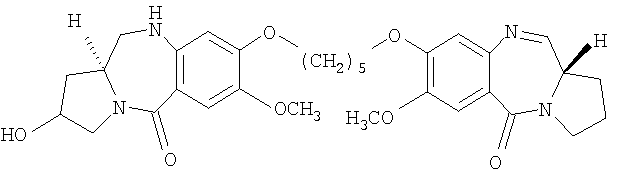
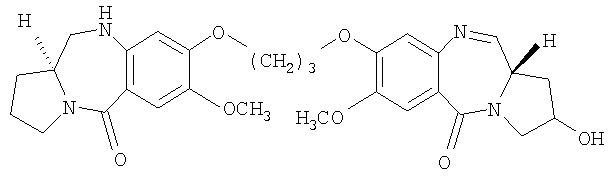
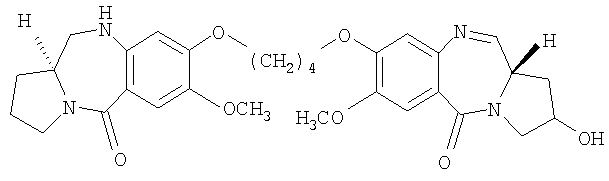
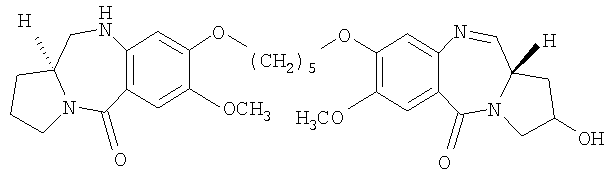
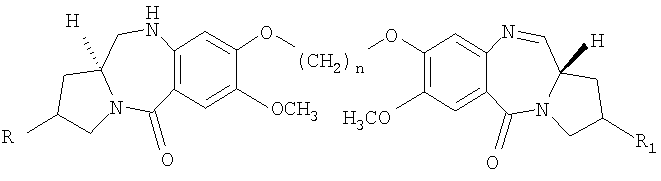
где R, R1 и n имеют значения, указанные в п.1,
заключающийся в том, что осуществляют следующие стадии:
а) взаимодействие соединения формулы (I)
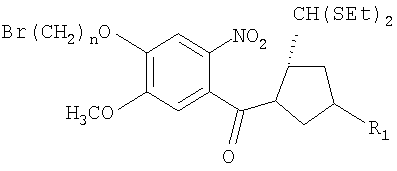
где R1 и n имеют значения, указанные в п.1,
с соединением формулы (II)
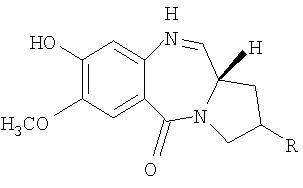
где R имеет значение указанное в п.1,
в присутствии слабого основания в апротонном органическом растворителе, смешивающемся с водой, при кипячении с обратным холодильником в течение периода от 16 до 48 ч,
с получением соединения формулы (III)
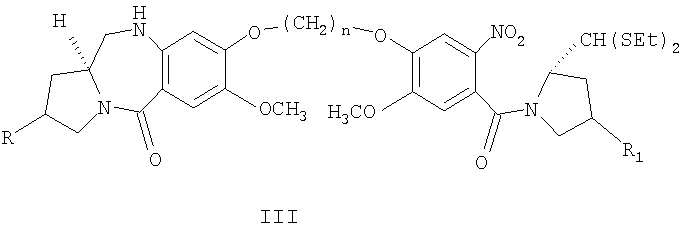
b) восстановление нитросоединения формулы (III) с помощью дигидрата хлорида олова (II) в галогенированном растворителе при кипячении с обратным холодильником в течение периода от 0,5 ч до 2 ч,
c) установление рН реакционной смеси со стадии (b) до 8 с помощью щелочного бикарбонатного раствора,
d) экстрагирование раствора со стадии (с) этилацетатом, упаривание этилацетатного экстракта при пониженном давлении с получением неочищенного соединения формулы (IV)
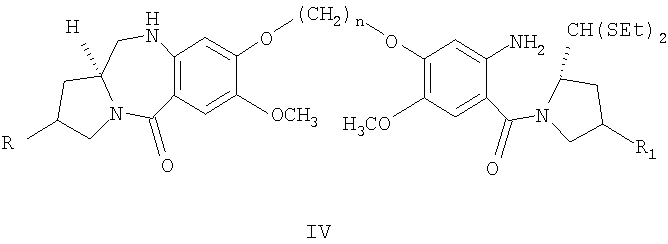
e) приготовление раствора соединения формулы (IV) в смеси ацетонитрил: Н2O при соотношении 4:1, добавление хлорида ртути(II), карбоната кальция, перемешивание при комнатной температуре от 6 до 12 ч,
f) фильтрование и упаривание органического слоя при пониженном давлении с получением остатка, который растворяли в этилацетате,
g) добавление насыщенного раствора бикарбоната натрия к этилацетатному раствору продукта, полученного со стадии (f) при комнатной температуре,
h) фильтрование раствора, полученного со стадии (g), через слой броунмиллерита, упаривание фильтрата с получением сырого соединения формулы V
 , и
, и
k) последующую очистку сырого соединения со стадии (h) на силикагеле в качестве адсорбента, используя в качестве элюента смесь метанол:этилацет при соотношении 2:8, с получением очищенного соединения формулы (V).
| KAMAL A | |||
| et al | |||
| J | |||
| Med | |||
| Chem | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Автономный скважинный прибор для промыслово-геофизических исследований | 1983 |
|
SU1193270A1 |
| ТРИЦИКЛИЧЕСКИЕ ДИАЗЕПИНОВЫЕ АНТАГОНИСТЫ ВАЗОПРЕССИНА И АНТАГОНИСТЫ ОКСИТОЦИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2126006C1 |
Авторы
Даты
2008-01-10—Публикация
2003-03-31—Подача