Область техники
[0001]
Настоящее изобретение относится к конъюгату антитело-лекарственное средство, подходящему для применения в качестве противоопухолевого лекарственного средства, где указанный конъюгат антитело-лекарственное средство содержит антитело, способное нацеливаться на опухолевые клетки, и производное пирролобензодиазепина, которые конъюгированы через линкерный структурный фрагмент.
Уровень техники
[0002]
Конъюгаты антитело-лекарственное средство (ADCs) содержат лекарственное средство с цитотоксической активностью, конъюгированное с антителом, которое связывается с антигеном, экспрессированным на поверхности раковых клеток, и способно к интернализации антигена в клетке посредством связывания. ADCs могут эффективно доставлять лекарственное средство к раковым клеткам и, как предполагается, вызывать тем самым накопление лекарственного средства в раковых клетках и убивать указанные раковые клетки.
Например, ADC Adcetris (ТМ) (брентуксимаб ведотин), который содержит монометилауристатин Е, конъюгированный с моноклональным антителом к CD30, был одобрен в качестве терапевтического лекарственного средства для лечения лимфомы Ходжкина и анапластической крупноклеточной лимфомы. Kadcyla (ТМ) (трастузумаб эмтанзин), который содержит эмтанзин, конъюгированный с моноклональным антителом к HER2, применяют для лечения HER2-положительного прогрессирующего и рецидивирующего рака молочной железы.
Подходящим для применения примером лекарственного средства, которое может быть конъюгировано с получением ADCs, является пирролобензодиазепин (PBD). PBD обладает цитотоксичностью, например, благодаря связыванию последовательности PuGPu в минорной борозде ДНК. Антрамицин, природный PBD, был впервые обнаружен в 1965 году, и с момента его обнаружения были также обнаружены различные природные PBDs и аналоги PBDs (непатентные документы 1-4).
Общая структурная формула PBDs представлена в следующем виде:
[Формула 1]
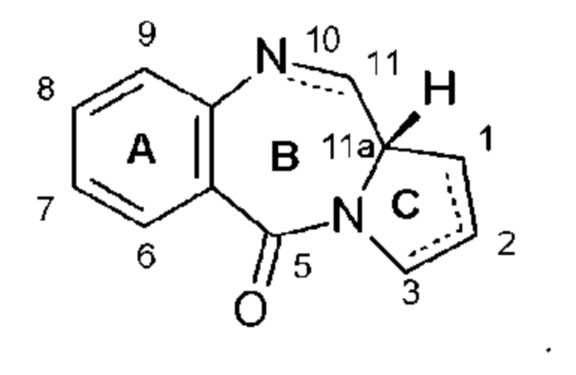
Известны PBDs, отличающиеся числом, типом и местами присоединения заместителей в кольцевых частях А и С, а также степенью ненасыщеннсти в кольцевых частях В и С.
Известно, что у PBDs резко возрастает цитотоксичность при образовании димерной структуры (непатентные документы 5 и 6), и сообщается о различных ADCs с димерными PBD (патентные документы 1-13). Однако PBD, содержащие спирокольцо в его С2-положении, и ADC с ним не известны.
CLDN6 человека (клаудин-6, далее обозначенный как hCLDN6), представитель семейства белков клаудинов (CLDN), представляет собой белок с четырьмя трансмембранными доменами, состоящий из 220 аминокислотных остатков. В ранее проведенных исследованиях предполагалось, что hCLDN6 сверхэкспрессирован при некоторых раковых заболеваниях и представляет собой перспективную терапевтическую мишень для лечения рака (непатентные документы 7-9). Белки семейства CLDN включаются в клетки путем эндоцитоза, и некоторые белки указанного семейства, как сообщалось, имеют короткий период обновления (непатентный документ 10), следовательно, белки семейства CLDN считаются подходящими в качестве мишени для конъюгатов антитело-лекарственное средство (ADCs).
В таких источниках информации, предполагающих связь с раком, описаны моноклональные антитела, способные специфично распознавать hCLDN6 (патентные документы 14 и 15), а также сообщается об ADCs, содержащих монометилауристатин Е (ММАЕ) или майтанзиноид (DM1), которые представляют собой ингибиторы полимеризации тубулина, конъюгированные с CLDN6-специфичным моноклональным антителом (непатентный документ 11).
С одной стороны антитела, способные распознавать несколько членов семейства CLDN, как считается, обеспечивают возможность широкого круга применений с целью лечения, и в свете этого, сообщалось о ADC, содержащем пирролобензодиазепин (PBD) с сильным цитоцидным эффектом, когъюгированный с антителом, способным распознавать CLDN6 и CLDN9 (патентный документ 16), (патентный документ 17).
Однако интенсивности активностей указанных ADCs все еще являются недостаточными, и существует насущная медицинская потребность в применении hCLDN6 в качестве терапевтической мишени.
Список литературы
Патентные документы
[0003]
Патентный документ 1: WO 2013/173496
Патентный документ 2: WO 2014/130879
Патентный документ 3: WO 2017/004330
Патентный документ 4: WO 2017/004025
Патентный документ 5: WO 2017/020972
Патентный документ 6: WO 2016/036804
Патентный документ 7: WO 2015/095124
Патентный документ 8: WO 2015/052322
Патентный документ 9: WO 2015/052534
Патентный документ 10: WO 2016/115191
Патентный документ 11: WO 2015/052321
Патентный документ 12: WO 2015/031693
Патентный документ 13: WO 2011/130613
Патентный документ 14: WO 2009/087978
Патентный документ 15: WO 2011/057788
Патентный документ 16: WO 2015/069794
Патентный документ 17: WO 2017/096163
Непатентные документы
[0004]
Непатентный документ 1: Julia Mantaj, et al., Angewandte Chemie biternationl Edition 2016, 55, 2-29
Непатентный документ 2: Dyeison Antonow, et al., Chemical Reviews 2010, 111, 2815-2864
Непатентный документ 3: In Antibiotics III. Springer Verlag, New York, pp. 3-11
Непатентный документ 4: Accounts of Chemical Research 1986, 19, 230
Непатентный документ 5: Journal of the American Chemical Society 1992, 114, 4939
Непатентный документ 6: Journal of Organic Chemistry 1996, 61, 8141
Непатентный документ 7: BMC Cancer, 2006, 6, 186.
Непатентный документ 8: Histopatholody, 2012, 61, 1043-1056.
Непатентный документ 9: hit J Cancer, 2014, 135, 2206-2214.
Непатентный документ 10: J Membrane Biol, 2004, 199, 29-38.
Непатентный документ 11: 14th Annu Meet Cancer Immunother (CIMT) (May 10-12, Mainz) 2016, Abst 185
Краткое описание изобретения
Проблемы, решаемые настоящим изобретением
[0005]
В настоящем изобретении предложен новый конъюгат антитело-производное пирролобензодиазепина (PBD) и новое производное пирролобензодиазепина (PBD).
В настоящем изобретении предложено новое антитело к CLDN6.
Кроме того, в настоящем изобретении предложена фармацевтическая композиция, содержащая конъюгат антитело-производное PBD, производное PBD или антитело к CLDN6 с противоопухолевой активностью.
Кроме того, в настоящем изобретении предложен способ лечения рака путем применения конъюгата антитело-производное PBD, производного PBD или антитела к CLDN6.
Средства решения указанных проблем
[0006]
Авторы настоящего изобретения в результате активно проводимых исследований обнаружили, что новый конъюгат антитело-производное пирролобензодиазепина (PBD) обладает сильной противоопухолевой активностью, и это позволило создать настоящее изобретение.
В частности, настоящее изобретение относится к следующему.
[0007]
[1] Конъюгат антитело-лекарственное средство, представленный следующей формулой:
[Формула 2]
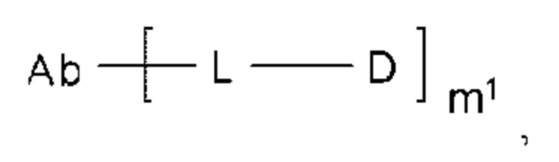
где
m1 представляет собой целое число от 1 до 10, предпочтительно целое число от 2 до 8;
Ab представляет собой антитело или функциональный фрагмент указанного антитела, где указанное антитело необязательно содержит ремоделированный гликан;
L представляет собой линкер, связывающий Ab и D;
Ab может связываться непосредственно через его аминокислотный остаток с L или может связываться через гликан или ремоделированный гликан Ab с L; и
D представляет собой лекарственное средство, представленное следующей формулой: [Формула 3]
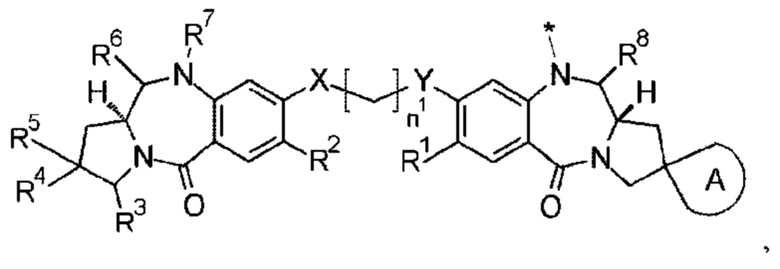
где
звездочка представляет собой связь с L;
n1 представляет собой целое число от 2 до 8;
А представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл, необязательно замещенный одним-четырьмя атомами галогена;
R1 и R2 каждый независимо представляют собой С1-С6 алкоксигруппу, С1-С6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтиогруппу, атом галогена или -NR'R'', где R' и R'' каждый независимо представляют собой атом водорода или С1-С6-алкильную группу;
R3, R4 и R5 выбраны из (i)-(iii):
(i) R3 и R4 объединены вместе с атомами углерода, с которыми связаны R3 и R4, с образованием двойной связи, и R5 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 1, или С1-С6-алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 2,
(ii) R3 представляет собой атом водорода, и R4 и R5 объединены вместе с атомом углерода, с которым R4 и R5 связаны, с образованием трех-пятичлеиного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, или СН2= и
(iii) R3, R4 и R5 объединены вместе с атомом углерода, с которым связан R3, и атомом углерода, с которым связаны R4 и R5, с образованием бензольного кольца или шестичленного гетероцикла, необязательно имеющего один или более заместителей, выбранных из группы 3;
R6 и R7 каждый представляют собой атом водорода, или R6 и R7 объединены и представляют собой иминную связь (C=N);
R8 представляет собой гидроксигруппу или С1-С3 алкоксигруппу;
X и Y каждый независимо представляют собой атом кислорода, атом азота или атом серы;
группа 1 представляет собой:
a) С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С6-алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR' или
j) гидроксигруппу,
где R' и R'' такие, как определено выше, и каждый R''' независимо представляет собой атом водорода или С1-С6-алкильную группу;
группа 2 представляет собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу; и
группа 3 представляет собой атом галогена, или С1-С6-алкильную группу или С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена.
[2] Конъюгат антитело-лекарственное средство в соответствии с [1], где
А представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R1 и R2 каждый независимо представляют собой С1-С3 алкоксигруппу;
R3 и R4 объединены вместе с атомами углерода, с которыми R3 и R4 связаны, с образованием двойной связи;
R5 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 4, или С1-С3 алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 5;
X и Y каждый представляют собой атом кислорода;
группа 4 представляет собой:
a) С1-С3 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С3 алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) С3-С5-циклоалкоксигруппу,
d) -C(=NR')-NR''R''',
e) -NHC(=NR')-NR''R''' или
f) гидроксигруппу,
где R', R'' и каждый R''' независимо представляют собой атом водорода или С1-С3 алкильную группу; и
группа 5 представляет собой атом галогена, гидроксигруппу или С1-С3 алкоксигруппу.
[3] Конъюгат антитело-лекарственное средство по п. [1], где
А представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R1 и R2 каждый независимо представляют собой С1-С3 алкоксигруппу;
R3 представляет собой атом водорода;
R4 и R5 объединены вместе с атомом углерода, с которым связаны R4 и R5, с образованием трех-пяти-членного насыщенного углеводородного кольца или= CH2; и
X и Y каждый представляют собой атом кислорода.
[4] Конъюгат антитело-лекарственное средство по п. [1], где
А представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R1 и R2 каждый независимо представляют собой С1-С3 алкоксигруппу;
R3, R4 и R5 объединены вместе с атомом углерода, с которым связан R3, и атомом углерода, с которым R4 и R5 связаны, с образованием бензольного кольца, необязательно имеющего один или более заместителей, выбранных из группы 6;
X и Y каждый представляют собой атом кислорода; и
группа 6 представляет собой атом галогена, или С1-С3 алкильную группу, или С1-С3 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена.
[5] Конъюгат антитело-лекарственное средство по п. [1] или [2], где D представлен любой из следующих двух формул: [Формула 4]
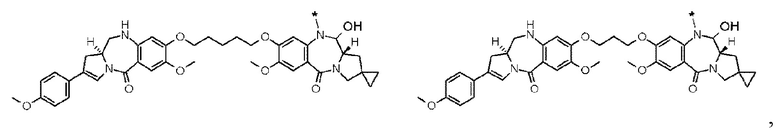
где каждая звездочка представляет собой связь с L.
[6] Конъюгат антитело-лекарственное средство в п. [1] или [3], где D представлен любой из следующих двух формул:
[Формула 5]
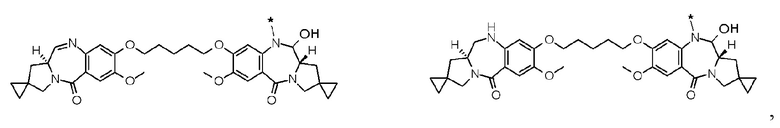
где каждая звездочка представляет собой связь с L.
[7] Конъюгат антитело-лекарственное средство по любому из пп. [1]-[6], где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, звездочка представляет собой связь с D;
В представляет собой фенильную группу или гетероарильную группу;
Lp представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой в клетке-мишени;
La представляет собой любой заместитель, выбранный из группы:
-C(=O)-(СН2СН2)n2-С(=O)-, -C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2)n3-С(=O)-,
-C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2O)n3-CH2-C(=O)-,
-C(=O)-(CH2CH2)n2-NH-C(=O)-(CH2CH2O)n3-CH2CH2-C(=O)- и -(CH2)n4-O-С(=O)-;
n2 представляет собой целое число от 1 до 3, n3 представляет собой целое число от 1 до 5, и n4 представляет собой целое число от 0 до 2; и
Lb представляет собой спейсер, связывающий La и гликан или ремоделированный гликан Ab.
[8] Конъюгат антитело-лекарственное средство по п. [7], где В выбран из 1,4-фенильной группы, 2,5-пиридильной группы, 3,6-пиридильной группы, 2,5-пиримидильной группы и 2,5-тиенильной группы.
[9] Конъюгат антитело-лекарственное средство по п. [8], где В представляет собой 1,4-фенильную группу.
[10] Конъюгат антитело-лекарственное средство по любому из [7]-[9], где Lp представляет собой аминокислотные остатки, состоящие из двух-семи аминокислот.
[11] Конъюгат антитело-лекарственное средство по любому из пп. [7]-[10], где Lp представляет собой аминокислотные остатки, состоящие из аминокислот, выбранных из глицина, валина, аланина, фенилаланина, глутаминовой кислоты, изолейцина, пролина, цитруллина, лейцина, серина, лизина и аспарагиновой кислоты.
[12] Конъюгат антитело-лекарственное средство по любому из пп. [7]-[11], где Lp выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI- и -GGPL-.
[13] Конъюгат антитело-лекарственное средство по любому из [7]-[12], где La выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-С(=O)-СН2СН2-NH-С(=O)-(CH2CH2O)4-СН2СН2-С(=O)-, -СН2-OC(=O)-и -OC(=O)-.
[14] Конъюгат антитело-лекарственное средство по любому из [7]-[13], где Lb представлен следующей формулой:
[Формула 6]
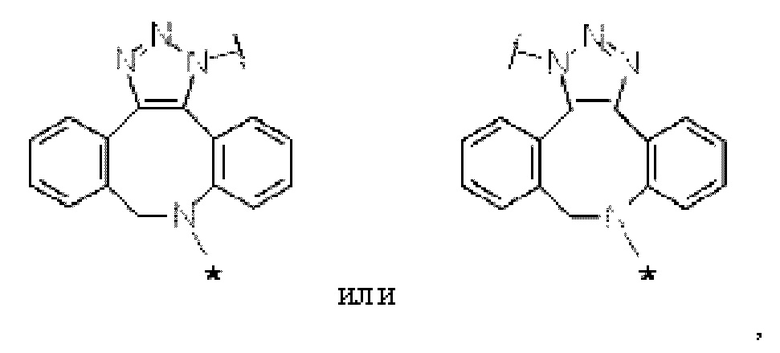
[Формула 7]
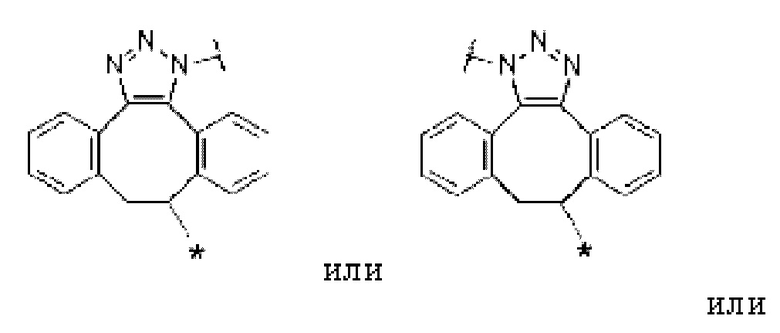
[Формула 8]
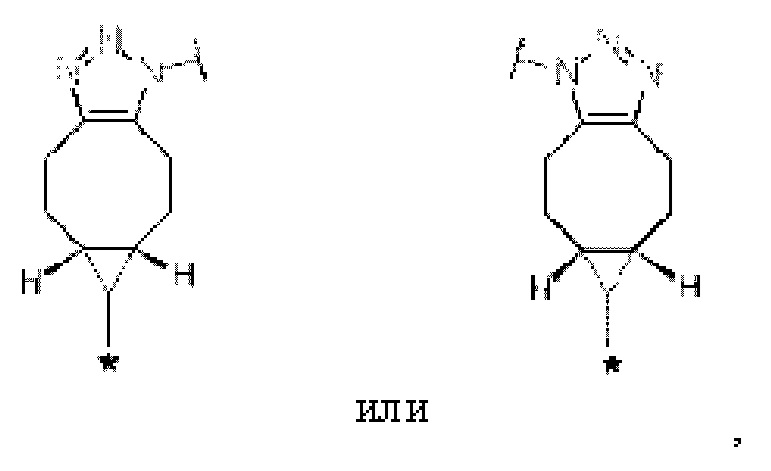
где в каждой структурной формуле для Lb, представленной выше,
каждая звездочка представляет собой связь с La, и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
[15] Конъюгат антитело-лекарственное средство по любому из [7]-[14], где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, где
B представляет собой 1,4-фенильную группу,
Lp выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVGit-, -GGVK- и -GGPL-;
La выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-СН2СН2)2-С(=O)-,
-С(=O)-СН2СН2-С(=O)-NH-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -СН2-ОС(=O)- и -OC(=O)-; н
Lb представлен следующей формулой:
[Формула 9]
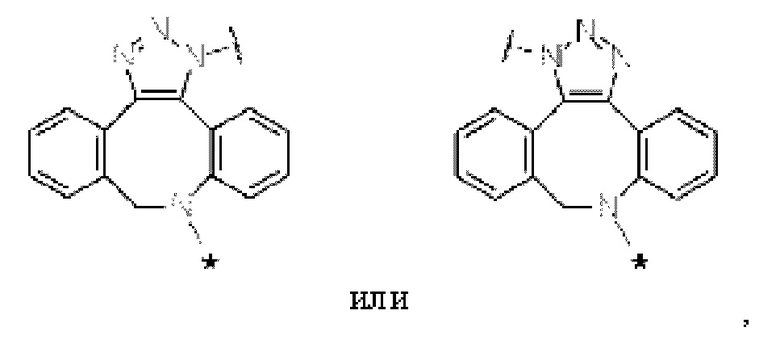
[Формула 10]
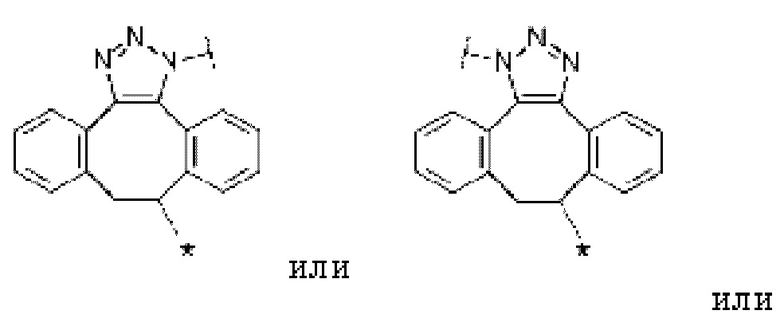
[Формула 11]
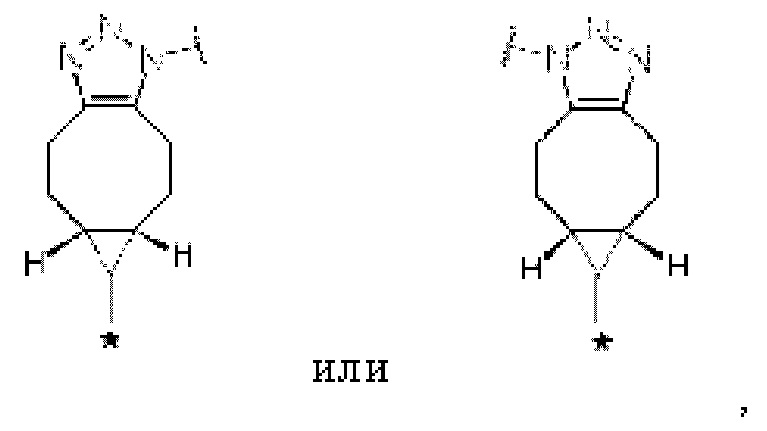
где в каждой структурной формуле для Lb, представленной выше,
каждая звездочка представляет собой связь с La, и каждая волнистая линия представляет собой связь с гликаном или ремоделированный гликаном Ab.
[16] Конъюгат антитело-лекарственное средство по любому из [7]-[15], где
L выбран из следующей группы:
-Z1-С(=O)-СН2СН2-С(=O)-GGVA-NH-B-СН2-ОС(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-GG-(D-)VA-NH-B-СН2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-(CH2CH2)2-С(=O)-VA-NH-В-СН2-ОС(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-GGPI-NH-B-СН2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B-СН2-OC(=О)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B-СН2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-СН2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-ОС(=O)-,
-Z2-OC(=O)-GGVA-NH-B-CH2-OC(=O)- и -Z3-CH2-OC(=O)-GGVA-NH-B-СН2-ОС(=O)-, где
Z1 представляет собой следующую структурную формулу:
[Формула 12]
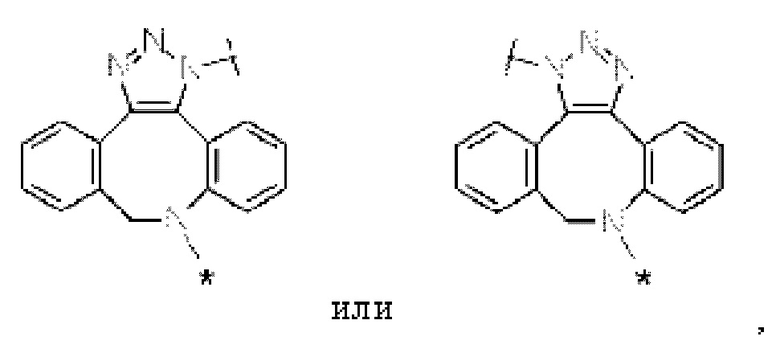
Z2 представляет собой следующую структурную формулу:
[Формула 13]
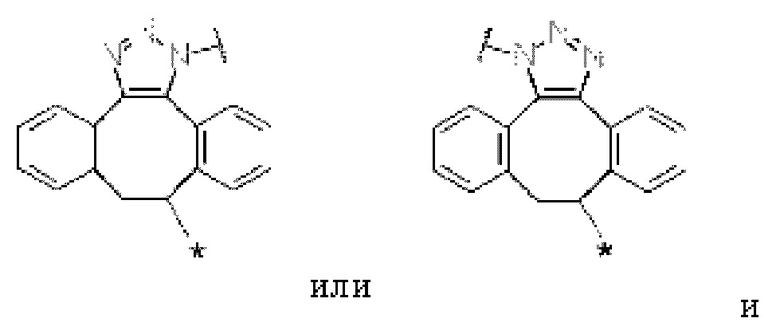
Z3 представляет собой следующую структурную формулу:
[Формула 14]
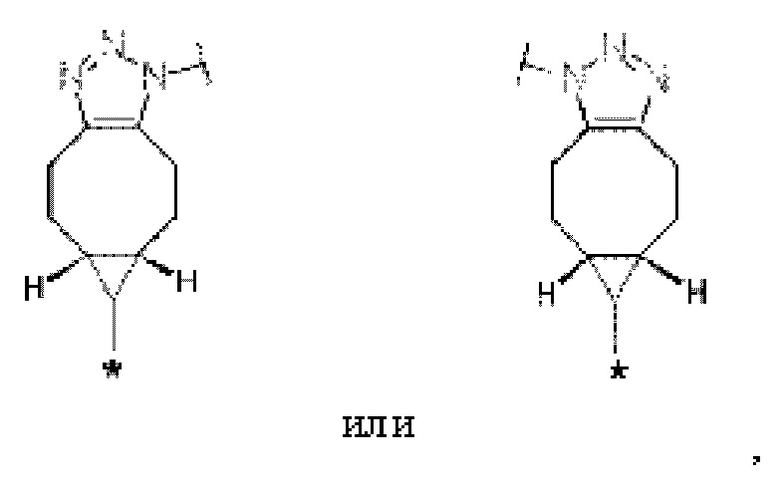
где в каждой структурной формуле для Z1, Z2 и Z3,
каждая звездочка представляет собой связь с La, каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab; и
B представляет собой 1,4-фенильную группу.
[17] Конъюгат антитело-лекарственное средство по п. [16], где
L выбран из следующей группы:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-СН2-ОС(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-VA-NH-В-СН2-ОС(=О)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-GGVCit-NH-B-СН2-OC(=О)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-СН2-ОС(=O)- и
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-ОС(=O)-, где
В представляет собой 1,4-фенильную группу, и Z1 представляет собой следующую структурную формулу:
[Формула 15]
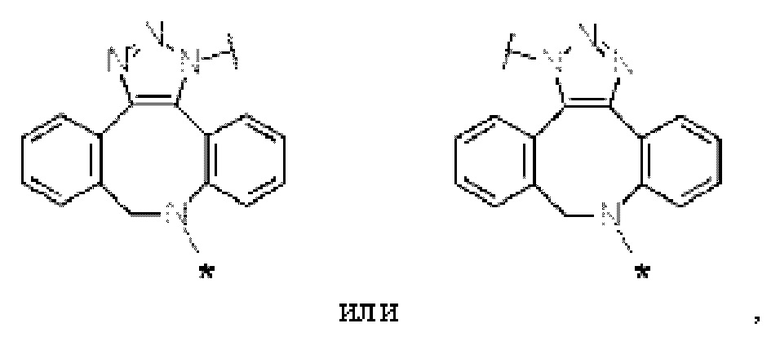
где в структурной формуле для Z1,
каждая звездочка представляет собой связь с C(=O), соседним с Z1, и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
[18] Конъюгат антитело-лекарственное средство по любому из [1]-[6], где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, где
звездочка представляет собой связь с D;
B представляет собой 1,4-фенильную группу,
Lp представляет собой -GGVA- или -VA;
La представляет собой -(СН2)n9-С(=O)- или -(CH2CH2)n10-C(=O)-NH-(CH2CH2O)n11-CH2CH2-C(=O)-, где n9 представляет собой целое число от 2 до 7, n10 представляет собой целое число от 1 до 3, и n11 представляет собой целое число от 6 до 10; и
Lb представляет собой -(сукцинимид-3-ил-N)-.
[19] Конъюгат антитело-лекарственное средство по п. [18], где
L выбран из следующей группы:
-(сукцинимид-3-ил-N)-(СН2)5-С(=O)-VA-NH-В-СН2-ОС(=O)-,
-(сукцинимид-3-ил-N)-(CH2)5-C(=O)-GGVA-NH-B-CH2-OC(=O)- и
-(сукцинимид-3-ил-N)-СН2СН2-С(=O)-NH-(CH2CH2O)8-СН2СН2-С(=О)-VA-NH-B-СН2-ОС(=O)-, где В представляет собой 1,4-фенильную группу.
[20] Конъюгат антитело-лекарственное средство по любому из [1]-[19], причем указанное антитело представляет собой IgG.
[21] Конъюгат антитело-лекарственное средство по п. [20], причем указанное антитело представляет собой IgG1, IgG2 или IgG4.
[22] Конъюгат антитело-лекарственное средство по любому из [1]-[21], причем указанное антитело связывается с опухолевой клеткой и внедряется и интернализируется в опухолевую клетку.
[23] Конъюгат антитело-лекарственное средство по п. [22], причем указанное антитело дополнительно обладает противоопухолевым эффектом.
[24] Конъюгат антитело-лекарственное средство по любому из [1]-[17] и [20]-[23], причем указанное антитело связывается посредством гликановой связи с Asn297 антитела (N297-гликан) с L.
[25] Конъюгат антитело-лекарственное средство по п. [24], причем указанный N297-гликан представляет собой ремоделированный гликан.
[26] Конъюгат антитело-лекарственное средство по п. [24] или [25], причем указанный N297-гликан представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или их смесь, или N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 16]
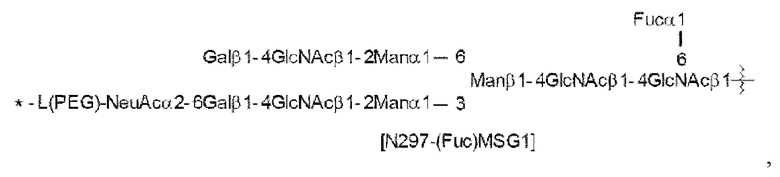
где
волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(СН2СН2-O)n5-СН2СН2-NH-, причем указанная аминогруппа на правом конце связана посредством амидной связи с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в 1-3 разветвленной цепи β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10,
[Формула 17]
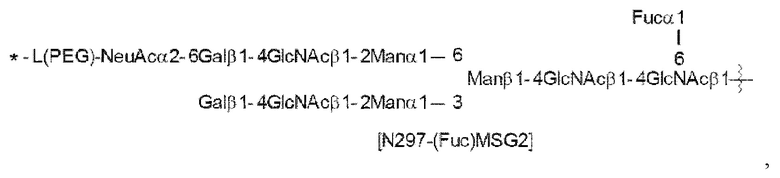
где
волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(СН2СН2-O)n5-СН2СН2-NH-, причем указанная аминогруппа на правом конце связана через амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в 1-6 разветвленной цепи β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10 и
[Формула 18]
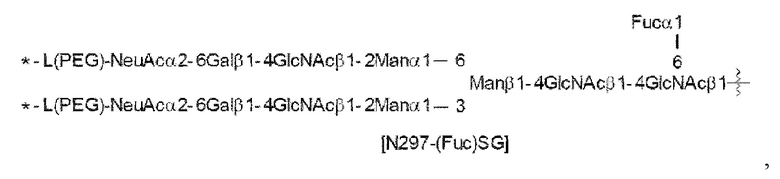
где
волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, причем указанная аминогруппа связана через амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10.
[27] Конъюгат антитело-лекарственное средство по п. [26], где n5 представляет собой целое число от 2 до 5.
[28] Конъюгат антитело-лекарственное средство по любому из [24]-[27], представленный следующей формулой:
[Формула 19]
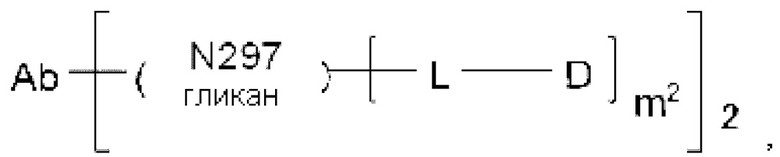
где
m2 представляет собой целое число, равное 1 или 2;
L представляет собой линкер, связывающий N297-гликан Ab и D, и представляет собой любой линкер, выбранный из следующей группы:
-Z1 -С(=O)-СН2СН2-С(=O)-GGVA-NH-B-СН2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-GGVCit-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-С(=O)-СН2СН2-С(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)- и
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-, где
В представляет собой 1,4-фенильную группу, и Z1 представляет собой следующую структурную формулу:
[Формула 20]
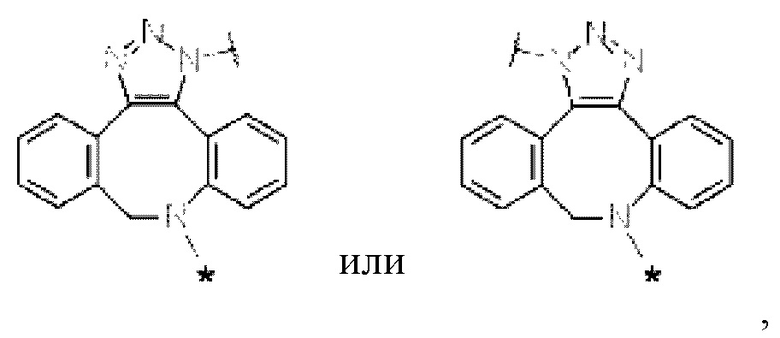
где в структурных формулах для Z1,
каждая звездочка представляет собой связь с С(=O), соседним с Z1, и каждая волнистая линия представляет собой связь с гликаном N297 Ab;
Ab представляет собой антитело IgG или функциональный фрагмент указанного антитела;
N297-гликан Ab представляет собой одно из N297-(Fuc)MSG1, N297-(Fuc)MSG2 и их смеси, и N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 21]
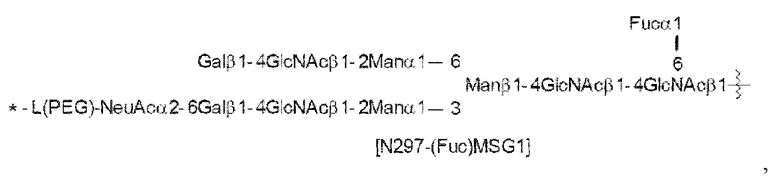
[Формула 22]
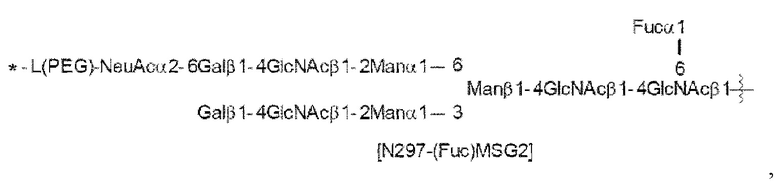
[Формула 23]
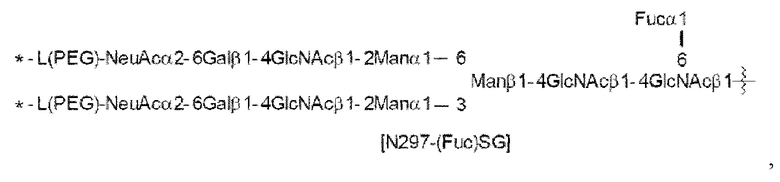
где
каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) в N297-гликане представляет собой -NH-CH2CH2-(O-CH2CH2)n5-*,
где
n5 представляет собой целое число от 2 до 5, аминогруппа на левом конце связана амидной связью с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой или в одной из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане, и каждая звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца Z1 в линкере L; и
D выбран из следующей группы:
[Формула 24]
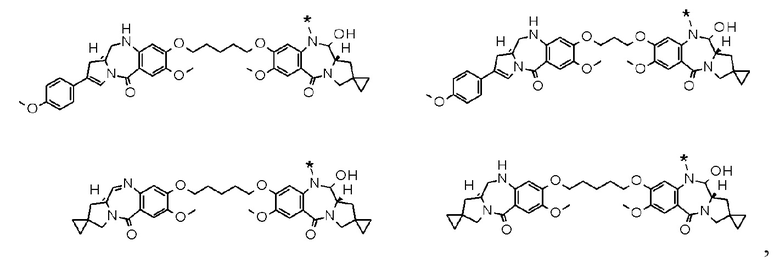
где
каждая звездочка представляет собой связь с L.
[29] Конъюгат антитело-лекарственное средство, выбранный из следующей группы:
[Формула 25]
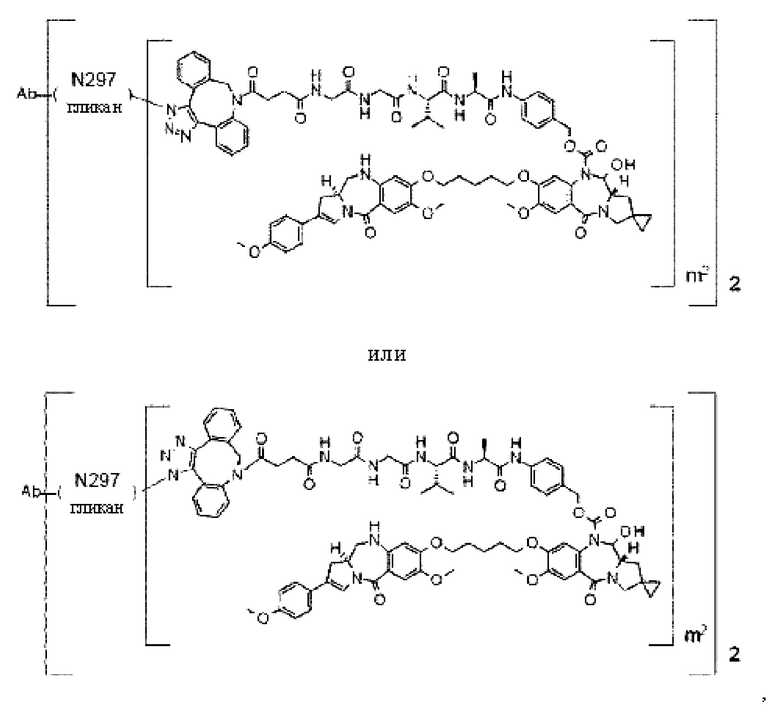
[Формула 26]
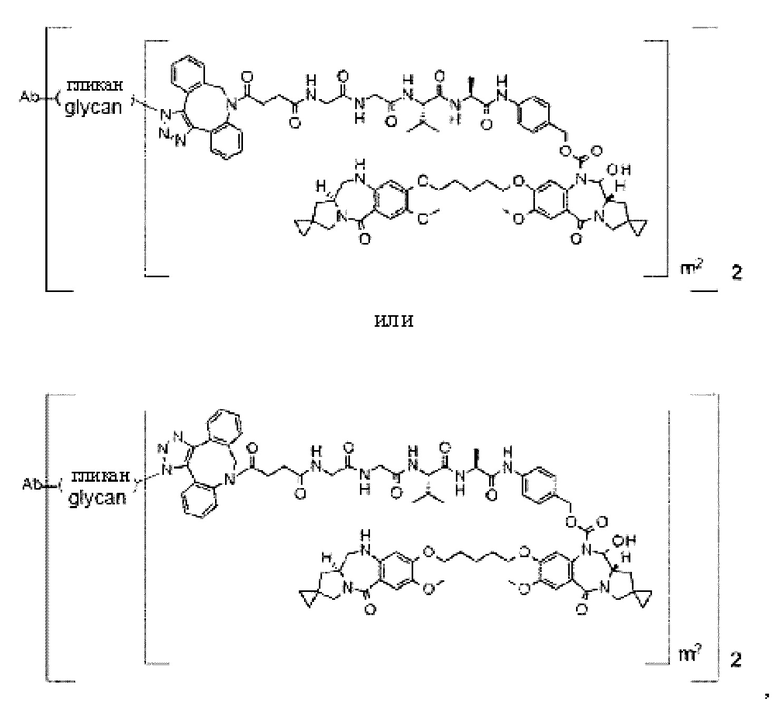
[Формула 27]
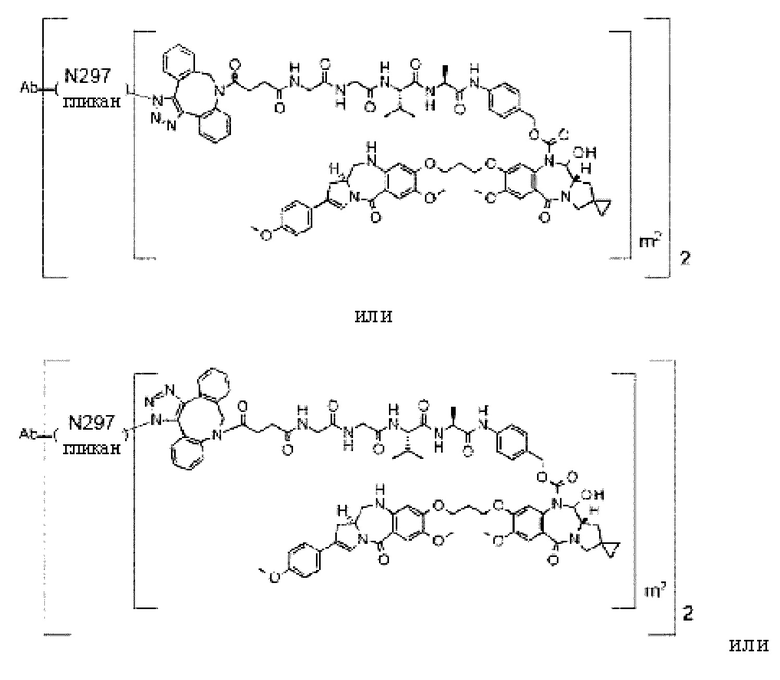
[Формула 28]
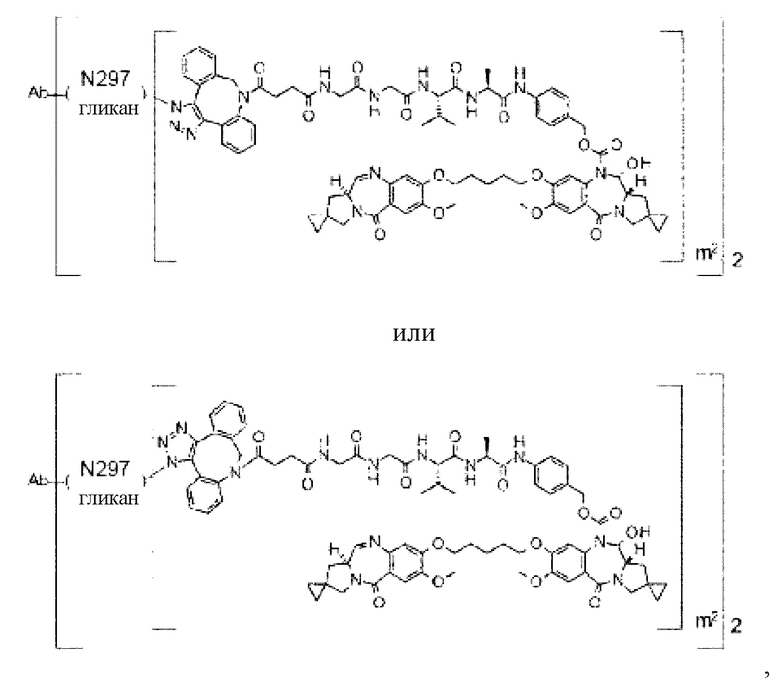
где в каждой структурной формуле, представленной выше,
m2 представляет собой целое число, равное 1 или 2;
Ab представляет собой антитело IgG или функциональный фрагмент указанного антитела;
N297-гликан Ab представляет собой одно из N297-(Fuc)MSG1, N297-(Fuc)MSG2, и их смеси, и N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 29]
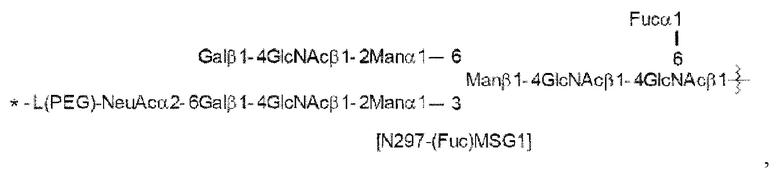
[Формула 30]
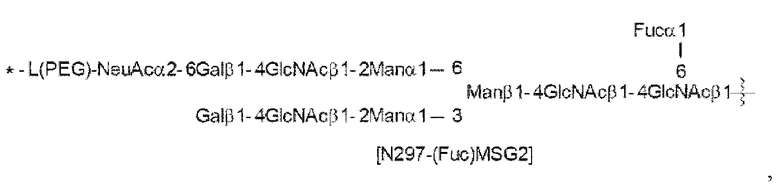
[Формула 31]
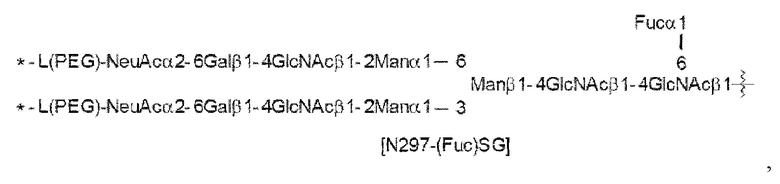
где
каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) в N297-гликане представляет собой -NH-CH2CH2-(O-CH2CH2)3-*,
где
аминогруппа на левом конце связана амидной связью с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой или в одной из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане, и каждая звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца в соответствующей структурной формуле.
[30] Антитело, которое связывается с CLDN6 и/или CLDN9, или функциональный фрагмент указанного антитела.
[31] Антитело по п. [30] или функциональный фрагмент указанного антитела, где CLDN6 представляет собой молекулу, состоящую из аминокислотной последовательности, представленной SEQ IN NO: 1, и CLDN9 представляет собой молекулу, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 3.
[32] Антитело по п. [30] или [31] или функциональный фрагмент указанного антитела, причем указанное антитело содержит тяжелую цепь, содержащую CDRH1, CDRH2 и CDRH3, и легкую цепь, содержащую CDRL1, CDRL2 и CDRL3, описанные в любом из следующих (а) и (b):
(a) CDRH1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 9, CDRH2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 10, и CDRH3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 11, и CDRL1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 5, CDRL2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 6, и CDRL3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 7 или аминокислотной последовательности, содержащей одну или две аминокислотные замены в аминокислотной последовательности, представленной SEQ ID NO: 7; и
(b) CDRH1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 15, CDRH2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 16, и CDRH3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 17, и CDRL1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 12, CDRL2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 13, и CDRL3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 14.
[33] Антитело по п. [32] или функциональный фрагмент указанного антитела, причем указанное антитело содержит тяжелую цепь, содержащую CDRH1, CDRH2 и CDRH3, и легкую цепь, содержащую CDRL1, CDRL2 и CDRL3, описанные в любом из следующих (а) и (b):
(a) CDRH1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 9, CDRH2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 10, и CDRH3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 11, и CDRL1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 5, CDRL2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 6, и CDRL3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 7 или аминокислотной последовательности, представленной SEQ ID NO: 8; и
(b) CDRH1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 15, CDRH2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 16, и CDRH3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 17, и CDRL1, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 12, CDRL2, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 13, и CDRL3, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 14.
[34] Антитело по любому из [30]-[33] или функциональный фрагмент указанного антитела, причем указанное антитело содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, описанные в любом из следующих (а) и (b):
(a) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 21, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 19; и
(b) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 25, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 23.
[35] Антитело по любому из [30]-[34] или функциональный фрагмент указанного антитела, причем указанное антитело, содержит вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из следующих (а)-(е) и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из следующих (f)-(k):
(a) аминокислотная последовательность, представленная SEQ ID NO: 54;
(b) аминокислотная последовательность, представленная SEQ ID NO: 58;
(c) аминокислотная последовательность, представленная SEQ ID NO: 62;
(d) аминокислотная последовательность с гомологией по меньшей мере 95% или выше по отношению к последовательности каркасной области, исключая последовательности CDR, в любой из последовательностей (а)-(с);
(e) аминокислотная последовательность, содержащая от одной до нескольких аминокислотных делеций, замен или добавлений в последовательности каркасной области, исключая последовательности CDR, в любой из последовательностей (а)-(с);
(f) аминокислотная последовательность, представленная SEQ ID NO: 38;
(g) аминокислотная последовательность, представленная SEQ ID NO: 42;
(h) аминокислотная последовательность, представленная SEQ ID NO: 46;
(i) аминокислотная последовательность, представленная SEQ ID NO: 50;
(j) аминокислотная последовательность с гомологией по меньшей мере 95% или выше по отношению к последовательности каркасной области, исключая последовательности CDR, в любой из последовательностей (f)-(i); и
(k) аминокислотная последовательность, содержащая одну или несколько аминокислотных делеций, замен или добавлений в последовательности каркасной области, исключая последовательности CDR, в любой из последовательностей (f)-(i).
[36] Антитело по п. [35] или функциональный фрагмент указанного антитела, причем указанное антитело содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи, выбранные из группы, состоящей из следующих (а)-(е):
(a) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 54, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 38;
(b) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 58, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 42;
(c) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 54, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 46;
(d) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 58, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 50; и
(e) вариабельная область тяжелой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 62, и вариабельная область легкой цепи, состоящая из аминокислотной последовательности, представленной SEQ ID NO: 46.
[37] Антитело по любому из [30]-[36] или функциональный фрагмент указанного антитела, причем указанное антитело представляет собой химерное антитело. [38] Антитело по любому из [30]-[36] или функциональный фрагмент указанного антитела, причем указанное антитело представляет собой гуманизированное антитело.
[39] Антитело по любому из [30]-[38] или функциональный фрагмент указанного антитела, причем указанное антитело содержит константную область тяжелой цепи IgG1 человека, IgG2 человека или IgG4 человека.
[40] Антитело по п. [38] или [39] или функциональный фрагмент указанного антитела, антитело содержит тяжелую цепь и легкую цепь, выбранные из группы, состоящей из следующих (а)-(е):
(a) тяжелая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 52, и легкая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 из SEQ ID NO: 36 (H1L1);
(b) тяжелая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 56, и легкая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 из SEQ ID NO: 40 (H2L2);
(c) тяжелая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 52, и легкая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 из SEQ ID NO: 44 (H1L3);
(d) тяжелая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 56, и легкая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 из SEQ ID NO: 48 (H2L4); и
(e) тяжелая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 60, и легкая цепь, состоящая из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 из SEQ ID NO: 44 (H3L3).
[41] Антитело по п. [30] или [31] или функциональный фрагмент указанного антитела, причем указанное антитело связывается с сайтом антигена, распознаваемого антителом, по любому из [32]-[36] и [40].
[42] Антитело по п. [30] или [31] или функциональный фрагмент указанного антитела, причем указанное антитело конкурирует с антителом по любому из [32]-[36] и [40] за связывание с CLDN6 и/или CLDN9.
[43] Полинуклеотид, кодирующий антитело по любому из [30]-[42].
[44] Полинуклеотид по п. [43], содержащий полинуклеотид, выбранный из группы, состоящей из следующих (a)-(j):
(a) полинуклеотид, кодирующий вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 54, и полинуклеотид, кодирующий вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 38;
(b) полинуклеотид, кодирующий вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 58, и полинуклеотид, кодирующий вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 42;
(c) полинуклеотид, кодирующий вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 54, и полинуклеотид, кодирующий вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 46;
(d) полинуклеотид, кодирующий вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 58, и полинуклеотид, кодирующий вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 50;
(e) полинуклеотид, кодирующий вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 62, и полинуклеотид, кодирующий вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 46;
(f) полинуклеотид, кодирующий тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 52, и полинуклеотид, кодирующий легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 SEQ ID NO: 36;
(g) полинуклеотид, кодирующий тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 56, и полинуклеотид, кодирующий легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 SEQ ID NO: 40;
(h) полинуклеотид, кодирующий тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 52, и полинуклеотид, кодирующий легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 SEQ ID NO: 44;
(i) полинуклеотид, кодирующий тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 56, и полинуклеотид, кодирующий легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 SEQ ID NO: 48; а также
(j) полинуклеотид, кодирующий тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 20 по 471 SEQ ID NO: 60, и полинуклеотид, кодирующий легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 234 SEQ ID NO: 44.
[45] Вектор экспрессии, содержащий полинуклеотид по п. [43] или [44].
[46] Клетка-хозяин, трансформированная вектором экспрессии по п. [45].
[47] Клетка-хозяин по п. [46], причем указанная клетка-хозяин представляет собой эукариотическую клетку.
[48] Клетка-хозяин по п. [47], причем указанная клетка-хозяин представляет собой клетку животного.
[49] Способ получения антитела по любому из [30]-[42] или функционального фрагмента антитела, причем указанный способ включает стадии: культивирования клетки-хозяина по любому из [46]-[48]; и сбор целевого антитела из культуры, полученной на стадии культивирования.
[50] Антитело, полученное с применением способа по п. [49], или функциональный фрагмент указанного антитела.
[51] Антитело по любому из [30]-[42] и [50] или функциональный фрагмент указанного антитела, причем указанное антитело содержит одну, две или более модификаций, выбранных из группы, состоящей из N-связанного гликозилирования, O-связанного гликозилирования, N-концевого процессинга, C-концевого процессинга, дезамидирования, изомеризации аспарагиновой кислоты, окисления метионина, добавления метионинового остатка на N-конце, амидирования пролинового остатка и делеции одного или двух аминокислотных остатков на карбоксильном конце тяжелой цепи.
[52] Антитело по п. [51] или функциональный фрагмент указанного антитела, где один или несколько аминокислотных остатков удалены на карбоксильном конце тяжелой цепи.
[53] Антитело по п. [52] или функциональный фрагмент указанного антитела, где на карбоксильном конце каждой из двух тяжелых цепей удален один аминокислотный остаток.
[54] Антитело по любому из [50]-[53] или функциональный фрагмент указанного антитела, где пролиновый остаток на карбоксильном конце тяжелой цепи дополнительно амидирован.
[55] Способ получения гликан-ремоделированного антитела, причем указанный способ включает следующие стадии:
i) культивирование клетки-хозяина по любому из [46]-[48] и сбор целевого антитела из полученной культуры;
ii) обработка антитела, полученного на стадии i) гидролазой с получением (Fucα1,6)GlcNAc-антитела; и
iii)-1 проведение полученного реакции (Fucα1,6)GlcNAc-антитела с молекулой-донором гликана в присутствии трансгликозидазы, причем указанную молекулу-донор гликана получают путем введения ПЭГ-линкера, содержащего азидную группу, в карбонильную группу карбоновой кислоты в положении 2 сиаловой кислоты в MSG (9) или SG (10) и оксазолинирования восстанавливающего конца, или
iii)-2 проведение реакции (Fucα1,6)GlcNAc-антитела и молекулы-донор а гликана в присутствии трансгликозидазы, где указанная молекула-донор гликана получена путем введения ПЭГ-линкера, содержащего азидную группу, в карбонильную группу карбоновой кислоты в положении 2 сиаловой кислоты в (MSG-)Asn или (SG-)Asn с необязательно защищенной α-аминогруппой и в карбонильную группу карбоновой кислоты в Asn, вызывая действие гидролазы с последующим оксазолинированием восстанавливающего конца.
[56] Способ по п. [55], дополнительно включающий стадию очистки (Fucα1,6)ClcNAc-антитела путем очистки реакционного раствора, полученного на стадии ii), на колонке с гидроксиапатитом.
[57] Способ получения конъюгата антитело-лекарственное средство по любому из [1]-[29], включающий следующие стадии:
i) получение гликан-ремоделированного антитела с применением способа по п. [55] или [56] и
ii) проведение реакции лекарственного средства-линкера, содержащего дибензоциклооктин (DBCO) (промежуточное соединение), и азидной группы в гликане гликан-ремоделированного антитела, полученного на стадии i).
[58] Гликан-ремоделированное антитело, полученное с применением способа по п. [55] или [56].
[59] Конъюгат антитело-лекарственное средство, полученный с применением способа по п. [57].
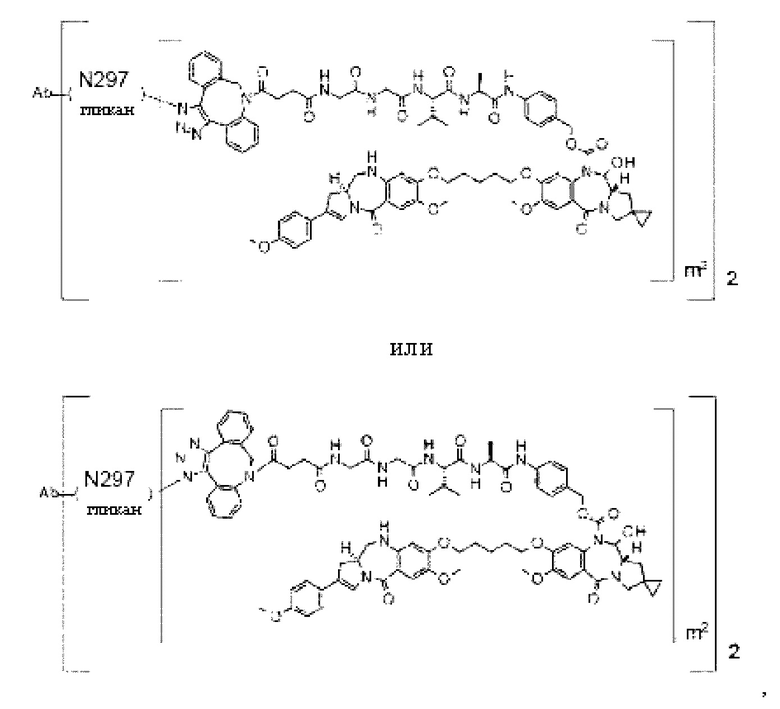
[60] Конъюгат антитело-лекарственное средство, выбранный из следующей группы:
[Формула 32]
[Формула 33]
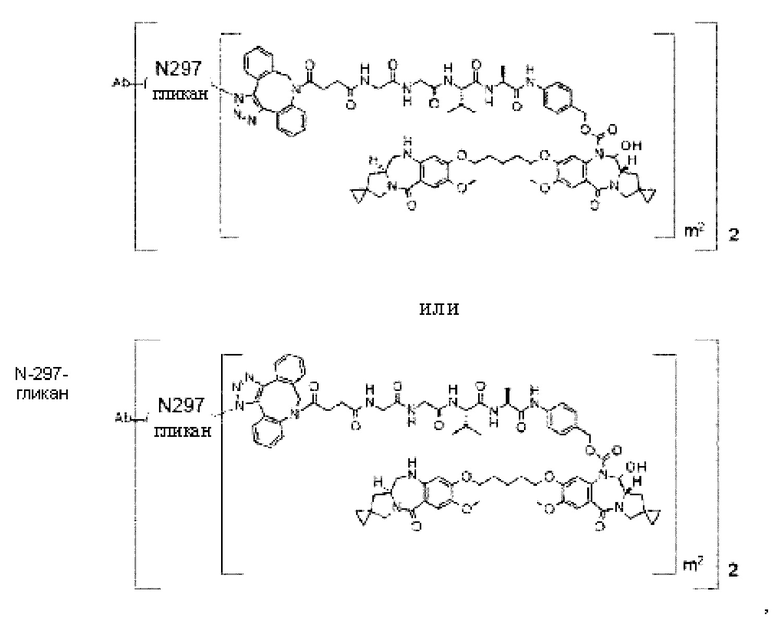
[Формула 34]
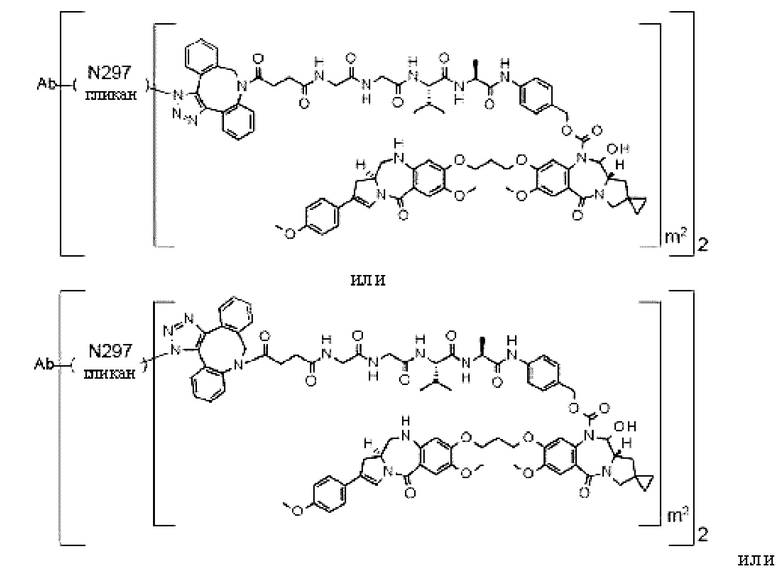
[Формула 35]
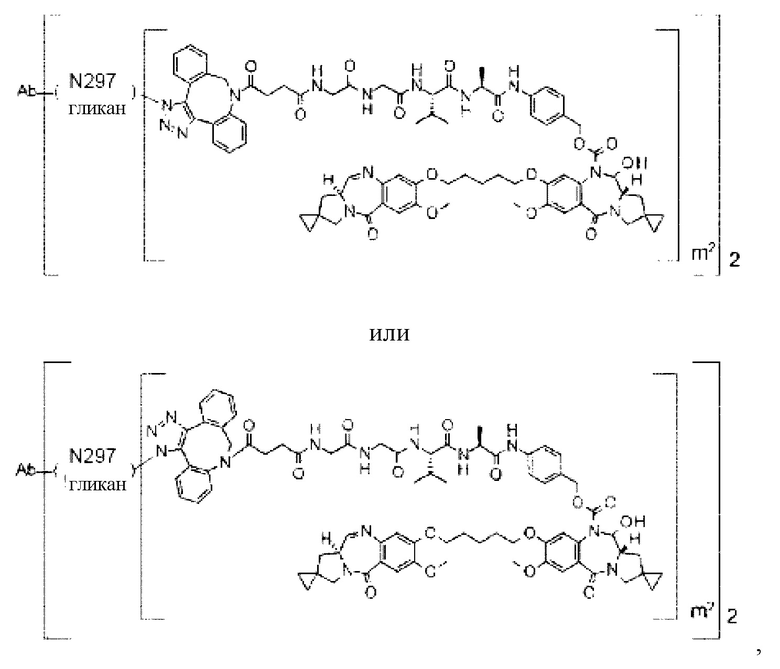
где в каждой структурной формуле, представленной выше,
m2 представляет собой целое число, равное 1 или 2;
Ab представляет собой антитело по любому из [30]-[42], [50]-[54] и [58], или функциональный фрагмент указанного антитела, или антитело к HER2; и
N297-гликан Ab представляет собой одно из N297-(Fuc)MSG1, N297-(Fuc)MSG2, и их смеси, и N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 36]
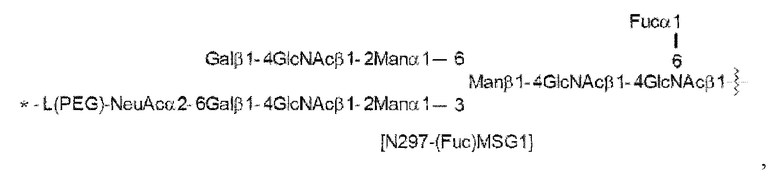
[Формула 37]
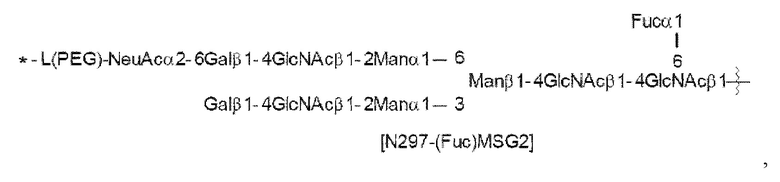
[Формула 38]
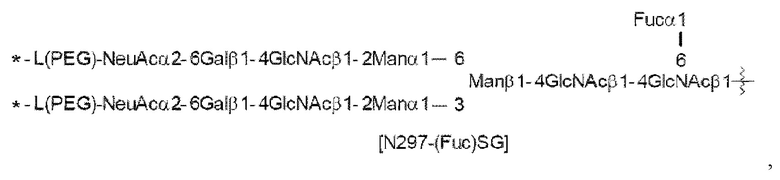
где
каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) представляет собой -NH-CH2CH2-(O-CH2CH2)3-*, причем указанная аминогруппа на левом конце связана амидной связью с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой или в одной из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане, и каждая звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца в соответствующей структурной формуле.
[61] Конъюгат антитело-лекарственное средство по любому из [1]-[29], [59] и [60], причем среднее количество конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитела-лекарственного средства составляет от 1 до 3 или от 3 до 5.
[62] Соединение, соль соединения или гидрат соединения или его соли, причем указанное соединение представлено следующей формулой:
[Формула 39]
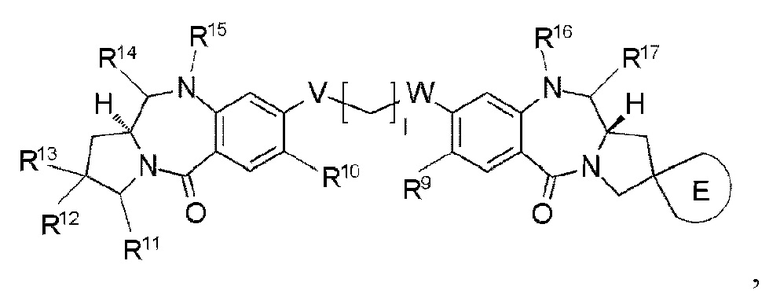
где
l представляет собой целое число от 2 до 8;
Е представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл, необязательно замещенный одним-четырьмя атомами галогена;
R9 и R10 каждый независимо представляют собой С1-С6 алкоксигруппу, С1-С6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтиогруппу, атом галогена или -NR'R'', где
R' и R'' каждый независимо представляют собой атом водорода или С1-С6-алкильную группу;
R11, R12 и R13 выбраны из следующий (i)-(iii):
(i) R11 и R12 объединены вместе с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи, и R13 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 7, или С1-С6-алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 8,
(ii) R11 представляет собой атом водорода, и R12 и R13 объединены совместно с образованием трех-пятичленного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, или СН2= и
(iii) R11 и R12 объединены совместно с образованием бензольного кольца или шестичленного гетероцикла, необязательно имеющего один или более заместителей, выбранных из группы 9, и R13 представляет собой одинарную связь;
R14 и R15 каждый представляют собой атом водорода, или R14 и R15 объединены и представляют собой иминную связь (C=N);
R16 и R17 представляет собой одно из следующих (а) и (b):
(a) R16 и R17 объединены с образованием иминной связи (N=C) и
(b) R16 представляет собой J-La'-Lp'-NH-B'-CH2-O (С=O)-*,
где
звездочка представляет собой связь с атомом азота, соседним с R16,
В' представляет собой фенильную группу или гетероарильную группу,
Lp' представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой в клетке-мишени,
La' представляет собой одно из следующих группы:
-C(=O)-(CH2CH2)n6-C(=O)-, -C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2)n7-С(=O)-,
-C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2O)n7-CH2-C(=O)-,
-C(=O)-(CH2CH2)n6-NH-C(=O)-(CH2CH2O)n7-CH2CH2-C(=O)-, -(CH2)n8-O-С(=O)-,
-(CH2)n12-C(=O)- и -(CH2CH2)n13-C(=O)-NH-(CH2CH2O)n14-CH2CH2-C(=O)-,
где n6 представляет собой целое число от 1 до 3, n7 представляет собой целое число от 1 до 5, n8 представляет собой целое число от 0 до 2, n12 представляет собой целое число от 2 до 7, n13 представляет собой целое число от 1 до 3, и n14 представляет собой целое число от 6 до 10,
J представляет собой одно из следующих:
[Формула 40]
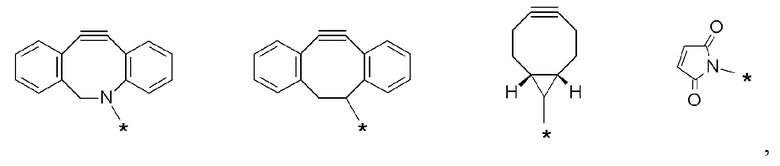
где в структурных формулах для J, представленных выше,
каждая звездочка представляет собой связь с La';
R17 представляет собой гидроксигруппу или С1-С3 алкоксигруппу;
V и W каждый независимо представляют собой атом кислорода, атом азота или атом серы;
группа 7 представляет собой:
a) С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С6-алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR' или
j) гидроксигруппу,
где
R' и R'' такие, как определено выше, и каждый R''' независимо представляет собой атом водорода или С1-С6-алкильную группу;
группа 8 представляет собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу; и
группа 9 представляет собой атом галогена, или С1-С6-алкильную группу или С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена.
[63] Соединение по п. [62], соль соединения или гидрат соединения или его соли, где
Е представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R9 и R10 каждый независимо представляют собой С1-С3 алкоксигруппу;
R11 и R12 объединены вместе с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи;
R13 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 10, или С1-С3 алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 11;
V и W каждый представляют собой атом кислорода;
группа 10 представляет собой:
a) С1-С3 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С3 алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) С3-С5-циклоалкоксигруппу,
d) -C(=NR')-NR''R''',
e) -NHC(=NR')-NR''R''' или
f) гидроксигруппу,
где
R', R'' и каждый R''' независимо представляют собой атом водорода или С1-С3 алкильную группу; и
группа 11 представляет собой атом галогена, гидроксигруппу или С1-С3 алкоксигруппу.
[64] Соединение по п. [62], соль соединения или гидрат соединения или его соли, где
Е представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R9 и R10 каждый независимо представляют собой С1-С3 алкоксигруппу;
R11 представляет собой атом водорода;
R12 и R13 объединены вместе с атомом углерода, с которым связаны R12 и R13, с образованием трех-пяти-членного насыщенного углеводородного кольца или =CH2; и
V и W каждый представляют собой атом кислорода.
[65] Соединение по п. [62], соль соединения или гидрат соединения или его соли, где
Е представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, необязательно замещенное одним или двумя атомами галогена;
R9 и R10 каждый независимо представляют собой С1-С3 алкоксигруппу;
R11, R12 и R13 объединены вместе с атомом углерода, с которым связан R11, и атомом углерода, с которым связаны R12 и R13, с образованием бензольного кольца, необязательно имеющего один или более заместителей, выбранных из группы 12;
V и W каждый представляют собой атом кислорода; и
группа 12 представляет собой атом галогена, или С1-С3 алкильную группу, или С1-С3 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена.
[66] Соединение по любому из [62]-[65], соль соединения или гидрат соединения или его соли, где
В' выбран из 1,4-фенильной группы, 2,5-пиридильной группы, 3,6-пиридильной группы, 2,5-пиримидильной группы и 2,5-тиенильной группы.
[67] Соединение по п. [66], соль соединения или гидрат соединения или его соли, где В' представляет собой 1,4-фенильную группу.
[68] Соединение по любому из [62]-[67], соль соединения или гидрат соединения или его соли, где Lp' представляет собой аминокислотные остатки, выбранные из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)P-I-и -GGPL-.
[69] Соединение по любому из [62]-[68], соль соединения или гидрат соединения или его соли, где La' выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -СН2-ОС(=O)-, -ОС(=O)-,
-(СН2)5-С(=O)- и -CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-.
[70] Соединение по любому из [62]-[69], соль соединения или гидрат соединения или его соли, где
R16 представлен формулой J-La'-Lp'-NH-B'-CH2-O (С=O)-*, где
В' представляет собой 1,4-фенильную группу;
Lp' выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK- и -GGPL-;
La' выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -СН2-ОС(=O)-, -OC(=O)-,
-(СН2)5-С(=O)- и -CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-; и
J представляет собой одно из следующих:
[Формула 41]
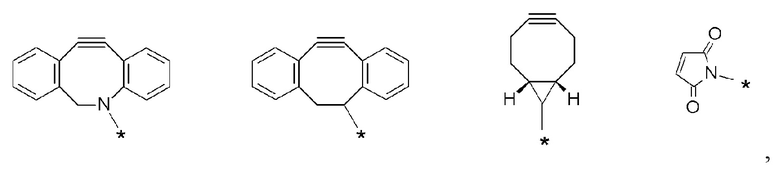
где в структурных формулах для J
каждая звездочка представляет собой связь с La'.
[71] Соединение по любому из [62]-[70], соль соединения или гидрат соединения или его соли, где
R16 выбран из следующей группы:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GG-(D-)VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPI-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J3-CH2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)- и J4-CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-, где
J1, J2, J3 и J4 представлены следующими структурными формулами:
[Формула 42]
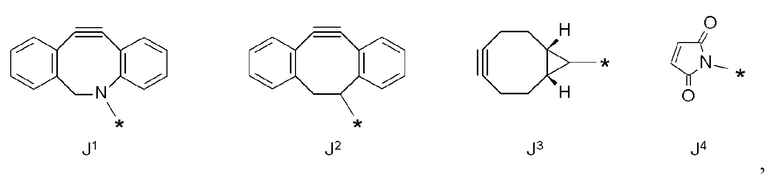
где в структурных формулах для J1, J2, J3 и J4 каждая звездочка представляет собой связь с соседней группой и
В' представляет собой 1,4-фенильную группу.
[72] Соединение по любому из [62]-[71], соль соединения или гидрат соединения или его соли, где
R16 выбран из следующей группы:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-GGVA-NH-B'-CH2-OC(=O)- и
J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)-, где
В' представляет собой 1,4-фенильную группу и
J1 и J4 представлены следующими структурными формулами:
[Формула 43]
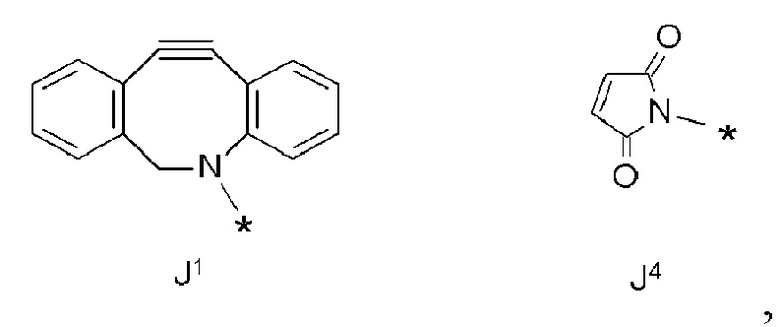
где в структурных формулах для J1 и J4
каждая звездочка представляет собой связь с соседней группой.
[73] Соединение, соль соединения или гидрат соединения или его соли, причем указанное соединение представляет собой любое соединение, выбранное из следующих формул:
[Формула 44]
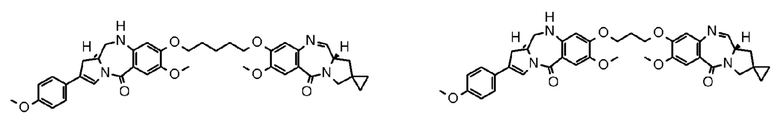
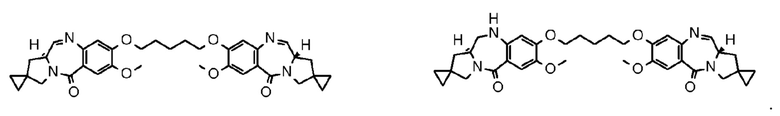
[74] Соединение, соль соединения или гидрат соединения или его соли, причем указанное соединение представляет собой любое соединение, выбранное из следующих формул:
[Формула 45]
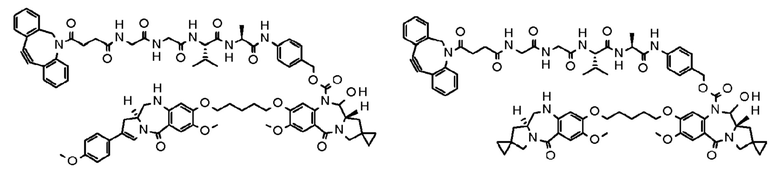
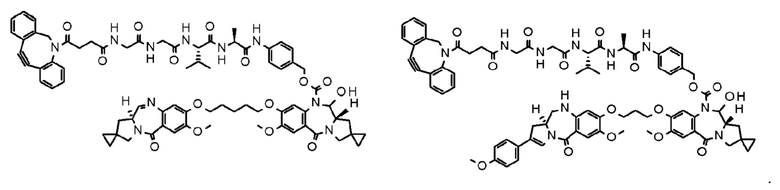
[75] Конъюгат антитело-лекарственное средство по любому из [1]-[29] и [59]-[61], где D представлен следующей формулой:
[Формула 46]
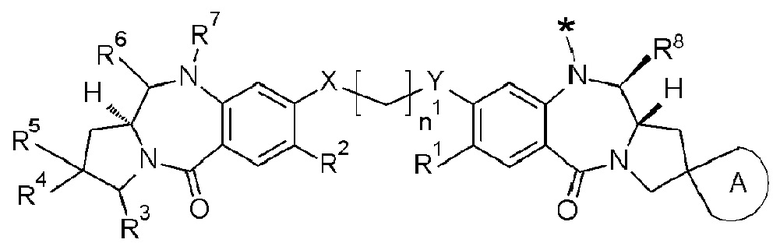
[76] Соединение по любому из [62]-[72] и [74], соль соединения или гидрат соединения или его соли, причем указанное соединение представлено следующей формулой:
[Формула 47]
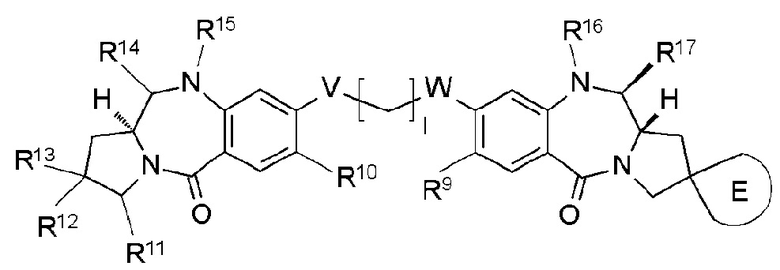
[77] Конъюгат антитело-лекарственное средство по любому из [1]-[29] и [59]-[61], где D представлен следующей формулой:
[Формула 48]
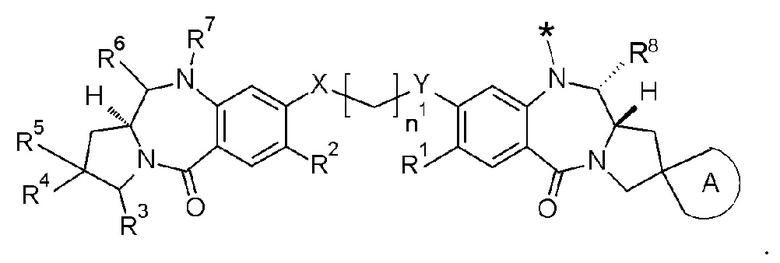
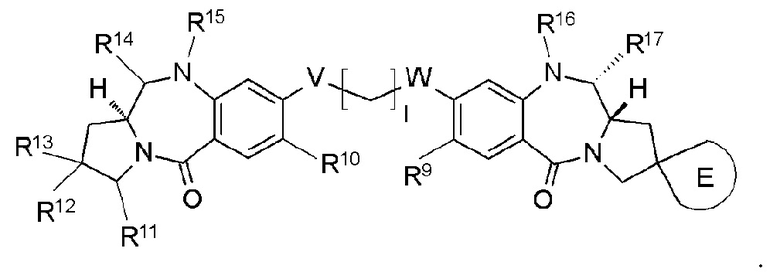
[78]
Соединение по любому из [62]-[72] и [74], соль соединения или гидрат соединения или его соли, причем указанное соединение представлено следующей формулой:
[Формула 49]
[79] Фармацевтическая композиция, содержащая любой из конъюгата антитело-лекарственное средство по любому из [1]-[29] и [59]-[61], [75] и [77], соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; антитела по любому из [30]-[42], [50]-[54] и [58] или функционального фрагмента указанного антитела; и соединения по любому из [62]-[74], [76] и [78], соли указанного соединения или гидрата указанного соединения или его соли.
[80] Фармацевтическая композиция по п. [79], причем указанная композиция представляет собой противоопухолевое лекарственное средство.
[81] Фармацевтическая композиция по п. [80], причем указанная опухоль представляет собой опухоль, экспрессирующую CLDN6 и/или CLDN9.
[82] Фармацевтическая композиция по п. [80] или [81], причем указанная опухоль представляет собой рак яичников (поверхностную эпителиальную опухоль, стромальную опухоль или опухоль зародышевой клетки), рак легкого (немелкоклеточный рак легкого или мелкоклеточный рак легкого), рак желудка, рак эндометрия, рак яичка (семиному или несеминому), рак шейки матки, плацентарную хориокарциному, рак почки, уротериальный рак, колоректальный рак, рак простаты, мультиформную глиобластому, рак головного мозга, рак поджелудочной железы, рак молочной железы, меланому, рак печени, рак мочевого пузыря или рак пищевода.
[83] Способ лечения опухоли, где любой из конъюгата антитело-лекарственное средство по любому из [1]-[29] и [59]-[61], [75] и [77], соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; антитело по любому из [30]-[42], [50]-[54] и [58] или функционального фрагмента указанного антитела; и соединения по любому из [62]-[74], [76] и [78], соли указанного соединения или гидрата указанного соединения или его соли вводят индивидууму.
[84] Способ по п. [83], причем указанная опухоль представляет собой опухоль, экспрессирующую CLDN6 и/или CLDN9.
[85] Способ по п. [83] или [84], причем указанная опухоль представляет собой рак яичников (поверхностную эпителиальную опухоль, стромальную опухоль или опухоль зародышевой клетки), рак легкого (немелкоклеточный рак легкого или мелкоклеточный рак легкого), рак желудка, рак эндометрия, рак яичка (семиному или несеминому), рак шейки матки, плацентарную хориокарциному, рак почки, уротериальный рак, колоректальный рак, рак простаты, мультиформную глиобластому, рак головного мозга, рак поджелудочной железы, рак молочной железы, меланому, рак печени, рак мочевого пузыря или рак пищевода.
[86] Способ лечения опухоли, согласно которому фармацевтическую композицию, содержащую по меньшей мере одно, выбранное из конъюгата антитело-лекарственное средство по любому из [1]-[29] и [59]-[61], [75] и [77], соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; антитела по любому из [30]-[42], [50]-[54] и [58] или функционального фрагмента указанного антитела; и соединения по любому из [62]-[74], [76] и [78], соли указанного соединения или гидрата указанного соединения или его соли, и по меньшей мере одно противоопухолевое лекарственное средство вводят индивидууму одновременно, раздельно или последовательно.
[87] Соединение, демонстрирующее спектр протонного ЯМР с положениями пиков, по существу аналогичными положениям пиков, приведенных в таблице 1 или таблице 2.
Предпочтительные эффекты, достигаемые изобретением
[0008]
Новый конъюгат антитело-производное пирролобензодиазепина (PBD), предложенный в настоящем изобретении, обладает превосходной противоопухолевой активностью и безопасностью и, соответственно, является подходящим для применения в качестве противоопухолевого агента. Производное PBD согласно настоящему изобретению обладает противоопухолевой активностью и, таким образом, является подходящим для применения в качестве лекарственного средства для конъюгата. Кроме того, антитело согласно настоящему изобретению распознает опухолевые клетки или связывается с опухолевыми клетками и, соответственно, является подходящим для применения в качестве антитела для конъюгата.
Краткое описание чертежей
[0009]
[Фигура 1] На фигуре 1 представлено схематическое изображение конъюгата лекарственного средства согласно настоящему изобретению (молекулы (I)). (а) обозначает лекарственное средство D, (b) обозначает линкер L, (с) обозначает N3-L(PEG)- и (d) обозначает N297-гликан (эллипс без заливки: NeuAc(Sia), шестиугольник без заливки: Man, шестиугольник с заливкой: GlcNAc, ромб без заливки: Gal, перевернутый треугольник без заливки: Fuc). (b) и (с) объединены с образованием триазольного кольцо путем реакции между азидной группой (каплевидная форма с заливкой) (с) и спейсера (полукруг без заливки) (b). Y-образное изображение представляет собой антитело Ab. Для удобства на данном схематическом изображении N297-гликан обозначен как N297-(Fuc)MSG, и на указанном изображении продемонстрирован вариант реализации, когда любая одна из двух ветвей каждого из гликанов N297 содержит сиаловую кислоту, с которой связывается ПЭГ-линкер, содержащий азидную группу (N3-L(PEG)-), а при этом другая ветвь не содержит сиаловой кислоты на невосстанавливающем конце (т.е. N297-(Fuc)MSG); однако также приемлемым является другой вариант реализации, где каждая из двух ветвей N297-гликана содержит сиаловую кислоту, к которой ПЭГ-линкер, содержащий азидную группу, связывается на невосстанавливающем конце (то есть N297-(Fuc)SG). Если не указано иное, такой формат изображения применяется во всем настоящем описании.
[Фигура 2] На фигуре 2 представлены схематические изображения, иллюстрирующие структуры (Fucα1,6)GlcNAc-антитела (молекула А в (II) на фигуре 2), которое является промежуточным соединением при получении конъюгата лекарственного средства согласно настоящему изобретению и антитела, ремоделированного гликаном MSG-типа (молекула (III) в В на фигуре 2). На каждом из изображений Y-образное изображение представляет собой антитело Ab, как на фигуре 1. В молекуле А на фигуре 2 (е) обозначает N297-гликан, содержащий только GlcNAc в положении 6, соединенный с Fuc в положении 1 посредством α-гликозидной связи. В молекуле В на фигуре 2 (d) обозначает тот же N297-гликан, что и на фигуре 1, и (f) обозначает структуру ПЭГ-линкерной части, содержащую азидную группу, в частности, азидную группу, присоединяемую к линкеру L на конце. Связывающий вариант ПЭГ-линкера, содержащего азидную группу, является таким, как описано на фигуре 1.
[Фигура 3] На фигуре 3 представлено схематическое изображение стадии получения антитела, ремоделированного гликаном MSG-типа, из антитела, полученного из клетки животного. Как и на фигуре 2, молекулы (II) и (III) на данной фигуре представляют собой (Fucα1,6)GlcNAc-антитело и антитело, ремоделированное гликаном MSG-типа, соответственно. Молекула (IV) представляет собой антитело, полученное в клетке жиотного, и является смесью молекул с фрагментами гетерогенного N297-гликана. Фигура 3А иллюстрирует стадию получения гомогенного (Fucα1,6)GlcNAc-антитела (II) путем обработки фрагментов гетерогенного N297-гликана (IV) гидролазой, такой как EndoS. Фигура 3В иллюстрирует стадию получения антитела (III), ремоделированного гликаном MSG-типа, путем воздействия на GlcNAc N297-гликана в антителе (II) действию трансгликозидазы, такой как вариант EndoS D233Q/Q303L, для трансгликозилирования гликана молекулы-донора гликана MSG-типа. Молекула-донор гликана MSG-типа, используемая в данном случае, содержит сиаловую кислоту на невосстанавливающем конце MSG, модифицированного ПЭГ-линкером, содержащим азидную группу. Таким образом, полученное антитело, ремоделированное гликаном N297 MSG-типа, также содержит сиаловую кислоту на невосстанавливающем конце, модифицированную таким же образом, как описано для фигуры 2В. Для удобства на фигуре 3В представлен MSG в качестве донорной молекулы. Однако гликан-ремоделированное антитело, в котором линкерная молекула, содержащая азидную группу, связывается с каждым невосстанавливающим концом N297-гликана, также может быть синтезировано как ремоделированное антитело (III) с применением SG (10) в качестве донора гликана.
[Фигура 4] На фигуре 4 представлено действие конъюгатов ADC26, ADC19 и ADC54 антитело к HER2-лекарственное средство на подкожно трансплантированные клетки NCI-N87 линии клеток рака желудка человека.
[Фигура 5] На фигуре 5 представлено действие конъюгата ADC49 антитело к HER2-лекарственное средство, трастузумаба и конъюгата ADC53 антитело к LPS-лекарственное средство на подкожно трансплантированные клетки NCI-N87 линии клеток рака желудка человека.
[Фигура 6] На фигуре 6 представлено действие конъюгата ADC49 антитело к HER2-лекарственное средство, конъюгата ADC53 антитело к LPS-лекарственное средство и трастузумаба-тезирина (сравнительный пример 1) на подкожно трансплантированные клетки KPL-4 линии клеток рака молочной железы человека.
[Фигура 7] На фигуре 7 представлено действие конъюгата ADC49 антитело к HER2-лекарственное средство и трастузумаба-тезирина (сравнительный пример 1) на подкожно трансплантированные клетки ЛМТ-1 линии клеток рака молочной железы человека.
[Фигура 8] На фигуре 8 представлено действие конъюгата ADC40 антитело к CLDN6-лекарственное средство и антитело (H1L1) к CLDN6-тезирин (сравнительный пример 1) на подкожно трансплантированные клетки OV-90 линии клеток рака яичников человека.
[Фигура 9] На фигуре 9 представлено действие конъюгата ADC40 антитело к CLDN6-лекарственное средство и антитело (H1L1) к CLDN6-тезирин (сравнительный пример 1) на подкожно трансплантированные клетки NIH:OVCAR-3 линии клеток рака яичников человека.
[Фигура 10] На фигуре 10 представлено действие конъюгата ADC50 антитело к TROP2-лекарственное средство и конъюгата ADC53 антитело к LPS-лекарственное средство на подкожно трансплантированные клетки FaDu линии клеток рака головы и шеи.
[Фигура 11] На фигуре 11 представлена полноразмерная аминокислотная последовательность CLDN6 человека (SEQ ID NO: 1) и нуклеотидная последовательность полноразмерной кДНК для CLDN6 человека (SEQ ID NO: 2).
[Фигура 12] На фигуре 12 представлена полноразмерная аминокислотная последовательность CLDN9 человека (SEQ ID NO: 3) и нуклеотидная последовательность полноразмерной кДНК для CLDN9 человека (SEQ ID NO: 4).
[Фигура 13] На фигуре 13 представлены аминокислотные последовательности CDRL1-3 легкой цепи антитела B1 (SEQ ID NO: 5-7).
[Фигура 14] На фигуре 14 представлена аминокислотная последовательность CDRL3 легкой цепи L4 гуманизированного антитела B1 (SEQ ID NO: 8).
[Фигура 15] На фигуре 15 представлены аминокислотные последовательности CDRH1-3 тяжелой цепи антитела B1 (SEQ ID NO: 9-11).
[Фигура 16] На фигуре 16 представлены аминокислотные последовательности CDRL1-3 легкой цепи антитела С7 (SEQ ID NO: 12-14).
[Фигура 17] На фигуре 17 представлены аминокислотные последовательности CDRH1-3 тяжелой цепи антитела С7 (SEQ ID NO: 15-17).
[Фигура 18] На фигуре 18 представлена нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела B1 (SEQ ID NO: 18), и аминокислотная последовательность вариабельной области легкой цепи антитела B1 (SEQ ID NO: 19). Каждое подчеркивание в аминокислотной последовательности обозначает последовательность CDR.
[Фигура 19] На фигуре 19 представлена нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела B1 (SEQ ID NO: 20), и аминокислотная последовательность вариабельной области тяжелой цепи антитела B1 (SEQ ID NO: 21). Каждое подчеркивание в аминокислотной последовательности обозначает последовательность CDR.
[Фигура 20] На фигуре 20 представлена нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела С7 (SEQ ID NO: 22), и аминокислотная последовательность вариабельной области легкой цепи антитела С7 (SEQ ID NO: 23). Каждое подчеркивание в аминокислотной последовательности обозначает последовательность CDR.
[Фигура 21] На фигуре 21 представлена нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела С7 (SEQ ID NO: 24), и аминокислотная последовательность вариабельной области тяжелой цепи антитела С7 (SEQ ID NO: 25). Каждое подчеркивание в аминокислотной последовательности обозначает последовательность CDR.
[Фигура 22] На фигуре 22 представлена аминокислотная последовательность легкой цепи chB1 (SEQ ID NO: 28) и фрагмент ДНК, включающий последовательность ДНК, кодирующую аминокислотную последовательность легкой цепи chB1 (SEQ ID NO: 29). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 23] На фигуре 23 представлена аминокислотная последовательность вариабельной области легкой цепи chB1 (SEQ ID NO: 30) и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи chB1 (SEQ ID NO: 31). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 24] На фигуре 24 представлена аминокислотная последовательность тяжелой цепи chB1 (SEQ ID NO: 32) и нуклеотидная последовательность, кодирующая тяжелую цепь chB1 (SEQ ID NO: 33). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 25] На фигуре 25 представлена аминокислотная последовательность вариабельной области тяжелой цепи chB1 (SEQ ID NO: 34) и нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи chB1 (SEQ ID NO: 35). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 26] На фигуре 26 представлена аминокислотная последовательность легкой цепи hL1 гуманизированного антитела (SEQ ID NO: 36) и нуклеотидная последовательность, кодирующая легкую цепь hL1 гуманизированного антитела (SEQ ID NO: 37). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 27] На фигуре 27 представлена аминокислотная последовательность вариабельной области легкой цепи hL1 гуманизированного антитела (SEQ ID NO: 38) и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL1 гуманизированного антитела (SEQ ID NO: 39). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 28] На фигуре 28 представлена аминокислотная последовательность легкой цепи hL2 гуманизированного антитела (SEQ ID NO: 40) и нуклеотидная последовательность, кодирующая легкую цепь hL2 гуманизированного антитела (SEQ ID NO: 41). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 29] На фигуре 29 представлена аминокислотная последовательность вариабельной области легкой цепи hL2 гуманизированного антитела (SEQ ID NO: 42) и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL2 гуманизированного антитела (SEQ ID NO: 43).
[Фигура 30] На фигуре 30 представлена аминокислотная последовательность легкой цепи hL3 гуманизированного антитела (SEQ ID NO: 44) и нуклеотидная последовательность, кодирующая легкую цепь hL3 гуманизированного антитела (SEQ ID NO: 45). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 31] На фигуре 31 представлена аминокислотная последовательность вариабельной области легкой цепи hL3 гуманизированного антитела (SEQ ID NO: 46) и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL3 гуманизированного антитела (SEQ ID NO: 47). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 32] На фигуре 32 представлена аминокислотная последовательность легкой цепи hL4 гуманизированного антитела (SEQ ID NO: 48) и нуклеотидная последовательность, кодирующая легкую цепь hL4 гуманизированного антитела (SEQ ID NO: 49). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 33] На фигуре 33 представлена аминокислотная последовательность вариабельной области легкой цепи hL4 гуманизированного антитела (SEQ ID NO: 50) и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL4 гуманизированного антитела (SEQ ID NO: 51). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 34] На фигуре 34 представлена аминокислотная последовательность тяжелая цепь hH1 гуманизированного антитела (SEQ ID NO: 52) и нуклеотидная последовательность, кодирующая тяжелую цепь hH1 гуманизированного антитела (SEQ ID NO: 53). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 35] На фигуре 35 представлена аминокислотная последовательность вариабельной области тяжелой цепи hH1 гуманизированного антитела (SEQ ID NO: 54) и нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи гуманизированного антитела hH1 (SEQ ID NO: 55). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 36] На фигуре 36 представлена аминокислотная последовательность тяжелой цепи hH2 гуманизированного антитела (SEQ ID NO: 56) и нуклеотидная последовательность, кодирующая тяжелую цепь hH2 гуманизированного антитела (SEQ ID NO: 57). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 37] На фигуре 37 представлена аминокислотная последовательность вариабельной области тяжелой цепи hH2 гуманизированного антитела (SEQ ID NO: 58) и нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи hH2 гуманизированного антитела (SEQ ID NO: 59).
[Фигура 38] На фигуре 38 представлена аминокислотная последовательность тяжелой цепи hH3 гуманизированного антитела (SEQ ID NO: 60) и нуклеотидная последовательность, кодирующая тяжелую цепь hH3 гуманизированного антитела (SEQ ID NO: 61). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 39] На фигуре 39 представлена аминокислотная последовательность вариабельной области тяжелой цепи hH3 гуманизированного антитела (SEQ ID NO: 62) и нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи hH3 гуманизированного антитела (SEQ ID NO: 63). Каждое подчеркивание в аминокислотной последовательности означает последовательность CDR.
[Фигура 40] На фигуре 40 представлены связывающие способности антитела В1 и антитела С7 с CLDN6 человека и молекулами семейства CLDN3, CLDN4 и CLDN9, определенные методом проточной цитометрии.
[Фигура 41] На фигуре 41 представлены интернализирующие активности антител для антитела В1 и антитела С7, измеренные посредством Mab-ZAP.
[Фигура 42] На фигуре 42 представлены связывающие способности гуманизированных антител к CLDN6 H1L1, H2L2, H1L3, H2L4 и H3L3 в отношении CLDN6 и молекул указанных семейств, определенные методом проточной цитометрии.
[Фигура 43] На фигуре 43 представлена аминокислотная последовательность легкой цепи трастузумаба (SEQ ID NO: 64) и аминокислотная последовательность тяжелой цепи трастузумаба (SEQ ID NO: 65).
[Фигура 44] На фигуре 44 представлена аминокислотная последовательность легкой цепи варианта трастузумаба (SEQ ID NO: 73) и аминокислотная последовательность тяжелой цепи варианта трастузумаба (SEQ ID NO: 75).
[Фигура 45] На фигуре 45 представлено сравнение аминокислотных последовательностей chB1H, которая представляет собой тяжелую цепь химеризованного человеческого антитела к CLDN6 chB1, и тяжелых цепей hH1, hH2 и hH3 гуманизированных антител. Символ «.» обозначает аминокислотный остаток, идентичный соответствующему аминокислотному остатку chB1_Н, и каждое положение с символом аминокислотного остатка обозначает замещенный аминокислотный остаток.
[Фигура 46] На фигуре 46 представлено сравнение аминокислотных последовательностей chB1_L, которая представляет собой легкую цепь химеризованного человеческого антитела к CLDN6 chB1, и легких цепей hL1, hL2, hL3 и hL4 гуманизированных антител. Символ «.» обозначает аминокислотный остаток, идентичный соответствующему аминокислотному остатку chB1_L, и каждое положение с символом аминокислотного остатка обозначает замещенный аминокислотный остаток.
[Фигура 47] На фигуре 47 представлено действие конъюгатов ADC49 и ADC55 антитело к HER2-лекарственное средство на подкожно трансплантированные клетки KPL-4 линии клеток рака молочной железы человека.
[Фигура 48] На фигуре 48 представлено действие конъюгата ADC55 антитело к HER2-лекарственное средство на подкожно трансплантированные клетки JIMT-1 линии клеток рака молочной железы человека.
[Фигура 49] На фигуре 49 представлено действие конъюгатов ADC49 и ADC55 антитело к HER2-лекарственное средство и конъюгата ADC53 антитело к LPS-лекарственное средство на подкожно трансплантированные клетки CFPAC-1 линии клеток рака поджелудочной железы человека.
Описание вариантов реализации
[0010]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению представляет собой противоопухолевое лекарственное средство, содержащее противоопухолевое соединение, конъюгированное через фрагмент линкерной структуры с антителом, способным распознавать или связываться с опухолевыми клетками.
[0011]
В настоящем изобретении примеры «атома галогена» могут включать, но не ограничиваются ими, атом фтора, атом хлора, атом брома и атом иода.
[0012]
В настоящем изобретении «С1-С6-алкильная группа» относится к линейной или разветвленной алкильной группе, содержащей от одного до шести атомов углерода. Примеры «С1-С6-алкильной группы» могут включать, но не ограничиваются ими, метильную группу, этильную группу, н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, втор-бутильную группу, т-бутил, н-пентильную группу и н-гексил.
[0013]
В настоящем изобретении термин «С1-С6 алкоксигруппа» относится к алкоксигруппе, содержащей линейную или разветвленную алкильную группу, содержащую от одного до шеста атомов углерода. Примеры «С1-С6 алкоксигруппы» могут включать, но не ограничиваются ими, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, н-бутоксигруппу, изобутокси, втор-бутоксигруппу, н-пентилоксигруппу и н-гексилокси.
[0014]
В настоящем изобретении «С1-С6 алкилтиогруппа» относится к алкилтиогруппе, содержащей линейную или разветвленную алкильную группу, содержащую от одного до шеста атомов углерода. Примеры «С1-С6 алкилтиогруппы» могут включать, но не ограничиваются ими, метилтиогруппу, этилтиогруппу, н-пропилтиогруппу, изопропилтиогруппу, н-бутилтиогруппу, изобутилтиогруппу, втор-бутилтиогруппу, т-бутилтиогруппу, н-пентилтиогруппу и н-гексилтиогруппу.
[0015]
В настоящем изобретении термин «трех-пяти-членное насыщенное углеводородное кольцо» относится к насыщенной циклической углеводородной группе, содержащей от трех до пяти атомов углерода. Примеры «трех-пяти-членного насыщенного углеводородного кольца» могут включать, но не ограничиваются ими, циклопропильную группу, циклобутильную группу и циклопентильную группу.
[0016]
В настоящем изобретении термин «С3-С5 циклоалкоксигруппа» относится к циклоалкоксигруппе, содержащей насыщенную циклическую углеводородную группу, содержащую от трех до пяти атомов углерода. Примеры «С3-С5 циклоалкоксигруппы» могут включать, но не ограничиваются ими, циклопропоксигруппу, циклобутокси группу и циклопентилоксигруппу.
[0017]
В настоящем изобретении, примеры «трех-пятичленного насыщенного гетероцикла» могут включать, но не ограничиваются ими, 1,3-пропиленоксид, азациклобутан, триметиленсульфид, тетрагидрофуран и пирролидин.
[0018]
В настоящем изобретении, примеры «арильной группы» могут включать, но не ограничиваются ими, фенильную группу, бензильную группу, инденильную группу, нафтильную группу, флуоренильную группу, антранильную группу и фенантренильную группу.
[0019]
В настоящем изобретении примеры «гетероарильной группы» могут включать, но не ограничиваются ими, тиенильную группу, пирролильную группу, пиразолильную группу, триазолильную группу, оксазолильную группу, оксадиазолильную группу, тиазолильную группу, пиридильную группу, пиримидильную группу, пиридазильную группу, пиразинильную группу, хинолильную группу, хиноксалильную группу, бензотиофенильную группу, бензимидазолильную группу, бензотриазолильную группу и бензофуранильную группу.
[0020]
В настоящем изобретении, примеры «шестичленного гетероцикла» могут включать, но не ограничиваются ими, пиридиновое кольцо, пиримидиновое кольцо и пиридазиновое кольцо.
[0021]
В настоящем изобретении термин «спиросвязанный» относится к случаю, когда, как представлено в примерах, А и пирролидиновое кольцо, с которыми связано А, или Е и пирролидиновое кольцо, с которыми связано Е, образуют спирокольцо.
[0022]
[Конъюгат антитело-лекарственное средство]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению представлен следующей формулой:
[Формула 50]

m1 представляет собой количество конъюшированных молекул лекарственного средства на молекулу антитела в конъюгате антитело-лекарственное средство, Ab представляет собой антитело или функциональный фрагмент указанного антитела, L представляет собой линкер, связывающий Ab и D, и D представляет собой лекарственное средство.
<Лекарственное средство>
В данном разделе будет описано лекарственное средство D, конъюгированное в конъюгате антитело-лекарственное средство согласно настоящему изобретению. Лекарственное средство D согласно настоящему изобретению предпочтительно представляет собой противоопухолевое соединение. Указанное противоопухолевое соединение развивает противоопухолевый эффект, когда часть линкера или весь линкер расщепляется в опухолевой клетке и фрагмент противоопухолевого соединения высвобождается. Когда линкер и лекарственное средство отщепляются друг от друга по связующей части, противоопухолевое соединение высвобождается в исходной структуре, и осуществляется исходное противоопухолевое действие указанного соединения.
Противоопухолевое соединение в конъюгате антитело-лекарственное средство согласно настоящему изобретению представляет собой производное пирролобензодиазепина (производное PBD), представленное общей формулой (V):
[0023]
[Формула 51]
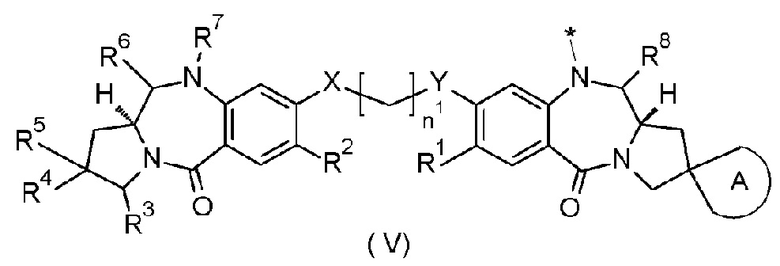
Далее приводится описание указанного соединения.
Звездочка представляет собой связь с линкером L.
[0024]
n1 представляет собой целое число от 2 до 8 и предпочтительно представляет собой целое число от 2 до 6 и более предпочтительно целое число от 3 до 5.
Алкильная цепь с индексом n1, представляющим собой целое число от 2 до 8, предпочтительно целое число от 2 до 6 и более предпочтительно целое число от 3 до 5, может включать двойную связь.
[0025]
А представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл, и предпочтительно представляет собой трех-пятичленное насыщенное углеводородное кольцо (циклопропан, циклобутан или циклопентан), более предпочтительно циклопропан или циклобутан и наиболее предпочтительно циклопропан.
Спиросвязанное трех-пятичленное насыщенное углеводородное кольцо может быть замещено одним-четырьмя атомами галогена и может быть предпочтительно замещено одним или двумя атомами фтора (например, представляет собой 2,2-дифторциклопропан).
[0026]
R1 и R2 каждый независимо представляют собой С1-С6 алкоксигруппу, С1-С6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтиогруппу, атом галогена или -NR'R'' и каждый предпочтительно представляет собой С1-С6 алкоксигруппу, С1-С6-алкильную группу или гидроксигруппу, более предпочтительно С1-С3 алкоксигруппу и наиболее предпочтительно метоксигруппу.
[0027]
R3, R4 и R5 являются такими, как описано в следующих пунктах (i)-(iii).
(i) Если R3 и R4 объединены вместе с атомами углерода, с которыми R3 и R4 связаны, с образованием двойной связи, как показано в следующей формуле:
[Формула 52]
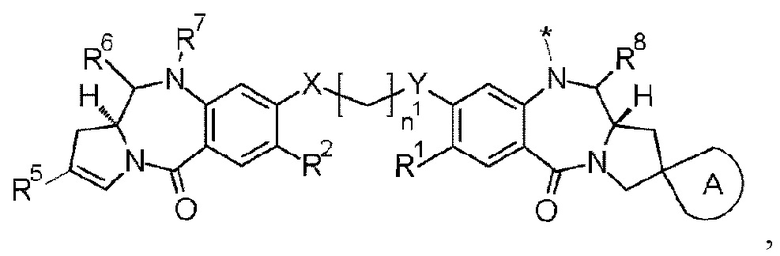
R5 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 1, или С1-С6-алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 2, и предпочтительно представляет собой арильную группу, необязательно имеющую один или более заместителей, выбранных из группы 1.
[0028]
«Арильная группа» в «арильной группе или гетероарильной группе, необязательно имеющей один или более заместителей, выбранных из группы 1» для R5 предпочтительно представляет собой фенильную группу или нафтильную группу и более предпочтительно фенильную группу.
[0029]
«Гетероарильная группа» в «арильной группе или гетероарильной группе, необязательно имеющей один или более заместителей, выбранных из группы 1» для R5 предпочтительно представляет собой тиенильную группу, пиридильную группу, пиримидильную группу, хинолильную группу, хиноксалильную группу или бензотиофенильную группу, более предпочтительно 2-тиенильную группу, 3-тиенильную группу, 2-пиридильную группу, 3-пиридильную группу или 4-пиридильную группу и наиболее предпочтительно 3-пиридильную группу или 3-тиенильную группу.
[0030]
Примеры заместителей арильной группы или гетероарильной группы для R5 могут включать, но не ограничиваются ими, следующие a)-j):
a) С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С6-алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR' и
j) гидроксигруппу,
Здесь R', R'' и R''' в b) и f)-i) каждый независимо представляют собой атом водорода или С1-С6-алкильную группу и предпочтительно каждый представляет собой атом водорода или С1-С3 алкильную группу.
[0031]
a)-j) предпочтительно являются следующими:
a) С1-С3 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена, более предпочтительно метоксигруппу, этоксигруппу, н-пропокси группу, изопропоксигруппу или трифторметокси, наиболее предпочтительно метоксигруппу, этоксигруппу или трифторметоксигруппу и наиболее предпочтительно метоксигруппу;
b) С1-С3 алкильную группу, необязательно замещенную одним-тремя атомами галогена, гидроксигруппу, -OCOR', -C(=NR')-NR''R''' или -NHC(=NR')-NR''R'', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно С1-С3 алкильную группу, необязательно замещенная любым выбранным из одного-трех атомов галогена, гидроксигруппу, -OCOR, -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или метильную группу, наиболее предпочтительно метильную группу, этильную группу, н-пропильную группу, изопропильную группу, фторметильную группу, дифторметильную группу, трифторметильную группу, гидроксиметильную группу, -СН2ОСОМе, -СН2-NHC(=NH)-NH2 или -CH2-NHC(=NMe)-NH2;
c) атом галогена, предпочтительно атом фтора или атом хлора;
d) С3-С5-циклоалкоксигруппу, более предпочтительно циклопропоксигруппу;
e) С1-С3 алкилтиогруппу, более предпочтительно метилтиогруппу или этилтиогруппу;
f) -NR'R'', где R' и R'' каждый независимо представляют собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NH2, -NHMe, -NMe2, -NHEt или -NEt2;
g) -C(=NR')-NR''R'', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -C(=NH)-NH2 или -C(=NMe)-NH2;
h) -NHC(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NHC(=NH)-NH2 или -NHC(=NMe)-NH2;
i) -NHCOR', где R' представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NHCOMe или -NHCOEt; и
j) гидроксигруппу.
[0032]
Арильная группа (предпочтительно, фенильная группа) или гетероарильная группа (предпочтительно, пиридильная группа) для R5 может иметь по меньшей мере один заместитель в любом положении. Если присутствует много заместителей, заместители могут быть одинаковыми или различными.
[0033]
Если R5 представляет собой арильную группу, каждый заместитель предпочтительно представляет собой a), b), d), g), h) или j) и более предпочтительно а), b), d) или j).
[0034]
Если R5 представляет собой фенильную группу, R5 может иметь заместитель в любом положении и может иметь множество заместителей и предпочтительно один или два заместителя присутствуют в положении 3 и/или положении 4 и более предпочтительно один заместитель присутствует в положении 4.
Если R5 представляет собой нафтильную группу, R5 может иметь заместитель в любом положении и может иметь множество заместителей и предпочтительно один заместитель присутствует в положении 6.
[0035]
Если R5 представляет собой фенильную группу, R5 более предпочтительно представляет собой фенильную группу, 4-метоксифенильную группу, 3-метоксифенильную группу, 4-этоксифенильную группу, 4-(н-пропокси)-фенильную группу, 4-(изопропокси)-фенильную группу, 4-циклопропокси-фенильную группу, 4-трифторметилфенильную группу, 4-гидроксиметил-фенильную группу, 4-ацетоксиметил-фенильную группу или 4-карбамимидамидо метил-фенильную группу и наиболее предпочтительно фенильную группу, 4-метоксифенильную группу, 3-метоксифенильную группу, 4-циклопропокси-фенильную группу, 4-гидроксиметил-фенильную группу, 4-ацетоксиметил-фенильную группу, 4-карбамимидамидометил-фенильную группу или 4-трифторметилфенильную группу.
Если R5 представляет собой нафтильную группу, R5 более предпочтительно представляет собой нафтильную группу или 6-метокси-2-нафтильную группу.
Наиболее предпочтительна 4-метоксифенильная группа.
[0036]
Если R5 представляет собой гетероарильную группу, каждый заместитель предпочтительно представляет собой a), b), d), g), h) или j) и более предпочтительно а) или b).
[0037]
Если R5 представляет собой гетероарильную группу, R5 может иметь по меньшей мере один заместитель в любом положении. Если R5 представляет собой 3-пиридильную группу, его заместитель(-и) предпочтительно присутствуют в положении 6 и/или положении 5. Если R5 представляет собой 2-пиридил, его заместитель(-и) предпочтительно присутствуют в положении 5 и/или положении 4 или в положении 5 и/или в положении 6. Если R5 представляет собой 4-пиридил, его заместитель(-и) предпочтительно присутствует в положении 2 и/или в положении 6.
[0038]
Если R5 представляет собой гетероарильную группу, R5 может иметь множество заместителей и предпочтительно имеет один или два заместителя и предпочтительно имеет один заместитель.
[0039]
Если R5 представляет собой пиридильную группу, R5 предпочтительно представляет собой 6-метокси-3-пиридильную группу или 6-метил-3-пиридильную группу.
Если R5 представляет собой 3-тиенильную группу или 6-хиноксалильную группу, R5 предпочтительно является незамещенным.
[0040]
«С1-С6-алкильная группа» в «С1-С6-алкильной группе, необязательно имеющей один или более заместителей, выбранных из группы 2» для R5 предпочтительно представляет собой С1-С3 алкильную группу и более предпочтительно метильную группу или этильную группу.
[0041]
Каждый из заместителей в «С1-С6-алкильной группе, необязательно имеющей один или более заместителей, выбранных из группы 2» для R5 представляет собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу (предпочтительно, С1-С3 алкоксигруппу), предпочтительно гидроксигруппу, метоксигруппу или этоксигруппу и более предпочтительно гидроксигруппу.
[0042]
(ii) Если R3 представляет собой атом водорода, R4 и R5 объединены вместе с атомом углерода, с которым R4 и R5 связаны, с образованием трех-пятичленного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, или СН2=, как показано в следующей формуле:
[Формула 53]
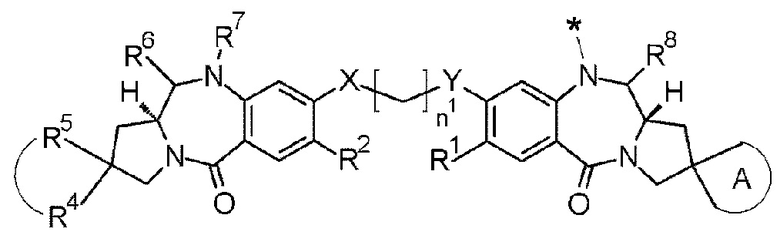
или
[Формула 54]
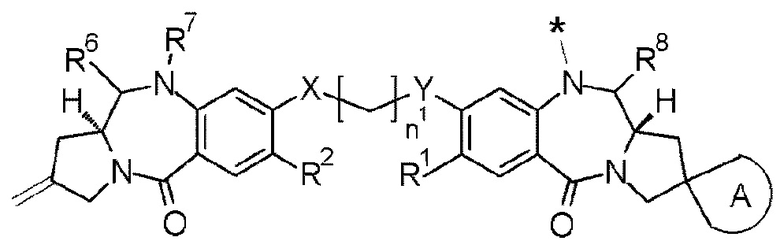
Трех-пяти-членное насыщенное углеводородное кольцо может быть замещено одним-четырьмя атомами галогена и может быть предпочтительно замещено одним или двумя атомами фтора.
R4 и R5 предпочитительно объединены с образованием трех-пятичленного насыщенного углеводородного кольца или CH2=, более предпочтительно с образованием циклопропана, циклобутана или CH2= (эксометиленовая группа) и наиболее предпочтительно с образованием циклопропана.
Если R4 и R5 объединены с образованием трех-пятичленного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл предпочтительно такие же, как А. Более предпочтительно, А представляет собой трех-пятичленное насыщенное углеводородное кольцо, и R4 и R5 объединены с образованием трех-пяти-членного насыщенного углеводородного кольца и наиболее предпочтительно А представляет собой циклопропановое кольцо, и R4 и R5 объединены с образованием циклопропанового кольца.
[0043]
(iii) R3, R4 и R5 объединены вместе с атомом углерода, с которым связан R3, и атомом углерода, с которым связаны R4 и R5, с образованием бензольного кольца или шестичленного гетероцикла, необязательно имеющего один или более заместителей, выбранных из группы 3.
Следующая формула показывает случай, в котором R3 и R4 объединены с образованием бензольного кольца, необязательно имеющего один или более заместителей:
[Формула 55]
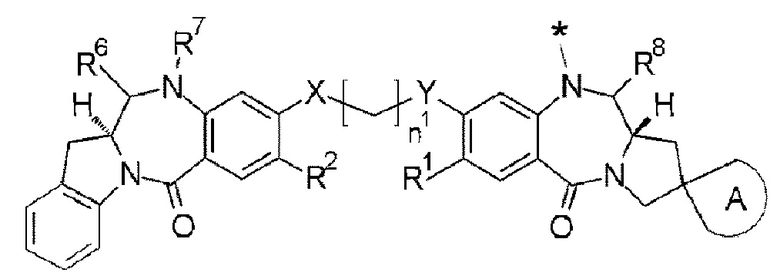
Бензольное кольцо или гетероцикл могут иметь по меньшей мере один заместитель в любом положении. Если присутствует много заместителей, заместители могут быть одинаковыми или различными.
[0044]
Каждый заместитель бензольного кольца или гетероцикла представляет собой атом галогена, С1-С6-алкильную группу, необязательно замещенную одним-тремя атомами галогена, или С1-С6 алкоксигруппу, предпочтительно атом галогена, С1-С3 алкильную группу, необязательно замещенную одним-тремя атомами галогена, или С1-С3 алкокси и более предпочтительно атом галогена, метильную группу или метоксигруппу.
[0045]
«Бензольное кольцо или шестичленный гетероцикл, необязательно имеющий один или более заместителей» предпочтительно представляет собой незамещенное бензольное кольцо.
[0046]
R3, R4 и R5 наиболее предпочтительно удовлетворяет указанному выше (i).
[0047]
R6 и R7 каждый представляют собой атом водорода, или R6 и R7 объединены и представляют собой иминную связь (C=N).
[0048]
R8 представляет собой гидроксигруппу или С1-С3 алкоксигруппу, предпочтительно гидроксигруппу или метоксигруппу и более предпочтительно гидроксигруппу. R8 может быть гидрогенсульфитным аддуктом (OSO3M, где М является катионом металла).
Поскольку R8 связывается с асимметричным атомом углерода, обеспечивается стерическая конфигурация, представленная частичной структурой (Va) или (Vb) ниже. Каждая волнистая линия представляет собой связь с Y в общей формуле (V), и каждая звездочка представляет собой связь с L.
[Формула 56]
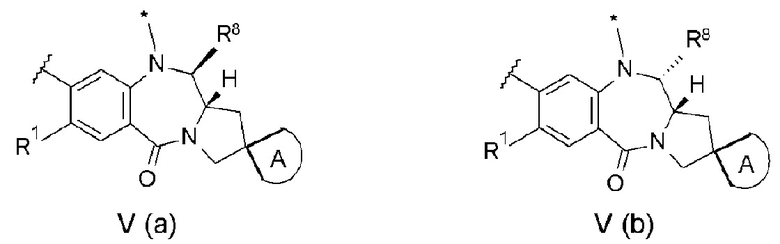
[0049]
X и Y каждый независимо представляют собой атом кислорода, атом азота или атом серы и предпочтительно атом кислорода.
[0050]
Лекарственное средство D согласно настоящему изобретению предпочтительно представляет собой любой соединение, выбранное из следующей группы:
[Формула 57]
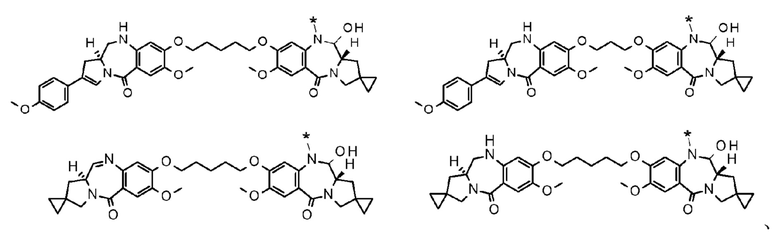
[Формула 58]
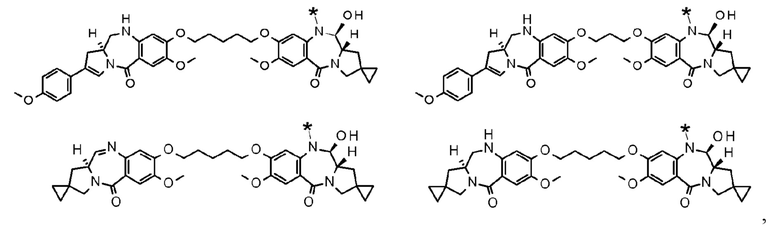
[Формула 59]
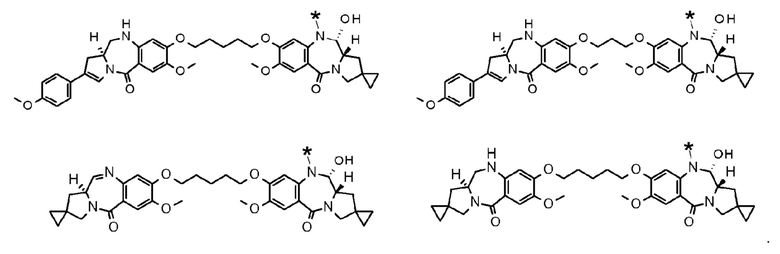
[0051]
<Линкерная структура>
В данном разделе будет описана линкерная структура для связывания противоопухолевого лекарственного средства с антителом в конъюгате антитело-лекарственное средство согласно настоящему изобретению.
Линкер L представлен следующей формулой:
-Lb-La-Lp-NH-B-CH2-O(C=O)-*
Звездочка обозначает связь с атомом азота в N10'-положении лекарственного средства D, Lb обозначает спейсер, который соединяет La с гликаном или ремоделированным гликаном Ab, или спейсер, который соединяет La с боковой цепью аминокислотного остатка (например, цистеина или лизина) антитела Ab.
[0052]
В представляет собой фенильную группу или гетероарильную группу и предпочтительно представляет собой 1,4-фенильную группу, 2,5-пиридильную группу, 3,6-пиридильную группу, 2,5-пиримидильную группу или 2,5-тиенильную группу и более предпочтительно 1,4-фенильную группу.
[0053]
Lp представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой in vivo или в клетке-мишени. Lp, например, расщепляется под действием фермента, такого как эстераза и пептидаза.
Lp представляет собой пептидный остаток, состоящий из двух-семи (предпочтительно, двух-четырех) аминокислот. Таким образом, Lp состоит из олигопептидного остатка, в котором две-семь аминокислот связаны через пептидную связь.
Lp связан на N-конце с карбонильной группой La в Lb-La- и образует на С-конце амидную связь с аминогруппой (-NH-) части -NH-B-CH2-O(C=O)- линкера. Связь между С-концом Lp и -NH- расщепляется ферментом, таким как эстераза.
[0054]
Аминокислоты, составляющие Lp, не ограничиваются конкретными аминокислотами и, например, представляют собой L- или D-аминокислоты и предпочтительно L-аминокислоты. Аминокислоты могут быть не только α-аминокислотами, но могут включать аминокислоту со структурой, например, β-аланина, ε-аминокапроновой кислоты или γ-аминомасляной кислоты, и могут дополнительно включать неприродную аминокислоту, такую как N-метилированная аминокислота.
[0055]
Аминокислотная последовательность Lp не ограничена конкретной аминокислотной последовательностью, и примеры аминокислот, которые составляют Lp, могут включать, но не ограничиваются ими, глицин (Gly; G), валин (Val; V), аланин (Ala); А), фенилаланин (Phe; F), глутаминовую кислоту (Glu; Е), изолейцин (Не; I), пролин (Pro; Р), цитруллин (Cit), лейцин (Leu; L), серии (Ser; S), лизин (Lys; K) и аспарагиновую кислоту (Asp; D). Предпочтительными среди них являются глицин (Gly; G), валин (Val; V), аланин (Ala; А) и цитруллин (Cit).
Любая из этих аминокислот может встречаться несколько раз, и Lp имеет аминокислотную последовательность, включающую произвольно выбранные аминокислоты. Схема высвобождения лекарственного средства может контролироваться по типу аминокислот.
[0056]
Конкретные примеры линкера Lp могут включать, но не ограничиваются ими, -GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI-, -GGPL-, -EGGVA, -PI-, -GGF-, DGGF-, (D-)D-GGF-, -EGGF-, -SGGF-, -KGGF-, -DGGFG-, -GGFGG-, -DDGGFG-, -KDGGFG- и -GGFGGGF-.
Здесь "(D-)V" обозначает D-валин, "(D)-P" обозначает D-пролин и "(D-)D" обозначает D-аспарагиновую кислоту.
[0057]
Линкер Lp предпочтительно представляет собой любой из следующих:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI- и -GGPL-.
[0058]
Линкер Lp более предпочтительно представляет собой любой из следующих:
-GGVA-, -GGVCit- и -VA-.
[0059]
Lb представляет собой: i) спейсер, который соединяет La с гликаном или ремоделированным гликаном Ab; или ii) спейсер, который соединяет La с боковой цепью аминокислотного остатка (например, цистеина или лизина) антитела Ab.
Если Lb представляет собой i), Lb выбран из следующей группы:
-C(=O)-(CH2CH2)n2-C(=O)-, -C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2)n3-C(=O)-, -C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2O)n3-CH2-C(=O)-, -C(=O)-(CH2CH2)n2-NH-C(=O)-(CH2CH2O)n3-CH2CH2-C(=O)-, -(CH2)n4-O-C(=O)-
где
n2 представляет собой целое число от 1 до 3 (предпочтительно, 1 или 2), n3 представляет собой целое число от 1 до 5 (предпочтительно, целое число от 2 до 4, более предпочтительно, 2 или 4) и n4 представляет собой целое число от 0 до 2 (предпочтительно, 0 или 1).
[0060]
Если Lb представляет собой i), La предпочтительно выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-,-С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-,
-СН2-ОС(=O)- и -ОС(=O)- и
La более предпочтительно представляет собой -С(=O)-СН2СН2-С(=O)- или -С(=O) -(СН2СН2)2-С(=O)-.
[0061]
Спейсер Lb не ограничен конкретным спейсером, и его примеры могут включать, но не ограничиваются этим, спейсер, представленный следующими формулами.
[Формула 60]
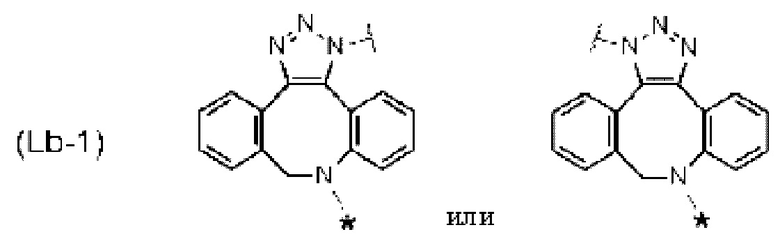
[Формула 61]
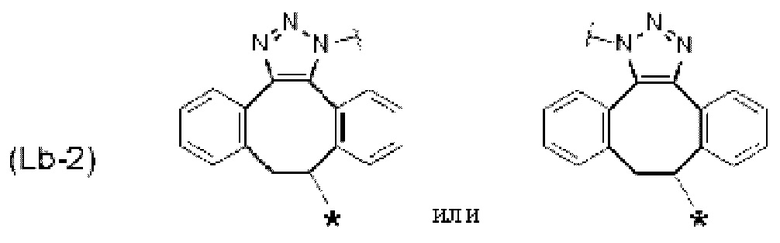
[Формула 62]
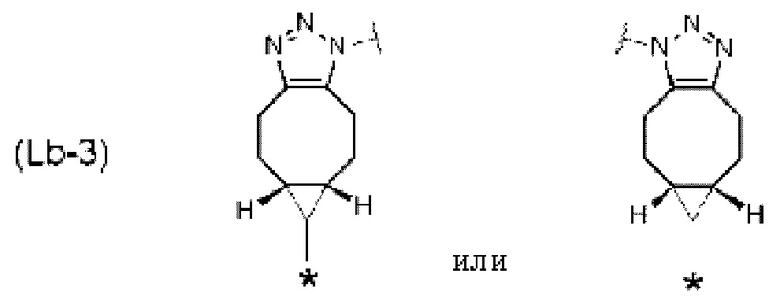
Б структурных формулах для Lb, представленных выше, каждая звездочка представляет собой связь с -(С=O) или -(СН2)n4 на левом конце La, и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
В каждой структурной формуле для Lb (Lb-1, Lb-2 или Lb-3), представленной выше, центр триазольного кольца, образованный клик-реакцией азидной группы и DBCO обеспечивает структуры геометрических изомеров, и молекулы Lb существуют в виде любых одной из двух структур или как смесь их обоих. На молекулу конъюгата антитело-лекарственное средство согласно настоящему изобретению существуют фрагменты m1 "-LD", и существует либо одна из двух структур, либо обе они сосуществуют в виде Lb (Lb-1, Lb-2 или Lb-3) в L каждого из фрагментов m1 "-LD".
[0062]
Если Lb представляет собой i), L предпочтительно представлен -Lb-La-Lp-NH-B-CH2-O(C=O)-*, где
В представляет собой 1,4-фенильную группу,
Lp выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI- и -GGPL-,
La выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -СН2-ОС(=O)-, ОС(=O)-
и
Lb представляет собой любую из структурных формул, приведенных выше Lb.
[0063]
Если Lb представляет собой i), L более предпочтительно представляет собой любое, выбранное из следующей группы:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GG-(D-)VA-NH-B-CH2-OC(=O)-I
-Z1-С(=O)-CH2CH2-С(=O)-VA-NH-В-CH2-ОС(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGPI-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-В-CH2-ОС(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z2-OC(=O)-GGVA-NH-B-CH2-OC(=O)-, -Z3-CH2-OC(=O)-GGVA-NH-B-CH2-OC(=O)-
где
Z1 представляет собой следующую структурную формулу, как описано для Lb:
[Формула 63]
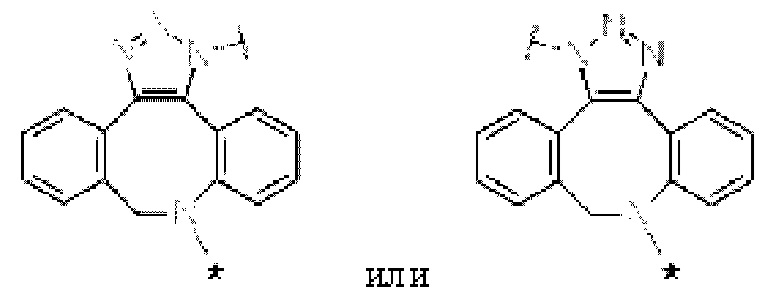
Z2 представляет собой следующую структурную формулу, как описано для Lb:
[Формула 64]
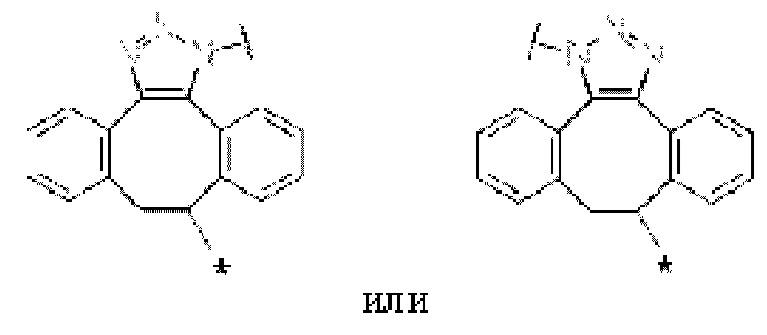
Z3 представляет собой следующую структурную формулу, как описано для Lb:
[Формула 65]
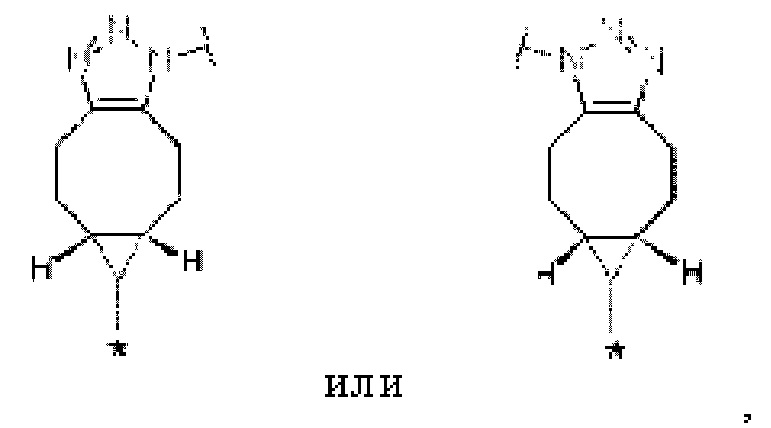
и В представляет собой 1,4-фенильную группу.
[0064]
L наиболее предпочтительно представляет собой любое из следующего:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-В-CH2-ОС(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)- и
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-, где
В представляет собой 1,4-фенильную группу, и Z1 представляет собой следующую структурную формулу, как описано для Lb:
[Формула 66]
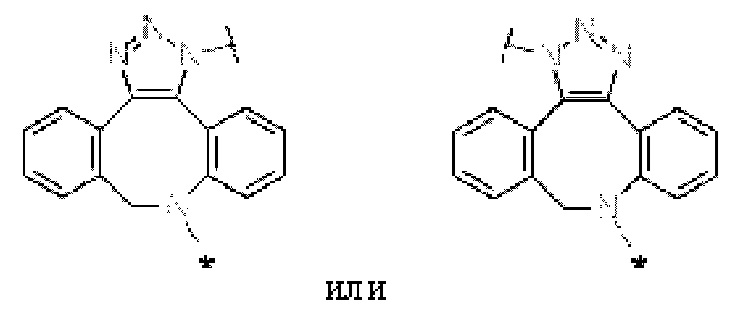
[0065]
Если Lb представляет собой ii) и аминокислотный остаток представляет собой истеиновый остаток, спейсер Lb не ограничен конкретным спейсером, и его примеры могут включать, но не ограничиваются, -(сукцинимид-3-ил-N)-. «-(сукцинимид-3-ил-N)-» имеет структуру, представленную следующей структурой:
[0066]
[Формула 67]
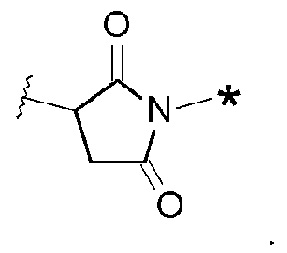
В приведенной выше структурной формуле звездочка обозначает связь с La. Волнистая линия обозначает связь с тиольной группой цистеинового остатка антитела через тиоловую связь, и указанная связь может представлять собой сайт-специфическое конъюгирование цистеина (RSC Adv., 2017, 7, 24828-24832 и т.д.).
[0067]
Если Lb представляет собой ii), L представлен формулой -Lb-La-Lp-NH-B-СН2-O(С=O)-*, где
В представляет собой 1,4-фенильную группу;
Lp представляет собой один из -GGVA-, -GG-(D-)VA-, -VA- и -GGFG-;
La представляет собой -(СН2)n9-С(=O)- или -(CH2CH2)n10-C(=O)-NH-(CH2CH2O)n11-СН2СН2-С(=O)-, где
n9 представляет собой целое число от 2 до 7 (предпочтительно, целое число от 2 до 5, более предпочтительно 2 или 5), n10 представляет собой целое число от 1 до 3 (предпочтительно, 1) и n11 представляет собой целое число от 6 до 10 (предпочтительно, 8); и
Lb представляет собой -(сукцинимид-3-ил-N)-.
[0068]
Если Lb представляет собой ii), L предпочтительно представляет собой любое из следующих:
-(Сукцинимид-3-ил-N)-(СН2)5-С(=O)-VA-NB-В-СН2-ОС(=O)-,
-(Сукцинимид-3-ил-N)-(СН2)5-С(=O)-GGVA-НН-В-СН2-ОС(=O)-, или,
-(Сукцинимид-3-ил-N)-СН2СН2-С(=O)-NH-(CH2CH2O)8-СН2СН2-С(=O)-VA-NH-В-СН2-ОС(=O)-
где В представляет собой 1,4-фенильную группу.
[0069]
Предполагается, что конъюгат антитело-лекарственное средство согласно настоящему изобретению проявляет противоопухолевую активность посредством процесса, в котором большинство молекул конъюгата антитело-лекарственное средство мигрируют в опухолевые клетки, и линкерная часть (например, Lp) затем расщепляется ферментом или ему подобным, чтобы активировать конъюгат антитело-лекарственное средство, который высвобождает порцию лекарственного средства D (далее обозначаемую как свободное лекарственное средство (описано ниже)).
Следовательно, предпочтительно, чтобы конъюгат антитело-лекарственное средство согласно настоящему изобретению был стабильным вне опухолевых клеток.
<Свободное лекарственное средство и промежуточное соединение>
Промежуточное соединение и свободное лекарственное средство конъюгата антитело-лекарственное средство согласно настоящему изобретению представлено следующей формулой:
[0070]
[Формула 68]
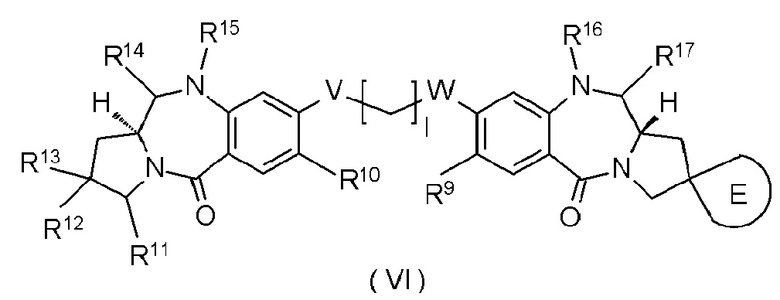
Указанное соединение будет описано далее.
[0071]
Свободное лекарственное средство согласно настоящему изобретению получают с помощью способа, согласно которому обеспечивают миграцию конъюгата антитело-лекарственное средство в опухолевые клетки, и затем часть линкера L в конъюгате антитело-лекарственное средство расщепляется. Примеры свободного лекарственного средства могут включать, но не ограничиваются ими, лекарственные средства 1-16 в примерах 45-54 и 150-152.
Конъюгат антитело-лекарственное средство согласно настоящему изобретению получают с применением промежуточного соединения.
[0072]
Свободное лекарственное средство для конъюгата антитело-лекарственное средство согласно настоящему изобретению соответствует случаю, когда (a) R16 и R17 объединены с образованием иминной связи (N=C).
Промежуточное соединение для получения конъюгата антитело-лекарственное средство согласно настоящему изобретению соответствует случаю, когда (b) R16 представлен формулой J-La'-Lp'-NH-B'-CH2-O (С=O)-*.
Соответственно, 1 и n1, Е и A, R9 и R1, R10 и R2, R11 и R3, R12 и R4, R13 и R5, R14 и R6, R15 и R7, V и X, W и Y, группа 7 и группа 1, группа 8 и группа 2, группа 9 и группа 3, группа 10 и группа 4, группа 11 и группа 5 и группа 12 и группа 6 в формулах являются синонимичными друг другу.
[0073]
1 представляет собой целое число от 2 до 8 и предпочтительно представляет собой целое число от 2 до 6 и более предпочтительно целое число от 3 до 5.
Алкильная цепь, для которой 1 представляет собой целое число от 2 до 8, предпочтительно целое число от 2 до 6 и более предпочтительно целое число от 3 до 5, может содержать двойную связь.
[0074]
Е представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл и предпочтительно представляет собой трех-пятичленное насыщенное углеводородное кольцо (циклопропан, циклобутан или циклопентан), более предпочтительно циклопропан или циклобутан и наиболее предпочтительно циклопропан.
Спиросвязанное трех-пятичленное насыщенное углеводородное кольцо может быть замещено одним-четырьмя атомами галогена и может быть предпочтительно замещено одним или двумя атомами фтора (например, 2,2-дифторциклопропан).
[0075]
R9 и R10 каждый независимо представляют собой С1-С6 алкоксигруппу, С1-С6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтио группу, атом галогена или -NR'R'' и каждый предпочтительно представляет собой С1-С6 алкоксигруппу, С1-С6-алкильную группу или гидроксигруппу, более предпочтительно С1-С3 алкоксигруппу и наиболее предпочтительно метоксигруппу.
[0076]
R11, R12 и R13 такие, как описано в любом из следующих (i)-(iii).
(i) Если R11 и R12 объединены вместе с атомами углерода, с которыми R3 и R4 связаны с образованием двойной связи, R13 представляет собой арильную группу или гетероарильную группу, необязательно имеющую один или более заместителей, выбранных из группы 7, или С1-С6-алкильную группу, необязательно имеющую один или более заместителей, выбранных из группы 8 и предпочтительно представляет собой арильную группу, необязательно имеющую один или более заместителей, выбранных из группы 7.
[0077]
«Арильная группа» в «арильной группе или гетероарильной группе, необязательно имеющей один или более заместителей, выбранных из группы 7» для R13 предпочтительно представляет собой фенильную группу или нафтильную группу и более предпочтительно фенильную группу.
[0078]
«Гетероарильная группа» в «арильной группе или гетероарильной группе, необязательно имеющей один или более заместителей, выбранных из группы 7» для R13 предпочтительно представляет собой тиенильную группу, пиридильную группу, пиримидильную группу, хинолильную группу, хиноксалильную группу или бензотиофенильную группу, более предпочтительно 2-тиенильную группу, 3-тиенильную группу, 2-пиридильную группу, 3-пиридильную группу или 4-пиридильную группу и наиболее предпочтительно 3-пиридильную группу или 3-тиенильную группу.
[0079]
Примеры заместителей арильной группы или гетероарильной группы для R13 могут включать, но не ограничиваются ими, следующие a)-j):
a) С1-С6 алкоксигруппу, необязательно замещенную одним-тремя атомами галогена,
b) С1-С6-алкильную группу, необязательно замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR и
j) гидроксигруппу,
Здесь R', R'' и R''' в b) и f)-i) каждый независимо представляют собой атом водорода или С1-С6-алкильную группу и предпочтительно каждый представляет собой атом водорода или С1-С3 алкильную группу.
[0080]
a)-j) предпочтительно являются следующими:
a) С1-С3 алкоксигруппа, необязательно замещенная одним-тремя атомами галогена, более предпочтительно метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа или трифторметоксигруппа, наиболее предпочтительно метоксигруппа, этоксигруппа или трифторметоксигруппа, наиболее предпочтительно метоксигруппа;
b) С1-С3 алкильная группа, необязательно замещенная любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -C(=NR')- NR''R''' и -NHC(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно С1-С3 алкильная группа, необязательно замещенная любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -C(=NR')-NR''R''' и - NHC(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или метильную группу, наиболее предпочтительно метильную группу, этильную группу, н-пропильную группу, изопропильную группу, фторметильную группу, дифторметильную группу, трифторметильную группу, гидроксиметильную группу, -CH2OCOMe, -CH2-NHC(=NH)-NH2 или -CH2-NHC(=NMe)-NH2;
c) атом галогена, предпочтительно атом фтора или атом хлора;
d) С3-С5-циклоалкоксигруппа, более предпочтительно циклопропоксигруппа;
e) С1-С3 алкилтиогруппа, более предпочтительно метилтиогруппа или этилтиогруппа;
f) -NR'R'', где R' и R'' каждый независимо представляют собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NH2, -NHMe, -NMe2, -NHEt или -NEt2;
g) -C(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -C(=NH)-NH2 или -C(=NMe)-NH2;
h) -NHC(=NR')-NR''R''', где R', R'' и каждый R''' независимо представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NHC(=NH)-NH2 или -NHC(=NMe)-NH2;
i) -NHCOR', где R' представляет собой атом водорода или С1-С3 алкильную группу, более предпочтительно -NHCOMe или -NHCOEt; и
j) гидроксигруппа.
[0081]
Арильная группа (предпочтительно фенильная группа) или гетероарильная группа (предпочтительно пиридильная группа) для R13 может иметь по меньшей мере один заместитель в любом положении. Если присутствует много заместителей, заместители могут быть одинаковыми или различными.
[0082]
Если R13 представляет собой арильную группу, каждый заместитель предпочтительно представляет собой a), b), d), g), h) или j) и более предпочтительно a), b), d) или j).
[0083]
Если R13 представляет собой фенильную группу, R13 может иметь заместитель в любом положении и может иметь множество заместителей и предпочтительно один или два заместителя присутствуют в положении 3 и/или положении 4 и более предпочтительно один заместитель присутствует в положении 4.
Если R5 представляет собой нафтильную группу, R5 может иметь заместитель в любом положении и может иметь множество заместителей и предпочтительно один заместитель присутствует в положении 6.
[0084]
Если R13 представляет собой фенильную группу, R13 более предпочтительно представляет собой фенильную группу, 4-метоксифенильную группу, 3-метоксифенильную группу, 4-этоксифенильную группу, 4-(н-пропокси)-фенильную группу, 4-(изопропокси)-фенильную группу, 4-циклопропокси-фенильную группу, 4-трифторметилфенильную группу, 4-гидроксиметил-фенильную группу, 4-ацетоксиметил-фенильную группу или 4-карбамимидамидо метил-фенильную группу и наиболее предпочтительно фенильную группу, 4-метоксифенильную группу, 3-метоксифенильную группу, 4-циклопропокси-фенильную группу, 4-гидроксиметил-фенильную группу, 4-ацетоксиметил-фенильную группу, 4-карбамимидамидометил-фенильную группу или 4-трифторметилфенильную группу.
Если R13 представляет собой нафтильную группу, R13 более предпочтительно представляет собой нафтильную группу или 6-метокси-2-нафтильную группу.
Наиболее предпочтительно представляет собой 4-метоксифенильную группу.
[0085]
Если R13 представляет собой гетероарильную группу, каждый заместитель предпочтительно представляет собой a), b), d), g), h) или j) и более предпочтительно а) или b).
Если R13 представляет собой гетероарильную группу, R13 может иметь по меньшей мере один заместитель в любом положении. Если R13 представляет собой 3-пиридильную группу, его заместитель(-и) предпочтительно присутствуют в положении 6 и/или положении 5. Если R13 представляет собой 2-пиридил, его заместитель(-и) предпочтительно присутствуют в положении 5 и/или положении 4 или в положении 5 и/или в положении 6. Если R13 представляет собой 4-пиридил, его заместитель предпочтительно присутствует в положении 2 и/или в положении 6.
Если R13 представляет собой гетероарильную группу, R13 может иметь множество заместителей и предпочтительно имеет один или два заместителя и предпочтительно имеет один заместитель.
Если R13 представляет собой пиридильную группу, R13 предпочтительно представляет собой 6-метокси-3-пиридильную группу или 6-метил-3-пиридильную группу.
Если R13 представляет собой 3-тиенильную группу или 6-хиноксалильную группу, R13 предпочтительно является незамещенным.
[0086]
«С1-С6-алкильная группа» в «С1-С6-алкильной группе, необязательно имеющей один или более заместителей, выбранных из группы 8» для R13 предпочтительно представляет собой С1-С3 алкильную группу и более предпочтительно метильную группу или этильную группу.
Заместители в «С1-С6-алкильной группе, необязательно имеющей один или более заместителей, выбранных из группы 8» для R13 каждый представляют собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу (предпочтительно, С1-С3 алкоксигруппу), предпочтительно гидроксигруппу, метоксигруппу или этоксигруппу и более предпочтительно гидроксигруппу.
[0087]
(ii) Если R11 представляет собой атом водорода, R12 и R13 объединены вместе с атомом углерода, с которым связаны R12 и R13, с образованием трех-пятичленного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, или CH2=.
Трех-пяти-членное насыщенное углеводородное кольцо может быть замещено одним-четырьмя атомами галогена и может быть предпочтительно замещено одним или двумя атомами фтора.
R12 и R13 предпочтительно объединены с образованием трех-пяти-членного насыщенного углеводородного кольца или CH2=, более предпочтительно с образованием циклопропана, циклобутана или СН2= (эксометиленовая группа) и наиболее предпочтительно с образованием циклопропана.
Если R12 и R13 объединены с образованием трех-пятичленного насыщенного углеводородного кольца или трех-пятичленного насыщенного гетероцикла, указанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл предпочтительно являются такими же, как Е. Более предпочтительно, Е представляет собой трех-пятичленное насыщенное углеводородное кольцо, и R12 и R13 объединены с образованием трех-пятичленного насыщенного углеводородного кольца и наиболее предпочтительно Е представляет собой циклопропановое кольцо, и R12 и R13 объединены с образованием циклопропанового кольца.
[0088]
(iii) R11, R12 и R13 объединены вместе с атомом углерода, с которым связан R11, и атомом углерода, с которым связаны R12 и R13, с образованием бензольного кольца или шестичленного гетероцикла, необязательно имеющего один или более заместителей, выбранных из группы 9.
Бензольное кольцо или гетероцикл могут иметь по меньшей мере один заместитель в любом положении. Если присутствует много заместителей, заместители могут быть одинаковыми или различными.
Каждый заместитель бензольного кольца или гетероцикла представляет собой атом галогена, С1-С6-алкильную группу, необязательно замещенную одним-тремя атомами галогена, или С1-С6 алкоксигруппу, предпочтительно атом галогена, С1-С3 алкильную группу, необязательно замещенную одним-тремя атомами галогена, или С1-С3 алкокси и более предпочтительно атом галогена, метильную группу или метоксигруппу.
«Бензольное кольцо или шестичленный гетероцикл, необязательно имеющий один или более заместителей» предпочтительно представляет собой незамещенное бензольное кольцо.
[0089]
R11, R12 и R13 наиболее предпочтительно удовлетворяет указанному выше (i).
[0090]
R14 и R15 каждый представляют собой атом водорода, или R14 и R15 объединены и представляют собой иминную связь (C=N).
[0091]
V и W каждый независимо представляют собой атом кислорода, атом азота или атом серы и предпочтительно атом кислорода.
[0092]
R16 и R17 такие, что:
(a) R16 и R17 объединены с образованием иминной связи (N=C); или
(b) R16 представляет собой J-La'-Lp'-NH-B'-CH2-O(C=O)-*, и R17 представляет собой гидроксигруппу или С1-С3 алкоксигруппу.
[0093]
В случае (b) R16 представляет собой J-La'-Lp'-NH-B'-CH2-O(C=O)-*, звездочка в формуле представляет собой связь с N10'-положением пирролобензодиазепинового кольца, представленного указанной выше формулой.
[0094]
В' представляет собой фенильную группу или гетероарильную группу и предпочтительно представляет собой 1,4-фенильную группу, 2,5-пиридильную группу, 3,6-пиридильную группу,2,5-пиримидильную группу или 2,5-тиенильную группу и более предпочтительно 1,4-фенильную группу.
[0095]
Lp' представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой in vivo или в клетке-мишени. Lp, например, расщепляется под действием фермента, такого как эстераза и пептидаза.
[0096]
Конкретные примеры линкера Lp' могут включать, но не ограничиваются ими, -GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI-, -GGPL-, -EGGVA, -PI-, -GGF-, DGGF-, (D-)D-GGF-, -EGGF-, -SGGF-, -KGGF-, -DGGFG-, -GGFGG-, -DDGGFG-, -KDGGFG- и -GGFGGGF-.
Здесь "(D-)V" обозначает D-валин, "(D)-P" обозначает D-пролин и "(D-)D" обозначает D-аспарагиновую кислоту.
[0097]
Линкер Lp' предпочтительно представляет собой следующее: -GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI- или -GGPL-.
Более предпочтительными примерами являются -GGVA-, -GGVCit- и -VA-.
[0098]
La' выбран из следующей группы:
-С(=O)-(СН2СН2)n6-С(=O)-, -C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2)n7-C(=O)-,
-C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2O)n7-CH2-C(=O)-,
-C(=O)-(CH2CH2)n6-NH-C(=O)-(CH2CH2O)n7-CH2CH2-C(=O)-, -(CH2)n8-O-C(=O)-,
-(CH2)n12-C(=O)- и, -(CH2CH2)n13-C(=O)-NH-(CH2CH2O)n14-CH2CH2-C(=O)-
B формулах n6 представляет собой целое число от 1 до 3 (предпочтительно, 1 или 2), n7 представляет собой целое число от 1 до 5 (предпочтительно, целое число от 2 до 4, более предпочтительно, 2 или 4), n8 представляет собой целое число от 0 до 2 (предпочтительно, 0 или 1), n12 представляет собой целое число от 2 до 7 (предпочтительно, целое число от 2 до 5, более предпочтительно, 2 или 5), n13 представляет собой целое число от 1 до 3 (предпочтительно, 1) и n14 представляет собой целое число от 6 до 10 (предпочтительно, 8).
[0099]
La' предпочтительно выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -СН2-ОС(=O)-, ОС(=O)-,
-(СН2)2-С(=O)-, -(СН2)5-С(=O)- и -CH2CH2-C(=O)-NH -(CH2CH2O)8-СН2СН2-С(=O)-.
[0100]
La' более предпочтительно представляет собой -С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)- или -(СН2)5-С(=O)-.
[0101]
J не ограничен конкретной структурой и может представлять собой любую циклическую структуру, включая структуру алкина, которая реагирует с азидной группой с образованием 1,2,3-триазольного кольца, и его примеры могут включать, но не ограничиваются ими, соединения, представленные следующими формулами:
[Формула 69]
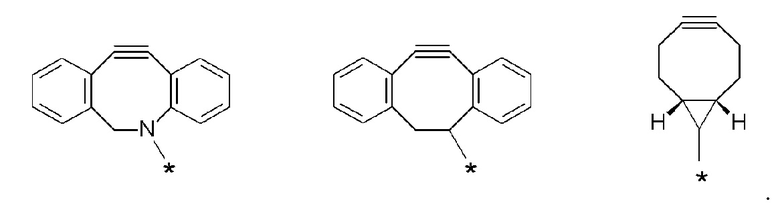
[0102]
В структурных формулах для J, представленных выше, каждая звездочка представляет собой связь с -(С=O) или -(СН2)n8 на левом конце La'.
[0103]
В качестве альтернативы, J может представлять собой соединение, которое связывается с боковой цепью аминокислотного остатка (например, цистеина или лизина) антитела Ab или атомом галогена, и примеры J могут включать, но не ограничиваются ими, малеимидильную группу, представленную следующей формулой:
[Формула 70]
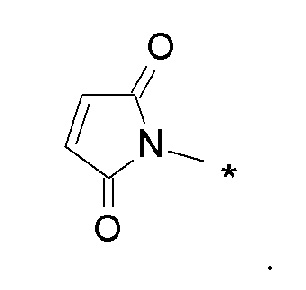
В малеимидильной группе, представленной выше, звездочка представляет собой связь с -(СН2)n12 или -(СН2СН2)n13 на левом конце La'.
[0104]
R16 предпочтительно представлен J-La'-Lp'-NH-B'-CH2-O(C=O)-*, где
В' представляет собой 1,4-фенильную группу;
Lp' выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, GG(D-)PI- и -GGPL-;
La' выбран из следующей группы:
-С(=O)-СН2СН2-С(=O)-, -С(=O)-(СН2СН2)2-С(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-, -ОС(=O)-,
-СН2-ОС(=O)-, -(СН2)5-С(=O)- и -CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-; и
J представляет собой любую из структурных формул:
[Формула 71]
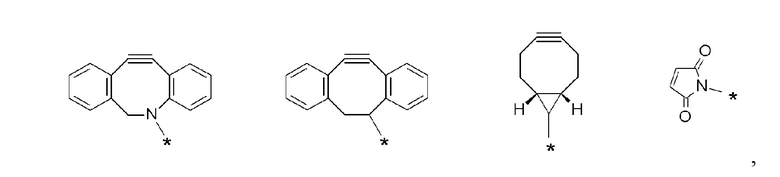
где в структурных формулах для J,
каждая звездочка представляет собой связь с La'.
[0105]
R16 более предпочтительно представляет собой любое, выбранное из следующей группы:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GG-(D-)VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPI-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-, J3-CH2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)- и
J4-CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-
где J1, J2, J3 и J4 представляют структурные формулы, представленные следующими:
[Формула 72]
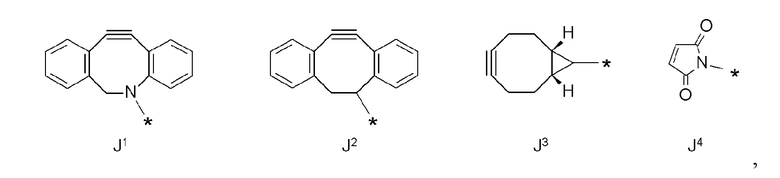
где в структурных формулах для J1, J2, J3 и J4
каждая звездочка представляет собой связь с группой, соседней с J1, J2, J3 или J4 и
В' представляет собой 1,4-фенильную группу.
[0106]
R16 наиболее предпочтительно представляет собой любой из следующего:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)-
где
В' представляет собой 1,4-фенильную группу и
J1 и J4 представлены следующими структурными формулами для J:
[Формула 73]
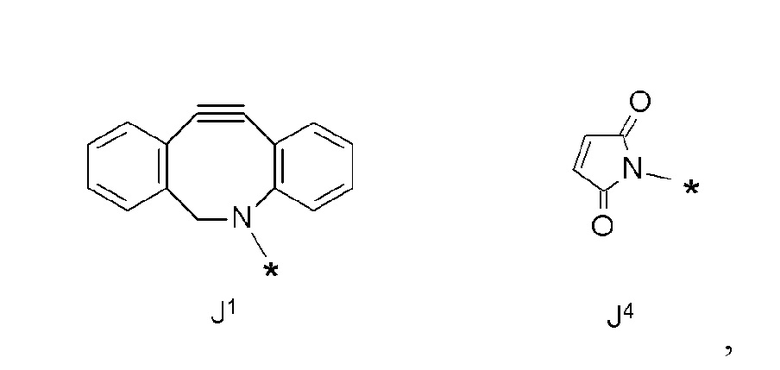
где в структурных формулах для J1 и J4
каждая звездочка представляет связь с группой, соседней с J1 или J4.
[0107]
R17 представляет собой гидроксигруппу или С1-С3 алкоксигруппу и предпочтительно гидроксигруппу или метоксигруппу.
R17 может быть гидрогенсульфитным аддуктом (OSO3M, где М представляет собой катион металла).
Поскольку R17 связывается с асимметричным атомом углерода, обеспечивается стерическая конфигурация, представленная частичной структурой (VIa) или (VIb) ниже. Каждая волнистая линия представляет связь с W в промежуточном соединении и свободном лекарственном средстве, представленном общей формулой (VI).
[Формула 74]
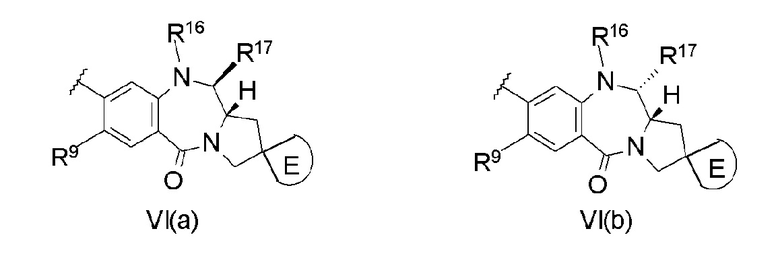
[0108]
Свободное лекарственное средство предпочтительно представляет собой одно соединение, выбранное из следующей группы:
[Формула 75]
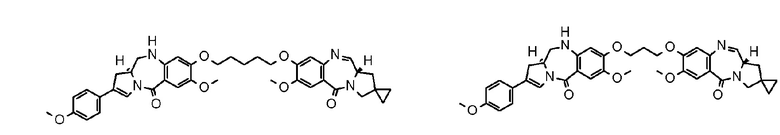

[0109]
Свободное лекарственное средство в некоторых случаях высвобождается в опухолевых клетках с частью связанного линкера L, но является превосходным лекарственным средством, которое оказывает превосходное противоопухолевое действие даже в таком состоянии. Свободное лекарственное средство после миграции в опухолевые клетки в некоторых случаях дополнительно окисляется, вызывая дегидрирование R16 и R17, но оказывает превосходное противоопухолевое действие даже в таком состоянии.
[0110]
Промежуточное соединение предпочтительно представляет собой одно соединение, выбранное из следующей группы:
[Формула 76]
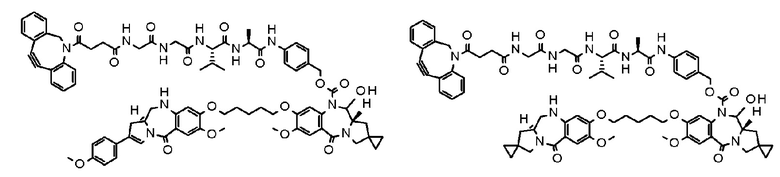
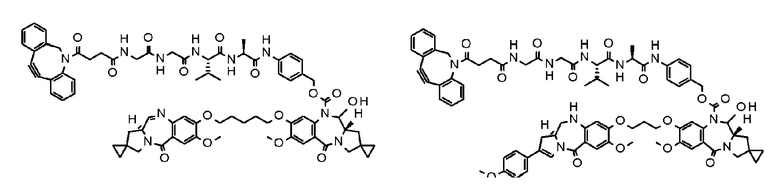
[Формула 77]
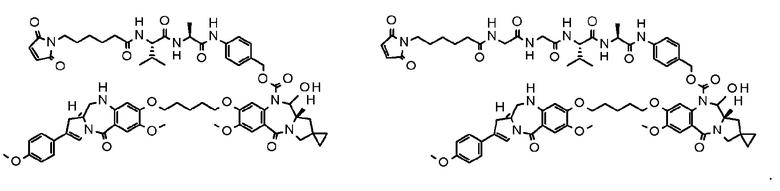
[0111]
Промежуточное соединение предпочтительно представляет собой одно соединение, выбранное из следующей группы:
[Формула 78]
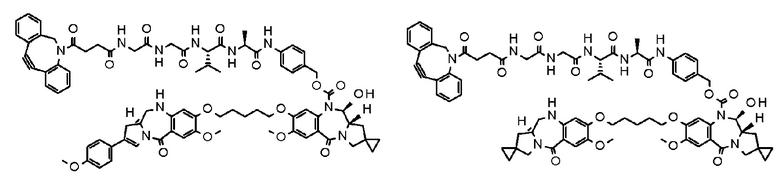
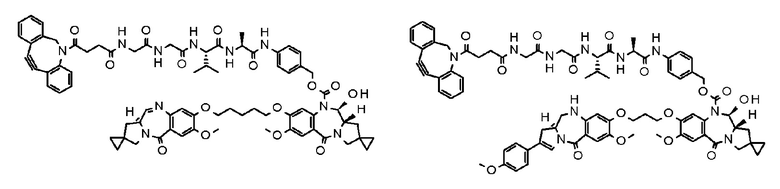
[Формула 79]
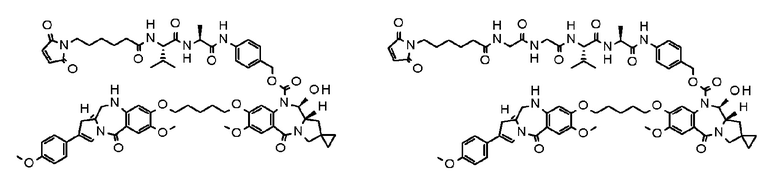
[Формула 80]
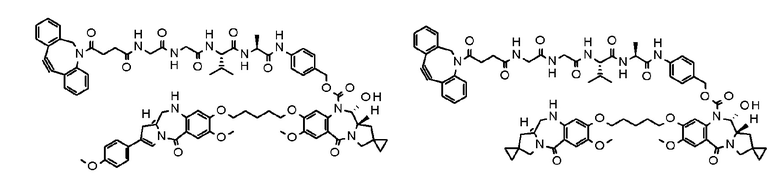
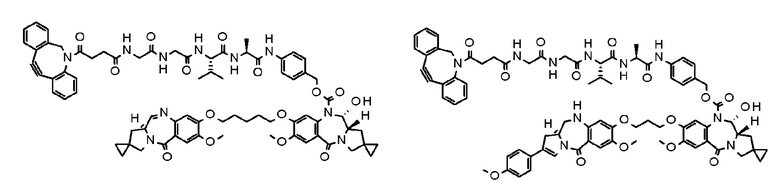
[Формула 81]
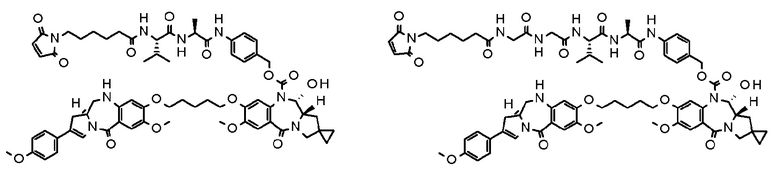
[0112]
<Антитело>
В настоящем изобретении термины «рак» и «опухоль» используются в одном и том же значении.
В настоящем изобретении термин «ген» относится к нуклеотидам или нуклеотидной последовательности, содержащей нуклеотидную последовательность, кодирующую аминокислоты белка, или ее комплементарной цепи. Значение термина «ген» охватывает, например, полинуклеотид, олигонуклеотид, ДНК, мРНК, кДНК и РНК в качестве нуклеотидной последовательности, содержащей нуклеотидная последовательность, кодирующую аминокислоты белка, или ее комплементарной цепи. Примеры «гена CLDN6» согласно настоящему изобретению включают ДНК, мРНК, кДНК и кРНК, содержащие нуклеотидная последовательность, кодирующую аминокислотную последовательность белка CLDN6.
В настоящем изобретении термины «нуклеотиды», «полинуклеотид» и «нуклеотидная последовательность» имеют то же значение, что и «нуклеиновые кислоты», и значение терминов «нуклеотиды» и «нуклеотидная последовательность» охватывает, например, ДНК, РНК, зонд, олигонуклеотид, полинуклеотид и праймер.
В настоящем изобретении термины «полипептид», «пептид» и «белок» используются взаимозаменяемо.
В настоящем изобретении «CLDN6» используется в том же значении, что и «белок CLDN6».
[0113]
В настоящем изобретении «клетки» включают клетки в организме животного и культивируемые клетки.
В настоящем изобретении «клеточная цитотоксическая активность» относится к обусловливанию патологического изменения в клетках любым способом, который включает причинение не только непосредственных повреждении, но также и всех типов повреждений структуры и функции клеток, таких как расщепление ДНК, образование димеров нуклеотидов, расщепление хромосомы, повреждение митотического аппарата и снижение активности различных ферментов.
[0114]
В настоящем изобретении «функциональный фрагмент антитела» также называется «антигенсвязывающим фрагментом антитела» и означает отдельный фрагмент антитела, обладающий связывающей активностью в отношении антигена, и его примеры могут включать, но не ограничиваются ими, Fab, F(ab')2, Fv, scFv, диатела, линейные антитела и полиспецифические антитела, получаемые из фрагментов антител. Помимо этого, значение термина «антигенсвязывающий фрагмент антитела» охватывает Fab', моновалентный фрагмент вариабельной области антитела, полученный путем обработки F(ab')2 в восстанавливающих условиях. Однако отсутствуют какие-либо ограничения для этих молекул в том случае, если указанные молекулы обладают способностью связываться с антигеном. Эти антигенсвязывающие фрагменты включают не только фрагменты, полученные путем обработки полноразмерной молекулы белка антитела соответствующим ферментом, но также белок, получаемый в соответствующей клетке-хозяине с применением гена генетически сконструированного антитела.
Функциональный фрагмент согласно настоящему изобретению включает функциональный фрагмент, содержащий высококонсервативный аспарагин (Asn297), подлежащий модификации N-связанным гликаном, в Fc-области тяжелой цепи IgG, и аминокислоты вблизи Asn297, сохраняющий при этом связывающую активность в отношении антигена.
[0115]
В настоящем изобретении термин «эпитоп» относится к отдельному пептиду или отдельной трехмерной структуре антигена, с которой связывается конкретное антитело (например, антитело к CLDN6) (отдельный пептид или отдельная трехмерная структура CLDN6). Эпитоп в виде такого отдельного пептида (например, отдельного пептида CLDN6) может быть определен с применением любого способа, хорошо известного специалистам в данной области техники, такого как иммунологический анализ.
[0116]
Термин «CDR» в настоящем изобретении относится к области, определяющей комплементарность. Известно, что каждая из тяжелых цепей и легких цепей молекулы антитела имеет три CDR. CDR, которые также называют гипервариабельной областью, расположены в вариабельных областях тяжелых цепей и легких цепей антитела и представляют собой сайт с особенно высокой вариативностью первичной структуры. Три CDR расположены отдельно в первичной структуре полипептидной цепи каждой из тяжелых цепей и легких цепей. Что касается CDR антител, в данном случае CDR тяжелой цепи представлены CDRH1, CDRH2 и CDRH3 с аминного конца аминокислотной последовательности тяжелой цепи, и CDR легкой цепи представлены CDRL1, CDRL2 и CDRL3 с аминного конца аминокислотной последовательности легкой цепи. Эти сайты расположены в непосредственной близости друг от друга в трехмерной структуре, определяющей специфичность связывания антитела.
[0117]
В настоящем изобретении «гибридизация в жестких условиях» относится к гибридизации в коммерчески доступном растворе для гибридизации ExpressHyb Hybridization Solution (Clontech) при 68°C, или гибридизации с использованием фильтра с фиксированной на нем ДНК в присутствии 0,7-1,0 М NaCl при 68°С и промывкой при 68°С 0,1-2 × раствором SSC (1 × раствор SSC содержит 150 мМ NaCl и 15 мМ цитрата натрия), или гибридизации в условиях, эквивалентных описанным.
В настоящем изобретении «от одного до нескольких» относится к диапазону от 1 до 10, от одного до девяти, от одного до восьми, от одного до семи, от одного до шести, от одного до пяти, от одного до четырех, от одного до трех или от одного до двух.
[0118]
В настоящем изобретении антитело, способное к распознаванию CLDN6 или связыванию с CLDN6, и антитело, способное к распознаванию CLDN6 и CLDN9 или связыванию с CLDN6 и CLDN9, в ряде случаев называют «антителом к CLDN6» и «антителом к CLDN6/CLDN9», соответственно. Такие антитела включают химерные антитела, гуманизированные антитела и антитела человека. Антитело, способное к распознаванию CLDN6 и CLDN9 или связыванию с CLDN6 и CLDN9, в ряде случаев называют «антителом к CLDN6».
[0119]
«Антитело, подлежащее применению для получения конъюгата антитело-лекарственное средство согласно настоящему изобретению» относится к иммуноглобулину и представляет собой молекулу, содержащую антигенсвязывающий сайт, который иммуноспецифически связывается с антигеном. Антитело согласно настоящему изобретению может принадлежать к любому классу IgG, IgE, IgM, IgD, IgA и IgY, и предпочтительным является IgG. Подкласс может быть любым из IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2, и предпочтительными являются IgG1, IgG2 и IgG4. Если применяют IgG1 или IgG4, эффекторную функцию можно регулировать путем замены некоторых аминокислотных остатков в константной области (см. WO 88/07089, WO 94/28027, WO 94/29351).
Антитело может быть получено от любых видов, которые предпочтительно включают, но не ограничиваются ими, человека, крысу, мышь и кролика. Если антитело получено от видов, отличных от человека, его предпочтительно подвергают химеризации или гуманизации с применением хорошо известной методики. Антитело согласно настоящему изобретению может представлять собой поликлональное антитело или моноклональное антитело, и предпочтительно представляет собой моноклональное антитело. Примеры моноклональных антител могут включать, но не ограничиваются ими, моноклональные антитела, полученные от животных, не являющихся человеком, такие как антитела крысы, антитела мыши и антитела кролика; химерные антитела; гуманизированные антитела; антитела человека; их функциональные фрагменты и их модифицированные варианты.
[0120]
Антитело согласно настоящему изобретению предпочтительно представляет собой антитело, способное к нацеливанию на опухолевую клетку. В частности, антитело, с которым лекарственное средство, обладающее противоопухолевой активностью, конъюгировано посредством линкера, предпочтительно обладает одним или более из свойств распознавания опухолевой клетки, связывания с опухолевой клеткой, включения и интернализации в опухолевую клетку и повреждения опухолевой клетки.
Активность связывания антитела в отношении опухолевых клеток может быть подтверждена с помощью проточной цитометрии. Включение антитела в опухолевые клетки может быть подтверждено посредством (1) анализа визуализации антитела, включенного в клетки, под флуоресцентным микроскопом с использованием вторичного антитела (флуоресцентно меченного), связывающегося с терапевтическим антителом (Cell Death and Differentiation (2008) 15, 751-761), (2) анализа определения интенсивности флуоресценции, включенной в клетки, с использованием вторичного антитела (флуоресцентно меченного), связывающегося с терапевтическим антителом (Molecular Biology of the Cell, Vol. 15, 5268-5282, December 2004), или (3) анализа Mab-ZAP с использованием иммунотоксина, связывающегося с терапевтическим антителом, при котором указанный токсин высвобождается при включении в клетки, что приводит к подавлению роста клеток (Bio Techniques 28: 162-165, January 2000). В качестве иммунотоксина может быть применен рекомбинантный комплексный белок каталитического домена дифтерийного токсина и белка G.
В настоящем изобретении «высокая способность к интернализации» относится к ситуации, когда уровень выживаемости (который является относительным уровнем, когда уровень выживаемости клеток без добавления антитела принимают за 100%) целевых антиген-экспрессирующих клеток (например, клеток, экспрессирующих CLDN6) при добавлении исследуемого антитела и меченного сапорином антитела к IgG мыши или крысы предпочтительно составляет 70% или менее, и более предпочтительно составляет 60% или менее.
[0121]
Поскольку соединение, входящее в состав конъюгата антитело-лекарственное средство согласно настоящему изобретению, проявляет противоопухолевое действие, предпочтительно, но не обязательно, чтобы само антитело обладало противоопухолевым действием. В целях специфического и избирательного проявления цитотоксичности противоопухолевого соединения в отношении опухолевых клеток важно, а также предпочтительно, чтобы антитело обладало способностью к интернализации для обеспечения миграции в опухолевые клетки. Для проявления противоопухолевого действия важно, а также предпочтительно, чтобы антитело обладало способностью к интернализации и миграции в опухолевые клетки в соответствии с тем, что лекарственное средство специфически и избирательно повреждает опухолевые клетки. Противоопухолевая активность антитела относится к клеточной цитотоксической активности или противоклеточному действию в отношении опухолевых клеток. Противоопухолевая активность может быть подтверждена с помощью любой известной системы оценки in vitro или in vivo.
Примеры такого антитела могут включать, но не ограничиваются ими, антитела к связанным с опухолью антигенам, включая антитело к CLDN6, антитело к CLDN6/CLDN9, антитело к HER2, антитело к DLL3 (дельта-подобному белку 3), антитело к А33, антитело к CanAg, антитело к CD19, антитело к CD20, антитело к CD22, антитело к CD30, антитело к CD33, антитело к CD56, антитело к CD70, антитело к CD98, антитело к TROP2, антитело к CEA, антитело к Cripto, антитело к EphA2, антитело к FGFR2 (например, WO 201315206), антитело к G250, антитело к MUC1 (например, WO 2011012309), антитело к GPNMB, антитело к интегрину, антитело к PSMA, антитело к тенасцину-С, антитело к SLC44A4, антитело к мезотелину, антитело к EGFR и антитело к DR5.
Антитело согласно настоящему изобретению предпочтительно представляет собой антитело к CLDN6, антитело к CLDN6/CLDN9, антитело к HER2, антитело к CD98 или антитело к TROP2, и более предпочтительно антитело к CLDN6 или антитело к HER2 (например, трастузумаб, вариант трастузумаба).
[0122]
Антитело согласно настоящему изобретению может быть получено с применением способа, обычно применяемого в данной области техники, который включает иммунизацию животных антигенным полипептидом, а также сбор и очистку продуцируемых in vivo антител. Происхождение антигена не ограничивается человеком, и животные могут быть иммунизированы антигеном, полученным от животного, не являющегося человеком, такого как мышь, крыса или тому подобное. В этом случае может быть проверена перекрестная реактивность антител, связывающихся с полученным гетерологичным антигеном, с антигенами человека с целью скрининга для поиска антитела, применимого при заболевании человека.
В качестве альтернативы продуцирующие антитела клетки, которые продуцируют антитела к антигену, подвергают слиянию с клетками миеломы в соответствии со способом, известным в данной области техники (например, Nature (1975) 256, р. 495-497, Monoclonal Antibodies, p. 365-367, Plenum Press, N.Y. (1980)), с получением гибридом, от которых, в свою очередь, могут быть получены моноклональные антитела (описанные ниже).
Антиген может быть получен путем модификации клеток-хозяев методами генетической инженерии с получением гена, кодирующего антигенный белок.
[0123]
Химерное антитело и гуманизированное антитело согласно настоящему изобретению могут быть получены в соответствии с известным способом (например, Proc. Natl. Acad. Sci. U.S.A., 81, 6851-6855, (1984), Nature (1986) 321, p. 522-525, WO 90/07861).
[0124]
Антитело к HER2 (например, патент США №5821337), антитело к TROP2 (например, WO 2003/074566) и антитело к CD98 (например, WO 2015/146132) могут быть получены с применением известного подхода.
[0125]
Далее будет описано антитело к CLDN6, применяемое в настоящем изобретении. Вариант реализации, описанный ниже, является примером типичных вариантов реализации настоящего изобретения, и объем настоящего изобретения не следует интерпретировать как более узкий в связи с указанным вариантом реализации.
[0126]
1. CLDN6 и CLDN9
CLDN6, содержащий четыре трансмембранных домена белок, принадлежащий к семейству клаудинов и состоящий из 220 аминокислот, имеет N-конец и С-конец, расположенные внутри клетки.
Аминокислотная последовательность и последовательность ДНК CLDN6 человека опубликованы в общедоступных базах данных и могут быть обозначены, например, номерами доступа NP_067018 (SEQ ID NO: 1 (фигура 11)) и NM_021195 (SEQ ID NO: 2 (фигура 11) (обе опубликованы в NCBI).
В аминокислотной последовательности белка CLDN6 человека (далее в настоящем описании называемой «аминокислотной последовательностью CLDN6») внеклеточная область состоит из внеклеточного домена (ЕС1), состоящего из аминокислотных остатков 29-81 SEQ ID NO: 1 в перечне последовательностей, и внеклеточного домена (ЕС2), состоящего из аминокислотных остатков 138-160 SEQ ID NO: 1 в перечне последовательностей.
CLDN9, содержащий четыре трансмембранных домена белок, принадлежащий к семейству клаудинов и состоящий из 217 аминокислот, имеет N-конец и С-конец, расположенные внутри клетки. CLDN9 высокогомологичен CLDN6.
Аминокислотная последовательность и последовательность ДНК CLDN9 человека опубликованы в общедоступных базах данных, и могут быть обозначены, например, номерами доступа NP_066192 (SEQ ID NO: 3 (фигура 12)) и NM_020982 (SEQ ID NO: 4 (фигура 12)) (обе опубликованы в NCBI).
[0127]
2. Антитело к CLDN6
Примером антитела к CLDN6 согласно настоящему изобретению является антитело к CLDN6, которое распознает структуру более высокого порядка, включающую две внеклеточные области, в частности, аминокислотную последовательность в положениях 29-81 и аминокислотную последовательность в положениях 138-160 с N-конца CLDN6, представленного SEQ ID NO: 1 в перечне последовательностей, и обладает способностью к интернализации.
Антитело к CLDN6 согласно настоящему изобретению представляет собой антитело, способное к нацеливанию на опухолевые клетки, и, в частности, обладает способностью распознавать опухолевую клетку, способностью связываться с опухолевой клеткой, способностью к включению и интернализации в опухолевую клетку, и так далее. Соответственно, антитело к CLDN6 согласно настоящему изобретению может быть применено для получения конъюгата антитело-лекарственное средство путем конъюгирования через линкер с соединением, обладающим противоопухолевой активностью.
Антитело к CLDN6 согласно настоящему изобретению может обладать противоопухолевой активностью.
[0128]
Антитело к CLDN6 может быть получено с применением способа, обычно применяемого в данной области техники, который включает иммунизацию животных антигенным полипептидом, а также сбор и очистку продуцируемых in vivo антител. CLDN6 представляет собой содержащий четыре трансмембранных домена белок, и, следовательно, белок, сохраняющий трехмерную структуру, может быть применен в качестве антигена, и примеры таких способов могут включать иммунизацию клетками, но не ограничиваются ею.
В качестве альтернативы продуцирующие антитела клетки, которые продуцируют антитела к антигену, подвергают слиянию с клетками миеломы в соответствии со способом, известным в данной области техники, с получением гибридом, от которых, в свою очередь, могут быть получены моноклональные антитела.
[0129]
Далее будет конкретно описан способ получения антитела к CLDN6.
1) Получение антигена
CLDN6 может быть непосредственно очищен для применения из ткани опухоли или опухолевых клеток человека, или может быть приготовлена фракция мембран клеток для применения в качестве CLDN6. В качестве альтернативы CLDN6 может быть получен путем синтеза CLDN6 in vitro (например, Rapid Translation System (RTS) производства Roche Diagnostics K.K.) или путем обеспечения выработки CLDN6 клетками-хозяевами с помощью методов генетической инженерии.
Для получения антигена методами генетической инженерии кДНК для CLDN6 встраивают в вектор, способный обеспечивать экспрессию кДНК, и осуществляют синтез CLDN6 в растворе, содержащем фермент, субстрат и вещество, обеспечивающее энергию, необходимые для транскрипции и трансляции, или осуществляют трансформацию клеток-хозяев другого прокариотического или эуокариотического организма для обеспечения экспрессии CLDN6 указанными клетками. В качестве альтернативы в качестве белка CLDN6 могут быть применены клетки, экспрессирующие CLDN6, полученные методами генетической инженерии, или линия клеток, экспрессирующих CLDN6.
Антиген может быть получен в виде секреторного белка путем обеспечения возможности экспрессии соответствующей системой вектор-хозяин белка слияния, содержащего внеклеточную область мембранного белка CLDN6 и константную область антитела, объединенные совместно.
В качестве антигена может быть применен сам описанный выше трансформант.
Помимо этого, в качестве антигена может быть применена линия клеток, экспрессирующих CLDN6. Примеры таких линий клеток могут включать линию клеток рака поджелудочной железы человека NOR-P1; линии клеток рака яичника человека NIH:OVCAR-3, OV-90 и OAW28; линию клеток тератомы яичника человека РА-1; линию клеток рака печени человека НиН-7; линию клеток гестационной хориокарциномы человека JEG-3 и клон D1 линии плюрипотентных клеток эмбриональной карциномы человека NTERA-2, но не ограничиваются ими, и любая линия клеток, экспрессирующих CLDN6, является приемлемой.
Белок CLDN9, предназначенный для применения в настоящем изобретении, может быть приготовлен для применения таким же образом.
2) Получение моноклонального антитела к CLDN6
Антитело к CLDN6, применяемое в настоящем изобретении, не ограничивается конкретным антителом, и, например, предпочтительно может быть применено антитело, соответствующее любой из аминокислотных последовательностей, перечисленных в прилагаемом перечне последовательностей. Желательно, чтобы антитело к CLDN6, предназначенное для применения в настоящем изобретении, обладало следующими свойствами.
(1) Антитело, обладающее следующими свойствами (а) и (b).
(а) Распознавание или связывание с белками семейства CLDN.
Антитело согласно настоящему изобретению распознает белки семейства CLDN. Другими словами, антитело согласно настоящему изобретению связывается с белками семейства CLDN. Антитело согласно настоящему изобретению предпочтительно связывается с CLDN6, и более предпочтительно избирательно связывается с CLDN6. Помимо этого, антитело согласно настоящему изобретению может распознавать CLDN9 или связываться с CLDN9.
В настоящем изобретении «специфическое распознавание», что означает «специфическое связывание», относится к связыванию, которое не является неспецифической адсорбцией. Примеры критериев определения того, является ли связывание специфическим или не является, могут включать константы диссоциации (далее в настоящем описании называемые «KD»), но не ограничиваются ими. Предпочтительное значение KD антитела согласно настоящему изобретению при связывании с CLDN6 и/или CLDN9 составляет 1×10-5 М или менее, 5×10-6 М или менее, 2×10-6 М или менее, или 1×10-6 М или менее, и более предпочтительно 5×10-7 М или менее, 2×10-7 М или менее, или 1×10-7 М или менее.
Связывание между антигеном и антителом в настоящем изобретении может быть оценено или определено с помощью такого метода анализа, как метод ELISA, метод радиоиммунологического анализа (RIA) и метод поверхностного плазмонного резонанса (далее в настоящем описании называемого «SPR»). Связывание между антигеном, экспрессируемым на поверхности клетки, и антителом может быть оценено, например, методом проточной цитометрии.
(b) Наличие способности к интернализации в клетки, экспрессирующие CLDN6 и/или CLDN9, посредством связывания с CLDN6 и/или CLDN9. (2) Антитело по п. (1), где CLDN6 и/или CLDN9 представляют собой CLDN6 человека и/или CLDN9 человека.
[0130]
Способ согласно настоящему изобретению для получения антитела к CLDN6, как правило, включает следующие стадии, но не ограничивается следующим.
(Способ с применением гибридомы)
(a) Очистка биополимера для применения в качестве антигена или получение экспрессирующих антиген клеток и введение полученного биополимера или экспрессирующих антиген клеток животному;
(b) получение ткани (например, лимфатического узла), содержащей продуцирующие антитело клетки, от животного, у которого была вызвана иммунная реакция;
(c) получение клеток миеломы (например, клеток миеломы мыши SP2/0-ag14);
(d) слияние продуцирующих антитело клеток и клеток миеломы;
(e) отбор группы гибридом, продуцирующих целевое антитело;
(f) разделение на отдельные клоны клеток (клонирование);
(g) необязательная стадия культивирования гибридомы для крупномасштабного получения моноклонального антитела или выращивания животного, которому была трансплантирована гибридома; и
(h) исследование физиологической активности (активности интернализации) и специфичности связывания полученного таким образом моноклонального антитела или проверка его свойств в качестве реагента для мечения.
Примеры способов, которые следует применять согласно настоящему описанию для определения титров антител, могут включать, но не ограничиваются ими, проточную цитометрию и метод клеточного ELISA (Cell-ELISA).
[0131]
Примеры полученного таким образом моноклонального антитела к CLDN6 могут включать, но не ограничиваются ими, антитела мыши к CLDN6 В1 и С7. В настоящем изобретении «В1» и «С7» в ряде случаев называют «антителом В1» и «антителом С7», соответственно.
Нуклеотидная последовательность и аминокислотная последовательность для вариабельной области тяжелой цепи антитела В1 представлены SEQ ID NO: 20 (фигура 19) и SEQ ID NO: 21 (фигура 19) в перечне последовательностей, соответственно. Нуклеотидная последовательность и аминокислотная последовательность для вариабельной области легкой цепи антитела В1 представлены SEQ ID NO: 18 (фигура 18) и SEQ ID NO: 19 (фигура 18) в перечне последовательностей, соответственно.
Аминокислотные последовательности для CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 антитела В1 представлены SEQ ID NO: 9 (фигура 15), SEQ ID NO: 10 (фигура 15), SEQ ID NO: 11 (фигура 15), SEQ ID NO: 5 (фигура 13), SEQ ID NO: 6 (фигура 13) и SEQ ID NO: 7 (фигура 13), соответственно.
Нуклеотидная последовательность и аминокислотная последовательность для вариабельной области тяжелой цепи антитела С7 соответственно представлены SEQ ID NO: 24 (фигура 21) и SEQ ID NO: 25 (фигура 21) в перечне последовательностей. Нуклеотидная последовательность и аминокислотная последовательность для вариабельной области легкой цепи антитела С7 соответственно представлены SEQ ID NO: 22 (фигура 20) и SEQ ID NO: 23 (фигура 20) в перечне последовательностей.
Аминокислотные последовательности для CDRH1, CDRH2, CDRH3, CDRL1, CDRL2 и CDRL3 антитела С7 представлены SEQ ID NO: 15 (фигура 17), SEQ ID NO: 16 (фигура 17), SEQ ID NO: 17 (фигура 17), SEQ ID NO: 12 (фигура 16), SEQ ID NO: 13 (фигура 16) и SEQ ID NO: 14 (фигура 16), соответственно.
[0132]
Помимо этого, даже если моноклональное антитело было независимо получено на стадиях (a)-(h) раздела «Получение антитела к CLDN6» повторно, или моноклональное антитело было отдельно получено с применением другого способа, может быть получено антитело, обладающее активностью интернализации, эквивалентной таковой для антитела В1 или антитела С7. Примером таких антител является антитело, которое связывается с эпитопом для антитела В1 или антитела С7. Если вновь полученное моноклональное антитело связывается с отдельным пептидом или отдельной трехмерной структурой, с которой связывается антитело В1 или антитело С7, можно определить, что указанное моноклональное антитело связывается с эпитопом для антитела В1 или антитела С7. Посредством подтверждения того, что указанное моноклональное антитело конкурирует с антителом В1 или антителом С7 за связывание с CLDN6 (то есть указанное моноклональное антитело препятствует связыванию между антителом В1 или антителом С7 и CLDN6), даже если конкретная последовательность или структура эпитопа не была установлена, можно определить, что указанное моноклональное антитело связывается с эпитопом для антитела к CLDN6. Если идентичность эпитопа была подтверждена, можно в высокой степени ожидать, что указанное моноклональное антитело будет обладать антигенсвязывающей способностью, биологической активностью и/или активностью интернализации, эквивалентной таковой для антитела В1 или антитела С7.
[0133]
Антитело согласно настоящему изобретению включает, помимо моноклонального антитела к CLDN6, генетически рекомбинантное антитело, полученное путем искусственной модификации с целью снижения гетерологичной антигенности для людей, такое как химерное антитело, гуманизированное антитело и антитело человека. Эти антитела могут быть получены с применением известного способа.
(1) Химерное антитело
Примеры химерного антитела могут включать, но не ограничиваются ими, антитело, в котором вариабельные и константные области антитела получены от различных видов, например, химерное антитело, в котором вариабельная область антитела мыши или крысы соединена с константной областью антитела человека (см. Proc.Natl. Acad. Sci. USA, 81, 6851-6855, (1984)).
Химерное антитело, полученное из антитела В1 мыши к CLDN6 человека, в качестве примера химерного антитела согласно настоящему изобретению, представляет собой антитело, содержащее тяжелую цепь, содержащую вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 21 (фигура 19), и легкую цепь, содержащую вариабельную область легкой цепи, представленную SEQ ID NO: 19 (фигура 18), которое может содержать любую константную область антитела человека.
Конкретные примеры химерного антитела, полученного из антитела В1 мыши к CLDN6 человека, могут включать химерное антитело chB1 (далее в настоящем описании также называемое «chB1»), полученное из антитела мыши В1 к CLDN6 человека, но не ограничиваются им. Примеры антитела chB1 с точки зрения аминокислотной последовательности могут включать, но не ограничиваются ими, антитело, содержащее тяжелую цепь, имеющую аминокислотную последовательность, состоящую из аминокислотных остатков 20-471 SEQ ID NO: 32 (фигура 24) в перечне последовательностей, и легкую цепь, имеющую аминокислотную последовательность, состоящую из аминокислотных остатков 21-234 SEQ ID NO: 28 (фигура 22) в перечне последовательностей.
В последовательности тяжелой цепи, представленной SEQ ID NO: 32 (фигура 24) в перечне последовательностей, аминокислотная последовательность, состоящая из аминокислотных остатков 1-19, представляет собой сигнальную последовательность, аминокислотная последовательность, состоящая из аминокислотных остатков 20-141, представляет собой вариабельную область тяжелой цепи, и аминокислотная последовательность, состоящая из аминокислотных остатков 142-471, представляет собой константную область тяжелой цепи. В последовательности легкой цепи, представленной SEQ ID NO: 28 (фигура 22) в перечне последовательностей, аминокислотная последовательность, состоящая из аминокислотных остатков 1-20, представляет собой сигнальную последовательность, аминокислотная последовательность, состоящая из аминокислотных остатков 21-127, представляет собой вариабельную область легкой цепи, и аминокислотная последовательность, состоящая из аминокислотных остатков 128-234, представляет собой константную область легкой цепи.
Аминокислотные последовательности вариабельных областей тяжелой цепи и легкой цепи антитела chB1 соответственно представлены SEQ ID NO: 34 (фигура 25) и SEQ ID NO: 30 (фигура 23) в перечне последовательностей.
Аминокислотная последовательность тяжелой цепи антитела chB1 кодируется последовательностью нуклеотидов, представленной SEQ ID NO: 33 (фигура 24) в перечне последовательностей. Нуклеотидная последовательность, состоящая из нуклеотидных остатков 1-57 нуклеотидной последовательности, представленной SEQ ID NO: 33 в перечне последовательностей, кодирует сигнальную последовательность тяжелой цепи антитела chB1, нуклеотидная последовательность, состоящая из нуклеотидных остатков 58-423 нуклеотидной последовательности, представленной SEQ ID NO: 33 в перечне последовательностей, кодирует вариабельную область тяжелой цепи антитела chB1, и нуклеотидная последовательность, состоящая из нуклеотидных остатков 424-1413 нуклеотидной последовательности, представленной SEQ ID NO: 33 в перечне последовательностей, кодирует константную область тяжелой цепи антитела chB1.
Нуклеотидная последовательность для вариабельной области тяжелой цепи антитела chB1 представлена SEQ ID NO: 35 (фигура 25) в перечне последовательностей.
Аминокислотная последовательность легкой цепи антитела chB1 кодируется нуклеотидной последовательностью, представленной SEQ ID NO: 29 (фигура 22) в перечне последовательностей. Нуклеотидная последовательность, состоящая из нуклеотидных остатков 26-85 нуклеотидной последовательности, представленной SEQ ID NO: 29 в перечне последовательностей, кодирует сигнальную последовательность легкой цепи антитела chB1, нуклеотидная последовательность, состоящая из нуклеотидных остатков 86-406 нуклеотидной последовательности, представленной SEQ ID NO: 29 в перечне последовательностей, кодирует вариабельную область легкой цепи антитела chB1, и нуклеотидная последовательность, состоящая из нуклеотидных остатков 407-727 нуклеотидной последовательности, представленной SEQ ID NO: 29 в перечне последовательностей, кодирует константную область легкой цепи антитела chB1.
Нуклеотидная последовательность для вариабельной области легкой цепи антитела chB1 представлена SEQ ID NO: 31 (фигура 23) в перечне последовательностей. (2) Гуманизированное антитело
Примеры гуманизированного антитела могут включать, но не ограничиваются ими, антитело, полученное путем включения только областей, определяющих комплементарность (CDR), в антитело человека (см. Nature (1986) 321, р. 522-525), антитело, полученное путем прививки части аминокислотных остатков каркасной области, а также последовательностей CDR в антитело человека с помощью способа прививки CDR (WO 90/07861), и антитело, в котором часть аминокислотных последовательностей CDR была модифицирована с сохранением связывающей способности в отношении антигена.
Однако если гуманизированное антитело получено из антитела В1 или антитела СТ, то указанное гуманизированное антитело может представлять собой любое гуманизированное антитело, без ограничения конкретным гуманизированным антителом, которое сохраняет все шесть последовательностей CDR антитела В1 или антитела С1 и обладает CLDN6-связывающей активностью, и помимо этого гуманизированное антитело может представлять собой любое гуманизированное антитело, без ограничения конкретным гуманизированным антителом, таким образом, что его вариант гуманизированного антитела, в котором от одной до нескольких (предпочтительно одна или две, более предпочтительно одна) аминокислотных последовательностей CDR были модифицированы, а также распознает белок CLDN6, или обладает связывающей активностью исходного антитела в отношении белка CLDN6.
Примеры гуманизированного антитела к CLDN6 согласно настоящему изобретению или его функционального фрагмента могут включать, но не ограничиваются ими, антитело, содержащее тяжелую цепь, имеющую вариабельную область, содержащую:
CDRH1, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 9 (фигура 15) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности;
CDRH2, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 10 (фигура 15) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности; и
CDRH3, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 11 (фигура 15) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности; и
легкую цепь, имеющую вариабельную область, содержащую:
CDRL1, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 5 (фигура 13) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности;
CDRL2, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 6 (фигура 13) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности; и
CDRL3, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 7 (фигура 13) в перечне последовательностей, или аминокислотной последовательности, полученной путем замены одной или нескольких (предпочтительно одной или двух) аминокислот в указанной выше аминокислотной последовательности, и
распознающее белок CLDN6 согласно настоящему изобретению или сохраняющее связывающую активность антитела в отношении белка CLDN6, или функциональный фрагмент указанного антитела.
Предпочтительные примеры аминокислотной замены в CDR в гуманизированном антителе к CLDN6 или его функциональном фрагменте могут включать, но не ограничиваются ими, замену одной или нескольких (предпочтительно одной или двух) аминокислот в CDRL3, как описано выше, и примером этого является CDRL3, представленная SEQ ID NO: 8 (фигура 14) в перечне последовательностей, которую получают путем замены аминокислотных остатков 4 и 5 SEQ ID NO: 7 в перечне последовательностей.
[0134]
Примеры вариабельной области тяжелой цепи гуманизированного антитела, содержащей описанные выше CDRH, могут включать, но не ограничиваются ими, аминокислотную последовательность, представленную SEQ ID NO: 54 (фигура 35) в перечне последовательностей, аминокислотную последовательность, представленную SEQ ID NO: 58 (фигура 37) в перечне последовательностей, и аминокислотную последовательность, представленную SEQ ID NO: 62 (фигура 39) в перечне последовательностей, и примеры вариабельной области легкой цепи гуманизированного антитела, содержащей описанные выше CDRL, могут включать, но не ограничиваются ими, аминокислотную последовательность, представленную SEQ ID NO: 38 (фигура 27) в перечне последовательностей, аминокислотную последовательность, представленную SEQ ID NO: 42 (фигура 29) в перечне последовательностей, и аминокислотную последовательность, представленную SEQ ID NO: 46 (фигура 31) в перечне последовательностей.
[0135]
Предпочтительные примеры гуманизированных антител, содержащих комбинацию указанных выше вариабельной области тяжелой цепи и вариабельной области легкой цепи, могут включать, но не ограничиваются ими:
гуманизированное антитело, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 54 (фигура 35) в перечне последовательностей, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 38 (фигура 27) в перечне последовательностей;
гуманизированное антитело, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 58 (фигура 37) в перечне последовательностей, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 42 (фигура 29) в перечне последовательностей;
гуманизированное антитело, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 54 (фигура 35) в перечне последовательностей, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 46 (фигура 31) в перечне последовательностей;
гуманизированное антитело, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 58 (фигура 37) в перечне последовательностей, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 50 (фигура 33) в перечне последовательностей; и
гуманизированное антитело, содержащее вариабельную область тяжелой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 62 (фигура 39) в перечне последовательностей, и вариабельную область легкой цепи, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 46 (фигура 31) в перечне последовательностей.
Примеры полноразмерных последовательностей гуманизированных антител, содержащих комбинацию указанных выше вариабельной области тяжелой цепи и вариабельной области легкой цепи, могут включать, но не ограничиваются ими:
гуманизированное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-471 SEQ ID NO: 52 (фигура 34) в перечне последовательностей, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 36 (фигура 26) в перечне последовательностей (H1L1);
гуманизированное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-471 SEQ ID NO: 56 (фигура 36) в перечне последовательностей, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 40 (фигура 28) в перечне последовательностей (H2L2);
гуманизированное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-471 SEQ ID NO: 52 (фигура 34) в перечне последовательностей, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 44 (фигура 30) в перечне последовательностей (H1L3);
гуманизированное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-471 SEQ ID NO: 56 (фигура 36) в перечне последовательностей, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 48 (фигура 32) в перечне последовательностей (H2L4); и
гуманизированное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-471 SEQ ID NO: 60 (фигура 38) в перечне последовательностей, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 44 (фигура 30) в перечне последовательностей (H3L3).
В аминокислотной последовательности тяжелой цепи, представленной SEQ ID NO: 52 (фигура 34), 56 (фигура 36) или 60 (фигура 38) в перечне последовательностей, аминокислотная последовательность, состоящая из аминокислотных остатков 1-19, представляет собой сигнальную последовательность, аминокислотная последовательность, состоящая из аминокислотных остатков 20-141, представляет собой вариабельную область тяжелой цепи, и аминокислотная последовательность, состоящая из аминокислотных остатков 142-471, представляет собой константную область тяжелой цепи.
В аминокислотной последовательности легкой цепи, представленной SEQ ID NO: 36 (фигура 26), 40 (фигура 28), 44 (фигура 30) или 48 (фигура 32), аминокислотная последовательность, состоящая из аминокислотных остатков 1-20, представляет собой сигнальную последовательность, аминокислотная последовательность, состоящая из аминокислотных остатков 21-127, представляет собой вариабельную область легкой цепи, и аминокислотная последовательность, состоящая из аминокислотных остатков 128-234, представляет собой константную область легкой цепи.
[0137]
Нуклеотидная последовательность, кодирующая аминокислотную последовательность тяжелой цепи гуманизированного антитела H1L1, и нуклеотидная последовательность, кодирующая аминокислотную последовательность легкой цепи гуманизированного антитела H1L1, представляют собой полинуклеотид, представленный SEQ ID NO: 53 (фигура 34), и полинуклеотид, представленный SEQ ID NO: 37 (фигура 26), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность тяжелой цепи гуманизированного антитела H2L2, и нуклеотидная последовательность, кодирующая аминокислотную последовательность легкой цепи гуманизированного антитела H2L2, представляют собой полинуклеотид, представленный SEQ ID NO: 57 (фигура 36), и полинуклеотид, представленный SEQ ID NO: 41 (фигура 28), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность тяжелой цепи гуманизированного антитела H1L3, и нуклеотидная последовательность, кодирующая аминокислотную последовательность легкой цепи гуманизированного антитела H1L3, представляют собой полинуклеотид, представленный SEQ ID NO: 53 (фигура 34), и полинуклеотид, представленный SEQ ID NO: 45 (фигура 30), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность тяжелой цепи гуманизированного антитела H2L4, и нуклеотидная последовательность, кодирующая аминокислотную последовательность легкой цепи гуманизированного антитела H2L4, представляют собой полинуклеотид, представленный SEQ ID NO: 57 (фигура 36), и полинуклеотид, представленный SEQ ID NO: 49 (фигура 32), соответственно; и
нуклеотидная последовательность, кодирующая аминокислотную последовательность тяжелой цепи гуманизированного антитела H3L3, и нуклеотидная последовательность, кодирующая аминокислотную последовательность легкой цепи гуманизированного антитела H3L3, представляют собой полинуклеотид, представленный SEQ ID NO: 61 (фигура 38), и полинуклеотид, представленный SEQ ID NO: 45 (фигура 30), соответственно.
Нуклеотидная последовательность, кодирующая аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела HIL1, и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи гуманизированного антитела H1L1, представляют собой полинуклеотид, представленный SEQ ID NO: 55 (фигура 35), и полинуклеотид, представленный SEQ ID NO: 39 (фигура 27), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела H2L2, и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи гуманизированного антитела H2L2, представляют собой полинуклеотид, представленный SEQ ID NO: 59 (фигура 37), и полинуклеотид, представленный SEQ ID NO: 43 (фигура 29), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела H1L3, и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи гуманизированного антитела H1L3, представляют собой полинуклеотид, представленный SEQ ID NO: 55 (фигура 35), и полинуклеотид, представленный SEQ ID NO: 47 (фигура 31), соответственно;
нуклеотидная последовательность, кодирующая аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела H2L4, и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи гуманизированного антитела H2L4, представляют собой полинуклеотид, представленный SEQ ID NO: 59 (фигура 37), и полинуклеотид, представленный SEQ ID NO: 51 (фигура 33), соответственно; и
нуклеотидная последовательность, кодирующая аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела H3L3, и нуклеотидная последовательность, кодирующая вариабельную область легкой цепи гуманизированного антитела H3L3, представляют собой полинуклеотид, представленный SEQ ID NO: 63 (фигура 39), и полинуклеотид, представленный SEQ ID NO: 47 (фигура 31), соответственно.
В нуклеотидной последовательности, представленной SEQ ID NO: 53 (фигура 34), 57 (фигура 36) или 61 (фигура 38) в перечне последовательностей, нуклеотидная последовательность, состоящая из нуклеотидных остатков 1-57, кодирует сигнальную последовательность тяжелой цепи гуманизированного антитела, нуклеотидная последовательность, состоящая из нуклеотидных остатков 58-423, кодирует аминокислотную последовательность вариабельной области тяжелой цепи гуманизированного антитела, и нуклеотидная последовательность, состоящая из нуклеотидных остатков 424-1413, кодирует константную область тяжелой цепи антитела.
В нуклеотидной последовательности, представленной SEQ ID NO: 37 (фигура 26), 41 (фигура 28), 45 (фигура 30) или 49 (фигура 32) в перечне последовательностей, нуклеотидная последовательность, состоящая из нуклеотидных остатков 1-60, кодирует сигнальную последовательность легкой цепи гуманизированного антитела, нуклеотидная последовательность, состоящая из нуклеотидных остатков 61-381, кодирует аминокислотную последовательность вариабельной области легкой цепи гуманизированного антитела, и нуклеотидная последовательность, состоящая из нуклеотидных остатков 382-702, кодирует константную область легкой цепи антитела.
[0138]
В том случае, если антитело обладает активностью связывания с CLDN6, любое антитело, которое имеет идентичность или гомологию 80% или выше, предпочтительно 90% или выше, более предпочтительно 95% или выше, еще более предпочтительно 97% или выше, наиболее предпочтительно 99% или выше, с аминокислотной последовательностью любого из антител, содержащих указанные выше комбинации вариабельной области тяжелой цепи и вариабельной области легкой цепи, и антител, содержащих указанные выше комбинации тяжелой цепи и легкой цепи, также включены в определение антитела согласно настоящему изобретению.
В том случае, если оно обладает активностью связывания с CLDN6, любое антитело, которое содержит CDR, состоящие из аминокислотных последовательностей CDR любого из антител, содержащих указанные выше комбинации вариабельной области тяжелой цепи и вариабельной области легкой цепи, и антител, содержащих указанные выше комбинации тяжелой цепи и легкой цепи, где аминокислотная последовательность антитела, исключая аминокислотные последовательности CDR, имеет идентичность или гомологию аминокислот 80% или выше, предпочтительно 90% или выше, более предпочтительно 95% или выше, еще более предпочтительно 97% или выше, наиболее предпочтительно 99% или выше, также включены в определение антитела согласно настоящему изобретению.
Помимо этого, антитело, обладающее биологической активностью, эквивалентной биологической активности каждого из указанных выше антител, может быть выбрано путем объединения аминокислотных последовательностей, полученных путем замены, делеции или добавления одного или нескольких аминокислотных остатков в аминокислотной последовательности тяжелой цепи или легкой цепи. Замена аминокислоты в настоящем описании предпочтительно представляет собой консервативную замену аминокислоты (WO 2013154206).
Консервативная замена аминокислоты представляет собой замену, которая происходит в группе аминокислот с родственными боковыми цепями аминокислот. Такую замену аминокислоты предпочтительно проводят до такой степени, чтобы свойства, характерные для вещества, имеющего исходную аминокислотную последовательность, не уменьшались.
Гомология между двумя аминокислотными последовательностями может быть определена с использованием параметров по умолчанию алгоритма Blast версии 2.2.2 (Altschul, Stephen F., Thomas L.Madden, Alejandro A. Schaaffer, Jinghui Zhang, Zheng Zhang, Webb Miller, and David J. Lipman (1997), "Gapped BLAST and PSI-BLAST: a new generation of protein database search programs", Nucleic Acids Res. 25: 3389-3402)
Алгоритм Blast можно использовать с помощью сайта www.ncbi.nlm.nih.gov/blast в сети Интернет.
(3) Антитело человека
Дополнительно примеры антитела согласно настоящему изобретению могут включать, но не ограничиваются ими, антитела человека, способные связываться с CLDN6 и/или CLDN9. Антитело человека к CLDN6 и/или CLDN9 относится к антителу человека, имеющему только последовательность гена антитела, полученную из хромосомы человека. Антитело человека к CLDN6 может быть получено с применением способа с использованием мыши, продуцирующей антитело человека, имеющей фрагмент хромосомы человека, содержащий гены тяжелой цепи и легкой цепи антитела человека (см. Nature Genetics (1997) 16, p. 133-143; Nucl. Acids Res. (1998) 26, p.3447-3448; Animal Cell Technology: Basic and Applied Aspects vol. 10, p. 69-73, Kluwer Academic Publishers, 1999; Proc. Natl. Acad. Sci. USA (2000) 97, p. 722-727 и так далее).
В частности, такая мышь, продуцирующая антитело человека, может быть создана путем получения нокаутного животного или трансгенного животного в качестве генетически рекомбинантного животного с разрушенными локусами генов для тяжелой цепи и легкой цепи эндогенного иммуноглобулина, с введенными на их место локусами генов для тяжелой цепи и легкой цепи иммуноглобулина человека, например, через вектор дрожжевой искусственной хромосомы (YAC), и скрещивания таких животных.
В качестве альтернативы, такое антитело может быть получено следующим образом: эукариотическую клетку подвергают трансформации кДНК, кодирующей тяжелую цепь и легкую цепь антитела человека, предпочтительно вектором, содержащим указанную кДНК, с помощью методики рекомбинации генов, и трансформированную клетку, продуцирующую генетически рекомбинантное моноклональное антитело человека, культивируют, и из культурального супернатанта получают антитело.
Например, в качестве хозяина может быть использована эукариотическая клетка, предпочтительно клетка млекопитающего, такая как клетка СНО, лимфоцит и клетка миеломы.
Помимо этого, известен способ получения антитела человека на основе фагового дисплея, выбранного из библиотеки антител человека (см. Investigative Ophthalmology & Visual Science (2002) 43 (7), p. 2301-2308; Briefings in Functional Genomics and Proteomics (2002), 1 (2), p. 189-203; Ophthalmology (2002) 109 (3), p. 427-431, и так далее).
Например, может быть применен метод фагового дисплея (Nature Biotechnology (2005), 23, (9), p. 1105-1116), в котором вариабельная область антитела человека экспрессируется в виде одноцепочечного антитела (scFv) на поверхностях фагов, и проводят отбор фагов, которые связываются с антигеном.
Анализ генов фага, отобранных по критерию связывания с антигеном, позволяет определить последовательность ДНК, кодирующую вариабельную область антитела человека, которая связывается с антигеном.
После выяснения последовательности ДНК scFv, который связывается с антигеном, антитело человека может быть получено путем получения вектора экспрессии, содержащего указанную последовательность, и введения полученного вектора экспрессии в подходящего хозяина для экспрессии (WO 92/01047, WO 92/20791, WO 93/06213, WO 93/11236, WO 93/19172, WO 95/01438, WO 95/15388, Annu. Rev. Immunol (1994) 12, р. 433-455, Nature Biotechnology (2005) 23(9), p. 1105-1116)
[0139]
Химерные антитела, гуманизированное антитела, антитела человека и так далее, полученные с применением указанного выше способа, могут быть оценены в отношении активности связывания с антигеном, например, с применением известного способа скрининга для выявления предпочтительного антитела.
Другим примером показателей при сравнении характеристик антител является стабильность антител. Дифференциальный сканирующий калориметр (ДСК) представляет собой устройство, способное быстро и точно определить средние точки термической денатурации (Tm), хороший показатель относительной структурной стабильности белка. Различия в термической стабильности можно сравнить путем сравнения значений Tm, определенных с помощью ДСК. Известно, что стабильность антител при хранении до некоторой степени коррелирует с термической стабильностью антител (Pharmaceutical Development and Technology (2007) 12, p.265-273), и, следовательно, термическая стабильность может быть применена в качестве показателя для скрининга с целью выявления предпочтительного антитела. Примеры других показателей для скрининга антител могут включать, но не ограничиваются ими, высокий выход в соответствующих клетках-хозяевах и низкую способность к агглютинации в водном растворе. Необходимо проводить скрининг с целью выявления наиболее подходящего антитела для введения людям посредством всестороннего определения, основанного на описанных выше показателях, поскольку, например, антитело с самым высоким выходом не обязательно проявляет наибольшую термическую стабильность.
[0140]
Антитело согласно настоящему изобретению включает «антитела, которые связываются с сайтом, с которым связывается антитело к CLDN6, предложенное в настоящем изобретении». То есть настоящее изобретение включает антитела, которые связываются с сайтом на белке CLDN6, который распознает В1 или С7 согласно настоящему изобретению.
[0141]
Антитело согласно настоящему изобретению включает модифицированные варианты антитела. Модифицированный вариант относится к варианту, полученному путем воздействия на антитело согласно настоящему изобретению, приводящего к химической или биологической модификации. Примеры химически модифицированного варианта могут включать, но не ограничиваются ими, варианты, включающие связывание химического фрагмента с аминокислотным скелетом, и варианты с химической модификацией N-связанной или О-связанной углеводной цепи. Примеры биологически модифицированного варианта могут включать, но не ограничиваются ими, варианты, полученные путем посттрансляционной модификации (например, N-связанного или О-связанного гликозилирования, процессинга N- концевой или С-концевой части, деамидирования, изомеризации аспарагиновой кислоты, окисления метионина), и варианты, в которых остаток метионина был добавлен к N-концу путем экспрессии в прокариотической клетке-хозяине. Помимо этого, антитело, меченное таким образом, чтобы обеспечить обнаружение или выделение антитела согласно настоящему изобретению или антигена, например, меченное ферментом антитело, флуоресцентно меченное антитело и аффинно меченное антитело, также включены в определение модифицированного варианта. Такой модифицированный вариант антитела согласно настоящему изобретению пригоден для применения для улучшения стабильности и сохранения антитела в крови, снижения его антигенности, обнаружения или выделения антитела или антигена, и так далее.
Помимо этого, путем регулирования модификации гликана, который связан с антителом согласно настоящему изобретению (гликозилирование, дефукозилирование и так далее), может быть усилена антитело-зависимая клеточная цитотоксическая активность. В качестве методики регулирования модификации антител известны источники WO 1999/54342, WO 2000/61739, WO 2002/31140 и так далее. Однако указанная методика не ограничивается ими. В определение антитела согласно настоящему изобретению также включены антитела, в которых регулируют модификацию гликана.
Такая модификация может быть применена в любом положении или в желаемом положении антитела или функционального фрагмента антитела, и один и тот же тип, или два, или более различных типов модификаци могут быть применены в одном, или двух, или более положениях.
В настоящем изобретении значение «модифицированного варианта фрагмента антитела» также включает «фрагмент модифицированного варианта антитела».
[0142]
Если ген антитела временно выделяют и затем вводят в подходящего хозяина для получения антитела, может быть применена подходящая комбинация хозяина и вектора экспрессии. Конкретные примеры гена антитела могут включать, но не ограничиваются ими, комбинацию гена, кодирующего последовательность тяжелой цепи, или тому подобного, антитела, описанного в настоящем описании, и гена, кодирующего последовательность легкой цепи, или тому подобного, антитела, описанного в настоящем описании. Для трансформации клеток-хозяев ген последовательности тяжелой цепи или тому подобное и ген последовательности легкой цепи или тому подобное могут быть вставлены в один и тот же вектор экспрессии или вставлены в отдельные векторы экспрессии.
Если в качестве хозяина используют эукариотические клетки, могут быть применены клетки животных, растительные клетки и эукариотические микроорганизмы. В частности, примеры клеток животных могут включать, но не ограничиваются ими, клетки млекопитающих, такие как клетки COS (Cell (1981) 23, p. 175-182, АТСС CRL-1650), клетки обезьяны, фибробласты мыши NIH3T3 (АТСС №CRL-1658), штамм с дефицитом дигидрофолатредуктазы (Proc. Natl. Acad. Sci. U.S.A. (1980) 77, p. 4126-4220) клеток яичника китайского хомячка (клетки СНО, АТСС CCL-61) и клетки FreeStyle 293F (Invitrogen).
Если используют прокариотические клетки, могут быть применены, например, Escherichia coli или Bacillus subtilis.
Ген целевого антитела вводят в эти клетки путем трансформации, и трансформированные клетки культивируют in vitro с получением антитела. Различие в последовательностях антител может приводить к различным выходам в культуре, и, следовательно, антитела, которые обеспечивают возможность легкого получения лекарственного средства, может быть отделены от антител, имеющих эквивалентную активность связывания, при использовании выходов в качестве индикатора. Соответственно, антитело согласно настоящему изобретению включает антитела, полученные с применением способа получения антитела, включающего стадии: культивирования трансформированной клетки-хозяина и сбора целевого антитела или функционального фрагмента антитела из культуры, полученной на стадии культивирования.
[0143]
Ген антитела предпочтительно представляет собой полинуклеотид, содержащий полинуклеотид, описанный в любом из пунктов (а)-(е):
(a) комбинация полинуклеотид а, кодирующего аминокислотную последовательность тяжелой цепи, и полинуклеотида, кодирующего аминокислотную последовательность легкой цепи антитела любого из антител В1 или С7, антитела chB1 и гуманизированных антител H1L1, H2L2, H1L3, H2L4 и H3L3;
(b) комбинация полинуклеотида, кодирующего аминокислотную последовательность тяжелой цепи, содержащую последовательности CDRH1-CDRH3, и полинуклеотида, кодирующего аминокислотную последовательность легкой цепи, содержащую последовательности CDRL1-CDRL3 антитела любого из антител В1 или С7, антитела chB1 и гуманизированных антител H1L1, H2L2, H1L3, H2L4 и H3L3;
(c) комбинация полинуклеотида, кодирующего аминокислотную последовательность тяжелой цепи, содержащую аминокислотную последовательность вариабельной области тяжелой цепи, и полинуклеотида, кодирующего аминокислотную последовательность легкой цепи, содержащую аминокислотную последовательность вариабельной области легкой цепи антитела любого из антител В1 или С7, антитела chB1 и гуманизированных антител H1L1, H2L2, H1L3, H2L4 и H3L3;
(d) полинуклеотид, который способен к гибридизации с нуклеотидами, состоящими из полинуклеотида, комплементарного полинуклеотиду по любому из пунктов (а)-(с), в жестких условиях и кодирует аминокислотную последовательность антитела, способного связываться с CDLN6; и
(e) полинуклеотид, кодирующий аминокислотную последовательность полипептида, полученного путем замены, делеции, добавления или вставки от 1 до 50, от 1 до 45, от 1 до 40, от 1 до 35, от 1 до 30, от 1 до 25, от 1 до 20, от 1 до 15, от 1 до 10, от одной до восьми, от одной до шести, от одной до пяти, от одной до четырех, от одной до трех, одной или двух, или одной аминокислоты (аминокислот) в полинуклеотиде по любому из пп. (а)-(с), и кодирующий аминокислотную последовательность антитела, способного связываться с CDLN6.
Настоящее изобретение включает нуклеотид, кодирующий антитело согласно настоящему изобретению, или функциональный фрагмент указанного антитела, или модифицированный вариант антитела или функционального фрагмента; рекомбинантный вектор, содержащий встроенный в него ген; и клетку, содержащую введенный в нее ген или вектор.
Настоящее изобретение включает способ получения антитела или функционального фрагмента антитела, или модифицированного варианта антитела или функционального фрагмента, включающий стадии: культивирования клетки и сбора из культуры антитела, или функционального фрагмента антитела, или модифицированного варианта антитела или функционального фрагмента.
Известно, что остаток лизина на карбоксильном конце тяжелой цепи антитела, продуцируемого в культивируемой клетке млекопитающего, подвергается делеции (Journal of Chromatography А, 705: 129-134 (1995)), и также известно, что два аминокислотных остатка, глицин и лизин, на карбоксильном конце тяжелой цепи антитела, продуцируемого в культивируемой клетке млекопитающего, подвергаются делеции, и остаток пролина, вновь расположенный на карбоксильном конце, подвергается амидированию (Analytical Biochemistry, 360: 75-83 (2007)). Однако такая делеция и модификация последовательности тяжелой цепи не влияют на антигенсвязывающую способность и эффекторную функцию (активацию комплемента, антитело-зависимую клеточную цитотоксичность и так далее) антитела. Таким образом, в определение антитела согласно настоящему изобретению также включены антитела, подвергшиеся такой модификации, и функциональные фрагменты антитела, и также включены варианты, подвергшиеся делеции, в которых одна или две аминокислоты на карбоксильном конце тяжелой цепи были удалены, варианты, полученные путем амидирования вариантов, подвергшихся делеции (например, тяжелая цепь, в которой остаток пролина на карбоксильном конце был амидирован), и тому подобное. Тип вариантов, подвергшихся делеции, имеющих делецию на карбоксильном конце тяжелой цепи антитела согласно настоящему изобретению, не ограничивается указанными выше вариантами при условии, что антигенсвязывающая способность и эффекторная функция сохраняются. Две тяжелые цепи, составляющие антитело согласно настоящему изобретению, могут принадлежать к одному типу, выбранному из группы, состоящей из полноразмерной тяжелой цепи и описанного выше варианта, подвергшегося делеции, или могут принадлежать к двум выбранным из них типам в комбинации. На отношение количеств каждого варианта, подвергшегося делеции, может влиять тип культивируемых клеток млекопитающих, которые продуцируют антитело согласно настоящему изобретению, и условия культивирования; однако антитело, в котором один аминокислотный остаток на карбоксильном конце был удален в обеих из двух тяжелых цепей в антителе согласно настоящему изобретению, может предпочтительно являться примером основного компонента молекул антитела.
[0145]
Примеры изотипов антитела к CLDN6 согласно настоящему изобретению могут включать, но не ограничиваются ими, IgG (IgG1, IgG2, IgG3, IgG4), и их предпочтительные примеры включают IgG1, IgG2 и IgG4.
Если в качестве изотипа антитела согласно настоящему изобретению используют IgG1, эффекторную функцию можно регулировать путем замены некоторых аминокислотных остатков в константной области. Примеры вариантов IgG1 с пониженной или ослабленной эффекторной функцией могут включать, но не ограничиваются ими, IgG1 LALA (IgG1-L234A, L235A) и IgG1 LAGA (IgG1-L235A, G237A), и предпочтительным вариантом IgG1 является IgG1 LALA. L234A, L235A указывает на замену лейцина на аланин в положениях 234 и 235, указанных нумерацией в соответствии с индексом EU (Proc. Natl. Acad. Sci. U.S.A., Vol. 63, No. 1 (May 15, 1969), pp. 78-85), и G237A указывает на замену глицина на аланин в положении 237, указанном нумерацией в соответствии с индексом EU.
[0146]
Типичные примеры биологической активности антител могут включать, но не ограничиваются ими, антигенсвязывающую активность, активность интернализации в клетки, экспрессирующие антиген, посредством связывания с антигеном, способность к нейтрализации активности антигена, способность к усилению активности антигена, антитело-зависимую клеточную цитотоксичность (ADCC), комплемент-зависимую цитотоксичность (CDC) и антитело-зависимый клеточный фагоцитоз (ADCP), и функцией антитела согласно настоящему изобретению является активность связывания с CLDN6, и предпочтительно активность интернализации в клетки, экспрессирующие CLDN6, посредством связывания с CLDN6. Помимо активности интернализации в клетки, антитело согласно настоящему изобретению может обладать активностями ADCC, CDC и/или ADCP в комбинации.
[0147]
Полученное антитело может быть очищено до гомогенного состояния. Для разделения/очистки антител могут быть применены способы разделения/очистки, обычно используемые для белка. Например, антитело может быть отделено/очищено с помощью подходящего выбора и объединения колоночной хроматографии, фильтрации на фильтре, ультрафильтрации, высаливания, диализа, препаративного электрофореза в полиакриламидном геле, изоэлектрического фокусирования и так далее (Strategies for Protein Purification and Characterization: A Laboratory Course Manual, Daniel R. Marshak et al. eds., Cold Spring Harbor Laboratory Press (1996); Antibodies: A Laboratory Manual. Ed Harlow and David Lane, Cold Spring Harbor Laboratory (1988)), однако способы разделения/очистки не ограничиваются ими.
Примеры хроматографии могут включать, но не ограничиваются ими, аффинную хроматографию, ионообменную хроматографию, гидрофобную хроматографию, гельфильтрационную хроматографию, обращенно-фазовую хроматографию и адсорбционную хроматографию.
Эти типы хроматографии могут быть выполнены методами жидкостной хроматографии, такими как ВЭЖХ и жидкостная хроматография быстрого разрешения (FPLC).
Примеры колонок для аффинной хроматографии могут включать, но не ограничиваются ими, колонку с белком А и колонку с белком G.
В качестве альтернативы, антитело может быть очищено с использованием связывающей активности в отношении антигена: с помощью носителя, на котором иммобилизован антиген.
[0148]
Желательно, чтобы антитело к HER2 согласно настоящему изобретению представляло собой антитело, которое имеет, например, какое-либо из следующих свойств, но антитело к HER2 не ограничивается ими.
(1) Антитело к HER2, обладающее следующими свойствами:
(a) специфическое связывание с HER2; и
(b) интернализация в клетки, экспрессирующие HER2, посредством связывания с HER2.
(2) Антитело по п. (1), связывающееся с внеклеточным доменом HER2.
(3) Антитело по пп. (1) или (2), представляющее собой моноклональное антитело.
(4) Антитело по любому из пп. (1)-(3), обладающее активностями или активностью антитело-зависимой клеточной цитотоксичности (ADCC) и/или комплемент-зависимой цитотоксичности (CDC).
(5) Антитело по любому из пп. (1)-(4), представляющее собой моноклональное антитело мыши, химерное моноклональное антитело или гуманизированное моноклональное антитело.
(6) Антитело по любому из пп. (1)-(3), где константная область тяжелой цепи представляет собой константную область тяжелой цепи IgG1 человека и содержит мутацию, которая вызывает снижение активностей или активности ADCC и/или CDC.
(7) Антитело по п. (6), где константная область тяжелой цепи представляет собой константную область тяжелой цепи IgG1 человека, и лейцин в положениях 234 и 235 согласно нумерации в соответствии с индексом EU заменен на аланин.
(8) Антитело по любому из пп. (1)-(4), представляющее собой гуманизированное моноклональное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 65, и легкую цепь, состоящую из аминокислотной последовательности, представленной SEQ ID NO: 64.
(9) Антитело по любому из пи. (1)-(3), (6) и (7), представляющее собой гуманизированное моноклональное антитело, содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-469 SEQ ID NO: 75, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 73.
(10) Антитело по любому из пп. (1)-(9), где одна или две аминокислоты на карбоксильном конце тяжелой цепи подвергаются делеции.
(11) Антитело по любому из пп. (1)-(3), (8) и (10), содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 1-449 SEQ ID NO: 65, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 1-214 SEQ ID NO: 64.
(12) Антитело по любому из пп. (1)-(3), (6), (7), (9) и (10), содержащее тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20-468 SEQ ID NO: 75, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21-234 SEQ ID NO: 73.
(13) Антитело, полученное с применением способа получения антитела по любому из пп. (1)-(12), включающего стадии культивирования клетки-хозяина, трансформированной с применением вектора экспрессии, содержащего полинуклеотид, кодирующий указанное антитело; и сбора целевого антитела из культуры, полученной на стадии культивирования.
[0149]
<Ремоделирование гликанов>
Недавно был описан способ ремоделирования гетерогенного гликопротеина антитела с помощью ферментативной реакции или тому подобного для обеспечения гомогенного введения гликана, имеющего функциональную группу (ACS Chemical Biology 2012, 7, 110, ACS Medicinal Chemistry Letters 2016, 7, 1005). Была предпринята попытка сайт-специфического введения лекарственного средства для синтеза гомогенного ADC с применением этой методики ремоделирования гликана (Bioconjugate Chemistry 2015, 26, 2233, Angew. Chem. Int. Ed. 2016, 55, 2361-2367, US. 2016361436).
[0150]
При ремоделировании гликанов согласно настоящему изобретению с использованием гидролазы гетерогенные гликаны, добавленные к белку (например, антителу), отщепляются, и остается только GlcNAc на каждом конце, вследствие этого получают гомогенный белковый фрагмент с GlcNAc (далее в настоящем описании называемый «акцептором»). Затем обеспечивают отдельно приготовленный произвольно выбранный гликан (далее в настоящем описании называемой «донором»), и акцептор и донор соединяют с помощью трансгликозидазы. Таким образом может быть синтезирован гомогенный гликопротеин с произвольно выбранной структурой гликана.
[0151]
В настоящем изобретении «гликан» относится к структурной единице из двух или более моносахаридов, связанных вместе посредством гликозидных связей. Конкретные моносахариды и гликаны в ряде случаев сокращенно обозначают, например, как «GlcNAc-», «MSG-» и так далее. Когда любое из этих сокращений используют в структурной формуле, указанное сокращение приведено с намерением показать, что атом кислорода или атом азота у восстанавливающего конца, участвующий в гликозидной связи с другой структурной единицей, не включен в сокращение, обозначающее гликан, если это не определено конкретно.
[0152]
В настоящем изобретении моносахарид в качестве основной единицы гликана указан для удобства таким образом, что в структуре кольца положение атома углерода, связывающегося с атомом кислорода, входящего в состав кольца, и непосредственно связывающегося с гидроксигруппой (или атомом кислорода, участвующим в гликозидной связи), определено как положение 1 (положение 2 только для сиаловых кислот), если не указано иное. Названия соединений в примерах приведены с учетом химической структуры в целом, и это правило не обязательно применяется.
[0153]
Когда гликан указан в виде знака (например, GLY, SG, MSG, GlcNAc) в настоящем изобретении, предполагается, что этот знак, если не указано иное, включает атомы углерода, расположенные по порядку по направлению к восстанавливающему концу, и не включает N или О, в участвующие в образовании N- или О-гликозидной связи.
[0154]
В настоящем изобретении, если не указано конкретно, частичная структура, когда гликан связывается с боковой цепью аминокислоты, указывается таким образом, что часть боковой цепи указывается в скобках, например, «(SG-)Asn».
[0155]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению представлен следующей формулой:
[Формула 82]
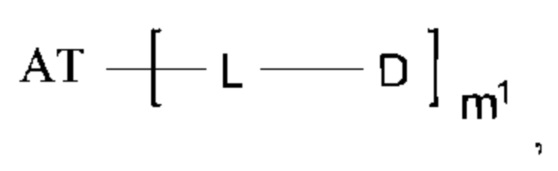
где антитело AT или функциональный фрагмент указанного антитела может связываться с L непосредственно через боковую цепь его аминокислотного остатка (например, цистеина, лизина), или связываться с L через гликан или ремоделированный гликан AT, и предпочтительно связывается с L через гликан или ремоделированный гликан AT, и более предпочтительно связывается с L через ремоделированный гликан AT.
[0156]
Гликаны в AT согласно настоящему изобретению представляют собой N-связанные гликаны или О-связанные гликаны, и предпочтительно N-связанные гликаны.
N-связанные гликаны и О-связанные гликаны связываются с боковой цепью аминокислоты антитела посредством N-гликозидной связи и О-гликозидной связи, соответственно.
[0157]
Ab согласно настоящему изобретению представляет собой IgG, и предпочтительно IgG1, IgG2 или IgG4.
[0158]
IgG содержит высококонсервативный N-связанный гликан при остатке аспарагина в положении 297 Fc-фрагмента тяжелой цепи (далее в настоящем описании называемом «Asn297» или «N297»), и известно, что указанный N-связанный гликан вносит вклад в активность и кинетику молекулы антитела. (Biotechnol. Prog., 2012, 28, 608-622, Sanglier-Cianferani, S., Anal. Chem., 2013, 85, 715-736.)
[0159]
Аминокислотная последовательность в константной области IgG высококонсервативна, и каждая аминокислота определена согласно нумерации в соответствии с индексом EU согласно источнику Edelman et al. (Proc. Natl. Acad. Sci. U.S.A., Vol. 63, No. 1 (May 15, 1969), pp. 78-85). Например, Asn297, к которому добавлен N-связанный гликан в Fc-фрагменте, соответствует положению 297 в нумерации в соответствии с индексом EU, и каждая аминокислота однозначно определяется нумерацией в соответствии с индексом EU, даже если фактическое положение аминокислоты изменилось вследствие фрагментации молекулы или делеции области.
[0160]
В коньюгате антитело-лекарстве иное средство согласно настоящему изобретению антитело или функциональный фрагмент указанного антитела более предпочтительно связывается с L через гликан, связывающийся с боковой цепью его Asn297 (далее в настоящем описании называемый «N297-гликан»), и антитело или функциональный фрагмент указанного антитела еще более предпочтительно связывается с L через N297-гликан, где указанный N297-гликан представляет собой ремоделированный гликан.
Следующая формула иллюстрирует ситуацию, когда конъюгат антитело-лекарственное средство согласно настоящему изобретению или функциональный фрагмент указанного антитела связывается с L через N297-гликан.
[Формула 83]
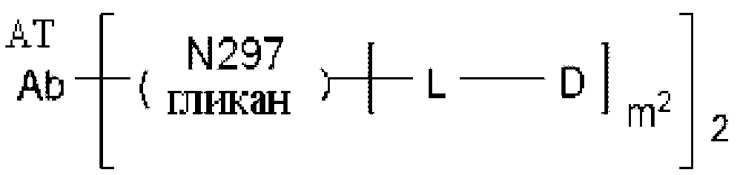
Антитело, содержащее ремоделированный гликан, называют антителом с ремоделированным гликаном.
[0161]
SGP (сокращение для сиалилгликопептида) является типичным N-связанным комплексным гликаном. SGP может быть выделен/очищен из желтка куриного яйца, например, с применением способа, описанного в WO 2011/0278681. Очищенные продукты SGP коммерчески доступны (Tokyo Chemical Industry Co., Ltd., FUSHIMI Pharmaceutical Co., Ltd.) и могут быть приобретены. Например, дисиалооктасахарид (Tokyo Chemical Industry Co., Ltd.), гликан, полученный путем удаления одного GlcNAc с восстанавливающего конца во фрагменте гликана SG (далее в настоящем описании называемый «SG (10)»), является коммерчески доступным.
[0162]
В настоящем изобретении структура гликана, полученная путем удаления сиаловой кислоты с невосстанавливающего конца только в одной из разветвленных цепей β-Man в SG (10), называется MSG (9), и структура, содержащая сиаловую кислоту только в разветвленной цепи 1-3, называется MSG1, и структура, содержащая сиаловую кислоту только в разветвленной цепи 1-6, называется MSG2.
[0163]
Ремоделированный гликан согласно настоящему изобретению представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2, или смесь N297-(Fuc)MSG1 и N297-(Fuc)MSG2, или N297-(Fuc)SG, и предпочтительно представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или N297-(Fuc)SG, и более предпочтительно представляет собой N297-(Fuc)MSG1 или N297-(Fuc)MSG2.
[0164]
N297-(Fuc)MSG1 представлен следующей структурной формулой или формулой последовательности:
[Формула 84]
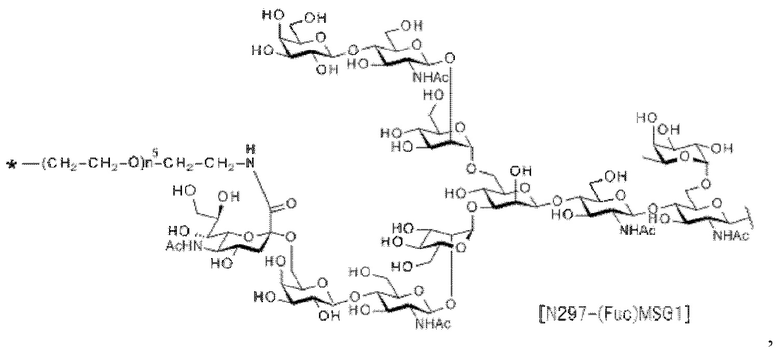
[Формула 85]
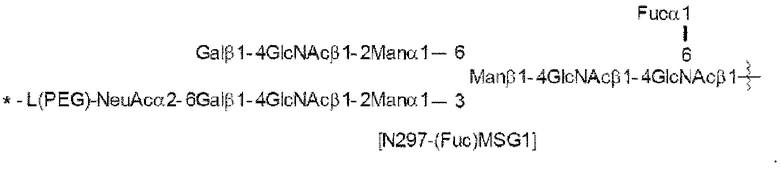
В указанных формулах каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, где аминогруппа на правом конце представляет собой амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в разветвленной цепи 1-3 β-Man в N297-гликане,
каждая звездочка представляет собой связь с линкером L, в частности, с атомом азота в положении 1 или 3 1,2,3-триазольного кольца Lb в линкере L, и
n5 представляет собой целое число от 2 до 10, и предпочтительно целое число от 2 до 5.
[0165]
N297-(Fuc)MSG2 представлен следующей структурной формулой или формулой последовательности:
[Формула 86]
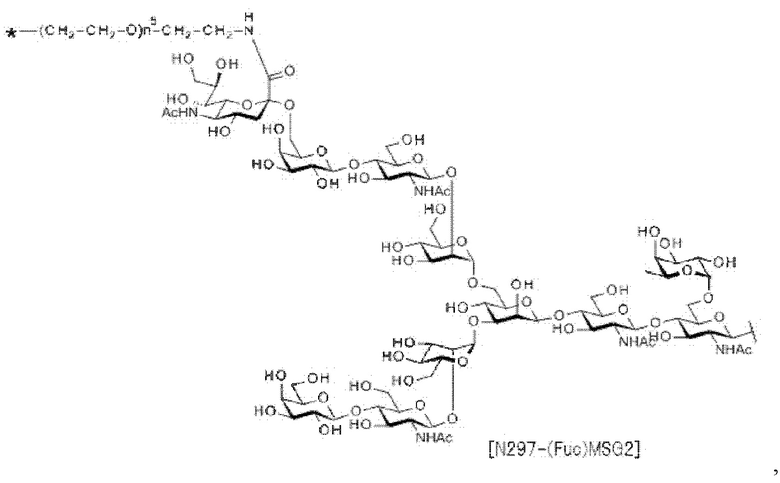
[Формула 87]
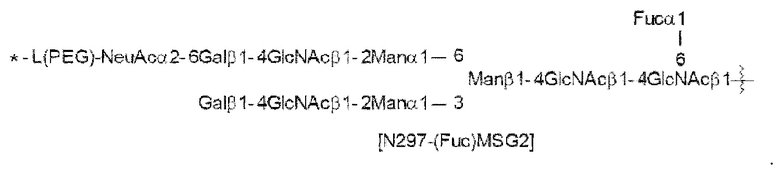
В указанных формулах каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, где аминогруппа на правом конце представляет собой амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в разветвленной цепи 1-6 β-Man в N297-гликане,
каждая звездочка представляет собой связь с линкером L, в частности, с атомом азота в положении 1 или 3 1,2,3-триазольного кольца Lb в линкере L, и
n5 представляет собой целое число от 2 до 10, и предпочтительно целое число от 2 до 5.
[0166]
N297-(Fuc)SG представлен следующей структурной формулой или формулой последовательности:
[Формула 88]
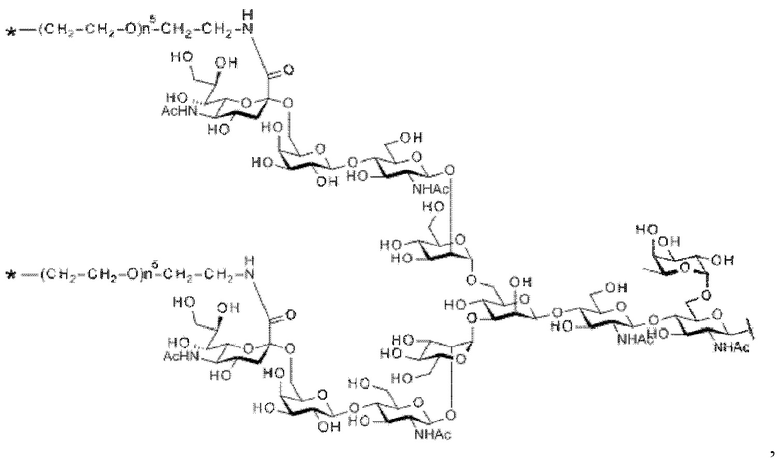
[Формула 89]
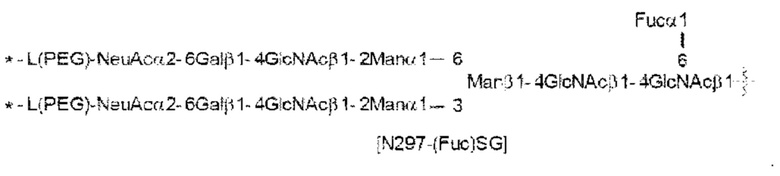
В указанных формулах каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, где аминогруппа на правом конце представляет собой амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой из разветвленных цепей 1-3 и 1-6 β-Man в N297-гликане,
каждая звездочка представляет собой связь с линкером L, в частности, с атомом азота в положении 1 или 3 1,2,3-триазольного кольца Lb в линкере L, и
n5 представляет собой целое число от 2 до 10, и предпочтительно целое число от 2 до 5.
[0167]
Если N297-гликан антитела в конъюгате антитело-лекарственное средство согласно настоящему изобретению представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или их смесь, конъюгат антитело-лекарственное средство представляет собой молекулу, в которой конъюгированы две молекулы линкера L и две молекулы лекарственного средства D (m2=1), поскольку антитело является димером (см. фигуру 1).
Например, пример 74: ADC8 является случаем, когда N297-гликан представляет собой N297-(Fuc)MSG1, и пример 67: ADC1 является случаем, когда N297-гликан представляет собой смесь N297-(Fuc)MSG1 и N297-(Fuc)MSG2.
[0168]
Если N297-гликан антитела в конъюгате антитело-лекарственное средство согласно настоящему изобретению представляет собой N297-(Fuc)SG, конъюгат антитело-лекарственное средство представляет собой молекулу, в которой конъюгированы четыре молекулы линкера L и четыре молекулы лекарственного средства D (m2=2), поскольку антитело является димером. Например, пример 72: ADC6 является случаем, когда N297-гликан представляет собой N297-(Fuc)SG.
[0169]
N297-гликан предпочтительно представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или N297-(Fuc)SG, и более предпочтительно N297-(Fuc)MSG1 или N297-(Fuc)MSG2.
Если №97-гликан антитела в конъюгате антитело-лекарственное средство согласно настоящему изобретению представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или N297-(Fuc)SG, может быть получен гомогенный ADC.
[0170]
В настоящем изобретении предложен способ получения ремоделированного антитела или функционального фрагмента антитела, включающий следующие стадии:
i) культивирование клетки-хозяина (например, клетки животного (такой как клетка СНО)) по любому из пп. [46]-[48] и сбор целевого антитела из полученной культуры;
ii) обработку антитела, полученного на стадии i), гидролазой для получения антитела, N297-гликан которого представляет собой (Fucα1,6)GlcNAc ((Fucα1,6)GlcNAc-антитела) (фигура 3А);
предпочтительно дальнейшую очистку полученного (Fucα1,6)GlcNAc-антитела на стадии, включающей очистку реакционного раствора с использованием колонки с гидроксиапатитом; и
любую из стадий iii)-1 и iii)-2 (фигура 3В):
iii)-1 проведение реакции полученного (Fucα1,6)GlcNAc-антитела с молекулой-донором гликана в присутствии трансгликозидазы с целью синтеза антитела, содержащего ремоделированный гликан с введенной в сиаловую кислоту азидной группой, причем молекулу-донор гликана получают путем введения ПЭГ-линкера, содержащего азидную группу (N3-L(PEG)), в карбонильную группу карбоновой кислоты в положении 2 сиаловой кислоты в MSG (9) или SG (10) и оксазолинирования восстанавливающего конца; и
iii)-2 проведение реакции полученного (Fucα1,6)GlcNAc-антитела с молекулой-донором гликана в присутствии трансгликозидазы с целью синтеза антитела, содержащего ремоделированный гликан с введенной в сиаловую кислоту азидной группой, причем указанную молекулу-донор гликана получают путем введения ПЭГ-линкера, содержащего азидную группу (N3-L(PEG)), в карбонильную группу карбоновой кислоты в положении 2 сиаловой кислоты в (MSG-)Asn или (SG-)Asn с необязательно защищенной или модифицированной a-аминогруппой, а также в карбонильную группу карбоновой кислоты в Asn с применением гидролазы и последующего оксазолинирования восстанавливающего конца.
Настоящее изобретение включает содержащие ремоделированный гликан антитела и функциональные фрагменты антител, а также модифицированные варианты антител и функциональных фрагментов, полученные с применением указанного способа получения.
[0171]
Промежуточное соединение для получения предложенного конъюгата антитело-лекарственное средство содержит алкиновую структуру, реагирующую с азидной группой, такую как DBCO (дибензоциклооктин). Таким образом, конъюгат антитело-лекарственное средство согласно настоящему изобретению может быть получен путем проведения реакции промежуточного соединения с антителом, содержащим ремоделированный гликан MSG1-типа, MSG2-типа или SG-типа, или функциональным фрагментом указанного антитела, где антитело, содержащее введенный в сиаловую кислоту гликана ПЭГ-линкер, содержащий азидную группу, получают посредством стадий i)-iii).
[0172]
Что касается N297-гликана в настоящем изобретении, фукозилированный на восстанавливающем конце GlcNAc ((Fucα1,6)GlcNAc) предпочтительно получают из антитела, продуцируемого в клетке животного, и часть гликана, расположенную со стороны невосстанавливающего конца (Fucα1,6)GlcNAc, предпочтительно подвергают ремоделированию с получением описанной выше структуры гликана, такой как MSG (MSG1, MSG2) или SG. В каждом случае карбоновую кислоту, связанную в положении 2 сиаловой кислоты на невосстанавливающем конце, применяют для связывания с L(PEG).
Такое содержащее ремоделированный гликан антитело, имеющее N297-гликан MSG- (MSG1-, MSG2-) или SG-типа, может быть получено с применением способа, представленного на фигуре 3, например, в соответствии со способом, описанным в WO 2013/120066. Если антитело продуцируется в виде генетически рекомбинантного белка с использованием клетки животного в качестве хозяина в соответствии с известным способом (стадия i), N297-гликан имеет в качестве основной структуры структуру фукозилированного N-связанного гликана, тогда как представлена смесь молекул антитела, содержащих гликаны различной структуры с различными модификациями структуры невосстанавливающего конца или составляющих сахаридов или фрагмент таких молекул антитела (IV на фигуре 3А). Обработка такого антитела, продуцируемого клеткой животного, гидролазой, такой как EndoS, вызывает гидролиз гликозидной связи GlcNAcβ1-4GlcNAc в структуре хитобиозы с восстанавливающего конца, обеспечивая молекулы антитела с единственной структурой гликана, содержащие только (Fucα1,6)GlcNAc в качестве N297-гликана (называемого «(Fucα1,6)GlcNAc-антитело», см. А на фигуре 2) (фигура 3А) (стадия ii)).
[0173]
В качестве фермента для реакции гидролиза N297-гликана могут быть применены, например, EndoS или вариант фермента, сохраняющий гидролитическую активность.
[0174]
При взаимодействии (Fucα1,6)GlcNAc-антитела, полученного в указанной выше реакции гидролиза, в качестве молекулы-акцептора гликана, и молекулы-донора гликана MSG- (MSG1-, MSG2-) или SG-типа с применением трансгликозидазы (например, WO 2017010559), такой как варианты EndoS D233Q и EndoS D233Q/Q303L, может быть получено антитело описанной выше структуры, содержащее N297-гликан MSG- (MSG1-, MSG2-) или SG-типа (см. В на фигуре 2) (фигура 3В) (стадия iii)-1, iii)-2).
[0175]
Если число конъюгированных молекул лекарственного средства на молекулу антитела, m2, в конъюгате антитело-лекарственное средство составляет 1, применяют молекулу-донор гликана, содержащую в качестве гликана MSG, MSG1 или MSG2. Для получения такого гликана коммерчески доступный в качестве исходного вещества свободный от моносиало-Asn (1S2G/1G2S-10NC-Asn, GlyTech, Inc., далее в настоящем описании называемый «(MSG-)Asn») может быть подвергнут разделению в соответствии со способом, описанным в примере 56, с получением (MSG-)Asn1 или (MSG2-)Asn, которые могут быть применены, или может быть применена их смесь без разделения.
[0176]
Если число конъюгированных молекул лекарственного средства на молекулу антитела, m2, в конъюгате антитело-лекарственное средство составляет 2, для реакции трансгликозилирования применяют молекулу-донор гликана, содержащую в качестве гликана SG (10). В качестве такого гликана SG (10) может быть применен гликан SG (10), например, полученный из SGP путем гидролиза или тому подобное, или может быть применен гликан SG (10), такой как коммерчески доступный дисиалооктасахарид (Tokyo Chemical Industry Co., Ltd.).
[0177]
Гликан MSG- (MSG1-, MSG2-) или SG-типа, включенный в молекулу-донор, содержит ПЭГ-линкер, имеющий азидную группу (N3-L(PEG)), в положении 2 сиаловой кислоты гликана. Для введения ПЭГ-линкера, имеющего азидную группу (N3-L(PEG)), в положение 2 сиаловой кислоты может быть применена реакция, известная в области синтетической органической химии (например, реакция конденсации), для MSG (MSG (9)), MSG1 или MSG2, или дисиалооктасахарида (SG (10)) и ПЭГ-линкера, имеющего азидную группу (N3-L(PEG)) N3-(СН2СН2-O)n5-CH2CH2-NH2, где 115 представляет собой целое число от 2 до 10, и предпочтительно представляет собой целое число от 2 до 5. В частности, карбоновая кислота в положении 2 сиаловой кислоты и аминогруппа на правом конце N3-(CH2CH2-O)n5-CH2CH2-NH2 подвергаются реакции конденсации с образованием амидной связи.
[0178]
В качестве альтернативы гликан MSG- (MSG1-, MSG2-) или SG-типа может быть получен путем введения ПЭГ-линкера, имеющего азидную группу (N3-(CH2CH2-O)n5-CH2CH2-NH2), в карбоновую кислоту в положении 2 сиаловой кислоты исходного вещества, такого как (MSG1-)Asn, (MSG2-)Asn и (SG-)Asn (GlyTech, Inc.), с необязательно защищенной или модифицированной α-аминогруппой, и в карбоновую кислоту Asn с применением реакции конденсации и использованием гидролазы, такой как EndoM и EndoRp (iii)-2). Примеры защитных групп для α-аминогрупп могут включать, но не ограничиваются ими, ацетильную (Ас) группу, m-бутоксикарбонильную (Boc) группу, бензоильную (Bz) группу, бензильную (Bzl) группу, карбобензокси (Cbz) группу и 9-флуоренилметоксикарбонильную (Fmoc) группу. Защитная группа для α-аминогрупп предпочтительно представляет собой Fmoc-группу.
Примеры модифицирующих групп для α-аминогрупп включают модифицирующие группы, которые повышают растворимость в воде с помощью гидроксиацетильной группы, структуры ПЭГ или тому подобного.
α-Аминогруппа (MSG1-)Asn, (MSG-2)Asn или (SG-)Asn предпочтительно защищена любой из защитных групп. Если α-аминогруппа защищена защитной группой (например, Fmoc-группой), указанная защитная группа может быть удалена, если это необходимо, после введения ПЭГ-линкера, имеющего азидную группу, и до приведения в действие гидролазы.
[0179]
Предпочтительно использовать активированную форму, такую как форма с введенной оксазолиновой группой, полученная путем обработки хлоридом 2-хлор-1,3-диметил-1H-бензимидазол-3-ия GlcNAc на восстанавливающем конце гликана MSG (MSG1, MSG2) или SG-типа, включенного в молекулу.
[0180]
Для применения в реакции трансгликозилирования могут быть использованы различные ферменты (трансгликозидазы), которые обладают способностью к переносу сложного гликана на М297-гликан; однако предпочтительной трансгликозидазой является EndoS D233Q, модифицированный продукт, для которого реакция гидролиза подавляется путем замены Asp в положении 233 EndoS на Gin. Реакция трансгликозилирования с использованием EndoS D233Q описана, например, в WO 2013/120066. В качестве альтернативы может быть применен модифицированный фермент, такой как EndoS D233Q/Q303L (WO 2017010559), который получают путем дополнительного добавления мутации в EndoS D233Q.
[0181]
Операция очистки антитела после ремоделирования гликана антитела (реакции гликогидролиза и трансгликозилирования) предназначена для отделения низкомолекулярных соединений и ферментов, используемых для реакции, и для такой очистки, как правило, используют гельфильтрационную хроматографию, ионообменную хроматографию, аффинную хроматографию и так далее, а также может быть дополнительно проведена дальнейшая очистка с использованием колонки с гидроксиапатитом. То есть в настоящем изобретении предложен способ получения конъюгата лекарственного средства, включающий следующую за стадией очистки промежуточного соединения из реакционного раствора после гликогидролиза антитела дополнительную стадию очистки с использованием колонки с гидроксиапатитом. Согласно одному из примеров в сообщениях о ремоделировании гликана (J. Am. Chem. Soc. 2012, 134, 12308-12318., Angew. Chem. Int. Ed. 2016, 55, 2361-2367) реакционный раствор после обработки антитела гидролазой очищают только с помощью колонки с белком А (колонка для аффинной хроматографии); однако оказалось, что этот способ очистки не обеспечивает полное удаление гидролазы (например, EndoS), что негативно сказывается на последующей реакции трансгликозилирования вследствие присутствия остаточного фермента. Ввиду такого результата была проведена проверка способов очистки с выявлением того факта, что когда очистку реакционного раствора после обработки антитела гидролазой проводили с использованием колонки с белком А и колонки с гидроксиапатитом (СНТ column, Bio-Rad Laboratories, Inc.) в представленном порядке, эффективность последующей реакции гликозилирования была выше вследствие отсутствия влияния остаточного фермента.
[0182]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению наиболее предпочтительно представляет собой один конъюгат антитело-лекарственное средство, выбранный из следующей группы:
[Формула 90]
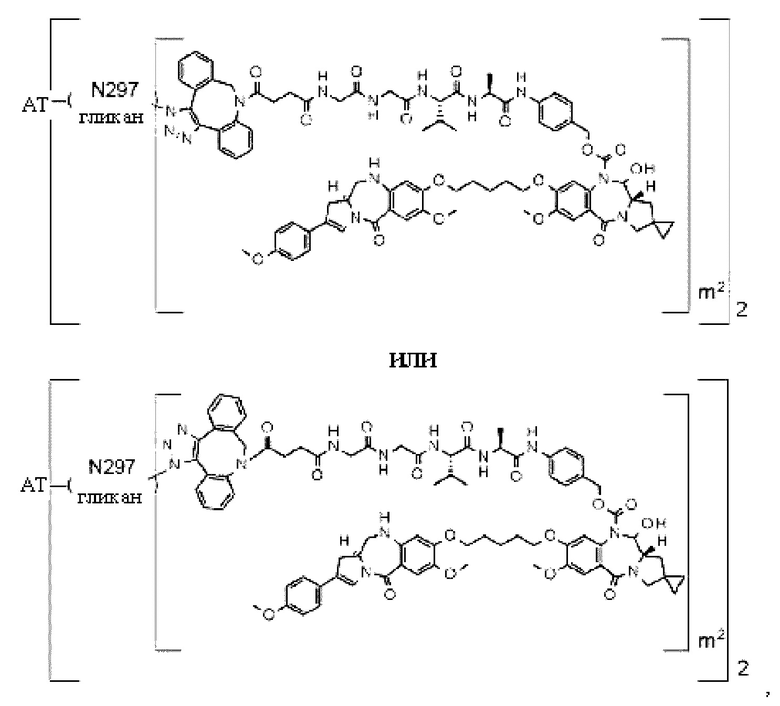
[Формула 91]
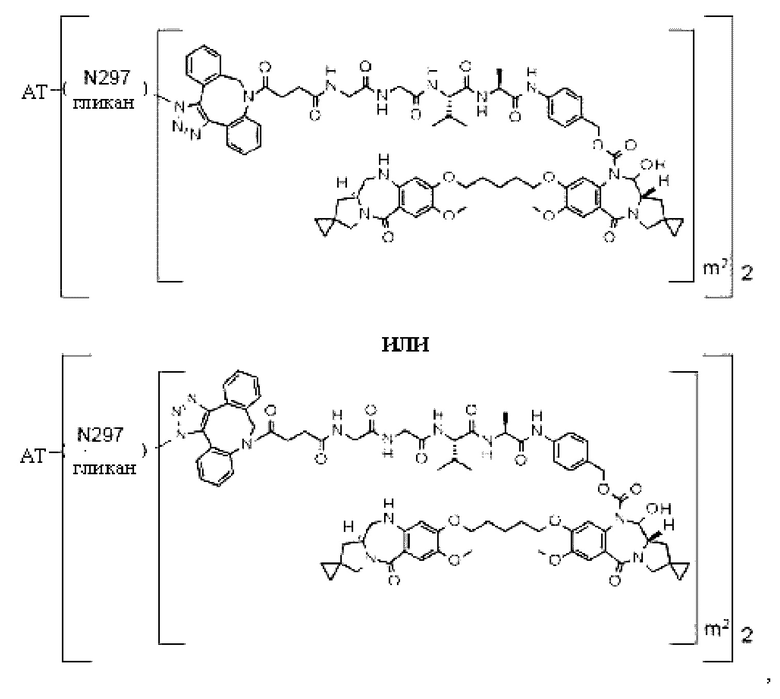
[Формула 92]
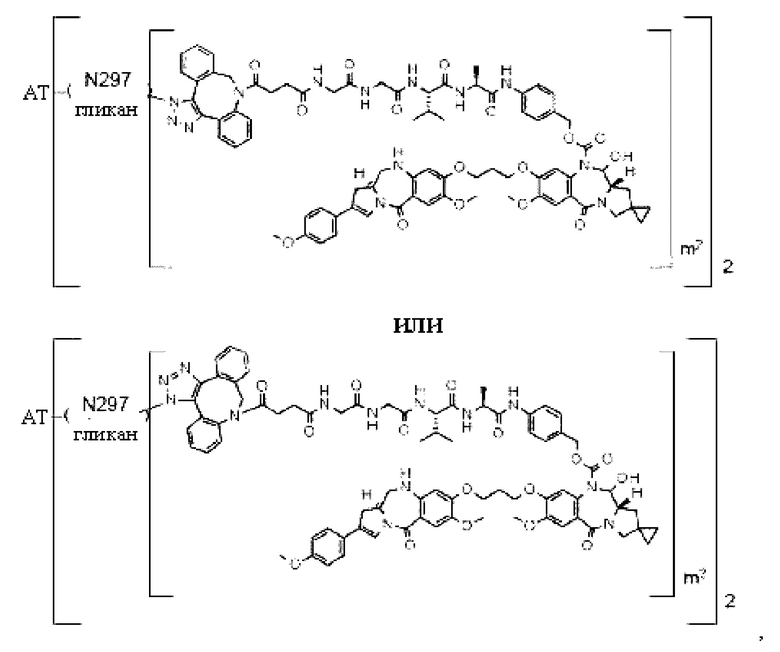
[Формула 93]
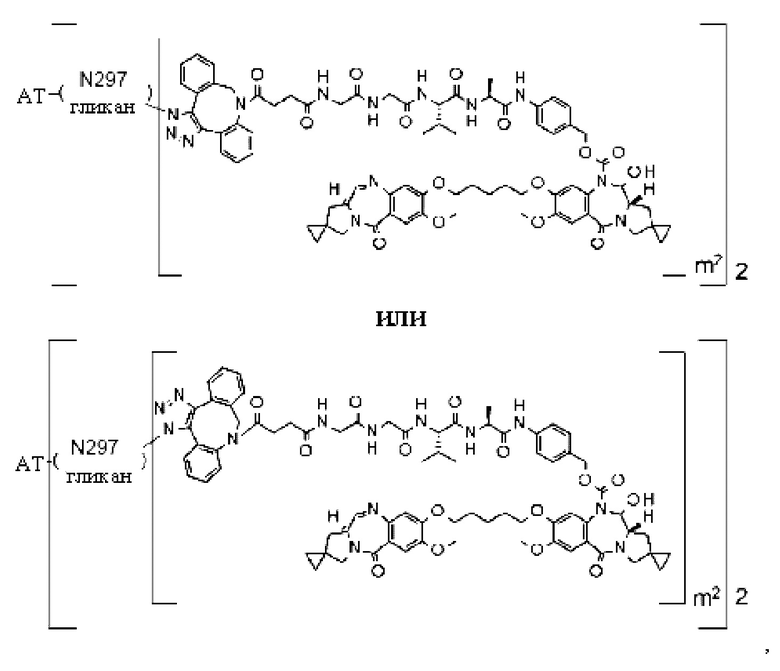
[Формула 94]
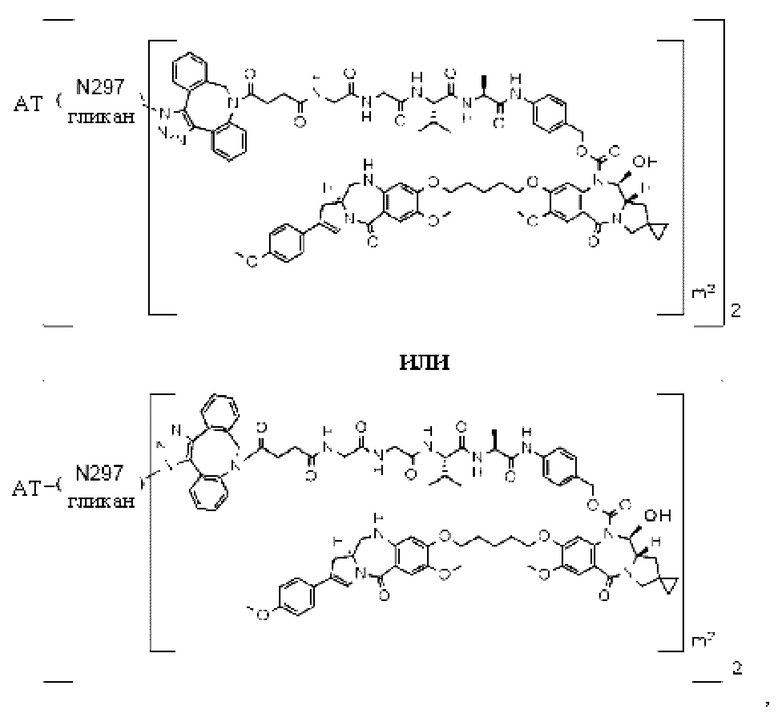
[Формула 95]
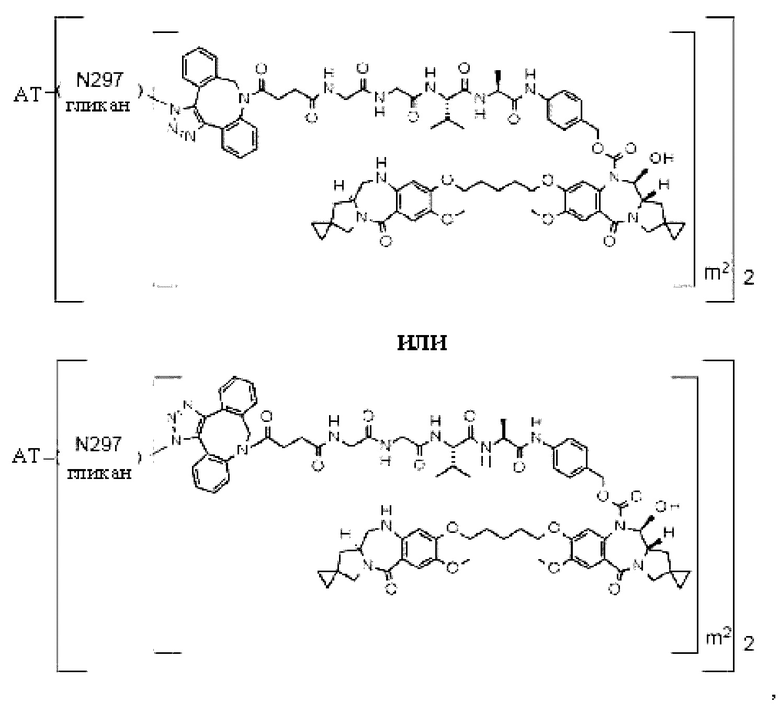
[Формула 96]
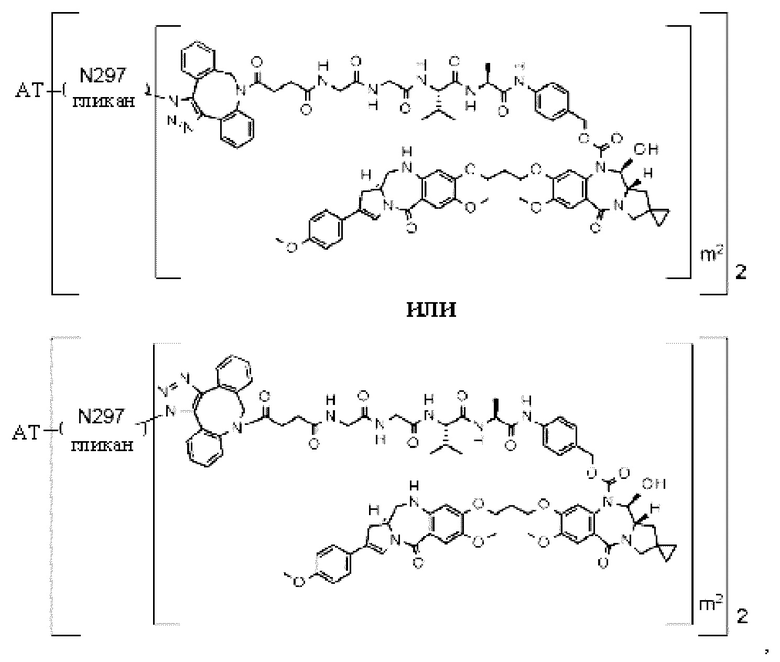
[Формула 97]
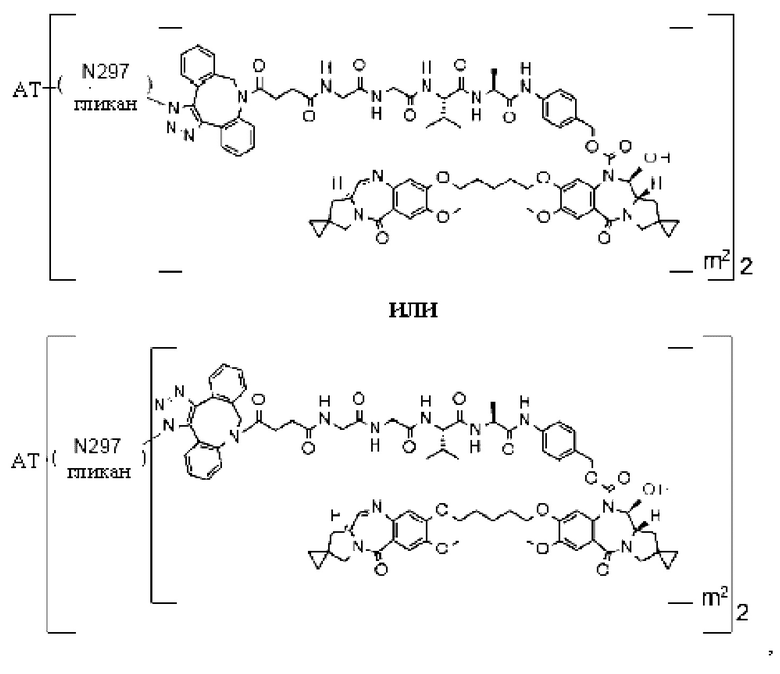
[Формула 98]
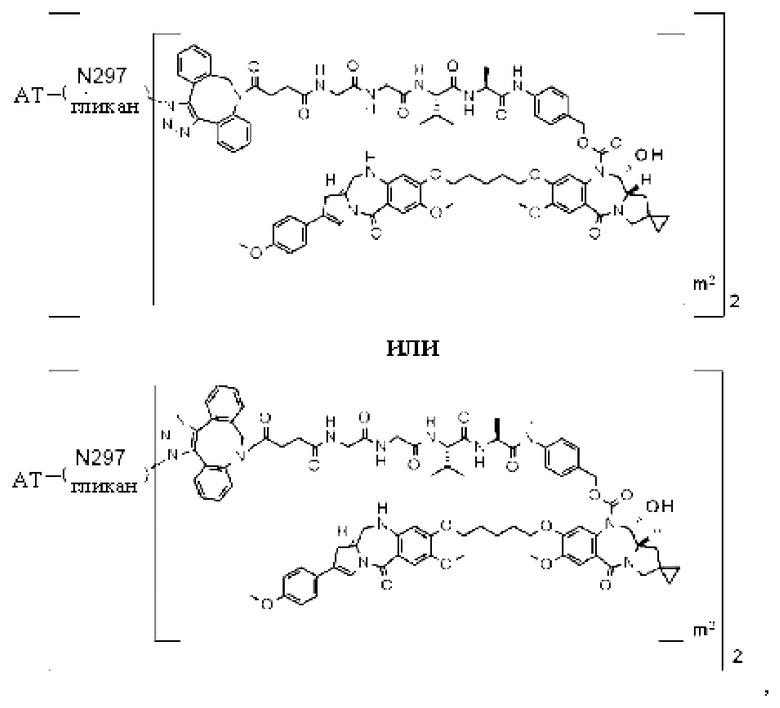
[Формула 99]
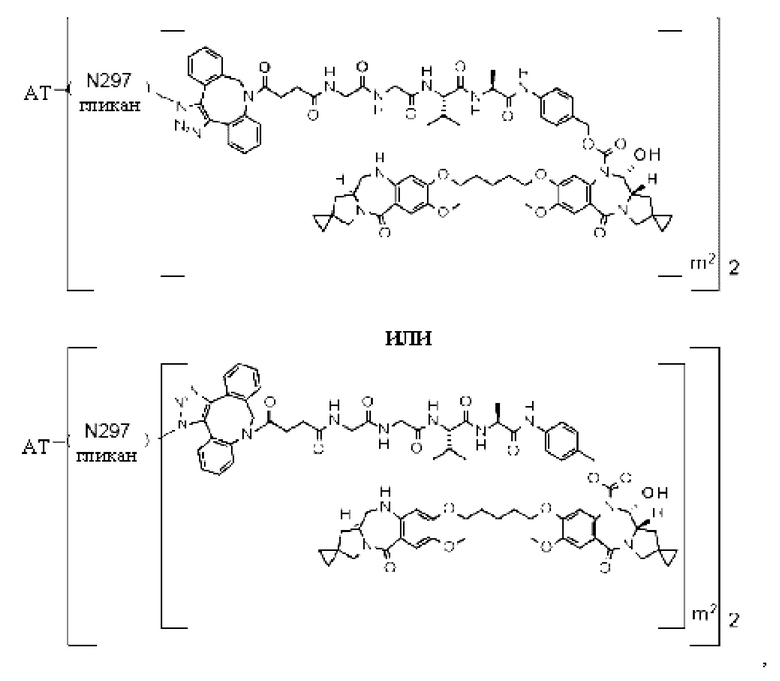
[Формула 100]
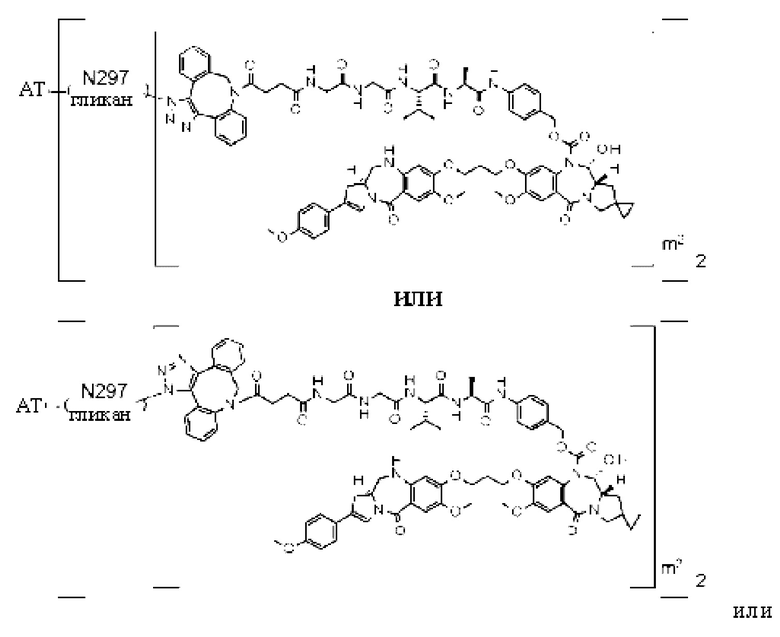
[Формула 101]
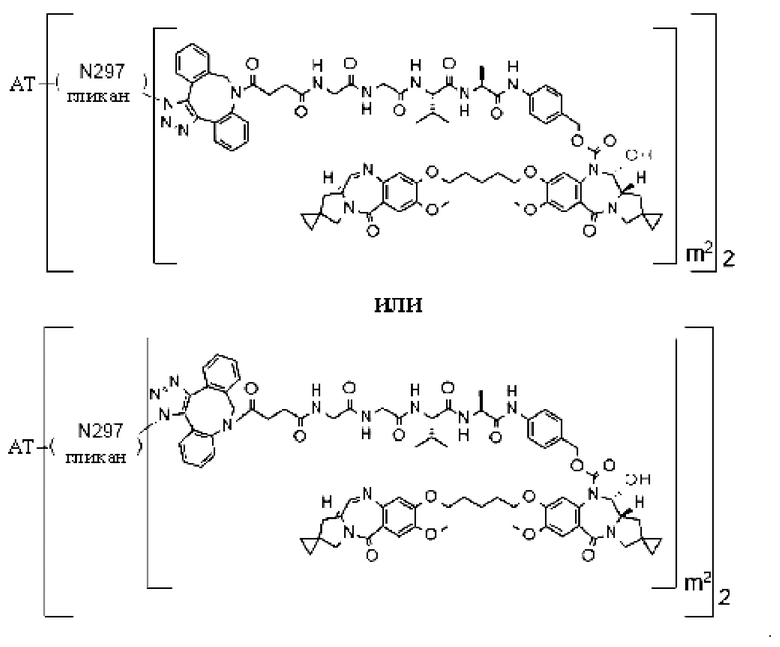
В каждой из представленных выше структурных формул
m2 представляет собой 1 или 2 (предпочтительно m2 представляет собой 1),
антитело AT представляет собой антитело IgG (предпочтительно IgG1, IgG2 или IgG4, более предпочтительно IgG1) или функциональный фрагмент указанного антитела,
N297-гликан представляет собой любой из N297-(Fuc)MSG1, N297-(Fuc)MSG2 и их смеси, и N297-(Fuc)SG (предпочтительно N297-(Fuc)MSG1),
L(PEG) представляет собой -NH-CH2CH2-(O-CH2CH2)3-*, где аминогруппа на левом конце представляет собой амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце каждой или любой из разветвленных цепей 1-3 и 1-6 (предпочтительно разветвленной цепи 1-3) β-Man в N297-гликане, и звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца Lb в линкере L.
Хотя структуры с двумя или четырьмя единицами (m2=1 или 2) «-(N297-гликан)-L-D», в каждой из которых N297-гликан связывается с атомом азота в положении 1 триазольного кольца Lb в L в одной молекуле конъюгата («(N297-гликан)-(N1Lb)L-D»), или структуры с двумя или четырьмя единицами (m2=1 или 2) «-(N297-гликан)-L-D», в каждой из которых N297-гликан связывается с атомом азота в положении 3 триазольного кольца Lb в L в одной молекуле конъюгата («(N297-гликан)-(N3Lb)L-D»), для удобства представлены в качестве наиболее предпочтительного конъюгата антитело-лекарственное средство, конъюгаты антитело-лекарственное средство, содержащие как «(N297-гликан)-(N1Lb)L-D» (если m2=1, то одна единица, если m2=2, то одна, две или три единицы), так и «(N297-гликан)-(N3Lb)L-D» (если m2=1, то одна единица, если m2=2, то три, две или одна единица) в одной молекуле конъюгата, также включены в настоящее изобретение. Другими словами, существует либо один из «(N297-гликан)-(N1Lb)L-D» и «(N297-гликан)-(N3Lb)L-D», либо оба они сосуществуют в одной молекуле конъюгата.
[0183]
Кроме того, AT предпочтительно представляет собой антитело к CLDN6, антитело к CLDN6/CLDN9, антитело к HER2, антитело к DLL3, антитело к FAP, антитело к CDH11, антитело к А33, антитело к CanAg, антитело к CD19, антитело к CD20, антитело к CD22, антитело к CD30, антитело к CD33, антитело к CD56, антитело к CD70, антитело к CD98, антитело к TROP2, антитело к СЕ А, антитело к Cripto, антитело к EphA2, антитело к FGFR2, антитело к G250, антитело к MUC1, антитело к GPNMB, антитело к интегрину, антитело к PSMA, антитело к тенасцину-С, антитело к SLC44A4, антитело к мезотелину, антитело к EGFR или антитело к DR5, более предпочтительно антитело к CLDN6, антитело к CLDN6/CLDN9, антитело к HER2, антитело к CD98 или антитело к TROP2, и еще более предпочтительно антитело к CLDN6 (например, пример 106, 107, 108, 109) или антитело к HER2 (например, трастузумаб, вариант трастузумаба).
[0184]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению и конъюгат антитело к CLDN6- или антитело к HER2-лекарственное средство согласно настоящему изобретению проявляют сильную противоопухолевую активность (противоопухолевую активность in vivo, противоклеточную активность in vitro), а также удовлетворительную кинетику in vivo и физические свойства, и характеризуются высокой безопасностью, и, следовательно, являются пригодными для применения в качестве фармацевтического препарата.
[0185]
Могут существовать стереоизомеры, оптические изомеры вследствие наличия асимметрического атома углерода, геометрические изомеры, таутомеры или оптические изомеры, такие как D-формы, L-формы и атропоизомеры для конъюгата антитело-лекарственное средство согласно настоящему изобретению, а также для свободного лекарственного средства или промежуточного соединения для получения конъюгата антитело-лекарственное средство, и эти изомеры, оптические изомеры и их смеси включены в настоящее изобретение. Производное PBD (V) или (VI) согласно настоящему изобретению имеет асимметрический атом углерода в положении 11', и, следовательно, существуют оптические изомеры. В настоящем описании эти изомеры и смеси этих изомеров представлены одной формулой, а именно общей формулой (V) или (VI). Соответственно, (V) или (VI) включают все оптические изомеры и смеси оптических изомеров в любом отношении. Абсолютная пространственная конфигурация в положении 11' (V) или (VI) может быть определена с помощью рентгеноструктурного анализа или ЯМР, такого как метод Мошера для кристаллического продукта, или промежуточного соединения, или его производного. Таким образом, абсолютная пространственная конфигурация может быть определена с использованием кристаллического продукта или промежуточного соединения путем получения производного с реагентом, содержащим асимметрический центр, пространственная конфигурация которого известна. Если желательно, стереоизомеры синтезированного соединения согласно настоящему изобретению могут быть получены путем выделения с помощью обычного метода разделения оптических изомеров или метода разделения.
[0186]
Число конъюгированных молекул лекарственного средства на молекулу антитела является важным фактором, влияющим на эффективность и безопасность конъюгата антитело-лекарственное средство согласно настоящему изобретению. Конъюгаты антитело-лекарственное средство получают при условиях реакции, таких как количества исходных веществ и реагентов, которые следует подвергать реакции, заданных таким образом, чтобы получить постоянное число конъюгированных молекул лекарственного средства, однако в отличие от химической реакции низкомолекулярных соединений, как правило, получают смесь с различным числом конъюгированных молекул лекарственного средства. Число конъюгированных молекул лекарственного средства на молекулу антитела указано в виде среднего значения, а именно среднего числа конъюгированных молекул лекарственного средства (DAR: Drug to Antibody Ratio, отношение лекарственного средства к антителу). Число молекул производного пирролобензодиазепина, конъюгированных с молекулой антитела, является контролируемым, и от 1 до 10 молекул производного пирролобензодиазепина могут быть конъюгированы в качестве среднего числа конъюгированных молекул лекарственного средства на молекулу антитела (DAR), однако предпочтительно данное число составляет от одного до восьми, и более предпочтительно от одного до пяти.
Если в конъюгате антитело-лекарственное средство согласно настоящему изобретению антитело связывается с L через ремоделированный гликан антитела, число конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитело-лекарственное средство, m2, представляет собой целое число 1 или 2. Если указанный гликан представляет собой N297-гликан, и указанный гликан представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или смесь N297-(Fuc)MSG1 и N297-(Fuc)MSG2, m2 составляет 1, и DAR находится в диапазоне от 1 до 3 (предпочтительно в диапазоне от 1,0 до 2,5, более предпочтительно в диапазоне от 1,2 до 2,2). Если N297-гликан представляет собой N297-(Fuc)SG, m2 составляет 2, и DAR находится в диапазоне от 3 до 5 (предпочтительно в диапазоне от 3,2 до 4,8, более предпочтительно в диапазоне от 3,5 до 4,2).
Специалисты в данной области техники могут разработать способ проведения реакции для конъюгирования необходимого числа молекул лекарственного средства с каждой молекулой антитела на основании описания в примерах, приведенных в настоящем описании, и получить антитело с контролируемым числом конъюгированных молекул производного пирролобензодиазепина.
[0187]
Конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению могут поглощать влагу, осуществлять адгезию адсорбированной воды или превращаться в гидрат, будучи оставленными на воздухе или при перекристаллизации, и такие соединения и соли, содержащие воду, также включены в настоящее изобретение.
[0188]
Конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению, если это желательно, могут быть превращены в фармацевтически приемлемую соль, если они содержат основную группу, такую как аминогруппа. Примеры таких солей могут включать, но не ограничиваются ими, гидрогалогениды, такие как гидрохлориды и гидроиодиды; соли неорганических кислот, такие как нитраты, перхлораты, сульфаты и фосфаты; низшие алкансульфонаты, такие как метансульфонаты, трифторметансульфонаты и этансульфонаты; арилсульфонаты, такие как бензолсульфонаты и n-толуолсульфонаты; соли органических кислот, такие как формиаты, ацетаты, малаты, фумараты, сукцинаты, цитраты, тартраты, оксалаты и малеаты; и соли аминокислот, такие как орнитинаты, глутаматы и аспартаты.
[0189]
Если конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению содержит кислотную группу, такую как карбоксигруппа, обычно может быть образована соль присоединения основания. Примеры фармацевтически приемлемых солей могут включать, но не ограничиваются ими, соли щелочных металлов, такие как соли натрия, соли калия и соли лития; соли щелочноземельных металлов, такие как соли кальция и соли магния; неорганические соли, такие как соли аммония; и соли органических аминов, такие как соли дибензиламина, соли морфолина, соли алкилового сложного эфира фенилглицина, соли этилендиамина, N-метилглюкаматы, соли диэтиламина, соли триэтиламина, соли циклогексиламина, соли дициклогексиламина, соли N,N'-дибензилэтилендиамина, соли диэтаноламина, соли N-бензил-N-(2-фенилэтокси)амина, соли пиперазина, соли тетраметиламмония и соли трис(гидроксиметил)аминометана.
[0190]
Конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению может существовать в виде гидрата, например, вследствие поглощения влаги из воздуха. Сольват согласно настоящему изобретению не ограничивается конкретным сольватом и может представлять собой любой фармацевтически приемлемый сольват, и, в частности, предпочтительными являются гидраты, этанольные сольваты, 2-пропанольные сольваты и так далее. Конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению может существовать в форме его N-оксида, если в нем присутствует атом азота, и эти сольваты и N-оксидные формы включены в объем настоящего изобретения.
[0191]
Настоящее изобретение включает соединения, меченные различными радиоактивными или нерадиоактивными изотопами. Конъюгат антитело-лекарственное средство, свободное лекарственное средство или промежуточное соединение согласно настоящему изобретению может содержать один или более составляющих атомов с неприродным отношением атомных изотопов. Примеры атомных изотопов могут включать, но не ограничиваются ими, дейтерий (2Н), тритий (3Н), иод-125 (125I) и углерод-14 (14С). Соединение согласно настоящему изобретению может быть мечено радиоактивным изотопом, таким как тритий (3Н), иод-125 (125I) и углерод-14 (14С). Соединение с радиоактивной меткой является пригодным для применения в качестве терапевтического или профилактического агента, реагента для исследований, такого как реагент для анализа, и диагностического агента, такого как диагностический агент для визуализации in vivo. Изотопные варианты конъюгата антитело-лекарственное средство согласно настоящему изобретению включены в объем настоящего изобретения независимо от того, являются ли они радиоактивными.
[0192]
[Способы получения]
Далее будут описаны типичные способы получения конъюгата антитело-лекарственное средство согласно настоящему изобретению и свободных лекарственных средств или промежуточных соединений для их получения. Далее номера соединений, представленные в схемах реакций, используются, чтобы отличать соединения друг от друга. В частности, будет приведено обозначение в виде «соединение формулы (1)», «соединение (1)» и так далее. Соединения с другими номерами будут обозначены таким же образом.
[0193]
1. Способ получения 1
Соединение (1) согласно настоящему изобретению может быть получено в соответствии со схемами A-Q, описанными ниже.
[Формула 102]
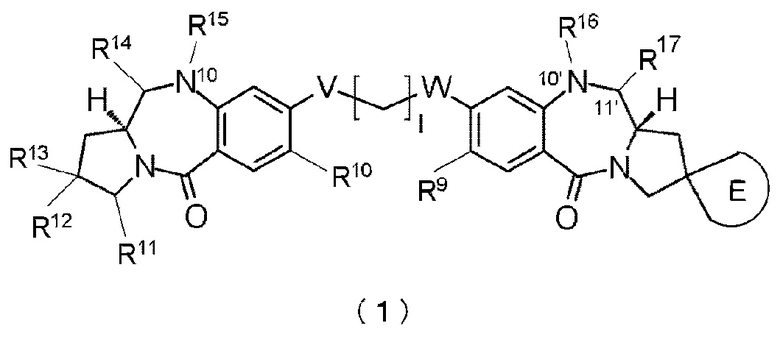
Каждая из схем от А до М представляет собой способ получения промежуточного соединения для получения конъюгата антитело-лекарственное средство согласно настоящему изобретению.
Каждая из схем от N до Q представляет собой способ получения свободного лекарственного средства согласно настоящему изобретению.
[0194]
На каждой стадии в схемах от А до Q, приведенных ниже, желаемая реакция может быть проведена с применением известной методики органической химии.
Растворитель, который следует использовать в реакции на каждой стадии в схемах от А до Q, приведенных ниже, не ограничивается конкретным растворителем и может представлять собой любой растворитель, который до некоторой степени растворяет исходные вещества, не ингибируя реакцию или не оказывая неблагоприятного влияния на реакцию.
На каждой стадии в схемах от А до Q, приведенных ниже, температура реакции зависит от растворителя, исходных веществ, реагентов и так далее, и время реакции зависит от растворителя, исходных веществ, реагентов, температуры реакции и так далее.
На каждой стадии в схемах от А до Q, приведенных ниже, после завершения реакции целевое соединение выделяют из реакционной смеси с применением обычного способа. Например, реакционную смесь подходящим образом нейтрализуют; если присутствует какое-либо нерастворимое вещество, указанное нерастворимое вещество удаляют фильтрованием; затем к полученному продукту добавляют несмешивающийся с водой органический растворитель, такой как этилацетат; органический слой, содержащий целевое соединение, отделяют и промывают водой или тому подобным и сушат над безводным сульфатом магния, безводным сульфатом натрия или тому подобным; и полученный продукт фильтруют, и затем растворитель отгоняют с получением целевого продукта. Полученный целевой продукт может быть при необходимости подвергнут разделению/очистке с помощью подходящего сочетания обычных способов, например, типичных способов, обычно применяемых для разделения/очистки органических соединений, таких как перекристаллизация, переосаждение и хроматография (например, подходящего сочетания методов адсорбционной колоночной хроматографии с использованием носителя, такого как силикагель, оксид алюминия, флоризил (Florisil) типа магний-силикагель и SO3H-силикагель (производства FUJI SILYSIA CHEMICAL LTD.); методов с применением синтезированного адсорбента, таких как распределительная колоночная хроматография с использованием носителя, такого как Sephadex LH-20 (производства Pharmacia), Amberlite XAD-11 (производства Rohm and Haas Company) и DIAION HP-20 (производства Meroubishi Chemical Corporation); методов с использованием ионообменной хроматографии; методов нормально-фазовой/обращенно-фазовой колоночной хроматографии (предпочтительно высокоэффективной жидкостной хроматографии) с использованием силикагеля или алкилированного силикагеля и элюирования с помощью подходящего элюента). В случае целевого соединения, нерастворимого в растворителе, неочищенный продукт полученного твердого вещества может быть промыт растворителем и очищен. Целевое соединение на каждой стадии может быть применено для последующей реакции без очистки.
[0195]
На каждой стадии в схемах от А до Q, приведенных ниже, J, La', Lp', В', Е, V, W, R9, R10, R11, R12, R13, R14, R15, R16, R17, l, n7, n6 и m1 имеют те же значения, что указаны выше. (Lp')' представляет собой любой из дипептидных остатков -VA-, -FG-, -PI-, -VCit-, -VK-, -(D-)PI-, -PL-, -(D-)VA- и -GF-. Если гидроксигруппа или аминогруппа присутствует при заместителе R13, может быть применена защитная группа для (R13)', и если защитная группа отсутствует, (R13)' представляет собой R13. (R17)' представляет собой либо гидроксигруппу, защищенную защитной группой, такой как трет-бутилдиметилсилилоксигруппа, либо R17.
[0196]
Каждая из PRO1, PRO4, PRO6, PRO8 и PRO9 представляет собой защитную группу для аминогруппы. Предпочтительно каждая из PRO1, PRO4, PRO8 и PRO9 представляет собой, например, аллилоксикарбонильную группу, 2,2,2-трихлорэтилоксикарбонильную группу, триметилсилилэтоксиметоксигруппу, бензилоксикарбонильную группу или 9-фторенилметилоксикарбонильную группу. PRO6 предпочтительно представляет собой, например, 2-(триметилсилил)этоксиметильную группу или метоксиметильную группу.
Каждая из PRO2, PRO3, PRO5, PRO7, PRO10, PRO11 и PRO12 представляет собой защитную группу, применяемую в области синтетической органической химии для гидроксигруппы, фенольной группы и карбоксильной группы. Предпочтительно каждая из PRO2, PRO3, PRO5, PRO7, PRO10, PRO11 и PRO12 представляет собой ацетильную группу, бензильную группу, трет-бутилдиметилсилильную (TBDMS) группу, триизопропилсилильную группу или трет-бутильную группу.
[0197]
X2 представляет собой уходящую группу, применяемую в области синтетической органической химии. Предпочтительно X2 представляет собой атом хлора, атом брома, атом иода, метансульфонильную группу или n-толуолсульфонильную группу.
Каждый из Ra и Rc представляет собой заместитель, связанный с карбоксильной группой, и предпочтительно представляет собой, например, метальную группу, этильную группу, бензильную группу или трет-бутильную группу.
Rb представляет собой уходящую группу для получения енолсульфоната, и предпочтительно представляет собой, например, трифторметансульфонильную группу.
Аминогруппы и гидроксигруппы без явного описания защиты в схемах от А до Q при необходимости могут быть защищены с помощью защитной группы. При необходимости может быть выполнено удаление защитной группы, и после введения защитной группы может быть выполнено удаление защитной группы для замены на другую защитную группу.
[0198]
Схема А
Данный способ получения представляет собой способ получения соединения (12а), синтезированного промежуточного соединения, необходимого для получения соединения (1).
[Формула 103]
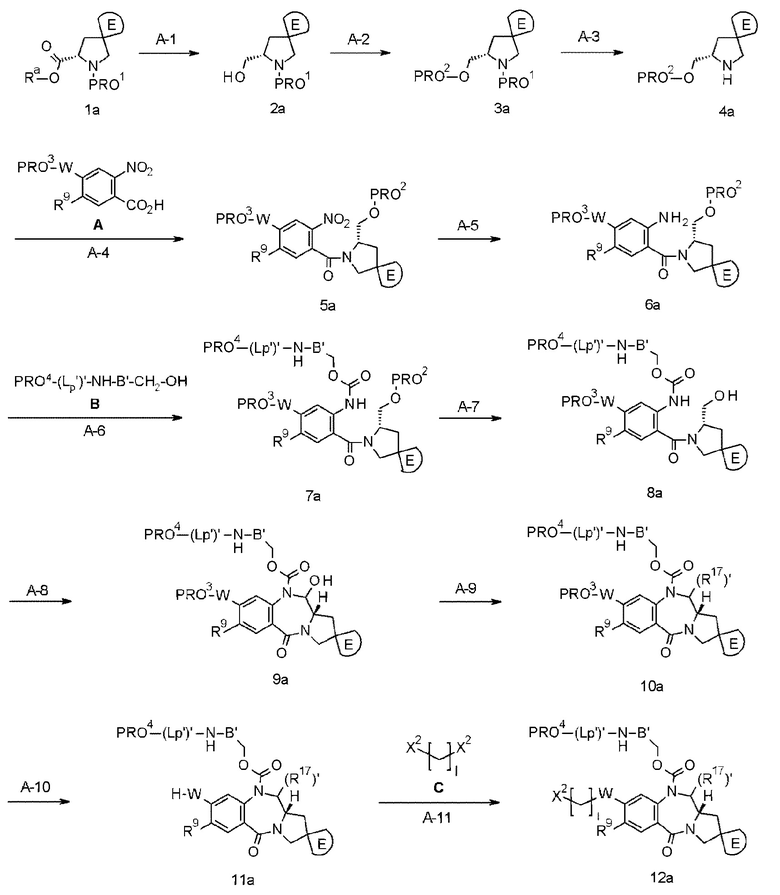
[0199]
Стадия А-1 (1а)→(2а): Реакция восстановления
Данную стадию выполняют путем обработки соединения (1а) восстанавливающим агентом (например, алюмогидридом лития, дибораном, боргидридом лития, боргидридом натрия, комплексом боран-тетрагидрофуран или бис(2-метоксиэтокси)алюмогидридом натрия) в растворителе (диэтиловом эфире, тетрагидрофуране (ТГФ), дихлорметане, этаноле или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -78°С до 50°С. Количество молей восстанавливающего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, по отношению к соединению (1а). При необходимости к реакционной смеси добавляют кислоту Льюиса (например, хлорид лития, хлорид кальция, хлорид олова, комплекс трифторборан-эфир). Время реакции составляет от 1 минуты до 60 часов, и предпочтительно от 5 минут до 24 часов.
[0200]
Стадия А-2 (2а)→(3а): Введение защитной группы (например, трет-бутилдиметилсилильной группы)
В случае, когда PRO2 представляет собой TBDMS-группу, данную стадию выполняют путем проведения реакции соединения (2а) с силилирующим реагентом (например, трет-бутилдиметилсилилхлоридом, трет-бутилдиметилсилилтрифторметансульфонатом) в растворителе (дихлорметане, ацетонитриле, тетрагидрофуране, N,N-диметилформамиде (ДМФА) или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до 120°С, предпочтительно при температуре от 0°С до 100°С. При необходимости к реакционной смеси добавляют основание (например, имидазол, пиридин, 2,6-лутидин, 4-диметиламинопиридин, гидрид натрия). Количество молей силилирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, по отношению к соединению (2а), и количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, по отношению к соединению (2а). Время реакции составляет от 1 минуты до 72 часов, и предпочтительно от 5 минут до 24 часов.
[0201]
Стадия А-3 (3а)→(4а): Реакция удаления защитных групп
В случае, когда PRO1 представляет собой бензилоксикарбонильную группу, данную стадию выполняют, подвергая соединение (3а) каталитическому гидрированию в растворителе (этаноле, пропаноле, метаноле, этилацетате, ТГФ, 1,4-диоксане или тому подобном, или растворителе, представляющем собой их смесь) в присутствии катализатора на основе переходного металла (например, палладия на угле) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Данную стадию, как правило, выполняют в атмосфере водорода; однако при необходимости циклогексен, 1,4-циклогексадиен или тому подобное могут быть применены в качестве доноров водорода. Время реакции составляет от 10 минут до 100 часов, и предпочтительно от 30 минут до 72 часов.
[0202]
Стадия А-4 (4а)→(5а): Реакция конденсации
Данную стадию выполняют путем проведения реакции соединения (4а) и карбоновой кислоты (соединения (А)) в растворителе (бензоле, толуоле, диэтиловом эфире, дихлорметане, ТГФ, ДМФА, воде или тому подобном, или растворителе, представляющем собой их смесь) в присутствии конденсирующего агента, такого как N,N-дициклогексилкарбодиимид, 1-этил-3-(3-диметиламинопропил)карбодиимид, O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторборат, N-этоксикарбонил-2-этокси-1,2-дигидрохинолин и 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид, при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей карбоновой кислоты (соединения (А)), которое следует использовать, составляет от 0,3 до 5 молей, предпочтительно от 0,4 до 2 молей, на моль соединения (4а), и количество молей конденсирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (4а). При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, N-метилморфолин, 4-диметиламинопиридин) и добавку (например, 1-гидроксибензотриазол, 1-гидрокси-7-азабензотриазол). Количество молей основания, которое следует использовать, составляет от каталитического количества до избыточного количества молей, предпочтительно от 0,2 до 3 молей, на моль соединения (4а). Количество молей добавки, которое следует использовать, составляет от каталитического количества до избыточного количества, предпочтительно от 0,01 до 3 молей, на моль соединения (4а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
В случае, когда карбоновую кислоту (соединение (А)) следует превратить в галогенангидрид и подвергнуть реакции конденсации, данную стадию выполняют путем проведения реакции соединения (4а) и галогенангидрида карбоновой кислоты (соединение (А)) в растворителе (бензоле, толуоле, диэтиловом эфире, дихлорметане, тетрагидрофуране, дихлорметане или тому подобном, или растворителе, представляющем собой их смесь) в присутствии основания (например, триэтиламина, диизопропилэтиламина, N-метилморфолина, 4-диметиламинопиридина) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -50°С до 100°С. Количество молей галогенангидрида, которое следует использовать, составляет от 0,3 моля до 5 молей, предпочтительно от 0,4 моля до 2 молей, на моль соединения (4а), и количество молей основания, которое следует использовать, составляет от каталитического количества до избыточного количества молей, предпочтительно от 0,2 до 5 молей, на моль соединения (4а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
Для получения соединения-галогенангидрида карбоновой кислоты (соединения (А)) карбоновую кислоту (соединение (А)) обрабатывают оксалилхлоридом, тионилхлоридом или тому подобным в растворителе (бензоле, толуоле, дихлорметане, дихлорэтане или тому подобном, или растворителе, представляющем собой их смесь) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 100°С. При необходимости к реакционной смеси добавляют каталитическое количество N,N-диметилформамида или тому подобного. Количество молей оксалилхлорида или тионилхлорида, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 10 молей, по отношению к карбоновой кислоте (соединению (А)). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0203]
Стадия А-5 (5а)→(6а): Реакция восстановления
Данную стадию выполняют, подвергая соединение (5а) каталитическому гидрированию в растворителе (этаноле, пропаноле, метаноле, этилацетате, ТГФ, 1,4-диоксане, ДМФА или тому подобном, или растворителе, представляющем собой их смесь) в присутствии катализатора на основе переходного металла (палладия на угле, никеля или тому подобного) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Данную стадию, как правило, выполняют в атмосфере водорода; однако в качестве донора водорода могут быть применены циклогексен, 1,4-циклогексадиен, гидразин или тому подобное. Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
Восстановление нитрогруппы может быть выполнено при следующих условиях.
Данную стадию выполняют путем проведения реакции соединения (5а) и восстанавливающего агента (например, железа, цинка, хлорида олова) в растворителе (этаноле, метаноле, диэтиловом эфире, этилацетате или воде, или растворителе, представляющем собой их смесь) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 90°С. При необходимости к реакционной смеси добавляют кислоту (например, уксусную кислоту, муравьиную кислоту, хлорид аммония). Количество молей восстанавливающего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 100 молей, на моль соединения (5а), и количество молей кислоты, которое следует добавить, составляет от 1 моля до избыточного количества молей на моль соединения (5а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0204]
Стадия А-6 (6а)→(7а): Реакция введения карбаматной группы
Данную стадию выполняют путем проведения реакции соединения (6а) и трифосгена (агента для получения изоцианата) в растворителе (ТГФ, дихлорметане, ДМФА или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С, с получением промежуточного соединения-изоцианата в указанной системе с последующей обработкой спиртом, представленным общей формулой (В). При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, карбонат натрия, гидроксид натрия). Количество молей трифосгена (агента для получения изоцианата), которое следует использовать, составляет от 0,3 моля до избыточного количества молей, предпочтительно от 0,35 до 3 молей, на моль соединения (6а), и количество молей основания, которое следует добавить, составляет от 0,5 до 5 молей на моль соединения (6а). Время реакции до получения промежуточного соединения-изоцианата составляет от 10 минут до 24 часов, и предпочтительно от 30 минут до 1 часа. Время реакции для взаимодействия между промежуточным соединением-изоцианатом и спиртом (В) составляет от 10 минут до 72 часов, и предпочтительно от 1 часа до 24 часов.
Спирт (В), который следует использовать на данной стадии, может быть получен в соответствии со схемой L, описанной ниже.
[0205]
Стадия А-7 (7а)→(8а): Реакция удаления защитных групп
В случае, когда PRO2 представляет собой TBDMS-группу, данную стадию выполняют путем проведения реакции соединения (7а) и любого из кислоты (например, уксусной кислоты), десилилирующего реагента (например, фтороводородной кислоты-пиридина, фтороводородной кислоты-триэтиламина, гидрофтората, фтороводородной кислоты, тетра(н-бутиламмоний)фторида) и смеси кислоты и десилилирующего реагента в растворителе (дихлорметане, хлороформе, ацетонитриле, метаноле, этаноле, ТГФ, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до 100°С, предпочтительно при температуре от 0°С до 50°С. Количество молей кислоты, которое следует использовать, составляет от 1 моля до избыточного количества молей на моль соединения (7а), и количество кислоты или десилилирующего реагента, которое следует использовать, составляет от 1 моля до избыточного количества молей, и предпочтительно от 1 до 10 молей, на моль соединения (7а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0206]
Стадия А-8 (8а)→(9а): Реакция окисления
Данную стадию выполняют путем проведения реакции соединения (8а) и окислителя (например, соли хлорсульфония, реагента Десса-Мартина (Dess-Martin), рутената тетрабутиламмония, хлорхромата пиридиния, катализатора окисления нитроксильного радикала) в растворителе (ацетоне, дихлорметане, пиридине или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -78°С до 30°С. При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, гидрокарбонат натрия, карбонат натрия, гидроксид натрия) и агент для повторного окисления (например, N-оксид N-метилморфолина, диацетат иодбензола, гипохлорит натрия) или добавку (например, бромид тетрабутиламмония, бромид калия). Количество молей окислителя, которое следует использовать, составляет от 0,005 моля до избыточного количества молей, предпочтительно от 0,005 до 10 молей, на моль соединения (8а). Количество молей основания или агента для повторного окисления, которое следует добавить, составляет от 1 до 10 молей на моль соединения (8а), и количество молей добавки, которое следует добавить, составляет от 0,02 до 1 моля на моль соединения (8а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0207]
Стадия А-9 (9а)→(10а): Введение защитной группы
В случае, когда (R17)' представляет собой трет-бутилдиметилсилилоксигруппу, получение выполняют в соответствии со стадией А-2.
[0208]
Стадия А-10 (10а)→(11а): Реакция удаления защитных групп
В случае, когда PRO3 представляет собой триизопропилсилильную группу, получение выполняют путем обработки соединения (10а) ацетатом лития в растворителе (ДМФА, воде или тому подобном, или их смеси) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей ацетата лития, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (10а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0209]
Стадия А-11 (11а)→(12а): Реакция алкилирования
Получение выполняют путем проведения реакции соединения (11а) и алкилирующего агента (С) (например, 1,5-дибромпентана, 1,3-дибромпропана) в растворителе (ТГФ, ДМФА или N,N-диметилацетамиде, или растворителе, представляющем собой их смесь) при температуре от -20°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до температуры кипения. При необходимости к реакционной смеси добавляют основание (например, карбонат калия, карбонат цезия). Количество молей алкилирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 10 молей, на моль соединения (11а), и количество молей основания, которое следует использовать, составляет от 0,4 моля до избыточного количества молей, предпочтительно от 0,5 до 5 молей, на моль соединения (11а). Время реакции составляет от 1 минуты до 60 часов, и предпочтительно от 5 минут до 24 часов.
[0210]
Схема В
Данный способ получения представляет собой способ получения соединения (10b), промежуточного соединения, необходимого для получения соединения (1), в котором R11 и R12 объединены совместно с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи, и каждый из R14 и R15 представляет собой водород.
[Формула 104]
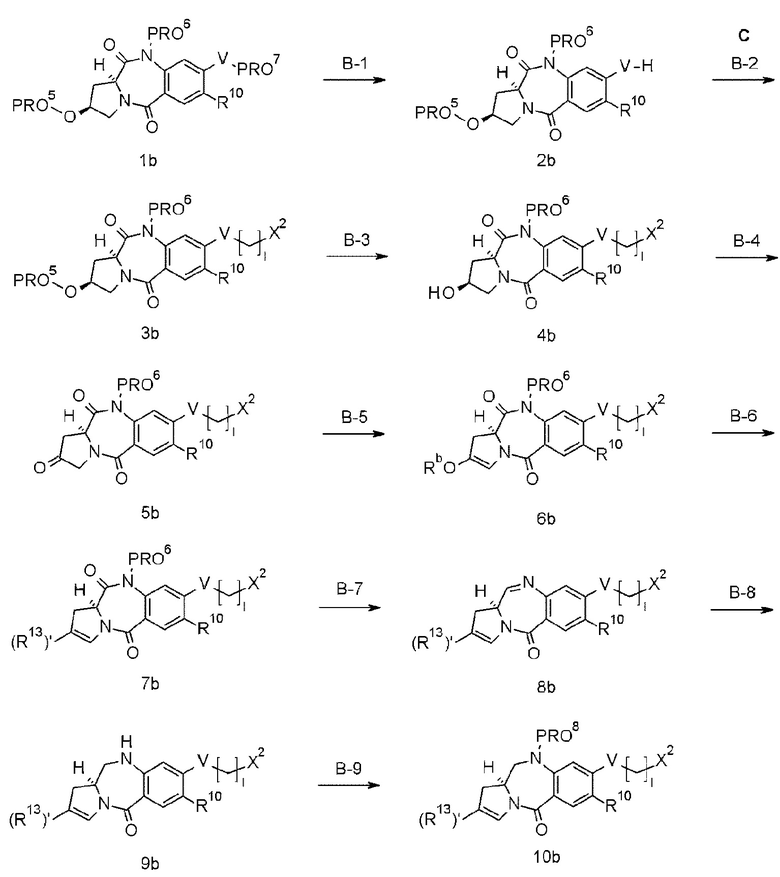
[0211]
Стадия B-1 (1b)→(2b): Реакция удаления защитных групп
В случае, когда PRO7 представляет собой триизопропилсилильную группу, получение выполняют в соответствии со стадией А-10 схемы А.
В случае, когда PRO7 представляет собой бензильную группу, получение выполняют в соответствии со стадией А-3 схемы А.
[0212]
Стадия В-2 (2b)→(3b): Реакция алкилирования
Получение выполняют в соответствии со стадией А-11 схемы А.
[0213]
Стадия В-3 (3b)→(4b): Реакция удаления защитных групп
В случае, когда PRO5 представляет собой TBDMS-группу, получение выполняют в соответствии со стадией А-7 схемы А.
В случае, когда PRO5 представляет собой ацетильную группу, данную стадию выполняют путем проведения реакции соединения (3b) и соответствующего основания (например, карбоната калия, метоксида натрия, гидроксида натрия) в растворителе (метаноле, этаноле, ТГФ, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей основания, которое следует использовать, составляет от каталитического количества до избыточного количества молей, и предпочтительно от 0,1 до 10 молей. Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0214]
Стадия В-4 (4b)→(5b): Реакция окисления
Получение выполняют в соответствии со стадией А-8 схемы А.
[0215]
Стадия В-5 (5b)→(6b): Реакция сульфонилирования енола
В случае, когда Rb представляет собой трифторметансульфонильную группу, данную стадию выполняют путем проведения реакции соединения (5b) и трифторметансульфонового ангидрида или тому подобного в растворителе (например, дихлорметане) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -78°С до 30°С. При необходимости к реакционной смеси добавляют основание (например, 2,6-лутидин). Количество молей трифторметансульфонового ангидрида, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (5b). Количество молей основания, которое следует использовать, составляет от 1 моля до 10 молей. Время реакции составляет от 10 минут до 24 часов, и предпочтительно от 30 минут до 6 часов.
[0216]
Стадия В-6 (6b) → (7b): Реакция кросс-сочетания (например, реакция Сузуки-Мияуры) с катализатором на основе переходного металла
Данную стадию выполняют с применением соединения (6b) и органического соединения бора (например, 4-метоксифенилбороновой кислоты) в растворителе (этаноле, толуоле, 1,4-диоксане, ДМФА, тетрагидрофуране, воде или тому подобном, или растворителе, представляющем собой их смесь) в присутствии катализатора на основе переходного металла (например, тетракис(трифенилфосфин)палладия, дихлорбис(бензонитрил)палладия (II)) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 120°С. При необходимости к реакционной смеси добавляют основание (например, карбонат натрия, карбонат калия, карбонат цезия, гидрокарбонат натрия, гидроксид натрия) или добавку (например, оксид серебра, трифениларсин). Количество молей палладиевого катализатора, которое следует использовать, составляет от 0,01 моля до 1 моля, предпочтительно от 0,01 моля до 0,5 моля, на моль соединения (6b). Количество молей органического соединения бора, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 10 молей, на моль соединения (6b), количество молей основания, которое следует использовать, составляет от 1 моля до 5 молей на моль соединения (6b), и количество молей добавки, которое следует использовать, составляет от 0,1 моля до 5 молей на моль соединения (6b). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0217]
Стадия В-7 (7b) → (8b): Реакция восстановления
В случае, когда PRO6 представляет собой 2-(триметилсилил)этоксиметильную группу, например, данную стадию выполняют путем обработки соединения (7b) восстанавливающим агентом (например, лития борогидридом, натрия борогидридом) в растворителе (диэтиловом эфире, ТГФ, дихлорметане, этаноле или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -78°С до 50°С. Количество молей восстанавливающего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 30 молей, на 1 моль соединения (7b). Время реакции составляет от 1 минуты до 24 часов, и предпочтительно 5 минут до 6 часов. Соединение (8b) могут быть получено путем добавления силикагеля к раствору (в дихлорметане, этаноле, воде или растворителе, представляющем собой их смесь) неочищенного продукта, полученного в реакции восстановления, с последующей обработкой при перемешивании. Силикагель, который следует использовать, находится в избыточном количестве по отношению к соединению (7b). Время обработки составляет от 12 часов до 150 часов, и предпочтительно от 12 часов до 100 часов.
[0218]
Стадия В-8 (8b) → (9b): Восстановление иминогруппы
Данную стадию выполняют путем обработки соединения (8b) восстанавливающим агентом (например, боргидридом натрия, цианоборогидридом, триацетоксиборогидридом натрия, 2-пиколин-бораном, пиридин-бораном) в растворителе (ТГФ, дихлорметане, N,N-диметилформамиде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -78°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от -78°С до 50°С. Количество молей восстанавливающего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на 1 моль соединения (8b). Время реакции составляет от 1 минуты до 60 часов, и предпочтительно от 5 минут до 24 часов.
[0219]
Стадия В-9 (9b) → (10b): Введение защитной группы
В случае, когда PRO8 представляет собой аллилоксикарбонильную группу, данную стадию выполняют путем проведения реакции соединения (9b) и аллилхлорформиата, диаллилдикарбоната или тому подобного в растворителе (бензоле, толуоле, пиридине, диэтиловом эфире, дихлорметане, ТГФ, 1,4-диоксане, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, пиридин, карбонат натрия, карбонат калия, гидроксид натрия). Количество молей аллилхлорформиата, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 10 молей, на моль соединения (9b), и количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 10 молей, на моль соединения (9b). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 10 минут до 48 часов.
В случае, когда PRO8 представляет собой 2,2,2-трихлорэтоксикарбонильную группу, данную стадию выполняют путем проведения реакции соединения (9b) и 2,2,2-трихлорэтилхлорформиата в растворителе (бензоле, толуоле, пиридине, диэтиловом эфире, дихлорметане, ТГФ, 1,4-диоксане, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, пиридин, карбонат натрия, гидроксид натрия). Количество молей 2,2,2-трихлорэтилхлорформиата, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 10 молей, на моль соединения (9b), и количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества, предпочтительно от 1 до 10 молей, на моль соединения (9b). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 48 часов.
[0220]
Схема С
Данный способ получения представляет собой способ получения соединения (14с), промежуточного соединения, необходимого для получения соединения (1), в котором R11 и R12 объединены совместно с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи, и каждый из R14 и R15 представляет собой водород. Соединение (10b) может быть получено с помощью указанного способа получения.
[Формула 105]
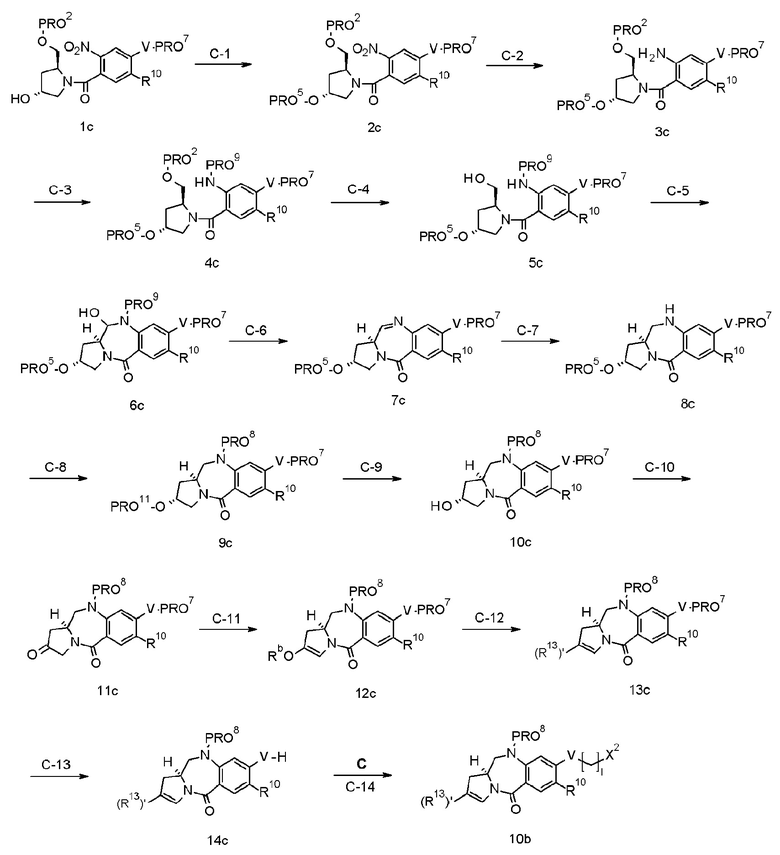
[0221]
Стадия С-1 (1 с) → (2 с): Введение защитной группы
В случае, когда PRO5 представляет собой ацетильную группу, данную стадию выполняют путем проведения реакции соединения (1с) и ацетилирующего реагента (например, уксусного ангидрида, ацетилхлорида) в растворителе (дихлорметане, ДМФА, пиридине, ТГФ, 1,4-диоксане или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 100°С. При необходимости к реакционной смеси добавляют основание (например, триэтиламин, диизопропилэтиламин, пиридин, 4-диметиламинопиридин). Количество молей ацетилирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 20 молей, на моль соединения (1 с), и количество молей основания, которое следует использовать, составляет от каталитического количества до избыточного количества молей, предпочтительно от 0,1 до 20 молей, на моль соединения (1с). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
В случае, когда PRO5 представляет собой TBDMS-группу, получение выполняют в соответствии со стадией А-2 схемы А.
[0222]
Стадия С-2-стадия С-5 и стадия С-7-стадия С-14
Получение на стадии С-2 выполняют в соответствии со стадией А-5 схемы А, получение на стадии С-3 выполняют в соответствии со стадией В-9 схемы В, получение на стадии С-4 выполняют в соответствии со стадией А-7 схемы А, получение на стадии С-5 выполняют в соответствии со стадией А-8 схемы А, получение на стадии С-7 выполняют в соответствии со стадией В-8 схемы В, получение на стадии С-8 выполняют в соответствии со стадией В-9 схемы В, получение на стадии С-9 выполняют в соответствии со стадией В-3 схемы В, получение на стадии С-10 выполняют в соответствии со стадией А-8 схемы А, получение на стадии С-11 выполняют в соответствии со стадией В-5 схемы В, получение на стадии С-12 выполняют в соответствии со стадией В-6 схемы В, получение на стадии С-13 выполняют в соответствии со стадией А-10 схемы А, и получение на стадии С-14 выполняют в соответствии со стадией А-11 схемы А.
[0223]
Стадия С-6 (6 с) → (7 с): Реакция удаления защитных групп
В случае, когда PRO9 представляет собой 2,2,2-трихлорэтоксикарбонильную группу, данную стадию выполняют путем проведения реакции соединения (6с) и металлического реагента (например, цинка, сплава цинка-свинца, кадмия, кадмия-свинца) в растворителе (ТГФ, уксусной кислоте, водном растворе ацетата аммония, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до температуры кипения растворителя, предпочтительно при температуре от 0°С до 40°С. Количество молей металлического реагента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 10 молей, на моль соединения (6с). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
В случае, когда PRO9 представляет собой аллилоксикарбонильную группу, данную стадию выполняют с применением соединения (6с), палладиевого катализатора (например, тетракис(трифенилфосфин)палладия), и скавенджера аллильных групп (например, пирролидина, морфолина, барбитуровой кислоты) в растворителе (дихлорметане, ДМФА, ТГФ или тому подобном, или их смеси) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 30°С. Количество молей палладиевого катализатора, которое следует использовать, составляет от 0,005 моля до 1 моля, предпочтительно от 0,005 моля до 0,5 моля, на моль соединения (6с). Количество молей скавенджера аллильных групп, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 10 молей. Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0224]
Схема D
Соединение (13с) может быть получено с использованием представленной схемы.
[Формула 106]
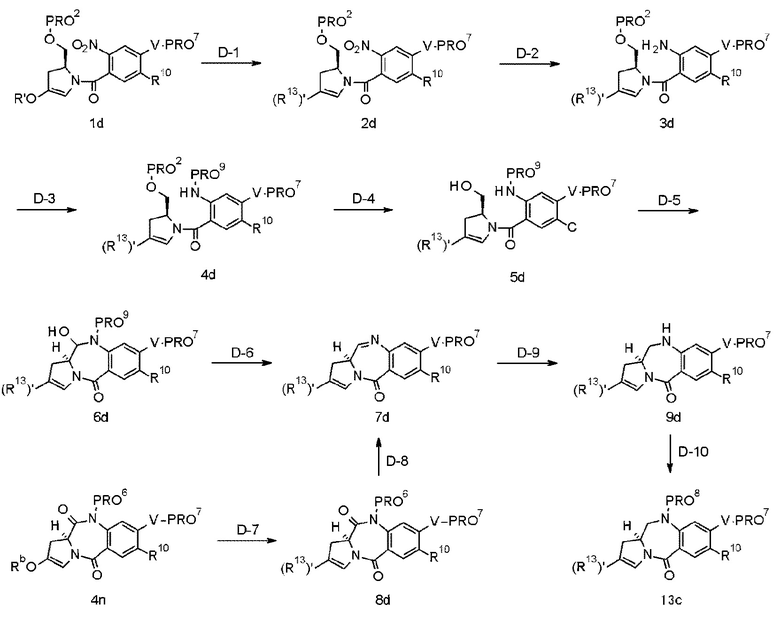
[0225]
Стадия D-1-стадия D-6, стадия D-9 и стадия D-10
Получение на стадии D-1 выполняют в соответствии со стадией В-6 схемы В, получение на стадии D-2 выполняют в соответствии со стадией А-5 схемы А, получение на стадии D-3 выполняют в соответствии со стадией В-9 схемы В, получение на стадии D-4 выполняют в соответствии со стадией А-7 схемы А, получение на стадии D-5 выполняют в соответствии со стадией А-8 схемы А, получение на стадии D-6 выполняют в соответствии со стадией С-6 схемы С, получение на стадии D-9 выполняют в соответствии со стадией В-8 схемы В, и получение на стадии D-10 выполняют в соответствии со стадией В-9 схемы В.
[0226]
Стадия D-7 и стадия D-8
В качестве альтернативы соединение (7d) может быть получено в соответствии со стадией D-7, которая является такой же, как стадия В-6 схемы В, и стадии D-8, которая является такой же, как стадия В-7 схемы В.
[0227]
Схема Е
Схема Е представляет собой способ получения соединения (4е) путем сочетания соединений (11а) и (12а), полученных согласно схеме А, и соединений (10b) и (14с), полученных согласно схеме В или схеме С.
[Формула 107]
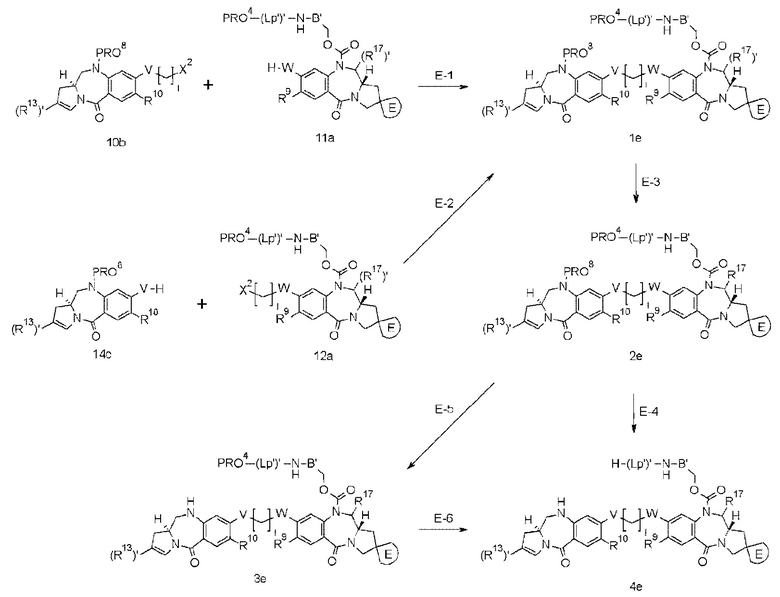
[0228]
Стадия Е-1
Данная стадия представляет собой стадию получения соединения (1е) посредством реакции сочетания соединения (11а), полученного согласно схеме А, и соединения (10b), полученного согласно схеме В.
Получение выполняют, подвергая соединение (11а) реакции сочетания с соединением (10b) в растворителе (ТГФ, ДМФА, N,N-диметилацетамиде или растворителе, представляющем собой их смесь) в присутствии основания (например, карбоната калия, карбоната цезия) при температуре от -20°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей соединения (10b), которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 0,7 до 1,5 молей, по отношению к 0,5 моля соединения (11а). Количество молей основания, которое следует использовать, составляет от 1 моля до 5 молей по отношению к 0,5 моля соединения (11а). Время реакции составляет от 1 минуты до 60 часов, и предпочтительно от 5 минут до 24 часов.
[0229]
Стадия Е-2
В качестве альтернативы соединение (1е) можно получить, подвергая соединение (12а), полученное согласно схеме А, и соединение (14с), полученное согласно схеме С, реакции сочетания, как на стадии Е-1.
[0230]
Стадия Е-3
Получение на стадии Е-3 выполняют в соответствии со стадией А-7 схемы А.
[0231]
Стадия Е-4
Данная стадия представляет собой стадию получения соединения (4е) в случае, когда защитные группы PRO4 и PRO8 в соединении (2е) являются одинаковыми, на которой соединение (2е) подвергают реакции удаления защитных групп, как на стадии С-6 схемы С.
[0232]
В случае, когда защитные группы PRO4 и PRO8 в соединении (2е) различны, соединение (4е) может быть получено путем ступенчатой реакции удаления защитных групп на стадии Е-5 и стадии Е-6.
[0233]
Получение на стадии Е-5 и стадии Е-6 выполняют в соответствии со стадией С-6 схемы С.
[0234]
Схема F
В качестве альтернативы соединение (4е) может быть получено из промежуточного соединения (10f) посредством способа синтеза. Данный способ получения представляет собой способ получения соединения (10f) и соединения (4е).
[Формула 108]
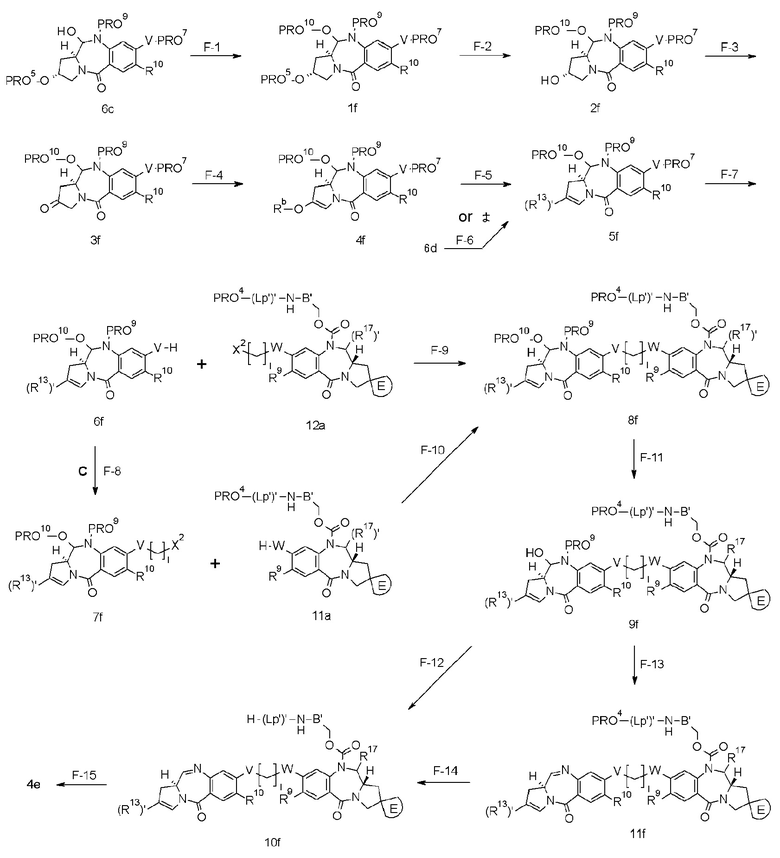
[0235]
Стадия F-1 -стадия F-10 и стадия F-15
Получение на стадии F-1 выполняют в соответствии со стадией А-2 схемы А, получение на стадии F-2 выполняют в соответствии со стадией В-3 схемы В, получение на стадии F-3 выполняют в соответствии со стадией А-8 схемы А, получение на стадии F-4 выполняют в соответствии со стадией В-5 схемы В, получение на стадии F-5 выполняют в соответствии со стадией В-6 схемы В, получение на стадии F-6 выполняют в соответствии со способом конструирования А-2 схемы А, получение на стадии F-7 выполняют в соответствии со стадией А-10 схемы А, получение на стадии F-8 выполняют в соответствии со стадией А-11 схемы А, получение на стадии F-9 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии F-10 выполняют в соответствии со стадией Е-1 схемы Е, и получение на стадии F-15 выполняют в соответствии со стадией В-8 схемы В.
[0236]
Стадия F-11
В случае, когда каждая из PRO10 и защитной группы для гидроксигруппы в (R17)' представляет собой TBDMS-группу, получение выполняют в соответствии со стадией А-7 схемы А.
[0237]
Стадия F-12
Данная стадия представляет собой стадию получения соединения (10f), когда защитные группы PRO4 и PRO9 в соединении (9f) являются одинаковыми, на которой соединение (9f) подвергают реакции удаления защитных групп, как на стадии С-6 схемы С.
[0238]
Стадия F-13 и стадия F-14
В случае, когда защитные группы PRO4 и PRO9 в соединении (9f) различны, соединение (10f) может быть получено путем ступенчатой реакции удаления защитных групп на стадии F-13 и стадии F-14. Получение на стадии F-13 и стадии F-14 выполняют в соответствии со стадией С-6 схемы С.
[0239]
Схема G
Данный способ получения представляет собой способ получения соединения (11g), промежуточного соединения для получения соединения (1), в котором R11 представляет собой атом водорода, R12 и R13 объединены с образованием спироцикла, и каждый из R14 и R15 представляет собой атом водорода.
[Формула 109]
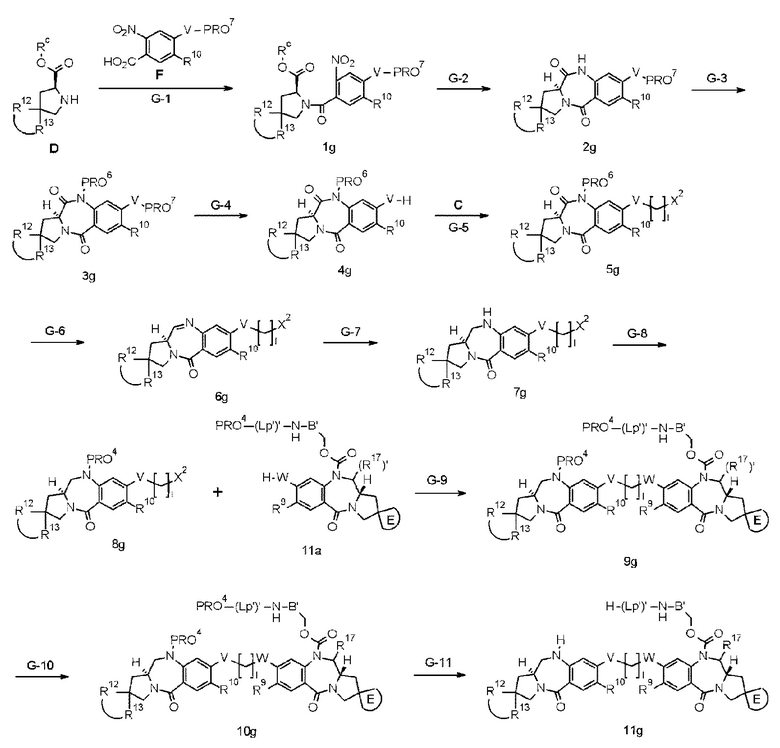
[0240]
Стадии G-1 и G-2 и стадии G-5-G-11
Получение на стадии G-1 выполняют в соответствии со стадией А-4 схемы А, получение на стадии G-2 выполняют в соответствии со стадией А-5 схемы А, получение на стадии G-5 выполняют в соответствии со стадией А-11 схемы А, получение на стадии G-6 выполняют в соответствии со стадией В-7 схемы В, получение на стадии G-7 выполняют в соответствии со стадией В-8 схемы В, получение на стадии G-8 выполняют в соответствии со стадией В-9 схемы В, получение на стадии G-9 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии G-10 выполняют в соответствии со стадией А-7 схемы А, и получение на стадии G-11 выполняют в соответствии со стадией С-6 схемы С.
[0241]
Стадия G-3: Введение защитной группы
Данную стадию выполняют путем проведения реакции соединения (2g) и реагента на основе хлорметоксипроизводного простого эфира (например, 2-(хлорметокси)этилтриметилсилана, хлорметилметилового эфира, бензилхлорметилового эфира) в растворителе (ТГФ, ДМФА, диоксане или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -78°С до температуры кипения растворителя, предпочтительно при температуре от 0°С до 50°С. При необходимости к реакционной смеси добавляют основание (гидрид натрия, н-бутиллитий, гексаметилдисилазан лития). Количество молей реагента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (2g). Количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (2g). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0242]
Стадия G-4
В случае, когда PRO7 представляет собой бензильную группу, получение выполняют в соответствии со стадией А-3 схемы А.
В случае, когда PRO7 представляет собой триизопропилсилильную группу, получение выполняют в соответствии со стадией А-10 схемы А.
[0243]
Схема Н
Данный способ получения представляет собой способ получения соединения (9h), промежуточного соединения для получения соединения (1), в котором R11 представляет собой атом водорода, R12 и R13 объединены с образованием спирокольца, и R14 и R15 объединены с образованием иминной связи (C=N). В данном способе получения спирокольцо, образованное R12 и R13, является синонимом структуры Е, и, следовательно, представлено структурой Е.
[Формула 110]
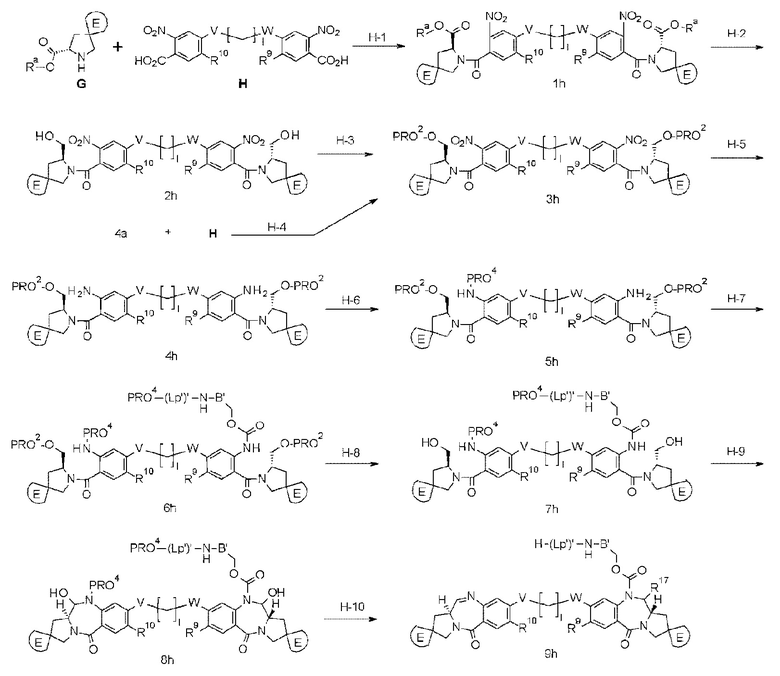
[0244]
Стадия Н-1-стадия Н-10
Получение на стадии Н-1 выполняют в соответствии со стадией А-4 схемы А, получение на стадии Н-2 выполняют в соответствии со стадией А-1 схемы А, получение на стадии Н-3 выполняют в соответствии со стадией С-1 схемы С, получение на стадии Н-4 выполняют в соответствии со стадией А-4 схемы А, получение на стадии Н-5 выполняют в соответствии со стадией А-5 схемы А, получение на стадии Н-6 выполняют в соответствии со стадией В-9 схемы В, получение на стадии Н-7 выполняют в соответствии со стадией А-6 схемы А, получение на стадии Н-8 выполняют в соответствии со стадией В-3 схемы В, получение на стадии Н-9 выполняют в соответствии со стадией А-8 схемы А, и получение на стадии Н-10 выполняют в соответствии со стадией С-6 схемы С.
[0245]
Схема I
Данный способ получения представляет собой способ получения соединения (11i), промежуточного соединения для получения соединения (1), в котором R11 и R12 объединены с образованием бензольного кольца, R13 представляет собой одинарную связь, и R14 и R15 объединены с образованием имина.
[Формула 111]
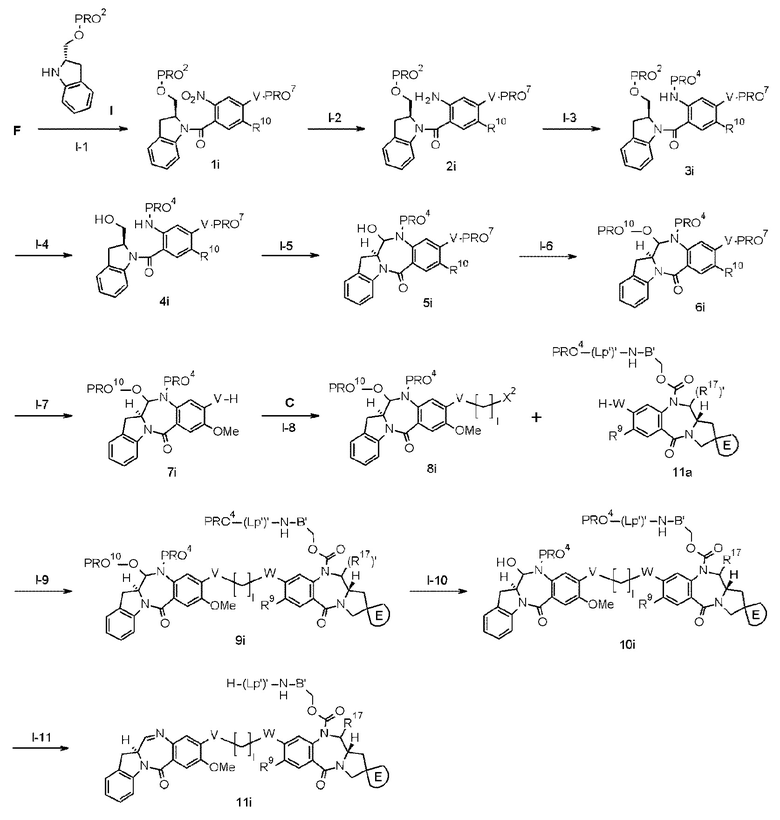
[0246]
Стадия I-1-стадия I-11
Получение на стадии I-1 выполняют в соответствии со стадией А-4 схемы А, получение на стадии I-2 выполняют в соответствии со стадией А-5 схемы А, получение на стадии I-3 выполняют в соответствии со стадией В-9 схемы В, получение на стадии I-4 выполняют в соответствии со стадией А-7 схемы А, получение на стадии I-5 выполняют в соответствии со стадией А-8 схемы А, получение на стадии I-6 выполняют в соответствии со стадией А-2 схемы А, получение на стадии I-7 выполняют в соответствии со стадией А-10 схемы А, получение на стадии I-8 выполняют в соответствии со стадией А-11 схемы А, получение на стадии I-9 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии I-10 выполняют в соответствии со стадией А-7 схемы А, и получение на стадии I-11 выполняют в соответствии со стадией С-6 схемы С.
[0247]
Схема J
Данный способ получения представляет собой способ получения соединения (12j), промежуточного соединения для получения соединения (1), в котором R12 и R13 объединены с образованием CH2=, R11 представляет собой водород, и R14 и R15 объединены с образованием имина.
[Формула 112]
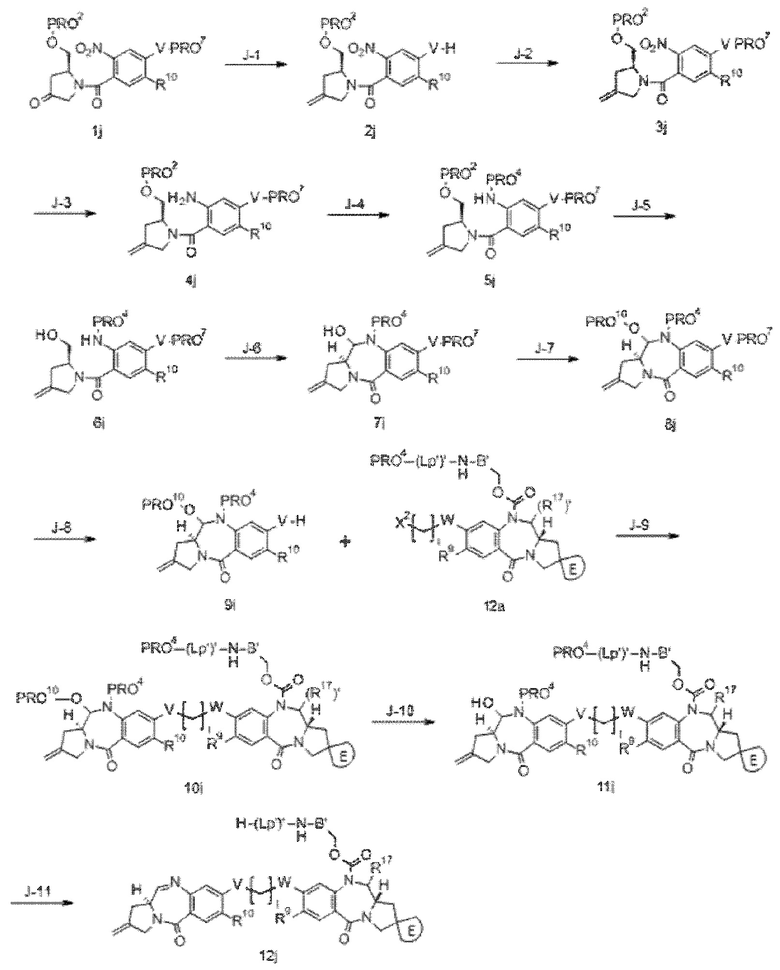
[0248]
Стадия J-1
Данная стадия представляет собой стадию получения соединения (2j), на которой соединение (1j) подвергают реакции Виттига.
[0249]
Стадия J-2: Введение защитной группы
В случае, когда PRO7 представляет собой триизопропилсилильную группу, данную стадию выполняют путем проведения реакции соединения (2j) и силилирующего реагента (например, триизопропилсилилхлорида, триизопропилсилилтрифлата) в растворителе (дихлорметане, ацетонитриле, ТГФ, ДМФА или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до 120°С, предпочтительно при температуре от 0°С до 100°С. При необходимости к реакционной смеси добавляют основание (например, имидазол, пиридин, 2,6-лутидин, 4-диметиламинопиридин, гидрид натрия). Количество молей силилирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 3 молей, на моль соединения (2а), и количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (2а). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0250]
Стадия J-3-стадия J-11
Получение на стадии J-3 выполняют в соответствии со стадией А-5 схемы А, получение на стадии J-4 выполняют в соответствии со стадией В-9 схемы В, получение на стадии J-5 выполняют в соответствии со стадией А-7 схемы А, получение на стадии J-6 выполняют в соответствии со стадией А-8 схемы А, получение на стадии J-7 выполняют в соответствии со стадией А-2 схемы А, получение на стадии J-8 выполняют в соответствии со стадией А-10 схемы А, получение на стадии J-9 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии J-10 выполняют в соответствии со стадией А-7 схемы А, и получение на стадии J-11 выполняют в соответствии со стадией С-6 схемы С.
[0251]
Схема K
Схема K представляет собой способ получения соединения (7k), промежуточного соединения, необходимого для получения соединения (1), в котором R11 и R12 объединены совместно с атомами углерода, с которыми связаны R11 и R12, с образованием с ними двойной связи, R13 представляет собой гидроксиметильную группу, и R14 и R15 совместно образуют имин.
[Формула 113]
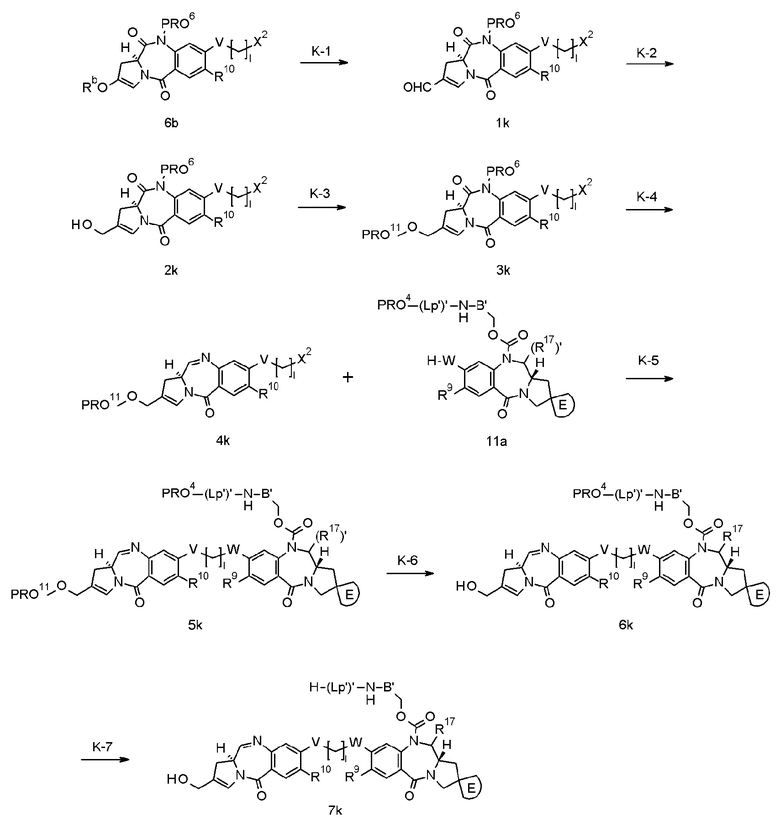
[0252]
Стадия K-1
Данная стадия представляет собой стадию получения соединения (1k), на которой соединение (6b) подвергают реакции карбонилирования.
[0253]
Стадия K-2
Данная стадия представляет собой стадию получения соединения (2k), на которой соединение (1k) подвергают реакции селективного восстановления альдегида.
[0254]
Стадия K-3-стадия K-7
Получение на стадии K-3 выполняют в соответствии со стадией А-2 схемы А, получение на стадии K-4 выполняют в соответствии со стадией В-7 схемы В, получение на стадии K-5 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии K-6 выполняют в соответствии со стадией А-7 схемы А, и получение на стадии K-7 выполняют в соответствии со стадией С-6 схемы С.
[0255]
Схема L
Схема L представляет собой типичный способ получения соединения (В).
[Формула 114]
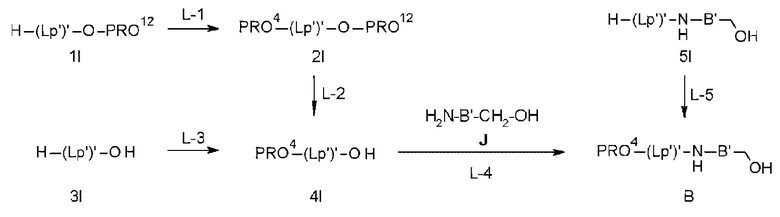
[0256]
Пептидные остатки, представленные общей формулой (Lp')', могут быть получены посредством реакции конденсации аминокислот.
PRO4 защищает N-конец пептидных остатков (Lp')', и PRO12 защищает С-конец.
[0257]
Стадия L-1
Получение на стадии L-1 выполняют в соответствии со стадией В-9 схемы В.
[0258]
Стадия L-2: Реакция удаления защитных групп
В случае, когда PRO12 представляет собой трет-бутильную группу, данную стадию выполняют путем проведения реакции соединения (21) и кислоты (например, трифторуксусной кислоты, n-толуолсульфоновой кислоты, соляной кислоты, уксусной кислоты) в растворителе (дихлорметане или тому подобном) при температуре от 0°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 40°С. Количество молей кислоты, которое следует использовать, составляет от каталитического количества до избыточного количества молей на моль соединения (21). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0259]
Стадия L-3 и стадия L-4
Получение на стадии L-3 выполняют в соответствии со стадией В-9 схемы В, и получение на стадии L-4 выполняют в соответствии со стадией А-4 схемы А.
[0260]
Стадия L-5
В качестве альтернативы соединение (В) может быть получено на стадии L-5 в соответствии со стадией В-9 схемы В.
[0261]
Схема М
Схема М представляет собой способ получения соединения (2).
Соединение (2), представленное в данном способе получения, является синонимом соединения (1), таким образом, R16 в промежуточном соединении согласно настоящему изобретению представляет собой J-La'-Lp'-NH-B'-CH2-О(C=О)-*.
[Формула 115]
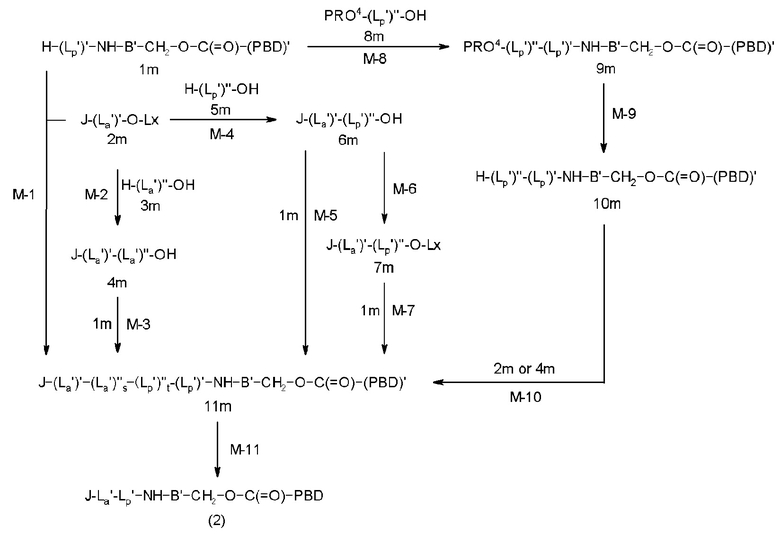
[0262]
Соединение (1m), представленное в данном способе получения, представляет собой соединение (4е), (4f), (11g), (9h), (11i), (12j), (7k) или (8k), полученное в любой из схем от Е до K.
[0263]
(PBD)', представленный в данном способе получения, представляет собой:
[Формула 116]
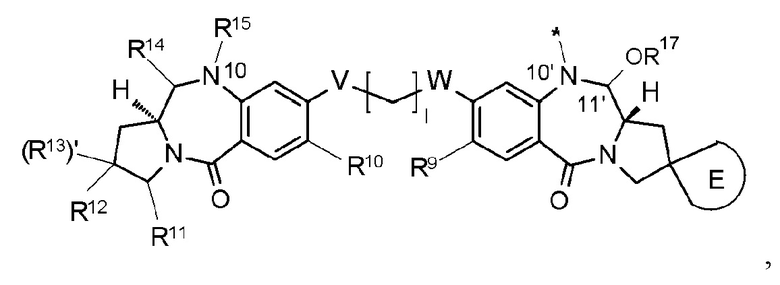
и PBD представляет собой:
[Формула 117]
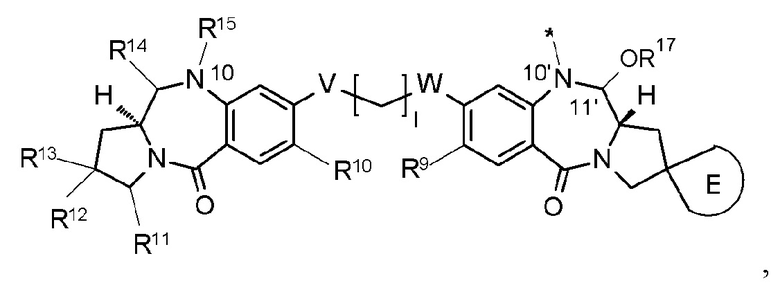
где (PBD)' может быть защищен заместителем (например, гидроксигруппой) при R13 в PBD, а при отсутствии защитной группы (PBD)' является синонимом PBD (R13=(R13)').
В пептидных остатках, представленных (Lp')''t-(Lp')' в данном способе получения, функциональная группа (например, аминогруппа) в боковой цепи аминокислотных остатков, представленных Lp', может быть защищена защитной группой, и в случае, когда защитная группа является незамещенной, (Lp')''t-(Lp')' является синонимом Lp'.
(Lp')' представляет собой аминокислотную последовательность двух аминокислот, представленную ниже, и когда функциональная группа (аминогруппа, гидроксигруппа) присутствует в боковой цепи, (Lp')' может быть защищен: -VA-, (D-)VA-, -FG-, -PI-, -VCit-, -VK-, -PL-, -(D-)P-I- или -GF-.
(Lp')'' представляет собой аминокислотную последовательность двух аминокислот, представленную ниже, и когда функциональная группа (аминогруппа, гидроксигруппа) присутствует в боковой цепи, (Lp')'' может быть защищен:
-GG-, -EGG-, -DG-, -(D-)DG-, -EG-, -GGF-, -SG-, -KG-, -DGG-, -GGF-, -DDGG-, -KDGG- или -GGFG-.
[0264]
(La')' представляет собой любую группу, выбранную из следующих:
-C(=O)-(CH2CH2)n6-C(=O), -C(=O)-(CH2CH2)n6-NH-C(=O)-(CH2CH2O)n7-CH2CH2-С(=O)-, -(СН2)n8-O-С(=O)-, -(СН2)n12-С(=O)- и -(CH2CH2)n13-C(=O)-NH-(CH2CH2O)n14-CH2CH2-C(=O)-
[0265]
(La')'' представляет собой любую группу, выбранную из следующих:
-NH-(CH2CH2)n7-C(=O)- и -NH-(CH2CH2O)n7-CH2-C(=O)-,
и каждый из s и t независимо равен 0 или 1. Например, каждый из s и t равен 0 на стадии М-1, s равен 1 и t равен 0 на стадии М-3, и s равен 0 и t равен 1 на стадии М-5.
[0266]
(La')'-(La')''s является синонимом La'.
При наличии защитной группы (Lp')''t-(Lp')' превращается в Lp' посредством снятия защиты, и является синонимом Lp', если защитная группа отсутствует.
Lx, представленный в данном способе получения, представляет собой атом водорода или уходящую группу (например, гидроксисукцинимид).
PBD или (PBD)' в каждом из 1m, 9m, 10m, 11m и соединения (2), представленных в данном способе получения, образует связь в положении, отмеченном звездочкой (положении N10'), с С(=O)- с правого конца -O-С(=O)-.
[0267]
Стадия М-1
Данная стадия представляет собой способ получения соединения (11m), в котором соединение (1m), полученное в любой из схем от Е до K, и соединение (2m) подвергают реакции конденсации.
В случае, когда Lx=Н и соединение (2m) представляет собой карбоновую кислоту, соединение (2m) может быть получено в соответствии со стадией А-4 схемы А.
В случае, когда Lx представляет собой уходящую группу (например, гидроксисукцинимид, n-нитрофеноксигруппу), данную стадию выполняют путем проведения реакции соединения (1m) и соединения (2m) в растворителе (бензоле, толуоле, диэтиловом эфире, дихлорметане, ТГФ, ДМ ФА, метаноле, воде или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей соединения (2m), которое следует использовать, составляет от 0,9 моля до избыточного количества молей, предпочтительно от 0,9 до 2 молей, на моль соединения (1m). При необходимости к реакционной смеси добавляют основание (например, триэтиламин, N,N-диизопропилэтиламин, N-метилморфолин, 4-диметиламинопиридин, диазабициклоундецен). Количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества, предпочтительно от 1 до 5 молей, на моль соединения (1m). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 36 часов.
[0268]
Стадия М-2-стадия М-5 и стадия М-8
Получение на стадии М-2 выполняют в соответствии со стадией М-1, получение на стадии М-3 выполняют в соответствии со стадией А-4 схемы А, получение на стадии М-4 выполняют в соответствии со стадией М-1, получение на стадии М-5 выполняют в соответствии со стадией А-4 схемы А, и получение на стадии М-8 выполняют в соответствии со стадией А-4 схемы А.
[0269]
Стадия М-6
Данная стадия представляет собой стадию получения активного сложного эфира-промежуточного соединения (7m), на которой соединение (6m) подвергают реакции конденсации.
Данную стадию выполняют путем проведения реакции соединения (6m) и гидроксисукцинимида или тому подобного в растворителе (бензоле, толуоле, диэтиловом эфире, дихлорметане, ТГФ, ДМФА или тому подобном, или растворителе, представляющем собой их смесь) в присутствии конденсирующего агента, такого как N,N-дициклогексилкарбодиимид и 1-этил-3-(3-диметиламинопропил)карбодиимид, при температуре от -30°С до температуры кипения растворителя, используемого для реакции, предпочтительно при температуре от 0°С до 50°С. Количество молей конденсирующего агента, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 5 молей, на моль соединения (6m). Количество молей гидроксисукцинимида, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 моля до 5 молей, на моль соединения (6m). Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 30 минут до 24 часов.
[0270]
Стадия М-7
Данная стадия представляет собой стадию получения соединения (11m), на которой соединение (1m) и соединение (7m) подвергают реакции конденсации, как на стадии М-1.
[0271]
Стадия М-9
Данная стадия представляет собой стадию получения соединения (10m), на которой соединение (9m) подвергают реакции удаления защитных групп. В случае, когда PRO4 представляет собой 9-фторенилметилоксикарбонильную группу, данную стадию выполняют путем проведения реакции соединения (9m) и основания (например, 1,8-диазабицикло[5.4.0]-7-ундецена, пиперидина) в растворителе (ТГФ, дихлорметане, ДМФА или тому подобном, или растворителе, представляющем собой их смесь) при температуре от -20°С до температуры кипения растворителя, предпочтительно при температуре от 0°С до 40°С. Количество молей основания, которое следует использовать, составляет от 1 моля до избыточного количества молей, предпочтительно от 1 до 10 молей, на моль соединения (9m). Время реакции составляет от 1 минуты до 72 часов, и предпочтительно от 5 минут до 24 часов.
[0272]
Стадия М-10
Данная стадия представляет собой стадию получения соединения (11m), на которой соединение (10m) и соединение (2m) или (4m) подвергают реакции конденсации, как на стадии А-4 схемы А.
[0273]
Стадия М-11
Данная стадия представляет собой стадию получения соединения (2), когда (Lp')'t-(Lp')' или PBD' в соединении (11m) имеет защитную группу, путем снятия защиты соединения (11m). Получение выполняют в соответствии со стадией В-3 схемы В и стадией С-6 схемы С.
В случае, когда (Lp')' или PBD' не имеет защитной группы, стадию М-11 опускают, и в этом случае соединение (11m) является синонимом соединения (2).
[0274]
Схема N
Схема N представляет собой способ синтеза соединения в виде свободного лекарственного средства, представленного (1), в котором R11 и R12 объединены совместно с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи, каждый из R14 и R15 представляет собой водород, и R16 и R17 объединены с образованием иминной связи.
[Формула 118]
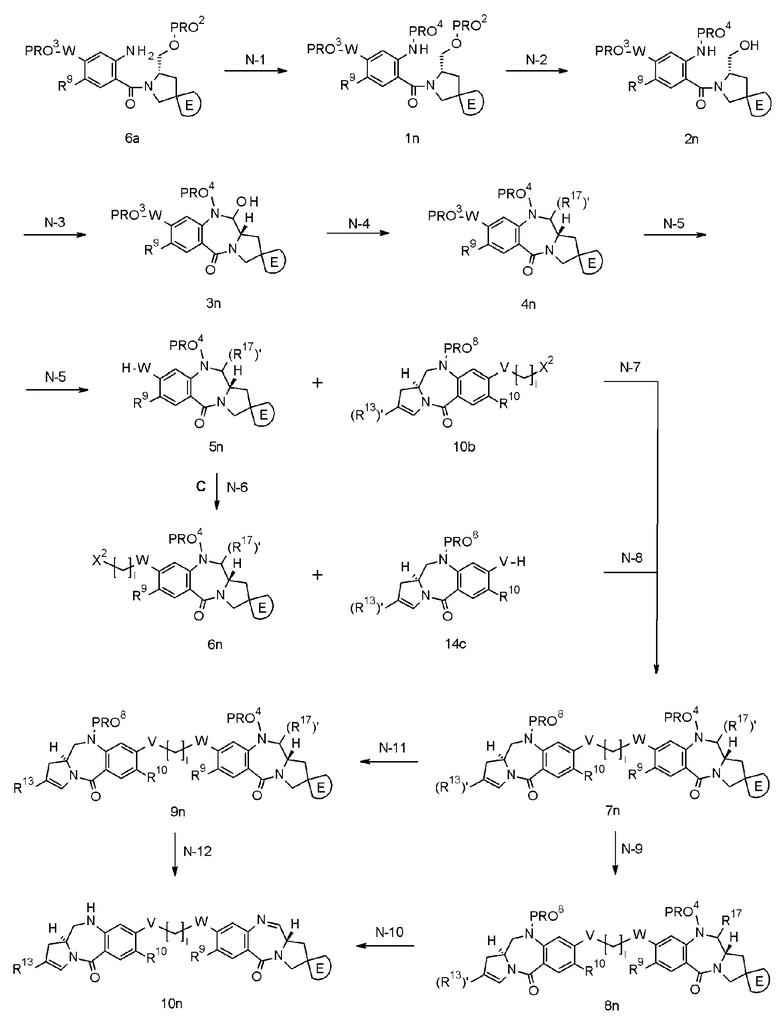
[0275]
Стадия N-1-стадия N-8
Получение на стадии N-1 выполняют в соответствии со стадией В-9 схемы В, получение на стадии N-2 выполняют в соответствии со стадией А-7 схемы А, получение на стадии N-3 выполняют в соответствии со стадией А-8 схемы А, получение на стадии N-4 выполняют в соответствии со стадией А-2 схемы А, получение на стадии N-5 выполняют в соответствии со стадией А-10 схемы А, получение на стадии N-6 выполняют в соответствии со стадией А-11 схемы А, получение на стадии N-7 выполняют в соответствии со стадией Е-1 схемы Е, и получение на стадии N-8 выполняют в соответствии со стадией Е-1 схемы Е.
[0276]
В случае, когда (R13)'=R13, получение выполняют в соответствии со стадией N-9 и стадией N-10, представленными ниже.
[0277]
Стадия N-9
Получение на стадии N-9 выполняют в соответствии со стадией А-7 схемы А.
[0278]
Стадия N-10
В случае, когда защитные группы PRO4 и PRO8 являются одинаковыми, получение выполняют в соответствии со стадией Е-4 схемы Е. В случае, когда защитные группы PRO4 и PRO8 различны, получение выполняют в соответствии со стадиями Е-5 и Е-6 схемы Е.
[0279]
В случае, когда (R13)' имеет защитную группу, получение выполняют в соответствии со стадией N-11 и стадией N-12, представленными ниже.
[0280]
Стадия N-11
Получение выполняют в соответствии со стадией В-3 схемы В.
[0281]
Стадия N-12
В случае, когда защитные группы PRO4 и PRO8 являются одинаковыми, получение выполняют в соответствии со стадиями Е-3 и Е-4 схемы Е. В случае, когда защитные группы PRO4 и PRO8 различны, получение выполняют в соответствии со стадиями Е-3, Е-5 и Е-6 схемы Е.
[0282]
Схема О
Схема О представляет собой способ получения соединения (6о) в виде свободного лекарственного средства, представленного (1), в котором R11 и R12 объединены совместно с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи, R14 и R15 объединены с образованием иминной связи (C=N), и R16 и R17 совместно образуют иминную связь (C=N).
[Формула 119]
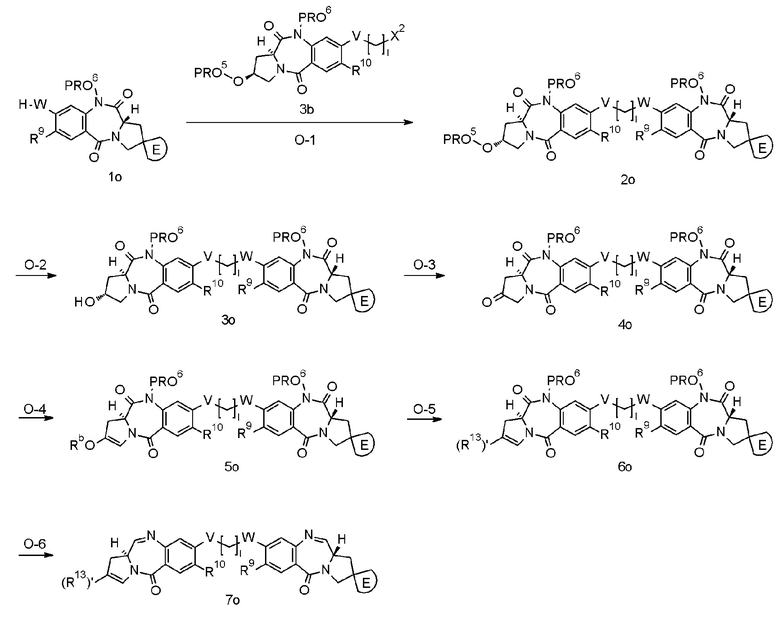
[0283]
Стадия O-1-стадия O-6
Получение на стадии O-1 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии O-2 выполняют в соответствии со стадией В-3 схемы В, получение на стадии O-3 выполняют в соответствии со стадией А-8 схемы А, получение на стадии O-4 выполняют в соответствии со стадией В-5 схемы В, получение на стадии O-5 выполняют в соответствии со стадией В-6 схемы В, и получение на стадии O-6 выполняют в соответствии со стадией В-7 схемы В.
[0284]
Схема Р
Данный способ получения представляет собой способ получения соединения в виде свободного лекарственного средства, представленного (1), в котором R11 представляет собой атом водорода, R12 и R13 объединены с образованием спирокольца, R14 и R15 объединены с образованием иминной связи (C=N), и R16 и R17 совместно образуют иминную связь (C=N). В данном способе получения спирокольцо, образуемое R12 и R13 в соединении (4h), применяемом в качестве исходного вещества, является синонимом Е, и, следовательно, обозначено как Е.
[Формула 120]
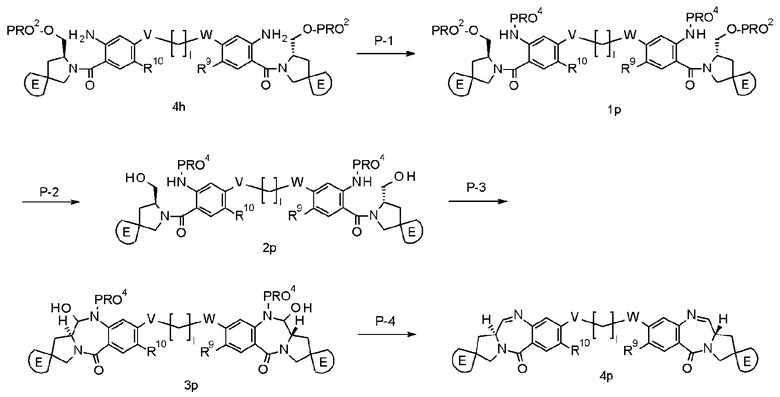
[0285]
Стадия Р-1-стадия Р-4
Получение на стадии Р-1 выполняют в соответствии со стадией В-9 схемы В, получение на стадии Р-2 выполняют в соответствии со стадией В-3 схемы В, получение на стадии Р-3 выполняют в соответствии со стадией А-8 схемы А, и получение на стадии Р-4 выполняют в соответствии со стадией С-6 схемы С.
[0286]
Схема Q
Данный способ получения представляет собой способ получения соединения в виде свободного лекарственного средства, представленного (1), в котором каждый из R11, R14 и R15 представляет собой атом водорода, R12 и R13 объединены с образованием спирокольца, и R16 и R17 объединены с образованием иминной связи (C=N).
[Формула 121]
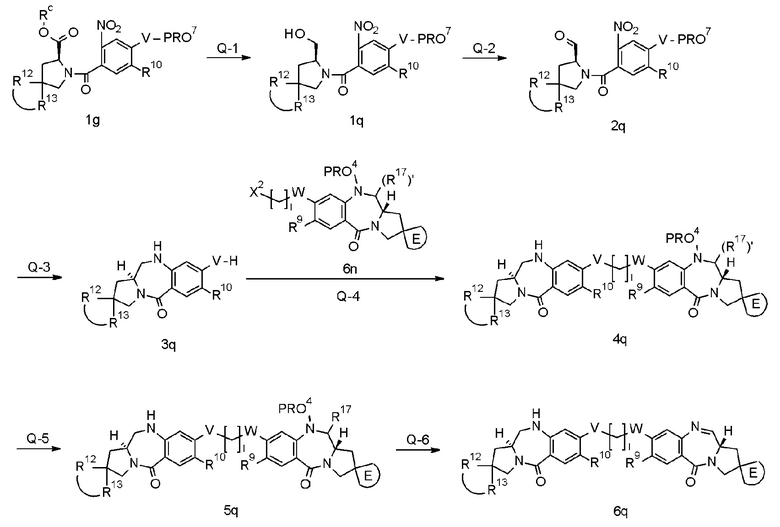
[0287]
Стадия Q-1 -стадия Q-6
Получение на стадии Q-1 выполняют в соответствии со стадией А-1 схемы А, получение на стадии Q-2 выполняют в соответствии со стадией А-8 схемы А, получение на стадии Q-3 выполняют в соответствии со стадией А-5 схемы А, получение на стадии Q-4 выполняют в соответствии со стадией Е-1 схемы Е, получение на стадии Q-5 выполняют в соответствии со стадией А-7 схемы А, и получение на стадии Q-6 выполняют в соответствии со стадией С-6 схемы С.
[0288]
Защитная группа для необязательно защищенных аминогрупп и гидроксигрупп в приведенном выше описании относится к защитной группе, расщепляемой химическим способом, таким как гидрогенолиз, гидролиз, электролиз и фотолиз, и представляет собой защитную группу, обычно используемую в синтетической органической химии (например, см. Protective groups in Organic Synthesis, 3rd Edition, John Wiley & Sons, Inc. (1999)).
«Защитная группа» для необязательно защищенных гидроксигрупп (например, алкилкарбонильная группа, силильная группа или аралкильная группа), «защитная группа» для необязательно защищенных карбоксигрупп (например, C1-С6 алкильная группа или аралкильная группа) и «защитная группа» для необязательно защищенных аминогрупп (например, алкоксикарбонильная группа) не ограничиваются конкретной защитной группой и могут представлять собой любую защитную группу, используемую для гидроксигрупп, карбоксигрупп и аминогрупп, для применения в области синтетической органической химии.
Стадии, для выполнения которых требуется введение или удаление защитных групп, проводят в соответствии с любым известным способом (например, способом, описанным в источнике "Protective groups in Organic Synthesis" (Theodora W. Greene, Peter G. M. Wuts, 1999, опубликованном Wiley-Interscience Publication)).
[0289]
Схема R: Получение антитела
Антитело с ремоделированным гликаном может быть получено с применением способа, представленного на фигуре 3, например, в соответствии со способом, описанным в WO 2013/120066.
[Формула 122]
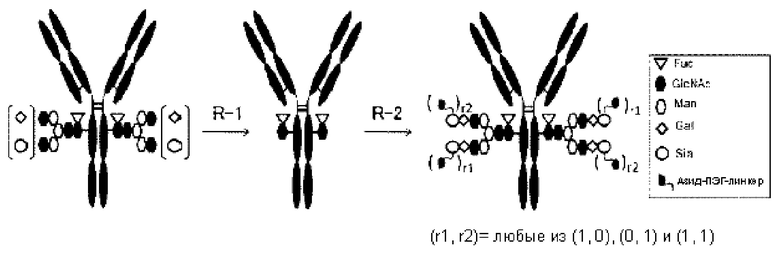
[0290]
Стадия R-1: Гидролиз гликозидной связи GlcNAcβ1-4GlcNAc структуры хитобиозы на восстанавливающем конце
Указанная стадия представляет собой стадию получения антитела, содержащего укороченную форму гликана, путем отщепления N-связанного гликана, присоединенного к аспарагину в положении 297 аминокислотной последовательности целевого антитела (N297-связанного гликана) с применением известной ферментативной реакции.
Целевое антитело (20 мг/мл) в буферном растворе (например, 50 мМ фосфатном буферном растворе) подвергают реакции гидролиза гликозидной связи между GlcNAcβ1 h4GlcNAc в структуре хитобиозы на восстанавливающем конце с применением гидролазы, такой как фермент EndoS, при температуре от 0°С до 40°С. Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 1 часа до 6 часов. Количество фермента EndoS дикого типа, которое следует использовать, составляет от 0,1 до 10 мг, предпочтительно от 0,1 до 3 мг на 100 мг антитела. После завершения реакции проводят очистку с помощью аффинной хроматографии и/или очистку с использованием колонки с гидроксиапатигом, каждая из которых описана ниже, с получением (Fucα1,6)GlcNAc-антитела, содержащего гликан, гидролизованный в положении между GlcNAcβ1 и 4GlcNAc.
[0291]
Стадия R-2: Реакция трансгликозилирования
Указанная стадия представляет собой стадию получения антитела, содержащего ремоделированный гликан, путем образования связи (Fucα1,6) GlcNAc-антитела с оксазолиновой формой гликана MSG- (MSG1-, MSG2-) или SG-типа (далее называемой в настоящем описании «оксазолиновой формой азид-содержащего гликана»), имеющей ПЭГ-линкер, содержащий азидную группу, с применением ферментативной реакции.
Содержащее укороченную форму гликана антитело в буферном растворе (например, фосфатном буферном растворе) подвергают реакции трансгликозилирования путем проведения реакции с оксазолиновой формой азид-содержащего гликана в присутствии каталитического количества трансгликозидазы, такой как EndoS (D233Q/Q303L), при температуре от 0°С до 40°С. Время реакции составляет от 10 минут до 72 часов, и предпочтительно от 1 часа до 6 часов. Количество фермента EndoS (D233Q/Q303L), которое следует использовать, составляет от 1 до 10 мг, предпочтительно от 1 до 3 мг на 100 мг антитела, и количество оксазолиновой формы азид-содержащего гликана, которое следует использовать, составляет от 2 эквивалентов до избыточного количества эквивалентов, предпочтительно от 2 эквивалентов до 20 эквивалентов.
После завершения реакции проводят очистку с помощью аффинной хроматографии и очистку с использованием колонки с гидроксиапатитом с получением очищенного антитела, содержащего ремоделированный гликан.
Оксазолиновая форма азид-содержащего гликана может быть получена в соответствии со способами, описанными в примерах 55-57. С помощью реакции, известной в области синтетической органической химии (например, реакции конденсации), N3-(CH2CH2-O)n5-CH2CH2-NH2, ПЭГ-линкер, содержащий азидную группу (N3-L(ПЭГ)), может быть введен в MSG (MSG1, MSG2) или дисиалооктасахарид (Tokyo Chemical Industry Co., Ltd.). В частности, карбоновая кислота в положении 2 сиаловой кислоты и аминогруппа на правом конце N3-(CH2CH2-O)n5-CH2CH2-NH2 подвергаются реакции конденсации с образованием амидной связи.
Примеры конденсирующего агента при использовании реакции конденсации могут включать, но не ограничиваются ими, N,N'-дициклогексилкарбодиимид (DCC), 1-этил-3-(3-диметиламинопропил)-карбодиимид (EDCI), карбонилдиимидазол (CDI), 2-(2Н-бензотриазол-2-ил)-4-(1,1,3,3-тетраметилбутил)-фенол (ВОР), гексафторфосфат 1H-бензотриазол-1-илокситрипирролидинофосфония (РуВОР) и гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU), и примеры растворителя для указанной реакции могут включать, но не ограничиваются ими, дихлорметан, ДМФА, ТГФ, этилацетат и растворитель, представляющий собой их смесь.
Температура реакции, как правило, составляет от -20°С до 100°С или до температуры кипения растворителя, и предпочтительно находится в диапазоне от -5°С до 50°С. При необходимости может быть добавлено органическое основание, такое как триэтиламин, диизопропилэтиламин, N-метилморфолин и 4-диметиламинопиридин, или неорганическое основание, такое как карбонат калия, карбонат натрия, гидрокарбонат калия и гидрокарбонат натрия. Помимо этого, в качестве катализатора реакции может быть добавлен, например, 1-гидроксибензотриазол или N-гидроксисукцинимид.
MSG, MSG1 или MSG2 могут быть получены путем гидролиза (MSG-)Asn или выделенного/очищенного (MSG1-)Asn или (MSG2-)Asn (пример 56) с помощью гидролазы, такой как EndoM.
Оксазолиновая форма может быть получена из GlcNAc на восстанавливающем конце гликана MSG- (MSG1-, MSG2-) или SG-типа согласно известному источнику (J. Org Chem., 2009, 74(5), 2210-2212. Helv. Chim. Acta, 2012, 95, 1928-1936).
[0292]
При получении содержащего ремоделированный гликан антитела концентрирование водного раствора антитела, определение концентрации и замена буфера могут быть выполнены в соответствии с общими операциями А-С, приведенными ниже.
Общая операция А: Концентрирование водного раствора антитела
Раствор антитела или конъюгата антитело-лекарственное средство помещали в емкость Amicon Ultra (30000-50000 MWCO, Millipore Corporation), и раствор антитела или конъюгата антитело-лекарственное средство, описанного ниже, концентрировали путем центрифугирования (центрифугирование при 2000 G - 4000 G в течение 5-20 минут) с использованием центрифуги (Allegra X-15R, Beckman Coulter, Inc.).
Общая операция В: Определение концентрации антитела
Определение концентрации антитела проводили с помощью прибора для определения поглощения ультрафиолетового излучения (Nanodrop 1000, Thermo Fisher Scientific Inc.) в соответствии со способом, указанным производителем. Затем использовали коэффициенты поглощения при длине волны 280 нм, которые являются различными для антител (от 1,3 мл мг-1 см-1 до 1,8 мл мг-1 см-1).
Общая операция С: Замена буфера для антитела
К водному раствору антитела, который концентрировали в соответствии с общей операцией А, добавляли буферный раствор (например, фосфатно-солевой буфер (рН 6,0), фосфатный буфер (рН 6,0)). Эту операцию выполняли несколько раз, и затем определяли концентрацию антитела в соответствии с общей операцией В и доводили ее до 10 мг/мл с помощью буферного раствора (например, фосфатно-солевого буфера (рН 6,0), фосфатного буфера (рН 6,0)).
[0293]
Схема S: Конъюгирование
Указанный способ получения представляет собой способ получения конъюгата антитело-лекарственное средство путем конъюгирования описанного выше содержащего ремоделированный гликан антитела с промежуточным соединением (2) путем реакции SPAAC (промотируемого напряжением азид-алкинового циклоприсоединения: J. AM. СНЕМ. SOC. 2004, 126, 15046-15047). В приведенной формуле AT представляет собой содержащее ремоделированный гликан антитело.
[Формула 123]
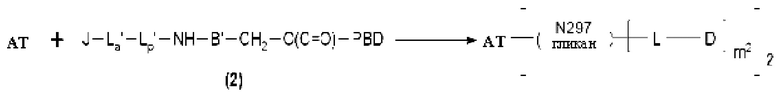
Реакцию SPAAC проводят путем смешивания буферного раствора (раствора ацетата натрия, фосфата натрия, раствора бората натрия, или тому подобного, или их смеси) антитела AT и раствора, содержащего растворенное соединение (2) в подходящем растворителе (диметилсульфоксиде (ДМСО), диметилформамиде (ДМФА), диметилацетамиде (ДМА), N-метил-2-пирролидоне (NMP), пропиленгликоле (ПГ), или тому подобном, или их смеси).
Количество молей соединения (2), которое следует использовать, составляет от 2 молей до избыточного количества молей, предпочтительно от 1 моля до 30 молей на моль антитела, и отношение органического растворителя к буферу для антитела предпочтительно составляет от 1 до 200% об./об. Температура реакции составляет от 0°С до 37°С, и предпочтительно от 10°С до 25°С, и время реакции составляет от 1 до 150 часов, и предпочтительно от 6 часов до 100 часов. рН реакционной смеси составляет от 5 до 9.
[0294]
Соединения-коньюгаты антитело-лекарственное средство (ADC) можно отличить друг от друга путем замены буфера, очистки и определения концентрации антитела и среднего числа молекул коньюгированного лекарственного средства на молекулу антитела в соответствии с общими операциями А-С, описанными выше, и общими операциями D-F, описанными ниже.
[0295]
Общая операция D: Очистка конъюгата антитело-лекарственное средство
Колонку NAP-25 уравновешивали буферным раствором уксусной кислоты (10 мМ, рН 5,5; в настоящем описании обозначен ABS), содержащим коммерчески доступный сорбитол (5%). На эту колонку NAP-25 наносили водный реакционный раствор конъюгата антитело-лекарственное средство (примерно 1,5-2,5 мл) и проводили элюцию буфером в количестве, указанном производителем, для отделения и сбора фракции антитела. Отделенную и собранную фракцию снова наносили на колонку NAP-25, и операцию очистки с помощью гельфильтрации с элюцией буфером повторяли всего два или три раза с получением конъюгата антитело-лекарственное средство, не содержащего несвязанного фрагмента лекарственное средство-линкер, диметилсульфоксида и пропиленгликоля. При необходимости концентрацию раствора конъюгата антитело-лекарственное средство корректировали с помощью общих операций А-С.
Общая операция Е: Определение концентрации антитела в конъюгате антитело-лекарственное средство
Концентрация конъюгированного лекарственного средства в конъюгате антитело-лекарственное средство может быть рассчитана с применением закона Ламберта-Бера, представленного ниже. Выражение (I) с применением закона Ламберта-Бера выглядит следующим образом:
[Выражение 1]
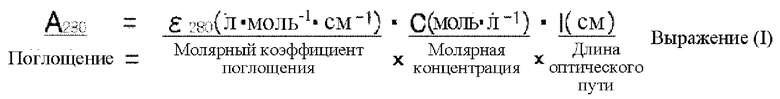
Здесь А280 обозначает поглощение водного раствора конъюгата антитело-лекарственное средство при 280 нм, ε280 обозначает молярный коэффициент поглощения конъюгата антитело-лекарственное средство при 280 нм, и С (моль⋅л-1) обозначает молярную концентрацию конъюгата антитело-лекарственное средство. Из выражения (I) можно определить молярную концентрацию конъюгата антитело-лекарственное средство, С (моль⋅л-1), с помощью выражения (II), представленного ниже.
[Выражение 2]
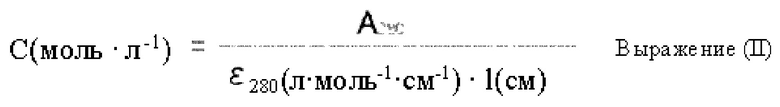
Затем обе части умножают на молярную массу конъюгата антитело-лекарственное средство, М.м. (г⋅моль-1), для определения массовой концентрации конъюгата антитело-лекарственное средство, С' (мг⋅мл-1) (выражение (III)).
[Выражение 3]
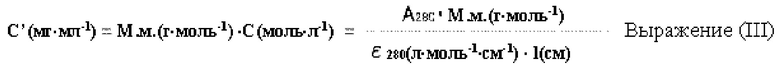
Далее будут описаны значения, используемые в выражениях и применяемые к примерам.
Используемое поглощение А280 представляло собой фактически определенное значение поглощения УФ излучения водным раствором конъюгата антитело-лекарственное средство при 280 нм. Для молярной массы, М.м. (г⋅моль-1), оценочное значение молекулярной массы антитела рассчитывали на основе аминокислотной последовательности антитела и использовали в качестве приблизительного значения молярной массы конъюгата антитело-лекарственное средство. Длина оптического пути, l (см), используемая при выполнении измерения, составляла 1 см.
Молярный коэффициент поглощения, ε280, конъюгата антитело-лекарственное средство может быть определен с помощью выражения (TV), представленного ниже.
[Выражение 4]

Здесь εAb, 280 обозначает молярный коэффициент поглощения антитела при 280 нм, и εDL, 280 обозначает молярный коэффициент поглощения лекарственного средства при 280 нм.
Используя известный метод расчета (Protein Science, 1995, vol. 4, 2411-2423), можно оценить εAb, 280 на основе аминокислотной последовательности антитела. В примерах используемый молярный коэффициент поглощения трастузумаба составлял εAb, 280=215400 (расчетное оценочное значение). Используемый молярный коэффициент поглощения антитела к CLDN6 составлял εAb, 280=221340 (расчетное оценочное значение), используемый молярный коэффициент поглощения антитела к TROP2 составлял εAb, 280=226400 (расчетное оценочное значение), используемый молярный коэффициент поглощения антитела к CD98 составлял εAb, 280=240400 (расчетное оценочное значение), используемый молярный коэффициент поглощения антитела к LPS составлял εAb, 280=230300 (расчетное оценочное значение), и используемый молярный коэффициент поглощения варианта трастузумаба составлял εAb, 280=215057 (расчетное оценочное значение).
εDL, 280 рассчитывали для использования на основе фактически определенного значения, полученного при каждом определении поглощения УФ излучения. В частности, определяли поглощение раствора, содержащего растворенный предшественник конъюгата (лекарственное средство), имеющего определенную молярную концентрацию, и к нему применяли выражение (I), закон Ламберта-Бера, и использовали полученное значение.
[0296]
Общая операция F: Определение среднего числа конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитело-лекарственное средство
Среднее число конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитело-лекарственное средство может быть определено с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) следующим способом.
[F-1. Получение образца для анализа методом ВЭЖХ (восстановление конъюгата антитело-лекарственное средство)]
Раствор конъюгата антитело-лекарственное средство (примерно 1 мг/мл, 60 мкл) смешивают с водным раствором дитиотреитола (ДТТ) (100 мМ, 15 мкл). Смесь инкубируют при 37°С в течение 30 минут для получения образца, в котором расщеплена дисульфидная связь между L-цепью и Н-цепью конъюгата антитело-лекарственное средство, и этот образец используют для анализа методом ВЭЖХ.
[F-2. Анализ методом ВЭЖХ]
Анализ методом ВЭЖХ выполняют при следующих условиях.
Система ВЭЖХ: Agilent 1290 HPLC system (Agilent Technologies)
Детектор: абсорбционный спектрометр ультрафиолетового излучения (определяемая длина волны: 280 нм, 329 нм)
Колонка: ВЕН Phenyl (2,1×50 мм, 1,7 мкм, Waters Acquity)
Температура колонки: 75°С
Подвижная фаза А: 0,1% трифторуксусная кислота (ТФУ)-15% водный раствор изопропилового спирта
Подвижная фаза В: 0,075% ТФУ-15% раствор ацетонитрила в изопропиловом спирте
Программа градиента: 14%-36% (от 0 мин до 15 мин), 36%-80% (от 15 мин до 17 мин), 80%-14% (от 17 мин до 17,1 мин), 14%-14% (от 17,1 мин до 23 мин)
Объем вводимого образца: 5 мкл
[0297]
[F-3. Анализ данных]
[F-3-1] L-цепь с конъюгированной молекулой лекарственного средства (L-цепь с одной конъюгированной молекулой лекарственного средства: L1) и Н-цепь с конъюгированной молекулой (молекулами) лекарственного средства (Н-цепь с одной конъюгированной молекулой лекарственного средства: H1, Н-цепь с двумя конъюгированными молекулами лекарственного средства: H2, Н-цепь с тремя конъюгированными молекулами лекарственного средства: Н3) имеют гидрофобность, повышающуюся пропорционально количеству конъюгированных молекул лекарственного средства, и имеют более длительное время удерживания по сравнению с L-цепью (L0) и Н-цепью (Н0) антитела, не имеющего конъюгированных молекул лекарственного средства, и, следовательно, L0, L1, Н0, H1, H2, и Н3 элюируются в представленном порядке. Хотя в некоторых случаях порядок L1 и Н0 инвертирован, Н0, не имеющая конъюгированных молекул лекарственного средства, не поглощает при длине волны 329 нм, характерной для лекарственных средств. Таким образом, L1 и Н0 можно различить путем определения поглощения при длине волны 329 нм. Посредством сравнения времен удерживания L0 и Н0 каждый обнаруженный пик может быть отнесен к L0, L1, Н0, H1, H2 или Н3.
[F-3-2] Поскольку каждый фрагмент лекарственное средство-линкер поглощает УФ излучение, значения площадей пиков корректируют с помощью следующего выражения с использованием молярных коэффициентов поглощения L-цепи, Н-цепи и фрагмента лекарственное средство-линкер в соответствии с числом конъюгированных молекул лекарственное средство-линкер.
[Выражение 5]
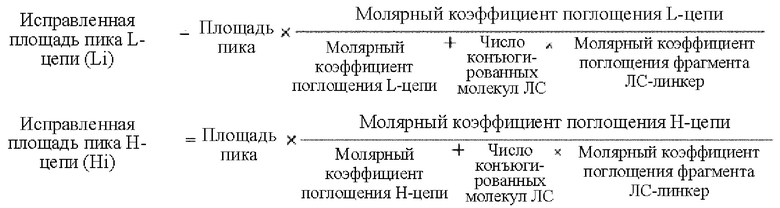
Здесь для молярных коэффициентов поглощения (280 нм) L-цепи и Н-цепи каждого антитела могут быть применены значения, рассчитанные на основе аминокислотных последовательностей L-цепи и Н-цепи антитела с помощью известного метода расчета (Protein Science, 1995, vol. 4, 2411-2423). В случае трастузумаба в качестве молярного коэффициента поглощения L-цепи, определенного на основе аминокислотной последовательности, использовали 26150, и в качестве молярного коэффициента поглощения Н-цепи, определенного на основе аминокислотной последовательности, использовали 81290. В случае антитела к CLDN6, схожим образом, в качестве молярного коэффициента поглощения L-цепи использовали 33140, и в качестве молярного коэффициента поглощения Н-цепи использовали 77280; в случае антитела к TROP2 в качестве молярного коэффициента поглощения L-цепи использовали 26210, и в качестве молярного коэффициента поглощения Н-цепи использовали 68990; в случае антитела к CD98 в качестве молярного коэффициента поглощения L-цепи использовали 41680, и в качестве молярного коэффициента поглощения Н-цепи использовали 78500; в случае антитела к LPS в качестве молярного коэффициента поглощения L-цепи использовали 31710, и в качестве молярного коэффициента поглощения Н-цепи использовали 77470; в случае варианта трастузумаба в качестве молярного коэффициента поглощения L-цепи использовали 26251, и в качестве молярного коэффициента поглощения Н-цепи использовали 81488; и в качестве молярного коэффициента поглощения (280 нм) каждого фрагмента лекарственное средство-линкер использовали молярный коэффициент поглощения (280 нм), определенный для соединения (1) как предшественника конъюгата.
[F-3-3] Отношение площадей пиков (%) каждой цепи к сумме исправленных площадей пиков рассчитывают с помощью следующего выражения.
[Выражение 6]
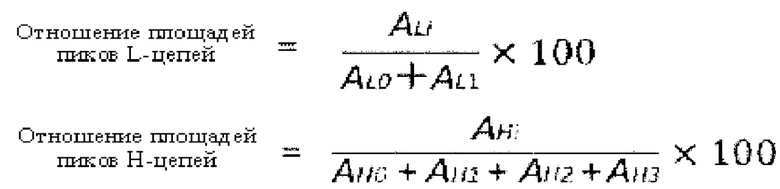
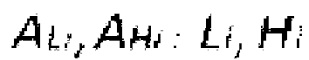 Относительные исправленные площади пиков
Относительные исправленные площади пиков
[F-3-4] Среднее число конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитело-лекарственное средство рассчитывают с помощью следующего выражения:
Среднее число конъюгированных молекул лекарственного средства = (отношение площадей пиков L0 × 0 + отношение площадей пиков L0 × 1 + отношение площадей пиков Н0 × 0 + отношение площадей пиков H1 × 1 + отношение площадей пиков Н2 × 2 + отношение площадей пиков Н3 × 3) / 100 × 2.
[0298]
<Применение в медицине>
Конъюгат антитело-лекарственное средство согласно настоящему изобретению проявляет цитотоксическую активность в отношении раковых клеток, и, следовательно, может быть применено в качестве лекарственного средства, в частности, терапевтического агента и/или профилактического агента против рака.
[0299]
Примеры раковых заболеваний, при которых применим конъюгат антитело-лекарственное средство согласно настоящему изобретению, могут включать рак легкого (например, немелкоклеточный рак легкого, мелкоклеточный рак легкого), рак почки, уротериальный рак, колоректальный рак, рак предстательной железы, мульти формную глиобластому, рак яичника (например, поверхностную эпителиальную опухоль, стромальную опухоль, эмбрионально-клеточную (герминогенную) опухоль), рак поджелудочной железы, рак молочной железы, меланому, рак печени, рак мочевого пузыря, рак желудка, рак пищевода или тому подобное, рак эндометрия, рак яичка (семиному, несеминому), рак шейки матки, плацентарную хориокарциному, опухоль головного мозга и рак головы и шеи, а также их метастатические формы, но не ограничиваются перечисленным в том случае, если раковые клетки в качестве терапевтической мишени экспрессируют белок, распознаваемый антителом, входящим в конъюгат антитело-лекарственное средство.
[0300]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению можно предпочтительно вводить млекопитающим и более предпочтительно вводить людям.
[0301]
Вещества, применяемые в фармацевтической композиции, содержащей конъюгат антитело-лекарственное средство согласно настоящему изобретению, могут быть подходящим образом выбраны и введены из составов с добавками, применяемыми для получения составов, или подобными добавками, которые обычно применяют в данной области, с учетом дозы или концентрации для введения.
[0302]
Конъюгат антитело-лекарственное средство согласно настоящему изобретению могут быть введен в виде фармацевтической композиции, содержащей один или более фармацевтически применимых компонентов. Например, фармацевтическая композиция, как правило, содержит один или более фармацевтических носителей (например, стерилизованную жидкость (в том числе воду и масло (минеральное масло или масло животного происхождения, растительного происхождения или синтетического происхождения (такие как арахисовое масло, соевое масло, минеральное масло и кунжутное масло)))). Вода является наиболее распространенным носителем для внутривенного введения вышеуказанной фармацевтической композиции. Солевой раствор, водный раствор декстрозы и водный раствор глицерина также можно применять в качестве жидкого носителя, в частности, для инъекционного раствора. Подходящие фармацевтические переносящие среды известны в данной области техники. При необходимости вышеуказанная композиция также может содержать следовое количество увлажняющего агента, эмульгирующего агента или буферного агента для доведения рН. Примеры подходящих фармацевтических носителей раскрыты в "Remington's Pharmaceutical Sciences" под ред. Е.W. Martin. Указанные составы соответствуют способу введения.
[0303]
Для введения конъюгата антитело-лекарственное средство согласно настоящему изобретению известны и могут быть применены различные системы доставки. Примеры способов введения могут включать, но не ограничиваются ими, внутрикожные, внутримышечные, внутрибрюшинные, внутривенные и подкожные способы. Введение может быть произведено, например, путем инъекции или болюсной инъекции. В соответствии с конкретным предпочтительным вариантом реализации введение указанной выше конъюгатной формы лиганд-лекарственное средство производят путем инъекции. Парентеральное введение является предпочтительным способом введения.
[0304]
В соответствии с репрезентативным вариантом реализации фармацевтическую композицию назначают в качестве фармацевтической композиции, подходящей для внутривенного введения людям, в соответствии с традиционными методиками. Композиция для внутривенного введения, как правило, представляет собой раствор в стерильном и изотоническом водном буфере. При необходимости лекарство может содержать солюбилизирующий агент и местный анестетик для облегчения боли в месте инъекции (например, лигнокаин). Как правило, вышеуказанные ингредиенты предоставляются либо индивидуально в виде сухого лиофилизированного порошка или безводного концентрата, заключенного в отдельную емкость, что обеспечивают путем запечатывания в ампулу или саше с указанием количества активного агента, либо в виде смеси в единичной лекарственной форме. Когда фармацевтическую композицию необходимо вводить путем инъекции, она может быть введена из резервуара для инъекции, содержащего воду или солевой раствор, которые являются стерильными и относятся к категории фармацевтических. Когда лекарство вводят путем инъекции, ампула стерильной воды или солевого раствора для инъекций может быть предоставлена таким образом, что вышеупомянутые ингредиенты будут добавлены друг к другу перед введением.
[0305]
Фармацевтическая композиция согласно настоящему изобретению может представлять собой фармацевтическую композицию, содержащую только конъюгат антитело-лекарственное средство согласно настоящему изобретению, или фармацевтическую композицию, содержащую конъюгат антитело-лекарственное средство и по меньшей мере один агент для лечения рака, отличный от указанного конъюгата антитело-лекарственное средство. Конъюгат антитело-лекарственное средство согласно настоящему изобретению может быть введен в комбинации с другим агентом для лечения рака и благодаря этому оказываемое противораковое действие может быть усилено. Другие противораковые агенты, применяемые для данной цели, могут быть введены индивидууму одновременно, раздельно или последовательно с конъюгатом антитело-лекарственное средство и могут быть введены с различным интервалом друг относительно друга. Примеры таких агентов для лечения могут включать абраксан, карбоплатин, цисплатин, гемцитабин, иринотекан (СРТ-11), паклитаксел, пеметрексед, сорафениб, винбластин, агенты, описанные в международной публикации №WO 2003/038043, аналоги LH-RH (например, лейпрорелин, гозерелин), эстрамустина фосфат, антагонисты эстрогена (например, тамоксифен, ралоксифен) и ингибиторы ароматазы (например, анастрозол, летрозол, экземестан), но не ограничиваются ими, если они являются агентами, обладающими противоопухолевой активностью.
[0306]
Фармацевтическая композиция может быть получена в виде лиофилизированного состава или жидкого состава в виде состава, имеющего выбранный состав и требуемую чистоту. При приготовлении в виде лиофилизированного состава это может быть состав, содержащий подходящие для получения составов добавки, которые применяют в данной области техники. Также в случае жидкого состава композиция может быть получена в виде жидкого состава, содержащего различные добавки для получения составов, которые применяют в данной области техники.
[0307]
Состав и концентрация фармацевтической композиции могут отличаться в зависимости от способа введения. Однако конъюгат антитело-лекарственное средство, содержащийся в фармацевтической композиции согласно настоящему изобретению, может демонстрировать фармацевтическое действие даже в небольшой дозировке, когда конъюгат антитело-лекарственное средство имеет более высокую аффинность в отношении антигена, что означает более высокую аффинность (меньшее значение Kd) с точки зрения константы диссоциации (значение Kd) в отношении антигена. Таким образом, для определения дозы конъюгата антитело-лекарственное средство такая доза может быть установлена с позиции ситуации, связанной с аффинностью конъюгата антитело-лекарственное средство по отношению к антигену. Когда конъюгат антитело-лекарственное средство согласно настоящему изобретению вводят человеку, может быть введено, например, примерно от 0,001 до 100 мг/кг одномоментно или несколькими порциями с интервалами от 1 до 180 дней.
[0308]
Антитело согласно настоящему изобретению или функциональный фрагмент указанного антитела может быть применены в качестве лекарственного средства. В данном случае указанное выше описание «конъюгата антитело-лекарственное средство» в указанном выше разделе «Применение в медицине» надлежит понимать как описание «антитела или функционального фрагмента антитела».
[0309]
Кроме того, в качестве лекарственного средства может быть применено свободное лекарственное средство согласно настоящему изобретению (новое соединение-производное PBD), соль свободного лекарственного средства и их гидраты. В данном случае указанное выше описание «конъюгата антитело-лекарственное средство» в указанном выше разделе «Применение в медицине» надлежит понимать как описание «свободного лекарственного средства (нового соединения-производного PBD), соли свободного лекарственного средства и их гидратов».
Примеры
[0310]
Настоящее изобретение будет конкретно описано со ссылкой на представленные ниже примеры, однако настоящее изобретение не ограничено указанными примерами. Примеры не следует рассматривать в качестве ограничения в любом смысле. Реагенты, растворители и исходные вещества без какого-либо описания в настоящем документе могут быть легко получены из коммерчески доступных источников поставки.
[0311]
Сравнительный пример 1: Трастузумаб-тезирин
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К 5 мМ раствора трастузумаба (сравнительный пример 3) в солевом растворе с добавлением этилендиаминтетраацетат-фосфатного буфера (рН 6,5) (9,91 мг/мл, 0,70 мл), добавляли при 20°С водный раствор дикалия фосфата (1,0 М, 0,0112 мл) и водный раствор трис(2-карбоксиэтил)фосфина гидрохлорида (10 мМ, 0,0086 мл) и проводили реакцию при 20°С в течение 60 минут, а затем при комнатной температуре в течение 30 минут. К раствору реакционной смеси добавляли раствор тезирина (0,36 мг), синтезированного в соответствии с литературой (Med. Chem. Lett. 2016, 7, 983-987), в диметилацетамиде (0,0415 мл) и проводили реакцию при комнатной температуре в течение 1 часа. К раствору реакционной смеси добавляли водный раствор N-ацетилцистеина (100 мМ, 0,0024 мл) и проводили реакцию в течение 30 минут до завершения реакции.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 3,5 мл раствора целевого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,40 мг/мл, выход антител: 4,90 мг (71%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 2,0.
[0312]
Сравнительный пример 2: Антитело к CLDN6 (H1L1)-тезирин
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К 5 мМ раствора антитела к CLDN6 (H1L1) в солевом растворе с добавлением этилендиаминтетраацетат-фосфатного буфера (рН 6,5) (9,87 мг/мл, 0,45 мл) добавляли при 20°С водный раствор дикалия фосфата (1,0 М, 0,0072 мл) и водный раствор трис(2-карбоксиэтил)фосфина гидрохлорида (10 мМ, 0,0041 мл) и проводили реакцию при 20°С в течение 90 минут. К раствору реакционной смеси добавляли раствор тезирина (0,15 мг), синтезированного в соответствии с литературой (Med. Chem. Lett. 2016, 7, 983-987) в N,N-диметилацетамиде (0,0277 мл) и проводили реакцию при 20°С в течение 1 часа. К раствору реакционной смеси добавляли водный раствор N-ацетилцистеина (100 мМ, 0,001 мл) и проводили реакцию в течение 30 минут до завершения реакции.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 3,5 мл раствора целевого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,56 мг/мл, выход антител: 3,90 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 2,1.
[0313]
Сравнительный пример 3: Антитело к HER2-трастузумаб
Антитело к HER2 получали в соответствии с US 5821337. Аминокислотные последовательности легкой цепи и тяжелой цепи трастузумаба представлены SEQ ID NO: 64 и SEQ ID NO: 65, соответственно.
[0314]
Сравнительный пример 4: Антитело к LPS h#1G5-H1L1
Антитело к LPS получали в соответствии с WO 2015/046505. Аминокислотные последовательности легкой цепи и тяжелой цепи h#1G5-H1L1 представлены SEQ ID NO: 66 и SEQ ID NO: 67, соответственно.
[0315]
Сравнительный пример 5: Антитело к TROP2 hRS7
Антитело к TROP2 получали в соответствии с WO 2003/074566 и WO 2015/098099 (сравнительный пример 1). Аминокислотные последовательности легкой цепи и тяжелой цепи hRS7 представлены SEQ ID NO: 68 и SEQ ID NO: 69, соответственно.
[0316]
Сравнительный пример 6: Антитело к CD98 hM23-H1L1
Антитело к CD98 получали в соответствии с WO 2015/146132. Аминокислотные последовательности легкой цепи и тяжелой цепи hM23-H1L1 представлены SEQ ID NO: 70 и SEQ ID NO: 71, соответственно.
[0317]
[Синтез промежуточного соединения]
Пример 1: Промежуточное соединение 1
[Формула 124]
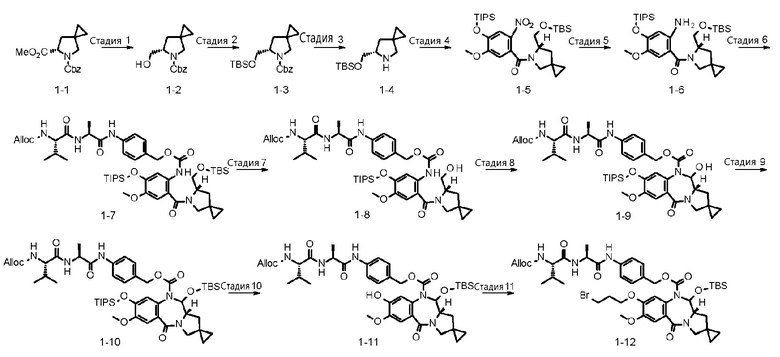
Стадия 1: Бензил-(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гептан-5-карбоксилат
К раствору 5-бензил-6-метил-(6S)-5-азаспиро[2,4]гептан-5,6-дикарбоксилата (104 ммоль, WO 2012087596) в ТГФ (500 мл) добавляли небольшими порциями борогидрид лития (4,30 г, 178 ммоль) при 0°С. Полученный продукт перемешивали при 0°С в течение 30 минут и затем перемешивали при комнатной температуре в течение 2 часов. Добавляли при 0°С воду (180 мл) и 2 н. соляную кислоту (186 мл) и полученный продукт подвергали перегонке при пониженном давлении. Полученный остаток подвергали экстракции этилацетатом четыре раза и органический слой промывали солевым раствором и затем сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток (27,9 г, 90%) непосредственно применяли для последующей реакции.
[0318]
Стадия 2: Бензил-(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гептан-5-карбоксилат
К раствору соединения, полученного на стадии 1 (27,9 г, 107 ммоль) и имидазолу (14,5 г, 214 ммоль) в дихлорметане (300 мл) добавляли при комнатной температуре трет-бутилдиметилсилилхлорид (24,2 г, 160 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 18 часов. Реакционный раствор промывали насыщенным водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и солевым раствором, сушили над безводным сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии насиликагеле [гексан:этилацетат = 100:0 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (32,5 г, 81%).
1Н-ЯМР (CDCl3) δ: 7,39-7,34(5Н,m), 5,23-5,11(2Н,m), 4,10-3,48(4Н,m), 3,16-3,14 (1Н,m), 2,15-2,04(1Н,m), 1,81-1,77(1Н,m), 0,91-0,88(9Н,m), 0,65-0,55(4Н,m), 0,08-0,01(6Н,m).
МС (ХИАД) m/z: 376(М+Н)+
[0319]
Стадия 3: (6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гептан
К раствору соединения, полученного на стадии 2 (32,5 г, 86,5 ммоль), в этаноле (400 мл) добавляли при комнатной температуре 7,5% палладий-углеродный катализатор (содержание влаги: 54%, 5,00 г) и полученный продукт перемешивали в атмосфере водорода при комнатной температуре в течение 6 часов. Реакционный раствор фильтровали через целит и фильтрат подвергали перегонке при пониженном давлении, получая желаемое соединение (21,3 г, количественный выход).
1H-ЯМР (CDCl3) δ: 3,79-3,77(1H,m), 3,71-3,69(1H,m), 3,65-,60(1H,m), 3,01-2,98(2H,m), 1,81-1,71(2H,m), 0,90(9H,s), 0,65-0,57(4H,m), 0,08(3H,s), 0,07(3H,s).
МС (ХИАД, ИЭР) m/z: 242(М+Н)+
[0320]
Стадия 4: [(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил](5-метокси-2-нитро-4-{[три(пропан-2-ил)силил]окси}фенил)метанон
К раствору 5-метокси-2-нитро-4-{три(пропан-2-ил)силил]окси}бензойной кислоты (52,2 г, 141 ммоль, US 20150283262) и 1-гидроксибензотриазола моногидрата (23,8 г, 155 ммоль) в дихлорметане (500 мл), добавляли N,N'-дициклогексилкарбодиимид (35,0 г, 170 ммоль) при охлаждении льдом. Реакционную смесь перемешивали при комнатной температуре. После того, как карбоновая кислота исчезла, медленно по каплям добавляли раствор соединения, полученного на стадии 3 (34,1 г, 141 ммоль) и триэтиламина (29,4 мл, 212 ммоль) в дихлорметане (100 мл). После перемешивания реакционного раствора при комнатной температуре в течение ночи к реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия и реакционную смесь подвергали экстракции хлороформом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом магния. Полученный продукт подвергали перегонке при пониженном давлении и к полученному остатку добавляли этилацетат и диэтиловый эфир и твердое содержимое удаляли фильтрованием и фильтрат подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 25:75 (об./об.)], получая желаемое соединение (55,0 г, 66%).
1H-ЯМР (CDCl3) δ: 7,72-7,66(1H,m), 6,80-6,73(1H,m), 4,53-4,49(1H,m), 4,04-3,95(1H,m), 3,91-3,88(3H,m), 3,59-3,54(1H,m), 3,36-3,25(0,5H,m), 3,01-2,96(1,5H,m), 2,24-2,20(0,3H,m), 2,09-2,05(0,7H,m), 2,00-1,97(0,7H,m), 1,69-1,67(0,3H,m), 1,32-1,24(3H,m), 1,12-1,05(18H,m), 0,93-0,91(6H,m), 0,79-0,77(3H,m), 0,71-0,62(2H,m), 0,57-0,40(2H,m), 0,12-0,10(4H,m), 0,11-0,15(2H,m).
MC (ХИАД, ИЭР) m/z: 593(M+H)+
[0321]
Стадия 5: (2-Амино-5-метокси-4- {[три(пропан-2-ил)силил]окси}фенил)[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]метанон
К раствору соединения, полученного на стадии 4 (55,0 г, 92,8 ммоль) в этаноле (300 мл), добавляли 7,5% палладий на углероде (10,0 г) в атмосфере азота. Баллон с азотом немедленно заменяли баллоном с водородом и реакционную смесь интенсивно перемешивали в атмосфере водорода при комнатной температуре. После того, как исходные вещества были израсходованы, реакционную смесь фильтровали и фильтрат подвергали перегонке при пониженном давлении, получая желаемое соединение (52,2 г, 100%), которое непосредственно применяли для последующей реакции.
1H-ЯМР (CDCl3) δ: 6,71(1H,s), 6,25(1H,s), 4,55-4,28(2H,m), 3,97(1H,m), 3,75-3,62(3H,m), 3,70(3H,s), 3,09-3,07(1H,m), 2,24-2,19(1H,m), 1,81-1,68(1H,m), 1,27-1,22(3H,m), 1,09-1,05(18H,m), 0,90(9H,s), 0,65-0,46(4H,m), 0,07-0,03(6H,m).
МС (ХИАД, ИЭР) m/z: 563(M+H)+
[0322]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-аланинамид
К раствору соединения, полученного на стадии 5 (18,6 г, 33,0 ммоль) и триэтиламину (6,26 мл, 45,2 ммоль) в ТГФ (300 мл) медленно добавляли трифосген (4,22 г, 14,2 ммоль) на этанол-ледяной бане. После добавления смешанный раствор N-[(проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-(гидроксиметил)фенил]-L-аланинамида (11,4 г, 30,2 ммоль, WO 2011130598) и триэтиламина (6,26 мл, 45,2 ммоль) в ТГФ (100 мл) и N,N-диметилформамиде (30 мл) медленно добавляли по каплям к охлажденной льдом реакционной смеси. После добавления по каплям ледяную баню удаляли и реакционную смесь перемешивали в атмосфере азота при 40°С. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и реакционную смесь подвергали экстракции этилацетатом. Органический слой промывали солевым раствором и сушили над безводным сульфатом натрия. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 40:60 (об./об.)], получая желаемое соединение (23,5 г, 74%).
1H-ЯМР (CDCl3) δ: 8,99(1H,m), 8,58(1H,s), 7,80(1H,s), 7,55-7,53(2H,m), 7,34-7,32(2H,m), 6,77-6,75(2H,m), 5,94-5,87(1H,m), 5,40-5,38(1H,m), 5,33-5,29(1H,m), 5,23-5,21(1H,m), 5,13(1H,m), 5,10(2H,m), 4,69-4,64(1H,m), 4,62-4,52(2H,m), 4,06-4,03(1H,m), 3,98(1H,m), 3,76-3,65(6H,m), 3,04(1H,m), 2,28-2,26(1H,m), 2,18-2,13(1H,m), 1,46(3H,m), 1,32-1,25(3H,m), 1,11-1,09(18H,m), 0,99-0,84(15H,m), 0,65-0,40(4H,m), 0,08-0,00(6H,m).
MC (ХИАД, ИЭР) m/z: 966(M+H)+
[0323]
Стадия 7: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-аланинамид
К раствору соединения, полученного на стадии 6 (23,5 г, 24,3 ммоль в ТГФ (50 мл), метаноле (50 мл) и воде (44 мл), добавляли уксусную кислоту (200 мл) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре. После того, как исходные вещества были израсходованы, реакционную смесь подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (18,0 г, 87%).
1Н-ЯМР (CDCl3) δ: 8,64-8,62(1Н,m), 8,50(1Н,m), 7,69(1Н,m), 7,55-7,53(2Н,m), 7,34-7,32(2Н,m), 6,79-6,75(3Н,m), 5,91-5,89(1Н,m), 5,39(1Н,m), 5,32-5,29(1Н,m), 5,23-5,21(1Н,m), 4,68-4,54(4Н,m), 4,31(1Н,m), 4,06-4,04(1Н,m), 3,81-3,79(3H,m), 3,76(3H,s), 3,63-3,61(1H,m), 3,13-3,11(1H,m), 2,16-2,13(1H,m), 1,87-1,81(2Н,m), 1,46-1,43(3Н,m), 1,30-1,24(3Н,m), 1,12-1,08(18Н,m), 0,98-0,91(6Н,m), 0,63-0,45(4Н,m).
МС (ХИАД, ИЭР) m/z: 852(M+H)+
[0324]
Стадия 8: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору диметилсульфоксида (3,75 мл, 52,8 ммоль) в дихлорметане (300 мл) медленно добавляли по каплям оксалилхлорид (2,17 мл, 25,3 ммоль) в атмосфере азота при -78°С. После указанного добавления по каплям реакционную смесь перемешивали при -78°С. К реакционной смеси медленно добавляли раствор соединения, полученного на стадии 7 (18,0 г, 21,1 ммоль), в дихлорметане (50,0 мл). К раствору реакционной смеси добавляли триэтиламин (14,6 мл, 105 ммоль) при -78°С. После добавления охлаждающую баню удаляли и температуру медленно повышали до комнатной температуры. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и реакционную смесь подвергали экстракции хлороформом (200 мл). Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом магния. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 0:60 (об./об.)], получая желаемое соединение (16,5 г, 92%).
1Н-ЯМР (CDCl3) δ: 8,51-8,36(1H,m), 7,54-7,38(2H,m), 7,22-7,07(3Н,m), 6,73-6,64(1Н,m), 5,94-5,87(2Н,m), 5,33-5,22(3Н,m), 5,09(1Н,m), 4,97(1Н,m), 4,64-4,58(4Н,m), 4,02-4,00(1Н,m), 3,86-3,83(3Н,m), 3,75-3,70(1Н,m), 3,61-3,54(2Н,m), 3,38-3,29(1Н,m), 2,40(1Н,m), 2,16-2,14(1Н,m), 1,74-1,71(1 Н,m), 1,44(3Н,m), 1,18-1,16(3Н,m), 1,05-1,00(18Н,m), 0,97-0,92(6Н,m), 0,72-0,60(4Н,m).
МС (ХИАД, ИЭР) m/z: 850(M+H)+
[0325]
Стадия 9: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 8 (12,0 г, 14,1 ммоль) и 2,6-лутидину (6,58 мл, 56,5 ммоль) в дихлорметане (200 мл) медленно добавляли по каплям трет-бутилдиметилсилилтрифторметилсульфонат (9,73 мл, 42,3 ммоль) в атмосфере азота при 0°С. После перемешивания при охлаждении льдом в течение 10 минут, ледяную баню удаляли и проводили перемешивание при комнатной температуре. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и реакционную смесь подвергали экстракции хлороформом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0(об./об.) до 25:75(об./об.)], получая желаемое соединение (8,12 г, 60%).
1Н-ЯМР (CDCl3) δ: 8,67-8,45(1Н,m), 7,50-7,44(2H,m), 7,19(1H,s), 7,13(2H,m), 6,95(2H,m), 6,62-6,57(2H,m), 6,01(1H,m), 5,95-5,86(1Н,m), 5,33-5,13(3Н,m), 4,82(1Н,m), 4,65-4,54(3Н,m), 4,03-4,01(1Н,m), 3,84-3,82(3Н,m), 3,73-3,66(1Н,m), 3,50-3,48(1Н,m), 3,27(1Н,m), 2,37-2,33(1Н,m), 2,19-2,13(1H,m), 1,54-1,43(3H,m), 1,22-1,13(3H,m), 1,10-1,00(18H,m), 0,97-0,91(6H,m), 0,81(9H,s), 0,76-0,59(4H,m), 0,19-0,09(6H,m).
MC (ХИАД, ИЭР) m/z: 964(M+H)+
[0326]
Стадия 10: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 9 (8,12 г, 8,42 ммоль) в N,N-диметилформамиде (90 мл) и воде (2 мл), добавляли ацетат лития (0,611 г, 9,26 ммоль) и полученный продукт перемешивали при комнатной температуре. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (5,48 г, 81%).
1H-ЯМР (CDCl3) δ: 8,76-8,60(1H,m), 8,02-7,56(1H,m), 7,45-7,44(2H,m), 7,21(1H,s), 7,10-7,09(2H,m), 6,81-6,74(1H,m), 6,65(1H,s), 6,23(1H,s), 6,01-5,99(1H,m), 5,95-5,84(1H,m), 5,41-5,20(2H,m), 5,16(1H,m), 4,84(1H,m), 4,67-4,54(4H,m), 4,05-4,03(1H,m), 3,87(3H,s), 3,71(1H,m), 3,55-3,51(1H,m), 3,26(1H,m), 2,35(1H,m), 2,18-2,12(1H,m), 1,55-1,42(3H,m), 0,97-0,92(6H,m), 0,81 (9H,s), 0,76-0,61 (4H,m), 0,20-0,06(6H,m).
MC (ХИАД, ИЭР) m/z: 808(M+H)+
[0327]
Стадия 11: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-8'-(3-бромпропокси)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 10 (2,40 г, 2,97 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 4, получая желаемое соединение (2,73 г, 99%).
1Н-ЯМР (ДМСО-D6) δ: 10,01-9,86(1Н,m), 8,24-8,04(2Н,m), 7,64-7,54(2Н,m), 7,32-7,14(4Н,m), 6,59-6,48(1Н,m), 5,94-5,88(2Н,m), 5,32-4,76(5Н,m), 4,44-4,38(3Н,m), 3,87-3,81(5Н,m), 3,64-3,55(2Н,m), 3,41(1Н,m), 3,14(1Н,m), 2,45-2,09(4Н,m), 1,97-1,94(1Н,m), 1,44-1,30(4H,m), 0,89-0,53(9H,m), 0,79(9H,s), 0,13-0,06(6Н,m).
МС (ХИАД, ИЭР) m/z: 930 [81Br,(M+H)+], 928 [79Br,(M+H)+].
[0328]
Пример 2: Промежуточное соединение 2
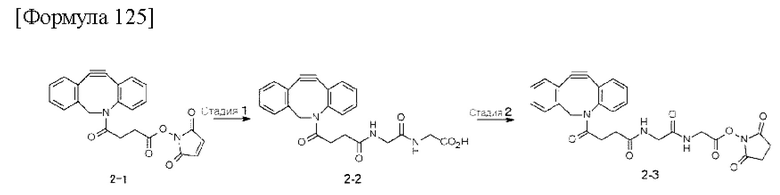
Стадия 1: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил] глицилглицин
К смеси глицилглицина (0,328 г, 2,49 ммоль), N,N-диизопропилэтиламина (0,433 мл, 2,49 ммоль) и N,N-диметилформамида (20 мл), добавляли при комнатной температуре 1-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]окси}пирролидин-2,5-дион (1,00 г, 2,49 ммоль, Click Chemistry Tools) и воду (10 мл) и полученный продукт перемешивали при комнатной температуре в течение ночи. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:CMW=100:0(об./об.) до 0:100(об./об.)], получая желаемое соединение (0,930 г, 89%). CMW означает органический слой для распределения с соотношением хлороформ:метанол:вода = 7:3:1 (об./об./об.).
1H-ЯМР (ДМСО-D6) δ: 12,58(1H,s), 8,14-8,12(1H,m), 8,08-8,07(1H,m), 7,69-7,68(1H,m), 7,62-7,61(1H,m), 7,53-7,45(3H,m), 7,40-7,29(3H,m), 5,05-5,01(1H,m), 3,73-3,72(2H,m), 3,66-3,60(3H,m), 2,66-2,60(1H,m), 2,33-2,24(1H,m), 2,08-2,04(1H,m), 1,81-1,77(1Н,m).
MC (ХИАД, ИЭР) m/z: 420[(M+H)+].
[0329]
Стадия 2: 2,5-диоксопирролидин-1-ил-N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицинат
К раствору соединения, полученного на стадии 1 (0,612 г, 1,46 ммоль)) и N-гидроксисукцинимиду (0,168 г, 1,459 ммоль) в дихлорметане (6 мл), добавляли 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид (0,420 г, 2,19 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 21 часа. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:CMW=100:0(об./об.) до 0:100(об./об.)], получая желаемое соединение (0,375 г, 50%). CMW означает органический слой для распределения с соотношением хлороформ:метанол:вода = 7:3:1(об./об./об.).
[0330]
Пример 3: Лекарственное средство-линкер 1
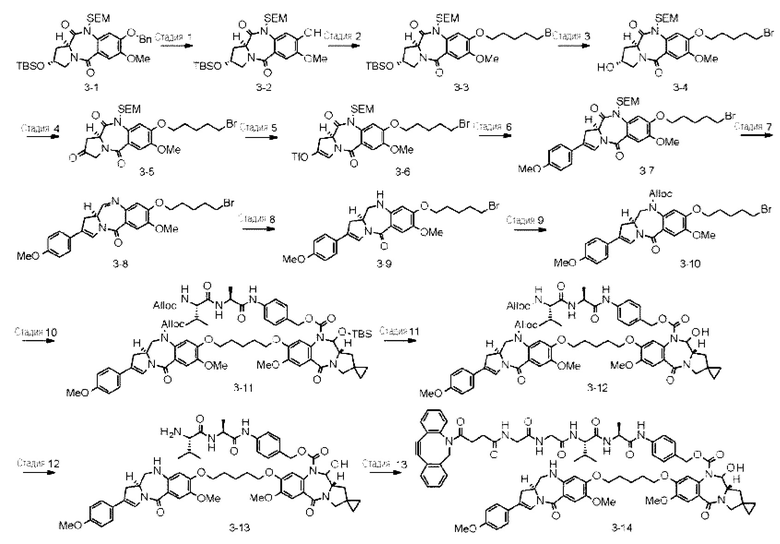
Стадия 1: (2R,11aS)-2-{[трет-бутил(диметил)силил]окси}-8-гидрокси-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11 (10Н,11аН)-дион
К раствору (2R,11aS)-8-(бензилокси)-2-{[трет-бутил(диметил)силил]окси}-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигадро-1Н-пирроло[2,1-с][1,4]бегосдиазепин-5,11(10Н,11аН)-диона (25,5 г, 41,6 ммоль, WO 2016149546) в ТГФ (150 мл) и этаноле (150 мл) добавляли 5% палладий на углероде (содержание влаги: 54%, 10,0 г) в атмосфере азота и реакционный раствор затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 дней. К раствору реакционной смеси добавляли хлороформ, полученную смесь фильтровали через целит и затем фильтрат подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 100:0 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (19,4 г, 89%).
1Н-ЯМР (CDCl3) δ: 7,36(1H,s), 7,25(1H,s), 6,01(1H,s), 5,45-5,43(1H,m), 4,69-4,67(1Н,m), 4,60-4,55(1H,m), 4,23-4,21(1H,m), 3,96(3H,s), 3,76-3,68(2H,m), 3,63-3,61(1H,m), 3,56-3,53(1H,m), 2,88-2,83(1H,m), 2,03-2,00(1H,m), 1,00-0,98(2H,m), 0,87(9H,s), 0,10(6H,s), 0,02(9H,s).
MC (ХИАД, ИЭР) m/z: 523(M+H)+
[0331]
Стадия 2: (2R,11aS)-8-[(5-Бромпентил)окси]-2-{[трет-бутил(диметил)силил]окси}-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11(10Н, 11аН)-дион
К раствору соединения, полученного на стадии 1 (10,8 г, 20,7 ммоль) в N,N-диметилформамиде (30 мл), добавляли 1,5-дибромпентан (23,8 г, 103 ммоль) и карбонат калия (3,43 г, 24,8 ммоль) при комнатной температуре. После перемешивания при комнатной температуре в течение 3 часов к раствору реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом. Полученный органический слой промывали солевым раствором и сушили над сульфатом натрия и подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 90:10 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (14,5 г, количественный выход).
1H-ЯМР (CDCl3) δ: 7,34(1H,s), 7,21(1H,s), 5,52-5,49(1H,m), 4,63-4,62(1H,m), 4,58-4,55(1H,m), 4,24-4,22(1H,m), 4,07-4,04(2H,m), 3,92(3H,s), 3,82-3,64(3H,m), 3,56-3,53(1H,m), 3,45-3,43(2H,m), 2,86-2,84(1H,m), 2,04-2,00(1H,m), 1,97-1,87(4H,m), 1,66-1,62(2H,m), 1,01-0,98(2H,m), 0,87(9H,s), 0,10(6H,s), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 673[81Br, (M+H)+], 671[79Br, (M+H)+].
[0332]
Стадия 3: (211,11aS)-8-[(5-Бромпентил)окси]-2-гидрокси-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11(10Н, 11аН)-дион
К раствору соединения, полученного на стадии 2 (21,5 ммоль) в ТГФ (40 мл), добавляли 1 моль/л раствора тетрабутиламмонийфторида (28,0 мл, 28,0 ммоль) в ТГФ при 0°С. После перемешивания при комнатной температуре в течение 30 минут, к раствору реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом и полученный органический слой промывали солевым раствором. Полученный продукт сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 97,5:2,5 (об./об.) до 92,5:7,5 (об./об.)], получая желаемое соединение (11,3 г, 94%).
1H-ЯМР (CDCl3) δ: 7,34(1H,s), 7,21(1H,s), 5,53-5,50(1H,m), 4,69-4,64(2H,m), 4,32-4,30(1H,m), 4,10-4,00(2H,m), 3,91(3H,s), 3,88-3,75(2H,m), 3,73-3,64(2H,m), 3,45-3,44(2H,m), 2,99-2,96(1Н,m), 2,15-2,09(1H,m), 1,99-1,85(5H,m), 1,68-1,62(2H,m), 1,01-0,95(2H,m), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 559[81Br, (M+H)+], 557[79Br, (M+H)+].
[0333]
Стадия 4: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-10-{[2-(триметилсилил)этокси]метил}-1H-пирроло [2,1-c][1,4]бензодиазепин-2,5,11 (3Н,10Н,11аН)-трион
Соединение, полученное на стадии 3 (11,3 г, 20,2 ммоль), тетрабутиламмония бромид (0,325 г, 1,01 ммоль) и бромид калия (0,240 г, 2,02 ммоль) растворяли в насыщенном водном растворе гидрокарбоната натрия (60 мл)/дихлорметане (60 мл), к которому добавляли nor-AZADO (0,0279 г, 0,202 ммоль) и пентагидрат гипохлорита натрия (2,03 г, 27,2 ммоль) при 0°С и полученный продукт перемешивали при 0°С в течение 30 минут. Поскольку оставались исходные материалы, к нему добавляли пентагидрат гипохлорита натрия (1,00 г, 13,4 ммоль) при 0°С и полученный продукт перемешивали при 0°С в течение 15 минут. К нему дополнительно добавляли пентагидрат гипохлорита натрия (0,300 г, 4,03 ммоль) при 0°С и полученный продукт перемешивали при 0°С в течение 15 минут и исчезновение исходных материалов подтверждали с помощью ТСХ. К раствору реакционной смеси добавляли водный раствор тиосульфат натрия и полученную смесь подвергали экстракции хлороформом и полученный органический слой сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 75:25(об./об.) до 40:60(об./об.)], получая желаемое соединение (9,74 г, 87%).
1H-ЯМР (CDCl3) δ: 7,33(1H,s), 7,24(1H,s), 5,56-5,53(1H,m), 4,71-4,69(1H,m), 4,66-4,63(1H,m), 4,27-4,22(1H,m), 4,12-4,02(2H,m), 3,93-3,88(4H,m), 3,82-3,75(1H,m), 3,69-3,67(1H,m), 3,61-3,56(1H,m), 3,46-3,44(2H,m), 2,82-2,77(1H,m), 1,97-1,89(4H,m), 1,68-1,64(2H,m), 1,05-0,93(2H,m), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 557[81Br, (M+H)+], 555[79Br, (M+H)+].
[0334]
Стадия 5: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-5,11-диоксо-10-{[2-(триметилсилил)этокси]метил}-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-2-илтрифторметансульфонат
К раствору соединения, полученного на стадии 4 (9,74 г, 17,5 ммоль) в дихлорметане (160 мл), добавляли 2,6-лутидин (8,17 мл, 70,1 ммоль) при -40°С и полученный продукт перемешивали при -40°С в течение 10 минут. К раствору реакционной смеси добавляли безводную трифторметансульфоновую кислоту (8,85 мл, 52,6 ммоль) при -40°С и полученный продукт перемешивали при -40°С в течение 30 минут. К реакционному раствору, добавляли 10% водный раствор лимонной кислоты и полученную смесь подвергали экстракции хлороформом и полученный органический слой сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 95:5 (об./об.) до 70:35 (об./об.)] и затем очищали с помощью NH2-силикагелевой хроматографии [гексан:этилацетат = 95:5 (об./об.) до 65:35 (об./об.)], получая желаемое соединение (7,10 г, 59%).
1H-ЯМР (CDCl3) δ: 7,32(1H,s), 7,24(1H,s), 7,15-7,14(1H,m), 5,56-5,53(1H,m), 4,70-4,68(1Н,m), 4,66-4,63(1Н,m), 4,11-4,01(2Н,m), 3,94-3,90(4Н,m), 3,84-3,75(1Н,m), 3,73-3,68(1Н,m), 3,46-3,44(2Н,m), 3,18-3,14(1Н,m), 1,96-1,88(4Н,m), 1,69-1,61(2Н,m), 1,02-0,92(2H,m), 0,04(9H,s).
МС (ХИАД, ИЭР) m/z: 689[81Br, (M+H)+], 687[79Br, (M+H)+].
[0335]
Стадия 6: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-2-(4-метоксифенил)-10-{[2-(триметилсилил)этокси]метил}-1H-пирроло[2,1-с][1,4]бензодиазепин-5,11(10Н,11аН)-дион
К смеси соединения, полученного на стадии 5 (2,00 г, 2,91 ммоль), 4-метоксифенилбороновой кислоты (0,884 г, 5,82 ммоль), тетракис(трифенилфосфин)палладия (0) (0,336 г, 0,291 ммоль) и карбоната натрия (1,23 г, 11,6 ммоль) добавляли при комнатной температуре толуол (20 мл), этанол (10 мл) и воду (10 мл). Реакционный раствор перемешивали при комнатной температуре в течение 30 минут и реакционный раствор затем экстрагировали этилацетатом и полученный экстракт промывали водой и солевым раствором. Органический слой сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 90:10 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (1,71 г, 91%).
1H-ЯМР (CDCl3) δ: 7,38-7,37(3H,m), 7,33(1H,s), 7,25(1H,s), 6,89-6,88(2H,m), 5,56-5,54(1H,m), 4,71-4,68(1H,m), 4,65-4,62(1H,m), 4,09-4,04(2H,m), 3,96-3,91(4H,m), 3,85-3,66(5H,m), 3,46-3,45(2H,m), 3,16-3,12(1H,m), 1,99-1,94(4H,m), 1,69-1,64(2H,m), 1,00-0,98(2H,m), 0,04(9H,s).
МС (ХИАД, ИЭР) m/z: 647[81Br, (M+H)+], 645[79Br, (M+H)+].
[0336]
Стадия 7: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-2-(4-метоксифенил)-1,11а-дигидро-5Н-пирроло[2,1-с][1,4]бензодиазепин-5-он
Соединение, полученное на стадии 6 (0,789 г, 1,22 ммоль), растворяли в этаноле (10 мл) и ТГФ (10 мл) и к нему добавляли 2,0 М тетрагидрофурановый раствор борогидрида лития (6,11 мл, 12,2 ммоль) при 0°С и полученный продукт перемешивали при 0°С в течение 3 часов. К раствору реакционной смеси добавляли воду и полученную смесь подвергали экстракции хлороформом и полученный органический слой сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток растворяли в дихлорметане (10 мл), этаноле (20 мл) и воде (10 мл), к полученной смеси добавляли силикагель (4 г) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 4 дней. Силикагель удаляли посредством фильтрации и к нему добавляли воду и полученный продукт подвергали экстракции хлороформом. Полученный органический слой сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 60:40 (об./об.) до 25:75 (об./об.)], получая желаемое соединение (0,496 г, 81%).
1H-ЯМР (CDCl3) δ: 7,90-7,89(1H,m), 7,53(1H,s), 7,40-7,40(1H,m), 7,35-7,34(2H,m), 6,92-6,90(2H,m), 6,83-6,81(1H,m), 4,43-4,40(1H,m), 4,13-4,06(2H,m), 3,96(3H,s), 3,84(3H,s), 3,61-3,57(1H,m), 3,47-3,36(3H,m), 2,00-1,92(4H,m), 1,67-1,63(2H,m).
MC (ХИАД, ИЭР) m/z: 501[81Br, (M+H)+], 499[79Br, (M+H)+].
[0337]
Стадия 8: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-2-(4-метоксифенил)-1,10,11,11а-тетрагидро-5Н-пирроло[2,1-c][1,4]бензодиазепин-5-он
К раствору соединения, полученного на стадии 7 (0,496 г, 0,992 ммоль) в дихлорметане (20 мл), добавляли триацетоксиборогидрид натрия (0,421 г, 1,99 ммоль) при 0°С. После перемешивания при комнатной температуре в течение 2 часов к нему добавляли насыщенный водный раствор гидрокарбоната натрия и полученный продукт подвергали экстракции хлороформом. Органический слой сушили над сульфатом натрия и подвергали перегонке при пониженном давлении и полученный остаток затем очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 60:40 (об./об.) до 25:75 (об./об.)], получая желаемое соединение (0,426 г, 86%).
1H-ЯМР (CDCl3) δ: 7,53-7,53(2H,m), 7,32-7,30(2H,m), 6,89-6,87(2H,m), 6,05(1H,s), 4,33-4,27(2H,m), 4,00-3,98(2H,m), 3,86(3H,s), 3,82(3H,s), 3,57-3,55(2H,m), 3,42-3,38(3H,m), 2,76-2,72(1Н,m), 1,96-1,88(4H,m), 1,65-1,62(2H,m).
MC (ХИАД, ИЭР) m/z: 503[81Br, (M+H)+], 501[79Br, (M+H)+].
[0338]
Стадия 9: Проп-2-ен-1-ил (11aS)-8-[(5-бромпентил)окси]-7-метокси-2-(4-метоксифенил)-5-оксо-11,11а-дигидро-1Н-пирроло[2,1-с][1,4] бензодиазепин-10(5Н)-карбоксилат
К раствору соединения, полученного на стадии 8 (0,426 г, 0,849 ммоль) в дихлорметане (30 мл), добавляли пиридин (0,102 мл 1,27 ммоль) и аллилхлорформиат (0,374 мл, 3,54 ммоль) при 0°С и полученный продукт перемешивали при 0°С в течение 15 минут. К реакционному раствору, добавляли 10% водный раствор лимонной кислоты и полученную смесь подвергали экстракции хлороформом и полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и затем сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 90:10 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (0,465 г, 94%).
1H-ЯМР (CDCl3) δ: 7,38(1H,s), 7,31-7,29(2H,m), 7,26-7,25(1H,m), 6,89-6,87(2H,m), 6,71(1H,s), 5,80-5,78(1H,m), 5,14-5,11(2H,m), 4,65-4,62(1H,m), 4,39-4,26(3H,m), 4,03-4,01(2H,m), 3,92(3H,s), 3,82(3H,s), 3,66-3,64(1H,m), 3,46-3,44(2H,m), 3,30-3,27(1H,m), 2,72-2,68(1H,m), 1,96-1,88(4H,m), 1,68-1,60(2H,m).
МС (ХИАД, ИЭР) m/z: 587[81Br, (M+H)+], 585[79Br, (M+H)+].
[0339]
Стадия 10: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-{[5-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил}окси)пентил]окси}-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 10 примера 1 (0,130 г, 0,161 ммоль) и соединения, полученного на стадии 9 (0,104 г, 0,177 ммоль) в N,N-диметилформамиде (3 мл) добавляли карбонат калия (0,0266 г, 0,193 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение ночи. Реакционный раствор разбавляли этилацетатом и промывали воду и солевым раствором и затем сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток затем очищали с помощью NH2-колоночной хроматографии на силикагеле [гексан:этилацетат = 70:30 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (0,184 г, 87%).
1H-ЯМР (CDCl3) δ: 8,76(1H,s), 7,58-7,56(2H,m), 7,39(1H,s), 7,32-7,30(2H,m), 7,26-7,24(2H,m), 7,19-7,17(3H,m), 6,90-6,88(2H,m), 6,78(1H,s), 6,68-6,66(1H,m), 6,37(1H,s), 5,99-5,93(3H,m), 5,34-5,20(6H,m), 4,66-4,01(11H,m), 3,90(3H,s), 3,89(3H,s), 3,78-3,54(9H,m), 3,31-3,28(2H,m), 2,73-2,69(1H,m), 2,38-2,35(1H,m), 2,19-2,13(1H,m), 1,82-1,80(2H,m), 1,46-1,29(6H,m), 0,98-0,90(6H,m), 0,83(9H,s), 0,69-0,63(4H,m), 0,19-0,16(6H,m).
MC (ХИАД, ИЭР) m/z: 1312(M+H)+
[0340]
Стадия 11: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-{[5-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пентил]окси}-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 10 (0,1837 г, 0,140 ммоль) и уксусной кислоты (0,048 мл, 0,840 ммоль) в ТГФ (5,00 мл) добавляли 1 моль/л тетрагидрофуранового раствора фторида тетрабутиламмония (0,700 мл, 0,700 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 3 часов. Реакционный раствор разбавляли этилацетатом и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и солевым раствором и затем сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью хроматографии на силикагеле [хлороформ:метанол = 99,5:0,5(об./об.) до 95:5(об./об.)], получая желаемое соединение (0,178 г, количественный выход).
1H-ЯМР (CDCl3) δ: 8,86(1H,s), 7,60-7,59(2H,m), 7,39(1H,s), 7,32-7,20(7H,m), 6,90-6,88(2H,m), 6,78(1H,s), 6,68(1H,s), 6,38(1H,s), 5,90-5,87(3H,m), 5,39-5,22(6H,m), 4,72-4,02(11H,m), 3,90(3H,s), 3,88(3H,s), 3,83(3H,s), 3,70-3,63(6H,m), 3,32-3,29(3H,m), 2,73-2,69(1Н,m), 2,43-2,40(1Н,m), 2,12-2,06(1H,m), 1,77-1,74(2H,m), 1,39-1,25(6H,m), 0,96-0,89(6H,m), 0,73-0,66(4H,m).
MC (ХИАД, ИЭР) m/z: 1198(M+H)+
[0341]
Стадия 12: L-Валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 11 (0,140 ммоль) в дихлорметане (2 мл) добавляли пирролидин (0,0579 мл, 0,700 ммоль) и тетракис(трифенилфосфин)палладий (0) (0,0162 г, 0,0140 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 15 минут. После перегонки при пониженном давлении полученный остаток очищали с помощью хроматографии на силикагеле [хлороформ:метанол = 99,5:0,5(об./об.) до 92,5:7,5(об./об.)], получая желаемое соединение (0,143 г, 99%).
1H-ЯМР (CDCl3) δ: 9,12(1H,s), 7,94-7,92(1H,m), 7,57-7,53(4H,m), 7,33-7,31(2H,m), 7,20-7,18(3H,m), 6,90-6,88(2H,m), 6,36(1H,s), 6,07(1H,s), 5,91-5,88(1H,m), 5,47-5,44(1H,m), 5,21-5,13(1H,m), 4,66-4,58(3H,m), 4,32(1H,s), 4,03-3,49(17H,m), 3,38-3,29(4H,m), 3,15-3,14(1H,m), 2,77-2,73(1H,m), 2,57(2H,s), 2,43-2,40(1H,m), 2,32-2,27(1H,m), 1,81-1,39(8H,m), 0,98-0,96(3H,m), 0,85-0,83(3H,m), 0,75-0,62(4H,m).
1H-ЯМР (CD3OD,50°C) δ: 7,84(1H,s), 7,56-7,48(2H,m), 7,44-7,32(4H,m), 7,26-7,13(3H,m), 6,89(2H,d, J=8,5 Гц), 6,78-6,66(1H,m), 6,26(1H,s), 5,96(1H,d,J=9,7 Гц,H11'), 5,27(1H,d,J=12,1 Гц), 4,96-4,78(1H,m), 4,63-4,58(2H,m), 4,49(1H,q,J=6,9Гц,4,28-4,19(1H,m), 4,07-3,89(4H,m), 3,85(3H,s), 3,79(3H,s), 3,76(3H,s), 3,67(1H,d,J=11,5Гц,3,61(1H,d,J=13,3Гц), 3,54(1H,dd,J=9,7,8,2Гц,H11'a), 3,43-3,31(2H,m), 3,21(1H,d,J=11,5Гц), 3,14(1H,d,J=4,8Гц), 2,78(1H,dd,J=16,6,4,5Гц), 2,43(1H,dd,J=13,0,8,2Гц,H1'b), 2,05-1,93(1H,m), 1,91-1,75(4H,m), 1,73-1,55(2H,m), 1,69(1H,d,J=13,3Гц,H1'a), 1,40(3H,d,J=7,3Гц), 0,96(3H,d,J=6,7Гц), 0,89(3H, d, J=7,3Гц), 0,76-0,58(4Н,m).
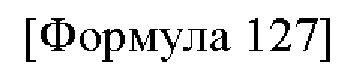
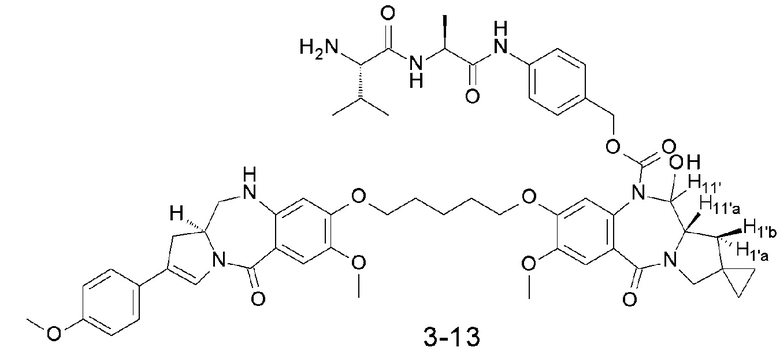
MC (ХИАД, ИЭР) m/z: 1030(M+H)+
[0342]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К смеси соединения, полученного на стадии 1 примера 2 (0,0640 г, 0,153 ммоль) и N-этоксикарбонил-2-этокси-1,2-дигидрохинолина (0,0446 г, 0,180 ммоль) добавляли дихлорметан (2 мл) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 15 минут. К реакционному раствору добавляли раствор соединения, полученного на стадии 13 (0,143 г, 0,139 ммоль) в дихлорметане (2 мл) и полученный продукт перемешивали при комнатной температуре в течение 5 часов и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 99,5:0,5 (об./об.) до 92,5:7,5 (об./об.)], получая желаемое соединение (0,103 г, 52%).
Таблица 1: Положения пиков протонного ЯМР и МС для лекарственного средства-линкера 1
1Н-ЯМР (ДМСО-D6) δ: 9,93(1Н,s), 8,21-8,16(2Н,m), 8,07-8,04(1Н,m), 7,83-7,64(2Н,m), 7,60-7,55(3Н,m), 7,51-7,28(10Н,m), 7,19-7,16(2Н,m), 7,10-7,04(1Н,m), 6,92-6,90(2Н,m), 6,76-6,70(1Н,m), 6,39(1H,s), 5,77-5,75(1Н,m), 5,21-5,18(1Н,m), 5,03-4,99(1Н,m), 4,82-4,79(1Н,m), 4,37-4,35(1Н,m), 4,21-4,20(2Н,m), 4,02-3,24(26Н,m), 3,16-3,13(1Н,m), 2,79-2,59(2Н,m), 2,39-2,28(2Н,m), 2,05-1,97(2Н,m), 1,91-1,77(4Н,m), 1,57-1,54(3Н,m), 1,28-1,23(3Н,m), 0,85-0,80(6Н,m), 0,67-0,61(4Н,m).
МС (ХИАД, ИЭР) m/z: 1431 (М+Н)+
[0343]
Пример 4: Лекарственное средство-линкер 2
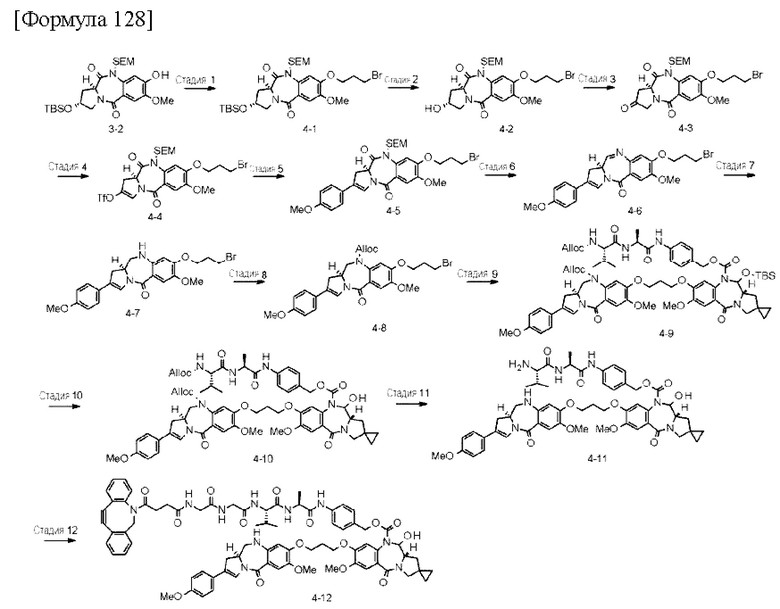
Стадия 1: (2R,11aS)-8-(3-Бромпропокси)-2-{[трет-бутил(диметил)силил]окси}-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11 (10Н, 11аН)-дион
Соединение, полученное на стадии 1 примера 3 (5,06 г, 9,67 ммоль), и 1,3-дибромпропан (4,93 мл, 48,4 ммоль) подвергали реакции таким же образом, как и на стадии 2 примера 3, получая желаемое соединение (4,85 г, 78%).
1H-ЯМР (CDCl3) δ: 7,35(1H,s), 7,26(1H,s), 5,52-5,50(1H,m), 4,65-4,63(1H,m), 4,61-4,55(1H,m), 4,25-4,14(3H,m), 3,92(3H,s), 3,82-3,62(5H,m), 3,57-3,54(1H,m), 2,86-2,84(1H,m), 2,41-2,39(2H,m), 2,06-1,99(1H,m), 1,03-0,97(2H,m), 0,87(9H,s), 0,10(6H,s), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 645[81Br, (M+H)+], 643[79Br, (M+H)+].
[0344]
Стадия 2: (2R,11aS)-8-(3-Бромпропокси)-2-гидрокси-7-метокси-10-{[2-(триметилсилил)этокси]метил}-2,3-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11(10Н,11аН)-дион
Соединение, полученное на стадии 1 (4,85 г, 7,54 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 3, получая желаемое соединение (4,05 г, количественный выход).
1H-ЯМР (CDCl3) δ: 7,35(1H,s), 7,26(1H,s), 5,53-5,51(1H,m), 4,66-4,61(2H,m), 4,32-4,30(1H,m), 4,21-4,16(2H,m), 3,91-3,85(4H,m), 3,82-3,74(1H,m), 3,71-3,59(4H,m), 2,99-2,96(1H,m), 2,43-2,37(2H,m), 2,15-2,09(2H,m), 1,04-0,96(2H,m), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 531[81Br, (M+H)+], 529[79Br, (M+H)+].
[0345]
Стадия 3: (11aS)-8-(3-Бромпропокси)-7-метокси-10-{[2-(триметилсилил)этокси]метил}-1H-пирроло[2,1-c][1,4]бензодиазепин-2,5,11 (3Н,10Н,11аН)-трион
Соединение, полученное на стадии 2 (7,54 ммоль), подвергали реакции таким же образом, как и на стадии 4 примера 3, получая желаемое соединение (3,73 г, 93%).
1H-ЯМР (CDCl3) δ: 7,34(1H,s), 7,29(1H,s), 5,56-5,53(1H,m), 4,72-4,69(1H,m), 4,67-4,61(1H,m), 4,23-4,17(3H,m), 3,97-3,88(4H,m), 3,82-3,75(1H,m), 3,74-3,56(4H,m), 2,82-2,77(1H,m), 2,43-2,3 8(2H,m), 1,06-0,94(2H,m), 0,08-0,00(9H,m).
[0346]
Стадия 4: (11aS)-8-(3-Бромпропокси)-7-метокси-5,11-диоксо-10-{[2-(триметилсилил)этокси]метил}-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-2-илтрифторметансульфонат
Соединение, полученное на стадии 3 (3,73 г, 7,08 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 3, получая желаемое соединение (3,27 г, 70%).
1H-ЯМР (CDCl3) δ: 7,33(1H,s), 7,29(1H,s), 7,15-7,15(1H,m), 5,56-5,54(1H,m), 4,70-4,65(2H,m), 4,21-4,18(2H,m), 3,94-3,91(4H,m), 3,81-3,79(1H,m), 3,70-3,64(3H,m), 3,19-3,15(1Н,m), 2,47-2,3 8(2H,m), 1,02- 1,00(2H,m), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 661[81Br, (M+H)+], 659[79Br, (M+H)+].
[0347]
Стадия 5: (11aS)-8-(3-Бромпропокси)-7-метокси-2-(4-метоксифенил-10-{[2-(триметилсилил)этокси]метил }-1H-пирроло [2,1-c] [1,4]бензодиазепин-5,11(10Н,11аН)-дион
Соединение, полученное на стадии 4 (3,27 г, 4,96 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (2,49 г, 81%).
1H-ЯМР (ДМСО-D6) δ: 7,49-7,47(2H,m), 7,40(1H,s), 7,31-7,24(2H,m), 6,93-6,88(2H,m), 5,33-5,31(1H,m), 5,25-5,18(1H,m), 4,81-4,80(1H,m), 4,23-4,10(2H,m), 3,85(3H,s), 3,77(3H,s), 3,70-3,59(3H,m), 3,52-3,40(2H,m), 3,15-3,08(1H,m), 2,33-2,27(2H,m), 0,86-0,74(2H,m), -0,07(9H,s).
MC (ХИАД, ИЭР) m/z: 619[81Br, (M+H)+], 617[79Br, (M+H)+].
[0348]
Стадия 6: (11aS)-8-(3-Бромпропокси)-7-метокси-2-(4-метоксифенил)-1,11а-дигидро-5Н-пирроло[2,1-с][1,4]бензодиазепин-5-он
Соединение, полученное на стадии 5 (2,49 г, 4,04 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (1,59 г, 84%).
МС (ХИАД, ИЭР) m/z: 473[81Br, (M+H)+], 471[79Br, (M+H)+].
[0349]
Стадия 7: (11aS)-8-(3-Бромпропокси)-7-метокси-2-(4-метоксифенил)-1,10,11,11а-тетрагидро-5Н-пирроло[2,1-c] [1,4]бензодиазепин-5-он
Соединение, полученное на стадии 6 (1,59 г, 3,38 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (1,39 г, 87%).
1H-ЯМР (CDCl3) δ: 7,54(1H,s), 7,54-7,51(1H,m), 7,32-7,29(2H,m), 6,89-6,87(2H,m), 6,10(1H,s), 4,32-4,28(2H,m), 4,14-4,13(2H,m), 3,85(3H,s), 3,82(3H,s), 3,63-3,62(2H,m), 3,57-3,55(2H,m), 3,40-3,36(1H,m), 2,76-2,72(1H,m), 2,40-2,37(2H,m).
МС (ХИАД, ИЭР) m/z: 475[81Br, (M+H)+], 473[79Br, (M+H)+].
[0350]
Стадия 8: Проп-2-ен-1-ил (11aS)-8-(3-бромпропокси)-7-метокси-2-(4-метоксифенил)-5-оксо-11,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 7 (1,40 г, 2,95 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,885 г, 54%).
1H-ЯМР (CDCl3) δ: 7,34(1H,s), 7,27-7,25(2H,m), 7,22(1H,s), 6,86-6,84(2H,m), 6,73(1H,s), 5,76-5,74(1H,m), 5,11-5,09(2H,m), 4,62-4,59(2H,m), 4,33-4,31(1H,m), 4,16-4,13(3H,m), 3,88(3H,s), 3,79(3H,s), 3,60-3,59(3H,m), 3,27-3,23(1Н,m), 2,69-2,65(1H,m), 2,37-2,34(2H,m).
МС (ХИАД, ИЭР) m/z: 559[81Br, (M+H)+], 557[79Br, (M+H)+].
[0351]
Стадия 9: N-{[(Проп-2-ен-1-ил)окси]карбонил}-L-валил-N-[4-({[(11'aS)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-{[(проп-2-ен-1-ил)окси]карбонил}-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11'а-дигидро-1'Н,3'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбонил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 8 (0,0381 г, 0,0683 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,0712 г, 81%).
МС (ХИАД, ИЭР) m/z: 1284(M+H)+.
[0352]
Стадия 10: N-{[(Проп-2-ен-1-ил)окси]карбонил}-L-валил-N-[4-({[(11'aS)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-{[(проп-2-ен-1-ил)окси]карбонил}-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11'а-дигидро-1'Н,3'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбонил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 9 (0,0712 г, 0,0554 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,0671 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 1170(M+H)+.
[0353]
Стадия 11: L-Валил-N-[4-({[(11'aS)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11'а-дигидро-1'Н,3'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбонил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 10 (0,0571 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0574 г, 99%).
1H-ЯМР (CDCl3) δ: 9,16(1H,s), 7,93-7,91(1H,m), 7,55-7,52(1H,m), 7,50-7,47(3H,m), 7,35-7,32(2H,m), 7,21 (1H,s), 7,13-7,11(2H,m), 6,90-6,87(2H,m), 6,40(1H,s), 6,08(1H,s), 5,90-5,87(1H,m), 5,37-5,34(1H,m), 4,73-4,53(3H,m), 4,23-4,08(5H,m), 3,89(3H,s), 3,82(3H,s), 3,78-3,72(5H,m), 3,57-3,51(3H,m), 3,38-3,30(3H,m), 2,76-2,71(1H,m), 2,36-2,24(4H,m), 1,78-1,42(6H,m), 1,00-0,98(3H,m), 0,87-0,84(3H,m), 0,74-0,62(4H,m).
MC (ХИАД, ИЭР) m/z: 1002(M+H)+.
[0354]
Стадия 12: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-[4-({[(11'aS)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11'а-дигидро-1'Н,3'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбонил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 11 (0,189 г, 0,189 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,169 г, 64%).
МС (ХИАД, ИЭР) m/z: 1402(M+H)+.
[0355]
Пример 5: Лекарственное средство-линкер 3
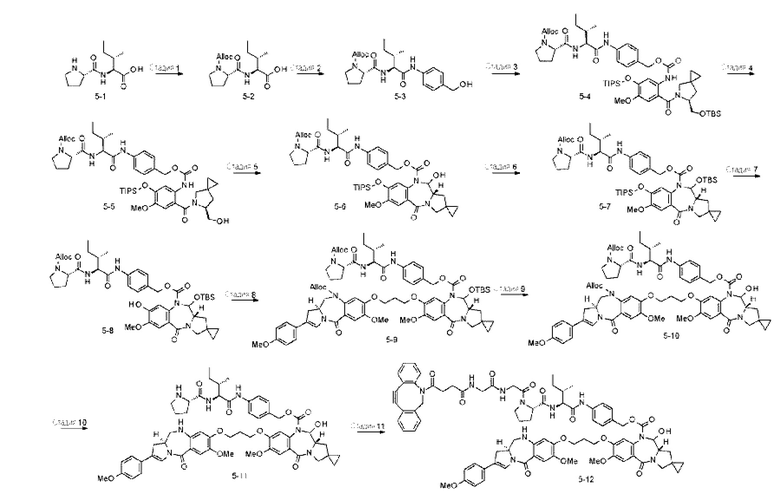
Стадия 1: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пропил-L-изолейцин
К 1 моль/л водного раствора гидроксида натрия (8,80 мл, 8,80 ммоль) с раствором L-пролил-L-изолейцина (1,00 г, 4,40 ммоль) в 1,4-диоксане (30 мл) медленно добавляли по каплям аллилхлорформиат (0,690 мл, 6,53 ммоль) при 0°С. Реакционную смесь перемешивали при комнатной температуре в течение 5 часов и затем к реакционной смеси добавляли водный раствор гидросульфата калия для доведения рН до примерно 4 и реакционную смесь подвергали экстракции хлороформом. Органический слой промывали солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт фильтровали и затем концентрировали при пониженном давлении и к остатку добавляли гексан. Полученное твердое вещество собирали путем фильтрации и сушили, получая желаемое соединение (1,20 г, 88%).
МС (ХИАД, ИЭР) m/z: 311(M-H)-
[0356]
Стадия 2: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-[4-(гидроксиметил)фенил]-L-изолейцинамид
К раствору (100 мл) соединения, полученного на стадии 1 (13,7 г, 43,4 ммоль) в ТГФ и 4-аминобензиловому спирту (6,00 г, 48,7 ммоль) добавляли N-этоксикарбонил-2-этокси-1,2-дигидрохинолин (12,0 г, 48,7 ммоль) при комнатной температуре. Реакционный раствор перемешивали при комнатной температуре в течение 23 часов, к полученной смеси добавляли диэтиловый эфир (200 мл) и полученное твердое вещество затем собирали путем фильтрации и полученное соединение (13,2 г, 65%) непосредственно применяли для последующей реакции.
[0357]
Стадия 3: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-изолейцинамид
Соединение, полученное на стадии 2 (6,87 г, 16,5 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (7,46 г, 56%).
1Н-ЯМР (CDCl3) δ: 8,99-8,97(1Н,m), 8,45-8,42(1Н,m), 7,81-7,49(3Н,m), 7,36-7,33(2Н,m), 6,81-6,77(2Н,m), 5,96-5,91(1Н,m), 5,32-5,23(2Н,m), 5,13-5,10(2Н,m), 4,73-4,30(6Н,m), 4,00-3,98(1Н,m), 3,78-3,52(7Н,m), 3,06-3,02(1Н,m), 2,37-2,12(5Н,m), 2,06-1,92(1Н,m), 1,77-1,48(2Н,m), 1,32-1,27(3Н,m), 1,11-1,09(18Н,m), 1,03-0,91(15Н,m), 0,66-0,44(4Н,m), 0,09-0,04(6Н,m).
[0358]
Стадия 4: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-изолейцинамид
Соединение, полученное на стадии 3 (7,46 г, 7,41 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (6,07 г, 92%).
МС (ХИАД, ИЭР) m/z: 892(M+H)+
[0359]
Стадия 5: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 4 (6,07 г, 6,80 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (4,18 г, 69%).
МС (ХИАД, ИЭР) m/z: 890(M+H)+
[0360]
Стадия 6: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 5 (4,18 г, 4,70 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (4,26 г, 90%).
МС (ХИАД, ИЭР) m/z: 1004(M+H)+
[0361]
Стадия 7: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спироциклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 6 (4,26 г, 4,70 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (2,48 г, 69%).
1H-ЯМР (CDCl3) δ: 8,44-8,41(1H,m), 7,53-7,37(1H,m), 7,24-7,23(1H,m), 7,14-7,11(2H,m), 6,82(1H,s), 6,67-6,65(1H,m), 6,11-6,07(1H,m), 5,99-5,95(2H,m), 5,33-5,02(4H,m), 4,84-4,41(5H,m), 3,94(3H,s), 3,73-3,70(1H,m), 3,59-3,52(4H,m), 3,29-3,26(1Н,m), 2,39-2,24(5Н,m), 1,99-1,97(2Н,m), 1,56-1,53(1Н,m), 1,10-0,64(19H,m), 0,20-0,16(3H,m), 0,09-0,07(3H,m).
MC (ХИАД, ИЭР) m/z: 848(M+H)+
[0362]
Стадия 8: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11'-[(триметилсилил)окси]-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 7 (0,200 г, 0,236 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,308 г, 99%).
МС (ХИАД, ИЭР) m/z: 1324(M+H)+
[0363]
Стадия 9: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 8 (0,308 г, 0,233 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,261 г, 93%).
МС (ХИАД, ИЭР) m/z: 1210(M+H)+
[0364]
Стадия 10: L-Пролил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 9 (0,261 г, 0,216 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,183 г, 81%).
1H-ЯМР (CDCl3) δ: 9,06(1H,s), 8,33-8,31(1H,m), 7,53-7,47(4H,m), 7,33-7,31(2H,m), 7,21(1H,s), 7,11-7,09(2H,m), 6,89-6,87(2H,m), 6,40(1H,s), 6,08(1H,s), 5,91-5,88(1Н,m), 5,35-5,32(1Н,m), 4,69-4,66(2H,m), 4,45-4,28(3H,m), 4,15-4,05(3H,m), 3,87(3H,s), 3,82(3H,s), 3,78(3H,s), 3,74-3,72(3H,m), 3,64-3,47(3H,m), 3,37-3,30(2H,m), 3,04-3,00(1H,m), 2,94-2,88(1H,m), 2,75-2,72(1H,m), 2,42-2,39(1H,m), 2,13-2,05(4H,m), 1,92-1,55(6H,m), 1,20-1,14(1H,m), 0,98-0,96(3H,m), 0,91-0,89(3H,m), 0,70-0,66(4H,m).
MC (ХИАД, ИЭР) m/z: 1042(M+H)+
[0365]
Стадия 11: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 10 (0,0474 г, 0,455 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0495 г, 75%).
МС (ХИАД, ИЭР) m/z: 1443(M+H)+
[0366]
Пример 6: Лекарственное средство-линкер 4
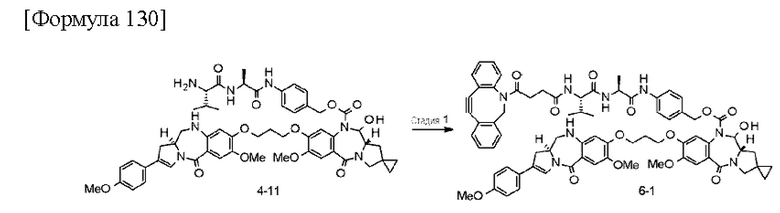
Стадия 1: К раствору соединения, полученного на стадии 11 примера 4 (0,0564 г, 0,0563 ммоль) и триэтиламина (0,00936 мл, 0,0675 ммоль) в N,N-диметилформамиде (5 мл) добавляли 1-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]окси}пирролидин-2,5-дион (0,0249 г, 0,0619 ммоль) при комнатной температуре. Полученный продукт перемешивали при комнатной температуре в течение 2 часов и затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 99,5:0,5 (об./об.) до 90:10 (об./об.)], получая желаемое соединение (0,0490 г, 68%).
МС (ХИАД, ИЭР) m/z: 1289(М+Н)+
[0367]
Пример 7: Лекарственное средство-линкер 5
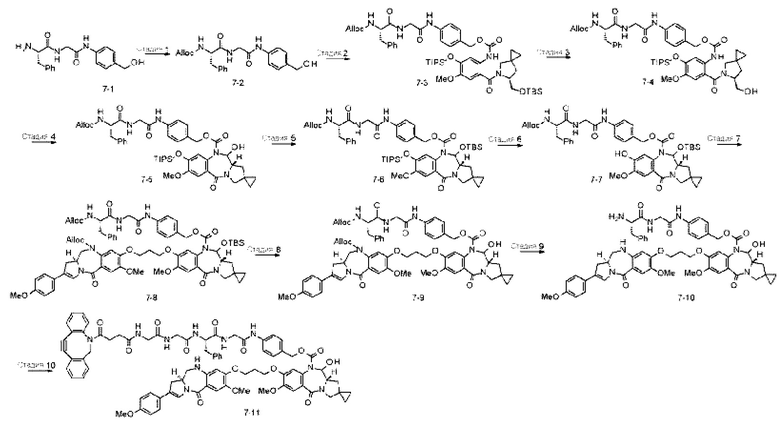
Стадия 1: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-[4-(гидроксиметил)фенил]глицинамид
К раствору исходного вещества 7-1 (1,24 г, 3,80 ммоль, Bioorganic & Medicinal Chemistry 2015, 3, 3237-3247) и карбоната калия (0,945 г, 6,84 ммоль) в ТГФ (18 мл) и воде (12 мл) добавляли аллилхлорформиат (0,482 мл, 4,560 ммоль) при 0°С и добавляли при комнатной температуре в течение 1 часа. После экстракции эцилацетатом полученный экстракт промывали водой и солевым раствором и сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток затем растворяли в небольшом количестве этилацетата, к полученной смеси добавляли диэтиловый эфир. Полученное твердое вещество (1,30 г, 83%) собирали путем фильтрации и непосредственно использовали для последующей реакции.
[0368]
Стадия 2: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-[4-({[(2-{[(6S)-6-({[трет-бугил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]глицинамид
Соединение, полученное на стадии 1 (1,30 г, 3,16 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (1,32 г, 54%).
1H-ЯМР (CDCl3) δ: 9,01(1H,s), 8,38(1H,s), 7,80(1H,s), 7,60-7,58(2H,m), 7,32-7,29(5H,m), 7,19-7,18(2H,m), 6,76(1H,s), 6,55(1H,s), 5,89-5,83(1H,m), 5,24-5,13(5H,m), 4,56-4,55(3H,m), 4,34-4,33(1H,m), 4,10-4,06(1H,m), 3,98-3,94(2H,m), 3,75-3,72(5H,m), 3,16-3,08(3H,m), 2,28-2,25(1H,m), 1,70-1,68(1H,m), 1,30-1,27(3H,m), 1,11-1,09(18H,m), 0,90(9H,s), 0,65-0,48(4H,m), 0,05-0,02(6H,m).
МС (ХИАД, ИЭР) m/z: 1000(M+H)+
[0369]
Стадия 3: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]глицинамид
Соединение, полученное на стадии 2 (1,32 г, 1,32 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,23 г, количественный выход).
1H-ЯМР (CDCl3) δ: 8,48-8,38(2H,m), 7,71(1H,s), 7,61-7,59(2H,m), 7,36-7,27(5H,m), 7,20-7,18(2H,m), 6,76(1H,s), 6,55-6,52(1H,m), 5,89-5,83(1H,m), 5,28-5,13(5H,m), 4,56-4,55(3H,m), 4,34-4,33(1H,m), 4,22-4,20(1H,m), 4,10-4,06(1H,m), 3,98-3,94(1H,m), 3,78-3,75(5H,m), 3,64-3,62(1Н,m), 3,17-3,07(3H,m), 1,84-1,83(2H,m), 1,30-1,26(3H,m), 1,11-1,09(18H,m), 0,61-0,49(4H,m).
МС (ХИАД, ИЭР) m/z: 886(M+H)+
[0370]
Стадия 4: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 3 (1,32 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (0,660 г, 57%).
1H-ЯМР (CDCl3) δ: 8,34(1H,s), 7,53-7,51(2H,m), 7,26-7,18(8H,m), 6,66-6,57(2H,m), 5,88-5,80(2H,m), 5,27-5,21(3H,m), 5,11-5,07(1H,m), 4,99-4,96(1H,m), 4,55-4,54(2H,m), 4,36-4,34(1H,m), 4,13-3,92(2H,m), 3,83(3H,s), 3,73-3,70(1H,m), 3,57-3,55(1H,m), 3,46-3,44(1H,m), 3,32-3,29(1H,m), 3,18-3,15(1H,m), 3,09-3,05(1H,m), 2,42-2,38(1H,m), 1,75-1,72(1H,m), 1,25-1,02(21H,m), 0,73-0,60(4H,m).
МС (ХИАД, ИЭР) m/z: 884(M+H)+
[0371]
Стадия 5: Н-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 4 (0,834 г, 0,943 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,555 г, 59%).
1Н-ЯМР (CDCl3) δ: 8,26-8,23(1Н,m), 7,51-7,50(2Н,m), 7,29-7,28(3Н,m), 7,18-7,13(5Н,m), 6,64-6,62(1Н,m), 6,52-6,49(1Н,m), 6,02-6,00(1Н,m), 5,88-5,83(1Н,m), 5,25-5,17(4Н,m), 4,84-4,81(1Н,m), 4,55-4,55(2Н,m), 4,34-4,33(1Н,m), 4,06-3,97(2H,m), 3,84(3H,s), 3,71-3,68(1H,m), 3,50-3,48(1H,m), 3,28-3,05(3H,m), 2,36-2,33(1Н,m), 1,56-1,53(1Н,m), 1,28-1,01(21Н,m), 0,81-0,61(13Н,m), 0,19(3H,s), 0,09(3H,s).
МС (ХИАД, ИЭР) m/z: 998(M+H)+
[0372]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 5 (0,555 г, 0,556 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,451 г, 96%).
1Н-ЯМР (CDCl3) δ: 8,42-8,40(1Н,m), 7,50-7,46(2Н,m), 7,28-7,26(3Н,m), 7,20-7,18(3Н,m), 7,10-7,08(2Н,m), 6,67-6,65(2Н,m), 6,16-6,13(1Н,m), 6,02-5,99(1Н,m), 5,88-5,82(1Н,m), 5,28-5,18(4Н,m), 4,87-4,84(1Н,m), 4,54-4,53(2Н,m), 4,38-4,36(1Н,m), 4,10-4,07(1Н,m), 3,93-3,90(4Н,m), 3,72-3,69(1Н,m), 3,54-3,52(1Н,m), 3,25-3,17(2Н,m), 3,08-3,04(1Н,m), 2,36-2,33(1Н,m), 1,57-1,54(1Н,m), 0,81-0,61(13Н,m), 0,19(3H,s), 0,10(3 H,s).
МС (ХИАД, ИЭР) m/z: 842(M+H)+
[0373]
Стадия 7: N-[(Проп-2-ен-1-илокси)карбонил]-L-фенилаланил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 6 (0,115 г, 0,137 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,160 г, 89%).
МС (ХИАД, ИЭР) m/z: 1318(M+H)+
[0374]
Стадия 8: N-[(Проп-2-ен-1-ил)карбонил]-L-фенилаланил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 7 (0,160 г, 0,121 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,136 г, 93%).
МС (ХИАД, ИЭР) m/z: 1204(M+H)+
[0375]
Стадия 9: L-Фенилаланил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11a-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 8 (0,136 г, 0,113 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0372 г, 32%).
1Н-ЯМР (CDCl3) δ: 8,84-8,81(1Н,m), 8,07-8,05(1Н,m), 7,53-7,39(4Н,m), 7,34-7,19(8Н,m), 7,12-7,10(2Н,m), 6,90-6,87(2Н,m), 6,44-6,42(1Н,m), 6,10-6,08(1Н,m), 5,90-5,88(1Н,m), 5,38-5,35(1Н,m), 4,76-4,72(1Н,m), 4,57-4,44(1Н,m), 4,32-4,29(1Н,m), 4,17-4,01(5Н,m), 3,89-3,52(17Н,m), 3,41-3,25(3Н,m), 2,72-2,69(2Н,m), 2,43-2,40(1Н,m), 2,19-2,16(2Н,m), 1,78-1,74(1Н,m), 1,59-1,56(1Н,m), 0,72-0,66(4Н,m).
МС (ХИАД, ИЭР) m/z: 1036(M+H)+
[0376]
Стадия 10: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-фенилаланил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11a-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}глицинамид
Соединение, полученное на стадии 9 (0,0372 г, 0,0359 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0170 г, 33%).
МС (ХИАД, ИЭР) m/z: 1437(M+H)+
[0377]
Пример 8:
Лекарственное средство-линкер 6
[Формула 132]
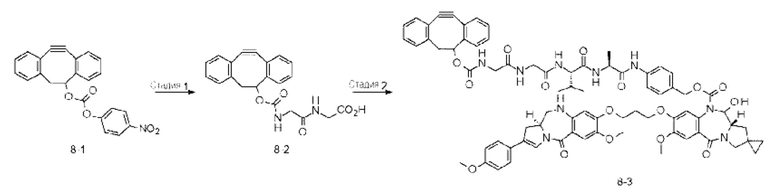
Стадия 1: N-[(11,12-дидегидро-5,6-дигидродибензо[а,е][8]аннулен-5-илокси)карбонил]глицилглицин
К раствору 11,12-дидегидро-5,6-дигидродибензо[а,е][8]аннулен-5-ил-4-нитрофенилкарбамата (0,437 г, 1,14 ммоль) и N,N-диизопропилэтиламина (0,198 мл, 1,14 ммоль) в N,N-диметилформамиде (6 мл) добавляли глицилглицин (0,150 г, 1,14 ммоль) и воду (3 мл) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение ночи. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:CMW = 100:0(об./об.) до 0:100(об./об.)], получая желаемое соединение (0,324 г, 75%).
МС (ХИАД, ИЭР) m/z: 378(M+H)+
[0378]
Стадия 2: N-[(11,12-дидегидро-5,6-дигидродибензо[а,е][8]аннулен-5-илокси)карбонил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси)пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил)окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 1 (0,0306 г, 0,0305 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0361 г, 87%).
МС (ХИАД, ИЭР) m/z: 1362 (M+H)+
[0379]
Пример 9: Лекарственное средство-линкер 7
[Формула 133]
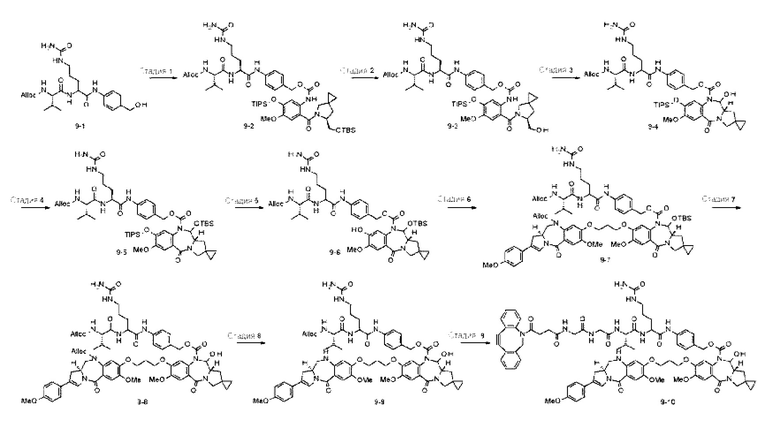
Стадия 1: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси)метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси)фенил}карбамоил]окси}метил)фенил]-N5-карбамоил-L-орнитинамид
Исходное вещество 9-1 подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (1,37 г, 45%).
1H-ЯМР (ДМСО-D6) δ: 10,06(1H,s), 9,16(1H,s), 8,10-8,06(1H,m), 7,62-7,60(2H,m), 7,33-7,31(2H,m), 7,27-7,24(2H,m), 6,84-6,81(1H,m), 5,94-5,89(2H,m), 5,41(2H,s), 5,32-5,28(1H,m), 5,18-5,16(1H,m), 5,03(2H,s), 4,48-4,42(3H,m), 4,30(1H,s), 3,93-3,73(6H,m), 3,47-3,14(3H,m), 3,00-2,95(2H,m), 2,00-1,89(2H,m), 1,65-1,60(2H,m), 1,42-1,39(2H,m), 1,26-1,19(3H,m), 1,04-1,01(18H,m), 0,88-0,75(15H,m), 0,51-0,49(4H,m), 0,05-0,17(6H,m).
MC (ХИАД, ИЭР) m/z: 1052(M+H)+
[0380]
Стадия 2: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N5-карбамоил-N-[4-({[2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-орнитинамид
Соединение, полученное на стадии 1 (1,37 г, 1,31 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,00 г, 82%).
1H ЯМР (ДМСО-D6) δ: 10,07(1H,s), 9,13(1H,s), 8,11-8,09(1H,m), 7,62-7,60(2H,m), 7,34-7,31(2H,m), 7,26-7,23(2H,m), 6,92-6,90(1H,m), 5,97-5,86(2H,m), 5,41(2H,s), 5,32-5,28(1H,m), 5,19-5,16(1H,m), 5,04(2H,s), 4,80(1H,s), 4,48-4,41(3H,m), 4,27(1H,s), 3,93-3,87(1H,m), 3,74(3H,s), 3,61-3,58(2H,m), 3,39-3,30(2H,m), 3,03-2,97(3H,m), 2,00-1,84(2H,m), 1,65-1,60(2H,m), 1,44-1,37(2H,m), 1,26-1,19(3H,m), 1,05-1,04(18H,m), 0,87-0,83(6H,m), 0,53-0,42(4H,m).
MC (ХИАД, ИЭР) m/z: 938(M+H)+
[0381]
Стадия 3: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N5-карбамоил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-5'-окси-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-орнитинамид
К смеси соединения, полученного на стадии 2 (1,00 г, 1,07 ммоль), дихлорметана (80 мл) и диметилформамида (10 мл) добавляли периодинан Десса-Мартина (0,455 г, 1,07 ммоль) при 0°С. После перемешивания при 0°С в течение 1 часа снова добавляли к полученной смеси периодинан Десса-Мартина (0,455 г, 1,07 ммоль) и полученный продукт перемешивали при 0°С в течение 1 часа. К реакционному раствору добавляли насыщенный водный раствор гидрокарбоната натрия и полученный продукт подвергали экстракции хлороформом и полученный экстракт затем промывали солевым раствором. Полученный продукт подвергали перегонке при пониженном давлении, затем добавляли этилацетат и твердое вещество собирали путем фильтрации. Фильтрат подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат - 50:50 до гексан:этилацетат = 0:100(об./об.)] и объединяли с твердым веществом, получая желаемое соединение (0,671 г, 67%).
1H-ЯМР (ДМСО-D6) δ: 10,05(1H,s), 8,11-8,09(1H,m), 7,56-7,54(2H,m), 7,25-7,23(1H,m), 7,13-7,09(3H,m), 6,62(1H,s), 6,53(1H,s), 5,94-5,88(2H,m), 5,78-5,76(1H,m), 5,40(2H,s), 5,32-5,28(1H,m), 5,17-5,14(2H,m), 4,81-4,78(1H,m), 4,48-4,41(3H,m), 3,92-3,90(1H,m), 3,79(3H,s), 3,54-3,51(1H,m), 3,16-3,14(1H,m), 3,02-2,89(2H,m), 2,37-2,34(2H,m), 1,97-1,92(1Н,m), 1,63-1,57(3H,m), 1,43-1,37(2H,m), 1,08-1,01(21Н,m), 0,87-0,83(6Н,m), 0,67-0,61(4Н,m).
МС (ХИАД, ИЭР) m/z:938(M+H)+
[0382]
Стадия 4: Н-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N5-карбамоил-L-орнитинамид
Используя смешанный растворитель дихлорметана (80 мл) и диметилформамида (5 мл), соединение, полученное на стадии 3 (0,671 г, 0,712 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,335 г, 44%).
1H-ЯМР (ДМСО-D6) δ: 10,04(1H,s), 8,12-8,10(1H,m), 7,56-7,54(2H,m), 7,26-7,24(1H,m), 7,14-7,ll(3H,m), 6,51(1H,s), 5,94-5,91(3H,m), 5,40-5,16(5H,m), 4,79-4,76(1H,m), 4,47-4,44(3H,m), 3,92-3,90(1H,m), 3,80(3H,s), 3,55-3,52(1H,m), 3,17-3,14(1H,m), 3,00-2,96(3H,m), 2,56-2,30(1H,m), 2,06-1,17(6H,m), 1,10-0,99(21H,m), 0,78-0,61 (19H,m), 0, 17(3H,s), 0,07(3H,s).
MC (ХИАД, ИЭР) m/z: 1050 (M+H)+
[0383]
Стадия 5: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11'11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N5-карбамоил-L-орнитинамид
Соединение, полученное на стадии 4 (0,355 г, 0,712 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,264 г, 93%).
1Н-ЯМР (ДМСО-D6) δ: 10,07-10,03(1Н,m), 9,89-9,86(1Н,m), 8,12-8,10(1Н,m), 7,63-7,54(2Н,m), 7,35-7,26(1Н,m), 7,14-7,12(2Н,m), 7,06(1H,s), 6,62-6,59(1Н,m), 5,97-5,87(3Н,m), 5,43-5,40(2Н,m), 5,32-5,28(1Н,m), 5,17-5,14(2Н,m), 4,86-4,82(1Н,m), 4,46-4,42(3H,m), 3,91-3,89(1H,m), 3,81(3H,s), 3,54-3,51(1H,m), 3,42-3,40(1H,m), 3,09-2,96(3Н,m), 2,40-2,34(1Н,m), 1,98-1,97(1Н,m), 1,68-1,59(2Н,m), 1,42-1,38(3Н,m), 0,77-0,64(19H,m), 0,16(3H,s), 0,08(3H,s).
MC (ХИАД, ИЭР) m/z: 894(M+H)+
[0384]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил] карбонил}окси)метил]фенил}-N5-карбамоил-L-орнитинамид
Соединение, полученное на стадии 5 (0,113 г, 0,126 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,149 г, 86%).
МС (ХИАД, ИЭР) m/z: 1370(M+H)+
[0385]
Стадия 7: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N5-карбамоил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-орнитинамид
Соединение, полученное на стадии 6 (0,149 г, 0,109 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,119 г, 87%).
МС (ХИАД, ИЭР) m/z: 1256(M+H)+
[0386]
Стадия 8: L-Валил-N5-карбамоил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,1la-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-орнитинамид
Соединение, полученное на стадии 7 (0,050 г, 0,0398 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0347 г, 80%).
1H-ЯМР (CDCl3) δ: 9,43(1H,s), 7,96-7,94(1H,m), 7,51-7,46(4H,m), 7,33-7,31(2H,m), 7,22(1H,s), 7,13-7,11(2H,m), 6,90-6,87(2H,m), 6,46(1H,s), 6,11(1H,s), 5,92-5,89(1H,m), 5,42-5,39(2H,m), 4,78-4,67(4H,m), 4,31-4,29(1H,m), 4,11-4,04(3H,m), 3,92-3,70(13H,m), 3,60-3,23(8H,m), 3,07-3,05(1H,m), 2,75-2,70(1H,m), 2,43-2,39(1H,m), 2,19-2,16(3H,m), 1,73-1,48(6H,m), 0,98-0,96(3H,m), 0,83-0,8l(3H,m), 0,71-0,65(4H,m).
МС (ХИАД ИЭР) m/z:1088(M+H)+
[0387]
Стадия 9: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N5-карбамоил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11,11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-орнитинамид
Соединение, полученное на стадии 8 (0,0347 г, 0,0319 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,00650 г, 14%).
МС (ХИАД, ИЭР) m/z: 1489(M+H)+
[0388]
Пример 10: Лекарственное средство-линкер 8
[Формула 134]
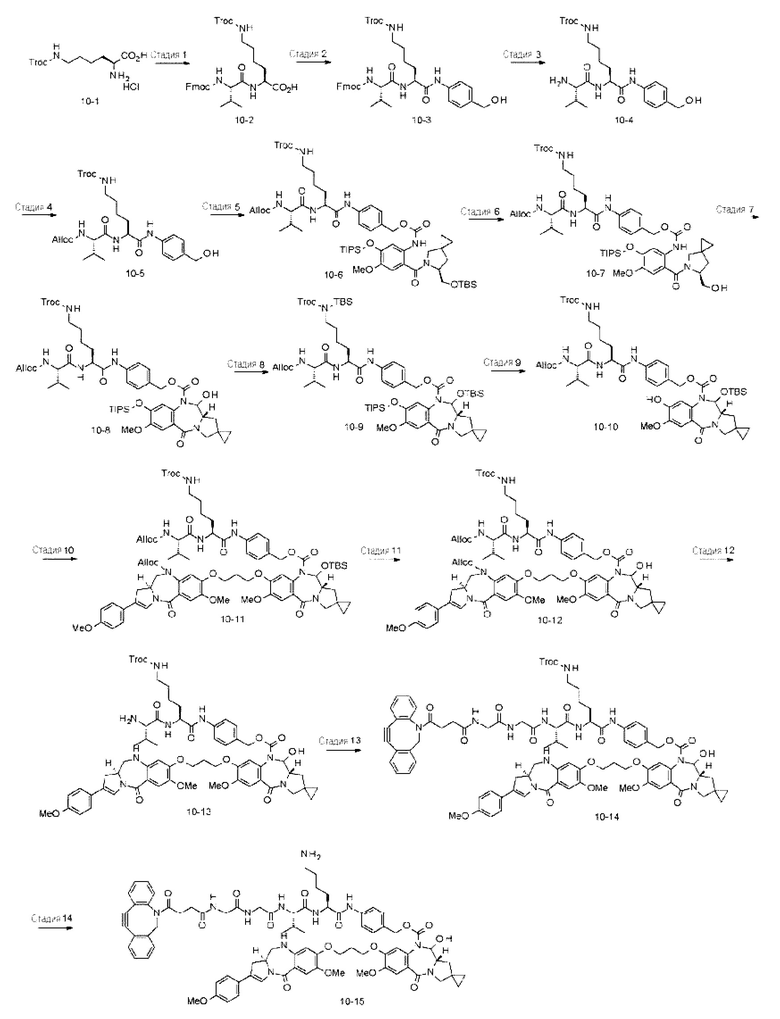
Стадия 1: N-[(9Н-Флуорен-9-илметокси)карбонил]-L-валил-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизин
К раствору исходного вещества 10-1 (2,78 г, 7,75 ммоль, Bioscience, Biotechnology, and Biochemistry 2012, 76, 205) в 1,2-диметоксиэтане (30 мл), воде (30 мл) и ТГФ (15 мл) добавляли гидрокарбонат натрия (1,30 г, 15,5 ммоль) и 2,5-диоксопирролидин-1-ил N-[(9Н-флуорен-9-илметокси)карбонил]-L-валинат (3,39 г, 7,76 ммоль) при комнатной температуре. Реакционный раствор перемешивали при комнатной температуре в течение пяти дней и затем экстрагировали смешанной жидкостью хлороформа и метанола (10:1, об./об.). Органический слой промывали водой и солевым раствором и затем подвергали перегонке при пониженном давлении. Полученный остаток промывали диэтиловым эфиром и твердое вещество удаляли путем фильтрации. Фильтрат подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 30:70(об./об.)до 0:100 (об./об.)], получая желаемое соединение (2,13 г, 43%).
1H-ЯМР (CDCl3) δ: 7,78-7,76(2H,m), 7,60-7,58(2H,m), 7,41-7,39(2H,m), 732-7,30(2Н,m), 6,85-6,83(1Н,m), 5,58-5,56(1Н,m), 5,32-5,30(1Н,m), 4,72-4,57(3Н,m), 4,46-4,34(2Н,m), 4,23-4,21(1Н,m), 4,05-4,03(1Н,m), 3,22-3,15(2Н,m), 2,06-1,88(3Н,m), 1,52-1,51(2Н,m), 1,40-1,38(2Н,m), 0,97-0,96(6Н,m).
МС (ХИАД, ИЭР) m/z: 642(M+H)+
[0389]
Стадия 2: N-[(9Н-Флуорен-9-илметокси)карбонил]-L-валил-N-[4-(гидроксиметил)фенил]-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 1 (2,11 г, 3,29 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 5 и полученное соединение (2,24 г, 91%) непосредственно применяли для последующей реакции.
[0390]
Стадия 3: L-Валил-N-[4-(гидроксиметил)фенил]-Н6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
К раствору соединения, полученного на стадии 2 (2,24 г, 3,00 ммоль), в N,N-диметилформамиде (20 мл) добавляли пиперидин (0,5934 мл, 5,994 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток (1,576 г, количественный выход) непосредственно применяли для последующей реакции.
[0391]
Стадия 4: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-(гидроксиметил)фенил]-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 3 (1,58 г, 3,00 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 7 и полученное соединение (1,50 г, 82%) непосредственно применяли для последующей реакции.
[0392]
Стадия 5: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-({[Трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-N6-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 4 (1,57 г, 2,57 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (1,691 г, 71%).
1H-ЯМР (CDCl3) δ: 9,04-9,02(1H,m), 8,48-8,45(1H,m), 7,81(1H,s), 7,55-7,53(2H,m), 7,35-7,33(2H,m), 6,76(1H,s), 6,68-6,66(1H,m), 5,94-5,86(1H,m), 5,32-5,23(4H,m), 5,14-5,10(2Н,m), 4,79-4,76(1Н,m), 4,69-4,67(1Н,m), 4,57-4,54(4Н,m), 4,03-4,02(2Н,m), 3,75-3,72(5Н,m), 3,29-3,22(2Н,m), 3,04-3,02(1Н,m), 2,27-2,01(4Н,m), 1,83-1,58(3Н,m), 1,46-1,44(2Н,m), 1,31-1,27(3Н,m), 1,11-1,09(18Н,m), 1,00-0,90(15Н,m), 0,65-0,48(4Н,m), 0,06-0,03(6Н,m).
МС (ХИАД, ИЭР) m/z: 1219 (M+Na)+
[0393]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 5 (1,69 г, 1,41 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,43 г, 94%).
1H-ЯМР (CDCl3) δ: 8,57-8,52(2H,m), 7,70(1H,s), 7,56-7,54(2H,m), 7,35-7,33(2H,m), 6,76-6,75(2H,m), 5,91-5,90(1H,m), 5,40-5,26(4H,m), 5,12(2H,s), 4,78-4,75(1H,m), 4,69-4,66(1Н,m), 4,58-4,55(4Н,m), 4,37-4,34(1Н,m), 4,04-4,02(1Н,m), 3,80-3,77(5Н,m), 3,65-3,62(1Н,m), 3,28-3,11(3Н,m), 2,13-2,04(2Н,m), 1,81-1,78(3Н,m), 1,60-1,58(2Н,m), 1,45-1,43(2Н,m), 1,33-1,25(3Н,m), 1,11-1,09(18Н,m), 0,98-0,94(6Н,m), 0,58-0,51(4Н,m).
МС (ХИАД, ИЭР) m/z: 1083 (M+H)+
[0394]
Стадия 7: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 6 (1,43 г, 1,32 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 9, получая желаемое соединение (0,714 г, 50%).
1H-ЯМР (CDCl3) δ: 8,49-8,46(1H,m), 7,52-7,45(2H,m), 7,19-7,18(3H,m), 6,72-6,68(2Н,m), 5,90-5,87(2Н,m), 5,33-5,23(4Н,m), 5,10-5,07(1Н,m), 4,98-4,95(1Н,m), 4,78-4,76(1Н,m), 4,69-4,66(1Н,m), 4,5 8-4,53(3 Н,m), 4,01(1 H,s), 3,83-3,81 (4Н,m), 3,73-3,70(1Н,m), 3,57-3,55(2Н,m), 3,29-3,25(3Н,m), 2,42-2,39(1Н,m), 2,15-2,13(1Н,m), 2,03-2,01(2Н,m), 1,74-1,71(2Н,m), 1,44-1,42(2Н,m), 1,23-1,17(3 Н,m), 1,03-0,93(24Н,m), 0,67-0,64(4Н,m).
МС (ХИАД, ИЭР) m/z: 1081 (M+H)+
[0395]
Стадия 8: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N6-[трет-бутил(диметил)силил]-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро [циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 7 (0,714 г, 0,660 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,476 г, 60%).
1H-ЯМР (CDCl3) δ: 8,63-8,51(1H,m), 7,49-7,48(2H,m), 7,18-7,14(3H,m), 6,61-6,53(2H,m), 5,99-5,94(2H,m), 5,33-5,17(4H,m), 4,81-4,78(3H,m), 4,59-4,57(3H,m), 4,03-4,01(1H,m), 3,88-3,85(4H,m), 3,70-3,67(2H,m), 3,50-3,47(1H,m), 3,24-3,17(3H,m), 2,37-2,34(1H,m), 2,13-2,07(2H,m), 1,59-1,54(3 H,m), 1,38(2H,s), 1,16-0,92(35H,m), 0,81-0,76(9H,m), 0,67-0,64(4H,m), 0,34-0,31(6H,m), 0,19(3H,s), 0,09(3H,s).
[0396]
Стадия 9: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N6-[трет-бутил(диметил)силил]-N-{4-[({[(11'S,11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 8 (0,476 г, 0,398 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,283 г, 68%).
1H-ЯМР (CDCl3) δ: 8,48(1H,s), 7,51-7,47(2H,m), 7,25-7,24(2H,m), 7,12-7,10(2H,m), 6,70-6,67(2Н,m), 6,09-6,07(1Н,m), 5,98-5,92(2Н,m), 5,33-5,20(5Н,m), 4,82-4,71(3Н,m), 4,59-4,56(3H,m), 4,03-4,00(1H,m), 3,91(3H,s), 3,72-3,69(1H,m), 3,54-3,52(1H,m), 3,28-3,25(3Н,m), 2,37-2,34(1Н,m), 2,18-2,16(1Н,m), 2,05-1,99(1Н,m), 1,78-1,75(1Н,m), 1,56-1,53(2Н,m), 1,43-1,41(2Н,m), 0,98-0,94(6Н,m), 0,82-0,75(9Н,m), 0,67-0,64(4H,m), 0,19(3H,s), 0,10(3H,s).
МС (ХИАД, ИЭР) m/z: 1039 (M+H)+
[0397]
Стадия 10: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 9 (0,119 г, 0,114 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,134 г, 77%).
[0398]
Стадия 11: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 10 (0,134 г, 0,0881 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,120 г, 97%).
МС (ХИАД, ИЭР) m/z: 1423 (M+Na)+
[0399]
Стадия 12: L-Валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 11 (0,120 г, 0,0855 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0813 г, 77%).
1H-ЯМР (CDCl3) δ: 9,10(1H,s), 7,94-7,92(1H,m), 7,58(1H,s), 7,47-7,45(3H,m), 7,35-7,33(2Н,m), 7,21 (2H,s), 7,13-7,11(2H,m), 6,90-6,88(2H,m), 6,43(1H,s), 6,11(1H,s), 5,90-5,88(1H,m), 5,51(1H,s), 5,39-5,36(1H,m), 4,73-4,70(3H,m), 4,52-4,51(2H,m), 4,32(1H,s), 4,13-4,08(3H,m), 3,89(3H,s), 3,80-3,76(9H,m), 3,60-3,50(4Н,m), 3,34-3,24(5Н,m), 2,76-2,72(1Н,m), 2,44-2,12(4Н,m), 1,94-1,27(7H,m), 1,00-0,98(3Н,m), 0,84-0,82(3Н,m), 0,70-0,66(4Н,m).
МС (ХИАД, ИЭР) m/z: 1233 (M+H)+
[0400]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизинамид
Соединение, полученное на стадии 12 (0,0813 г, 0,0659 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0721 г, 67%).
МС (ХИАД, ИЭР) m/z: 1656 (M+Na)+
[0401]
Стадия 14: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1H-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил)окси)метил]фенил}-L-лизинамид
Соединение, полученное на стадии 13 (0,0721 г, 0,0441 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 21, получая желаемое соединение (0,0348 г, 54%).
МС (ХИАД, ИЭР) m/z: 1460 (M+H)+
[0402]
Пример 11: Лекарственное средство-линкер 9
[Формула 135]
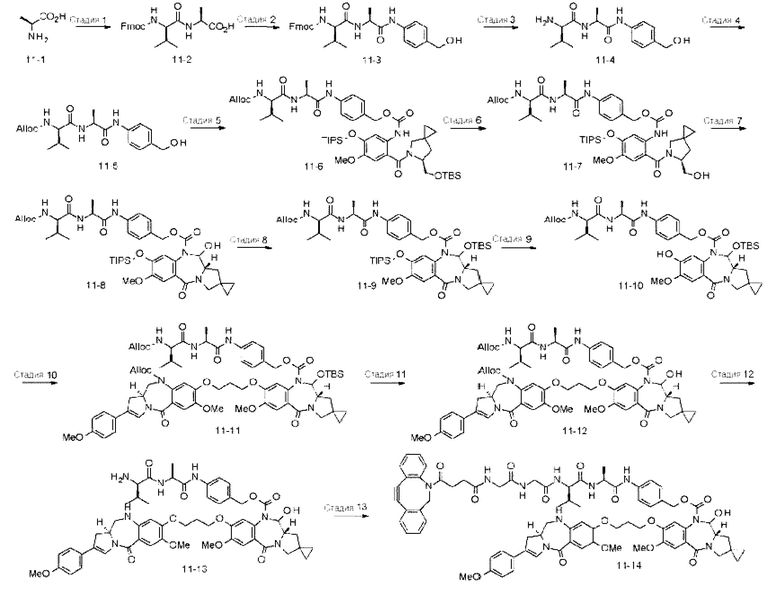
Стадия 1: N-[(9Н-Флуорен-9-илметокси)карбонил]-D-валил-L-аланин
L-аланин (0,0721 г, 0,0441 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 10, за исключением того, что 2,5-диоксопирролидин-1-ил N-[(9Н-флуорен-9-илметокси)карбонил]-D-валинат (0,528 г, 5,92 ммоль) использовали вместо 2,5-диоксопирролидин-1-ил N-[(9Н-флуорен-9-илметокси)карбонил]-L-валината. Полученное соединение (0,0348 г, 54%) непосредственно применяли для последующей реакции.
1H-ЯМР (ДМСО-D6) δ: 10,55(1H,s), 8,23-8,21(1H,m), 7,91-7,89(2H,m), 7,76-7,75(2Н,m), 7,42-7,40(3Н,m), 7,33-7,31(2Н,m), 4,31-4,20(4Н,m), 3,93-3,91(1Н,m), 1,97-1,93(1Н,m), 1,27-1,25(3Н,m), 0,86-0,84(6Н,m).
МС (ХИАД, ИЭР) m/z: 411 (М+Н)+
[0403]
Стадия 2: N-[(9Н-Флуорен-9-илметокси)карбонил]-D-валил-N-[4-(гидроксиметил)фенил]-L-аланинамид
Соединение, полученное на стадии 1 (2,05 г, 4,99 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 5, и полученное соединение (2,19 г, 85%) непосредственно применяли для последующей реакции.
[0404]
Стадия 3: D-Валил-N-[4-(гидроксиметил)фенил]-L-аланинамид
Соединение, полученное на стадии 2 (2,19 г, 4,25 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 10, и полученное соединение (0,966 г, 76%) непосредственно применяли для последующей реакции.
[0405]
Стадия 4: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-[4-(гидроксиметил)фенил]-L-аланинамид
Соединение (0,966 г, 3,29 ммоль), полученное на стадии 3, подвергали реакции таким же образом, как и на стадии 1 примера 7, и полученное соединение (1,11 г, 89%) непосредственно применяли для последующей реакции.
[0406]
Стадия 5: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 4 (1,11 г, 2,93 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (1,75 г, 80%).
1H-ЯМР (CDCl3) δ: 9,02(1H,s), 8,55(1H,s), 7,81(1H,s), 7,57-7,54(2H,m), 7,34-7,32(2H,m), 6,76(1H,s), 6,52-6,50(1H,m), 5,91-5,86(1H,m), 5,30-5,22(3H,m), 5,13-5,10(2H,m), 4,65-4,59(4H,m), 3,99-3,97(1H,m), 3,87-3,85(1H,m), 3,75-3,72(5H,m), 3,04-3,02(1H,m), 2,28-2,13(2H,m), 1,70-1,68(1H,m), 1,49-1,47(3 H,m), 1,31-1,27(3H,m), 1,11-1,09(18H,m), 1,00-0,90(15H,m), 0,65-0,48(4H,m), 0,06-0,03(6H,m).
MC (ХИАД, ИЭР) m/z: 966 (M+H)+
[0407]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 5 (1,75 г, 1,81 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,53 г, 99%).
1H-ЯМР (CDCl3) δ: 8,66(1H,s), 8,50(1H,s), 7,69(1H,s), 7,57-7,54(2H,m), 7,34-7,32(2Н,m), 6,75-6,71(2Н,m), 5,90-5,85(1Н,m), 5,40-5,38(1Н,m), 5,29-5,21(2H,m), 5,12(2H,s), 4,71-4,50(4H,m), 4,34-4,31(1H,m), 3,89-3,77(6H,m), 3,64-3,61(1Н,m), 3,13-3,10(1Н,m), 2,17-2,09(1Н,m), 1,87-1,84(2Н,m), 1,48-1,46(3Н,m), 1,32-1,28(3Н,m), 1,11-1,09(18Н,m), 0,97-0,94(6Н,m), 0,63-0,49(4Н,m).
MC (ХИАД, ИЭР) m/z: 852 (M+H)+
[0408]
Стадия 7: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-{4-[({[(11'S,11а'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 6 (1,53 г, 1,79 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 9, получая желаемое соединение (1,24 г, 81%).
1Н-ЯМР (CDCl3) δ: 8,51(1H,s), 7,51-7,49(2H,m), 7,18-7,15(3H,m), 6,65(1H,s), 6,56-6,54(1H,m), 5,90-5,85(2H,m), 5,31-5,19(3H,m), 5,10-5,07(1H,m), 4,97-4,94(1H,m), 4,67-4,50(3H,m), 3,90-3,88(1H,m), 3,84(3H,s), 3,73-3,70(1H,m), 3,58-3,56(2H,m), 3,31-3,28(1H,m), 2,42-2,39(1H,m), 2,18-2,15(1H,m), 1,74-1,71(1H,m), 1,48-1,46(3H,m), 1,19-0,88(27H,m), 0,69-0,65(4H,m).
MC (ХИАД, ИЭР) m/z: 850 (M+H)+
[0409]
Стадия 8: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (1,24 г, 1,45 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,979 г, 70%).
1H-ЯМР (CDCl3) δ: 8,48(1H,s), 7,51-7,49(2H,m), 7,19(1H,s), 7,14-7,12(2H,m), 6,62(1H,s), 6,53-6,51(1H,m), 6,01-5,99(1H,m), 5,91-5,85(1H,m), 5,30-5,28(2Н,m), 5,21-5,15(2Н,m), 4,82-4,79(1Н,m), 4,68-4,51(3Н,m), 3,88-3,84(4Н,m), 3,71-3,69(1Н,m), 3,50-3,47(1Н,m), 3,28-3,25(1Н,m), 2,37-2,34(1Н,m), 2,20-2,13(1Н,m), 1,52-1,47(4Н,m), 1,21-0,94(27Н,m), 0,80-0,77(9Н,m), 0,67-0,64(4H,m), 0,19(3H,s), 0,08(3H,s).
MC (ХИАД, ИЭР) m/z: 964 (M+H)+
[0410]
Стадия 9: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 8 (0,979 г, 1,02 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,769 г, 94%).
1H-ЯМР (CDCl3) δ: 8,71(1H,s), 7,37-7,35(2H,m), 7,23(1H,s), 7,04-7,02(2H,m), 6,86-6,84(1H,m), 6,74-6,72(1H,m), 6,65(1H,s), 6,05-5,85(2H,m), 5,64-5,62(1H,m), 5,32-5,20(3Н,m), 4,82-4,78(1Н,m), 4,70-4,52(3Н,m), 4,00-3,98(1Н,m), 3,93-3,90(3Н,m), 3,73-3,70(1Н,m), 3,55-3,53(1Н,m), 3,27-3,23(1Н,m), 2,38-2,18(2Н,m), 1,60-1,46(4Н,m), 1,00-0,92(6H,m), 0,80(9H,s), 0,68-0,63(4H,m), 0,20(3H,s), 0,10(3H,s).
МС (ХИАД, ИЭР) m/z: 808 (M+H)+
[0411]
Стадия 10: N-[(Проп-2-ene)-1-илокси)карбонил]-D-валил-N-{4-[({[(11а'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 9 (0,100 г, 0,124 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,148 г, 94%).
МС (ХИАД, ИЭР) m/z: 1284 (M+H)+
[0412]
Стадия 11: N-[(Проп-2-ен-1-илокси)карбонил]-D-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 10 (0,148 г, 0,124 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,132 г, 98%).
МС (ХИАД ИЭР) m/z: 1170 (M+H)+
[0413]
Стадия 12: D-Валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11a-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 11 (0,132 г, 0,113 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0963 г, 85%).
1H-ЯМР (CDCl3) δ: 9,12(1H,s), 7,85-7,84(1H,m), 7,54-7,52(1H,m), 7,49(1H,s), 7,44-7,42(2H,m), 7,34-7,32(2H,m), 7,21(1H,s), 7,13-7,11(2H,m), 6,90-6,88(2H,m), 6,41(1H,s), 6,10(1H,s), 5,90-5,87(1H,m), 5,35-5,32(1H,m), 4,74-4,71(1H,m), 4,60-4,56(2H,m), 4,30(1H,s), 4,13-4,10(4H,m), 3,89(3H,s), 3,83(3H,s), 3,80(3H,s), 3,74-3,71(1H,m), 3,60-3,49(4H,m), 3,39-3,35(1H,m), 3,31-3,27(2H,m), 2,75-2,72(1H,m), 2,44-2,18(4H,m), 1,78-1,44(6H,m), 0,98-0,97(3H,m), 0,74-0,68(7H,m).
МС (ХИАД, ИЭР) m/z: 1002 (M+H)+
[0414]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-D-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси)пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил)окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 12 (0,0455 г, 0,0454 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0416 г, 65%).
МС (ХИАД, ИЭР) m/z: 1403 (M+H)+
[0415]
Пример 12: Лекарственное средство-линкер 10
[Формула 136]
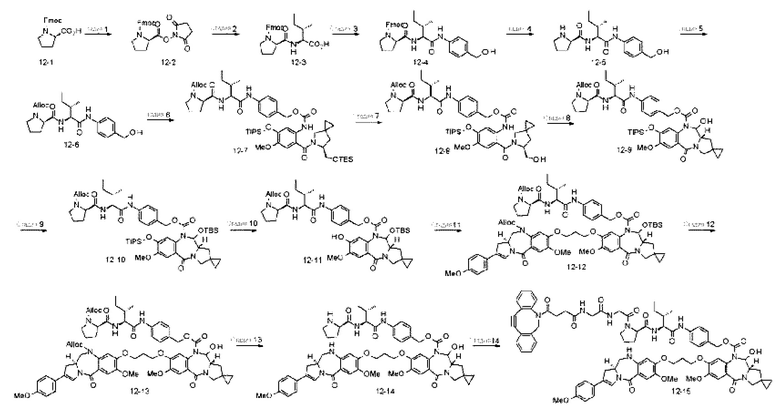
Стадия 1: Соединение 12-2
К исходному веществу 12-1 (2,01 г, 5,94 ммоль) в дихлорметане (50 мл) добавляли 1-(3-диметиламинопропил)-3-этилкарбодиимида гидрохлорид (1,37 г, 7,13 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 10 минут и затем добавляли к нему N-гидроксисукцинимид (0,821 г, 7,13 ммоль) при 0°С. Реакционный раствор перемешивали при комнатной температуре в течение ночи и затем растворитель удаляли при помощи перегонки при пониженном давлении. К полученному остатку добавляли этилацетат и воду и органический слой промывали водой, 10% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и солевым раствором и сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хромато графин на силикагеле [гексан:этилацетат = 90:10 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (2,11 г, 82%).
МС (ХИАД ИЭР) m/z: 435 (M+H)+
[0416]
Стадия 2: Соединение 12-3
Соединение, полученное на стадии 1 (2,11 г, 4,85 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 10, за исключением того, что вместо N6-[(2,2,2-трихлорэтокси)карбонил]-L-лизина гидрохлорида использовали L-изолейцин, получая желаемое соединение (2,16 г, 99%).
МС (ХИАД, ИЭР) m/z: 451 (M+H)+
[0417] Стадия 3: Соединение 12-4
Соединение, полученное на стадии 2 (2,16 г, 4,85 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 5, получая желаемое соединение (1,48 г, 56%).
[0418]
Стадия 4: Соединение 12-5
Соединение, полученное на стадии 3 (1,48 г, 2,67 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 10, получая желаемое соединение (0,794 г, 89%).
[0419] Стадия 5: Соединение 12-6
Соединение, полученное на стадии 4 (0,794 г, 2,38 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 7, получая желаемое соединение (0,886 г, 89%).
[0420]
Стадия 6: Соединение 12-7
Соединение, полученное на стадии 5 (0,794 г, 2,12 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (1,19 г, 72%).
МС (ХИАД, ИЭР) m/z: 1006 (M+H)+
[0421]
Стадия 7: Соединение 12-8
Соединение, полученное на стадии 6 (1,19 г, 1,18 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,07 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 892 (M+H)+
[0422]
Стадия 8: Соединение 12-9
Соединение, полученное на стадии 7 (1,18 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (0,800 г, 76%).
МС (ХИАД, ИЭР) m/z: 890 (M+H)+
[0423]
Стадия 9: Соединение 12-10
Соединение, полученное на стадии 8 (0,800 г, 0,899 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,567 г, 90%).
МС (ХИАД, ИЭР) m/z: 1004 (M+H)+
[0424]
Стадия 10: Соединение 12-11
Соединение, полученное на стадии 9 (0,567 г, 0,564 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,454 г, 94%).
МС (ХИАД, ИЭР) m/z: 848 (M+H)+
[0425]
Стадия 11: Соединение 12-12
Соединение, полученное на стадии 10 (0,100 г, 0,118 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,159 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 1324 (M+H)+
[0426]
Стадия 12: Соединение 12-13
Соединение, полученное на стадии 11 (0,118 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,139 г, 97%).
МС (ХИАД, ИЭР) m/z: 1210 (M+H)+
[0427]
Стадия 13: Соединение 12-14
Соединение, полученное на стадии 12 (0,139 г, 0,114 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0667 г, 56%).
1H-ЯМР (CDCl3) δ: 8,81(1H,s), 8,21-8,19(1H,m), 7,5 5-7,44(4H,m), 7,33-7,31(2H,m), 7,22(1H,s), 7,13-7,11(2H,m), 6,90-6,87(2H,m), 6,39(1H,s), 6,11(1H,s), 5,89-5,87(1H,m), 5,35-5,32(1H,m), 4,80-4,58(2H,m), 4,30(1H,s), 4,22-4,07(5H,m), 3,89(3H,s), 3,81-3,72(9H,m), 3,58-3,53(3H,m), 3,38-3,31(2H,m), 2,98-2,93(2H,m), 2,76-2,72(1H,m), 2,42-2,39(1H,m), 2,18-2,12(3 H,m), 1,94-1,5 l(7H,m), 1,31-1,13(1H,m), 0,97-0,90(6H,m), 0,71-0,66(4H,m).
МС (ХИАД, ИЭР) m/z: 1042 (M+H)+
[0428]
Стадия 14: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-D-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси)пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-изолейцинамид
Соединение, полученное на стадии 13 (0,0314 г, 0,0301 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0300 г, 69%).
МС (ХИАД, ИЭР) m/z: 1443 (M+H)+
[0429]
Пример 13: Лекарственное средство-линкер 11
[Формула 137]
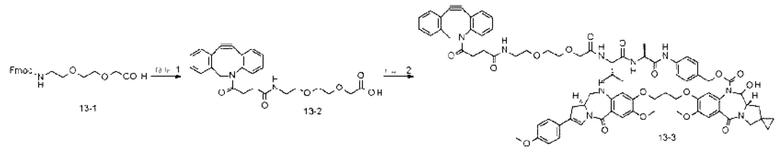
Стадия 1: [2-(2-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]амино)этокси)этокси]ацетат
К раствору исходного вещества 13-1 (3,00 г, 7,78 ммоль, Tokyo Chemical Industry Co., Ltd.) в N,N-диметилформамиде (10 мл) добавляли 1,8-диазабицикло[5,4.0]-7-ундецен (1,16 мл, 7,78 мл) и полученный продукт перемешивали при комнатной температуре в течение 2 часов и затем к нему добавляли 1-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]окси)пирролидин-2,5-дион (1,10 г, 2,72 ммоль) и триэтиламин (1,94 мл, 14,0 ммоль) при комнатной температуре. Реакционный раствор подвергали перегонке при пониженном давлении и полученный остаток затем очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 100:0 (об./об.) до хлороформ:метанол = 90:10 (об./об.)], получая желаемое соединение (0,410 г, 12%).
1H-ЯМР (CDCl3) δ: 7,68-7,66(1H,m), 7,55-7,53(1Н,m), 7,44-7,24(6Н,m), 6,58-6,56(1H,m), 5,16-5,12(1H,m), 4,16-4,11(2H,m), 3,80-3,57(5H,m), 3,48-3,44(2H,m), 3,30-3,18(2H,m), 2,90-2,86(1H,m), 2,52-2,45(1H,m), 2,26-2,22(1H,m), 2,02-1,98(1H,m).
MC (ХИАД, ИЭР) m/z: 451 (M+H)+
[0430]
Стадия 2: N-{[2-(2-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]амино}этокси)этокси]ацетил}-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 1 (0,050 г, 0,0499 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0590 г, 82%).
MC (ХИАД, ИЭР) m/z: 1434 (M+H)+
[0431]
Пример 14: Лекарственное средство-линкер 12
[Формула 138]
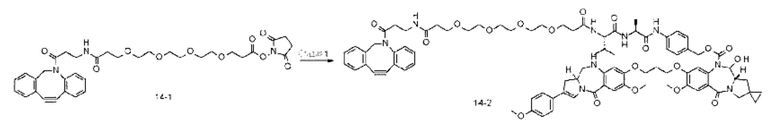
Стадия 1: N-[20-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-16,20-диоксо-4,7,10,13-тетраокса-17-азаикозан-1-оил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси)пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил)окси)метил]фенил}-L-аланинамид
Раствор соединения, полученного на стадии 11 примера 4 (0,0500 г, 0,0499 ммоль) исходного вещества 14-1 (0,050 г, 0,0499 ммоль, которое можно приобрести в Alfa Aesar) и триэтиламина (0,00830 мл, 0,0599 ммоль) в дихлорметане (3 мл) перемешивали при комнатной температуре в течение ночи. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток затем очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 100:0 (об./об.) до хлороформ: метанол = 90:10 (об./об.)], получая желаемое соединение (0,0490 г, 64%).
МС (ХИАД, ИЭР) m/z: 1536 (M+H]+
[0432]
Пример 15: Лекарственное средство-линкер 13
[Формула 139]
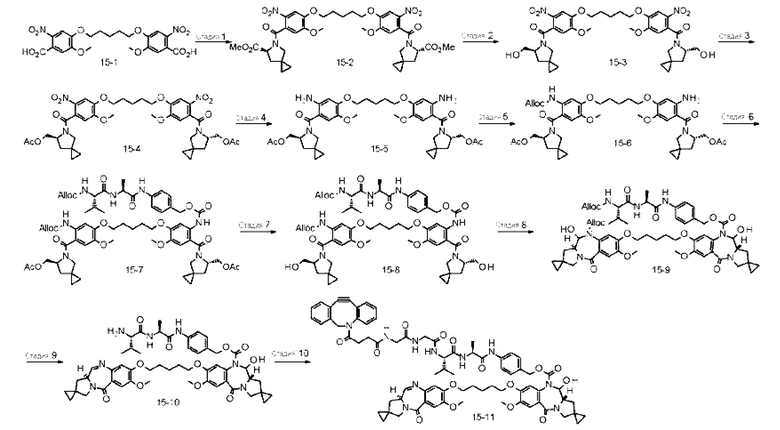
Стадия 1: Диметил-(6S,6'S)-5,5'-{1,5-пентандиилбис[окси(5-метокси-2-нитробензол-4,1-диил)карбонил])бис(5-азаспиро[2,4]гептан-6-карбоксилат)
К раствору исходного вещества 15-1 (5,41 г, 10,9 ммоль. Journal of Medicinal Chemistry 2004, 47, 1161) в дихлорметане (50 мл) добавляли оксалилхлорид (5,63 мл, 65,7 ммоль) при 0°С и затем к нему по каплям добавляли N,N-диметилформамид (0,0844 мл, 1,09 ммоль). Температуру реакционного раствора повышали до комнатной температуры и реакционный раствор перемешивали в течение 2 часов. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток растворяли в дихлорметане (100 мл), который добавляли по каплям к раствору (100 мл) метил(6S)-5-азаспиро[2,4]гептан-6-карбоксилата гидрохлорида (4,28 г, 24,1 ммоль. Tetrahedron Letters 2012. 53. 3847) и триэтиламин (6,07 мл, 43,8 ммоль) в дихлорметане в атмосфере азота при -40°С. Температуру реакционного раствора повышали до 0°С и реакционный раствор перемешивали в течение 2 часов. К реакционной смеси добавляли 1 п. соляную кислоту (100 мл) и органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении, получая желаемое соединение (8,40 г, количественный выход).
1H-ЯМР (ДМСО-D6) δ: 7,71(2H,s), 6,88(2H,s), 4,63(2H,m), 4,15-4,12(4H,m), 3,94(6H,s), 3,71(6H,s), 3,25(2H,m), 3,10(2H,m), 2,31-2,28(2H,m), 1,90-1,83(6Н,m), 1,60-1,58(2Н,m), 0,71-0,49(8Н,m).
МС (ХИАД, ИЭР) m/z: 769 (M+H)+.
[0433]
Стадия 2: {1,5-Пентандиилбис[окси(5-метокси-2-нитробензол-4,1-диил)]}бис{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]метанон}
К раствору соединения, полученного на стадии 1 (8,40 г, 10,9 ммоль) в ТГФ (100 мл) добавляли борогидрид лития (714 мг, 32,8 ммоль) и полученный продукт перемешивали при 0°С в течение 30 минут и температуру повышали до комнатной температуры и проводили перемешивание в течение 1 часа. Затем добавляли 1 н. соляную кислоту при 0°С, полученный продукт подвергали экстракции этилацетатом и промывали солевым раствором и затем сушили над безводным сульфатом натрия. Растворитель удаляли при помощи перегонки при пониженном давлении, получая желаемое соединение (7,70 г; 99%).
1H-ЯМР (ДМСО-D6) δ: 7,67(2H,s), 7,05(2H,s), 4,86-4,74(2H,m), 4,22-4,12(6H,m), 3,92(6H,s), 3,83-3,73(2H,m), 3,62-3,51(2Н,m), 3,29(1Н,m), 3,11(2Н,m), 2,96(1Н,m), 2,12-2,03(2Н,m), 1,82-1,77(6Н,m), 1,59-1,56(2Н,m), 0,67-0,41(8Н,m).
МС (ХИАД ИЭР) m/z: 713 (M+Н)+.
[0434]
Стадия 3: Пентан-1,5-диилбис[окси(5-метокси-2-нитробензол-4,1-диил)карбонил(6S)-5-азаспиро[2,4]гептан-5,6-диилметандиил]диацетат
Соединение, полученное на стадии 2 (7,70 г, 10,8 ммоль) растворяли в пиридине (20 мл) и уксусном ангидриде (10 мл, 105,9 ммоль) и полученную смесь перемешивали при комнатной температуре. Полученный продукт подвергали перегонке при пониженном давлении, получая желаемое соединение (8,38 г, 97%).
1H-ЯМР (ДМСО-D6) δ: 7,68(2H,s), 7,03(2H,s), 4,47-4,46(2H,m), 4,36-4,27(4H,m), 4,13-4,11(6H,m), 3,92(6H,s), 3,16(2H,m), 2,98(2H,m), 2,17(1H,m), 2,06(6H,s), 1,84(4H,m), 1,68 (1Н,m), 1,58(2Н,m), 0,64-0,45(8Н,m).
МС (ХИАД, ИЭР) m/z: 797 (M+H)+.
[0435]
Стадия 4: 1,5-Пентандиилбис[окси(2-амино-5-метоксибензол-4,1-диил)карбонил(6S)-5-азаспиро[2,4]гептан-5,6-диилметандиил]диацетат
К раствору соединения, полученного на стадии 3 (8,28 г, 10,4 ммоль), в N,N-диметилформамиде (100 мл) добавляли 5% палладий на углероде (содержание влаги: 54%, 1,00 г) и реакционный раствор затем интенсивно перемешивали в атмосфере водорода при комнатной температуре в течение 6 часов. Полученный продукт фильтровали через целит и фильтрат затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 100:0(об./об.) до 90:10(об./об.)], получая желаемое соединение (5,05 г, 66%).
1Н-ЯМР (ДМСО-D6) δ: 6,66(2H,s), 6,36(2H,s), 5,11(4H,s), 4,49(2H,s), 4,19(4H,m), 3,90(4H,m), 3,62(6H,s), 3,48-3,46(2H,m), 3,33(2H,s), 3,23-3,20(2H,m), 2,01(6H,s), 1,78-1,74(6H,m), 1,55(2H,m), 0,61-0,58(4H,m), 0,49-0,48(4H,m).
МС (ХИАД, ИЭР) m/z: 737 (M+H)+.
[0436]
Стадия 5: {(6S)-5-[4-({5-[4-({(6S)-6-[(Ацетилокси)метил]-5-азаспиро[2,4]гепт-5-ил}карбонил)-5-амино-2-метоксифенокси]пентил}окси)-5-метокси-2-{[(проп-2-ен-1-илокси)карбонил]амино}бензоил]-5-азаспиро[2,4]гепт-6-ил}метилацетат (моноаллилоксикарбонильная форма)
К раствору соединения, полученного на стадии 4 (5,05 г, 6,85 ммоль) в дихлорметане (100 мл) добавляли пиридин (1,10 мл, 13,7 ммоль) и к нему добавляли аллилхлорформиат (0,725 мл, 6,85 ммоль) в атмосфере азота при -78°С и полученный продукт перемешивали в течение 2 часов. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 70:30 (об./об.) до 100:0 (об./об.), хлороформ:метанол = 100:0 (об./об.) до 90:10 (об./об.)], получая бисаллилоксикарбонильную форму (1,36 г, 22%) и моноаллилоксикарбонильную форму (2,63 г, 47%) в качестве желаемого соединения.
Пентан-1,5-диилбис[окси(5-метокси-2-{[(проп-2-ен-1-илокси)карбонил]амино}бензол-4,1-диил)карбонил(6S)-5-азаспиро[2,4]гептан-5,6-диилметандиил]диацетат (бисаллилоксикарбонильная форма):
1H-ЯМР(ДМСО-D6) δ: 9,14(2H,s), 7,14(2H,s), 6,85(2H,s), 5,94(2H,m), 5,33(2H,m), 5,21(2H,m), 4,55(4H,m), 4,47(1H,s), 4,23(3H,s), 3,96(4H,m), 3,74(6H,s), 3,34(6H,s), 3,31(2H,m), 3,21(2H,m), 2,04(6H,s), 1,79(4H,m), 1,67(2H,m), 1,56(2H,m), 0,56-0,48(8H,m).
MC (ХИАД ИЭР) m/z: 905 (M+H)+.
Моноаллилоксикарбонильная форма:
1H-ЯМР (ДМСО-В6)
δ: 9,14(1H,s), 7,14(1H,s), 6,85(1H,s), 6,65(1H,s), 6,35(1H,s), 5,95(1H,m), 533(1H,m), 5,22(1Н,m), 5,11(2Н,s), 4,55(2Н,m), 4,48(2Н,s), 4,23-4,14(4H,m), 3,96(2H,m), 3,90(2H,m), 3,74(3H,s), 3,63(3H,s), 3,49(1H,m), 3,38-3,30(4H,m), 3,21(1H,m), 2,04(3H,s), 2,01(3H,s), 1,77(5H,m), 1,68(1H,m), 1,56(2H,m), 0,63-0,48(8Н,m).
MC (ХИАД ИЭР) m/z: 821 (M+H)+.
[0437]
Стадия 6: N-[(2-пропен-1-илокси)карбонил]-L-валил-N-{4-[({[2-({(6S)-6-[(ацетилокси)метил]-5-азаспиро[2,4]гепт-5-ил}карбонил)-5-({5-[4-({(6S)-6-[(ацетилокси)метил]-5-азаспиро[2,4]гепт-5-ил}карбонил)-2-метокси-5-{[(2-пропен-1-илокси)карбонил]амино}фенокси]пентил}окси)-4-метоксифенил]карбамоил}окси)метил]фенил}-L-аланинамид
Моноаллилоксикарбонильную форму, полученную на стадии 5 (2,00 г, 2,44 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (2,64 г, 89%).
1H-ЯМР (ДМСО-D6) δ: 10,02(1H,s), 9,14(2H,s), 8,18(1H,m), 7,59(2H,m), 7,33(2H,m), 7,27(1H,m), 7,14(2H,s), 6,85(2H,s), 5,99-5,86(2H,m), 5,31(2H,n), 5,19(2H,m), 5,03(2H,s), 4,55(2H,m), 4,48(2H,n), 4,41(2H,m), 4,23-4,21(3H,m), 3,94-3,91(4H,m), 3,88-3,86(2H,m), 3,74(3H,s), 3,74(3H,s), 3,34(4H,s), 3,32-3,30(2H,m), 3,20-3,18(2H,m), 2,03(6H,s), 1,96(1H,m), 1,79(4H,s), 1,66(1H,m), 1,55(2H,s), 1,30(3H,m), 0,88(3H,m), 0,83(3H,m), 0,54-0,49(8H,m).
MC (ХИАД ИЭР) m/z: 1224 (M+H)+.
[0438]
Стадия 7: N-[(2-пропен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-5-{[5-(4-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-2-метокси-5-{[(2-пропен-1-илокси)карбонил]амино}фенокси)пентил]окси}-4-метоксифенил)карбамоил]окси}метил)фенил]-L-аланинамид
К раствору соединения, полученного на стадии 6 (2,64 г, 2,16 ммоль), в метаноле (10 мл) добавляли карбонат калия (1,49 г, 10,8 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси добавляли насыщенный водный раствор хлорида аммония (100 мл) и полученную смесь подвергали экстракции этилацетатом. Органический слой сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении, получая желаемое соединение (2,21 г, 90%).
1H-ЯМР (ДМСО-D6) δ: 10,04(1H,s), 9,18(1H,s), 8,18(1H,m), 7,59(2H,m), 7,33(2H,m), 7,26(1H,m), 7,22(1H,s), 7,14(2H,s), 6,89(2H,s), 5,98-5,86(2H,m), 5,31(2H,m), 5,19(2H,m), 5,04(2H,s), 4,80(2H,m), 4,55(2H,m), 4,48(2H,m), 4,4 l(1H,m), 4,26(2H,s), 3,96-3,94(4H,m), 3,90-3,85(1H,m), 3,74(6H,s), 3,59(2H,m), 3,33(6H,s), 3,09(1H,m), 1,93-1,83(8H,m), 1,57-1,54(2H,m), 1,30(3H,m), 0,88(3H,m), 0,83(3H,m), 0,52-0,43(8H,m).
MC (ХИАД, ИЭР) m/z: 1140 (M+H)+
[0439]
Стадия 8: N-[(2-пропен-1-илокси)карбонил]-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-8'-{[5-({(11а'S)-11'-гидрокси-7'-метокси-5'-оксо-10'-[(2-пропен-1-илокси)карбонил]-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил}окси)пентил]окси}-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 7 (2,03 г, 1,78 ммоль), в дихлорметане (50 мл) добавляли периодинан Десса-Мартина (1,59 г, 3,74 ммоль) и полученный продукт перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия (100 мл) и полученную смесь подвергали экстракции хлороформом. Органический слой сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 100:0(об./об.) до 90:10(об./об.)], получая желаемое соединение (2,05 г, количественный выход).
1H-ЯМР (ДМСО-D6) δ: 9,99(1H,s), 8,16(1H,m), 7,54(2H,m), 7,32-7,22(3H,m), 7,08-7,04(2H,m), 6,80-6,72(2H,m), 6,55(2H,s), 5,94-5,86(2H,m), 5,75(2H,m), 5,31-5,04(2Н,m), 4,81(1Н,m), 4,62(1Н,m), 4,48-4,38(4Н,m), 4,00-3,87(4Н,m), 3,79-3,76(7H,m), 3,54(2H,m), 3,42-3,40(2H,m), 3,33(4H,s), 3,14(2H,m), 2,35(2H,m), 1,80-1,78(4Н,m), 1,59-1,56(4Н,m), 1,29(3Н,m), 0,87(3Н,m), 0,83(3Н,m), 0,70-0,59(8Н,m).
МС (ХИАД, ИЭР) m/z: 1136 (M+H)+.
[0440]
Стадия 9: L-Валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 8 (2,05 г, 1,80 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (1,02 г, 60%).
1H-ЯМР (ДМСО-D6) δ: 10,08(1H,s), 7,57(2H,m), 7,32-7,20(3H,m), 7,05(2H,s), 6,68-6,60(3Н,m), 5,74(1Н,m), 4,99-4,5 8(4Н,m), 3,99-3,94(4Н,m), 3,78-3,73(6Н,m), 3,66-3,38(4H,m), 3,1 5-3,01(3H,m), 2,40-2,34(3H,m), 1,89-1,81(6H,m), 1,57-1,53(4H,m), 1,28(3H,m), 0,88(3H,m), 0,78(3H,m), 0,64-0,55(8H,m).
МС (ХИАД, ИЭР) m/z: 950 (M+H)+.
[0441]
Стадия 10: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 9 (0,710 г, 0,747 ммоль), и соединение, полученное на стадии 1 примера 2 (0,313 г, 0,747 ммоль), растворяли в смешанном растворителе дихлорметана (1,5 мл) и метанола (0,1 мл). К этому добавляли 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолиния хлорид (0,264 г, 0,897 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:метанол = 100:0 (об./об.) до 80:20 (об./об.)], получая желаемое соединение (0,671 г, 66%).
Таблица 2: Пиковые позиции протонов ЯМР и МС для лекарственного средства-линкера 13
1H-ЯМР (ДМСО-D6) δ: 9,91(1H,s), 8,32(1H,s), 8,23-7,91(3H,m), 7,81-7,19(14Н,m), 7,04(1Н,m), 6,80-6,62(3Н,m), 5,77-5,75(1Н,m), 5,20(1Н,m), 5,01(1Н,m), 4,79(1Н,m), 4,46-4,35(1Н,m), 4,04(4Н,m), 3,86-3,38(18Н,m), 3,22-3,15(2Н,m), 2,67-2,63(1Н,m), 2,46-2,23(3Н,m), 2,09-1,91(2Н,m), 1,80- 1,78(5Н,m), 1,57(3Н,m), 1,27(3 H,s), 1,11- 1,04(1Н,m), 0,87-0,79(6Н,m), 0,63-0,5 5(6Н,m).
МС (ХИАД, ИЭР) m/z: 1351 (М+Н)+.
[0442]
Пример 16: Лекарственное средство-линкер 14
[Формула 140]
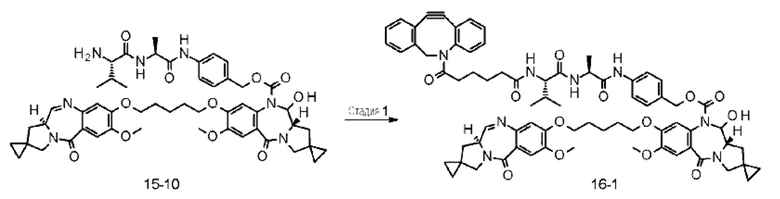
Стадия 1: N-[6-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-6-оксогексаноил]-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',11а'-дигадро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11,11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 9 примера 15 (0,100 г, 0,105 ммоль) и азадибензоциклооктиновую кислоту (0,0351 г, 0,105 ммоль) подвергали реакции таким же образом, как и на стадии 10 примера 15, получая желаемое соединение (0,0702 г, 53%).
1H-ЯМР (ДМСО-D6): δ 9,92(1H,s), 8,14(1H,m), 7,92-7,19(16H,m), 7,04(1H,m), 6,86-6,72(1H,m), 6,60-6,58(1H,m), 5,76(1H,m), 5,20(1H,m), 5,03(1H,m), 4,81-4,78(1H,m), 4,43-4,37(2H,m), 4,11-3,41 (14H,m), 3,21-3,15(3H,m), 2,43-2,37(2H,m), 2,19-2,15(1H,m), 2,03-1,92(3H,m), 1,77-1,75(5H,m), 1,55(4H,s), 1,26-1,18(6H,m), 1,09-1,04(1H,m), 0,87-0,77(6H,m), 0,69-0,50(8H,m).
MC (ХИАД, ИЭР) m/z: 1265 (M+H)+.
[0443]
Пример 17: Лекарственное средство-линкер 15
[Формула 141]
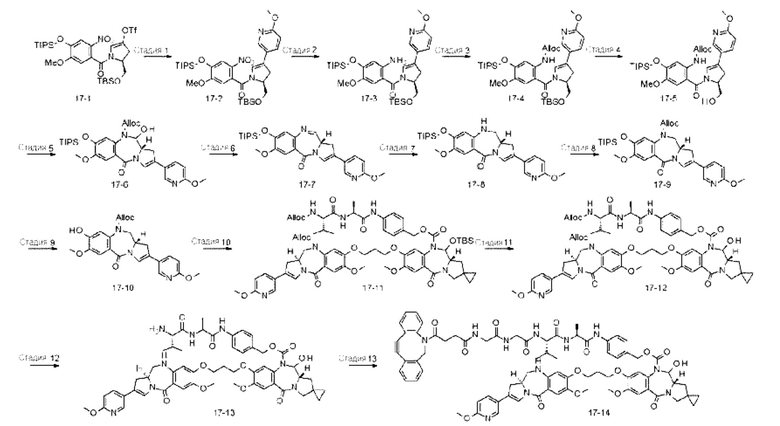
Стадия 1: Соединение 17-2
Исходное вещество 17-1 (2,00 г, 2,81 ммоль, WO 2013053872) и 2-метокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (2,00 г, 8,51 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (1,89 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 672 (M+H)+.
[0444]
Стадия 2: Соединение 17-3
Соединение, полученное на стадии 1 (1,89 г, 2,81 ммоль), растворяли в смешанном растворителе этанола (30 мл) и муравьиной кислоты (1,5 мл). К нему добавляли порошок цинка (3,68 г) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Полученный продукт фильтровали через целит и к фильтрату добавляли насыщенный водный раствор гидрокарбоната натрия (100 мл) и проводили экстракцию этилацетатом. Органический слой сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении, получая желаемое соединение (1,81 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 642(M+H)+.
[0445]
Стадия 3: Соединение 17-4
Соединение, полученное на стадии 2 (1,81 г, 2,82 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (1,76 г, 86%).
МС (ХИАД, ИЭР) m/z: 726 (M+H)+.
[0446]
Стадия 4: Соединение 17-5
Соединение, полученное на стадии 3 (1,76 г, 2,42 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (1,05 г, 71%).
МС (ХИАД, ИЭР) m/z: 612 (M+H)+.
[0447]
Стадия 5: Соединение 17-6
Соединение, полученное на стадии 4 (1,05 г, 1,71 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 9, получая желаемое соединение (0,686 г, 66%).
МС (ХИАД, ИЭР) m/z: 610 (М+Н)+.
[0448]
Стадия 6: Соединение 17-7
Соединение, полученное на стадии 5 (0,481 г, 0,789 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,288 г, 72%).
МС (ХИАД, ИЭР) m/z: 508 (M+H)+.
[0449] Стадия 7: Соединение 17-8
Соединение, полученное на стадии 6 (0,288 г, 0,567 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,268 г, 93%).
МС (ХИАД, ИЭР) m/z: 510 (M+Н)+.
[0450]
Стадия 8: Соединение 17-9
Соединение, полученное на стадии 7 (0,267 г, 0,525 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,278 г, 89%).
МС (ХИАД, ИЭР) m/z: 594 (M+H)+.
[0451]
Стадия 9: Соединение 17-10
Соединение, полученное на стадии 8 (0,278 г, 0,468 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,207 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 438(M+H)+.
[0452]
Стадия 10: Соединение 17-11
Используя соединение, полученное на стадии 11 примера 1 (0,307 г, 0,331 ммоль), соединение, полученное на стадии 9 (0,0964 г, 0,220 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,224 г, 79%).
МС (ХИАД, ИЭР) m/z: 1285 (M+H)+.
[0453]
Стадия 11: Соединение 17-12
Соединение, полученное на стадии 10 (0,294 г, 0,228 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,284 г, количественный выход).
МС (ХИАД ИЭР) m/z: 1171 (М+Н)+.
[0454]
Стадия 12: Соединение 17-13
Соединение, полученное на стадии 11 (0,284 г, 0,242 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,114 г, 47%).
МС (ХИАД ИЭР) m/z: 1003 (M+H)+.
[0455]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[7-метокси-2-(6-метокси-3-пиридинил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 12 (0,114 г, 0,113 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0121 г, 8%).
1Н-ЯМР (CDCl3) δ: 8,75(1H,s), 8,24-8,09(2Н,m), 7,85-6,98(13Н,m), 6,75-6,73(2H,m), 6,57-6,47(1H,m), 6,18(1H,s), 5,89(1H,s), 5,37-4,96(3H,m), 4,67-4,60(3H,m), 4,41-4,06(6H,m), 3,92(3H,s), 3,86-3,82(3H,m), 3,74-3,70(3H,m), 3,59-3,45(3Н,m), 3,32-3,23(2Н,m), 2,81-2,64(3Н,m), 2,28-2,04(4Н,m), 1,49-1,38(4Н,m), 1,23-1,22(2Н,m), 1,09-1,01(3Н,m), 0,96-0,90(5Н,m), 0,69-0,64(6Н,m).
МС (ХИАД, ИЭР) m/z: 1404 (M+H)+.
[0456]
Пример 18: Лекарственное средство-линкер 16
[Формула 142]
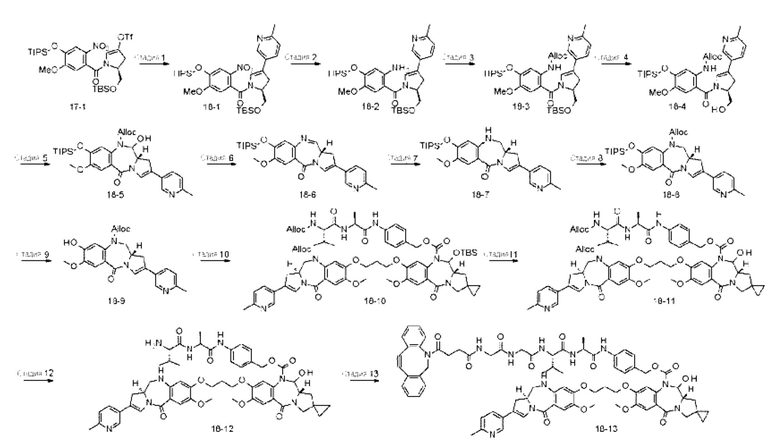
Стадия 1: Соединение 18-1
Исходное вещество 17-1 (2,00 г, 2,81 ммоль) и 2-метил-5-пиридинилбороновую кислоту (1,00 г, 7,30 ммоль) использовали и подвергали реакции сочетания Сузуки-Мияура таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,901 г, 49%).
МС (ХИАД, ИЭР) m/z: 656 (M+H)+.
[0457]
Стадия 2: Соединение 18-2
Соединение, полученное на стадии 1 (1,98 г, 3,02 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 17, получая желаемое соединение (1,86 г, 98%).
МС (ХИАД, ИЭР) m/z: 626 (M+H)+.
[0458]
Стадия 3: Соединение 18-3
Соединение, полученное на стадии 2 (1,86 г, 2,97 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (1,36 г, 65%).
МС (ХИАД, ИЭР) m/z: 710 (M+Н)+.
[0459]
Стадия 4: Соединение 18-4
Соединение, полученное на стадии 3 (1,36 г, 2,42 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (0,991 г, 87%).
МС (ХИАД, ИЭР) m/z: 596 (M+H)+.
[0460]
Стадия 5: Соединение 18-5
Соединение, полученное на стадии 4 (0,991 г, 1,66 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 9, получая желаемое соединение (0,608 г, 62%).
МС (ХИАД, ИЭР) m/z: 594 (M+H)+.
[0461]
Стадия 6: Соединение 18-6
Соединение, полученное на стадии 5 (0,405 г, 0,682 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,239 г, 71%).
1Н-ЯМР (ДМСО-D6) δ: 8,60(1H,s), 8,02(1H,m), 7,87(1H,m), 7,67(1H,s), 7,62(1H,m), 7,57-7,54(1H,m), 7,40(1H,s), 7,25(1H,m), 6,74(1H,s), 4,53-4,49(1H,m), 3,85(3H,s), 3,52(2H,m), 2,46(3 H,s), 1,30-1,24(3 H,m), 1,07-1,06(18H,m), получали в виде водного аддукта желаемого соединения.
МС (ХИАД, ИЭР) m/z: 492(M+H)+.
[0462]
Стадия 7: Соединение 18-7
Соединение, полученное на стадии 6 (0,239 г, 0,485 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,180 г, 75%).
МС (ХИАД, ИЭР) m/z: 494(M+H)+.
[0463]
Стадия 8: Соединение 18-8
Соединение, полученное на стадии 7 (0,180 г, 0,364 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,179 г, 85%).
МС (ХИАД, ИЭР) m/z: 578 (M+H)+.
[0464]
Стадия 9: Соединение 18-9
Соединение, полученное на стадии 8 (0,179 г, 0,309 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,137 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 422(M+H)+.
[0465]
Стадия 10: Соединение 18-10
Соединение, полученное на стадии 9 (0,0780 г, 0,185 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, за исключением того, что соединение, полученное на стадии 11 примера 1 (0,258 г, 0,278 ммоль) использовали вместо соединения, полученного на стадии 10 примера 1, получая желаемое соединение (0,213 г, 91%).
МС (ХИАД, ИЭР) m/z: 1269 (M+H)+.
[0466]
Стадия 11: Соединение 18-11
Соединение, полученное на стадии 10 (0,213 г, 0,168 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,182 г, 94%).
1H-ЯМР (ДМСО-D6) δ: 10,00-9,85(1H,m), 8,54(1H,s), 8,32(1H,m), 8,16(1H,s), 7,82(1H,m), 7,65-7,56(3H,m), 7,35-7,06(6H,m), 6,79(1H,m), 6,57(1H,s), 5,87-5,80(3H,m), 5,26-5,09(5H,m), 4,85-4,83(1H,m), 4,56-4,40(5H,m), 4J3(5H,m), 3,92-3,87(2H,m), 3,80(5H,s), 3,58-3,54(1H,m), 3,21-3,09(3H,m), 2,81(1H,m), 2,45(3H,s), 2,36-2,34(1H,m), 2,16-2,1 0(2H,m), 1,98-1,92(1Н,m), 1,57(2H,m), 1,30-1,28(4Н,m), 0,92-0,84(7Н,m), 0,67-0,62(4Н,m).
МС (ХИАД ИЭР) m/z: 1155 (M+H)+.
[0467] Стадия 12: Соединение 18-12
Соединение, полученное на стадии 11 (0,182 г, 0,157 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0751 г, 48%).
1H-ЯМР (ДМСО-D6) δ: 10,15(1H,s), 8,54(1H,m), 8,50(1H,s), 7,78(1H,m), 7,67(1H,s), 7,57(2H,m), 7,30(1H,s), 7,21-7J9(3H,m), 7,05(1H,s), 6,77(1H,s), 6,60-6,56(2H,m), 6,35(1H,s), 5,91-5,83(2H,m), 5,76(1H,m), 5,29-5,13(4H,m), 4,84(1H,m), 4,54-4,49(1H,m), 4,19-4,03(4H,m), 3,79(3H,s), 3,65(3H,s), 3,57-3,53(2H,m), 3,42-3,40(1H,m), 3,28-3,26(1H,m), 3,14(1H,m), 2,81(1H,m), 2,44(3H,s), 2,37-2,33(1H,m), 2,21-2,01(3H,m), 1,57(1H,m), 1,30-1,26(3H,m), 0,93-0,83(6H,m), 0,67-0,61(4H,m).
МС (ХИАД ИЭР) m/z:987(M+H)+.
[0468]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[7-метокси-2-(6-метил-3-пиридинил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 12 (0,0751 г, 0,0761 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0117 г, 11%).
1H-ЯМР (CDCl3) δ: 8,75(1H,s), 8,48-8,46(1H,m), 7,69-7,56(4H,m), 7,47-6,89(14Н,m), 6,45(1Н,m), 6,24-6,19(1Н,m), 5,91(1Н,m), 5,37(1Н,m), 5,01(1Н,m), 4,67-4,59(3Н,m), 4,30-3,19(22Н,m), 2,88-2,63(3Н,m), 2,55(3Н,s), 2,42-2,34(2Н,m), 2,27-2,04(4Н,m), 1,51-1,34(4Н,m), 1,12-1,06(3Н,m), 0,99-0,84(3Н,m), 0,71-0,66(4Н,m).
МС (ХИАД, ИЭР) m/z: 1388 (M+H)+.
[0469]
Пример 19: Лекарственное средство-линкер 17
[Формула 143]
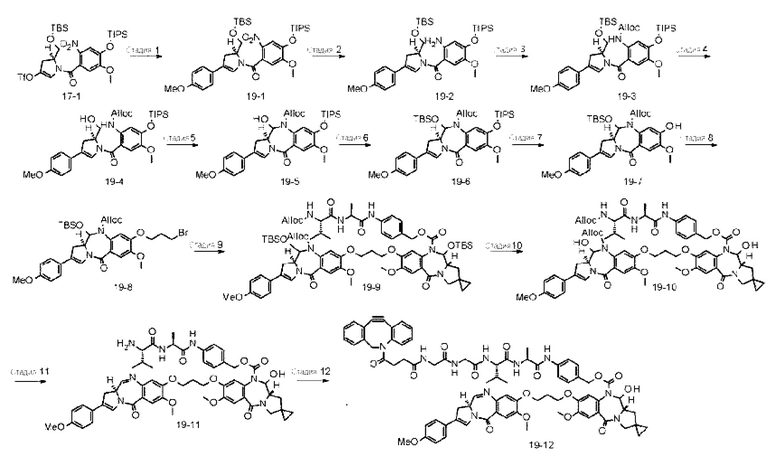
Стадия 1: [(2S)-2-({[трет-бутил(диметил)силил]окси)метил)-4-(4-метоксифенил)-2,3-дигидро-1Н-пиррол-1-ил](5-метокси-2-нитро-4-{[три(пропан-2-ил)силил]окси)фенил)метанон
Исходное вещество 17-1 (2,00 г, 2,81 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (1,31 г, 93%).
1Н-ЯМР (CDCl3) δ: 7,75-7,73(1H,m), 7,12(2H,m), 6,82-6,76(4H,m), 6,13-6,11(1H,m), 4,80-4,70(1H,m), 3,93-3,91(3H,m), 3,79-3,75(4H,m), 3,21-3,15(1H,m), 3,01-2,93(1H,m), 1,34-1,25(3H,m), 1,12(18H,m), 0,89(9H,s), 0,13-0,18(6H,m).
МС (ХИАД, ИЭР) m/z: 671 (M+Н)+
[0470]
Стадия 2: (2-Амино-5-метокси-4-{[три(пропан-2-ил)силил]окси}фенил)[(2S)-2-({[трет-бутил(диметил)силил]окси}метил)-4-(4-метоксифенил)-2,3-дигидро-1Н-пиррол-1-ил]метанон
Соединение, полученное на стадии 1 (1,31 г, 1,95 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 17, получая желаемое соединение (1,12 г, 90%).
1H-ЯМР (CDCl3) δ: 7,21-7,18(2H,m), 6,85-6,81(2H,m), 6,79-6,76(2H,m), 6,28(1H,s), 4,42(2H,m), 3,98-3,93(1H,m), 3,90-3,86(1H,m), 3,80(3H,s), 3,71(3H,s), 3,11(1H,m), 2,98(1H,m), 1,32-1,23(4H,m), 1,12-1,10(18H,m), 0,85(9H,s), 0,08-0,02(6H,m).
[0471]
Стадия 3: Проп-2-ен-1-ил-(2-{[(2S)-2-({[трет-бутил(диметил)силил]окси}метил)-4-(4-метоксифенил)-2,3-дигидро-1Н-пиррол-1-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамат
Соединение, полученное на стадии 2 (1,12 г, 1,59 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,890 г, 77%).
1H-ЯМР (CDCl3) δ: 8,57(1H,m), 7,77(1H,m), 7,18(2H,m), 6,86-6,78(4H,m), 5,95-5,90(1H,m), 5,32(1H,m), 5,20(1H,m), 4,79-4,77(1H,m), 4,64-4,57(2H,m), 4,00-3,98(1H,m), 3,93-3,91(1H,m), 3,80(3H,s), 3,76(3H,s), 3J4-3,09(1H,m), 3,00(1H,m), 1,36-1,25(3H,m), 1,14-1,11(18H,m), 0,85(9H,s), 0,11-0,03(6H,m).
MC (ХИАД, ИЭР) m/z: 725 (M+H)+
[0472]
Стадия 4: Проп-2-ен-1-ил-(2-{[(2S)-2-(гидроксиметил)-4-(4-метоксифенил)-2,3-дигидро-1Н-пиррол-1-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамат
Соединение, полученное на стадии 3 (0,890 г, 1,23 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (0,696 г, 93%).
1H-ЯМР (CDCl3) δ: 8,54-8,36(1H,m), 7,71(1H,m), 7,18-7,17(2H,m), 6,68-6,84(3Н,m), 6,77(1Н,m), 5,94-5,90(1Н,m), 5,32(1Н,m), 5,21(1Н,m), 4,87-4,85(1Н,m), 4,61(2Н,m), 4,50(1Н,m), 3,96-3,84(2H,m), 3,80(3H,s), 3,76(3H,s), 3,28(1H,m), 2,64(1H,m), 1,36-1,25(3Н,m), 1,13(18Н,m).
МС (ХИАД, ИЭР) m/z:611 (М+Н)+
[0473]
Стадия 5: Проп-2-ен-1-ил-(11aS)-11-гидрокси-7-метокси-2-(4-метоксифенил)-5-оксо-8-{[три(пропан-2-ил)силил]окси}-11,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 4 (0,696 г, 1,14 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (0,532 г, 77%).
1H-ЯМР(CDCl3) δ: 7,36(1H,s), 7,31-7,29(2H,m), 7,22(1H,s), 6,90-6,87(2Н,m), 6,72(1Н,m), 5,82-5,76(2Н,m), 5,19-5,14(2Н,m), 4,60(1Н,m), 4,49-4,46(1Н,m), 3,98-3,96(1H,m), 3,86(3H,s), 3,82(3H,s), 3,44(1H,m), 3,36(1H,m), 3,05(1H,m), 1,28-1,21(3Н,m), 1,10-1,07(18Н,m).
МС (ХИАД, ИЭР) m/z: 609 (M+H)+
[0474]
Стадия 6: Проп-2-ен-1-ил-(11aS)-11-{[трет-бутил(диметил)силил]окси}-7-метокси-2-(4-метоксифенил)-5-оксо-8-{[три(пропан-2-ил)силил]окси}-11,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 5 (0,532 г, 0,874 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,532 г, 95%).
1H-ЯМР(CDCl3) δ: 7,35(1Н,8), 7,29(2Н,m), 7,23(1Н,8), 6,89(2Н,m), 6,70(1Н,8), 5,90(1Н,m), 5,76(1Н,m), 5,14-5,10(2Н,m), 4,60(1Н,m), 4,38(1Н,m), 3,93-3,85(1H,m), 3,87(3H,s), 3,82(3H,s), 3,32(1H,m), 2,82-2,78(1H,m), 1,29-1,22(3H,m), 1,12-1,07(18H,m), 0,89(9H,s), 0,27(3H,s), 0,20(3H,s).
МС (ХИАД, ИЭР) m/z: 723(M+H)+
[0475]
Стадия 7: Проп-2-ен-1-ил (11aS)-11-{[трет-бутил(диметил)силил]окси}-8-гидрокси-7-метокси-2-(4-метоксифенил)-5-оксо-11,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 6 (0,532 г, 0,756 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,359 г, 86%).
1H-ЯМР(CDCl3) δ: 7,34(1H,s), 7,30-7,27(3H,m), 6,90-6,88(2H,m), 6,76(1H,s), 5,93-5,90(2H,m), 5,81-5,73(1H,m), 5,12-5,08(2H,m), 4,61(1H,m), 4,42(1H,m), 3,97(3H,s), 3,93-3,88(1H,m), 3,83(3H,s), 3,31(1H,m), 2,83-2,79(1H,m), 0,91(9H,s), 0,27(3H,s), 0,22(3H,s).
МС (ХИАД, ИЭР) m/z: 567(M+H)+
[0476]
Стадия 8: Проп-2-ен-1-ил-(11aS)-8-(3-бромпропокси)-11-{[трет-бутил(диметил)силил]окси}-7-метокси-2-(4-метоксифенил)-5-оксо-11,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 7 (0,405 г, 0,715 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 4, получая желаемое соединение (0,490 г, 99%).
1H-ЯМР(CDCl3) δ: 7,35(1H,s), 7,29(2H,m), 6,89(2H,m), 6,69(1H,s), 5,94(1H,m), 5,82-5,75(1Н,m), 5,13-5,08(1Н,m), 5,13-5,08(2Н,m), 4,65(1Н,m), 4,41(1Н,m), 4,20-4,13(2H,m), 3,94-3,88(1H,m), 3,92(3H,s), 3,83(3H,s), 3,62(2H,m), 3,32(1H,m), 2,83-2,80(1H,m), 2,41-2,36(2H,m), 0,91(9H,s), 0,27(3H,s), 0,24(3H,s).
MC (ХИАД, ИЭР) m/z: 687(M+H)+
[0477]
Стадия 9: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-8'-[3-({(11aS)-11-{[трет-бутил(диметил)силил]окси}-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11a-тетрагидро-1H-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-11'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 8 (0,490 г, 0,713 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,600 г, 60%).
МС (ХИАД, ИЭР) m/z: 1414(M+H)+
[0478]
Стадия 10: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-8'-[3-({(11aS)-11-гидрокси-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 9 (0,600 г, 0,424 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,500 г, 99%).
МС (ХИАД, ИЭР) m/z: 1184(M-H)+
[0479]
Стадия 11: L-Валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 9 (0,500 г, 0,421 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,113 г, 27%).
1H-MMP(CDCl3) δ: 8,94(1H,s), 7,70(1H,s), 7,56-7,53(2H,m), 7,46-7,44(2H,m), 7,36(1H,s), 7,31(2H,m), 7,23(1H,s), 7,03(2H,m), 6,90-6,88(2H,m), 6,68(1H,m), 6,57(1H,s), 6,40(1H,s), 5,92(1H,m), 5,43(1H,m), 4,67(1H,m), 4,55-4,53(1H,m), 4,46(1H,m), 4,35-4,33(1H,m), 4,28-4,24(1H,m), 4,15-4,13(1H,m), 3,88(3H,s), 3,87(3H,s), 3,83(3H,s), 3,77-3,72(1H,m), 3,62-3,60(1H,m), 3,52-3,47(2H,m), 3,34(1H,m), 3,30-3,28(1H,m), 3,00-2,91(2H,m), 2,50-2,41(2H,m), 2,24-2,22(1H,m), 2,10-2,08(1H,m), 1,77- 1,75(1H,m), 1,40-1,37(1H,m), 1,16(3H,m), 0,82(3H,m), 0,76-0,62(4H,m), 0,69(3H,m).
MC (ХИАД, ИЭР) m/z: 1000(M+H)+
[0480]
Стадия 12: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 11 (0,157 г, 0,157 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,120 г, 49%).
МС (ХИАД, ИЭР) m/z: 1401(M+H)+
[0481]
Пример 20: Лекарственное средство-линкер 18
[Формула 144]
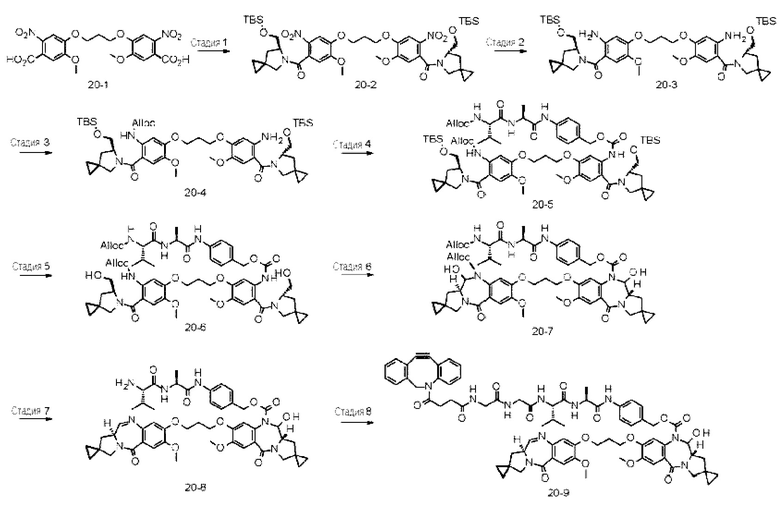
Стадия 1: {Пропан-1,3-Диилбис[окси(5-метокси-2-нитробензол-4,1-диил)]}бис{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]метанон}
Исходное вещество 20-1 (3,00 г, 6,43 ммоль, Journal of the American Chemical Society 1992, 13,4939) и соединение, полученное на стадии 3 примера 1 (3,42 г, 14,2 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 15, получая желаемое соединение (3,74 г, 64%).
1Н-ЯМР(CDCl3) δ: 7,79-7,70(2Н,m), 6,83-6,75(2Н,m), 4,52-4,50(1,5Н,m), 4,35-4,29(4,5Н,m), 4,03(0,5Н,m), 3,97-3,92(6Н,m), 3,88(0,5Н,m), 3,60-3,52(1Н,m), 3,38-3,33(0,5Н,m), 3,26-3,24(0,5Н,m), 3,04-2,93(3Н,m), 2,45-2,39(2Н,m), 2,25-2,21(1Н,m), 2,09-1,98(1Н,m), 1,68(1Н,m), 1,56(1Н,m), 0,93-0,90(14Н,m), 0,77-0,74(4Н,m), 0,71-0,62(4Н,m), 0,57-0,49(4Н,m), 0,44-0,40(2Н,m), 0,11(9Н,m), -0,14(3Н,m).
МС (ХИАД, ИЭР) m/z: 912(M+H)+
[0482]
Стадия 2: {Пропан-1,3-диилбис[окси(2-амино-5-метоксибензол-4,1-диил)]}бис{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]метанон}}
Соединение, полученное на стадии 1 (3,74 г, 4,10 ммоль), подвергали реакции таким же образом, как и на стадии 4 примера 15, получая желаемое соединение (2,97 г, 85%).
1H-MMP(CDCl3) δ: 7,79-7,69(2H,m), 6,82-6,75(2H,m), 4,54-4,47(1,5H,m), 4,36-4,26(4,5H,m), 4,03(0,5H,m), 3,98-3,92(6H,m), 3,88(0,5H,m), 3,61-3,51(1H,m), 3,39-3,32(0,5H,m), 3,28-3,21(0,5H,m), 3,05-2,93(3H,m), 2,45-2,39(2H,m), 2,24-2,21(1H,m), 2,08-2,06(1H,m), 2,00-1,99(1H,m), 1,69-1,66(1H,m), 1,57-1,54(5H,m), 0,94-0,88(14H,m), 0,78-0,74(4H,m), 0,71-0,62(4H,m), 0,57-0,49(4H,m), 0,44-0,40(2H,m), 0,13-0,10(9H,m), -0,11--0,17(3H,m).
МС (ХИАД, ИЭР) m/z: 853(M+H)+
[0483]
Стадия 3: Проп-2-ен-1-ил (5-[3-(5-амино-4-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-2-метоксифенил)пропокси]-2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метоксифенил)карбамат
Соединение, полученное на стадии 2 (2,97 г, 3,48 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 15, получая желаемое соединение (0,549 г, 17%).
1H-ЯМР(CDCl3) δ: 9,18(1Н,m), 7,88(1Н,m), 6,80(1Н,m), 6,73(1Н,8), 6,31(1Н,s), 5,96(1Н,m), 5,36(1Н,m), 5,24(1Н,m), 4,68-4,59(4Н,m), 4,59-4,43(2Н,m), 4,27-4,25(2Н,m), 4,20-4,18(2Н,m), 4,00(2Н,m), 3,79-3,72(9Н,m), 3,05(1Н,m), 2,35(2Н,m), 2,32-0,48(2Н,m), 0,05(12Н,m).
МС (ХИАД, ИЭР) m/z: 1021(M+H)+
Стадия 4: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-5-[3-(4-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-2-метокси-5-{[(проп-2-ен-1-илокси)карбонил]амино}фенокси)пропокси]-4-метоксифенил)карбамоил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 3 (0,549 г, 0,586 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (0,402 г, 51%).
МС (ХИАД, ИЭР) m/z: 1341 (М+Н)+
[0485]
Стадия 5: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-[4-({[(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-5-[3-(4-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-2-метокси-5-{[(проп-2-ен-1-илокси)карбонил]амино}фенокси)пропокси]-4-метоксифенил)карбамоил]окси}метил)фенил]-L-аланинамид
Соединение, полученное на стадии 4 (0,402 г, 0,300 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (0,282 г, 85%).
МС (ХИАД, ИЭР) m/z: 1120 (М+Н)+
[0486]
Стадия 6: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-8'-[3-({(11а'S)-11'-гидрокси-7'-метокси-5'-оксо-10'-[(проп-2-ен-1-илокси)карбонил]-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил}окси)пропокси]-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 5 (0,282 г, 0,253 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (0,0600 г, 21%).
МС (ХИАД, ИЭР) m/z: 1106 (М-Н)+
[0487]
Стадия 7: L-Валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11а'S)-7'-метокси-5'-оксо-5',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пропокси)-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 6 (0,0600 г, 0,0541 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0347 г, 70%).
МС (ХИАД, ИЭР) m/z: 922 (М+Н)+
[0488]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11а'S)-7'-метокси-5'-оксо-5',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (0,0347 г, 0,0376 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,00770 г, 16%).
МС (ХИАД, ИЭР) m/z:1323 (М+Н)+
[0489]
Пример 21: Лекарственное средство-линкер 19
[Формула 145]
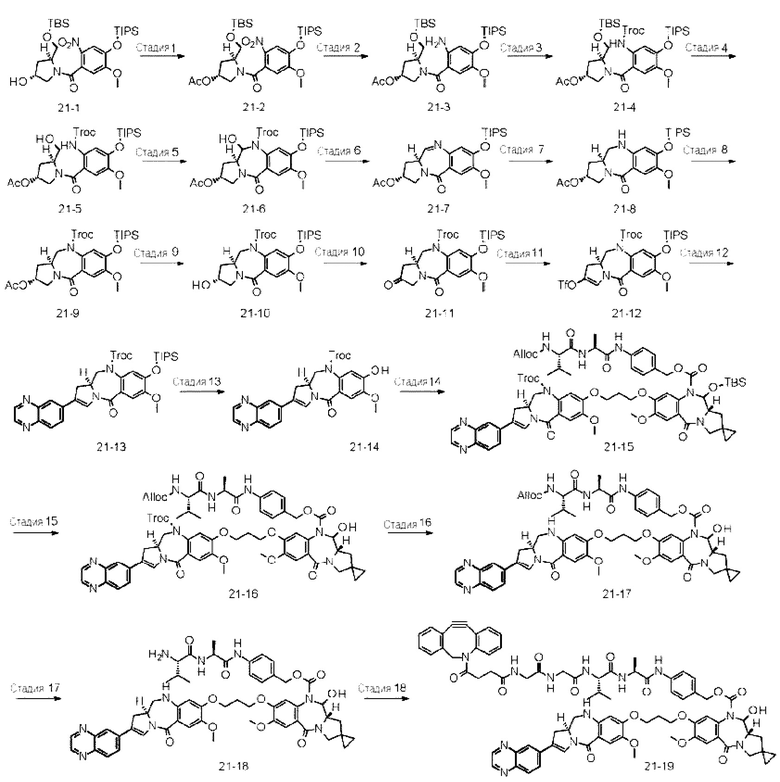
Стадия 1: Соединение 21-2
К раствору исходного вещества 21-1 (11,8 г, 20,2 ммоль, WO 2013053872) и пиридина (1,79 мл, 22,2 ммоль) в ТГФ (50 мл) медленно добавляли уксусный ангидрид (2,10 мл, 22,3 ммоль) при охлаждении льдом. Затем к нему добавляли 4-диметиламинопиридин (0,459 г, 3,76 ммоль) и полученный продукт перемешивали при комнатной температуре. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт фильтровали и затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат = 90:10 (об./об.) до 60:40 (об./об.)], получая желаемое соединение (12,3 г, 97%).
МС (ХИАД, ИЭР) m/z: 625(M+H)+
[0490]
Стадия 2: Соединение 21-3
Соединение, полученное на стадии 1 (12,3 г, 19,7 ммоль), подвергали реакции таким же образом, как и на стадии 4 примера 15, получая желаемое соединение (11,3 г, 97%)
МС (ХИАД, ИЭР) m/z: 595(M+H)+
[0491]
Стадия 3: Соединение 21-4
Соединение, полученное на стадии 2 (11,3 г, 19,0 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, за исключением того, что вместо аллилхлорформиата использовали 2,2,2-трихлорэтилхлорформиат (2,93 мл, 21,9 ммоль), получая желаемое соединение (12,4 г, 85%).
МС (ХИАД, ИЭР) m/z: 769(M+H)+
[0492]
Стадия 4: Соединение 21-5
Соединение, полученное на стадии 3 (12,4 г, 16,1 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (9,90 г, 94%).
МС (ХИАД, ИЭР) m/z: 655(M+H)+
[0493]
Стадия 5: Соединение 21-6
Соединение, полученное на стадии 4 (9,90 г, 15,1 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (8,19 г, 83%).
МС (ХИАД, ИЭР) m/z: 653(M+H)+
[0494]
Стадия 6: Соединение 21-7
К соединению, полученному на стадии 5 (3,00 г, 4,59 ммоль), в тетрагидрофуране (10 мл) и 10% водном растворе ацетата аммония (10 мл), добавляли 10% Cd/Pb (3,00 г, 24,0 ммоль, 90 масс. %) и полученный продукт интенсивно перемешивали в атмосфере азота. После того, как исходные вещества были израсходованы, реакционную смесь фильтровали. Фильтрат подвергали экстракции дихлорметаном. Органический слой промывали солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт фильтровали и затем подвергали перегонке при пониженном давлении и полученное соединение (2,10 г, 99%) непосредственно применяли для последующей реакции.
МС (ХИАД, ИЭР) m/z: 461(M+H)+
[0495]
Стадия 7: Соединение 21-8
Соединение, полученное на стадии 6 (2,10 г, 4,56 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (2,09 г, 99%).
МС (ХИАД, ИЭР) m/z: 463(M+H)+
[0496]
Стадия 8: Соединение 21-9
Соединение, полученное на стадии 7 (2,09 г, 4,52 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 21, получая желаемое соединение (2,88 г, 100%).
1H-ЯМР(CDCl3) δ: 7,23(1H,s), 6,81(1H,s), 5,40-5,37(1Н,m), 4,95(1Н,m), 4,41(1Н,m), 4,21(1Н,m), 4,05(1Н,m), 3,96-3,92(1H,m), 3,86(3H,s), 3,79-3,75(1H,m), 3,64(1H,m), 2,34-2,28(1H,m), 2,18-2,13(1H,m), 2,05(3H,s), 1,30-1,19(3H,m), 1,11-1,04(18H,m).
МС (ХИАД, ИЭР) m/z: 637(M+H)+
[0497]
Стадия 9: Соединение 21-10
К смешанному раствору соединения, полученного на стадии 8 (2,28 г, 4,51 ммоль), в метаноле (15 мл) и тетрагидрофуране (5 мл) медленно добавляли по каплям раствор карбонат калия (0,624 г, 4,52 ммоль) в воде (15 мл) и полученный продукт перемешивали при комнатной температуре. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом. Органический слой промывали солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт фильтровали и затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 90:10 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (2,08 г, 77%).
1H-ЯМР(CDCl3) δ: 7,18(1H,s), 6,80(1H,s), 4,96(1H,m), 4,64-4,59(1H,m), 4,40(1H,m), 4,18(1H,m), 4,00-3,92(2H,m), 3,82(3H,s), 3,65(2H,m), 2,28-2,20(2H,m), 2,04-1,97(1Н,m), 1,27-1,20(3H,m), 1,09-1,05(18H,m).
МС (ХИАД, ИЭР) m/z: 595(M+H)+
[0498]
Стадия 10: Соединение 21-11
К раствору соединения, полученного на стадии 9 (2,08 г, 3,49 ммоль), и 2,2,6,6-тетраметил-1-пиперидилоксирадикала (0,109 г, 0,698 ммоль) в дихлорметане (50 мл) медленно добавляли иодбензола диацетат (2,00 г, 6,21 ммоль) при охлаждении льдом. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов. После того, как исходные вещества были израсходованы, к реакционной смеси добавляли воду и реакционную смесь подвергали экстракции дихлорметаном. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом магния. Полученный продукт фильтровали и затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 90:10 (об./об.) до 60:40 (об./об.)], получая желаемое соединение (1,94 г, 94%).
1H-MMP(CDCl3) δ: 7,21(1H,s), 6,84(1H,s), 4,96(1H,m), 4,44(1H,m), 4,34-4,23(3H,m), 3,99-3,92(1H,m), 3,86(3H,s), 3,68-3,62(1H,m), 2,94(1H,m), 2,50-2,46(1Н,m), 1,29-1,21(3H,m), 1,21-1,21(18H,m).
МС (ХИАД, ИЭР) m/z: 593(M+H)+
[0499]
Стадия 11: Соединение 21-12
Соединение, полученное на стадии 10 (1,94 г, 3,27 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 3, получая желаемое соединение (2,17 г, 92%).
1H-ЯМР(CDCl3) δ: 7,22-7,18(2H,m), 6,84(1H,s), 4,95(1H,m), 4,45-4,39(2H,m), 4,23-4,15(1H,m), 3,85(3H,s), 3,64(1H,m), 3,36-3,30(1H,m), 2,74-2,68(1H,m), 1,29-1,19(3H,m), 1,11-1,04(18H,m).
[0500]
Стадия 12: Соединение 21-13
Соединение, полученное на стадии 11 (0,837 г, 1,15 ммоль) и сложный эфир пинакола хиноксалин-6-бороновой кислоты (1,18 г, 4,61 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,713 г, 88%).
1H-ЯМР(CDCl3) δ: 8,82-8,77(2H,m), 8,05(1H,m), 7,95(1H,m), 7,79-7,75(2H,m), 7,25(1H,s), 6,88(1H,s), 4,96(1H,m), 4,49-4,40(2H,m), 4,37-4,28(1H,m), 3,88(3H,s), 3,75(1H,m), 3,48(1H,m), 2,90(1H,m), 1,30-1,22(3H,m), 1,13-1,06(18H,m).
МС (ХИАД, ИЭР) m/z: 705(M+H)+
[0501]
Стадия 13: Соединение 21-14
Соединение, полученное на стадии 12 (0,713 г, 1,01 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,400 г, 72%).
1H-MMP(CDCl3) δ: 8,81-8,80(2H,m), 8,05(1H,m), 7,95(1H,m), 7,80-7,75(2H,m), 7,29(1H,s), 6,96(1H,s), 6,10(1H,m), 5,07(1H,m), 4,45-4,32(3H,m), 3,98(3H,s), 3,80-3,73(1H,m), 3,51-3,46(1H,m), 2,91(1H,m).
МС (ХИАД, ИЭР) m/z: 549(M+H)+
[0502]
Стадия 14: Соединение 21-15
Используя соединение, полученное на стадии 11 примера 1 (0,321 г, 0,346 ммоль), соединение, полученное на стадии 13 (0,200 г, 0,364 ммоль), подвергали реакции сочетания таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,475 г, 99%).
1H-MMP(CDCl3) δ: 8,83-8,79(2H,m), 8,65-8,55(1H,m), 8,09-7,98(2H,m), 7,92-7,82(2H,m), 7,47-7,31(2H,m), 7,24-7,19(1H,m), 7,14-7,02(2H,m), 6,97-6,88(1H,m), 6,80-6,66(1H,m), 6,55-6,47(1H,m), 6,06-6,00(1H,m), 5,97-5,85(1H,m), 5,51-5,09(3H,m), 4,82-4,71(2H,m), 4,63-4,52(2H,m), 4,48-4,30(2H,m), 4,26-4,17(2H,m), 4,16-4,09(1H,m), 4,08-3,98(3H,m), 3,9-3,73(6H,m), 3,53-3,44(2H,m), 3,28-3,26(1H,m), 2,94-2,91(1H,m), 2,40-2,33(2H,m), 2,21-2,13(1H,m), 2,07-2,03(4H,m), 1,67-1,50(2H,m), 1,46-1,39(2H,m), 1,29-1,24(2H,m), 1,00-0,60(18H,m), 0,22-0,06(6H,m).
МС (ХИАД, ИЭР) m/z: 1395(M+H)+
[0503]
Стадия 15: Соединение 21-16
Соединение, полученное на стадии 14 (0,475 г, 0,340 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,310 г, 71%).
1Н-ЯМР(CDCl3) δ: 8,83-8,79(2Н,m), 8,72(1Н,m), 8,07-8,01(2Н,m), 7,88(2Н,m), 7,41-7,39(2H,m), 7,23(1H,m), 7,13(2H,m), 6,84(1H,m), 6,56(1H,s), 5,95-5,88(2H,m), 5,48-5,47(1Н,m), 5,32-5,10(3Н,m), 4,87-4,72(2Н,m), 4,61-4,55(2Н,m), 4,47-4,20(3Н,m), 4,07-4,03(2H,m), 3,90(3H,s), 3,83(3H,s), 3,80-3,72(3Н,m), 3,58(1Н,m), 3,49(1Н,m), 3,31(1Н,m), 2,92(1Н,m), 2,41(1Н,m), 2,36-2,29(1Н,m), 2,19-2,11(1Н,m), 1,77-1,72(1Н,m), 1,68-1,66(3Н,m), 1,65-1,63(1Н,m), 1,42-1,41(3Н,m), 0,97(3Н,m), 0,93(3Н,m), 0,76-0,61(4Н,m).
МС (ХИАД, ИЭР) m/z: 1282(M+H)+
[0504]
Стадия 16: Соединение 21-17
Соединение, полученное на стадии 15 (0,310 г, 0,242 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 21, получая желаемое соединение (0,168 г, 63%).
1H-ЯМР(CDCl3) δ: 8,85-8,76(3H,m), 8,04-7,99(3H,m), 7,86(1H,s), 7,49-7,41(3H,m), 7,25-7,06(3H,m), 6,96-6,83(1H,m), 6,49(1H,m), 6,13(1H,s), 5,51-5,45(2H,m), 5,34-5,28(2H,m), 5,21(1H,m), 4,80-4,37(4H,m), 4,17-4,02(6H,m), 3,88(3H,s), 3,84-3,70(6H,m), 3,68-3,50(5H,m), 3,31(1H,m), 2,93-2,90(1H,m), 2,42(1H,m), 2,29-2,12(3H,m), 1,78-1,75(1H,m), 1,44(3H,m), 0,97(3H,m), 0,94(3H,m), 0,79-0,60(4H,m).
МС (ХИАД, ИЭР) m/z: 1108(M+H)+
[0505]
Стадия 17: Соединение 21-18
Соединение, полученное на стадии 16 (0,168 г, 0,152 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,112 г, 72%).
1Н-ЯМР(CDCl3) δ: 9,18(1Н,m), 8,78(2Н,m), 8,04-8,02(2Н,m), 7,95-7,93(2H,m), 7,77(1H,s), 7,50-7,44(3H,m), 7,23-7,21(1Н,m), 7,11(2Н,m), 6,44(1Н,m), 6,11(1Н,m), 5,90(1Н,m), 5,34(1Н,m), 4,74-4,63(3H,m), 4,42(1H,m), 4,16-4,03(3H,m), 3,89(3H,s), 3,80(3H,s), 3,74-3,72(1H,m), 3,65-3,51(4Н,m), 3,32-3,28(3Н,m), 2,92(1Н,m), 2,41(1Н,m), 2,34-2,28(1Н,m), 2,20-2,18(2Н,m), 1,76(4Н,m), 1,43(3Н,m), 1,00(3Н,m), 0,84(3Н,m), 0,75-0,62(4Н,m).
МС (ХИАД, ИЭР) m/z: 1024(M+H)+
[0506]
Стадия 18: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-5-оксо-2-(хиноксалин-6-ил)-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 18 (0,112 г, 0,109 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,110 г, 71%).
МС (ХИАД, ИЭР) m/z: 1425 (М+Н)+
[0507]
Пример 22: Лекарственное средство-линкер 20
[Формула 146]
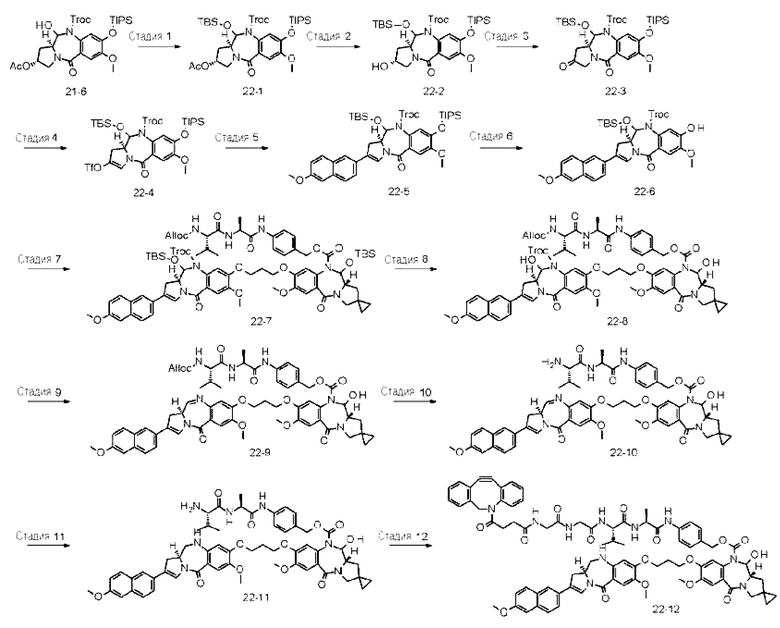
Стадия 1: Соединение 22-1
Соединение, полученное на стадии 5 примера 21 (5,11 г, 7,81 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (5,70 г, 95,0%).
МС (ХИАД, ИЭР) m/z: 767(M+H)+
[0508]
Стадия 2: Соединение 22-2
Соединение, полученное на стадии 1 (5,70 г, 7,42 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 21, получая желаемое соединение (5,07 г, 94%).
МС (ХИАД, ИЭР) m/z: 725(M+H)+
[0509]
Стадия 3: Соединение 22-3
Соединение, полученное на стадии 2 (5,07 г, 6,98 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 21, получая желаемое соединение (4,44 г, 88%).
МС (ХИАД, ИЭР) m/z: 723(M+H)+
[0510]
Стадия 4: Соединение 22-4
Соединение, полученное на стадии 3 (4,44 г, 6,13 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 3, получая желаемое соединение (4,85 г, 92%).
1H-ЯМР(CDCl3) δ: 7,24-7,16(1H,m), 6,78(1H,s), 5,92(1H,m), 5,05(1H,m), 4,34(1H,m), 3,91-3,87(2H,m), 3,86(3H,s), 3,35-3,29(1H,m), 2,80(1H,m), 1,28-1,22(3H,m), 1,10-1,05(18H,m), 0,86(9H,s), 0,28(3H,s), 0,21(3H,s).
[0511]
Стадия 5: Соединение 22-5
Соединение, полученное на стадии 4 (1,20 г, 1,40 ммоль), и 6-метокси-2-нафтилбороновую кислоту (0,850 г, 4,21 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (1,06 г, 88%).
1H-MMP(CDCl3) δ: 7,72-7,69(2H,m), 7,59-7,51(3H,m), 7,30(1H,s), 7,16-7,07(2H,m), 6,82(1H,s), 5,94(1H,m), 5,06(1H,m), 4,34(1H,m), 3,99-3,95(1H,m), 3,93(3H,s), 3,88(3H,s), 3,46(1H,m), 2,94(1H,m), 1,30-1,23(3H,m), 1,12-1,07(18H,m), 0,93(9H,s), 0,31(3H,s), 0,23(3H,s).
[0512]
Стадия 6: Соединение 22-6
Соединение, полученное на стадии 5 (1,06 г, 1,23 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,6126 г, 71%).
МС (ХИАД, ИЭР) m/z: 707(M+H)+
[0513]
Стадия 7: Соединение 22-7
Соединение, полученное на стадии 6 (0,205 г, 0,290 ммоль), и соединение, полученное на стадии 11 примера 1 (0,255 г, 0,274 ммоль), подвергали реакции сочетания таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,375 г, 83%).
1H-MMP(CDCl3) δ: 8,68(1H,s), 7,72(2H,m), 7,67-7,55(3H,m), 7,36-7,21(4H,m), 7,16-7,06(4H,m), 6,82-6,79(2H,m), 6,53(1H,s), 6,03-6,02(1H,m), 5,97-5,89(2H,m), 5,36-5,30(2H,m), 5,23-5,16(3H,m), 4,83-4,80(1H,m), 4,75-4,72(1H,m), 4,61-4,55(3H,m), 4,33-4,29(1H,m), 4,17-4,ll(2H,m), 4,06-4,01(2H,m), 3,94(3H,s), 3,92-3,90(2H,m), 3,81(3H,s), 3,72-3,70(1H,m), 3,51-3,47(2H,m), 3,26(1H,m), 2,99-2,95(1H,m), 2,42-2,32(2H,m), 2,20-2,13(1H,m), 1,55-1,40(4H,m), 0,97-0,92(18H,m), 0,84-0,81 (9H,m), 0,69-0,63(4H,m), 0,30-0,05(12H,m).
[0514]
Стадия 8: Соединение 22-8
Соединение, полученное на стадии 7 (0,375 г, 0,241 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,236 г, 74%).
1H-MMP(CDCl3) δ: 8,70(1H,s), 7,72-7,68(3H,m), 7,63-7,58(2H,m), 7,43-7,41(2H,m), 7,27-7,22(2H,m), 7,16-7,12(2H,m), 6,91-6,86(2H,m), 6,56(1H,s), 5,95-5,84(2H,m), 5,49(1H,m), 5,34-5,14(4H,m), 4,78(1H,m), 4,64-4,53(4H,m), 4,27-4,24(2H,m), 4,17-4,02(3H,m), 3,97-3,88(2H,m), 3,93(3H,s), 3,89(3H,s), 3,88(3H,s), 3,75-3,72(2H,m), 3,61-3,48(3H,m), 3,33-3,30(2H,m), 3,23-3,19(1H,m), 2,44-2,39(2H,m), 2,29-2,27(2H,m), 2,17-2,11(1H,m), 1,76-1,72(1H,m), 1,43(3H,m), 0,95(3H,m), 0,92(3H,m), 0,77-0,61 (4H,m).
[0515]
Стадия 9: Соединение 22-9
Соединение, полученное на стадии 8 (0,236 г, 0,178 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 21, получая желаемое соединение (0,201 г, 99%).
МС (ХИАД, ИЭР) m/z: 1134(М+Н)+
[0516]
Стадия 10: Соединение 22-10
Соединение, полученное на стадии 9 (0,201 г, 0,177 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,180 г, 97%).
1H-MMP(CDCl3) δ: 9,17(1H,s), 7,90(1H,s), 7,72-7,68(2H,m), 7,63-7,53(4H,m), 7,44-7,42(2H,m), 7,25-7,22(1H,m), 7,16-7,12(3H,m), 7,02-6,99(2H,m), 6,76-6,74(1H,m), 6,59(1H,s), 6,41(1H,s), 5,94-5,87(2H,m), 5,42(1H,m), 4,66(1H,m), 4,56-4,49(2H,m), 4,40-4,38(1H,m), 4,29-4,24(1H,m), 4,17-4,11(1H,m), 3,93(3H,s), 3,89(3H,s), 3,87(3H,s), 3,85-3,70(2H,m), 3,65-3,59(2H,m), 3,37-3,31(2H,m), 3,06(1H,m), 2,46-2,41 (2H,m), 2,20(1H,m), 2,10-2,06(1H,m), 1,76-1,74(2H,m), 1,17(3H,m), 0,88-0,63(4H,m), 0,78(3H,m), 0,67(3H,m).
МС (ХИАД, ИЭР) m/z: 1050(M+H)+
[0517]
Стадия 11: Соединение 22-11
Соединение, полученное на стадии 10 (0,0870 г, 0,0828 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,0650 г, 75%).
1H-ЯМР(CDCl3) δ: 9,19(1H,s), 7,92(1H,m), 7,73-7,64(4H,m), 7,55-7,44(4H,m), 7,22(1H,s), 7,15-7,09(4H,m), 6,43(1H,s), 6,09(1H,s), 5,90(2H,m), 5,34(1H,m), 4,72(1H,m), 4,65-4,63(1H,m), 4,36-4,34(1H,m), 4,17-4,02(4H,m), 3,92(3H,s), 3,89(3H,s), 3,80(3H,s), 3,78-3,72(3H,m), 3,60-3,46(5H,m), 3,31-3,27(2H,m), 2,89-2,85(1H,m), 2,41(1H,m), 2,33-2,26(1Н,m), 2,21-2,15(2Н,m), 1,77-1,75(1Н,m), 1,43(3Н,m), 0,98(3Н,m), 0,83(3Н,m), 0,76-0,61(4Н,m).
МС (ХИАД, ИЭР) m/z: 1051 (М+Н)+
[0518]
Стадия 12: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(6-метоксинафтален-2-ил)-5-оксо-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 11 (0,065 г, 0,062 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,048 г, 54%).
МС (ХИАД, ИЭР) m/z: 1453 (М+Н)+
[0519]
Пример 23: Лекарственное средство-линкер 21
[Формула 147]
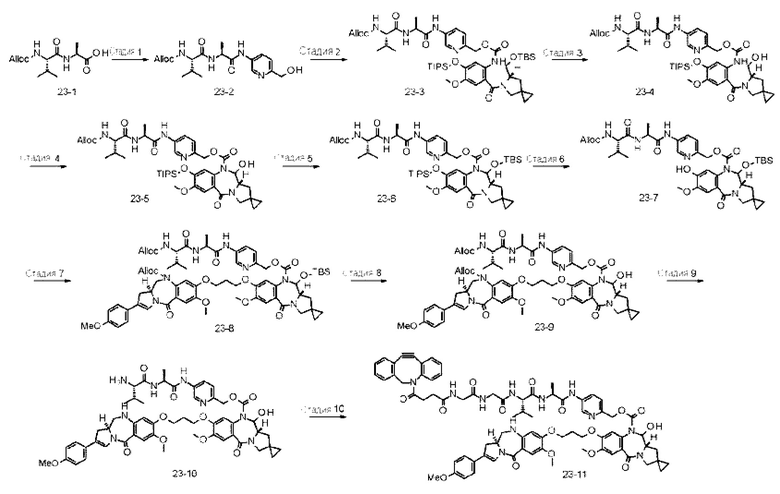
Стадия 1: Соединение 23-2
Исходное вещество 23-1 (14,8 г, 54,4 ммоль, WO 2011130613), подвергали реакции таким же образом, как и на стадии 2 примера 5, получая желаемое соединение (12,2 г, 63%).
МС (ХИАД, ИЭР) m/z: 379 (M+H)+
[0520]
Стадия 2: Соединение 23-3
Соединение, полученное на стадии 1 (3,78 г, 10,0 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (3,86 г, 40%).
МС (ХИАД, ИЭР) m/z: 967(M+H)+
[0521]
Стадия 3: Соединение 23-4
Соединение, полученное на стадии 2 (3,860 г, 3,99 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (3,11 г, 92%).
1Н-ЯМР(CDCl3) δ: 9,03(1Н,m), 8,70-8,63(2Н,m), 8,17-8,13(1H,m), 7,68(1H,s), 7,35(1H,m), 6,82-6,76(2H,m), 5,93-5,83(1H,m), 5,49-5,42(1H,m), 5,32-5,17(4H,m), 4,73-4,52(5H,m), 4,03(1H,m), 3,86(1H,s), 3,80-3,75(2H,m), 3,77(3H,s), 3,65-3,63(1H,m), 3,12-3,10(1H,m), 2,20-2,14(1H,m), 1,93-1,88(1Н,m), 1,45(3Н,m), 1,31-1,23(3Н,m), 1,10-1,08(18Н,m), 0,98(3Н,m), 0,94(3Н,m), 0,64-0,47(4Н,m).
[0522]
Стадия 4: Соединение 23-5
Соединение, полученное на стадии 3 (3,11 г, 3,65 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (2,58 г, 84%).
1H-ЯМР(CDCl3) δ: 9,02-8,88(1H,m), 8,69-8,59(1H,m), 8,17-8,02(1H,m), 7,22-7,17(1Н,m), 7,02(1Н,m), 6,79-6,78(2Н,m), 6,63(1Н,m), 5,95-5,87(2Н,m), 5,33-5,11(4Н,m), 4,65-4,53(3H,m), 4,01(1H,m), 3,83(3H,s), 3,73(1H,m), 3,59(1H,m), 3,32(1H,m), 2,43-2,39(1Н,m), 2,18-2,16(1Н,m),1,75-1,67(2Н,m), 1,48-1,43(3Н,m), 1,20-1,14(3Н,m),1,10-0,94(24Н,m), 0,73-0,60(4Н,m).
[0523]
Стадия 5: Соединение 23-6
Соединение, полученное на стадии 4 (2,58 г, 3,03 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (2,75 г, 94%).
1H-ЯМР(CDCl3) δ: 8,78(1Н,m), 8,58(1Н,m), 8,03(1Н,m), 7,21(1Н,s), 6,97(1Н,m), 6,73(1Н,s), 6,59-6,55(1Н,m), 6,02(1Н,m), 5,93-5,85(1Н,m), 5,32-5,04(4Н,m), 4,72-4,55(3H,m), 3,99(1H,m), 3,84(3H,s), 3,73-3,70(1Н,m), 3,53(1Н,m), 3,28(1Н,m), 2,36(1Н,m), 2,21-2,14(1Н,m), 1,55-1,53(1Н,m), 1,47-1,44(4Н,m), 1,23-1,16(3Н, m), 1,10-1,00(18H,m), 0,98(3H,m), 0,94(3H,m), 0,83(9H,s), 0,81-0,60(4H,m), 0,21-0,19(3Н,m), 0,18-0,16(3Н, m).
[0524]
Стадия 6: Соединение 23-7
Соединение, полученное на стадии 5 (2,75 г, 2,85 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (2,28 г, 99%).
МС (ХИАД, ИЭР) m/z: 809(M+H)+
[0525]
Стадия 7: Соединение 23-8
Соединение, полученное на стадии 6 (0,340 г, 0,420 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,530 г, 98%).
МС (ХИАД, ИЭР) m/z: 1285(M+H)+
[0526]
Стадия 8: Соединение 23-9
Соединение, полученное на стадии 7 (0,530 г, 0,412 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,362 г, 75%).
МС (ХИАД, ИЭР) m/z: 1171(M+H)+
[0527]
Стадия 9: Соединение 23-10
Соединение, полученное на стадии 8 (0,444 г, 0,379 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,347 г, 91%).
МС (ХИАД, ИЭР) m/z: 1103(M+H)+
[0528]
Стадия 10: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{6-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]пиридин-3-ил}-L-аланинамид
Соединение, полученное на стадии 9 (0,100 г, 0,0997 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,067 г, 48%).
МС (ХИАД, ИЭР) m/z: 1404 (М+Н)+
[0529]
Пример 24: Лекарственное средство-линкер 22
[Формула 148]
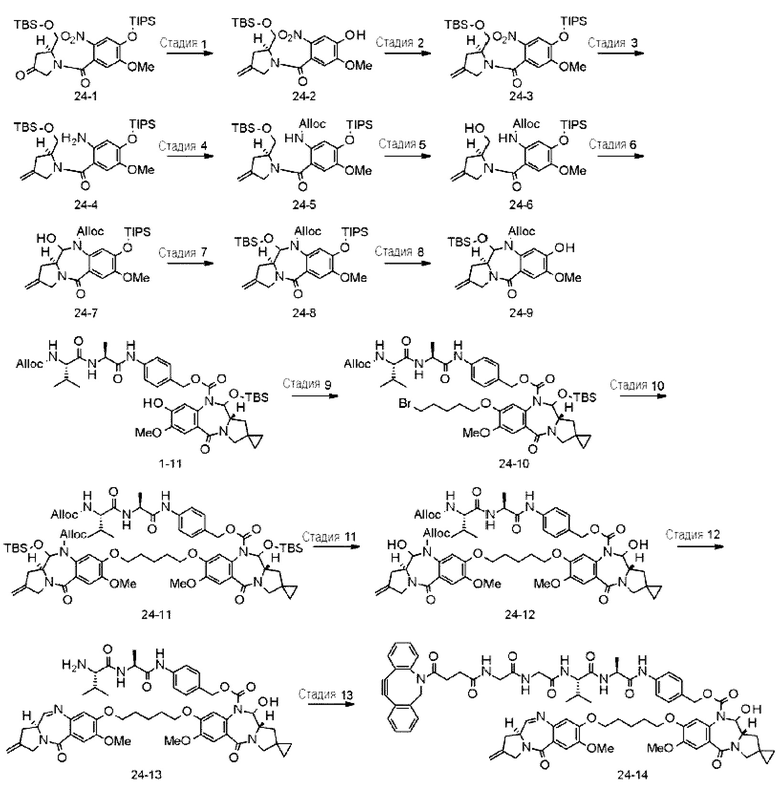
Стадия 1: Соединение 24-2
К суспензионному раствору метилтрифенилфосфония бромида (7,28 г, 20,4 ммоль) в тетрагидрофуране (30 мл) добавляли небольшими порциями калий трет-бутоксид (2,06 г, 18,3 ммоль) в атмосфере азота при 0°С и полученный продукт затем перемешивали в течение 2 часов. Затем к нему по каплям добавляли раствор соединения 24-1 (1,18 г, 2,04 ммоль, WO 2013053872) в ТГФ (10 мл) в течение 2 минут и полученный продукт перемешивали при 0°С в течение 28 часов. К раствору реакционной смеси добавляли воду и водный раствор лимонной кислоты (рН=4,0), полученную смесь затем экстрагировали этилацетатом. Органический слой промывали солевым раствором и сушили над сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (0,450 г, 52%).
МС (ХИАД, ИЭР) m/z: 423(M+H)+.
[0530]
Стадия 2: Соединение 24-3
К раствору соединения, полученного на стадии 1 (0,668 г, 1,58 ммоль), в N,N-диметилформамиде (10 мл) добавляли имидазол (0,211 г, 3,16 ммоль) в атмосфере азота. После этого к нему по каплям добавляли триизопропилсилилхлорид (0,502 мл, 2,37 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 6 часов. К реакционному раствору добавляли 10% водный раствор лимонной кислоты, полученную смесь дважды экстрагировали этилацетатом. Органический слой промывали солевым раствором, сушили над безводным сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (0,520 г, 57%).
МС (ХИАД, ИЭР) m/z: 579(M+H)+.
[0531]
Стадия 3: Соединение 24-4
Соединение, полученное на стадии 2 (0,520 г, 0,898 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 17, получая желаемое соединение (0,478 г, 97%).
МС (ХИАД, ИЭР) m/z: 547(M-H)+.
[0532]
Стадия 4: Соединение 24-5
Соединение, полученное на стадии 3 (0,478 г, 0,871 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, в атмосфере азота. После перегонки при пониженном давлении полученный остаток (0,570 г) непосредственно применяли для последующей реакции.
[0533]
Стадия 5: Соединение 24-6
Соединение, полученное на стадии 4 (0,570 г), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (0,446 г, 95%).
МС (ХИАД, ИЭР) m/z: 519(M+H)+.
[0534]
Стадия 6: Соединение 24-7
Соединение, полученное на стадии 5 (0,446 г, 0,859 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (0,196 г, 44%).
1H-ЯМР(CDCl3) δ: 7,19(1H,s), 6,68(1H,s), 5,78-5,76(1H,m), 5,55(1H,m), 5,19-5,13(4H,m), 4,61-4,58(1H,m), 4,49-4,46(1H,m), 4,29(1H,m), 4,15(1H,m), 3,85(3H,s), 3,61(1H,m), 3,38(1H,s), 2,93-2,90(1Н,m), 2,71 (1H,m), 1,30-1,18(3H,m), 1,12-1,06(18H,m).
МС (ХИАД, ИЭР) m/z: 517(M+H)+.
[0535]
Стадия 7: Соединение 24-8
Соединение, полученное на стадии 6 (0,195 г, 0,377 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,230 г, 97%).
1H-ЯМР(CDCl3) δ: 7,19(1H,s), 6,66(1H,s), 5,75-5,65(1H,m), 5,66(1H,m), 5,12-5,10(4H,m), 4,59(1H,m), 4,35(1H,m), 4,28(1H,m), 4,11(1H,m), 3,86(3H,s), 3,53(1H,m), 2,90-2,84(1H,m), 2,48(1H,m), 1,26-1,19(3H,m), 1,09-1,06(18H,m), 0,86(9H,s), 0,23(3H,s), 0,17(3H,s).
[0536]
Стадия 8: Соединение 24-9
Соединение, полученное на стадии 7 (0,230 г, 0,365 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1. На этой стадии после завершения реакции проводили операцию разделения жидкости и для последующей реакции использовали неочищенный продукт (0,238 г, количественный выход), полученный удалением органического растворителя посредством перегонки при пониженном давлении.
[0537]
Стадия 9: Соединение 24-10
Соединение, полученное на предыдущей стадии, и соединение, полученное на стадии 10 примера 1 (0,251 г, 0,311 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 3, получая желаемое соединение (0,185 г, 62%).
МС (ХИАД, ИЭР) m/z: 958[81Br, (M+H)+ ], 956[79Br, (M+H)+].
[0538]
Стадия 10: Соединение 24-11
Соединение, полученное на стадии 8 (0,0660 г, 0,139 ммоль), и соединение, полученное на стадии 9 (0,133 г, 0,139 ммоль) подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,123 г, 66%).
МС (ХИАД, ИЭР) m/z: 1350(M+H)+.
[0539]
Стадия 11: Соединение 24-12
Соединение, полученное на стадии 10 (0,123 г, 0,0910 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,0950 г, 92%).
1H-ЯМР(CDCl3) δ: 8,65(1H,s), 7,59(2H,m), 7,31-7,29(2H,m), 7,23-7,21(3H,m), 6,89-6,86(1H,m), 6,78(1H,s), 6,38(1H,s), 5,92-5,88(2H,m), 5,81-5,79(1H,m), 5,61-5,52(2H,m), 5,31(2H,m), 5,23(1H,n), 5,13-5,10(4H,m), 5,05-5,02(1H,m), 4,69-4,67(2H,m), 4,58-4,55(2H,m), 4,49-4,46(1H,m), 4,30(2H,m), 4,16(1H,m), 3,98-3,96(3H,m), 3,93(3H,s), 3,89(3H,s), 3,81-3,78(2H,m), 3,74(1H,m), 3,69-3,66(1Н,m), 3,61(1Н,m), 3,43-3,41(1Н,m), 3,32(1Н,m), 2,89-2,87(1Н,m), 2,73(1Н,m), 2,42(1Н,m), 2,10-2,08(1Н,m), 1,80-1,73(4Н,m), 1,53-1,50(2H,m), 1,25-1,24(3H,m), 0,93-0,89(6H,m), 0,75-0,63(4H,m).
МС (ХИАД, ИЭР) m/z: 1122(M+H)+ .
[0540]
Стадия 12: Соединение 24-13
Соединение, полученное на стадии 11 (0,0950 г, 0,0847 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0610 г, 76%).
1Н-ЯМР(CDCl3) δ: 9,12-8,96(1Н,m), 7,82-7,60(4Н,m), 7,22-7,19(3Н,m), 6,94-6,66(1Н,m), 6,40-6,34(2Н,m), 5,89-5,86(1Н,m), 5,55(1Н,m), 5,40-5,07(3Н,m), 4,60-4,42(4Н,m), 4,23-4,09(5Н,m), 3,91-3,88(8Н,m), 3,81-3,75(8Н,m), 3,60(1Н,m), 3,32-3,30(2Н,m), 3,24-3,22(1Н,m), 3,12-3,09(1Н,m), 2,65-2,61(1Н,m), 2,41(1Н,m), 2,12-2,11(1Н,m), 1,89-1,84(9Н,m), 1,75(3Н,m), 1,40-1,38(2Н,m), 1,25-1,21(3Н,m), 0,99(3Н,m), 0,84(3Н,m), 0,74-0,66(6Н,m).
МС (ХИАД, ИЭР) m/z: 936(M+H)+.
[0541]
Стадия 13: N-[4-(11,12-дидегидродибензо[b,r]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11aS)-7-метокси-2-метилиден-5-оксо-2,3,5,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 12 (0,0600 г, 0,0629 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,075 г, 89%).
1Н-ЯМР(ДМСО-D6) δ: 9,91(1Н,s), 8,21-8,16(2Н,m), 8,07-8,03(1H,m), 7,74-7,65(3Н,m), 7,60-7,44(6Н,m), 7,39-7,29(5Н,m), 7,21-7,19(2H,m), 7,03(1H,s), 6,85(1H,s), 6,72(1H,s), 6,58-6,56(1H,m), 5,77-5,74(1H,m), 5,19-5,16(3Н,m), 5,03-5,00(1Н,m), 4,82-4,79(1Н,m), 4,36-4,33(1Н,m), 4,21-4,19(1Н,m), 4,14-4,11(2Н,m), 4,00-3,95(3Н,m), 3,80-3,73(10Н,m), 3,65-3,52(4Н,m), 3,41-3,38(2Н,m), 3,15-3,30(1Н,m), 3,14(1Н,m), 3,04-3,01(1Н,m), 2,68-2,66(1Н,m), 2,32-2,28(2Н,m), 2,05-1,98(2Н,m), 1,78-1,77(5Н,m), 1,57-1,54(3Н,m), 1,28-1,25(3Н,m), 0,86-0,81(6Н,m), 0,67-0,62(4Н,m).
МС (ХИАД, ИЭР) m/z: 1337(M+H)+ .
[0542]
Пример 25: Лекарственное средство-линкер 23
[Формула 149]
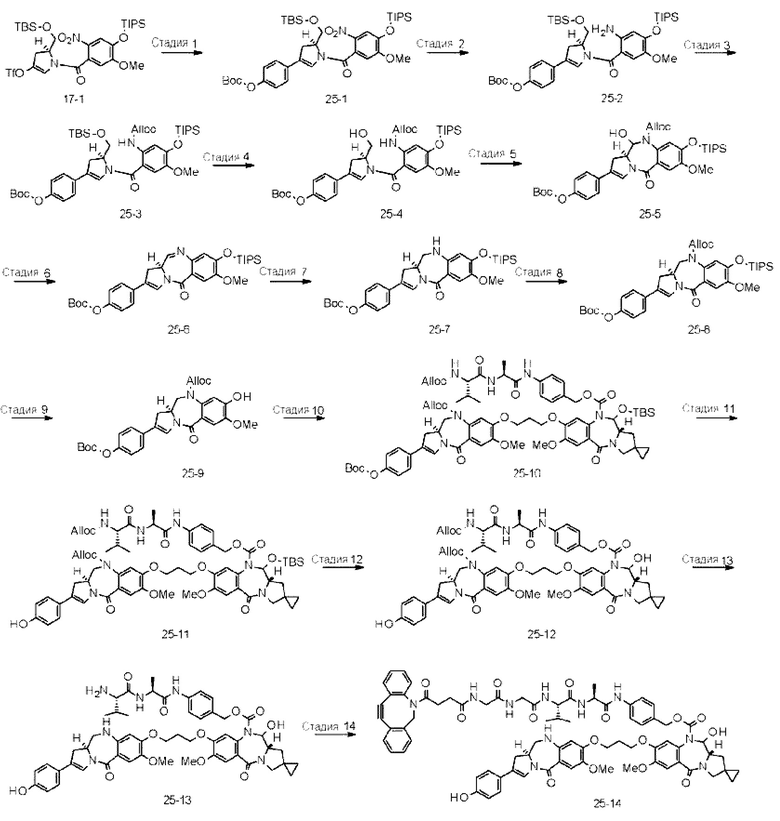
Стадия 1: Соединение 25-1
Исходное вещество 17-1 (3,81 г, 5,34 ммоль) и трет-бутил-4-(4,4,5,5-тетраметил-1,3,2-Диоксаборан-2-ил)фенижарбонат (5,13 г, 16,0 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (3,05 г, 75%).
МС (ХИАД, ИЭР) m/z: 757(M+H)+.
[0543]
Стадия 2: Соединение 25-2
Соединение, полученное на стадии 1 (3,05 г, 4,09 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 17, получая желаемое соединение (2,67 г, 91%).
МС (ХИАД, ИЭР) m/z: 727(M+H)+.
[0544]
Стадия 3: Соединение 25-3
Соединение, полученное на стадии 2 (2,67 г, 3,67 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3. На этой стадии после завершения реакции проводили операцию разделения жидкости и неочищенный продукт (3,00 г, количественный выход), полученный концентрированием органического растворителя при пониженном давлении, непосредственно использовали для последующей реакции.
[0545]
Стадия 4: Соединение 25-4
Соединение, полученное на стадии 3 (3,05 г), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (2,67 г, количественный выход).
1H-ЯМР(CDCl3) δ: 8,34(1H,m), 7,70(1H,m), 7,24(2H,m), 7,12(2H,m), 6,86(1H,s), 6,84(1H,s), 5,95-5,89(1H,m), 5,31(1H,m), 5,21(1H,m), 4,87-4,86(1H,m), 4,61-4,61(2H,m), 4,41(1H,m), 3,93-3,90(2H,m), 3,76(3H,s), 3,29(1H,m), 2,68-2,66(1H,m), 1,55(9H,s), 1,33-1,26(3H,m), 1,13-1,1 l(18H,m).
МС (ХИАД, ИЭР) m/z: 697(M+H)+.
[0546]
Стадия 5: Соединение 25-5
Соединение, полученное на стадии 4 (1,22 г, 1,75 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 9, получая желаемое соединение (0,838 г, 69%).
1H-ЯМР(CDCl3) δ: 7,45(1H,s), 7,37(2H,m), 7,22(1H,s), 7,15(2H,m), 7,11-7,09(1H,m), 6,72(1H,s), 5,82-5,79(1H,m), 5,19-5,16(2H,m), 4,61-4,59(2H,m), 4,50-4,47(1H,m), 4,00(1H,m), 3,86(3H,s), 3,41-3,28(1H,m), 3,09-3,05(1H,m), 1,57(9H,s), 1,29-1,25(3H,m), 1,14-1,07(18H,m).
МС (ХИАД, ИЭР) m/z: 695(M+H)+.
[0547]
Стадия 6: Соединение 25-6
Соединение, полученное на стадии 5 (0,838 г, 1,21 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,745 г, количественный выход).
1H-ЯМР(CDCl3) δ: 7,88(1H,m), 7,50(1H,s), 7,48-7,48(1H,m), 7,40(2H,m), 7,18(2H,m), 6,86(1H,s), 4,45-4,43(1H,m), 3,90(3H,s), 3,60-3,56(1Н,m), 3,38(1H,m), 1,57(9H,s), 1,31-1,26(3H,m), 1,11-1,10(18H,m).
МС (ХИАД, ИЭР) m/z: 593(M+H)+.
[0548]
Стадии 7-9: Соединение 25-9
Соединение, полученное на стадии 6 (0,745 г, 1,26 ммоль), подвергали реакции таким же образом, как и на стадиях 8 и 9 примера 3 и стадии 10 примера 1, получая желаемое соединение (0,516 г, выход на трех стадиях: 78%).
1H-MMP(CDCl3) δ: 7,46(1H,s), 7,35(2H,m), 7,27-7,25(2H,m), 7,15(2H,m), 6,82(1H,s), 5,93(1H,s), 5,84-5,81(1H,m), 5,12(1H,m), 4,61(1H,m), 4,49-4,46(1H,m), 4,35-4,32(1H,m), 4,23-4,21(1H,m), 3,96(3H,s), 3,65-3,62(1H,m), 3,29(1H,m), 2,71(1H,m), 1,57(9H,s).
МС (ХИАД, ИЭР) m/z: 523(M+H)+.
[0549]
Стадия 10: Соединение 25-10
Соединение, полученное на стадии 9 (0,105 г, 0,200 ммоль) и соединение, полученное на стадии 11 примера 1 (0,186 г, 0,200 ммоль), подвергали реакции сочетания таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,248 г, 90%).
1H-ЯМР(CDCl3) δ: 8,72-8,50(1H,m), 7,52(1H,s), 7,40-7,38(4H,m), 7,23-7,21(2H,m), 7,16(2H,m), 7,09(1H,m), 6,84-6,82(2H,m), 6,51-6,49(1H,m), 6,02(1H,m), 5,92-5,90(1H,m), 5,30-5,21(5H,m), 4,71-4,61(6H,m), 4,36-4,24(5H,m), 4,02-4,00(3H,m), 3,93-3,88(1H,m), 3,87(3H,s), 3,81(3H,s), 3,71(2H,m), 3,51-3,49(1H,m), 3,32-3,28(2H,m), 2,72(1H,m), 2,37-2,34(3H,m), 2,16-2,13(1H,m), 1,66(9H,s), 1,50-1,46(4H,m), 0,97-0,93(7H,m), 0,82(9H,s), 0,68-0,65(4H,m), 0,20(3H,s), 0,14(3H,s).
МС (ХИАД, ИЭР) m/z: 1370(M+H)+.
[0550]
Стадия 11: Соединение 25-11
К раствору соединения, полученного на стадии 10 (0,248 г, 0,181 ммоль) в дихлорметане (3 мл), добавляли пиперидин (3 мл) и полученный продукт перемешивали при комнатной температуре в течение 2 часов. Реакционный раствор разбавляли водным раствором лимонной кислоты и дважды экстрагировали этилацетатом. Органический слой промывали солевым раствором и сушили над сульфатом натрия. После фильтрации органический растворитель удаляли при помощи перегонки при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : метанол = 100:0 (об./об.) до 90:10 (об./об.)], получая желаемое соединение (0,153 г, 93%).
1H-MMP(CDCl3) δ: 8,77-8,69(1H,m), 7,40-7,36(3H,m), 7,23-7,21(4H,m), 7,07(2H,m), 6,88-6,86(1H,m), 6,82(2H,m), 6,51(1H,s), 6,03(1H,m), 5,92-5,90(1H,m), 5,30-5,21(4H,m), 4,75-4,72(2H,m), 4,58-4,55(3H,m), 4,37-4,35(1H,m), 4,23-4,21(3H,m), 4,01-3,99(2H,m), 3,86(3H,s), 3,79(3H,s), 3,72(2H,m), 3,66-3,64(1H,m), 3,51-3,48(1H,m), 3,28(2H,m), 2,67(1H,m), 2,37-2,12(4H,m), 1,55-1,52(2H,m), 1,45-1,42(4H,m), 0,95-0,91(6H,m), 0,81(9H,s), 0,81-0,78(2H,m), 0,68-0,65(3H,m), 0,20-0,15(6H,m).
МС (ХИАД, ИЭР) m/z: 1270(M+H)+.
[0551]
Стадия 12: Соединение 25-12
Соединение, полученное на стадии 11 (0,175 г, 0,138 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,162 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 1156 (М+Н)+.
[0552]
Стадия 13: Соединение 25-13
Соединение, полученное на стадии 12 (0,116 г, 0,100 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0410 г, 41%).
МС (ХИАД, ИЭР) m/z: 988 (М+Н)+.
[0553]
Стадия 14: N-[4-(11,12-дидегидродибензо[b,r]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-8'-(3-{[(11aS)-2-(4-гидроксифенил)-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 13 (0,00500 г, 0,00506 ммоль) и соединение, полученное на стадии 2 примера 2 (0,0100 г, 0,0202 ммоль), растворяли в дихлорметане (0,3 мл) и метаноле (0,3 мл) и добавляли к нему N,N-диизопропилэтиламин (3,5 мкл, 0,0202 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Реакционный раствор подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : CMW = 100:0 (об./об.) до 0:100(об./об.)], получая желаемое соединение (0,00350 г, 50%).
МС (ХИАД, ИЭР) m/z: 1389 (М+Н)+.
[0554]
Пример 26: Лекарственное средство-линкер 24
[Формула 150]
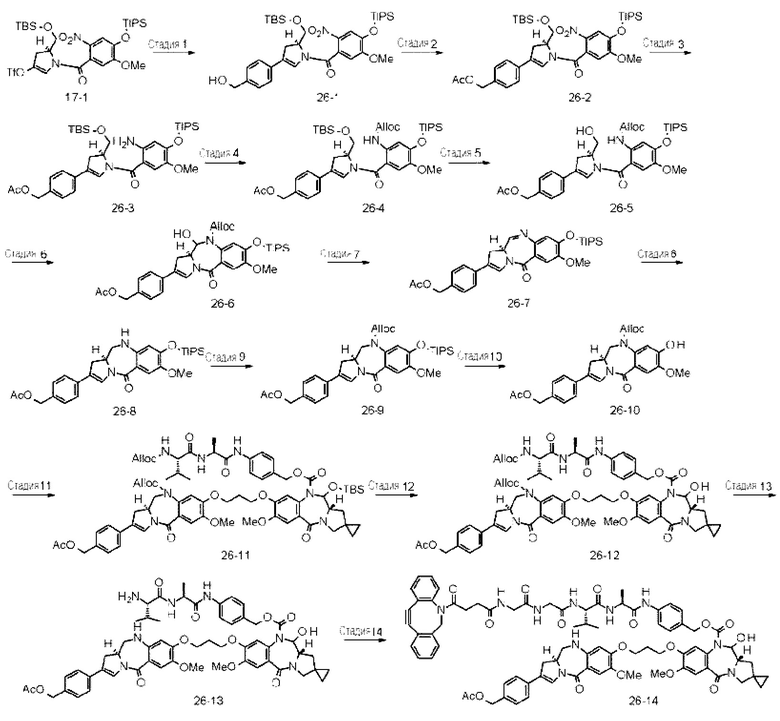
Стадия 1: Соединение 26-1
Исходное вещество 17-1 (3,93 г, 5,51 ммоль) и 4-(гидроксиметил)фенилбороновую кислоту подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (3,09 г, 84%).
МС (ХИАД, ИЭР) m/z: 671 (M+H)+.
[0555]
Стадия 2: Соединение 26-2
Раствор соединения, полученного на стадии 1 (3,09 г, 4,61 ммоль), в дихлорметане (100 мл) охлаждали льдом, к нему добавляли триэтиламин (1,60 мл, 11,5 ммоль) и затем к нему по каплям добавляли ацетилхлорид (0,491 мл, 6,91 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 2 часов. Реакционный раствор разбавляли водным раствором лимонной кислоты и три раза экстрагировали хлороформом. Органический слой промывали насыщенным водным раствором карбоната натрия и солевым раствором и сушили над безводным сульфатом натрия и затем растворитель удаляли при помощи перегонки при пониженном давлении. Полученное соединение (3,75 г, количественный выход) непосредственно применяли для последующей реакции.
[0556]
Стадия 3: Соединение 26-3
Соединение, полученное на стадии 2 (3,28 г, 4,60 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 17, получая желаемое соединение (2,09 г, 67%).
МС (ХИАД, ИЭР) m/z: 682(M+H)+.
[0557]
Стадия 4: Соединение 26-4
Соединение, полученное на стадии 3 (1,01 г, 1,48 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3. Полученный продукт подвергали перегонке при пониженном давлении и полученное соединение (1,19 г, количественный выход) непосредственно применяли для последующей реакции.
[0558]
Стадия 5: Соединение 26-5
Соединение, полученное на стадии 4 (1,19 г, 1,55 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (0,885 г, 87%).
1H-ЯМР(CDCl3) δ: 8,34(1H,m), 7,71(1H,s), 7,31(2H,m), 7,24(2H,m), 6,91(1H,s), 6,84(1H,s), 5,97-5,88(1H,m), 5,35-5,29(1H,m), 5,22-5,20(1H,m), 5,07(2H,s), 4,88-4,87(1H,m), 4,62-4,61(3H,m), 4,33-4,31(1H,m), 3,94-3,91(2H,m), 3,76(3H,s), 3,33-3,29(1H,m), 2,68(1H,m), 1,33-1,29(4H,m), 1,15-1,12(18H,m).
МС (ХИАД, ИЭР) m/z: 653(M+H)+.
[0559]
Стадии 6 и 7: Соединение 26-7
Соединение, полученное на стадии 5 (0,885 г, 1,36 ммоль), обрабатывали таким же образом, как и на стадии 3 примера 9 и стадии 12 примера 3, получая желаемое соединение (0,515 г, 85%).
МС (ХИАД, ИЭР) m/z: 549 (М+Н)+.
[0560]
Стадия 8-10: Соединение 26-10
Соединение, полученное на стадии 7 (0,515 г, 0,983 ммоль), подвергали реакции таким же образом, как и на стадиях 8 и 9 примера 3 и стадии 10 примера 1, получая желаемое соединение (0,448 г, количественный выход).
1H-ЯМР(CDCl3) δ: 7,51(1H,s), 7,37-7,30(4H,m), 7,26-7,25(1H,m), 6,82(1H,s), 5,94(1H,s), 5,86-5,79(1H,m), 5,15-5,13(1H,m), 5,09(3H,s), 4,61(1H,m), 4,48-4,46(1H,m), 4,35-4,32(1H,m), 4,25-4,23(1H,m), 3,96(3H,s), 3,64(1H,d,m), 3,33-3,29(1H,m), 2,73(1H,m), 2,11(3H,s).
МС (ХИАД, ИЭР) m/z: 479(M+H)+.
[0561]
Стадия 11: Соединение 26-11
Соединение, полученное на стадии 10 (0,0690 г, 0,144 ммоль) и соединение, полученное на стадии 11 примера 1 (0,134 г, 0,144 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,118 г, 62%).
МС (ХИАД, ИЭР) m/z: 1325(M+H)+.
[0562]
Стадии 12 и 13: Соединение 26-13
Соединение, полученное на стадии 11 (0,134 г, 0,101 ммоль), подвергали реакции таким же образом, как и на стадиях 11 и 12 примера 3, получая желаемое соединение (0,0950 г, выход на двух стадиях: 90%)
1H-ЯМР(CDCl3) δ: 9,14(1H,s), 7,91(1H,m), 7,69(1H,s), 7,47(4H,m), 7,40-7,38(2H,m), 7,34-7,32(2H,m), 7,21(1H,s), 7,18(2H,m), 7,13(2H,m), 6,40(1H,s), 6,08(1H,s), 5,88(1H,m), 5,36(1H,m), 5,09(2H,s), 4,72(1H,m), 4,62-4,59(2H,m), 4,35-4,32(1H,m), 4,12-4,07(4H,m), 3,89(3H,s), 3,80(3H,s), 3,74-3,71(2H,m), 3,58-3,53(3H,m), 3,41-3,38(1H,m), 3,31-3,29(2H,m), 2,78-2,74(1H,m), 2,41(1H,m), 2,31-2,31(1H,m), 2,18-2,15(1H,m), 2,11(3H,s), 1,76(1H,m), 1,44-1,42(3H,m), 0,99(3H,m), 0,83(3H,m), 0,71-0,66(4H,m).
МС (ХИАД, ИЭР) m/z: 1044(M+H)+.
[0563]
Стадия 14: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-8'-(3-{[(11aS)-2-{4-[(ацетилокси)метил]фенил}-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-11'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 13 (0,0700 г, 0,0670 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0520 г, 54%).
МС (ХИАД, ИЭР) m/z: 1445 (М+Н)+.
[0564]
Пример 27: Лекарственное средство-линкер 25
[Формула 151]
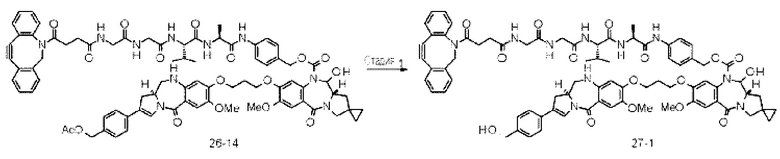
Стадия 1: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-8'-[3-({(11aS)-2-[4-(гидроксиметил)фенил]-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
К раствору соединения, полученного на стадии 14 примера 26 (0,0230 г, 0,0159 ммоль) в метаноле (2 мл) добавляли 1 н. раствор гидроксида натрия (0,0175 мл, 0,0175 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. К нему дополнительно добавляли 1 н. раствор гидроксида натрия (0,0175 мл, 0,0175 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 30 минут. К реакционному раствору добавляли 1 н. водный раствор соляной кислоты (0,0350 мл) и воду и полученный продукт три раза экстрагировали хлороформом. Органический слой сушили над сульфатом натрия и подвергали перегонке при пониженном давлении и полученный остаток затем очищали с помощью колоночной хроматографии на силикагеле [хлороформ : CMW = 100:0 (об./об.) до 0:100(об./об.)], получая желаемое соединение (0,0190 г, 85%).
МС (ХИАД, ИЭР) m/z: 1403 (М+Н)+.
[0565]
Пример 28: Лекарственное средство-линкер 26
[Формула 152]
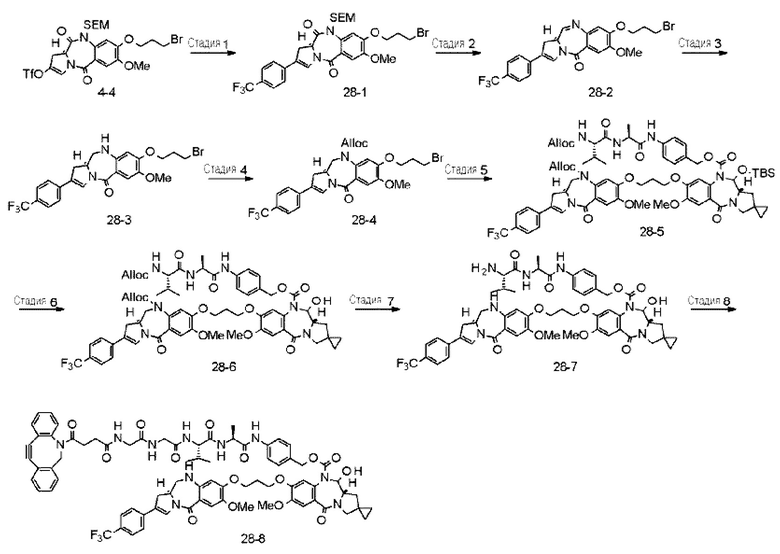
Стадия 1: Соединение 28-1
Соединение, полученное на стадии 4 примера 4 (1,12 г, 1,70 ммоль) и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборан-2-ил)трифторметилбензол (0,924 г, 3,40 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,918 г, 83%).
МС (ХИАД, ИЭР) m/z: 657[81Br, (M+H)+],655[79Br, (M+H)+].
[0566]
Стадия 2: Соединение 28-2
Соединение, полученное на стадии 1 (0,918 г, 1,40 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,425 г, 60%).
МС (ХИАД, ИЭР) m/z: 511[81Br, (М+Н)+],509[79Br, (М+Н)+].
[0567]
Стадия 3: Соединение 28-3
Соединение, полученное на стадии 2 (0,425 г, 0,834 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3. После операции отделения жидкости полученный продукт подвергали перегонке при пониженном давлении и полученное соединение (0,410 г) непосредственно применяли для последующей реакции.
[0568]
Стадия 4: Соединение 28-4
Соединение, полученное на стадии 2 (0,425 г, 0,834 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3 и стадии 9 примера 3, получая желаемое соединение (0,420 г, 85%). МС (ХИАД, ИЭР) m/z: 597[81Br, (М+Н)+],595 [79Br, (М+Н)+].
[0569]
Стадия 5: Соединение 28-5
Соединение, полученное на стадии 4 (0,0960 г, 0,160 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,212 г, 99%).
МС (ХИАД, ИЭР) m/z: 1321(M+H)+.
[0570]
Стадия 6: Соединение 28-6
Соединение, полученное на стадии 5 (0,210 г, 0,159 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,162 г, 84%).
МС (ХИАД, ИЭР) m/z: 1208(M+H)+.
[0571]
Стадия 7: Соединение 28-7
Соединение, полученное на стадии 6 (0,160 г, 0,132 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,103 г, 75%).
МС (ХИАД, ИЭР) m/z: 1039(M+H)+.
[0572]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-5-оксо-2-[4-(трифторметил)фенил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Исходное вещество 4-4 и соединение, полученное на стадии 7 (0,101 г, 0,0971 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,107 г, 76%).
МС (ХИАД, ИЭР) m/z: 1441 (М+Н)+.
[0573]
Пример 29: Лекарственное средство-линкер 27
[Формула 153]
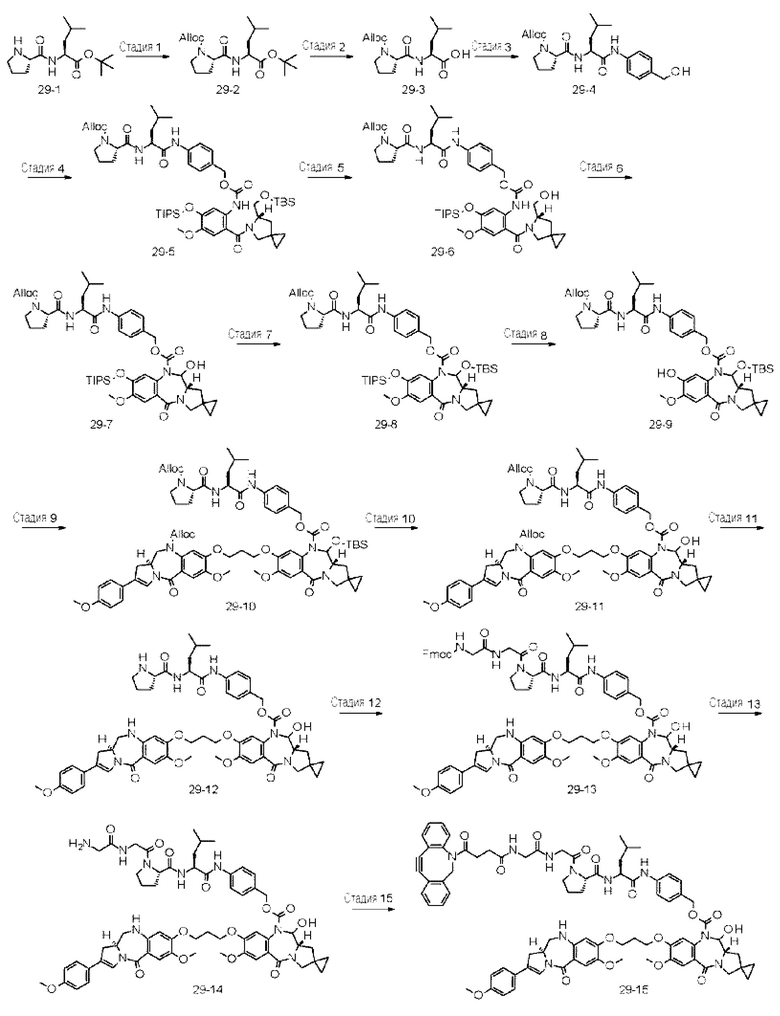
Стадия 1: Трет-бутал-1-[(проп-2-ен-1-илокси)карбонил]-L-пролил-L-лейцинат
Трет-бутил-L-пролил-L-лейцинат (4,64 г, 16,3 ммоль) подвергали реакции таким же образом, как и на стадии 9 примера 3, за исключением того, что вместо пиридина использовали триэтиламин (3,41 мл, 24,5 ммоль). После завершения реакции проводили операцию отделения жидкости, органический растворитель удаляли при помощи перегонки при пониженном давлении и полученное соединение (5,79 г, 96%) непосредственно применяли для последующей реакции.
[0574]
Стадия 2: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-L-лейцин
К раствору соединения, полученного на стадии 1 (5,79 г, 15,7 ммоль) в дихлорметане (60 мл) добавляли трифторуксусную кислоту (20 мл) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. К раствору реакционной смеси добавляли толуол и полученную смесь подвергали перегонке при пониженном давлении и полученное соединение (2,69 г, 55%) непосредственно применяли для последующей реакции.
[0575]
Стадия 3: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-[4-(гидроксиметил)фенил]-L-лейцинамид
К раствору соединения, полученного на стадии 2 (6,10 г, 19,5 ммоль) в ТГФ (100 мл) добавляли М-этоксикарбонил-2-этокси-1,2-дигидрохинолин (5,07 г, 20,5 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. К нему добавляли 4-аминобензиловый спирт (2,16 г, 20,5 ммоль) и полученный продукт перемешивали в течение ночи. Реакционный раствор подвергали перегонке при пониженном давлении и полученный остаток растворяли в этилацетате. Полученный продукт промывали разбавленной соляной кислотой, насыщенным водным раствором гидрокарбоната натрия и солевым раствором и органический слой сушили над безводным сульфатом натрия. После фильтрации растворитель удаляли при помощи перегонки при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 90:10 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (1,60 г, 20%).
1H-ЯМР(CDCl3) δ: 8,62-8,33(1H,m), 7,68-7,49(2H,m), 7,31-7,30(2H,m), 6,66-6,43(1H,m), 5,97-5,70(1H,m), 5,39-4,96(2H,m), 4,64-4,53(5H,m), 4,40-4,35(1H,m), 3,57-3,50(2H,m), 2,20-2,19(2H,m), 1,98-1,97(3H,m), 1,66-1,64(3H,m), 0,97-0,94(6H,m).
МС (ХИАД, ИЭР) m/z: 418(M+H)+.
[0576]
Стадия 4: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-[4-({[(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамоил]окси}метил)фенил]-L-лейцинамид
Соединение, полученное на стадии 3 (0,838 г, 2,01 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 1, получая желаемое соединение (0,535 г, 37%).
1H-ЯМР(CDCl3) δ: 8,98(1H,m), 8,62(1H,s), 7,80(1H,s), 7,65-7,50(2H,m), 7,33-7,31(2H,m), 6,76(1H,s), 6,67-6,34(1H,m), 5,95-5,92(1H,m), 5,33-5,25(1H,m), 5,30-5,27(1H,m), 5,12(2H,s), 4,66-4,63(3H,m), 4,58-4,55(3H,m), 4,38-4,36(1H,m), 3,99-3,96(1H,m), 3,73(3H,s), 3,70-3,65(2H,m), 3,57-3,55(2H,m), 3,04-3,02(1H,m), 2,21-2,20(3H,m), 1,98-1,95(3H,m), 1,74-1,62(3H,m), 1,32-1,30(3H,m), 1,11-1,09(16H,m), 0,97-0,94(6H,m), 0,90(9H,s), 0,60-0,52(4H,m), 0,05-0,04(6H,m).
[0577]
Стадии 5 и 6: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 4 (0,535 г, 0,531 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1 и стадии 3 примера 9, получая желаемое соединение (0,367 г, 78%).
1H-ЯМР(CDCl3) δ: 8,60(1H,s), 7,58-7,42(2H,m), 7,19-7,16(3H,m), 6,69-6,64(2H,m), 5,89-5,87(2H,m), 5,32-5,24(2H,m), 5,10(1H,m), 4,93(1H,m), 4,65-4,63(1H,m), 4,57-4,54(2H,m), 4,37-4,34(1H,m), 3,84(3H,s), 3,72(1H,m), 3,57-3,55(3H,m), 3,40-3,38(1Н,ш), 3,31(1Н,m), 2,41(1Н,m), 2,20-2,18(2Н,m), 1,98-1,95(3Н,m), 1,73(1Н,m), 1,66-1,63(1Н,m), 1,16-1,10(4Н,m), 1,05-0,99(18Н,m) 0,97-0,93(6Н,m), 0,71-0,64(4Н,m).
МС (ХИАД, ИЭР) m/z: 890(M+H)+ .
[0578]
Стадия 7: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 6 (0,367 г, 0,412 ммоль) использовали и подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (0,181 г, 44%).
1H-ЯМР(CDCl3) δ: 8,54(1H,s), 7,52-7,45(2H,m), 7,19(1H,s), 7,14(2H,m), 6,71-6,68(1H,m), 6,61(1H,s), 6,01(1H,m), 5,94-5,92(1H,m), 5,34-5,17(2H,m), 4,77(1H,m), 4,64-4,56(3H,m), 4,38-4,35(1H,m), 3,85(3H,s), 3,72-3,69(1H,m), 3,55-3,46(3H,m), 3,27(1H,m), 2,35(1H,m), 2,21-2,18(2H,m), 1,97-1,95(3H,m), 1,54-1,51(2H,m), 1,16-1,09(5H,m), 1,02-1,01(18H,m), 0,97-0,93(6H,m), 0,81(9H,s), 0,68-0,63(4H,m), 0,19(3H,s), 0,09(3H,s).
[0579]
Стадия 8: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 7 (0,181 г, 0,180 ммоль) обрабатывали таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,153 г, количественный выход).
1H-ЯМР (CDCl3) δ: 8,57-8,27(1H,m), 7,69-7,41(2H,m), 7,23(1H,s), 7,12(2H,m), 6,69-6,66(1H,m), 6,64(1H,s), 5,99-5,92(3H,m), 5,34-5,19(3H,m), 4,81(1H,m), 4,63-4,57(4H,m), 4,38-4,36(1H,m), 3,94(3H,s), 3,71(1H,m), 3,54-3,52(3H,m), 3,27(1H,m), 2,35(1H,m), 2,19(2H,m), 1,97-l,95(3H,m), 1,55-1,52(2H,m), 0,97-0,93(6H,m), 0,81(9H,s), 0,76-0,61(4H,m), 0,21(3H,s), 0,09(3H,s).
MC (ХИАД, ИЭР) m/z: 848 (M+H)+.
[0580]
Стадия 9: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]- 10'(5'Н)-ил] карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 8 (0,153 г, 0,180 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 4, получая желаемое соединение (0,137 г, 57%).
1H-ЯМР(CDCl3) δ: 8,79(1H,s), 7,54-7,51(1H,m), 7,39-7,37(2H,m), 7,30-7,29(2H,m), 7,23-7,21(3H,m), 7,13-7,11(2H,m), 6,88(2H,m), 6,82-6,80(1H,m), 6,50-6,48(1H,m), 6,03-6,01(1H,m), 5,92-5,89(1H,m), 5,75-5,72(1H,m), 5,28-5,26(3H,m), 5,06-5,03(2H,m), 4,74-4,71(1H,m), 4,62-4,60(4H,m), 4,36-4,34(2H,m), 4,22-4,19(3H,m), 4,01-3,99(1H,m), 3,88(3H,s), 3,84-3,81(6H,m), 3,71(2H,m), 3,53-3,50(4H,m), 3,28-3,25(2H,m), 2,72-2,68(1H,m), 2,37-2,34(4H,m), 2,19-2,16(3H,m), 1,97-1,94(2H,m), 1,49-1,43(2H,m), 0,95-0,92(7H,m), 0,81(9H,s), 0,68-0,65(4H,m), 0,19(3H,s), 0,13(3H,s). MC (ХИАД, ИЭР) m/z: 1324 (M+H)+.
[0581]
Стадия 10: 1-[(Проп-2-ен-1-илокси)карбонил]-L-пролил-N-{4-[({[(11а'8)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 9 (0,136 г, 0,103 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,116 г, 93%).
1H-ЯМР(CDCl3) δ: 8,83(1H,s), 7,57-7,52(1H,m), 7,39-7,37(2H,m), 7,30-7,29(2H,m), 7,24-7,20(5H,m), 6,88(2H,m), 6,81(1H,s), 6,54-6,51(1H,m), 5,90-5,88(2H,m), 5,76-5,74(1H,m), 5,55-5,53(1H,m), 5,33-5,05(3H,m), 4,79-4,76(1H,m), 4,63-4,60(4H,m), 4,35-4,33(2H,m), 4,22-4,19(3H,m), 4,04-4,03(1H,m), 3,88(3H,s), 3,85-3,83(6H,m), 3,72(2H,m), 3,62-3,56(4H,m), 3,32-3,29(2H,m), 2,70(1H,m), 2,45-2,38(2H,m), 2,30-2,27(2H,m), 2,20-2,10(3H,m), 1,94-1,89(4H,m), 1,75-1,71(2H,m), 0,95(7H,m), 0,72-0,66(4H,m).
MC (ХИАД, ИЭР) m/z: 1210 (M+H)+.
[0582]
Стадия 11: L-Пролил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
Соединение, полученное на стадии 10 (0,116 г, 0,0958 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0530 г, 53%).
1H-ЯМР(CDCl3) δ: 9,15(1H,s), 8,11(1H,m), 7,50-7,45(4H,m), 7,32-7,31(2H,m), 7,21(1H,s), 7,13(2H,m), 6,89(2H,m), 6,37(1H,s), 6,08(1H,s), 5,88(1H,m), 5,38(1H,m), 4,69(1H,m), 4,63-4,60(1H,m), 4,53-4,51(1H,m), 4,31-4,28(1H,m), 4,13-4,08(3H,m), 3,89(3H,s), 3,83(3H,s), 3,81(3H,s), 3,75-3,70(4H,m), 3,57-3,55(3H,m), 3,37-3,33(2H,m), 3,01-2,99(1H,m), 2,90-2,86(1H,m), 2,76-2,73(1H,m), 2,41(1H,m), 2,17-2,15(3H,m), 1,90-1,87(1H,m), 1,74(4H,m), l,25(2H,m), 0,97-0,91(7H,m), 0,67(4H,m). MC (ХИАД, ИЭР) m/z: 1042 (M+H)+.
[0583]
Стадия 12: N-[(9Н-Флуорен-9-илокси)карбонил]глицилглицил-L-пролил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил] карбонил}окси)метил]фенил}-L-лейцинамид
К раствору соединения, полученного на стадии 11 (0,0410 г, 0,0393 ммоль) и N-[(9Н-флуорен-9-илметокси)карбонил]глицилглицину (0,0410 г, 0,0393 ммоль) в N,N-диметилформамиде (1 мл) добавляли 1-гидроксибензотриазола моногидрат (0,000602 г, 0,00393 ммоль) и 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид (0,00905 г, 0,0472 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле (хлороформ:метанол = 100:0 до 90:10), получая желаемое соединение (0,0520 г, 94%).
1H-ЯМР(CDCl3) δ: 8,57(1H,s), 7,77-7,75(3H,m), 7,63-7,61(2H,m), 7,51-7,48(2H,m), 7,40-7,38(3H,m), 7,31-7,29(4H,m), 7,21-7,11(5H,m), 6,88(2H,m), 6,47(1H,s), 6,08(1H,s), 5,93(1H,m), 5,21-5,19(1H,m), 5,13(1H,m), 4,78(1H,m), 4,66-4,59(1H,m), 4,53-4,51(1H,m), 4,42-4,39(1H,m), 4,33-4,31(1H,m), 4,19-4,11(6H,m), 4,10-3,86(4H,m), 3,82(3H,s), 3,76(3H,s), 3,73-3,71(3H,m), 3,56-3,51(7H,m), 3,32-3,29(2H,m), 2,73-2,69(1H,m), 2,40(1H,m), 2,29-2,27(3H,m), 2,06-2,04(4H,m), 1,73-1,70(2H,m), 1,25(2H,m), 0,96-0,93(6H,m), 0,66(4H,m).
MC (ХИАД, ИЭР) m/z: 1378 (M+H)+.
[0584]
Стадия 13: Глицилглицил-L-пролил-N-{4-[({[(11а'8)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1H-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
К раствору соединения, полученного на стадии 12 (0,0520 г, 0,0377 ммоль), в N,N-диметилформамиде (2 мл) добавляли 1,8-диазабицикло[5,4.0]-7-ундецен (67 мкл, 0,0453 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 1 часа. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ:CMW = 100:0(об./об.) до 0:100(об./об.)], получая желаемое соединение (0,0420 г, 92%).
1H-MMP(CDCl3) δ: 8,64(1H,s), 7,74(1H,m), 7,66-7,64(1H,m), 7,50(1H,s), 7,45(1H,s), 7,33-7,30(3H,m), 7,24-7,21(2H,m), 7,18-7,16(3H,m), 6,89(2H,m), 6,51(1H,s), 6,15(1H,s), 5,89(1H,m), 5,27(1H,m), 4,82-4,78(1H,m), 4,74(1H,m), 4,56-4,54(1H,m), 4,49-4,47(1H,m), 4,23-4,20(3H,m), 4,13-4,10(3H,m), 3,96-3,92(1H,m), 3,90(3H,s), 3,83(3H,s), 3,76(3H,s), 3,72(2H,m), 3,62-3,56(5H,m), 3,40-3,36(1H,m), 3,31(1H,m), 3,04(1H,m), 2,90-2,86(1H,m), 2,75-2,71(1H,m), 2,42-2,39(1H,m), 2,36(2H,s), 2,29-2,27(3H,m), 2,07-2,05(3H,m), 1,97-1,95(1H,m), l,75-l,72(2H,m), 0,94(6H,m), 0,69(4H,m).
MC (ХИАД, ИЭР) m/z: 1156 (M+H)+.
[0585]
Стадия 14: N-[4-(11,12-дидегидродибензо[b,f1]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-пролил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1H-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-лейцинамид
К раствору соединения, полученного на стадии 13 (0,0400 г, 0,0346 ммоль), в N,N-диметилформамиде (1 мл) добавляли 1-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]окси}пирролидин-2,5-дион (0,0140 г, 0,0346 ммоль, Click Chemistry Tools) и диизопропиламин (0,0240 мл, 0,138 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 18 часов. Реакционный раствор подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : метанол = 100:0(об./об.) до 90:10(об./об.)], получая желаемое соединение (0,0230 г, 46%).
МС (ХИАД, ИЭР) m/z: 1443 (М+Н)+.
[0586]
Пример 30: Лекарственное средство-линкер 28
[Формула 154]
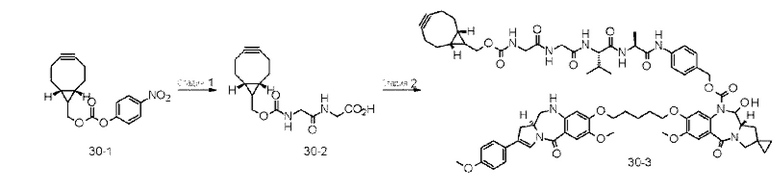
Стадия 1: N-{[(1R,8S)-Бицикло[6,1.0]нон-4-ин-9-илметокси]карбонил}глицилглицин
К раствору исходного вещества 30-1 (0,215 г, 0,682 ммоль, Chemistry-A European Journal 2016, 22, 639) в N,N-диметилформамиде (4 мл) добавляли N,N-диизопропилэтиламин (0,119 мл, 0,682 ммоль), глицил-глицин (0,0900 г, 0,682 ммоль) и воду (2 мл) и полученный продукт перемешивали при комнатной температуре в течение ночи. Реакционный раствор подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : CMW = 100:0(об./об.) до 0:100(об./об.)], получая желаемое соединение (0,205 г, 98%).
МС (ХИАД, ИЭР) m/z: 309(M+H)+.
[0587]
Стадия 2: N-{[(1R,8S)-Бицикло[6,1.0]нон-4-ин-9-илметокси]карбонил}глицилглицил-L-валил-N-{4-[({[(11а'S)-1Г-гидрокси-7'-метокси-8'-[(5-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 1 (0,0180 г, 0,0587 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0420 г, 60%).
1H-ЯМР(ДМСО-D6) δ: 9,93(1H,s), 8,25(1H,m), 8,05(1H,s), 7,85(1H,m), 7,60-7,54(2H,m), 7,45(1H,s), 7,39-7,37(3H,m), 7,29(1H,s), 7,20(1H,m), 7,04(1H,s), 6,91(2H,m), 6,72(1H,s), 6,56-6,53(2H,m), 6,31(1H,s), 5,76-5,74(1H,m), 5,19(1H,m), 4,80(1H,m), 4,38-4,36(1H,m), 4,23-4,21(2H,m), 4,04(2H,m), 3,95-3,92(3H,m), 3,78-3,76(9H,m), 3,66(3H,s), 3,60(2H,m), 3,55-3,52(2H,m), 3,45-3,38(2H,m), 3,26-3,23(1H,m), 3,14(1H,m), 2,77-2,74(1H,m), 2,35-2,33(1H,m), 2,20-2,11(6H,m), 1,99-1,96(1H,m), 1,81-1,78(4H,m), 1,56-1,54(5H,m), 1,29-1,26(4H,m), 0,87-0,82(9H,m), 0,67-0,62(4H,m).
MC (ХИАД, ИЭР) m/z: 1320 (M+H)+.
[0588]
Пример 31: Лекарственное средство-линкер 29
[Формула 155]
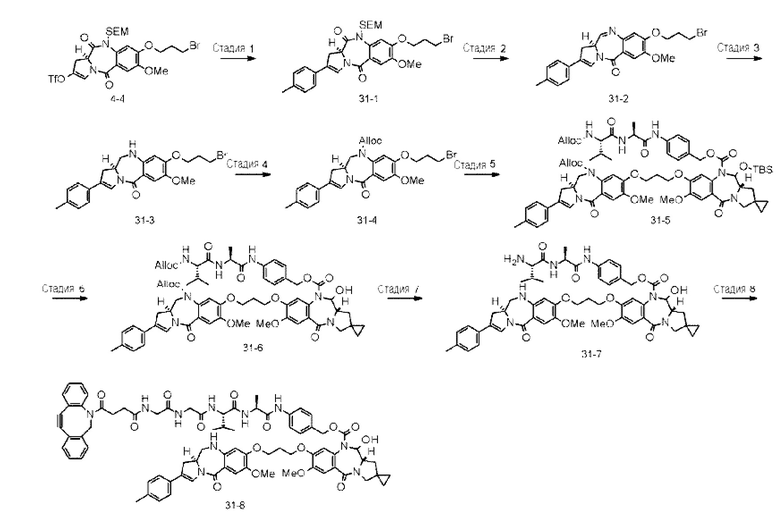
Стадия 1: Соединение 31-1
Соединение, полученное на стадии 4 примера 4 (1,00 г, 1,52 ммоль), и 4-метилфенилбороновую кислоту (0,309 г, 2,27 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,653 г, 72%).
[0589]
Стадия 2: Соединение 31-2
Соединение, полученное на стадии 1 (0,653 г, 1,09 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,377 г, 76%).
МС (ХИАД, ИЭР) m/z: 457[81Br,(M+H)+],455[79Br,(M+H)+].
[0590]
Стадия 3: Соединение 31-3
Соединение, полученное на стадии 2 (0,377 г, 0,828 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,311 г, 82%).
МС (ХИАД, ИЭР) m/z: 459[81Br,(M+H)+],457[79Br,(M+H)+].
[0591]
Стадия 4: Соединение 31-4
Соединение, полученное на стадии 3 (0,311 г, 0,68 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,320 г, 87%).
МС (ХИАД, ИЭР) m/z: 543[81Br,(M+H)+],541[79Br,(M+H)+].
Стадия 5: Соединение 31-5
Соединение, полученное на стадии 4 (0,0737 г, 0,136 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,145 г, 92%).
МС (ХИАД, ИЭР) m/z: 1272(M+H)+.
[0592]
Стадия 6: Соединение 31-6
Соединение, полученное на стадии 5 (0,145 г, 0,114 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,122 г, 93%).
МС (ХИАД, ИЭР) m/z: 1158 (M+H)+.
[0593]
Стадия 7: Соединение 31-7
Соединение, полученное на стадии 6 (0,122 г, 0,114 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0598 г, 53%).
МС (ХИАД, ИЭР) m/z: 990 (M+H)+.
[0594]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (0,0300 г, 0,0304 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0184 г, 44%).
МС (ХИАД, НЭР) m/z: 1391 (М+Н)+.
[0595]
Пример 32: Лекарственное средство-линкер 30
[Формула 156]
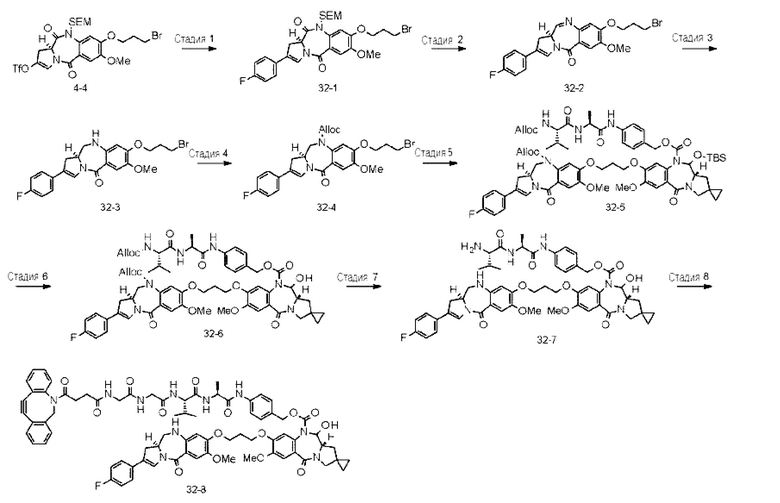
Стадия 1: Соединение 32-1
Соединение, полученное на стадии 4 примера 4(1,00 г, 1,52 ммоль), и 4-фторфенилбороновую кислоту (0,318 г, 2,27 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,623 г, 68%).
[0596]
Стадия 2: Соединение 32-2
Соединение, полученное на стадии 1 (0,623 г, 1,03 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,244 г, 52%).
МС (ХИАД, ИЭР) m/z: 461[81Br,(M+H)+],459[79Br,(M+H)+].
[0597]
Стадия 3: Соединение 32-3
Соединение, полученное на стадии 2 (0,244 г, 0,531 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,144 г, 59%).
МС (ХИАД, ИЭР) m/z: 463[81Br,(M+H)+],461[79Br,(M+H)+].
[0598]
Стадия 4: Соединение 32-4
Соединение, полученное на стадии 3 (0,144 г, 0,312 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,139 г, 82%).
МС (ХИАД, ИЭР) m/z: 547[81Br,(M+H)+],545[79Br,(M+H)+].
[0599]
Стадия 5: Соединение 32-5
Соединение, полученное на стадии 4 (0,0742 г, 0,136 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,138 г, 88%).
МС (ХИАД, ИЭР) m/z: 1284(M+H)+.
[0600]
Стадия 6: Соединение 32-6
Соединение, полученное на стадии 5 (0,138 г, 0,108 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,109 г, 87%).
МС (ХИАД, ИЭР) m/z: 1170 (M+H)+.
[0601]
Стадия 7: Соединение 32-7
Соединение, полученное на стадии 6 (0,109 г, 0,101 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0613 г, 61%).
МС (ХИАД, ИЭР) m/z: 1002 (M+H)+.
[0602]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-8'-(3-{[(11aS)-2-(4-фторфенил)-7-метокси-5-оксо-5,10,11,11a-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-11'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (0,0300 г, 0,0333 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0191 г, 45%).
МС (ХИАД, ИЭР) m/z: 1402 (М+Н)+.
[0603]
Пример 33: Лекарственное средство-линкер 31
[Формула 157]
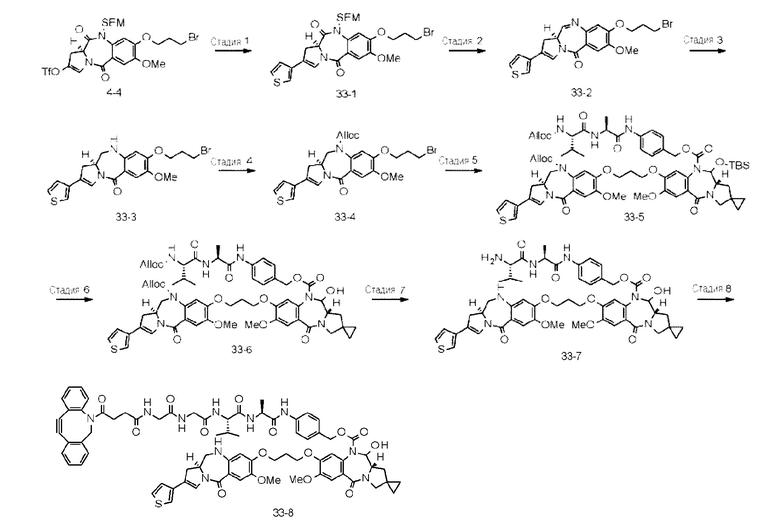
Стадия 1: Соединение 33-1
Использовали соединение, полученное на стадии 4 примера 4 (1,00 г, 1,52 ммоль), и тиофен-3-бороновую кислоту (0,582 г, 4,55 ммоль) и их подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,611 г, 68%).
[0604]
Стадия 2: Соединение 33-2
Использовали соединение, полученное на стадии 1 (0,611 г, 1,03 ммоль), и подвергали его реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,397 г, 86%).
МС (ХИАД, ИЭР) m/z: 449[81Br,(M+H)+],447[79Br,(M+H)+].
[0605]
Стадия 3: Соединение 33-3
Использовали соединение, полученное на стадии 2 (0,397 г, 0,887 ммоль), и подвергали его реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,341 г, 86%).
МС (ХИАД, ИЭР) m/z: 451[81Br,(M+H)+],449[79Br,(M+H)+].
[0606]
Стадия 4: Соединение 33-4
Использовали соединение, полученное на стадии 3 (0,341 г, 0,759 ммоль), и подвергали его реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,368 г, 91%).
МС (ХИАД, ИЭР) m/z: 535[81Br,(M+H)+],533[79Br,(M+H)+].
[0607]
Стадия 5: Соединение 33-5
Использовали соединение, полученное на стадии 4 (0,0726 г, 0,136 ммоль), и подвергали его реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,125 г, 80%).
МС (ХИАД, ИЭР) m/z: 1260 (М+Н)+.
[0608]
Стадия 6: Соединение 33-6
Использовали соединение, полученное на стадии 5 (0,125 г, 0,0992 ммоль), и подвергали его реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,109 г, 96%).
МС (ХИАД, ИЭР) m/z: 1146 (М+Н)+.
[0609]
Стадия 7: Соединение 33-7
Использовали соединение, полученное на стадии 6 (0,109 г, 0,0951 ммоль), и подвергали его реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0723 г, 78%).
1H-ЯМР(CDCl3) δ: 9,13-9,04(1H,m), 7,89-7,87(1H,m), 7,47-7,42(4H,m), 7,27-7,23(3Н,m), 7,18(1Н,8), 7,12-7,08(2Н,m), 6,97-6,96(1Н,m), 6,42-6,37(1Н,m), 6,08-6,04(1Н,m), 5,86-5,84(1Н,m), 5,34-5,31(1Н,m), 4,65-4,58(3Н,m),4,23-3,95(5H,m), 3,85(3H,s), 3,75-3,69(6H,m), 3,57-3,47(3H,m), 3,34-3,29(3H,m), 2,72-2,68(1Н,m), 2,38-2,29(2Н,m), 2,15-2,14(2Н,m), 1,72-1,69(1Н,m), 1,40-1,38(3Н,m), 0,96-0,95(3Н,m), 0,80-0,61(7Н,m).
[0610]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-5-оксо-2-(тиорпеп-3-ил)-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил] карбонил}окси)метил]фенил}-L-аланинамид
Использовали соединение, полученное на стадии 7 (0,0300 г, 0,0307 ммоль), и подвергали его реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0101 г, 24%).
МС (ХИАД, ИЭР) m/z: 1379 (М+Н)+.
[0611]
Пример 34: Лекарственное средство-линкер 32
[Формула 158]
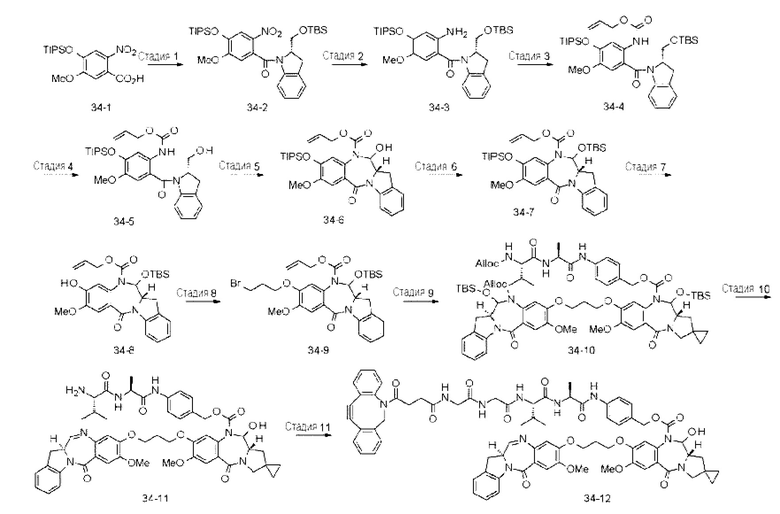
Стадия 1: Соединение 34-2
К раствору исходного вещества 34-1 (4,00 г, 10,8 ммоль, US 20150283262) в дихлорметане (100 мл) добавляли N,N-диметилформамид (0,2 мл) и оксалилхлорид (2,75 г, 21,7 ммоль) при 0°С, затем перемешивали при комнатной температуре в течение 30 минут. После растворитель удаляли при помощи перегонки при пониженном давлении, остаток сушили при пониженном давлении и растворяли в дихлорметане (60 мл). К нему добавляли (2S)-2-({[трет-бутил(диметил)силил]окси}метил)-2,3-дигидро-1Н-индол (4,28 г, 16,2 ммоль, Journal of the American Chemical Society 2006, 128, 14264) и триэтиламин (1,64 г, 16,2 ммоль) при 0°С, затем перемешивали при комнатной температуре в течение 15 минут. К раствору реакционной смеси добавляли воду и полученную смесь подвергали экстракции дихлорметаном. Полученный органический слой промывали солевым раствором и сушили над сульфатом магния и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 80:20 (об./об.)], получая желаемое соединение (6,10 г, 92%).
МС (ХИАД, ИЭР) m/z: 615 (М+Н)+
[0612]
Стадия 2: Соединение 34-3
К раствору соединения, полученного на стадии 1 (6,10 г, 9,90 ммоль), в этаноле (100 мл) добавляли 5% палладий на углероде (содержание влаги: 54%, 1,00 г) в атмосфере азота и реакционный раствор затем перемешивали в атмосфере водорода при комнатной температуре в течение 4 часов. После этого реакционный раствор фильтровали через целит, фильтрат подвергали перегонке при пониженном давлении, получая желаемое соединение (5,80 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 585(M+H)+
[0613]
Стадия 3: Соединение 34-4
Соединение, полученное на стадии 2 (2,90 г, 5,00 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (3,20 г, 96%).
1H-ЯМР(CDCl3) δ: 8,26(1H,s), 7,78(1H,s), 7,18-7,17(1H,m), 6,94-6,83(3H,m), 5,94-5,90(1H,m), 5,35-5,19(2H,m), 4,74(1H,m), 4,65-4,60(2H,m), 3,76-3,61(6H,m), 3,31-3,27(1H,m), 3,10(1H,m), 1,35-1,17(3H,m), 1,10(18H,m), 0,79-0,70(9H,m), -0,03(3H,s), -0,08(3H,s).
[0614]
Стадия 4: Соединение 34-5
Соединение, полученное на стадии 3 (3,20 г, 4,80 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (2,32 г, 87%).
МС (ХИАД, ИЭР) m/z: 555 (M+H)+
[0615]
Стадия 5: Соединение 34-6
Соединение, полученное на стадии 4 (2,32 г, 4,18 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (1,68 г, 73%).
МС (ХИАД, ИЭР) m/z: 553 (M+H)+
[0616]
Стадия 6: Соединение 34-7
Соединение, полученное на стадии 5 (1,68 г, 3,04 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (2,32 г, количественный выход).
1H-MMP(CDCl3) δ: 8,16(1H,m), 7,28-7,20(3H,m), 7,09-7,07(1H,m), 6,70(1H,s), 5,80-5,76(2H,m), 5,14-5,12(2H,m), 4,60(1H,m), 4,37(1H,m), 4,01-3,99(1H,m), 3,87(3H,s), 3,45-3,41(1H,m), 2,99-2,95(1H,m), 1,28-1,23(3H,m), 1,10-1,07(18H,m), 0,92(9H,s), 0,26(3H,s), 0,19(3H,s).
[0617]
Стадия 7: Соединение 34-8
Соединение, полученное на стадии 6 (2,32 г, 3,48 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (1,42 г, 80%).
МС (ХИАД, ИЭР) m/z: 511 (М+Н)+
[0618]
Стадия 8: Соединение 34-9
Соединение, полученное на стадии 7 (0,720 г, 1,41 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 4, получая желаемое соединение (0,580 г, 65%).
МС (ХИАД, ИЭР) m/z: 633[81Br,(M+H)+],631[79Br,(M+H)+].
[0619]
Стадия 9: Соединение 34-10
Соединение, полученное на стадии 8 (0,235 г, 0,371 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 10, получая желаемое соединение (0,347 г, 83%).
МС (ХИАД, ИЭР) m/z: 1359 (M+H)+
[0620]
Стадия 10: Соединение 34-11
Соединение, полученное на стадии 9 (0,347 г, 0,255 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая форму со снятой силильной защитой (0,265 г, 92%). Указанную форму со снятой силильной защитой (0,265 г, 0,234 ммоль) подвергали реакции таким же образом, как и на стадии 12 примера 1, получая желаемое соединение (0,086 г, 39%).
МС (ХИАД, ИЭР) m/z: 944 (М+Н)+
[0621]
Стадия 11: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(5aS)-10-метокси-12-оксо-5а,12-дигидро-5Н-индоло[2,1-с][1,4]бензодиазепин-9-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 10 (0,0860 г, 0,0911 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0800 г, 65%).
МС (ХИАД, ИЭР) m/z: 1345 (М+Н)+
[0622]
Пример 35: Лекарственное средство-линкер 33
[Формула 159]
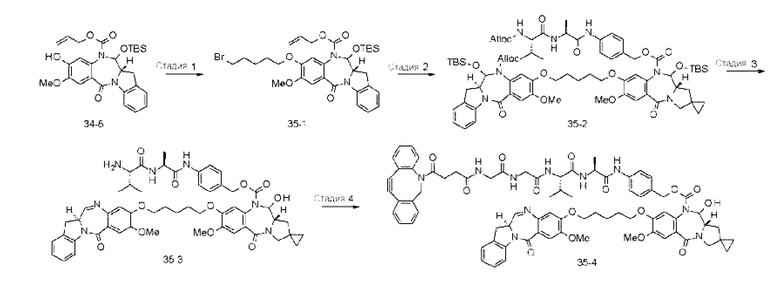
Стадия 1: Соединение 35-1
Соединение, полученное на стадии 7 примера 34 (0,700 г, 1,37 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 3, получая желаемое соединение (0,790 г, 87%).
МС (ХИАД, ИЭР) m/z: 661[81Br,(M+H)+],659[79Br,(M+H)+].
[0623]
Стадия 2: Соединение 35-2
Соединение, полученное на стадии 1 (0,245 г, 0,371 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,368 г, 86%).
МС (ХИАД, ИЭР) m/z: 1387 (М+Н)+
[0624]
Стадия 3: Соединение 35-3
Соединение, полученное на стадии 2 (0,368 г, 0,265 ммоль), подвергали реакции таким же образом, как и на стадиях 11 и 12 примера 3, получая желаемое соединение (0,180 г, 81%).
МС (ХИАД, ИЭР) m/z: 972 (М+Н)+
[0625]
Стадия 4: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(5aS)-10-метокси-12-оксо-5а,12-дигидро-5Н-индоло[2,1-с][1,4]бензодиазепин-9-ил]окси}пентил)окси]-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 3 (0,0700 г, 0,0720 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0440 г, 44%).
МС (ХИАД, ИЭР) m/z: 1373 (М+Н)+
[0626]
Пример 36: Лекарственное средство-линкер 34
[Формула 160]
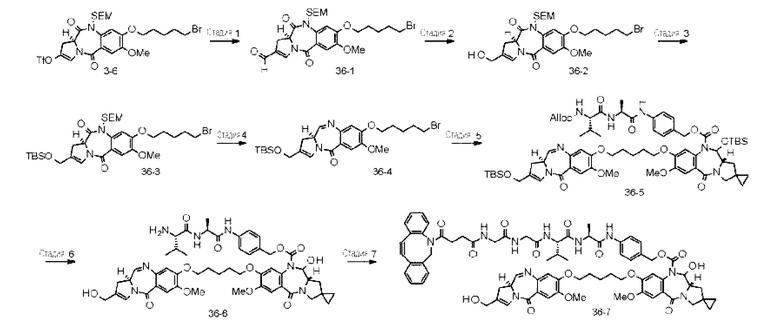
Стадия 1: (11aS)-8-[(5-Бромпентил)окси]-7-метокси-5,11-диоксо-10-{[2-(триметилсилил)этокси]метил}-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-2-карбальдегид
Соединение, полученное на стадии 5 примера 3 (3,54 г, 5,15 ммоль), растворяли в N,N-диметилформамиде (52 мл), к нему добавляли N-формилсахарин (5,44 г, 25,7 ммоль), ацетат палладия (0,0578 г, 0,257 ммоль), 1,4-бис(дифенилфосфино)бутан (0,154 г, 0,360 ммоль), карбонат натрия (2,73 г, 25,7 ммоль) и триэтилсилан (1,20 г, 10,3 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 19 часов. К раствору реакционной смеси добавляли воду и реакционный раствор подвергали экстракции этилацетатом и полученный экстракт промывали водой и солевым раствором. Органический слой сушили над сульфатом магния и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 40:60 (об./об.)], получая желаемое соединение (0,760 г, 26%).
1H-ЯМР(CDCl3) δ: 9,74(1H,s), 7,79(1H,s), 7,32(1H,s), 7,24(1H,s), 5,54(1H,m), 4,76-4,69(2H,m), 4,07-4,05(2H,m), 3,93(3H,s), 3,83-3,65(3H,m), 3,45(2H,m), 3,02-2,98(1Н,m), 1,95-1,9 l(4H,m), 1,69-1,58(2H,m), 1,02-0,92(2H,m), 0,06-0,03(9H,m).
[0627]
Стадия 2: (11aS)-8-[(5-Бромпентил)окси]-2-(гидроксиметил)-7-метокси-10-{[2-(триметилсилил)этокси]метил}-1H-пирроло[2,1-c][1,4]бензодиазепин-5,11(10Н,11аН)-дион
Соединение, полученное на стадии 1 (0,760 г, 1,34 ммоль), растворяли в дихлорметане (14 мл), к нему добавляли борогидрид натрия (0,101 г, 2,68 ммоль) при -78°С и затем температуру повышали до комнатной температуры. К реакционному раствору добавляли 1 н. соляную кислоту и органический слой промывали водой и солевым раствором. Органический слой сушили над сульфатом магния и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (0,432 г, 57%).
1H-ЯМР(CDCl3) δ: 7,35(1H,s), 7,23(1H,s), 6,93(1H,s), 5,53(1H,m), 4,67(1H,m), 4,57-4,54(1H,m), 4,32-4,31(2H,m), 4,10-4,01(2H,m), 3,92(3H,s), 3,83-3,57(3H,m), 3,45(2H,m), 2,90-2,88(1H,m), 1,99-1,88(4H,m), 1,69-1,61(2H,m), 1,00-0,98(2H,m), 0,03(9H,s).
МС (ХИАД, ИЭР) m/z: 571[81Br,(M+H)+],569[79Br,(M+H)+].
[0628]
Стадия 3: (11aS)-8-[(5-Бромпентил)окси]-2-({[трет-бутил(диметил)силил]окси}метил)-7-метокси-10-{[2-(триметилсилил)этокси]метил}-1H-пирроло[2,1-c][1,4]бензодиазепин-5,11(10Н,11аН)-дион
Соединение, полученное на стадии 2 (0,432 г, 0,758 ммоль), растворяли в N,N-диметилформамиде (8 мл), к нему добавляли имидазол (0,0775 г, 1,14 ммоль) и трет-бутилдиметилсилилхлорид (0,137 г, 0,910 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 10 минут. К раствору реакционной смеси добавляли воду и реакционный раствор подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над сульфатом магния. После перегонки при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 30:70 (об./об.)], получая желаемое соединение (0,485 г, 94%).
1H-ЯМР(CDCl3) δ: 7,35(1H,s), 7,22(1H,s), 6,87(1H,m), 5,53(1H,m), 4,68(1H,m), 4,54-4,52(1H,m), 4,33-4,28(2H,m), 4,11-4,00(2H,m), 3,92(3H,s), 3,80-3,78(1H,m), 3,69-3,66(1H,m), 3,52-3,50(1H,m), 3,45(2H,m), 2,86-2,82(1H,m), 1,99-1,87(4H,m), 1,68-1,60(2H,m), 1,00-0,98(2H,m), 0,91(9H,s), 0,09(6H,m), 0,04(9H,s).
MC (ХИАД, ИЭР) m/z: 685[81Br,(M+H)+],683[79Br,(M+H)+].
[0629]
Стадия 4: (11а8)-8-[(5-Бромпентил)окси]-2-({[трет-бутил(диметил)силил]окси}метил)-7-метокси-1,11а-дигидро-5Н-пирроло[2,1-с][1,4]бензодиазепин-5-он
Соединение, полученное на стадии 3 (0,103 г, 0,151 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,0590 г, 73%).
1H-ЯМР(CDCl3) δ: 7,83(1H,m), 7,51(1H,s)6,92(1H,m), 6,79(1H,s), 4,32-4,30(3H,m), 4,12-4,04(2H,m), 3,93(3H,s), 3,86-3,84(1H,m), 3,46-3,39(2H,m), 3,26-3,23(1H,m), 3,07-3,03(1H,m), 1,97-l,85(4H,m), 1,68-1,63(2H,m), 0,92(9H,s), 0,09(6H,s).
MC (ХИАД, ИЭР) m/z: 539[81Br,(M+H)+],537[79Br,(M+H)+].
[0630]
Стадия 5: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-[(5-{[(11aS)-2-({[трет-бутил(диметил)силил]окси}метил)-7-метокси-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 4 (0,251 г, 0,467 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,300 г, 51%).
[0631]
Стадия 6: L-Валил-N-{4-[({[(11а'S)-11'-гидрокси-8'-[(5-{[(11aS)-2-(гидроксиметил)-7-метокси-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 5 (0,300 г, 0,237 ммоль), подвергали реакции таким же образом, как и на стадиях 11 и 12 примера 33, получая желаемое соединение (0,0540 г, 53%).
МС (ХИАД, ИЭР) m/z: 952 (М+Н)+
[0632]
Стадия 7: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-8'-[(5-{[(11aS)-2-(гидроксиметил)-7-метокси-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пентил)окси]-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 6 (0,0500 мг, 0,0525 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0340 мг, 48%).
МС (ХИАД, ИЭР) m/z: 1351 (М-Н)-
[0633]
Пример 37: Лекарственное средство-линкер 35
[Формула 161]
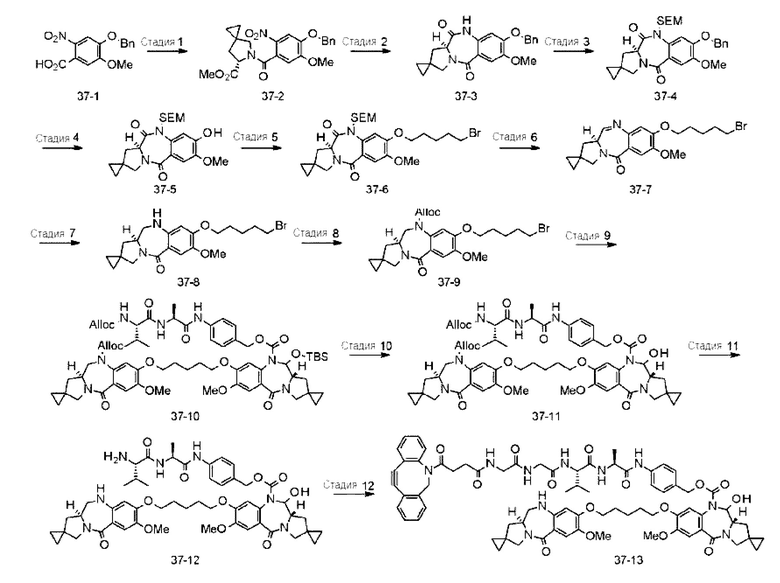
Стадия 1: Метил-(6S)-5-[4-(бензилокси)-5-метокси-2-нитробензоил]-5-азаспиро[2,4]гептан-6-карбоксилат
К раствору 4-(бензилокси)-5-метокси-2-нитробензойной кислоты (6,07 г, 20,0 ммоль, Tetrahedron 1995, 51, 5617) и N,N-диметилформамида (1,08 мл, 13,9 ммоль) в дихлорметане (100 мл) по каплям добавляли оксалилхлорид (3,43 мл, 40,0 ммоль) при охлаждении льдом в течение 5 минут. Реакционный раствор перемешивали при комнатной температуре в течение 5 часов и затем подвергали перегонке при пониженном давлении и полученный остаток растворяли в дихлорметане (20 мл) и полученную смесь подвергали перегонке при пониженном давлении. После указанную операцию повторяли три раза, остаток суспендировали в дихлорметане (5 мл), к нему добавляли избыточное количество диэтилового эфира и гексана и последующая очистка и сушка при пониженном давлении давала неочищенный ацилхлорид. Полученный ацилхлорид растворяли в дихлорметане и охлаждали до -40°С (баня с сухим льдом и ацетонитрилом), к нему постепенно добавляли метил(6S)-5-азаспиро[2,4]гептан-6-карбоксилата гидрохлорид (4,22 г, 22,0 ммоль, Tetrahedron Letters 2012. 53. 3847) и триэтиламин (3,36 мл, 24,2 ммоль). Температуру реакционной смеси повышали до комнатной температуры в течение ночи. К реакционной смеси добавляли 1 н. соляную кислоту и реакционную смесь подвергали экстракции дихлорметаном. Органический слой промывали водой, насыщенным водным раствором гидрокарбоната натрия и солевым раствором и сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 до 50:50], получая желаемое соединение (6,55 г, 80%).
МС (ХИАД, ИЭР) m/z: 441 (М+Н)+
[0634]
Стадия 2: (11а'S)-8'-(Бензилокси)-7'-метокси-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5',11'(10'Н,11а'Н)-дион
К раствору соединения, полученного на стадии 1 (6,55 г, 16,0 ммоль) в этаноле (150 мл) и ТГФ (150 мл) добавляли Никель Ренея (7,00 г) в атмосфере азота. К реакционной смеси добавляли гидразина моногидрат (7 мл) и температуру постепенно повышали до 50°С. После перемешивания при 50°С в течение 2 часов к ней добавляли Никель Ренея (3,00 г) и гидразина моногидрат (3 мл) и полученный продукт перемешивали в течение 1 часа. ТГФ (100 мл) добавляли к реакционной смеси и полученную смесь фильтровали через целит. Полученный продукт подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0(об./об.) до 25:75(об./об.)], получая желаемое соединение (4,42 г, 73%).
1H-ЯМР(CDCl3) δ: 7,82(1H,s), 7,48(1H,s), 7,42-7,35(4H,m), 7,32-7,31(1H,m), 6,44(1H,s), 5,16(2H,s), 4,16-4,10(1H,m), 3,93(3H,s), 3,78-3,76(1H,m), 3,39-3,37(1H,m), 2,45-2,43(1H,m), 2,24-2,21(1H,m), 0,83-0,61(4H,m).
МС (ХИАД, ИЭР) m/z: 379(M+H)+
[0635]
Стадия 3: (11а'S)-8'-(Бензилокси)-7'-метокси-10'-{[2-(триметилсилил)этокси]метил}-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5',11'(10'Н, 11а'Н)-дион
К раствору соединения, полученного на стадии 2 (10,0 г, 26,4 ммоль), в ТГФ (150 мл) медленно по каплям добавляли 2,6 моль/л раствор н-гексана в н-бутиллитии (12,0 мл, 31,8 ммоль) при -40°С. Реакционный раствор перемешивали при -40°С в течение 15 минут затем к нему медленно по каплям добавляли и 2-(хлорметокси)этилтриметилсилан (5,57 мл, 31,7 ммоль). После этого реакционный раствор перемешивали при комнатной температуре в течение 3 часов, добавляли к нему воду и полученный продукт подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. После перегонки при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0(об./об.) до 30:70(об./об.)], получая желаемое соединение (11,8 г, 88%).
1H-ЯМР(CDCl3) δ: 7,45-7,44(2H,m), 7,37-7,32(4H,m), 7,28(1H,s), 5,48-5,46(1H,m), 5,21(2H,s), 4,50-4,48(1H,m), 4,22-4,20(1H,m), 3,95(3H,s), 3,73-3,70(2H,m), 3,62-3,60(1H,m), 3,41-3,38(1H,m), 2,45-2,43(1H,m), 2,23-2,20(1H,m), 0,98-0,96(2H,m), 0,83-0,68(4H,m), 0,04(9H,s).
МС (ХИАД, ИЭР) m/z: 509(M+H)+
[0636]
Стадия 4: (11а'S)-8'-Гидрокси-7'-метокси-10'-{[2-(триметилсилил)этокси]метил}-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4] бензодиазепин]-5',11'(10'Н, 11a'H)-дион
К раствору соединения, полученного на стадии 3 (18,7 г, 36,8 ммоль), в ТГФ (50 мл) и этаноле (100 мл) добавляли 5% палладий-углеродный катализатор (5,00 г) в атмосфере азота. Баллон с азотом немедленно заменяли баллоном с водородом и реакционную смесь перемешивали в атмосфере водорода в течение 6 часов. Реакционную смесь разбавляли путем добавления хлороформа и фильтровали через целит и фильтрат затем подвергали перегонке при пониженном давлении и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0(об./об.) до 25:75(об./об.)], получая желаемое соединение (15,1 г, 98%).
1H-ЯМР(CDCl3) δ: 7,38(1H,s), 7,28(1H,s), 6,01(1H,s), 5,49-5,47(1H,m), 4,70-4,68(1H,m), 4,24-4,22(1H,m), 3,96(3H,s), 3,76-3,71(2H,m), 3,66-3,64(1H,m), 3,42-3,39(1H,m), 2,47-2,45(1H,m), 2,23-2,21(1H,m), 1,01-0,99(2H,m), 0,89-0,63(4H,m), 0,03(9H,s).
МС (ХИАД, ИЭР) m/z: 419(M+H)+
[0637]
Стадия 5: (11а'S)-8'-[(5-Бромпентил)окси]-7'-метокси-10'-{[2-(триметилсилил)этокси]метил}-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5',11'(10'Н, 11а'Н)-дион
Соединение, полученное на стадии 4 (2,77 г, 6,62 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 3, получая желаемое соединение (3,31 г, 88%).
1H-ЯМР(CDCl3) δ: 7,36(1H,s), 7,25(1H,s), 5,55(1H,m), 4,659(1H,m), 4,240-4,23(1H,m), 4,11-4,03(2H,m), 3,93(3H,s), 3,85-3,78(1H,m), 3,72-3,69(2H,m), 3,46-3,39(3Н,m),2,47-2,44(1Н,m),2,25-2,22(1Н,m),1,95-1,91(4Н,m),1,67-1,59(1Н,m),1,03-0,95(2H,m), 0,90-0,85(1H,m), 0,70-0,66(4H,m), 0,05(9H,s).
[0638]
Стадия 6: (11а'S)-8'-[(5-Бромпентил)окси]-7'-метокси-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 5 (3,31 г, 5,83 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (1,11 г, 45%).
1H-ЯМР(CDCl3) δ: 7,81(1H,m), 7,53(1H,s), 6,82(1H,s), 4,13-4,06(2H,m), 3,97(3H,s), 3,88-3,83(1H,m), 3,69(1H,m), 3,52-3,39(3H,m), 2,55-2,52(1H,m), 2,06-l,89(5H,m), 1,67-1,63(2H,m), 0,76-0,72(4H,m).
[0639]
Стадия 7: (11а'S)-8'-[(5-Бромпентил)окси]-7'-метокси-1',10,'11',11а'-тетрагидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 6 (2,56 г, 6,08 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (1,15 г, 45%).
1H-ЯМР(CDCl3) δ: 7,60(1H,s), 6,07(1H,s), 4,11-4,04(1H,m), 3,99(2H,m), 3,87-3,84(1H,m), 3,85(3H,s), 3,73(1H,m), 3,58-3,53(2H,m), 3,47-3,42(3H,m), 2,03-l,78(6H,m), 1,65-1,63(2H,m), 0,77-0,56(4H,m).
[0640]
Стадия 8: Проп-2-ен-1-ил (11а'S)-8'-[(5-бромпентил)окси]-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 7 (1,15 г, 2,72 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (1,14 г, 82%).
1H-ЯМР(CDCl3) δ: 7,23(1H,s), 6,69(1H,s), 5,79(1H,s), 5,13-5,10(2H,m), 4,68-4,66(1H,m), 4,48-4,45(2H,m), 4,01(2H,m), 3,92(3H,s), 3,76(1H,m), 3,54-3,37(3H,m), 2,39(1H,m), 1,95-1,90(4H,m), 1,68-1,61(3H,m), 1,44(1H,m), 0,75-0,66(4H,m).
[0641]
Стадия 9: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'Г-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-{[5-({(11а'S)-7'-метокси-5'-оксо-10'-[(проп-2-ен-1-илокси)карбонил]-5',10',11',11a'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил}окси)пентил]окси}-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 8 (0,374 г, 0,737 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,589 г, 65%).
МС (ХИАД, ИЭР) m/z: 1234 (М+Н)+
[0642]
Стадия 10: N-[(Проп-2-ен-1-илокси)карбонил]-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-{[5-({(11а'S)-7'-метокси-5'-оксо-10'-[(проп-2-ен-1-илокси)карбонил]-5',10',11',11a'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил}окси)пентил]окси}-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 5 (0,589 г, 0,477 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,382 г, 71%).
1H-ЯМР(CDCl3) δ: 8,90(1H,s)7,55(2H,m), 7,25-7,21(2H,m), 6,74(2H,m), 6,38(1H,s),5,90-5,87(5H,m), 5,33-5,09(8H,m), 4,66-4,60(8H,m), 3,98-3,91(10H,m), 3,77-3,30(12H,m), 2,42-2,36(2H,m), 1,77-l,39(6H,m), 0,91-0,70(14H,m).
[0643]
Стадия 11: L-Валил-N-{4-[({[(11а'8)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'8)-7'-метокси-5'-оксо-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 10 (0,382 г, 0,341 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,200 г, 62%).
МС (ХИАД, ИЭР) m/z: 952 (М+Н)+
[0644]
Стадия 12: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 11 (0,0560 г, 0,0588 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,0500 г, 63%).
МС (ХИАД, ИЭР) m/z: 1354 (М+Н)+
[0645]
Пример 38: Лекарственное средство-линкер 36
[Формула 162]
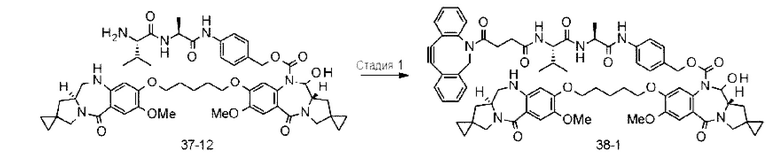
Стадия 1: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]-L-валил-N-{4-[({[(11а'S)-11'-гадрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',10',11',11a'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[пиклопропан-1,2'-пирроло[2,1-с][1,4] бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 11 примера 37 (0,0410 г, 0,0430 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 6, получая желаемое соединение (0,0210 г, 39%).
МС (ХИАД, ИЭР) m/z: 1240 (М+Н)+
[0646]
Пример 39: Лекарственное средство-линкер 37
[Формула 163]
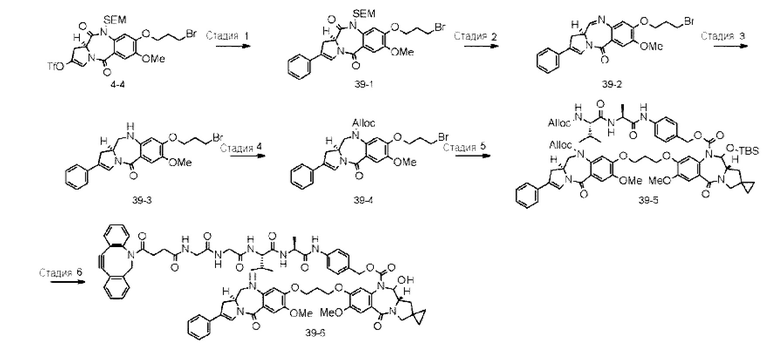
Стадия 1: Соединения 39-1
Использовали соединение, полученное на стадии 4 примера 4 (1,00 г, 1,52 ммоль), и фенилбороновую кислоту (0,370 г, 3,03 ммоль) и подвергали их реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,726 г, 81%).
МС (ХИАД, ИЭР) m/z: 589[81Br,(M+H)+],587[79Br,(M+H)+].
[0647]
Стадия 2: Соединение 39-2
Соединение, полученное на стадии 1 (0,726 г, 1,24 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,344 г, 63%).
МС (ХИАД, ИЭР) m/z: 443[81Br,(M+H)+],441[79Br,(M+H)+].
[0648]
Стадия 3: Соединение 39-3
Соединение, полученное на стадии 2 (0,344 г, 0,779 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,248 г, 72%).
МС (ХИАД, ИЭР) m/z: 445[81Br,(M+H)+],443[79Br,(M+H)+].
[0649]
Стадия 4: Соединение 39-4
Соединение, полученное на стадии 3 (0,248 г, 0,559 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,267 г, 90%).
МС (ХИАД, ИЭР) m/z: 529[81Br,(M+H)+],527[79Br,(M+H)+].
[0650]
Стадия 5: Соединение 39-5
Соединение, полученное на стадии 4 (0,100 г, 0,190 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,201 г, 85%).
МС (ХИАД, ИЭР) m/z: 1255(М+Н)+.
[0651]
Стадия 6: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]гаииилглицил-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-5-оксо-2-фенил-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазегаш-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}оксо)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 5 (0,201 г, 0,160 ммоль), подвергали реакции таким же образом, как и на стадиях 11, 12 и 13 примера 3, получая желаемое соединение (0,080 г, 36%).
МС (ХИАД, ИЭР) m/z: 1372 (М+Н)+.
[0652]
Пример 40: Лекарственное средство-линкер 38
[Формула 164]
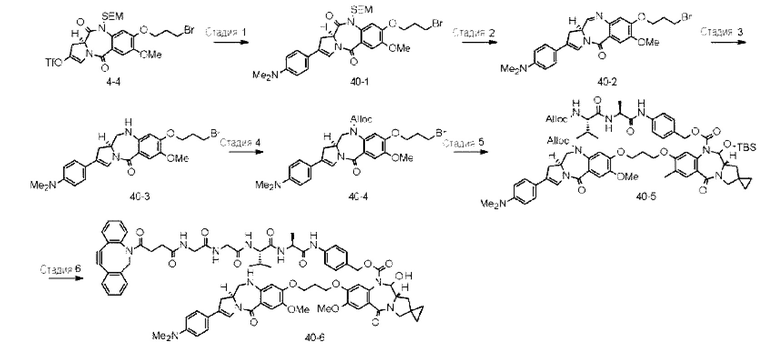
Стадия 1: Соединение 40-1
Соединение, полученное на стадии 4 примера 4 (1,48 г, 2,24 ммоль), и 4-(диметиламино)фенилбороновую кислоту (0,741 г, 4,49 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,520 г, 37%).
МС (ХИАД, ИЭР) m/z: 632[81Br,(M+H)+],630[79Br,(M+H)+].
[0653]
Стадия 2: Соединение 40-2
Соединение, полученное на стадии 1 (0,520 г, 0,825 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,167 г, 42%).
[0654]
Стадия 3: Соединение 40-3
Соединение, полученное на стадии 2 (0,167 г, 0,345 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,0650 г, 39%).
МС (ХИАД, ИЭР) m/z: 488[81Br,(M+H)+],486[79Br,(M+H)+].
[0655]
Стадия 4: Соединение 40-4
Соединение, полученное на стадии 3 (0,0650 г, 0,134 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,0690 г, 90%).
МС (ХИАД, ИЭР) m/z: 572[81Br,(M+H)+],570[79Br,(M+H)+].
[0656]
Стадия 5: Соединение 40-5
Соединение, полученное на стадии 4 (0,0690 г, 0,121 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,0660 г, 42%).
МС (ХИАД, ИЭР) m/z: 1297(M+H)+.
[0657]
Стадия 6: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11а'S)-8'-[3-({(11aS)-2-[4-(диметиламино)фенил]-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пропокси]-11'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 5 (0,0660 г, 0,0509 ммоль), подвергали реакции таким же образом, как и на стадиях 11, 12 и 13 примера 3, получая желаемое соединение (0,0350 г, 49%).
МС (ХИАД, ИЭР) m/z: 1417 (М+Н)+.
[0658]
Пример 41: Лекарственное средство-линкер 39
[Формула 165]
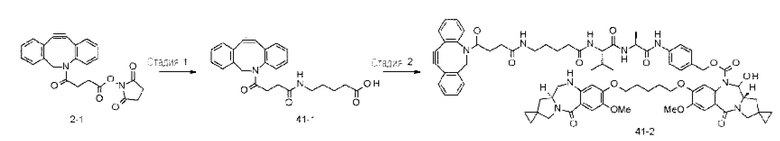
Стадия 1: Аддукт N,N-диметилформамида и 5-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]амино}валериановой кислоты
В N,N-диметилформамиде (10 мл) растворяли 5-аминовалериановую кислоту (0,436 г, 3,72 ммоль) к полученной смеси добавляли 1-{[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил] окси}пирролидин-2,5-дион (1,36 г, 3,38 ммоль) и триэтиламин (0,937 мл, 6,76 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 1,5 часов. К реакционному раствору добавляли 1 н. соляную кислоту и полученную смесь подвергали экстракции хлороформом и полученный органический слой промывали водой и солевым раствором и затем сушили над сульфатом магния. После перегонки при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [органический слой для распределения с хлороформом - хлороформ:метанол : вода = 7:3:1 (об./об./об.)], получая желаемое соединение (0,730 г, 45%) в виде твердого вещества.
1H-ЯМР(CDCl3) δ: 8,06(1H,s), 7,71(1H,m), 7,54-7,52(1H,m), 7,46-7,32(6H,m), 6,04(1H,m), 5,18(1H,m), 3,72(1H,m), 3,17-3,10(2H,m), 3,00(3H,s), 2,92(3H,s), 2,84-2,80(1H,m), 2,45-2,34(3H,m), 2,28-2,24(1H,m), 2,03-1,99(1H,m), 1,66-1,58(2H,m), 1,47-1,40(2H,m).
МС (ХИАД, ИЭР) m/z: 405(M+H)+
[0659]
Стадия 2: N-(5-{[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]амино}пентаноил)-L-валил-N-{4-[({[(11а'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',10',11',11a'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 1 (0,0176 г, 0,0368 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,00880 г, 18%).
МС (ХИАД, ИЭР) m/z: 1339 (М+Н)+
[0660]
Пример 42: Лекарственное средство-линкер 40
[Формула 166]
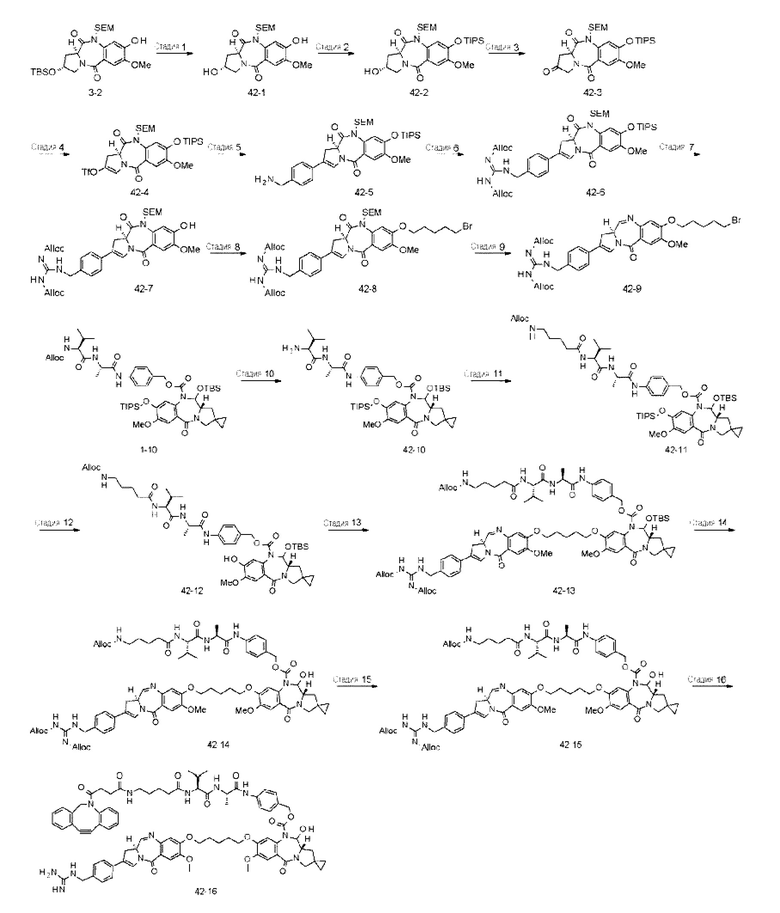
Стадия 1: Соединение 42-1
Соединение, полученное на стадии 1 примера 3 (5,00 г, 9,66 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 3, получая желаемое соединение (3,95 г, 100%).
МС (ХИАД, ИЭР) m/z: 409(M+H)+
[0661]
Стадия 2: Соединение 42-2
Соединение, полученное на стадии 1 (3,95 г, 9,67 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 24, получая желаемое соединение (4,78 г, 87%).
МС (ХИАД, ИЭР) m/z: 565(M+H)+
[0662]
Стадия 3: Соединение 42-3
Соединение, полученное на стадии 2 (4,78 г, 8,43 ммоль), подвергали реакции таким же образом, как и на стадии 4 примера 3, получая желаемое соединение (2,36 г, 50%). МС (ХИАД, ИЭР) m/z: 563(M+H)+
[0663]
Стадия 4: Соединение 42-4
Соединение, полученное на стадии 3 (1,53 г, 2,72 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 3, получая желаемое соединение (1,27 г, 69%).
1H-ЯМР(CDCl3)δ:7,31(2H,s), 7,15(1H,m), 5,52(1H,m), 4,65(1H,m), 4,57(1H,m), 3,95-3,89(1H,m), 3,87(3H,s), 3,75-3,58(2H,m), 3,18-3,14(1H,m), 1,33-1,25(3H,m), 1,10(18H,m), 1,00-0,96(2H,m), 0,03(9H,s).
[0664]
Стадия 5: Соединение 42-5
Соединение, полученное на стадии 4 (0,255 г, 0,367 ммоль), и 4-(аминометил)фенилбороновую кислоту (0,344 г, 1,84 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,148 г, 62%).
МС (ХИАД, ИЭР) m/z: 652(M+H)+
[0665]
Стадия 6: Соединение 42-6
К раствору соединения (0,142 г, 0,218 ммоль), полученного на стадии 5 и дипроп-2-ен-1-ил [(Z)-(метилсульфанил)метилиден]бискарбамату (0,079 г, 0,079 ммоль, WO 9920628) в диметилформамиде (2,2 мл) добавляли триэтиламин (0,090 мл, 0,653 ммоль) и хлорид ртути (II) (0,083 г, 0,305 ммоль) при комнатной температуре. После этого реакционный раствор перемешивали при комнатной температуре в течение 30 минут, реакционный раствор разбавляли путем добавления этилацетата и соли ртути удаляли путем фильтрации. Полученный органический слой промывали 0,1 н. фосфатным буфером и солевым раствором. Органический слой сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 60:40 (об./об.)], получая желаемое соединение (0,157 г, 83%).
МС (ХИАД, ИЭР) m/z: 863(M+H)+
[0666]
Стадия 7: Соединение 42-7
К раствору соединения, полученного на стадии 6 (0,153 г, 0,177 ммоль), в ТГФ (1,8 мл) добавляли 1 моль/л тетрагидрофуранового раствора фторида тетрабутиламмония (0,266 мл, 0,266 ммоль) при комнатной температуре. После перемешивания при комнатной температуре в течение 50 минут к раствору реакционной смеси добавляли 0,1 н. фосфатный буфер (рН 7,0) и полученную смесь подвергали экстракции этилацетатом и полученный органический слой промывали 0,1 н. фосфатным буфером (рН 7,0). Полученный продукт сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (0,115 г, 92%).
МС (ХИАД, ИЭР) m/z:706(M+H)+
[0667]
Стадия 8: Соединение 42-8
К раствору соединения, полученного на стадии 7 (0,115 г, 0,163 ммоль) в N,N-диметилформамиде (1,0 мл) добавляли 1,5-дибромпентан (0,088 мл, 0,652 ммоль) и карбонат цезия (0,032 г, 0,098 ммоль) при комнатной температуре. После перемешивания при комнатной температуре в течение 2 часов к реакционному раствору добавляли 0,1 н. фосфатный буфер (рН 7,0) и полученную смесь подвергали экстракции этилацетатом. Полученный органический слой промывали 0,1 н. фосфатным буфером (рН 7,0) и солевым раствором и сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (0,111 г, 80%).
МС (ХИАД, ИЭР) m/z: 856[81Br,(M+H)+],854[79Br,(M+H)+]
[0668]
Стадия 9: Соединение 42-9
Соединение, полученное на стадии 8 (0,105 г, 0,123 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,036 г, 41%).
МС (ХИАД, ИЭР) m/z: 772[81Br,(M+H)+],770[79Br,(M+H)+]
[0669]
Стадия 10: Соединение 42-10
Соединение, полученное на стадии 9 (0,163 г, 0,169 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,132 г, 88%).
МС (ХИАД, ИЭР) m/z:880(M+H)+
[0670]
Стадия 11: Соединение 42-11
К раствору соединения, полученного на стадии 10 (0,13 г, 0,147 ммоль), 5-{[(проп-2-ен-1-илокси)карбонил]амино}пентановой кислоте (0,0386 г, 0,192 ммоль) и 1-гидроксибензотриазолу моногидрату (0,038 г, 0,251 ммоль) в дихлорметане (3 мл) добавляли триэтиламин (0,035 мл, 0,251 ммоль) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (0,048 г, 0,251 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 1 часа. К реакционному раствору добавляли 0,1 н. фосфатный буфер (рН 7,0) и полученный продукт подвергали экстракции этилацетатом. Полученный органический слой промывали 0,1 н. фосфатным буфером (рН 7,0) и этилацетат удаляли при помощи перегонки при пониженном давлении. Полученный продукт подвергали азеотропной перегонке с помощью толуола и полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 100:0 (об./об.) до 50:50 (об./об.)], получая желаемое соединение (0,150 г, 95%).
МС (ХИАД, ИЭР) m/z:1063(M+H)+
[0671]
Стадия 12: Соединение 42-12
К раствору соединения, полученного на стадии 11 (0,150 г, 0,141 ммоль), в N,N-диметилформамиде (3,5 мл) добавляли водный раствор ацетата лития (1,52 М, 0,088 мл) при комнатной температуре. После перемешивания при комнатной температуре в течение 1,5 часов к раствору реакционной смеси добавляли воду и полученную смесь подвергали экстракции этилацетатом. Органический слой промывали водой и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : метанол = 100:0 (об./об.) до 95:5 (об./об.)], получая желаемое соединение (0,135 г, 96%).
МС (ХИАД, ИЭР) m/z: 907(M+H)+
[0672]
Стадия 13: Соединение 42-13
К раствору соединения, полученного на стадии 12 (0,048 г, 0,053 ммоль) и соединения, полученного на стадии 9 (0,034 г, 0,048 ммоль), в N,N-диметилформамиде (0,5 мл) добавляли карбонат цезия (0,011 г, 0,034 ммоль) при комнатной температуре. Перемешивание проводили при комнатной температуре в течение 1,5 часов и затем при 45°С в течение 5 часов. К реакционному раствору добавляли 0,1 н. фосфатный буфер (рН 7,0) и полученный продукт подвергали экстракции этилацетатом. Полученный органический слой промывали 0,1 н. фосфатным буфером (рН 7,0) и сушили над сульфатом натрия и затем подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : метанол = 100:0 (об./об.) до 97:3 (об./об.)], получая желаемое соединение (0,038 г, 52%).
МС (ХИАД, ИЭР) m/z: 1534 (М+Н)+
[0673]
Стадия 14: Соединение 42-14
Соединение, полученное на стадии 13 (0,038 г, 0,247 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3. После этого реакционный раствор подвергали жидкостному разделению, удаляли органический растворитель при помощи перегонки при пониженном давлении и полученное соединение непосредственно применяли для последующей реакции.
МС (ХИАД, ИЭР) m/z: 1420 (М+Н)+
[0674]
Стадия 15: Соединение 42-15
К раствору соединения, полученного на стадии 14 (0,034 г, 0,140 ммоль), в диметилформамиде (2 мл) добавляли пирролидин (0,048 мл, 0,574 ммоль) и тетракис(трифенилфосфин)палладий (0) (0,0054 г, 0,0046 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 50 минут. После этого органический растворитель удаляли при помощи перегонки при пониженном давлении, полученный остаток растворяли в диметилсульфоксиде и очищали с помощью колоночной хроматографии с обращенной фазой (колонка: Develosil Соmbi-RР-5 (NomurChemical Co., Ltd.), 20 мм × 100 мм: 0,1% водный раствор муравьиной кислоты: 0,1% раствор ацетонитрила с добавлением муравьиной кислоты = от 79,2:20,8 до 51,4:48,6, скорость потока: 25 мл/мин, температура: 25°С), получая желаемое соединение (0,020 г, 72%).
МС (ХИАД, ИЭР) m/z: 1168 (М+Н)+
[0675]
Стадия 16: Соединение 42-16
К раствору соединения, полученного на стадии 15 (0,002 г, 0,0017 ммоль), в диметилформамиде (0,5 мл) добавляли триэтиламин (0,007 мл, 0,051 ммоль) и коммерчески доступной 1-{[4-(11,12-дидегидробензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]оксопирролидин-2,5-дион (0,083 г, 0,0205 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 10 часов. Органический растворитель удаляли при помощи перегонки при пониженном давлении и полученный остаток растворяли в диметилсульфоксиде и очищали с помощью колоночной хроматографии с обращенной фазой (колонка: Develosil Combi-RP-5 (NomurChemical Co., Ltd.), 20 мм × 100 мм: 0,1% водный раствор муравьиной кислоты: 0,1% раствор ацетонитрила с добавлением муравьиной кислоты = от 62,5:37,5 до 34,7:65,3, скорость потока: 25 мл/мин, температура: 25°С) и колоночной хроматографии на силикагеле [органический слой для распределения с хлороформом - хлороформ : метанол : вода = 7:3:1 (об./об./об.)], получая желаемое соединение (0,033 г, 14%).
МС (ХИАД, ИЭР) m/z: 1455 (М+Н)+
[0676]
Пример 43: Лекарственное средство-линкер 41
[Формула 167]
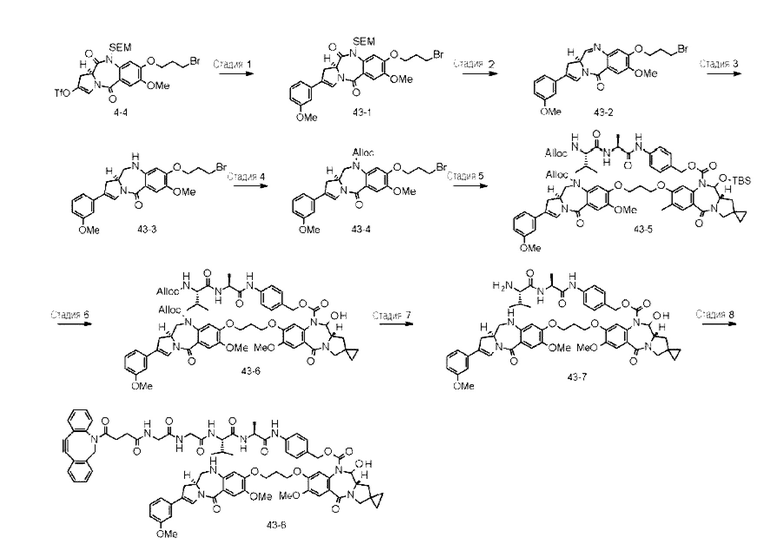
Стадия 1: Соединение 43-1
Соединение, полученное на стадии 4 примера 4 (0,72 г, 1,09 ммоль), и 3-метоксифенилбороновую кислоту (0,332 г, 2,18 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,526 г, 78%).
МС (ХИАД, ИЭР) m/z: 619[81Br,(M+H)+],617[79Br,(M+H)+]
[0677]
Стадия 2: Соединение 43-2
Соединение, полученное на стадии 1 (0,526 г, 0,851 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,195 г, 49%).
МС (ХИАД, ИЭР) m/z: 473[81Br,(M+H)+],471[79Br,(M+H)+]
[0678]
Стадия 3: Соединение 43-3
Соединение, полученное на стадии 2 (0,195 г, 0,414 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,195 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 475[81Br,(M+H)+],473[79Br,(M+H)+]
[0679]
Стадия 4: Соединение 43-4
Соединение, полученное на стадии 3 (0,413 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,106 г, 46%).
МС (ХИАД, ИЭР) m/z: 559[81Br,(M+H)+],557[79Br,(M+H)+]
[0680]
Стадия 5: Соединение 43-5
Соединение, полученное на стадии 4 (0,069 г, 0,124 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,128 г, 80%).
МС (ХИАД, ИЭР) m/z: 1284(M+H)
[0681]
Стадия 6: Соединение 43-6
Соединение, полученное на стадии 5 (0,128 г, 0,099 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,105 г, 90%).
МС (ХИАД, ИЭР) m/z: 1170(M+H)
[0682]
Стадия 7: Соединение 43-7
Соединение, полученное на стадии 6 (0,105 г, 0,089 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,072 г, 80%).
МС (ХИАД, ИЭР) m/z:1002(M+H)+
[0683]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5 (6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-11'-гидрокси-7'-метокси-8'-(3-{[(11aS)-7-метокси-2-(3-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1H-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (0,072 г, 0,072 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,053 г, 52%).
МС (ХИАД, ИЭР) m/z: 1403 (М+Н)+
[0684]
Пример 44: Лекарственное средство-линкер 42
[Формула 168]
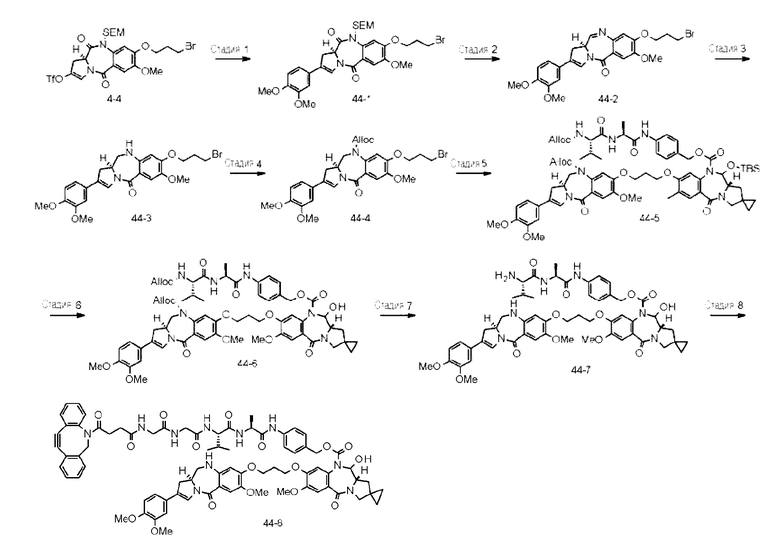
Стадия 1: Соединение 44-1
Соединение, полученное на стадии 4 примера 4 (0,68 г, 1,03 ммоль) и 3,4-диметоксифенилбороновую кислоту (0,375 г, 2,06 ммоль) подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,506 г, 75%).
МС (ХИАД, ИЭР) m/z: 649[81Br, (M+H)+], 647[79Br, (M+H)+]
[0685]
Стадия 2: Соединение 44-2
Соединение, полученное на стадии 1 (0,506 г, 0,781 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,199 г, 50%).
МС (ХИАД, ИЭР) m/z: 503[81Br, (M+H)+], 501[79Br, (M+H)+]
[0686]
Стадия 3: Соединение 44-3
Соединение, полученное на стадии 2 (0,169 г, 0,337 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,231 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 505[81Br, (M+H)+], 503[79Br, (M+H)+]
[0687]
Стадия 4: Соединение 44-4
Соединение, полученное на стадии 3 (0,337 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,170 г, 86%).
МС (ХИАД, ИЭР) m/z: 589[81Br, (M+H)+], 587[79Br, (M+H)+]
[0688]
Стадия 5: Соединение 44-5
Соединение, полученное на стадии 4 (0,076 г, 0,136 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,116 г, 71%).
МС (ХИАД, ИЭР) m/z: 1314(M+H)+
[0689]
Стадия 6: Соединение 44-6
Соединение, полученное на стадии 5 (0,116 г, 0,088 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,108 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 1200(M+H)+
[0690]
Стадия 7: Соединение 44-7
Соединение, полученное на стадии 6 (0,090 моль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,066 г, 71%).
МС (ХИАД, ИЭР) m/z: 1032(M+H)+
[0691]
Стадия 8: N-[4-(11,12-дидегидродибензо[b,f]азоцин-5(6Н)-ил)-4-оксобутаноил]глицилглицил-L-валил-N-{4-[({[(11a'S)-8'-(3-{[(11aS)-2-(3,4-диметоксифенил)-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-11'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-ил]карбонил}окси)метил]фенил}-L-аланинамид
Соединение, полученное на стадии 7 (0,066 г, 0,064 ммоль), подвергали реакции таким же образом, как и на стадии 13 примера 3, получая желаемое соединение (0,053 г, 58%).
МС (ХИАД, ИЭР) m/z: 1434 (М+Н)+
[0692]
[Синтез лекарственного средства D]
Пример 45: Лекарственное средство 1
[Формула 169]
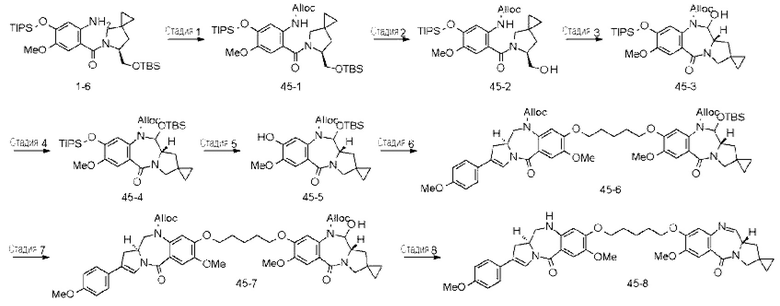
Стадия 1: Проп-2-ен-1-ил-(2-{[(6S)-6-({[трет-бутил(диметил)силил]окси}метил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамат
Соединение, полученное на стадии 5 примера 1 (4,59 г, 8,15 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (4,86 г, 92%).
1Н-ЯМР(CDCl3) δ: 8,97(1H,s), 7,77(1H,s), 6,77(1H,s), 5,97-5,94(1H,m), 5,39-5,21(2H,m), 4,67-4,59(3H,m), 4,00-3,98(1H,m), 3,74-3,66(5H,m), 3,05-3,03(1H,m), 2,30-2,28(1H,m), 1,72-1,70(1H,m), 1,30-1,27(3H,m), 1,11-1,05(18H,m), 0,99-0,91(9H,m), 0,61-0,53(4H,m), 0,10-0,06(6H,m).
MC (ХИАД, ИЭР) m/z: 647(M+H)+
[0693]
Стадия 2: Проп-2-ен-1-ил-(2-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метокси-5-{[три(пропан-2-ил)силил]окси}фенил)карбамат
Соединение, полученное на стадии 1 (4,86 г, 7,51 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 1, получая желаемое соединение (3,42 г, 86%).
1H-MP(CDCl3) δ: 8,52(1H,s), 7,71(1H,s), 6,77(1H,s), 6,00-5,94(1H,m), 5,35-5,27(2H,m), 4,65-4,64(3H,m), 4,33-4,31(1H,m), 3,82-3,77(5H,m), 3,68-3,66(1H,m), 3,15-3,13(1H,m), 1,89-1,86(2H,m), 1,30-1,26(3H,m), 1,14-1,10(18H,m), 0,66-0,51(4H,m).
МС (ХИАД, ИЭР) m/z: 533(M+H)+
[0694]
Стадия 3: Проп-2-ен-1-ил-(11а'S)-11'-гидрокси-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 2 (6,68 г, 12,5 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (6,44 г, 97%).
1H-MMP(CDCl3) δ: 7,20(1H,s), 6,69(1H,s), 5,89-5,78(2H,m), 5,18-5,15(2H,m), 4,62-4,60(1H,m), 4,49-4,47(1H,m), 3,85(3H,s), 3,74-3,71(1H,m), 3,59-3,57(1H,m), 3,33-3,30(2H,m), 2,43-2,40(1H,m), 1,76-1,73(1H,m), 1,28-1,20(3H,m), 1,09-1,07(18H,m), 0,74-0,65(4H,m).
MC (ХИАД, ИЭР) m/z: 531(M+H)+
[0695]
Стадия 4: Проп-2-ен-1-ил-(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-8'-{[три(пропан-2-ил)силил]окси}-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 3 (3,24 г, 6,10 ммоль), подвергали реакции таким же образом, как и на стадии 9 примера 1, получая желаемое соединение (3,86 г, 98%).
1H-ЯМР(CDCl3) δ: 7,20(1H,s), 6,67(1H,s), 6,01-5,98(1H,m), 5,79-5,73(1H,m), 5,14-5,10(2H,m), 4,64-4,61(1H,m), 4,37-4,34(1H,m), 3,86(3H,s), 3,72-3,69(1H,m), 3,52-3,50(1H,m), 3,29-3,26(1H,m), 2,38-2,34(1H,m), 1,55-1,51(1H,m), 1,28-1,24(3H,m), 1,15-1,07(18H,m), 0,81-0,66(13H,m), 0,21(3H,s), 0,18(3H,s).
MC (ХИАД, ИЭР) m/z: 645(M+H)+
[0696]
Стадия 5: Проп-2-ен-1-ил-(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-8'-гидрокси-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 4 (4,49 г, 6,96 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (3,24 г, 95%).
1H-ЯМР(CDCl3) δ: 7,25(1H,s), 6,73(1H,s), 6,02-6,00(1H,m), 5,91(1H,s), 5,77-5,75(1H,m), 5,11-5,09(2H,m), 4,64-4,62(1H,m), 4,41-4,40(1H,m), 3,95(3H,s), 3,72-3,70(1H,m), 3,54-3,53(1H,m), 3,29-3,26(1H,m), 2,36-2,34(1H,m), 1,56-1,54(1H,m), 0,79-0,67(13H,m), 0,21(3H,s), 0,20(3H,s).
МС (ХИАД, ИЭР) m/z: 489(M+H)+
[0697]
Стадия 6: Проп-2-ен-1-ил-(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-{[5-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил}окси)пентил]окси}-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 5 (0,080 г, 0,164 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,160 г, 98%).
1Н-ЯМР(ДМСО-D6) δ: 7,44-7,42(3Н,m), 7,12-7,10(2Н,m), 7,05-7,03(1H,m), 6,92-6,90(2Н,m), 6,61-6,59(1Н,m), 5,87-5,81(3Н,m), 5,10-5,07(4Н,m), 4,66-4,55(3Н,m), 4,43-4,39(2H,m), 4,21-3,94(5H,m), 3,83(3H,s), 3,81(3H,s), 3,76(3H,s), 3,65-3,62(1H,m), 3,56-3,54(1Н,m), 3,42-3,39(1Н,m), 3,22-3,14(2Н,m), 2,77-2,73(1Н,m), 2,42-2,33(1Н,m), 1,81-1,79(4H,m), 1,55-1,44(3H,m), 0,82(9H,s), 0,72-0,53(4H,m), 0,19(3H,s), 0,17(3H,s).
МС (ХИАД, ИЭР) m/z:993(M+H)+
[0698]
Стадия 7: Проп-2-ен-1-ил-(11а'S)-11'-гидрокси-7'-метокси-8'-{[5-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11a-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил}окси)пентил]окси}-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 6 (160 мг, 0,161 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (141 мг, количественный выход).
1Н-ЯМР(ДМСО-D6) δ: 7,44-7,42(3Н,m), 7,08-7,06(3Н,m), 6,92-6,90(2Н,m), 6,82-6,79(1H,m), 6,56-6,54(1H,m), 5,77-5,74(3H,m), 5,09(4H,s), 4,58-4,55(3H,m), 4,43-4,41(2H,m), 4,16-4,01(5H,m), 3,81-3,81(6H,m), 3,76(3H,s), 3,64(1H,s), 3,56-3,53(1Н,m), 3,42-3,38(1Н,m), 3,25-3,13(2Н,m), 2,74-2,70(1Н,m), 2,37-2,34(1Н,m), 1,82-1,79(4Н,m), 1,59-1,56(3Н,m), 0,66-0,62(4Н,m).
МС (ХИАД, ИЭР) m/z:879(M+H)+
[0699]
Стадия 8: (11а'S)-7'-Метокси-8'-[(5-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси}пентил)окси]-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 7 (141 мг, 0,161 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (109,8 мг, 99%).
1H-ЯМР(ДМСО-D6) δ: 7,92-7,91(1H,m), 7,45(1H,s), 7,39-7,37(2H,m), 7,33(1H,s), 7,29(1H,s), 6,92-6,89(2H,m), 6,85(1H,s), 6,56-6,54(1H,m), 6,31(1H,s), 4,19-4,12(2H,m), 4,05-3,99(1H,m), 3,95-3,93(2H,m), 3,82-3,79(4H,m), 3,76(3H,s), 3,66(3H,s), 3,52-3,46(3H,m), 3,30-3,21(2H,m), 2,78-2,74(1H,m), 2,45-2,42(1H,m), 2,06-2,05(1H,m), 1,89-1,82(4H,m), 1,60-1,58(2H,m), 0,80-0,63(4H,m).
МС (ХИАД, ИЭР) m/z:693(M+H)+
[0700]
Пример 46: Лекарственное средство 2
[Формула 170]
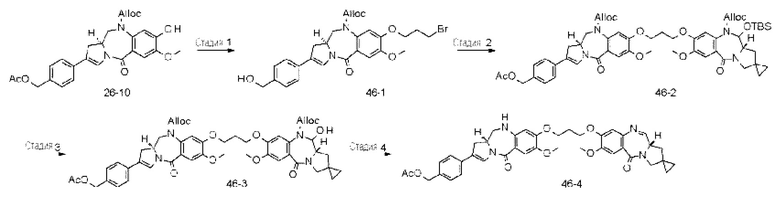
Стадия 1: Соединение 46-1
Использовали соединение, полученное на стадии 10 примера 26 (0,246 г, 0,514 ммоль), и подвергали его реакции таким же образом, как и на стадии 1 примера 4, получая желаемое соединение (0,122 г, 40%).
МС (ХИАД, ИЭР) m/z: 601[81Br, (M+H)+], 599[79Br, (M+H)+].
[0701]
Стадия 2: Соединение 46-2
Соединение, полученное на стадии 1 (0,122 г, 0,204 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 45, получая желаемое соединение (0,176 г, 86%). [0702]
Стадия 3: Соединение 46-3
Соединение, полученное на стадии 2 (0,0870 г, 0,0864 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,0660 г, 86%). МС (ХИАД, ИЭР) m/z: 892(M+H)+
[0703]
Стадия 4: 4-[(11aS)-7-Метокси-8-(3-{[(11а'S)-7'-метокси-5'-оксо-5',11а'дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пропокси)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-2-ил]бензилацетат
Соединение, полученное на стадии 3 (0,0660 г, 0,0793 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0444 г, 85%).
1H-ЯМР(CDCl3) δ: 7,80-7,79(1H,m), 7,66-7,65(1Н,m), 7,52-7,50(2Н,m), 7,39-7,33(5H,m), 6,86-6,85(1H,m), 6,14-6,13(1H,m), 5,09(2H,s), 4,32-4,23(6H,m), 3,95-3,95(3Н,m), 3,85-3,82(4Н,m), 3,71-3,68(2Н,m), 3,55-3,49(3Н,m), 3,42-3,33(1Н,m), 2,79-2,72(1Н,m), 2,54-2,50(1Н,m), 2,40-2,36(2Н,m), 2,02-1,98(1Н,m), 1,26-1,24(1Н,m), 0,76-0,72(4Н,m).
МС (ХИАД, ИЭР) m/z:706(M+H)+
[0704]
Пример 47: Лекарственное средство 3
[Формула 171]
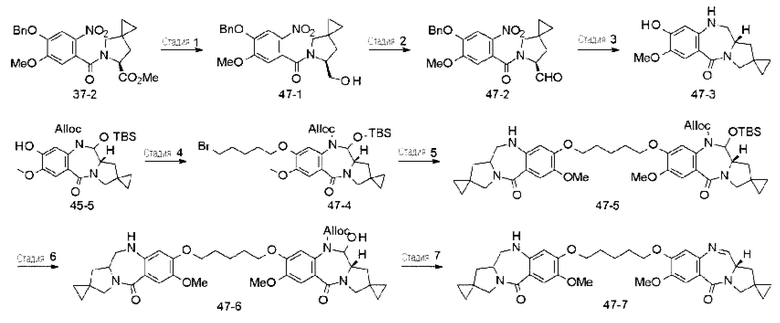
Стадия 1: [4-(Бензил)-5-метокси-2-нитрофенил][(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]метанон
К раствору соединения, полученного на стадии 1 примера 37 (6,49 г, 14,7 ммоль), в тетрагидрофуране (147 мл) добавляли борогидрид лития (0,642 г, 29,5 ммоль) при 0°С и полученный продукт перемешивали при комнатной температуре в течение 2 часов. К реакционному раствору добавляли 1 и. соляную кислоту и полученную смесь подвергали экстракции этилацетатом. Полученный органический слой промывали солевым раствором и сушили над сульфатом магния и затем подвергали перегонке при пониженном давлении. Полученный остаток (6,94 г, количественный выход) использовали на следующей стадии без очистки.
МС (ХИАД, ИЭР) m/z:413 (М+Н)+
[0705]
Стадия 2: (6S)-5-[4-(Бензилокси)-5-метокси-2-нитробензоил]-5-азаспиро[2,4]гептан-6-карбальдегид
Соединение, полученное на стадии 1 (4,50 г, 11,0 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 1, получая желаемое соединение (1,94 г, 43%).
МС (ХИАД, ИЭР) m/z:411 (М+Н)+
[0706]
Стадия 3: (11а'S)-8'-Гидрокси-7'-метокси-1',10',11',11а'-тетрагидро-5'Н-спиро [циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-5'-он
К смешанному раствору соединения, полученного на стадии 2 (1,94 г, 4,73 ммоль), в тетрагидрофуране (25 мл), этилацетате (25 мл) и метаноле (25 мл) добавляли 5% палладий на углероде (содержание влаги: 54%, 1,0 г) в атмосфере азота и реакционный раствор затем перемешивали в атмосфере водорода при комнатной температуре в течение 22 часов. После этого реакционный раствор фильтровали через целит, фильтрат подвергали перегонке при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан : этилацетат = 80:20 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (1,20 г, 93%).
1H-ЯМР(CDCl3) δ: 7,55(1H,s), 6,16(1H,s), 5,86(1H,s), 4,08-4,02(2H,m), 3,86(3H,s), 3,72-3,69(1H,m), 3,57-3,37(3H,m), 2,04-2,01(1H,m), 1,78-1,75(1H,m), 0,79-0,53(4H,m).
МС (ХИАД, ИЭР) m/z: 275(M+H)+
[0707]
Стадия 4: Проп-2-ен-1-ил-(11а'S)-8'-[(5-бромпентил)окси]-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 3 примера 45 (0,300 г, 0,614 ммоль), подвергали реакции таким же образом, как и на стадии 2 примера 3, получая желаемое соединение (0,388 г, 99%).
1H-ЯМР(CDCl3) δ: 7,24(1H,s), 6,60(1H,s), 6,02-5,98(1H,m), 5,80-5,75(1H,m), 5,11-5,06(2H,m), 4,68-4,64(1H,m), 4,40-4,38(1H,m), 4,02-3,98(2H,m), 3,92(3H,s), 3,72-3,69(1H,m), 3,54-3,52(1H,m), 3,46-3,41(2H,m), 3,29-3,26(1H,m), 2,38-2,34(1H,m), 1,94-1,87(4H,m), 1,65-1,62(2H,m), 1,55-1,55(1H,m), 0,86(9H,s), 0,75-0,67(4H,m), 0,24-0,22(6H,m).
МС (ХИАД, ИЭР) m/z: 639[81Br, (M+H)+], 637[79Br, (M+H)+].
[0708]
Стадия 5: Проп-2-ен-1-ил-(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 4 (0,203 г, 0,318 ммоль), подвергали реакции с соединением, полученным на стадии 3 (0,131 г, 0,478 ммоль) таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,0880 г, 33%).
МС (ХИАД, ИЭР) m/z: 831 (М+Н)+
[0709]
Стадия 6: Проп-2-ен-1-ил-(11a'S)-11'-гидрокси-7'-метокси-8'-[(5-{[(11a'S)-7'-метокси-5'-оксо-5',10',11',11а'-тетрагидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 5 (0,0880 г, 0,106 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,0500 г, 66%).
МС (ХИАД, ИЭР) m/z: 717 (М+Н)+
[0710]
Стадия 7: (11а'S)-7'-Метокси-8'-[(5-{[(11а'S)-7'-метокси-5'-оксо-5',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-8'-ил]окси}пентил)окси]-1',10',11',11а'-тетрагидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 6 (0,0500 г, 0,0698 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0330 г, 77%).
1Н-ЯМР(CDCl3) δ: 7,80(1 H,m), 7,58(1H,s), 7,52(1H,s), 6,81 (1H,s), 6,05(1H,s), 4,17-3,97(5H,m), 3,94(3H,s), 3,87(1H,m), 3,84(3H,s), 3,72-3,68(3H,m), 3,51-3,45(5H,m), 2,54-2,51(1H,m), 2,03-1,90(6H,m), 1,75-1,68(2H,m), 0,66(8H,m).
МС (ХИАД, ИЭР) m/z: 615(M+H)+
[0711]
Пример 48: Лекарственное средство 4
[Формула 172]
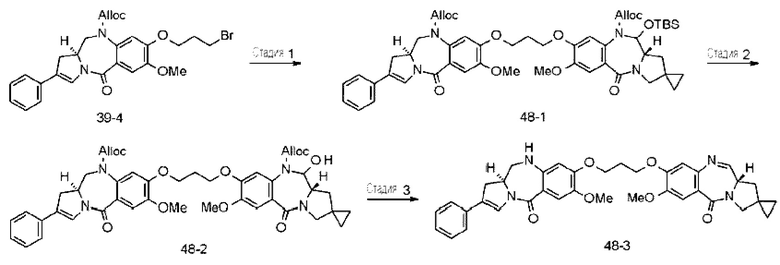
Стадия 1: Соединение 48-1
Соединение, полученное на стадии 4 примера 39 (0,165 г, 0,313 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 45, получая желаемое соединение (0,270 г, 92%).
МС (ХИАД, ИЭР) m/z:935 (М+Н)+.
[0712]
Стадия 2: Соединение 48-2
Соединение, полученное на стадии 1 (0,270 г, 0,289 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,208 г, 88%).
МС (ХИАД, ИЭР) m/z: 821 (М+Н)+.
[0713]
Стадия 3: (11а'S)-7'-Метокси-8'-(3-{[(11aS)-7-метокси-5-оксо-2-фенил-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-1',11а'-дигидро-5'Н-спиро[никлопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 2 (0,208 г, 0,253 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,130 г, 80%).
МС (ХИАД, ИЭР) m/z: 635 (М+Н)+.
[0714]
Пример 49: Лекарственное средство 5
[Формула 173]
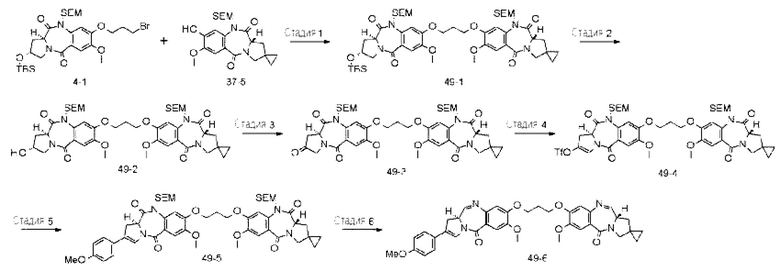
Стадия 1: Соединение 49-1
Соединение 4-1 (8,52 г, 13,2 ммоль) и соединение 37-5 (6,09 г, 14,5 ммоль), полученное на стадии 4 примера 37 использовали и подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (10,7 г, 83%).
1H ЯМР(CDCl3) δ: 7,36(1H,s), 7,34(1H,s), 7,26(1H,s), 7,23(1H,s), 5,53-5,46(2H,m), 4,72-4,69(2H,m), 4,59-4,55(1H,m), 4,28-4,20(6H,m), 3,90-3,89(6H,m), 3,80-3,63(6H,m), 3,57-3,54(1H,m), 3,42-3,39(1H,m), 2,87-2,82(1H,m), 2,47-2,40(3H,m), 2,24-2,20(1H,m), 2,04-1,99(1H,m), 0,99-0,95(4H,m), 0,87(9H,s), 0,70-0,63(4H,m), 0,09(6H,s), 0,02-0,00(18H,m).
[0715]
Стадия 2: Соединение 49-2
Соединение, полученное на стадии 1 (10,7 г, 10,9 ммоль), подвергали реакции таким же образом, как и на стадии 3 примера 3, получая желаемое соединение (9,45 г, 100%).
1H-ЯМР(CDCl3) δ: 7,36-7,34(2H,m), 7,26(1H,s), 7,23(1H,s), 5,53-5,47(2H,m), 4,72-4,64(3H,m), 4,30-4,20(6H,m), 3,89(6H,s), 3,85-3,62(7H,m), 3,42-3,39(1H,m), 2,99-2,93(1H,m), 2,47-2,39(3H,m), 2,25-2,07(3H,m), 0,99-0,95(4H,m), 0,89-0,86(1H,m), 0,70-0,64(3H,m), 0,02-0,00(18H,m).
[0716]
Стадия 3: Соединение 49-3
Соединение, полученное на стадии 2 (9,45 г, 10,9 ммоль), подвергали реакции таким же образом, как и на стадии 4 примера 3, получая желаемое соединение (9,14 г, 97%).
1H-ЯМР(CDCl3) δ: 7,37(1H,s), 7,33(1H,s), 7,27-7,26(2H,m), 5,54-5,51(2H,m), 4,77-4,70(2H,m), 4,64-4,61(1H,m), 4,31-4,20(6H,m), 3,91(3H,s), 3,90(3H,s), 3,80-3,65(6H,m), 3,60-3,55(1H,m), 3,42-3,39(1H,m), 2,83-2,75(1H,m), 2,47-2,41(3H,m), 2,25-2,20(1H,m), 1,00-0,95(4H,m), 0,92-0,85(1H,m), 0,71-0,63(3H,m), 0,02-0,01(18H,m).
[0717]
Стадия 4: Соединение 49-4
Соединение, полученное на стадии 3 (4,27 г, 4,94 ммоль), подвергали реакции таким же образом, как и на стадии 5 примера 3, получая желаемое соединение (3,16 г, 64%).
1H ЯМР(CDCl3) δ: 7,37(1H,s), 7,32(1H,s), 7,27-7,25(2H,m), 7,15-7,14(1H,m), 5,53-5,50(2H,m), 4,77-4,70(2H,m), 4,64-4,60(1H,m), 4,30-4,20(6H,m), 3,90(6H,s), 3,81-3,66(4H,m), 3,42-3,39(1H,m), 3,18-3,13(1H,m), 2,47-2,41(3H,m), 2,25-2,20(1H,m), 0,99-0,94(4H,m), 0,89-0,86(1H,m), 0,69-0,64(3H,m), 0,02-0,00(18H,m).
[0718]
Стадия 5: Соединение 49-5
Соединение, полученное на стадии 4 (1,00 г, 1,00 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,900 г, 94%).
1Н-ЯМР(CDCl3) δ: 7,69-7,65(1Н,m), 7,57-7,53(1Н,m), 7,49-7,45(1Н,m), 7,39-7,36(4H,m), 7,33(1H,s), 7,27(1H,s), 6,90-6,88(2H,m), 5,53-5,50(2H,m), 4,77-4,71(2H,m), 4,62-4,59(1H,m), 4,30-4,20(5H,m), 3,91(3H,s), 3,91(3H,s), 3,82(3H,s), 3,80-3,65(4Н,m), 3,42-3,39(1Н,m), 3,16-3,10(1Н,m), 2,47-2,41(3Н,m), 2,25-2,20(1Н,m), 1,00-0,96(4Н,m), 0,89-0,85(1Н,m), 0,70-0,63(3Н,m), 0,02-0,01(18Н,m).
[0719]
Стадия 6: (11а'S)-7'-Метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,11а-дигидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
К раствору соединения, полученного на стадии 5 (0,900 г, 0,942 ммоль), в ТГФ (30 мл) и этаноле (3 мл) медленно добавляли борогидрид лития (0,456 г, 18,8 ммоль) при 0°С. После реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов, к реакционной смеси добавляли воду и полученную смесь интенсивно перемешивали. Реакционную смесь подвергали экстракции хлороформом. Органический слой подвергали перегонке при пониженном давлении и полученный остаток растворяли в дихлорметане (10 мл), этаноле (20 мл) и воде (5 мл). К реакционной смеси добавляли силикагель (15,0 г), полученную смесь перемешивали в атмосфере азота в течение 3 дней. Реакционную смесь фильтровали и органический слой промывали солевым раствором и сушили над безводным сульфатом натрия. После фильтрации с последующей перегонкой при пониженном давлении полученный остаток очищали с помощью колоночной хроматографии на силикагеле [хлороформ : метанол = 100:0 (об./об.) до 92:8 (об./об.)], получая желаемое соединение (0,308 г, 49%).
МС (ХИАД, ИЭР) m/z:663 (М+Н)+
[0720]
Пример 50: Лекарственное средство 6
[Формула 174]
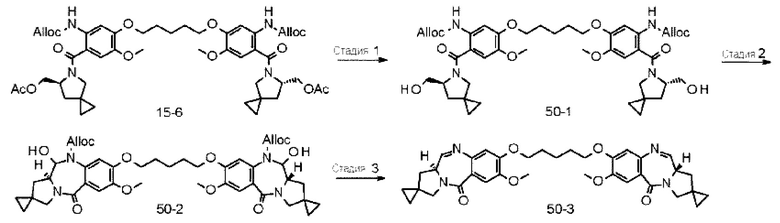
Стадия 1: Ди-2-пропен-1-ил-{1,5-пентандиилбис[окси(6-{[(6S)-6-(гидроксиметил)-5-азаспиро[2,4]гепт-5-ил]карбонил}-4-метоксибензол-3,1-диил)]}бискарбамат
Бисаллилоксикарбонильную форму 15-6 (0,460 г, 0,508 ммоль), полученную на стадии 5 примера 15, растворяли в метаноле (10 мл) и затем к ней добавляли карбонат калия (351 мг, 2,54 ммоль) и полученный продукт перемешивали при комнатной температуре в течение 30 минут. К нему добавляли 50 мл насыщенный водный раствор хлорида аммония и полученный продукт подвергали экстракции этилацетатом. Органический слой сушили над безводным сульфатом натрия. Полученный продукт подвергали перегонке при пониженном давлении, получая желаемое соединение (0,421 г, количественный выход).
1H ЯМР(ДМСО-D6) δ: 9,19(2H,s), 7,22(2H,s), 6,89(2H,s), 5,97-5,92(2Н,m), 5,33(2Н,m), 5,22(2Н,m), 4,81(2Н,m), 4,55(4Н,m), 4,26(2Н,s), 3,96(4Н,m), 3,74(6H,s), 3,62(2H,m), 3,56(2H,s), 3,37(2H,m), 3,11(2H,m), 1,88-1,78(8H,m), 1,56-1,54(2H,m), 0,54-0,43(8H,m).
МС (ХИАД, ИЭР) m/z: 821(M+H)+.
[0721]
Стадия 2: Дипроп-2-ен-1-ил-(11a'S,11а''''S)-8',8''-[пентан-1,5-диилбис(окси)]бис(11'-гидрокси-7'-метокси-5'-оксо-11',11a'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбоксилат)
Соединение, полученное на стадии 1 (0,421 г, 0,513 ммоль), подвергали реакции таким же образом, как и на стадии 8 примера 15, получая желаемое соединение (0,326 г, 78%).
1H ЯМР(ДМСО-D6) δ: 7,07(2H,s), 6,80(2H,s), 6,55(2H,m), 5,84-5,81(2Н,m), 5,75(2Н,m), 5,09-5,05(4H,m), 4,62(2H,mz), 4,40(2H,m), 3,98(4H,m), 3,81(6H,s), 3,54(2H,m), 3,43-3,37(2Н,m), 3,14(2Н,m), 2,35(2Н,m), 1,81-1,79(4Н,m), 1,59-1,56(4Н,m), 0,70-0,59(8Н,m).
МС (ХИАД, ИЭР) m/z: 817(M+H)+.
[0722]
Стадия 3: (11a'S,11а''''S)-8',8''-[1,5-Пентандиилбис(окси)]бис(7'-метокси-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он)
Соединение, полученное на стадии 2 (0,326 г, 0,399 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,208 г, 85%).
1H-ЯМР(ДМСО-D6) δ: 7,91(2H,m), 7,32(2H,s), 6,84(2H,s), 4,11(2H,m), 4,06(2H,m), 3,82(6H,s), 3,51-3,31(6Н,m), 2,43(2Н,m), 2,05(2Н,m), 1,82-1,80(4Н,m), 1,60-1,58(2Н,m), 0,79-0,77(2H,m), 0,68-0,64(6H,m).
МС (ХИАД, ИЭР) m/z:613(M+H)+.
[0723]
Пример 51: Лекарственное средство 7
[Формула 175]
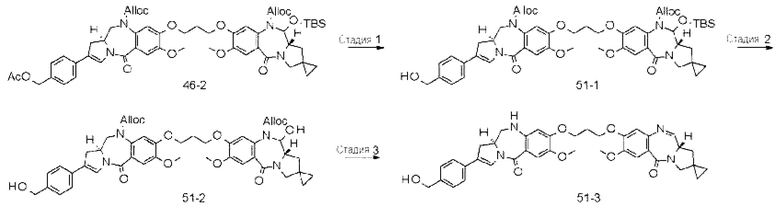
[0724]
Стадия 1: Соединение 51-1
Соединение 46-2 (0,0870 г, 0,0863 ммоль) подвергали реакции таким же образом, как и на стадии 1 примера 27, получая желаемое соединение (0,0660 мг, 79%).
1H ЯМР(CDCl3) δ: 7,50(1H,s), 7,36-7,34(4H,m), 7,27-7,24(2H,m), 6,80(1H,s), 6,64(1H,s), 6,03(1H,m), 5,80-5,74(2H,m), 5,10-5,06(3H,m), 4,70(2H,m), 4,67-4,60(2H,m), 4,41-4,37(3H,m), 4,23-4,20(6H,m), 3,90(3H,s), 3,89(3H,s), 3,72(1H,m), 3,65-3,62(1H,m), 3,51(1H,m), 3,34-3,26(2H,m), 2,75-2,71(1H,m), 2,39-2,35(3H,m), 1,74(1H,m), 1,56-1,52(1H,m), 0,85(9H,s), 0,80-0,62(4H,m), 0,22(3H,s), 0,21(3H,s).
МС (ХИАД, ИЭР) m/z: 965 (M+H)+.
[0725]
Стадия 2: Соединение 51-2
Соединение, полученное на стадии 1 (0,0660 г, 0,0683 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,0590 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 851(М+Н)+.
[0729]
Стадия 3: (11a'S)-8'-[3-({(11aS)-2-[4-(Гидроксиметил)фенил]-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил}окси)пропокси]-7'-метокси-1',11а'-дигадро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 2 (0,0590 г, 0,0693 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,0290 г, 63%).
1Н-ЯМР(CDCl3) δ: 7,80-7,79(1Н,m), 7,64-7,64(1Н,m), 7,52-7,51(2Н,m), 7,36-7,33(4Н,m), 6,85(1Н,m), 6,14(1Н,m), 4,69(2Н,m), 4,30-4,26(6Н,m), 3,95-3,95(3Н,m), 3,86-3,84(3Н,m), 3,67(1Н,m), 3,56-3,54(2Н,m), 3,50-3,48(2Н,m), 3,39-3,30(1Н,m), 2,80-2,73(1Н,m), 2,52(1Н,m), 2,41 -2,39(2Н,m), 2,00(1Н,m), 1,73-1,72(1Н,m), 0,76-0,70(4Н,m).
МС (ХИАД, ИЭР) m/z: 665(М+Н)+.
[0727]
Пример 52: Лекарственное средство 8
[Формула 176]
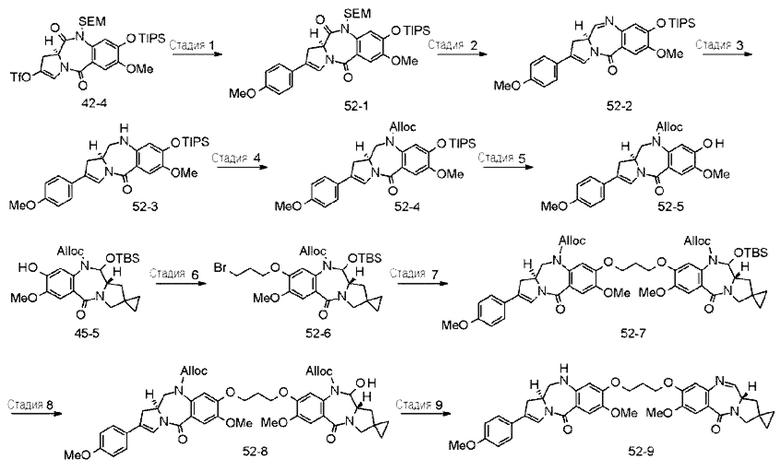
Стадия 1: (11aS)-7-Метокси-2-(4-метоксифенил)-10-{[2-(триметилсилил)этокси]метил}-8-{[три(пропан-2-ил)силил]окси}-1Н-пирроло[2,1-с][1,4]бензодиазепин-5,11(10Н, 11аН)-дион
Соединение, полученное на стадии 4 примера 42 (0,519 г, 0,747 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 3, получая желаемое соединение (0,511 г, количественный выход).
1H-ЯМР(CDCl3) δ: 7,41-7,31 (5H,m), 6,91-6,85(2H,m), 5,52(1H,m), 4,64(1H,m), 4,57(1H,m), 3,97-3,90(1H,m), 3,88(3H,s), 3,83(3H,s), 3,75-3,56(2H,m), 3,19-3,09(1H,m), 1,36-1,23(3H,m), 1,11(18H,m), 1,02-0,97(2H,m), 0,03(9H,s).
MC (ХИАД, ИЭР) m/z: 653[(M+H)+]
[0728]
Стадия 2: (11aS)-7-Метокси-2-(4-метоксифенил)-8-{[три(пропан-2-ил)силил]окси}-1,11а-дигидро-5Н-пирроло[2,1-с][1,4]бензодиазепин-5-он
Соединение, полученное на стадии 1 (0,178 г, 0,272 ммоль), подвергали реакции таким же образом, как и на стадии 7 примера 3, получая желаемое соединение (0,094 г, 68%).
1H-ЯМР(CDCl3) δ: 7,87(1H,m), 7,51(1H,s), 7,41-7,39(1H,m), 7,36-7,33(2H,m), 6,93-6,89(2H,m), 6,86(1H,s), 4,44-4,38(1H,m), 3,90(3H,s), 3,83(3H,s), 3,61-3,53(1H,m), 3,41-3,34(1Н,m), 1,33-1,25(3H,m), 1,11-1,06(18H,m).
MC (ХИАД, ИЭР) m/z: 507(M+H)+
[0729]
Стадия 3: (11aS)-7-Метокси-2-(4-метоксифенил)-8-{[три(пропан-2-ил)силил]окси}-1,10,11,11а-тетрагидро-5Н-пирроло[2,1-c][1,4]бензодиазепин-5-он
Использовали соединение, полученное на стадии 2 (0,063 г, 0,124 ммоль), и его подвергали реакции таким же образом, как и на стадии 8 примера 3, получая желаемое соединение (0,046 г, 72%).
1H-ЯМР(CDCl3) δ: 7,53-7,48(2H,m), 7,33-7,29(2H,m), 6,90-6,86(2H,m), 6,13-6,11(1H,m), 4,36-4,29(1H,m),4,11(1H,s), 3,82(3H,s), 3,79(3H,s), 3,59-3,50(2H,m), 3,40-3,31(1Н,m), 2,78-2,68(1Н,m), 1,31-1,20(3Н,m), 1,13-1,02(18Н,m).
МС (ХИАД, ИЭР) m/z: 509(M+H)+
[0730]
Стадия 4: Проп-2-ен-1-ил-(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-8-{[три(пропан-2-ил)силил]окси}-11,11а-дигидро- Ш-пиррол о [2,1-с][1,4]бензодиазепин-10(5Н)-карбоксилат
Использовали соединение, полученное на стадии 3 (0,046 г, 0,090 ммоль), и подвергали его реакции таким же образом, как и на стадии 9 примера 3, получая желаемое соединение (0,03 г, 56%).
1H ЯМР(CDCl3) δ: 7,39-7,36(1H,m), 7,31-7,28(2H,m), 7,22(1H,s), 6,90-6,86(3H,m), 6,75-6,72(1H,m), 5,82-5,69(1H,m), 5,18-5,08(2H,m), 4,59-4,52(1H,m), 4,48-4,39(1H,m), 4,39-4,29(1H,m), 4,23-4,12(1H,m), 3,86(3H,s), 3,82(3H,s), 3,64-3,58(1H,m), 3,32-3,25(1Н,m), 2,73-2,65(1Н,m), 1,30-1,20(2H,m), 1,12-1,06(18H,m).
МС (ХИАД, ИЭР) m/z: 593 (M+H)+
[0731]
Стадия 5: Проп-2-ен-1-ил-(11aS)-8-гидрокси-7-метокси-2-(4-метоксифенил)-5-оксо-11,11а-дигидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-10(5Н)-карбоксилат
Соединение, полученное на стадии 4 (0,030 г, 0,050 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 1, получая желаемое соединение (0,015 г, 0,034 ммоль).
1H-ЯМР(CDCl3) δ: 7,39-7,25(4H,m), 6,92-6,78(3H,m), 6,03-5,92(1H,m), 5,86-5,68(1H,m), 5,20-5,07(2H,m), 4,66-4,57(1H,m), 4,52-4,40(1H,m), 4,40-4,27(1H,m), 4,27-4,16(1H,m), 3,95(3H,s), 3,82(3H,s), 3,66-3,59(1H,m), 3,32-3,21(1H,m), 2,74-2,64(1H,m).
МС (ХИАД, ИЭР) m/z:437(M+H)+
[0732]
Стадия 6: Проп-2-ен-1-ил-(11а'S)-8'-(3-бромпропокси)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-5'-оксо-11', 11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 5 примера 45 (0,131 г, 0,268 ммоль), подвергали реакции таким же образом, как и на стадии 1 примера 4, получая желаемое соединение (0,086 г, 52%).
1H-ЯМР(CDCl3) δ: 7,24(1H,s), 6,65(1H,s), 6,02(1H,m), 5,87-5,71(1H,m), 5,15-5,04(2H,m), 4,72-4,62(1H,m), 4,44-4,32(1H,m), 4,23-4,07(3H,m), 3,92(3H,s), 3,77-3,47(4H,m), 3,28(1H,m), 2,37(3H,m), 1,57-1,52(1H,m), 0,86(9H,s), 0,82-0,57(4H,m), 0,21(6H,m).
МС (ХИАД, ИЭР) m/z: 611[81Br, (M+H)+], 609[79Br, (M+H)+]
[0733]
Стадия 7: Проп-2-ен-1-ил-(11a'S)-11'-{[трет-бутил(диметил)силил]окси}-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро [циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 5 (0,015 г, 0,034 ммоль), и соединение, полученное на стадии 6 (0,030 г, 0,048 ммоль), подвергали реакции таким же образом, как и на стадии 10 примера 3, получая желаемое соединение (0,032 г, 96%).
МС (ХИАД, ИЭР) m/z: 965 (М+Н)+
[0734]
Стадия 8: Проп-2-ен-1-ил-(11а'S)-11'-гидрокси-7'-метокси-8'-[3-({(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-10-[(проп-2-ен-1-илокси)карбонил]-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил}окси)пропокси]-5'-оксо-11',11а'-дигидро-1'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-10'(5'Н)-карбоксилат
Соединение, полученное на стадии 7 (0,031 г, 0,032 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,026 г, 95%).
МС (ХИАД, ИЭР) m/z: 851 (М+Н)+
[0735]
Стадия 9: (11а'S)-7'-Метокси-8'-(3-{[(11aS)-7-метокси-2-(4-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 8 (0,026 г, 0,030 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,018 г, 88%).
1Н-ЯМР(CDCl3) δ: 7,80(1Н,m), 7,54-7,51 (3Н,m), 7,33-7,29(2Н,m), 6,91-6,85(3H,m), 6,14(1H,s), 4,35-4,17(6H,m), 3,95(3H,s), 3,85(3H,s), 3,82(3H,s), 3,76-3,25(5Н,m), 2,79-2,69(1Н,m), 2,52(1 Н,m), 2,45-2,35(1Н,m), 2,03-1,96(1Н,m), 1,28-1,23(2Н,m), 0,78-0,69(4Н,m).
МС (ХИАД, ИЭР) m/z: 665(M+H)+
[0736]
Пример 53: Лекарственное средство 9
[Формула 177]
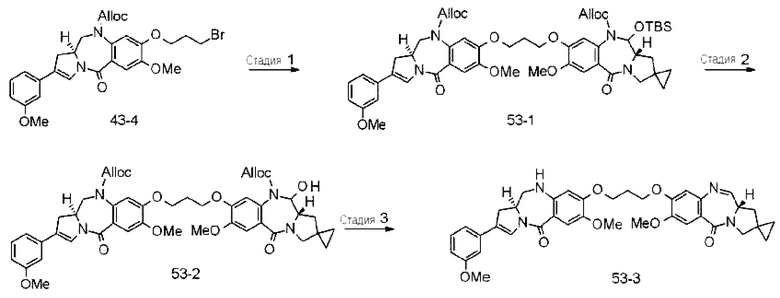
Стадия 1: Соединение 53-1
Соединение, полученное на стадии 4 примера 43 (0,027 г, 0,048 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 45, получая желаемое соединение (0,037 г, 79%).
МС (ХИАД, ИЭР) m/z: 965 (М+Н)+
[0737]
Стадия 2: Соединение 53-2
Соединение, полученное на стадии 1 (0,037 г, 0,038 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (35 мг, количественный выход).
МС (ХИАД, ИЭР) m/z: 851[(M+H)+]
[0738]
Стадия 3: (11а'S)-7'-Метокси-8'-(3-{[(11aS)-7-метокси-2-(3-метоксифенил)-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-c][1,4]бензодиазепин-8-ил]окси}пропокси)-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-с][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 2 (0,038 ммоль), подвергали реакции таким же образом, как и на стадиях 6-8 примера 45, получая желаемое соединение (25 мг, 99%).
1H-ЯМР(CDCl3) δ: 7,81-7,78(1H,m), 7,65-7,62(1H,m), 7,53-7,49(2H,m), 7,24(1H,m), 6,96(1H,m), 6,91-6,88(1H,m), 6,85(1H,m), 6,78(1H,m), 6,14(1H,m), 4,41-4,18(5H,m), 3,97-3,92(3H,m), 3,88-3,84(3H,m), 3,83(3H,s), 3,76-3,25(5H,m), 2,78-2,71(1H,m), 2,52(1H,m), 2,45-2,35(2H,m), 2,03-1,96(1H,m), 1,29-1,21(2H,m), 0,78-0,69(4H,m).
MC (ХИАД, ИЭР) m/z: 664(M+H)+
[0739]
Пример 54: Лекарственное средство 10
[Формула 178]
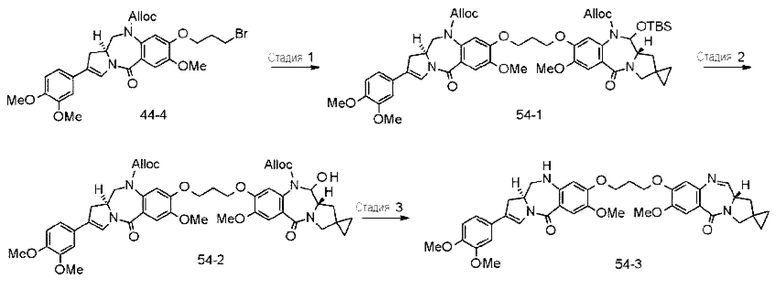
Стадия 1: Соединение 54-1
Соединение, полученное на стадии 4 примера 44 (0,027 г, 0,046 ммоль), подвергали реакции таким же образом, как и на стадии 6 примера 45, получая желаемое соединение (0,037 г, 81%).
МС (ХИАД, ИЭР) m/z: 995 (М+Н)+
[0740]
Стадия 2: Соединение 54-2
Соединение, полученное на стадии 1 (0,037 г, 0,037 ммоль), подвергали реакции таким же образом, как и на стадии 11 примера 3, получая желаемое соединение (0,034 г, количественный выход).
МС (ХИАД, ИЭР) m/z: 881 (М+Н)+
[0741]
Стадия3: (11a'S)-8'-(3-{[(11aS)-2-(3,4-диметоксифенил)-7-метокси-5-оксо-5,10,11,11а-тетрагидро-1Н-пирроло[2,1-с][1,4]бензодиазепин-8-ил]окси}пропокси)-7'-метокси-1',11а'-дигидро-5'Н-спиро[циклопропан-1,2'-пирроло[2,1-c][1,4]бензодиазепин]-5'-он
Соединение, полученное на стадии 2 (0,037 ммоль), подвергали реакции таким же образом, как и на стадии 12 примера 3, получая желаемое соединение (0,027 г, количественный выход).
1Н-ЯМР(CDCl3) δ: 7,81-7,78(1Н,m), 7,55-7,49(3Н,m), 6,99-6,96(1H,m), 6,87-6,82(3Н,m), 6,14(1Н,m), 4,41-3,28(22Н,m), 2,77-2,71(1Н,m), 2,57-2,48(1Н,m), 2,45-2,34(2Н,m), 2,04-1,96(1Н,m), 1,43-1,11 (2Н,m), 0,79-0,67(4Н,m).
МС (ХИАД, ИЭР) m/z:695(M+H)+
[0742]
[Синтез донора-гликана]
Пример 55: [N3-PEG (3)]2-SG (10)-Ох
[Формула 179]
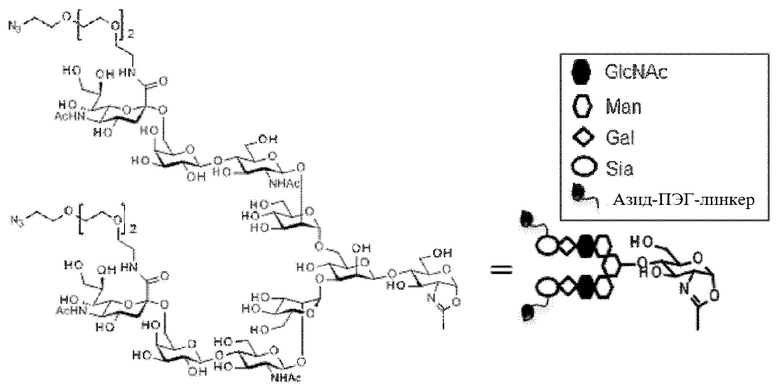
(На данной фигуре схематическая диаграмма в правой части структурной формулы представляет соответствующую структуру на схематической диаграмме промежуточного соединения, содержащего линкерную структуру, в которую была введена азидная группа, как представлено формулой реакции примера 58.)
[0743]
Стадия 1: [N3-PEG (3)]2-SG (10)
В 5 мл пробирку для образцов (Ina-OpticCo., Ltd) добавляли водный раствор (0,5 мл) 11-азид-3,6,9-триоксаундекан-1-амина (0,096 мл, 0,485 ммоль) и дисиалооктасахарид (50 мг, 0,24 ммоль) и полученный продукт перемешивали в течение 1 часа и затем сушили с помощью сублимационной сушки. В 5 мл пробирку для образцов после сублимационной сушки добавляли раствор O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфата в N,N-диметилформамиде (0,6 мл) (92 мг, 0,24 ммоль) и диизопропилэтиламин (0,042 мл, 0,24 ммоль), затем перемешивали при 37°С в течение 4 часов. После завершения реакции реакционный раствор переносили в центрифужную пробирку (50 мл) в которую заранее добавляли диэтиловый эфир (20 мл). Твердое вещество осаждали с помощью небольшой центрифуги (Hitachi Koki Co., Ltd., CF16RX) и удаляли супернатант. Добавляли диэтиловый эфир (20 мл) и полученный продукт декантировали. Затем добавляли ацетонитрил (20 мл) и полученный продукт декантировали и затем сушили при пониженном давлении, получая неочищенный продукт. Полученное твердое вещество растворяли в соответствующем количестве 0,2% водного раствора трифторуксусной кислоты и подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила и трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемое соединение, детектируемое УФ-излучением (220 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая желаемое соединение (42 мг).
[0744]
Стадия 2: [N3-PEG (3)]2-SG (10)-Ох
В 5 мл пробирку для образцов (производства Ina-OpticCo., Ltd) добавляли соединение, синтезированное на стадии 1 (40 мг), и водный раствор (200 мкл) 2-хлор-1,3-диметил-1H-бензимидазол-3-ий-хлорида (производства FUSHIMI Pharmaceutical Co., Ltd. 17,9 мг, 0,083 ммоль). К реакционному раствору после охлаждения льдом добавляли водный раствор (200 мкл) трикалийфосфата (52,6 мг, 0,25 ммоль), затем перемешивали при охлаждении льдом в течение 2 часов. Полученный реакционный раствор подвергали ультрафильтрации с помощью Amicon Ultra (Ultracel 30K, производства Merck Millipore) для удаления твердого вещества. Отфильтрованный раствор очищали с помощью гель-фильтрационной хроматографии. Используемое устройство представляло собой Purif-Rp2 (производства Shoko Scientific Co., Ltd.), используемая колонка представляла собой HiPrep 26/10 Desalting (производства GE Healthcare), используемая подвижная фаза представляла собой 0,03%-водный раствор NH3 и скорость потока составляла 10 мл/мин и объем фракции составлял 10 мл. Фракции, содержащие желаемое соединение, детектируемое УФ-излучением (220 нм) во время элюирования, объединяли, к ним добавляли 1 н. водный раствор гидроксида натрия (33 мкл, 0,033 ммоль) и полученный продукт сушили с помощью сублимационной сушки, получая желаемое соединение (34 мг).
[0745]
Пример 56: [N3-PEG (3)]-MSG1-Ox
[Формула 180]
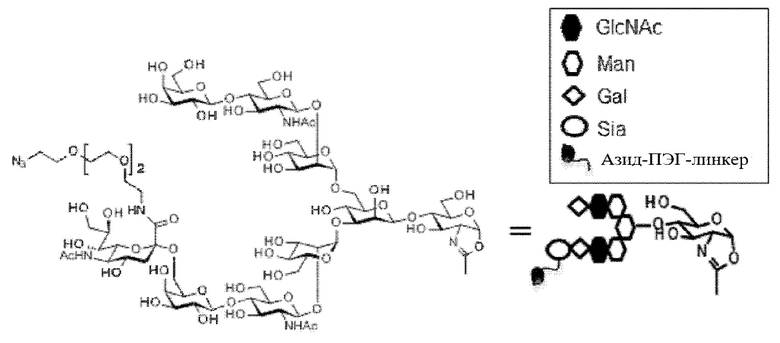
(На данной фигуре схематическая диаграмма в правой части структурной формулы представляет соответствующую структуру на схематической диаграмме промежуточного соединения, содержащего линкерную структуру, в которую введена азидная группа, как представлено формулой реакции каждого из примеров 60, 61, 62, 63, 64, 65 и 66.)
[0746]
Стадия 1: (MSG1-)Asn
Коммерчески доступный продукт, не содержащий моносиало-Asn (1S2G/1G2S-10NC-Asn, производства GlyTech, Inc.) (обозначаемый как "(MSG-)Asn") (500 мг) подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ в условиях, указанных ниже, для разделения на (MSG1-)Asn элюированный в качестве 1-го основного пика (время удерживания: примерно 15-19 мин) и (MSG2-)Asn элюированный в качестве 2-го основного пика (время удерживания: примерно 21-26 мин). В качестве элюента использовали 0,1% водный раствор муравьиной кислоты, в качестве устройства использовали триггерную препаративную систему ELS-PDA (производства JASCO Corporation) используемая колонка представляла собой Inertsil ODS-3 (10 мкм, 30φ × 250 мм, производства GL Sciences, Inc.) и скорость потока составляла 30 мл/мин. Фракции, относящиеся к первому пику УФ-детектирования (210 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая желаемое соединение (238 мг).
[0747]
Стадия 2: MSG1
Соединение, полученное на стадии 1 (229 мг), растворяли в 200 мМ фосфатного буферного раствора (рН 6,25) (1145 мкл), к которому добавляли водный раствор (100 мкл) EndoM (производства Tokyo Chemical Industry Co., Ltd., 1 ед/мл) и полученный продукт инкубировали при 35°С в течение 6 дней. После завершения реакции реакционный раствор подвергали ультрафильтрации с использованием VIVASPIN 15R (мембрана Hydrosart, 30K, 6,000 г) и полученный фильтрованный раствор подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. В качестве элюента использовали 0,1% водный раствор трифторуксусной кислоты, в качестве устройства использовали триггерную препаративную систему ELS-PDA (производства JASCO Corporation), а используемая колонка представляла собой Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемое соединение, детектируемое УФ-излучением (210 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая желаемое соединение (117 мг).
[0748]
Стадия 3: [N3-PEG (3)]-MSG1
Соединение, синтезированное на стадии 2 (169 мг), подвергали реакции таким же образом, как и на стадии 1 примера 55, получая желаемое соединение (94,2 мг).
[0749]
Стадия 4 [N3-PEG (3)]-MSG1-Ox
Соединение (100 мг), синтезированное на стадии 3 подвергали реакции таким же образом, как и на стадии 2 примера 55, получая желаемое соединение (89 мг).
[0750]
Пример 57: [N3-PEG (3)]-MSG-Ox
[Формула 181]
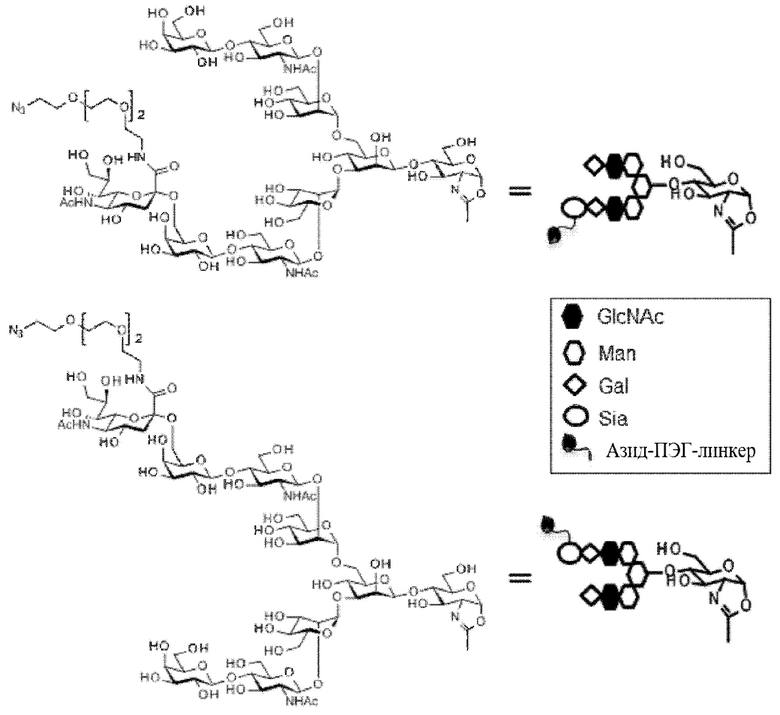
(На фигуре схематическая диаграмма в правой части структурной формулы представляет соответствующую структуру на схематической диаграмме промежуточного соединения, содержащего линкерную структуру, в которую введена азидная группа, как представлено формулой реакции примера 59.)
[0751]
Стадия 1: Получение (MSG-)Asn
Коммерчески доступный продукт 1S2G/1G2S-10NC-Asn-Fmoc (производства GlyTech, Inc.) (обозначаемый как "Fmoc-(MSG-)Asn") (1000 мг) растворяли в этаноле/воде (1/1) (10 мл), к нему добавляли 1 н. водный раствор гидроксида натрия (1,75 мл, 4 эквивалента), затем перемешивали при комнатной температуре в течение 3 часов. После завершения реакции реакционный раствор подвергали ультрафильтрации с использованием Amicon Ultra (30K, производства Millipore Corporation) для удаления твердого вещества и к полученному фильтрованному раствору добавляли 1 н. соляную кислоту (832 мкл, 1,9 эквивалента). Растворитель удаляли с помощью высокоскоростного испарителя V-10 (производства Biotage). К нему добавляли ацетонитрил и растворитель удаляли с помощью высокоскоростного испарителя V-10 (производства Biotage) и полученный продукт затем подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемое соединение, детектируемое УФ-излучением (220 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки. Получившееся вещество снова растворяли в чистой воде и бумажная полоска для определения рН показала, что раствор был кислым. Следовательно, туда добавляли 18% водный раствор аммиака (150 мкл) и с помощью бумажной полоски для теста на рН подтверждали, что раствор стал основным и раствор снова сушили с помощью сублимационной сушки. Полученное желаемое соединение (840 мг) непосредственно применяли для последующей реакции.
[0752]
Стадия 2: Синтез MSG
Соединение, полученное на стадии 1 (840 мг), растворяли в 200 мМ фосфатного буферного раствора (рН 6,25) (6000 мкл), к нему добавляли водный раствор (200 мкл) EndoM (производства Tokyo Chemical Industry Co., Ltd., 1 ед./мл)) и полученный продукт инкубировали при 28°С в течение 26 часов. Поскольку реакция не была завершена, добавляли водный раствор (50 мкл) EndoM (производства Tokyo Chemical Industry Co., Ltd., 1 ед./мл)) и полученный продукт инкубировали при 28°С в течение 2 часов и затем оставляли стоять при комнатной температуре до завершения реакции. После завершения реакции реакционный раствор подвергали ультрафильтрации с использованием Amicon Ultra (30K, производства Millipore Corporation). К полученному фильтрованному раствору добавляли трифторуксусную кислоту (80 мкл) и полученную смесь подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемое соединение, детектируемое УФ-излучением (220 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки. Его снова растворяли в чистой воде, чтобы удалить остаточную трифторуксусную кислоту и, таким образом, получали желаемое соединение (618 мг) в виде бесцветного твердого вещества.
ИЭР-МС: Расчетное значение для C66H110N4O49: [М+Н]+1743,62, найденное значение 1743,63
[0753]
Стадия 3: Синтез [N3-PEG (3)]-MSG
В соответствии с методикой проведения стадии 1 примера 55 с использованием соединения, полученного на стадии 2 (120 мг), получали желаемое соединение (88,6 мг).
ИЭР-МС: Расчетное значение для C73H124N8O51: [М+2Н]2+ 965,37, найденное значение 965,37
[0754]
Стадия 4 Синтез [N3-PEG (3)]-MSG-Ox
В соответствии с методикой проведения стадии 2 примера 55 с использованием соединения, полученного на стадии 4 (100 мг), получали желаемое соединение (88 мг).
[0755]
[Получение гликан-ремоделированного антитела]
Пример 58: Ремоделирование сахарной цепи 1 (T-SG)
[Формула 182]
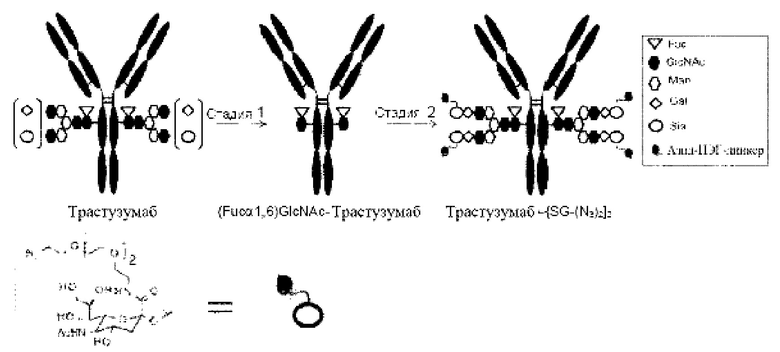
(В данной формуле представлена линкерная структура, в которой в сиаловую кислоту на невосстанавливающем конце N297-гликана типа SG введена азидная группа. В примере 58 ликерные структуры промежуточных соединений, образованных введением азидной группы в N297-гликан, являются такими же, как структура, представленная формулой)
[0756]
Стадия 1: Получение (Fucα1,6) GlcNAc-трастузумаба
Раствор трастузумаба с концентрацией 22 мг/мл (25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола) (45,5 мл), полученный в сравнительном примере 3, делили пополам и в соответствии с общей операцией С два раза отдельно проводили замену буфера на 50 мМ фосфатного буфера (рН 6,0). К полученному раствору трастузумаба с концентрациями 28,1 мг/мл (18 мл) и 28,0 мг/мл (18 мл) (50 мМ фосфатного буфера (рН 6,0)) соответственно добавляли 1,26 мл и 1,27 мл раствор EndoS дикого типа (2,0 мг/мл, ФСБ) и полученные растворы инкубировали при 37°С в течение 4 часов. Ход реакции контролировали с помощью системы для электрофореза Experion (производетва Bio-Rad Laboratories, Inc.). После завершения реакции очистку методом аффинной хроматографией и очистку на гидроксиапатитовой колонке проводили в соответствии со следующими способами.
(1) Очистка методом аффинной хроматографии
Аппарат для очистки: АКТА pure150 (производства GE Healthcare)
Колонка: HiTrap rProtein A FF (5 мл) (производства GE Healthcare)
Скорость потока: 5 мл/мин (1,25 мл/мин при нанесении)
Каждый реакционный раствор, полученный выше, очищали в процессе нескольких отдельных операций. Две колонки соединяли в одну и при соединении с колонкой в верхнюю часть колонки вносили реакционный раствор и пропускали 2 объема колонки (CV) связующего буфера (20 мМ фосфатного буфера (рН 6,0)) со скоростью 1,25 мл/мин и далее пропускали 5 CV указанного буфера дополнительно пропускали со скоростью 5 мл/мин. При промежуточной промывке пропускали 15 CV промывочного раствора (20 мМ фосфатного буфера (рН 7,0), 0,5 М раствора хлорида натрия). При элюировании пропускали 6 CV буфера для элюирования (буфер ImmunoPure IgG Eution Buffer, производства Pierce). Элюат сразу же нейтрализовали с помощью 1 М трис-буфера (рН 9,0). Фракции, полученные при детектировании УФ-излучением (280 нм) во время элюирования, проверяли с применением микрообъемного спектрофотометра Xpose (производства Trinean NV) и системы для электрофореза Experion (производства Bio-Rad Laboratories, Inc.). Для фракций, содержащих желаемого соединение, проводили замену буфера на 5 мМ фосфатный буфер/50 мМ раствор 2-морфолиноэтансульфоновой кислоты (MES) (рН 6,8) с применением общей операции С.
(2) Очистка методом хроматографии на гидроксиапатите
Аппарат для очистки: АКТА avant25 (производства GE Healthcare)
Колонка: картридж Bio-Scale Mini СНТ Type I (5 мл) (производства Bio-Rad Laboratories, Inc.)
Скорость потока: 5 мл/мин (1,25 мл/мин при нанесении)
Две колонки соединяли в одну и раствор, полученный на стадии (1), очищали в процессе нескольких отдельных операций. Раствор вносили в верхнюю часть колонки и пропускали 2 CV раствора А (5 мМ фосфатного буфера, 50 мМ раствора 2-морфолиноэтансульфоновой кислоты (MES) (рН 6,8)) со скоростью 1,25 мл/мин и далее пропускали 3 CV указанного раствора со скоростью 5 мл/мин. После этого проводили элюирование раствором А и раствором В (5 мМ фосфатного буфера/50 мМ раствора 2-морфолиноэтансульфоновой кислоты (MES) (рН 6,8), 2 М раствора хлорида натрия). Условия элюирования: раствор А: раствор В = 100:0 до 0:100 (15 CV). Далее пропускали 5 CV промывочного раствора (500 мМ фосфатного буфера (рН6,5)).
Для фракций, содержащих желаемое соединение, проводили замену буфера с применением общей операции С, получая раствор (35 мл) (Fucα1,6)GlcNAc-трастузумаба с концентрацией 25,5 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)).
[0757]
Стадия 2: Получение трастузумаб[SG-(N3)2]2
К раствору (Fucα1,6)GlcNAc-трастузумаба с концентрацией 23,9 мг/мл (50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1 (3,37 мл), добавляли раствор (0,258 мл) соединения, синтезированного на стадии 2 примера 55 (12,9 мг) в 50 мМ фосфатного буфера (рН 6,0) и добавляли раствор (ФСБ) EndoS D233Q/Q303L с концентрацией 4,90 мг/мл (0,328 мл) и полученный продукт инкубировали при 30°С в течение 4,5 часов. Данные операции выполняли с разделением на две партии. Ход реакции контролировали с использованием системы для электрофореза Experion (производства Bio-Rad Laboratories, Inc.). После завершения реакции проводили очистку методом аффинной хроматографии и очистку методом хроматографии на гидроксиапатите на стадии 1 и затем фрации, содержащие желаемого соединение, проводили замену буфера на фосфатно-солевой буфер (рН 6,0) с применением общей операции С, получая раствор (15,5 мл) трастузумаба с концентрацией 10,0 мг/мл [SG-(N3)2]2 (в фосфатно-солевом буфере (рН 6,0)).
[0758]
Пример 59: Ремоделирование сахарной цепи 2 (T-MSG)
[Формула 183]
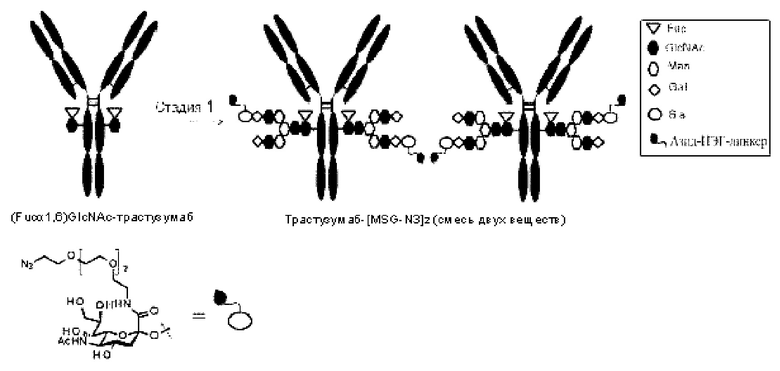
(В данной формуле представлена линкерная структура, в которой к сиаловой кислоте на невосстанавливающем конце N297-гликана MSG-типа введена азидная группа. В примере 59 линкерные структуры промежуточных соединений, образованные путем введения азидной группы в N297-гликан, все являются такими же, как структуры, представленные данной формулой).
[0759]
Стадия 1: Трастузумаб[MSG-N3]2
Следующие операции проводили с разделением напять партий. Соединение, полученное на стадии 1 примера 58 (20 мг/мл, 15,0 мл), использовали совместно с соединением, полученным на стадии 4 примера 57 (25,5 мг), в качестве донора гликана, инкубировали при 30°С в течение 3 часов и проводили те же операции, что и на стадии 2 примера 59. При объединении пяти партий по луча ли раствор (93,5 мл) Трастузумаб[MSG-N3]2 с концентрацией 14,4 мг/мл (в фосфатно-солевом буфере (рН 6,0)).
[0760]
Пример 60: Ремоделирование сахарной цепи 3 (T-MSG1)
[Формула 184]
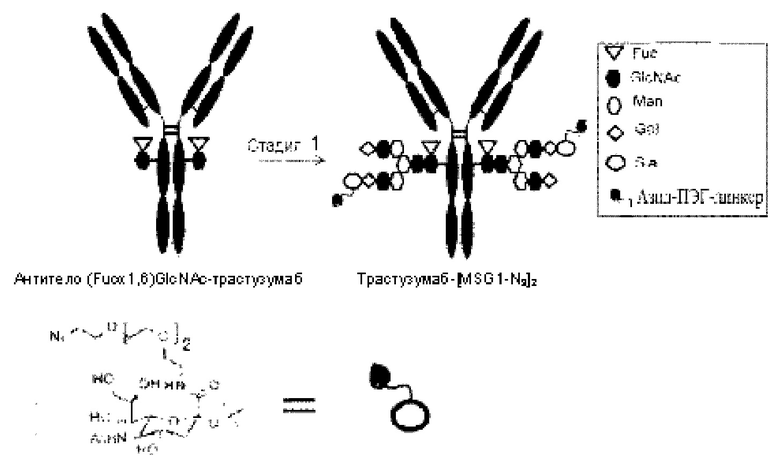
(В данной формуле представлена линкерная структура, в которой к сиаловой кислоте на невосстанавливающем конце N297-гликана MSG1-типа введена азидная группа. В примере 60 линкерные структуры промежуточных соединений, образованные путем введения азидной группы в N297-гликан, все являются такими же, как структуры, представленные данной формулой. Это же относится, например, к примерам 61-66).
Стадия 1: Трастузумаб[MSG1-N3]2
Следующие операции проводили с разделением на две партии. Соединение, полученное на стадии 1 примера 58 (25,5 мл, 7,8 мл), использовали совместно с соединением, полученным на стадии 4 примера 56 (25,5 мг), в качестве донора гликана, инкубировали при 30°С в течение 3 часов и проводили те же операции, что и на стадии 2 примера 59. При объединении двух партий получали раствор (31 мл) Трастузумаб[MSG1-N3]2 с концентрацией 10,6 мг/мл (в фосфатно-солевом буфере (рН6,0)).
[0761]
Пример 61: Ремоделирование сахарной цепи 4 (CLDN6-MSG1 (H1L1))
[Формула 185]
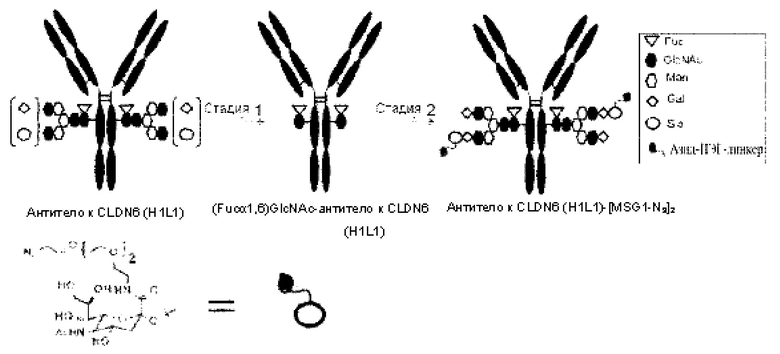
Стадия 1: (Fucα1,6)GlcNAc-антитело к CLDN6 (H1L1)
Операции, аналогичные пред став ленным на стадии 1 примера 58, проводили с применением раствора антитела к CLDN6 с концентрацией приблизительно 37,7 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сор бито л а), полученного в примере 136 (2,5 мл), получая раствор (4,8 мл) (Fucα1,6)GlcNAc-антитела к CLDN6 (H1L1) с концентрацией 19,2 мг/мл (50 мМ фосфатного буфера (pH 6,0)).
[0762]
Стадия 2: Антитело к CLDN6 (H1L1)-[MSG1-N3]2
Операции, аналогичные пред став ленным на стадии 1 примера 60, проводили с применением раствора (Fucα1,6)GlcNAc-антитела к CLDN6 (H1L1) с концентрацией 19,2 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1 (4,8 мл), получая раствор антитело к CLDN6 (H1L1)-[MSG1-Т3]2 с концентрацией 10,2 мг/мл (в фосфатно-солевом буфере (рН 6,0)) (7,2 мл).
[0763]
Пример 62: Ремоделирование сахарной цепи 5 (CLDN6-MSG1 (H2L2))
[Формула 186]
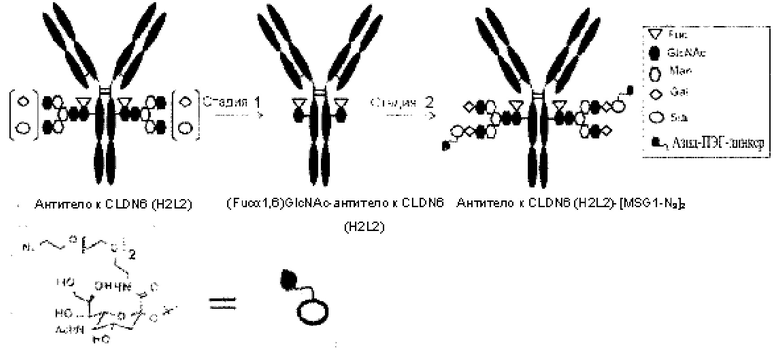
Стадия 1: (Fucα1,6)GlcNAc-антитело к CLDN6 (H2L2)
Операции, аналогичные представленным на стадии 1 примера 58, проводили с применением раствора антитела к CLDN6 с концентрацией приблизительно 20 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола), полученного в примере 136 (6 мл), получая раствор (5,7 мл) (Fucα1,6) GlcNAc-антитела к CLDN6 (H2L2) с концентрацией 21,84 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)).
[0764]
Стадия 2: Антитело к CLDN6 (H2L2)-[MSG1-N3]2
Операции, аналогичные представленным на стадии 1 примера 60, проводили с применением раствора (5,7 мл) (Fucα1,6)GlcNAc-антитела к CLDN6 (H2L2) с концентрацией 21,8 мг/мп (в 50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1, получая раствор (11,1 мл) антитело к CLDN6 (H2L2)-[MSG1-N3]2 с концентрацией 10,2 мг/мл (в фосфатно-солевом буфере (рН 6,0)).
[0765]
Пример 63: Ремоделирование сахарной цепи 6 (CLDN6-MSG1 (H1L3))
[Формула 187]
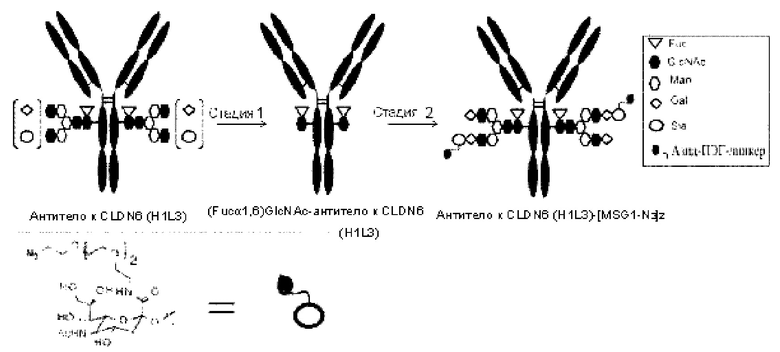
Стадии 1: (Fucα1,6) GlcNAc-антитело к CLDN6 (H1L3)
Операции, аналогичные представленным на стадии 1 примера 58, проводили с применением раствора (3 мл) антитела к CLDN6 с концентрацией приблизительно 39,4 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола), полученного в примере 136, получая раствор (4,5 мл) (Fucα1,6)GlcNAc-антитела к CLDN6 (H1L3) с концентрацией 39,2 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)).
[0766]
Стадия 2: Антитело к CLDN6 (H1L3)-[MSG1-N3]2
Операции, аналогичные представленным на стадии 1 примера 60, проводили с применением раствора (4,5 мл) (Fucα1,6)GlcNAc-антитела к CLDN6 (H1L3) с концентрацией 39,2 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1, получая раствор (7,2 мл) антитела к CLDN6 (H1L3)-[MSG1-N3]2 с концентрацией 9,83 мг/мл (в фосфатно-солевом буфере (рН6,0)).
[0767]
Пример 64: Ремоделирование сахарной цепи 7 (CD98-MSG1)
[Формула 188]
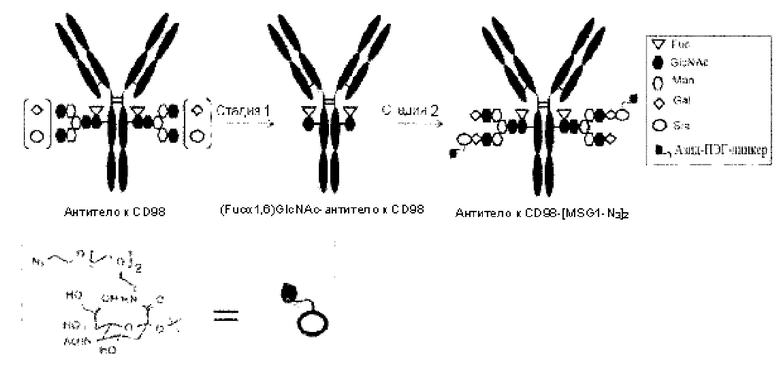
Стадия 1: (Fucα1,6)GlcNAc-антитело к CD98
Операции, аналогичные представленным на стадии 1 примера 58, проводили с применением раствора (6 мл) антитела к CD98 с концентрацией приблизительно 20 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола), полученного в сравнительном примере 6, получая раствор (4,7 мл) (Fucα1,6)GlcNAc-антитела к CD98 с концентрацией 21,7 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)).
[0768]
Стадия 2: Антитело к CD98-[MSG1-N3]2
Операции, аналогичные представленным на стадии 1 примера 60, проводили с применением раствора (4,7 мл) (Fucα1,6) GlcNAc-антитела к CD98 с концентрацией 21,7 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)), полученный на стадии 1, получая раствор (7,6 мл) антитело к CD98-[MSG1-N3]2 с концентрацией 10,1 мг/мл (в фосфатно-солевом буфере (рН6,0)).
[0769]
Пример 65: Ремоделирование сахарной цепи 8 (TROP2-MSG1)
[Формула 189]
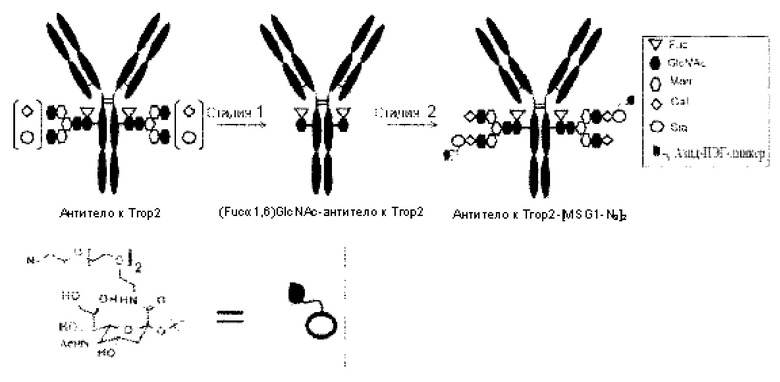
Стадия 1: (Fucα1,6)GlcNAc-антитело к Trop2
Операции, аналогичные представленным на стадии 1 примера 58, проводили с применением раствора (6 мл) антитела к Trop2 с концентрацией приблизительно 20 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола), полученного в сравнительном примере 5, получая раствор (3,3 мл) (Fucα1,6) GlcNAc-антитела к Trop2 с концентрацией 21,69 мг/мл (в 50 мМ фосфатного буф ера (рН 6,0)).
[0770]
Стадия 2: Антитело к Trop2-[MSG1-N3]2
Операции, аналогичные представленным на стадии 1 примера 60, проводили с применением раствора (3,35 мл) (Fucα1,6) GlcNAc-антитела к Trop2 с концентрацией 21,69 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1, получая раствор (6,4 мл) антитело к Trop2-[MSG1-N3]2 с концентрацией 10,3 мг/мл (в фосфатно-солевом буфере (рН 6,0)).
[0771]
Пример 66: Ремоделирование сахарной цепи 9 (LPS-MSG1)
[Формула 190]
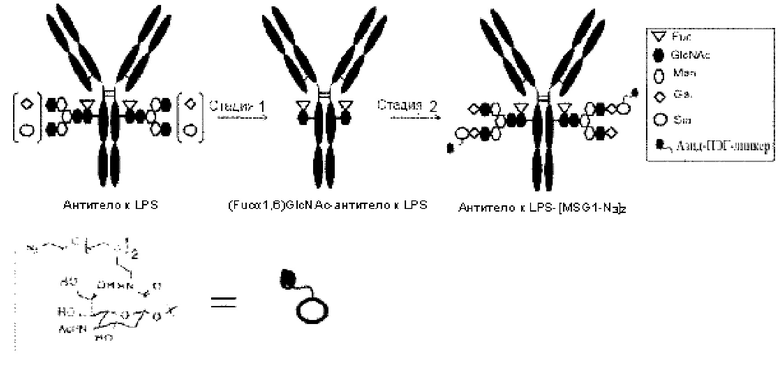
Стадия 1: (Fucα1,6) GlcNAc-антитело к LPS
Операции, аналогичные представленным на стадии 1 примера 58, проводили с применением раствора (6,6 мл) антитела к LPS с концентрацией приблизительно 17 мг/мл (в 25 мМ раствора гистидина (рН 6,0), 5% раствора сорбитола), полученного в сравнительном примере 4, получая раствор (5,4 мл) (Fucα1,6)GlcNAc-антитела к LPS с концентрацией 21,03 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)).
[0772]
Стадия 2: Антитело к LPS-[MSG1-N3]2
Операции, аналогичные представленным на стадии I примера 60, проводили с применением раствора (5,4 мл) (Fucα1,6)GlcNAc-антитела к LPS с концентрацией 21,03 мг/мл (в 50 мМ фосфатного буфера (рН 6,0)), полученного на стадии 1, получая раствор (7,9 мл) антитело к LPS-[MSG1-N3)2 с концентрацией 9,89 мг/мл (в фосфатно-солевом буфере (рН6,0)).
[0773]
[Синтез ADC]
ADCs, описанных в примерах 67-71, 77-80, 82-88, 92-95, 109-114 и 120, синтезировали, как показано на следующих схемах реакций, путем конъюгирования антитела, полученного на стадии 1 примера 59, с лекарственным средством-линкером. В представленной формуле R отличается в зависимости от лекарственного средства-линкера, применяемого в указанных примерах.
[Формула 191]
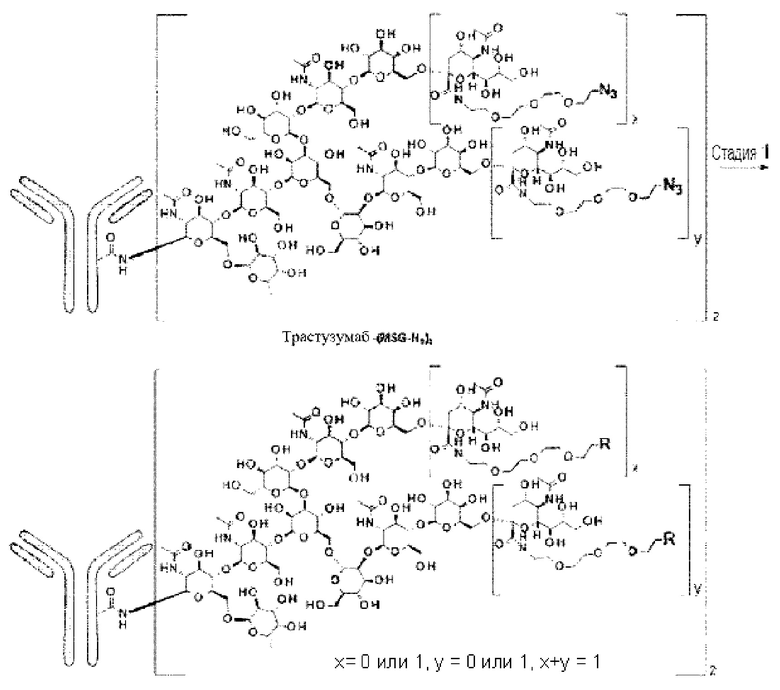
ADCs, описанные в примерах 72, 73, 75 и 91, синтезировали, как показано на следующих схемах реакций, путем коньюгирования антитела, полученного на стадии 2 примера 58, с лекарственным средством-линкером. В представленной формуле R отличается в зависимости от лекарственного средства-линкера, применяемого в указанных примерах.
[Формула 192]
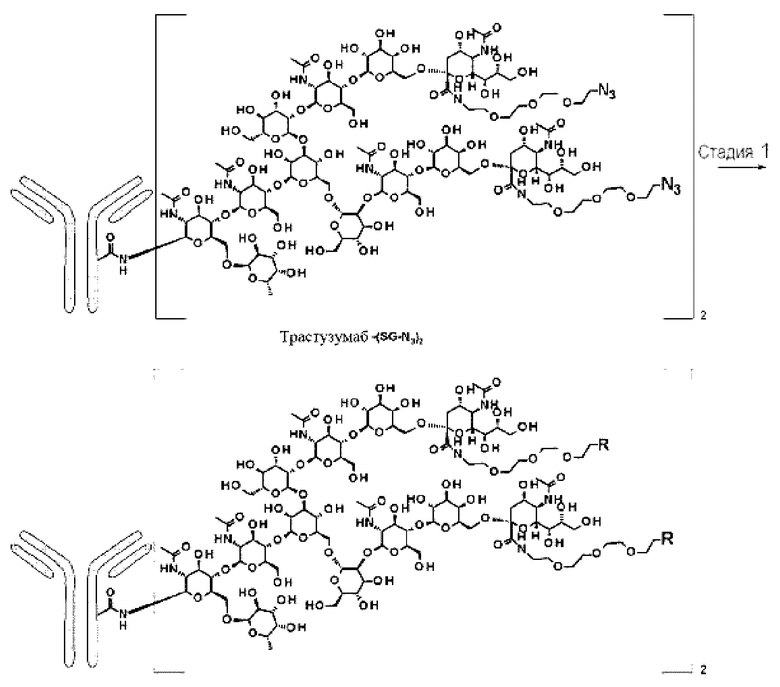
ADCs, описанные примерах 74, 81, 89, 90, 96-105, 115 и 118, синтезировали, как показано на следующих схемах реакций, путем конъюгирования антитела, полученного на стадии 1 примера 60, с лекарственным средством-линкером. В представленной формуле группа R отличается в зависимости от лекарственного средства-линкера, применяемого в указанных примерах.
[Формула 193]
ИЛИ
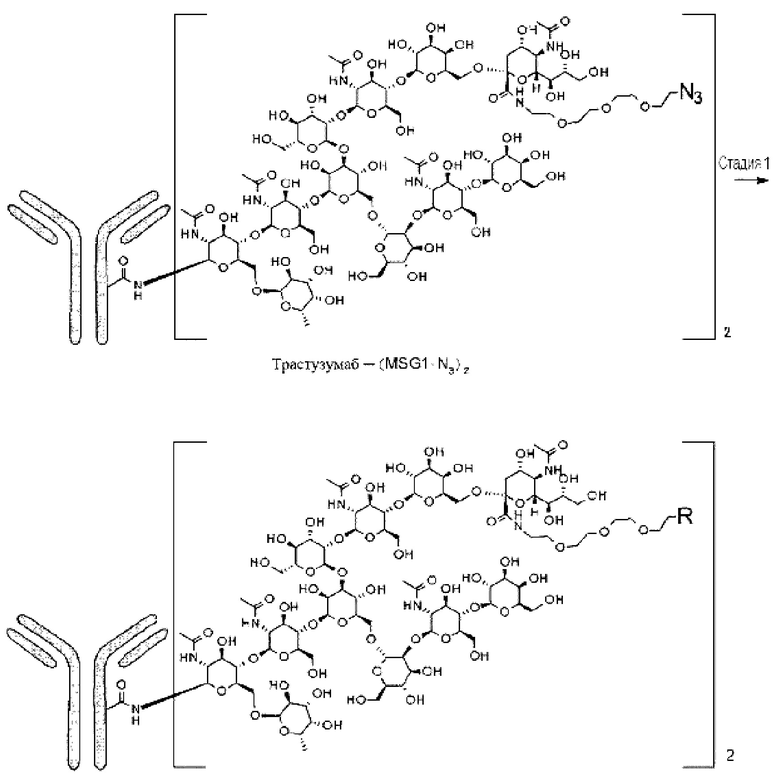
[0774]
Пример 67: ADC1
[Формула 194]
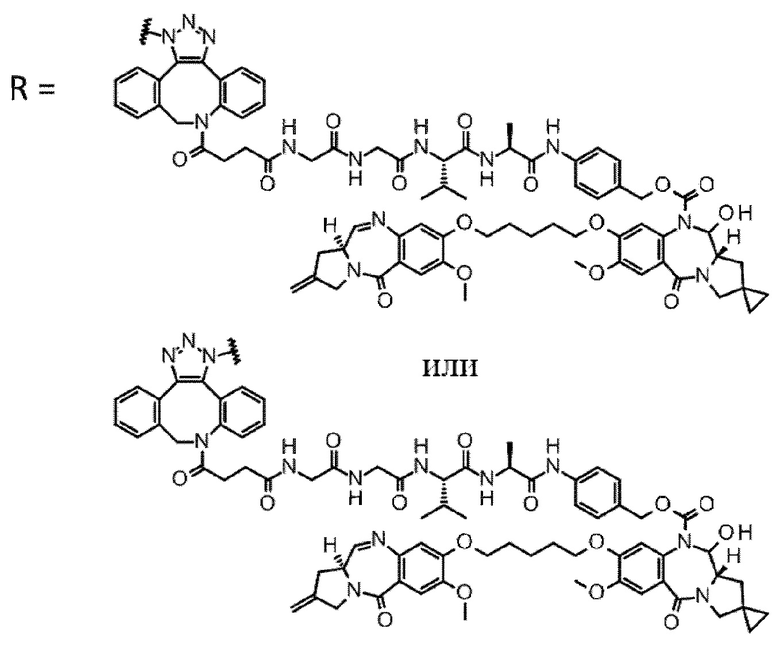
Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, а соединение, полученное на стадии 1 примера 67, содержит линкер в виде смеси двух структур, показанных выше как R.
[0775]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученному на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 24 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 14,00 мл раствора желаемого соединения. Данный раствор концентрировали путем применения общей операции А, получая 0,75 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 11,4 мг/мл, выход антител: 8,56 мг (86%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0776]
Пример 68: ADC2
[Формула 195]
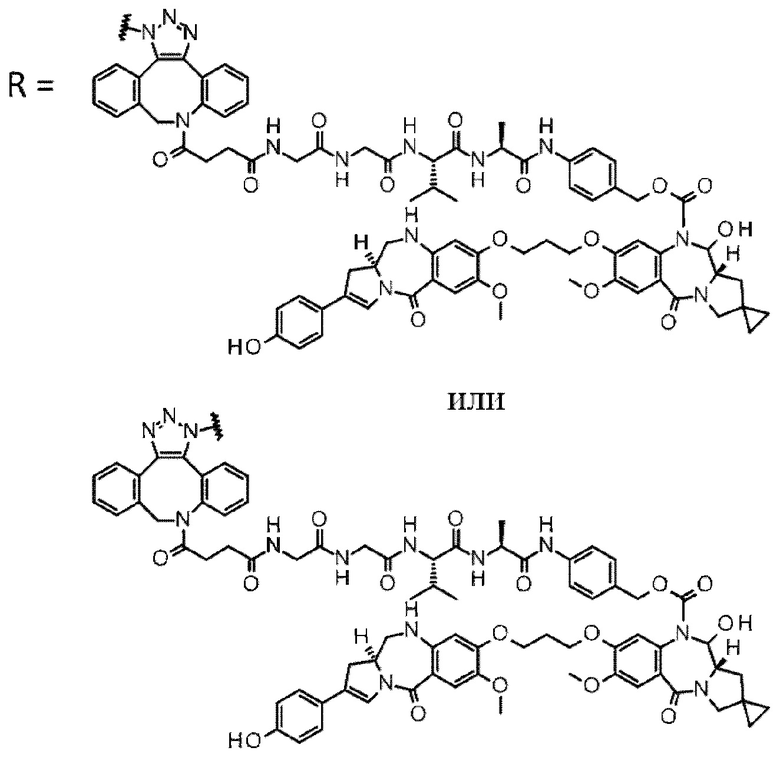
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 68, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0777]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 14 примера 25 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,48 мг/мл, выход антител: 8,88 мг (89%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0778]
Пример 69: ADC3
[Формула 196]
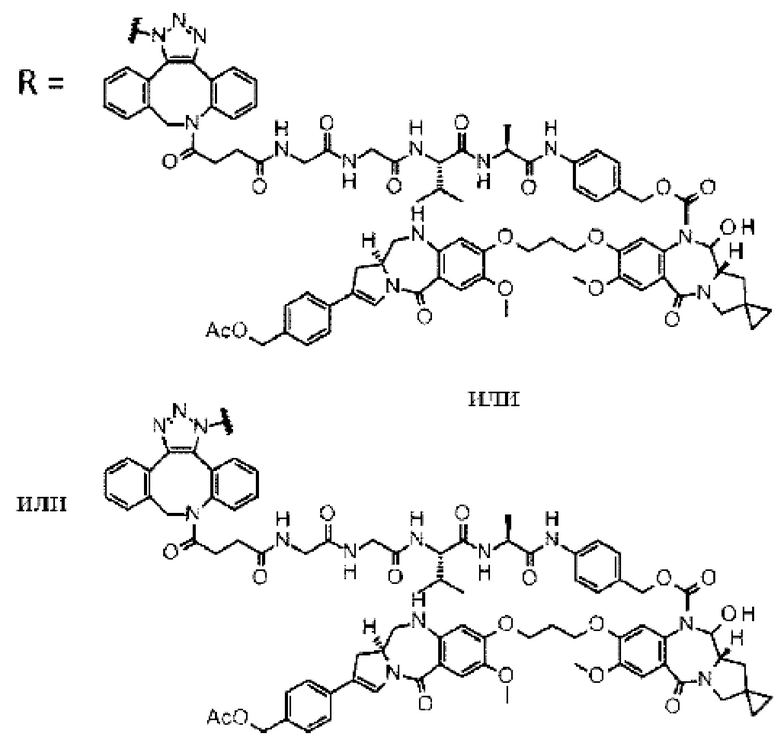
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 69, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0779]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 14 примера 26 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,45 мг/мл, выход антител: 8,67 мг (89%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0780]
Пример 70: ADC4
[Формула 197]
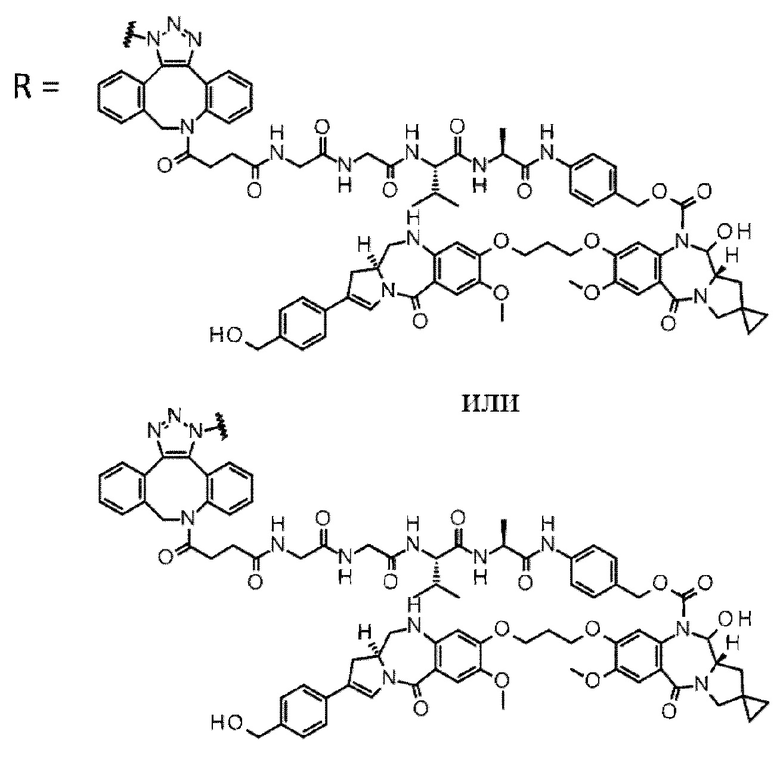
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 70, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0781]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 27 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,30 мг/мл, выход антител: 7,80 мг (78%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0782]
Пример 71: ADC5
[Формула 198]
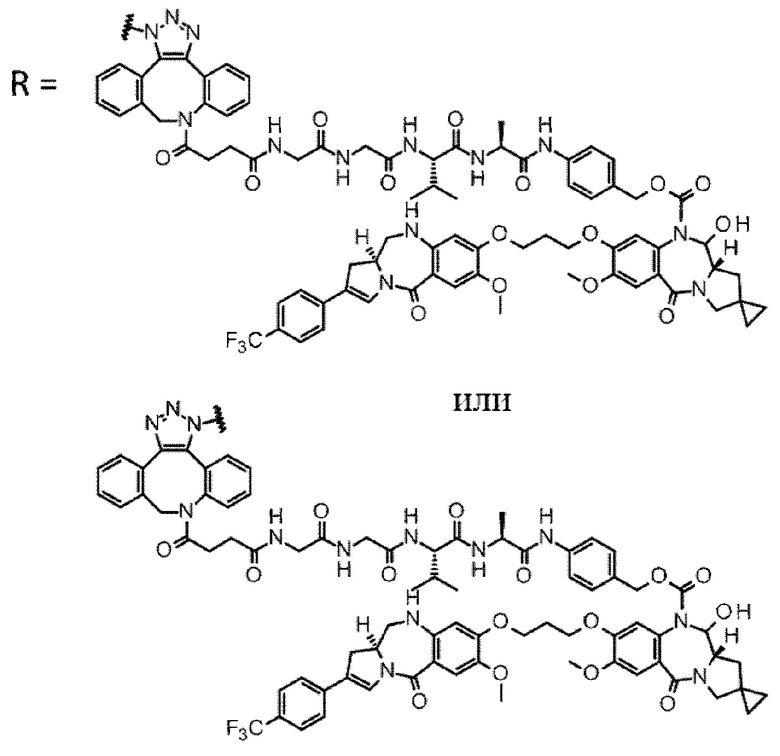
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 71, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0783]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 28 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,08 мг/мл, выход антител: 6,48 мг (65%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,6
[0784]
Пример 72: ADC6
[Формула 199]
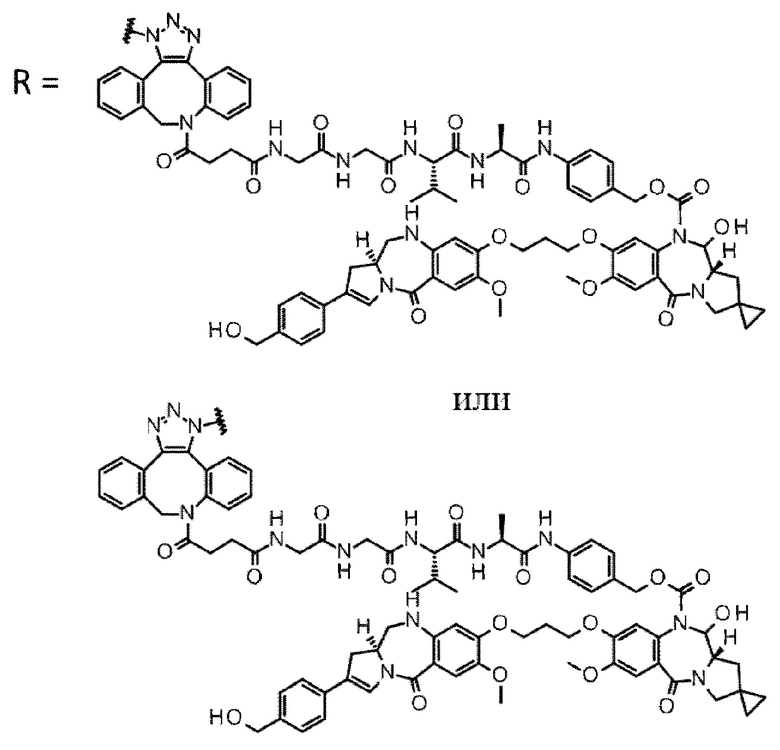
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 72, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0785]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 2 примера 58, добавляли 1,2-пропандиол (0,835 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 27 (0,165 мл; 24 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 4,50 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,75 мг/мл, выход антител: 7,86 мг (79%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 3,8
[0786]
Пример 73: ADC7
[Формула 200]
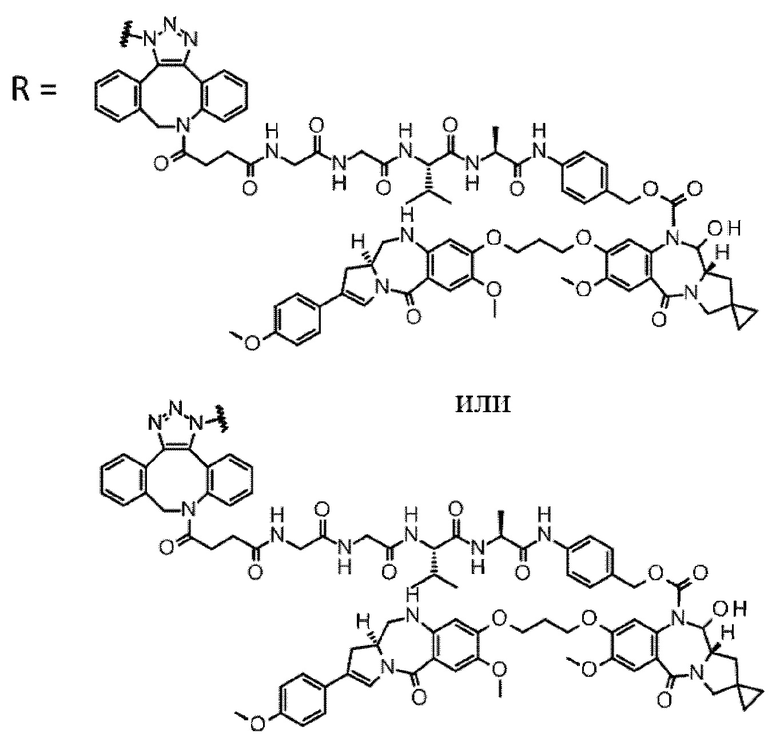
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 73, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0787]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 2 примера 58, добавляли 1,2-пропандиол (0,835 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 4 (0,165 мл; 24 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 4,50 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,66 мг/мл, выход антител: 7,48 мг (75%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 3,8
[0788]
Пример 74: ADC8
[Формула 201]
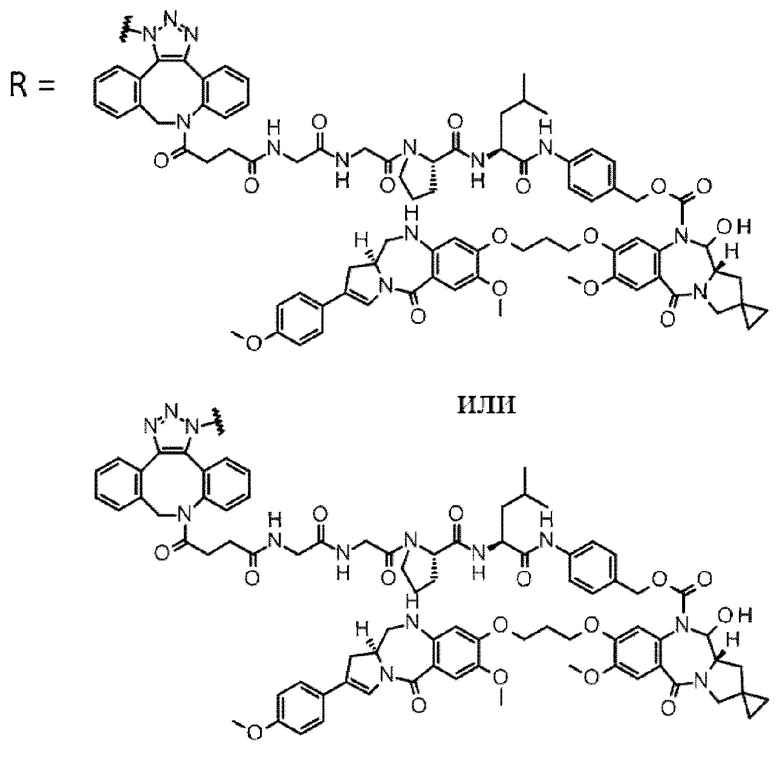
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 74, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0789]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 14 примера 29 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,36 мг/мл, выход антител: 8,17 мг (82%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0790]
Пример 75: ADC9
[Формула 202]
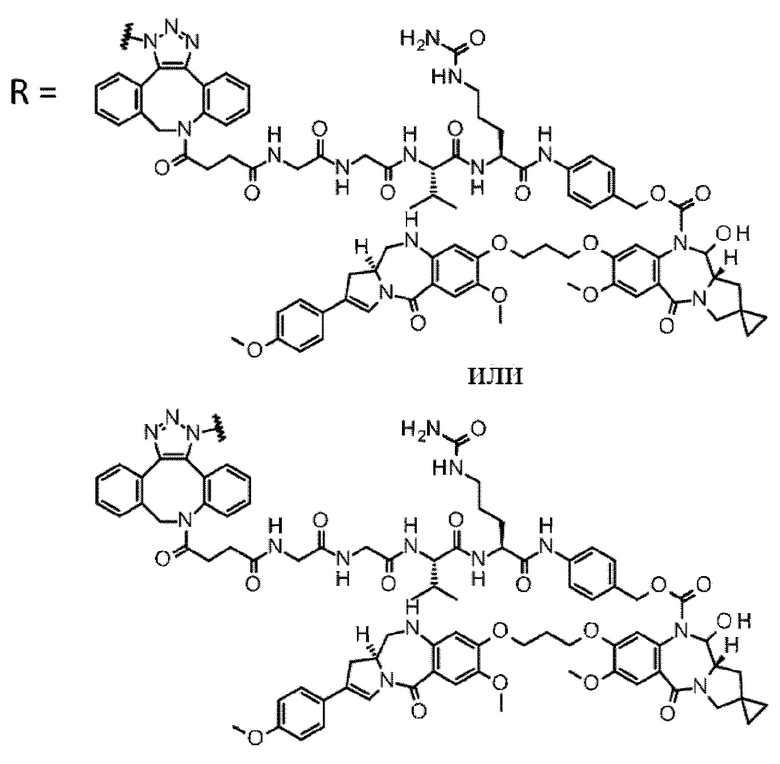
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 75, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0791]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 2 примера 58, добавляли 1,2-пропандиол (0,835 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 9 примера 9 (0,165 мл; 24 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 8,50 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 0,86 мг/мл, выход антител: 7,35 мг (73%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 3,6
[0792]
Пример 76: ADC10
[Формула 203]
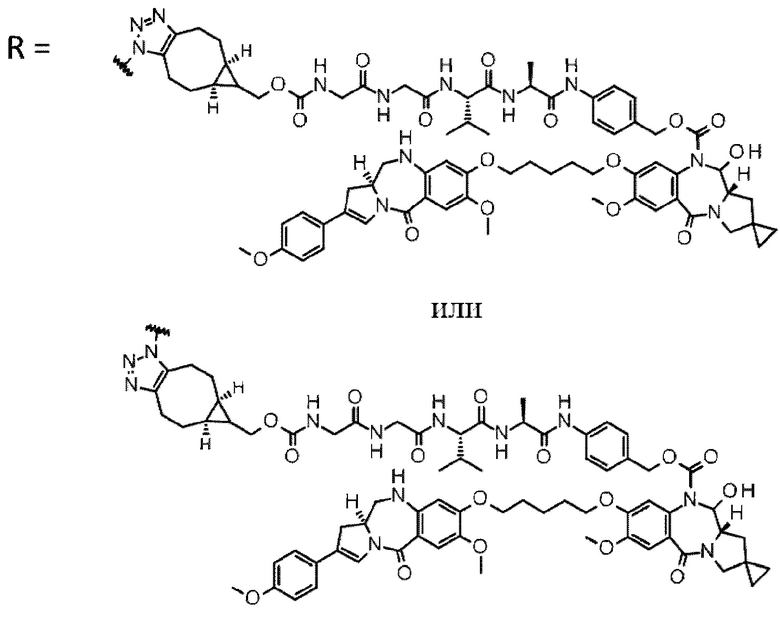
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 76, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0793]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
Как показано в формуле реакции в примере 106, к раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 0,400 мл), полученного на стадии 2 примера 61, добавляли 1,2-пропандиол (0,200 мл), 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 2 примера 30 (0,0549 мл; 20 эквивалентов на молекулу антитела) и диметилсульфоксид (0,145 мл) при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 72 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 2,50 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,19 мг/мл, выход антител: 2,98 мг (75%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0794]
Пример 77: ADC11
[Формула 204]
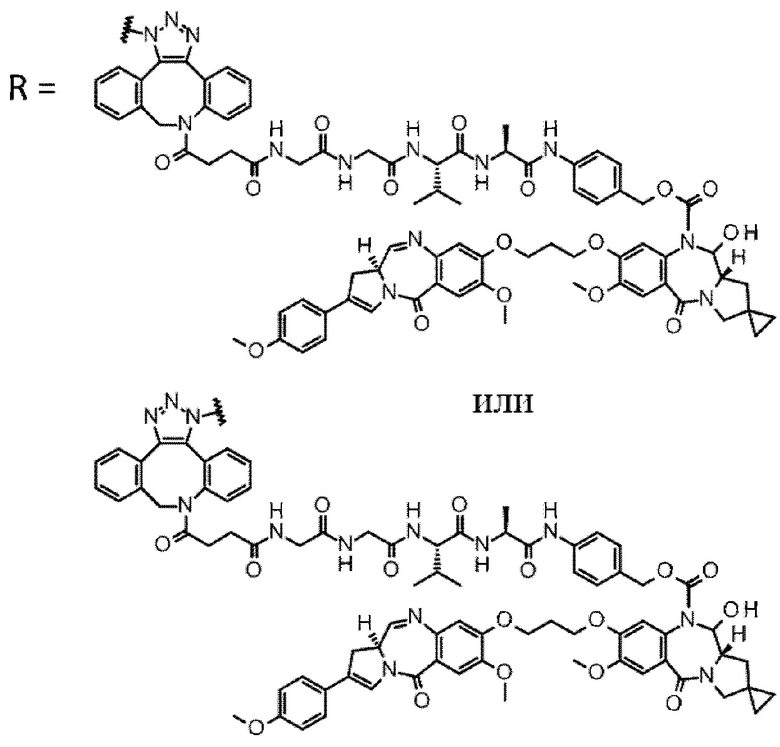
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 77, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0795]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,88 мг/мл, 0,500 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,459 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 19 (0,0408 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D и полученный раствор концентрировали путем применения общей операции А, получая 0,470 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 8,31 мг/мл, выход антител: 3,90 мг (79%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0796]
Пример 78: ADC12
[Формула 205]
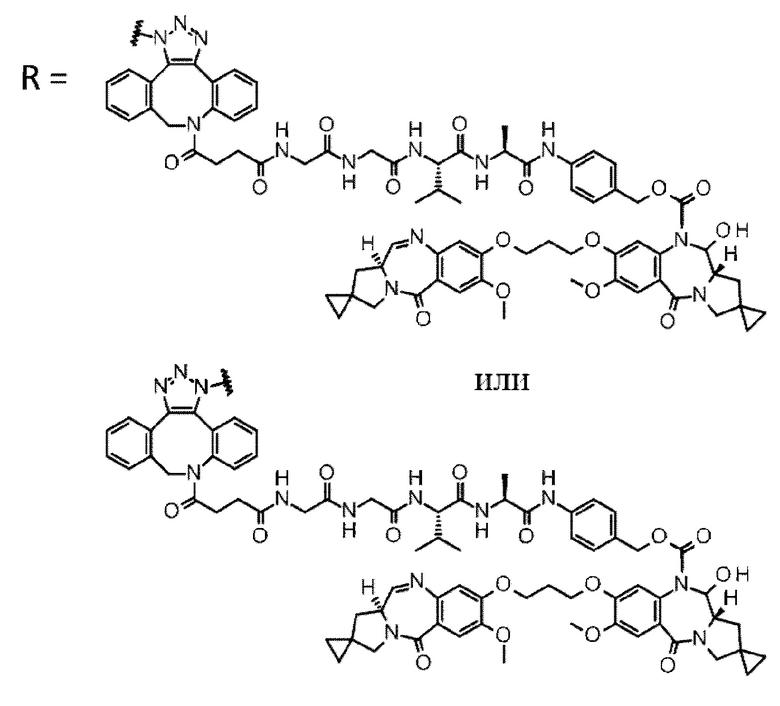
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 78, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0797]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 20 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D и полученный раствор затем концентрировали путем применения общей операции А, получая 0,75 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 8,70 мг/мл, выход антител: 6,94 мг (69%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,7
[0798]
Пример 79: ADC13
[Формула 206]
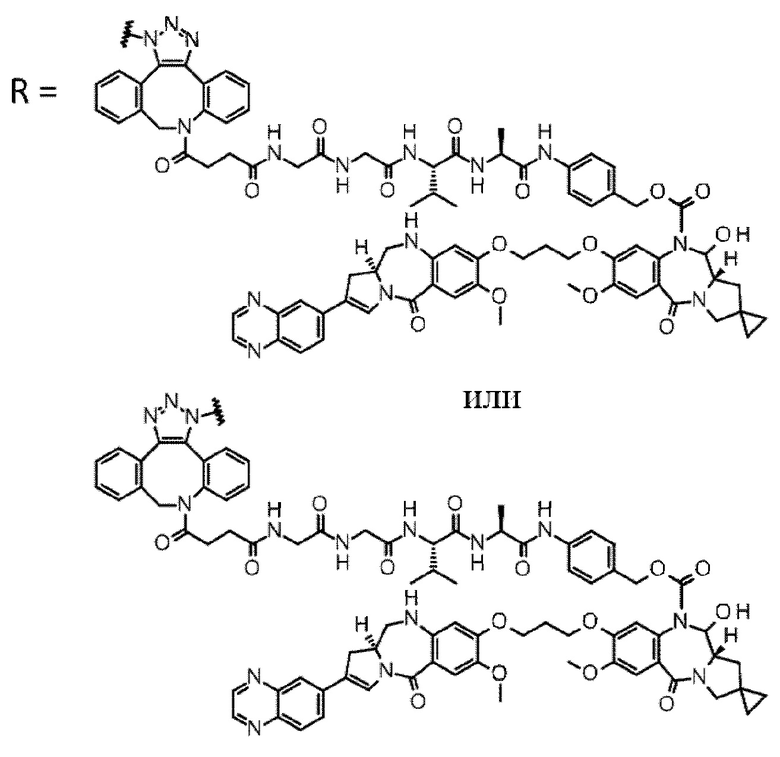
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 79, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0799]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 18 примера 21 (0,0825 мл; 12 эквивалентов на молекулу антитела), добавляли при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 0,96 мг/мл, выход антител: 5,77 мг (58%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0800]
Пример 80: ADC14
[Формула 207]
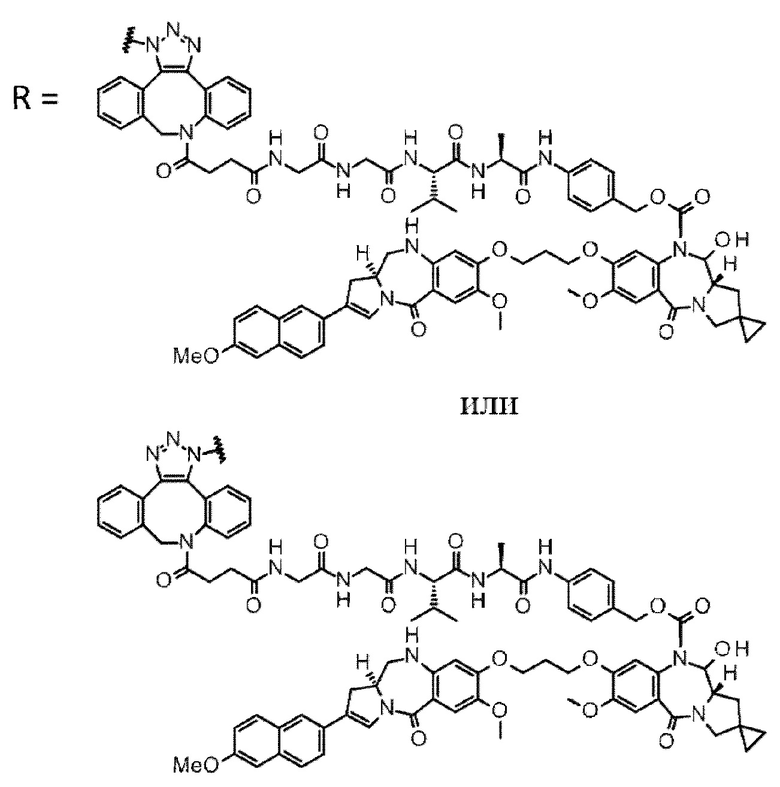
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 80, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0801]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 22 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,28 мг/мл, выход антител: 7,70 мг (77%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0802]
Пример 81: ADC15
[Формула 208]
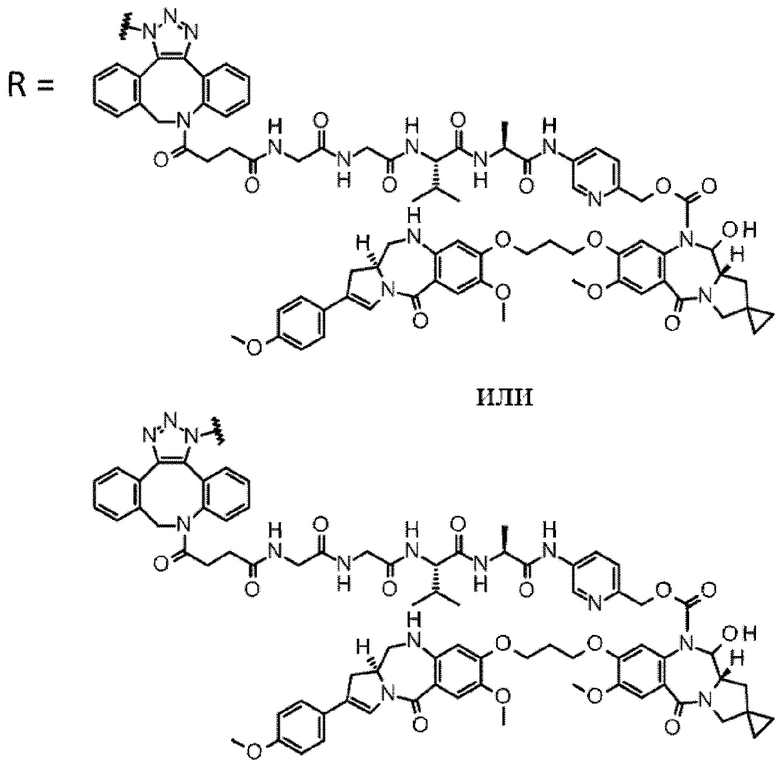
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 81, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0803]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 10 примера 23 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,60 мг/мл, выход антител: 9,60 мг (96%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0804]
Пример 82: ADC16
[Формула 209]
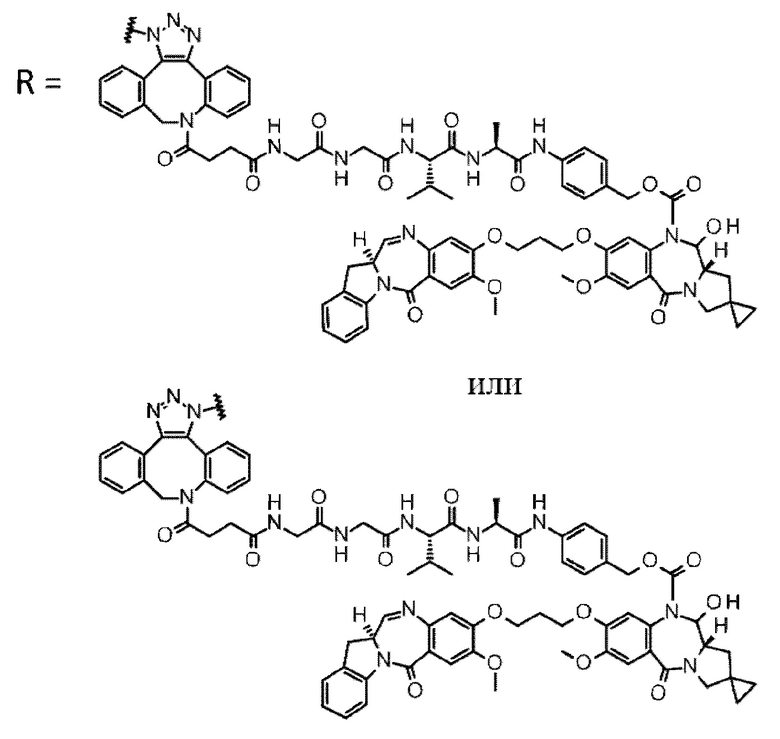
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 82, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0805]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,88 мг/мл, 0,500 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,459 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 11 примера 34 (0,0408 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 1 дня.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 10,5 мл раствора желаемого соединения. Данный раствор концентрировали путем применения общей операции А, получая 0,500 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 6,94 мг/мл, выход антител: 3,47 мг (70%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0806]
Пример 83: ADC17
[Формула 210]
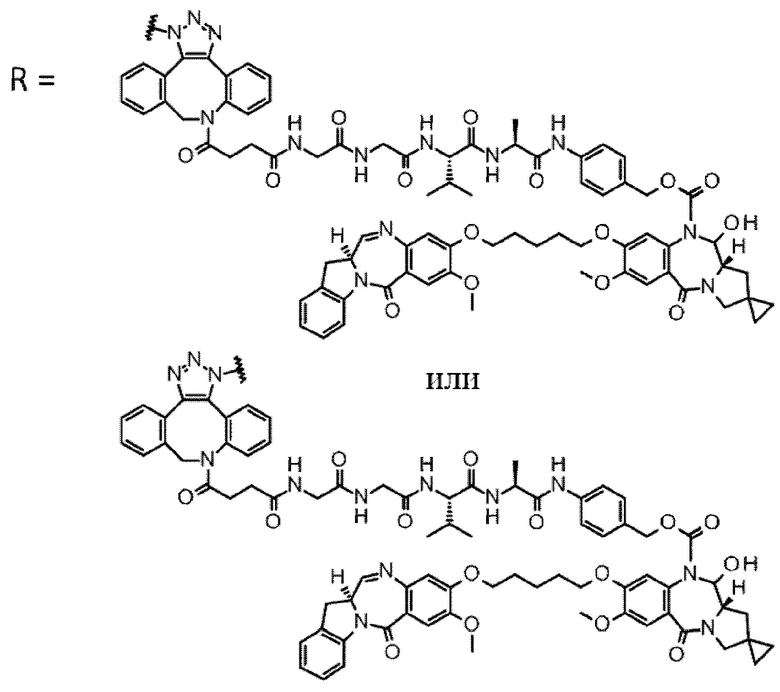
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 83, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0807]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,88 мг/мл, 0,500 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,459 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 4 примера 35 (0,0408 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 1 дня.
Операция очистки: Раствор очищали с помощью применения общей операции D и полученный раствор концентрировали путем применения общей операции А, получая 0,500 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 8,07 мг/мл, выход антител: 4,03 мг (82%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0808]
Пример 84: ADC18
[Формула 211]
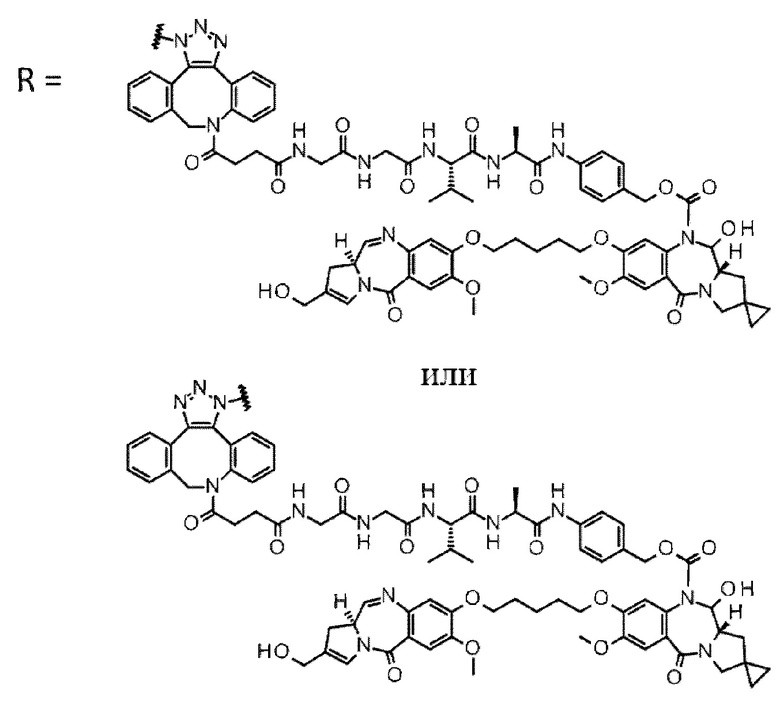
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 86, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0809]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 7 примера 36 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 1 дня.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 14,0 мл раствора желаемого соединения. Данный раствор концентрировали путем применения общей операции А, получая 0,700 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 12,9 мг/мл, выход антител: 9,00 мг (90%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0810]
Пример 85: ADC19
[Формула 212]
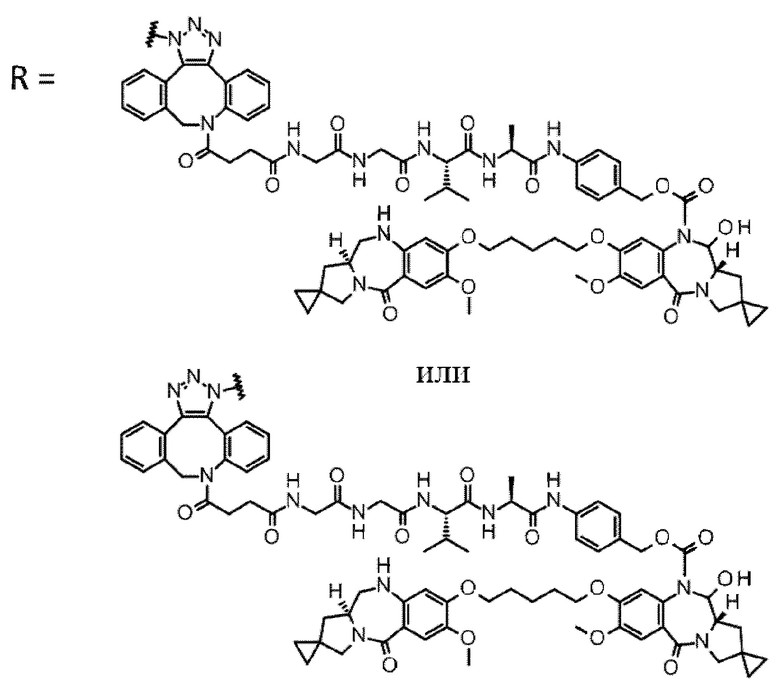
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 85, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0811]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 37 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,33 мг/мл, выход антител: 7,97 мг (80%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0812]
Пример 86: ADC20
[Формула 213]
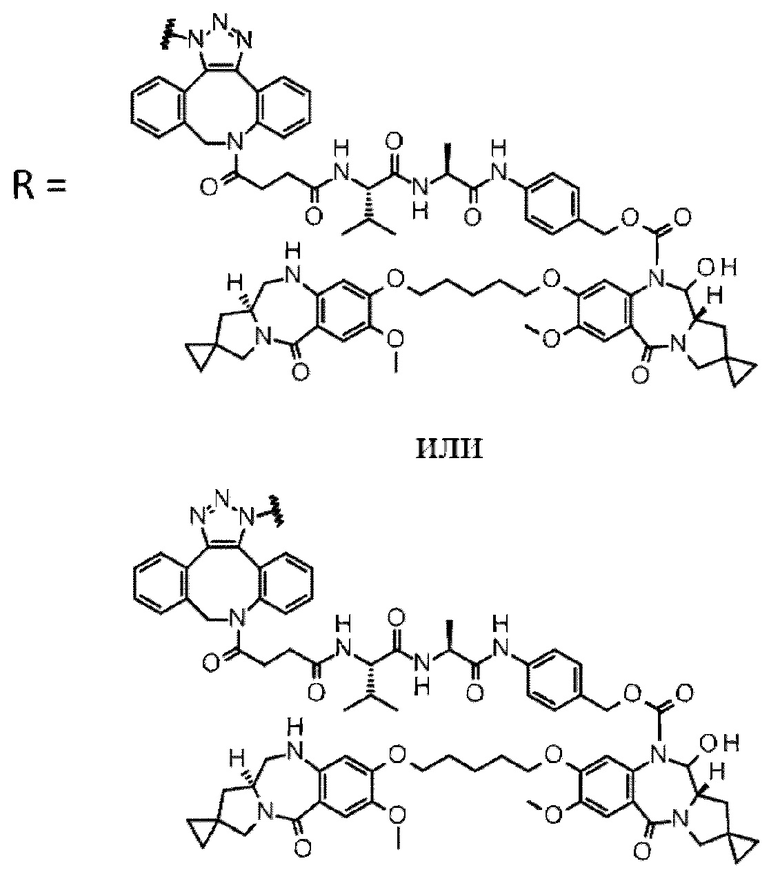
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 86, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0813]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 38 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,56 мг/мл, выход антител: 9,37 мг (94%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 2,0
[0814]
Пример 87: ADC21
[Формула 214]
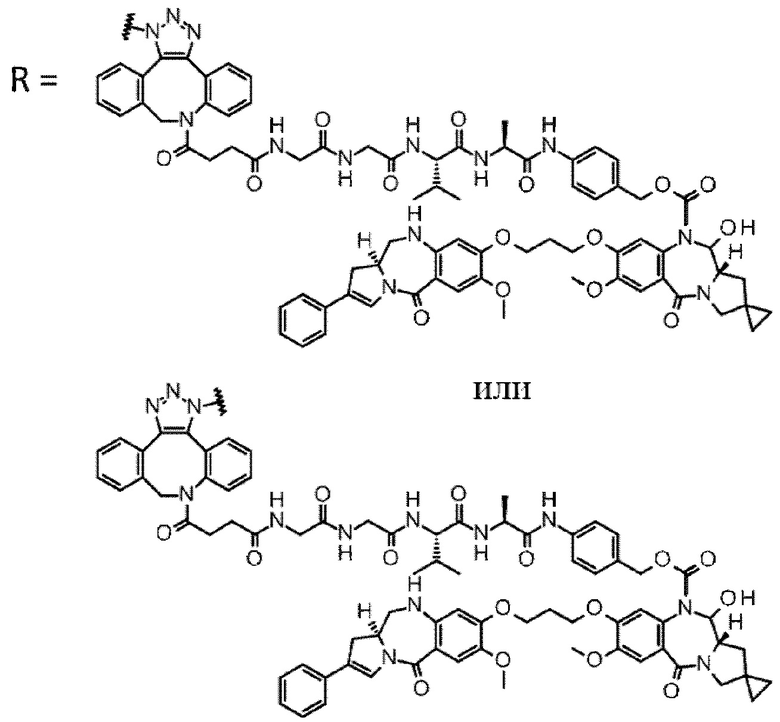
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 87, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0815]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 6 примера 39 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,89 мг/мл, выход антител: 11,4 мг (количественный выход), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0816]
Пример 88: ADC22
[Формула 215]
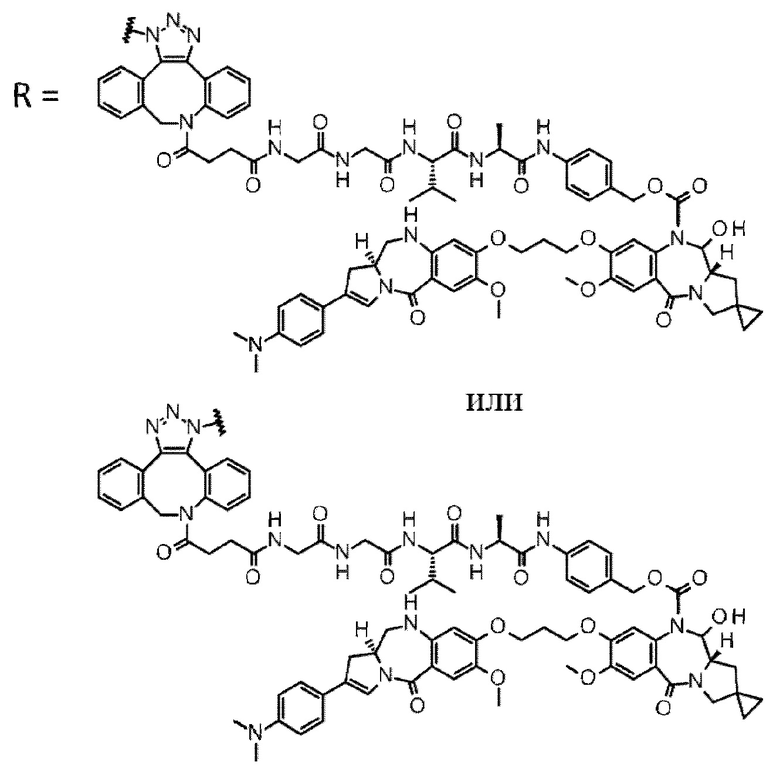
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное в примере 88, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0817]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 6 примера 40 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,47 мг/мл, выход антител: 8,84 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0818]
Пример 89: ADC23
[Формула 216]
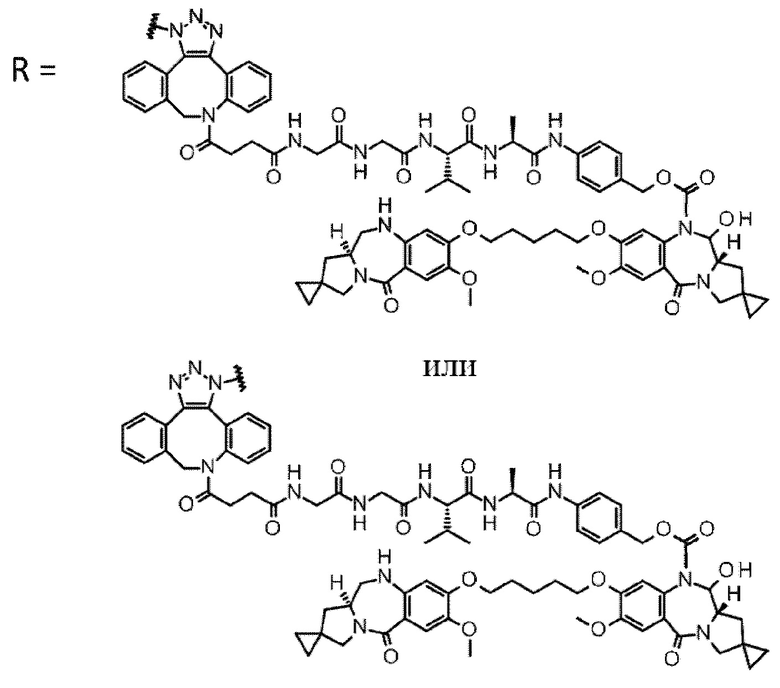
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 89, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0819]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 37 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,46 мг/мл, выход антител: 8,76 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0820]
Пример 90: ADC24
[Формула 217]
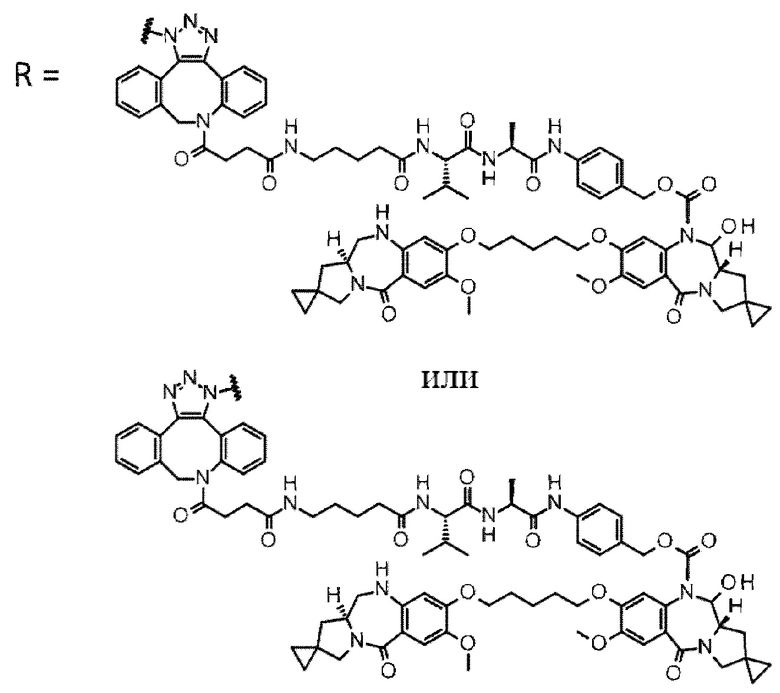
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 90, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0821]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 2 примера 41 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,53 мг/мл, выход антител: 9,17 мг (92%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0822]
Пример 91: ADC25
[Формула 218]
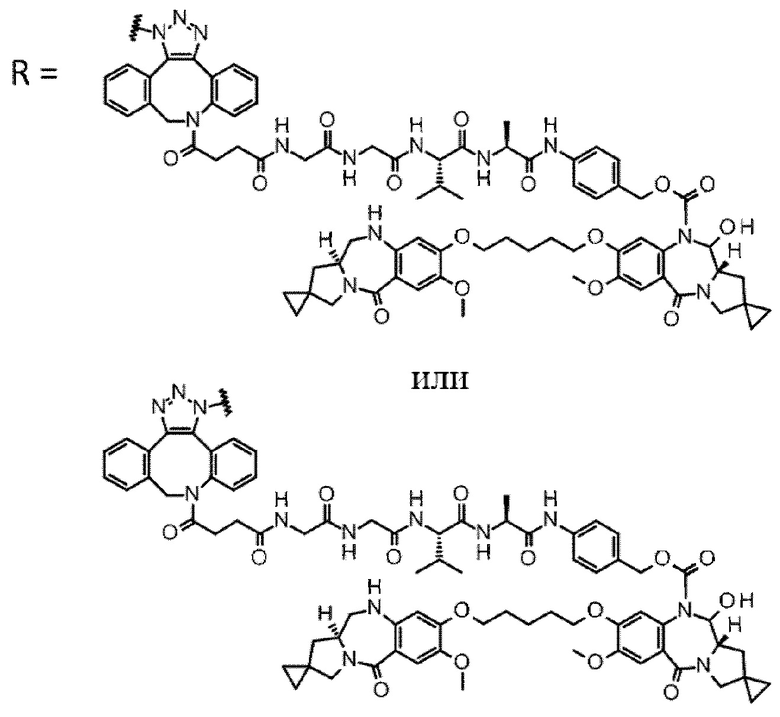
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное в примере 91, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0823]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 2 примера 58, добавляли 1,2-пропандиол (0,835 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 37 (0,165 мл; 24 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 10,5 мл раствора желаемого соединения. Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 0,73 мг/мл, выход антител: 7,70 мг (77%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 3,8
[0824]
Пример 92: ADC26
[Формула 219]
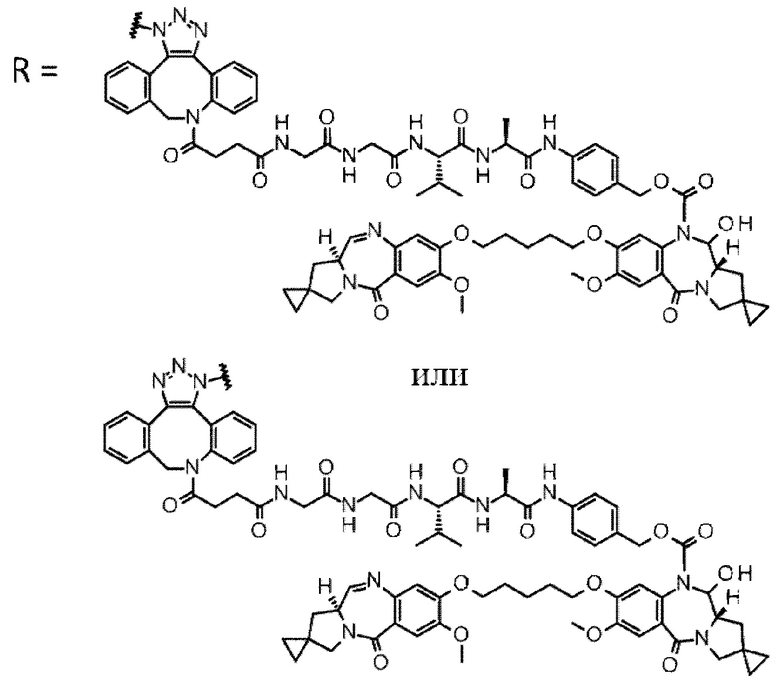
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 92, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0825]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,88 мг/мл, 0,500 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,459 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 10 примера 15 (0,0408 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 1 дня.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения. Данный раствор концентрировали путем применения общей операции А, получая 0,420 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 7,27 мг/мл, выход антител: 3,54 мг (72%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0826]
Пример 93: ADC27
[Формула 220]
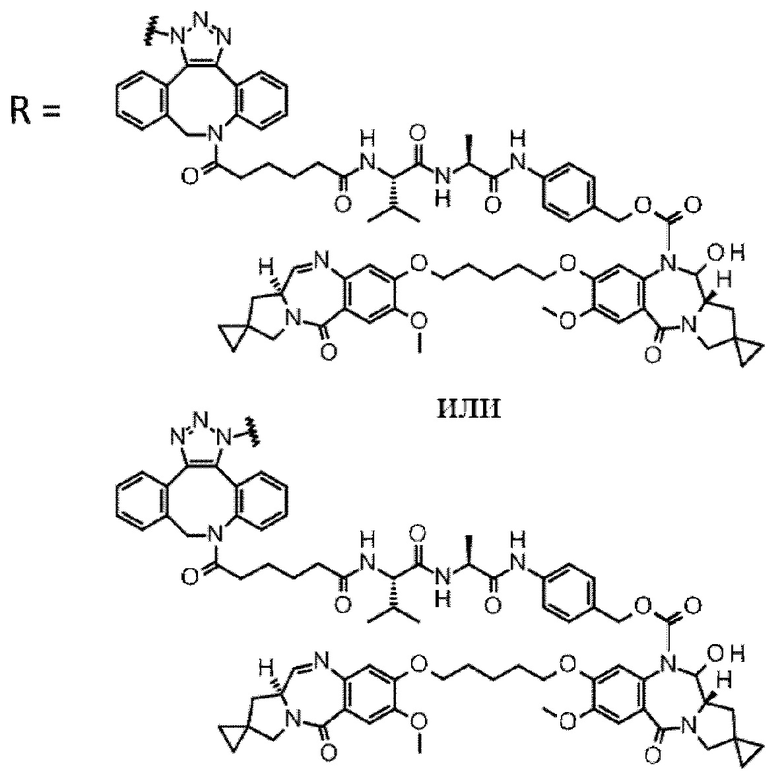
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 93, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0827]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,88 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 16 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 1 дня.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 10,5 мл раствора желаемого соединения. Данный раствор концентрировали путем применения общей операции А, получая 0,850 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 8,90 мг/мл, выход антител: 7,56 мг (77%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0828]
Пример 94: ADC28
[Формула 221]
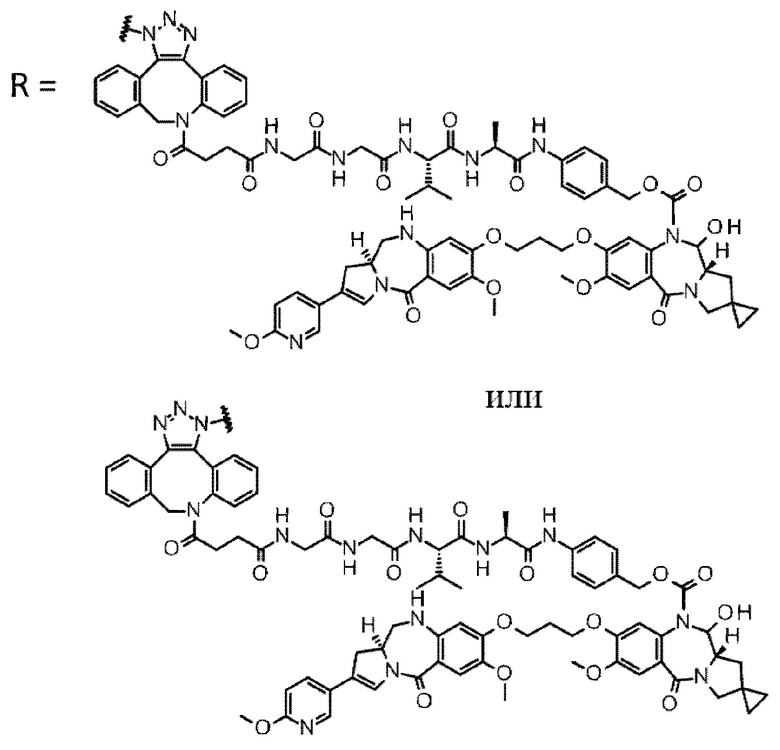
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 94, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0829]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 17 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,24 мг/мл, выход антител: 7,43 мг (73%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,5
[0830]
Пример 95: ADC29
[Формула 222]
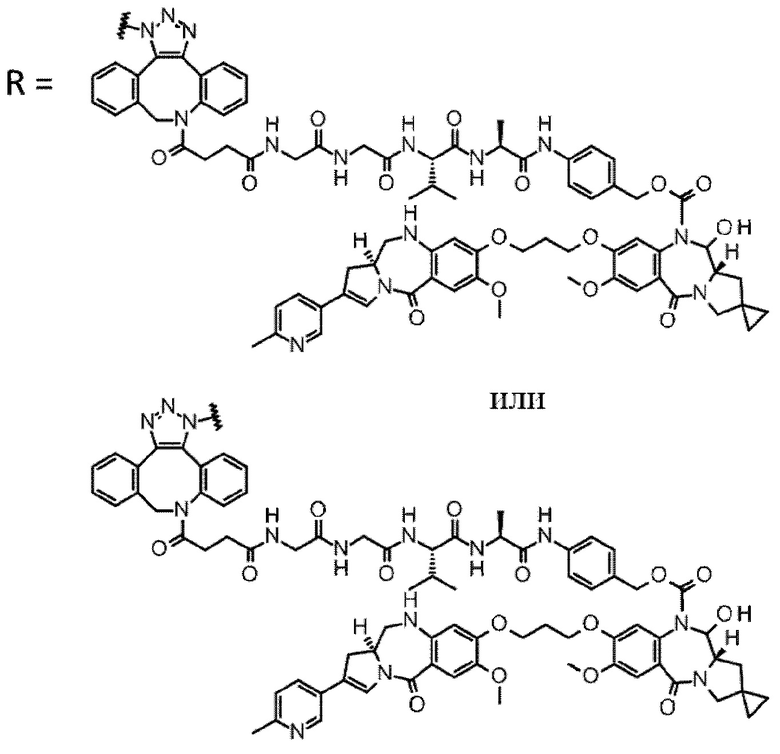
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 95, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0831]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 18 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,29 мг/мл, выход антител: 7,76 мг (76%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0832]
Пример 96: ADC30
[Формула 223]
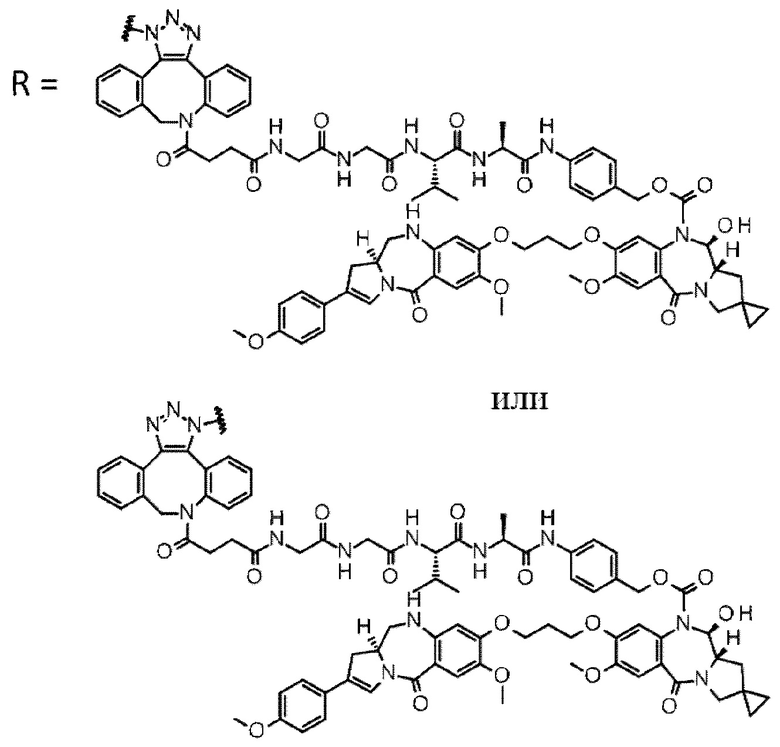
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 96, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0833]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 5,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (4,59 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 4 (0,413 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 30,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,30 мг/мл, выход антител: 38,9 мг (78%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0834]
Пример 97: ADC31
[Формула 224]
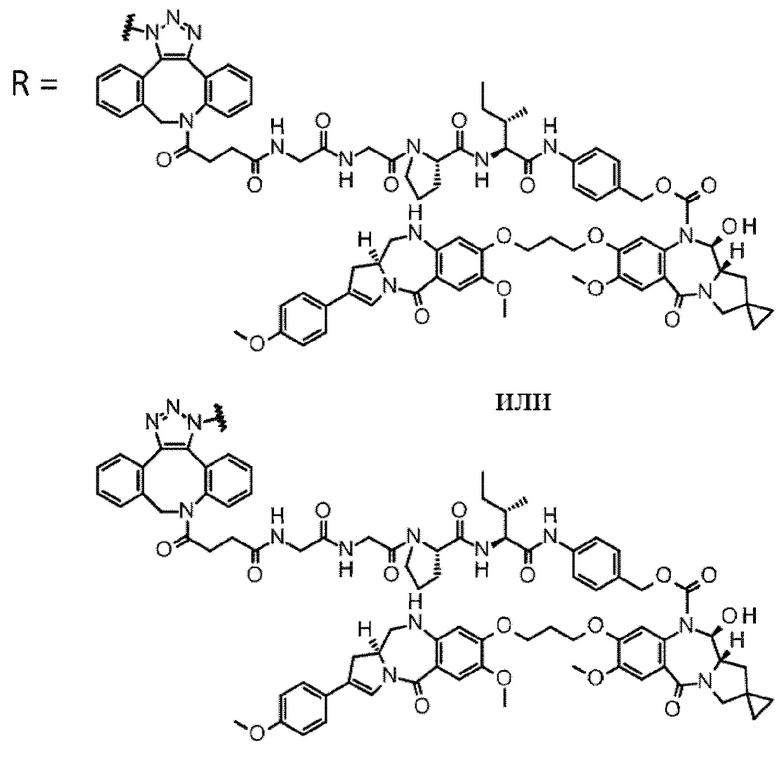
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 97, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0835]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 11 примера 5 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,47 мг/мл, выход антител: 8,82 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0836]
Пример 98: ADC32
[Формула 225]
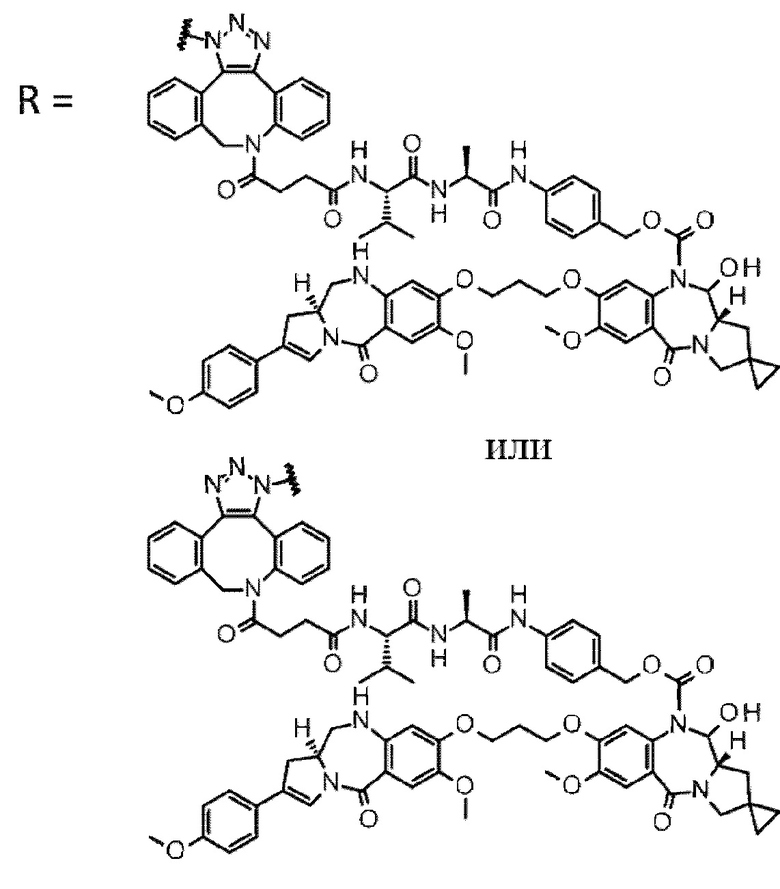
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 98, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0837]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 6 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,35 мг/мл, выход антител: 8,10 мг (81%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0838]
Пример 99: ADC33
[Формула 226]
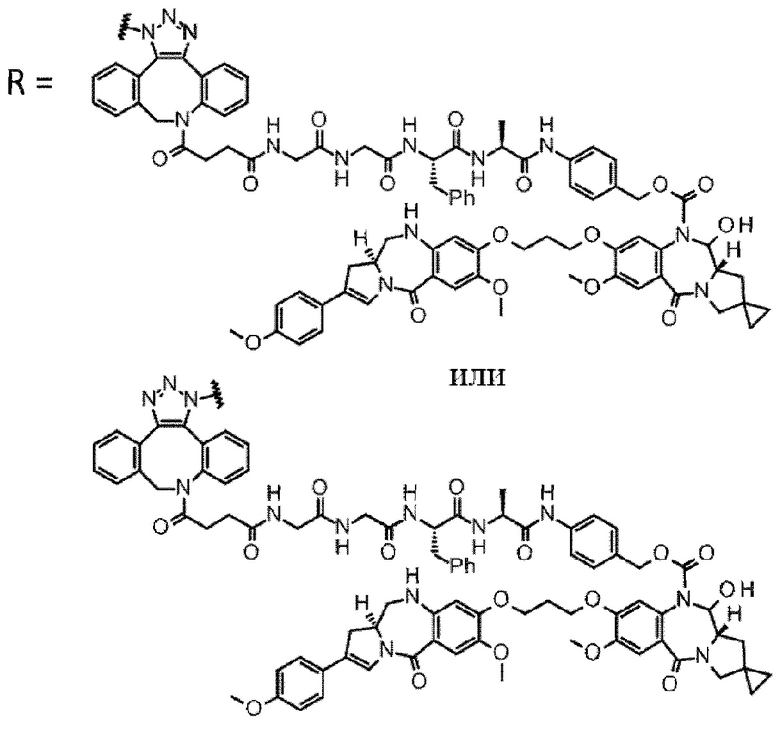
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 99, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0839]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 10 примера 7 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,41 мг/мл, выход антител: 8,44 мг (84%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0840]
Пример 100: ADC34
[Формула 227]
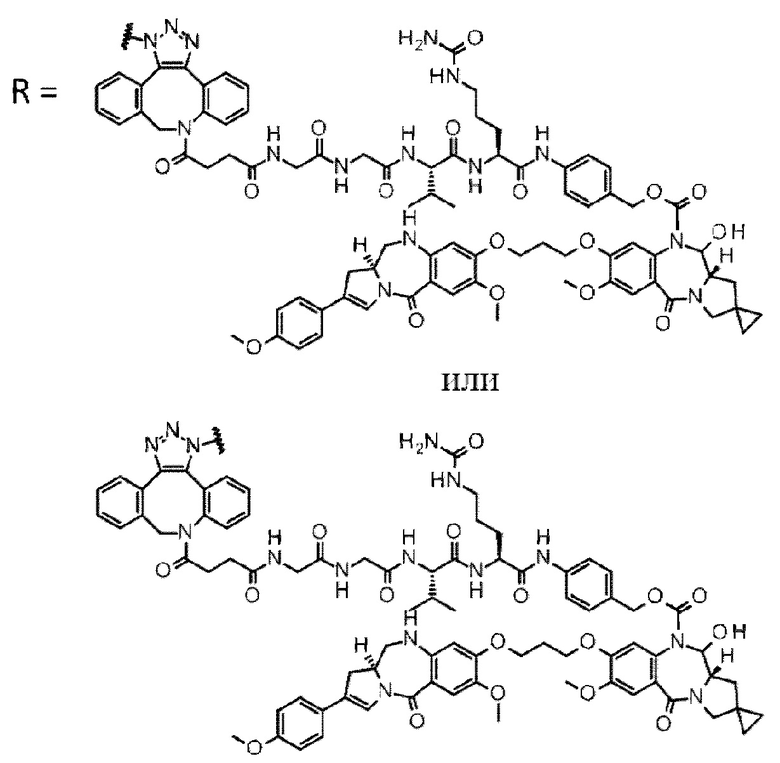
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 100, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0841]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 9 примера 9 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,47 мг/мл, выход антител: 8,79 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0842]
Пример 101: ADC35
[Формула 228]
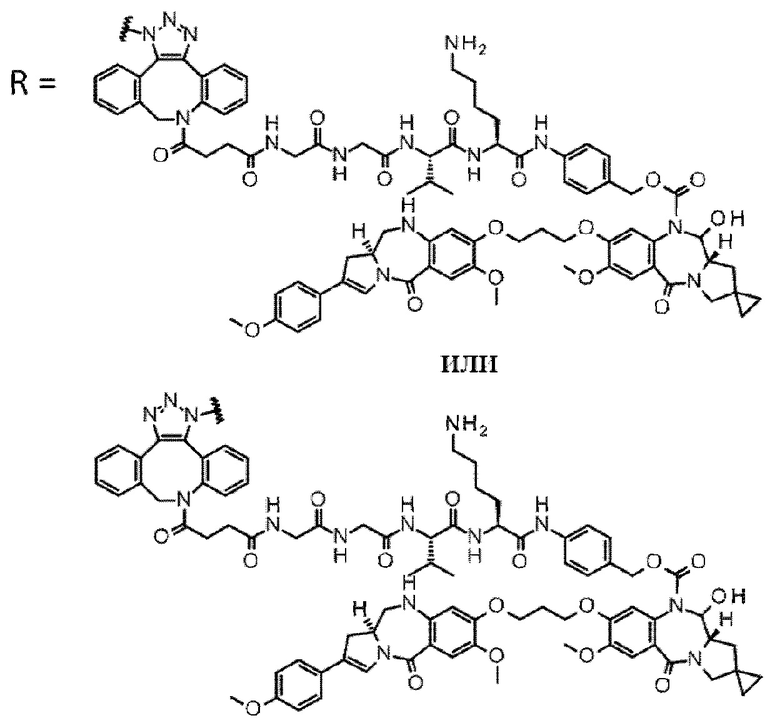
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 101, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0843]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 14 примера 10 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,67 мг/мл, выход антител: 10,0 мг (количественный выход), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0844]
Пример 102: ADC36
[Формула 229]
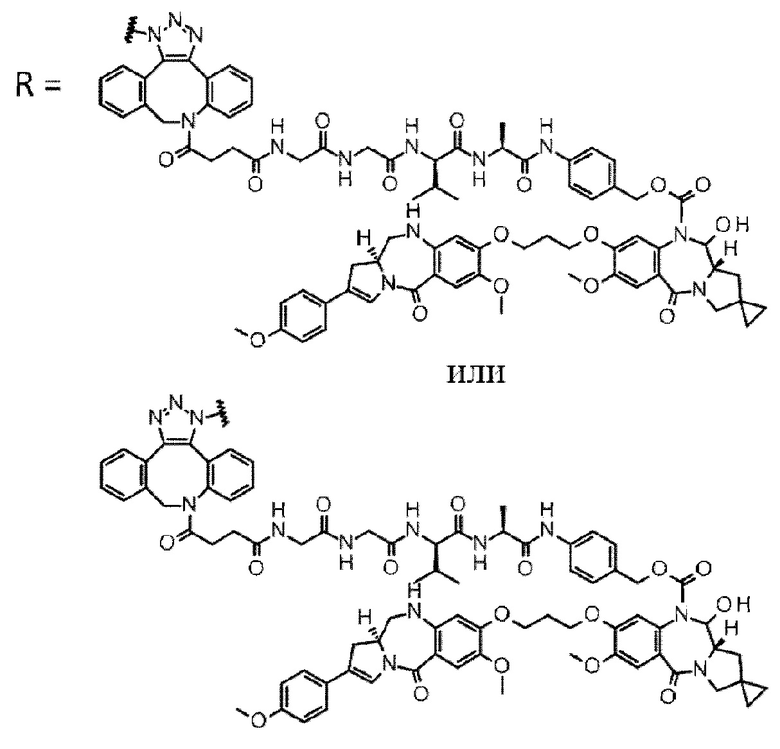
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 103, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0845]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 11 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,40 мг/мл, выход антител: 8,39 мг (84%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0846]
Пример 103: ADC37
[Формула 230]
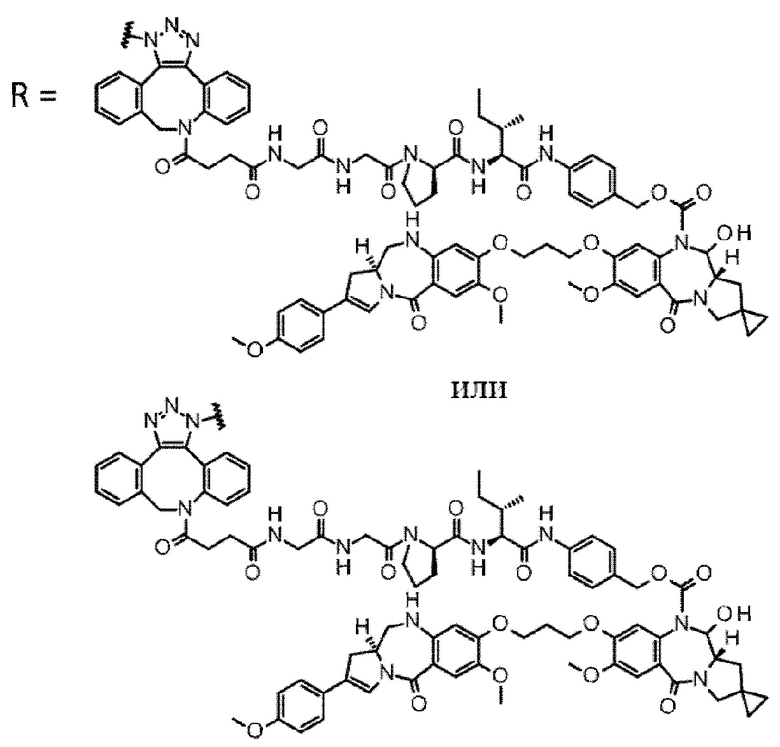
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 103, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0847]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 14 примера 12 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,41 мг/мл, выход антител: 8,49 мг (85%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0848]
Пример 104: ADC:38
[Формула 231]
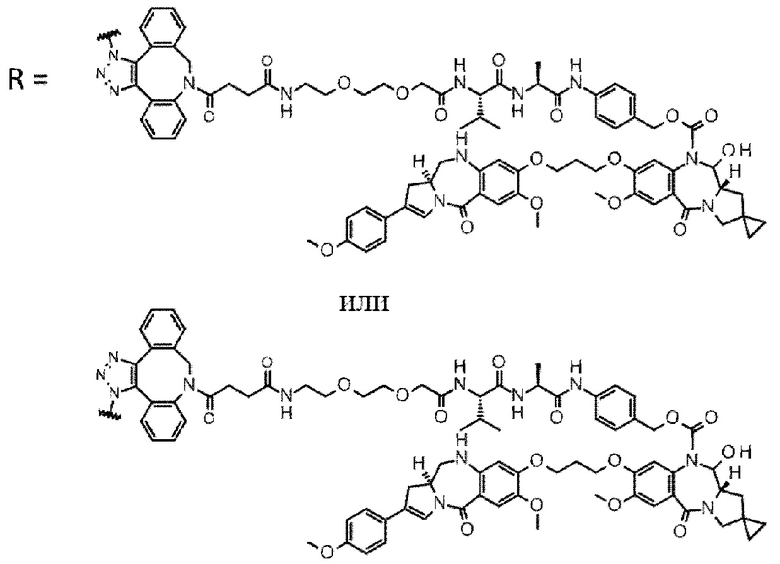
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 104, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0849]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 2 примера 13 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,63 мг/мл, выход антител: 9,80 мг (98%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0850]
Пример 105: ADC39
[Формула 232]
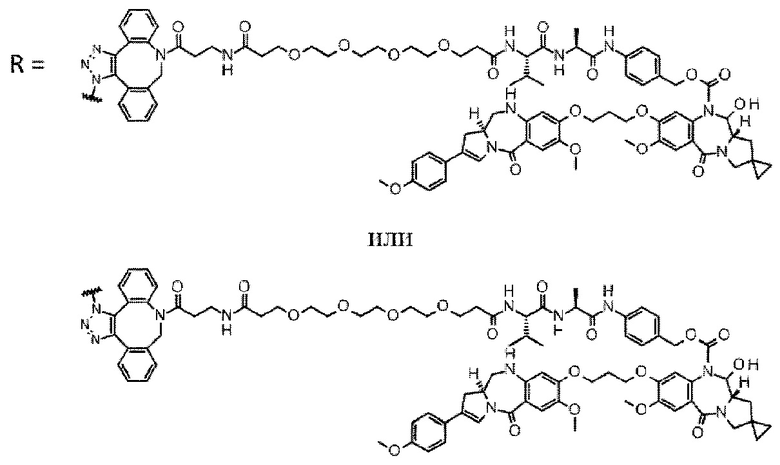
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 105, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0851]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 1 примера 14 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,72 мг/мл, выход антител: 10,3 мг (количественный выход), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0852]
Пример 106: ADC40
[Формула 233]|
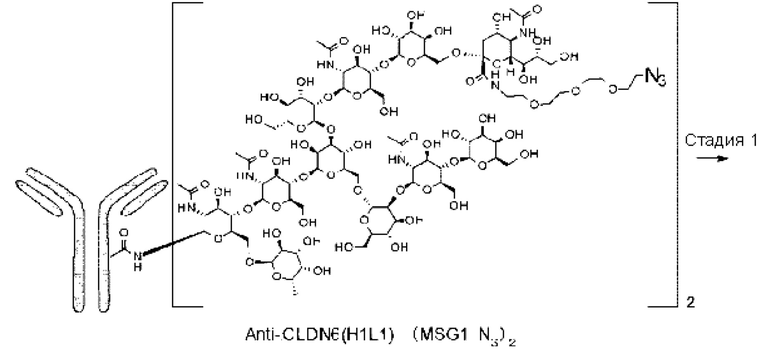
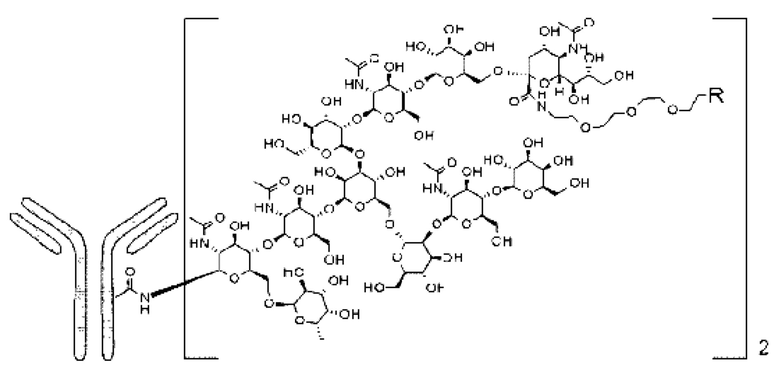
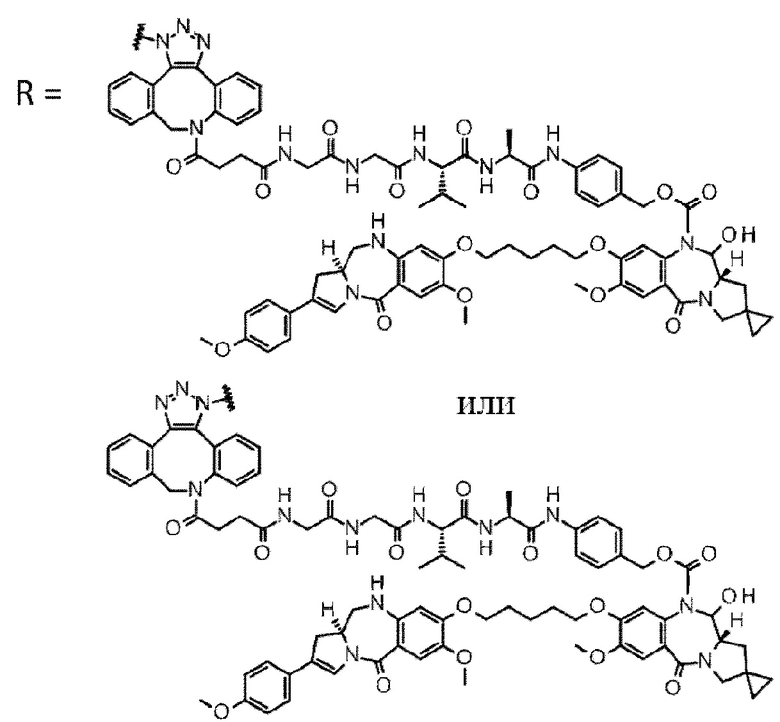
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 106, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0853]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 2,50 мл), полученного на стадии 2 примера 61, добавляли 1,2-пропандиол (2,29 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,206 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 14,5 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,54 мг/мл, выход антител: 22,3 мг (89%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0854]
Пример 107: ADC41
[Формула 234]
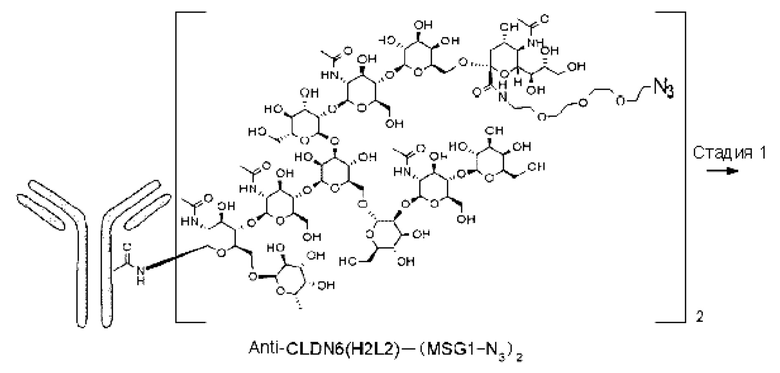
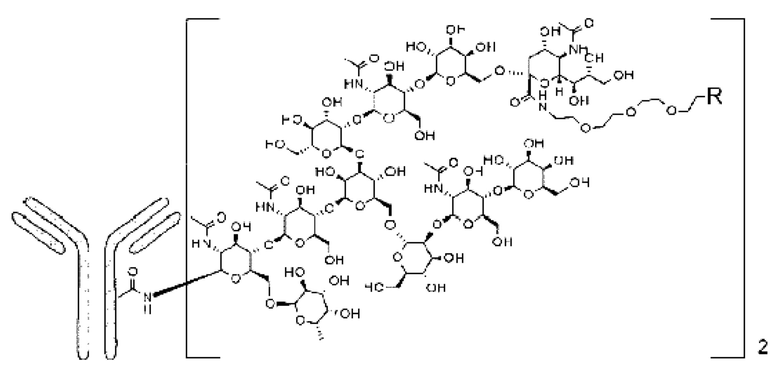
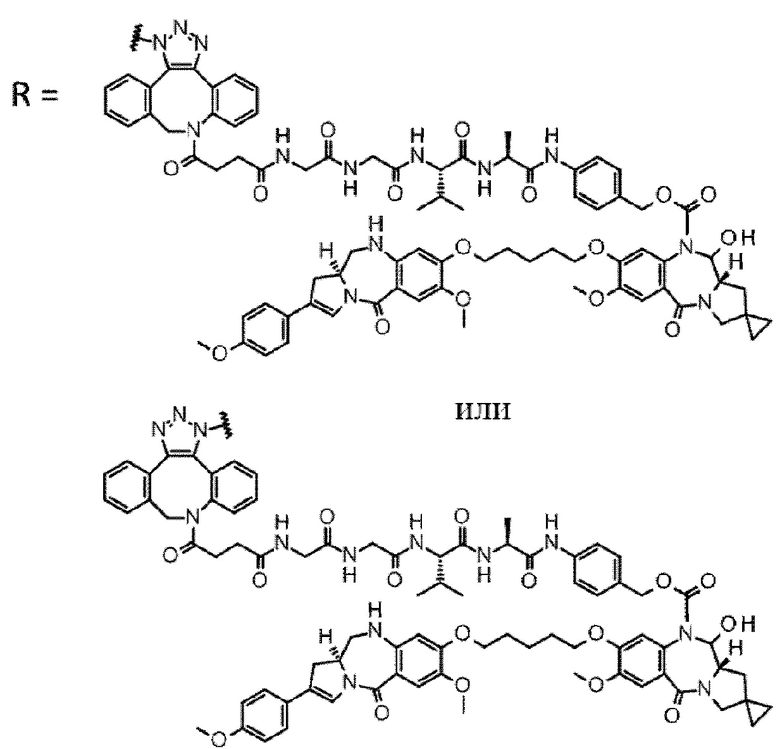
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 107, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0855]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,96 мг/мл, 2,50 мл), полученного на стадии 2 примера 62, добавляли 1,2-пропандиол (2,29 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,206 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 14,5 мл раствора желаемого соединения. Определение характеристик:
Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,52 мг/мл, выход антител: 22,0 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0856]
Пример 108: ADC42
[Формула 235]
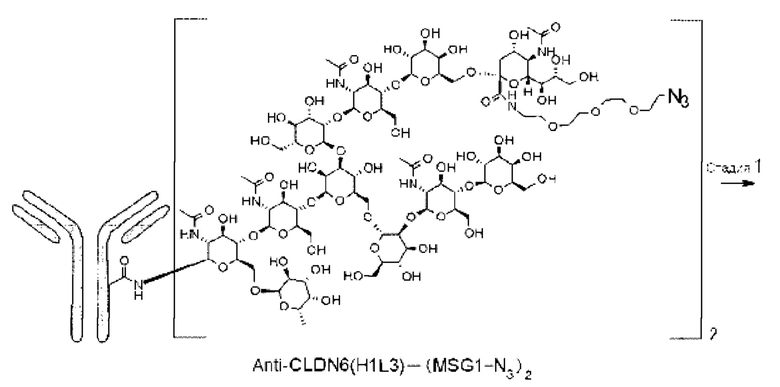
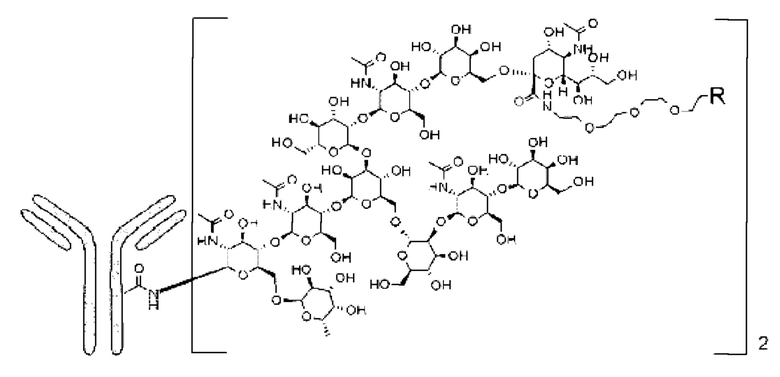
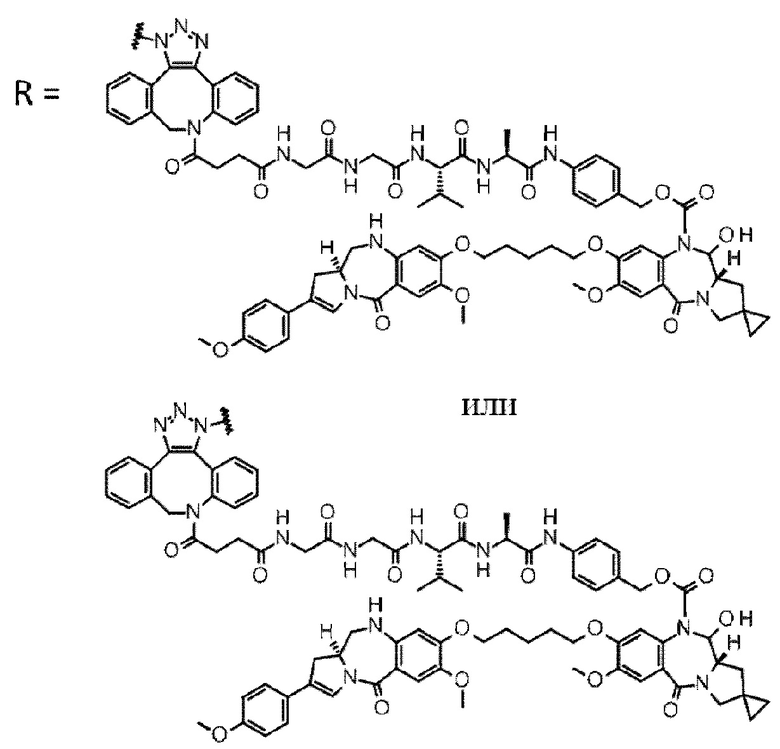
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 108, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0857]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,83 мг/мл, 2,50 мл), полученного на стадии 2 примера 63, добавляли 1,2-пропандиол (2,29 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,206 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 14,5 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,45 мг/мл, выход антител: 21,0 мг (84%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0858]
Пример 109: ADC43
[Формула 236]
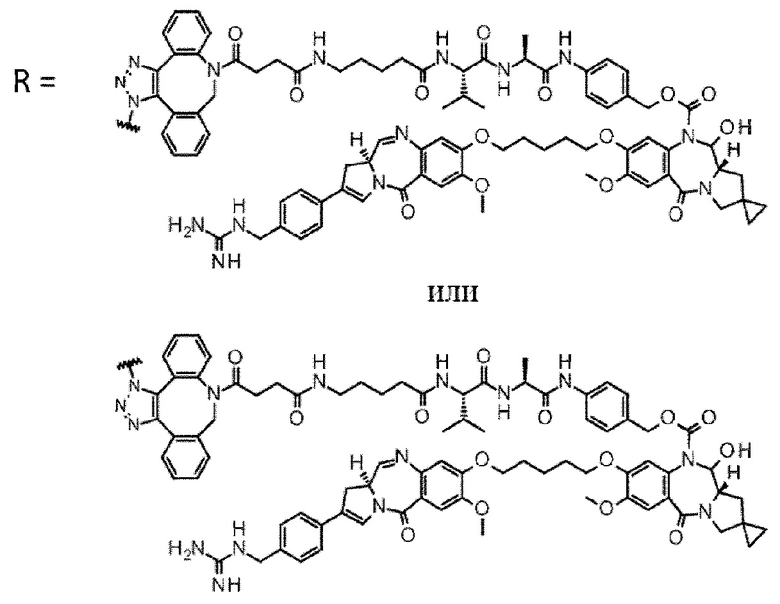
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 109, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0859]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 16 примера 42 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 3,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,30 мг/мл, выход антител: 7,79 мг (78%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0860]
Пример 110: ADC44
[Формула 237]
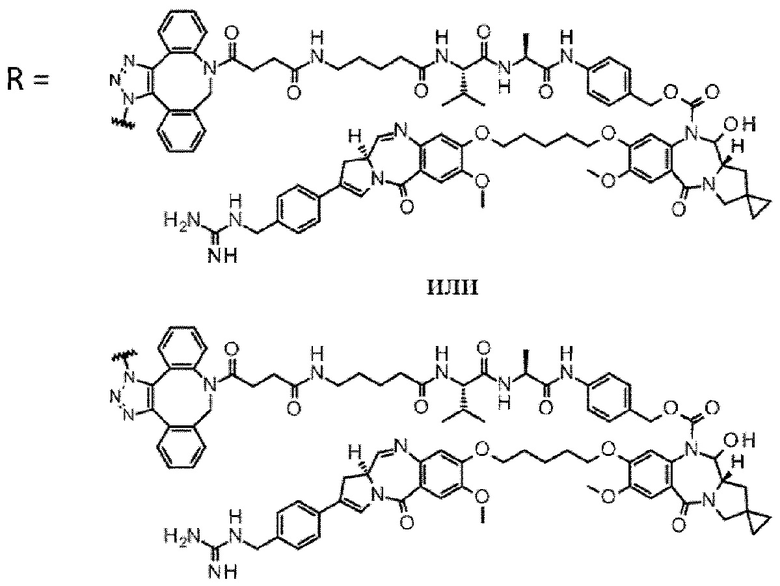
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 110, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0861]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 43 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 0,93 мг/мл, выход антител: 5,58 мг (56%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0862]
Пример 111: ADC45
[Формула 238]
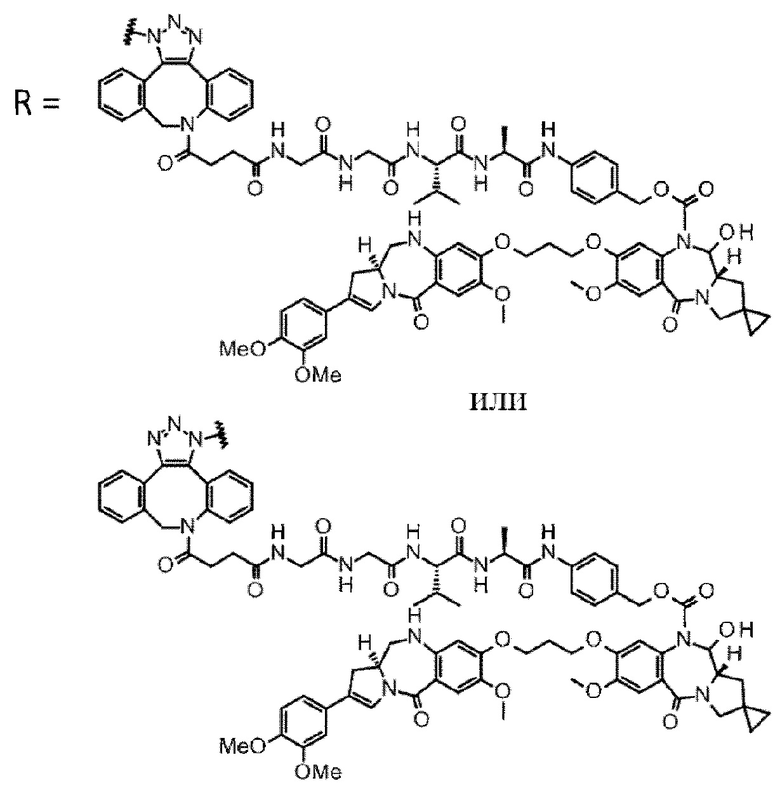
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 111, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0863]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 44 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,0 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 0,99 мг/мл, выход антител: 5,95 мг (59%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0864]
Пример 112: ADC46
[Формула 239]
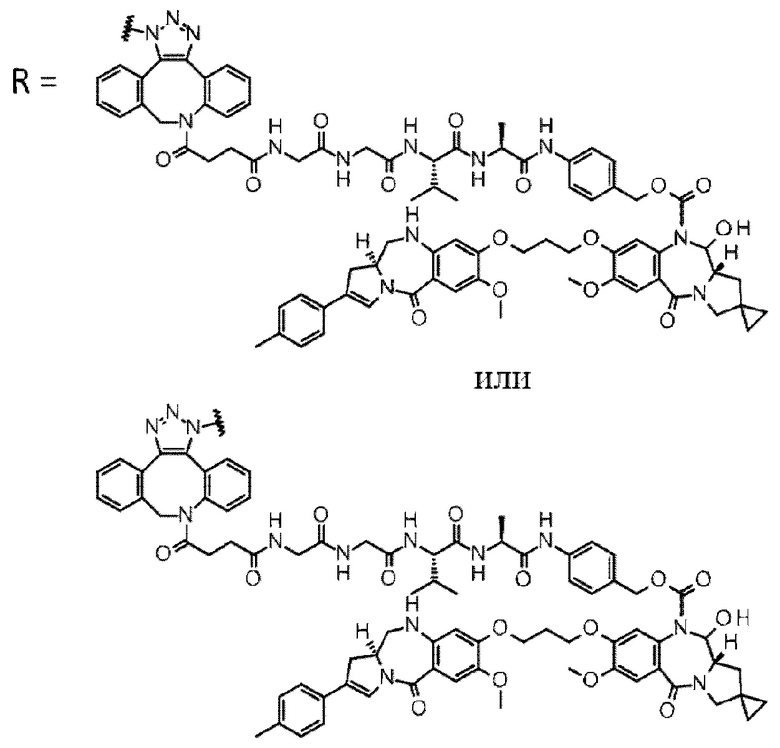
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 112, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0865]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 31 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,49 мг/мл, выход антител: 8,94 мг (89%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0866]
Пример 113: ADC47
[Формула 240]
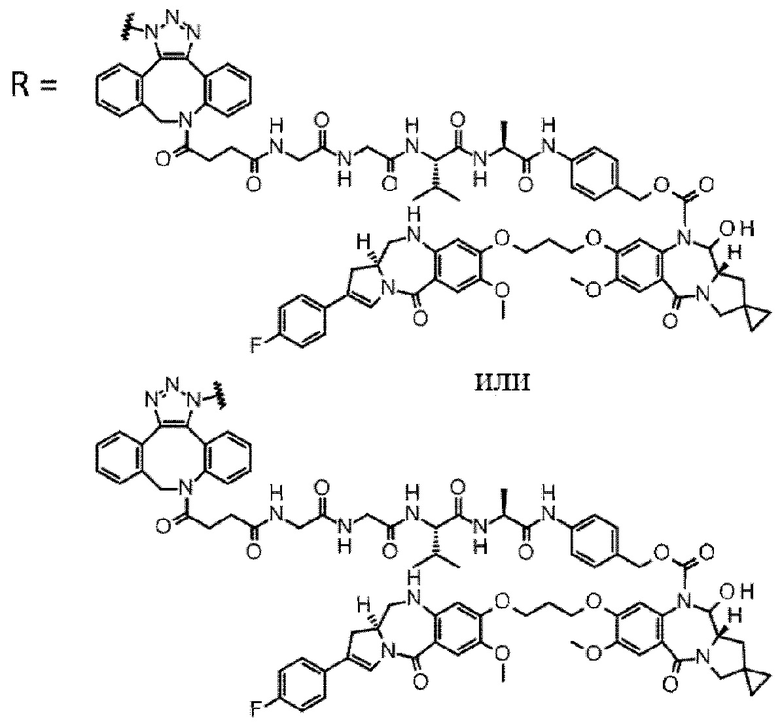
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 113, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0867]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 32 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,45 мг/мл, выход антител: 8,73 мг (87%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0868]
Пример 114: ADC48
[Формула 241]
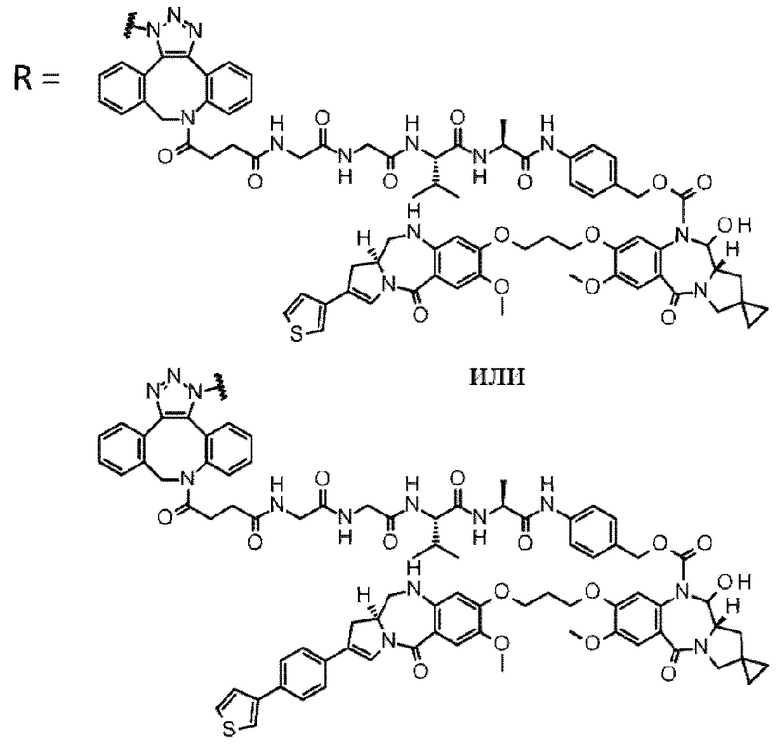
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 114, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0869]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 8 примера 33 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,45 мг/мл, выход антител: 8,70 мг (87%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0870]
Пример 115: ADC49
[Формула 242]
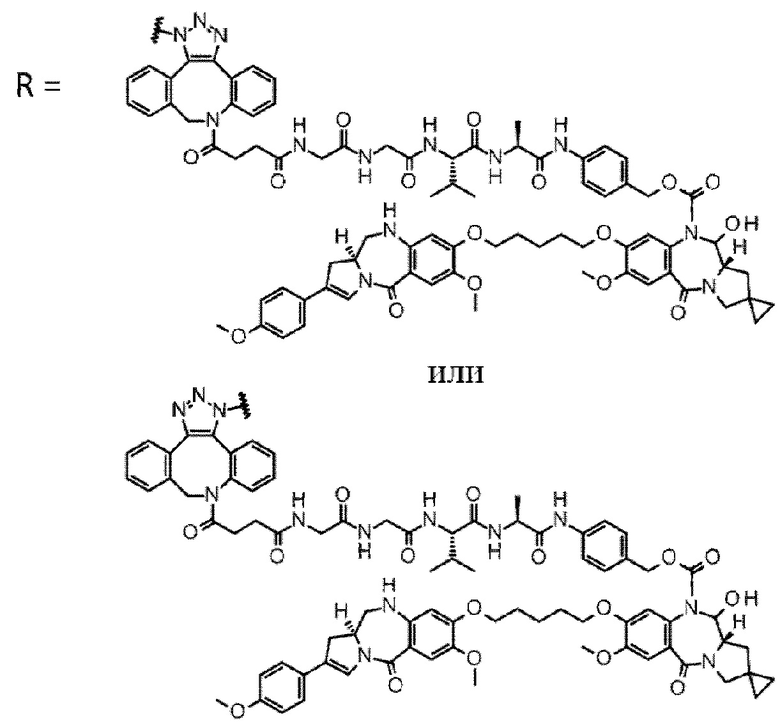
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 115, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0871]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,41 мг/мл, выход антител: 8,45 мг (85%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0872]
Пример 116: ADC50
[Формула 243]
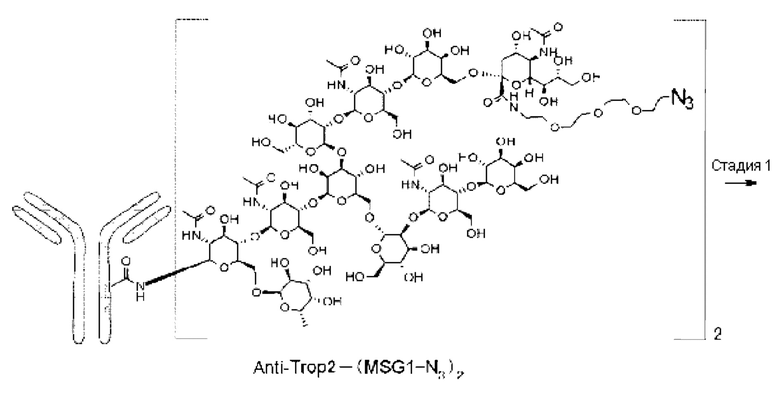
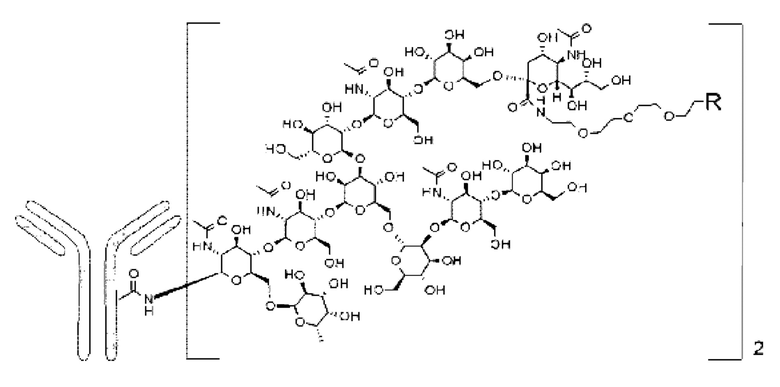
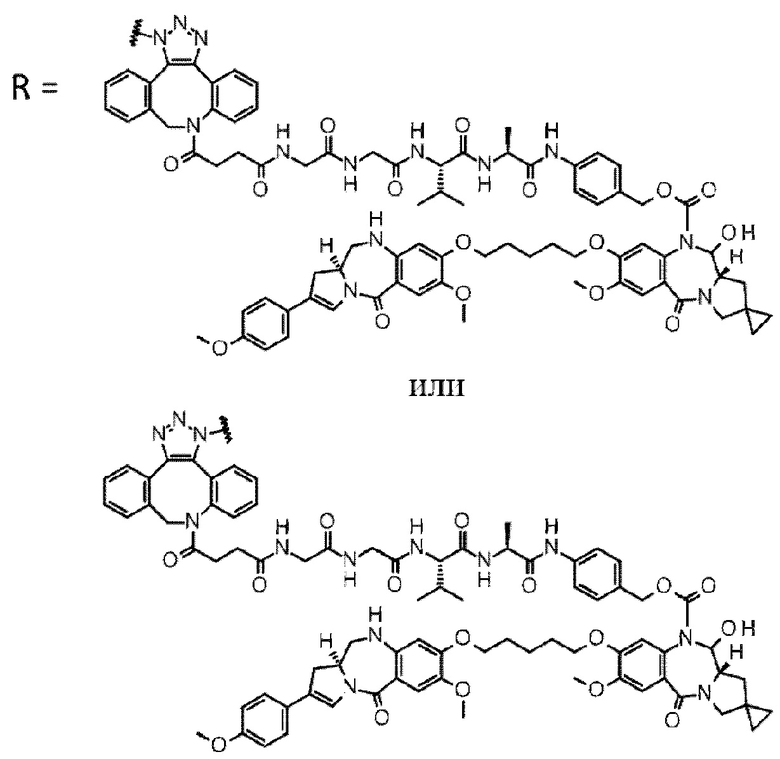
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 116, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0873]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10 мг/мл, 1,00 мл), полученного на стадии 2 примера 65, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,47 мг/мл, выход антител: 8,8 мг (88%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,9
[0874]
Пример 117: ADC51
[Формула 244]
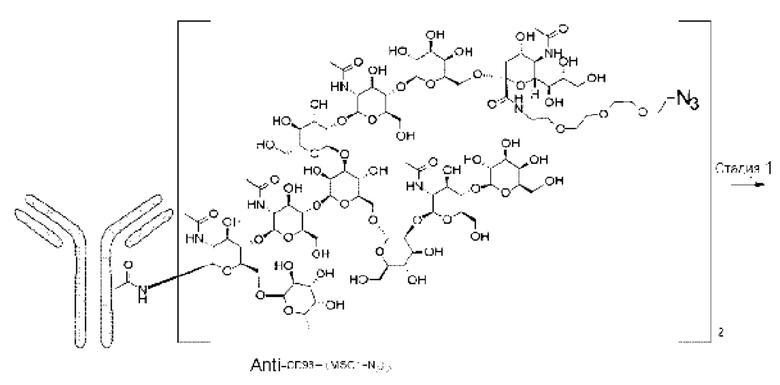
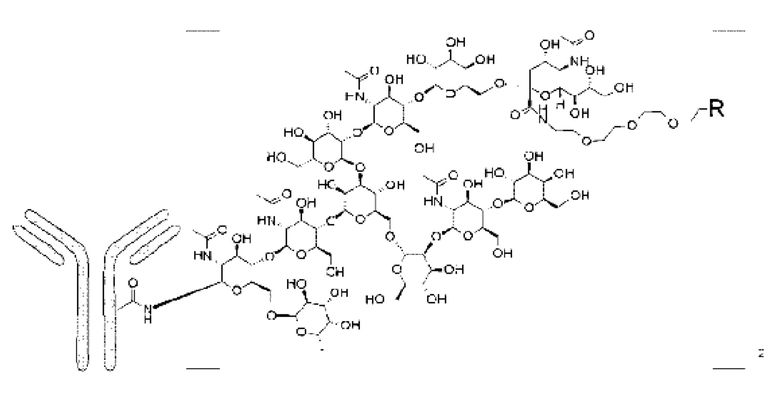
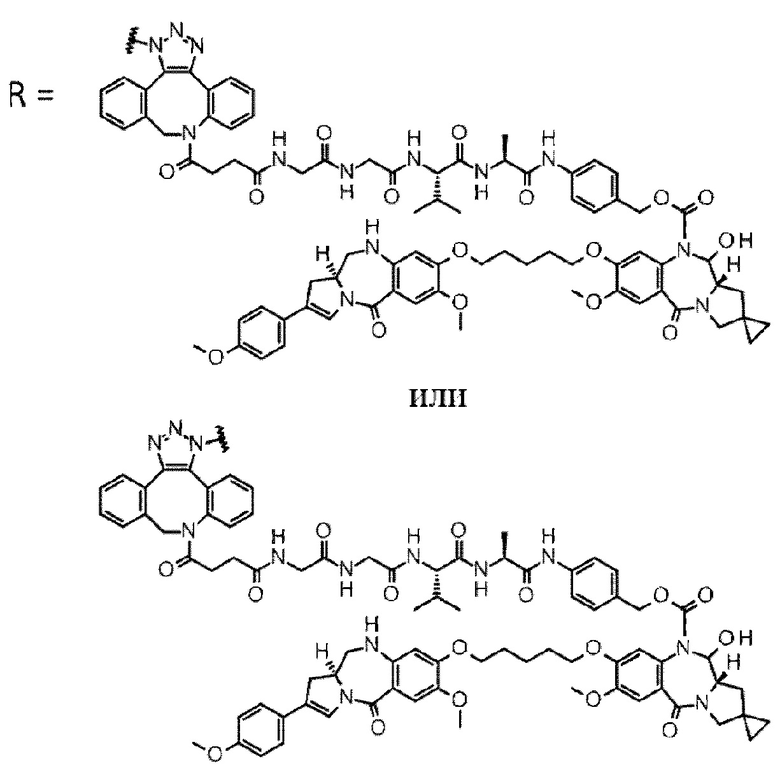
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 117, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0875]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,2 мг/мл, 1,00 мл), полученного на стадии 2 примера 64, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 30,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путе м применения общ их операций Е и F.
Концентрация антител: 1,36 мг/мл, выход антител: 3,19 мг (82%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0876]
Пример 118: ADC52
[Формула 245]
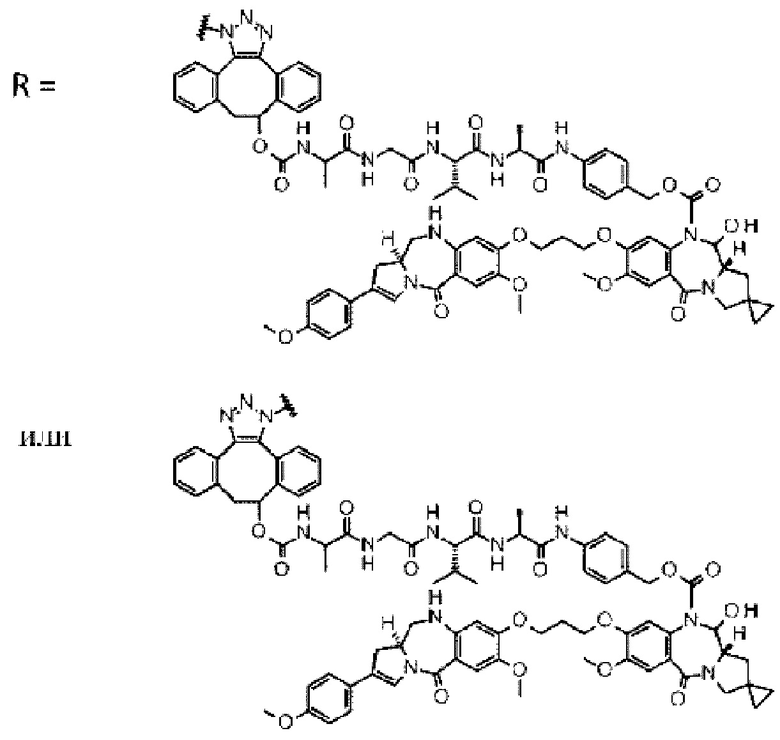
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 118, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0877]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 60, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 2 примера 8 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 3 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6,00 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,06 мг/мл, выход антител: 6,35 мг (63%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,2
[0878]
Пример 119: ADC53
[Формула 246]


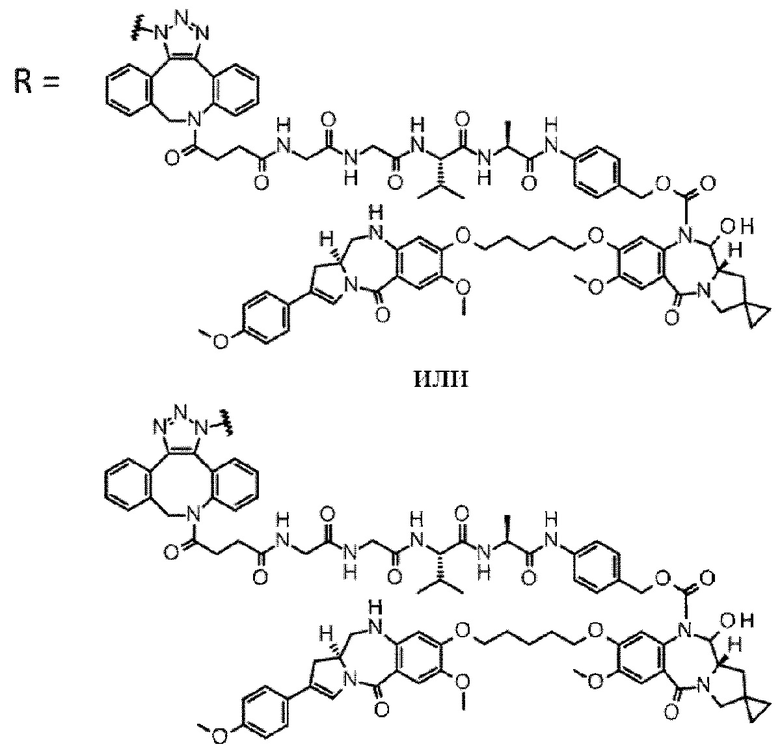
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 119, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0879]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (9,89 мг/мл, 0,40 мл), полученного на стадии 2 примера 66, добавляли 1,2-пропандиол (0,367 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 13 примера 3 (0,0328 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 2 дней.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 2,50 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,16 мг/мл, выход антител: 2,89 мг (72%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0880]
Пример 120: ADC54
[Формула 247]
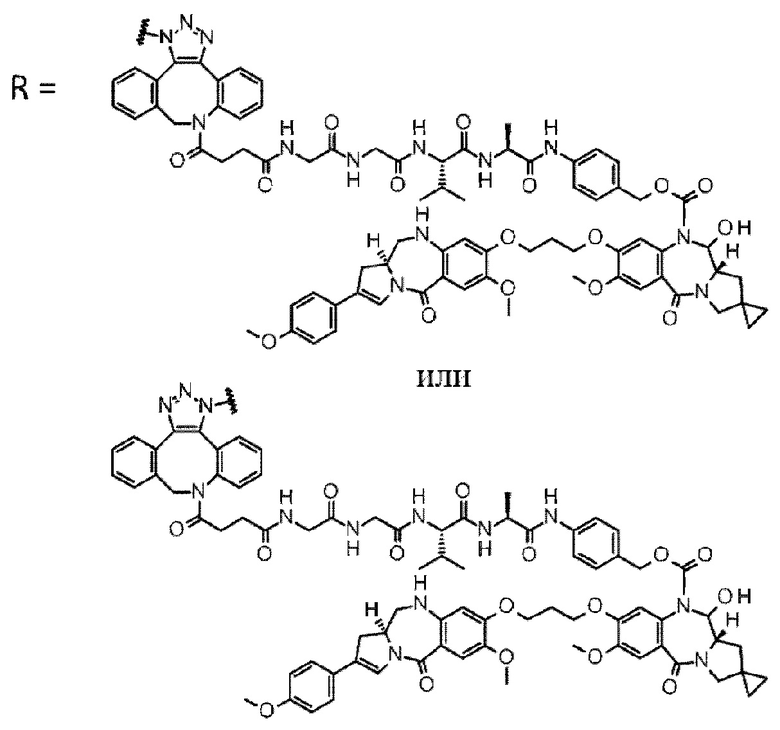
(Триазольное кольцо, которое должно образоваться на стадии 1, имеет геометрические изомеры, и соединение, полученное на стадии 1 примера 120, содержит линкер в виде смеси двух структур, показанных выше как R.)
[0881]
Стадия 1: Конъюгация антитела и лекарственного средства-линкера
К раствору в фосфатно-солевом буфере (рН 6,0) антитела (10,0 мг/мл, 1,00 мл), полученного на стадии 1 примера 59, добавляли 1,2-пропандиол (0,917 мл) и 10 мМ диметилсульфоксидный раствор соединения, полученного на стадии 12 примера 4 (0,0825 мл; 12 эквивалентов на молекулу антитела), при комнатной температуре и полученный продукт подвергали реакции с применением вращателя пробирок (MTR-103, AS ONE Corporation) при комнатной температуре в течение 48 часов.
Операция очистки: Раствор очищали с помощью применения общей операции D, получая 6 мл раствора желаемого соединения.
Определение характеристик: Следующие значения характеристик были получены путем применения общих операций Е и F.
Концентрация антител: 1,49 мг/мл, выход антител: 8,94 мг (89%), среднее количество конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0882]
Пример 121: Противоклеточное действие конъюгата антитело-лекарственное средство (1)
NCI-N87 (Американская коллекция типовых культур; АТСС CRL-5822), линию НЕР2-антиген-положительных клеток рака желудка человека, культивировали в среде RPMI1640 (Thermo Fisher Scientific; далее в настоящем описании называемой «средой RPMI»), содержащей 10% эмбриональной бычьей сыворотки (Hyclone). MDA-MB-468 (АТСС НТВ-132), НЕР2-антиген-отрицательные клетки, культивировали в среде Лейбовица L-15 (Leibovitz's L-15 Medium) (Thermo Fisher Scientific; далее в настоящем описании называемой средой Лейбовица), содержащей 10% эмбриональной бычьей сыворотки (Hyclone). Клетки NCI-N87 и MDA-MB-468 готовили с применением среды RPMI и среды Лейбовица, соответственно, до достижения концентрации 2,5×104 клеток/мл, и их аликвоты объемом 80 мкл добавляли в 96-луночный микропланшет для клеточных культур. После добавления клеток NCI-N87 культивировали при 37°C и 5% СО2 в течение ночи, и MDA-MB-468 культивировали при 37°C в течение ночи без регулирования концентрации СО2.
На следующий день в микропланшет добавляли аликвоты конъюгата антитело к HER2-лекарственное средство объемом 20 мкл, разбавленные средой RPMI или средой Лейбовица до 100 нМ, 10 нМ, 1 нМ, 0,1 нМ, 0,01 нМ и 0,001 нМ. В каждую лунку, не содержащую какого-либо конъюгата антитело-лекарственное средство, добавляли 20 мкл среды RPMI или среды Лейбовица. NCI-N87 культивировали при 37°C и 5% СО2 в течение 6 дней, и MDA-MB-468 культивировали при 37°C в течение 6 дней без регулирования концентрации СО2. После культивирования микропланшет вынимали из инкубатора и оставляли при комнатной температуре на 30 минут. Добавляли люминесцентный тест для определения количества жизнеспособных клеток CellTiter-Glo Luminescent Cell Viability Assay (Promega Corporation) в количестве, эквивалентном количеству культурального раствора, и перемешивали с помощью шейкера для планшетов. Микропланшет оставляли при комнатной температуре на 10 минут, и затем определяли величину испускания с помощью планшетного ридера (PerkinElmer). Уровни выживаемости клеток рассчитывали с помощью следующей формулы.
Уровень выживаемости клеток (%)=а÷b×100
а: Среднее значение величины испускания лунок с исследуемым веществом
b: Среднее значение величины испускания лунок со средой
Значения IC50 рассчитывали с помощью следующей формулы.
IC50 (нМ)=antilog((50-d)×(LOG10(b)-LOG10(a))÷(d-c)+LOG10(b))
а: Концентрация исследуемого вещества, а
b: Концентрация исследуемого вещества, b
с: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации а
d: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации b
а и b удовлетворяют условию а > b в точках, лежащих в пределах уровня выживаемости клеток, составляющего 50%.
Каждый из конъюгатов антитело-лекарственное средство ADC17, ADC18, ADC1, ADC54, ADC20, ADC34, ADC23, ADC24 и ADC25 проявлял противоклеточное действие с IC50 < 0,001 (нМ) в отношении клеток NCI-N87. Каждый из конъюгатов антитело-лекарственное средство ADC26, ADC27, ADC16, ADC11, ADC12, ADC2, ADC3, ADC4, ADC43, ADC5, ADC21, ADC48, ADC44, ADC6, ADC7, ADC28, ADC29, ADC13, ADC14, ADC30, ADC31, ADC32, ADC33, ADC35, ADC36, ADC8, ADC9, ADC38 и ADC39 проявлял противоклеточное действие с 0,001≤IC50<0,1 (нМ). Ни один из конъюгатов антитело-лекарственное средство не проявлял противоклеточного действия в отношении клеток MDA-MB-468 (IC50>0,1 (нМ)).
[0883]
Пример 122: Противоклеточное действие конъюгата антитело-лекарственное средство (2)
NCI-N87 (Американская коллекция типовых культур; АТСС CRL-5822), линию HER2-антиген-положительных клеток рака желудка человека, культивировали в среде RPMI1640 (Thermo Fisher Scientific; далее в настоящем описании называемой средой RPMI), содержащей 10% эмбриональной бычьей сыворотки (Hyclone). JIMT-1 (Немецкая коллекция микроорганизмов и клеточных культур (Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH); DSMZ ACC 589), линию HER2-антиген-положительных клеток рака молочной железы человека, культивировали в среде Игла в модификации Дульбекко (Thermo Fisher Scientific; далее в настоящем описании называемой средой DMEM), содержащей 10% эмбриональной бычьей сыворотки (Hyclone). Клетки NCI-N87 готовили в среде RPMI до достижения концентрации 5,0×104 клеток/мл, и клетки JIMT-1 готовили в среде DMEM до достижения концентрации 1,3×104 клеток/мл, затем их аликвоты объемом 80 мкл добавляли в 96-луночный микропланшет для клеточных культур и культивировали клетки при 37°C и 5% СО2 в течение ночи.
На следующий день в микропланшет добавляли аликвоты конъюгата антитело к HER2-лекарственное средство ADC49 или конъюгата антитело к LPS-лекарственное средство ADC53 объемом 20 мкл, разбавленные средой RPMI или средой DMEM до 400 нМ, 80 нМ, 16 нМ, 3,2 нМ, 0,64 нМ, 0,13 нМ, 0,026 нМ, 0,0051 нМ и 0,0010 нМ. В каждую лунку, не содержащую какого-либо конъюгата антитело-лекарственное средство, добавляли 20 мкл среды RPMI или среды DMEM. Клетки культивировали при 37°C и 5% СО2 в течение 6 дней. После культивирования микропланшет вынимали из инкубатора и оставляли при комнатной температуре на 30 минут. Добавляли люминесцентный тест для определения количества жизнеспособных клеток (Promega Corporation) в количестве, эквивалентном количеству культурального раствора, и перемешивали с помощью шейкера для планшетов. Микропланшет оставляли при комнатной температуре на 10 минут и затем определяли величину испускания с помощью планшетного ридера (PerkinElmer). Уровни выживаемости клеток рассчитывали с помощью следующей формулы.
Уровень выживаемости клеток (%)=а÷b×100
а: Среднее значение величины испускания лунок с исследуемым веществом
b: Среднее значение величины испускания лунок со средой
Значения IC50 рассчитывали с помощью следующей формулы.
IC50 (нМ)=antilog((50-d)×(LOG10(b)-LOG10(a))÷(d-c)+LOG10(b))
а: Концентрация исследуемого вещества, а
b: Концентрация исследуемого вещества, b
с: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации а
d: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации b
а и b удовлетворяют условию а > b в точках, лежащих в пределах уровня выживаемости клеток, составляющего 50%.
Конъюгат антитело к HER2-лекарственное средство ADC49 проявлял противоклеточное действие с 0,001<IC50<0,1 (нМ) в отношении как клеток NCI-N87, так и клеток JIMT-1. Конъюгат антитело к LPS-лекарственное средство ADC53, напротив, не проявлял противоклеточного действия в отношении обоих типов клеток (IC50>0,1 (нМ)).
[0884]
Пример 123: Противоклеточное действие конъюгата антитело-лекарственное средство (3)
OV-90 (АТСС CRL-11732), линию CLDN6-антиген-положительных клеток рака яичника человека, культивировали в смешанной среде (далее в настоящем описании называемой средой), состоящей из среды 199 (Thermo Fisher Scientific) и среды MCDB 105 (Sigma-Aldrich Co. LLC) в отношении 1:1, содержащей 15% эмбриональной бычьей сыворотки (Hyclone). Клетки OV-90 готовили в среде до достижения концентрации 1,9×104 клеток/мл, затем их аликвоты объемом 80 мкл добавляли в 96-луночный микропланшет для клеточных культур и культивировали клетки при 37°C и 5% СО2 в течение ночи.
На следующий день в микропланшет добавляли аликвоты конъюгата антитело к CLDN6-лекарственное средство ADC40, ADC41 или ADC42 объемом 20 мкл, разбавленные средой до 50 нМ, 10 нМ, 2,0 нМ, 400 пМ, 80 пМ, 16 пМ, 3,2 пМ, 0,64 пМ и 0,13 пМ. В каждую лунку, не содержащую какого-либо конъюгата антитело-лекарственное средство, добавляли 20 мкл среды. Клетки культивировали при 37°C и 5% СО2 в течение 6 дней. После культивирования микропланшет вынимали из инкубатора и оставляли при комнатной температуре на 30 минут. Добавляли люминесцентный тест для определения количества жизнеспособных клеток (Promega Corporation) в количестве, эквивалентном количеству культурального раствора, и перемешивали с помощью шейкера для планшетов. Микропланшет оставляли при комнатной температуре на 10 минут, и затем определяли величину испускания с помощью планшетного ридера (PerkinElmer). Уровни выживаемости клеток рассчитывали с помощью следующей формулы.
Уровень выживаемости клеток (%)=а÷b×100
а: Среднее значение величины испускания лунок с исследуемым веществом
b: Среднее значение величины испускания лунок со средой
Значения IC50 рассчитывали с помощью следующей формулы.
IC50 (нМ)=antilog((50-d)×(LOG10(b)-LOG10(a))÷(d-c)+LOG10(b))
а: Концентрация исследуемого вещества, а
b: Концентрация исследуемого вещества, b
с: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации а
d: Уровень выживаемости клеток при добавлении исследуемого вещества в концентрации b
а и b удовлетворяют условию а > b в точках, лежащих в пределах уровня выживаемости клеток, составляющего 50%.
Каждый из конъюгатов антитело к CLDN6-лекарственное средство ADC40, ADC41 и ADC42 проявлял противоклеточное действие с 0,001<IC50<0,1 (нМ) в отношении клеток OV-90.
[0885]
Пример 124: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (1)
Мыши: перед использованием в эксперименте осуществляли адаптацию самок бестимусных (nude) мышей BALB/c в возрасте от четырех до пяти недель (Charles River Laboratories Japan, Inc.) в условиях SPF («specific pathogen free» - свободных от специфической патогенной микрофлоры) в течение 4-7 дней. Мыши получали стерелизованный гранулированный корм (FR-2, Funabashi Farms Co., Ltd.) и стерелизованную водопроводную воду (приготовленную путем добавления 5-15 ppm раствора гипохлорита натрия).
Анализ и формула расчета: Во всех экспериментах измеряли длинную ось и короткую ось опухоли два или три раза в неделю с помощью штангенциркуля с электронным цифровым отсчетом (CD-15CX, Mitutoyo Corp.) и рассчитывали объем опухоли (мм3). Формула расчета представлена ниже.
Объем опухоли (мм3) = длинная ось (мм) × [короткая ось (мм)]2 × 1/2
Каждый из конъюгатов антитело-лекарственное средство и каждое из антител разбавляли с использованием 10 мМ ацетатного буфера, 5% сорбитола, рН 5,5 (NACALAI TESQUE, INC.; буфер ABS), и вводили в хвостовую вену объем жидкости в дозе 10 мл/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Клетки NCI-N87 (АТСС CRL-5822) суспендировали в физиологическом солевом растворе (Otsuka Pharmaceutical Factory, Inc.), и 1×107 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 7 день мышей случайным образом распределяли по группам. Конъюгат антитело к HER2-лекарственное средство ADC26, ADC19 или ADC54 вводили в хвостовую вену на 7 день в дозе 0,3 мг/кг в случае ADC26 и в дозе 1 мг/кг в случае ADC19 и ADC54. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 4. Было обнаружено, что конъюгаты антитело к HER2-лекарственное средство ADC26, ADC19 и ADC54 обладают сильным противоопухолевым действием, вызывающим регрессию опухоли. При введении любого из конъюгатов антитело к HER2-лекарственное средство не обнаруживали снижения массы тела ни у одной из мышей.
В следующих примерах оценки, относящихся к оценке противоопухолевого действия, применяли способ, используемый в настоящем примере оценки, если не указано иное.
[0886]
Пример 125: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (2)
Клетки NCI-N87 (АТСС CRL-5822) суспендировали в фосфатно-солевом буфере Дульбекко (Sigma-Aldrich Co. LLC), и 1×107 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 4 день мышей случайным образом распределяли по группам. Конъюгат антитело к HER2-лекарственное средство ADC49, антитело к HER2 трастузумаб (справочный пример 3) или конъюгат антитело к LPS-лекарственное средство ADC53 вводили в хвостовую вену на 4 день в дозе 0,33 мг/кг во всех случаях. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 5. Было обнаружено, что конъюгат антитело к HER2-лекарственное средство ADC49 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. Напротив, антитело к HER2 трастузумаб и конъюгат антитело к LPS-лекарственное средство ADC53 не подавляли рост опухоли. Не было обнаружено снижения массы тела мышей, обусловленного введением конъюгата антитело-лекарственное средство ADC49, или ADC53, или антитела к HER2.
[0887]
Пример 126: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (3)
Клетки KPL-4 (Dr. Junichi Kurebayashi, Kawasaki Medical School, British Journal of Cancer, (1999) 79(5/6). 707-717) суспендировали в фосфатно-солевом буфере Дульбекко (Sigma-Aldrich Co. LLC), и 1,5×107 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 14 день мышей случайным образом распределяли по группам. Конъюгат антитело к HER2-лекарственное средство ADC49, конъюгат антитело к LPS-лекарственное средство ADC53 или трастузумаб тезирин (справочный пример 1) вводили в хвостовую вену на 14 день в дозе 0,4 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 6. Было обнаружено, что конъюгат антитело к НЕР2-лекарственное средство ADC49 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. Напротив, не было обнаружено регрессии опухоли в случае ADC53 и трастузумаба тезирина. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC49 или трастузумаба тезирина.
[0888]
Пример 127: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (4)
Клетки JIMT-1 (DSMZ АСС 589) суспендировали в физиологическом солевом растворе (Otsuka Pharmaceutical Factory, hie), и 5×106 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 10 день мышей случайным образом распределяли по группам. Конъюгат антитело к HER2-лекарственное средство ADC49 или трастузумаб тезирин (справочный пример 1) вводили в хвостовую вену на 10 день в дозе 0,4 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 7. Было обнаружено, что конъюгат антитело к НЕР2-лекарственное средство ADC49 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. В случае трастузумаба тезирина, напротив, было обнаружено противоопухолевое действие, однако не было обнаружено регрессии опухоли. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC49 или трастузумаба тезирина.
[0889]
Пример 128: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (5)
Клетки OV-90 (АТСС CRL-11732) суспендировали в матригеле (Matrigel, Corning Incorporated), и 2,5×106 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 15 день мышей случайным образом распределяли по группам. Конъюгат антитело к CLDN6-лекарственное средство ADC40 или антитело к CLDN6 (H1L1)-тезирин вводили в хвостовую вену на 15 день в дозе 0,33 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 8. Было обнаружено, что конъюгат антитело к CLDN6-лекарственное средство ADC40 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. Напротив, регрессии опухоли не было обнаружено в случае антитела к CLDN6 (H1L1)-тезирина. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC40 или H1L1-тезирина.
[0890]
Пример 129: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (6)
Клетки NIH:OVCAR-3 (АТСС НТВ-161) суспендировали в матригеле (Corning Incorporated), и 1×107 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 25 день мышей случайным образом распределяли по группам. Конъюгат антитело к CLDN6-лекарственное средство ADC40 или антитело к CLDN6 (H1L1)-тезирин вводили в хвостовую вену на 25 день в дозе 0,33 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 9. Было обнаружено, что конъюгат антитело к CLDN6-лекарственное средство ADC40 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. В случае H1L1-тезирина, напротив, было обнаружено противоопухолевое действие, однако не было обнаружено регрессии опухоли. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC40 или H1L1-тезирина.
[0891]
Пример 130: Оценка противоопухолевого действия конъюгата антитело-лекарственное средство (7)
Клетки FaDu (АТСС НТВ-43) суспендировали в физиологическом солевом растворе (Otsuka Pharmaceutical Factory, Inc.), и 3×106 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 10 день мышей случайным образом распределяли по группам. Конъюгат антитело к TROP2-лекарственное средство ADC50 или конъюгат антитело к LPS-лекарственное средство ADC53 вводили в хвостовую вену на 10 день в дозе 0,4 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 10. Было обнаружено, что конъюгат антитело к TROP2-лекарственное средство ADC50 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли. Напротив, конъюгат антитело к LPS-лекарственное средство ADC53 не подавлял рост опухоли. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC50 или ADC53.
[0892]
Пример 131: Мышиная гибридома, продуцирующая антитело к CLDN6 Bl (218 В1) и мышиная гибридома, продуцирующая антитело к CLDN6 С7 (218С7)
131-1. Иммунизация мышей и получение гибридом
1-1) Подготовка клеток для иммунизации мышей
2×106 или 5×106 клеток NOR-P1 (линия клеток рака поджелудочной железы человека, RIKEN RCB-2139) культивировали в содержащей 10% ЭБС (эмбриональной бычьей сыворотки) (+) среде RPMI-1640 (Roswell Park Memorial Institute-1640) (10 мл или 20 мл) в течение 5 дней, и затем собирали и дважды промывали ФСБ (фосфатно-солевым буфером) и ресуспендировали в ФСБ (300 мкл).
1-2) Иммунизация мышей
Каждую мышь BALB/c (в возрасте 12 недель) внутрибрюшинно иммунизировали клетками NOR-P1 (2×106 клеток) с интервалами, составляющими примерно 1 неделю в случае иммунизации с первой по пятую. Примерно через 2 недели после пятой иммунизации каждую мышь BALB/c внутрибрюшинно иммунизировали клетками NOR-P1 (5×106 клеток). Примерно через 3 недели после шестой иммунизации каждую мышь BALB/c внутрибрюшинно иммунизировали клетками NOR-P1 (2×106 клеток). Каждую мышь BALB/c внутрибрюшинно иммунизировали клетками NOR-P1 (2×106 клеток) с интервалами, составляющими примерно 2 недели в случае иммунизаций с 8-й по 10-ю. Примерно через 3 недели после 10-й иммунизации (11-я иммунизация) и через 3 дня после этого (12-я иммунизация, последняя иммунизация) каждую мышь BALB/c внутрибрюшинно иммунизировали клетками NOR-P1 (5×106 клеток). Спленоциты выделяли через 3 дня после последней иммунизации.
1-3) Получение спленоцитов иммунизированных мышей
Селезенку выделяли от каждой иммунизированной мыши, растирали и суспендировали в среде RPMI1640 10% ЭБС (+). Полученную суспензию клеток пропускали через клеточное сито (70 мкм, BD Falcon) и затем центрифугировали при 1500 об./мин при комнатной температуре в течение 5 минут для удаления супернатанта. Затем добавляли раствор Трис-NH4Cl (20 мМ Трис-HCl, pH 7,2, 77,6 мМ NH4Cl; 20 мл), и полученный продукт обрабатывали при комнатной температуре в течение 5 минут. Затем добавляли ФСБ (20 мл), и полученный продукт центрифугировали при 1500 об./мин при комнатной температуре в течение 5 минут. После удаления супернатанта к остатку добавляли среду RPMI1640 ЭБС (+) (10 мл).
1-4) Получение клеток миеломы
Клетки P3U1 (линия клеток мышиной миеломы) культивировали в среде RPMI1640 ЭБС (+) в течение 5 дней, и затем собирали и ресуспендировали в среде RPMI1640 ЭБС (+) (20 мл).
1-5) Слияние клеток
Спленоциты и клетки миеломы смешивали в отношении 5:1 и центрифугировали при 1500 об./мин при комнатной температуре в течение 5 минут. Клетки дважды промывали средой RPMI1640 ЭБС (-) (10 мл) и затем центрифугировали (1500 об./мин, 5 минут). Группу клеток в полученной осажденной фракции в достаточной степени разрыхляли, и затем постепенно добавляли к ним полиэтиленгликоль-1500 (ПЭГ-1500; 1 мл) при перемешивании в течение примерно 1 минуты. После перемешивания в течение 3 минут 30 секунд полученный продукт оставляли при комнатной температуре на 30 секунд. Затем к полученному раствору клеток добавляли среду RPMI 10% ЭБС с низким содержанием IgG (+) (10 мл) в течение 1 минуты. Полученную суспензию клеток центрифугировали (1500 об./мин, 5 минут), и клетки в полученной осажденной фракции осторожно разрыхляли, и затем осторожно суспендировали в среде ПАТ (среде РРМП640, содержащей 10% ЭБС с низким содержанием IgG, добавку к среде HAT и 5% BriClone; 200 мл). Суспензию вносили в 96-луночный культуральный планшет в виде аликвот объемом 200 мкл/лунку и культивировали в инкубаторе при 37°С и 5% CO2 в течение 6 дней.
1-6) Скрининг гибридом/получение зонда
DT3C, рекомбинантный комплексный белок, получали с целью проведения анализа интернализации антител и активности иммунотоксина. Данный DT3C представляет собой белок, полученный путем слияния каталитического домена дифтерийного токсина (DT) и антитело-связывающего домена стрептококкового белка G методами генетической инженерии. DT3C избирательно связывается с Fc-фрагментом антител и вызывает гибель клеток посредством ингибирования синтеза белка при включении в клетку. Использование этой системы позволяет одновременно наблюдать интернализацию антитела и разрушающее действие иммунотоксина на клетки (Yamaguchi, M. et al., Biochemical and Biophysical Research Communications 454 (2014) 600-603).
1-7) Скрининг гибридом с помощью DT3C
В 96-луночный планшет добавляли 4 мкг/мл DT3C (25 мкл), а затем добавляли культуральный супернатант гибридомы, полученный на стадии 1-5 (25 мкл), и полученный продукт инкубировали при комнатной температуре в течение 30 минут. Клетки NOR-P1 (50 мкл) высевали в концентрации 2×105 клеток/мл (среда RPMI 10% ЭБС с низким содержанием IgG (+)) и культивировали в СО2-инкубаторе при 37°С в течение 3 дней. При микроскопическом наблюдении после культивирования лунки, содержащие прикрепившиеся клетки в количестве, составляющем примерно 25% или менее от количества прикрепившихся клеток при применении отрицательного контрольного антитела, определяли как положительные. Отобранные клоны подвергали одной или двум стадиям субклонирования для получения восьми моноклональных линий клеток гибридомы.
[0893]
131-2: Идентификация антигена, с которым связывается антитело, продуцируемое гибридомой
Антигены идентифицировали для двух клонов, 218 В1 и 218С7, антител, продуцируемых гибридомами, полученными в примере 131-1.
2-1) Иммунопреципитация меченного биотином белка клеточной поверхности антителом 218 В1 и антителом 218С7
Культуральный супернатант 2×106 клеток NTERA-2 (линия клеток рака яичка человека, АТСС CRL-1973) удаляли, и остаток дважды промывали ФСБ. Реагент EZ-Link Sulfo-NHS-Biotin (Thermo Fisher Scientific) суспендировали в ФСБ до концентрации 0,1 мг/мл. После удаления ФСБ добавляли раствор биотина/ФСБ, и полученный продукт инкубировали на шейкере в течение 30 минут, и затем дважды промывали 100 мМ раствором глицина/ФСБ (25 мл), и затем один раз промывали ФСБ (10 мл). Промытые клетки ресуспендировали в 200 мкл лизирующего буфера (150 мМ Nad, 50 мМ Трис-HCl, pH 7,4, 1% DDM, готовый ингибитор протеаз без ЭДТА (F. Hoffmann-La Roche, Ltd.) - 1 доза/50 мл) и обрабатывали при 4°С в течение 30 минут. Полученный продукт центрифугировали (13000 об./мин, 20 минут, 4°С) с получением лизата клеток. К полученному лизату клеток добавляли суспензию сефарозы с иммобилизованным белком G (белок G-сефарозы) в лизирующем буфере (50% суспензия; 30 мкл), полученную путем замены буфера белок G-сефарозы (Protein G Sepharose 4 Fast Flow (GE Healthcare)) на лизирующий буфер, и полученный продукт подвергали ротации при 4°С в течение 30 минут, и затем центрифугировали при 4°С в течение 1 минуты и собирали супернатант. К этому супернатанту добавляли антитело 218 В1 или антитело 218С7 (примерно 3 мкг), и полученный продукт подвергали ротации при 4°С в течение 30 минут, затем к нему добавляли белок G-сефарозу/лизирующий буфер (50% суспензия; 60 мкл), и полученный продукт подвергали ротации при 4°С в течение 1 часа. Белок G-сефарозу промывали шесть раз лизирующим буфером (1 мл), и затем ресуспендировали в 1 × буфере для образцов, содержащем ДСП (Bio-Rad Laboratories, Inc.). После обработки полученной суспензии при 100°С в течение 5 минут раствор собирали для использования в качестве образца для SDS-ПАГЭ (электрофореза в полиакриламидном геле).
2-2) SDS-ПАГЭ и вестерн-блоттинг
Образец для ДСН-ПАГЭ, полученный на стадии 2-1), концентрировали в готовом геле SuperSep Асе 5-20% (Wako Pure Chemical Industries, Ltd.) при 50 мВ в течение 30 минут, и затем подвергали электрофорезу при 200 мВ в течение 1 часа и переносили из геля на мембрану методом блоттинга при 12 мВ в течение 47 минут. Мембрану промывали ФСБ-Т (ФСБ (-)-0,02% Tween 20) и затем проводили блокирование в течение 1 часа. Мембрану три раза промывали ФСБ-Т в течение 5 минут, и затем подвергали реакции с конъюгатом стрептавидин-пероксидаза хрена (GE Healthcare; при применении разбавленный ФСБ-Т в 2000 раз) в течение 1 часа. Мембрану дважды промывали ФСБ-Т в течение 5 минут, и затем выявляли целевой бэнд методом усиленной хемилюминесценции (ECL). Бэнд, соответствующий молекулярной массе 18 кДа, был обнаружен во всех случаях при применении антитела 218 В 1 и при применении антитела 218С7, независимо от присутствия или отсутствия добавленного ДТТ.
2-3) Масс-спектрометрия продукта иммунопреципитации белка клеток антителом 218 В1 и антителом 218С7
2×107 клеток NTERA-2 собирали и дважды промывали ФСБ. Клетки собирали с помощью скребка для клеток и центрифугировали при 1500 об./мин в течение 5 минут. После удаления супернатанта клетки ресуспендировали в 2 мл лизирующего буфера и обрабатывали при 4°С в течение 30 минут. Полученный продукт центрифугировали (13000 об./мин, 20 минут, 4°С) с получением лизата клеток. К полученному лизату клеток добавляли белок G-сефарозу/лизирующий буфер (50% суспензия; 180 мкл), и полученный продукт подвергали ротации при 4°С в течение 30 минут, и затем центрифугировали при 4°С в течение 1 часа и собирали супернатант. К супернатанту добавляли антитело 218 В1 (примерно 9 мкг), и полученный продукт подвергали ротации при 4°С в течение 30 минут, затем к нему добавляли белок G-сефарозу/лизирующий буфер (50% суспензия; 180 мкл), и полученный продукт подвергали ротации при 4°С в течение 1 часа. Белок G-сефарозу промывали шесть раз лизирующим буфером (1 мл) и затем ресуспендировали в 1 × буфере для образцов, содержащем ДСП. После обработки суспензии при 100°С в течение 5 минут раствор собирали для использования в качестве образца для ДСН-ПАГЭ. ДСН-ПАГЭ проводили таким же образом, как и в 2-2), и гель после электрофореза окрашивали с помощью СВВ. Часть, соответствующую 18 кДа, вырезали из геля после электрофореза и подвергали масс-спектрометрии. Результаты масс-спектрометрии показали, что указанная часть геля содержала клаудин-6.
2-4) Анализ методом сортировки клеток с активированной флуоресценцией (FACS)
Поскольку, согласно данным масс-спектрометрии, антигеном для антитела 218 В1 и антитела 218С7 является клаудин-6, был проведен анализ форсированной экспрессии с помощью трансфекции кДНК. Результаты анализа методом FACS показали, что антитело 218 В1 и антитело 218С7 демонстрировали сильный положительный ответ на клетки СНО-K1, экспрессирующие клаудин-6 человека, что показывает, что антигеном для антитела 218 В1 и антитела 218С7 является клаудин-6.
[0894]
Пример 132: Очистка антитела из культурального супернатанта гибридомы
Мышиную гибридому, продуцирующую антитело В1 к CLDN6 (218 В1), и мышиную гибридому, продуцирующую антитело С7 к CLDN6 (218С7), полученные в примере 131, культивировали в среде Hybridoma-SFM (Thermo Fisher Scientific), содержащей 10% эмбриональной бычьей сыворотки с ультранизким содержанием IgG (Thermo Fisher Scientific). Культуральный супернатант собирали путем центрифугирования и фильтровали через фильтр с диаметром пор 0,45 мкм (производства Coming Incorporated). Антитело очищали из культурального супернатанта в одну стадию с помощью аффинной хроматографии на сорбенте с рекомбинантным белком A (rProtein А) (при 4-6°С). Стадию замены буфера после аффинной хроматографии на rProtein А проводили при 4-6°С. Сначала культуральный супернатант наносили на колонку, заполненную MabSelectSuRe (производства GE Healthcare Bioscience), уравновешенную ФСБ. После того, как культуральный раствор полностью поступил в колонку, колонку промывали ФСБ в количестве, в два или более раза превышающем объем колонки. Затем проводили элюирование 2 М раствором гидрохлорида аргинина (pH 4,0) и собирали фракцию, содержащую антитело. Указанную фракцию подвергали замене растворителя на ФСБ (-) путем диализа (Thermo Scientific, Slide-A-Lyzer Dialysis Cassette). Затем фракцию концентрировали с помощью устройства Centrifugal UF Filter Device VIVASPIN20 (отсечение по молекулярной массе: UF10K, Sartorius AG, при 4°С) до достижения концентрации IgG 1 мг/мл или более. Полученную фракцию фильтровали через фильтр Minisart-Plus (Sartorius AG), и полученный продукт использовали в качестве очищенного образца.
[0895]
Пример 133: Оценка антител мыши к CLDN6 В1 и С7 in vitro
133-1: Оценка связывающей способности антител мыши к CLDN6 с помощью проточной цитометрии
Активность связывания антител мыши к CLDN6, полученных в примере 132, с CLDN6 человека и молекулами его семейства, CLDN3, CLDN4 и CLDN9, оценивали методом проточной цитометрии. Осуществляли временный перенос векторов CLDN3 человека/pCMV6-Entry, CLDN4 человека/pCMV6-Entry, CLDN6 человека/pCMV-Entry, CLDN9 человека/pCMV6-Entry или pCMV6-Entry, приобретенных у OriGene Technologies, Inc., в клетки 293Т (Thermo Fisher Scientific, HCL4517) с помощью липофектамина 2000 (Lipofectamine 2000, Thermo Fisher Scientific), и культивировали клетки в условиях 37°С и 5% CO2 в течение ночи, и затем готовили суспензию клеток. Полученную суспензию трансфицированных клеток 293Т центрифугировали для удаления супернатанта, и затем добавляли антитело мыши к CLDN6 (номер клона: В1 или С7) или контрольное антитело IgG1 мыши (R&D Systems, Inc.) и суспендировали до достижения конечной концентрации 30 мкг/мл, 10 мкг/мл, 3,3 мкг/мл или 1,1 мкг/мл, и полученный продукт оставляли при 4°С на 1 час. Клетки дважды промывали фосфатно-солевым буфером Дульбекко (Sigma-Aldrich Co. LLC), содержащим 5% эмбриональной бычьей сыворотки (Hyclone) (далее в настоящем описании называемым ФСБ, содержащим 5% ЭБС), и затем добавляли к ним конъюгированную с флюоресцеином фракцию IgG козы против IgG мыши (FLUORESCEIN-CONJUGATED GOAT IGG FRACTION TO MOUSE IGG (WHOLE MOLECULE), MP Biomedicals, Inc.), разбавленную в 500 раз ФСБ, содержащим 5% ЭБС, и клетки суспендировали и оставляли при 4°С на 1 час. После двукратной промывки ФСБ, содержащим 5% ЭБС, проводили детекцию с помощью проточного цитометра (FC500; Beckman Coulter, Inc.). Анализ данных проводили с использованием программного обеспечения FlowJo (Tree Star, Inc.). Для подтверждения каждой трансфекции клетки подвергали пермеабилизации с применением ФСБ, содержащего 0,25% Tween 20, и затем использовали антитело мыши к FLAG (Sigma-Aldrich Co. LLC). Результаты представлены на фигуре 40. На каждом графике на фигуре 40 ордината соответствует интенсивности флуоресценции FITC, отражающей количество связывающегося антитела, и абсцисса соответствует концентрациям антител. Полученные антитела мыши к CLDN6 связывались с CLDN6 человека и CLDN9 человека в одинаковой степени, и не связывались с CLDN3 человека или CLDN4 человека. Контрольное антитело IgG1 мыши не связывалось ни с одним видом клеток.
[0896]
133-2: Активность интернализации антител
Активность интернализации антител мыши к CLDN6 В1 и С7 оценивали с использованием реагента, содержащего антитело к IgG мыши, конъюгированное с токсином, который ингибирует синтез белка (сапорин), Mab-ZAP (Advanced Targeting Systems). В этом методе анализа Mab-ZAP включается в клетки в зависимости от активности интернализации антитела мыши к CLDN6, и сапорин, который ингибирует синтез белка, высвобождается в клетках, что приводит к подавлению роста клеток.
Клетки JEG-3(ATCC HTB-36), линию положительных по CLDN6 человека клеток хориокарциномы человека, клетки NIH:OVCAR-3 (ATCC НТВ-161), линию положительных по CLDN6 человека клеток рака яичника человека, или клетки В×РС-3 (ATCC CRL-1687), линию отрицательных по CLDN6 человека клеток рака поджелудочной железы человека, высевали в 96-луночный микропланшет для клеточных культур в концентрации 2×103 клеток/лунку и культивировали в условиях 37°С и 5% CO2 в течение ночи. На следующий день добавляли смешанный раствор, полученный путем смешивания каждого антитела мыши к CLDN6 или антитела мыши IgG1 (R&D Systems, Inc.) до конечной концентрации 1 нМ с Mab-ZAP (конечная концентрация: 0,5 нМ) или AffiniPure Goat Anti-Mouse IgG, Feγ Fragment Specific (Jackson ImmunoResearch Laboratories Inc.) (конечная концентрация: 0,5 нМ) без конъюгированного токсина, и клетки культивировали в условиях 37°С и 5% CO2 в течение 5 дней. Количество выживших клеток определяли путем количественной оценки активности АТФ с использованием люминесцентного теста для определения количества жизнеспособных клеток (Promega Corporation). Подавляющее рост клеток действие, достигаемое при добавлении каждого из антител к CLDN6, определяли как относительный уровень выживаемости, принимая за 100% значение для лунки, не содержащей смешанного раствора. Результаты представлены на фигуре 41. Было обнаружено, что антитела мыши к CLDN6 (B1, C7) оказывают подавляющее рост клеток действие на линии положительных по CLDN6 человека клеток JEG-3 и NIH:OVCAR-3. С другой стороны, было обнаружено, что они не оказывают подавляющего рост клеток действия на линию отрицательных по CLDN6 человека клеток В×РС-3. Было обнаружено, что антитело мыши IgG1 не оказывает подавляющего рост клеток действия ни на одну из линий клеток. Эти результаты позволяют предположить, что полученные антитела к CLDN6 (B1, C7) обладают способностью к интернализации, и каждое из них является подходящим в качестве антитела для конъюгатов антитело-лекарственное средство.
[0897]
Пример 134: Секвенирование нуклеотидов кДНК, кодирующей вариабельную область каждого из антител мыши к CLDN6 B1 и C7
134-1: Секвенирование нуклеотидов кДНК, кодирующей вариабельную область антитела B1
134-1-1: Получение общей РНК гибридомы, продуцирующей антитело B1
Для амплификации кДНК, кодирующей вариабельную область антитела В1, получали общую РНК гибридомы, продуцирующей антитело В1, с применением реагента TRIzol (Ambion).
134-1-2: Амплификация и секвенирование кДНК, кодирующей вариабельную область легкой цепи антитела В 1, посредством 5'-РАСЕ-ПЦР (Rapid Amplification of cDNA Ends PCR - ПЦР с быстрой амплификацией концов кДНК)
Амплификацию кДНК, кодирующей вариабельную область легкой цепи, проводили с использованием примерно 1 мкг общей РНК, полученной в примере 134-1-1, и набора SMARTer RACE++5'/3' Kit (Clontech). В качестве праймера для амплификации кДНК, кодирующей ген вариабельной области легкой цепи антитела В1, посредством ПЦР использовали UPM (Universal Primer A Mix: входит в набор SMARTer RACE 5'/3' Kit) и праймер, созданный на основе последовательности известной константной области легкой цепи антитела мыши.
кДНК, кодирующую вариабельную область легкой цепи, амплифицированную посредством 5'-RACE-ПЦР, клонировали в плазмиду, и затем проводили секвенирование нуклеотидной последовательности кДНК, кодирующей вариабельную область легкой цепи.
Определенная нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела В1, представлена SEQ ID NO: 18, и соответствующая аминокислотная последовательность представлена SEQ ID NO:
19.
134-1-3: Амплификация и секвенирование кДНК, кодирующей вариабельную область тяжелой цепи антитела В1, посредством 5'-РАСЕ-ПЦР
Амплификацию кДНК, кодирующей вариабельную область тяжелой цепи, проводили с использованием примерно 1 мкг общей РНК, полученной в примере 134-1-1, и набора SMARTer RACE 5'/3' Kit (Clontech). В качестве праймера для амплификации кДНК, кодирующей ген вариабельной области тяжелой цепи антитела LB1, посредством ПЦР использовали UPM (Universal Primer A Mix: входит в набор SMARTer RACE++5'/3' Kit) и праймер, созданный на основе последовательности известной константной области тяжелой цепи антитела мыши.
кДНК, кодирующую вариабельную область тяжелой цепи, амплифицированную посредством 5'-RACE-ПНР, клонировали в плазмиду, и затем проводили секвенирование нуклеотидной последовательности кДНК, кодирующей вариабельную область тяжелой цепи.
Определенная нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела В1, представлена SEQ ID NO: 20, и соответствующая аминокислотная последовательность представлена SEQ ID NO: 21.
134-2: Секвенирование нуклеотидов кДНК, кодирующей вариабельную область антитела С7
Секвенирование нуклеотидов проводили таким же образом, как в примере 134-1. Определенная нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела С7, представлена SEQ ID NO: 22, и соответствующая аминокислотная последовательность представлена SEQ ID NO: 23. Нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела С7, представлена SEQ ID NO: 24, и соответствующая аминокислотная последовательность представлена SEQ ID NO: 25.
[0898]
Пример 135: Получение химерного антитела к CLDN6 chB1
135-1: Конструирование вектора экспрессии для химерного антитела к CLDN6 chB1
135-1-1: Конструирование вектора экспрессии pCMA-LK для химерных и гуманизированных легких цепей
Примерно 5,4 т.п.н. фрагмента, полученного путем расщепления плазмиды pcDNA3.3-TOPO/LacZ (Invitrogen) рестриктазами XbaI и PmeI, соединяли с фрагментом ДНК, содержащим последовательность ДНК, кодирующую сигнальную последовательность легкой цепи человека и константную область κ-цепи человека, представленным SEQ ID NO: 26, с помощью набора In-Fusion HD PCR Cloning Kit (Clontech) с получением pcDNA3.3/LK. Для конструирования pCMA-LK из pcDNA3.3/LK удаляли единицу экспрессии устойчивости к неомицину.
135-1-2: Конструирование вектора экспрессии pCMA-G1LALA для химерных и гуманизированных тяжелых цепей типа IgG1LALA
Фрагмент ДНК, полученный путем расщепления pCMA-LK под действием XbaI и PmeI для удаления сигнальной последовательности легкой цепи и константной области κ-цепи человека, соединяли с фрагментом ДНК, содержащим последовательность ДНК, кодирующую сигнальную последовательность тяжелой цепи человека и константную область IgG1LALA человека, представленным SEQ ID NO: 27, с помощью набора In-Fusion HD PCR Cloning Kit (Clontech) для конструирования pCMA-GlLALA.
135-1-3: Конструирование вектора экспрессии тяжелой цепи химерного chB1
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 36-440 нуклеотидной последовательности для тяжелой цепи chB1, представленной SEQ ID NO: 33 (GeneArt). pCMA-G1LALA подвергали расщеплению рестриктазой BipI, и синтезированный фрагмент ДНК вставляли в расщепленную часть с помощью набора In-Fusion HD PCR Cloning Kit (Clontech) для конструирования вектора экспрессии тяжелой цепи chB1. Аминокислотная последовательность тяжелой цепи chB1 представлена SEQ ID NO: 32.
135-1-4: Конструирование вектора экспрессии легкой цепи химерного chB1
Синтезировали фрагмент ДНК, содержащий последовательность ДНК, кодирующую легкую цепь chBl, представленный SEQ ID NO: 29 (GeneArt). С помощью набора In-Fusion HD PCR Cloning Kit (Clontech) синтезированный фрагмент ДНК соединяли с фрагментом ДНК, полученным путем расщепления pCMA-LK под действием XbaI и PmeI для удаления сигнальной последовательности легкой цепи и константной области κ-цепи человека для конструирования вектора экспрессии легкой цепи chB1. Аминокислотная последовательность легкой цепи chBl представлена SEQ ID NO: 28.
135-2: Получение и очистка химерного антитела к CLDN6 chB1
135-2-1: Получение химерного антитела chB1
Клетки FreeStyle 293F (Invitrogen) высевали и культивировали в соответствии с руководством по применению. В колбу Фернбаха/Эрленмейера объемом 3 л (Coming Incorporated) высевали 1,2×109 клеток FreeStyle 293F (Invitrogen) в логарифмической фазе роста и разбавляли средой для экспрессии FreeStyle293 (Invitrogen) до достижения концентрации 2,0×106 клеток/мл. К 40 мл среды Opti-Pro SFM (Invitrogen) добавляли 0,24 мг вектора экспрессии тяжелой цепи, 0,36 мг вектора экспрессии легкой цепи и 1,8 мг полиэтиленимина (Polyscience, Inc., #24765) и осторожно перемешивали, и затем оставляли на 5 минут, и затем добавляли полученную смесь к клеткам FreeStyle 293F. После культивирования при встряхивании при 90 об./мин в инкубаторе при 37°С и 8% CO2 в течение 4 часов добавляли 600 мл среды EX-CELL VPRO (SAFC Biosciences, Inc.), 18 мл добавки GlutaMAX I (Gibco) и 30 мл ультрафильтрата дрожжевого экстракта (Gibco), и полученный продукт культивировали при встряхивании при 90 об./мин в инкубаторе при 37°С и 8%CO2 в течение 7 дней, и полученный культуральный супернатант фильтровали через одноразовый капсульный фильтр (ADVANTEC, #CCS-045-E1H). Полученное химерное антитело к CLDN6 обозначали как «chB1».
135-2-2: Очистка химерного антитела chB1
Антитело очищали из культурального супернатанта, полученного в примере 135-2-1, в одну стадию с помощью аффинной хроматографии на rProtein A. Культуральный супернатант наносили на колонку, заполненную MabSelectSuRe (производства GE Healthcare Bioscience), уравновешенную ФСБ, и затем колонку промывали ФСБ в количестве, в два или более раза превышающем объем колонки. Затем проводили элюирование 2 М раствором гидрохлорида аргинина (pH 4,0) и собирали фракцию; содержащую антитело. Антитело подвергали замене буфера на ФСБ (-) путем диализа (Thermo Scientific, Slide-A-Lyzer Dialysis Cassette). Полученную фракцию концентрировали с помощью устройства Centrifugal UF Filter Device VIVASPIN20 (отсечение по молекулярной массе: UF10K, Sartorius AG) до достижения концентрации IgG 1 мг/мл или более. Затем полученную фракцию фильтровали через фильтр Minisart-Plus (Sartorius AG), и полученный продукт использовали в качестве очищенного образца.
[0899]
Пример 136: Получение гуманизированного антитела к С LDN6 136-1: Конструирование гуманизированной формы антитела к CLDN6
136-1-1: Молекулярное моделирование вариабельной области химерного антитела chB1
Для молекулярного моделирования вариабельной области chB1 применяли способ, известный как гомологичное моделирование (Methods in Enzymology, 203, 121-153 (1991)). Молекулярное моделирование осуществляли с помощью коммерчески доступной программы конформационного анализа белка BioLuminate (Schrodinger, Inc.) с использованием в качестве матрицы структуры (PDB ID: 1XIW), зарегистрированной в Protein Data Bank (Nuc. Acid Res. 35, D301-D303 (2007)), имеющей высокую степень идентичности последовательностей с вариабельными областями тяжелой цепи и легкой цепи chB1.
136-1-2: Конструирование гуманизированной аминокислотной последовательности
chB1 гуманизировали путем прививки CDR (CDR grafting) (Proc. Natl. Acad. Sci. USA 86, 10029-10033 (1989)). Консенсусная последовательность гамма-цепи подгруппы 1 человека и консенсусная последовательность каппа-цепи подгруппы 1 человека, определенные в источнике Kabat et al. (Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service National Institutes of Health, Bethesda, MD. (1991)), имели высокую идентичность с каркасными участками chB1, и, следовательно, были выбраны в качестве акцепторов для тяжелой цепи и легкой цепи, соответственно. Донорные остатки, которые должны быть перенесены на акцепторы, выбирали путем анализа трехмерной модели, например, согласно критериям, предложенным Queen et al. (Proc. Natl. Acad. Sci. USA 86, 10029-10033 (1989)). Поскольку CDRL3 была богата гидрофобными аминокислотами, дополнительно конструировали гуманизированную легкую цепь с мутацией в CDRL3.
136-2: Гуманизация тяжелой цепи chB1
Три сконструированные тяжелые цепи обозначали как hH1, hH2 и hH3. Полноразмерная аминокислотная последовательность тяжелой цепи hH1 представлена SEQ ID NO: 52 (фигура 34). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 52, представлена SEQ ID NO: 53 (фигура 34). Полноразмерная аминокислотная последовательность тяжелой цепи hH2 представлена SEQ ID NO: 56 (фигура 36). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 56, представлена SEQ ID NO: 57 (фигура 36). Полноразмерная аминокислотная последовательность тяжелой цепи hH3 представлена SEQ ID NO: 60 (фигура 38). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 60, представлена SEQ ID NO: 61 (фигура 38).
На фигуре 45 показано сравнение аминокислотных последовательностей chB1_H, которая представляет собой тяжелую цепь химерного антитела человека к CLDN6 chBl, представленного в примере 135, и тяжелых цепей гуманизированного антитела hH1, hH2 и hH3. Каждый символ «⋅» в последовательностях hH1, hH2 и hH3 обозначает аминокислотный остаток, идентичный остатку chB1_H в указанном положении, и каждое положение с буквенным символом аминокислотного остатка обозначает, что аминокислотный остаток является замещенным аминокислотным остатком.
136-3: Гуманизация легкой цепи chB1
Четыре сконструированные легкие цепи обозначали как hL1, hL2, hL3 и hL4. Полноразмерная аминокислотная последовательность легкой цепи hL1 представлена SEQ ID NO: 36 (фигура 26). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 36, представлена SEQ ID NO: 37 (фигура 26). Полноразмерная аминокислотная последовательность легкой цепи hL2 представлена SEQ ID NO: 40 (фигура 28). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 40, представлена SEQ ID NO: 41 (фигура 28). Полноразмерная аминокислотная последовательность легкой цепи hL3 представлена SEQ ID NO: 44 (фигура 30). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 44, представлена SEQ ID NO: 45 (фигура 30). Полноразмерная аминокислотная последовательность легкой цепи hL4 представлена SEQ ID NO: 48 (фигура 32). Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 48, представлена SEQ ID NO: 49 (фигура 32).
На фигуре 46 показано сравнение аминокислотных последовательностей chB1_L, которая представляет собой легкую цепь химерного антитела человека к CLDN6 chB1, представленного в примере 135, и легких цепей гуманизированного антитела hL1, hL2, hL3 и hL4. Каждый символ «⋅» в последовательностях hL1, hL2, hL3 и hL4 обозначает аминокислотный остаток, идентичный остатку chB1_L в указанном положении, и каждое положение с буквенным символом аминокислотного остатка обозначает, что аминокислотный остаток является замещенным аминокислотным остатком.
136-4: Конструирование гуманизированного антитела с комбинацией тяжелой цепи и легкой цепи Антитело, состоящее из hH1 и hL1, обозначено как «антитело H1L1» или «H1L1». Антитело, состоящее из hH2 и hL2, обозначено как «антитело H2L2» или «H2L2». Антитело, состоящее из hH1 и hL3, обозначено как «антитело H1L3» или «H1L3». Антитело, состоящее из hH2 и hL4, обозначено как «антитело H2L4» или «H2L4». Антитело, состоящее из hH3 и hL3, обозначено как «антитело H3L3» или «H3L3».
136-5: Получение гуманизированного антитела к CLDN6
136-5-1: Конструирование вектора экспрессии гуманизированной тяжелой цепи
136-5-1-1: Конструирование вектора экспрессии hH1
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 36-440 нуклеотидной последовательности SEQ ID NO: 53 для hH1 (GeneArt). Вектор экспрессии hH1 конструировали таким же образом, как и в примере 135-1-3.
136-5-1-2: Конструирование вектора экспрессии hH2
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 36-440 нуклеотидной последовательности SEQ ID NO: 57 для hH2 (GeneArt). Вектор экспрессии hH2 конструировали таким же образом, как и в примере 135-1-3.
136-5-1-3: Конструирование вектора экспрессии hH3
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 36-440 нуклеотидной последовательности SEQ ID NO: 61 для hH3 (GeneArt). Вектор экспрессии hH3 конструировали таким же образом, как и в примере 135-1-3.
136-5-2: Конструирование вектора экспрессии гуманизированной легкой цепи
136-5-2-1: Конструирование вектора экспрессии hL1
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 37-402 нуклеотидной последовательности SEQ ID NO: 37 для hL1 (GeneArt). pCMA-LK подвергали расщеплению рестриктазой BsiWI, и синтезированный фрагмент ДНК вставляли в расщепленную часть с помощью набора In-Fusion HD PCR Cloning Kit (Clontech) для конструирования вектора экспрессии hL1.
136-5-2-2: Конструирование вектора экспрессии hL2
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 37-402 нуклеотидной последовательности SEQ ID NO: 41 для hL2 (GeneArt). Вектор экспрессии hL2 конструировали таким же образом, как и в примере 136-5-2-1.
136-5-2-3: Конструирование вектора экспрессии hL3
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 37-402 нуклеотидной последовательности SEQ ID NO: 45 для hL3 (GeneArt). Вектор экспрессии hL3 конструировали таким же образом, как и в примере 136-5-2-1.
136-5-2-4: Конструирование вектора экспрессии hL4
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 37-402 нуклеотидной последовательности SEQ ID NO: 49 для hL4 (GeneArt). Вектор экспрессии hL4 конструировали таким же образом, как и в примере 136-5-2-1.
136-5-3: Получение гуманизированных антител
136-5-3-1: Получение гуманизированных антител H1L1, H2L2, H1L3, H2L4 HH3L3
Их получали таким же образом, как и в примере 135-2-1. H1L1, H2L2, H1L3, H2L4 и H3L3 получали с применением комбинаций вектора экспрессии тяжелой цепи и вектора экспрессии легкой цепи, соответствующих комбинациям тяжелой цепи и легкой цепи, представленным в примере 136-4.
136-5-3-2: Двухстадийная очистка гуманизированных антител H1L1, H2L2, H1L3, H2L4 и H3L3
Культуральный супернатант, полученный в примере 136-5-3-1, очищали в две стадии с помощью аффинной хроматографии на rProtein А и керамическом гидроксиапатите. Культуральный супернатант наносили на колонку, заполненную MabSelectSuRe (производства GE Healthcare Bioscience), уравновешенную ФСБ, и затем колонку промывали ФСБ в количестве, в два или более раза превышающем объем колонки. Затем элюировали антитело 2 М раствором гидрохлорида аргинина (pH 4,0). Фракцию, содержащую антитело, подвергали замене буфера на ФСБ путем диализа (Thermo Scientific, Slide-A-Lyzer Dialysis Cassette), разбавляли в 5 раз буфером, содержащим 5 мМ фосфат натрия/50 мМ MES/pH 7,0, и затем наносили на колонку с керамическим гидроксиапатитом (Bio-Rad Laboratories Japan, Inc., Bio-Scale CHT Type-1 Hydro xyapatite Column), уравновешенную буфером, содержащим 5 мМ NaPi/50 мМ MES/30 мМ NaCl/рН 7,0. Проводили элюцию линейным градиентом концентрации хлорида натрия, и собирали фракцию, содержащую антитело. Указанную фракцию подвергали замене буфера на HBSor (25 мМ гистидин/5% сорбитол, pH 6,0) путем диализа (Thermo Scientific, Slide-A-Lyzer Dialysis Cassette). Антитело концентрировали с помощью устройства Centrifugal UF Filter Device VIVASPIN20 (отсечение по молекулярной массе: UF10K, Sartorius AG) до достижения концентрации IgG 50 мг/мл. Затем полученную фракцию фильтровали через фильтр Minisart-Plus (Sartorius AG), и полученный продукт использовали в качестве очищенного образца.
[0900]
Пример 137: Оценка связывающей способности гуманизированного антитела к CLDN6 с помощью проточной цитометрии
Активность связывания гуманизированного антитела к CLDN6, полученного в примере 136, с CLDN6 человека и молекулами его семейства, CLDN3, CLDN4 и CLDN9, оценивали методом проточной цитометрии. Использовали клетки 293Т, временно трансфицированные таким же образом, как и в примере 133-1. К клеткам, в которые был перенесен ген CLDN6 человека или CLDN9 человека, добавляли гуманизированное антитело к CLDN6 H1L1, H2L2, H1L3, H2L4 или H3L3 или контрольное антитело IgG1 человека (Calbiochem) и суспендировали до достижения конечной концентрации 100 нМ, 20 нМ, 4 нМ или 0,8 нМ, и полученный продукт оставляли при 4°С на 30 минут. К клеткам, в которые был перенесен ген CLDN3 человека или CLDN4 человека или пустой вектор, добавляли гуманизированное антитело к CLDN6 H1L1, H2L2, H1L3, H2L4 или H3L3 и суспендировали до достижения конечной концентрации 100 нМ, и полученный продукт оставляли при 4°С на 30 минут. Клетки промывали фосфатно-солевым буфером Дульбекко (Sigma-Aldrich Co. LLC), содержащим 5% эмбриональной бычьей сыворотки (Hyclone) (далее в настоящем описании называемым ФСБ, содержащим 5% ЭБС), и затем к ним добавляли реагент FITC AffiniPureF (ab')2 Fragment Goat Anti-Human IgG (H+L) (Jackson ImmunoResearch Laboratories Inc.), разбавленный в 150 раз ФСБ, содержащим 5% ЭБС, и клетки суспендировали и оставляли при 4°С на 30 минут. После промывки ФСБ, содержащим 5% ЭБС, проводили обнаружение с помощью проточного цитометра (FC500; Beckman Coulter, Inc.). Анализ данных проводили с помощью программного обеспечения FlowJo (Tree Star, Inc.), и рассчитывали среднюю интенсивность флуоресценции (MFI) FITC, которая отражает количество связывающегося антитела. Результаты представлены на фигуре 42. На каждом графике на фигуре 42 абсцисса соответствует концентрациям антител, и ордината соответствует MFI. Полученное гуманизированное антитело к CLDN6 связывалось с CLDN6 человека и CLDN9 человека в одинаковой степени, и не связывалось с CLDN3 человека или CLDN4 человека. Контрольное антитело IgG1 человека не связывалось ни с одним видом клеток.
[0901]
Пример 138: Получение варианта трастузумаба
138-1: Конструирование вектора экспрессии тяжелой цепи для трастузумаба- LALA
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 36-434 нуклеотидной последовательности SEQ ID NO: 74 для тяжелой цепи трастузумаба-LALA (GeneArt). Вектор экспрессии конструировали таким же образом, как и в примере 135-1-3. Аминокислотная последовательность тяжелой цепи трастузумаба-LALA представлена SEQ ID NO: 75.
138-2: Конструирование вектора экспрессии легкой цепи для трастузумаба-LALA
Синтезировали фрагмент ДНК, состоящий из нуклеотидных остатков 37-402 нуклеотидной последовательности SEQ ID NO: 72 для легкой цепи трастузумаба-LALA (GeneArt). Вектор экспрессии конструировали таким же образом, как и в примере 136-5-2-1. Аминокислотная последовательность легкой цепи трастузумаба-LALA представлена SEQ ID NO: 73.
138-3: Получение варианта трастузумаба
Вариант трастузумаба получали таким же образом, как и в примере 135-2-1.
138-4: Очистка варианта трастузумаба
Трастузумаб-LALA очищали из культурального супернатанта, полученного в примере 138-3, таким же образом, как и в примере 135-2-2, за исключением того, что проводили замену буфера не на ФСБ (-), а на 50 мМ фосфатный буферный раствор (pH 6,0).
[0902]
Пример 139: Ремоделирование углеводной цепи (вариант трастузумаба-MSG1) Стадия 1: (Fucα1,6)GlcNAc-вариант трастузумаба
Проводили операцию, описанную для стадии 1 в примере 58, с использованием раствора варианта трастузумаба с концентрацией примерно 22,3 мг/мл (50 мМ фосфатный буфер (рН 6,0)) (2,7 мл), полученного в примере 138, с получением раствора (Fucα1,6)GlcNAc-варианта трастузумаба с концентрацией 6,1 мг/мл (50 мМ фосфатный буфер (pH 6,0)) (6,1 мл).
[0903]
Стадия 2: Вариант трастузумаба-[MSG1-N3]2
Проводили операцию, описанную для стадии 1 в примере 60, с использованием раствора (Fucα1,6)GlcNAc-варианта трастузумаба с концентрацией примерно 6,1 мг/мл (50 мМ фосфатный буфер (pH 6,0)) (6,1 мл), полученного на стадии 1, с получением раствора варианта трастузумаба-[MSG1-N3]2 с концентрацией 10,2 мг/мл (фосфатно-солевой буфер (pH 6,0)) (3,7 мл).
[0904]
Пример 140: ADC55
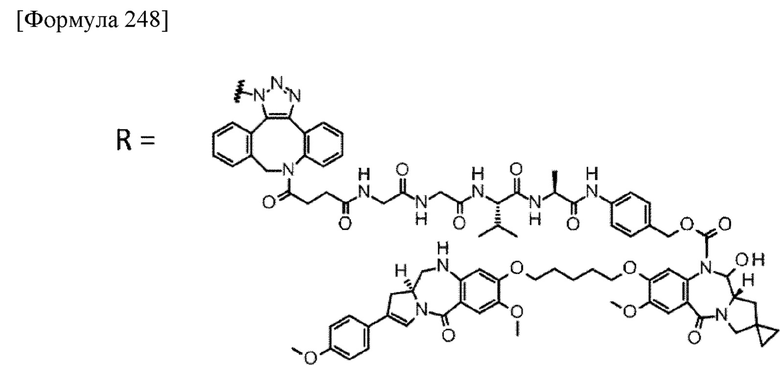
или
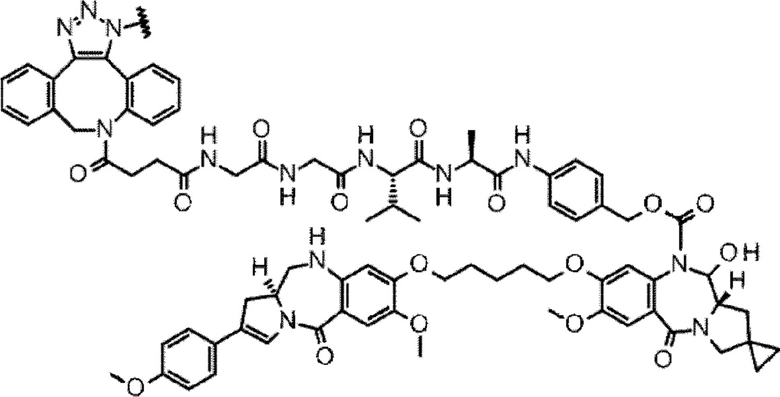
(Соединение, которое должно быть получено на стадии 1, имеет геометрические изомеры триазольного кольца, как показано на этой формуле, и соединение, полученное на стадии 1 примера 140, сохраняет линкер в виде смеси двух структур, представленных выше в качестве R.)
Стадия 1: Конъюгирование антитела и фрагмента лекарственное средство-линкер
К раствору антитела, полученного на стадии 2 примера 139, в фосфатно-солевом буфере (pH 6,0) (10,2 мг/мл, 0,40 мл) при комнатной температуре добавляли фосфатно-солевой буфер (pH 6,0) (0,40 мл), 1,2-пропандиол (0,767 мл), диметилформамид (0,20 мл) и 10 мМ раствор в диметилформамиде соединения, полученного на стадии 13 примера 3 (0,033 мл; 12 эквивалентов на молекулу антитела), и полученную смесь подвергали реакции при комнатной температуре на ротационном перемешивателе для пробирок (MTR-103, AS ONE Corporation) в течение 48 часов.
Операция очистки: Раствор очищали с использованием общей операции D с получением 7,00 мл раствора, содержащего целевое соединение. Характеристика: Следующий характеристические значения были получены с использованием общих операций Е и F.
Концентрация антитела: 0,39 мг/мл, выход антитела: 1,38 мг (35%), среднее число конъюгированных молекул лекарственного средства на молекулу антитела (n): 1,8
[0905]
Пример 141: Противоклеточное действие конъюгата антитело к HER2-лекарственное средство
Клетки KPL-4 (Dr. Junichi Kurebayashi, Kawasaki Medical School), линию HER2-антиген-положительных клеток рака молочной железы человека, готовили в среде RPMI1640 (Thermo Fisher Scientific; далее в настоящем описании называемой средой RPMI), содержащей 10% эмбриональной бычьей сыворотки (Hyclone), до достижения концентрации 6,25×103 клеток/мл, и их аликвоты объемом 80 мкл добавляли в 96-луночный микропланшет для клеточных культур. После добавления клеток клетки культивировали при 37°С и 5% CO2 в течение ночи.
На следующий день в микропланшет добавляли аликвоты конъюгата антитело к HER2-лекарственное средство объемом 20 мкл, разбавленные средой RPMI до 100 нМ, 20 нМ, 4 нМ, 0,8 нМ, 0,16 нМ, 0,032 нМ, 6,4 пМ, 1,3 пМ и 0,26 пМ. В каждую лунку, не содержащую какого-либо конъюгата антитело-лекарственное средство, добавляли 20 мкл среды RPMI. Клетки KPL-4 культивировали при 37°С и 5% CO2 в течение 6 дней. После культивирования микропланшет вынимали из инкубатора и оставляли при комнатной температуре на 30 минут. Добавляли люминесцентный тест для определения количества жизнеспособных клеток (Promega Corporation) в количестве, эквивалентном количеству культурального раствора, и перемешивали с помощью шейкера для планшетов. Микропланшет оставляли при комнатной температуре на 10 минут и затем определяли величину испускания с помощью планшетного ридера (PerkinElmer). Уровни выживаемости клеток рассчитывали таким же образом, как и в примере 123.
Каждый из конъюгатов антитело к HER2-лекарственное средство ADC49 и ADC55 проявлял противоклеточное действие в отношении клеток KPL-4 с 0,001<IC50<0,01 (нМ).
[0906]
Пример 142: Оценка противоопухолевого действия конъюгата антитело к HER2-лекарственное средство (1)
Противоопухолевое действие конъюгатов антитело к НЕР2-лекарственное средство определяли с использованием тех же экспериментальных животных и применением того же способа, что и в примере 124.
Клетки KPL-4 (Dr. Junichi Kurebayashi, Kawasaki Medical School) суспендировали в фосфатно-солевом буфере Дульбекко (Sigma-Aldrich Co. LLC), и 1,5×107 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 14 день мышей случайным образом распределяли по группам. Конъюгат антитело к HER2-лекарственное средство ADC49 или конъюгат антитело к HER2-лекарственное средство ADC55 вводили в хвостовую вену на 14 день в дозе 0,33 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 47. ADC49 и ADC55 проявляли сравнимую противоопухолевую активность при введении в дозе 0,33 мг/кг. Не было обнаружено снижения массы тела мышей, обусловленного введением ADC49 или ADC55.
[0907]
Пример 143: Оценка противоопухолевого действия конъюгата антитело к HER2- лекарственное средство (2)
Клетки JIMT-1 (DSMZ АСС 589) суспендировали в физиологическом солевом растворе (Otsuka Pharmaceutical Factory, Inc.), и 5×106 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 11 день мышей случайным образом распределяли по группам. ADC55 вводили в хвостовую вену на 11 день в дозе 0,4 мг/кг или 0,2 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 48. Было обнаружено, что ADC55 обладает сильным противоопухолевым действием, вызывающим регрессию опухоли, при введении в дозе 0,4 мг/кг. При введении любой из указанных доз не было обнаружено снижения массы тела мышей, обусловленного введением ADC55. [0908]
Пример 144: Оценка противоопухолевого действия конъюгата антитело к HER2-лекарственное средство (3)
Клетки CFPAC-1 (ATCC CRL-1918) суспендировали в физиологическом солевом растворе (Otsuka Pharmaceutical Factory, Inc.), и 5×106 клеток подкожно трансплантировали в правый бок каждой самки бестимусной мыши (день 0), и на 10 день мышей случайным образом распределяли по группам. Конъюгат антитело к НЕР2-лекарственное средство ADC49 или ADC55, или конъюгат антитело к LPS-лекарственное средство ADC53 вводили в хвостовую вену на 10 день в дозе 0,4 мг/кг. Контрольной группе (группе, получавшей носитель) таким же образом вводили буфер ABS.
Результаты представлены на фигуре 49. Было обнаружено сильное противоопухолевое действие, вызывающее регрессию опухоли, для любых мышей, которым вводили ADC49 или ADC55. Снижения массы тела мышей, обусловленного введением ADC49, ADC55 или ADC53, обнаружено не было.
[0909]
Пример 145: Лекарственное средство-линкер 43
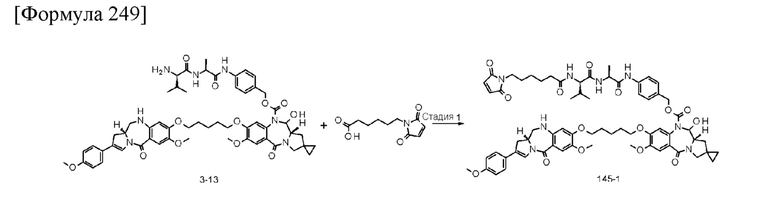
К раствору соединения, полученного на стадии 12 примера 3 (0,051 г, 0,049 ммоль), и коммерчески доступной малеимидокапроновой кислоты (0,011 г, 0,054 ммоль) в дихлорметане (5 мл) добавляли 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид (0,010 г, 0,054 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 2 часов. После этого реакционный раствор разбавляли хлороформом, органический слой промывали водой и сушили над сульфатом натрия. После этого органический растворитель концентрировали, полученный остаток очищали с помощью хроматографии на силикагеле (хлороформ: метанол=97,5:2,5 (об./об.) до 90:10 (об./об.)), получая желаемое соединение (41 мг, 69%).
1H-ЯМР(ДМСО-D6) δ: 9,94(1Н,s), 8,20-8,12(1Н,m), 7,86-7,77(1Н,m), 7,65-7,52(2H,m), 7,45(1H,s),7,38(2H,d,J=7,9 Гц), 7,30(1H,s), 7,24-7,16(2H,m), 7,11-7,01(1H,m), 7,00(2H,s), 6,91(2H,d,J=8,5 Гц), 6,83-6,67(1H,m), 6,63-6,45(2H,m), 6,31(1H,s), 5,81-5,71(1H,m), 5,23-5,14(1H,m), 4,86-4,74(1H,m), 4,43-4,32(1Н,m), 4,24-4,11(2Н,m), 4,03-3,88(3Н,m), 3,88-3,69(4H,m), 3,76(3H,s), 3,66(3H,s), 3,60-3,49(2H,m), 3,47-3,08(5H,m), 2,82-2,64(1Н,M), 2,40-2,29(1Н,m), 2,25-2,04(2Н,m), 2,04-1,89(1Н,m), 1,88-1,67(4Н,m), 1,63-1,38(7Н,m), 1,35-1,09(6Н,m), 0,90-0,76(6Н,m), 0,76-0,50(4Н,m).
МС (ХИАД, ИЭР) m/z:1224(M+H)+
Конъюгат (ADC) антитело к CLDN6 (пример 136 (H1L1))-PBD (конъюгация с цистеином, m1=2) лекарственного средства-линкера 43 и лекарственного средства-линкера 44 (пример 146) получали с использованием известного способа (WO 2014/057687). Полученный ADC проявлял сильное противоопухолевое действие.
[0910]
Пример 146: Лекарственное средство-линкер 44
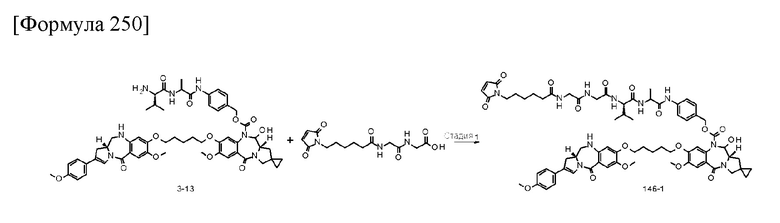
Соединение, полученное на стадии 12 примера 3 (0,047 г, 0,046 ммоль) и коммерчески доступный N-[6-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)гексаноил]глицилглицин (0,016 г, 0,050 ммоль) подвергали реакции таким же образом, как и в примере 145, получая желаемое соединение (30 мг, 50%).
1Н-ЯМР(ДМСО-D6) δ: 9,92(1Н,s), 8,23(1Н,d,J=6,7 Гц), 8,12-8,02(2H,m), 7,84(1H,d,J=9,1 Гц), 7,65-7,50(2H,m), 7,45(1H,s), 7,38(2H,d,J=9,1 Гц), 7,30(1H,s), 7,26-7,16(2H,m), 7,10-7,02(1H,m), 7,00(2H,s), 6,91(2H,d,J=9,1 Гц), 6,82-6,67(1H,m), 6,62-6,48(2H,m), 6,31(1H,s), 5,80-5,72(1H,m), 5,25-5,15(1H,m), 4,85-4,77(1H,m), 4,43-4,30(1H,m), 4,25-4,14(2H,m), 4,06-3,87(3H,m), 3,86-3,71(6H,m), 3,76(3H,s), 3,71-3,62(2H,m), 3,66(3H,s), 3,61-3,45(2H,m), 3,45-3,08(1H,m), 2,81-2,64(2H,m), 2,39-2,29(1H,m), 2,14-2,04(2H,m), 2,05-1,90(1H,m), 1,90-1,68(1H,m), 1,62-1,39(7H,m), 1,35-1,26(6H,m), 1,26-1,13(6H,m), 0,91-0,77(6H,m) 0,75-0,52(4H,m).
MC (ХИАД, ИЭР) m/z: 1338(M+H)+
[0911]
Пример 147: Лекарственное средство-линкер 45
[Формула 251]
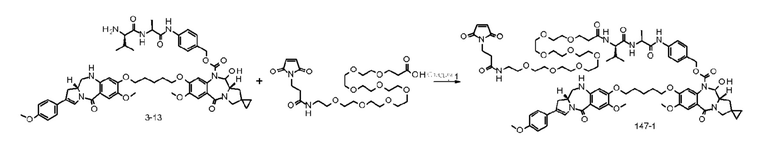
Соединение, полученное на стадии 12 примера 3 (0,050 г, 0,049 ммоль), и коммерчески доступную 31-(2,5-диоксо-2,5-дигидро-1H-пиррол-1-ил)-29-оксо-4,7,10,13,16,19,22,25-октаокса-28-азагентриаконтан-1-оевую кислоту (0,029 г, 0,049 ммоль) подвергали реакции таким же образом, как и в примере 145, получая желаемое соединение (45 мг, 57%).
МС (ХИАД, ИЭР) m/z: 1604 (М+Н)+
[0912]
Пример 148: Лекарственное средство-линкер 46
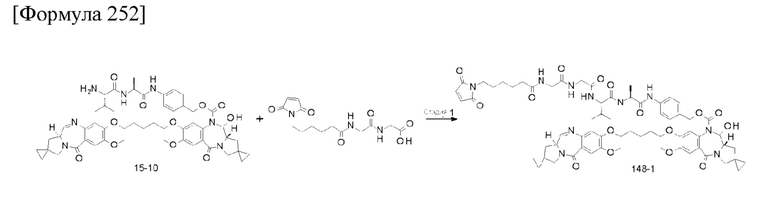
Соединение, полученное на стадии 9 примера 15 (0,081 г, 0,085 ммоль), и коммерчески доступный N-[6-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)гексаноил]глицилглицин (0,042 г, 0,13 ммоль) подвергали реакции таким же образом, как и на стадии 1 примера 16, получая желаемое соединение (0,089 г, 82%).
МС (ХИАД, ИЭР) m/z: 1257 (М+Н)+
[0913]
Пример 149: Лекарственное средство-линкер 47
[Формула 253]
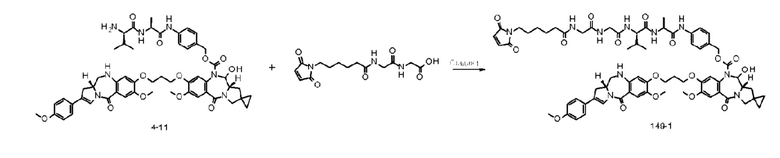
К раствору коммерчески доступного N-[6-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)гексаноил]глицилглицина (0,036 г, 0,11 ммоль) в дихлорметане (10 мл) добавляли N-этоксикарбонил-2-этокси-1,2-дигидрохинолин (0,035 г, 0,14 ммоль) при комнатной температуре и полученный продукт перемешивали при комнатной температуре в течение 1 часа. К реакционному раствору добавляли соединение, полученное на стадии 11 примера 4 (0,10 г, 0,10 ммоль), и метанол (1 мл) и полученный продукт перемешивали при комнатной температуре в течение 18 часов. После этого реакционный раствор концентрировали, полученный остаток очищали с помощью хроматографии на силикагеле (хлороформ - хлороформ:метанол=80:20 (об./об.)), получая желаемое соединение (0,078 г, 60%).
МС (ХИАД, ИЭР) m/z:1309 (M+H)+
[0914]
Пример 150: Лекарственное средство 11
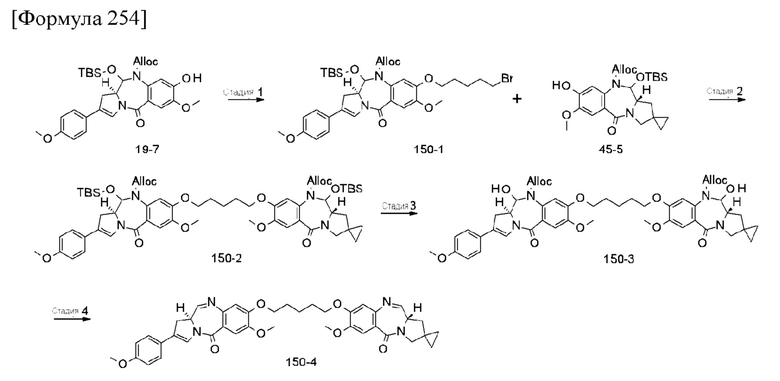
[Стадии 1-4]
Соединение, полученное на стадии 7 примера 19, подвергали реакции таким же образом, как и на стадии 2 примера 3, стадии 10 примера 3, стадии 11 примера 3 и стадии 12 примера 3, получая лекарственное средство 11.
1H-ЯМР(CDCl3) δ: 7,89-7,80(1H,m), 7,60-7,51(2H,m), 7,43-7,40(1H,m), 7,34-7,30(2Н,m), 6,91-6,88(2Н,m), 6,81(1Н,d,J=3,0 Гц), 4,39-4,32(1Н,m), 4,11-4,06(4H,m), 3,95(4H,d,J=3,0 Гц), 3,87-3,84(5H,m), 3,68-3,61(2H,m), 3,51-3,49(3H,m), 3,44-3,34(2H,m), 2,53(1H,dd,J=13,0,8,2 Гц), 2,01-1,96(4H,m), 1,69-1,68(2Н,m), 1,30-1,25(1Н,m), 0,93-0,77(4Н,m).
MC (ХИАД, ИЭР) m/z: 691(M+H)+.
[0915]
Пример 151: Лекарственное средство 12
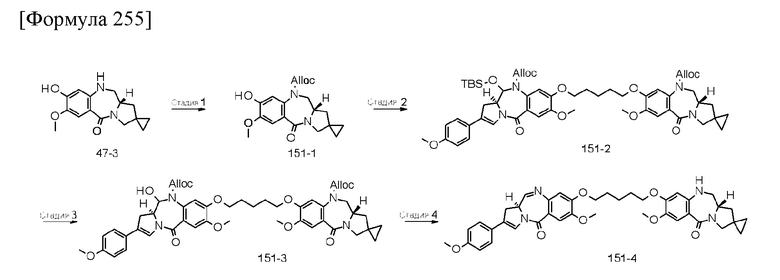
[Стадия 1]
Соединение, полученное на стадии 3 примера 47 (0,77 г, 2,8 ммоль), растворяли в дихлорметане (20 мл) и к нему добавляли пиридин (0,338 мл, 4,20 ммоль) и аллилхлорформиат (0,355 мл, 3,36 ммоль) при 0°С и полученный продукт перемешивали при комнатной температуре в течение 2 часов. После этого реакционный раствор концентрировали, полученный остаток растворяли в метаноле (20 мл) и добавляли к нему карбонат калия (1,93 г, 14,0 ммоль) при комнатной температуре и полученный продукт безостановочно перемешивали в течение 3 часов. К раствору реакционной смеси добавляли воду и удаляли метанол при помощи перегонки при пониженном давлении и к полученному остатку добавляли 1 н. соляную кислоту и полученную смесь подвергали экстракции хлороформом. Органический слой сушили над сульфатом натрия и фильтровали и затем растворитель удаляли при помощи перегонки при пониженном давлении. Полученный остаток очищали с помощью колоночной хроматографии на силикагеле [гексан:этилацетат - 100:0 (об./об.) до 0:100 (об./об.)], получая желаемое соединение (0,921 г, 92%) в виде бледно-желтого твердого вещества.
МС (ХИАД ИЭР) m/z:359 (M+H)+.
[Стадии 2-4]
Соединение; полученное на стадии 1, подвергали реакции таким же образом, как и на стадиях 10 до 12 примера 3, получая лекарственное средство 12.
1HЯMP(CDCl3) δ: 7,89(1H,d,J=4,2 Гц), 7,59(1H,s), 7,53(1H,s), 7,40(1H,s), 734(2H,d,J=8, 5 Гц), 6,91(2H,d,J-8,5 Гц), 6,82(1H,s), 6,05(1H,s), 4,44-4,39(1H,m), 4,16-4,11(2Н,m), 4,09-4,04(2H,m), 3,99(2H,t,J=6,7 Гц), 3,95(3H,s), 3,84(6H,s), 3,72(1H,d,J-12,1 Гц), 3,59-3,49(3H,m), 3,45-3,34(2H,m), 2,00-1,92(4H,m), 1,79(1H,dd,J=12,4,7,0 Гц), 1,70-1,64(2Н,m), 1,25(1Н,t,J=7,0 Гц), 0,73-0,55(4Н,m).
МС (ХИАД, ИЭР) m/z:693(M+H)+.
[0916]
Пример 152: Лекарственные средства 13-16
[Формула 256]
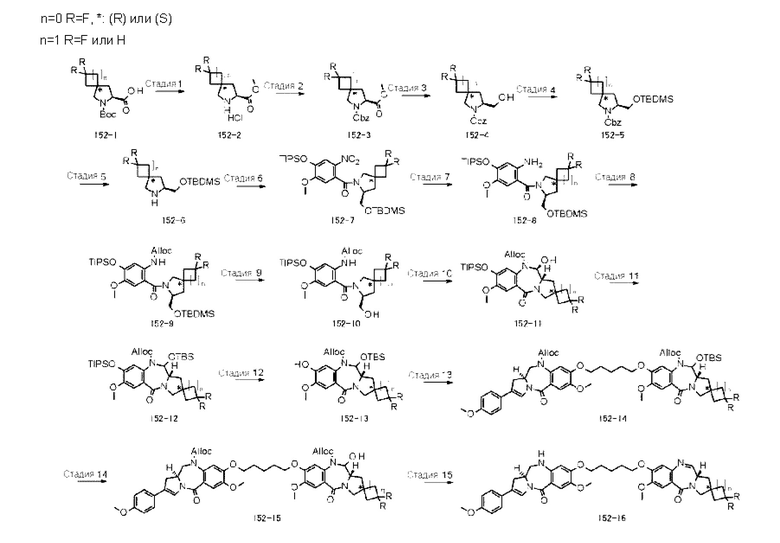
[Циклобутильное производное: лекарственное средство 13] n=1, R=F
[Стадия 1]
К раствору коммерчески доступного N-Т-ВОС-4-(3,3-дифторциклобутил)-L-пролина (OmegaChem Inc., ОС-0707) (12 г, 41 ммоль) в метаноле (200 мл), медленно добавляли по каплям тионилхлорид (10 мл, 138 ммоль) при -78°С (баня с сухим льдом и ацетоном). После добавления по каплям охлаждающую баню удаляли и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь концентрировали при пониженном давлении и остаток промывали диэтиловым эфиром, получая желаемое соединение (10 г, количественный выход).
[Стадия 2]
К суспезионному раствору соединения, полученного на стадии 1 (10 г, 41,4 ммоль) и карбоната натрия (8,77 г, 82,7 ммоль) в 1,4-диоксане (200 мл) и воде (50 мл) медленно добавляли бензилхлорформиат (8,82 мл, 62,0 ммоль) при охлаждении льдом. После завершения реакции к нему добавляли воду и реакционную смесь подвергали экстракции этилацетатом. Органический слой промывали водой и солевым раствором и сушили над безводным сульфатом натрия. После фильтрации растворитель удаляли при помощи перегонки при пониженном давлении, получая желаемое соединение.
[Стадии 3-15]
Соединение, полученное на предыдущей стадии, подвергали реакции таким же образом, как и на стадиях 1-5 примера 1 и стадиях 1-8 примера 45, получая лекарственное средство 13.
1HЯMP(CDCl3) δ: 7,72-7,71(1H,m), 7,53-7,49(3H,m), 7,34-7,28(2H,m), 6,91-6,78(3Н,m), 6,06-6,03(1Н,m), 4,35-4,28(1Н,m), 4,16-4,04(2Н,m), 4,02-3,96(1H,m), 3,94(3H,s), 3,90-3,76(2H,m), 3,84(2H,s), 3,82(3H,s), 3,59-3,31(2H,m), 2,76-2,44(8Н,m), 1,99-1,88(4Н,m), 1,71-1,59(4Н,m).
МС (ХИАД, ИЭР) m/z:743(M+H)+.
[0917]
[Циклобутильное производное: лекарственное средство 14] n=1, R=Н
[Стадии 2-15]
Коммерчески доступный гидрохлорид метилового эфира 4-циклобутил-L-пролина (OmegaChem Inc., ОС-0728) подвергали реакции таким же образом, как и на стадии 2, стадиях 1-5 примера 1 и стадиях 1-8 примера 45, получая лекарственное средство-линкер 14.
1HЯMP(CDCl3) δ: 7,73-7,45(3H,m), 7,34-7,14(2H,m), 6,94-6,42(3H,m), 6,05-5,99(1Н,m), 5,30-5,06(2Н,m), 4,49-4,28(2Н,m), 4,17-3,96(2Н,m), 3,95-3,79(9Н,m), 3,77-3,30(6Н,m), 2,77-2,70(1Н,m), 2,37-2,30(1Н,m), 2,19-1,85(8Н,m), 1,73-1,55(4Н,m), 1,30-1,16(2Н,m).
МС (ХИАД, ИЭР) m/z:707(M+H)+.
[Циклопропильное производное: лекарственное средство 15] n=0, R=F, *: (S)
Коммерчески доступный N-t-ВОС-4S-(2,2-дифторциклопропил)-L-пролин (OmegaChem Inc., ОС-0732) подвергали реакции таким же образом, как и на стадиях 1-15, получая лекарственное средство-линкер 15.
1HЯMP(CDCl3) δ: 7,76-7,75(1H,m), 7,54-7,47(3H,m), 7,33-7,27(2H,m), 6,93-6,85(2Н,m), 6,83-6,79(1Н,m), 6,08-5,96(1Н,m), 4,32-4,30(1Н,m), 4,16-3,96(3H,m), 3,94(3H,s), 3,84(3H,s), 3,82(3H,s), 3,74-3,67(3H,m), 3,59-3,51(2H,m), 3,39-3,34(1Н,m), 2,76-2,69(2Н,m), 2,38-2,33(1Н,m), 1,98-1,89(4Н,m), 1,69-1,54(4Н,m), 1,30-1,22(2Н,m).
МС (ХИАД, ИЭР) m/z:729(M+H)+.
[0918]
[Циклопропильное производное: лекарственное средство 16] n=0, R=F, *: (R)
Коммерчески доступный N-t-ВОС-4R-(2,2-дифторциклопропил)-L-пролин (OmegaChem Inc., ОС-0722) подвергали реакции таким же образом, как и на стадиях 1-15, получая лекарственное средство-линкер 16.
1HЯMP(CDCl3) δ: 7,76-7,69(1H,m), 7,55-7,44(3H,m), 7,33-7,28(2H,m), 6,94-6,80(2Н,m), 6,59-6,42(1Н,m), 6,08-5,97(1Н,m), 4,36-4,24(1Н,m), 4,20-3,95(3Н,m), 3,95-3,76(12Н,m), 3,75-3,50(2Н,m), 3,42-3,31(1Н,m), 2,79-2,52(2Н,m), 2,48-2,32(1Н,m), 2,06-1,83(4Н,m), 1,72-1,41(4Н,m), 1,28-1,15(2Н,m).
МС (ХИАД, ИЭР) m/z:729(M+H)+.
[0919]
Пример 153: [N3-PEG(3)]2-SG(10)
Стадия 1: Fmoc-(SG-)Asn, свободная форма
Fmoc-(SG-)Asn (1S2S-11NC-Asn-Fmoc, производства GlyTech, Inc., 2 г) растворяли в соответствующем количестве 0,1% водного раствора трифторуксусной кислоты и подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ с помощью нескольких отдельных операций. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила с добавлением трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемый продукт, детектируемый УФ-излучением (220 им) во время элюирования, объединяли и сушили с помощью сублимационной сушки. Получали бесцветное твердое вещество (1,8 г).
[0920]
Стадия 2: Синтез ([N3-PEG (3)]2-SG)-Asn-PEG (3)-N3
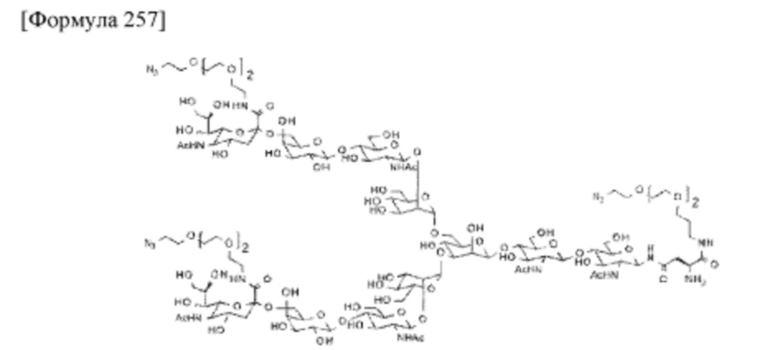
К раствору (10 мл) Fmoc-(SG-)Asn свободной формы в N,N-диметилформамиде, полученному на стадии 1 (1000 мг), добавляли раствор HATU (891 мг, 2,34 ммоль) в N,N-диметилформамиде (3 мл) и раствор 11-азид-3,6,9-триоксаундекан-1-амина (Tokyo Chemical Industry Co., Ltd., 511 мг, 2,34 ммоль) в N,N-диметилформамиде (3 мл) и диизопропилэтиламин (816 мкл, 4,69 ммоль) и полученный продукт перемешивали при 37°С в течение 3 часов. Дополнительно к нему добавляли раствор HATU (148 мг, 0,39 ммоль) в N,N-диметилформамиде (500 мкл) и полученный продукт перемешивали при 37°С в течение 1 часа. После этого к нему добавляли пиперидин (386 мкл, 3,91 ммоль) и полученный продукт перемешивали при 37°С в течение 1 часа. После завершения реакции к нему добавляли уксусную кислоту (469 мкл).
Реакционный раствор делили пополам и переносили в две большие конические пробирки (175 мл), к каждой из которых заранее добавляли диэтиловый эфир (100 мл). Твердое вещество осаждали с помощью небольшой центрифуги (Hitachi Koki Co., Ltd., CF16RX) и удаляли супернатант. Смолообразное твердое вещество переносили в центрифужную пробирку (50 мл) и добавляли к нему диэтиловый эфир (30 мл) и ацетонитрил (10 мл) и полученный продукт декантировали. Указанную операцию повторяли дважды. Таким же образом добавляли соответствующее количество ацетонитрила или соответствующее количество диэтилового эфира и полученный продукт декантировали и затем сушили при пониженном давлении, получая неочищенный продукт. Полученное твердое вещество растворяли в соответствующем количестве 0,2% водного раствора трифторуксусной кислоты и подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила с добавлением трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемый продукт, детектируемый УФ-излучением (220 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая указанное в заголовке желаемое соединение (637 мг) в виде бесцветного твердого вещества.
ИЭР-МС: Расчетное значение для C112H192N20O70:[М+3Н]3+980,6(сред.), найденное значение 980,4
[0921]
Стадия 3: Синтез [N3PEG (3)]2-SG (10)
[Формула 258]
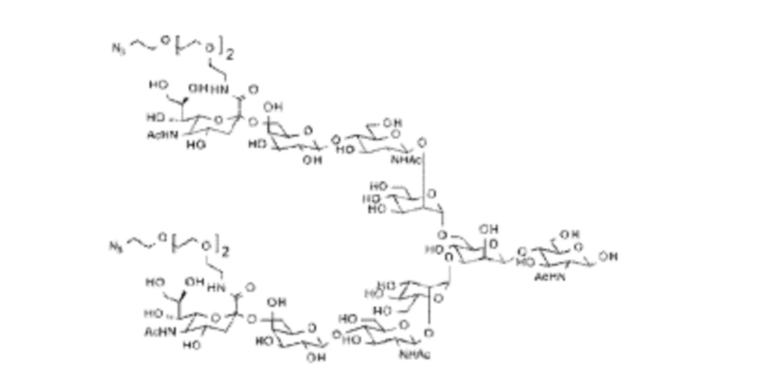
В 2 мл пробирке ([N3-PEG (3)]2-SG)-Asn-PEG (3)-N3, синтезированный на стадии-2 (78,6 мг), растворяли в 100 мМ фосфатного буфера (NACALAI TESQUE, INC., 465 мкл) при pH 6,0. К нему добавляли 1 ед./мл EndoM (Tokyo Chemical Industry Co., Ltd., 70 мкл) и полученный продукт встряхивали при 28°С в течение 5 часов и затем оставляли стоять при комнатной температуре в течение 4 дней. После завершения реакции к нему добавляли соответствующем количестве 0,2% водного раствора трифторуксусной кислоты и полученный продукт подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемый продукт, детектируемый УФ-излучением (220 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая указанное в заголовке желаемое соединение (40 мг) в виде бесцветного твердого вещества.
ИЭР-МС: Расчетное значение для C92H157N13O61: [M+2H]2+1211,7(сред.), найденное значение 1211,5
[0922]
Пример 154: [N3-PEG (3)]-MSG2 (9), [N3-PEG (3)]-MSG1 (9)
Стадия 1: (MSG1-)Asn и (MSG2-)Asn
Коммерчески доступный продукт, не содержащий моносиало-Asn (1S2G/1G2S-10NC-Asn, производства GlyTech, Inc.) (обозначаемый как "(MSG-)Asn") (500 мг), подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ в условиях, указанных ниже, для разделения на (MSG1-)Asn, элюированный в качестве 1-го основного пика (время удерживания: примерно 15 to 19 мин) и (MSG2-)Asn, элюированный в качестве 2-го основного пика (время удерживания: примерно 21-26 мин). В качестве элюента использовали 0,1% водный раствор муравьиной кислоты, в качестве устройства использовали триггерную препаративную систему ELS-PDA (производства JASCO Corporation) используемая колонка представляла собой Inertsil ODS-3 (10 мкм, 30ф×250 мм, производства GL Sciences, Inc.), и скорость потока составляла 30 мл/мин. Фракции, относящиеся к первому пику УФ-детектирования (210 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая (MSG1-)Asn (238 мг) в виде бесцветного твердого вещества. Фракции, относящиеся ко второму пику УФ-детектирования, объединяли и сушили с помощью сублимационной сушки, получая (MSG2-)Asn (193 мг) в виде бесцветного твердого вещества.
[0923]
Стадия-2: Fmoc-(MSG2-)Asn, свободная форма
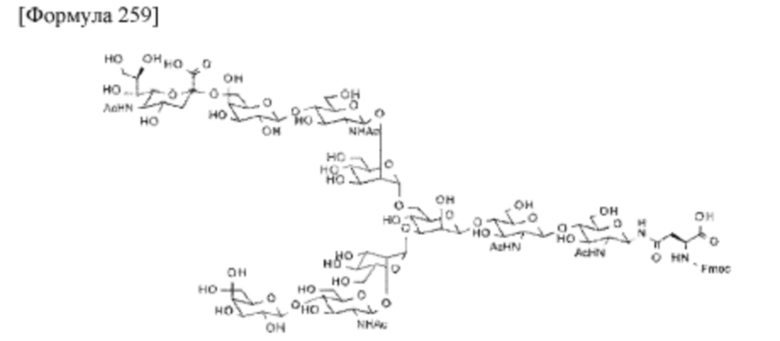
(MSG2-)Asn, синтезированный на стадии 1 (900 мг), растворяли в растворе N,N-диметилформамида (6 мл)/дистиллированной воды (2 мл) и добавляли к нему диизопропилэтиламин (0,23 мл) и 9-флуоренилметил-N-сукцинимидилкарбонат (223 мг) и полученный продукт перемешивали при комнатной температуре в течение 30 минут .Дополнительно добавляли к нему диизопропилэтиламин (0,16 мл), 9-флуоренилметил-N-сукцинимидилкарбонат (74 мг) и раствор N,N-диметилформамида (1 мл) и полученный продукт перемешивали при комнатной температуре в течение 30 минут.
Реакционный раствор делили пополам и переносили в две большие конические пробирки (175 мл), к каждой из которых заранее добавляли диэтиловый эфир (80 мл)/ацетонитрил (4 мл). Твердое вещество осаждали с помощью небольшой центрифуги (Hitachi Koki Co., Ltd., CF16RX) и удаляли супернатант. Смолообразное твердое вещество переносили в центрифужную пробирку (50 мл) и добавляли к нему диэтиловый эфир (30 мл) и ацетонитрил (10 мл) и полученный продукт декантировали. Указанную операцию повторяли дважды. Таким же образом добавляли соответствующее количество ацетонитрила или соответствующее количество диэтилового эфира и полученный продукт декантировали и затем сушили при пониженном давлении, получая неочищенный продукт. Полученное твердое вещество растворяли в соответствующем количестве 0,2% водного раствора трифторуксусной кислоты и подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор трифторуксусной кислоты и 0,1% раствор ацетонитрила трифторуксусной кислоты, использовали устройство Purif-Rp2 (производства Shoko Scientific Co., Ltd.) и колонку Inertsil ODS-3 (производства GL Sciences, Inc.). Во время элюирования фракции, содержащие УФ-детектированный (220 нм) желаемый продукт, объединяли и сушили с помощью сублимационной сушки, получая указанное в заголовке желаемое соединение (830 мг) в виде бесцветного твердого вещества.
[0924]
Стадия 3: ([N3-PEG (3)]-MSG2)-Asn-PEG (3)-N3
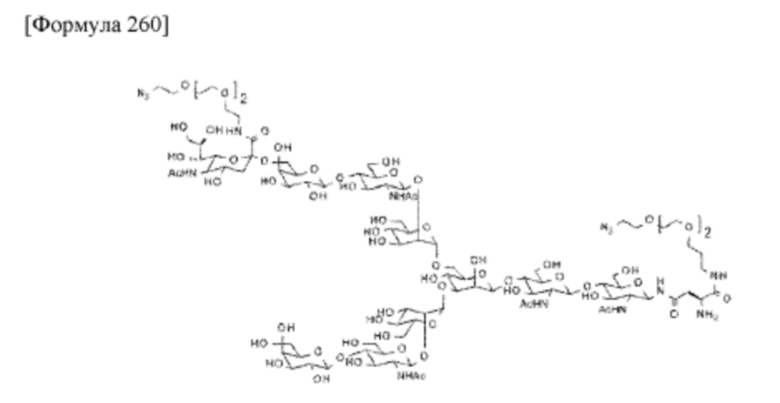
Применяя Fmoc-(MSG2-)Asn, синтезированный на стадии 2 (830 мг), неочищенный указанный в заголовке желаемый продукт (1,06 г) получали таким же образом, как и на стадии 2 примера 153. Его использовали для последующей реакции без дополнительной очистки.
[0925]
Аналогичным образом следующее ([N3-PEG (3)]-MSG1)-Asn-PEG (3)-N3 может быть синтезировано из Fmoc-(MSG1-)Asn.
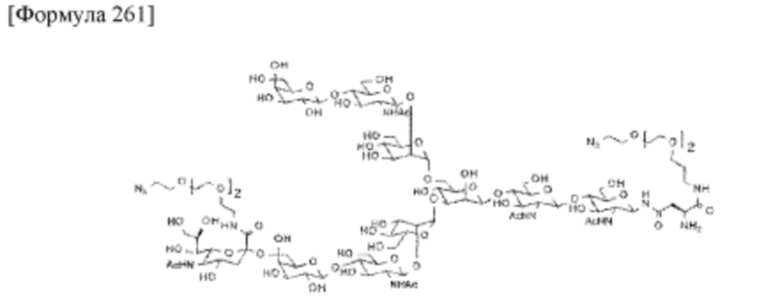
Стадия 4: [N2-PEG (3)]-MSG2 (9)
[Формула 262]
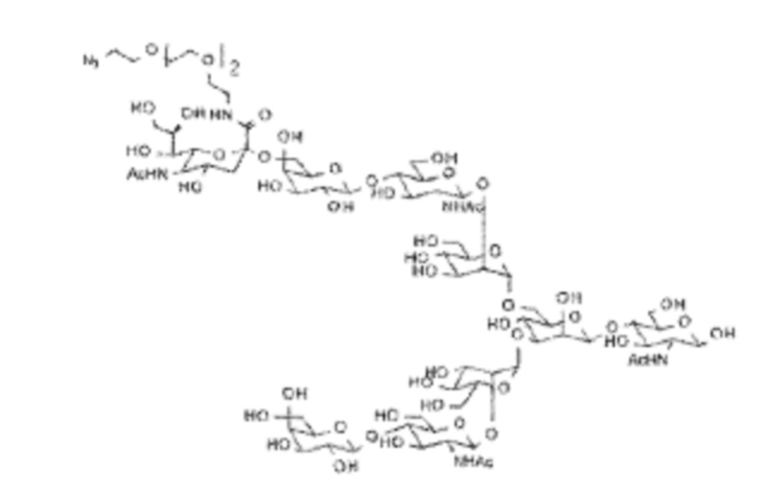
В 2 мл флаконе для сбора неочищенный продукт ([N3-PEG (3)]-MSG2)-Asn-PEG (3)-N3, синтезированный на стадии 3 (150 мг), растворяли в 200 мМ калий-фосфатного буфера (750 мкл) при pH 6,25, полученного с 200 мМ KH2PO4 и 200 мМ KH2PO4. К нему добавляли Endo-Rp (3 мкг) и полученный продукт оставляли стоять при 50°С в течение 16 часов. После завершения реакции к нему добавляли 5% водный раствор трифторуксусной кислоты(150 мкл) и полученный продукт подвергали разделению/очистке с помощью обращенно-фазовой ВЭЖХ. Элюент представлял собой 0,1% водный раствор водного раствора трифторуксусной кислоты и 0,1% раствор ацетонитрила трифторуксусной кислоты, в качестве устройства использовали триггерную препаративную систему ELS-PDA (производства JASCO Corporation), а используемая колонка представляла собой Inertsil ODS-3 (производства GL Sciences, Inc.). Фракции, содержащие желаемый продукт, детектируемый УФ-излучением (210 нм) во время элюирования, объединяли и сушили с помощью сублимационной сушки, получая указанное в заголовке желаемое соединение (62 мг) в виде бесцветного твердого вещества.
ИЭР-МС: Расчетное значение для C73H124O51: [М+2H]2+965,3(сред.), найденное значение 965,4
[0926]
Аналогично, следующее [N3-PEG (3)]-MSG1 (9) может быть синтезировано из ([N3-PEG (3)]-MSG1)-Asn-PEG (3)-N3.
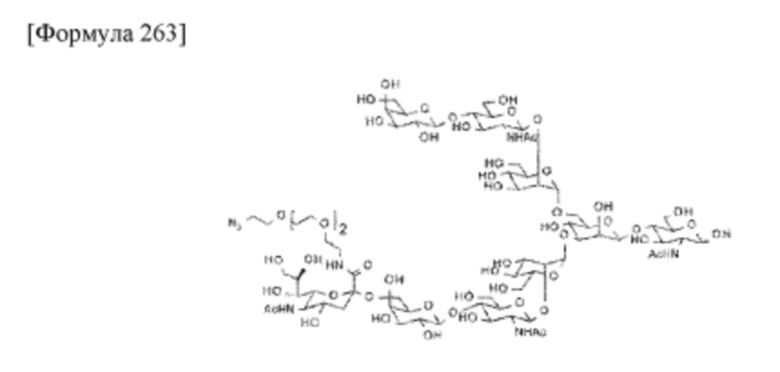
Промышленная применимость
[0927]
Применение конъюгата антитело-лекарственное средство, антитела и/или производного PBD и так далее согласно настоящему изобретению обеспечивает лечение или предотвращение различных видов раковых заболеваний.
Перечень последовательностей
[0928]
SEQ ID NO: 1 - Аминокислотная последовательность CLDN6 человека
SEQ ID NO: 2 - Нуклеотидная последовательность кДНК, кодирующей аминокислотную последовательность CLDN6 человека
SEQ ID NO: 3 - Аминокислотная последовательность CLDN9 человека
SEQ ID NO: 4 - Нуклеотидная последовательность к ДНК, кодирующей аминокислотную последовательность CLDN9 человека
SEQ ID NO: 5 - Аминокислотная последовательность CDRL1 легкой цепи антитела В1
SEQ ID NO: 6 - Аминокислотная последовательность CDRL2 легкой цепи антитела В1
SEQ ID NO: 7 - Аминокислотная последовательность CDRL3 легкой цепи антитела В1
SEQ ID NO: 8 - Аминокислотная последовательность CDRL3 легкой цепи L4 гуманизированного антитела В1
SEQ ID NO: 9 - Аминокислотная последовательность CDRH1 тяжелой цепи антитела В1
SEQ ID NO: 10 - Аминокислотная последовательность CDRH2 тяжелой цепи антитела В1
SEQ ID NO: 11 - Аминокислотная последовательность CDRH3 тяжелой цепи антитела В1
SEQ ID NO: 12 - Аминокислотная последовательность CDRL1 легкой цепи антитела С7
SEQ ID NO: 13 - Аминокислотная последовательность CDRL2 легкой цепи антитела С7
SEQ ID NO: 14 - Аминокислотная последовательность CDRL3 легкой цепи антитела С7
SEQ ID NO: 15 - Аминокислотная последовательность CDRH1 тяжелой цепи антитела С7
SEQ ID NO: 16 - Аминокислотная последовательность CDRH2 тяжелой цепи антитела С7
SEQ ID NO: 17 - Аминокислотная последовательность CDRH3 тяжелой цепи антитела С7
SEQ ID NO: 18 - Нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела В1
SEQ ID NO: 19 - Аминокислотная последовательность вариабельной область легкой цепи антитела В1
SEQ ID NO: 20 Нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела В1
SEQ ID NO: 21 - Аминокислотная последовательность вариабельной области тяжелой цепи антитела В1
SEQ ID NO: 22 Нуклеотидная последовательность кДНК, кодирующей вариабельную область легкой цепи антитела С7
SEQ ID NO: 23 - Аминокислотная последовательность вариабельной области легкой цепи антитела С7
SEQ ID NO: 24 Нуклеотидная последовательность кДНК, кодирующей вариабельную область тяжелой цепи антитела С7
SEQ ID NO: 25 - Аминокислотная последовательность вариабельной области тяжелой цепи антитела С7
SEQ ID NO: 26 - Фрагмент ДНК, включающий последовательность ДНК, кодирующую сигнальную последовательность легкой цепи человека и константный участок κ-цепи человека
SEQ ID NO: 27 Фрагмент ДНК, включающий последовательность ДНК, кодирующую сигнальную последовательность тяжелой цепи человека и константную область LALA IgG1 человека
SEQ ID NO: 28 - Аминокислотная последовательность легкой цепи chB1
SEQ ID NO: 29 Фрагмент ДНК, включающий последовательность ДНК, кодирующую аминокислотную последовательность легкой цепи chB1
SEQ ID NO: 30 - Аминокислотная последовательность вариабельной области легкой цепи chB1
SEQ ID NO: 31 - Нуклеотидная последовательность, кодирующая вариабельную область легкой цепи chB1
SEQ ID NO: 32 - Аминокислотная последовательность тяжелой цепи chB1
SEQ ID NO: 33 - Нуклеотидная последовательность, кодирующая тяжелую цепь chB1
SEQ ID NO: 34 - Аминокислотная последовательность вариабельной области тяжелой цепи chB1
SEQ ID NO: 35 - Нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи chB1
SEQ ID NO: 36 - Аминокислотная последовательность легкой цепи hL1 гуманизированного антитела
SEQ ID NO: 37 - Нуклеотидная последовательность, кодирующая легкую цепь hL1 гуманизированного антитела
SEQ ID NO: 38 - Аминокислотная последовательность вариабельной области легкой цепи hL1 гуманизированного антитела
SEQ ID NO: 39 - Нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL1 гуманизированного антитела
SEQ ID NO: 40 - Аминокислотная последовательность легкой цепи hL2 гуманизированного антитела
SEQ ID NO: 41 - Нуклеотидная последовательность, кодирующая легкую цепь гуманизированного антитела hL2
SEQ ID NO: 42 - Аминокислотная последовательность вариабельной области легкой цепи hL2 гуманизированного антитела
SEQ ID NO: 43 - Нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL2 гуманизированного антитела
SEQ ID NO: 44 - Аминокислотная последовательность легкой цепи hL3 гуманизированного антитела
SEQ ID NO: 45 - Нуклеотидная последовательность, кодирующая легкую цепь hL3 гуманизированного антитела
SEQ ID NO: 46 - Аминокислотная последовательность вариабельной области легкой цепи hL3 гуманизированного антитела
SEQ ID NO: 47 - Нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL3 гуманизированного антитела
SEQ ID NO: 48 - Аминокислотная последовательность легкой цепи hL4 гуманизированного антитела
SEQ ID NO: 49 - Нуклеотидная последовательность, кодирующая легкую цепь hL4 гуманизированного антитела
SEQ ID NO: 50 - Аминокислотная последовательность вариабельной области легкой цепи hL4 гуманизированного антитела
SEQ ID NO: 51 - Нуклеотидная последовательность, кодирующая вариабельную область легкой цепи hL4 гуманизированного антитела
SEQ ID NO: 52 - Аминокислотная последовательность тяжелой цепи hH1 гуманизированного антитела
SEQ ID NO: 53 - Нуклеотидная последовательность, кодирующая тяжелую цепь hH1 гуманизированного антитела
SEQ ID NO: 54 - Аминокислотная последовательность вариабельной области тяжелой цепи hH1 гуманизированного антитела
SEQ ID NO: 55 - Нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи hH1 гуманизированного антитела
SEQ ID NO: 56 - Аминокислотная последовательность тяжелой цепи hH2 гуманизированного антитела
SEQ ID NO: 57 - Нуклеотидная последовательность, кодирующая тяжелую цепь hH2 гуманизированного антитела
SEQ ID NO: 58 - Аминокислотная последовательность вариабельной области тяжелой цепи hH2 гуманизированного антитела
SEQ ID NO: 59 - Нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи hH2 гуманизированного антитела
SEQ ID NO: 60 - Аминокислотная последовательность тяжелой цепи hH3 гуманизированного антитела
SEQ ID NO: 61 - Нуклеотидная последовательность, кодирующая тяжелую цепь hH3 гуманизированного антитела
SEQ ID NO: 62 - Аминокислотная последовательность вариабельной области тяжелой цепи hH3 гуманизированного антитела
SEQ ID NO: 63 - Нуклеотидная последовательность, кодирующая вариабельную область тяжелой цепи hH3 гуманизированного антитела
SEQ ID NO: 64 - Аминокислотная последовательность легкой цепи трастузумаба SEQ ID NO: 65 - Аминокислотная последовательность тяжелой цепи трастузумаба
SEQ ID NO: 66 - Аминокислотная последовательность легкой цепи антитела к LPS (h#1G5-H1L1)
SEQ ID NO: 67 - Аминокислотная последовательность тяжелой цепи антитела к LPS (h#1G5-H1L1)
SEQ ID NO: 68 - Аминокислотная последовательность легкой цепи антитела к TROP2 (hRS7)
SEQ ID NO: 69 - Аминокислотная последовательность тяжелой цепи антитела к TROP2 (hRS7)
SEQ ID NO: 70 - Аминокислотная последовательность легкой цепи антитела к CD98 (hM23-H1L1)
SEQ ID NO: 71 - Аминокислотная последовательность тяжелой цепи антитела к CD98 (hM23-H1L1)
SEQ ID NO: 72 - Нуклеотидная последовательность, кодирующая легкую цепь варианта трастузумаба
SEQ ID NO: 73 - Аминокислотная последовательность легкой цепи варианта трастузумаба
SEQ ID NO: 74 - Нуклеотидная последовательность, кодирующая тяжелую цепь трастузумаба
SEQ ID NO: 75 - Аминокислотная последовательность тяжелой цепи варианта трастузумаба
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> DAIICHI SANKYO COMPANY, LIMITED
<120> Конъюгат антитело-производное пирролобензодиазепина
<130> SAP-850-PCT
<141> 2018-09-28
<150> JP 2017190713
<151> 2017-09-29
<160> 75
<170> PatentIn, версия 3.5
<210> 1
<211> 220
<212> PRT
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CLDN6 человека
<400> 1
Met Ala Ser Ala Gly Met Gln Ile Leu Gly Val Val Leu Thr Leu Leu
1 5 10 15
Gly Trp Val Asn Gly Leu Val Ser Cys Ala Leu Pro Met Trp Lys Val
20 25 30
Thr Ala Phe Ile Gly Asn Ser Ile Val Val Ala Gln Val Val Trp Glu
35 40 45
Gly Leu Trp Met Ser Cys Val Val Gln Ser Thr Gly Gln Met Gln Cys
50 55 60
Lys Val Tyr Asp Ser Leu Leu Ala Leu Pro Gln Asp Leu Gln Ala Ala
65 70 75 80
Arg Ala Leu Cys Val Ile Ala Leu Leu Val Ala Leu Phe Gly Leu Leu
85 90 95
Val Tyr Leu Ala Gly Ala Lys Cys Thr Thr Cys Val Glu Glu Lys Asp
100 105 110
Ser Lys Ala Arg Leu Val Leu Thr Ser Gly Ile Val Phe Val Ile Ser
115 120 125
Gly Val Leu Thr Leu Ile Pro Val Cys Trp Thr Ala His Ala Ile Ile
130 135 140
Arg Asp Phe Tyr Asn Pro Leu Val Ala Glu Ala Gln Lys Arg Glu Leu
145 150 155 160
Gly Ala Ser Leu Tyr Leu Gly Trp Ala Ala Ser Gly Leu Leu Leu Leu
165 170 175
Gly Gly Gly Leu Leu Cys Cys Thr Cys Pro Ser Gly Gly Ser Gln Gly
180 185 190
Pro Ser His Tyr Met Ala Arg Tyr Ser Thr Ser Ala Pro Ala Ile Ser
195 200 205
Arg Gly Pro Ser Glu Tyr Pro Thr Lys Asn Tyr Val
210 215 220
<210> 2
<211> 663
<212> ДНК
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей
аминокислотную
последовательность CLDN6 человека
<400> 2
atggcctctg ccggaatgca gatcctggga gtcgtcctga cactgctggg ctgggtgaat
60
ggcctggtct cctgtgccct gcccatgtgg aaggtgaccg ctttcatcgg caacagcatc
120
gtggtggccc aggtggtgtg ggagggcctg tggatgtcct gcgtggtgca gagcaccggc
180
cagatgcagt gcaaggtgta cgactcactg ctggcgctgc cacaggacct gcaggctgca
240
cgtgccctct gtgtcatcgc cctccttgtg gccctgttcg gcttgctggt ctaccttgct
300
ggggccaagt gtaccacctg tgtggaggag aaggattcca aggcccgcct ggtgctcacc
360
tctgggattg tctttgtcat ctcaggggtc ctgacgctaa tccccgtgtg ctggacggcg
420
catgccatca tccgggactt ctataacccc ctggtggctg aggcccaaaa gcgggagctg
480
ggggcctccc tctacttggg ctgggcggcc tcaggccttt tgttgctggg tggggggttg
540
ctgtgctgca cttgcccctc gggggggtcc cagggcccca gccattacat ggcccgctac
600
tcaacatctg cccctgccat ctctcggggg ccctctgagt accctaccaa gaattacgtc
660
tga
663
<210> 3
<211> 217
<212> PRT
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CLDN9 человека
<400> 3
Met Ala Ser Thr Gly Leu Glu Leu Leu Gly Met Thr Leu Ala Val Leu
1 5 10 15
Gly Trp Leu Gly Thr Leu Val Ser Cys Ala Leu Pro Leu Trp Lys Val
20 25 30
Thr Ala Phe Ile Gly Asn Ser Ile Val Val Ala Gln Val Val Trp Glu
35 40 45
Gly Leu Trp Met Ser Cys Val Val Gln Ser Thr Gly Gln Met Gln Cys
50 55 60
Lys Val Tyr Asp Ser Leu Leu Ala Leu Pro Gln Asp Leu Gln Ala Ala
65 70 75 80
Arg Ala Leu Cys Val Ile Ala Leu Leu Leu Ala Leu Leu Gly Leu Leu
85 90 95
Val Ala Ile Thr Gly Ala Gln Cys Thr Thr Cys Val Glu Asp Glu Gly
100 105 110
Ala Lys Ala Arg Ile Val Leu Thr Ala Gly Val Ile Leu Leu Leu Ala
115 120 125
Gly Ile Leu Val Leu Ile Pro Val Cys Trp Thr Ala His Ala Ile Ile
130 135 140
Gln Asp Phe Tyr Asn Pro Leu Val Ala Glu Ala Leu Lys Arg Glu Leu
145 150 155 160
Gly Ala Ser Leu Tyr Leu Gly Trp Ala Ala Ala Ala Leu Leu Met Leu
165 170 175
Gly Gly Gly Leu Leu Cys Cys Thr Cys Pro Pro Pro Gln Val Glu Arg
180 185 190
Pro Arg Gly Pro Arg Leu Gly Tyr Ser Ile Pro Ser Arg Ser Gly Ala
195 200 205
Ser Gly Leu Asp Lys Arg Asp Tyr Val
210 215
<210> 4
<211> 654
<212> ДНК
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей
аминокислотную
последовательность CLDN9 человека
<400> 4
atggcttcga ccggcttaga actgctgggc atgaccctgg ctgtgctggg ctggctgggg
60
accctggtgt cctgcgccct gcccctgtgg aaggtgaccg ccttcatcgg caacagcatc
120
gtggtggccc aggtggtgtg ggagggcctg tggatgtcct gcgtggtgca gagcacgggc
180
cagatgcagt gcaaggtgta cgactcactg ctggctctgc cgcaggacct gcaggccgca
240
cgtgccctct gtgtcattgc cctcctgctg gccctgcttg gcctcctggt ggccatcaca
300
ggtgcccagt gtaccacgtg tgtggaggac gaaggtgcca aggcccgtat cgtgctcacc
360
gcgggggtca tcctcctcct cgccggcatc ctggtgctca tccctgtgtg ctggacggcg
420
cacgccatca tccaggactt ctacaacccc ctggtggctg aggccctcaa gcgggagctg
480
ggggcctccc tctacctggg ctgggcggcg gctgcactgc ttatgctggg cggggggctc
540
ctctgctgca cgtgcccccc gccccaggtc gagcggcccc gcggacctcg gctgggctac
600
tccatcccct cccgctcggg tgcatctgga ctggacaaga gggactacgt gtga
654
<210> 5
<211> 11
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL1 легкой цепи антитела
B1
<400> 5
Arg Ala Ser Gln Asp Ile Asn Asn Tyr Leu Asn
1 5 10
<210> 6
<211> 7
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL2 легкой цепи антитела
B1
<400> 6
Phe Thr Ser Arg Leu His Ser
1 5
<210> 7
<211> 9
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL3 легкой цепи антитела
B1
<400> 7
Gln Gln Gly Tyr Pro Leu Pro Trp Thr
1 5
<210> 8
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL3 легкой цепи L4
гуманизированного
антитела B1
<400> 8
Gln Gln Gly Asn Thr Leu Pro Trp Thr
1 5
<210> 9
<211> 10
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH1 тяжелой цепи антитела
B1
<400> 9
Gly Tyr Thr Phe Thr Glu Tyr Thr Met His
1 5 10
<210> 10
<211> 10
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH2 тяжелой цепи антитела
B1
<400> 10
Gly Val Asn Pro Asn Ser Gly Asp Thr Ser
1 5 10
<210> 11
<211> 13
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH3 тяжелой цепи антитела
B1
<400> 11
Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr
1 5 10
<210> 12
<211> 11
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL1 легкой цепи антитела
C7
<400> 12
Arg Ala Ser Gln Asp Ile Asn Asn Tyr Leu Asn
1 5 10
<210> 13
<211> 7
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL2 легкой цепи антитела
C7
<400> 13
Ser Thr Ser Arg Leu His Ser
1 5
<210> 14
<211> 9
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRL3 легкой цепи антитела
C7
<400> 14
Gln Gln Gly Tyr Pro Leu Pro Trp Thr
1 5
<210> 15
<211> 10
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH1 тяжелой цепи антитела
C7
<400> 15
Gly Tyr Thr Phe Thr Glu Tyr Thr Met His
1 5 10
<210> 16
<211> 10
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH2 тяжелой цепи антитела
C7
<400> 16
Gly Val Asn Pro Asn Ser Gly Asp Thr Ser
1 5 10
<210> 17
<211> 13
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность CDRH3 тяжелой цепи антитела
C7
<400> 17
Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr
1 5 10
<210> 18
<211> 321
<212> ДНК
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей вариабельную
область
легкой цепи антитела B1
<400> 18
gatatccaga tgacacagac tgcatcctcc ctgtctgcct ctcttggaga cagagtcacc
60
atcagttgca gggcaagtca ggacattaac aattatttaa actggtatca gcagaaacca
120
gatggaactg ttaaactcct gatctacttc acatcaagat tacactcagg agtcccatca
180
aggttcagtg gcagtgggtc tggaacacat tattctctca ccattactaa cctggaacaa
240
gaagatattg ccacttactt ttgccaacag ggttatccgc ttccgtggac gttcggtgga
300
ggcaccaaac tggaaatcaa a
321
<210> 19
<211> 107
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
легкой цепи антитела B1
<400> 19
Asp Ile Gln Met Thr Gln Thr Ala Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Tyr Ser Leu Thr Ile Thr Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 20
<211> 366
<212> ДНК
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей вариабельную
область тяжелой цепи антитела B1
<400> 20
gaggtccagc ttcaacagtc tggacctgaa ctggtgaagc ctggggcttc agtgaagata
60
tcctgcaaga cttctggata cacattcact gaatacacca tgcactgggt gcagcagagc
120
catggaaaga gccttgagtg gattggaggt gttaatccta atagtggtga tactagctac
180
aaccagaagt tcaagggcaa ggccacattg actgttgaca agtcctccag cacagcctac
240
atggagctcc gcagcctgac atctgaggat tctgcagtct attactgtgc aagacccggg
300
gggtacgacg tgggttacta tgctatggac tactggggtc aaggaacctc agtcaccgtc
360
tcctca
366
<210> 21
<211> 122
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
тяжелой цепи антитела B1
<400> 21
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Gln Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 22
<211> 321
<212> ДНК
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей вариабельную
область
легкой цепи антитела C7
<400> 22
gatatccaga tgacacagac tgcatcctcc ctgtctgcct ctcttggaga cagagtcacc
60
atcagttgca gggcaagtca ggacattaac aattatttaa actggtatca gcagaaacca
120
gatggaactg ttaaactcct gatctactcc acatcaagat tacactcagg agtcccatca
180
aggttcagtg gcagtgggtc tggaacacat tattctctca ccattactca cctggaacaa
240
gaagatattg ccacttactt ttgccaacag ggttatccgc ttccgtggac gttcggtgga
300
ggcaccaaac tggaaatcaa a
321
<210> 23
<211> 107
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
легкой цепи антитела C7
<400> 23
Asp Ile Gln Met Thr Gln Thr Ala Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Ser Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Tyr Ser Leu Thr Ile Thr His Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 24
<211> 366
<212> ДНК
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность кДНК, кодирующей вариабельную
область
тяжелой цепи антитела C7
<400> 24
gaggtccagc ttcaacagtc tggacctgaa ctggtgaagc ctggggcttc agtgaagata
60
tcctgcaaga cttctggata cacattcact gaatacacca tgcactgggt gcagcagagc
120
catggaaaga gccttgagtg gattggaggt gttaatccta atagtggtga tactagctac
180
aaccagaagt tcaagggcaa ggccacattg actgttgaca agtcctccag cacagcctac
240
atggagctcc gcagcctgac atctgaggat tctgcagtct attactgtgc aagacccggg
300
gggtacgacg tgggttacta tgctatggac tactggggtc aaggaacctc agtcaccgtc
360
tcctca
366
<210> 25
<211> 122
<212> PRT
<213> Mus musculus
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
тяжелой цепи антитела C7
<400> 25
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Gln Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 26
<211> 449
<212> ДНК
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> Фрагмент ДНК, содержащий последовательность ДНК, кодирующую
сигнальную последовательность легкой цепи человека и
константную
область каппа-цепи человека
<400> 26
gcctccggac tctagagcca ccatggtgct gcagacccag gtgttcatct ccctgctgct
60
gtggatctcc ggcgcgtacg gcgatatcgt gatgattaaa cgtacggtgg ccgccccctc
120
cgtgttcatc ttccccccct ccgacgagca gctgaagtcc ggcaccgcct ccgtggtgtg
180
cctgctgaat aacttctacc ccagagaggc caaggtgcag tggaaggtgg acaacgccct
240
gcagtccggg aactcccagg agagcgtgac cgagcaggac agcaaggaca gcacctacag
300
cctgagcagc accctgaccc tgagcaaagc cgactacgag aagcacaagg tgtacgcctg
360
cgaggtgacc caccagggcc tgagctcccc cgtcaccaag agcttcaaca ggggggagtg
420
ttaggggccc gtttaaacgg gggaggcta
449
<210> 27
<211> 1137
<212> ДНК
<213> Homo sapiens
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> ДНК-фрагмент, содержащий последовательность ДНК, кодирующую
сигнальную последовательность тяжелой цепи человека и
константную
область LALA IgG1 человека
<400> 27
ccagcctccg gactctagag ccaccatgaa acacctgtgg ttcttcctcc tgctggtggc
60
agctcccaga tgggtgctga gccaggtgca attgtgcagg cggttagctc agcctccacc
120
aagggcccaa gcgtcttccc cctggcaccc tcctccaaga gcacctctgg cggcacagcc
180
gccctgggct gcctggtcaa ggactacttc cccgaacccg tgaccgtgag ctggaactca
240
ggcgccctga ccagcggcgt gcacaccttc cccgctgtcc tgcagtcctc aggactctac
300
tccctcagca gcgtggtgac cgtgccctcc agcagcttgg gcacccagac ctacatctgc
360
aacgtgaatc acaagcccag caacaccaag gtggacaaga gagttgagcc caaatcttgt
420
gacaaaactc acacatgccc accctgccca gcacctgaag ccgcgggggg accctcagtc
480
ttcctcttcc ccccaaaacc caaggacacc ctcatgatct cccggacccc tgaggtcaca
540
tgcgtggtgg tggacgtgag ccacgaagac cctgaggtca agttcaactg gtacgtggac
600
ggcgtggagg tgcataatgc caagacaaag ccccgggagg agcagtacaa cagcacgtac
660
cgggtggtca gcgtcctcac cgtcctgcac caggactggc tgaatggcaa ggagtacaag
720
tgcaaggtct ccaacaaagc cctcccagcc cccatcgaga aaaccatctc caaagccaaa
780
ggccagcccc gggaaccaca ggtgtacacc ctgcccccat cccgggagga gatgaccaag
840
aaccaggtca gcctgacctg cctggtcaaa ggcttctatc ccagcgacat cgccgtggag
900
tgggagagca atggccagcc cgagaacaac tacaagacca cccctcccgt gctggactcc
960
gacggctcct tcttcctcta cagcaagctc accgtggaca agagcaggtg gcagcagggc
1020
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac ccagaagagc
1080
ctctccctgt ctcccggcaa atgagatatc gggcccgttt aaacggggga ggctaac
1137
<210> 28
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи chB1
<400> 28
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Thr Ala Ser Ser Leu Ser
20 25 30
Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp
35 40 45
Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val
50 55 60
Lys Leu Leu Ile Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr His Tyr Ser Leu Thr Ile Thr
85 90 95
Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Tyr
100 105 110
Pro Leu Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Ala Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 29
<211> 752
<212> ДНК
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> фрагмент ДНК, содержащий последовательность ДНК, кодирующую
аминокислотную последовательность легкой цепи chB1
<400> 29
ccagcctccg gactctagag ccaccatggt gctgcagacc caggtgttca tcagcctgct
60
gctgtggatc agcggcgcct acggcgacat ccagatgacc cagacagcca gcagcctgag
120
cgccagcctg ggcgatagag tgaccatcag ctgcagagcc agccaggaca tcaacaacta
180
cctgaactgg tatcagcaga aacccgacgg caccgtgaag ctgctgatct acttcaccag
240
cagactgcac agcggcgtgc ccagcagatt ttctggcagc ggctctggca cccactacag
300
cctgaccatc accaacctgg aacaggaaga tatcgctacc tacttctgtc agcaaggcta
360
ccccctgccc tggacctttg gcggcggaac aaagctggaa atcaagcggg ccgtggccgc
420
tccctccgtg ttcatctttc cacccagcga cgagcagctg aagtccggca cagctagcgt
480
cgtgtgcctg ctgaacaact tctacccccg cgaggccaag gtgcagtgga aggtggacaa
540
tgccctgcag agcggcaaca gccaggaaag cgtgaccgag caggacagca aggactccac
600
ctactccctg agcagcaccc tgaccctgag caaggccgac tacgagaagc acaaggtgta
660
cgcctgcgaa gtgacccacc agggcctgtc tagccccgtg accaagagct tcaaccgggg
720
cgagtgttga gtttaaacgg gggaggctaa ct
752
<210> 30
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области легкой
цепи chB1
<400> 30
Asp Ile Gln Met Thr Gln Thr Ala Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Tyr Ser Leu Thr Ile Thr Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 31
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая аминокислотную
последовательность вариабельной области легкой цепи chB1
<400> 31
gacatccaga tgacccagac agccagcagc ctgagcgcca gcctgggcga tagagtgacc
60
atcagctgca gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
120
gacggcaccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
180
agattttctg gcagcggctc tggcacccac tacagcctga ccatcaccaa cctggaacag
240
gaagatatcg ctacctactt ctgtcagcaa ggctaccccc tgccctggac ctttggcggc
300
ggaacaaagc tggaaatcaa g
321
<210> 32
<211> 471
<212> PRT
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи chB1
<400> 32
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys
20 25 30
Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe
35 40 45
Thr Glu Tyr Thr Met His Trp Val Gln Gln Ser His Gly Lys Ser Leu
50 55 60
Glu Trp Ile Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
145 150 155 160
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
210 215 220
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
225 230 235 240
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
245 250 255
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
260 265 270
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
275 280 285
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
290 295 300
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
305 310 315 320
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
325 330 335
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
340 345 350
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
355 360 365
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
370 375 380
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
385 390 395 400
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
405 410 415
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
420 425 430
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
435 440 445
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
450 455 460
Leu Ser Leu Ser Pro Gly Lys
465 470
<210> 33
<211> 1413
<212> ДНК
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая тяжелую цепь chB1
<400> 33
atgaaacacc tgtggttctt cctcctgctg gtggcagctc ccagatgggt gctgagcgaa
60
gtgcagctgc agcagtctgg ccccgagctc gtgaaacctg gcgcctccgt gaagatcagc
120
tgcaagacca gcggctacac cttcaccgag tacaccatgc actgggtgca gcagagccac
180
ggcaagagcc tggaatggat cggcggcgtg aaccccaaca gcggcgacac cagctacaac
240
cagaagttca agggcaaggc caccctgacc gtggacaaga gcagcagcac cgcctacatg
300
gaactgcgga gcctgaccag cgaggacagc gccgtgtact actgtgccag acctggcggc
360
tacgacgtgg gctactacgc catggattac tggggccagg gcaccagcgt gaccgtcagc
420
tcagcctcca ccaagggccc aagcgtcttc cccctggcac cctcctccaa gagcacctct
480
ggcggcacag ccgccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg
540
agctggaact caggcgccct gaccagcggc gtgcacacct tccccgctgt cctgcagtcc
600
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag
660
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gagagttgag
720
cccaaatctt gtgacaaaac tcacacatgc ccaccctgcc cagcacctga agccgcgggg
780
ggaccctcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc
840
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac
900
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccccggga ggagcagtac
960
aacagcacgt accgggtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc
1020
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc
1080
tccaaagcca aaggccagcc ccgggaacca caggtgtaca ccctgccccc atcccgggag
1140
gagatgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac
1200
atcgccgtgg agtgggagag caatggccag cccgagaaca actacaagac cacccctccc
1260
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg
1320
tggcagcagg gcaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac
1380
acccagaaga gcctctccct gtctcccggc aaa
1413
<210> 34
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области тяжелой
цепи chB1
<400> 34
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Gln Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 35
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> химерное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
тяжелой цепи chB1
<400> 35
gaagtgcagc tgcagcagtc tggccccgag ctcgtgaaac ctggcgcctc cgtgaagatc
60
agctgcaaga ccagcggcta caccttcacc gagtacacca tgcactgggt gcagcagagc
120
cacggcaaga gcctggaatg gatcggcggc gtgaacccca acagcggcga caccagctac
180
aaccagaagt tcaagggcaa ggccaccctg accgtggaca agagcagcag caccgcctac
240
atggaactgc ggagcctgac cagcgaggac agcgccgtgt actactgtgc cagacctggc
300
ggctacgacg tgggctacta cgccatggat tactggggcc agggcaccag cgtgaccgtc
360
agctca
366
<210> 36
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкую цепь hL1
гуманизированного антитела
<400> 36
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
35 40 45
Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr
100 105 110
Pro Leu Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 37
<211> 702
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая легкую цепь hL1
гуманизированного антитела
<400> 37
atggtgctgc agacccaggt gttcatctcc ctgctgctgt ggatctccgg cgcgtacggc
60
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
120
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaagccc
180
ggcaaggccc ccaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
240
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
300
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccttggac atttggccag
360
ggcaccaagg tggaaatcaa gcgtacggtg gccgccccct ccgtgttcat cttccccccc
420
tccgacgagc agctgaagtc cggcaccgcc tccgtggtgt gcctgctgaa taacttctac
480
cccagagagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg gaactcccag
540
gagagcgtga ccgagcagga cagcaaggac agcacctaca gcctgagcag caccctgacc
600
ctgagcaaag ccgactacga gaagcacaag gtgtacgcct gcgaggtgac ccaccagggc
660
ctgagctccc ccgtcaccaa gagcttcaac aggggggagt gt
702
<210> 38
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области легкой
цепи hL1 гуманизированного антитела
<400> 38
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 39
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
легкой цепи hL1 гуманизированного антитела
<400> 39
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
60
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaagccc
120
ggcaaggccc ccaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
180
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
240
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccttggac atttggccag
300
ggcaccaagg tggaaatcaa g
321
<210> 40
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи hL2
гуманизированного антитела
<400> 40
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
35 40 45
Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Val
50 55 60
Lys Leu Leu Ile Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr His Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr
100 105 110
Pro Leu Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 41
<211> 702
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая легкую цепь hL2
гуманизированного антитела
<400> 41
atggtgctgc agacccaggt gttcatctcc ctgctgctgt ggatctccgg cgcgtacggc
60
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
120
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
180
ggcaaggccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
240
agattttctg gcagcggctc tggcacccac tacaccctga caatcagcag cctgcagccc
300
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccttggac atttggccag
360
ggcaccaagg tggaaatcaa gcgtacggtg gccgccccct ccgtgttcat cttccccccc
420
tccgacgagc agctgaagtc cggcaccgcc tccgtggtgt gcctgctgaa taacttctac
480
cccagagagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg gaactcccag
540
gagagcgtga ccgagcagga cagcaaggac agcacctaca gcctgagcag caccctgacc
600
ctgagcaaag ccgactacga gaagcacaag gtgtacgcct gcgaggtgac ccaccagggc
660
ctgagctccc ccgtcaccaa gagcttcaac aggggggagt gt
702
<210> 42
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области легкой
цепи hL2 гуманизированного антитела
<400> 42
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 43
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
легкой цепи hL2 гуманизированного антитела
<400> 43
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
60
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
120
ggcaaggccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
180
agattttctg gcagcggctc tggcacccac tacaccctga caatcagcag cctgcagccc
240
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccttggac atttggccag
300
ggcaccaagg tggaaatcaa g
321
<210> 44
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи hL3
гуманизированного антитела
<400> 44
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
35 40 45
Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gly Ala Val
50 55 60
Lys Leu Leu Ile Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr
100 105 110
Pro Leu Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 45
<211> 702
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая легкую цепь hL3
гуманизированного антитела
<400> 45
atggtgctgc agacccaggt gttcatctcc ctgctgctgt ggatctccgg cgcgtacggc
60
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
120
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
180
ggcggagccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
240
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
300
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccctggac atttggcggc
360
ggaacaaagg tggaaatcaa gcgtacggtg gccgccccct ccgtgttcat cttccccccc
420
tccgacgagc agctgaagtc cggcaccgcc tccgtggtgt gcctgctgaa taacttctac
480
cccagagagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg gaactcccag
540
gagagcgtga ccgagcagga cagcaaggac agcacctaca gcctgagcag caccctgacc
600
ctgagcaaag ccgactacga gaagcacaag gtgtacgcct gcgaggtgac ccaccagggc
660
ctgagctccc ccgtcaccaa gagcttcaac aggggggagt gt
702
<210> 46
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
легкой цепи hL3 гуманизированного антитела
<400> 46
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gly Ala Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Tyr Pro Leu Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 47
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
легкой цепи hL3 гуманизированного антитела
<400> 47
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
60
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
120
ggcggagccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
180
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
240
gaggacttcg ccacctacta ctgccagcag ggctaccccc tgccctggac atttggcggc
300
ggaacaaagg tggaaatcaa g
321
<210> 48
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи hL4
гуманизированного антитела
<400> 48
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
35 40 45
Ile Asn Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gly Ala Val
50 55 60
Lys Leu Leu Ile Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn
100 105 110
Thr Leu Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 49
<211> 702
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая легкую цепь hL4
гуманизированного антитела
<400> 49
atggtgctgc agacccaggt gttcatctcc ctgctgctgt ggatctccgg cgcgtacggc
60
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
120
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
180
ggcggagccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
240
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
300
gaggacttcg ccacctacta ctgccagcag ggcaacaccc tgccctggac atttggcgga
360
ggcaccaagg tggaaatcaa gcgtacggtg gccgccccct ccgtgttcat cttccccccc
420
tccgacgagc agctgaagtc cggcaccgcc tccgtggtgt gcctgctgaa taacttctac
480
cccagagagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg gaactcccag
540
gagagcgtga ccgagcagga cagcaaggac agcacctaca gcctgagcag caccctgacc
600
ctgagcaaag ccgactacga gaagcacaag gtgtacgcct gcgaggtgac ccaccagggc
660
ctgagctccc ccgtcaccaa gagcttcaac aggggggagt gt
702
<210> 50
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области легкой
цепи hL4 гуманизированного антитела
<400> 50
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gly Ala Val Lys Leu Leu Ile
35 40 45
Tyr Phe Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 51
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
легкой цепи hL4 гуманизированного антитела
<400> 51
gacatccaga tgacccagag ccctagcagc ctgagcgcca gcgtgggcga cagagtgacc
60
atcacctgta gagccagcca ggacatcaac aactacctga actggtatca gcagaaaccc
120
ggcggagccg tgaagctgct gatctacttc accagcagac tgcacagcgg cgtgcccagc
180
agattttctg gcagcggctc cggcaccgac tacaccctga caatcagcag cctgcagccc
240
gaggacttcg ccacctacta ctgccagcag ggcaacaccc tgccctggac atttggcgga
300
ggcaccaagg tggaaatcaa g
321
<210> 52
<211> 471
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи hH1
гуманизированного антитела
<400> 52
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Glu Tyr Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
50 55 60
Glu Trp Met Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala
65 70 75 80
Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
145 150 155 160
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
210 215 220
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
225 230 235 240
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
245 250 255
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
260 265 270
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
275 280 285
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
290 295 300
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
305 310 315 320
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
325 330 335
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
340 345 350
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
355 360 365
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
370 375 380
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
385 390 395 400
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
405 410 415
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
420 425 430
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
435 440 445
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
450 455 460
Leu Ser Leu Ser Pro Gly Lys
465 470
<210> 53
<211> 1413
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая тяжелую цепь hH1
гуманизированного антитела
<400> 53
atgaaacacc tgtggttctt cctcctgctg gtggcagctc ccagatgggt gctgagccag
60
gtgcagctgg tgcagtctgg cgccgaagtg aagaaaccag gcgccagcgt gaaggtgtcc
120
tgcaaggcca gcggctacac ctttaccgag tacaccatgc actgggtgcg ccaggctcca
180
ggccagggac tggaatggat gggcggcgtg aaccccaaca gcggcgatac aagctacgcc
240
cagaaattcc agggcagagt gaccatcacc gccgacacca gcacctccac cgcctacatg
300
gaactgagca gcctgcggag cgaggacacc gccgtgtact actgtgctag acctggcggc
360
tacgacgtgg gctactacgc catggattac tggggccagg gcaccctcgt gaccgtcagc
420
tcagcctcca ccaagggccc aagcgtcttc cccctggcac cctcctccaa gagcacctct
480
ggcggcacag ccgccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg
540
agctggaact caggcgccct gaccagcggc gtgcacacct tccccgctgt cctgcagtcc
600
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag
660
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gagagttgag
720
cccaaatctt gtgacaaaac tcacacatgc ccaccctgcc cagcacctga agccgcgggg
780
ggaccctcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc
840
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac
900
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccccggga ggagcagtac
960
aacagcacgt accgggtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc
1020
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc
1080
tccaaagcca aaggccagcc ccgggaacca caggtgtaca ccctgccccc atcccgggag
1140
gagatgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac
1200
atcgccgtgg agtgggagag caatggccag cccgagaaca actacaagac cacccctccc
1260
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg
1320
tggcagcagg gcaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac
1380
acccagaaga gcctctccct gtctcccggc aaa
1413
<210> 54
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области тяжелой
цепи hH1 гуманизированного антитела
<400> 54
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 55
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
тяжелой цепи hH1 гуманизированного антитела
<400> 55
caggtgcagc tggtgcagtc tggcgccgaa gtgaagaaac caggcgccag cgtgaaggtg
60
tcctgcaagg ccagcggcta cacctttacc gagtacacca tgcactgggt gcgccaggct
120
ccaggccagg gactggaatg gatgggcggc gtgaacccca acagcggcga tacaagctac
180
gcccagaaat tccagggcag agtgaccatc accgccgaca ccagcacctc caccgcctac
240
atggaactga gcagcctgcg gagcgaggac accgccgtgt actactgtgc tagacctggc
300
ggctacgacg tgggctacta cgccatggat tactggggcc agggcaccct cgtgaccgtc
360
agctca
366
<210> 56
<211> 471
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи hH2
гуманизированного антитела
<400> 56
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Thr Phe
35 40 45
Thr Glu Tyr Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Ser Leu
50 55 60
Glu Trp Met Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala
65 70 75 80
Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
145 150 155 160
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
210 215 220
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
225 230 235 240
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
245 250 255
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
260 265 270
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
275 280 285
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
290 295 300
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
305 310 315 320
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
325 330 335
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
340 345 350
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
355 360 365
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
370 375 380
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
385 390 395 400
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
405 410 415
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
420 425 430
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
435 440 445
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
450 455 460
Leu Ser Leu Ser Pro Gly Lys
465 470
<210> 57
<211> 1413
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая тяжелую цепь hH2
гуманизированного антитела
<400> 57
atgaaacacc tgtggttctt cctcctgctg gtggcagctc ccagatgggt gctgagcgaa
60
gtgcagctgg tgcagtctgg cgccgaagtg aagaaaccag gcgccagcgt gaaggtgtcc
120
tgcaagacca gcggctacac ctttaccgag tacaccatgc actgggtgcg ccaggcccct
180
ggcaagagcc tggaatggat gggcggcgtg aaccccaaca gcggcgatac aagctacgcc
240
cagaaattcc agggcagagt gaccatcacc gccgacacca gcacctccac cgcctacatg
300
gaactgagca gcctgcggag cgaggacacc gccgtgtact actgtgctag acctggcggc
360
tacgacgtgg gctactacgc catggattac tggggccagg gcaccctcgt gaccgtcagc
420
tcagcctcca ccaagggccc aagcgtcttc cccctggcac cctcctccaa gagcacctct
480
ggcggcacag ccgccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg
540
agctggaact caggcgccct gaccagcggc gtgcacacct tccccgctgt cctgcagtcc
600
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag
660
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gagagttgag
720
cccaaatctt gtgacaaaac tcacacatgc ccaccctgcc cagcacctga agccgcgggg
780
ggaccctcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc
840
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac
900
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccccggga ggagcagtac
960
aacagcacgt accgggtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc
1020
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc
1080
tccaaagcca aaggccagcc ccgggaacca caggtgtaca ccctgccccc atcccgggag
1140
gagatgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac
1200
atcgccgtgg agtgggagag caatggccag cccgagaaca actacaagac cacccctccc
1260
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg
1320
tggcagcagg gcaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac
1380
acccagaaga gcctctccct gtctcccggc aaa
1413
<210> 58
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области тяжелой
цепи hH2 гуманизированного антитела
<400> 58
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Ser Leu Glu Trp Met
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 59
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
тяжелой цепи hH2 гуманизированного антитела
<400> 59
gaagtgcagc tggtgcagtc tggcgccgaa gtgaagaaac caggcgccag cgtgaaggtg
60
tcctgcaaga ccagcggcta cacctttacc gagtacacca tgcactgggt gcgccaggcc
120
cctggcaaga gcctggaatg gatgggcggc gtgaacccca acagcggcga tacaagctac
180
gcccagaaat tccagggcag agtgaccatc accgccgaca ccagcacctc caccgcctac
240
atggaactga gcagcctgcg gagcgaggac accgccgtgt actactgtgc tagacctggc
300
ggctacgacg tgggctacta cgccatggat tactggggcc agggcaccct cgtgaccgtc
360
agctca
366
<210> 60
<211> 471
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи hH3
гуманизированного антитела
<400> 60
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Thr Phe
35 40 45
Thr Glu Tyr Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
50 55 60
Glu Trp Met Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala
65 70 75 80
Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Val Asp Lys Ser Thr Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
130 135 140
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
145 150 155 160
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
165 170 175
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
180 185 190
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
195 200 205
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
210 215 220
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu
225 230 235 240
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
245 250 255
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
260 265 270
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
275 280 285
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
290 295 300
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
305 310 315 320
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
325 330 335
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
340 345 350
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
355 360 365
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
370 375 380
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
385 390 395 400
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
405 410 415
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
420 425 430
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
435 440 445
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
450 455 460
Leu Ser Leu Ser Pro Gly Lys
465 470
<210> 61
<211> 1413
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая тяжелую цепь hH3
гуманизированного антитела
<400> 61
atgaaacacc tgtggttctt cctcctgctg gtggcagctc ccagatgggt gctgagcgaa
60
gtgcagctgg tgcagtctgg cgccgaagtg aagaaaccag gcgccagcgt gaaggtgtcc
120
tgcaagacca gcggctacac ctttaccgag tacaccatgc actgggtgcg ccaggctcca
180
ggccagggac tggaatggat gggcggcgtg aaccccaaca gcggcgatac aagctacgcc
240
cagaaattcc agggcagagt gaccctgacc gtggacaaga gcaccagcac cgcctacatg
300
gaactgagca gcctgcggag cgaggacacc gccgtgtact actgtgctag acctggcggc
360
tacgacgtgg gctactacgc catggattac tggggccagg gcaccctcgt gaccgtcagc
420
tcagcctcca ccaagggccc aagcgtcttc cccctggcac cctcctccaa gagcacctct
480
ggcggcacag ccgccctggg ctgcctggtc aaggactact tccccgaacc cgtgaccgtg
540
agctggaact caggcgccct gaccagcggc gtgcacacct tccccgctgt cctgcagtcc
600
tcaggactct actccctcag cagcgtggtg accgtgccct ccagcagctt gggcacccag
660
acctacatct gcaacgtgaa tcacaagccc agcaacacca aggtggacaa gagagttgag
720
cccaaatctt gtgacaaaac tcacacatgc ccaccctgcc cagcacctga agccgcgggg
780
ggaccctcag tcttcctctt ccccccaaaa cccaaggaca ccctcatgat ctcccggacc
840
cctgaggtca catgcgtggt ggtggacgtg agccacgaag accctgaggt caagttcaac
900
tggtacgtgg acggcgtgga ggtgcataat gccaagacaa agccccggga ggagcagtac
960
aacagcacgt accgggtggt cagcgtcctc accgtcctgc accaggactg gctgaatggc
1020
aaggagtaca agtgcaaggt ctccaacaaa gccctcccag cccccatcga gaaaaccatc
1080
tccaaagcca aaggccagcc ccgggaacca caggtgtaca ccctgccccc atcccgggag
1140
gagatgacca agaaccaggt cagcctgacc tgcctggtca aaggcttcta tcccagcgac
1200
atcgccgtgg agtgggagag caatggccag cccgagaaca actacaagac cacccctccc
1260
gtgctggact ccgacggctc cttcttcctc tacagcaagc tcaccgtgga caagagcagg
1320
tggcagcagg gcaacgtctt ctcatgctcc gtgatgcatg aggctctgca caaccactac
1380
acccagaaga gcctctccct gtctcccggc aaa
1413
<210> 62
<211> 122
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность вариабельной области
тяжелой цепи hH3 гуманизированного антитела
<400> 62
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Asn Pro Asn Ser Gly Asp Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Gly Gly Tyr Asp Val Gly Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 63
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая вариабельную
область
тяжелой цепи hH3 гуманизированного антитела
<400> 63
gaagtgcagc tggtgcagtc tggcgccgaa gtgaagaaac caggcgccag cgtgaaggtg
60
tcctgcaaga ccagcggcta cacctttacc gagtacacca tgcactgggt gcgccaggct
120
ccaggccagg gactggaatg gatgggcggc gtgaacccca acagcggcga tacaagctac
180
gcccagaaat tccagggcag agtgaccctg accgtggaca agagcaccag caccgcctac
240
atggaactga gcagcctgcg gagcgaggac accgccgtgt actactgtgc tagacctggc
300
ggctacgacg tgggctacta cgccatggat tactggggcc agggcaccct cgtgaccgtc
360
agctca
366
<210> 64
<211> 214
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи трастузумаба
<400> 64
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Thr Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 65
<211> 450
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи трастузумаба
<400> 65
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 66
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи антитела
к LPS (h#1G5-H1L1)
<400> 66
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala
20 25 30
Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ala Ser Glu Asn
35 40 45
Val Gly Asn Ser Val Ser Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
50 55 60
Lys Leu Leu Ile Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gly Gln Ser Tyr
100 105 110
Ser Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 67
<211> 474
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи антитела
к LPS (h#1G5-H1L1)
<400> 67
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Ser Tyr Trp Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
50 55 60
Glu Trp Met Gly Asn Ile Tyr Pro Gly Ser Ser Ser Ile Asn Tyr Asn
65 70 75 80
Glu Lys Phe Lys Ser Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Thr Ile Tyr Asn Tyr Gly Ser Ser Gly Tyr Asn
115 120 125
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
145 150 155 160
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
165 170 175
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
180 185 190
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
195 200 205
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
210 215 220
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
225 230 235 240
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
245 250 255
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
260 265 270
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
275 280 285
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
290 295 300
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
305 310 315 320
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
325 330 335
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
340 345 350
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
355 360 365
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
370 375 380
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
385 390 395 400
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
405 410 415
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
420 425 430
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
435 440 445
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
450 455 460
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470
<210> 68
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи антитела
к TROP2 (hRS7)
<400> 68
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp
35 40 45
Val Ser Ile Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Tyr
100 105 110
Ile Thr Pro Leu Thr Phe Gly Ala Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 69
<211> 470
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи антитела
к TROP2 (hRS7)
<400> 69
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Gln Val Gln Leu Gln Gln Ser Gly Ser Glu Leu Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu
50 55 60
Lys Trp Met Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Thr
65 70 75 80
Asp Asp Phe Lys Gly Arg Phe Ala Phe Ser Leu Asp Thr Ser Val Ser
85 90 95
Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala Asp Asp Thr Ala Val
100 105 110
Tyr Phe Cys Ala Arg Gly Gly Phe Gly Ser Ser Tyr Trp Tyr Phe Asp
115 120 125
Val Trp Gly Gln Gly Ser Leu Val Thr Val Ser Ser Ala Ser Thr Lys
130 135 140
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
145 150 155 160
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
165 170 175
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
180 185 190
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
195 200 205
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
210 215 220
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro
225 230 235 240
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
245 250 255
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
260 265 270
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
275 280 285
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
290 295 300
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
305 310 315 320
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
325 330 335
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
340 345 350
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
355 360 365
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
370 375 380
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
385 390 395 400
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
405 410 415
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
420 425 430
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
435 440 445
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
450 455 460
Ser Leu Ser Pro Gly Lys
465 470
<210> 70
<211> 240
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи антитела
к CD98 (hM23-H1L1)
<400> 70
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala
20 25 30
Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser
35 40 45
Leu Leu Tyr Ser Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg
65 70 75 80
Glu Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Gln Arg Tyr Tyr Gly Tyr Pro Trp Thr Phe Gly Gln Gly Thr
115 120 125
Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe
130 135 140
Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys
145 150 155 160
Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val
165 170 175
Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln
180 185 190
Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser
195 200 205
Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His
210 215 220
Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235 240
<210> 71
<211> 465
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи антитела
к CD98 (hM23-H1L1)
<400> 71
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys
20 25 30
Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ala Phe
35 40 45
Ser Asn Tyr Leu Ile Glu Trp Val Arg Gln Ala Pro Gly Gln Gly Leu
50 55 60
Glu Trp Met Gly Val Ile Asn Pro Gly Ser Gly Val Thr Asn Tyr Asn
65 70 75 80
Glu Lys Phe Lys Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Ala Glu Ala Trp Phe Ala Tyr Trp Gly Gln Gly
115 120 125
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
130 135 140
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
145 150 155 160
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
165 170 175
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
180 185 190
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
195 200 205
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
210 215 220
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
225 230 235 240
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
245 250 255
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
260 265 270
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
275 280 285
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
290 295 300
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
305 310 315 320
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
325 330 335
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
340 345 350
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
355 360 365
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
370 375 380
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
385 390 395 400
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
405 410 415
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
420 425 430
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
435 440 445
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455 460
Lys
465
<210> 72
<211> 702
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая легкую цепь
мутанта трастузумаба
<400> 72
atggtgctgc agacccaggt gttcatctcc ctgctgctgt ggatctccgg cgcgtacggc
60
gacatccaga tgacacagag ccctagcagc ctgtctgcca gcgtgggaga cagagtgacc
120
atcacctgta gagccagcca ggacgtgaac acagccgtgg cttggtatca gcagaagcct
180
ggcaaggccc ctaagctgct gatctacagc gccagctttc tgtacagcgg cgtgcccagc
240
agattcagcg gctctagaag cggcaccgac ttcaccctga ccataagcag tctgcagccc
300
gaggacttcg ccacctacta ctgtcagcag cactacacca cacctccaac ctttggccag
360
ggcaccaagg tggaaatcaa gcgtacggtg gccgccccct ccgtgttcat cttccccccc
420
tccgacgagc agctgaagtc cggcaccgcc tccgtggtgt gcctgctgaa taacttctac
480
cccagagagg ccaaggtgca gtggaaggtg gacaacgccc tgcagtccgg gaactcccag
540
gagagcgtga ccgagcagga cagcaaggac agcacctaca gcctgagcag caccctgacc
600
ctgagcaaag ccgactacga gaagcacaag gtgtacgcct gcgaggtgac ccaccagggc
660
ctgagctccc ccgtcaccaa gagcttcaac aggggggagt gt
702
<210> 73
<211> 234
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность легкой цепи мутанта
трастузубмаба
<400> 73
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
35 40 45
Val Asn Thr Ala Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Leu Leu Ile Tyr Ser Ala Ser Phe Leu Tyr Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Arg Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr
100 105 110
Thr Thr Pro Pro Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210> 74
<211> 1407
<212> ДНК
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> нуклеотидная последовательность, кодирующая тяжелую цепь
мутанта трастузумаба
<400> 74
atgaaacacc tgtggttctt cctcctgctg gtggcagctc ccagatgggt gctgagcgag
60
gtgcagctgg ttgaatctgg cggaggactg gttcagcctg gcggatctct gagactgtct
120
tgtgccgcca gcggcttcaa catcaaggac acctacatcc actgggtccg acaggcccct
180
ggcaaaggac ttgaatgggt cgccagaatc taccccacca acggctacac cagatacgcc
240
gactctgtga agggcagatt caccatcagc gccgacacca gcaagaacac cgcctacctg
300
cagatgaaca gcctgagagc cgaggacacc gccgtgtact actgttctag atggggaggc
360
gacggcttct acgccatgga ttattggggc cagggcaccc tggttaccgt tagctcagcc
420
tccaccaagg gcccaagcgt cttccccctg gcaccctcct ccaagagcac ctctggcggc
480
acagccgccc tgggctgcct ggtcaaggac tacttccccg aacccgtgac cgtgagctgg
540
aactcaggcg ccctgaccag cggcgtgcac accttccccg ctgtcctgca gtcctcagga
600
ctctactccc tcagcagcgt ggtgaccgtg ccctccagca gcttgggcac ccagacctac
660
atctgcaacg tgaatcacaa gcccagcaac accaaggtgg acaagagagt tgagcccaaa
720
tcttgtgaca aaactcacac atgcccaccc tgcccagcac ctgaagccgc ggggggaccc
780
tcagtcttcc tcttcccccc aaaacccaag gacaccctca tgatctcccg gacccctgag
840
gtcacatgcg tggtggtgga cgtgagccac gaagaccctg aggtcaagtt caactggtac
900
gtggacggcg tggaggtgca taatgccaag acaaagcccc gggaggagca gtacaacagc
960
acgtaccggg tggtcagcgt cctcaccgtc ctgcaccagg actggctgaa tggcaaggag
1020
tacaagtgca aggtctccaa caaagccctc ccagccccca tcgagaaaac catctccaaa
1080
gccaaaggcc agccccggga accacaggtg tacaccctgc ccccatcccg ggaggagatg
1140
accaagaacc aggtcagcct gacctgcctg gtcaaaggct tctatcccag cgacatcgcc
1200
gtggagtggg agagcaatgg ccagcccgag aacaactaca agaccacccc tcccgtgctg
1260
gactccgacg gctccttctt cctctacagc aagctcaccg tggacaagag caggtggcag
1320
cagggcaacg tcttctcatg ctccgtgatg catgaggctc tgcacaacca ctacacccag
1380
aagagcctct ccctgtctcc cggcaaa
1407
<210> 75
<211> 469
<212> PRT
<213> Искусственная последовательность
<220>
<223> гуманизированное антитело
<220>
<221> ПЕРЕМЕННЫЙ ПРИЗНАК
<223> аминокислотная последовательность тяжелой цепи мутанта
трастузумаба
<400> 75
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
20 25 30
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile
35 40 45
Lys Asp Thr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
50 55 60
Glu Trp Val Ala Arg Ile Tyr Pro Thr Asn Gly Tyr Thr Arg Tyr Ala
65 70 75 80
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn
85 90 95
Thr Ala Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ser Arg Trp Gly Gly Asp Gly Phe Tyr Ala Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
130 135 140
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
145 150 155 160
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
165 170 175
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
180 185 190
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
195 200 205
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
210 215 220
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
225 230 235 240
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
245 250 255
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
260 265 270
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
275 280 285
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
290 295 300
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
305 310 315 320
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
325 330 335
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
340 345 350
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
355 360 365
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
370 375 380
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
385 390 395 400
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
405 410 415
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
420 425 430
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
435 440 445
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
450 455 460
Leu Ser Pro Gly Lys
465
<---
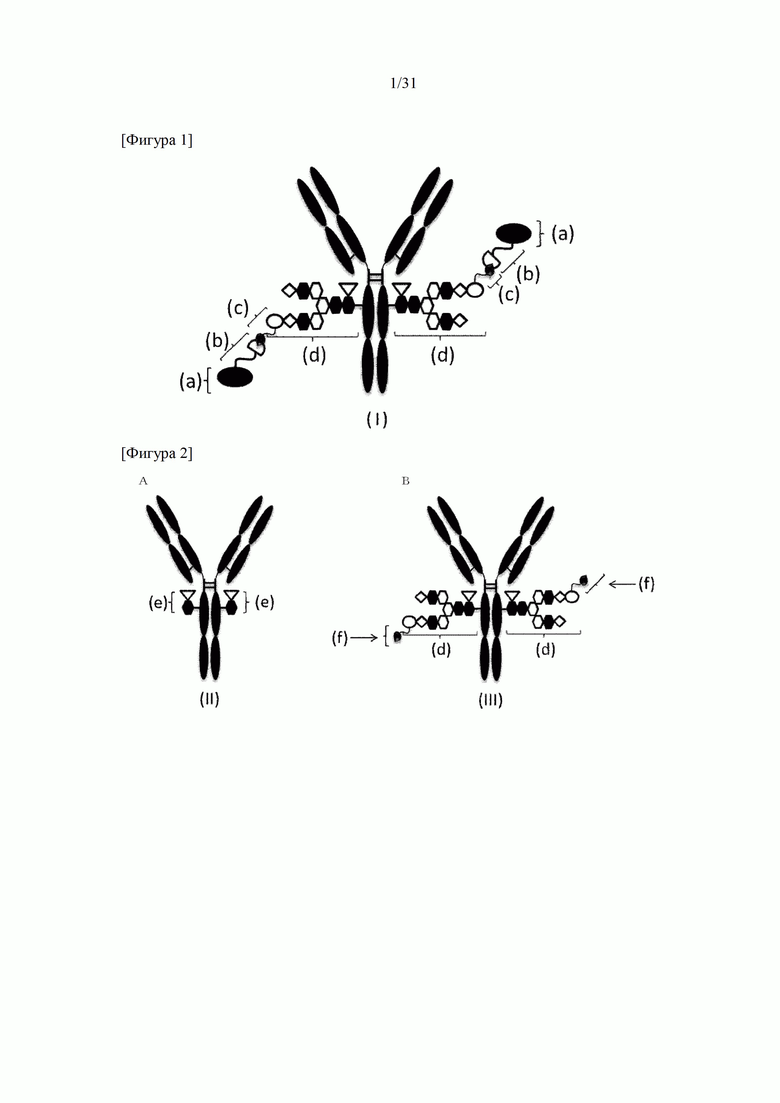
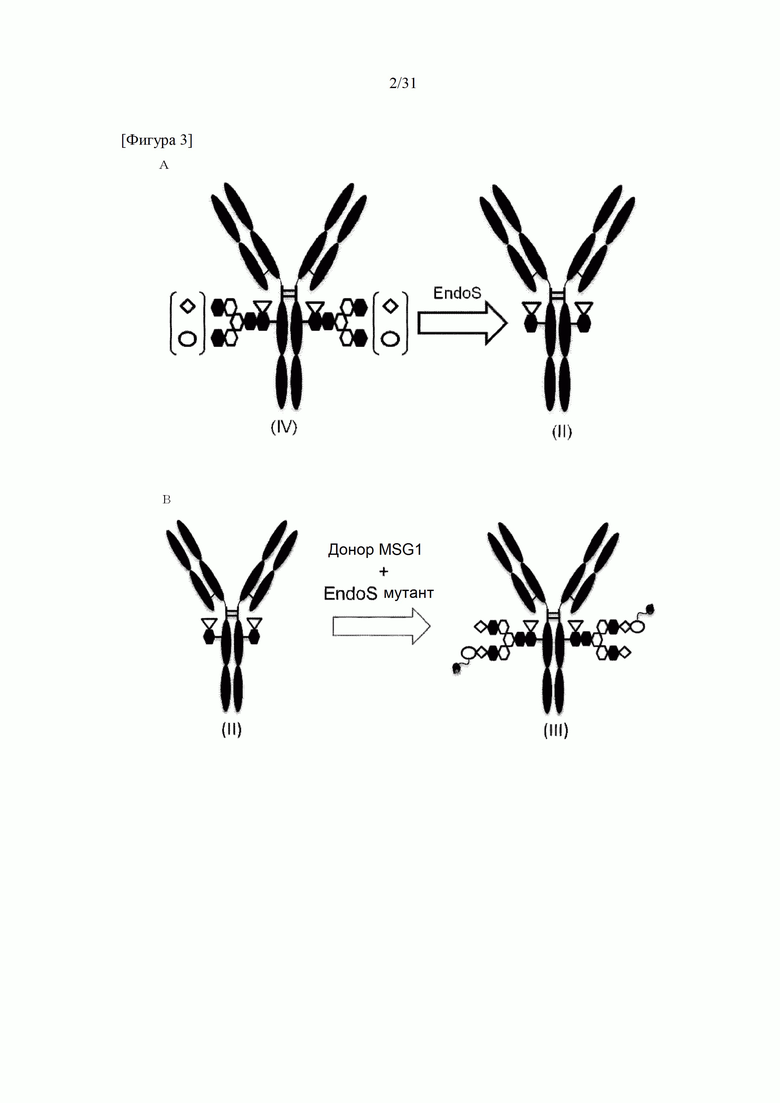
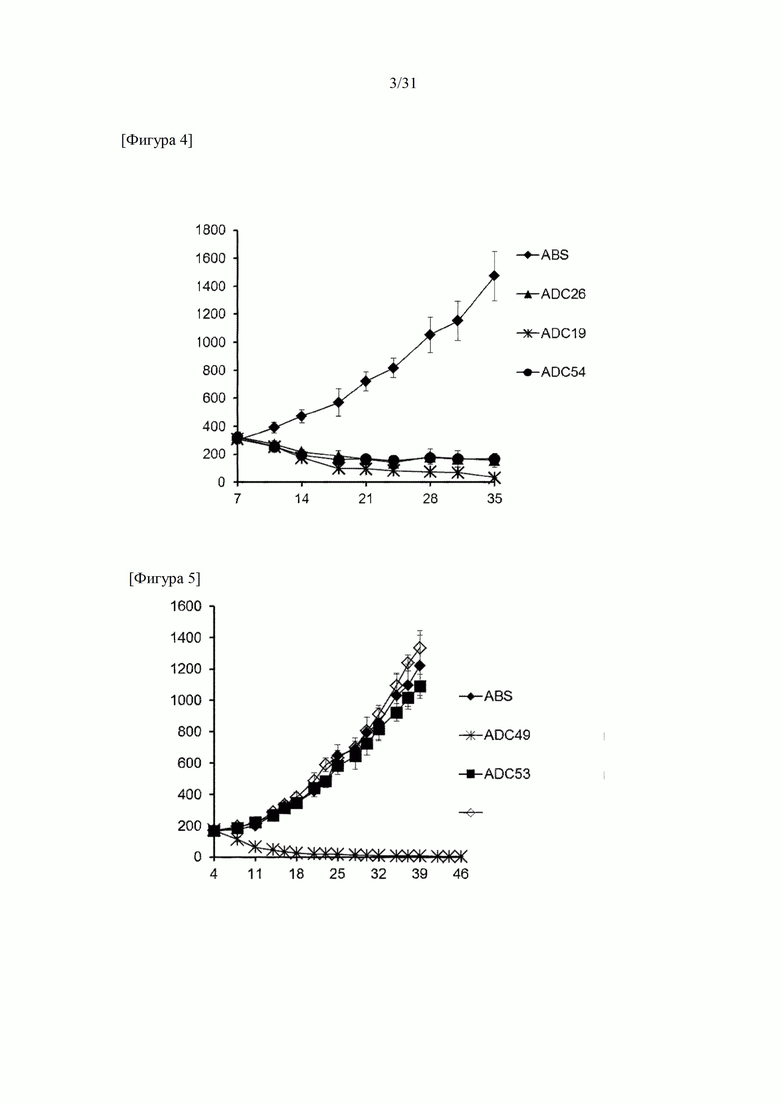
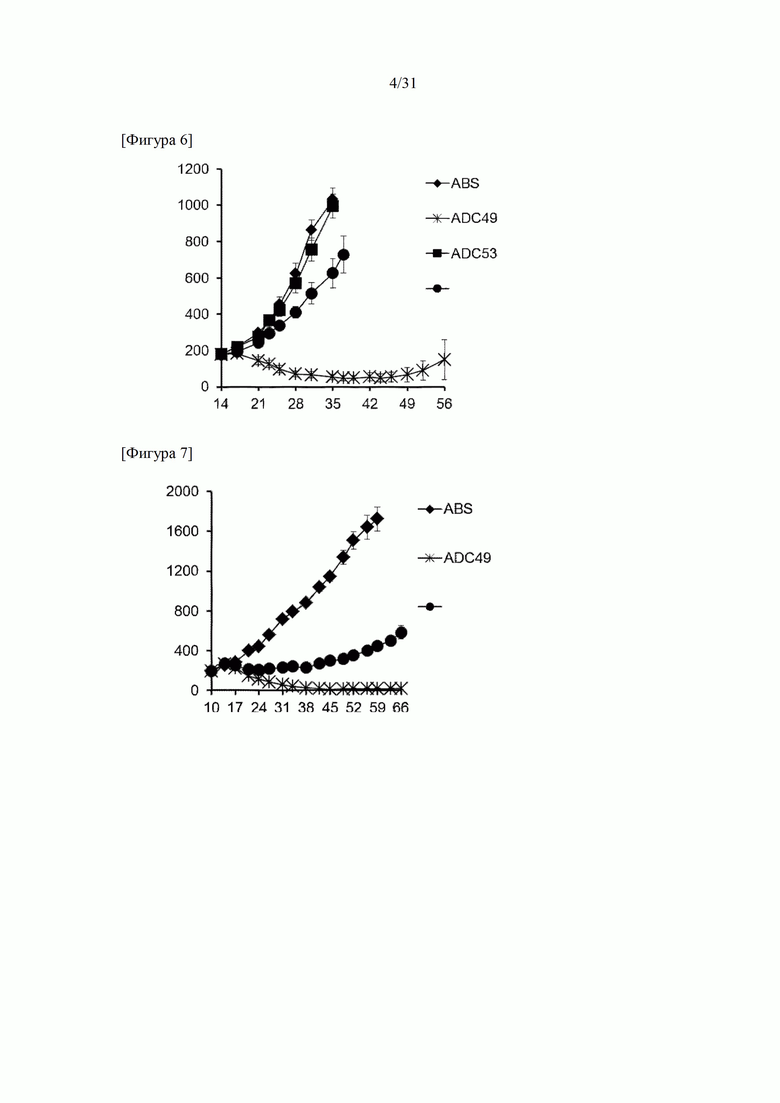
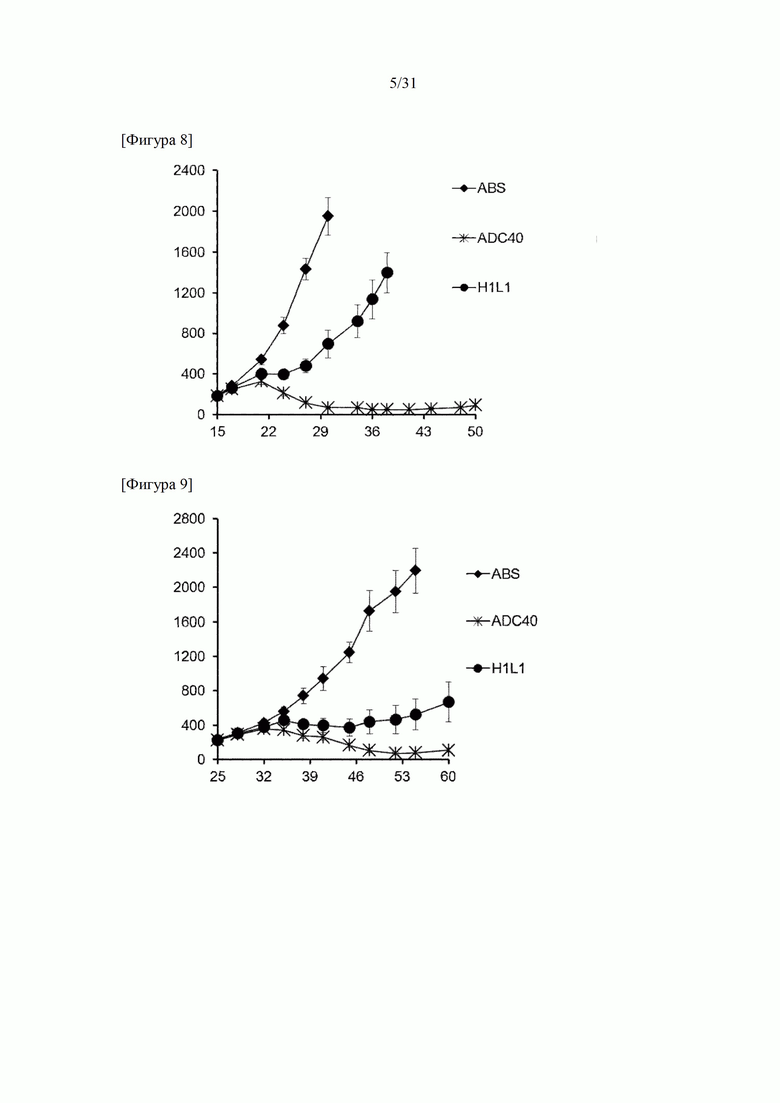
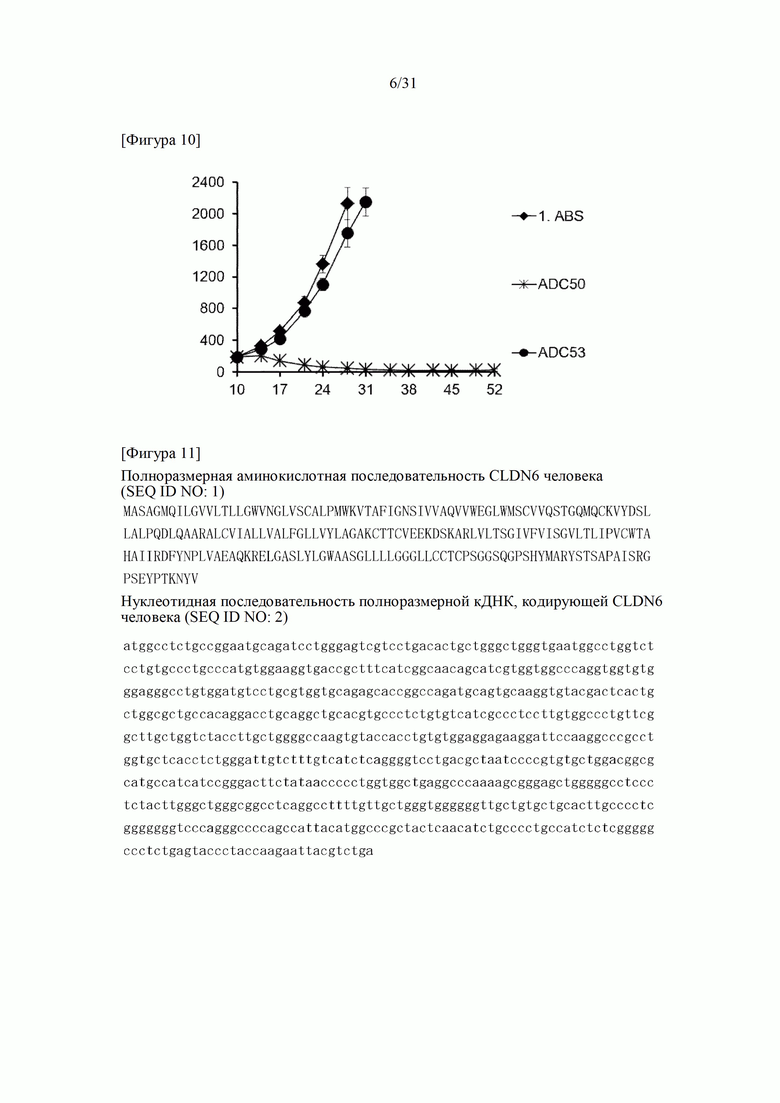


















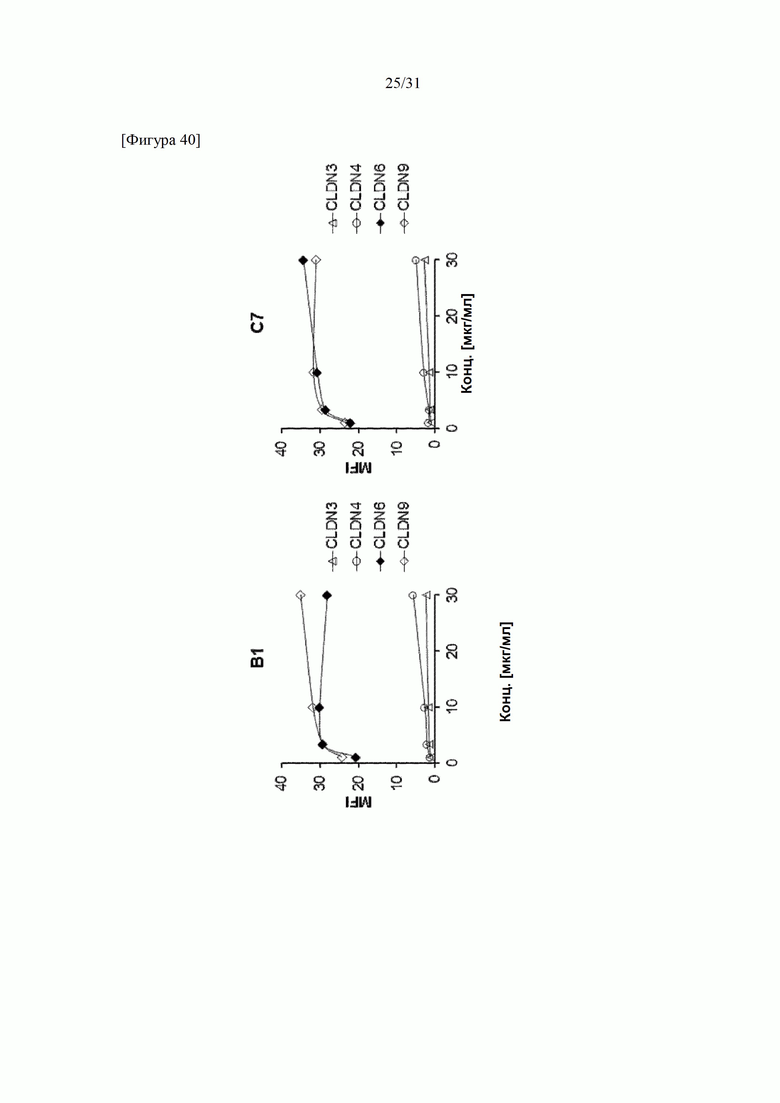
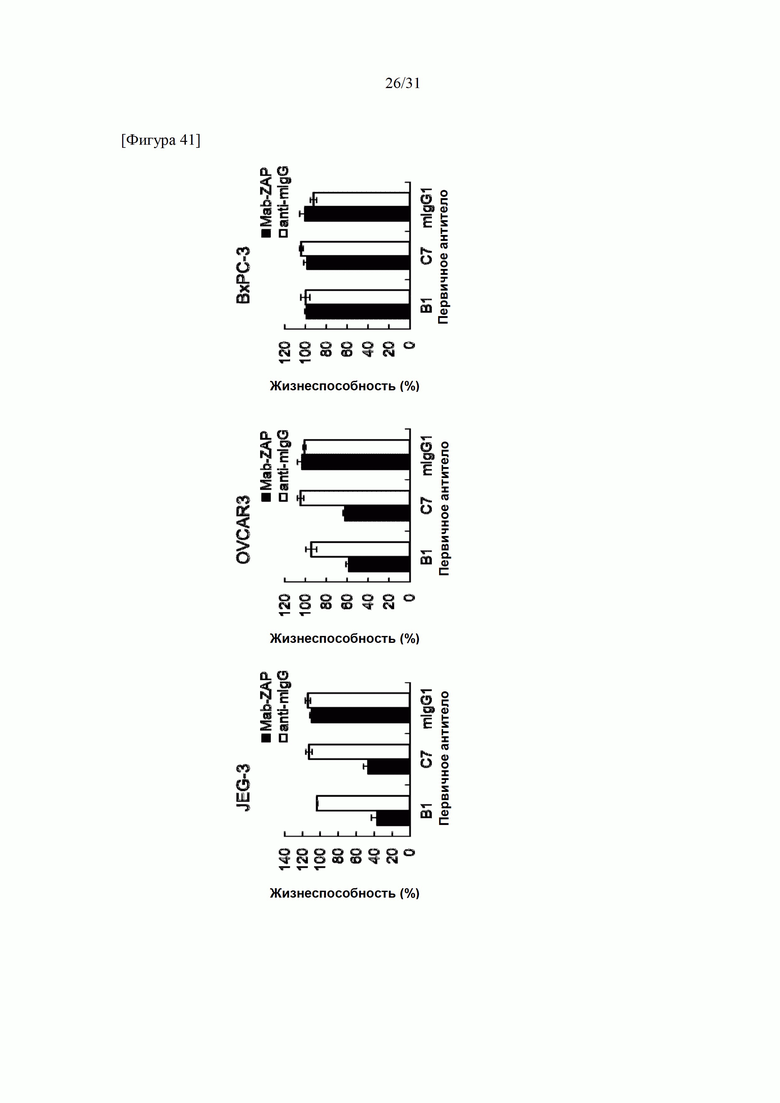
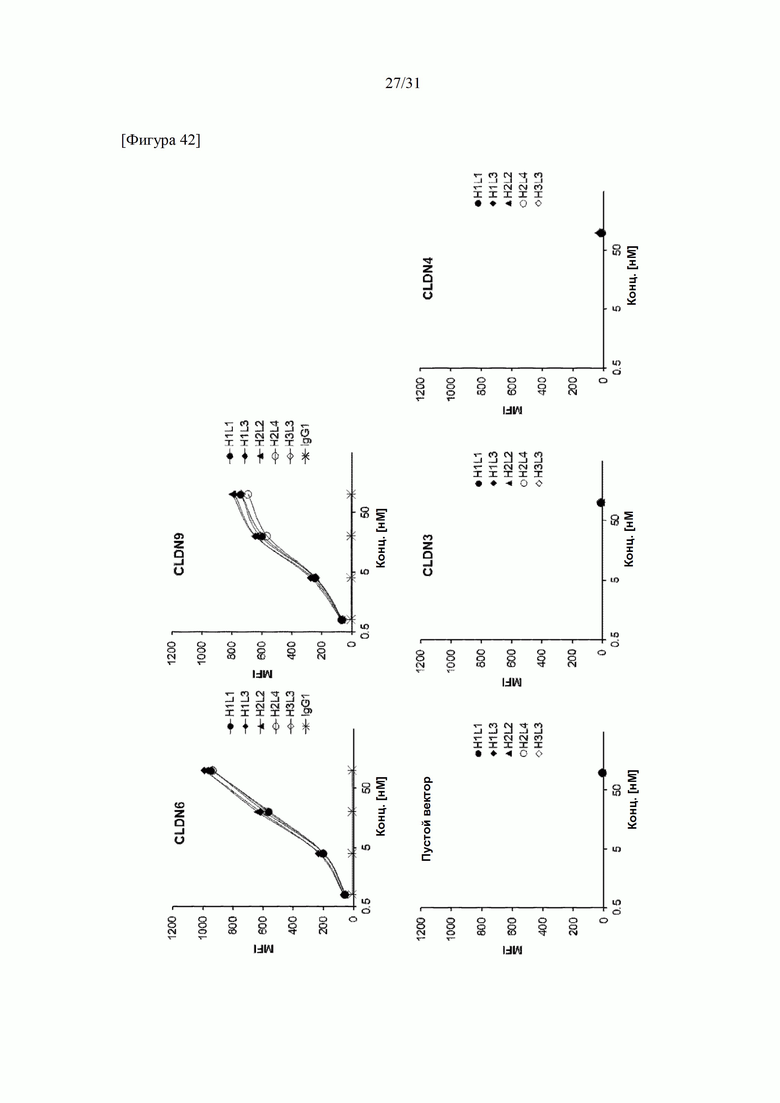



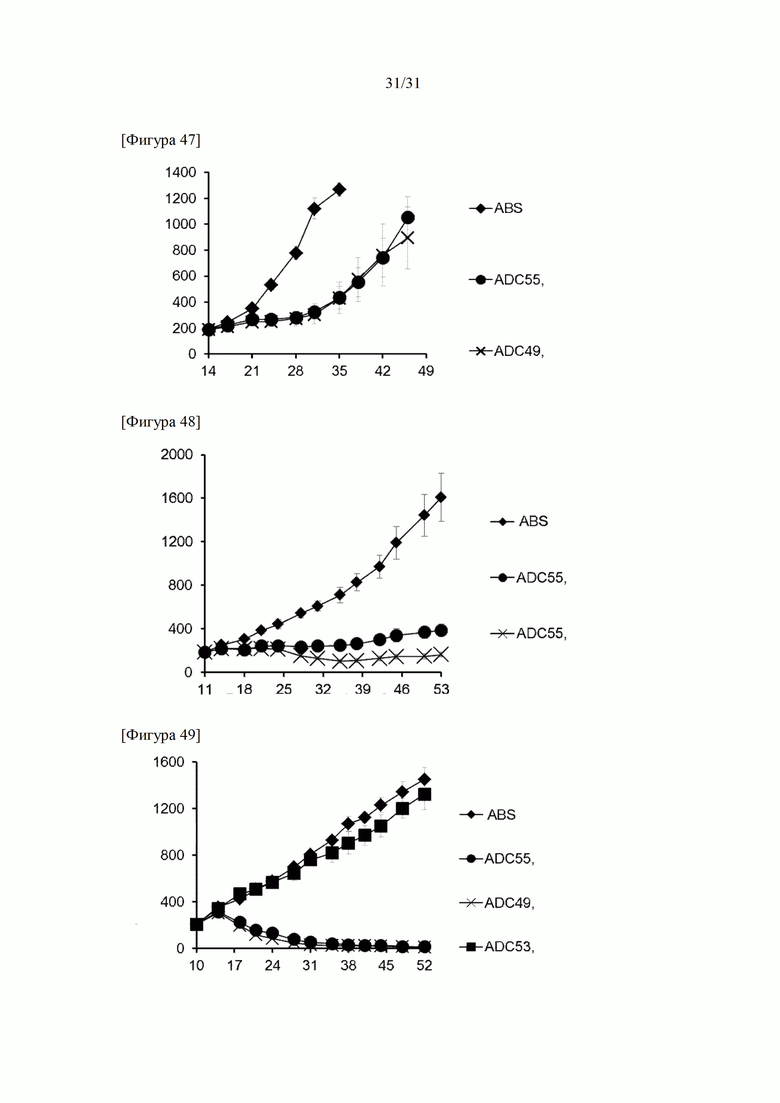
Изобретение относится к области биохимии, в частности к конъюгату антитело-лекарственное средство для лечения и профилактики рака. Раскрыты соединение, которое используют для получения указанного конъюгата; фармацевтическая композиция, содержащая указанный конъюгат. Также раскрыт способ лечения опухоли с помощью указанного конъюгата. Изобретение позволяет эффективно лечить рак. 5 н. и 61 з.п. ф-лы, 2 табл., 49 ил., 154 пр.
1. Конъюгат антитело-лекарственное средство для лечения и профилактики рака, представленный следующей формулой:
[Формула 1]
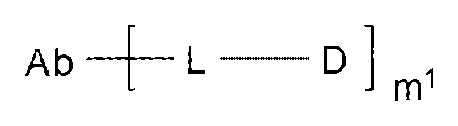 ,
,
где m1 представляет собой целое число от 1 до 10;
Ab представляет собой антитело или функциональный фрагмент указанного антитела, где указанное антитело содержит или не содержит ремоделированный гликан;
L представляет собой линкер, связывающий Ab и D;
Ab может связываться непосредственно через его аминокислотный остаток с L или может связываться через гликан или ремоделированный гликан Ab с L; и
D представляет собой лекарственное средство, представленное следующей формулой:
[Формула 2]
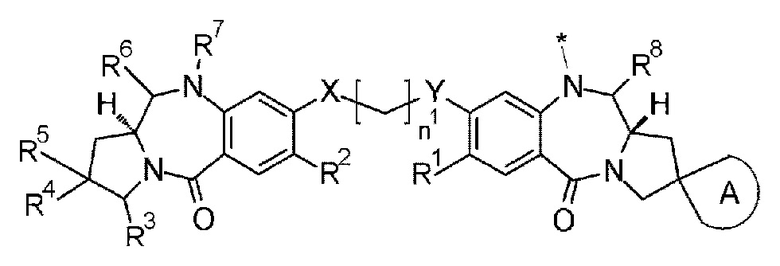 ,
,
где звездочка представляет собой связь с L;
n1 представляет собой целое число от 2 до 8;
A представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл, незамещенный или замещенный одним-четырьмя атомами галогена;
R1 и R2, каждый, независимо представляют собой С1-С6 алкоксигруппу, C1-C6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтиогруппу, атом галогена или -NR'R'', где R' и R'', каждый, независимо представляют собой атом водорода или С1-С6-алкильную группу;
R3, R4 и R5 выбраны из (i)-(iii):
(i) R3 и R4 объединены вместе с атомами углерода, с которыми связаны R3 и R4, с образованием двойной связи и R5 представляет собой арильную группу или гетероарильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 1, или С1-С6-алкильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 2,
(ii) R3 представляет собой атом водорода и R4 и R5 объединены вместе с атомом углерода, с которым R4 и R5 связаны, с образованием трех-пятичленного насыщенного углеводородного кольца, или трех-пятичленного насыщенного гетероцикла, или CH2= и
(iii) R3, R4 и R5 объединены вместе с атомом углерода, с которым связан R3, и атомом углерода, с которым связаны R4 и R5, с образованием бензольного кольца или шестичленного гетероцикла, имеющего или не имеющего один или более заместителей, выбранных из группы 3;
R6 и R7, каждый, представляют собой атом водорода или R6 и R7 объединены и представляют собой иминную связь (C=N);
R8 представляет собой гидроксигруппу или C1-C3 алкоксигруппу;
X и Y, каждый, независимо представляют собой атом кислорода, атом азота или атом серы;
группа 1 представляет собой:
a) С1-С6 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена,
b) C1-C6-алкильную группу, незамещенную или замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR' или
j) гидроксигруппу,
где R' и R'' являются такими, как определено выше, и каждый R''' независимо представляет собой атом водорода или С1-С6-алкильную группу;
группа 2 представляет собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу; и
группа 3 представляет собой атом галогена, или С1-С6-алкильную группу, или С1-С6 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена,
причем раковые клетки в качестве терапевтической мишени экспрессируют белок, распознаваемый антителом, входящим в конъюгат антитело-лекарственное средство.
2. Конъюгат антитело-лекарственное средство по п. 1, где
A представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R1 и R2, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R3 и R4 объединены вместе с атомами углерода, с которыми R3 и R4 связаны, с образованием двойной связи;
R5 представляет собой арильную группу или гетероарильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 4, или C1-C3 алкильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 5;
X и Y, каждый, представляют собой атом кислорода;
группа 4 представляет собой:
a) C1-C3 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена,
b) C1-C3 алкильную группу, незамещенную или замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) С3-С5-циклоалкоксигруппу,
d) -C(=NR')-NR''R''',
e) -NHC(=NR')-NR''R''' или
f) гидроксигруппу,
где R', R'' и каждый R''' независимо представляют собой атом водорода или C1-C3 алкильную группу; и
группа 5 представляет собой атом галогена, гидроксигруппу или C1-C3 алкоксигруппу.
3. Конъюгат антитело-лекарственное средство по п. 1, где
A представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R1 и R2, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R3 представляет собой атом водорода;
R4 и R5 объединены вместе с атомом углерода, с которым связаны R4 и R5, с образованием трех-пятичленного насыщенного углеводородного кольца или =CH2; и
X и Y, каждый, представляют собой атом кислорода.
4. Конъюгат антитело-лекарственное средство по п. 1, где
A представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R1 и R2, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R3, R4 и R5 объединены вместе с атомом углерода, с которым связан R3, и атомом углерода, с которым связаны R4 и R5, с образованием бензольного кольца, имеющего или не имеющего один или более заместителей, выбранных из группы 6;
X и Y, каждый, представляют собой атом кислорода; и
группа 6 представляет собой атом галогена, или C1-C3 алкильную группу, или C1-C3 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена.
5. Конъюгат антитело-лекарственное средство по п. 1 или 2, где D представлен любой из следующих двух формул:
[Формула 3]
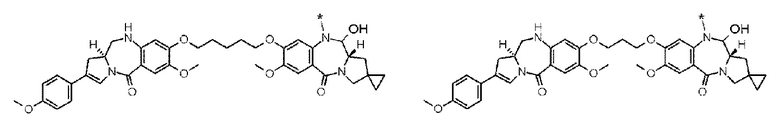 ,
,
где каждая звездочка представляет собой связь с L.
6. Конъюгат антитело-лекарственное средство по п. 1 или 3, где D представлен любой из следующих двух формул:
[Формула 4]
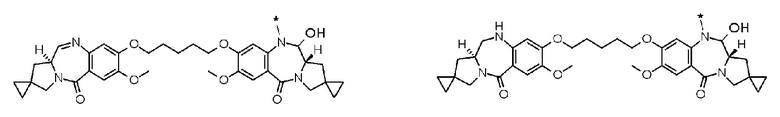 ,
,
где каждая звездочка представляет собой связь с L.
7. Конъюгат антитело-лекарственное средство по любому из пп. 1-6, где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, звездочка представляет собой связь с D;
B представляет собой фенильную группу или гетероарильную группу;
Lp представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой в клетке-мишени;
La представляет собой любой заместитель, выбранный из группы:
-C(=O)-(CH2CH2)n2-C(=O)-,
-C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2)n3-C(=O)-,
-C(=O)-(CH2CH2)n2-C(=O)-NH-(CH2CH2O)n3-CH2-C(=O)-,
-C(=O)-(CH2CH2)n2-NH-C(=O)-(CH2CH2O)n3-CH2CH2-C(=O)- и
-(CH2)n4-O-C(=O)-;
n2 представляет собой целое число от 1 до 3, n3 представляет собой целое число от 1 до 5 и n4 представляет собой целое число от 0 до 2; и
Lb представляет собой спейсер, связывающий La и гликан или ремоделированный гликан Ab.
8. Конъюгат антитело-лекарственное средство по п. 7, где B выбран из 1,4-фенильной группы, 2,5-пиридильной группы, 3,6-пиридильной группы, 2,5-пиримидильной группы и 2,5-тиенильной группы.
9. Конъюгат антитело-лекарственное средство по п. 8, где B представляет собой 1,4-фенильную группу.
10. Конъюгат антитело-лекарственное средство по любому из пп. 7-9, где Lp представляет собой аминокислотные остатки, состоящие из двух-семи аминокислот.
11. Конъюгат антитело-лекарственное средство по любому из пп. 7-10, где Lp представляет собой аминокислотные остатки, состоящие из аминокислот, выбранных из глицина, валина, аланина, фенилаланина, глутаминовой кислоты, изолейцина, пролина, цитруллина, лейцина, серина, лизина и аспарагиновой кислоты.
12. Конъюгат антитело-лекарственное средство по любому из пп. 7-11, где Lp выбран из следующей группы: -GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)PI- и -GGPL-.
13. Конъюгат антитело-лекарственное средство по любому из пп. 7-12, где La выбран из следующей группы:
-C(=O)-CH2CH2-C(=O)-, -C(=O)-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-,
-CH2-OC(=O)- и -OC(=O)-.
14. Конъюгат антитело-лекарственное средство по любому из пп. 7-13, где Lb представлен следующей формулой:
[Формула 5]
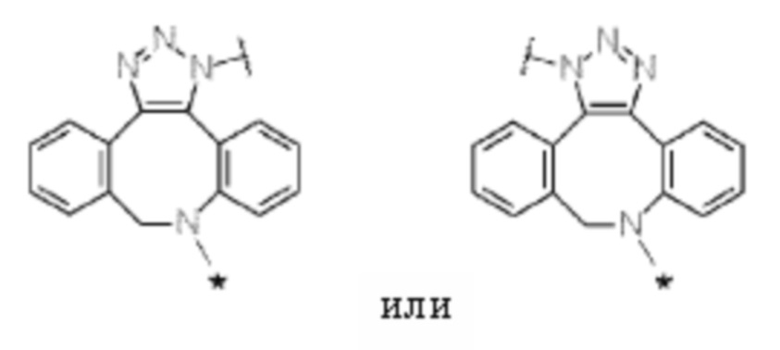 ,
,
[Формула 6]
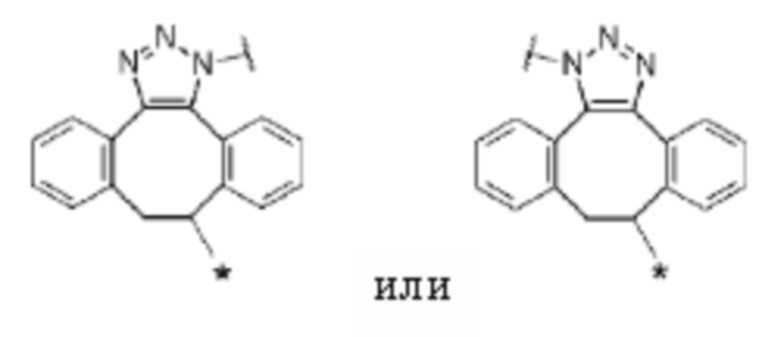 или
или
[Формула 7]
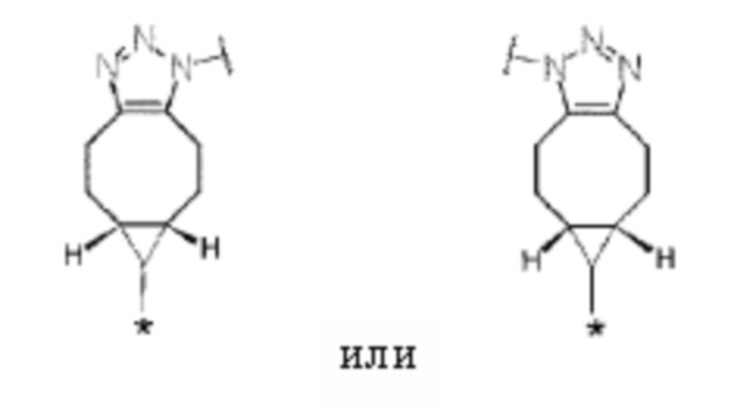 ,
,
где в каждой структурной формуле для Lb, представленной выше,
каждая звездочка представляет собой связь с La и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
15. Конъюгат антитело-лекарственное средство по любому из пп. 7-14, где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, где
B представляет собой 1,4-фенильную группу;
Lp выбран из следующей группы: -GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK- и -GGPL-;
La выбран из следующей группы:
-C(=O)-CH2CH2-C(=O)-, -C(=O)-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-,
-CH2-OC(=O)- и -OC(=O)-; и
Lb представлен следующей формулой:
[Формула 8]
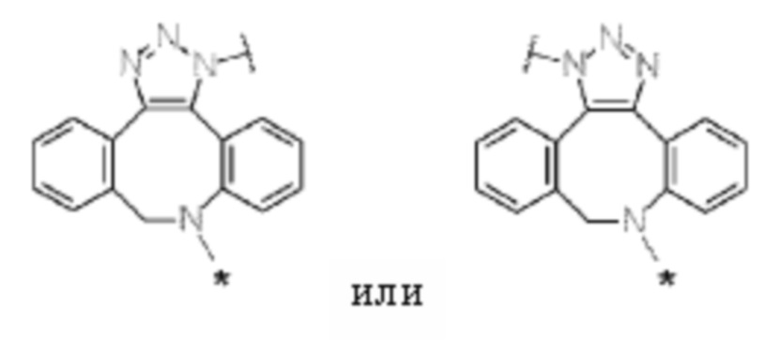 ,
,
[Формула 9]
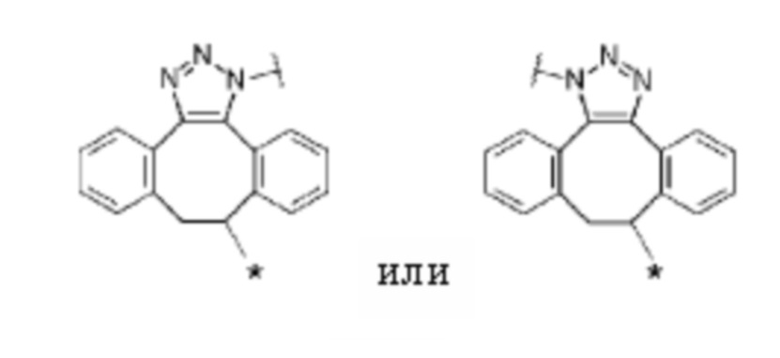 или
или
[Формула 10]
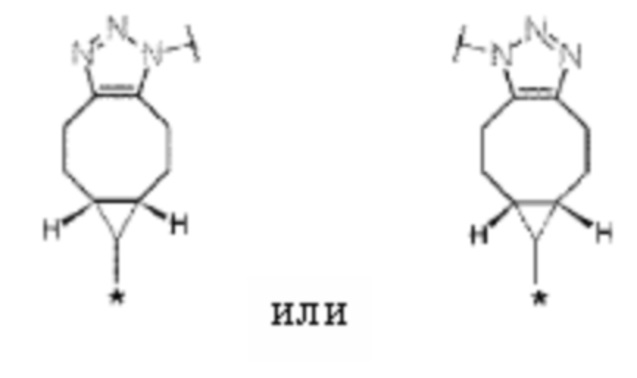 ,
,
где в каждой структурной формуле для Lb, представленной выше,
каждая звездочка представляет собой связь с La и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
16. Конъюгат антитело-лекарственное средство по любому из пп. 7-15, где
L выбран из следующей группы:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GG-(D-)VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGPI-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z2-OC(=O)-GGVA-NH-B-CH2-OC(=O)- и
-Z3-CH2-OC(=O)-GGVA-NH-B-CH2-OC(=O)-, где
Z1 представляет собой следующую структурную формулу:
[Формула 11]
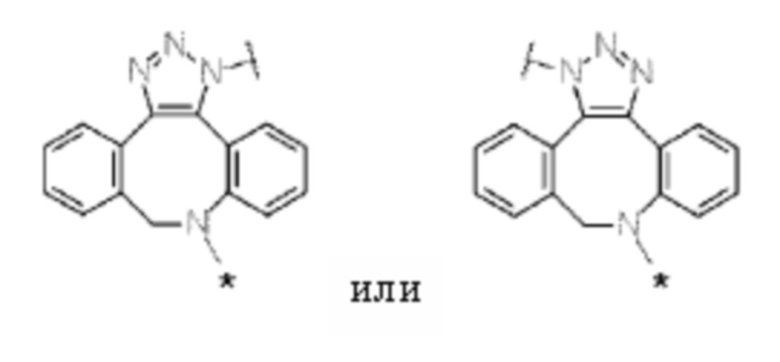 ,
,
Z2 представляет собой следующую структурную формулу:
[Формула 12]
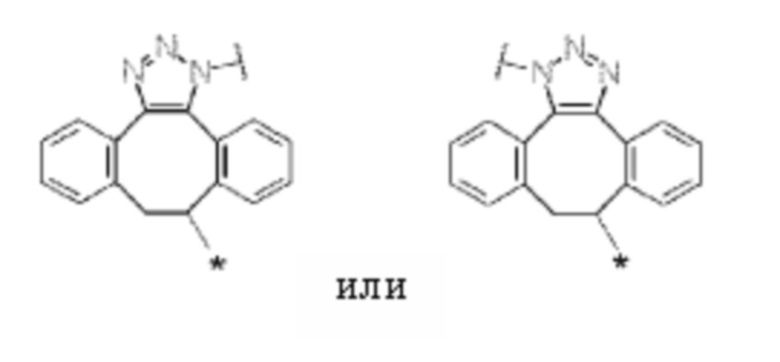 и
и
Z3 представляет собой следующую структурную формулу:
[Формула 13]
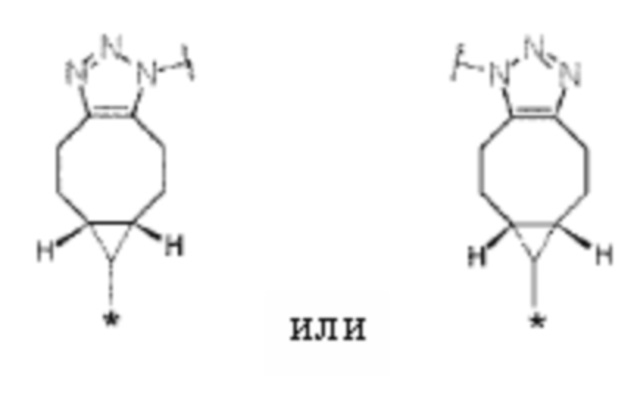 ,
,
где в каждой структурной формуле для Z1, Z2 и Z3
каждая звездочка представляет собой связь с La, каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab; и
B представляет собой 1,4-фенильную группу.
17. Конъюгат антитело-лекарственное средство по п. 16, где
L выбран из следующей группы:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)- и
-Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-, где
B представляет собой 1,4-фенильную группу и Z1 представляет собой следующую структурную формулу:
[Формула 14]
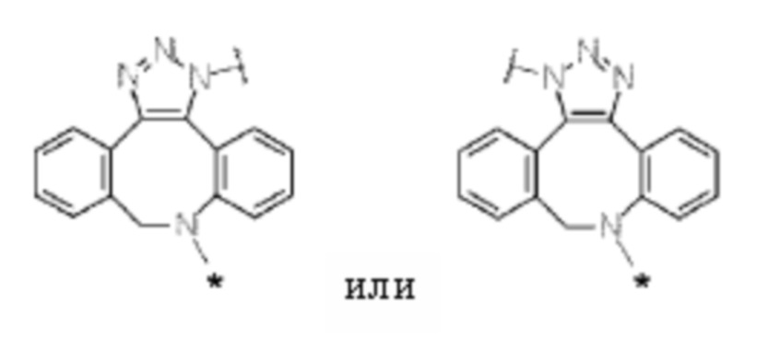 ,
,
где в структурной формуле для Z1
каждая звездочка представляет собой связь с C(=O), соседним с Z1 и каждая волнистая линия представляет собой связь с гликаном или ремоделированным гликаном Ab.
18. Конъюгат антитело-лекарственное средство по любому из пп. 1-6, где
L представлен формулой -Lb-La-Lp-NH-B-CH2-O(C=O)-*, где
звездочка представляет собой связь с D;
B представляет собой 1,4-фенильную группу;
Lp представляет собой -GGVA- или -VA;
La представляет собой -(CH2)n9-C(=O)- или -(CH2CH2)n10-C(=O)-NH-(CH2CH2O)n11-CH2CH2-C(=O)-, где n9 представляет собой целое число от 2 до 7, n10 представляет собой целое число от 1 до 3 и n11 представляет собой целое число от 6 до 10; и
Lb представляет собой -(сукцинимид-3-ил-N)-.
19. Конъюгат антитело-лекарственное средство по п. 18, где
L выбран из следующей группы:
-(сукцинимид-3-ил-N)-(CH2)5-C(=O)-VA-NH-B-CH2-OC(=O)-,
-(сукцинимид-3-ил-N)-(CH2)5-C(=O)-GGVA-NH-B-CH2-OC(=O)- и
-(сукцинимид-3-ил-N)-CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-, где B представляет собой 1,4-фенильную группу.
20. Конъюгат антитело-лекарственное средство по любому из пп. 1-19, причем указанное антитело представляет собой IgG.
21. Конъюгат антитело-лекарственное средство по п. 20, причем указанное антитело представляет собой IgG1, IgG2 или IgG4.
22. Конъюгат антитело-лекарственное средство по любому из пп. 1-21, причем указанное антитело связывается с опухолевой клеткой и внедряется и интернализируется в опухолевую клетку.
23. Конъюгат антитело-лекарственное средство по п. 22, причем указанное антитело дополнительно обладает противоопухолевым эффектом.
24. Конъюгат антитело-лекарственное средство по любому из пп. 1-17 и 20-23, причем указанное антитело связывается посредством гликановой связи с Asn297 антитела (N297-гликан) с L.
25. Конъюгат антитело-лекарственное средство по п. 24, причем указанный N297-гликан представляет собой ремоделированный гликан.
26. Конъюгат антитело-лекарственное средство по п. 24 или 25, причем указанный N297-гликан представляет собой N297-(Fuc)MSG1, N297-(Fuc)MSG2 или их смесь или N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 15]
 ,
,
где волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, причем указанная аминогруппа на правом конце связана посредством амидной связи с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в 1-3 разветвленной цепи β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10,
[Формула 16]
 ,
,
где волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, причем указанная аминогруппа на правом конце связана через амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в 1-6 разветвленной цепи β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10, и
[Формула 17]
 ,
,
где волнистая линия представляет собой связь с Asn297 антитела;
L(PEG) представляет собой -(CH2CH2-O)n5-CH2CH2-NH-, причем указанная аминогруппа на правом конце связана через амидную связь с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане;
звездочка представляет собой связь с линкером L; и
n5 представляет собой целое число от 2 до 10.
27. Конъюгат антитело-лекарственное средство по п. 26, где n5 представляет собой целое число от 2 до 5.
28. Конъюгат антитело-лекарственное средство по любому из пп. 24-27, представленный следующей формулой:
[Формула 18]
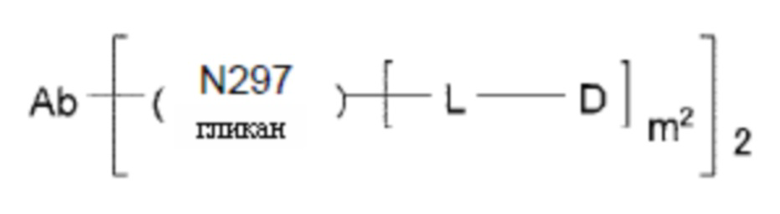 ,
,
где m2 представляет собой целое число, равное 1 или 2;
L представляет собой линкер, связывающий N297-гликан Ab и D, и представляет собой любой линкер, выбранный из следующей группы:
-Z1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B-CH2-OC(=O)-,
-Z1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B-CH2-OC(=O)- и -Z1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B-CH2-OC(=O)-, где
B представляет собой 1,4-фенильную группу и Z1 представляет собой следующую структурную формулу:
[Формула 19]
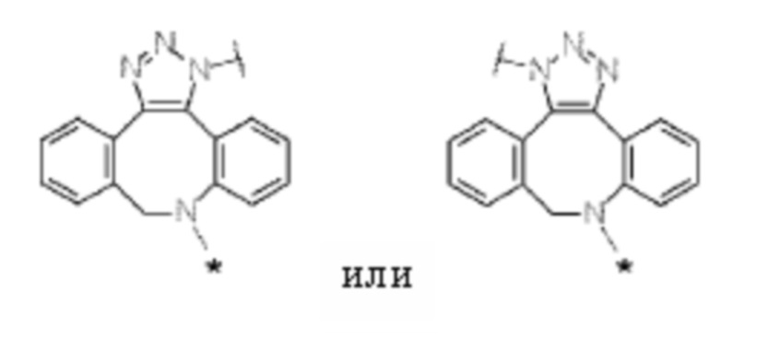 ,
,
где в структурных формулах для Z1
каждая звездочка представляет собой связь с C(=O), соседним с Z1, и каждая волнистая линия представляет собой связь с гликаном N297 Ab;
Ab представляет собой антитело IgG или функциональный фрагмент указанного антитела;
N297-гликан Ab представляет собой одно из N297-(Fuc)MSG1, N297-(Fuc)MSG2 и их смеси и N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 20]
 ,
,
[Формула 21]
 ,
,
[Формула 22]
 ,
,
где каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) в N297-гликане представляет собой -NH-CH2CH2-(O-CH2CH2)n5-*, где
n5 представляет собой целое число от 2 до 5, аминогруппа на левом конце связана амидной связью с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой или в одной из 1-3 и 1-6-разветвленных цепей β-Man в N297-гликане и каждая звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца Z1 в линкере L; и
D выбран из следующей группы:
[Формула 23]
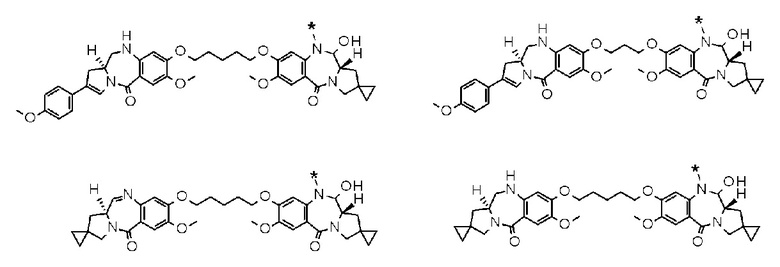 ,
,
где каждая звездочка представляет собой связь с L.
29. Конъюгат антитело-лекарственное средство по п. 1, выбранный из следующей группы:
[Формула 24]
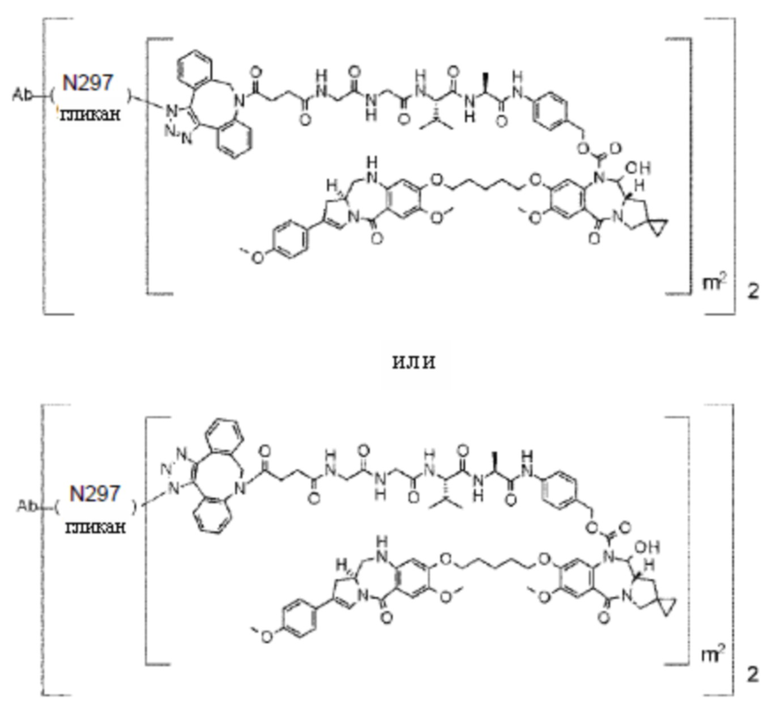 ,
,
[Формула 25]
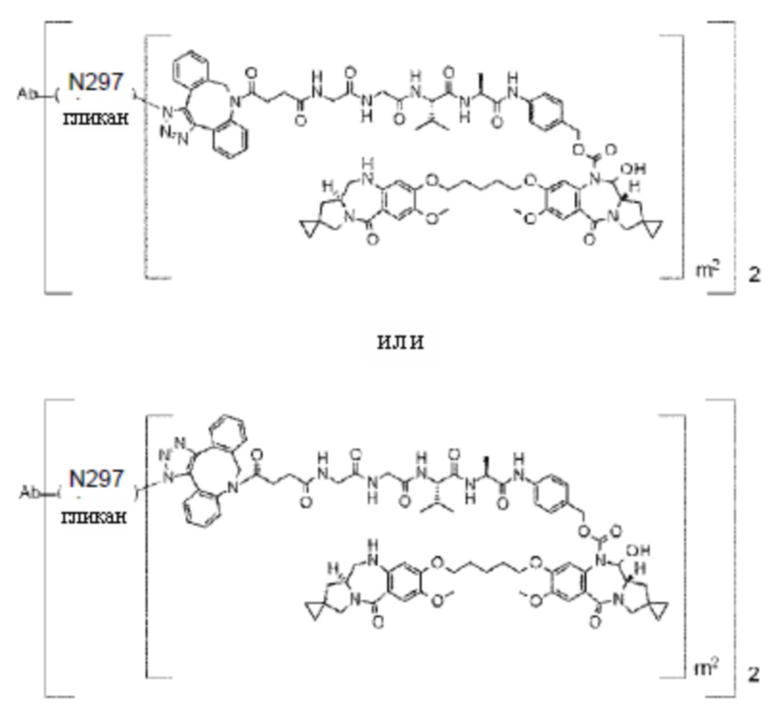 ,
,
[Формула 26]
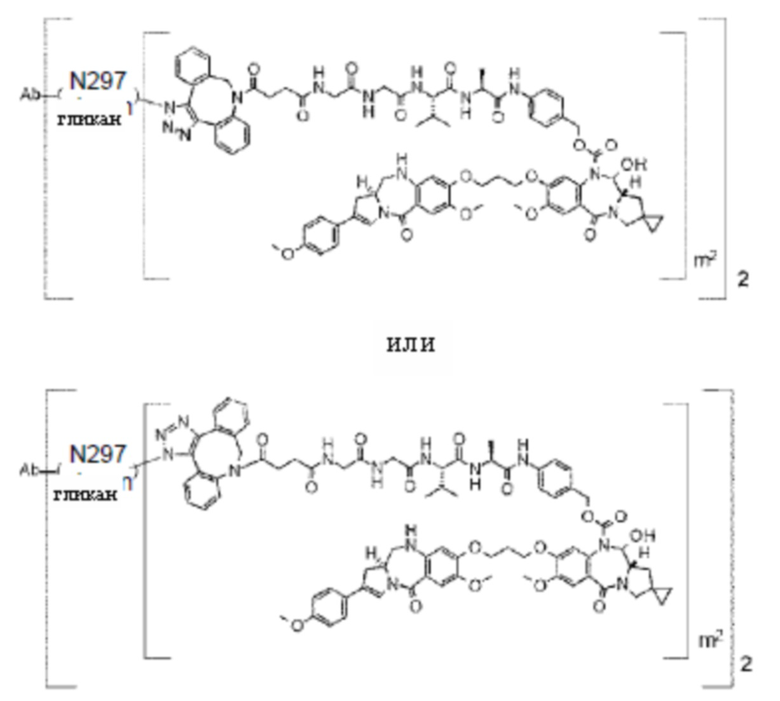 или
или
[Формула 27]
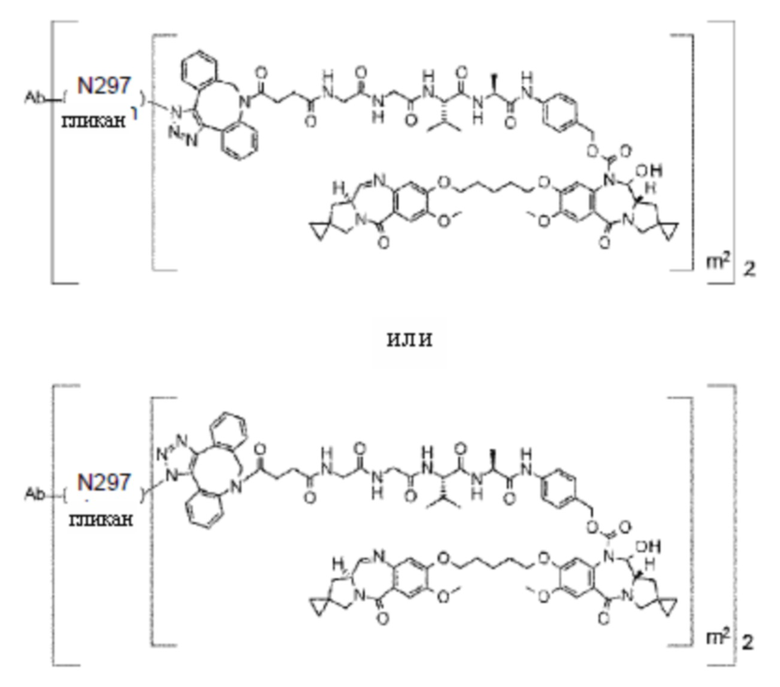 ,
,
где в каждой структурной формуле, представленной выше,
m2 представляет собой целое число, равное 1 или 2;
Ab представляет собой антитело IgG или функциональный фрагмент указанного антитела;
N297-гликан Ab представляет собой одно из N297-(Fuc)MSG1, N297-(Fuc)MSG2 и их смеси и N297-(Fuc)SG, где N297-(Fuc)MSG1, N297-(Fuc)MSG2 и N297-(Fuc)SG имеют структуры, представленные следующими формулами:
[Формула 28]
 ,
,
[Формула 29]
 ,
,
[Формула 30]
 ,
,
где каждая волнистая линия представляет собой связь с Asn297 антитела,
L(PEG) в N297-гликане представляет собой -NH-CH2CH2-(O-CH2CH2)3-*, где
аминогруппа на левом конце связана амидной связью с карбоновой кислотой в положении 2 сиаловой кислоты на невосстанавливающем конце в каждой или в одной из 1-3 и 1-6 разветвленных цепей β-Man в N297-гликане и каждая звездочка представляет собой связь с атомом азота в положении 1 или 3 триазольного кольца в соответствующей структурной формуле.
30. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 29, отличающийся тем, что указанное антитело представляет собой антитело к CLDN6, антитело к CLDN6/CLDN9, антитело к HER2, антитело к DLL3 (дельта-подобный белок 3), антитело к A33, антитело к CanAg, антитело к CD19, антитело к CD20, антитело к CD22, антитело к CD30, антитело к CD33, антитело к CD56, антитело к CD70, антитело к CD98, антитело к TROP2, антитело к CEA, антитело к Cripto, антитело к EphA2, антитело к FGFR2, антитело к G250, антитело к MUC1, антитело к GPNMB, антитело к интегрину, антитело к PSMA, антитело к тенасцину-C, антитело к SLC44A4, антитело к мезотелину, антитело к EGFR или антитело к DR5.
31. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 30, отличающийся тем, что указанное антитело представляет собой моноклональное антитело.
32. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 31, отличающийся тем, что указанное антитело обладает антителозависимой клеточной цитотоксической (ADCC) и/или комплементзависимой цитотоксической (CDC) активностями или активностью.
33. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 32, отличающийся тем, что указанное антитело содержит константную область тяжелой цепи IgG1 человека и содержит мутацию, вызывающую снижение ADCC и/или CDC активностей или активности.
34. Конъюгат антитело-лекарственное средство по п. 33, отличающийся тем, что указанное антитело содержит константную область тяжелой цепи IgG1 человека и лейцин в положениях 234 и 235, определенных нумерацией в соответствии с индексом EU, заменен аланином.
35. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 32, отличающийся тем, что указанное антитело представляет собой гуманизированное моноклональное антитело, содержащее тяжелую цепь, состоящее из аминокислотной последовательности, представленной в SEQ ID NO: 65, и легкую цепь, состоящую из аминокислотной последовательности, представленной в SEQ ID NO: 64.
36. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 31, 33 и 34, отличающийся тем, что указанное антитело представляет собой гуманизированное моноклональное антитело, содержащее тяжелую цепь, состоящее из аминокислотной последовательности, состоящей из аминокислотных остатков 20 - 469 последовательности SEQ ID NO: 75, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21 - 234 последовательности SEQ ID NO: 73.
37. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 36, отличающийся тем, что у указанного антитела отсутствуют одна или две аминокислоты на карбоксильном конце тяжелой цепи.
38. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 32 и 35, отличающийся тем, что указанное антитело содержит тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 1 - 449 последовательности SEQ ID NO: 65, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 1 - 214 последовательности SEQ ID NO: 64.
39. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 31, 33, 34 и 36, отличающийся тем, что указанное антитело содержит тяжелую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 20 - 468 последовательности SEQ ID NO: 75, и легкую цепь, состоящую из аминокислотной последовательности, состоящей из аминокислотных остатков 21 - 234 последовательности SEQ ID NO: 73.
40. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 39, отличающийся тем, что указанное антитело получено с применением способа получения, включающего стадии: культивирования клетки-хозяина, трансформированной с применением вектора экспрессии, содержащего полинуклеотид, кодирующий антитело по любому из пп. 35-39; и сбора целевого антитела из культуры, полученной на стадии культивирования.
41. Конъюгат антитело-лекарственное средство по любому из пп. 1-40, причем среднее количество конъюгированных молекул лекарственного средства на молекулу антитела в конъюгате антитела-лекарственного средства составляет от 1 до 3 или от 3 до 5.
42. Соединение, соль соединения или гидрат соединения или его соли, причем указанное соединение представлено следующей формулой:
[Формула 38]
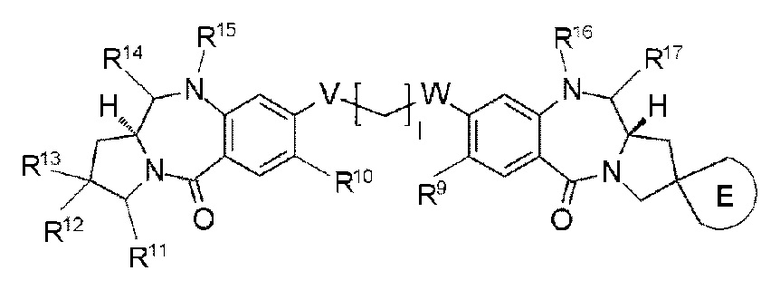 ,
,
где l представляет собой целое число от 2 до 8;
E представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо или трех-пятичленный насыщенный гетероцикл, незамещенный или замещенный одним-четырьмя атомами галогена;
R9 и R10, каждый, независимо представляют собой С1-С6 алкоксигруппу, C1-C6-алкильную группу, атом водорода, гидроксигруппу, тиольную группу, С1-С6-алкилтиогруппу, атом галогена или -NR'R'', где
R' и R'', каждый, независимо представляют собой атом водорода или С1-С6-алкильную группу;
R11, R12 и R13 выбраны из следующих (i)-(iii):
(i) R11 и R12 объединены вместе с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи и R13 представляет собой арильную группу или гетероарильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 7, или С1-С6-алкильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 8,
(ii) R11 представляет собой атом водорода и R12 и R13 объединены вместе с атомом углерода, с которым связаны R12 и R13, с образованием трех-пятичленного насыщенного углеводородного кольца, или трех-пятичленного насыщенного гетероцикла, или CH2= и
(iii) R11, R12 и R13 объединены вместе с атомом углерода, с которым связан R11, и атомом углерода, с которым связаны R12 и R13, с образованием бензольного кольца или шестичленного гетероцикла, имеющего или не имеющего один или более заместителей, выбранных из группы 9, и R13 представляет собой одинарную связь;
R14 и R15, каждый, представляют собой атом водорода или R14 и R15 объединены и представляют собой иминную связь (C=N);
R16 и R17 представляют собой одно из следующих (a) и (b):
(a) R16 и R17 объединены с образованием иминной связи (N=C) и
(b) R16 представляет собой J-La'-Lp'-NH-B'-CH2-O (C=O)-*, где
звездочка представляет собой связь с атомом азота, соседним с R16,
B' представляет собой фенильную группу или гетероарильную группу,
Lp' представляет собой линкер, состоящий из аминокислотной последовательности, расщепляемой в клетке-мишени,
La' представляет собой одну из следующих групп:
-C(=O)-(CH2CH2)n6-C(=O)-,
-C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2)n7-C(=O)-,
-C(=O)-(CH2CH2)n6-C(=O)-NH-(CH2CH2O)n7-CH2-C(=O)-,
-C(=O)-(CH2CH2)n6-NH-C(=O)-(CH2CH2O)n7-CH2CH2-C(=O)-,
-(CH2)n8-O-C(=O)-,
-(CH2)n12-C(=O)- и
-(CH2CH2)n13-C(=O)-NH-(CH2CH2O)n14-CH2CH2-C(=O)-, где
n6 представляет собой целое число от 1 до 3, n7 представляет собой целое число от 1 до 5, n8 представляет собой целое число от 0 до 2, n12 представляет собой целое число от 2 до 7, n13 представляет собой целое число от 1 до 3 и n14 представляет собой целое число от 6 до 10,
J представляет собой одно из следующих:
[Формула 39]
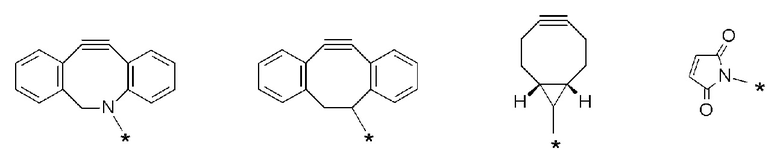 ,
,
где в структурных формулах для J, представленных выше,
каждая звездочка представляет собой связь с La';
R17 представляет собой гидроксигруппу или C1-C3 алкоксигруппу;
V и W, каждый, независимо представляют собой атом кислорода, атом азота или атом серы;
группа 7 представляет собой:
a) С1-С6 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена,
b) C1-C6-алкильную группу, незамещенную или замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR', -NR'R'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) атом галогена,
d) С3-С5-циклоалкоксигруппу,
e) С1-С6-алкилтиогруппу,
f) -NR'R'',
g) -C(=NR')-NR''R''',
h) -NHC(=NR')-NR''R''',
i) -NHCOR' или
j) гидроксигруппу,
где R' и R'' такие, как определено выше, и каждый R''' независимо представляет собой атом водорода или С1-С6-алкильную группу;
группа 8 представляет собой атом галогена, гидроксигруппу или С1-С6 алкоксигруппу; и
группа 9 представляет собой атом галогена, или С1-С6-алкильную группу, или С1-С6 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена.
43. Соединение по п. 42, соль соединения или гидрат соединения или его соли, где
E представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R9 и R10, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R11 и R12 объединены вместе с атомами углерода, с которыми связаны R11 и R12, с образованием двойной связи;
R13 представляет собой арильную группу или гетероарильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 10, или C1-C3 алкильную группу, имеющую или не имеющую один или более заместителей, выбранных из группы 11;
V и W, каждый, представляют собой атом кислорода;
группа 10 представляет собой:
a) C1-C3 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена,
b) C1-C3 алкильную группу, незамещенную или замещенную любым заместителем, выбранным из одного-трех атомов галогена, гидроксигруппы, -OCOR'', -C(=NR')-NR''R''' и -NHC(=NR')-NR''R''',
c) С3-С5-циклоалкоксигруппу,
d) -C(=NR')-NR''R''',
e) -NHC(=NR')-NR''R''' или
f) гидроксигруппу,
где R', R'' и R''', каждый, независимо представляют собой атом водорода или C1-C3 алкильную группу; и
группа 11 представляет собой атом галогена, гидроксигруппу или C1-C3 алкоксигруппу.
44. Соединение по п. 42, соль соединения или гидрат соединения или его соли, где
E представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R9 и R10, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R11 представляет собой атом водорода;
R12 и R13 объединены вместе с атомом углерода, с которым связаны R12 и R13, с образованием трех-пятичленного насыщенного углеводородного кольца или =CH2; и
V и W, каждый, представляют собой атом кислорода.
45. Соединение по п. 42, соль соединения или гидрат соединения или его соли, где
E представляет собой спиросвязанное трех-пятичленное насыщенное углеводородное кольцо, незамещенное или замещенное одним или двумя атомами галогена;
R9 и R10, каждый, независимо представляют собой C1-C3 алкоксигруппу;
R11, R12 и R13 объединены вместе с атомом углерода, с которым связан R11, и атомом углерода, с которым связаны R12 и R13, с образованием бензольного кольца, имеющего или не имеющего один или более заместителей, выбранных из группы 12;
V и W, каждый, представляют собой атом кислорода; и
группа 12 представляет собой атом галогена, или C1-C3 алкильную группу, или C1-C3 алкоксигруппу, незамещенную или замещенную одним-тремя атомами галогена.
46. Соединение по любому из пп. 42-45, соль соединения или гидрат соединения или его соли, где B' выбран из 1,4-фенильной группы, 2,5-пиридильной группы, 3,6-пиридильной группы, 2,5-пиримидильной группы и 2,5-тиенильной группы.
47. Соединение по п. 46, соль соединения или гидрат соединения или его соли, где B' представляет собой 1,4-фенильную группу.
48. Соединение по любому из пп. 42-47, соль соединения или гидрат соединения или его соли, где Lp' представляет собой аминокислотные остатки, выбранные из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK-, -GG(D-)P-I- и -GGPL-.
49. Соединение по любому из пп. 42-48, соль соединения или гидрат соединения или его соли, где La' выбран из следующей группы:
-C(=O)-CH2CH2-C(=O)-, -C(=O)-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-,
-CH2-OC(=O)-, -OC(=O)-,
-(CH2)5-C(=O)- и -CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-.
50. Соединение по любому из пп. 42-49, соль соединения или гидрат соединения или его соли, где
R16 представлен формулой J-La'-Lp'-NH-B'-CH2-O (C=O)-*, где
B' представляет собой 1,4-фенильную группу;
Lp' выбран из следующей группы:
-GGVA-, -GG-(D-)VA-, -VA-, -GGFG-, -GGPI-, -GGVCit-, -GGVK- и -GGPL-;
La' выбран из следующей группы:
-C(=O)-CH2CH2-C(=O)-, -C(=O)-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-,
-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-,
-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-,
-CH2-OC(=O)-, -OC(=O)-,
-(CH2)5-C(=O)- и -CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-; и
J представляет собой одно из следующих:
[Формула 40]
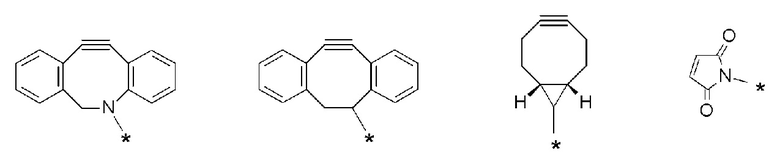 ,
,
где в структурных формулах для J
каждая звездочка представляет собой связь с La'.
51. Соединение по любому из пп. 42-50, соль соединения или гидрат соединения или его соли, где
R16 выбран из следующей группы:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GG-(D-)VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPI-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGFG-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVK-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGPL-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J3-CH2-OC(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)- и J4-CH2CH2-C(=O)-NH-(CH2CH2O)8-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-, где
J1, J2, J3 и J4 представлены следующими структурными формулами:
[Формула 41]
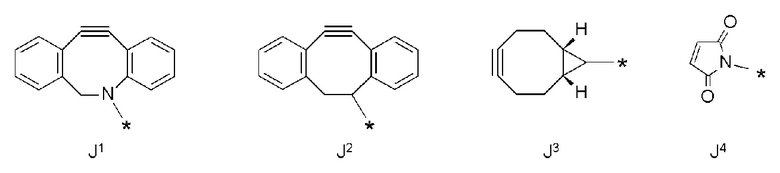 ,
,
где в структурных формулах для J1, J2, J3 и J4 каждая звездочка представляет собой связь с соседней группой и
B' представляет собой 1,4-фенильную группу.
52. Соединение по любому из пп. 42-51, соль соединения или гидрат соединения или его соли, где
R16 выбран из следующей группы:
J1-C(=O)-CH2CH2-C(=O)-GGVA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-GGVCit-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2)2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-C(=O)-NH-(CH2CH2O)2-CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J1-C(=O)-CH2CH2-NH-C(=O)-(CH2CH2O)4-CH2CH2-C(=O)-VA-NH-B'-CH2-OC(=O)-,
J4-(CH2)5-C(=O)-GGVA-NH-B'-CH2-OC(=O)- и J4-(CH2)5-C(=O)-VA-NH-B'-CH2-OC(=O)-, где
B' представляет собой 1,4-фенильную группу и
J1 и J4 представлены следующими структурными формулами:
[Формула 42]
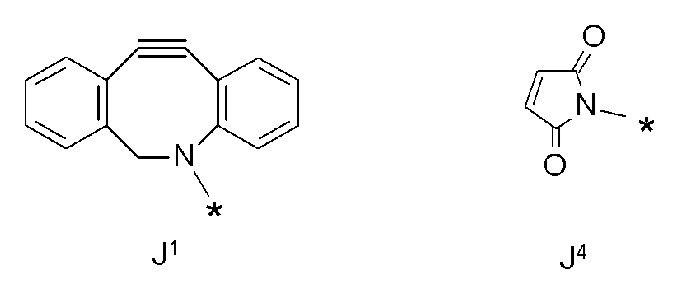 ,
,
где в структурных формулах для J1 и J4
каждая звездочка представляет собой связь с соседней группой.
53. Соединение, соль соединения или гидрат соединения или его соли по п. 42, причем указанное соединение представляет собой любое соединение, выбранное из следующих формул:
[Формула 43]
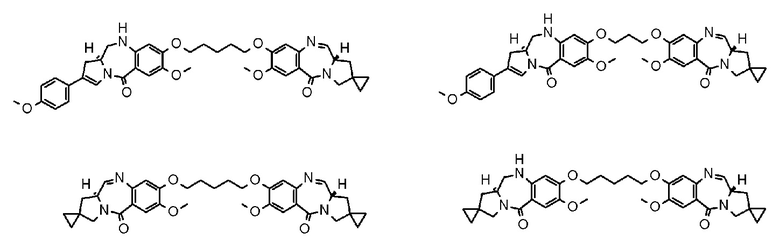 .
.
54. Соединение, соль соединения или гидрат соединения или его соли по п. 42, причем указанное соединение представляет собой любое соединение, выбранное из следующих формул:
[Формула 44]
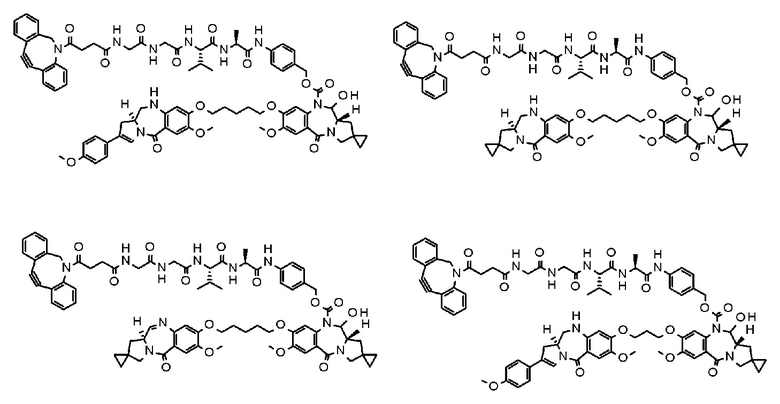 .
.
55. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 41, отличающийся тем, что D представлена следующей формулой:
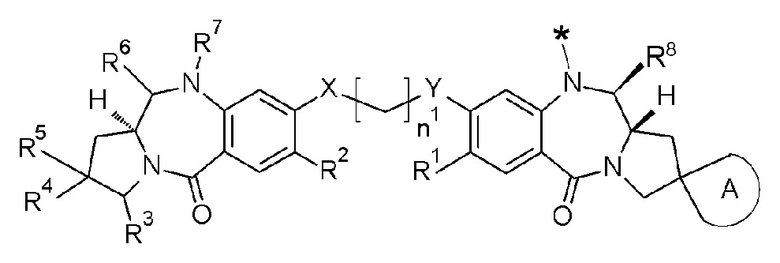 .
.
56. Соединение по любому из пп. 42 - 52 и 54, представленное следующей формулой:
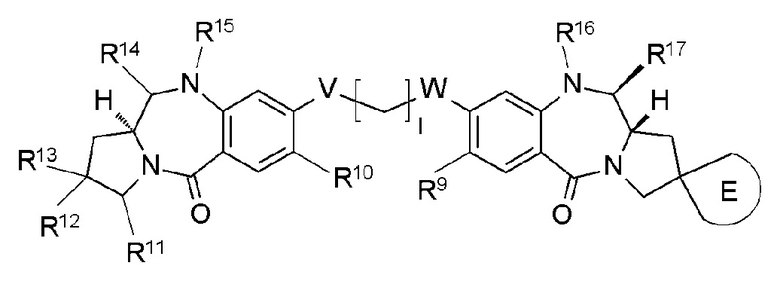 ,
,
соль указанного соединения или гидрат указанного соединения или соли.
57. Конъюгат антитело-лекарственное средство по любому из пп. 1 - 41, отличающийся тем, что D представлена следующей формулой:
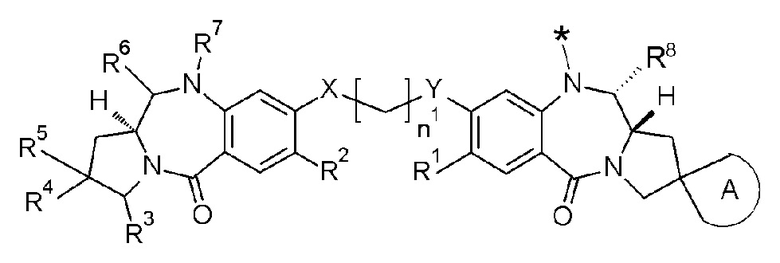 .
.
58. Соединение по любому из пп. 42 - 52 и 54, представленное следующей формулой:
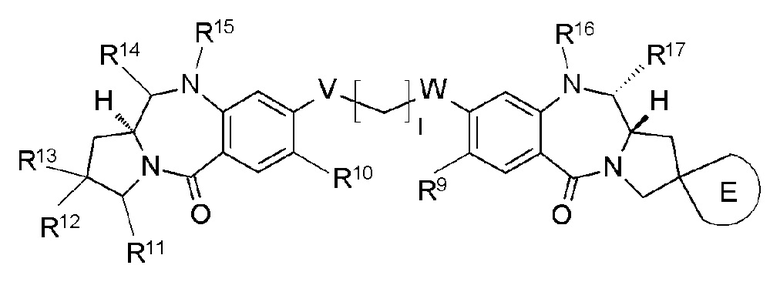
соль указанного соединения или гидрат указанного соединения или соли.
59. Соединение по п. 42, демонстрирующее протонный ЯМР с положениями пиков, по существу аналогичными положениям пиков:
1H-ЯМР (DMSO-D6) δ: 9,93 (1H, s), 8,21-8,16 (2H, m), 8,07-8,04 (1H, m), 7,83-7,64 (2H, m), 7,60-7,55 (3H, m),7,51-7,28 (10H, m), 7,19-7,16 (2H, m), 7,10-7,04 (1H, m), 6,92-6,90 (2H, m), 6,76-6,70 (1H, m), 6,39 (1H, s), 5,77-5,75 (1H, m), 5,21-5,18 (1H, m), 5,03-4,99 (1H, m), 4,82-4,79 (1H, m), 4,37-4,35 (1H, m), 4,21-4,20 (2H, m), 4,02-3,24 (26H, m), 3,16-3,13 (1H, m), 2,79-2,59 (2H, m), 2,39-2,28 (2H, m), 2,05-1,97 (2H, m), 1,91-1,77 (4H, m), 1,57-1,54 (3H, m), 1,28-1,23 (3H, m), 0,85-0,80 (6H, m), 0,67-0,61 (4H, m) или
1H-ЯМР (DMSO-D6) δ: 9,91 (1H, s), 8,32 (1H, s), 8,23-7,91 (3H, m), 7,81-7,19 (14H, m), 7,04 (1H, m), 6,80-6,62 (3H, m), 5,77-5,75 (1H, m), 5,20 (1H, m), 5,01 (1H, m), 4,79 (1H, m), 4,46-4,35 (1H, m), 4,04 (4H, m), 3,86-3,38 (18H, m), 3,22-3,15 (2H, m), 2,67-2,63 (1H, m), 2,46-2,23 (3H, m), 2,09-1,91 (2H, m), 1,80-1,78 (5H, m), 1,57 (3H, m), 1,27 (3H, s), 1,11-1,04 (1H, m), 0,87-0,79 (6H, m), 0,63-0,55 (6H, m), или
соль указанного соединения или гидрат указанного соединения или соли.
60. Фармацевтическая композиция для лечения и профилактики рака, содержащая эффективное количество любого из конъюгата антитело-лекарственное средство по любому из пп. 1-41, 55 и 57, соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; и соединения по любому из пп. 42-54, 56, 58 и 59, соли указанного соединения или гидрата указанного соединения или его соли, и один или более фармацевтически приемлемых вспомогательных веществ,
причем раковые клетки в качестве терапевтической мишени экспрессируют белок, распознаваемый антителом, входящим в конъюгат антитело-лекарственное средство.
61. Фармацевтическая композиция по п. 60, причем указанная опухоль представляет собой опухоль, экспрессирующую CLDN6 и/или CLDN9.
62. Фармацевтическая композиция по п. 60 или 61, причем указанная опухоль представляет собой рак яичников (поверхностную эпителиальную опухоль, стромальную опухоль или опухоль зародышевой клетки), рак легкого (немелкоклеточный рак легкого или мелкоклеточный рак легкого), рак желудка, рак эндометрия, рак яичка (семиному или несеминому), рак шейки матки, плацентарную хориокарциному, рак почки, уротериальный рак, колоректальный рак, рак простаты, мультиформную глиобластому, рак головного мозга, рак поджелудочной железы, рак молочной железы, меланому, рак печени, рак мочевого пузыря или рак пищевода.
63. Способ лечения опухоли, где любой из конъюгата антитело-лекарственное средство по любому из пп. 1-41, 55 и 57, соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; и соединения по любому из пп. 42-54, 56, 58 и 59, соли указанного соединения или гидрата указанного соединения или его соли вводят индивидууму,
причем раковые клетки в качестве терапевтической мишени экспрессируют белок, распознаваемый антителом, входящим в конъюгат антитело-лекарственное средство.
64. Способ по п. 63, причем указанная опухоль представляет собой опухоль, экспрессирующую CLDN6 и/или CLDN9.
65. Способ по п. 63 или 64, причем указанная опухоль представляет собой рак яичников (поверхностную эпителиальную опухоль, стромальную опухоль или опухоль зародышевой клетки), рак легкого (немелкоклеточный рак легкого или мелкоклеточный рак легкого), рак желудка, рак эндометрия, рак яичка (семиному или несеминому), рак шейки матки, плацентарную хориокарциному, рак почки, уротериальный рак, колоректальный рак, рак простаты, мультиформную глиобластому, рак головного мозга, рак поджелудочной железы, рак молочной железы, меланому, рак печени, рак мочевого пузыря или рак пищевода.
66. Способ лечения опухоли, согласно которому фармацевтическую композицию, содержащую по меньшей мере одно, выбранное из конъюгата антитело-лекарственное средство по любому из пп. 1-41, 55 и 57, соли конъюгата антитело-лекарственное средство или гидрата конъюгата антитело-лекарственное средство или его соли; и соединения по любому из пп. 42-54, 56, 58 и 59, соли указанного соединения или гидрата указанного соединения или его соли, и по меньшей мере одно противоопухолевое лекарственное средство вводят индивидууму одновременно, раздельно или последовательно,
причем раковые клетки в качестве терапевтической мишени экспрессируют белок, распознаваемый антителом, входящим в конъюгат антитело-лекарственное средство.
| US 20090149449 A1, 11.06.2009 | |||
| WO 2017137556 A1, 17.08.2017 | |||
| ПИРРОЛО [2.1-C][1.4] БЕНЗОДИАЗЕПИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2314309C2 |
Авторы
Даты
2024-06-13—Публикация
2018-09-28—Подача