Изобретение относится к области фармацевтической химии, а именно к определению чувствительности к химиотерапии солидных опухолей человека, и может быть использовано в онкологической практике для подбора адекватной терапии солидных опухолей.
Важнейшей проблемой современной химиотерапии злокачественных новообразований является разработка методов индивидуального прогнозирования течения заболевания и чувствительности к терапии, в частности, на основании данных об экспрессии в опухолях разных видов лекарственной устойчивости. Множественная лекарственная устойчивость опухолей - это врожденная или приобретенная невосприимчивость клеток к противоопухолевым препаратам, различным по структуре и механизму действия (так называемым МЛУ-цитостатикам). К МЛУ-цитостатикам относят антрациклины, винкаалкалоиды, таксаны, подофилотоксины, камптотецины, актиномицин Д, митоксантрон, амскарин, топотекан и иринотекан, митрамицини, митомицин С [1]. Один из наиболее часто встречаемых механизмов лекарственной устойчивости к цитостатикам - это выброс входящих в клетку препаратов энергозависимыми насосами семейства АВС-транспортеров. К семейству АВС-транспортеров относят Pgp (Р-glycoprotein), MRP (multidrug resistance protein), BCRP (breast cancer resistance protein), но только Pgp и MRP являются признанными маркерами лекарственной устойчивости [2,3]. За исключением таксанов, обладающих сродством только к Pgp [4], остальные МЛУ-цитостатики являются универсальными субстратами для всех АВС-транспортеров.
В клетке АВС-транспортеры образуют два защитных барьера от цитостатиков: первый барьер - АВС-транспортеры, располагающиеся на плазматической мембране и определяющие сколько препарата попадет извне в клетку, то есть регулирующие тотальную внутриклеточную концентрацию цитостатиков. Второй барьер составляют обратные транспортеры, защищающие ядро, в котором локализованы мишени большинства цитостатиков, от их проникновения из цитоплазмы. В дальнейшем в зависимости от выполняемой функции мы будем называть транспортеры первого барьера как плазматические, второго - ядерные.
Экспрессию АВС-транспортеров, на основании которой прогнозируют чувствительность к химиотерапии и агрессивность течения некоторых злокачественных новообразований, в частности лейкозов, определяют с помощью метода проточной цитофлюориметрии и методами обратной полимеразной цепной реакции и иммуногистохимии. При этом именно оценка функциональной активности АВС-транспортеров методом проточной цитофлюориметрии позволяет с большей вероятностью протезировать эффективность противоопухолевой химиотерапии и течение лейкозов [5].
В случае лейкозов используется метод цитометрии в потоке для определения индивидуальной чувствительности к химиотерапии путем выявления функциональной активности АВС-транспортеров [6]. Функциональную активность транспортных белков оценивают по накоплению клетками субстрата АВС-транспортеров после воздействия специфических ингибиторов их активности (верапамила и генистеина) в сравнении с контролем. Используя ингибиторы в одной концентрации при одной концентрации субстрата, невозможно дифференцировать активность ядерных и плазматических транспортных белков и охарактеризовать выраженность экспрессии транспортной системы, что не позволяет с достаточной степенью точности определить индивидуальную чувствительность лейкозов к химиотерапии. Кроме того, проведение оценки функциональной активности АВС-транспортеров методом проточной цитофлюориметрии ограничено необходимостью работы с клеточными суспензиями. Применение даже самых "мягких" методов получения суспензии клеток из плотной ткани с использованием протеолитеческих ферментов приводит к неконтролируемому повреждению плазматической мембраны клетки, а следовательно, к искажению результатов тестирования функциональной активности транспортных белков и, в конечном итоге, к неадекватному определению чувствительности клеток к цитостатикам. Отсутствие адекватного способа приготовления клеточной суспензии из плотной ткани делают невозможным использование существующего способа определения индивидуальной чувствительности к химиотерапии с помощью метода проточной цитофлюорметрии в случае солидных опухолей.
Известен способ определения индивидуальной чувствительности к химиотерапии солидных опухолей методом обратной полимеразной цепной реакции, который выявляет строго количественно активность генов транспортных белков на уровне синтеза РНК [7]. К существенным недостаткам этого метода относится то, что он выявляет активность генов АВС-транспортеров на уровне синтеза РНК, то есть не позволяет получить информацию о наличии в клетке транспортного белка, а тем более - о его функциональной активности. Последнее является определяющим в адекватной диагностике фенотипа множественной лекарственной устойчивости, а следовательно, в прогнозе чувствительности опухоли к химиотерапии. Кроме того, адекватно определять чувствительность к химиотерапии рассматриваемым способом не позволяет отсутствие информации об активности ядерных и плазматических транспортных белков, а также об активности транспортной системы в целом. К недостаткам метода относятся также необходимость использования дорогостоящих реактивов. Таким образом, метод обратной полимеразной цепной реакции неадекватен для определения индивидуальной чувствительности к химиотерапии солидных опухолей.
Способ иммуногистохимии, суть которого заключается в выявлении присутствующего в клетке белка с помощью моноклональных антител при окрашивании гистологических срезов, является еще одним методом определения индивидуальной чувствительности к химиотерапии солидных опухолей [8]. Иммуногистохимия, как микроскопический метод, идентифицирующий в клетке белок, позволяет дифференцировать экспрессию АВС-транспортеров именно в опухолевых клетках, а также охарактеризовывать внутриклеточное распределение транспортных белков. Присутствие транспортных белков в опухоли оценивается визуально по положительной реакции окрашенных срезов ткани, то есть рассматриваемый способ оценки экспрессии АВС-транспортеров является качественным, то есть субъективным. Однако помимо субъективной ошибки присутствует и объективная ошибка, связанная с отсутствием высокоспецифичных антител к исследуемым транспортным белкам. К упомянутым недостаткам необходимо добавить следующее, имеющее принципиальное значение для адекватного определения чувствительности к химиотерапии. Метод иммуногистохимии выявляет присутствие в клетке белка, но не его функциональную активность, что не позволяет получить информацию об экспрессии реально функционирующего белка, и, в конечном итоге, адекватно определить чувствительность к химиотерапии. Невозможность выявления активности транспортной системы в целом иммуногистохимическим методом также не позволяет адекватно определять чувствительность к химиотерапии. И, наконец, оценка экспрессии АВС-транспортеров иммуногистохимическим методом включает в себя использование дорогостоящих реактивов и большие временные затраты, связанные с приготовлением гистологических препаратов. Таким образом, метод иммуногистохимии неадекватен для определения индивидуальной чувствительности к химиотерапии солидных опухолей.
Результатом описанных недостатков является то, что применение методов обратной полимерзаной цепной реакции и иммуногистохимии не позволяет выявить взаимосвязь между экспрессией АВС-транспортеров в солидных опухолях и чувствительностью к химиотерапии и агрессивностью течения заболевания [9, 10]. Такая противоречивость результатов оценки прогностической значимости экспрессии АВС-транспортеров в солидных опухолях способствовала поиску новых подходов к определению их экспрессии в опухолевых клетках.
Ввиду неадекватности методов обратной полимеразной цепной реакции и иммуногистохимии для прогнозирования эффективности химиотерапии и отсутствия адекватной методики определения функциональной активности АВС-транспортеров в солидных опухолях человека задачей данного изобретения является создание способа определения индивидуальной чувствительности к химиотерапии солидных опухолей человека, лишенного вышеуказанных недостатков и позволяющего с высокой степенью точности определять индивидуальную чувствительность к химиотерапии солидных опухолей, что позволяет проводить адекватную терапию.
Решение поставленной задачи достигается тем, что предложен способ определения индивидуальной чувствительности к химиотерапии, заключающийся в том, что готовят суспензию опухолевых клеток из образца опухолевой ткани, помещают в пробирки, добавляют в опытные пробирки ингибиторы верапамил в конечной концентрации 3,3·10-4 и 1,7·10-5 M, генистеин в конечной концентрации 3,2·10-5 и 1,6·10-6 М, и азид натрия, в конечной концентрации 5·10-3 М, инкубируют 20 мин при 37°С, затем во все пробирки добавляют доксорубицин, причем в одну половину пробирок добавляют доксорубицин в конечной концентрации 7,7·10-5 М, а во вторую половину пробирок - в конечной концентрации 7,7·10-6 М, снова инкубируют в течение 5 мин при 37°С, а затем во все пробирки добавляют формалин в конечной концентрации 10%, пробы анализируют на проточном цитофлюориметре при λ=576 нм со скоростью 500 клеток/с при значении шторки 100, определяют значение средней геометрической внутриклеточной флюоресценции для каждой пробы и индивидуальную чувствительность к химиотерапии солидных опухолей определяют по общей формуле:
KC-inh X=GmeanC-inh X/GmeanC,
где KC-inh X - относительное изменение средней геометрической внутриклеточной флюоресценции доксорубицина после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
GmeanC-inh X - средняя геометрическая флюоресценция популяции клеток после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
GMeanC - средняя геометрическая флюоресценция популяции клеток в контрольной пробе при концентрации доксорубицина С.
Концентрация доксорубицина С:
С1 - концентрация доксорубицина 7,7·10-5 М
С2 - концентрация доксорубицина 7,7·10-6 М
Ингибитор активности АВС-транспортеров Inh X:
Inh1.1 - верапамил в концентрации 3,3·10-4 М
Inh1.2 - верапамил в концентрации 1,7·10-5 М
Inh2.1 - генистеин в концентрации 3,2·10-5 М
Inh2.2 - генистеин в концентрации 1,6·10-6M
Inh3 - азид натрия и концентрации 5·10-3 М
Для определения индивидуальной чувствительности к химиотерапии солидных опухолей человека используют следующие критерии:
заключение о чувствительности опухоли к химиотерапии МЛУ-цитостатиками делают при значениях
1) Кc1,c2-inh1.1,1.2,2.1,2.2,3=1;
или
2) Kc1-inh1.1,1.2,2.1,2.2,3=1;
если хотя бы одно из Kc2-inh1.1, Kc2-inh1.2, Kc2-inh2.1, Kc2-inh2.2≠1 и Kc2-inh3≠1;
или
3) Kc1-inh1.1,1.2,2.1,2.2,3=1; Kc2-inh1.1,1.2,2.1,2.2=1 и Кc2-inh3≠1,
заключение о нечувствительности опухоли к терапии МЛУ-цитостатиками, кроме таксанов, делают при значениях
Kc1,c2-inh 1.1,1.2=1 и
1) если хотя бы одно из Kc1,c2-inh2.1, Kc1,c2-inh2.2≠1 и Kc1,c2-inh3≠1;
или
2) Kc1,c2-inh2.1,2.2=1 и Kc1,c2-inh3≠1,
заключение о чувствительности опухоли к терапии высокими дозами МЛУ-цитостатиков делают
если значения Kc1,c2-inh1.1, Kc1,c2-inh1.2>1 и
1) Kc1,c2-inh2.1,2.2=1 и Kc1,c2-inh3>1;
или
2) если значения Kc1,c2-inh2.1, Kc1,c2-inh2.2>1 И Kc1,c2-inh3>1,
заключение о нечувствительности опухоли к терапии МЛУ-цитостатиками делают
а) если хотя бы одно из значений Kc1,c2-inh1.1, Kc1,c2-inh1.2<1 и
1) Kc1,c2-inh1.2.2=1 и Кс1,c2-inh3<1;
или
2) если хотя бы одно из Kc1,c2-inh2.1, Kc1,c2-inh2.2<1 и Kc1,c2-inh3<1;
б) если значения Kc1,c2-inh1.1 и Kc1,c2-inh1.2>1 и
значения Kc1,c2-inh2.1, Kc1,c2-inh2.2<1 и Kc1,c2-inh3<1.
Технический результат при использовании изобретения заключается в том, что заявленный способ позволяет полно, с высокой степенью точности (80%) определять индивидуальную чувствительность опухоли к химиотерапии, а также несложен для технического выполнения. Определение функциональной активности АВС-транспортеров с использованием заявленного способа не включает в себя использование дорогостоящих реактивов, как в случае метода обратной полимеразной цепной реакции и иммуногистохимии. Определение индивидуальной чувствительности к химиотерапии заявленным способом занимает меньшее время, чем в случае иммуногистохимии. Временные затраты при использовании заявленного способа для 10 образцов составляют не более 4 часов, в то же время для метода иммуногистохимии вся процедура занимает больше суток. Таким образом, высокая точность, надежность, быстрота и дешевизна делают пригодным разработанный способ для рутинного использования в клинической практике. Основным достоинством заявленного способа является получение информации о функциональной активности АВС-транспортеров и всей транспортной системы в целом, что является необходимым условием для адекватного определения чувствительности опухоли к химиотерапии, а следовательно, для выбора и проведения адекватного лечения.
В качестве флюоресцентного зонда, по накоплению которого клетками судят о функциональной активности АВС-транспортеров, выбран доксорубицин. Этот выбор обусловлен следующими свойствами препарата. Во-первых, доксорубицин является субстратом всех известных к настоящему времени АВС-транспортеров. Во-вторых, антибиотики антрациклинового ряда, к которым относится доксорубицин, входят в группу противоопухолевых препаратов, развитие множественной лекарственной устойчивости к которым связано с активацией функции АВС-транспортеров, и соответственно по накоплению клетками доксорубицина судят об устойчивости ко всем МЛУ-цитостатикам.
Оценку функциональной активности АВС-транспортеров проводят, сравнивая количество накопленного клетками доксорубицина после воздействия ингибитора активности АВС-транспортера с контролем. Если в опухоли присутствуют АВС-транспортеры, то внутриклеточное содержание доксорубицина увеличивается. В качестве ингибиторов активности АВС-транспортеров используют специфические ингибиторы (верапамил - ингибитор активности Pgp, генистеин - ингибитор активности MRP) и азид натрия - блокатор транспортной системы в целом. Введение в панель ингибиторов азида натрия с одной стороны позволяет контролировать достоверность выявляемых ответных реакций на воздействие специфических ингибиторов (верапамила и генистеина), а с другой - определять экспрессию функционально активных АВС-транспортеров, отличных от Pgp и MRP, что дает возможность адекватно оценивать чувствительность солидных опухолей к химиотерапии. Использование ингибиторов активности АВС-транспортеров в двух концентрациях при двух концентрациях доксорубицина позволяет дифференцировать активность ядерных и плазматических транспортных белков и охарактеризовать выраженность экспрессии транспортной системы в целом, что повышает точность определения индивидуальной чувствительности к химиотерапии.
Сущность заявленного способа заключается в следующем.
Преинкубируют операционный материал опухоли в течение 40 мин в растворе Хенкса с глюкозой при 37°С для стимуляции заингибированной активности АВС-транспортеров, после чего раствор отбрасывают, а опухолевый образец разрезают при помощи скальпеля на кусочки размером 2×2×2 мм.
Суспензию опухолевых клеток получают путем механического встряхивания (достаточно 5-6 встряхиваний) 10 кусочков опухоли, взятых из ее разных участков, в 5 мл раствора Хенкса с глюкозой. Суспензию опухолевых клеток фильтруют через марлевый фильтр, осадок отбрасывают.
Раскапывают по 350 мкл суспензии опухолевых клеток в 13 пробирок. 1-ая пробирка является контрольной, по которой определяют автофлюоресценцию клеток и в нее добавляют только формалин. 2-ая и 8-ая пробирка являются контролем, по которому судят о том, как изменилось внутриклеточное накопление доксорубицина в результате воздействия ингибиторов, и в нее добавляют доксорубицин и формалин.
После раскапывания суспензии клеток в пробирки 3, 4, 5, 6, 7, 9, 10, 11, 12, 13 добавляют ингибиторы активности АВС-транспортеров: верапамил в конечной концентрации 3,3·10-4 и 1,7·10-5, генистеин в конечной концентрации 3,2·10-5 и 1,6·10-6 М, азид натрия в конечной концентрации 5·10-3 М; затем инкубируют в течение 20 мин при 37°С.
Со 2-ой по 7-ую пробирки добавляют доксорубицин в конечной концентрации 7,7·10-5 М; с 8-ой по 13-ую добавляют доксорубицин в конечной концентрации 7,7·10-6 М; после 5 мин инкубации при 37°С клетки фиксируют формалином в конечной концентрации 10%.
Далее пробы анализируют на проточном цитофлюориметре при λ=576, при значении шторки 100, со скоростью сбора клеток 500 клеток/с. Число анализируемых событий не менее 10 тысяч.
Коэффициент, используемый при определении чувствительности к химиотерапии солидных опухолей:
KС-inh X=GmeanC-inh X/GmeanC, где
KC-inh X - относительное изменение средней геометрической внутриклеточной флюоресценции доксорубицина после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
GmeanC-inh X - средняя геометрическая флюоресценция популяции клеток после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
GMeanC - средняя геометрическая флюоресценция популяции клеток в контрольной пробе при концентрации доксорубицина С.
Концентрация доксорубицина С может принимать следующие значения:
С1 - концентрация доксорубицина 7,7·10-5 М
С2 - концентрация доксорубицина 7,7·10-6 М
Ингибитор активности АВС-транспортеров Inh X может принимать следующие значения:
Inh1.1 - верапамил в концентрации 3,3·10-4 М
Inh1.2 - верапамил в концентрации 1,7·10-5 М
Inh2.1 - генистеин в концентрации 3,2·10-5 М
Inh2.2 - генистеин в концентрации 1,16·10-6 M
Inh3 - азид натрия в концентрации 5·10-3 M
Как видно из формулы, К может принимать значение меньшее, большее и равное единице. Изменение внутриклеточной флюоресценции в 1,3 и более раз (К≤0,8 и К≥1,3) означает присутствие в опухолевых клетках функционально активных АВС-транспортеров.
Ниже приведены варианты KС-inh X для каждой из проб, клетки которой инкубируются с ингибитором, а именно:
проба №3: Kc1-inh1.1=Gmeanc1-inh1.1/GMeanc1
проба №4: Kc1-inh1.2=Gmeanc1-inh1.2/GMeanc1
проба №5: Kc1-inh2.1=Gmeanc1-inh2.1/GMeanc1
проба №6: Kc1-inh2.2=Gmeanc1-inh2.2/GMeanc1
проба №7: Kc1-inh3=Gmeanc1-inh3/GMeanc1,
где GMeanc1 соответствует флюоресценции клеток в контрольной пробе №2;
проба №9: Kc2-inh1.1=Gmeanc2-inh1.1/GMeanc1
проба №10: Kc2-inh1.2=Gmeanc2-inh1.2/GMeanc2
проба №11: Kc2-inh2.1=Gmeanc2-inh2.1/GMeanc2
проба №12: Kc2-inh2.2=Gmeanc2-inh2.2/GMeanc2
проба №13: Kc2-inh3=Gmeanc2-inh3/GMeanc2
где GMeanc2 соответствует флюоресценции клеток в контрольной пробе №8.
Способ иллюстрируется следующими примерами.
Пример 1
А.Р.Ф. и/б 02/11499
Диагноз: немелкоклеточный рак легкого
Операционный материал опухоли преинкубируют в течение 40 мин в растворе Хенкса с глюкозой при 37°С, после чего раствор отбрасывают, а опухолевый образец разрезают при помощи скальпеля на кусочки размером 2×2×2 мм. Суспензию опухолевых клеток получают путем механического встряхивания (достаточно 5-6 встряхиваний) 10 кусочков опухоли, взятых из ее разных участков, в 5 мл раствора Хенкса с глюкозой. Суспензию опухолевых клеток фильтруют через марлевый фильтр, осадок отбрасывают. Раскапывают по 350 мкл суспензии опухолевых клеток в 13 пробирок. 1-ая пробирка является контрольной и в нее формалин не добавляют. 2-ая и 8-ая пробирка являются контролем внутриклеточного накопления доксорубицина в результате воздействия ингибиторов, и в нее добавляют доксорубицин и формалин. После раскапывания суспензии клеток в пробирки, кроме 3, 4, 5, 6, 7, 9, 10, 11, 12, 13 добавляют ингибиторы активности АВС-транспортеров: верапамил в конечной концентрации 3,3·10-4 и 1,7·10-5 М, генистеин в конечной концентрации 3,2·10-5 и 1,6·10-6 М, азид натрия в конечной концентрации 5·10-3 М: затем инкубируют в течение 20 мин при 37°С. Со 2-ой по 7-ую пробирки добавляют доксорубицин в конечной концентрации 7,7·10-5 М; с 8-ой по 13-ую добавляют доксорубицин в конечной концентрации 7,7·10-6 M; после 5 мин инкубации при 37°С клетки фиксируют формалином в конечной концентрации 10%. Далее пробы анализируют на проточном цитофлюориметре при λ=576, при значении шторки 100, со скоростью сбора клеток 500 клеток/с. Число анализируемых событий составляет не менее 10 тысяч.
В результате анализа проб на проточном цитофлюориметре были получены следующие данные о средней внутриклеточной флюоресценции доксорубицина в присутствии и отсутствии ингибиторов:

Исходя из полученных данных по приведенным ниже формулам были рассчитаны коэффициенты, по которым проводят определение чувствительности к химиотерапии солидной опухоли данного больного.

В таблице 1, приведенной ниже, сведены первичные данные о средней геометрической внутриклеточной флюоресценции доксорубицина в присутствии и отсутствии ингибиторов активности АВС-транспортеров и коэффициенты, рассчитанные исходя из них.
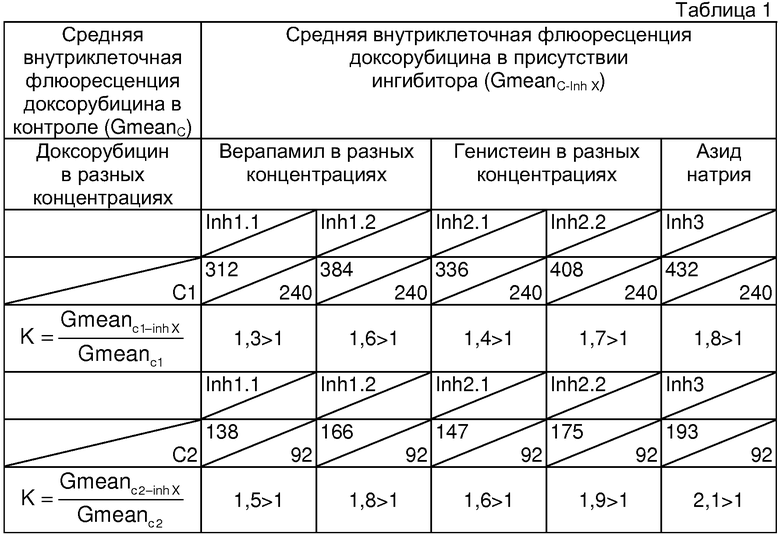
Как видно из таблицы 1, все значения коэффициента К для данного больного имеют значения большие 1, К>1. Верапамил и генистеин в обеих концентрациях вызывает увеличение внутриклеточной флюоресценции доксорубицина (К>1), из чего следует присутствие в опухолевых клетках активного плазматического транспортного белка Pgp и MRP. Доступность ядра для МЛУ-цитостатиков в данном случае высокая, так как в опухолевых клетках активны только плазматические транспортеры. Ответная реакция на воздействие ингибиторов активности АВС-транспортеров выявляется при обеих концентрациях доксорубицина С1 и С2 (К>1), что означает высокий уровень функциональной активности Pgp и MRP. Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К>1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp + MRP+, который характеризуется высоким уровнем функциональной активности транспортных белков и высокой доступностью ядра для МЛУ-цитостатиков. Солидная опухоль больного чувствительна к высоким дозам МЛУ-цитостатиков, так как в отсутствии ядерных АВС-транспортеров ядерные мишени для МЛУ-цитостатиков доступны для высоких доз цитостатиков, способных блокировать функциональную активность плазматических транспортеров. Методом выбора является высокодозная терапия МЛУ-цитостатиками.
Пример 2
В.А.С. и/б 02/11677
Диагноз: рак молочной железы
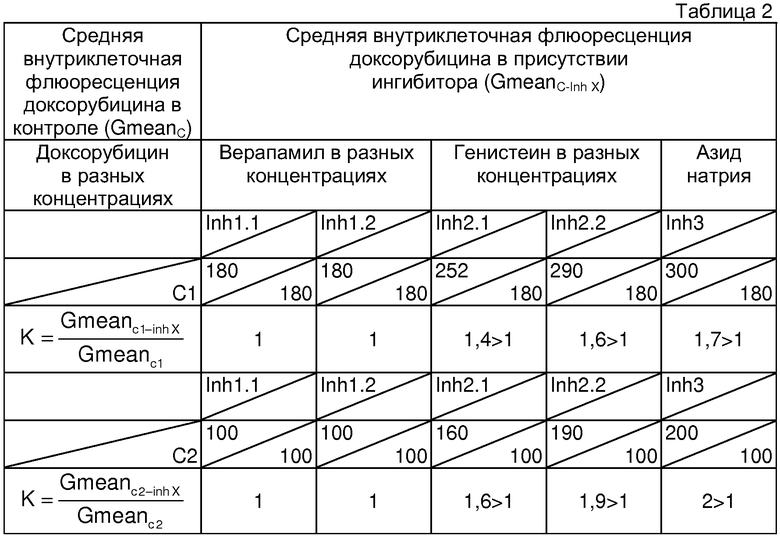
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 2.
Как следует из данных таблицы 2, верапамил в обеих концентрациях не изменяет внутриклеточную флюоресценцию доксорубицина (К=1), из чего следует, что в опухоли транспортный белок Pgp не экспрессирован. Генистеин в обеих концентрациях вызывает увеличение внутриклеточной флюоресценции доксорубицина (К>1), что означает присутствие в клетках плазматического MRP. Функциональная активность MRP в опухоли высока, так как она выявляется при обеих концентрациях доксорубицина С1 и С2 (К>1). Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К>1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp - MRP+, который характеризуется высоким уровнем функциональной активности плазматического MRP. Опухоль не чувствительна к терапии МЛУ-цитостатиками, кроме таксанов, так как последние являются субстратами только Pgp, функциональная активность которого в опухоли не выявлена.
Пример 3
Р.И.Г. и/б 02/11451
Диагноз: рак желудка
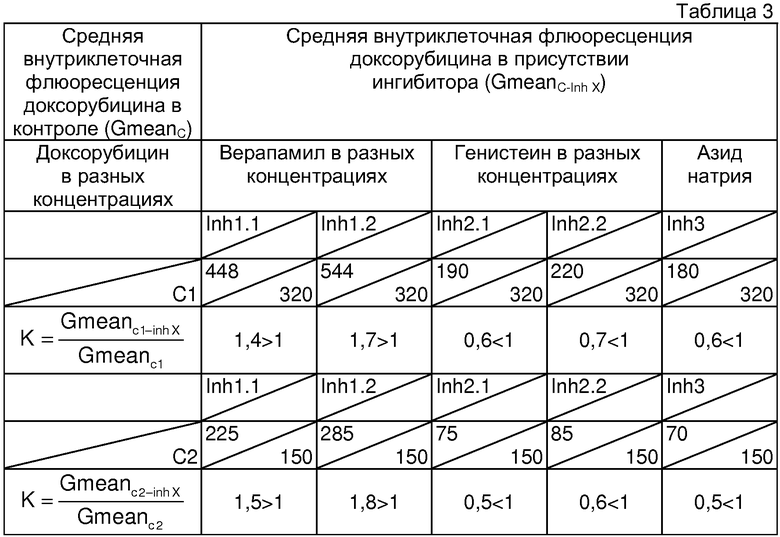
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 3.
Как следует из данных таблицы 3, верапамил в обеих концентрациях вызывает увеличение внутриклеточной флюоресценции доксорубицина (К>1), из чего следует присутствие в опухолевых клетках активного плазматического транспортного белка Pgp. Генистеин в обеих концентрациях вызывает уменьшение внутриклеточной флюоресценции доксорубицина (К<1), что означает экспрессию ядерного транспортного белка MRP, благодаря функциональной активности которого доступность ядра для цитостатиков низкая. Активность АВС-транспортеров (Pgp и MRP) в опухоли высокая, так как она выявляется при обеих концентрациях доксорубицина С1 и С2. Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К<1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp + MRP+, который характеризуется низкой доступностью ядра для цитостатиков и высоким уровнем функциональной активности Pgp и MRP. В данном случае солидная опухоль нечувствительна ко всем МЛУ-цитостатиком. Препаратом выбора являются цитостатики, не относящиеся к группе МЛУ-цитостатиков, так как проникновению последних в ядро и взаимодействию с ядерными мишенями препятствует активность ядерных транспортеров.
Пример 4
П.Т.Н. и/б 02/12347
Диагноз: рак молочной железы
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 4.
Как видно из данных таблицы 4, верапамил и генистеин в обеих концентрациях вызывает увеличение внутриклеточной флюоресценции доксорубицина (К>1) только при
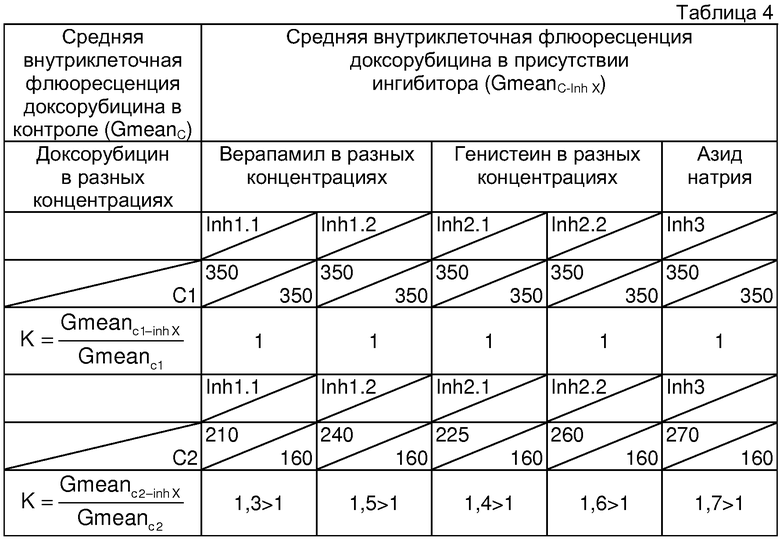
концентрации доксорубицина C2, из чего следует присутствие в опухолевых клетках конститутивного уровня экспрессии плазматических транспортных белков Pgp и MRP. Такого уровня функциональной активности АВС-транспортеров не достаточно для проявления опухолевыми клетками устойчивости к МЛУ-цитостатикам. Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К>1) только при концентрации доксорубицина C2.
По результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, не выявлен фенотип множественной лекарственной устойчивости: Pgp - MRP -. Солидная опухоль в данном случае чувствительна к МЛУ-цитостатикам, и больному рекомендована терапия МЛУ-цитостатиками.
Пример 5
С.А.Р. и/б 02/97957
Диагноз: немелкоклеточный рак легкого
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 5.
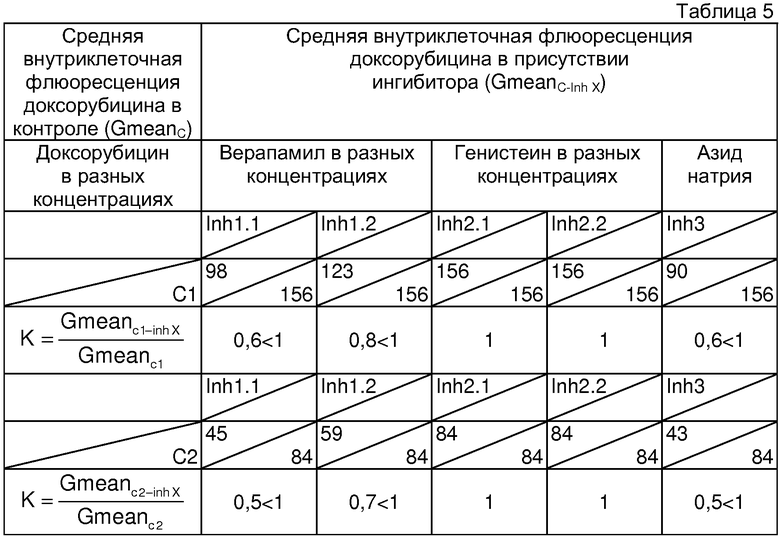
Как видно из таблицы 5, верапамил в обеих концентрациях вызывает уменьшение внутриклеточной флюооресценции доксорубицина (К<1), что означает экспрессию ядерного транспортного белка Pgp, благодаря функциональной активности которого доступность ядра для цитостатиков низкая. Генистеин в обеих концентрациях не изменяет внутриклеточную флюоресценцию доксорубицина (К=1), Активность Pgp в опухоли высокая, так как она выявляется при обеих концентрациях доксорубицина С1 и С2 (К<1). Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К<1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp + MRP -, который характеризуется низкой доступностью ядра для цитостатиков и высоким уровнем функциональной активности Pgp. В типом случае солидная опухоль нечувствительна ко всем МЛУ-цитостатикам. Препаратом выбора являются цитостатики, не относящиеся к группе МЛУ-цитостатиков, так как проникновению последних в ядро и взаимодействию с ядерными мишенями препятствует активность ядерных транспортеров.
Пример 6
С.Н.В. и/б 02/16988
Диагноз: рак желудка
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 6.
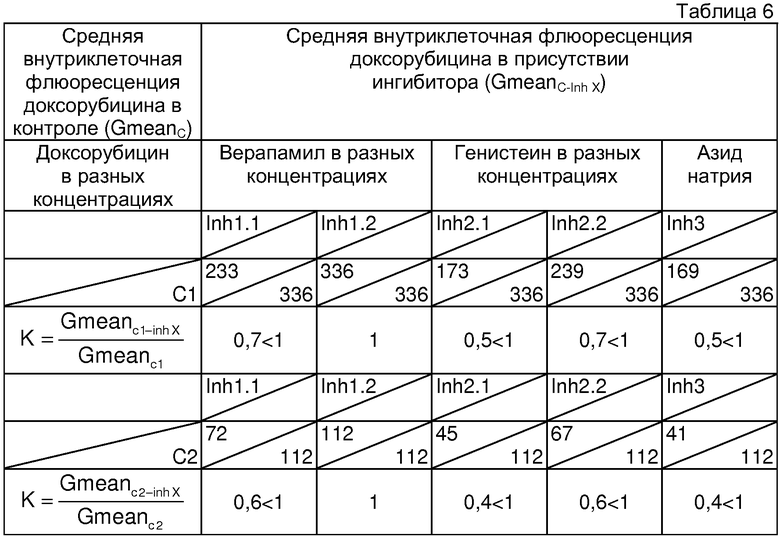
Как следует из данных таблицы 6, верапамил в одной из концентраций вызывает уменьшение внутриклеточной флюоресценции доксорубицина (К<1), из чего следует присутствие в опухолевых клетках ядерного транспортного белка Pgp, активность которого снижает доступность ядра для цитостатиков. Генистеин в обеих концентрациях вызывает уменьшение внутриклеточной флюоресценции доксорубицина (К<1), что означает экспрессию ядерного транспортного белка MRP. Активность АВС-транспортеров (Pgp и MRP) в опухоли высокая, так как она выявляется при обеих концентрациях доксорубицина C1 u С2 (К<1). Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К<1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp + MRP +, который характеризуется низкой доступностью ядра для цитостатиков и высоким уровнем функциональной активности Pgp и MRP. В данном случае солидная опухоль нечувствительна ко всем МЛУ-цитостатикам. Препаратом выбора являются цитостатики, не относящиеся к группе МЛУ-цитостатиков, так как проникновению последних в ядро и взаимодействию с ядерными мишенями препятствует активность ядерных транспортеров.
Пример 7
З.С.А. и/б 02/16911
Диагноз: рак молочной железы
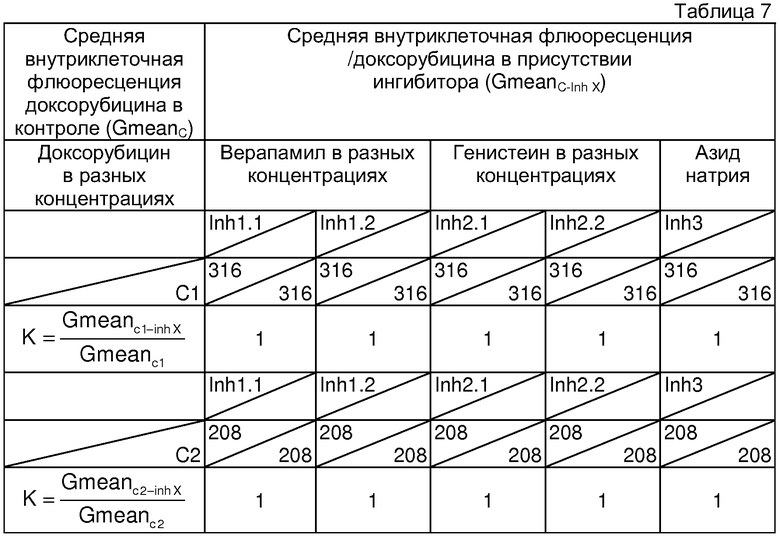
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 7.
Как видно из данных таблицы 7, верапамил и генистеин в обеих концентрациях и при обеих концентрациях доксорубицина (C1 и С2) не вызывают увеличения внутриклеточной флюоресценции доксорубицина (К=1), из чего следует отсутствие в опухолевых клетках экспрессии транспортных белков Pgp и MRP. Правильность проведенной оценки подтверждает и отсутствие реакции клеток на азид натрия (К=1).
По результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, не выявлен фенотип множественной лекарственной устойчивости: Pgp - MRP -. Солидная опухоль в данном случае чувствительна к МЛУ-цитостатикам, и больному рекомендована терапия МЛУ-цитостатиками.
Пример 8
М.В.Н. и/б 02/16960
Диагноз: рак молочной железы
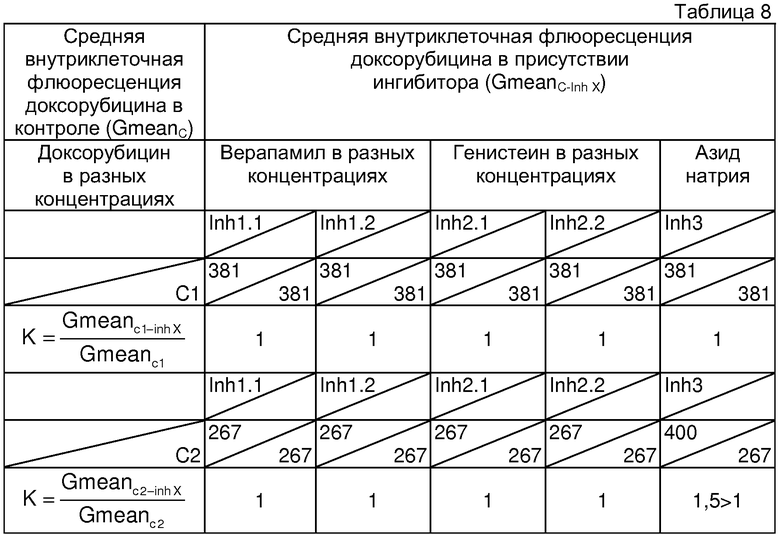
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 8.
Как видно из данных таблицы 8, верапамил и генистеин в обеих концентрациях и при обеих концентрациях доксорубицина (С1 и C2) не вызывают увеличения внутриклеточной флюоресценции доксорубицина (К=1), из чего следует отсутствие в опухолевых клетках экспрессии транспортных белков Pgp и MRP. Однако воздействие на клетки данной опухоли азида натрия при концентрации доксорубицина C2 привело к увеличению внутриклеточной флюоресценции доксорубицина (К>1), из чего следует присутствие в опухолевых клетках конститутивного уровня экспрессии плазматических транспортных белков, отличных от Pgp и MRP. Такого уровня функциональной активности АВС-транспортеров не достаточно для проявления опухолевыми клетками устойчивости к МЛУ-цитостатикам.
По результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, не выявлен фенотип множественной лекарственной устойчивости: Pgp - MRP -. Солидная опухоль в данном случае чувствительна к МЛУ-цитостатикам, и больному рекомендована терапия МЛУ-цитостатиками.
Пример 9
С.Т.В. и/б 02/16565
Диагноз: рак молочной железы
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 9.
Как следует из данных таблицы 9, верапамил в обеих концентрациях не изменяет внутриклеточную флюоресценцию доксорубицина (К=1), из чего следует, что в опухоли транспортный белок Pgp не экспрессирован. Генистеин в обеих концентрациях также не изменяет внутриклеточную флюоресценцию доксорубицина (К=1), из чего следует, что и транспортный белок MRP в опухоли не экспрессирован. Однако в клетках данной опухоли при воздействии азида натрия отмечается существенное изменение внутриклеточной флюоресценции доксорубицина (К>1), из чего следует присутствие в опухолевых клетках экспрессии транспортных белков, отличных от Pgp и MRP. При этом функциональная активность таких транспортных белков в опухоли высока, так как она выявляется при обеих концентрациях доксорубицина С1 и С2 (К>1).
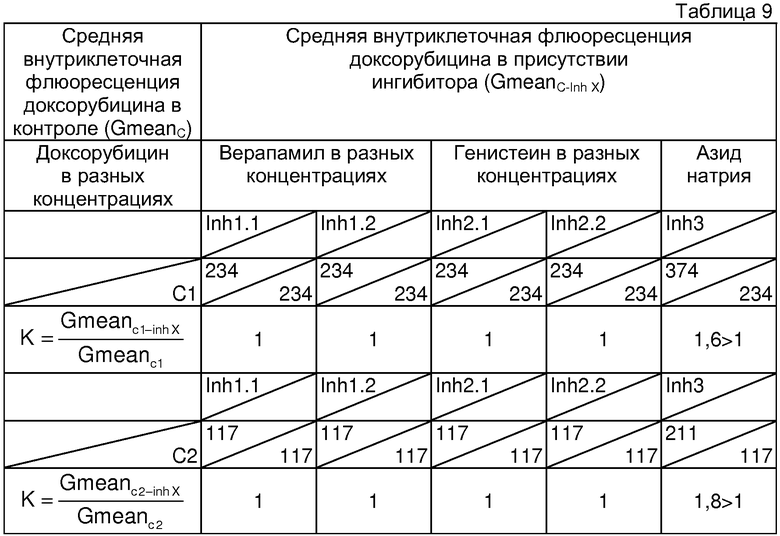
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp - MRP -, но при этом данная опухоль характеризуется высоким уровнем функциональной активности транспортных белков, отличных от Pgp и MRP. Опухоль не чувствительна к терапии МЛУ-цитостатиками, кроме таксанов, так как последние являются субстратами только Pgp, функциональная активность которого в опухоли не выявлена.
Пример 10
М.А.В. и/б 02/13171
Диагноз: рак желудка
Определение чувствительности опухоли к химиотерапии и расчет коэффициентов проводили аналогично примеру 1. Для данного больного получены следующие показатели чувствительности к химиотерапии. Результаты представлены в таблице 10.
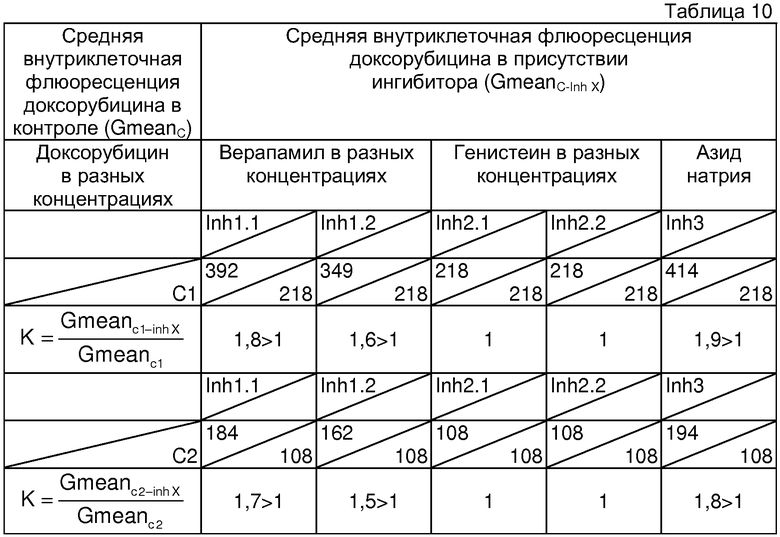
Как следует из данных таблицы 10, генистеин в обеих концентрациях не изменяет внутриклеточную флюоресценцию доксорубицина (К=1), из чего следует, что в опухоли транспортный белок MRP не экспрессирован. Верапамил же в обеих концентрациях вызывает увеличение внутриклеточной флюоресценции доксорубицина (К>1), из чего следует присутствие в опухолевых клетках активного плазматического транспортного белка Pgp. Доступность ядра для МЛУ-цитостатиков в данном случае высокая, так как в опухолевых клетках активны только плазматические транспортеры. Ответная реакция на воздействие верапамила выявляется при обеих концентрациях доксорубицина С1 и С2 (К>1), что означает высокий уровень функциональной активности Pgp. Правильность проведенной оценки подтверждает ответная реакция на азид натрия (К>1).
Таким образом, по результатам оценки в операционном материале опухоли функциональной активности АВС-транспортеров, экспрессия которых определяет множественную лекарственную устойчивость, установлен следующий фенотип множественной лекарственной устойчивости - Pgp + MRP -, который характеризуется высоким уровнем функциональной активности транспортных белка Pgp и высокой доступностью ядра для МЛУ-цитостатиков. Солидная опухоль больного чувствительна к высоким дозам МЛУ-цитостатиков, так как в отсутствии ядерных АВС-транспортеров ядерные мишени для МЛУ-цитостатиков доступны для высоких доз цитостатиков, способных блокировать функциональную активность плазматических транспортеров. Методом выбора является высокодозная терапия МЛУ-цитостатиками.
Представленные примеры иллюстрируют все возможные заключения об индивидуальной чувствительности к химиотерапии и рекомендации к выбору адекватного лечения, вытекающие из установленного диагноза.
Предложенным способом проведено определение индивидуальной чувствительности к химиотерапии у 15 больных. Точность способа составила 80%.
Таким образом, предложенный способ позволяет точно и быстро определять индивидуальную чувствительность к химиотерапии солидных опухолей, что позволяет проводить адекватную терапию.

СПИСОК ЛИТЕРАТУРЫ
1. Fisher GA, Lum BL, Hausdorff J, Sikic BI. "Pharmacological considerations in the modulation of multidrug resistance". - Eur J Cancer. 1996 Jun; 32A(6): 1082-8.
2. Arts HJ, Katsaros D, de Vries EG, Massobrio M, Genta F, Danese S, Arisio R, Scheper RJ, Kool M, Scheffer GL, Willemse PH, van der Zee AG, Suurmeijer AJ. "Drug resistance-associated markers P-glycoprotein, multidrug resistance-associated protein 1, multidrug resistance-associated protein 2, and lung resistance protein as prognostic factors in ovarian carcinoma". - Clin Cancer Res. l999 Oct; 5(10): 2798-805.
3. Litman T, Brangi M, Hudson E, Fetsch P, Abati A, Ross DD, Miyake K, Resau JH, Bates SE. "The multidrug-resistant phenotype associated with overexpression of the new ABC half-transporter, MXR (ABCG2)". - J Cell Sci. 2000 Jun; 113 (Pt 11): 2011-21.
4. Jang SH, Wientjes MG, Au JL. "Kinetics of P-glycoprotein-mediated efflux of paclitaxel". - J Pharmacol Exp Ther. 2001 Sep: 298(3): 1236-42.
5. Broxterman H.J., Lankelma J., Pinedo H.M., Eekman C.A., Wahrer D.C., Ossenkoppele G.J., Schuurhuis G.J., "Theoretical and practical considerations for the measurement of P-glycoprotein function in acute myeloid leukemia". - Leukemia 1997; 11(7): 1110-8.
6. Davey MW. Hargrave RM, Davey RA. "Comparison of drug accumulation in P-glycoprotein-expressing and MRP-expressing human leukaemia cells". - Leuk Res. 1996 Aug; 20(8): 657-64.
7. Goldstein U, Galski H, Fojo A, Willingham M, Lai SL, Gazdar A, Pirker R, Green A, Crist W, Brodeur GM, el al. "Expression of a multidrug resistance gene in human cancers". - J Natl Cancer Inst. 1989 Jan 18; 81(2): 116-24
8. Verrelle P, Meissonnier F, Fonck Y, Feillel V, Dionet C, Kwiatkowski F, Plagne R, Chassagne J. "Clinical relevance of immunohistochemical detection of multidrug resistance P-glycoprotein in breast carcinoma". - J Natl Cancer Inst. 1991 Jan 16; 83(2): 111-6.
9. Yokoyama H., Ishida Т., Sugio K., Inoue Т., Sugimachi К. "Immunohistochemical evidence that P-glycoprotein in non-small cell lung cancers is associated with shorter survival". - Surg Today 1999; 29(11): 1141-7.
10. Ferrero J.М., Etienne M.C., Formento J.L., Francoual M., Rostagno P., Peyrottes I., Ettore F., Teissier E., Leblanc-Talent P., Namer M., Milano G. "Application of an original RT-PCR-ELISA multiplex assay for MDR 1 and MRP, along with p53 determination in node-positive breast cancer patients". - Br J Cancer 2000: 82(1): 171-7.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИММУНОФЛУОРЕСЦЕНТНОГО АНАЛИЗА МАРКЕРОВ МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ РЕЗИСТЕНТНОСТИ В СОЛИДНЫХ ОПУХОЛЯХ ЧЕЛОВЕКА | 2009 |
|
RU2413948C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ С ПОМОЩЬЮ ОПРЕДЕЛЕНИЯ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ К ХИМИОТЕРАПИИ КУЛЬТУРАЛЬНЫМ МЕТОДОМ И ПРИМЕНЕНИЯ КОМБИНАЦИИ РАСТИТЕЛЬНЫХ ЦИТОСТАТИКОВ | 2011 |
|
RU2470658C1 |
| СПОСОБ ПЕРСОНАЛИЗИРОВАННОГО НАЗНАЧЕНИЯ НЕОАДЪЮВАНТНОЙ ХИМИОТЕРАПИИ БОЛЬНЫМ ЛЮМИНАЛЬНЫМ В РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2015 |
|
RU2594251C1 |
| Противоопухолевая композиция доксорубицина с ингибитором АТФ-зависимых обратных транспортеров клеток | 2018 |
|
RU2680834C1 |
| СРЕДСТВО ДЛЯ ПРЕОДОЛЕНИЯ МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТИ | 2008 |
|
RU2434879C2 |
| СПОСОБ ОПТИМИЗАЦИИ ПРОЦЕДУРЫ ОБЩЕЙ УПРАВЛЯЕМОЙ ГИПЕРТЕРМИИ С ТЕМПЕРАТУРОЙ РАЗОГРЕВА 43-44єC ПУТЕМ ИЗМЕРЕНИЯ ПРОТОКОЛА ХИМИОТЕРАПИИ | 2002 |
|
RU2232581C2 |
| СРЕДСТВО, ИНГИБИРУЮЩЕЕ МНОЖЕСТВЕННУЮ ЛЕКАРСТВЕННУЮ УСТОЙЧИВОСТЬ ОПУХОЛЕВЫХ КЛЕТОК | 2012 |
|
RU2494742C1 |
| ПРОТИВООПУХОЛЕВЫЙ ПРЕПАРАТ | 2011 |
|
RU2451509C1 |
| ПОЛИМЕРОСОДЕРЖАЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ПРОТИВООПУХОЛЕВОГО ПРЕПАРАТА ЭТОПОЗИДА | 2015 |
|
RU2595859C1 |
| КЛЕТОЧНАЯ ЛИНИЯ ОСТЕОГЕННОЙ САРКОМЫ ЧЕЛОВЕКА793 OsSar RVV | 2019 |
|
RU2722867C1 |
Изобретение относится к области медицины и касается определения индивидуальной чувствительности к химиотерапии солидных опухолей человека. Сущность способа заключается в том, что в суспензию опухолевых клеток пациента добавляют ингибиторы активности АВС-транспортеров-верапамил и генистеин в двух разных концентрациях и азид натрия, инкубируют, затем добавляют доксорубицин в двух разных концентрациях, снова инкубируют, затем добавляют формалин и определяют значения флюоресценции в каждой пробе. Рассчитывают относительное изменение внутриклеточной флюоресценции доксорубицина после воздействия каждого из используемых ингибиторов в исследуемых концентрациях при каждой исследуемой концентрации доксорубицина. Исходя из полученных данных делают заключение об индивидуальной чувствительности опухоли к химиотерапии МЛУ-цитостатиками. Использование способа позволяет повысить точность определения, провести исследования в короткие сроки. 10 табл., 2 з.п. ф-лы.
Kc-inh x=Gmeanc-inh х/Gmeanс,
где Kc-inh x - относительное изменение внутриклеточной флюоресценции доксорубицина после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
Gmeanc-inh x - средняя геометрическая флюоресценция популяции клеток после воздействия одного из используемых ингибиторов в концентрации Х при концентрации доксорубицина С;
Gmeanc - средняя геометрическая флюоресценция популяции клеток в контрольной пробе при концентрации доксорубицина С;
Концентрация доксорубицина С:
С1 - концентрация доксорубицина 7,7·10-5 М
С2 - концентрация доксорубицина 7,7·10-6 М
Ингибитор активности АВС-транспортеров Inh X:
Inh1.1 - верапамил в концентрации 3,3·10-4 М
Inh1.2 - верапамил в концентрации 1,7·10-5 М
Inh2.1 - генистеин в концентрации 3,2·10-5 М
Inh2.2 - генистеин в концентрации 1,6·10-6 М
Inh3 - азид натрия в концентрации 5·10-3 М
и заключение о чувствительности опухоли к химиотерапии МЛУ-цитостатиками делают при значениях:
1) Кc1,c2-inh1.1,1.2,2.1,2.2,3=1;
или
2) Kc1-inh1.1,1.2,2.1,2.2,3=1;
если хотя бы одно из Kc2-inh1.1, Kc2-inh1.2, Kc2-inh2.1, Kc2-inh2.2≠1 и Kc2-inh3≠1;
или
3) Kc1-inh1.1,1.2,2.1,2.2,3=1; Kc2-inh1.1,1.2,2.1,2.2=1 и Кc2-inh3≠1;
заключение о нечувствительности опухоли к терапии МЛУ-цитостатиками, кроме таксанов, делают при значениях
Kc1,c2-inh 1.1,1.2=1 и 1) если хотя бы одно из Kc1,c2-inh2.1, Kc1,c2-inh2.2≠1 и Kc1,c2-inh3≠1;
или
2) Kc1,c2-inh2.1,2.2=1 и Kc1,c2-inh3≠1,
заключение о чувствительности опухоли к терапии высокими дозами МЛУ-цитостатиков делают,
если значения Kc1,c2-inh1.1, Kc1,c2-inh1.2>1 и 1) Kc1,c2-inh2.1,2.2=1 и Kc1,c2-inh3>1;
или
2) если значения Kc1,c2-inh2.1, Kc1,c2-inh2.2>1 и Kc1,c2-inh3>1,
заключение о нечувствительности опухоли к терапии МЛУ-цитостатиками делают
а) если хотя бы одно из значений Kc1,c2-inh1.1, Kc1,c2-inh1.2<1 и
1) Kc1,c2-inh2.1,2=1 и Кс1,c2-inh3<1
или
2) если хотя бы одно из Kc1,c2-inh2.1, Kc1,c2-inh2.2<1 и Kc1,c2-inh3<1;
б) если значения Kc1,c2-inh1.1 и Kc1,c1-inh1.2>1 и
значения Kc1,c2-inh2.1, Kc1,c2-inh2.2<1 и Kc1,c2-inh3<1.
| VERRELLE P | |||
| et al | |||
| Clinical relevance of immunohistochemical detection of multidrug resistance P-glycoprotein in breast carcinoma | |||
| J | |||
| Nath Cancer Inst | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧУВСТВИТЕЛЬНОСТИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ К ХИМИОТЕРАПИИ | 1999 |
|
RU2161444C1 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ДИАГНОСТИКИ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ РЕЗИДУАЛЬНЫХ ОПУХОЛЕЙ ЯИЧНИКОВ К ХИМИОТЕРАПИИ | 2002 |
|
RU2239362C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНДИВИДУАЛЬНОЙ ЧУВСТВИТЕЛЬНОСТИ ОПУХОЛИ К ХИМИОТЕРАПИИ | 2000 |
|
RU2179725C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНДИВИДУАЛЬНОЙ ХИМОЧУВСТВИТЕЛЬНОСТИ ОПУХОЛИ У БОЛЬНЫХ IN VITRO | 1994 |
|
RU2094802C1 |
Авторы
Даты
2008-01-27—Публикация
2005-06-23—Подача