Область техники, к которой относится изобретение.
Настоящее изобретение относится к способу получения спироизомера пентаэритритдифосфитов. Более подробно, настоящее изобретение относится к способу получения пентаэритритдифосфитов по реакции переэтерификации в вакууме, при этом получают дифосфит с высоким содержанием спироизомера.
Уровень техники
Различные органические фосфиты используют в качестве эффективных полимерных добавок и ингибиторов термоокислительного разложения полимеров в процессе переработки. Прежде всего пентаэритритдифосфиты используют в тех случаях, когда требуется повышенная гидролитическая устойчивость и повышенная совместимость с некоторыми полимерами, такими как полиолефины, что позволяет использовать такие дифосфиты в качестве стабилизаторов полимеров.
Пентаэритритдифосфиты образуют по крайней мере две изомерные формы: спиро- и мостиковые изомеры. В качестве коммерческих препаратов более предпочтительными являются спироизомеры. Таким образом, наиболее предпочтительным является получение пентаэритритдифосфитов с высоким содержанием спироизомера.
В большинстве случаев пентаэритритдифосфиты получают с использованием по крайней мере двух различных способов. Согласно первому способу проводят две последовательные реакции переэтерификации, сначала реакцию пентаэритрита с трифенилфосфитом с образованием дифенилпентаэритритдифосфита, а затем реакцию промежуточного дифенилпентаэритритдифосфита с соответствующим алкилфенолом или спиртом с образованием требуемого пентаэритритдифосфита.
Согласно другому способу дихлорпентаэритритдифосфит взаимодействует с соответствующим алкилфенолом или спиртом с образованием требуемого пентаэритритдифосфита. С использованием последнего способа получают бис(алкилфенил)пентаэритритдифосфит, содержащий следовые количества мостикового изомера, но такой способ требует использования более сложной и дорогостоящей технологии. Первый способ переэтерификации является более дешевым и технологичным, однако в большинстве случаев при использовании такого способа получают смесь изомеров, в которой содержание спироизомера составляет от 50 до 75% в зависимости от способа получения и реагентов. Таким образом, полученные по реакции переэтерификации бис(алкилфенил)пентаэритритдифосфиты представляют собой смесь спиро- и мостиковых изомеров, которые необходимо подвергать дополнительной очистке с использованием селективной кристаллизации с целью получения в основном спироизомера. Однако такой подход на практике приводит к получению продукта с относительно низким выходом.
Подобные способы получения пентаэритритдифосфита представлены, в частности, в заявке на патент США №5438086.
Один подход к повышению содержания спироизомера бис(2,4-ди-трет-бутилфенил)пентаэритритдифосфита по реакции переэтерификации заключается во взаимодействии дифенилпентаэритритдифосфита (ДФПЭДФ) с 2,4-ди-трет-бутилфенолом в растворителе, таком как (С10-С18)н-алканы или циклоалканы. По данному способу получают продукт с содержанием спироизомера вплоть до 90%, однако выход дифосфита является относительно низким и составляет приблизительно 77%.
Экономически более выгодным и, следовательно, предпочтительным способом переэтерификации является способ, который будет позволять получить бис(алкилфенил)пентаэритритдифосфит с содержанием спироизомера по крайней мере 90% и с высоким выходом дифосфита, по крайней мере 95%.
Раскрытие изобретения
Целью настоящего изобретения является разработка способа получения пентаэритритдифосфитов по реакции переэтерификации с высоким содержанием спироизомера и высоким выходом.
В основном, в настоящем изобретении предлагается способ получения бис(алкилфенил)пентаэритритдифосфитов, в котором высокое содержание спироизомера составляет более 90%, по реакции переэтерификации, при этом выход составляет более 95%. Способ по настоящему изобретению включает стандартные реакции переэтерификации, которые позволяют повысить содержание спироизомера и выход конечного продукта за счет 1) уникальных условий реакции, которые используют для получения промежуточного продукта и конечного продукта, при этом сведено к минимуму образование продуктов конкурентных реакций и 2) использования перегонки для концентрирования содержания дифосфита в промежуточном продукте и конечных продуктах.
В связи с этим объектом настоящего изобретения является разработка последовательности реакций переэтерификации, которые приводят к повышанию содержания спироизомера пентаэритритдифосфита до максимальной величины.
Другой объект настоящего изобретения заключается в воздействии на указанную выше последовательность реакций переэтерификации в предпочтительном варианте воплощения настоящего изобретения с использованием пентаэритрита и трифенилфосфита с образованием промежуточного пентаэритритдифосфита и последующей второй реакцией переэтерификации в присутствии замещенного фенола или низшего спирта, при этом образуется пентаэритритдифосфит с высоким содержанием спироизомера.
Эти и другие объекты настоящего изобретения подробно описаны в следующем разделе и определены в прилагаемых пунктах формулы изобретения.
Осуществление изобретения
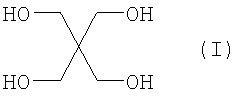
Способ по настоящему изобретению включает последовательные реакции переэтерификации, которые позволяют получить промежуточный и конечный продукты реакции. Первая реакция является реакцией переэтерификации пентаэритрита (формулы I)

с монофосфитом в присутствии щелочного катализатора. Монофосфит выбирают из группы триарилфосфитов, например трифенилфосфит (формулы II)
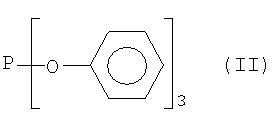
или триалкилфосфитов, например триметилфосфит или триэтилфосфит. В общем случае, триалкил- или триарилфосфит имеют общую формулу Р-(OR1)3, где R1 выбирают из группы, включающей линейные или разветвленные алкильные группы, циклоалифатические группы, которые могут содержать заместители, линейные или разветвленные алкенильные группы, незамещенные или алкилзамещенные арильные группы или арилалкильные группы.
В частности, примеры линейных или разветвленных алкильных групп, без ограничения перечисленным, включают (С1-С20)алкильные группы, например метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил или стеарил.
Примеры циклоалифатических или циклических алкильных групп, которые содержат заместители, без ограничения перечисленным, включают циклоалкильные группы, содержащие от 5 до 7 атомов углерода, такие как циклопентил, циклогексил и циклогептил, и алкилциклоалкильные группы, содержащие от 6 до 11 атомов углерода, в которых положение алкильной группы может изменяться, такие как группы метилциклопентил, диметилциклопентил, метилэтилциклопентил, диметилциклопентил, метилциклогексил, диметилциклогексил, метилэтилциклогексил, диэтилциклогексил, метилциклогептил, диметилциклогептил, метилциклогептил и диэтилциклогептил.
Примеры линейных или разветвленных алкенильных групп, без ограничения перечисленным, включают группы, содержащие от 2 до 30 атомов углерода, в которых положение двойной связи может изменяться, такие как бутенил, пентенил, гексенил, гептенил, октенил, ноненил, деценил, ундеценил, додеценил, тридеценил, тетрадеценил, пентадеценил, гексадеценил, гептадеценил и октадеценил.
Примеры незамещенных или алкилзамещенных арильных групп включают арильные группы, содержащие от 6 до 18 атомов углерода, такие как фенил, дифенил и нафтил, и арилалкильные группы, содержащие от 7 до 40 атомов углерода, в которых алкильная группа является линейной или разветвленной и присоединена в любое положение арильной группы, такие как толил, ксилил, этилфенил, пропилфенил, бутилфенил, пентилфенил, гексилфенил, гептилфенил, октилфенил, нонилфенил, децилфенил, ундецилфенил, додецилфенил, диэтилфенил, дибутилфенил и диоктилфенил. Алкиларильные группы могут дополнительно содержать заместители, включающие функциональные группы, такие как алкокси, гидрокси, циано, нитро, галоген, карбокси и т.п.
Примеры арилалкильных групп включают группы, содержащие от 7 до 40 атомов углерода, в которых алкильная группа является линейной или разветвленной, такие как бензил, фенилэтил, фенилпропил, фенилбутил, фенилпентил и фенилгексил.
Первая реакция переэтерификаци приводит к образованию промежуточного продукта пентаэритритдифосфита, содержащего спироизомер формулы (III)

где R1 определен выше, и мостиковый изомер формулы (IV)
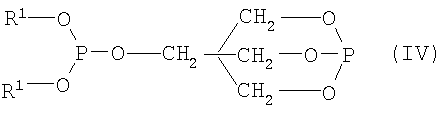
В предпочтительном варианте пентаэритрит вступает в реакцию переэтерификации в присутствии трифенилфосфита с образованием промежуточного соединения дифенилпентаэритритдифосфита формулы (V)

Вторая реакция является реакцией переэтерификации промежуточного пентаэритритдифосфита со спиртом R2-OH, причем спирт выбирают из группы, включающей (С8-С22)алканолы, (С8-С22)алкенолы, фенолы и их производные, (С7-С40)алкиларилфенолы и их производные, (С7-С40)арилалкилфенолы и их производные, где указанные производные являются химическими остатками, выбранными из группы, включающей галогены, (С1-С4)алкильные группы, (С1-С4)алкоксисоединения, аминогруппы, остатки (C1-C6)карбоновых кислот, цианогруппы, нитрогруппы и т.п., в присутствии щелочного катализатора с образованием пентаэритритдифосфита формулы (VI)

где R2 предпочтительно выбирают из группы, включающей 2,4-ди-трет-бутилфенил, 2,4-дикумилфенил и (низш.)(С8-С20)алканы, например стеарил, изодецил и децилпроизводные, предпочтительно полученные из спиртов, которые предпочтительно выбирают из группы, включающей 2,4-ди-трет-бутилфенол, 2,4-дикумилфенол формулы (VII)

и в более общем случае, как описано выше.
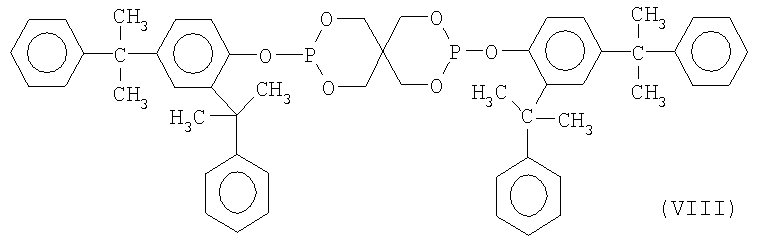
В предпочтительном варианте в процессе второй реакции переэтерификации промежуточное соединение дифенилпентаэритритдифосфита, полученное в результате первой реакции переэтерификации по настоящему изобретению, вступает в реакцию переэтерификации в присутствии 2,4-дикумилфенола и щелочного катализатора с образованием бис(2,4-дикумилфенил)пентаэритритдифосфита с высоким выходом и высоким содержанием спиро-изомера формулы (VIII)

При получении реакционной смеси для первой реакции переэтерификации монофосфит и пентаэритрит используют в соотношении приблизительно от 1 до 3 моль монофосфита на 1 моль пентаэритрита. В предпочтительном варианте первой реакции переэтерификации используют стехиометрические количества реагентов: 2 моль монофосфита на 1 моль пентаэритрита. В реакционной смеси можно использовать растворитель для снижения вязкости, повышения реакционной способности и/или для проведения последовательной очистки с использованием фракционной кристаллизации реакционной смеси. Таким образом, растворитель не требуется и является необязательным. Пригодные растворители включают ароматические, алифатические и циклические углеводороды, содержащие от 6 до 24 атомов углерода. Пригодные растворители включают нормальные или циклические алканы. В качестве растворителя предпочтительно используют насыщенный углеводород или смесь насыщенных углеводородов, которые выбирают из группы, включающей (С6-С24)н-алканы и циклоалканы. Примеры пригодных углеводородов включают н-декан, н-додекан, н-тридексан, н-гексадекан и т.п., и циклические и полициклические аналоги, такие как циклододекан, бицикло[4,4,0]декан (декагидронафталин) и т.п. В большинстве случаев растворителем является смесь растворителей, которая включает низшие алканы, например гексан, гептан и циклогексан. В настоящем изобретении используют также ненасыщенные растворители, например бензол и толуол. При использовании в составе реакционной смеси растворителей их используют в количестве от приблизительно 10 мас.% до приблизительно 200 мас.% в расчете на массу полученного промежуточного пентаэритритдифосфита.
При проведении первой реакции переэтерификации используют также щелочной катализатор. Щелочным катализатором предпочтительно является щелочное неорганическое соединение и наиболее предпочтительно оксид, гидроксид, карбонат или алкоголят щелочного или щелочноземельного металла, которые представляют собой известные в данной области техники катализаторы. В составе реакционной смеси используют щелочной катализатор в количестве от приблизительно 0,1 мас.% до приблизительно 5 мас.% в расчете на массу полученного промежуточного пентаэритритдифосфита.
Первую реакцию переэтерификации проводят в условиях контролируемых температуры и давления. В предпочтительном варианте первую реакцию переэтерификации проводят при атмосферном давлении. Реакцию проводят также в вакууме (от высокого вакуума до приблизительно 200 мм рт.ст.) с удалением выделяющегося фенола перегонкой. Температуру первой реакции поддерживают в интервале от приблизительно 60°С до приблизительно ниже 125°С, предпочтительно от 70°С до приблизительно 105°С. При указанных температурах сводится к минимуму образование нежелательных побочных продуктов и соответственно повышается до максимального выход пентаэритритдифосфита.
Без ограничения какой-либо теорией можно предположить, что использование стехиометрических количеств и низких температур при проведении первой реакции переэтерификации при атмосферном давлении обеспечивает селективное образование спиро- и мостиковых изомеров промежуточного дифенилпентаэритритдифосфита за счет других нежелательных побочных продуктов реакции. Побочный продукт переэтерификации отделяют от всех остаточных реагентов, а побочные продукты реакции отделяют перегонкой или фракционной кристаллизацией дифосфита в растворителе. Такая уникальная обработка приводит к получению спиро- и мостиковых изомеров промежуточного пентаэритритдифосфита, суммарная масса которых составляет выход более 95% в расчете на массу монофосфита.
В предпочтительном варианте первой реакции переэтерификации фенол образуется при переэтерификации пентаэритрита и трифенилфосфита в присутствии щелочного катализатора с образованием в качестве промежуточного производного пентаэритритдифосфита дифенилпентаэритритдифосфита. Выделяющийся фенол, весь непрореагировавший монофосфит и все побочные продукты реакции удаляют при перегонке. Перегонку проводят при температуре в интервале от приблизительно 100°С до приблизительно 300°С и при давлении от высокого вакуума до 200 мм рт.ст. При этом получают фенольный побочный продукт и монофосфитные реагенты высокого качества, их можно использовать в качестве исходного материала для проведения других реакций. Побочные компоненты реакции можно повторно использовать в первой реакции переэтерификации (рециклинг), при этом они превращаются в спиро- и мостиковые изомеры пентаэритритдифосфитов.
Другие способы очистки первой реакционной смеси включают фракционную кристаллизацию в растворителе и фракционную кристаллизацию расплава. При проведении реакции в растворителе для фракционной кристаллизации пентаэритритдифосфита используют тот же раворитель, что и для разбавления реакционной смеси.
После проведения первой реакции переэтерификации полученное очищенное промежуточное соединение пентаэритритдифосфита используют во второй реакции переэтерификации с образованием второго производного пентаэритритдифосфита. При получении реакционной смеси для второй реакции переэтерификации замещенный фенол или спирт и промежуточное производное пентаэритритдифосфита используют в количествах от приблизительно стехиометрических до избытка в приблизительно 300 мас.% от стехиометрического количества замещенного фенола или спирта. Замещенный фенол (или избыток спирта) используют для снижения вязкости второй реакционной смеси и для смещения реакции в сторону конечного продукта (до завершения реакции). В предпочтительном варианте замещенным фенолом является 2,4-дикумилфенол или 2,4-ди-трет-бутилфенол. Таким образом, при использовании замещенного фенола вторым производным пентаэритритдифосфита, образующимся в процессе второй реакции переэтерификации, является бис(замещенный фенол)пентаэритритдифосфит.
Растворитель в составе реакционной смеси используют для снижения вязкости, увеличения реакционной способности и/или для проведения последовательной очистки реакционной массы с использованием фракционной кристаллизации. Однако растворитель не требуется и является необязательным. Пригодные растворители включают ароматические, алифатические и циклические углеводороды, содержащие от 6 до 24 атомов углерода. Пригодные растворители включают нормальные или циклические алканы. Предпочтительным растворителем является насыщенный углеводород или смесь насыщенных углеводородов, которые выбирают из группы, включающей (С6-С24)-алканы и циклоалканы. Примеры пригодных углеводородов включают н-декан, н-додекан, н-тридекан, н-гексадекан и т.п., и циклические и полициклические аналоги, такие как циклододекан, бицикло[4,4,0]декан (декагидронафталин) и т.п. В большинстве случаев растворителем является смесь растворителей, которая включает (низш.)алканы, например гексан, гептан и циклогексан. В настоящем изобретении используют также ненасыщенные растворители, например бензол, толуол и т.п. При использовании в составе реакционной смеси растворителей их используют в количестве от приблизительно 10 мас.% до приблизительно 200 мас.% в расчете на массу полученного промежуточного пентаэритритдифосфита.
При проведении второй реакции этерификации используют также щелочной неорганический катализатор. В качестве щелочного катализатора предпочтительным является щелочное неорганическое соединение, наиболее предпочтительно оксид, гидроксид, карбонат, алкоголят щелочного или щелочноземельного металла, которые представляют собой известные в данной области техники катализаторы. В составе второй реакционной смеси используют щелочной катализатор в количестве от приблизительно 0,1 мас.% до приблизительно 5 мас.% в расчете на массу полученого второго производного пентаэритритдифосфита.
Вторую реакцию переэтерификации проводят в условиях контролируемых температуры и давления. Температуру второй реакционной смеси поддерживают в интервале от приблизительно 120°С до приблизительно менее 175°С, предпочтительно от 120°С до приблизительно 170°С и более предпочтительно поддерживают при приблизительно 150°С. Реакцию проводят в вакууме, при этом давление поддерживают в интервале от высокого вакуума до 200 мм рт.ст. В предпочтительном варианте фенол образуется при переэтерификации промежуточного производного дифенилпентаэритритдифосфита и 2,4-дикумилфенола с образованием в качестве второго производного пентаэритритдифосфита промежуточного бис(2,4-дикумилфенил)пентаэритритдифосфита. Побочный фенол, выделяющийся при второй реакции переэтерификации, удаляют при перегонке. Фенольный побочный продукт получают высокого качества и его можно использовать в качестве исходного материала для проведения других реакций.
Без ограничения какой-либо теорией можно предположить, что использование стехиометрических количеств и удаление фенольного побочного продукта в ходе второй реакции переэтерификации наряду с высокой чистотой пентаэритритдифосфита обеспечивает селективное образование спироизомера второго пентаэритритдифосфита за счет мостикового изомера. Особые условия в ходе второй реакции переэтерификации и первой реакции переэтерификации позволяют получить продукт, в котором содержание спироизомера составляет более 90% в расчете на общую массу спиро- и мостикового изомера второго производного пентаэритритдифосфита, который образуется в результате второй реакции переэтерификации. Суммарная масса спиро- и мостикового изомеров второго производного пентаэритритдифосфита составляет более 95% в расчете на массу промежуточного пентаэритритдифосфита.
Второй пентаэритритдифосфит, полученный в результате второй реакции переэтерификации, отделяют от реакционной смеси перегонкой. В предпочтительном варианте второй реакции переэтерификации реакционную смесь перегоняют для удаления всех непрореагировавших материалов, избытка замещенного фенола (или спирта, если его используют), растворителя (если его используют) и/или любого остаточного фенола, при этом получают очищенный второй пентаэритритдифосфит, в котором содержание спиро- и мостикового изомеров второго пентаэритритдифосфита предпочтительно составляет 99 мас.% в расчете на общую массу второго пентаэритритдифосфита и остаточных примесей. Перегонку проводят при температуре в интервале от приблизительно 100°С до приблизительно 300°С и при давлении от высокого вакуума до 200 мм рт.ст. В предпочтительном варианте вторым пентаэритритдифосфитом является бис(2,4-дикумилфенил)пентаэритритдифосфит.
Другие способы очистки второй реакционной смеси включают фракционную кристаллизацию в растворителе и фракционную кристаллизацию расплава. При использовании растворителя для очистки реакционной смеси второй реакции переэтерификации для фракционной кристаллизации используют тот же растворитель, что и для разбавления реакционной смеси. Пригодные растворители включают ароматические, алифатические и циклические углеводороды, содержащие от 6 до 24 атомов углерода. Пригодные растворители включают нормальные или циклические алканы. Предпочтительным растворителем является насыщенный углеводород или смесь насыщенных углеводородов, которые выбирают из группы, включающей (С6-С24)н-алканы и циклоалканы. Примеры пригодных углеводородов включают н-декан, н-додекан, н-тридекан, н-гексадекан и т.п., и циклические и полициклические аналоги, такие как циклододекан, бицикло[4,4,0]декан (декагидронафталин) и т.п. В большинстве случаев растворителем является смесь растворителей, которая включает низшие алканы, например гексан и циклогексан. В настоящем изобретении используют также ненасыщенные растворители, например бензол, толуол и т.п. При использовании в составе реакционной смеси растворителей их используют в количестве от приблизительно 10 мас.% до приблизительно 200 мас.% в расчете на массу полученного пентаэритритдифосфита.
Ниже описан лучший способ воплощения настоящего изобретения для его иллюстрации. Примеры приведены для иллюстрации настоящего изобретения и не ограничивают его сущность и объем, как определено в пунктах формулы настоящего изобретения.
Пример. Получение бис-1,4-дикумилпентаэритритдифосфита
Реакцию переэтерификации монопентаэритрита и трифенилфосфита (ТФФ) проводят с использованием стехометрических количеств ТФФ и пентаэритрита в растворителе в присутствии щелочного катализатора при температуре от 70°С до не более 125°С, предпочтительно от 105°С до 120°С, при атмосферном давлении. Фенол, образующийся в процессе реакции, удаляют перегонкой в вакууме при температуре от 100°С до 300°С и давлении от 0,01 до 100 мм рт.ст., при этом выход превращения составляет более 95% от теоретически рассчитаного количества, а в реакционной смеси остается менее 5%. Непрореагировавшие материалы остаются в промежуточном продукте на уровне менее 1%, предпочтительно менее 0,1%. При этом получают фенольный побочный продукт высокого качества, который можно использовать в качестве исходного материала в других реакциях. Неожиданно было установлено, что в указанных условиях получают спироизомер ДФПЭДФ в преимущественном количестве по сравнению с мостиковым изомером, и выход ДФПЭДФ составляет более 95% в расчете на ТФФ. Растворитель не является определяющим фактором при выборе реагентов и предназначен в основном для снижения вязкости и вследствие этого является необязательным. Пригодные растворители включают различные ароматические углеводородные растворители, содержащие от 6 до 20 атомов углерода. Загрузка щелочного катализатора составляет 0,01-5 мас.% в расчете на образующийся ДФПЭДФ. Растворитель (если используется) добавляют в реакционную смесь в количестве от 10 до 200 мас.% в расчете на образующийся ДФПЭДФ. При использовании схемы реакции и рабочих условий реакции получают неочищенный продукт, содержащий ДФПЭДФ, в котором содержание спироизомера составляет более 90%, при этом продукт содержит также растворитель (если используется) и следовые количества ТФФ, фенола и мостикового изомера ДФПЭДФ.
Высоко очищенный спироизомер ДФПЭДФ является стабильным и его хранят в расплавленном или твердом виде или продают в качестве промежуточного продукта. Перегнанный ТФФ, следовые количества фенола и/или растворителя повторно используют для получения ДФПЭДФ. Следующая стадия заключается в переэтерификации обогащенного спироизомера ДФПЭДФ в присутствии 2,4-дикумилфенола с образованием обогащенного спироизомера бис-2,4-дикумилпентаэритритдифосфита.
ДФПЭДФ с высоким содержанием спироизомера, полученный на предыдущей стадии, добавляют в реакционную смесь, содержащую щелочной катализатор и 2,4-дикумилфенол при температуре приблизительно 150°С. Содержание щелочного катализатора составляет 0,1-5 мас.% в расчете на массу образующегося бис-2,4-дикумилпентаэритритдифосфита. Реагенты добавляют в количествах от стехиометрических (2 моль 2,4-дикумилфенола и 1 моль дифенилпентаэритритдифосфита) до больших, чем стехиометрические, то есть избытков (300% или более для снижения вязкости) 2,4-дикумилфенола. Фенол, образующийся в реакции переэтерификации, перегоняют в вакууме при 0,01-100 мм рт.ст., при этом в смеси остаются следовые количества фенола. В результате реакции получают бис-2,4-дикумилпентаэритритдифосфит, в котором содержание спироизомера составляет более 90%, а выход фосфита (в расчете на ДФПЭДФ) составляет более 95%. При этом получают фенольный побочный продукт высокого качества, который можно использовать в качестве исходного материала в других реакциях.
Реакционную массу очищают тонкослойной перегонкой при 150-300°С и давлении 0,01-50 мм рт.ст., при этом удаляют избыточное количество 2,4-дикумилфенола до уровня менее 0,5%. Полученные продукты содержат более 90% спироизомера бис-2,4-дикумилфенилпентаэритритдифосфита, который затем перерабатывают в пастилки, лепешки или хлопья, и т.п., придавая ему требуемую форму продукта. Перегнанный 2,4-дикумилфенол и следовые количества фенола повторно используют в следующих реакциях. При использовании условий реакции, описанных выше, конечный дифосфит можно использовать без дополнительной очистки перекристаллизацией.
Пентаэритритдифосфиты с высоким содержанием спироизомера, полученные по способам согласно настоящему изобретению, используют для стабилизации полимеров, известных в данной области техники, таких как полиолефины, сложные полиэфиры, полиуретаны, полиалкилентерефталаты, полисульфоны, полиимиды, полифенилен(простые эфиры), полимеры на основе стирола, поликарбонаты, акриловые полимеры, полиамиды, полиацетали, галогенсодержащие полимеры и гомополимеры и сополимеры на основе полиолефинов. Используют также смеси различных полимеров, такие как смеси полифениленовый простой эфир/стирольные смолы, поливинилхлорид/АБС или смеси других модифицированных полимеров, таких как метакрилонитрил, содержащий АБС, полиэфир/АБС или сложный полиэфир плюс другой модификатор. Такие полимеры выпускаются в виде коммерческих препаратов или их получают по методикам, известным в данной области техники. Однако дифосфиты по настоящему изобретению прежде всего используют в термопластичных полимерах, таких как полиолефины, поликарбонаты, сложные полиэфиры и полифениленовые простые эфиры в составе термопластичных полимеров, таких как полиолефины, поликарбонаты, сложные полиэфиры, полифениленовые простые эфиры и полимеры на основе стирола, причем дифосфиты добавляют вследствие чрезвычайно высоких температур, при которых обрабатывают термопластичные полимеры и/или используют.
Используют также полимеры на основе моноолефинов и диолефинов, например, включающие полипропилен, полиизобутилен, полибутен-1, полиметилпентен-1, полиизопрен или полибутадиен, а также на основе циклоолефинов, например, циклопентен или норборнен, полиэтилен (который необязательно может быть сшитым), например полиэтилен высокой плотности (ПЭВП), полиэтилен низкой плотности (ПЭНП) и линейный полиэтилен низкой плотности (ЛПЭНП). Используют также смеси таких полимеров, например смеси полипропилена с полиизобутиленом, полипропилена с полиэтиленом (например, ПП/ПЭВП). Используют также сополимеры моноолефинов и диолефинов друг с другом или с другими виниловыми мономерами, такими как, например, этилен/пропилен, ЛПЭНП и его смеси с ПЭНП, пропилен/бутен-1, этилен/гексен, этилен/этилпентен, этилен/гептен, этилен/октен, пропилен/бутадиен, изобутилен/изопрен, этилен/алкилакрилаты, этилен/алкилметакрилаты, этилен/винилацетат(ЭВА) или сополимеры этилен/акриловая кислота (ЭАК) или их соли (иономеры) и терполимеры этилена с пропиленом и диеном, таким как гексадиен, дициклопентадиен или этилиденнорборнен, а также смеси указанных сополимеров и их смеси с указанными выше полимерами, например полипропилен/сополимеры этилена-пропилена, ПЭНП/ЭВА, ПЭНП/ЭАК, ЛПЭНП/ЭВА и ЛПЭНП/ЭАК.
Термопластичные полимеры включают также стирольные полимеры, такие как полистирол, поли(пара-метилстирол), поли(α-метилстирол), сополимеры стирола, пара-метилстирола или α-метилстирола с производными диенов или акриловыми производными, такими как, например, стирол/бутадиен, стирол/акрилонитрил, стирол/акрилметакрилат, стирол/малеиновый ангидрид, стирол/бутадиен/этилакрилат, стирол/акрилонитрил/метакрилат; смеси с высокой ударной вязкостью, содержащие сополимеры стирола и другой полимер, такие как, например, смеси полиакрилата, диенового полимера или терполимера этилен/пропилен/диен, и блоксополимеры стирола, такие как, например, стирол/бутадиен/стирол, стирол/изопрен/стирол, стирол/этилен/бутилен/ стирол или стирол/этилен/пропилен/стирол. Дополнительно или в другом варианте стирольные полимеры включают привитые сополимеры стирола или α-метилстирола, такие как, например, стирол на полибутадиене, стирол на сополимере полибутадиена-стирола или полибутадиена-акрилонитрила, стирол и акрилонитрил (или метакрилонитрил) на полибутадиене; стирол и малеиновый анигидрид или имид малеиновой кислоты на полибутадиене; стирол, акрилонитрил и малеиновый ангидрид или имид малеиновой кислоты на полибутадиене; стирол, акрилонитрил и метилметакрилат на полибутадиене, стирол и алкилакрилаты или метакрилаты на полибутадиене, стирол и акрилонитрил на этилен/пропилен/диеновом терполимере, стирол и акрилонитрил на полиакрилатах или полиметакрилатах, стирол и акрилонитрил на сополимерах акрилата/бутадиена, а также смеси стирольных сополимеров, описанных выше.
Используют также полимеры на основе нитрила. Такие полимеры включают гомоплимеры и сополимеры акрилонитрила и его аналогов, такие как метакрилонитрил, такой как полиакрилонитрил, полимеры акрилонитрила/бутадиена, полимеры акрилонитрила/алкилакрилата, полимеры акрилонитрила/алкилметакрилата/бутадиена, сополимер акрилонитрила/бутадиена/стирола (АБС) и АБС, содержащий метакрилонитрил.
Используют также полимеры на основе акриловых кислот, таких как акриловая кислота, метакриловая кислота, метилметакриловая кислота и этакриловая кислота и их сложные эфиры. Такие полимеры включают полиметилметакрилат и привитые сополимеры типа АБС, в которых все или часть мономеров акрилонитрильного типа замещены эфиром акриловой кислоты или амидом акриловой кислоты. Используют также полимеры, включающие другие мономеры акрилового типа, такие как акролеин, метакролеин, акриламид и метакриламид.
Используют также галогенсодержащие полимеры. Такие полимеры включают смолы, такие как полихлоропрен, гомополимеры и сополимеры эпихлоргидрина, поливинилхлорид, поливинилбромид, поливинилфторид, поливинилиденхлорид, хлорированный полиэтилен, хлорированный полипропилен, фторированный поливинилиден, бромированный полиэтилен, хлорированный каучук, сополимер винилхлорида-винилацетата, сополимер винилхлорида-этилена, сополимер винилхлорида и пропилена, сополимер винилхлорида и стирола, сополимер винилхлорида и изобутилена, сополимер винилхлорида и винилидена, терполимер винилхлорид-стирол-малеиновый ангидрид, сополимер винилхлорид-стирол-акрилонитрил, сополимер винилхлорид-изопрен, сополимер винилхлорид-хлорированный пропилен, терполимер винилхлорид-винилиденхлорид-винилацетат, сополимеры винилхлорид-эфиры акриловой кислоты, сополимеры винилхлорид-эфиры малеиновой кислоты, сополимеры винилхлорид-эфир метакриловой кислоты, сополимер винилхлорид-акрилонитрил и внутренне пластифицированный поливинилхлорид.
Другие пригодные термолпастичные полимеры включают гомополимеры и сополимеры циклических простых эфиров, таких как полиалкиленгликоли, полиэтиленоксид, полипропиленоксид или их сополимеры с бис-глицидиловыми эфирами; полиацетали, такие как полиоксиметилен и полиоксиметилен, содержащий в качестве сомономера этиленоксид; полиацетали, модифицированные термопластичными полиуретанами, акрилаты или метакрилонитрил, содержащий АБС; полифениленоксиды и сульфиды, и смеси полифениленоксидов с полистиролом и полиамидами; поликарбонаты и полиэфиркарбонаты; полисульфоны, поли(простой эфир)сульфоны и поли(простой эфир)кетоны, а также полиэфирдикарбоновых кислот и диодов и/или оксикарбоновых кислот или соответствующих лактонов, такие как полиэтилентерефталат, полибутилентерефталат, поли-1,4-диметилолциклогексантерефталат, поли-[2,2,4-(4-гидроксифенил)пропан]терефталат и полигидроксибензоаты, а также блоксополимеры простых и сложных эфиров на основе полиэфиров, содержащих гидроксильные концевые группы.
Используют также полиамиды и сополиамиды на основе диаминов и дикарбоновых кислот и/или аминокарбоновых кислот или соответствующих лактамов, такие как полиамид-4, полиамид-6, полиамид-6/6, полиамид-6/10, полиамид-6/9, полиамид-6/12, полиамид-4/6, полиамид-11, полиамид-12, ароматические полиамиды, полученные при конденсации мета-ксилола, диамина и адипиновой кислоты, полиамиды, полученные из гексаметилендиамина и изофталевой и/или терефталевой кислоты и необязательно эластомера в качестве модификатора, например поли-2,4,4-триметилгексаметилентерефталамид или поли-мета-фениленизофталамид. Используют также сополимеры указанных выше полиамидов с полиолефинами, сополимеры олефинов, иономеров или химичеки связанных или привитых эластомеров, или с простыми полиэфирами, такими как, например, полиэтиленгликоль, полипропиленгликоль или политетраметиленгликоль, и полиамиды или сополиамиды, модифицированные каучуком на основе сополимера этилена, пропилена и диенового мономера, или АБС.
Полученные стабилизированные полимерные композиции, включающие фосфиты, полученные согласно способу по настоящему изобретению, необязательно содержат различные стандартные добавки, такие как, например:
(1) Антиоксиданты
(1.1) Алкилированные монофенолы, например 2,6-ди-трет-бутил-4-метилфенол, 2-трет-бутил-4,6-диметилфенол, 2,6-ди-трет-бутил-4-этилфенол, 2,6-ди-трет-бутил-4-н-бутилфенол, 2,6-ди-трет-бутил-4-бутилфенол, 2,6-дициклопентил-4-метилфенол, 2-(α-метилциклогексил)-4,6-диметилфенол, 2,6-диоктадецил-4-метилфенол, 2,4,6-трициклогексилфенол и 2,6-ди-трет-бутил-4-метоксиметилфенол.
(1.2) Алкилированные гидрохиноны, например 2,6-ди-трет-бутил-4-метоксифенол, 2,5-ди-трет-бутилгидрохинон, 2,5-ди-трет-амилгидрохинон и 2,6-дифенил-4-октадецилоксифенол.
(1.3) Гидроксилированные тиодифенильные простые эфиры, например 2,2′-тио-бис-(6-трет-бутил-4-метилфенол), 2,2′-тио-бис-(4-октилфенол), 4,4′-тио-бис-(6-трет-бутил-3-метилфенол) и 4,4′ -тио-бис-(6-трет-бутил-2-метилфенол).
(1.4) Алкилиденбисфенолы, например 2,2′-метилен-бис-(6-трет-бутил-4-метилфенол), 2,2′-метилен-бис-(6-трет-бутил-4-этилфенол), 2,2′-метилен-бис-[4-метил-6-(α-метилциклогексил)фенол], 2,2′-метилен-бис-(4-метил-6-циклогексилфенол), 2,2′ -метилен-бис-(6-нонил-4-метилфенол), 2,2′-метилен-бис-[6-(α-метилбензил)-4-нонилфенол], 2,2′-метилен-бис-[6-(α,α-диметилбензил)-4-нонилфенол], 2,2′-метилен-бис-(4,6-ди-трет-бутилфенол),4,4′-метилен-бис-(б-трет-бутил-2-метилфенол), 1,1-бис-(5-трет-бутил-4-гидрокси-2-метилфенил)бутан, 2,6-ди-(3-трет-бутил-5-метил-2-гидроксибензил)-4-метилфенол, 1,1,3-трис-(5-трет-бутил-4-гидрокси-2-метилфенил)бутан, 1,1-бис-(5-трет-бутил-4-гидрокси-2-метилфенил)-3-додецилмеркаптобутан, этиленгликоль-бис-[3,3-бис-(3′-трет-бутил-4′-гидроксифенил)бутират], ди-(3-трет-бутил-4-гидрокси-5-метилфенил)дициклопентадиен и ди-[2-(3′-трет-бутил-2′-гидрокси-5′-метилбензил)-6-трет-бутил-4-метилфенил]терефталат.
(1.5) Бензилсодержащие соединения, например 1,3,5-трис-(3,5-ди-трет-бутил-4-гидроксибензил)-2,4,6-триметилбензол, бис(3,5-ди-трет-бутил-4-гидроксибензил)сульфид, изооктил-3,5-ди-трет-бутил-4-гидроксибензилмеркаптоацетат, бис-(4-трет-бутил-3-гидрокси-2,6-диметилбензил)дитиотерефталат, 1,3,5-трис-(3,5-ди-трет-бутил-4-гидроксибензил)изоцианурат, 1,3,5-трис-(4-трет-бутил-3-гидрокси-2,6-диметилбензил)изоцианурат, диоктадецил-3,5-ди-трет-бутил-4-гидроксибензилфосфонат, кальциевая соль моноэтилового эфира 3,5-ди-трет-бутил-4-гидроксибензилфосфоновой кислоты и 1,3,5-трис-1,3,5-дициклогексил-4-гидроксибензил)изоцианурат.
(1.6) Ациламинофенолы, например анилид 4-гидроксилауриновой кислоты, анилид 4-гидроксистеариновой кислоты, 2,4-бис-октилмеркапто-6-(3,5-трет-бутил-4-гидроксианилино)-s-триазин и октил-N-(3,5-ди-трет-бутил-4-гидроксифенил)карбамат.
(1.7) Сложные эфиры α-(3,5-ди-трет-бутил-4-гидроксифенил)пропионовой кислоты и моно- или полиатомных спиртов, например, таких как метанол, диэтиленгликоль, октадеканол, триэтиленгликоль, 1,6-гександиол, пентаэритрит, неопентилгликоль, трис-гидроксиэтилизоцианурат, тиодиэтиленгликоль и диамид дигидроксиэтилщавелевой кислоты.
(1.8) Сложные эфиры α-(5-трет-бутил-4-гидрокси-3-метилфенил)пропионовой кислоты и моно- и полиатомных спиртов, например, таких как метанол, диэтиленгликоль, октадеканол, триэтиленгликоль, 1,6-гександиол, пентаэритрит, неопентилгликоль, трис-гидроксиэтилизоцианурат, тиодиэтиленгликоль и диамид дигидроксиэтилщавелевой кислоты.
(1.9) Сложные эфиры β-(5-трет-бутил-4-гидрокси-3-метилфенил)пропионовой кислоты и моно- и полиатомных спиртов, например, таких как метанол, диэтиленгликоль, октадеканол, триэтиленгликоль, 1,6-гександиол, пентаэритрит, неопентилгликоль, трис-гидроксиэтилизоцианурат, тиодиэтиленгликоль и диамид N,N′-бис(гидроксиэтил)щавелевой кислоты.
(1.10) Амиды β-(3,5-ди-трет-бутил-4-гидроксифенил)пропионовой кислоты, например N,N′-ди-(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гексаметилендиамин, N,N′-ди-(3,5-ди-трет-бутил-4-гидроксифенилпропионил)триметилендиамин и N,N′-ди-(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гидразин.
(2) Поглотители УФ-излучения и светостабилизаторы
(2.1) 2-(2′-Гидроксифенил)бензотриазолы, например 5′-метил-,3′,5′-ди-трет-бутил-, 5′-трет-бутил-, 5′-(1,1,3,3-тетраметилбутил)-, 5-хлор-3′,5′-ди-трет-бутил-, 5-хлор-3′-трет-бутил-5′-метил-, 3′-втор-бутил-5′-трет-бутил-, 4′-октокси, 3′,5′-ди-трет-амил- и 3′,5′-бис-(α,α-диметилбензил)производные.
(2.2) Гидроксибензофеноны, например 4-гидрокси-, 4-метокси-, 4-октокси-, 4-децилокси-, 4-додецилокси-, 4-бензилокси-, 4,2′,4′-тригидрокси-и 2′-гидрокси-4,4′-диметоксипроизводные.
(2.3) Сложные эфиры замещенных и незамещенных бензойных кислот, например фениловый эфир салициловой кислоты, 4-трет-бутилфениловый эфир салициловой кислоты, октилфениловый эфир салициловой кислоты, дибензоилрезорцинол, бис-(4-трет-бутилбензоил)резорцинол, бензоилрезорцинол, 2,4-ди-трет-бутилфенил-3,5-ди-трет-бутил-4-гидроксибензоат и гексадецил-3,5-ди-трет-бутил-4-гидроксибензоат.
(2.4) Акрилаты, напимер, этиловый или изооктиловый эфир α-циано-β,β-дифенилакриловой кислоты, метиловый эфир α-карбометоксикоричной кислоты, метиловый или бутиловый эфир α-циано-β-метил-пара-карбометоксикоричной кислоты, метиловый эфир α-карбометокси-пара-метоксикоричной кислоты и N-(β-карбометокси-β-циановинил)-2-метилиндолин.
(2.5) Соединения никеля, например комплексы никеля и 2,2′-тио-бис-[4-(1,1,3,3-тетраметилбутил)фенола], такие как комплекс 1:1 или 1:2, необязательно с дополнительными лигандами, такими как н-бутиламин, триэтаноламин или N-циклогексил-диэтаноламин, дибутилдитиокарбамат никеля, никелевые соли моноалкиловых эфиров 4-гидрокси-3,5-ди-трет-бутилбензилфосфоновой кислоты, такие как метиловый, этиловый или бутиловый эфиры, комплексы никеля и кетоксимов, такие как 2-гидрокси-4-метилпентилундецилкетоксим, и комплексы никеля и 1-фенил-4-лауроил-5-гидроксипиразола, необязательно с дополнительными лигандами.
(2.6) Стерически заторможенные амины, например бис-(2,2,6,6-тетраметилпиперидил)себакат, бис-(1,2,2,6,6-пентаметилпиперидил)себакат, н-бутил-3,5-ди-трет-бутил-4-гидроксибензилмалоновая кислота, бис-(1,2,2,6,6-пентаметилпиперидил)сложный эфир, продукт конденсации 1-гидроксиэтил-2,2,6,6-тетраметил-4-гидроксипиперидина и янтарной кислоты, продукт конденсации N,N′-(2,2,6,6-тетраметилпиперидил)-гексаметилендиамина и 4-трет-октиламино-2,6-дихлор-1,3,5-s-триазина, трис-(2,2,6,6-тетраметилпиперидил)нитрилотриацетат, тетракис-(2,2,6,6-тетраметил-4-пиперидил)-1,2,3,4-бутантетраугольная кислота, 1,1′-(1,2-этандиил)-бис-(3,3,5,5-тетраметилпиперазинон). Такие амины включают гидроксиламины, полученные из заторможенных аминов, таких как ди(1-гидрокси-2,2,6,6-тетраметилпиперидин-4-ил)себацат, 1-гидрокси-2,2,6,6-тетраметил-4-бензоксипиперидин,1-гидрокси-2,2,6,6-тетраметил-4-(3,5-ди-трет-бутил-4-гидроксигидроциннамоилокси)пиперидин и N-(1-гидрокси-2,2,6,6-тетраметилпиперидин-4-ил)-ε-капролактам.
(2.7) Диамиды щавелевой кислоты, например 4,4′-диоктилоксиоксанилид, 2,2′-диоктилокси-5,5-ди-трет-бутилоксанилид, 2,2′-дидодецилокси-5,5′-ди-трет-бутилоксанилид, 2-этокси-2′-этилоксанилид, N,N′-бис(3-диметиламинопропил)оксанилид, 2-этокси-5-трет-бутил-2′-этилоксанилид и их смеси с 2-этокси-2′-этил-5,4′-ди-трет-бутилоксанилидом и смеси орто-метокси- и пара-метокси-, а также орто-этокси- и пара-этоксидизамещенных оксанилидов.
(3) Дезактиваторы металлов, например диамид N,N′-дифенилщавелевой кислоты, N-салицилаль-N′-салицилоилгидразин, N,N′-бис-салицилоилгидразин, N,N′-бис-(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гидразин, салицилоиламино-1,2,4-триазол, дигидразид бис-бензилиденщавелевой кислоты.
(4) Фосфиты и фосфониты, отличающиеся от аналогичных по настоящему изобретению, например, трифенилфосфит, дифенилалкилфосфиты, фенилдиалкилфосфиты, трис(нонилфенил)фосфит, трилаурилфосфит, триоктадецилфосфит, дистеарилпентаэритритдифосфит, трис(2,4-ди-трет-бутилфенил)фосфит, диизодецилпентаэритритдифосфит, бис(2,4-ди-трет-бутилфенил)пентаэритритдифосфит, тристеарилсорбиттрифосфит и тетракис(2,4-ди-трет-бутилфенил)-4,4'-бифенилендифосфонит.
(5) Тушители пероксида водорода, например сложные эфиры β-тиодипропионовой кислоты, например лауриловые, стеариловые, миристиловые или тридециловые сложные эфиры, меркаптобензимидазол или цинковая соль 2-меркаптобензимидазола, цинк-дибутилдитиокарбамат, диоктадецилдисульфид, пентаэритриттетракис(β-додецилмеркапто)пропионат.
(6) Стабилизаторы полиамидов, например соли меди в комбинации с иодидами и/или соединениями фосфора и солями двухвалентного магния.
(7) Основные со-стабилизаторы, например меламин, поливинилпирролидон, дициандиамид, триаллилцианурат, производные мочевины, производные гидразина, амины, полиамиды, полиуретаны, соли щелочных и щелочноземельных металлов высших жирных кислот, например стеарат кальция, стеарат бария, стеарат магния, рицинолеат натрия, пальмитат калия, пирокатехолат сурьмы и пирокатехолат цинка.
(8) Зародышеобразующие агенты, например 4-трет-бутилбензойная кислота, адипиновая кислота, дифенилуксусная кислота.
(9) Наполнители и армирующие наполнители, например карбонат кальция, силикаты, стекловолокно, асбест, тальк, каолин, слюда, сульфат бария, оксиды и гидроксиды металлов, угольная сажа, графит.
(10) Производные аминоксипропаноата, такие как метил-3-[N,N-дибензиламинокси]пропаноат, этил-3-[N,N-дибензиламинокси]пропаноат, 1,6-гексаметилен-бис-[3-(N,N-дибензиламинокси]пропаноат, метил-[2-(метил)-3-(N,N-дибензиламинокси]пропаноат, октадецил-3-[N,N-дибензиламинокси]пропановая кислота, тетракис[(N,N-дибензиламинокси)этилкарбонилоксиметил]метан, октадецил-3-[N,N-дибензиламинокси]пропаноат, калиевая соль 3-[N,N-дибензиламинокси]пропановой кислоты и 1,6-гексаметилен-бис[3-(N-аллил-N-додециламинокси)пропаноат].
(11) Другие добавки, напимер пластификаторы, замасливатели, эмульгаторы, пигменты, оптические осветлители, огнестойкие агенты, антистатики, порообразователи и тиосинергисты, такие как дилаурилтиодипропионат или дистеариотиодипропионат.
В состав полимерной композиции включены фенольные антиоксиданты с заторможенной конформацией. Использование бис(алкилфенил)пентаэритритдифосфитов по настоящему изобретению приводит к повышению защиты полимера от окрашивания за счет присутствия фенолов. Кроме указанных выше, такие фенольные антиоксиданты включают:
н-октадецил-3,5-ди-трет-бутил-4-гидроксигидроциннамат, неопентантераил-тетракис-(3,5-ди-трет-бутил-4-гидроксилгидроциннамат), ди-н-октадецил-3,5-ди-трет-бутил-4-гидроксибензилфосфонат, 1,3,5-трис(3,5-ди-трет-бутил-4-гидроксибензил)изоцианурат, тиодиэтилен-бис(3,5-ди-трет-бутил-4-гидроксигидроциннамат), 1,3,5-триметил-2,4,6-трис(3,5-ди-трет-бутил-4-гидроксибензил)бензол, 3,6-диоксаоктаметилен-бис(3-метил-5-трет-бутил-4-гидроксигидроциннамат), 2,6-ди-трет-бутил-пара-крезол, 2,2'-этилиден-бис(4,6-ди-трет-бутилфенол), 1,3,5-трис(2,6-диметил-4-трет-бутил-3-гидроксибензил)изоцианурат, 1,1,3-трис(2-метил-4-гидрокси-5-трет-бутилфенил)бутан, 1,3,5-трис[2-(3,5-ди-трет-бутил-4-гидроксигидроциннаинолокси)этил]изоцианурат, 3,5-ди(3,5-ди-трет-бутил-4-гидроксибензил)мезитол, гексаметилен-бис(3,5-ди-трет-бутил-4-гидроксигидроциннамат), 1-(3,5-ди-трет-бутил-4-гидроксианилино)-3,5-ди(октилтио)-s-триазин, N,N′-гексаметилен-бис(3,5-ди-трет-бутил-4-гидроксигидроциннамамид), бис(этил-3,5-ди-трет-бутил-4-гидроксибензилфосфонат) кальция, этилен-бис[3,3-ди(3-трет-бутил-4-гидроксифенил)бутират], октиловый эфир 3,5-ди-трет-бутил-4-гидроксибензилмеркаптоуксусной кислоты, бис(3,5-ди-трет-бутил-4-гидроксициннамоил)гидразид, N,N′-бис-[2-(3,5-ди-трет-бутил-4-гидроксигидроксоциннамоилокси)этил]оксамид, неопентантетраил-тетракис(3,5-ди-трет-бутил-4-гидроксигидроциннамат), н-октадецил-3,5-ди-трет-бутил-4-гидроксигидроциннамат, 1,3,5-триметил-2,4,6-трис(3,5-ди-трет-бутил-4-гидроксибензил)бензол, 1,3,5-трис(3,5-ди-трет-бутил-4-гидроксибензил)изоцианурат, 2,6-ди-трет-бутил-пара-крезол или 2,2′ -этилиден-бис(4,6-ди-трет-бутилфенол).
(12) Лактоны, например 5,7-ди-трет-бутил-3-фенил-3Н-бензофуран-2-он, 5,7-дикумил-3-фенил-3Н-бензофуран-2-он, нонил-ε-фенил-3Н-бензофуран-2-он, динонил-3-фенил-3Н-бензофуран-2-он, 5-трет-бутил-3-фенил-3Н-бензофуран-2-он, 5-кумил-3-фенил-3Н-бензофуран-2-он, октил-3-фенил-3Н-бензофуран-2-он и другие 3-арилбензофуран-2-оны.
Дополнительно или необязательно присутствуют другие добавки, такие как оксазафосфолидины. Аналогичным образом настоящие соединения препятствуют окрашиванию в присутствии аминных светостабилизаторов с заторможенной конформацией, причем такие заторможенные амины включают бис(1,2,2,6,6-пентаметил-4-пиперидил)-2-н-бутил-2-(3,5-ди-трет-бутил-4-гидроксибензил)малонат, бис(2,2,6,6-тетраметил-4-пиперидил)себакат, сополимер диметилсукцината и 4-гидрокси-2,2,6,6-тетраметил-1-пиперидинэтанола и сополимеры 2,4-дихлор-6-октиламино-s-триазина и N′-(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамина.
В настоящем изобретении описаны примеры предпочтительных и альтернативных вариантов осуществления настоящего изобретения. Специалистам в данной области техники представляется очевидным, что возможны определенные изменения и модификации изобретения, не выходя за пределы объема изобретения, который определен в прилагаемой формуле изобретения.
В настоящем изобретении описан способ получения пентаэритритдифосфитов с высоким содержанием спироизомера. Пентаэритритдифосфиты получают методом последовательной переэтерификации пентаэритрита в присутствии монофосфита, а затем - замещенного фенола или другого спирта, причем указанные реакции переэтерификации проводят в условиях контролируемых температуры и давления. Технический результат - условия реакции позволяют получить промежуточное производное и конечные пентаэритритдифосфиты с высоким содержанием спироизомера и высоким общим выходом дифосфитов. 25 з.п. ф-лы.
с монофосфитом с образованием смеси продуктов, содержащей промежуточный пентаэритритдифосфита в форме спироизомера формулы (III)

и в форме мостикового изомера формулы (IV)

непрореагировавший монофосфит и побочные продукты реакции,
где R1 выбирают из группы, включающей линейные или разветвленные (С1-С20)алкильные группы, (С5-С7)циклоалифатические группы и их (C6-С11)замещенные производные, линейные или разветвленные (С2-С30)алкенильные группы, (С7-С40)алкиларильные группы и (С7-С40)арилалкильные группы и смеси указанных соединений;
затем осуществляют удаление побочных продуктов из полученной смеси продуктов, и осуществляют переэтерификацию указанного промежуточного пентаэритритдифосфита в присутствии спирта, причем спирт выбирают из группы, включающей С8-С22алканолы, С8-С22алкенолы, фенолы и С7-С40арилспирты, с образованием смеси конечных продуктов, которая содержит конечный пентаэритритдифосфит формулы (VI)

где R2 выбирают из группы, включающей (С8-С20)алкильные группы, (С8-С22)алкенильные группы, фенил, (С7-С40)алкиларильные группы и (С7-С40)арилалкильные группы.

указанным промежуточным пентаэритритдифосфитом является дифенилпентаэритритдифосфит формулы (V)

указанным спиртом является 2,4-дикумилфенол формулы (VII)

а указанным конечным пентаэритритдифосфитом является бис(2,4-дикумилфенил)пентаэритритдифосфит формулы (VIII)
| US 5438086 A, 01.08.1995 | |||
| ЦИКЛИЧЕСКИЕ ФОСФОРСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И СПОСОБ НЕПРЕРЫВНОГО ПОЛУЧЕНИЯ γ-АМИНО-1-ГИДРОКСИАЛКИЛИДЕН-1,1-БИСФОСФОНОВЫХ КИСЛОТ | 1994 |
|
RU2154647C2 |
Авторы
Даты
2008-02-10—Публикация
2004-11-23—Подача