Изобретение относится к новому биологически активному веществу ряда пирроло[3,4-с]пиразола, а именно к 1,4,5,6-тетрагидро-6-оксо-5-(2-гиперазиноэтил)-4-фенил-3-(4-хлорфенил)пирроло[3,4-с]пиразола дигидрохлориду формулы:
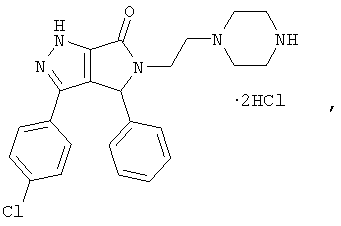
обладающему гипотензивной и антикоагулянтной активностью, что позволяет предполагать возможность использования его в медицине в качестве препарата, эффективно снижающего артериальное давление и свертываемость крови и тем самым оказывающего лечебное действие и предотвращающего развитие различных осложнений при гипертонической болезни.
Ближайшим структурным аналогом заявляемого соединения является 5-(2-аминоэтил)-1,4,5,6-тетрагидро-3-метил-6-оксо-4-фенилпирроло[3,4-с]пиразола гидрохлорид (Касимова Н.Н. Синтез, свойства и биологическая активность 1-аминоалкил- и 1-диалкиламиноалкил-4-ацил-5-арил-3-гидрокси-3-пирролин-2-онов: Дисс. ... канд. фармацевт. наук / Перм. гос. фармацевт. акад. - Пермь, 2002. - с.119) формулы:
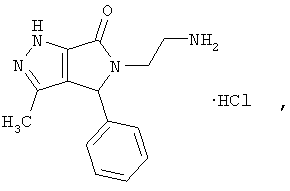
который взят за прототип и не обладает гипотензивным и антикоагулянтным действием.
Эталонами сравнения являются гепарин (Машковский М.Д. Лекарственные средства: Практ. пособие. - 15 изд. - М.: «Новая волна», 2005. - с.475), который применяется в медицинской практике и является аналогом по антикоагулянтному действию, и папаверин (там же, с.412) формулы:
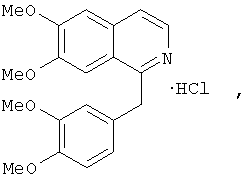
который применяется в медицинской практике и является аналогом по гипотензивному действию.
Сущность изобретения - поиск в ряду пирроло[3,4-с]пиразолов соединения с выраженной гипотензивной и антикоагулянтной активностью, снижающего артериальное давление и свертываемость крови. Это достигается синтезом 1,4,5,6-тетрагидро-6-оксо-5-(2-пиперазиноэтил)-4-фенил-3-(4-хлорфенил)пирроло[3,4-с]пиразола дигидрохлорида, обладающего гипотензивным и антикоагулянтным действием.
Заявляемое соединение получают взаимодействием 1-(2-пиперазиноэтил)-5-фенил-4-(4-хлорбензоил)-3-гидрокси-3-пирролин-2-она дигидрохлорида с гидразин гидратом по схеме:
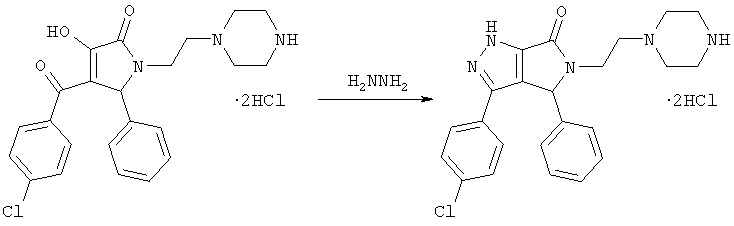
Пример получения заявляемого соединения.
Пример
1,4,5,6-Тетрагидро-6-оксо-5-(2-пиперазиноэтил)-4-фенил-3-(4-хлорфенил)пирроло[3,4-с]пиразола дигидрохдорид.
К раствору 4.99 г (0.01 М) 1-(2-пиперазиноэтил)-5-фенил-4-(4-хлорбензоил)-3-гидрокси-3-пирролин-2-она дигидрохлорида в 5 мл ледяной уксусной кислоты добавляют 0.54 мл (0.011 М) 98%-го гидразин гидрата и кипятят в течение 1.5 ч. После охлаждения реакционную смесь выпаривают, остаток перекристаллизовывают из этанола. Выход 1.63 г (33%). Т.пл.: >310°С. Найдено, %: С 55.79; Н 5.25; N 14.11. С23Н26Cl3N5O. Вычислено, %: С 55.82; Н 5.30; N 14.15.
Заявляемое соединение представляет собой бесцветное кристаллическое вещество, растворимое в воде, этаноле, диметилформамиде, диметилсульфоксиде.
ИК спектр (SPECORD, вазелиновое масло, ν, см-1): 1703 (CON), 3100 (NH), 3400 (N+H, N+H2).
ПМР спектр (MERCURY 300, 300.055 МГц, DMSO-D6, GMDS, δ, м.д.): 2.75 (1Н, m, C(1)HAHB), 3.32 (10H, m, N(CH2)5), 3.95 (1H, m, C(1)HAHB), 6.07 (1H, s, С(4)H), 7.32 (7H, Hаром), 7.43 (2Н, Нпром), 9.56 (2Н, b.s, N+H2), 14.13 (1H, b.s, NH).
Заявляемое соединение и аналог по структуре испытывали на гипотензивную активность. Эксперименты проведены на наркотизированных мединалом (400 мг/кг, внутрибрюшинно) кошках. Вещества испытывали в одинаковой дозе 5 мг/кг, вводили растворенными в 3 мл изотонического раствора хлорида натрия в бедренную вену в течение 2 мин. Артериальное давление измеряли в сонной артерии прямым способом с помощью ртутного манометра, фиксируя уровень давления на ленте кимографа через определенные промежутки времени. В качестве эталона сравнения использовали известное гипотензивное лекарственное средство папаверина гидрохлорид, который испытывали в дозе 3 мг/кг (1/10 ЛД50). Результаты обрабатывали с использованием коэффициента Стъюдента (Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии, М., 2000, с.312-313).
Гипотензивная активность соединения МС-13 в дозе 5 мг/кг
Как видно из табл.1, заявляемое соединение оказывает выраженное гипотензивное действие, снижая артериальное давление с 5 мин после введения (р<0.01), при этом гипотензивный эффект сохраняется на протяжении всего времени наблюдения (более 6 часов). Максимальное снижение давления наблюдается через 5-15 мин после введения и составляет 41.5-38.8%.
Аналог по структуре активности не проявил.
Результаты испытания эталона сравнения приведены в табл.2, из которой видно, что под влиянием папаверина гидрохлорида артериальное давление снижается максимально на 34.4% и сохраняется на протяжении только 2 мин.
Гипотензивная активность папаверина гидрохлорида в дозе 3 мг/кг (1/10 ЛД50)
Заявляемое соединение и аналог по структуре исследовали на наличие антикоагулянтной активности. Опыты проведены с помощью коагулометра «Минилаб 701». Для исследования использовали цитратную (3.8%) кровь (9:1) собаки. Влияние соединений на свертываемость крови испытывали в концентрации 1 мг/мл крови. В качестве эталона антикоагулянтной активности использовали раствор гепарина, который испытывали в концентрации 1 ЕД/мл крови. В каждой серии опытов было использовано восемь животных. Степень антикоагулянтной активности соединений определяли по изменению времени свертывания цитратной крови в сравнении с контролем и эталоном. Результаты обрабатывали с использованием коэффициента Стъюдента. (Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии, М., 2000, с.312-313). Результаты испытаний представлены в таблице 3.
Влияние на свертывающую систему крови заявляемого соединения и эталона сравнения
Как видно из табл.3, заявляемое соединение проявляет прямое антикоагулянтное действие, так как достоверно увеличивает время свертывания цитратной крови на 30.4%. Его структурный аналог достоверным антикоагулянтным эффектом не обладает. Эталон сравнения гепарин замедляет свертывание на 22.4%.
Таким образом, заявляемое соединение проявляет 2 вида активности - гипотензивную и прямую антикоагулянтную. Такое сочетание активностей имеет большое практическое значение, т.к. при гипертонической болезни помимо повышения артериального давления обычно наблюдается повышение свертывающей активности крови, что приводит к различным тромбоэмболических осложнениям (инфаркт миокарда, ишемический инсульт).
Острую токсичность заявляемого соединения определяли на беспородных белых мышах обоего пола массой 16-18 г. Соединение вводили внутрибрюшинно и внутривенно в виде водного раствора из расчета 0.1 мл на 10 г массы животного в возрастающих дозах. Результаты обрабатывали по Прозоровскому с вычислением средней смертельной дозы ЛД50 при Р=0.05 (Прозоровский, В.Б. Экспресс-метод определения средней эффективной дозы и ее ошибки / В.Б.Прозоровский, М.П.Прозоровская, В.М.Демченко // Фармакол. и токсикол. - 1978. - Т.41, №4. - с.497-502).
Установлено, что острая токсичность (ЛД50) заявляемого соединения при внутрибрюшинном введении составляет 1460.0 (610.4-2734.4) мг/кг, а при внутривенном - 467.2 (195.3-875.0) мг/кг.
Работа выполнена при финансовой поддержке РФФИ (проект №04-03-96042).
Источники информации
1. Касимова Н.Н. Синтез, свойства и биологическая активность 1-аминоалкил- и 1-диалкиламиноалкил-4-ацил-5-арил-3-гидрокси-3-пирролин-2-онов: Дисс. ... канд. фармацевт. наук / Перм. гос. фармацевт. акад. - Пермь, 2002. - с.119.
2. Машковский М.Д. Лекарственные средства: Практ. пособие. - 15 изд. - М.: Новая волна, 2005. - с.475.
3. Там же, с.412.
4. Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии, М., 2000, с.312-313.
5. Прозоровский, В.Б. Экспресс-метод определения средней эффективной дозы и ее ошибки / В.Б.Прозоровский, М.П.Прозоровская, В.М.Демченко // Фармакол. и токсикол. - 1978. - Т.41, №4. - с.497-502.
| название | год | авторы | номер документа |
|---|---|---|---|
| 4-АЦЕТИЛ-3-ГИДРОКСИ-1-(2-ГИДРОКСИЭТИЛАМИНОЭТИЛ)-5-ФЕНИЛ-3-ПИРРОЛИН-2-ОН, ПРОЯВЛЯЮЩИЙ АНТИКОАГУЛЯНТНУЮ АКТИВНОСТЬ | 2005 |
|
RU2312660C2 |
| 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)-2-БУТЕНОАТ ТИАЗОЛИНАММОНИЯ, ОБЛАДАЮЩИЙ АНТИКОАГУЛЯНТНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2461550C2 |
| 1-(3,4-ДИЭТОКСИФЕНИЛ)-2,3,5,6-ТЕТРАГИДРО-(3,4-ДИЭТОКСИБЕНЗО)[g]ХИНОКСАЛИНО[2,3-b]ИНДОЛИЗИНА ГИДРОХЛОРИД, ПРОЯВЛЯЮЩИЙ ПРЯМОЕ АНТИКОАГУЛЯНТНОЕ ДЕЙСТВИЕ | 2006 |
|
RU2330850C1 |
| ПРИМЕНЕНИЕ ЗАМЕЩЕННЫХ 2-(2-(4,4,6-ТРИМЕТИЛ-2-ОКСО-4Н-ПИРРОЛО[3,2,1-IJ]ХИНОЛИН-1(2Н)-ИЛИДЕН)ГИДРАЗИНИЛ)ТИАЗОЛ-4(5Н)-ОНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ XA И XIA И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2023 |
|
RU2819271C1 |
| Этил 4-(5-бензоил-6-(4-(диэтиламино)фенил)-4-гидрокси-2-тиоксогексагидропиримидин-4-карбоксамино)бензоат, проявляющий анальгетическое и противовоспалительное действие | 2019 |
|
RU2717246C1 |
| СИГМА-ЛИГАНДЫ ДЛЯ ПРИМЕНЕНИЯ ПРИ ПРОФИЛАКТИКЕ И/ИЛИ ЛЕЧЕНИИ ПОСЛЕОПЕРАЦИОННОЙ БОЛИ | 2011 |
|
RU2569055C2 |
| ГИДРОХЛОРИДЫ 4-ОКСО-1,4-ДИГИДРОПИРИМИДИНА, ОБЛАДАЮЩИЕ ГИПОТЕНЗИВНОЙ, ИММУНОСТИМУЛИРУЮЩЕЙ И АНТИАЛЛЕРГИЧЕСКОЙ АКТИВНОСТЬЮ | 1991 |
|
SU1822149A1 |
| 2-ГИДРОКСИ-4-ОКСО-4-(4'-ХЛОРФЕНИЛ)-БУТ-2-ЕНОАТ 4-МЕТИЛ-2-ПИРИДИЛАММОНИЯ, ОБЛАДАЮЩИЙ ПРЯМЫМ АНТИКОАГУЛЯНТНЫМ ДЕЙСТВИЕМ | 2015 |
|
RU2649140C2 |
| 2,2-ДИМЕТИЛ-4-(4,6-ДИМЕТИЛ-2-ПИРИДОН-3-ИЛ)-1,2-ДИГИДРО-БЕНЗО[f]ИЗОХИНОЛИНА ГИДРОХЛОРИД, ПРОЯВЛЯЮЩИЙ ПРЯМОЕ АНТИКОАГУЛЯНТНОЕ ДЕЙСТВИЕ | 2006 |
|
RU2320654C1 |
| МЕТИЛ 4-ГИДРОКСИ-4-МЕТИЛ-6-ФЕНИЛ-2-ЦИАНОАЦЕТИЛГИДРАЗОНОЦИКЛОГЕКСАН-1-КАРБОКСИЛАТ, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2446150C2 |
Изобретение относится к 1,4,5,6-тетрагидро-6-оксо-5-(2-пиперазиноэтил)-4-фенил-3-(4-хлорфенил)пирроло[3,4-с]пиразола дигидрохлориду, который может быть использован в медицине в качестве средства, снижающего артериальное давление и свертываемость крови. Его получают взаимодействием 1-(2-пиперазиноэтил)-5-фенил-4-(4-хлорбензоил)-3-гидрокси-3-пирролин-2-она дигидрохлорида с гидразин гидратом. Технический результат - получение не описанного ранее соединения, обладающего одновременно гипотензивным и антикоагулянтным действием. 3 табл.
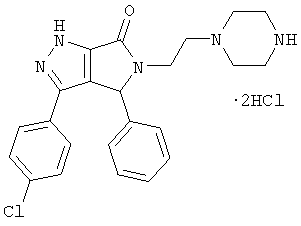
1,4,5,6-Тетрагидро-6-оксо-5-(2-пиперазиноэтил)-4-фенил-3-(4-хлорфенил)пирроло[3,4-с]пиразола дигидрохлорид формулы
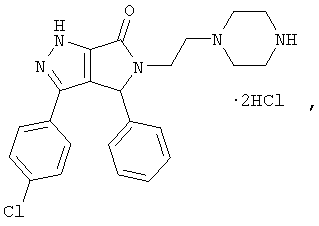
обладающий гипотензивной и антикоагулянтной активностями.
| Касимова Н.Н | |||
| Синтез, свойства и биологическая активность 1-аминоалкил- и 1-диалкиламиноалкил-4-ацил-5-арил-3-гидрокси-3-пирролин-2-онов, Диссертация на соискание ученой степени канд | |||
| фарм | |||
| наук., Пермский государственный университет, 2002 | |||
| Гейн В.Л | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| соед | |||
| в | |||
Авторы
Даты
2008-03-27—Публикация
2006-03-15—Подача