Настоящее изобретение относится к новым производным тиазола для применения в качестве лигандов рецептора нейропептида Y (NPY), прежде всего антагонистов нейропептида Y (NPY).
Изобретение прежде всего относится к соединениям формулы I

и к их фармацетически приемлемым солям и сложным эфирам, где
R1 означает арил, гетероциклил, амино или алкокси;
R2 означает водород, алкил или галоген;
R3 означает алкил, галоген или трифторметил;
А1 означает C-R или атом азота;
А2 означает пиперидин или пирролидин, причем атом азота в пиперидиновом или пирролидиновом цикле присоединен к А3;
А3 означает -S(O)2- или -С(O)-;
n равно 0, 1 или 2.
Соединения формулы I и их фармацевтически приемлемые соли и сложные эфиры являются новыми соединениями и обладают ценными фармакологическими свойствами. Указанные соединения являются нейропептидными лигандами, например антагонистами рецептора нейропептида, прежде всего селективными антагонистами рецептора Y5 нейропептида Y.
Нейропептид Y, содержащий 36 аминокислотных остатков, широко распространен в центральной и периферической нервной системе. Этот пептид опосредует ряд физиологических эффектов за счет различных подвидов рецептора. При испытании на животных было установлено, что нейропептид Y является мощным стимулом к потреблению корма, а активация рецепторов Y5 нейропептида Y приводит к гиперфагии и к пониженному теплообразованию. Следовательно, соединения, которые являются антагонистами подвида рецептора Y5 нейропептида Y, представляют собой новый подход к лечению расстройств питания, таких как ожирение и гиперфагия.
Современным подходом является медицинское вмешательство с целью снижения массы тела или предотвращения увеличения массы тела. Указанный подход заключается в подавлении аппетита, который опосредуется гипоталамусом, важным отделом головного мозга, регулирующим потребление пищи. При этом установлено, что нейропептид Y (NPY) является одним из наиболее эффективных центральных медиаторов потребления корма у разных видов животных. При повышенном уровне NPY наблюдается повышенное потребление пищи. Установлено, что в регуляции аппетита и увеличении массы тела важную роль играют различные рецепторы нейропептида Y (NPY).
Воздействие на эти рецепторы может снижать аппетит и соответственно приводить к увеличению массы тела. Снижение и долговременное поддержание массы тела может также оказывать благоприятные последствия на ассоциированные факторы риска, такие как артрит, сердечно-сосудистые заболевания, диабет и почечная недостаточность.
Таким образом, соединения формулы I можно использовать для профилактики или лечения артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения.
Объектами настоящего изобретения являются соединения формулы I и их вышеуказанные соли и сложные эфиры, а также их применение в качестве терапевтически активных соединений, способ получения указанных соединений, промежуточных соединений, фармацевтических композиций, лекарственных средств, содержащих указанные соединения, их фармацевтически приемлемых солей и сложных эфиров, применение указанных соединений, сложных эфиров и солей для профилактики и/или лечения заболеваний, прежде всего для лечения или профилактики артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания, таких как гиперфагия и прежде всего ожирение, и применение указанных соединений, солей и сложных эфиров для получения лекарственных средств, предназначенных для лечения или профилактики артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения.
В описании заявки термин "алкил", используемый отдельно или в комбинации, означает алкильную группу с прямой или разветвленной цепью, содержащую от 1 до 8 атомов углерода, предпочтительно алкильную группу с прямой или разветвленной цепью, содержащую от 1 до 6 атомов углерода, и прежде всего алкильную группу с прямой или разветвленной цепью, содержащую от 1 до 4 атомов углерода. Примерами С1-С8алкильных групп с прямой и разветвленной цепью являются метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил и изомерные пентилы, изомерные гексилы, изомерные гептилы и изомерные октилы, предпочтительно метил и этил, и наиболее предпочтительно метил.
Термин "циклоалкил", используемый отдельно или в комбинации, означает циклоалкильное кольцо, содержащее 3-8 атомов углерода, и предпочтительно циклоалкильное кольцо, содержащее 3-6 атомов углерода. Примерами С1-С8циклоалкильной группы являются циклопропил, метилциклопропил, диметилциклопропил, циклобутил, метилциклобутил, циклопентил, метилциклопентил, циклогексил, метилциклогексил, диметилциклогексил, циклогептил и циклооктил, предпочтительно циклопропил.
Термин "алкокси", используемый отдельно или в комбинации, означает группу формулы алкил-O-, где термин "алкил" имеет значения, указанные выше, такую, как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси, предпочтительно метокси и этокси, и наиболее предпочтительно метокси.
Термин "арил", используемый отдельно или в комбинации, означает группу фенил или нафтил, предпочтительно фенил, необязательно содержащую один или более заместителей, предпочтительно один-три заместителя, каждый из которых независимо выбирают из группы, включающей галоген, трифторметил, трифторметокси, амино, алкил, циклоалкил, алкокси, алкилкарбонил, циано, карбамоил, алкоксикарбамоил, метилендиокси, карбокси, алкоксикарбонил, аминокарбонил, алкиламинокарбонил, диалкиламинокарбонил, гидрокси, нитро, алкил-SO2-, амино-SO2-, циклоалкил и т.п. Предпочтительны фенил или нафтил, прежде всего фенил, необязательно замещенный одним-тремя заместителями, предпочтительно одним или двумя заместителями, независимо выбранными из группы, включающей алкил, галоген, алкокси, трифторметокси, нитро и трифторметил.
Термин "гетероциклил", используемый отдельно или в комбинации, означает ароматический 5-10-членный гетероцикл, включающий один или более, предпочтительно один или два, более предпочтительно один гетероатом, выбранный из атома азота, кислорода и серы, и замещенный по одному или более атомам углерода группой циано, трифторметил, трифторметокси, алкил-SO2-, амино-SO2-, галоген, алкокси, гидрокси, амино, циклоалкил, алкилкарбонил, аминокарбонил, нитро, алкил и/или алкоксикарбонил. Предпочтительными гетероциклильными кольцами являются прежде всего пирролидинил и тиофенил, причем тиофенил и пирролидинил необязательно замещены одним-тремя заместителями, предпочтительно одним или двумя, независимо выбранными из группы, включающей алкил, алкокси, трифторметил, трифторметокси, нитро и галоген.
Термин "амино", используемый отдельно или в комбинации, означает первичную, вторичную или третичную аминогруппу, связанную через атом азота, причем вторичная аминогруппа содержит алкильный или циклоалкильный заместитель, а третичная аминогруппа содержит два одинаковых или различных алкильных или циклоалкильных заместителя или два заместителя по атому азота вместе образуют цикл. Примерами аминогрупп являются такие группы, как -NH2, метиламино, этиламино, диметиламино, диэтиламино, метилэтиламино, пирролидин-1-ил или пиперидино и т.п., предпочтительны первичная аминогруппа, диметиламиногруппа и диэтиаминогруппа, прежде всего диметиламиногруппа.
Термин "галоген" означает фтор, хлор, бром или иод, предпочтительно фтор, хлор или бром.
Термин "карбонил", используемый отдельно или в комбинации, означает группу -С(O)-.
Термин "нитро", используемый отдельно или в комбинации, означает группу -NO2.
Термин "циано", используемый отдельно или в комбинации, означает группу -CN.
Термин «фармацевтически приемлемые соли» означает такие соли, которые сохраняют биологическую активность и свойства свободных оснований или свободных кислот и которые являются безопасными в биологическом и ином отношении. Такие соли включают соли неорганических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, и т.п., предпочтительно хлористоводородная кислота, и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, пара-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин и т.п. Кроме того, такие соли можно получить за счет присоединения неорганического или органического основания к свободной кислоте. Соли неорганического основания включают без ограничения перечисленными соли натрия, калия, лития, аммония, кальция, магния и т.п. Соли органического основания включают без ограничения перечисленными соли первичных, вторичных или третичных аминов, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы, такие как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, лизин, аргинин, N-этилпиперидин, пиперидин, полиаминовые смолы и т.п. Соединения формулы I могут также присутствовать в форме цвиттерионов. Более предпочтительными фармацевтически приемлемыми солями соединений формулы I являются гидрохлориды.
Соединения формулы I могут присутствовать в сольватированной, например гидратированной, форме. Сольватация происходит в процессе получения соединений или, например, за счет гигроскопических свойств первоначально безводного соединения формулы I (гидратация). Термин фармацевтически приемлемые соли включает также физиологически приемлемые сольваты.
Термин "фармацевтически приемлемые сложные эфиры" означает, что соединения общей формулы (I) могут образовывать производные по функциональным группам с образованием производных, которые способны превращаться в исходное соединение in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически лабильные сложные эфиры, такие как метоксиметиловые эфиры, метилтиометиловые эфиры и пивалоилоксиметиловые эфиры. Кроме того, изобретение включает любые физиологически приемлемые эквиваленты соединений общей формулы (I), аналогичные метаболически лабильным сложным эфирам, которые способны превращаться в исходные соединения общей формулы I in vivo.
Термин "ингибитор липазы" означает соединения, которые способны ингибировать действие липаз, например желудочных липаз или липаз поджелудочной железы. Например, как описано в патенте US 4598089, липстатин и орлистат являются эффективными ингибиторами липаз. Липстатин представляет собой природное соединение микробиологического происхождения, а орлистат является продуктом гидрирования липстатина. Прочие ингибиторы липаз включают класс соединений, которые обычно относятся к панклицинам. Панклицины являются аналогами орлистата (Mutoh и др., 1994). Термин "ингибитор липаз" относится также к ингибиторам липазы, связанным на полимере, например описанным в опубликованной международной патентной заявке WO 99/34786 (фирма Geltex Pharmaceuticals Inc.). Указанные полимеры характеризуются тем, что они содержат одну или более групп, ингибирующих липазы. Термин "ингибитор липазы" включает также фармацевтически приемлемые соли указанных соединений. Термин "ингибитор липазы" предпочтительно означает орлистат.
Орлистат представляет собой известное соединение, которое применяется для лечения или профилактики ожирения и гиперлипидемии. См. патент US 4598089, от 1 июля 1986 г., в котором заявлен способ получения орлистата, и патент США 6004996, в котором заявлены пригодные фармацевтические композиции. Кроме того, пригодные фармацевтические композиции описаны, например, в международных патентных заявках WO 00/09122 и WO 00/09123. Другие способы получения орлистата заявлены в европейских патентных заявках 185359, 189577, 443449 и 524495.
Орлистат предпочтительно вводят перорально в количестве от 60 до 720 мг в сутки разделенными дозами два или три раза в день. Предпочтительно ингибитор липазы вводят субъекту в количестве от 180 до 360 мг, наиболее предпочтительно 360 мг в сутки, предпочтительно разделенными дозами два или прежде всего три раза в сутки. Субъект предпочтительно означает человека с ожирением или избыточной массой тела, т.е. человека, индекс массы тела которого составляет 25 или выше. В общем случае ингибитор липазы предпочтительно принимают в течение приблизительно одного или двух часов после приема жирной пищи. В общем случае для введения ингибитора липазы, указанного выше, предпочтительно, чтобы пациент обладал достоверной наследственной предрасположенностью к ожирению, а индекс массы тела такого пациента составлял 25 или более.
Орлистат можно вводить в форме соответствующих композиций для перорального введения, таких как таблетки, таблетки в оболочке, твердые и мягкие желатиновые капсулы, эмульсии или суспензии. Примеры носителей, которые используются при получении таблеток, таблеток в оболочке, драже и твердых желатиновых капсул, включают лактозу, другие сахара и полиспирты, такие как сорбит, маннит, мальтодекстрин или другие наполнители; ПАВ, такие как лаурилсульфат натрия, бридж 96 или твин 80; дезинтегрирующие агенты, такие как крахмалгликолят натрия, кукурузный крахмал, или его производные; полимеры, такие как повидон и кросповидон; тальк; стеариновую кислоту или ее соли и т.п. Пригодными носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для регуляции осмотического давления, буферные вещества, обволакивающие агенты и антиоксиданты. Кроме того, они могут содержать другие терапевтически ценные вещества. Составы обычно получают в виде стандартных лекарственных форм любыми методами, известными в данной области техники. Орлистат предпочтительно вводят в виде композиции, приведенной в примерах и патенте US 6004996 соответственно.
Соединения формулы (I) могут содержать несколько асимметрических центров и существовать в форме оптически чистых энантиомеров, смесей энантиомеров, таких как, например, рацематы, оптически чистых диастереоизомеров, смесей диастереоизомеров, диастереоизомерных рацематов или смесей диастереоизомерных рацематов.
Предпочтительны соединения формулы I и их фармацевтически приемлемые соли, прежде всего соединения формулы I.
Кроме того, предпочтительны соединения формулы I, в которых R1 означает нафтил, пирролидинил, диалкиламино, морфолинил, алкокси, фенил или тиофенил, причем фенил и тиофенил необязательно замещены одним-тремя заместителями, независимо выбранными из группы, включающей алкил, алкокси, трифторметил, трифторметокси, нитро и галоген.
Предпочтительны, прежде всего, вышеуказанные соединения формулы I, в которых термин тиофенил означает тиофен-2-ил, тиофен-3-ил или 5-хлортиофен-2-ил. Кроме того, предпочтительны прежде всего вышеуказанные соединения формулы I, в которых термин фенил означает 2-фторфенил, 3-фторфенил, 4-фторфенил, 2,4-дифторфенил, 2-метилфенил, 2,5-диметилфенил, 2-метил-5-фторфенил, 3-метоксифенил, 4-метоксифенил, 4-трифторметоксифенил, 2-хлор-4-трифторметилфенил, 4-хлорфенил, 4-нитрофенил или 2-метокси-5-метилфенил.
Другим предпочтительным вариантом настоящего изобретения являются соединения формулы I, в которых R1 означает тиофенил, хлортиофенил, нафтил, пирролидинил, диметиламино, морфолинил, трет-бутокси или фенил, замещенный одним-тремя заместителями, независимо выбранными из группы, включающей фтор, хлор, метил, этил, метокси, этокси, трифторметокси, трифторметил и нитро. Предпочтительны, прежде всего, вышеуказанные соединения формулы I, в которых термин тиофенил означает тиофен-2-ил или 10 тиофен-3-ил. Предпочтительны, прежде всего, вышеуказанные соединения формулы I, в которых термин хлортиофенил означает 5-хлортиофен-2-ил. Кроме того, предпочтительны, прежде всего, вышеуказанные соединения формулы I, в которых термин фенил означает 2-фторфенил, 3-фторфенил, 4-фторфенил, 2,4-дифторфенил, 2-метилфенил, 2,5-диметилфенил, 2-метил-5-фторфенил, 3-метоксифенил, 4-метоксифенил, 4-трифторметоксифенил, 2-хлор-4-трифторметилфенил, 4-хлорфенил, 4-нитрофенил или 2-метокси-5-метилфенил.
Предпочтительны также соединения формулы I, в которых R2 означает водород.
Предпочтительны соединения формулы I, в которых А1 означает атом азота.
Кроме того, предпочтительны соединения формулы I, в которых А1 означает C-R3. Предпочтительны прежде всего соединения формулы I, в которых R3 означает метил, этил или трифторметил.
Кроме того, предпочтительны прежде всего соединения формулы I, в которых А1 означает C-R3, a R3 означает алкил, предпочтительно метил или этил. Предпочтительны прежде всего такие соединения формулы I, в которых R3 означает метил.
Другим предпочтительным объектом настоящего изобретения являются соединения формулы I, в которых А3 означает -С(O)-. Предпочтительны прежде всего такие соединения формулы I, где А3 означает -S(O)2-.
Кроме того, предпочтительны соединения формулы I, в которых А2 означает пирролидин, причем атом азота пирролидинового цикла присоединен к А3. Предпочтительны прежде всего такие соединения формулы I, где А2 означает пиперидин, причем атом азота пиперидинового цикла присоединен к А3.
Предпочтительны соединения формулы I, в которых n равно 0 или 1. Предпочтительны прежде всего такие соединения, в которых n равно 0.
Примерами предпочтительны соединений формулы (I) являются
1. (2-{[1-(тиофен-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
2. (2-{[1-(тиофен-3-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
3. (2-{[1-(5-хлортиофен-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
4. (2-{[1-(2-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
5. (2-{[1-(3-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
6. (2-{[1-(4-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
7. (2-{[1-(2,4-дифторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
8. (2-{[1-(толуол-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
9. (2-{[1-(2,5-диметилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
10. (2-{[1-(5-фтор-2-метилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
11. (2-{[1-(3-метоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
12. (2-{[1-(4-метоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
13. о-толил-(2-{[1-(4-трифторметоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)метанон,
14. (2-{[1-(2-хлор-4-трифторметилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
15. (2-{[1-(4-хлорбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
16. (2-{[1-(4-нитробензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
17. (2-{[1-(пирролидин-1-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
18. диметиламид 4-{[5-(2-метилбензоил)тиазол-2-иламино]метил}пиперидин-1-сульфоновой кислоты,
19. (2-{[1-(морфолин-4-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
20. (2-{2-[1-(тиофен-3-сульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон,
22. (2-{2-[1-(3-фторбензолсульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон,
23. трет-бутиловый эфир (S)-2-{[5-(2-этилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты,
24. трет-бутиловый эфир (S)-2-{[5-(2-трифторметилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты,
25. (S)-(2-этилфенил)-(2-{[1-(тиофен-2-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)метанон,
26. (S)-(2-{[1-(тиофен-2-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)-(2-трифторметилфенил)метанон,
27. (S)-(2-{[1-(нафталин-1-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)(2-трифторметилфенил)метанон,
28. трет-бутиловый эфир 4-[5-(2-этилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
29. трет-бутиловый эфир 4-[5-(2-метилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
30. трет-бутиловый эфир 4-[5-(2-трифторметилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
31. трет-бутиловый эфир 4-[5-(пиридин-2-карбонил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
32. (2-этилфенил){2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
33. (2-этилфенил)-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
34. (2-этилфенил)-{2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
34. {2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}пиридин-2-илметанон,
35. пиридин-2-ил-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
36. {2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}пиридин-2-ил-метанон,
37. {2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}(2-трифторметилфенил)метанон,
38. {2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}(2-трифторметилфенил)метанон,
39. {2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}(2-трифторметилфенил)метанон,
40. {2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон,
41. {2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон, и
42. {2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон.
Примерами предпочтительных соединений формулы (I) являются:
диметиламид 4-{[5-(2-метилбензоил)тиазол-2-иламино]метил}пиперидин-1-сульфоновой кислоты,
(2-этилфенил)-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон, и
{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон.
Объектом изобретения являются также способы получения соединений формулы I.
Получение соединений формулы I по настоящему изобретению проводят по последовательным или сходящимся схемам синтеза. Синтезы по изобретению показаны на следующих схемах. Реакции и способы очистки полученных продуктов известны специалистам в данной области техники. Если не указано иное, используемые в следующем описании способов заместители и индексы имеют значения, указанные выше.
Соединения общей формулы I можно получить по следующей последовательности реакций, показанной на схеме 1.
а) Из Вос-защищенных аминопиперидинов и Вос-защищенных аминопирролидинов IA, которые являются коммерческими препаратами или которые описаны в литературе, можно получить тиомочевины различными способами, описанными в литературе. Обычно соединения IA вводят в реакцию с бензоилизотиоцианатом в растворителе с последующим удалением бензоильной группы в основной среде с образованием тиомочевин IB. Более подробно условия проведения подобных реакций описаны в литературе, см., например, Tetrahedron, 19, 1603 (1963).
б) Тиомочевины IB обычно вводят в реакцию с диметилацеталем N,N-диметилформамида в присутствии или в отсутствие растворителя с образованием соответствующих диметиламинометилентиоуреидопроизводных IC. К природе используемого растворителя не предъявляется специальных требований, при условии что он не подавляет реакцию или не воздействует на реагенты и в той или иной мере способен их растворять. Примеры пригодных растворителей включают ДМФА и диоксан и т.п. Реакцию можно проводить в широком интервале температур, и в настоящем изобретении точное значение температуры не является решающим фактором. Обычно реакцию проводят в интервале от комнатной температуры до температуры кипения растворителя. Продолжительность реакции также варьирует в широком интервале в зависимости от множества факторов, главным образом от температуры реакции и природы реагентов. Однако для получения диметиламинометилентиоуреидопроизводных IC обычно достаточно от 0,5 ч до нескольких суток. Более подробно условия проведения подобных реакций описаны в литературе, см., например, Heterocycles, 11, 313-318 (1978).
в) Из диметиламинометилентиоуреидопроизводных IC можно получить производные тиазола ID по реакции соединения IC с α-бромкетонами в растворителе, таком как этанол и т.п., в присутствии или в отсутствие основания. α-Бромкетоны являются известными соединениями, или их получают известными методами. Соответствующие источники α-бромкетонов приводятся в описании. К природе используемого растворителя не предъявляется специальных требований, при условии что он не подавляет реакцию или не воздействует на реагенты, и в той или иной мере способен их растворять. Примеры пригодных растворителей включают дихлорметан, хлороформ, диоксан, метанол, этанол и т.п. К природе используемого на этой стадии основания не предъявляется специальных требований, и в данном случае в равной степени можно использовать любое основание, которое принято использовать в реакциях этого типа. Примеры таких оснований включают триэтиламин и диизопропилэтиламин и т.п. Реакцию можно проводить в широком интервале температур, и в настоящем изобретении точное значение температуры не является решающим фактором. Обычно реакцию проводят при нагревании от комнатной температуры до температуры кипения растворителя. Продолжительность реакции также варьирует в широком интервале в зависимости от множества факторов, главным образом от температуры реакции и природы реагентов. Однако для получения производных тиазола ID обычно достаточно от 0,5 ч до нескольких суток. Более подробно условия проведения подобных реакций описаны в литературе, см., например, J. Heterocycl. Chem., 16(7), 1377-1383 (1979). Полученное соединение формулы ID является соединением по настоящему изобретению и требуемым продуктом.
г) В другом варианте указанные соединения можно ввести в последовательные реакции, такие как удаление Вос-защитной группы известным методом, описанным в литературе, с образованием производных тиазола IE. Обычно Вос-защитную группу в соединениях ID удаляют в кислотных условиях в присутствии или в отсутствие растворителя. К природе используемого растворителя не предъявляется специальных требований, при условии что он не подавляет реакцию или не воздействует на реагенты, и в той или иной мере способен их растворять. Примеры пригодных растворителей включают диоксан, ТГФ и т.п. К природе используемой на этой стадии кислоты не предъявляется специальных требований, и в данном случае в равной степени можно использовать любую кислоту, которую принято использовать в реакциях этого типа. Примеры таких кислот включают HCl, ТФУ и т.п. Реакцию можно проводить в широком интервале температур, и в настоящем изобретении точное значение температуры не является решающим фактором. Обычно реакцию проводят в интервале от комнатной температуры до температуры кипения растворителя. Продолжительность реакции также варьирует в широком интервале в зависимости от множества факторов, главным образом от температуры реакции и природы реагентов. Однако для получения производных тиазола IE или их соответствующих солей обычно достаточно от 0,5 ч до нескольких суток. Более подробно условия проведения подобных реакций описаны в литературе, см., например, Heterocycles, 32, 1699 (1991).
д) Сульфонамиды, производные сульфоновых кислот, амиды, карбаматы и мочевины можно получать из пригодных исходных материалов известными методами. Модификацию аминов IE с образованием сульфонамидов, производных сульфоновых кислот, амидов, карбаматов и мочевин проводят по описанным в литературе методам. Например, превращение аминов IE или их соответствующих солей в соединения общей формулы I проводят по реакции соединений IE с соответствующими хлорангидридами кислот, сульфонилхлоридами, сульфамоилхлоридами, изоцианатами, хлорформиатами или эфирами угольной кислоты (которые являются известными соединениями или соединениями, полученными известными методами), соответственно в присутствии или в отсутствие растворителя и в присутствии основания. К природе используемого растворителя не предъявляется специальных требований, при условии что он не подавляет реакцию или не воздействует на реагенты, и в той или иной мере способен их растворять. Примеры пригодных растворителей включают ДХМ, хлороформ, диоксан, МеОН или ТГФ и т.п. К природе используемого на этой стадии основания не предъявляется специальных требований, и данном случае в равной степени можно использовать любое основание, которое принято использовать в реакциях этого типа. Примеры таких оснований включают триэтиламин и диизопропилэтиламин и т.п. Реакцию можно проводить в широком интервале температур, и в настоящем изобретении точное значение температуры не является решающим фактором. Обычно реакцию проводят в интервале от комнатной температуры до температуры кипения растворителя. Продолжительность реакции также варьирует в широком интервале в зависимости от множества факторов, главным образом от температуры реакции и природы реагентов. Однако для получения производных тиазола I обычно достаточно от 0,5 ч до нескольких суток. Более подробно условия проведения подобных реакций описаны в литературе, см., например, Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 10 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY (1999).
Схема 1

Превращение соединения формулы I в фармацевтически приемлемую соль проводят при обработке такого соединения неорганической кислотой, например галогенводородной кислотой, такой, например, как хлористоводородная кислота или бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, или органической кислотой, такой, как уксусная кислота, лимонная кислота, малеиновая кислота, фумаровая кислота, винная кислота, метансульфоновая кислота или пара-толуолсульфоновая кислота. Соответствующие соли карбоновых кислот получают при обработке соединений формулы I физиологически совместимыми основаниями.
Превращение соединений формулы I в фармацевтически приемлемые сложные эфиры или амиды проводят, например, при взаимодействии амино- или гидроксигрупп с карбоновыми кислотами, такими как уксусная кислота, в присутствии конденсирующего агента, такого, как гексафторфосфат бензотриазол-1-илокситрис(диметиламино)фосфония (ВОР) или N,N-дициклогексилкарбодиимид (DCCI), с образованием сложного эфира карбоновой кислоты или ациламида.
Предпочтительный способ получения соединения формулы I включает взаимодействие соединения формулы

с соединением формулы

с образованием соединения формулы I, где R1-R3, А1, А2, А3 и n имеют значения, указанные выше, а R4 означает хлор или гидрокси. Предпочтительным является способ, где R4 означает хлор. Предпочтителен прежде всего способ, в котором реакцию проводят в присутствии или в отсутствие растворителя и в присутствии основания. Предпочтительными растворителями являются, например, ДХМ, хлороформ, диоксан, МеОН и ТГФ. Примерами предпочтительных оснований являются триэтиламин и диизопропилэтиламин.
Предпочтительными промежуточными соединениями являются:
гидрохлорид {2-[(пиперидин-4-илметил)амино]тиазол-5-ил}-орто-толилметанона,
гидрохлорид [2-(2-пиперидин-2-илэтиламино)тиазол-5-ил]-орто-толилметанона,
трет-бутиловый эфир (S)-2-{[5-(2-этилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты.
Кроме того, объектом изобретения являются вышеуказанные соединения формулы I для применения в качестве терапевтически активных веществ.
Кроме того, объектом изобретения являются вышеуказанные соединения для получения лекарственных средств, предназначенных для профилактики и лечения заболеваний, которые вызываются нарушениями, ассоциированными с рецептором NPY, прежде всего для получения лекарственных средств, предназначенных для профилактики и лечения артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения.
Аналогичным образом объектом изобретения являются фармацевтические композиции, содержащие вышеуказанное соединение формулы I и терапевтически инертный носитель.
Объектом изобретения является также применение вышеуказанные соединений для получения лекарственных средств, предназначенных прежде всего для лечения и профилактики артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения.
Кроме того, объект изобретения включает соединения, полученные по одному из описанных способов.
Кроме того, объектом изобретения является способ лечения и профилактики артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения, который включает введение эффективного количества вышеуказанного соединения.
Еще одним объектом изобретения является способ лечения ожирения у человека, который нуждается в таком лечении, причем указанный способ включает введение пациенту терапевтически эффективного количества соединения формулы I и терапевтически эффективного количества ингибитора липазы, предпочтительно орлистата. Объектом изобретения является также вышеуказанный способ, при котором введение осуществляют одновременно, раздельно или последовательно.
Кроме того, предпочтительным вариантом настоящего изобретения является применение соединения формулы I для получения лекарственного средства, предназначенного для лечения и профилактики ожирения у пациента, который проходит также курс лечения ингибитором липазы, причем ингибитор липазы означает орлистат.
Объектом изобретения являются также вышеуказанные соединения для получения лекарственных средств, предназначенных для профилактики и лечения алкоголизма.
Кроме того, объектом изобретения является способ лечения и профилактики алкоголизма.
Методики определения активности
Клонирование кДНК рецептора NPY5 мыши
Полноразмерную кДНК, кодирующую рецептор NPY5 мыши (mNPY5), из кДНК ткани мозга мыши амплифицировали с использованием специфичных праймеров, сконструированных на основе опубликованной последовательности, и ДНК-полимеразы Pfu. Продукт амплификации субклонировали в вектор экспрессии млекопитающих pcDNA3 с использованием сайтов рекстрикции Есо RI и Xhol. Позитивные клоны секвенировали и клон, кодирующий опубликованную последовательность, отбирали для выделения стабильных клеточных клонов.
Стабильная трансфекция
Клетки почек эмбриона человека 293 (НЕК293) трансфектировали 10 мкг mNPY5 ДНК с использованием реагента липофектамина. Через двое суток после трансфекции инициировали селекцию генетицином (1 мг/мл) и выделяли несколько стабильных клонов. Затем один из клонов использовали для определения фармакологических характеристик.
Конкурентное связывание радиоактивного лиганда
Клетки почек эмбриона человека 293 (НЕК293), экспрессирующие рекомбинантный рецептор NPY5 мыши (mNPY5), разрушали трехкратным циклом замораживания/оттаивания в гипотоническом трис-буферном растворе (5 мМ, рН 7,4, 1 мМ MgCl2), гомогенизировали и центрифугировали при 72000g в течение 15 мин. Осадок дважды промывали 75 мМ трио-буферным раствором, рН 7,4, содержащим 25 мМ MgCl2, 250 мМ сахарозу, 0,1 мМ фенилметилсульфонилфторид и 0,1 мМ 1,10-фенантролин, ресуспендировали в указанном буферном растворе и аликвотные части хранили при -80°С. 10 Содержание белка определяли по методу Лоури, в качестве стандарта использовали бычий сывороточный альбумин (БСА).
Реакцию связывания с радиоактивным лигандом проводили в 250 мкл 25 мМ Hepes-буферного раствора (рН 7,4, 2,5 мМ CaCl2, 1 мМ MgCl2, 1% бычий сывороточный альбумин и 0,01% NaN3), содержащего 5 мкг белка, 100 пМ [125I]-меченного пептида YY (PYY), и 10 мкл ДМСО, содержащего возрастающие количества немеченых анализируемых соединений. После инкубации при 22°С в течение 1 ч связанный и свободный лиганд разделяли фильтрованием на стекловолоконных фильтрах. Неспецифичное связывание определяли в присутствии 1 мкл немеченого PYY. Специфичное связывание определяли по разности между общим связыванием и неспецифичным связыванием. Величины IC50 определяли как концентрацию антагониста, которая вытесняет 50% связанного [125I]-меченного нейропептида Y. Для расчетов использовали анализ линейной регрессии после обработки полученных результатов методом логит/логарифмических преобразований.
Результаты анализа с использованием в качестве анализируемых веществ типичных соединений по изобретению приведены в следующей таблице:
Описанные выше соединения характеризуются значениями IC50 менее 1000 нМ, более предпочтительные соединения характеризуются значениями IC50 менее 100 нМ, прежде всего менее 10 нМ. Наиболее предпочтительные соединения характеризуются значениями IC50 менее 2 нМ. Указанные результаты получены при использовании вышеописанного анализа.
Соединения формулы I и их фармацевтически приемлемые соли и сложные эфиры можно использовать в качестве лекарственных средств (например, в форме фармацевтических препаратов). Фармацевтические препараты можно вводить различными способами, такими как пероральный способ (например, в форме таблеток, таблеток в оболочке, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий), интраназальным способом (например, в форме назальных спреев) или ректальным способом (например, в форме суппозиториев). Однако введение можно также проводить парентеральным способом, таким, как внутримышечный или внутривенный способ (например, в форме инъекционных растворов).
Соединения формулы I и их фармацевтически приемлемые соли и сложные эфиры можно перерабатывать в смеси с фармацевтически инертными, неорганическими или органическими адъювантами, например, для получения таблеток, таблеток в оболочке, драже и твердых желатиновых капсул. При получении таблеток, драже или твердых желатиновых капсул в качестве таких адъювантов используются, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли.
Пригодными адъювантами для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п.
Пригодными адъювантами при получении растворов и сиропов являются, например, вода, полиолы, сахароза, инвертированный сахар и глюкоза и т.п.
Пригодными адъювантами для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.п.
Пригодными адъювантами для суппозиториев являются, например, природные или отвержденные масла, воски, жиры, полутвердые или жидкие полиолы и т.п.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизирующие агенты, загустители, стабилизирующие агенты, смачивающие агенты, эмульгирующие агенты, подсластители, красители, ароматизаторы, соли для регуляции осмотического давления, буферные вещества, обволакивающие агенты или антиоксиданты. Кроме того, они могут содержать другие терапевтически ценные соединения.
По настоящему изобретению соединения формулы I и их фармацевтически приемлемые соли можно использовать для профилактики и лечения артрита, сердечно-сосудистых заболеваний, диабета, почечной недостаточности и прежде всего расстройств питания и ожирения. Дозы могут варьировать в широком диапазоне в соответствии с индивидуальными требованиями в каждом конкретном случае. В общем случае при пероральном введении пригодная суточная доза может составлять от приблизительно 0,1 до 20 мг на кг массы тела, предпочтительно от приблизительно 0,5 до 4 мг на кг массы тела (например, приблизительно 300 мг на одного человека), причем суточную дозу можно вводить предпочтительно в виде 1-3 разделенных доз. Однако очевидно, что верхний предел можно превысить в соответствии с показанием.
Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Примеры
Пример А
трет-Бутиловый эфир 4-(3-диметиламинометилентиоуреидометил)пиперидин-1-карбоновой кислоты

К раствору 17,7 г (82,6 ммоль) трет-бутилового эфира 4-аминометилпиперидин-1-карбоновой кислоты (коммерческий продукт) в 150 мл ТГФ добавляли 11,1 мл (82,6 ммоль) бензоилизотиоцианата и смесь перемешивали при комнатной температуре в течение 1 ч. Растворитель выпаривали, остаток растворяли в 100 мл МеОН, добавляли раствор 34,2 г (248 ммоль) карбоната калия в 100 мл воды и смесь перемешивали при комнатной температуре в течение 16 ч. Летучие компоненты удаляли, остаток экстрагировали этилацетатом, объединенные органические слои промывали насыщенным раствором NaHCO3, сушили над MgSO4 и упаривали. К остатку добавляли 88,1 мл (661 ммоль) диметилацеталя N,N-диметилформамида и смесь нагревали при 110°С в течение 16 ч. Осадок отделяли фильтрованием, промывали н-гексаном и высушивали, при этом получали 21,5 г (79%) указанного в заголовке соединения в виде твердого аморфного вещества розового цвета. МС (m/e): 329,4 (МН+ 100%)
Пример В
трет-Бутиловый эфир 2-[2-(3-диметиламинометилентиоуреидо)этил]пиперидин-1 -карбоновой кислоты
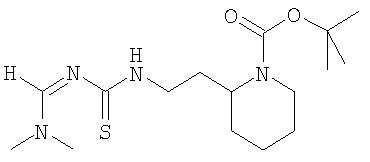
трет-Бутиловый эфир 2-[2-(3-диметиламинометилентиоуреидо)этил]пиперидин-1 -карбоновой кислоты
(пример В) синтезировали из трет-бутилового эфира 2-(2-аминоэтил)пиперидин-1-карбоновой кислоты (коммерчески доступны) по методике, описанной при синтезе трет-бутилового эфира 4-(3-диметиламинометилентиоуреидометил)пиперидин-1-карбоновой кислоты (пример А). МС (m/e): 343,4 (MH+, 100%)
Пример С
2-Бром-1 -(2-этилфенил)этанон

К раствору 15,2 г (88 ммоль) дибромэтана в 120 мл ТГФ при -75°С последовательно добавляли 44 мл (88 ммоль) 2 М раствора LDA в ТГФ и 6,57 г (40 ммоль) метилового эфира этилбензойной кислоты в 80 мл ТГФ. Затем добавляли 37,5 мл 1,6 М раствора н-бутиллития в н-гексане и через 30 мин к 10 смеси при температуре менее -65°С осторожно добавляли 35 мл HCl (37%).
Смесь промывали водой и раствором NaHCO3, органическую фазу сушили над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток дважды очищали экспресс-хроматографией на колонке с силикагелем (элюент:этилацетат/гексан, 1:9), при этом получали 3,8 г (41%) указанного в заголовке 15 соединения в виде масла желтого цвета. МС (m/e): 227,1 (М+Н, 100%).
Пример D
Гидрохлорид {2-[(пиперидин-4-илметил)амино1тиазол-5-ил}-орто-толилметанона

Смесь 0,787 г (2,4 ммоль) трет-бутилового эфира 4-(3-диметиламинометилентиоуреидометил)пиперидин-1-карбоновой кислоты, 0,61 г (2,88 ммоль) 2-бром-1-орто-толилэтанона и 1002 мкл (7,2 ммоль) NEt3 в 3 мл EtOH нагревали при 90°С в течение 16 ч. Затем смесь концентрировали в вакууме, добавляли разбавленный раствор NaHCO3 и экстрагировали этилацетатом. Объединенные органические слои фильтровали через слой MgSO4, расположенный на слое силикагеля, и концентрировали в вакууме, при этом получали 707 мг (71%) промежуточного трет-бутилового эфира 4-{[5-(2-метилбензоил)тиазол-2-иламино]метил}пиперидин-1-карбоновой кислоты, МС (m/e): 416,3 (MH+, 100%). Остаток растворяли в диоксане, добавляли 10 мл 4н. раствора HCl в диоксане и смесь перемешивали при комнатной температуре в течение 16 ч. После упаривания растворителя получали 598 мг (выход колич.) указанного в заголовке соединения. МС (m/e): 315,7 (МН+, 100%)
Пример Е
Гидрохлорид [2-(2-пиперидин-2-илэтиламино)тиазол-5-ил]-орто-толилметанона
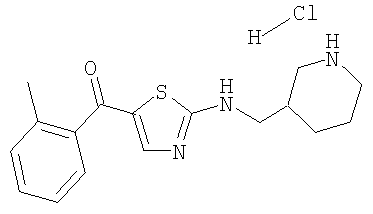
Смесь 0,787 г (2,4 ммоль) трет-бутилового эфира 2-[2-(3-диметиламинометилентиоуреидо)этил]пиперидин-1-карбоновой кислоты, 0,61 г (2,88 ммоль) 2-бром-1-орто-толилэтанона и 1002 мкл (7,2 ммоль) NEt3 в 3 мл EtOH нагревали при 90°С в течение 16 ч. Затем смесь концентрировали в вакууме, добавляли разбавленный раствор NaHCO3 и экстрагировали этилацетатом. Объединенные органические слои фильтровали через слой MgSO4, расположенный на слое силикагеля, и концентрировали в вакууме, при этом получали 710 мг (69%) промежуточного трет-бутилового эфира 2-{2-[5-(2-метилбензоил)тиазол-2-иламино]этил}пиперидин-1-карбоновой кислоты, МС (m/e): 430,5 (МН, 100%). Остаток растворяли в диоксане, добавляли 10 мл 4н. раствора HCl в диоксане и смесь перемешивали при комнатной температуре в течение 16 ч. После упаривания растворителя получали 606 мг (выход колич.) указанного в заголовке соединения. МС (m/e): 329,8 (МН+, 100%)
Пример 1 (2-{[1-(Тиофен-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон
Смесь 35,2 мг (0,1 ммоль) гидрохлорида {2-[(пиперидин-4-илметил)амино]тиазол-5-ил}-орто-толилметанона, 21,9 мг (0,12 ммоль) тиофен-2-сульфонилхлорида (коммерчески доступны) и 44,6 мкл (0,32 ммоль) NEt3 в ДХМ/МеОН (3:1) перемешивали при 60°С в течение 16 ч. После охлаждения до комнатной температуры смесь концентрировали, добавляли МеОН (1 мл) и муравьиную кислоту (0,5 мл) и продукт очищали методом обращенно-фазовой ЖХВР (элюент:градиент ацетонитрил/вода). После упаривания фракций, содержащих конечный продукт, получали 22 мг (48%) указанного в заголовке соединения. МС (m/e): 460,2 (МН-, 100%)
Соединения, описанные как примеры 2-19, получали по методике, описанной в примере 1. Соответствующие исходные материалы указаны в таблице 1.
Пример 20
(2-{2-[1-(Тиофен-3-сульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон
Смесь 35,2 мг (0,1 ммоль) гидрохлорида [2-(2-пиперидин-2-илэтиламино)тиазол-5-ил]-орто-толилметанона, 21,9 мг (0,12 ммоль) тиофен-3-сульфонилхлорида (коммерчески доступны) и 44,6 мкл (0,32 ммоль) NEt3 в ДХМ/МеОН (3:1) перемешивали при 60°С в течение 16 ч. После охлаждения до комнатной температуры смесь концентрировали, добавляли МеОН (1 мл) и муравьиную кислоту (0,5 мл) и продукт очищали методом обращенно-фазовой ЖХВР (элюент:градиент ацетонитрил/вода). После упаривания фракций, содержащих конечный продукт, получали 7 мг (15%) указанного в заголовке соединения. МС (m/e): 474,0 (МН-, 100%)
Пример 21
(2-{2-[1-(3-Фторбензолсульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон
(2-{2-[1-(3-Фторбензолсульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон синтезировали из гидрохлорида [2-(2-пиперидин-2-илэтиламино)тиазол-5-ил]-орто-толилметанона и 3-фторфенилсульфонилхлорида по методике, описанной в примере 20. МС (m/e): 486,2 (МН-, 100%)
Пример F
1,1-Диметилэтиловый эфир 2-(S)-(3-диметиламинометилентиоуреидометил)пирролидин-1-карбоновой кислоты
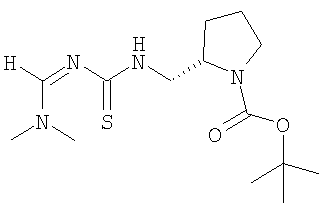
1,1-Диметилэтиловый эфир 2-(S)-(3-диметиламинометилентиоуреидометил)пирролидин-1-карбоновой кислоты получали из 1,1-диметилэтилового эфира (S)-2-(аминометил)-1-пирролидинкарбоновой кислоты по методике, описанной в примере А (трет-бутиловый эфир 4-(3-диметиламинометилентиоуреидометил)пиперидин-1-карбоновой кислоты). Продукт очищали хроматографией на колонке с силикагелем (элюент:градиент этилацетат/гексан, от 2:1 до 3:1), при этом получали твердое вещество желтого цвета. МС: 315,4 (М+Н)+.
Пример G
1,1-Диметилэтиловый эфир 4-(3-15 диметиламинометилентиоуреидо)пиперидин-1-карбоновой кислоты
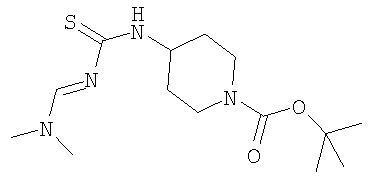
1,1-Диметилэтиловый эфир 4-(3-диметиламинометилентиоуреидо)пиперидин-1-карбоновой кислоты получали из 1,1-диметилэтилового эфира 4-амино-1-пиперидинкарбоновой кислоты по методике, описанной в примере А (трет-бутиловый эфир 4-(3-диметиламинометилентиоуреидометил)пиперидин-1-карбоновой кислоты). Указанное соединение получали в виде твердого вещества белого цвета. tпл. 170°С. МС: 315,4 (М+Н)+.
Пример 22
трет-Бутиловый эфир (8)-2-{[5-(2-этилбензоил)тиазол-2-иламино1 метил }пирролидин-1-карбоновой кислоты
К раствору 1,1-диметилэтилового эфира 2-(S)-(3-диметиламинометилентиоуреидометил)пирролидин-1-карбоновой кислоты (150 мг) в N,N-диметилформамиде (2 мл) добавляли 2-бром-1-(2-этилфенил)этанон (109 мг) и смесь перемешивали при комнатной температуре в течение 65 ч. Затем смесь разбавляли дихлорметаном, дважды промывали водой, однократно солевым раствором, сушили над сульфатом магния и упаривали при пониженном 10 давлении. Остаток очищали хроматографией на колонке с силикагелем (элюент:этилацетат/гексан, 2:1), при этом получали продукт в виде масла желтого цвета (129 мг, 65%).
Соединения, описанные как примеры 23 и 27-30, получали по методике, описанной в примере 1. Соответствующие исходные материалы указаны в 15 таблице 1.
Пример 24
(S)-(2-Этилфенил)-(2-{[1-(тиофен-2-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)метанон
трет-Бутиловый эфир (S)-2-{[5-(2-этилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты (50 мг) растворяли в диоксане (2 мл) и раствор охлаждали до 0°С на ледяной бане. Затем к раствору добавляли 25% соляную кислоту (0,2 мл), смесь перемешивали при комнатной температуре в течение 4 ч и упаривали досуха. Остаток растворяли в дихлорметане (2 мл), добавляли триэтиламин (0,02 мл), а затем раствор тиофен-2-сульфонилхлорида (23 мг) в дихлорметане (0,5 мл). Смесь перемешивали при комнатной температуре в течение 5 ч, разбавляли дихлорметаном, промывали водой, сушили над сульфатом магния и упаривали. Остаток очищали хроматографией на колонке с силикагелем (элюент:градиент этилацетат/гексан, от 5:1 до 1:0), при этом получали продукт в виде пены грязно-белого цвета (36 мг, 65%).
Соединения, описанные как примеры 25, 26 и 31-42, получали по методике, описанной в примере 24. Соответствующие исходные материалы указаны в таблице 1.
Пример А
Соединения формулы I можно использовать известным способом в качестве активного ингредиента для получения таблеток, содержащих следующую композицию.
Пример Б
Соединения формулы I можно использовать известным способом в качестве активного ингредиента для получения капсул, содержащих следующую композицию.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИАМИНОТИАЗОЛЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ИНГИБИТОРА ЦИКЛИН-ЗАВИСИМОЙ КИНАЗЫ 4 | 2003 |
|
RU2311414C2 |
| НОВОЕ ПРОИЗВОДНОЕ АМИНОПИРИДИНА С ИНГИБИТОРНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ SYK. | 2006 |
|
RU2363699C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 1-ОКСА-2,8-ДИАЗАСПИРО[4.5]ДЕЦ-2-ЕНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ АНАЛЬГЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2002 |
|
RU2296128C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ МОДУЛЯЦИИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ, СПОСОБ ПОЛУЧЕНИЯ ЭТИХ СОЕДИНЕНИЙ | 2000 |
|
RU2255937C2 |
| ЦИС-2, 4, 5-ТРИАРИЛ-ИМИДАЗОЛИНЫ | 2004 |
|
RU2319696C2 |
| ИНДОЛ-2-КАРБОКСАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха И/ИЛИ VIIa, ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2299881C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОАРИЛПИРРОЛИДИНИЛ- И ПИПЕРИДИНИЛКЕТОНА | 2007 |
|
RU2479575C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,4-ДИАМИНОТИАЗОЛ-5-ОНА | 2005 |
|
RU2395501C2 |
| 2-ИМИДАЗОБЕНЗОТИАЗОЛЫ КАК ЛИГАНДЫ АДЕНОЗИНОВОГО РЕЦЕПТОРА | 2004 |
|
RU2340612C2 |
| ПРОИЗВОДНЫЕ 2-АМИНО-ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ JNK | 2011 |
|
RU2572247C2 |
Изобретение относится к новым соединениям формулы (I) и их фармацевтически приемлемым солям и сложным эфирам. Соединения настоящего изобретения обладают свойствами антагонистов рецептора NPY и могут найти применение для лечения таких заболеваний, как артрит, диабет, расстройство питания, ожирение и т.п. В общей формуле I

R1 означает фенил, нафтил, 5-6-членный гетероциклил, содержащий в качестве гетероатомов О, N или S, причем фенил, нафтил и гетероциклил необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С6алкила, C1-С6алкокси, галогенС1-С6алкила, галогенС-С6алкокси и нитро; диС1-С6алкиламино, или C1-С6алкокси; R2 означает водород; R3 означает C1-С6алкил или трифторметил; А1 означает C-R3 или атом азота; А2 означает пиперидин или пирролидин, причем атом азота в пиперидиновом или пирролидиновом цикле присоединен к А3; А3 означает -S(O)2- или -С(O)-, а n равно 0, 1 или 2. Изобретение также относится к фармкомпозиции на основе соединений изобретения. 2 н. и 14 з.п. ф-лы, 1 табл.

где R1 означает фенил, нафтил, 5-6-членный гетероциклил, содержащий в качестве гетероатомов О, N или S, причем фенил, нафтил и гетероциклил необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С6алкила, C1-С6алкокси, галогенС1-С6алкила, галогенС1-С6алкокси и нитро;
диС1-С6алкиламино, или C1-С6алкокси;
R2 означает водород;
R3 означает C1-С6алкил или трифторметил;
А1 означает C-R3 или атом азота;
А2 означает пиперидин или пирролидин, причем атом азота в пиперидиновом или пирролидиновом цикле присоединен к А3;
А3 означает -S(O)2- или -С(O)-, а
n равно 0, 1 или 2,
и их фармацевтически приемлемые соли и сложные эфиры.
(2-{[1-(тиофен-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(тиофен-3-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(5-хлортиофен-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(2-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(3-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(4-фторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(2,4-дифторбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(толуол-2-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(2,5-диметилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(5-фтор-2-метилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(3-метоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(4-метоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
орто-толил-(2-{[1-(4-трифторметоксибензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)метанон,
(2-{[1-(2-хлор-4-трифторметилбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(4-хлорбензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(4-нитробензолсульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{[1-(пирролидин-1-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
диметиламид 4-{[5-(2-метилбензоил)тиазол-2-иламино]метил}пиперидин-1-сульфоновой кислоты,
(2-{[1-(морфолин-4-сульфонил)пиперидин-4-илметил]амино}тиазол-5-ил)-орто-толилметанон,
(2-{2-[1-(тиофен-3-сульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон,
(2-{2-[1-(3-фторбензолсульфонил)пиперидин-2-ил]этиламино}тиазол-5-ил)-орто-толилметанон,
трет-бутиловый эфир (S)-2-{[5-(2-этилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты,
трет-бутиловый эфир (S)-2-{[5-(2-трифторметилбензоил)тиазол-2-иламино]метил}пирролидин-1-карбоновой кислоты,
(S)-(2-этилфенил)-(2-{[1-(тиофен-2-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)метанон,
(S)-(2-{[1-(тиофен-2-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)-(2-трифторметилфенил)метанон,
(S)-(2-{[1-(нафталин-1-сульфонил)пирролидин-2-илметил]амино}тиазол-5-ил)(2-трифторметилфенил)метанон,
трет-бутиловый эфир 4-[5-(2-этилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
трет-бутиловый эфир 4-[5-(2-метилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
трет-бутиловый эфир 4-[5-(2-трифторметилбензоил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
трет-бутиловый эфир 4-[5-(пиридин-2-карбонил)тиазол-2-иламино]пиперидин-1-карбоновой кислоты,
(2-этилфенил){2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
(2-этилфенил)-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
(2-этилфенил)-{2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
{2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}пиридин-2-илметанон,
пиридин-2-ил-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон,
{2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}пиридин-2-ил-метанон,
{2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}(2-трифторметилфенил)метанон,
{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}(2-трифторметилфенил)метанон,
{2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил} (2-трифторметилфенил)метанон,
{2-[1-(нафталин-1-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон,
{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон, и
{2-[1-(2-метокси-5-метилбензолсульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон.
(2-этилфенил)-{2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}метанон, и {2-[1-(тиофен-2-сульфонил)пиперидин-4-иламино]тиазол-5-ил}-орто-толилметанон.
| RU 95122453 А, 27.11.1997 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДСОДЕРЖАЩИХ ГЛИФТАЛЕВЫХ СМОЛ | 0 |
|
SU164675A1 |
| WO 9962892 A1, 09.12.1999. | |||
Авторы
Даты
2008-04-10—Публикация
2004-08-04—Подача