Настоящее изобретение относится к новому способу получения витамин K-зависимых белков и, в частности фактора свертывания VII (FVII). Кроме того, настоящее изобретение относится к новым котрансфицируемым эукариотическим клеткам-хозяевам и рекомбинантным векторам, которые должны использоваться в этом усовершенствованном способе, для получения витамин K-зависимых белков.
Предпосылки изобретения
Биосинтез витамин K-зависимых белков включает в себя несколько стадий посттрансляционного процессинга до того, как будет получен зрелый функциональный белок.
Витамин K представляет собой необходимый кофактор для гамма-карбоксилирования остатков глутаминовой кислоты в этих витамин K-зависимых белках, включая прокоагулянтные факторы: тромбин, фактор VII, IX и X; антикоагулянты, белок C и белок S и другие белки, такие как остеокальцин (белок Gla костей), матриксный белок Gla и обогащенный пролином белок Gla 1. Это карбоксилирование является необходимым для нормального гемостаза, поскольку оно делает возможным связывания кальция и присоединение прокоагулянтов и антикоагулянтов к фосфолипидам.
Гамма-глутамилкарбоксилаза представляет собой интегрированный мембранный микросомальный фермент, находящийся в грубом эндоплазматическом ретикулуме. Она карбоксилирует глутаматные остатки, расположенные в домене Gla витамин K-зависимых белков. кДНК гамма-глутамилкарбоксилазы человека недавно выделена и секвенирована (Wu SM et al. Science 254:1634, 1991). Исследования биологического синтеза витамин K-зависимых белков в клетках BHK и CHO показали, что карбоксилаза присутствует как в эндоплазматическом ретикулуме (ER), так и в комплексе Гольджи и что пропептид, содержащий участок распознавания карбоксилазы, расщепляется после завершения гамма-карбоксилирования.
Обсуждалось, может ли пропептид стимулировать активность карбоксилазы (Sigiura, I. et al. (1997) Proc. Natl. Acad. Sci., 9, 9069-9074, Knobloch and Suttie (1987) J. Biol. Chem. 262, 15334-15337, Furie et al. (1999) Blood, 93, 1798-1808).
Свертывание крови представляет собой процесс, состоящий из сложного взаимодействия различных компонентов крови или факторов, которые, возможно, приводят к образованию фибринового тромба. В целом, компоненты крови, которые принимают в этом участие, упоминаются как "система" свертывания, представляют собой проферменты или зимогены, ферментативно неактивные белки, которые преобразуются в протеолитические ферменты под действием активатора, самого активированного фактора свертывания. Факторы свертывания, которые подвергаются такому преобразованию, в целом упоминаются как "активные факторы" и обозначаются путем добавления нижнего индекса "a" (например, активированный фактор VII (FVIIa)).
Активированный фактор X (FXa) является необходимым для преобразования протромбина в тромбин, который затем преобразует фибриноген в фибрин, в качестве конечной стадии при формировании фибринового тромба. Существуют две системы или два пути, которые способствуют активации FX. "Внутренний путь" относится к тем реакциям, которые приводят к образованию тромбина путем использования факторов, присутствующих только в плазме. В конце концов, ряд опосредованных протеазами процессов активирования генерирует фактор IXa, который в сочетании с фактором VIIIa расщепляет FX до FXa. Подобный же протеолиз осуществляется с помощью FVIIa и его кофактора, тканевого фактора, на "внешнем пути" свертывания крови. Тканевый фактор представляет собой связанный с мембраной белок и обычно не может циркулировать в плазме крови. Однако при разрушении сосуда он может образовывать комплекс с FVIIa с катализом активирования FX или активированием фактора IX в присутствии Ca++ и фосфолипида. Хотя относительная важность двух путей свертывания при гемостазе является неясной, в последние годы, как было обнаружено, FVII и тканевой фактор играют главную роль в регуляции свертывания крови.
FVII представляет собой гликопротеин, присутствующий в малых количествах в плазме, который циркулирует в крови в виде одноцепочечного зимогена. Зимоген не является активным по отношению к свертыванию. Одноцепочечный FVII может быть преобразован в двухцепочечный FVIIa с помощью FXa, фактора XIIa, фактора IXa или тромбина in vitro. FXa, как предполагается, является главным физиологическим активатором FVII. Подобно нескольким другим белкам плазмы, вовлеченным в гемостаз, FVII зависит от витамина K при его биосинтезе, который является необходимым для гамма-карбоксилирования 10 остатков глутаминовой кислоты в аминоокончании белка. Внутриклеточная посттрансляционная обработка FVII имеет место в эндоплазматическом ретикулуме (ER) и в комплексе Гольджи. Наряду с витамин K-зависимым гамма-карбоксилированием FVII подвергается ограниченному протеолизу для удаления пропептида с N-окончанием и для гликозилирования аспарагина-145 и -322 и серина-52 и -60 (фиг.1).
Остатки гамма-карбоксилированной глутаминовой кислоты (Gla) являются необходимыми для связанного с металлом взаимодействия FVII с фосфолипидами.
В присутствии фактора тканей, фосфолипидов и ионов кальция двухцепочечный FVIIa быстро активирует FX или фактор IX с помощью ограниченного протеолиза.
Белок C представляет собой серинпротеазу и встречающийся в природе антикоагулянт, который играет определенную роль в регуляции гомеостаза путем инактивирования факторов Va и VIIIa в системе свертывания крови. Белок C человека in vivo производится, прежде всего, в печени в виде одного полипептида из 461 аминокислоты. Эта одноцепочечная молекула-предшественник подвергается множеству посттрансляционных модификаций, включая карбоксилирование девяти остатков глутаминовой кислоты, приводящее к возникновению девяти остатков Gla.
Белок S также демонстрирует антикоагулянтную активность в анализах свертывания in vitro. Белок S демонстрирует активность антикоагулянтного кофактора для активированного белка C. Также, как показано, белок S представляет собой антикоагулянтный фактор в отсутствие активированного белка C, поскольку он может ингибировать активность протромбиназы в анализах, не использующих активированный белок C, и связывается с фактором Va или фактором Xa и функционирует в качестве антикоагулянта без активированного белка C.
Белок S представляет собой физиологически очень важный противотромботический фактор, поскольку наследственные или приобретенные дефициты белка S ассоциируются с венозным и артериальным тромботическим заболеванием. Дефицит свободного белка S при нормальном уровне белка S, в целом, описан у некоторых пациентов с тромботическим заболеванием.
Часто является необходимым селективно блокировать систему свертывания крови у пациента. Антикоагулянты, такие как белок C или белок S, могут быть использованы, например, во время почечного диализа или для лечения глубокого тромбоза вен, диссеминированного внутрисосудистого свертывания (DIG), пациента с риском острого тромбоза, дефицита белка S, сепсиса, воспаления, рака пациентов, подвергающихся хирургической операции, и обладателей других медицинских расстройств.
Остеокальцин состоит из 49 аминокислотных остатков, которые включают в себя три остатка Gla. Функция этого белка, как предполагается, заключается в подавлении избыточной минерализации. Остеокальцин представляет собой специфический белок костей, который секретируется остеобластами. Фракция вновь синтезированного остеокальцина высвобождается в поток крови, где его концентрация коррелирует с показателями активности остеобластов и скорости формирования костей. У людей изменения в уровнях циркулирующего остеокальцина связываются с метаболическими заболеваниями костей, такими как остеопороз и гиперпаратироидизм.
Матриксный белок Gla (MGP) состоит из 79 аминокислот, включая 5 остатков Gla. Этот белок обычно обнаруживается в деминерализованном матриксе и, как предполагается, выполняет определенную функцию при инициации формирования костей.
В данной области продолжает существовать необходимость в усовершенствованных системах для получения рекомбинантных витамин K-зависимых белков и конкретных рекомбинантных факторов свертывания. Настоящее изобретение удовлетворяет эту необходимость путем создания способа, который дает более эффективное, быстрое получение и/или более высокий выход рекомбинантных витамин K-зависимых белков, в частности FVII.
Описание изобретения
Настоящее изобретение относится к новому способу для получения витамин K-зависимых белков и, в частности, фактора свертывания VII (FVII).
Стадии процессинга N-окончаний и, в частности, гамма-карбоксилирования остатков глутаминовой кислоты витамин K-зависимых белков, как показано, представляют собой лимитирующие стадии при биосинтезе этих белков, как показано авторами настоящего изобретения относительно FVII. Способ для увеличения гамма-карбоксилирования, как показано, увеличивает экспрессию рекомбинантных витамин K-зависимых белков.
Пропептид витамин K-зависимых белков является наиболее важным для связывания с карбоксилазой и он должно быть ковалентно присоединен к витамин K-зависимому белку в том же порядке, как для остатков Glu, где будет карбоксилироваться N-окончание будущего зрелого белка. Авторы предполагают, что свободный пропептид функционирует в качестве молекулы для аллостерической регуляции, в том смысле, что, когда концентрация свободного пропептида увеличивается, активность процесса гамма-карбоксилирования также увеличивается.
Прямое увеличение концентрации свободных пропептидов может быть получено путем совместной экспрессии свободного пропептида (свободных пропептидов) самого по себе. Это может быть проделано путем трансфицирования с помощью полинуклеотида, кодирующего свободный пропептид (свободные пропептиды), с мутациями и посттрансляционными модификациями или без них, в одной или нескольких копиях, и совместной экспрессии его вместе с полинуклеотидом, кодирующим витамин K-зависимый белок. Последний может содержать пропептидную последовательность, иную, чем та, которая обычно ассоциируется с витамин K-зависимым белком. Экспрессия полинуклеотида, кодирующего витамин K- зависимый белок, может быть получена либо путем трансфекции в клетку гена, представляющего интерес, либо путем активирования (то есть включения) эндогенного гена, кодирующего витамин K- зависимый белок, уже присутствующего в первичных, вторичных или иммортализованных клетках, взятых у позвоночных, который обычно не экспрессируется в клетках или не экспрессируется в клетках при физиологически значимых уровнях в том виде, в котором эти клетки получены. Для активирования генов, представляющих интерес, гомологичная рекомбинация может быть использована для замены или выключения регуляторной области, обычно ассоциируемой с геном, в клетках в том виде, как они получены, с помощью регуляторной последовательности, которая вызывает экспрессию гена при уровнях, более высоких, чем это проявляется в соответствующей нетрансфицированной клетке, или для проявления структуры регуляции или индукции, которая отличается от той, которую демонстрирует соответствующая нетрансфицированная клетка.
В первом аспекте настоящее изобретение относится к эукариотической клетке-хозяину, экспрессирующей первый полинуклеотид, кодирующий первый пропептид и FVII или его варианты, в первой единице экспрессии и экспрессирующей второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии. Необходимо понять, что первый полинуклеотид располагается в первой единице экспрессии и что второй полинуклеотид располагается во второй единице экспрессии, где первая и вторая единицы экспрессии являются различными.
Во втором аспекте настоящее изобретение относится к эукариотической клетке-хозяину, трансфицированной первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицированной вторым полинуклеотидом, кодирующим второй свободный пропептид во второй единице экспрессии. Необходимо понять, что первый полинуклеотид располагается в первой единице экспрессии и что второй полинуклеотид располагается во второй единице экспрессии, где первая и вторая единицы экспрессии являются различными. Реальный порядок трансфицирования является, разумеется, тривиальным и, таким образом, клетка-хозяин может трансфицироваться сначала вторым полинуклеотидом или наоборот. Использование терминов "первый пропептид" и "второй пропептид" производится исключительно для удобства, таким образом, первый и второй пропептиды могут быть одинаковыми или различными.
Термин "эукариотическая клетка-хозяин", как здесь используется, представляет любую клетку, включая гибридные клетки, в которые может экспрессироваться гетерологичная ДНК. Типичные клетки-хозяева включают в себя, но не ограничиваются этим, клетки насекомых, клетки дрожжей, клетки млекопитающих, включая клетки человека, такие как клетки BHK, CHO, HEK и COS. При осуществлении настоящего изобретения клетки-хозяева, которые культивируются, предпочтительно, представляют собой клетки млекопитающих, более предпочтительно, устоявшуюся линию клеток млекопитающего, включая, без ограничения, линии клеток CHO (например, ATCC CCL 61), COS-1 (например, ATCC CRL 1650), почек детеныша хомячка (BHK) и HEK 293 (например, ATCC CRL 1573; Graham et al., J. Gen. Virol. 36:59-72, 1977).
Предпочтительная линия клеток BHK представляет собой линию клеток BHK tk- ts13 (Waechter and Baserga, Proc. Natl. Acad. Sci. USA 79:1106-1110, 1982), далее упоминаемые как клетки BHK 570. Линия клеток BHK 570 является доступной от Американской коллекции типовых культур, 12301 Parklawn Dr., Rockville, MD 20852, под номером доступа ATCC CRL 10314. Линия клеток BHK tk- ts13 является также доступной от ATCC под номером доступа CRL 1632.
Другие пригодные для использования линии клеток включают в себя, без ограничения, Rat Hep I (гепатома крысы; ATCC CRL 1600), Rat Hep II (гепатома крысы; ATCC CRL 1548), TCMK (ATCC CCL 139), легкие человека (ATCC HB 8065), NCTC 1469 (ATCC CCL 9.1) и клетки DUKX (Urlaub and Chasin, Proc. Natl. Acad. Sci. USA 77:4216-4220, 1980). Также пригодными для использования являются клетки 3T3, клетки Namalwa, миеломы и продукты слияния миелом с другими клетками.
Термин "полинуклеотид" обозначает одно- или двухцепочечный полимер из деоксирибонуклеотидных или рибонуклеотидных оснований, отсчитываемых от 5' до конца 3'. Полинуклеотиды включают в себя РНК и ДНК и могут быть выделены из природных источников, синтезированы in vitro или получены из сочетания природных и синтетических молекул. Длина полинуклеотидной молекулы приводится здесь как число нуклеотидов (сокращенно "nt") или пар оснований (сокращенно "bp"). Термин "нуклеотиды" используется как для одно-, так и для двухцепочечных молекул, когда контекст это позволяет. Когда термин применяется к двухцепочечным молекулам, он используется для обозначения общей длины и понимается как эквивалент термина "пары оснований". Специалист в данной области заметит, что две цепочки двухцепочечного полинуклеотида могут слегка отличаться по длине и что их концы могут не совпадать друг с другом, как результат ферментативного расщепления; таким образом, не все нуклеотиды внутри двухцепочечной полинуклеотидной молекулы могут быть парными. Такие непарные концы, как правило, не превосходят в длину 20 nt.
Термин "пропептид", как используется здесь, представляет любую последовательность аминокислот, которая может связывать гамма-глутамилкарбоксилазу. Типичные пропептиды, которые управляют гамма-карбоксилированием витамин K-зависимых белков, обнаружены на N-окончании витамин K-зависимого белка и служат в качестве участка стыковки или распознающей последовательности для взаимодействия с гамма-глутамилкарбоксилазой, которая карбоксилирует глутаматные остатки, обычно расположенные в домене Gla витамин K-зависимых белков. В одном пропептиде может существовать более чем один участок связывания для гамма-глутамилкарбоксилазы, то есть распознающая последовательность гамма-глутамилкарбоксилазы. Один из примеров пропептида, попадающего под это определение, представляет собой таким образом последовательность природного пропептида FVII. Другой пример, попадающий под это определение, представляет собой последовательность природного пропептида FVII, соединенную с последовательностью природного пропептида фактора IX, внутри одной и той же аминокислотной последовательности.
Термин "свободный пропептид", как используется здесь, предназначается для обозначения пропептида, который не связан с витамин K-зависимым белком, который должен быть гамма-карбоксилирован. Пример свободного пропептида представляет собой таким образом пропептид FVII, который не связан с аминокислотной последовательностью FVII.
Термины "фактор VII" или "FVII", как используются здесь, обозначают продукт, состоящий из неактивированной формы (фактор VII). Термины "фактор VIIa" или "FVIIa", как используются здесь, обозначают продукт, состоящий из активированной формы (фактор VIIa). Это включает в себя белки, которые имеют аминокислотную последовательность 1-406 нативного фактора FVII или FVIIa человека. Это также включает в себя белки со слегка модифицированной аминокислотной последовательностью, например модифицированный конец с N-окончанием, включая добавления или устранение аминокислот N-окончания, постольку, поскольку эти белки, по существу, сохраняют активность FVIIa. "FVII" или "FVIIa", попадающие под это определение, также включают в себя природные аллельные вариации, которые могут существовать и переходить от одного индивидуума к другому. Кроме того, степень и расположение гликозилирования или других посттрансляционных модификаций может изменяться в зависимости от выбранных клеток-хозяев и природы окружающей среды для клеток-хозяев.
Термин "варианты", как используется здесь, предназначен для обозначения FVII, где один или несколько аминокислотных остатков исходного белка замещены другим аминокислотным остатком, и/или где один или несколько аминокислотных остатков исходного белка устранены, и/или где один или несколько аминокислотных остатков добавлены к исходному белку. Такое добавление может иметь место либо на N-окончании, либо на C-окончании исходного белка, либо на них обоих.
Термин "единица экспрессии", как используется здесь, обозначает полинуклеотид, содержащий следующие соединенные при их действии элементы: (a) промотор транскрипции; (b) полинуклеотидную последовательность, кодирующую аминокислотную последовательность; и (c) терминатор транскрипции. Пример единицы экспрессии, таким образом, представляет собой ДНК вектор, содержащий следующие связанные элементы: (a) промотор транскрипции, (b) последовательность кДНК, кодирующую свободный пропептид; и (c) терминатор транскрипции.
Термин "вектор", как используется здесь, обозначает любой объект из нуклеиновых кислот, способный к амплификации в клетке-хозяине. Таким образом, вектор может представлять собой автономно реплицирующийся вектор, то есть вектор, который существует в виде экстрахромосомального объекта, репликация которого является независимой от хромосомальной репликации, например плазмиду. Альтернативно, вектор может быть таким, который, когда он вводится в клетку-хозяина, интегрируется в геном клетки-хозяина и реплицируется вместе с хромосомой (хромосомами), в которые он интегрируется. Выбор вектора часто зависит от клетки-хозяина, в которую он должен вводиться. Векторы включают в себя, но не ограничиваются этим, плазмидные векторы, фаговые векторы, вирусные векторы или космиды. Векторы обычно содержат репликатор и, по меньшей мере, один селектируемый ген, то есть ген, который кодирует продукт, который является легкодетектируемым или присутствие которого является существенным для роста клеток.
Термин "промотор" обозначает часть гена, содержащую последовательности ДНК, которые обеспечивают связывание РНК полимеразы и инициацию транскрипции. Промоторные последовательности часто, но не всегда, находятся в 5' некодирующих областях генов.
В третьем аспекте настоящее изобретение относится к эукариотической клетке-хозяину, экспрессирующей первый полинуклеотид, кодирующий первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и экспрессирующей второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии.
В дополнительном аспекте настоящее изобретение относится к эукариотической клетке-хозяину, трансфицированной первым полинуклеотидом, кодирующим первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и трансфицированной вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии.
Термин "витамин K-зависимый белок", как используется здесь, обозначает любой белок, который является гамма-карбоксилированным по остаткам глутаминовой кислоты. Типичные витамин K-зависимые белки включают в себя, но не ограничиваются этим, прокоагулянтные факторы: тромбин, фактор VII, IX и X; антикоагулянты: белок C и белок S и другие белки, такие как остеокальцин (белок Gla костей), матричный белок Gla и обогащенный пролином белок Gla 1.
В дополнительном аспекте настоящее изобретение относится к способу получения FVII или его вариантов, включающему a) экспрессию в эукариотическую клетку первого полинуклеотида, кодирующего первый пропептид и FVII или его варианты, в первой единице экспрессии и экспрессию второго полинуклеотида, кодирующего второй свободный пропептид, во второй единице экспрессии с получением коэкспрессирующей эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде коэкспрессирующей эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к способу получения FVII или его вариантов, включающему a) экспрессию в эукариотическую клетку первого полинуклеотида, кодирующего первый пропептид и FVII или его варианты, в первой единице экспрессии и экспрессию второго полинуклеотида, кодирующего второй свободный пропептид, во второй единице экспрессии с получением коэкспрессирующей эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде коэкспрессирующей эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение FVII или его вариантов из среды.
В дополнительном аспекте настоящее изобретение относится к способу получения FVII или его вариантов, включающему a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к способу получения FVII или его вариантов, включающему a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение FVII или его вариантов из среды.
В дополнительном аспекте настоящее изобретение относится к способу получения FVIIa или его вариантов, включающему a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение и активирование FVII или его вариантов из среды.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному вектору, где указанный вектор содержит полинуклеотид, кодирующий свободный пропептид, в единице экспрессии. Воплощения, описанные ниже по отношению ко второму полинуклеотиду, второму свободному пропептиду и второй единице экспрессии, являются предопределенными, индивидуально или в сочетании, также для представления воплощений полинуклеотида, свободного пропептида и единицы экспрессии, заключенных в рекомбинантном векторе.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному вектору, где указанный вектор содержит первый полинуклеотид, кодирующий первый пропептид и FVII или его варианты, в первой единице экспрессии и второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному вектору, где указанный вектор содержит первый полинуклеотид, кодирующий первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии.
В дополнительном аспекте настоящее изобретение относится к способу получения эукариотической клетки-хозяина, продуцирующей FVII, включающему a) генную активацию в эукариотической клетке-хозяине первого полинуклеотида, кодирующего аминокислотную последовательность от -18 до 406, FVII и его пропептида, в первой единице экспрессии и b) трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии. В этой связи аминокислотная последовательность от -18 до -1 является идентичной пропептиду FVII, идентифицируемому как SEQ ID NO:7.
В дополнительном аспекте настоящее изобретение относится к способу получения эукариотической клетки-хозяина, продуцирующей FVII или его варианты, включающему a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и b) трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии.
В дополнительном аспекте настоящее изобретение относится к способу получения витамин K-зависимого белка, включающему a) экспрессию в эукариотическую клетку-хозяина первого полинуклеотида, кодирующего первый пропептид и витамин K- зависимый белок, в первой единице экспрессии и экспрессию второго полинуклеотида, кодирующего второй свободный пропептид, во второй единице экспрессии с получением коэкспрессирующей эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде коэкспрессирующей эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к способу получения витамин K-зависимого белка, включающему a) экспрессию в эукариотическую клетку-хозяина первого полинуклеотида, кодирующего первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и экспрессию второго полинуклеотида, кодирующего второй свободный пропептид, во второй единице экспрессии с получением коэкспрессироующей эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде коэкспрессирующей эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение витамин K-зависимого белка из среды.
В дополнительном аспекте настоящее изобретение относится к способу получения витамин K-зависимого белка, включающему a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к способу получения витамин K-зависимого белка, включающему a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение витамин K-зависимого белка из среды.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному FVII или к его вариантам, получаемым с помощью способа, включающего a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному FVII или к его вариантам, получаемым с помощью способа, включающего a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение FVII или его вариантов из среды.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному FVIIa или его вариантам, получаемым с помощью способа, включающего a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его варианты, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение и активирование FVII или его вариантов из среды.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному витамин K-зависимому белку, получаемому с помощью способа, включающего a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида.
В дополнительном аспекте настоящее изобретение относится к рекомбинантному витамин K-зависимому белку, получаемому с помощью способа, включающего a) трансфицирование эукаротической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и витамин K-зависимый белок, в первой единице экспрессии и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии с получением котрансфицированной эукариотической клетки-хозяина; b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина при условиях, которые дают возможность для экспрессии первого полинуклеотида и второго полинуклеотида; и c) выделение витамин K-зависимого белка из среды.
Первый пропептид может быть таким пропептидом, обычно ассоциируемым с витамин K-зависимым белком, или он может быть любым другим пропептидом, таким как пропептид, обычно ассоциируемый с другим витамин K-зависимым белком.
В одном из воплощений первый пропептид содержит одну связывающую последовательность для гамма-глутамилкарбоксилазы. В другом воплощении первый пропептид содержит две или более связывающих последовательностей для гамма-глутамилкарбоксилазы. Пример первого пропептида представляет собой таким образом пропептиды, обычно ассоциируемые с FVII и с протромбином, ковалентно присоединенным к той же единице экспрессии.
В дополнительном воплощении второй свободный пропептид содержит одну связывающую последовательность для гамма-глутамилкарбоксилазы. В дополнительном воплощении второй свободный пропептид содержит две или более связывающих последовательностей для гамма-глутамилкарбоксилазы. Пример второго свободного пропептида представляет собой таким образом пропептиды, обычно ассоциируемые с FVII и протромбином, ковалентно присоединенным к той же единице экспрессии.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин экспрессирует первый полинуклеотид, кодирующий первый пропептид и FVII, в первой единице экспрессии и экспрессирует второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии. В конкретном воплощении FVII представляет собой FVII человека.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин трансфицируется первым полинуклеотидом, кодирующим первый пропептид и FVII, в первой единице экспрессии и трансфицируется вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии. В конкретном воплощении FVII представляет собой FVII человека.
В дополнительном воплощении настоящего изобретения витамин K-зависимый белок независимо выбирается из протромбина, фактора IX, FVII, фактора X, белка C, белка S, остеокальцина, обогащенного пролином белка Gla 1 или матриксного белка Gla. Необходимо понять, что любой из этих белков составляет альтернативное воплощение настоящего изобретения.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин дополнительно трансфицируется полинуклеотидом, кодирующим гамма-глутамилкарбоксилазу, в единице экспрессии. Эта единица экспрессии может быть единицей экспрессии, отличной от первой или второй единицы экспрессии, или полинуклеотид, кодирующий гамма-глутамилкарбоксилазу, может быть расположен в первой или второй единице экспрессии. Примеры гамма-глутамилкарбоксилаз выбираются из рекомбинантной карбоксилазы человека, крысы, дрозофилы, гамма-глутамилкарбоксилазы мышц мыши или хомячка.
В дополнительном воплощении настоящего изобретения первый пропептид содержит аминокислотную последовательность формулы:
X1X2FX3X4X5X6X7X8X9X10X11X12X13X14X15X16X17,
где X1, X4, X5, X6, X7, X9, X10 и X13 являются независимо выбранными из
G, P, A, V, L, I, M, C, F, Y, W, H, K, R, Q, N, E, D, S и T
и где X2, X3, X11 и X12 являются независимо выбранными из
V, L, P, N, A, I, S, F, M, W, Q, T и Y,
и где X8 является независимо выбранным из
G и A,
и где X14, X15, X16 и X17 являются независимо выбранными из
R, H, A, T, W, L, I, V, Q, K, Y, P или отсутствуют.
В одном из воплощений первого пропептида X1 является выбранным из A, S, N, R, T и H.
В дополнительном воплощении первого пропептида X2 является выбранным из V, L, P, N и A.
В дополнительном воплощении первого пропептида X3 является выбранным из L, I, V и S.
В дополнительном воплощении первого пропептида X4 является
выбранным из S, R, N, T, D и A.
В дополнительном воплощении первого пропептида X5 является выбранным из R, Q, K, G, H, S и P.
В дополнительном воплощении первого пропептида X6 является выбранным из E, R и Q.
В дополнительном воплощении первого пропептида X7 является выбранным из Q, N, E, K и R.
В дополнительном воплощении первого пропептида X8 является выбранным из A и G.
В дополнительном воплощении первого пропептида X9 является выбранным из N, H, S и R.
В дополнительном воплощении первого пропептида X10 является выбранным из Q, N, T, G, S, K и E.
В дополнительном воплощении первого пропептида X11 является выбранным из V, I, F и L.
В дополнительном воплощении первого пропептида X12 является выбранным из L, I и V.
В дополнительном воплощении первого пропептида X13 является выбранным из Q, A, S, H, V, K, N и R.
В дополнительном воплощении первого пропептида X14 является выбранным из R, H, K, I и P или отсутствует.
В дополнительном воплощении первого пропептида X15 является выбранным из R, H, K, Q, V, Y, P, A, T, W и L или отсутствует.
В дополнительном воплощении первого пропептида X16 является выбранным из R, H, T, Q, K, Y и P или отсутствует.
В дополнительном воплощении первого пропептида X17 является выбранным из R, H и K или отсутствует.
В дополнительном воплощении первого пропептида X17 представляет собой R.
В настоящем описании аминокислотные остатки представлены с использованием сокращений, как указано в таблице 1, одобренных комиссией IUPAC-IUB по Биохимической номенклатуре (CBN). По отношению к аминокислотам и тому подобному, имеющим изомеры, те которые представлены следующими далее сокращениями, находятся в природной L-форме. Далее, левые и правые концы аминокислотной последовательности пептида представляют собой соответственно N- и C-окончания, если не указано иного.
В дополнительном воплощении настоящего изобретения первый пропептид содержит аминокислотную последовательность с константой ингибирования (Ki), меньшей чем 1 мМ. В дополнительном воплощении аминокислотная последовательность имеет Ki, меньшую чем 0,5 мм. Еще в одном воплощении аминокислотная последовательность имеет Ki в пределах между 0,1 нм и 0,5 мм.
В дополнительном воплощении настоящего изобретения первый пропептид содержит аминокислотную последовательность, по меньшей мере, с 30% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении первый пропептид содержит аминокислотную последовательность, по меньшей мере, с 40% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении первый пропептид содержит аминокислотную последовательность, по меньшей мере, с 50% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения первый пропептид содержит аминокислотную последовательность с Ki, меньшей чем 1 мМ, и по меньшей мере, с 30% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения первый пропептид содержит конкретную аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения второй свободный пропептид содержит аминокислотную последовательность формулы:
X1X2FX3X4X5X6X7X8X9X10X11X12X13X14X15X16X17,
где X1, X4, X5, X6, X7, X9, X10 и X13
являются независимо выбранными из
G, P, A, V, L, I, M, C, F, Y, W, H, K, R, Q, N, E, D, S и T
и где X2, X3, X11 и X12 являются независимо выбранными из
V, L, P, N, A, I, S, F, M, W, Q, T и Y,
и где X8 является независимо выбранным из
G и A,
и где X14, X15, X16 и X17 являются независимо выбранными из
R, H, A, T, W, L, I, V, Q, K, Y, P или отсутствуют.
В одном из воплощений второго свободного пропептида X1 является выбранным из A, S, N, R, T и H.
В дополнительном воплощении второго свободного пропептида X2 является выбранным из V, L, P, N и A.
В дополнительном воплощении второго свободного пропептида X3 является выбранным из L, I, V и S.
В дополнительном воплощении второго свободного пропептида X4 является выбранным из S, R, N, T, D и A.
В дополнительном воплощении второго свободного пропептида X5 является выбранным из R, Q, K, G, H, S и P.
В дополнительном воплощении второго свободного пропептида X6 является выбранным из E, R и Q.
В дополнительном воплощении второго свободного пропептида X7 является выбранным из Q, N, E, K и R.
В дополнительном воплощении второго свободного пропептида X8 является выбранным из A и G.
В дополнительном воплощении второго свободного пропептида X9 является выбранным из N, H, S и R.
В дополнительном воплощении второго свободного пропептида X10 является выбранным из Q, N, T, G, S, K и E.
В дополнительном воплощении второго свободного пропептида X11 является выбранным из V, I, F и L.
В дополнительном воплощении второго свободного пропептида X12 является выбранным из L, I и V.
В дополнительном воплощении второго свободного пропептида X13 является выбранным из Q, A, S, H, V, K, N и R.
В дополнительном воплощении второго свободного пропептида X14 является выбранным из R, H, K, I и P или отсутствует.
В дополнительном воплощении второго свободного пропептида X15 является выбранным из R, H, K, Q, V, Y, P, A, T, W и L или отсутствует.
В дополнительном воплощении второго свободного пропептида X16 является выбранным из R, H, T, Q, K, Y и P или отсутствует.
В дополнительном воплощении второго свободного пропептида X17 является выбранным из R, H, T, Q, K, Y и P или отсутствует.
В дополнительном воплощении настоящего изобретения второй свободный пропептид содержит аминокислотную последовательность с Ki, меньшей чем 1 мМ. В дополнительном воплощении аминокислотная последовательность имеет Ki, меньшую чем 0,5 мМ. Еще в одном воплощении аминокислотная последовательность имеет Ki в пределах между 0,1 нМ и 0,5 мМ.
В дополнительном воплощении настоящего изобретения второй пропептид содержит аминокислотную последовательность, по меньшей мере, с 30% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении второй пропептид содержит аминокислотную последовательность, по меньшей мере, с 40% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении второй пропептид содержит аминокислотную последовательность, по меньшей мере, с 50% гомологией с последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения второй свободный пропептид содержит аминокислотную последовательность с Ki, меньшей чем 1 мМ и, по меньшей мере, с 30% гомологией с конкретной последовательностью, независимо выбранной из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения второй свободный пропептид содержит конкретную аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин представляет собой клетку дрожжей.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин представляет собой клетку насекомого.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин представляет собой клетку млекопитающего.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин представляет собой клетку человека.
В дополнительном воплощении настоящего изобретения эукариотическая клетка-хозяин является независимо выбранной из клеток BHK, клеток HEK, клеток COS или клеток CHO.
В дополнительном воплощении настоящего изобретения первый полинуклеотид представляет собой ДНК.
В дополнительном воплощении настоящего изобретения второй полинуклеотид представляет собой ДНК.
В дополнительном воплощении настоящего изобретения первый полинуклеотид представляет собой РНК.
В дополнительном воплощении настоящего изобретения второй полинуклеотид представляет собой РНК.
В дополнительном воплощении настоящего изобретения первая единица экспрессии присутствует на первом векторе и вторая единица экспрессии присутствует на втором отдельном векторе.
В дополнительном воплощении настоящего изобретения первая единица экспрессии и вторая единица экспрессии присутствуют на одном и том же векторе.
В дополнительном воплощении настоящего изобретения первый вектор представляет собой плазмидный вектор.
В дополнительном воплощении настоящего изобретения второй вектор представляет собой плазмидный вектор.
В дополнительном воплощении настоящего изобретения первый вектор представляет собой фаговый вектор.
В дополнительном воплощении настоящего изобретения второй вектор представляет собой фаговый вектор.
В дополнительном воплощении настоящего изобретения культуральная среда представляет собой среду, не содержащую сыворотки.
В дополнительном воплощении настоящего изобретения первый полинуклеотид представляет собой плазмидную ДНК.
В дополнительном воплощении настоящего изобретения второй полинуклеотид представляет собой плазмидную ДНК.
Термин "связывающая последовательность для гамма-глутамилкарбоксилазы", как используется здесь, обозначает необходимые аминокислотные остатки в последовательности (то есть в распознающей последовательности) для связывания или стыковки, или взаимодействия с гамма-глутамилкарбоксилазой.
В дополнительном воплощении настоящего изобретения первый пропептид имеет более высокое сродство (как измеряется с помощью константы ингибирования (Ki)) к карбоксилазе, чем второй свободный пропептид. Предусматриваются две раздельные функции пропептидов витамин K-зависимого белка относительно карбоксилазы, связывание субстрата и регуляция активности, различные степени сродства и концентрации ковалентно присоединенного пропептида и свободного пропептида могут воздействовать на общую способность продуцирующей клетки к карбоксилированию рекомбинантного витамин K-зависимого белка. Совместную экспрессию свободного пропептида и ковалентно присоединенного пропептида и их сочетаний может увеличить продуцирование функционального рекомбинантного FVII (rFVII). В порядке того, чтобы не ингибировать карбоксилирование вновь синтезируемого Glu-содержащего витамин K-зависимого белка, является предпочтительным, чтобы второй свободный пропептид имел более низкое сродство, чем пропептид, ковалентно присоединенный к витамин K-зависимому белку, который должен гамма-карбоксилироваться.
Ki для свободных пропептидов определяются согласно Stanley et al. (Biochemistry, 38, 15681-15687 (1999) и J. Biol. Chem. 274, 16940-16944).
В дополнительном воплощении свободный пропептид, который должен коэкспрессироваться вместе с витамин K-зависимым белком, предпочтительно, выбирается из списков, представленных в таблицах 2 и 3:
Сокращения для аминокислотных остатков
Аминокислотная последовательность пропептидов из витамин K- зависимых белков и консенсусного пропептида
* Stanley et al. (1999) Biochemistry, 38, 15681-15687 и J. Biol. Chem. 274, 16940-16944
Примеры свободных пропептидов, которые должны коэкспрессироваться с витамин K-зависимым белком
Настоящее изобретение также относится к способу получения витамин K-зависимых белков, как рассмотрено выше. Витамин K-зависимые белки, предпочтительно, получают с помощью методик рекомбинантной ДНК. С этой точки зрения, последовательности ДНК, кодирующие витамин K-зависимые белки, могут быть выделены путем приготовления геномной библиотеки или библиотеки кДНК и просмотра на последовательности ДНК, кодирующие весь белок или его часть, путем гибридизации, используя образцы синтетических олигонуклеотидов, в соответствии со стандартными методиками (см., Sambrook et al., Molecular Cloning: A Laboratory Manual. Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, 1989). Для настоящей цели последовательность ДНК, кодирующая белок, предпочтительно, должна происходить от человека, то есть получаться из геномной библиотеки ДНК или библиотеки кДНК человека.
Настоящее изобретение также относится к способу активирования (то есть включения) гена, кодирующего витамин K-зависимый белок, присутствующего в первичных, вторичных или иммортализованных клетках, происходящих от позвоночных, который обычно не экспрессируется в клетках или не экспрессируется в клетках на физиологически значимых уровнях в том виде, как они получены. Гомологичная рекомбинация может быть использована для замены или выключения регуляторной области, обычно ассоциируемой с геном, в клетках в том виде, как они получены, с регуляторной последовательностью, которая должна вызывать экспрессию гена при уровнях, более высоких, чем проявляются у соответствующей нетрансфицированной клетки, или для проявления структуры регуляции или индукции, которая является иной, чем та, которая проявляется в соответствующей нетрансфицированной клетке. Настоящее изобретение, следовательно, также относится к способу получения витамин K-зависимых белков путем включения или активирования эндогенного гена, который кодирует витамин K-зависимый белок в трансфицированных первичных, вторичных или иммортализованных клетках. Активирование эндогенных генов может быть осуществлено, как описывается в патенте США 5968502. Последовательности ДНК, кодирующие витамин K-зависимые белки, могут также быть получены синтетически с помощью установившихся стандартных способов, например фосфоамидитного метода, описанного Beaucage and Caruthers, Tetrahedron Letters 22 (1981), 1859-1869, или метода, описанного Matthes et al., EMBO Journal 3 (1984), 801-805. В соответствии с фосфоамидитным методом олигонуклеотиды синтезируются, например, в автоматическом синтезаторе ДНК, очищаются, отжигаются, лигируются и клонируются в соответствующие векторы.
Последовательности ДНК могут также быть получены с помощью цепной полимеразной реакции с использованием конкретных праймеров, как, например, описывается в патенте США 4683202, Saiki et al., Science 239 (1988), 487-491, или Sambrook et al., выше.
Последовательности ДНК, кодирующие витамин K-зависимые белки, обычно вставляются в рекомбинантный вектор, который может представлять собой любой вектор, который удобно подвергнуть процедурам с рекомбинантной ДНК, и выбор вектора часто будет зависеть от клетки-хозяина, в которую он должен вводиться. Таким образом, вектор может представлять собой автономно реплицирующийся вектор, то есть вектор, который существует в виде экстрахромосомального объекта, репликация которого является не зависимой от хромосомальной репликации, например плазмиду. Альтернативно, вектор может быть таким, который, когда он вводится в клетку-хозяина, интегрируется в геном клетки-хозяина и реплицируется вместе с хромосомой (хромосомами), в которые он интегрируется.
Вектор, предпочтительно, представляет собой экспрессионный вектор, в котором последовательность ДНК, кодирующая витамин K-зависимые белки, при действии является связанной с дополнительными сегментами, требующимися для транскрипции ДНК. Как правило, экспрессионный вектор получают из плазмидной или вирусной ДНК или он может содержать элементы их обоих. Термин "связанный при действии" указывает на то, что сегменты располагаются таким образом, что они функционируют в соответствии с их предполагаемыми задачами, например, транскрипция инициируется в промоторе и осуществляется вдоль последовательности ДНК, кодирующей полипептид.
Промотор может представлять собой любую последовательность ДНК, которая демонстрирует транскрипционную активность в выбранной клетке-хозяине и может быть получена из генов, кодирующих белки, либо гомологичных, либо гетерологичных по отношению к клетке-хозяину.
Примеры соответствующих промоторов для управления транскрипцией ДНК, кодирующей витамин K-зависимый белок в клетках млекопитающих, представляют собой промотор SV40 (Subramani et al., Mol. Cell Biol. 1 (1981), 854-864), промотор MT-1 (ген металлотионеина) (Palmiter et al., Science 222 (1983), 809-814), промотор CMV (Boshart et al., Cell 41:521-530, 1985) или главный поздний промотор аденовируса 2 (Kaufman and Sharp, Mol. Cell. Biol, 2:1304-1319, 1982).
Пример соответствующего промотора для использования в клетках насекомых представляет собой полигедриновый промотор (патент США № 4745051; Vasuvedan et al., FEBS Lett. 311, (1992) 7-11), промотор P10 (J.M. Vlak et al., J. Gen. Virology 69, 1988, pp. 765-776), промотор основного белка вируса полигедроза Autographa californica (Европейский патент EP 397485), непосредственный ранний промотор гена бакуловируса 1 (патент США 5155037; патент США 5162222) или замедленный ранний промотор гена бакуловируса 39K (патент США 5155037; патент США 5162222).
Примеры соответствующих промоторов для использования в клетках-хозяевах дрожжей включают в себя промоторы из гликолитических генов дрожжей (Hitzeman et al., J. Biol. Chem. 255 (1980), 12073-12080; Alber and Kawasaki, J. Mol. Appl. Gen. 1 (1982), 419-434) или гена алкогольдегидрогеназы (Young et al., in Genetic Engineering of Microorganisms for Chemicals (Hollaender et al, eds.), Plenum Press, New York, 1982), или промоторы TPI1 (патент США 4599311) или ADH2-4c (Russell et al., Nature 304 (1983), 652-654).
Примеры соответствующих промоторов для использования в клетках-хозяевах нитеобразных грибов представляют собой, например, промотор ADH3 (McKnight et al., The EMBO J. 4 (1985), 2093-2099) или промотор tpiA. Примеры других пригодных для использования промоторов представляют собой такие, которые получают из гена, кодирующего TAKA-амилазу A.oryzae, аспарагиновую протеиназу Rhizomucor miehei, нейтральную α- амилазу A.niger, стабильную кислотную α-амилазу A.niger, глукоамилазу (gluA) A.niger или A.awamori, липазу Rhizomucor miehei, щелочную протеазу A.oryzae, триозофосфатную изомеразу A.oryzae или ацетамидазу A.nidulans. Предпочтительными являются промоторы TAKA-амилазы и gluA. Соответствующие промоторы рассмотрены, например, в Европейском патенте EP 238023 и Европейском патенте EP 383779.
Последовательности ДНК, кодирующие витамин K-зависимые белки, могут также, если это необходимо, соединяться при действии с соответствующим терминатором, таким как терминатор гормона роста человека (Palmiter et al., Science 222, 1983, pp. 809-814), или терминаторы TPI1 (Alber and Kawasaki, J. Mol. Appl. Gen. 1, 1982, pp. 419-434) или ADH3 (McKnight et al., The EMBO J. 4, 1985, pp. 2093-2099). Вектор может также содержать набор сплайсированных участков РНК, расположенных после промотора и перед участком инсерции самой последовательности VII. Предпочтительные сплайсированные участки РНК могут быть получены из генов аденовируса и/или иммуноглобулина. Также в экспрессируемых векторах содержится сигнал полиаденилирования, расположенный после участка инсерции. Особенно предпочтительные сигналы полиаденилирования включают в себя ранний или поздний сигнал полиаденилирования из SV40 (Kaufman and Sharp, там же), сигнал полиаденилирования из области Elb аденовируса 5, терминатор гена гормона роста человека (DeNoto et al., Nuc. Acids Res. 9:3719-3730, 1981) или сигнал полиаденилирования из гена FVII человека или гена бычьего FVII. Экспрессируемые векторы могут также включать в себя некодирующую лидерную последовательность вируса, такую как тройственная лидерная последовательность аденовируса 2, расположенная между сплайсированными участками промотора и РНК; и энхансерные последовательности, такие как энхансерная последовательность SV40.
Рекомбинантный вектор может дополнительно содержать последовательность ДНК, дающую возможность вектору для репликации в рассматриваемой клетке-хозяине. Пример такой последовательности (когда клетка-хозяин является клеткой млекопитающего) представляет собой репликатор SV40.
Когда клетка-хозяин представляет собой клетку дрожжей, соответствующие последовательности, дающие возможность вектору для репликации, представляют собой гены репликации плазмиды дрожжей 2μ REP 1-3 и репликаторы.
Вектор может также содержать селектируемый маркер, например ген, продукт которого является комплементарным к дефекту в клетке-хозяине, такой как ген, кодирующий дигидрофолиатредуктазу (DHFR) или ген TPI Schizosaccharomyces pombe (описанный P.R. Russell, Gene 40, 1985, pp. 125-130), или ген, который отвечает за устойчивость к лекарственному средству, например ампицилину, канамицину, тетрациклину, хлорамфениколу, неомицину, гигромицину или метотрексату. Для нитеобразных грибов селектируемые маркеры включают в себя amdS, pyrG, argB, niaD или sC.
Для направления витамин K-зависимых белков по настоящему изобретению в секреторный путь клеток-хозяев секреторная сигнальная последовательность (также известная как лидерная последовательность, препропоследовательность или препоследовательность) может быть предусмотрена в рекомбинантном векторе. Секреторная сигнальная последовательность соединяется с последовательностями ДНК, кодирующими витамин K-зависимые белки, в корректной рамке считывания. Секреторные сигнальные последовательности часто располагаются в положении 5' по отношению к последовательности ДНК, кодирующей пептид. Секреторная сигнальная последовательность может представлять собой последовательность, обычно ассоциируемую с белком, или может быть взята из гена, кодирующего другой секретируемый белок.
Для секреции из клеток дрожжей секреторная сигнальная последовательность может кодировать любой сигнальный пептид, который обеспечивает эффективное направление экспрессированных витамин K-зависимых белков в секреторный путь клетки. Сигнальный пептид может представлять собой природный сигнальный пептид или его функциональную часть или это может быть синтетический пептид. Пригодными для использования сигнальными пептидами, как обнаружено, являются α-факторный сигнальный пептид (см., патент США 4870008), сигнальный пептид амилазы слюны мыши (см., O. Hagenbuchle et al., Nature 289, 1981, pp. 643-646), сигнальный пептид модифицированной карбоксипептидазы (см., L.A. Vails et al., Cell 48, 1987, pp. 887-897), сигнальный пептид дрожжей BAR1 (см., заявку на Европейский патент WO 87/02670) или сигнальный пептид аспарагинпротеазы дрожжей 3 (YAP3) (см., M. Egel-Mitani et al., Yeast 6, 1990, pp. 127-137).
Для эффективной секреции в дрожжах последовательность, кодирующая лидерный пептид, также может быть вставлена после сигнальной последовательности и перед последовательностью ДНК, кодирующей витамин K-зависимые белки. Функция лидерного пептида заключается в том, чтобы дать возможность направления экспрессированного пептида из эндоплазматического ретикулума в аппарат Гольджи и далее в секреторный везикул для секреции в культурную среду (то есть для выделения витамин K-зависимых белков через клеточную стенку или, по меньшей мере, через клеточную мембрану в периплазматическое пространство клетки дрожжей). Лидерный пептид может представлять собой лидерную последовательность α-фактора дрожжей (использование которого описано, например, в патенте США 4546082, патенте США 4870008, в Европейском патенте EP 16201, Европейском патенте EP 123294, Европейском патенте EP 123544 и Европейском патенте EP 163529). Альтернативно, лидерный пептид может представлять собой синтетический лидерный пептид, который, так сказать, представляет собой лидерный пептид, который не встречается в природе. Синтетические лидерные пептиды могут, например, быть сконструированы таким образом, как описано в заявке на Европейский патент WO 89/02463 или в заявке на Европейский патент WO 92/11378.
Для использования в нитеобразных грибах сигнальный пептид удобно получать из гена, кодирующего амилазу или глюкоамилазу Aspergillus sp., гена, кодирующего липазу или протеазу Rhizomucor miehei, или липазу Humicola lanuginosa. Предпочтительно, сигнальный пептид получают из гена, кодирующего TAKA-амилазу A.oryzae, нейтральную α-амилазу A.niger, стабильную кислотную амилазу A.niger или глукоамилазу A.niger. Соответствующие сигнальные пептиды описываются, например, в Европейском патенте EP 238023 и в Европейском патенте EP 215594.
Для использования в клетках насекомых сигнальный пептид удобно получать из гена насекомого (см. заявку на Европейский патент WO 90/05783), такой как сигнальный пептид предшественника адипокинетического гормона чешуекрылых Manduca sexta (см. патент США 5023328).
Процедуры, используемые для лигирования последовательностей ДНК, кодирующих витамин K-зависимые белки, промотор и, необязательно, терминатор и/или секреторную сигнальную последовательность, соответственно, и то, как вставлять их в соответствующие векторы, содержащие информацию, необходимую для репликации, хорошо известны специалистам в данной области (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor, New York, 1989).
Способы трансфицирования клеток млекопитающих и экспрессии последовательностей ДНК, введенных в клетки, описываются, например, в Kaufman and Sharp, J. Mol. Biol. 159 (1982), 601-621; Southern and Berg. J. Mol. Appl. Genet. 1 (1982). 327-341; Loyter et al., Proc. Natl. Acad. Sci. USA 79 (1982), 422-426; Wigler et al., Cell 14 (1978), 725; Corsaro and Pearson, Somatic Cell Genetics 7 (1981), 603, Graham and van der Eb. Virology 52 (1973), 456; и Neumann et al., EMBO J. 1 (1982), 841-845.
Селектируемые маркеры могут вводиться в клетку на отдельной плазмиде одновременно с геном, представляющим интерес, или они могут вводиться на той же самой плазмиде. Если они вводятся на одной и той же плазмиде, селектируемый маркер и ген, представляющий интерес, могут находиться под контролем различных промоторов или одного и того же промотора, последняя структура производит двухцистронный сигнал. Конструкции этого типа известны в данной области (например, Levinson and Simonsen, патент США № 4713339). Может также быть выгодным добавление дополнительной ДНК, известной как "ДНК-носитель", к смеси, которая вводится в клетки.
После того как клетки поглощают ДНК, они выращиваются в соответствующей среде роста, как правило, 1-2 дня, чтобы они начали экспрессировать ген, представляющий интерес. Как используется здесь, термин "соответствующая среда роста" обозначает среду, содержащую питательные вещества и другие компоненты, требуемые для роста клеток и экспрессии витамин K-зависимого белка, представляющего интерес. Среды, как правило, включают в себя источник углерода, источник азота, основные аминокислоты, основные сахара, витамины, соли, фосфолипиды, факторы белков и роста. Для получения гамма-карбоксилированных белков среда должна содержать витамин K, предпочтительно, при концентрации примерно от 0,1 мкг/мл примерно до 5 мкг/мл. Затем применяется селекция с помощью лекарственного средства, чтобы выбрать рост клеток, которые экспрессируют селектируемый маркер стабильным образом. Для клеток, которые трансфицированы амплифицирующимся селектируемым маркером, концентрация лекарственного средства может быть увеличена, чтобы выбрать повышенное количество копий клонируемых последовательностей, тем самым повышая уровни экспрессии. Затем клоны стабильно трансфицированных клеток просматриваются на экспрессию витамин K-зависимого белка, представляющего интерес.
Клетка-хозяин, в которую вводятся последовательности ДНК, кодирующие витамин K-зависимые белки, может представлять собой любую клетку, которая способна продуцировать посттрансляционно-модифицированные витамин K-зависимые белки, и включает в себя клетки дрожжей, грибов и высшие эукариотические клетки.
Примеры линий клеток млекопитающих для использования в настоящем изобретении представляют собой линии клеток COS-1 (ATCC CRL 1650), почек детеныша хомячка (BHK) и 293 (ATCC CRL 1573; Graham et al., J. Gen. Virol. 36:59-72, 1977). Предпочтительная линия клеток BHK представляет собой линию клеток BHK tk.sup.-ts13 (Waechterand Baserga, Proc. Natl. Acad. Sci. USA 79:1106-1110, 1982, включен сюда в качестве ссылки), далее упоминаемые как клетки BHK 570. Линия клеток BHK 570 находится в Американской коллекции типовых культур, 12301 Parklawn Dr., Rockville, Md. 20852, под номером доступа ATCC CRL 10314. Линия клеток BHK tk.sup.-ts13 является также доступной под номером доступа ATCC CRL 1632. Кроме того, в настоящем изобретении может быть использован ряд линий клеток, включая Rat Hep I (гепатома крысы; ATCC CRL 1600), Rat Hep II (гепатома крысы; ATCC CRL 1548), TCMK (ATCC CCL 139), легкие человека (ATCC HB 8065), NCTC 1469 (ATCC CCL 9.1), CHO (ATCC CCL 61) и клетки DUKX (Urlaub and Chasin, Proc. Natl. Acad. Sci. USA 77:4216-4220, 1980).
Примеры пригодных для использования клеток дрожжей включают в себя клетки Saccharomyces spp. или Schizosaccharomyces spp. в конкретных штаммах Saccharomyces cerevisiae или Saccharomyces kluyveri. Способы для трансформирования клеток дрожжей с помощью гетерологичной ДНК и продуцирования ими гетерологичных полипептидов описаны, например, в патенте США 4599311, патенте США 4931373, патенте США 4870008, 5037743 и патенте США 4845075, все они включаются сюда в качестве ссылок. Трансформированные клетки выбираются по фенотипу, определяемому селектируемым маркером, часто, по устойчивости к лекарственному средству или по способности расти в отсутствие конкретного питательного вещества, например лейцина. Предпочтительный вектор для использования в дрожжах представляет собой вектор POT1, описанный в патенте США 4931373. Последовательностям ДНК, кодирующим витамин K-зависимые белки, может предшествовать сигнальная последовательность и, необязательно, лидерная последовательность, как, например, описано выше. Другие примеры пригодных для использования клеток дрожжей представляют собой штаммы Kluyveromyces, такие как K.lactis, Hansenula, например H.polymorpha, или Pichia, например P.pastoris (см. Gleeson et al., J. Gen. Microbiol. 132, 1986, p. 3459-3465; патент США 4882279).
Примеры других клеток грибов представляют собой клетки нитеобразных грибов, например Aspergillus spp., Neurospora spp., Fusarium spp. или Trichoderma spp., в частности штаммы A.oryzae, A.nidulans или A.niger. Использование Aspergillus spp. для экспрессии белков описано, например, в Европейском патенте EP 272277, Европейском патенте EP 238023, Европейском патенте EP 184438. Трансформация F. oxysporum может быть осуществлена, например, как описывается в Malardier et al., 1989, Gene 78: 147-156. Трансформация Trichoderma spp. может быть осуществлена, например, как описывается в Европейском патенте EP 244234.
Когда в качестве клетки-хозяина используется клетка нитеобразного гриба, она может быть трансформирована с помощью конструкции ДНК по настоящему изобретению, при этом удобно интегрировать конструкцию ДНК в хромосому хозяина для получения рекомбинантной клетки-хозяина. Эта интеграция, в целом, рассматривается как преимущество, поскольку последовательность ДНК имеет большую вероятность стабильного поддержания в клетке. Интеграция конструкций ДНК в хромосому хозяина может быть осуществлена в соответствии с обычными способами, например, путем гомологичной или гетерологичной рекомбинации.
Трансформация клеток насекомых и продуцирование в них гетерологичных полипептидов может осуществляться, как описывается в патенте США 4745051; патенте США 4879236; патенте США 5155037; 5162222; в Европейском патенте EP 397485; все они включаются сюда в качестве ссылок. Линия клеток насекомых, используемых в качестве хозяев, может соответствующим образом представлять собой линию клеток Lepidoptera, таких как клетки Spodoptera frugiperda или клетки Trichoplusia ni (см. патент США 5077214). Условия культивирования могут соответствующим образом быть такими, как описано, например, в заявках на Европейский патент WO 89/01029 или WO 89/01028 или в любой из указанных выше ссылок.
Трансформированная или трансфицированная клетка-хозяин, описанная выше, затем культивируется в соответствующей питательной среде при условиях, дающих возможность для экспрессии витамин K-зависимого белка, после чего часть полученного пептида (или весь он) может быть извлечена из культуры. Среда, используемая для культивирования клеток, может представлять собой любую обычную среду, пригодную для использования при выращивании клеток-хозяев, такую как минимальные или комплексные среды, содержащие соответствующие вспомогательные вещества. Соответствующие среды являются доступными от коммерческих поставщиков или могут быть приготовлены в соответствии с опубликованными рецептами (например, в каталогах Американской коллекции типовых культур). Затем витамин K-зависимый белок, произведенный клетками, может быть извлечен из культурной среды с помощью обычных процедур, включая выделение клеток-хозяев из среды путем центрифугирования или фильтрования, преципитации белковых компонентов супернатанта или фильтрата посредством соли, например сульфата аммония, очистки с помощью различных хроматографических процедур, например ионообменной хроматографии, гель-фильтрационной хроматографии, аффинной хроматографии или тому подобного в зависимости от типа рассматриваемого полипептида.
Для получения рекомбинантного FVII человека или его вариантов используется клонированная последовательность ДНК FVII дикого типа. Эта последовательность может быть модифицирована, чтобы она кодировала желаемый белок FVII или его варианты. Эта последовательность затем вставляется в экспрессируемый вектор, который, в свою очередь, трансформируется или трансфицируется в клетки-хозяева. Высшие эукариотические клетки, в частности культивируемые клетки млекопитающих, являются предпочтительными в качестве клеток-хозяев. Полные нуклеотидные и аминокислотные последовательности для FVII человека являются известными. См. патент США № 4784950, который включен сюда в качестве ссылки, где описано клонирование и экспрессия рекомбинантного FVII человека. Последовательность бычьего FVII описана в Takeya et al., J. Biol. Chem, 263:14868-14872 (1988), которая включена сюда в качестве ссылки.
Изменения аминокислотной последовательности могут быть получены с помощью различных методик. Модификация последовательности ДНК может представлять собой сайт-специфичный мутагенез. Методики сайт-специфичного мутагенеза хорошо известны в данной области и описаны, например, Zoller and Smith (DNA 3:479-488, 1984). Таким образом, используя нуклеотидные и аминокислотные последовательности FVII, можно вводить желаемые изменения.
Последовательности ДНК для использования в настоящем изобретении, как правило, должны кодировать препропептид на аминоокончании белка FVII для получения соответствующего посттрансляционного процессинга (например, гамма-карбоксилирования остатков глутаминовой кислоты) и секреции из клетки-хозяина. Препропептид может представлять собой пептид из FVII или другого витамин K-зависимого белка плазмы, такого как фактор IX, фактор X, протромбин, белок C или белок S. Как будет понятно специалисту в данной области, могут быть осуществлены дополнительные модификации в аминокислотной последовательности FVII там, где такие модификации не ослабляют значительно способность белка к действию в качестве фактора свертывания. Например, FVII в каталитической триаде также может быть модифицирован в сайте активации расщепления для ингибирования преобразования зимогена FVII в его активированную двухцепочечную форму, как описано в общем виде в патенте США № 5288629, который включен сюда в качестве ссылки.
В настоящем изобретении для производства витамин K- зависимого белка может быть использована технология трансгенных животных. Является предпочтительным производить белки с помощью молочных желез самки млекопитающего-хозяина. Экспрессия в молочные железы и последующая секреция белка, представляющего интерес, в молоко преодолевает многие трудности, встречающиеся при выделении белков из других источников. Молоко легко собирается, доступно в больших количествах и хорошо характеризуется биохимически. Кроме того, главные белки молока присутствуют в молоке при высоких концентрациях (как правило, примерно от 1 до 15 г/л). С коммерческой точки зрения явно является предпочтительным использовать в качестве хозяина виды, которые дают большой выход молока. Хотя более мелкие животные, такие как мыши и крысы, могут быть использованы (и являются предпочтительными на стадии принципиальной проверки), в настоящем изобретении является предпочтительным использовать млекопитающих, составляющих домашний скот, включая, но, не ограничиваясь этим, свиней, коз, овец и крупный рогатый скот. Овцы являются особенно предпочтительными благодаря таким факторам, как предыдущая история трансгенеза у этого вида, выход молока, стоимость и легкая доступность оборудования для сбора овечьего молока. См. WIPO публикацию заявки на Европейский патент WO 88/00239 для сравнения факторов, влияющих на выбор вида-хозяина. Как правило, является желательным выбирать породу животного-хозяина, которая выведена для использования в качестве молочной, такую как Восточно-Фрисландская овца, или для получения молочного скота путем выведения трансгенной линии в последнее время. В любом случае должны использоваться животные с известным хорошим состоянием здоровья.
Для получения экспрессии в молочной железе используется промотор транскрипции из гена белка молока. Гены белка молока включают такие гены, которые кодируют казеины (см. патент США № 5304489, включен сюда в качестве ссылки), бета-лактоглобулин, α-лактальбумин и кислый белок молочной сыворотки. Промотор бета-лактоглобулина (BLG) является предпочтительным. В случае гена овечьего бета-лактоглобулина, как правило, должна использоваться область, по меньшей мере, из ближайших 406 bp из последовательности гена, фланкирующей 5', хотя предпочтительными являются большие по размеру части последовательности, фланкирующей 5', вплоть до примерно 5 kbp, например примерно 4,25 kbp сегмент ДНК, охватывающий промотор, фланкирующий 5', и некодирующую часть гена бета-лактоглобулина. См. Whitelaw et al., Biochem J. 286: 31-39 (1992). Подобные же фрагменты ДНК промотора от других видов также являются пригодными для использования.
Другие области гена бета-лактоглобулина могут также быть включены в конструкции, если они могут содержать геномные области гена, который должен экспрессироваться. В данной области, в целом, принято, что конструкции, где, например, отсутствуют интроны, экспрессируются плохо по сравнению с теми, которые содержат такие последовательности ДНК (см. Brinster et al., Proc. Natl. Acad. Sci. USA 85: 836-840 (1988); Palmiter et al., Proc. Natl. Acad. Sci. USA 88: 478-482 (1991); Whitelaw et al., Transgenic Res. 1: 3-13 (1991); заявки на Европейский патент WO 89/01343 и WO 91/02318, каждая из которых включена сюда в качестве ссылки). В этом отношении является, в целом, предпочтительным там, где возможно, использовать геномные последовательности, содержащие все нативные интроны или некоторые из них, из гена, кодирующего белок или полипептид, представляющий интерес, таким образом, дополнительное включение, по меньшей мере, некоторых интронов, например, из гена бета-лактоглобулина является предпочтительным. Одна из таких областей представляет собой сегмент ДНК, который обеспечивает сплайсинг интрона и полиаденилирование РНК из 3' некодирующей области гена овечьего бета-лактоглобулина. Когда он замещает природные 3' некодирующие последовательности гена, этот сегмент овечьего бета-лактоглобулина может как увеличить, так и стабилизировать уровни экспрессии белка или полипептида, представляющего интерес. В других воплощениях область, окружающая ATG последовательность инициации последовательности, кодирующей витамин K-зависимый белок, заменяется соответствующими последовательностями из гена конкретного белка молока. Такое замещение обеспечивает благоприятное тканьспецифичное окружение инициации для усиления экспрессии. Удобно заменять целиком всю препропоследовательность витамина K-зависимого белка и 5' некодирующие последовательности последовательностями, например, гена BLG, хотя могут заменяться и более мелкие области.
Для экспрессии витамин K-зависимого белка в трансгенных животных сегмент ДНК, кодирующий витамин K-зависимый белок, при действии связан с дополнительными сегментами ДНК, необходимыми для его экспрессии, с целью создания единиц экспрессии. Такие дополнительные сегменты включают в себя указанный выше промотор, а также последовательности, которые обеспечивают терминацию транскрипции и полиаденилирования мРНК. Единицы экспрессии дополнительно должны включать сегмент ДНК, кодирующий секреторную сигнальную последовательность, связанную при действии с сегментом, кодирующим витамин K-зависимый белок. Секреторная сигнальная последовательность может представлять собой нативную секреторную сигнальную последовательность витамин K-зависимого белка или может быть последовательностью другого белка, такого как белок молока. См., например, von Heinje, Nuc. Acids Res. 14: 4683-4690 (1986) и Meade et al., патент США № 4873316, которые включаются сюда в качестве ссылок.
Конструирование единиц экспрессии для использования в трансгенных животных удобно осуществлять путем вставки последовательности, кодирующей витамин K-зависимый белок, в вектор плазмиды или фага, содержащий дополнительные сегменты ДНК, хотя единица экспрессии может быть сконструирована с помощью любой, по существу, последовательности лигирований. Особенно удобно создавать вектор, содержащий сегмент ДНК, кодирующий белок молока, и заменять кодирующую последовательность белка молока последовательностью витамин K-зависимого белка, тем самым создавая ген слияния, который включает контрольные последовательности экспрессии гена белка молока. В любом случае клонирование единиц экспрессии в плазмиды или другие векторы облегчает амплификацию витамин K-зависимого белка. Амплификацию удобно осуществлять в бактериальных (например, E.coli) клетках-хозяевах таким образом, что векторы, как правило, должны включать ориджин репликации и селектируемый маркер, функционирующий в бактериальных клетках-хозяевах.
Затем единица экспрессии вводится в оплодотворенные яйцеклетки (включая эмбрионы на ранних стадиях развития) выбранных видов-хозяев. Введение гетерологичной ДНК может осуществляться с помощью одного из нескольких способов, включая микроинъекцию (например, патент США № 4873191), ретровирусную инфекцию (Jaenisch, Science 240: 1468-1474 (1988)) или сайториентированную интеграцию с использованием эмбриональных стволовых (ES) клеток (обзор Bradley et al., Bio/Technology 10: 534-539 (1992)). Затем яйцеклетки имплантируются в яичники или матки псевдобеременных самок и им дают развиваться до определенного времени. Потомство, несущее ДНК в своей зараженной линии, может переносить ДНК к своему потомству обычным менделевским способом, давая возможность для разведения трансгенных стад.
Общие процедуры для разведения трансгенных животных известны в данной области. См., например, Hogan et al., Manipulating the Mouse Embryo: A Laboratory Manual, Cold Spring Harbor Laboratory, 1986; Simons et al., Biotechnology 6: 179-183 (1988); Wall et al., Biol. Reprod. 32: 645-651 (1985); Buhler et al., Biotechnology 8: 140-143 (1990); Ebert et al., Biotechnology 9: 835-838 (1991); Krimpenfort et al., Bio/Technology 9: 844-847 (1991); Walletal., J. Cell. Biochem. 49: 113-120 (1992); патенты США №№ 4873191 и 4873316; WIPO публикации заявок на Европейские патенты WO 88/00239, WO 90/05188, WO 92/11757 и патент Великобритании GB 87/00458, которые включаются сюда в качестве ссылок. Методики для введения посторонних последовательностей ДНК в млекопитающие и в их зараженные клетки исходно были разработаны для мышей. См., например, Gordon et al., Proc. Natl. Acad. Sci. USA 77: 7380-7384 (1980); Gordon and Ruddle, Science 214: 1244-1246 (1981); Palmiter and Brinster, Cell 41: 343-345 (1985); Brinster et al., Proc. Natl. Acad. Sci. USA 82: 4438-4442 (1985) и Hogan et al. (там же). Впоследствии эти методики были адаптированы для использования на более крупных животных, включая различные виды домашнего скота (см., например, WIPO публикации заявок на Европейские патенты WO 88/00239, WO 90/05188 и WO 92/11757 и Simons et al., Bio/Technology 6: 179-183 (1988)). В итоге, в наиболее эффективном способе, используемом до настоящего времени при генерации трансгенных мышей или домашнего скота, несколько сотен линейных молекул ДНК, представляющей интерес, инъецируются в одно из проядер оплодотворенной яйцеклетки в соответствии с установившимися методиками. Также может быть использована инъекция ДНК в цитоплазму зиготы. Также может быть использовано продуцирование в трансгенных растениях. Экспрессия может быть обобщенной или направленной на конкретный орган, такой как клубень. См. Hiatt, Nature 344:469-479 (1990); Edelbaum et al., J. Interferon Res. 12:449-453 (1992); Sijmons et al., Bio/Technology 8:217-221 (1990) и публикацию EP 255378.
FVII, получаемый по настоящему изобретению, может быть очищен с помощью аффинной хроматографии на колонке с антителом анти-FVII. Является предпочтительным, чтобы иммуноадсорбционная колонка содержала высокоспецифичное моноклональное антитело. Использование кальцийзависимых моноклональных антител, как описано Wakabayashi et al., J. Biol. Chem. 261:11097-11108, (1986) и Thim et al., Biochem. 27: 7785-7793 (1988), которые включаются сюда в качестве ссылок, является особенно предпочтительным. Дополнительная очистка может быть достигнута с помощью обычных средств химической очистки, таких как высокоэффективная жидкостная хроматография. В данной области известны и другие способы очистки, включая преципитацию цитратом бария, и они могут применяться для очистки FVII, описываемой здесь (см., в целом, Scopes, R., Protein, Purification, Springer-Verlag, N.Y., 1982). Для фармацевтических применений предпочтительным является, по существу, чистый FVII с гомогенностью, по меньшей мере, примерно 90-95%, а наиболее предпочтительно, с гомогенностью от 98 до 99% или более. После очистки, частичной или до гомогенности, по желанию, FVII затем может использоваться для терапии.
Преобразование одноцепочечного FVII в активный двухцепочечный FVIIa может быть достигнуто с использованием фактора XIIa, как описано Hedner and Kisiel (1983, J. Clin. Invest. 71: 1836-1841), или с помощью других протеаз, имеющих трипсинподобную специфичность (Kisiel and Fujikawa, Behring Inst. Mitt. 73: 29-42, 1983). Альтернативно, FVII может быть активирован путем пропускания его через ионообменную хроматографическую колонку, такую как mono Q.RTM (Pharmacia Fire Chemicals), или что-либо подобное (Bjoern et al., 1986, Research Disclosures 269:564-565). Молекулы FVII по настоящему изобретению и их фармацевтические композиции являются особенно полезными для введения людям с целью лечения различных состояний, включающих в себя внутрисосудистую коагуляцию.
Витамин K-зависимые белки по настоящему изобретению могут быть использованы для лечения определенных типов гемофилий. Гемофилия A характеризуется отсутствием активного фактора VIII, фактора VIIIa или присутствием ингибирования фактора VIII. Гемофилия B характеризуется отсутствием активного фактора IX, фактора IXa. Дефицит FVII, хотя и является редким, хорошо реагирует на введение фактора VII (Bauer, K. A., 1996, Haemostasis, 26:155-158, suppl. 1). Замещающая терапия с помощью фактора VIII является ограниченной из-за развития высокого титра ингибиторных антител к фактору VIII у некоторых пациентов. Альтернативно, FVIIa может быть использован при лечении гемофилий A и B. Фактор IXa и фактор VIIIa активируют фактор X. Фактор VIIa устраняет необходимость в факторах IX и VIII путем прямого активирования фактора X и может преодолеть проблемы дефицита фактора IX и VIII с немногими иммунологическими последствиями.
Краткое описание чертежей
Настоящее изобретение описывается более подробно в примерах со ссылками на прилагаемые чертежи, где
Фиг.1. Структура корректно процессированного FVII коагуляции человека, аминокислоты от 1 до 406, с гамма-карбоксилированными остатками Glu (γ) и гликозилирования (*). Стрелка на остатке аминокислоты 152 демонстрирует участок, где одноцепочечный FVII расщепляется с преобразованием в активированный двухцепочечный FVII (FVIIa).
Фиг.2. Конструирование плазмид для экспрессии свободных пропептидов и для экспрессии рекомбинантного FVII человека с присоединенным пропептидом. Плазмиды pLN171 и pLN174 экспрессируют FVII человека вместе с присоединенным пропептидом, ассоциированным с FVII в природе. Плазмида pLN329 содержит стоп-кодон, вставленный в кДНК, кодирующую FVII, после пропептида, ассоциированного с FVII, в природе, для экспрессии только свободного пропептида.
Фиг.3. Сравнение клеток CHO-K1, экспрессирующих FVII (контроль), и клеток, коэкспрессирующих FVII и свободный пропептид FVII (FVII пропептид). Результаты представлены в пг экспрессии FVII на одну клетку в день.
Настоящее изобретение далее иллюстрируется с помощью последующих примеров, которые, однако, не должны рассматриваться как ограничивающие рамки, защищаемые изобретением. Особенности, описанные в приведенном выше описании и в следующих далее примерах, могут как по отдельности, так и в любом их сочетании составлять материал для реализации настоящего изобретения в различных его формах.
ПРИМЕРЫ
Пример 1
Коэкспрессия FVII и пропептида FVII в клетки CHO-K1
Вектор плазмиды pLN174 для экспрессии FVII человека описан (Persson and Nielsen, 1996, FEBS Lett. 385: 241-243). Вкратце, он несет нуклеотидную последовательность кДНК, кодирующую FVII человека, включая пропептид, под контролем промотора металлотионеина мыши для транскрипции вставки кДНК и кДНК дигидрофолиат редуктазы мыши под контролем раннего промотора SV40 для использования в качестве селектируемого маркера.
Для конструирования вектора плазмиды, кодирующего гамма-распознающую последовательность карбоксилирования, используется вектор клонирования pBluescript II KS+ (Stratagene), содержащий кДНК, кодирующую FVII, включая его пропептид (pLN171) (Persson et al. 1997, J. Biol. Chem. 272: 19919-19924). Нуклеотидная последовательность, кодирующая стопкодон, вставляется в кДНК, кодирующую FVII, после пропептида FVII с помощью обратного PCR-опосредованного мутагенеза на этом векторе клонирования. Матричную плазмиду денатурируют путем обработки с помощью NaOH с последующей PCR с полимеразами Pwo (Boehringer-Mannheim) и Taq (Perkin-Elmer) со следующими праймерами:
a) 5'-AGC GTT TTA GCG CCG GCG CCG GTG CAG GAC-3' (SEQ ID NO: 19)
b) 5'-CGC CGG CGC TAA AAC GCT TTC CTG GAG GAG CTG CGG CC-3' (SEQ ID NO:20).
Полученную смесь переваривают с помощью DpnI, чтобы переварить остаток матричной ДНК, и Escherichia coli трансформируются с помощью продукта PCR. Клоны просматриваются путем секвенирования на присутствие мутации. кДНК из корректного клона переносится в виде фрагмента BamHI-EcoRI в плазмиду экспрессии pcDNA3 (Invitrogen). Полученная плазмида обозначается как pLN329.
Клетки CHO K1 (ATCC CCI61) трансфицируются равными количествами pLN174 и pLN329 с помощью способа Fugene6 (Boehriner-Mannheim). Трансфектанты подвергаются селекции путем добавления метотрексата до 1 мкМ и G-418 до 0,45 мг/мл. Пул трансфектантов клонируют путем граничного разбавления и измеряют экспрессию FVII из клонов.
Высокопродуктивный клон дополнительно субклонируют и выбирают клон E11 с удельной экспрессией FVII 2,4 пг/клетка/день в модифицированной по Дульбекко среде Игла с 10% фетальной сыворотки теленка. Клон адаптируется к культуре суспензии, не содержащей сыворотки, в коммерчески доступной среде CHO (JRH Bioscience).
Адаптированные клетки размножаются непрерывно в культурах с перемешиванием и, когда количество клеток возрастает, объем постепенно увеличивают путем добавления новой среды.
Через 25 дней 6 л культуры с перемешиванием инокулируют в 50-литровый биологический реактор. Клетки размножаются в биологическом реакторе и, когда количество клеток увеличивается, объем постепенно увеличивается путем добавления новой среды.
Наконец, 50 л посевной культуры инокулируют в 500-литровый промышленный биологический реактор, содержащий макропористые носители Cytopore 1 (Pharmacia), после чего суспендированные клетки иммобилизуются на носителях. Культуру поддерживают при 36°C, при значении pH 7,0-7,1 и при давлении растворенного кислорода (DOT) 50% от насыщения. Объем в промышленном биологическом реакторе постепенно увеличивается путем добавления новой среды по мере увеличения количества клеток. Когда плотность клеток достигает приблизительно 2×105 клеток/мл, инициируется фаза продуцирования и смену среды осуществляют каждые 24 часа: перемешивание прекращают, чтобы дать возможность для седиментации носителей, содержащих клетки, а затем 80% супернатанта культуры собирают и заменяют новой средой. Собранный супернатант культуры фильтруют для удаления незахваченных клеток (то есть клеток, которые не иммобилизуются на носителях) и остатков клеток, а затем транспортируют для дальнейшей обработки.
Во время фазы продуцирования плотность клеток достигает 2- 3×107 клеток/мл и титра 8 мг фактора VII/литр.
Пример 2
Сравнение клеток CHO-K1, экспрессирующих FVII, и клеток, коэкспрессирующих FVII и свободный пропептид FVII
Клетки CHO-K1 трансфицируются pLN174 и 1) пустым вектором pcDNA3.1+ или 2) пропептидом FVII в pcDNA3.1+, как описано в примере 1. Пулы трансфектантов анализируют на экспрессию FVII и на количество клеток. Выходы FVII за 24 часа показаны на фиг.3. Результаты показывают, что коэкспрессия пропептида FVII увеличивает FVII выходы клеток приблизительно от 1 пг/клетка/день до 4 пг/клетка/день. Результаты представлены на фиг.3.
Список последовательностей:
SEQ ID NO:1: AVFLSREQANQVLQRRRR
SEQ ID NO:2: SLFIRREQANNILARVTR
SEQ ID NO:3: NPFINRRNANTFISPQQR
SEQ ID NO:4: ANFLSKQQASQVLVRKRR
SEQ ID NO:5: RVFLTGEKANSILKRYPR
SEQ ID NO:6: HVFLAPQQARSLLQRVRR
SEQ ID NO:7: AVFVTQEEAHGVLHRRRR
SEQ ID NO:8: TVFLDHENANKILNRPKR
SEQ ID NO:9: SVFSSSERAHQVLRIRKR
SEQ ID NO:10: AAFVSKQEASEVLKRPRR
SEQ ID NO:11: AVFVTQEEGHGVLHRRRR
SEQ ID NO:12: AVFVTQEEARGVLHRRRR
SEQ ID NO:13: AVFVTQEEAKGVLHRRRR
SEQ ID NO:14: AVFVTQEEALGVLHRRRR
SEQ ID NO:15: AVFSTQEEAHGVLHRRRR
SEQ ID NO:16: AVFVTQEEAHGVLH
SEQ ID NO:17: TVFLDHENANKILN
SEQ ID NO:18: SVFSSSERAHQVLR
SEQ ID NO:19: 5'-AGC GTT TTA GCG CCG GCG CCG GTG CAG GAC-3'
SEQ ID NO:20: 5'-CGC CGG CGC TAA AAC GCT TTC CTG GAG GAG CTG CGG CC-3'





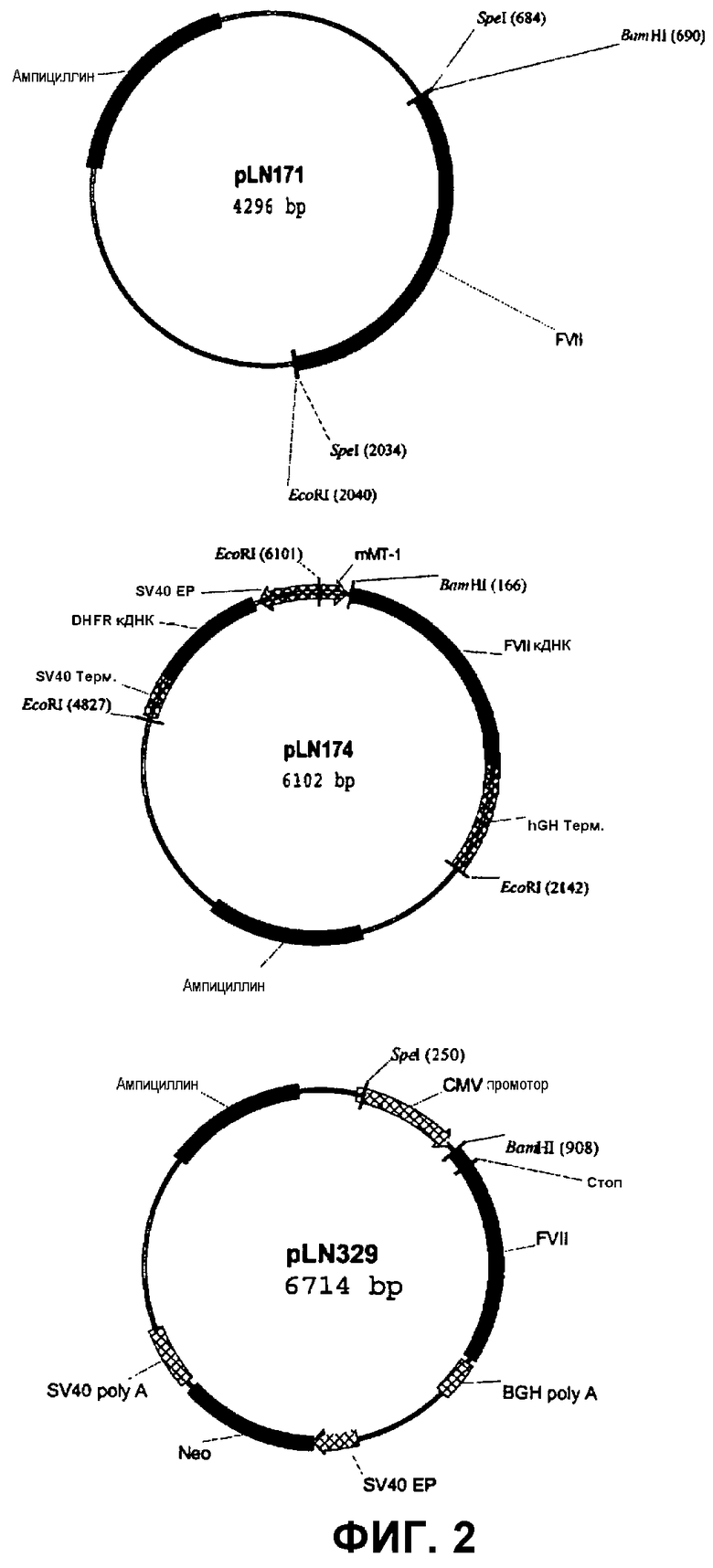
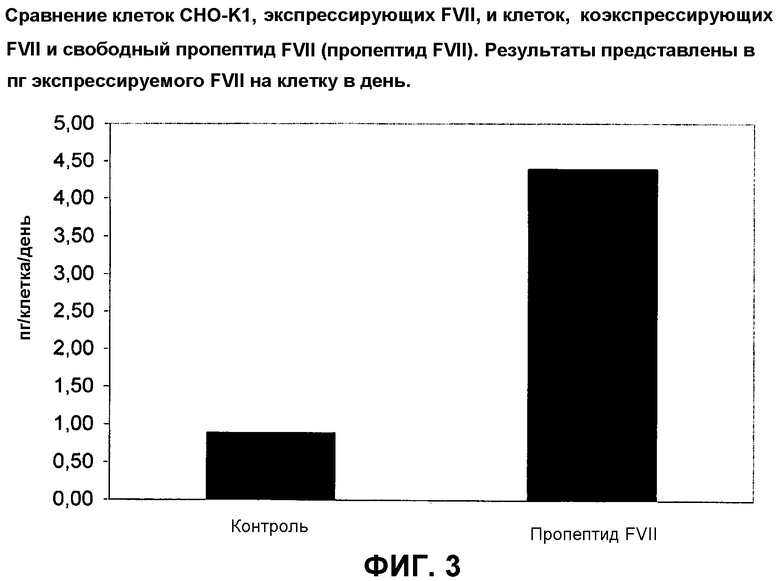
Изобретение относится к биотехнологии и представляет собой эукариотическую клетку-хозяина (варианты), которая экспрессирует первый полинуклеотид, кодирующий первый пропептид и FVII или его функциональные варианты, в первой единице экспрессии и экспрессирует второй полинуклеотид, кодирующий второй свободный пропептид, во второй единице экспрессии, причем каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18. Изобретение относится также и к способу получения витамин К-зависимых белков, в том числе и FVII, с использованием вышеупомянутой клетки-хозяина, а также к способу получения самой клетки-хозяина. Изобретение позволяет получать витамин К-зависимые белки с высокой степенью эффективности. 14 н. и 24 з.п. ф-лы, 3 ил, 3 табл.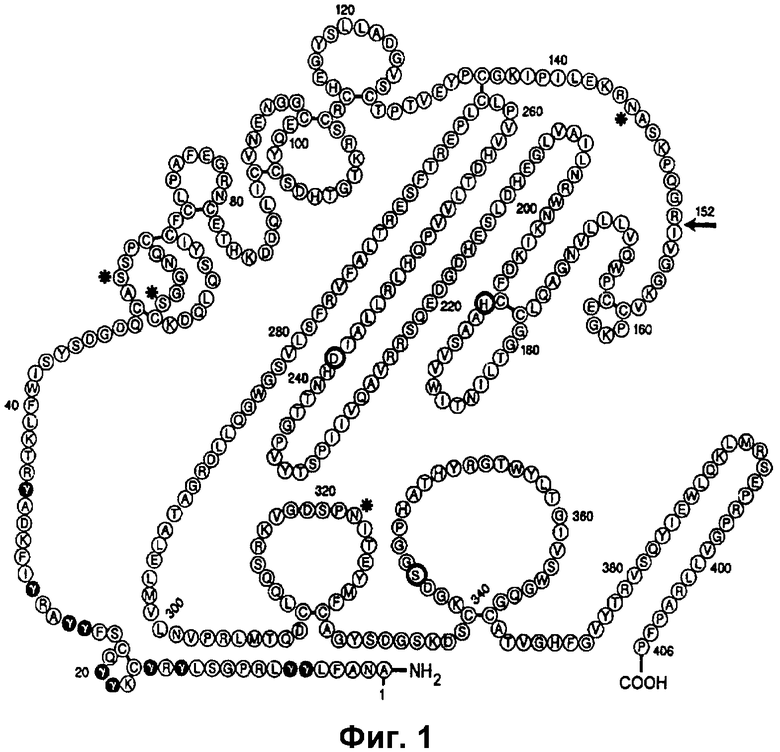
a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его функциональные варианты, в первой единице экспрессии, и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии, с получением котрансфицированной эукариотической клетки-хозяина;
b) культивирование котрансфицированной эукариотической клетки-хозяина в соответствующей культуральной среде в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
c) выделение FVII или его функциональных вариантов из среды где каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
а) культивирование эукариотической клетки-хозяина по любому из пп.1-3, 7-12 в соответствующей культуральной среде в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
b) выделение FVII или его функциональных вариантов из среды где каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его функциональные варианты, в первой единице экспрессии, и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии, с получением котрансфицированной эукариотической клетки-хозяина;
b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
c) выделение FVII или его функциональных вариантов из среды и их активирование,
где каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
а) культивирование эукариотической клетки-хозяина по любому из пп.1-3, 7-18 в соответствующей культуральной среде в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
b) выделение FVII или его функциональных вариантов из среды и их активирование.
a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и витамин К-зависимый белок, в первой единице экспрессии, и трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии, с получением котрансфицированной эукариотической клетки-хозяина;
b) культивирование в соответствующей культуральной среде котрансфицированной эукариотической клетки-хозяина в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
c) выделение витамин К-зависимых белков из среды, где каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
a) культивирование эукариотической клетки-хозяина по любому из пп.4-12 в соответствующей культуральной среде в условиях, которые обеспечивают возможность экспрессии первого полинуклеотида и второго полинуклеотида; и
b) выделение витамин К-зависимых белков из среды.
a) трансфицирование эукариотической клетки-хозяина первым полинуклеотидом, кодирующим первый пропептид и FVII или его функциональные варианты, в первой единице экспрессии, и
b) трансфицирование вторым полинуклеотидом, кодирующим второй свободный пропептид, во второй единице экспрессии, где каждый из указанных первого и второго пропептидов содержит аминокислотную последовательность, независимо выбранную из группы, состоящей из SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18.
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| US 4784950, 15.11.1988 | |||
| SUGIURA I et | |||
| al | |||
| Propeptide and glutamate-containing substrates bound to the vitamin K-dependent carboxylase convert its vitamin К epoxidase function from an inactive to an active state | |||
| Proc Natl Acad Sci USA | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА, ОБЛАДАЮЩЕГО ОПОСРЕДОВАННОЙ ФАКТОРОМ VII АКТИВНОСТЬЮ В СВЕРТЫВАНИИ КРОВИ | 1986 |
|
RU2122583C1 |
Авторы
Даты
2008-04-10—Публикация
2001-10-02—Подача