Пульсирующее высвобождение гормона роста на основе соматотропных гормонов гипофиза регулируется нейропептидами гипоталамуса: рилизинг-фактором ростового гормона и соматостатином. Рилизинг-фактор ростового гормона стимулирует высвобождение ростового гормона, тогда как соматостатин ингибирует секрецию ростового гормона (Frohman et al., Endocr. Rev. 1986, 7, 223-253 and Strobi et al., Pharmacol. Rev. 1994, 46, 1-34).
Высвобождение ростового гормона из соматотропных гормонов гипофиза может также регулироваться рилизинг-пептидами ростового гормона (РФРГ). Было показано, что гексапептид His-D-Trp-Ala-Trp-D-Phe-Lys амид (РФРГ-6, (GHRP-6)) зависимым от дозы образом высвобождает ростовой гормон из соматотропных гормонов у нескольких видов, включая человека (Bowers et al., Endocrinology 1984, 114, 1537-1545). Последующие исследования химии РФРГ-6 привели к идентификации других мощных средств, способствующих секреции ростового гормона, таких как РФРГ-1, РФРГ-2 и гексарелин (Cheng et al., Endocrinology 1989, 124, 2791-2798, Bowers, C.Y. Novel GH-Releasing Peptides. In: Molecular and Clinical Advances in Pituitary Disorders. Ed: Melmed, S. Endocrine Research and Education, Inc., Los Angeles, CA, USA, 1993, 153-157, and Deghenghi et al., Life Sci. 1994, 54, 1321-1328).
РФРГ-1, РФРГ-2, РФРГ-6 и гексарелин представляют собой синтетические средства, способствующие секреции гормона роста (СГР). СГР стимулируют секрецию ростового гормона по механизму, отличному от действия рилизинг-фактора ростового гормона (Bowers et al., Endocrinology 1984, 114, 1537-1545, Cheng et al., Endocrinology 1989, 124, 2791-2798, Bowers C.Y. Novel GH-Releasing Peptides. In: Molecular and Clinical Advances in Pituitary Disorders. Ed: Melmed, S.; Endocrine Research and Education, Inc., Los Angeles, CA, USA, 1993, 153-157, and Deghenghi et al., Life Sci. 1994, 54, 1321-1328).
Низкая пероральная биодоступность (<1%) пептидильных средств, способствующих секреции ростового гормона, стимулировала поиски непептидных соединений, имитирующих действие РФРГ-8 гипофиза. Имеются сообщения о нескольких бензолактамах и спироинданах, которые стимулируют высвобождение ростового гормона у разных видов животных и человека (Smith et al., Science 1993, 260, 1640-1643, Patchett et al., Proc. Natl. Acad. Sci. USA. 1995, 92, 7001-7005, and Chen et al., Bioorg. Med. Chem. Lett. 1996, 6, 2163-2169). Конкретным примером небольшого спироиндана является MK-0677 (Patchett et al., Proc. Natl. Acad. Sci. USA. 1995, 92, 7001-7005):
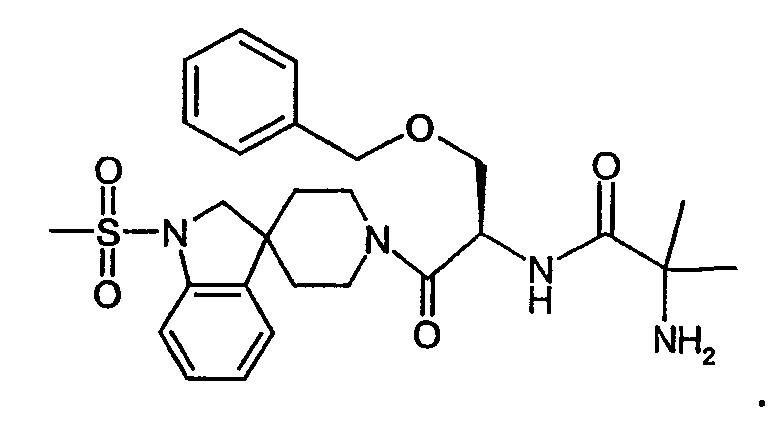
Действие указанных выше СГР (пептидной и непептидной природы), по всей видимости, опосредовано специфическим рецептором средств, способствующих секреции ростового гормона (рецептора СГР). (Howard et al., Science 1996, 273, 974-977, and Pong et al., Molecular Endocrinology 1996, 10, 57-61). Указанный рецептор присутствует в гипофизе и гипоталамусе разных видов млекопитающих (GHSR1a) и отличается от рецептора рилизинг-фактора ростового гормона (РФРГ). Рецептор СГР был также обнаружен в других зонах центральной нервной системы и в периферических тканях, например в надпочечнике и щитовидной железе, сердце, легком, почке и скелетных мышцах (Chen et al., Bioorg. Med. Chem. Lett. 1996, 6, 2163-2169, Howard et al., Science 1996, 273, 974-977, Pong et al., Molecular Endocrinology 1996, 10, 57-61, Guan et al., Mol. Brain Res. 1997, 48, 23-29 и McKee et al., Genomics 1997, 46, 426-434). Имеются сообщения о наличии усеченного варианта GHSR1a (Howard et al., Science 1996, 273, 974-977).
Рецептор СГР представляет собой рецептор, связанный с G-белком. Эффекты активации рецептора СГР включают деполяризацию и ингибирование калиевых каналов, повышение внутриклеточной концентрации трифосфата инозита (ИФ3) и временное повышение концентрации внутриклеточного кальция (Pong et al., Molecular Endocrinology 1996, 10, 57-61, Guan et al., Mol. Brain Res. 1997, 48, 23-29 and McKee et al., Genomics 1997, 46, 426-434).
Грелин представляет собой природный пептид, который рассматривают как эндогенный лиганд для рецептора СГР (Kojima et al., Nature 1999, 402, 656-660). Известны нативные структуры грелинов, полученные из нескольких видов млекопитающих и из животных, отличных от млекопитающих (Kalya et al., J. Biol. Chem. 2001, 276, 40441-40448; Заявка на Международный патент PCT/JP00/04907 (WO 01/07475)). Было показано, что присутствующий в грелине ядерный участок обеспечивает активность рецептора СГР. Ядерный участок включает четыре N-концевых аминокислоты, где серин в положении 3 в норме модифицирован N-октановой кислотой. Однако кроме ацилирования N-октановой кислотой грелин, как было показано, может быть ацилирован N-декановой кислотой (Kalya et al., J. Biol. Chem. 2001, 276, 40441-40448). Аналоги грелина обладают множеством различных направлений терапевтического применения, а также использования в качестве инструментов исследования.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к пептидильным аналогам, активным в отношении рецептора СГР. Аналоги по настоящему изобретению могут связываться с рецептором СГР и предпочтительно осуществлять сигнальную трансдукцию.
Таким образом, в первом аспекте настоящее изобретение относится к соединению формулы (I):
R1-A1-A2-A3-A4-A5-R2
или к его фармацевтически приемлемой соли, где:
А1 обозначает Aib, Apc или Inp;
А2 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp;
A3 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp;
А4 обозначает 2Fua, Orn, 2Pal, 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi, 3Thi, Thr(Bzl);
A5 обозначает Apc, Dab, Dap, Lys, Orn или делетирован;
R1 обозначает водород, (С1-6)алкил, (С5-14)арил, (С1-6)алкил(С5-14)арил, (С3-8)циклоалкил или (С2-10)ацил; и
R2 обозначает OH или NH2;
при условии, что
когда A5 обозначает Dab, Dap, Lys или Orn, то
А2 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
A3 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А4 обозначает 2Thi, 3Thi, Taz, 2Fua, 2Pal, 3Pal, 4Pal, Orn, Thr(Bzl) или Pff,
когда А5 делетирован, то
A3 обозначает D-Bip, D-Bpa или D-Dip; или
А4 обозначает 2Fua, Pff, Taz или Thr(Bzl); или
А1 обозначает Apc и
А2 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
A3 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А4 обозначает 2Thi, 3Thi, Orm, 2Pal, 3Pal или 4Pal.
Предпочтительное соединение формулы (I), обозначенное как соединение из группы 1, представляет собой соединение формулы (I), где:
А1 обозначает Aib, Apc или Н-Inp;
А2 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp;
A3 обозначает D-Bal, D-Bpa, D-Dip, D-1Nal, D-2Nal, или D-Trp;
А4 обозначает Orn, 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi или Thr(Bzl); и
A5 is Apc, Lys, или делетирован
или их фармацевтически приемлемые соли.
Предпочтительное соединение из группы 1, обозначенное как соединение из группы 1A, представляет собой соединение, определемое следующей формулой:
A1 обозначает Apc или H-Inp;
A2 обозначает D-Bal, D-Bip, D-1Nal или D-2Nal;
A3 обозначает D-Bal, D-1Nal, D-2Nal или D-Trp;
A4 обозначает 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi или Thr(Bzl);
или их фармацевтически приемлемые соли.
Другое предпочтительное соединение формулы (I), обозначенное как соединение из группы 2, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Trp-D-2Nal(ψ)-Pim;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-NH2;
H-Apc-D-1Nal-D-Trp-2Pal-NH2;
H-Apc-D-1Nal-D-Trp-3Pal-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-NH2;
H-Apc-D-1Nal-D-Trp-4Pal-NH2;
H-Apc-D-1Nal-D-Trp-Pff-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Pff-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Pff-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-NH2;
H-Apc-D-2Nal-D-Trp-2Pal-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-2Nal-D-Trp-3Pal-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-NH2;
H-Apc-D-2Nal-D-Trp-4Pal-NH2;
H-Apc-D-2Nal-D-Trp-Pff-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Apc-D-2Nal-D-Trp-Pff-NH2;
H-Apc-D-2Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Bal-2Fua-Apc-NH2;
H-Apc-D-Bal-D-Bal-2Fua-Lys-NH2;
H-Apc-D-Bal-D-Bal-2Fua-NH2;
H-Apc-D-Bal-D-Bal-2Pal-NH2;
H-Apc-D-Bal-D-Bal-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Bal-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Bal-2Thi-NH2;
H-Apc-D-Bal-D-Bal-3Pal-NH2;
H-Apc-D-Bal-D-Bal-3Thi-Apc-NH2;
H-Apc-D-Bal-D-Bal-3Thi-Lys-NH2;
H-Apc-D-Bal-D-Bal-3Thi-NH2;
H-Apc-D-Bal-D-Bal-4Pal-NH2;
H-Apc-D-Bal-D-Bal-Pff-Apc-NH2;
H-Apc-D-Bal-D-Bal-Pff-Lys-NH2;
H-Apc-D-Bal-D-Bal-Pff-NH2;
H-Apc-D-Bal-D-Bal-Phe-Apc-NH2;
H-Apc-D-Bal-D-Bal-Phe-Lys-NH2;
H-Apc-D-Bal-D-Bal-Phe-NH2;
H-Apc-D-Bal-D-Bal-Taz-Apc-NH2;
H-Apc-D-Bal-D-Bal-Taz-Lys-NH2;
H-Apc-D-Bal-D-Bal-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Fua-NH2;
H-Apc-D-Bal-D-Trp-2Pal-NH2;
H-Apc-D-Bal-D-Trp-3Pal-NH2;
H-Apc-D-Bal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-3Thi-NH2;
H-Apc-D-Bal-D-Trp-4Pal-NH2;
H-Apc-D-Bal-D-Trp-Pff-Apc-NH2;
H-Apc-D-Bal-D-Trp-Pff-Lys-NH2;
H-Apc-D-Bal-D-Trp-Pff-NH2;
H-Inp-D-1Nal-D-Bal-2Fua-Lys-NH2;
H-Inp-D-1Nal-D-Bal-2Fua-NH2;
H-Inp-D-1Nal-D-Bal-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Bal-3Thi-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Pff-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Pff-NH2;
H-Inp-D-1Nal-D-Bal-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Taz-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Taz-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-NH2;
H-Inp-D-1Nal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-1Nal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Pff-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Pff-NH2;
H-Inp-D-1Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-2Nal-D-Trp-2Fua-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Apc-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Bal-D-Bal-2Fua-Lys-NH2;
H-Inp-D-Bal-D-Bal-2Fua-NHa
H-Inp-D-Bal-D-Bal-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Bal-3Thi-Lys-NH2;
H-Inp-D-Bal-D-Bal-Pff-Lys-NH2;
H-Inp-D-Bal-D-Bal-Pff-NH2;
H-Inp-D-Bal-D-Bal-Phe-Lys-NH2;
H-Inp-D-Bal-D-Bal-Taz-Lys-NH2;
H-Inp-D-Bal-D-Bal-Taz-NH2;
H-Inp-D-Bal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Fua-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Fua-NH2;
H-Inp-D-Bal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Pff-Apc-NH2;
H-Inp-D-Bal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bal-D-Trp-Pff-NH2;
H-Inp-D-Bal-D-Trp-Taz-NH2;
H-Inp-D-Bip-D-Bal-2Fua-Lys-NH2;
H-Inp-D-Bip-D-Bal-2Fua-NH2;
H-Inp-D-Bip-D-Bal-2Thi-Lys-NH2;
H-Inp-D-Bip-D-Bal-3Thi-Lys-NH2;
H-Inp-D-Bip-D-Bal-Pff-Lys-NH2;
H-Inp-D-Bip-D-Bal-Pff-NH2; или
H-Inp-D-Bip-D-Bal-Taz-Lys-NH2;
H-Inp-D-Bip-D-Bal-Taz-NH2;
H-Inp-D-Bip-D-Trp-2Fua-Lys-NH2;
H-Inp-D-Bip-D-Trp-2Fua-NH2;
H-Inp-D-Bip-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bip-D-Trp-3Thi-Lys-NH2;
H-Inp-D-Bip-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bip-D-Trp-Pff-NH2;
H-Inp-D-Bip-D-Trp-Taz-Lys-NH2; или
H-Inp-D-Bip-D-Trp-Taz-NH2;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2, обозначенное как соединение из группы 2A, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Trp-D-2Nal(ψ)-Pim;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Fua-Lys-NH2;
H-Inp-D-Bal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-Bal-D-Trp-Pff-Apc-NH2;
H-Apc-D-Bal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-BalI-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bal-D-Bal-Phe-Lys-NH2;
H-Inp-D-Bal-D-Bal-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Bal-3Thi-Lys-NH2;
H-Inp-D-Bal-D-Bal-Taz-Lys-NH2;
H-Inp-D-Bal-D-Bal-2Fua-Lys-NH2;
H-Inp-D-Bal-D-Bal-Pff-Lys-NH2;
H-Apc-D-Bal-D-Bal-Phe-Lys-NH2;
H-Apc-D-Bal-D-Bal-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Bal-3Thi-Lys-NH2;
H-Apc-D-Bal-D-Bal-Taz-Lys-NH2;
H-Apc-D-Bal-D-Bal-2Fua-Lys-NH2;
H-Apc-D-Bal-D-Bal-Pff-Lys-NH2;
H-Inp-D-1Nal-D-Trp-3Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Bal-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Bal-3Thi-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Taz-Lys-NH2;
H-Inp-D-1Nal-D-Bal-2Fua-Lys-NH2;
H-Inp-D-1Nal-D-Bal-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Apc-NH2;
H-Inp-D-1Nal-D-Trp-3Thi-Apc-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Pff-Apc-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Pff-Lys-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-Lys-NH2;
H-Apc-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-Lys-NH2;
H-Apc-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bip-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bip-D-Trp-3Thi-Lys-NH2;
H-Inp-D-Bip-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bip-D-Trp-2Fua-Lys-NH2;
H-Inp-D-Bip-D-Trp-Pff-Lys-NH2;
H-Inp-D-Bip-D-Bal-2Thi-Lys-NH2;
H-Inp-D-Bip-D-Bal-3Thi-Lys-NH2;
H-Inp-D-Bip-D-Bal-Taz-Lys-NH2;
H-Inp-D-Bip-D-Bal-2Fua-Lys-NH2;
H-Inp-D-Bip-D-Bal-Pff-Lys-NH2;
H-Apc-D-Bal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-Bal-D-Trp-Pff-Apc-NH2;
H-Apc-D-Bal-D-Bal-Phe-Apc-NH2;
H-Apc-D-Bal-D-Bal-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Bal-3Thi-Apc-NH2;
H-Apc-D-Bal-D-Bal-Taz-Apc-NH2;
H-Apc-D-Bal-D-Bal-2Fua-Apc-NH2;
H-Apc-D-Bal-D-Bal-Pff-Apc-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Pff-Apc-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Pff-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-NH2;
H-Inp-D-Bal-D-Trp-2Fua-NH2;
H-Inp-D-Bal-D-Trp-Pff-NH2;
H-Apc-D-Bal-D-Trp-3Thi-NH2;
H-Apc-D-Bal-D-Trp-2Fua-NH2;
H-Apc-D-Bal-D-Trp-Pff-NH2;
H-Apc-D-Bal-D-Trp-4Pal-NH2;
H-Apc-D-Bal-D-Trp-3Pal-NH2;
H-Apc-D-Bal-D-Trp-2Pal-NH2;
H-Inp-D-Bal-D-Bal-Taz-NH2;
H-Inp-D-Bal-D-Bal-2Fua-NH2;
H-Inp-D-Bal-D-Bal-Pff-NH2;
H-Apc-D-Bal-D-Bal-Phe-NH2;
H-Apc-D-Bal-D-Bal-2Thi-NH2;
H-Apc-D-Bal-D-Bal-3Thi-NH2;
H-Apc-D-Bal-D-Bal-Taz-NH2;
H-Apc-D-Bal-D-Bal-2Fua-NH2;
H-Apc-D-Bal-D-Bal-Pff-NH2;
H-Apc-D-Bal-D-Bal-4Pal-NH2;
H-Apc-D-Bal-D-Bal-3Pal-NH2;
H-Apc-D-Bal-D-Bal-2Pal-NH2;
H-Inp-D-1Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-2Fua-NH2;
H-Inp-D-1Nal-D-Trp-Pff-NH2;
H-Inp-D-1Nal-D-Bal-Taz-NH2;
H-Inp-D-1Nal-D-Bal-2Fua-NH2;
H-Inp-D-1Nal-D-Bal-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Trp-2Fua-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Apc-D-1Nal-D-Trp-3Thi-NH2;
H-Apc-D-1Nal-D-Trp-2Fua-NH2;
H-Apc-D-1Nal-D-Trp-Pff-NH2;
H-Apc-D-1Nal-D-Trp-4Pal-NH2;
H-Apc-D-1Nal-D-Trp-3Pal-NH2;
H-Apc-D-1Nal-D-Trp-2Pal-NH2;
H-Apc-D-2Nal-D-Trp-3Thi-NH2;
H-Apc-D-2Nal-D-Trp-2Fua-NH2;
H-Apc-D-2Nal-D-Trp-Pff-NH2;
H-Apc-D-2Nal-D-Trp-4Pal-NH2;
H-Apc-D-2Nal-D-Trp-3Pal-NH2;
H-Apc-D-2Nal-D-Trp-2Pal-NH2;
H-Inp-D-Bip-D-Trp-Taz-NH2;
H-Inp-D-Bip-D-Trp-2Fua-NH2;
H-Inp-D-Bip-D-Trp-Pff-NH2;
H-Inp-D-Bip-D-Bal-Taz-NH2;
H-Inp-D-Bip-D-Bal-2Fua-NH2; или
H-Inp-D-Bip-D-Bal-Pff-NH2;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2А, обозначенное как соединение из группы 2В, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-Trp-D-2Nal(ψ)-Pim;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2; или
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2В, обозначенное как соединение из группы 2В-1, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2; или
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2В-1, обозначенное как соединение из группы 2В-1а, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
или его фармацевтически приемлемую соль.
Более предпочтительное соединение из группы 2В-1, обозначенное как соединение из группы 2В-1b, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2; или
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
или его фармацевтически приемлемую соль.
Еще более предпочтительное соединение из группы 2В-1, обозначенное как соединение из группы 2В-1с, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
или его фармацевтически приемлемую соль.
Особенно предпочтительное соединение из группы 2B-1c представляет собой соединение, определяемое формулой:
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
или его фармацевтически приемлемую соль.
Другое еще более предпочтительное соединение из группы 2В-1, обозначенное как соединение из группы 2В-1d, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
или его фармацевтически приемлемую соль.
Другое предпочтительное соединение из группы 2В, обозначенное как соединение из группы 2В-2, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-Nal-D-Dip-Phe-NH2;
H-Inp-D-Trp-D-2Nal(ψ)-Pim;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim; или
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2В-2, обозначенное как соединение из группы 2В-2а, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-1Nal-D-Trp(ψ)-Pim; или
H-Inp-D-Bal-D-Trp(ψ)-Pim;
или их фармацевтически приемлемую соль.
Другое предпочтительное соединение из группы 2, обозначенное как соединение из группы 2С, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-3Thi-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2; или
H-Apc-D-1Nal-D-Trp-Phe-NH2;
или его фармацевтически приемлемую соль.
Предпочтительное соединение из группы 2С, обозначенное как соединение из группы 2С-1, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2; или
H-Apc-D-1Nal-D-Trp-Phe-NH2;
или его фармацевтически приемлемую соль.
Особенно предпочтительное соединение по настоящему изобретению, обозначенное как соединение из группы 3, представляет собой соединение, определяемое следующей формулой:
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Apc-NH2; или
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2;
или его фармацевтически приемлемую соль.
В другом аспекте настоящее изобретение относится к способу определения способности соединения связываться с рецептором СГР, где указанный способ включает стадию определения способности соединения воздействовать на связывание соединения по настоящему изобретению формулы (I) или относящегося к любой из указанных ниже групп 1, 1A, 2, 2A, 2B, 2B-1, 2B-1a, 2B-1b, 2B-1c, 2B-1d, 2B-2, 2B-2a, 2C или 2C-1, к указанному рецептору, к фрагменту указанного рецептора, к полипептиду, включающему указанный фрагмент указанного рецептора, или к производному указанного полипептида.
В другом аспекте настоящее изобретение относится к способу достижения благоприятного эффекта у субъекта, включающему стадию введения указанному субъекту эффективного количества соединения формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество является эффективным для оказания помощи в лечении (например, для излечивания или снижения тяжести состояния) или для предупреждения (например, для снижения вероятности начала проявления или ухудшения состояния) заболевания или расстройства.
В другом аспекте настоящее изобретение относится к способу стимуляции секреции гормона роста у субъекта при необходимости такой стимуляции, включающему стадию введения указанному субъекту эффективного количества агониста грелина формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой количество, по меньшей мере, достаточное для достижения заметного повышения секреции гормона роста, и предпочтительно для достижения благоприятного эффекта у пациента.
В одном варианте указанного аспекта осуществления изобретения рассматриваемая стимуляция секреции гормона роста показана для лечения состояния, дефицитного по гормону роста, с целью повышения мышечной массы, повышения плотности кости, лечения расстройств половой функций у мужчин или у женщин, содействия наращиванию веса, для облегчения поддержания веса, для облегчения поддержания активного физического состояния, для облегчения восстановления физической функции и/или с целью содействия повышения аппетита. Предпочтительно указанное облегчение в наращивании веса, облегчение поддержания веса и/или содействие повышению аппетита показаны для пациента, имеющего соответствующее заболевание или расстройство, или который подготавливается к лечению, сопровождаемому снижением веса. Более предпочтительно указанные заболевания или расстройства, сопровождаемые снижением веса, включает анорексию, булимию, раковую кахексию, СПИД, (например, истощение), кахексию и истощение у слабых пожилых людей. Также предпочтительно указанные виды лечения, сопровождаемые снижением веса, включают химиотерапию, лучевую терапию, временную или постоянную иммобилизацию и диализ.
В другом аспекте настоящее изобретение относится к способу подавления секреции гормона роста у субъекта при необходимости в таком подавлении, включающему стадию введения указанному субъекту эффективного количества антагониста грелина формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой по меньшей мере количество, достаточное для достижения заметного снижения секреции гормона роста, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
В одном варианте осуществления указанного аспекта подавление секреции ростового гормона показано для лечения заболевания или состояния, характеризующегося избыточной секрецией ростового гормона, для содействия в снижении веса, для содействия в снижении аппетита, для облегчения поддержания веса, для лечения ожирения, для лечения диабета, для лечения осложнений диабета, включающих ретинопатию и/или для лечения сердечно-сосудистых заболеваний.
В предпочтительном варианте осуществления указанного аспекта настоящего изобретения избыточный вес представляет собой фактор, влияющий на течение заболевания или состояния, включающих гипертензию, диабет, дислипидемию, сердечно-сосудистые заболевания, камни желчного пузыря, остеоартрит и различные виды рака. Более предпочтительно указанное содействие в снижении веса позволяет уменьшить вероятность таких заболеваний или состояний. Кроме того, более предпочтительно указанное содействие в снижении веса включает, по меньшей мере частично, лечение таких заболеваний или состояний.
Способ проявления эффекта агониста грелина у субъекта, включающий стадию введения указанному субъекту эффективного количества одного или более агонистов грелина формулы (I), относящихся к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой количество, по меньшей мере, достаточное для достижения заметного повышения секреции ростового гормона и, предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
В другом аспекте настоящее изобретение относится к способу проявления эффекта антагониста грелина у субъекта, включающему стадию введения субъекту эффективного количества одного или более антагонистов грелина формулы (I), относящихся к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой количество, по меньшей мере, достаточное для достижения заметного снижения секреции ростового гормона, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
Соединения по настоящему изобретению являются соединениями активными в отношении рецептора СГР. Указанные соединения могут связываться с рецептором и предпочтительно стимулировать активность рецептора. Таким образом, соединение по настоящему изобретению является полезным в качестве функционального аналога грелина, причем как инструмент для исследования, так и/или как лекарственное средство.
В аспекте применения в качестве инструмента для исследований в основном рассматривается использование соединения по настоящему изобретению при наличии рецептора СГР или его фрагмента. Рецептор СГР может присутствовать в различном окружении, таком как субъект, относящийся либо к млекопитающему, либо к целой клетке, либо к фрагменту клеточной мембраны. Примеры применения в качестве инструмента для исследования включают скрининг соединений, активных в отношении рецептора СГР, определение наличия рецептора СГР в образце или препарате и выявление роли или эффекта грелина.
Один аспект настоящего изобретения относится к способу скрининга агонистов грелина и/или антагонистов грелина. Скрининг агонистов грелина может быть проведен, например, при использовании соединения формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, в конкурентном эксперименте с использованием исследуемых соединений. Скрининг антагонистов грелина может быть проведен, например, при использовании соединения формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, для генерирования активности в отношении рецептора СГР с последующим определением способности исследуемого соединения изменять активность рецептора СГР.
Другой аспект настоящего изобретения относится к способу скрининга соединения, способного связываться с рецептором СГР. Указанный способ включает стадию определения способности исследуемого соединения воздействовать на связывание соединения формулы (I), относящегося к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли с рецептором, с фрагментом рецептора, включающим сайт связывания грелина, полипептидом, включающим указанный фрагмент, или с производным такого полипептида.
Агонисты грелина могут использоваться для достижения благоприятного эффекта у субъекта. Например, грелин индуцирует высвобождение ростового гормона из клеток первичной культуры гипофиза зависимым от дозы образом, без стимуляции высвобождения других гормонов гипофиза. При внутривенной инъекции анестезированным крысам грелин стимулирует пульсирующее высвобождение ростового гормона (Kojima et al., Nature 1999, 402, 656-660). Таким образом, неисчерпывающий перечень примеров, для которых такой благоприятный эффект может быть показан, включает: лечение состояния, дефицитного по ростовому гормону, повышение мышечной массы, повышение плотности кости, лечение половых расстройств у мужчин или женщин, содействие наращиванию веса, облегчение поддержания веса, облегчение поддержания активного физического состояния, облегчение восстановления физической функции и/или содействие повышения аппетита. Содействие наращиванию веса, содействие поддержанию веса или повышению аппетита в особенности полезны в случае субъекта, имеющего соответствующее заболевание или состояние, или который подвергается лечению, сопровождаемому снижением веса. Заболевания или состояния, сопровождаемые снижением веса, включают, например, анорексию, булимию, раковую кахексию, СПИД, (например, истощение), кахексию, истощение у слабых пожилых людей и т.п. Виды лечения, сопровождаемые снижением веса, включают, например, химиотерапию, лучевую терапию, временную или постоянную иммобилизацию, диализ и т.п.
Таким образом, другой аспект настоящего изобретения относится к способу достижения благоприятного эффекта у субъекта, где указанный способ включает стадию введения указанному субъекту эффективного количества одного или более соединений формулы (I), относящихся к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество является эффективным для достижения благоприятного эффекта в помощи при лечении (например, для излечивания или снижения тяжести состояния) или для предупреждения (например, для снижения вероятности начала проявления или ухудшения состояния) заболевания или расстройства.
В предпочтительном варианте описанного выше способа осуществления настоящего изобретения указанное благоприятное воздействие включает стимуляцию секреции ростового гормона у субъекта при необходимости такой стимуляции, включающую стадию введения субъекту эффективного количества одного или более соединений формулы (I), относящихся к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой количество, по меньшей мере достаточное для достижения заметного повышения секреции ростового гормона, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
В более предпочтительном варианте описанного выше способа указанная стимуляция секреции ростового гормона показана для лечения состояния, дефицитного по гормону роста, для повышения мышечной массы, для повышения плотности кости, для лечения расстройств половой функций у мужчин или женщин, для содействия наращиванию веса, для облегчения поддержания веса, для облегчения поддержания активного физического состояния, для облегчения восстановления физической функции и/или с целью содействия повышению аппетита.
В другом предпочтительном варианте осуществления описанного выше способа указанные содействие в наращивании веса, облегчение поддержания веса и/или содействие в повышении аппетита показаны для пациента, имеющего соответствующее заболевание или расстройство, или который подвергается лечению, сопровождаемому снижением веса. Более предпочтительно указанные заболевания или расстройства, сопровождаемые снижением веса, включают анорексию, булимию, раковую кахексию, СПИД, (например, истощение), кахексию и истощение у слабых пожилых людей.
В другом более предпочтительном варианте описанного выше способа указанные виды лечения, сопровождаемые снижением веса, включают химиотерапию, лучевую терапию, временную или постоянную иммобилизацию, диализ и т.п.
Антагонисты грелина могут также использоваться для достижения благоприятного воздействия на человека. Например, антагонист грелина может использоваться для облегчения снижения веса, для содействия в снижении аппетита, для облегчения поддержания веса, для лечения ожирения, для лечения диабета, для лечения осложнений диабета, включающих ретинопатию, и/или для лечения сердечно-сосудистых заболеваний. Избыточный вес представляет собой фактор, вносящий дополнительный вклад в развитие различных заболеваний, включая гипертензию, диабет, дислипидемию, сердечно-сосудистые заболевания, камни желчного пузыря, остеоартрит и некоторые формы рака. Воздействие с целью снижения веса может использоваться, например, и для уменьшения вероятности развития таких заболеваний, и как составной компонент лечения таких заболеваний.
Соединения по настоящему изобретению могут также использоваться для антагонизации эффекта грелина in vitro и in vivo. Таким образом, еще один аспект настоящего изобретения относится к способу подавления секреции ростового гормона у субъекта, при необходимости такого подавления, включающему стадию введения субъекту эффективного количества одного или более соединений формулы (I), относящихся к группе 1, группе 1А, группе 2, группе 2А, группе 2В, группе 2В-1, группе 2В-1а, группе 2B-1b, группе 2B-1c, группе 2B-1d, группе 2B-2, группе 2B-2a, группе 2C или группе 2C-1, или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой количество, по меньшей мере достаточное для достижения заметного снижения секреции ростового гормона, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
В предпочтительном варианте описанного выше способа указанное подавление секреции ростового гормона показано для лечения заболевания или состояния, характеризующегося избыточной секрецией ростового гормона, для содействия в снижении веса, для содействия в снижении аппетита, для облегчения поддержания веса, для лечения ожирения, для лечения диабета, для лечения осложнений диабета, включающих ретинопатию, и/или для лечения сердечно-сосудистых заболеваний.
В более предпочтительном варианте осуществления указанного выше способа избыточный вес представляет собой фактор, вносящий дополнительный вклад в развитие указанного заболевания или состояния, включающего гипертензию, диабет, дислипидемию, сердечно-сосудистое заболевание, камни желчного пузыря, остеоартрит и разные формы рака.
В другом более предпочтительном варианте осуществления описанного выше способа указанное содействие в снижении веса уменьшает вероятность развития таких заболеваний или состояний и/или указанное содействие в снижении веса представляет собой по меньшей мере составную часть лечения таких заболеваний или состояний.
Как могут оценить специалисты в данной области, грелин и его агонисты могут использоваться для достижения благоприятного воздействия на сердечно-сосудистую систему (Nagaya et al., Regul Pept. 2003 Jul 15: 114(2-3): 71-77). Например, известно, что грелин ингибирует апоптоз кардиомиоцитов и эндотелиальных клеток in vitro, что повторное введение грелина улучшает структуру и функцию сердечной ткани и ослабляет развитие сердечной кахексии у крыс с сердечной недостаточностью и что грелин снижает системное сосудистое сопротивление и повышает минутный сердечный выброс у пациентов с сердечной недостаточностью (Id). Таким образом, показано, что грелин и агонисты грелина представляют собой потенциальные лекарственные средства для лечения серьезной хронической сердечной недостаточности.
В особенно предпочтительном варианте осуществления каждого из таких способов использования агониста грелина, приведенное в настоящем изобретении, агонист грелина представляет собой соединение формулы:
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
или его фармацевтически приемлемую соль.
Одно или более соединений по настоящему изобретению могут вводиться субъекту. Термин "субъект" в контексте настоящего описания относится к млекопитающему или животному, отличному от млекопитающего, включающему, без ограничения, человека, крысу, мышь или сельскохозяйственное животное. Ссылка на субъект необязательно указывает на то, что данный субъект имеет заболевания или расстройство. Так, термин "субъект" дополнительно включает млекопитающее или животное, отличное от млекопитающего, которому вводят дозу аналога грелина в рамках проводимого эксперимента, млекопитающее или животное, отличное от млекопитающего, которое подвергается лечению с целью облегчения заболевания или состояния, а также млекопитающее или животное, отличное от млекопитающего, которое подвергается профилактическому лечению с целью задержки или предупреждения проявления заболевания или расстройства.
Другие особенности и преимущества настоящего изобретения станут очевидными из приведенного ниже дополнительного описания, включающего различные примеры. Приведенные примеры иллюстрируют разные компоненты и методики, полезные в практике осуществления настоящего изобретения. Указанные примеры не ограничивают область изобретения. На основе приведенного описания любой специалист в данной области может определить и использовать другие компоненты и методики, полезные для осуществления настоящего изобретения.
Если особо не оговорено иное, все аминокислоты, которые имеют один хиральный центр, даны в виде L-энантиомера. Ссылка на производные означает ссылку на модифицированную аминокислоту, такую как соответствующая D-аминокислота, N-алкиламинокислота, β-аминокислота или меченая аминокислота.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к пептидильным аналогам, активным в отношении рецептора СГР. Человеческий грелин представляет собой модифицированный пептид из 28 аминокислот, в котором гидроксильная группа серина этерифицирована n-октановой кислотой (Kojima et al., Nature 1999, 402, 656-660, и Kojima, (Abstract), Third International Symposium on Growth Hormone Secretagogues, Keystone, Colorado, USA 2000, February 17-19).
Ряд аминокислот, встречающихся в соединениях по настоящему изобретению, представлены следующим образом:
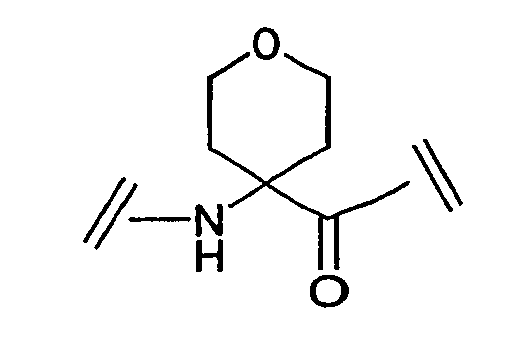
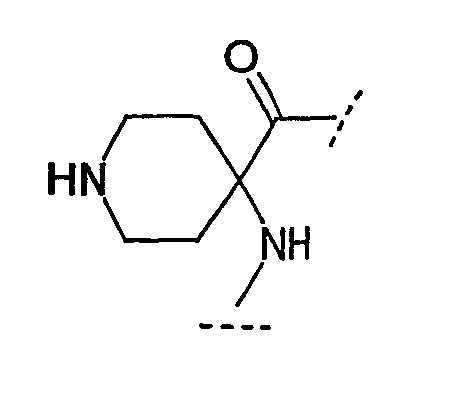
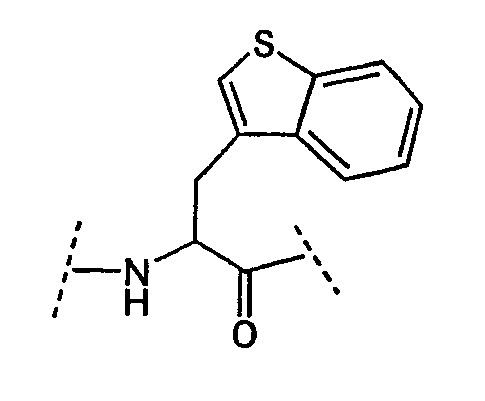
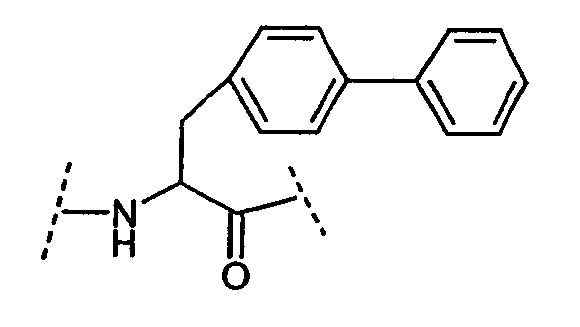
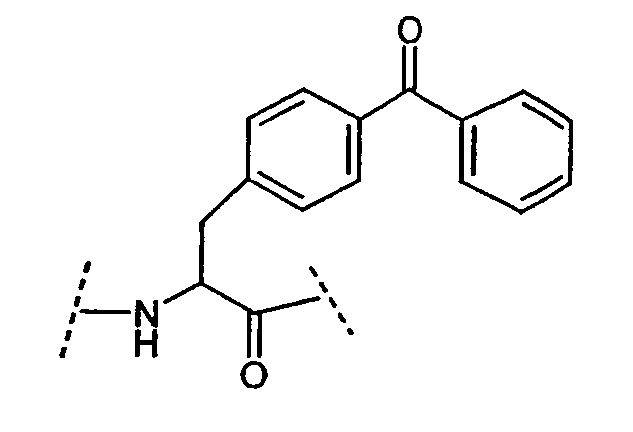
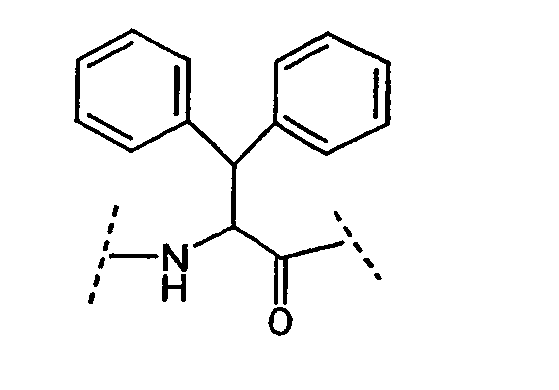
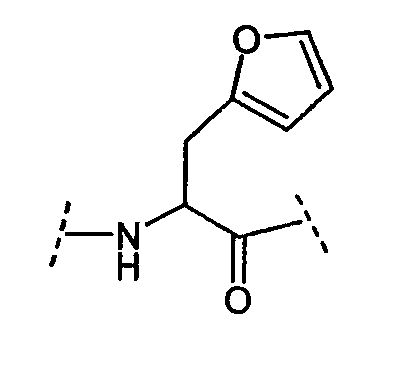
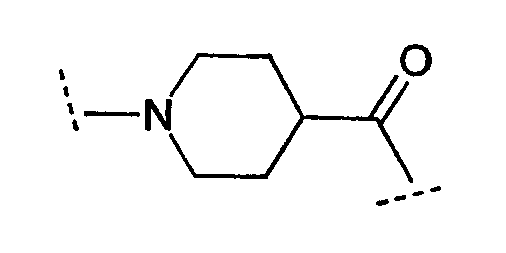
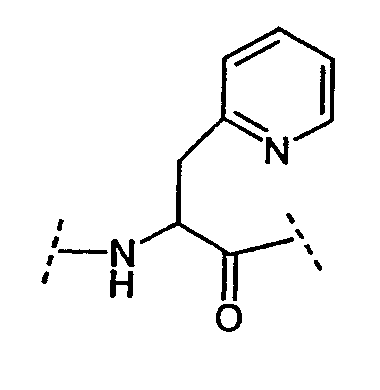
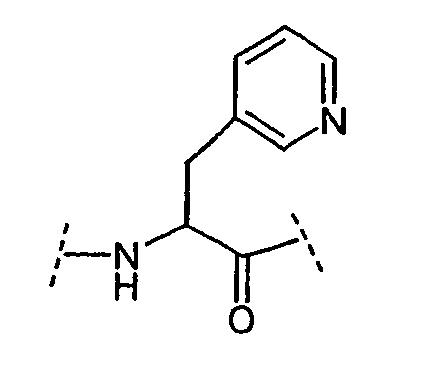
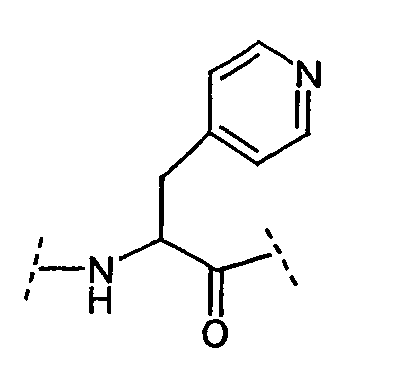
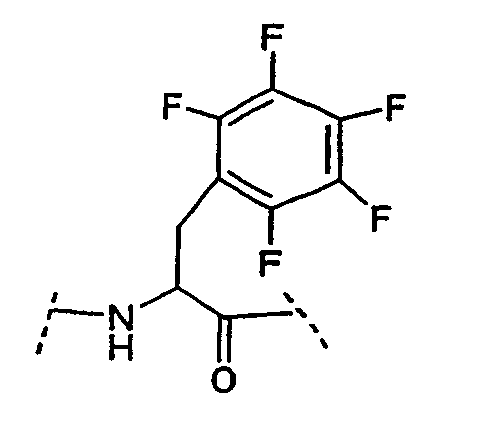
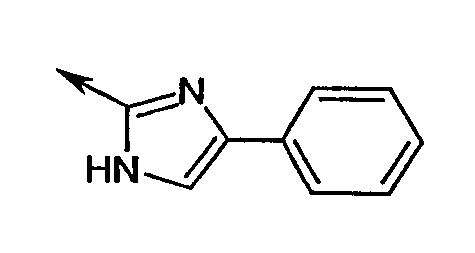
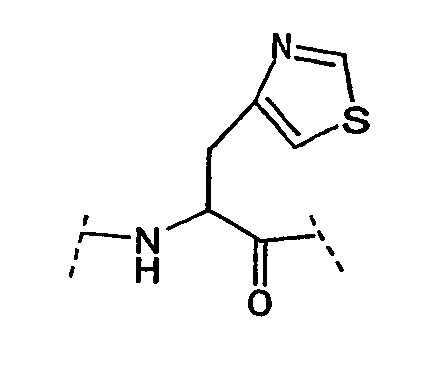
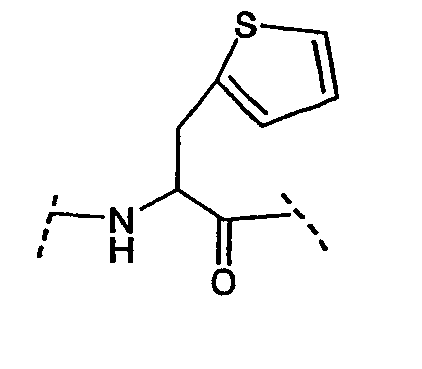
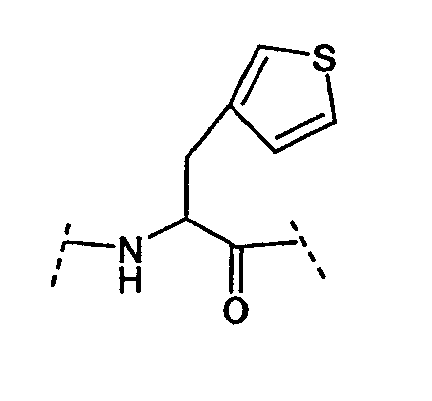
Некоторые другие сокращения, используемые в настоящем изобретении, определяются следующим образом:
Boc: трет-бутилоксикарбонил
Bzl: бензил
DCM: дихлорметан
DIC: N,N-диизопропилкарбодиимид
DIEA: диизопропилэтиламин
Dmab: 4-{N-(1-(4,4-диметил-2,6-диоксоциклогексилиден)-3-метилбутил)-амино}бензил
DMAP: 4-(диметиламино)пиридин
DMF: диметилформамид
DNP: 2,4-динитрофенил
Fmoc: флуоренилметилоксикарбонил
HMTU: гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония
cHex: циклогексил
HOAT: гексафторфосфат О-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония
HOBt: 1-гидрокси-бензотриазол
HOSu: N-гидроксисукцинимид
Mmt: 4-метокситритил
NMP: N-метилпирролидон
Pbf: 2,2,4,6,7,-пентаметилдигидробензофуран-5-сульфонил
tBu: трет-бутил
TIS: триизопропилсилан
TOS: тозил
trt: тритил
TFA: трифторуксусная кислота
TFFH: гексафторфосфат тетраметилфторамидиния
Z: бензилоксикарбонил
Если особо не оговорено иное, сокращенное обозначение аминокислот (например, Ala) в данном описании относится к структуре -NH-C(R)(R')-CO-, где R и R', каждый, обозначает независимо водород или боковую цепь аминокислоты (например, R=CH3 и R'=H в случае Ala) или R и R' могут соединяться с образованием циклической системы.
Термин "алкил" относится к углеводородной группе, содержащей один или более атомов углерода, где множество атомов углерода при их наличии соединяется одинарными связями. Алкильная углеводородная группа может быть линейной или содержать одну или более разветвленных или циклических групп.
Термин "замещенный алкил" относится к алкилу, в котором один или более атомов водорода в углеводородной группе замещены одним или более заместителями, выбранными из группы, состоящей из галогена (например, фтора, хлора, брома и йода), -OH, -CN, -SH, -NH2, -NHCH3, -NO2, -C1-2 алкила, замещенного 1-6 атомами галогена, -CF3, -OCH3, -OCF3 и -(CH2)0-4-COOH. В разных вариантах осуществления изобретения может присутствовать 1, 2, 3 или 4 заместителя. Присутствие -(CH2)0-4-COOH приводит к образованию алкильной кислоты. Примеры алкильных кислот, содержащих -(CH2)0-4-COOH или состоящих из указанного компонента, включают 2-норборнануксусную кислоту, трет-масляную кислоту и 3-циклопентилпропионовую кислоту.
Термин "гетероалкил" относится к алкилу, в котором один или более атомов углерода в углеводородной группе замещены одной или более группой из указанных ниже: амино, амидо, -О- или карбонил. В других вариантах осуществления изобретения присутствует один или два гетероатома.
Термин "замещенный гетероалкил" относится к гетероалкилу, в котором один или более атомов водорода в углеводородной группе замещены одним или более заместителями, выбранными из группы, состоящей из галогена (например, фтора, хлора, брома и йода), -OH, -CN, -SH, -NH2, -NHCH3, -NO2, -C1-2 алкила, замещенного 1-6 атомами галогена, -CF3, -OCH3, -OCF3 и -(CH2)0-4-COOH. В других вариантах осуществления изобретения присутствуют 1, 2, 3 или 4 заместителя.
Термин "алкенил" относится к углеводородной группе, построенной из двух или более атомов углерода, в которой имеется одна или более углерод-углеродных двойных связей. Алкенильная углеводородная группа может быть линейной или может содержать одну или более разветвленных циклических групп.
Термин "замещенный алкенил" относится к алкенилу, в котором один или более атомов водорода замещены одним или более заместителями, выбранными из группы, состоящей из галогена (например, фтора, хлора, брома и йода), -OH, -CN, -SH, -NH2, -NHCH3, -NO2, -C1-2 алкила, замещенного 1-6 атомами галогена, -CF3, -OCH3, -OCF3 и -(CH2)0-4-COOH. В других вариантах осуществления изобретения присутствуют 1, 2, 3 или 4 заместителя.
Термин "арил" относится к необязательно замещенной ароматической группе, в которой содержится по меньшей мере один цикл, имеющий конъюгированную систему пи-электронов, который содержит до двух конъюгированных или конденсированных циклических систем. Арил включает карбоциклический арил, гетероциклический арил и биарильные группы. Предпочтительно арил представляет собой 5- или 6-членный цикл. Предпочтительными атомами для гетероциклического арила являются один или более атомов серы, кислорода и/или азота. Примеры арила включают фенил, 1-нафтил, 2-нафтил, индол, хинолин, 2-имидазол и 9-антрацен. Арильные заместители выбирают из группы, состоящей из -С1-4 алкила, -С1-4 алкокси, галогена (например, фтора, хлора, брома и йода), -OH, -CN, -SH, -NH2, -NO2, -C1-2 алкила, замещенного 1-5 атомами галогена, -CF3, -OCF3, и -(CH2)0-4-COOH. В других вариантах осуществления изобретения арил содержит 0, 1, 2, 3 или 4 заместителя.
Термин "алкиларил" относится к алкилу, присоединенному к арилу.
В случае присутствия на С-конце соединения по настоящему изобретению имидазольного фрагмента, не относящегося к аминокислоте (например, Pim, определенного выше), следует понимать, что имидазольный фрагмент присоединяется к соседней аминокислоте через псевдопептидную связь, где указанная связь образуется между углеродом в положении 2 имидазольного кольца и альфа-углеродом аминокислоты. Например, в том случае, когда соседняя аминокислота представляет собой D-триптофан (D-Trp) и имидазольный фрагмент представляет собой Pim, С-конец пептида будет выглядеть следующим образом:
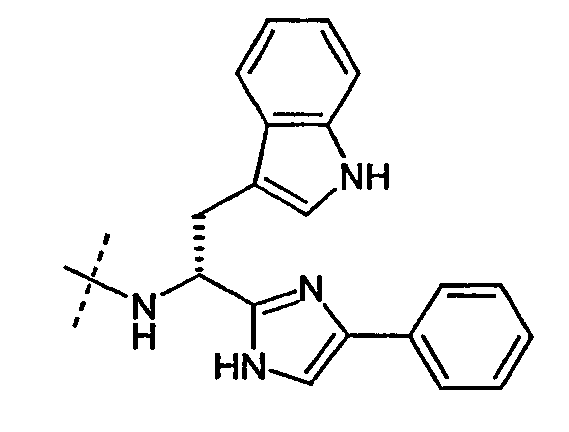
Для ясности следует отметить, что в формуле указанного соединения наличие связи обозначается одной греческой буквой "ψ". Например, записанная в виде H-Inp-D-Trp-D-2Nal(ψ)-Pim формула обозначает следующую структуру:
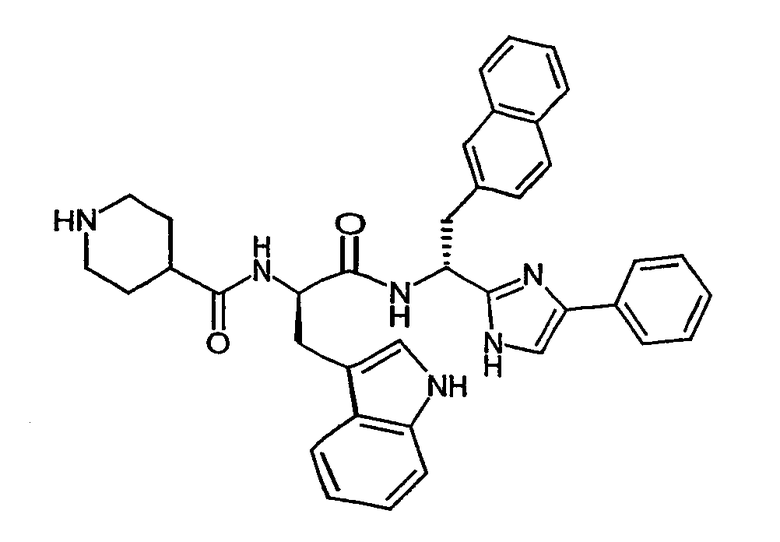
Настоящее изобретение включает диастереомеры, а также их рацемические и разрешенные энантиомерно чистые формы. Аналоги грелина могут содержать D-аминокислоты, L-аминокислоты или их сочетание. Предпочтительно аминокислоты присутствуют в аналоге грелина в виде L-энантиомеров.
Предпочтительные производные аналогов по настоящему изобретению включают D-аминокислоты, N-алкиламинокислоты, β-аминокислоты и/или одну или более меченых аминокислот (включая меченый вариант D-аминокислоты, N-алкиламинокислот или β-аминокислоты). Понятие "меченное производно" указывает на изменение аминокислоты или производного аминокислоты, достигаемое с помощью выявляемой метки. Примеры выявляемых меток включают люминесцентные, ферментативные и радиоактивные метки. Как тип метки, так и ее положение в молекуле могут воздействовать на активность аналога. Метки должны выбираться и встраиваться таким образом, чтобы существенно не изменять активность аналога грелина в отношении рецептора СГР. Влияние конкретной метки и ее положения на активность грелина может быть определено с помощью тестов, позволяющих измерить активность грелина и/или уровня его связывания.
Защитная группа, ковалентно присоединенная к С-концевой карбоксильной группе, снижает реакционную способность карбоксильного конца в условиях in vivo. Защитную группу для карбоксильного конца предпочтительно присоединяют к α-карбонильной группе последней аминокислоты. Предпочтительные защитные группы для карбоксильного конца включают амид, метиламид и этиламид.
Примеры
Ниже даны примеры для дополнительной иллюстрации различных особенностей настоящего изобретения. Приведенные примеры также поясняют методики, полезные для использования в практике осуществления настоящего изобретения. Указанные примеры не ограничивают настоящее изобретение.
Синтез
Соединения по настоящему изобретению могут быть получены с использованием методик, описанных в приведенных примерах, а также методик, известных в данной области техники. Например, полипептидный участок аналога РФРГ может быть химически или биохимически синтезирован и модифицирован. Примеры методик, используемых доля биохимического синтеза, включающих введение нуклеиновой кислоты в клетку и последующую экспрессию нуклеиновых кислот, описаны в работе Аусубеля (Ausubel, Current Protocols in Molecular Biology, John Wiley, 1987-1998 и Sambrook et al., in Molecular Cloning, A Laboratory Manual, 2nd Edition, Cold Spring Harbor Laboratory Press, 1989). Методики химического синтеза полипептидов также известны специалистам в данной области (См., например, Vincent in Peptide and Protein Drug Delivery, New York, N.Y., Dekker, 1990). Например, пептиды по настоящему изобретению могут быть получены с использованием стандартной методики твердофазного синтеза пептидов (См., например Stewart, J.M., et al., Solid Phase Synthesis (Pierce Chemical Co., 2d ed. 1984)).
Заместитель R1 в указанной выше формуле (I) может быть присоединен к свободному амину N-концевой аминокислоты с использованием стандартных способов, известных в данной области техники. Например, алкильные группы, такие как, в частности, (С1-С30)алкил, могут быть присоединены с помощью восстановительного алкилирования. Гидроксиалкильные группы, например, (С1-С30)гидроксиалкил, могут быть присоединены с помощью восстановительного алкилирования, в рамках которого свободную гидроксигруппу защищают с использованием сложного т-бутилового эфира. Ацильные группы, например, СОЕ1, могут быть присоединены за счет связывания свободной кислоты, например, E1COOH, со свободным амином N-концевой аминокислоты путем смешивания приготовленной смолы с тремя молярными эквивалентами свободной кислоты и диизопропилкарбодиимидом в метиленхлориде в течение примерно одного часа. Если свободная кислота содержит свободную гидроксигруппу, например, п-гидроксифенилпропионовую кислоту, то указанное связывание должно проводиться с использованием дополнительных трех молярных эквивалентов HOBT.
Пептиды по настоящему изобретению могут также синтезироваться в параллельном режиме на синтезаторе АСТ 396 (Multiple Biomolecular Synthesizer (Advanced ChemTech, Louisville, KY)) следующим образом. Синтезатор программируют для проведения следующего реакционного цикла: (1) промывка диметилформамидом (ДМФ), (2) удаление защитной группы Fmoc с помощью 20% пиперидина в ДМФ в течение 1×5 минут и 1×25 минут, (3) промывка ДМФ, (4) связывание Fmoc с аминокислотой в течение 1 часа при комнатной температуре в присутствии диизопропилкарбодиимида (ДИК) и 1-гидроксибензотриазола (HOBt) и (5) повторение стадии (4).
Примеры 1-65
Каждая из реакционных ячеек содержит по 0,0675 ммоль смолы Rink Amide MBHA (уровень замещения=0,72 ммоль/г (Novabiochem, San Diego, CA)). Используют следующие Fmoc аминокислоты (Novabiochem, San Diego, CA; Chem-Impex International, Wood Dale, IL; SyntheTech, Albany, OR; Pharma Core, High Point, NC): Fmoc-Lys(Boc)-OH, Fmoc-Phe-OH, Fmoc-H-Inp-OH, Fmoc-D-1Nal-OH, Fmoc-D-2Nal-OH, Fmoc-D-Trp(Boc)-OH, Fmoc-3Pal-OH, Fmoc-4Pal-OH, Fmoc-Orn(Boc)-OH, Fmoc-D-Bip-OH, Fmoc-Thr(Bzl)-OH, Fmoc-Pff-OH, Fmoc-2Thi-OH, Fmoc-Taz-OH, Fmoc-D-Dip-OH, Fmoc-D-Bpa-OH, Fmoc-D-Bal-OH и Fmoc-Apc(Boc)-OH.
Каждую из Fmoc-аминокислот растворяют в 0,3N растворе HOBt в ДМФ, где концентрация полученной Fmoc-аминокислоты составляет 0,3N. Для каждой реакции связывания используют четырехкратный избыток (0,27 ммоль, 0,9 мл 0,3N растворе) Fmoc-аминокислоты. В каждой реакции связывания используют ДИК (0,27 ммоль, 0,6 мл 0,45N раствора ДИК в ДМФ) в качестве сопрягающего реагента для каждой реакции связывания. Удаление защитной группы осуществляют путем использования 20% пиперидина в ДМФ (2×1,5 мл в расчете на остаток).
Пептиды выщепляют из смолы путем обработки сочетания пептид-смола 8% триизопропилсиланом (ТИП) в трифторуксусной кислоте (ТФУ) (1,5 мл на реакционную ячейку) при комнатной температуре в течение 2 часов. Смолу удаляют фильтрованием. Каждый полученный фильтрат разбавляют в центрифужной пробирке до 25 мл эфиром. Полученный в каждой пробирке осадок центрифугируют и растворители отделяют от осадка декантированием. Затем осадок в каждой пробирке растворяют в метаноле (3 мл) и разбавляют водой (1 мл). Очистку продуктов осуществляют методом препаративной ВЭЖХ с обращением фазы с использованием колонки (100×21,20 мм, 5 мкм) LUNA 5 мкм С8(2) (Phenomenex, Torrance, CA). Для получения каждого из пептидов проводят элюцию с колонки линейным градиентом от 85% А и 15% В до 25% А и 75% В в течение 15 минут со скоростью 25 мл/мин. А представляет 0,1% ТФУ в воде и В представляет 0,1% ТФУ в смеси ацетонитрил/вода (80/20, объем/объем). Фракции оценивают методом аналитической ВЭЖХ и те фракции, которые содержат чистый продукт, объединяют и лиофилизируют досуха.
Выход продукта варьирует от 13% до 71% и чистота каждого из продуктов, полученных в примерах 1-65, превышает 94% по результатам анализа методом аналитической ВЭЖХ. Проводят анализ методом спектрометрии с ионизацией электронапылением (ES-MS), и получаемое при этом значение молекулярной массы согласуется с вычисленными молекулярными массами. Результаты приведены в таблице 1 ниже.
Примеры 66-69
Продукты примеров 66-69 синтезируют по приведенной ниже процедуре.
1.а. BOC-(D)-Trp-OH (4,0 г, 13,1 ммоль) (Novabiochem San Diego, CA) в метаноле (36 мл) и Cs2CO3 (2,14 г, 6,57 ммоль) в воде (10 мл) объединяют и смесь взбалтывают до образования гомогенной смеси. Растворители удаляют в вакууме и остаток растворяют в ДМФ (45 мл). К раствору добавляют 2-бромацетофенон (2,61 г, 13,2 ммоль) в ДМФ (9 мл) и раствор перемешивают в течение 30 минут при комнатной температуре. Бромид цезия удаляют фильтрованием и фильтрат концентрируют в вакууме. Полученный концентрат растворяют в ксилолах (45 мл), добавляют NH4OAc (17,1 г) и раствор нагревают при температуре кипения с обратным холодильником в течение 1 часа. Охлажденный раствор промывают несколько раз насыщенным раствором NaHCO3 (45 мл) и затем насыщенным NaCl. Полученный органический слой очищают флэш-хроматографией с образованием 4,1 г (77%) промежуточного продукта 1А, показанного на схеме 1А ("Соединение 1А").
Схема 1А
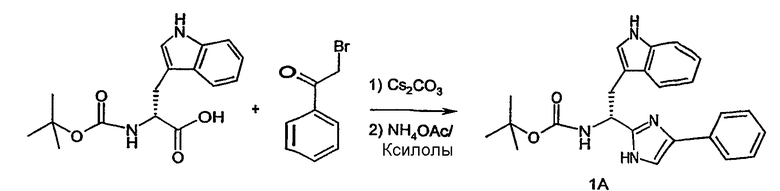
1b. Соединение 1А (403 мг) подвергают разблокированию с использованием смеси трифторуксусной кислоты (ТФУ) (8 мл) дихлорметана (ДХМ) (8 мл) и триизопропилсилана (ТИПС) (1,4 мл). После перемешивания в течение одного часа раствор концентрируют в потоке азота. Остаток растворяют в ДХМ (40 мл), промывают два раза насыщенным раствором NaHCO3 (40 мл) и затем сушат над Na2SO4 с получением раствора промежуточного продукта 1B, показанного на схеме 1В ниже.
Схема 1В
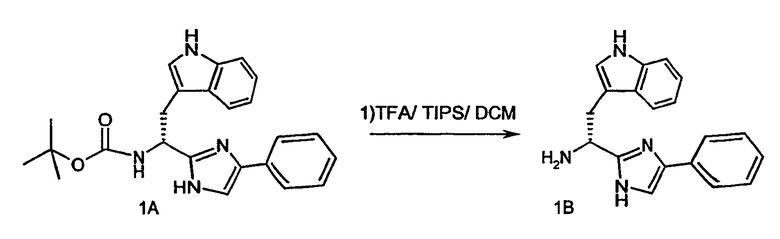
1с.-f. Указанный раствор промежуточного продукта 1В разделяют на четыре равные части и связывают с предварительными активированными сложными HOBT эфирами FMOC-защищенных аминокислот, как показано ниже на реакционных схемах 1C, 1D, 1E и 1F. В каждом из примеров 66, 67, 68 и 69 используемая аминокислота представляет собой следующую аминокислоту:
- Пример 66: FMOC-D-2Nal-OH (130 мг, 0,30 ммоль) (Synthetech Albany, Oregon)
- Пример 67: FMOC-D-1Nal-OH (130 мг, 0,30 ммоль) (Advanced Chemtech Louisville, KY)
- Пример 68: FMOC-D-Bal-OH (132 мг, 0,30 ммоль) (Chem Impex Wood Dale, IL)
- Пример 69: FMOC-DSer(Bzl)-OH (124 мг, 0,30 ммоль) (Chem Impex Wood Dale, IL).
Каждая из приведенных аминокислот подвергается предварительной активации под действием HOBT (46 мг, 0,30 ммоль) и ДИК (38 мг, 0,30 ммоль) в ДХМ (5 мл) в течение десяти минут перед добавлением к одной из четырех порций указанного выше раствора промежуточного продукта 1В. Затем проводят реакцию связывания в течение 30 минут при комнатной температуре.
Схема 1С
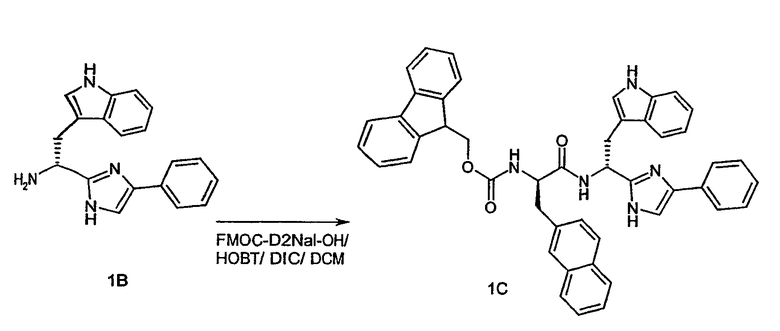
Схема 1D
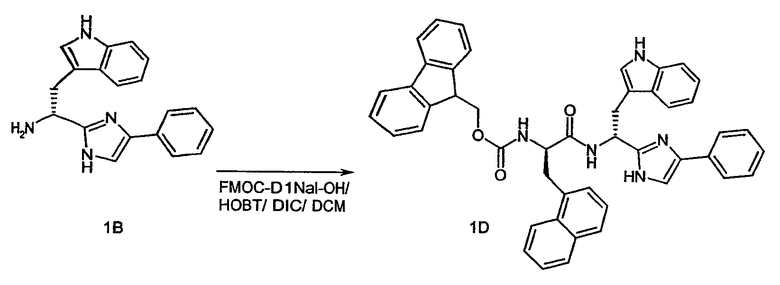
Схема 1E
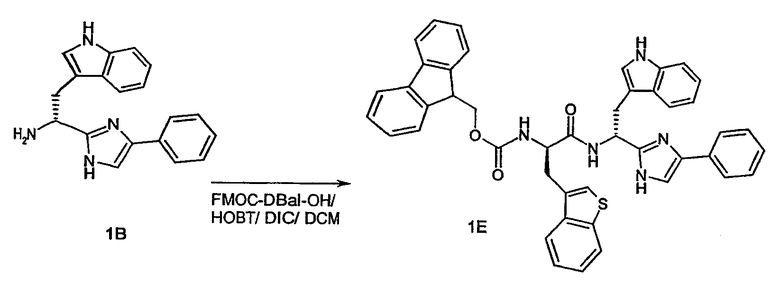
Схема 1F
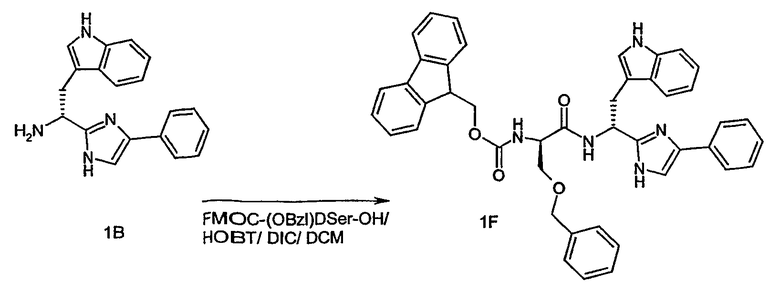
1g.-j. FMOC группу удаляют от каждого из полученных соединений 1C, 1D, 1E и 1F путем добавления трис(2-аминоэтил)амина (0,9 мл) к соответствующим реакционным смесям, полученным на предварительной стадии, и перемешивают в течение 30 минут при комнатной температуре. Затем реакционные смеси, содержащие разблокированные соединения, промывают три раза 10% фосфатным буфером, pH 5,5 (10 мл).
Полученные растворы со свободным амином связывают с предварительно активированными сложными HOBT эфирами FMOC- или BOC-защищенных аминокислот следующим образом:
- Пример 66: FMOC-Inp-OH (105 мг, 0,30 ммоль) (Chem Impex Wood Dale, IL)
- Пример 67: FMOC-Inp-OH (105 мг, 0,30 ммоль)
- Пример 68: BOC-Inp-OH (68,3 мг, 0,30 ммоль) (Bachem Torrance, Calif)
- Пример 69: BOC-Aib-OH (60,6 мг, 0,30 ммоль) (Bachem Torrance, Calif).
Каждая из приведенных аминокислот подвергается предварительной активации под действием HOBT (46 мг, 0,30 ммоль) и ДИК (38 мг, 0,30 ммоль) в ДХМ (5 мл) в течение десяти минут перед добавлением к соответствующему амину, от которого удалена защитная группа. Затем проводят реакцию связывания в течение одного часа при комнатной температуре.
Удаление защитной группы: соединения примеров 66-67. Группу FMOC удаляют от полученных FMOC-защищенных соединений путем добавления трис(2-аминоэтил)амина (0,9 мл) с последующим перемешиванием в течение 30 минут. Разблокированные соединения промывают три раза 10% фосфатным буфером, pH 5,5 (10 мл) и собирают неочищенные продукты в виде осадка.
Удаление защитной группы: соединения примеров 68-69. BOC-защищенные соединения очищают флэш-хроматографией и затем подвергают разблокированию в течение одного часа путем добавления ТИПС (0,50 мл), ТФУ (0,50 мл) в ДХМ (2,75 мл). Неочищенные продукты далее концентрируют и сушат в вакууме.
Очистка методом ВЭЖХ дает продукты с 5% и 29% выходом соединений из примеров 66 и 67 соответственно и с выходом 15% и 43% соединений из примеров 68 и 69 соответственно.
Указанные выше реакции введения защитных групп, связывания и удаления защитных групп показаны ниже на реакционных схемах 1G, 1H, 1I и 1J.
Схема 1G
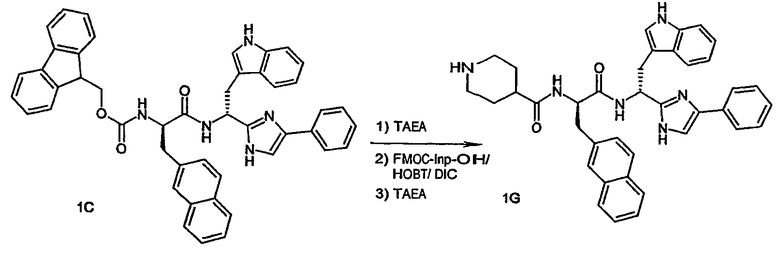
Схема 1H
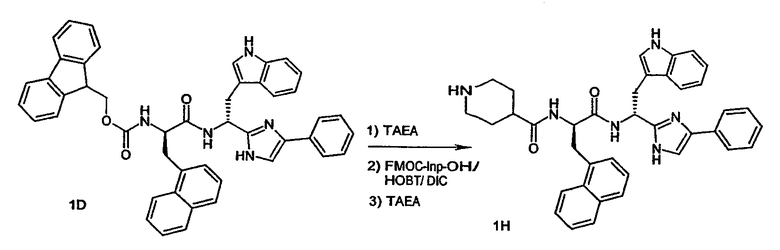
Схема 1I
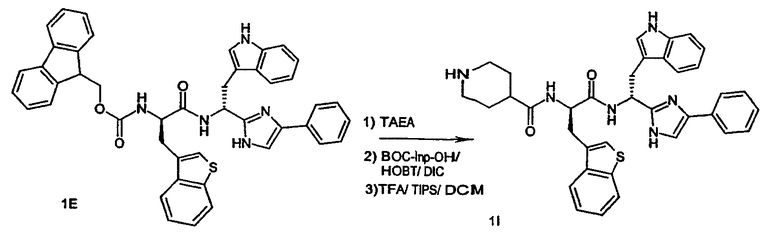
Схема 1J
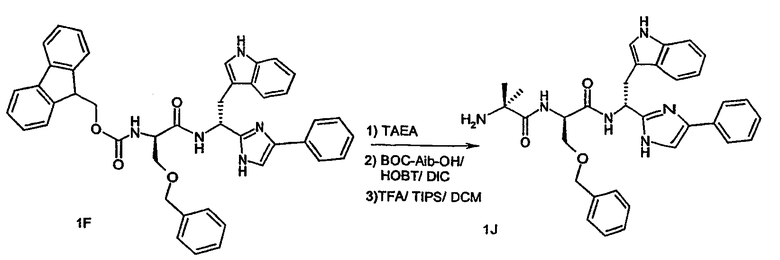
Пример 70: H-Inp-D-Trp-D-2Nal(ψ)-Pim
Соединение примера 70 синтезируют по приведенной ниже процедуре.
2.а.1 и 2.а.2.: Соединение 2А получают по способу, аналогичному способу получения соединения 1А, с использованием BOC-D-2Nal-OH и 2-бромацетофенона в качестве исходных продуктов.
Стадии 2.а.1 и 2.а.2. показаны на схеме 2А ниже.
Схема 2А
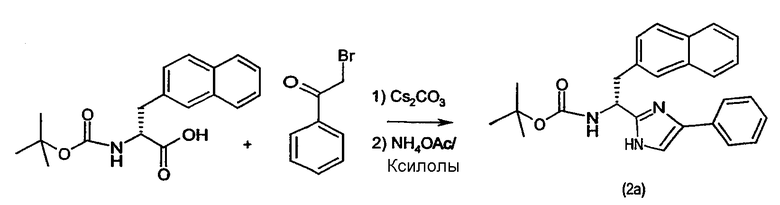
2.b.1. Соединение 2A (100 мг, 0,242 ммоль) подвергают разблокированию в ТФУ (2 мл) и ДХМ (2 мл) в течение одного часа. Летучие продукты удаляют в потоке азота и остаток растворяют в ДХМ (10 мл). Полученный раствор промывают три раза насыщенным раствором NaHCO3 (10 мл) с получением раствора соединения 2А со свободной аминогруппой.
2.b.2. Активный сложный эфир FMOC-D-Trp-(BOC)-OH (153 мг, 0,290 ммоль) получают с использованием N-гидроксисукцинимида (HOSu; 33 мг, 0,290 ммоль) и ДИК (37 мг, 0,290 ммоль) в ДХМ (1,5 мл). Через один час диизопропилмочевину удаляют фильтрованием и фильтрат добавляют к соединению раствора 2А (в форме свободного амина). Полученный раствор разбавляют ДХМ до 4 мл и проводят реакцию связывания в течение 30 минут.
Стадии 2.b.1 и 2.b.2. показаны на схеме 2B ниже.
Схема 2B
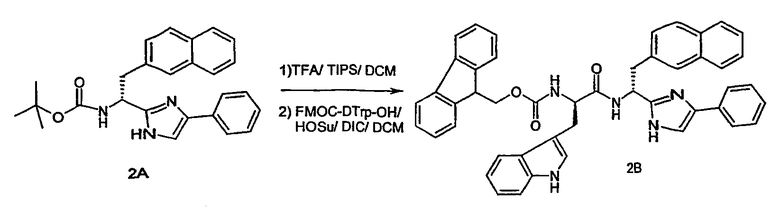
2.с.1. Соединение 2В подвергают разблокированию путем добавления трис(2-аминоэтил)амина (ТАЭА) (0,9 мл) к указанному выше раствору для реакции проведения реакции связывания и перемешивают в течение 30 минут при комнатной температуре. Далее раствор промывают три раза насыщенным раствором NaCl (10 мл) и затем три раза 10% фосфатным буфером, pH 5,5 (10 мл) с получением раствора соединения 2В со свободной аминогруппой.
2.с.2. Активный сложный эфир BOC-Inp-OH (66,5 мг, 0,290 ммоль) получают с использованием HOSu (33 мг, 0,290 ммоль) и ДИК (37 мг, 0,290 ммоль) в ДХМ (1,5 мл). Через один час диизопропилмочевину удаляют фильтрованием и фильтрат добавляют к соединению раствора 2В (со свободной аминогруппой). Полученный раствор разбавляют ДХМ до 4 мл и проводят реакцию связывания в течение 12 часов.
Реакционную смесь промывают три раза 10% фосфатным буфером, pH 5,5 (10 мл) и сушат над Na2SO4. Растворитель удаляют в вакууме и концентрат очищают флэш-хроматографией.
2.с.3. Промежуточный продукт подвергают разблокированию с использованием ТФУ (2,75 мл), и ТИПС (0,5 мл) в ДХМ (2,75 мл) в течение 30 минут. Летучие продукты удаляют из реакционной смеси в потоке азота и остаток растирают с эфиром (15 мл). После центрифугирования эфир удаляют декантированием и полученный твердый материал подвергают ВЭЖХ с получением очищенного соединения 70 с выходом 39%.
Стадии 2.с.1 и 2.с.2, и 2.с.3 показаны на схеме 2С ниже.
Схема 2С
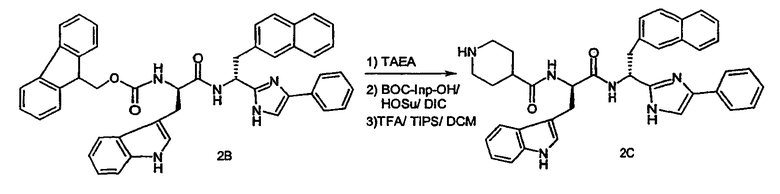
Другие пептиды по настоящему изобретению могут быть получены специалистом со средним уровнем знаний в данной области с использованием процедур синтеза, аналогичных процедурам, описанным в основном выше и/или конкретно раскрытых в приведенных выше примерах, как соединения, проиллюстрированные в Таблице 1.
Биологическое тестирование
Активность соединений по настоящему изобретению в отношении рецептора СГР может быть определена и была определена с использованием методик, таких как описаны в приведенном ниже разделе примеров. В разных вариантах осуществления настоящего изобретения аналог грелина обладает активностью, составляющей по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере примерно 80% или по меньшей мере примерно 90% от функциональной активности грелина, определенной с использованием одного или более тестов на функциональную активность, описанных ниже; и/или имеет показатель ИК50 выше, чем примерно 1000 нМ, выше, чем примерно 100 нМ, или выше, чем примерно 50 нМ при определении в рамках теста на связывание с рецептором, описанного ниже. Что касается показателя ИК50, то его большее значение соответствует более высокой активности и, таким образом, указывает на меньшее количество, необходимое для достижения ингибирования связывания.
В тестах на определение способности соединения связываться с рецептором СГР используют рецептор СГР, фрагмент рецептора, включающий сайт связывания грелина, полипептид, включающий такой фрагмент, или производное полипептида. Предпочтительно в тесте используют рецептор СГР или его фрагмент. Полипептид, включающий фрагмент рецептора СГР, который связывает грелин, также может содержать один или более участков полипептида, не входящих в рецептор СГР. Производное такого полипептида включает фрагмент рецептора СГР, который связывает грелин, вместе с одним или более компонентами не пептидной природы.
Аминокислотная последовательность рецептора СГР, участвующая в связывании, может быть легко идентифицирована с использованием меченого грелина или структурных или функциональных аналогов грелина и различных фрагментов рецептора. Могут использоваться различные стратегии для выбора фрагментов, подлежащих тестированию с целью определения участка связывания. Примеры таких стратегий включают определение последовательных фрагментов, содержащих в длину примерно 15 аминокислот с началом на N-конце, и тестирование более длинных фрагментов. Если тестируют более длинные фрагменты, то фрагмент, связывающий грелин, может быть подразделен на другие участки с целью выявления участка связывания с грелином. Используемые в исследованиях по связыванию фрагменты могут быть получены с помощью технологии рекомбинантной нуклеиновой кислоты.
Тест на связывание может быть проведен с использованием индивидуальных соединений или препаратов, содержащих различное число соединений. Препарат, содержащий различное число соединений, обладающих способностью связываться с рецептором СГР, может быть разделен на более мелкие группы соединений, которые могут исследоваться с целью идентификации одного или нескольких соединений, связывающихся с рецептором СГР. В одном варианте осуществления настоящего изобретения в тесте на связывание используют исследуемый препарат, который содержит по меньшей мере 10 соединений.
Тесты на связывание могут проводиться с использованием полученных рекомбинантными методами полипептидов рецептора СГР, присутствующих в различном окружении. Такие различные виды окружения включают, например, экстракты клеток и очищенные экстракты клеток, содержащие полипептид рецептора СГР, экспрессируемый на основе рекомбинантной нуклеиновой кислоты или природной нуклеиновой кислоты, а включает также, например, использование очищенного полипептида рецептора СГР, полученного рекомбинантными методами или из природной нуклеиновой кислоты, которую вводят в другое окружение.
Скрининг соединений, активных в отношении рецептора СГР
Скрининг соединений, активных в отношении рецептора СГР, проводят с использованием рекомбинантно экспрессированного рецептора. Использование рекомбинантно экспрессированного рецептора СГР дает несколько преимуществ, таких как способность экспрессировать рецептор в определенной клеточной системе, так что реакция на соединение на рецепторе СГР может быть легко дифференцирована от реакции на других рецепторах. Например, рецептор СГР может быть экспрессирован в клеточной линии, такой как HEK 293, COS 7, и CHO, который в норме не экспрессирует рецептор на основе вектора экспрессии, тогда как та же самая клеточная линия без вектора экспрессии может действовать в качестве контроля.
Скрининг соединений, снижающих активность СГР рецептора, проводят при использовании в тесте функционального аналога грелина. Использование функционального аналога грелина в скрининге поддерживает активность рецептора СГР. Влияние исследуемых соединений на такую активность может быть определено с целью идентификации, например, аллостерических модуляторов и антагонистов.
Активность рецептора СГР может быть измерена с использованием различных методик, таких как выявление изменений внутриклеточной конформации рецептора СГР, в активностях, сопряженных с G-белком, и/или в внутриклеточных переносчиках. Предпочтительно активность в отношении рецептора СГР определяют с использованием таких методов, как на основе измерения внутриклеточного Ca2+. Примеры методик, известных в данной области техники, которые могут использоваться для определения уровня Ca2+, включают использование красителей, таких как Fura-2, и использование Ca2+-биолюминесцентных чувствительных репортерных белков, таких как акворин. Примером клеточной линии, использующей акворин, которую применяют для определения активности G-белка, является HEK293/aeq17. (Button et al., 1993. Cell Calcium 14, 663-671, и Feighner et al., 1999, Science 284, 2184-2188).
Химерные рецепторы, содержащие участок связывания грелина, функционально сопряженный с другим G-белком, также может использоваться для определения активности рецептора СГР. Химерный рецептор СГР содержит N-концевой внеклеточный домен, трансмембранный домен, построенный из трансмембранных участков, внеклеточных петлевых участков и внутриклеточных петлевых участков, а также внутриклеточного карбоксильного конца. Методики получения химерных рецепторов и оценки сопряженных с G-белком реакций описаны, например, в заявке на Международный патент WO 97/05252 и в патенте США No. 5264565, которые, оба, включены в настоящее описание в качестве ссылки.
Стимуляция активности рецептора СГР
Структурные и/или функциональные аналоги грелина могут использоваться для стимуляции активности рецептора СГР. Такая стимуляция может применяться, например, для изучения эффекта модуляции рецептора СГР, для изучения эффекта секреции ростового гормона, для поиска или изучения антагонистов грелина или для достижения благоприятного эффекта у субъекта. Благоприятные эффекты, которые могут быть при этом достигнуты, включают один или более эффектов из числа приведенных ниже: лечение состояния, дефицитного по ростовому гормону, повышение мышечной массы, повышение плотности кости, лечение расстройств половой функции у мужчин или у женщин, содействие в наращивании веса, облегчение поддержания веса, облегчение поддержания активного физического состояния, облегчение восстановления физической функции и/или содействие в повышении аппетита.
Повышение веса или аппетита могут использоваться для поддержания веса, или для наращивания веса, или для улучшения аппетита у субъекта со сниженным весом или у пациента, имеющего заболевание или подвергающегоя лечению, которое воздействует на вес или аппетит. Кроме того, например, сельскохозяйственные животные, такие как свиньи, коровы и куры, могут подвергаться указанному воздействию с целью повышения веса.
Субъекты со сниженным весом включают тех субъектов, которые имеют вес тела на уровне 10% или менее, 20% или менее, или 30% или менее, чем нижний предел диапазона нормального веса или индекс массы тела (ИМТ). Показатель ИМТ основан на измерении соотношения рост/вес и определяется путем вычисления веса в килограммах с последующим делением на квадрат роста в метрах. "Нормальный" диапазон значений показателя ИМТ для человека в основном составляет в пределах 19-22. "Нормальный" диапазон известен в данной области и принимает во внимание такие факторы, как возраст субъекта, рост и тип организма.
Биологические тесты-примеры
1. Тест на связывание с рецептором
А. Получение клеток CHO-K1, экспрессирующих человеческий рекомбинантный рецептор СГР
кДНК для человеческого рецептора средства, способствующего секреции ростового гормона (hGHS-R или рецептор грелина), клонируют в рамках полимеразной цепной реакции с использованием РНК из мозга человека в качестве матрицы (Clontech, Palo Alto, CA), специфических генных праймеров, фланкирующих кодирующую последовательность полной длины hGHS-R (S:5'-ATGTGGAACGCGACGCCCAGCGAAGAG-3'(SEQ ID NO: 1) и AS: 5'-TCATGTATTAATACTAGATTCTGTCCA-3') (SEQ ID NO: 2) и набор для проведения ПЦР Advantage 2 PCR Kit (Clontech). Продукт ПЦР клонируют в векторе pCR2.1 с использованием набора для клонирования Original TA Cloning Kit (Invitrogen, Carlsbad, CA). Человеческий СГР-R полной длины субклонируют в векторе экспрессии млекопитающих pcDNA 3.1 (Invitrogen). Плазмиду трансфицируют в линию клеток яичников китайского хомячка CHO-K1 (American Type Culture Collection, Rockville, MD) по методу, использующему фосфат кальция (Wigler M, et al., Cell 11, 223, 1977). Клоны одной клетки, стабильно экспрессирующие hGHS-R, получают путем отбора трансфицированных линий, растущих в клонирующих кольцах в средах RPMI 1640 с добавкой 10% сыворотки теленка и 1 мМ пирувата натрия с содержанием 0,8 мг/мл G418 (Gibco, Grand Island, NY).
В. Тест на связывание с СГР-R
Мембраны для исследования связывания с радиоактивным лигандом могут быть получены и получали путем гомогенизации указанных выше клеток CHO-K1, экспрессирующих человеческий рекомбинантный рецептор СГР в 20 мл охлажденного на льду 50 мМ буфера Трис-HCl с использованием Brinkman Polytron (Westbury, NY) (установка 6, 15 секунд). Гомогенаты промывают два раза при проведении центрифугирования (39000 g/10 минут) и полученный при окончательном центрифугировании осадок ресуспендируют в 50 мМ буфера Трис-HCl, содержащего 2,5 мМ MgCl2 и 0,1% БСА. Для теста берут аликвоты (по 0,4 мл) и инкубируют с 0,05 нМ (125I)грелина (˜2000 Ci/ммоль, Perkin Elmer Life Sciences, Boston, MA) при добавлении или без добавления 0,05 мл немеченых конкурентных исследуемых соединений по настоящему изобретению. После 60 минут инкубации (4°С) связанный (125I)грелин отделяют от свободного грелина путем быстрого фильтрования через фильтры GF/C (Brandel, Gaithersburg, MD), которые были предварительно вымочены в 0,5% полиэтиленимине/0,1% БСА. Затем фильтры промывают три раза аликвотами по 5 мл охлажденного на льду 50 мМ буфера Трис-HCl с добавкой 0,1% бычьего сывороточного альбумина и связанную радиоактивность, оставшуюся на фильтрах, определяют количественно на гамма-спектрометре (Wallac LKB, Gaithersburg, MD). Специфическое связывание определяют как общий связанный (125I)грелин минус количество, которое было связанно в присутствии 1000 нМ грелина (Bachem, Torrence, CA).
2. Тест на функциональную активность СГР-R
А. Активность in vitro рецептора СГР,
опосредованная мобилизацией внутриклеточного Ca2+
Указанные выше клетки CHO-K1, экспрессирующие человеческий рецептор СГР, собирают после инкубации в 0,3% ЭДТА/фосфатном буферном солевом растворе (25°С) и промывают два раза при центрифугировании. Промытые клетки ресуспендируют в забуференном солевом растворе Хенкса (HBSS) для внесения флуоресцентного индикатора Ca2+ Fura-2AM. Клеточные суспензии, содержащие примерно 106 клеток/мл, инкубируют с 2 мкМ Fura-2AM в течение 30 минут при 25°С. Неосевший Fura-2AM удаляют путем двукратного центрифугирования в HBSS и окончательную суспензию переносят на спектрофотометр (Hitachi F-2000), снабженный магнитным механизмом для перемешивания и держателем кюветы с регулируемой температурой. После уравновешивания при 37°С добавляют соединения по настоящему изобретению для измерения мобилизации внутриклеточного Ca2+. Длины волн возбуждения и эмиссии составляют 340 и 510 нм, соответственно.
В. Высвобождение/супрессия РГ in vivo
Как известно в данной области, соединения могут оцениваться на их способность стимулировать или подавлять высвобождение ростового гормона (РГ) in vivo. (См., например, Deghenghi, R., et al., Life Sciences 54, 1321-1328 (1994); Заявка на Международный патент No. WO 02/08250). Так, например, для определения способности соединения стимулировать высвобождение РГ in vivo указанное соединение может быть инъецировано подкожно 10-дневным крысам в дозе, например, 300 мг/кг. Циркулирующий в крови РГ может быть определен, например, через 15 минут после инъекции и далее проводится сравнение с уровнем РГ у контрольных крыс, которым был инъецирован только растворитель.
Аналогично соединения могут оцениваться на их способность антагонизировать индуцированную грелином секрецию РГ in vivo. Так, соединение может быть инъецировано подкожно 10-дневным крысам в дозе, например, 300 мг/кг вместе с грелином. И снова уровень циркулирующего в крови РГ может быть определен, например, через 15 минут после инъекции и далее проводится сравнение с уровнями РГ у контрольных крыс, которым был инъецирован только грелин.
Введение
Соединения по настоящему изобретению могут быть включены в состав композиции и введены субъекту с использованием приведенного в настоящем описании руководства в соответствии с известными в данной области методиками. Предпочтительный способ введения гарантирует, что эффективное количество соединения достигнет органа-мишени. Руководства по введению фармацевтических препаратов в основном известны в данной области (например, Remington's Pharmaceutical Sciences 18th Edition, Ed. Gennaro, Mack Publishing, 1990 и Modem Pharmaceutical 2nd Edition, Eds. Banker and Rhodes, Marcel Dekker, Inc., 1990), которые приведены в настоящем описании в качестве ссылки.
Соединения по настоящему изобретению могут быть получены в виде кислых или основных солей. Фармацевтически приемлемые соли (в виде водо- или маслорастворимых или диспергируемых продуктов) включают традиционные нетоксичные соли или четвертичные аммониевые соли, образованные, например, с использованием неорганических или органических кислот или оснований. Примеры таких солей включают аддитивные соли кислоты, такие как ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат; а также аддитивные соли основания, такие как аммониевые соли, соли щелочного металла, такие как соли натрия и калия, соли щелочноземельного металла, такие как соли кальция и магния, соли, полученные с использованием органических оснований, такие как соли дициклогексиламина, N-метил-D-глюкамина и соли, полученные на основе аминокислот, таких как аргинин и лизин.
Соединения по настоящему изобретению могут вводиться с использованием различных способов, включающих пероральный, назальный способы, введение инъекций, чрескожные и чресслизистые инъекции. Активные ингредиенты, вводимые перорально в виде суспензии, могут быть получены в соответствии с известными в данной области методиками, используемыми для изготовления фармацевтических композиций, и могут содержать микрокристаллическую целлюлозу для придания объема, альгиновую кислоту или альгинат натрия в качестве средства, способствующего суспендированию, метилцеллюлозу в качестве усилителя вязкости и подсластители/вкусовые вещества. При изготовлении таблеток с быстрым высвобождением применяемые для таких целей композиции могут содержать микрокристаллическую целлюлозу, фосфат дикальция, крахмал, стеарат магния и лактозу и/или другие наполнители, связующие вещества, средства, создающие объем, дезинтегранты, разбавители и замасливатели.
Композиции, вводимые с помощью назального аэрозоля или путем ингаляции, могут быть получены, например, в виде растворов в солевом растворе с использованием бензилового спирта или других приемлемых консервантов, усилителей всасывания для повышения биодоступности, с использованием фторуглеродов и/или с использованием других солюбилизирующих или диспергирующих средств.
Соединения по настоящему изобретению могут также вводиться в форме, пригодной для внутривенного введения (путем болюса и инфузии), внутрибрюшинного, подкожного, местного введения, при использовании окклюзионной повязки или без нее, а также в форме, пригодной для внутримышечного введения. В случае введения инъекцией инъецируемый раствор или суспензия могут быть приготовлены с использованием соответствующих нетоксичных парентерально приемлемых разбавителей или растворителей, таких как раствор Рингера или изотонический раствор хлорида натрия, или с использованием подходящих диспергирующих или смачивающих и суспендирующих средств, таких как стерильные, легкие, жирные масла, включая синтетические, моно- или диглицериды жирных кислот, включающих олеиновую кислоту.
Подходящие режимы дозирования предпочтительно определяют, принимая во внимание такие известные в данной области факторы, как тип субъекта, подлежащего лечению, возраст, вес, пол и состояние здоровья субъекта, способ введения, функциональное состояние почек и печени субъекта, желательный эффект и природа конкретного используемого соединения.
Оптимальная точность в создании концентраций используемого лекарственного средства в диапазоне, который приводит к достижению эффективности без признаков токсичности, требует использования режима введения, основанного на изучении кинетики поступления лекарственного средства в сайты-мишени. Указанные исследования включают оценку распределения, достижения равновесного состояния и удаления лекарственного средства. Ожидается, что дневная доза для субъекта должна составлять от 0,01 до 1000 мг в день на субъекта.
Соединения по настоящему изобретению могут поставляться в виде набора. Такой набор в типичном случае содержит активное соединение в форме пригодной для введения дозы. Дозированная форма содержит достаточное количество активного соединения, так чтобы мог быть достигнут желательный эффект при введении субъекту с регулярными интервалами, например, от 1 до 6 раз в день, в течение курса, составляющего один или более дней. Предпочтительно набор содержит инструкции, определяющие правила, применяемые для достижения желательного воздействия и указывающие количества дозированной формы, которые должны приниматься в течение определенного периода времени.
Настоящее изобретение описано в иллюстративной форме, и следует понимать, что используемая терминология дана для пояснения описания, а не с целью ограничения. Очевидно, что возможны различные модификации и вариации настоящего изобретения в свете приведенного описания. Следует также понимать, что в рамках тематики, указанной в приведенной формуле изобретения, настоящее изобретение осуществляется независимо от конкретного описания.
Патентная и научная литература, приведенная в качестве ссылок, описывает уровень знаний, достигнутых в настоящей области. Все патенты, патентные публикации и другие цитированные в описании публикации включены полностью в качестве ссылок.
Другие варианты осуществления изобретения
Следует понимать, что несмотря на то что настоящее изобретение было представлено в сочетании с его подробным описанием, такое описание дано лишь с целью пояснения, но не с целью ограничения объема изобретения, который определяется объемом прилагаемой формулы изобретения. Другие аспекты, преимущества и модификации также определяются формулой изобретения.
Раскрываются рилизинг-пептиды ростового гормона формулы (I): R1-A1-A2-A3-A4-A5-R2, где: А1 обозначает Aib, Apc или Inp; А2 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp; А3 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-lNal, D-2Nal, D-2Ser(Bzl) или D-Trp; А4 обозначает 2Fua, Orn, 2Pal, 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi, 3Thi, Thr(Bzl); А5 обозначает Ape, Dab, Dap, Lys, Orn или делетирован; R1 обозначает водород; и R2 обозначает NH2; и их фармацевтически приемлемые соли, а также фармацевтические композиции и способы их применения. 9 н. и 18 з.п. ф-лы, 1 табл.
R1-A1-A2-A3-A4-A5-R2
или его фармацевтически приемлемая соль, где
А1 обозначает Aib, Ape или Inp;
А2 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp;
А3 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-2Ser(Bzl) или D-Trp;
А4 обозначает 2Fua, Orn, 2Pal, 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi, 3Thi, Thr(Bzl);
А5 обозначает Apc, Dab, Dap, Lys, Orm или делетирован;
R1 обозначает водород и
R2 обозначает NH2;
при условии, что
когда А5 обозначает Dab, Dap, Lys или Orn, то
А2 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А3 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А4 обозначает 2Thi, 3Thi, Taz, 2Fua, 2Pal, 3Pal, 4Pal, Orn, Thr(Bzl) или Pff,
когда А5 делетирован, то
А3 обозначает D-Bip, D-Bpa или D-Dip; или
А4 обозначает 2Fua, Pff, Taz или Thr(Bzl); или
А1 обозначает Apc и
А2 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А3 обозначает D-Bip, D-Bpa, D-Dip или D-Bal; или
А4 обозначает 2Тhi, 3Thi, Orn, 2Раl, 3Раl или 4Раl.
А1 обозначает Aib, Apc или Inp;
А2 обозначает D-Bal, D-Bip, D-Bpa, D-Dip, D-1Nal, D-2Nal, D-Ser(Bzl) или D-Trp;
А3 обозначает D-Bal, D-Bpa, D-Dip, D-1Nal, D-2Nal или D-Trp;
А4 обозначает Orn, 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi или Thr(Bzl) и
А5 обозначает Apc, Lys или делетирован,
или его фармацевтически приемлемая соль.
А1 обозначает Apc или Inp;
А2 обозначает D-Bal, D-Bip, D-1Nal или D-2Nal;
А3 обозначает D-Bal, D-1Nal, D-2Nal или D-Trp;
А4 обозначает 3Pal, 4Pal, Pff, Phe, Pim, Taz, 2Thi или Thr(Bzl),
или его фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2 или
H-Inp-D-2Nal-D-Trp-Taz-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2 или
H-Inp-D-2Nal-D-Trp-Taz-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2 или
H-Apc-D-2Nal-D-Trp-2Thi-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-Lys-NH2;
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2 или
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2,
или их фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-SPal-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2,
или их фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2 или
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
или его фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
или его фармацевтически приемлемая соль.
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-Orn-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2 или
H-Apc-D-1Nal-D-Trp-Phe-NH2,
или его фармацевтически приемлемая соль.
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Apc-NH2 или
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2,
или его фармацевтически приемлемая соль.
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim и
H-Inp-D-Trp-D-2Nal (ψ)-Pim.
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim или
H-Inp-D-Trp-D-2Nal(ψ)-Pim,
или его фармацевтически приемлемой соли.
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Tф-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-ZThi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim или
H-Inp-D-Trp-D-2Nal(ψ)-Pim,
или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой по меньшей мере количество, достаточное для достижения выявляемого повышения секреции ростового гормона, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp (ψ)-Pim или
H-Inp-D-Trp-D-2Nal(ψ)-Pim,
или его фармацевтически приемлемой соли, где указанное эффективное количество представляет собой по меньшей мере количество, достаточное для достижения выявляемого повышения секреции ростового гормона, и предпочтительно представляет собой количество, достаточное для достижения благоприятного воздействия на пациента.
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2
или его фармацевтически приемлемую соль.
H-Inp-D-Bal-D-Trp-Phe-Apc-NH2
или его фармацевтически приемлемую соль.
H-Inp-D-Bip-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Pff-Lys-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Dip-D-Trp-Phe-Lys-NH2;
H-Inp-D-Bpa-D-Trp-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Bpa-Phe-Lys-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-NH2;
H-Inp-D-2Nal-D-Trp-4Pal-NH2;
H-Inp-D-1Nal-D-Trp-3Pal-NH2;
H-Inp-D-Bip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Trp-Thr(Bzl)-NH2;
H-Inp-D-2Nal-D-Trp-Pff-NH2;
H-Inp-D-2Nal-D-Trp-2Thi-NH2;
H-Inp-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-Dip-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Dip-Phe-NH2;
H-Inp-D-Bal-D-Trp-Phe-NH2;
H-Inp-D-2Nal-D-Bal-Phe-NH2;
H-Inp-D-2Nal-D-Trp-3Pal-Lys-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-Bal-D-Trp-Phe-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-2Nal-D-Trp-Phe-Apc-NH2;
H-Inp-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-2Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-1Nal-D-Trp-Phe-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Inp-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-Taz-Lys-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Lys-NH2;
H-Inp-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Inp-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-Bal-D-Trp-2Thi-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Lys-NH2;
H-Apc-D-Bal-D-Trp-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-Phe-Apc-NH2;
H-Apc-D-Bal-D-Trp-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-1Nal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Apc-NH2;
H-Apc-D-Bal-D-1Nal-Phe-Lys-NH2;
H-Apc-D-Bal-D-2Nal-Phe-Lys-NH2;
H-Apc-D-1Nal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Phe-NH2;
H-Apc-D-1Nal-D-Trp-Taz-NH2;
H-Apc-D-Bal-D-Trp-2Thi-NH2;
H-Apc-D-Bal-D-Trp-Taz-NH2;
H-Apc-D-2Nal-D-Trp-2Thi-NH2;
H-Apc-D-2Nal-D-Trp-Taz-NH2;
H-Inp-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Inp-D-Bal-D-Trp-Taz-Apc-NH2;
H-Apc-D-1Nal-D-Trp-Taz-Apc-NH2;
H-Apc-D-Bal-D-Trp-Taz-Apc-NH2;
H-Inp-D-2Nal-D-Trp(ψ)-Pim;
H-Inp-D-1Nal-D-Trp(ψ)-Pim;
H-Inp-D-Bal-D-Trp(ψ)-Pim;
H-Aib-D-Ser(Bzl)-D-Trp(ψ)-Pim и
H-Inp-D-Trp-D-2Nal(ψ)-Pim,
или их фармацевтически приемлемых солей для получения лекарственного средства, предназначенного для стимуляции ростового гормона.
| RU 216014 C1, 10.02.1999 | |||
| ПОЛИПЕПТИДНЫЕ СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ D-2-АЛКИЛТРИПТОФАН, СТИМУЛИРУЮЩИЙ ВЫСВОБОЖДЕНИЕ ГОРМОНА РОСТА | 1995 |
|
RU2157378C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА, ОБЛАДАЮЩЕГО АНАБОЛИЧЕСКОЙ АКТИВНОСТЬЮ, СТИМУЛИРУЮЩЕГО УВЕЛИЧЕНИЕ МАССЫ ТЕЛА, РАЗВИТИЕ ЭПИДЕРМАЛЬНОГО СЛОЯ И РОСТА ВОЛОСЯНОГО ПОКРОВА | 1994 |
|
RU2110275C1 |
| US 5598337 A, 25.08.1998 | |||
| US 5804563 А, 08.09.1998. | |||
Авторы
Даты
2008-05-10—Публикация
2003-08-08—Подача