Изобретение относится к медицине, а именно к фармакологии, точнее к способам получения биологически активных веществ, и может найти применение в клинике, ветеринарии, а также в экспериментальных исследованиях.
Актуальность разработки способов получения новых биологически активных веществ, регулирующих анаболические процессы, ведущие к увеличению живой массы у животных и увеличению роста и качества волосяного покрова, подтверждается большим количеством исследований, проведенных в этой области.
Как правило, решение этой проблемы сводится либо к созданию целых композиций, включающих витамины, гормоны и другие биологические активные вещества (SU N 1664325, 1988; GB N 1460020, 1976), либо к поиску оптимальных технологий по очистке природного гормона роста, влияющего на процесс роста волос и вес тела (US N 4115375, 1978; US N 4332717, 1982; US N 4371462, 1983), либо к получению путем синтеза средств, подобных гормону роста (ЕП N 0137904, 1984). При этом особую группу составляют синтезированные физиологически активные субстанции пептидной или полипептидной природы, прямо либо опосредованно влияющие на гормон роста (Fr N 2266516, 1975; Fr N 2532308, 1983; ЕП N 0143850, 1984; PCT 89/0711, 1989; PCT N 90/13570, 1990; PCN /16923, 1991; US N 5008244, 1991).
Известно, однако, что гормон роста не проявляет строгой специфичности, одновременно воздействует на многие метаболистические пути и в эффективных дозах обладает широким терапевтическим действием (US N 4816439, 1989; PCT 90/12589, 1990; PCT 90/14839, 1990 US N 5006510, 1991; PCT 91/15227, 1991).
На сегодняшний день известны два препарата пептидной природы. У одного из которых отмечена специфическая направленность на стимулирование развития эпидермального слоя кожного покрова у человека (PCT N 90/13570, 1990), у другого - металлопептида, выраженная специфичность в отношении роста волос у теплокровных животных (PCT N 91/07431, 1991).
Однако известные способы получения биологически активных пептидов являются сложными, трудоемкими, выход продукта низким, а применение известных средств в большинстве своем сопровождается нежелательными побочными действиями.
Настоящим изобретением поставлена и решена задача создания эффективного способа получения нового, не известного ранее биологически активного пептида формулы:
H-Arg-Tyr-D-Ala-Phe-Gly-A,
где A - OH или замещенный амид (C1 - C3),
обладающего специфическим, стимулирующим действием на активность ростовой зоны эпителия, развитие эпидермального слоя, рост волос, а также влияющего на увеличение живой массы.
Сущность нового способа состоит из синтеза пептида в растворе путем последовательного наращивания цепи с C-конца молекулы, используя стратегию максимального блокирования функциональных групп, исходя из третбутилового эфира глицина с помощью метода активированных эфиров и метода смешанных ангидридов, используя карбобензокси- и третбутилоксикарбониламинокислоты.
Способ иллюстрируется следующим примером:
Пример 1. H-Arg-Tyr-D-Ala-Phe-Gly-OH
Получение BOC-Arg(BOC)-Tyr(OBut)-D-Ala-Phe-Gly-oBut.
1. Z-Phe-Gly-oBut
46,5 г (0,1 моля) Z-Phe-OPfP растворяли в 150 мл диметилформамида и при перемешивании добавляли раствор 21,3 г третбутилового эфира фосфата глицина и 11,5 мл N-метилморфолина в водном диметилформамиде. Реакционную смесь перемешивали сутки при комнатной температуре. Диметилформамид отгоняли в вакууме, остаток заливали 200 мл этилацетата и промывали 2%-ным раствором серной кислоты 2 раза по 150 мл, затем промывали насыщенным раствором бикарбоната натрия 2 раза по 150 мл, отмывали водой до нейтральной среды, высушивали над безводным сульфатом натрия. Этилацетатный слой упаривали в вакууме. Остаток кристаллизировали из эфира с гексаном. Выход: 37,3 г (90,5%). Rf = 0,68 (система: хлороформ : этилацетат : метанол = 3 : 6 : 1), Rf = 0,59 (система : этилацетат : гексан = 1 : 1).
2. Z-D-Ala-Phe-Gly-oBut
37,3 г (0,09 моля) Z-Phe-Gly-oBut растворяли в 200 мл этилового спирта, добавляли 4,0 г палладиевого катализатора и пропускали ток водорода в течение 4 ч. Катализатор отфильтровывали, растворители упаривали в вакууме до густого масла, до постоянного веса.
34,4 г (0,1 моля) Z-D-Ala-ONP растворяли в 100 мл диметилформамида и при перемешивании добавляли раствор 13,5 г (0,1 моля) гидроксибензотриазола и 25,2 г (0,09 моля) H-Phe-Gly-oBut в 70 мл диметилформамида. Реакционную смесь перемешивали сутки при 20oC. Диметилформамид отгоняли в вакууме, остаток заливали 200 мл этилацетата и промывали 2%-ным раствором серной кислоты 2 раза по 100 мл, затем промывали 2%-ным раствором аммиака 4 раза по 80 мл, отмывали водой до нейтральной среды, высушивали над безводным сульфатом натрия. Этилацетатный слой упаривали в вакууме. Остаток кристаллизовали из эфира. Выход: 39,5 г (90,8%). Rf - 0,76 (система: хлороформ:этилацетат:метанол = 6 : 3 : 1), Rf = 0,52 (система: хлороформ:метанол = 9 : 1).
3. Z-Tyr(oBut)-D-Ala-Phe-Gly-OBut
39,5 г (0,08 моля) Z-D-Ala-Phe-Gly-oBut растворяли в 200 мл этилового спирта, добавляли 4,0 г палладиевого катализатора и пропускали ток водорода в течение 4 ч. Катализатор отфильтровывали, растворители упаривали в вакууме до густого масла, до постоянного веса.
34,9 г (0,09 моля) Z-Tyr(oBut)-Oh и 10,3 мл (0,09 ммоля) N-метилморфолина в 150 мл диметилформамида охлаждали до -15oC и при перемешивании добавляли 12,6 г (0,09 моля) изобутилхлорформиата. Через 2 мин вносили охлажденный раствор 28,6 г (0,08 моля) третбутилового эфира трипептида: H-D-Ala-Phe-Gly-oBut. Реакционную смесь перемешивали при -15oC 30 мин и 2 ч при комнатной температуре. Диметилформамид отгоняли в вакууме, остаток заливали 200 мл этилацетата и экстрагировали 2%-ным раствором серной кислоты 2 раза по 80 мл, затем промывали насыщенным раствором бикарбоната натрия 2 раза по 80 мл, отмывали водой до нейтральной среды, высушивали над безводным сульфатом натрия. Этилацетатный слой упаривали в вакууме. Остаток кристаллизовали из этилацетата. Выход : 51,3 г (95,4%), Rf = 0,61 (система: хлороформ: этилацетат:метанол = 6 : 3 : 1), Rf = 0,55 (система: хлороформ:метанол = 9 : 1).
4. BOC-Arg(BOC)-Tyr(oBut)-D-Ala-Phe-Gly-OBut
51,3 г (0,07 моля) Z-Tyr-(BOC)-D-Ala-Phe-Gly-OBut растворители в 200 мл этилового спирта, добавляли 4,0 г палладиевого катализатора и пропускали ток водорода в течение 4 ч. Катализатор отфильтровывали, растворяли упаривали в вакууме до густого масла, до постоянного веса.
42,0 г (0,07 моль) H-Tyr(OBut)-D-Ala-Phe-Gly-OBut растворяли в 150 мл диметилформамида и добавляли 9,2 мл (0,08 моля) N-метилморфолина, 30,0 г (0,08 моля) BOC-Arg(BOC)-OH и 10,8 г оксибензотриазола. Реакционную смесь охлаждали при перемешивании до -10oC и вносили 16,5 г (0,08 моля) дициклогексилкарбодиимида. Реакционную смесь перемешивали 3 сут при комнатной температуре. Дициклогексилмочевину отфильтровывали, растворитель отгоняли в вакууме, остаток заливали 300 мл этилацетата и промывали 2%-ным раствором серной кислоты 2 раза по 150 мл, затем промывали насыщенным раствором бикарбоната натрия 2 раза по 100 мл, отмывали водой до нейтральной среды, высушивали над безводным сульфатом натрия. Этилацетатный слой упаривали в вакууме. Остаток кристаллизовали из этилацетата. Выход: 62,6 г (93,5%), Rf = 0,71 (система: хлороформ: этилацетат:метанол:уксусная кислота = 6:3:1:0.5), Rf = 0,22 (система: хлороформ:метанол = 9:1).
5. Получение H-Arg-Tyr-D-Ala-Phe-Gly-OH
62,6 г (0,065 моля) BOC-Arg(BOC)-Tyr(OBut)-D-Ala-Phe-Gly-OBut растворяли в 80 мл 50%-ной трифторуксусной кислоты в хлороформе. Через 1 ч растворители упаривали в вакууме до густого масла. Остаток заливали эфиром и затирали. Осадок отфильтровывали и промывали эфиром, высушивали на воздухе. Выход: 39,8 г (100%), Rf = 0,44 (система:бутанол:уксусная кислота:вода = 3:1:1).
Очистку пептида проводили с помощью ионнообменной хроматографии на колонке с Сефадексом в градиенте 0,1 - 1,0 М пиридинацетатного буфера. Выход: 35,8 г (90,0%).
В результате изучения физико-химических свойств нового пептида были получены следующие его характеристики:
Первичная структура - H-Arg-Tyr-D-Ala-Phe-Gly-OH
Брутто-формула - C29H40N8O7
Молекулярный вес - 612,6 Da
Внешний вид - белый с желтоватым или серый порошок
Растворитель - растворим в воде, 0,1%-ный водный раствор прозрачен, малорастворим в спирте, практически нерастворим в хлороформе
УФ-спектр - характерный максимум поглощения 0,02%-ного водного раствора 275 ± 2 нм, плечо 282 ± 2 нм.
В результате изучения биологической активности нового пептида были получены данные, свидетельствующие о его влиянии на такие физиологические процессы, как: увеличение живой массы тела; активация ростовой зоны эпителия, стимулирование развития эпидермиса и волосяного покрова у различных видов животных.
Влияние пептидного препарата на прирост веса.
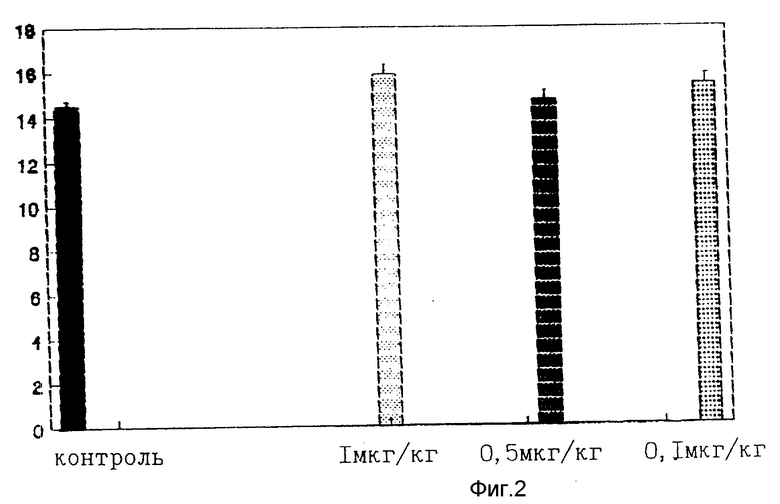
A. Эксперимент проводили на 4 группах беспородных белых крысят в возрасте одного месяца. Контрольная группа 1 получала инъекции физиологического раствора, 2,3 и 4 экспериментальным группам вводили препарат в дозах 0,1; 0,5; 1,0 мкг/кг веса внутрибрюшинно. Взвешивание крыс во всех группах проводили каждые 5 дней и параллельно фиксировали количество потребляемой пищи. Эксперимент длился в течение 35 дней. Результаты представлены на фиг. 1. Отмечен наибольший прирост веса в группе, получавшей 1,0 мкг/кг пептида. Данные, отражающие количество потребляемой крысами пищи, представлены на фиг. 2. Во всех экспериментальных группах отмечено отсутствие влияния пептида на количество потребляемой пищи, что свидетельствует о его анаболической активности.
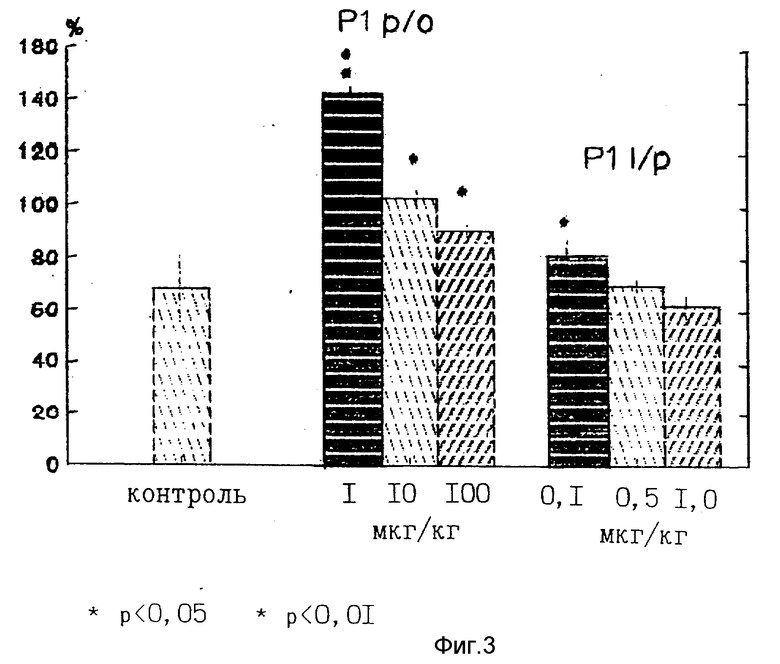
B. Эксперимент проведен на 7 группах мышей линии NMRI, находящихся в свободном рационе питания с неограниченным доступом к воде и пище. При этом 1 группа получала инъекции физиологического раствора, 2, 3 и 4 группы мышей получали пептид вместе с питьем из расчета 1,0, 10,0 и 100 мкг/кг соответственно 5, 6 и 7 группам пептид вводился ежедневно внутрибрюшинно в дозах 0,1, 0,5 и 1,0 мкг/кг соответственно. В течение 30 дней дважды в неделю определяли вес мышей и ежедневно фиксировали количество потребляемого корма. Суммарные результаты по изменению веса мышей при описанных способах введения пептида представлены на фиг. 3. Наиболее эффективным является прием пептида вместе с питьем в дозе 1 мкг/кг (p/o).
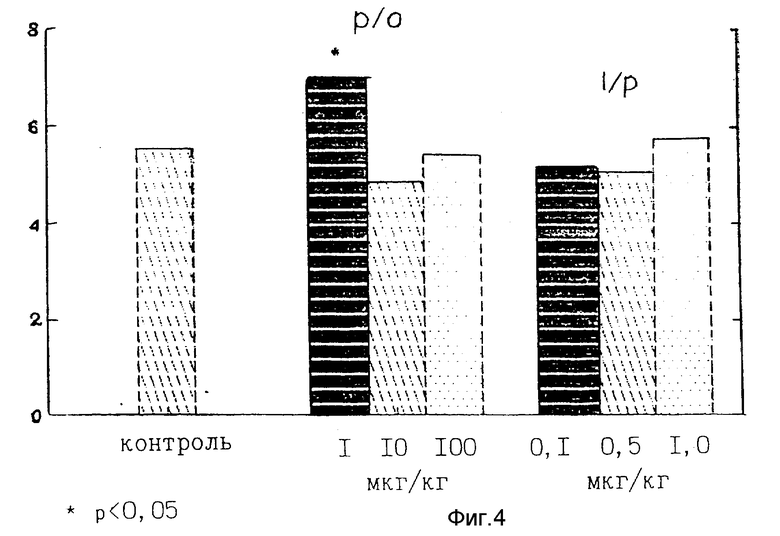
На фиг. 4 представлены результаты по количеству среднесуточного потребления пищи в разных группах. Статически значимо (p < 0,05) больше корма потребляли мыши, получавшие препарат с питьем в дозе 1,0 мкг/кг перорально, т.е. животные, которые дали максимальный привес.
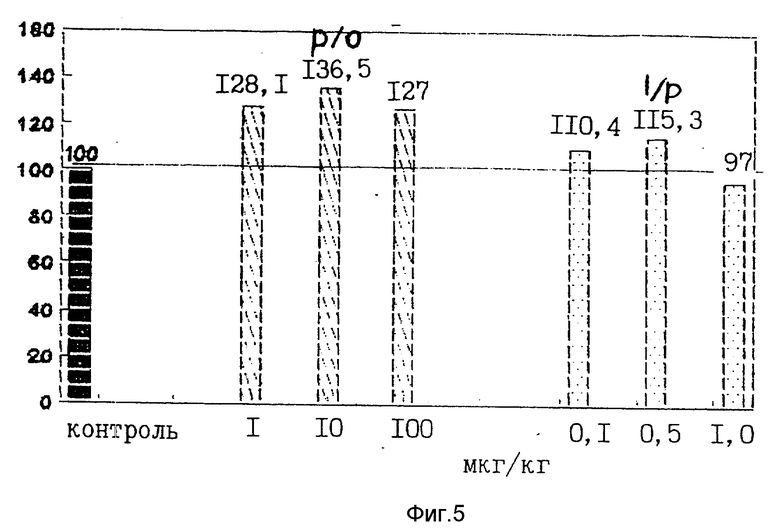
Учитывая, что под влиянием пептида меняются два параметра: прирост веса и потребления пищи, рассчитан прирост веса в процентах при потреблении 1 г пищи, что является показателем коммерческой выгоды применения пептида. На фиг. 5 представлены результаты. Видно, что наибольший прирост веса при потреблении 1 г пищи отмечен при приеме пептида с питьем в дозе 10,0 мкг/кг, что на 36,5% превышает прирост у контрольной группы.
Влияние пептида на морфологические изменения кожи и рост волосяного покрова.
Эксперимент проведен на 4 группах мышей линии NMRI: 1 группа - пассивный контроль, 2, 3 и 4 группы получали перорально при питье пептидный препарат в дозах 1,0, 10,0 и 100 мкг/кг соответственно. После биопсии образцы кожи, взятые в области холки размером 5х5 мм, фиксировали по методу Лилли в течение 48 ч, отмывали в спиртах нисходящей батареи и погружали в краситель Гемолаун Майера на 24 ч. Затем проводили проводку и заключение в целлодин. Изготовление гистологических препаратов осуществляли с помощью микротома фирмы Рейхард, ориентировав кусочки кожи в плоскости хода осевого волоса, срезы докрашивали по классической методике эозином.
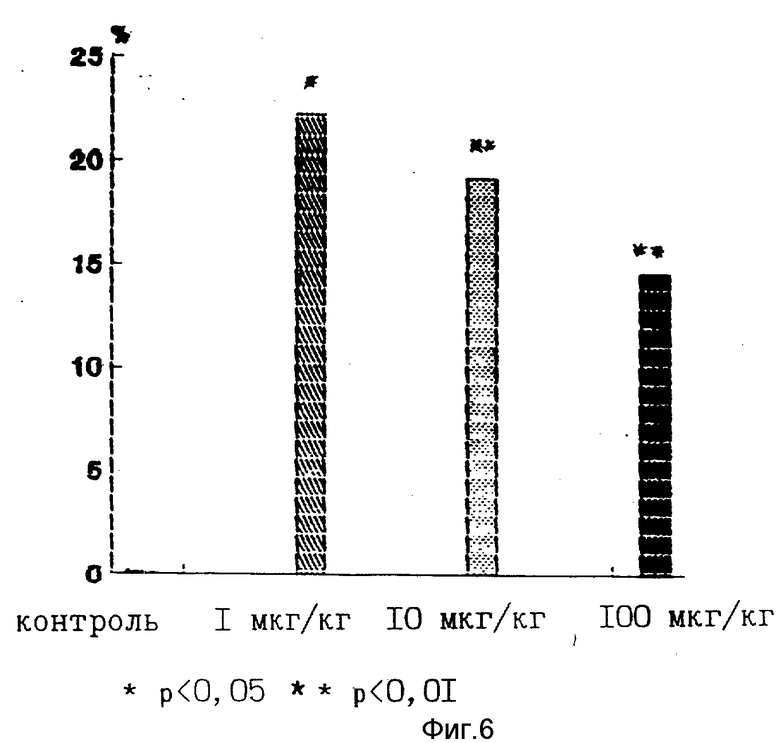
При изучении гистологических препаратов толщиной 10 мм оценивали качественное состояние эпидермиса и дермы, а также определяли число волосяных фоликул в 1 мм по методу Афтандилова у опытных и контрольных групп мышей. Результаты представлены на фиг. 6. Из диаграмм на фигуре видно, что у мышей, получавших 100, 10,0, 1,0 мкг/кг пептида, отмечалось увеличение числа волосяных фоликулов на 14, 19 и 22% соответственно по сравнению с контрольной группой.
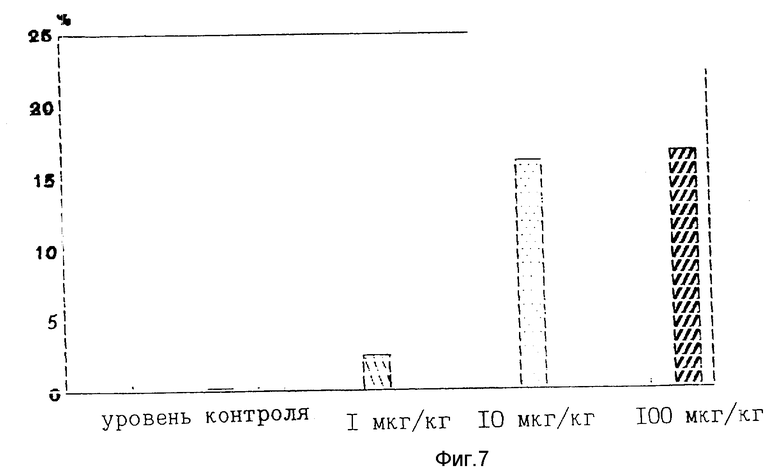
У указанных групп мышей оценивалась длина шерсти в области холки. С точностью до микрона у каждой мыши измерялась длина 10 волосков и рассчитывались средние значения по каждой группе. Результаты представлены на фиг. 6, 7.
Изучение токсичности препарата.
Исследования возможной токсичности нового пептида для определения ЛД-50 были проведены на 24 здоровых беспородных белых мышах массой 18 г, находившихся в одинаковых условиях питания и содержания. Во всех группах половину животных составляли самцы, а другую - самки. За 24 ч до испытаний и во время их проведения животные находились в помещении вивария с постоянной температурой и вентиляцией. За 2 ч до начала испытаний животным прекращали подачу воды и пищи.
Были выделены четыре группы мышей по 8 животных в каждой группе. При этом 1, 2 и 3 группах мышей вводили водный раствор препарата в дозе 800, 1100 и 1400 мг/кг соответственно. Мышам 4 группы, контрольной, вводили физиологический раствор в том же объеме. Наблюдения за животными проводили в течение 7 суток после введения. Установлено, что сразу после введения и в течение всего срока наблюдения каких-либо изменений в общем состоянии и поведении животных не наблюдали. Не было отмечено также в этот период случаев смертности животных.
Результаты проведенных исследований показали, что при внутрибрюшинном введении пептид в дозе 800, 1100 и 1400 мг/кг не оказывает токсического действия; при этих дозах оказалось невозможным достигнуть дозы ЛД-50.
Таким образом, новый пептид формулы: H-Arg-Tyr-D-Ala-Phe-Gly-OH не является токсичным и оказывает выраженное стимулирующее действие на активность ростовой зоны эпителия, на развитие эпидермального слоя кожи, способствует увеличению плотности волосяных фоликул и росту волос, а также оказывает влияние на увеличение живой массы тела.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА | 1994 |
|
RU2043769C1 |
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2107692C1 |
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2107691C1 |
| АДАПТОГЕН СТРЕСС-КОРРЕКТОР И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 1999 |
|
RU2155064C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2411248C2 |
| ПЕПТИД, ОБЛАДАЮЩИЙ ЗАЩИТНЫМ ДЕЙСТВИЕМ ПРОТИВ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2008 |
|
RU2372355C1 |
| СПОСОБ ОСЛАБЛЕНИЯ ЭРОЗИВНО-ЯЗВЕННОГО ПОВРЕЖДЕНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ ЖЕЛУДКА ПРИ ВОЗДЕЙСТВИИ АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ (АСК) С ПОМОЩЬЮ ПЕПТИДА ФОРМУЛЫ Arg-Tyr-D-Ala-Phe-Gly | 2005 |
|
RU2303983C1 |
| ДЕКАПЕПТИД, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2084458C1 |
| СПОСОБ СТИМУЛЯЦИИ РАЗВИТИЯ ОСЕТРОВЫХ РЫБ | 2005 |
|
RU2298921C1 |
Изобретение относится к медицине, а именно к фармакологии, точнее к способам получения биологически активных веществ, и может найти применение в клинике, ветеринарии, а также в экспериментальных исследованиях. Актуальность разработки способов получения новых биологически активных веществ, регулирующих анаболические процессы, ведущие к увеличению живой массы у животных и увеличению роста и качества волосяного покрова, подтверждается большим количеством исследований, проведенных в этой области. Изобретение связано со способом получения пептида, обладающего анаболической активностью, стимулирующего увеличение массы тела, развитие эпидермального слоя и роста волосяного покрова. Синтез заявляемого пептида проводили классическим методом в растворе последовательным наращиванием цепи с С-конца молекулы, используя стратегию максимального блокирования функциональных групп. Пентапептид получали, исходя из третбутилового эфира глицина с помощью метода активированных эфиров и метода смешанных ангидридов, используя карбобензокси- и трет-бутилоксикарбониламинокислоты, окончательное деблокирование проводили в кислой среде и целевой продукт очищали ионообменной хроматографией. 8 ил.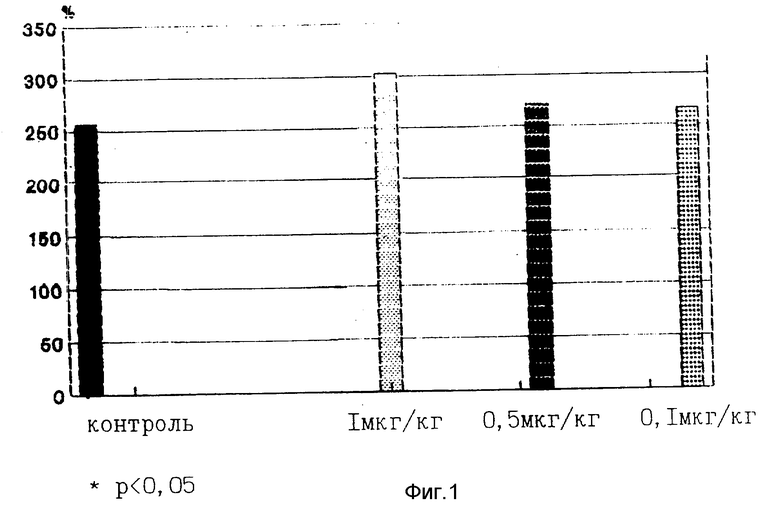
Способ получения пептида, обладающего анаболической активностью, стимулирующего увеличение массы тела, развитие эпидермального слоя и роста волосяного покрова, заключающийся в том, что вводят во взаимодействие в растворе третбутиловый эфир глицина с бензилоксикарбонилфенилаланином, затем постепенно наращивают пептидную цепь методом активированных эфиров и методом смешанных ангидридов, последовательно присоединяют карбобензоксиаминокислоты с предварительным отщеплением на каждой стадии карбобензоксигруппы путем обработки реакционной смеси током водорода в присутствии палладиевого катализатора и с последующим очищением промежуточных продуктов кристаллизацией, окончательно деблокируют в кислой среде и целевой продукт формулы
H - Arg - Tyr - D - Ala - Phe - Gly - A,
где A - OH или замещенный C1 - C3-амид,
очищают ионообменной хроматографией.
Авторы
Даты
1998-05-10—Публикация
1994-09-09—Подача