Область техники, к которой относится изобретение
Данное изобретение касается новой кристаллической формы N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина и способа ее получения.
Уровень техники
N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланин используется в терапии для понижения уровней глюкозы в крови при лечении сахарного диабета типа 2.
N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина раскрывается в японской патентной заявке номер 63-54321 (эквивалент ЕР-А-196222 и US 4816484). Японская заявка описывает, как данное соединение может быть выкристаллизовано из водно-метанольного раствора, давая кристаллы, имеющие точку плавления от 129 до 130°С. Эти кристаллы называются "В-типом". Данные кристаллы В-типа нестабильны, особенно когда они подвергаются механическому размельчению.
В J. Med. Chem. 32, 1436 (1989) обсуждается приготовление N-(циклогексилкарбонил)-D-фенилаланинов и родственных соединений, которые включают N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланин.
Патенты US 5463116 и 5488150 раскрывают приготовление новой кристаллической формы N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина, обозначенной как "Н-тип". В этих патентах также раскрыты способы обработки кристаллов формы "В" подводящими смесями растворителей для получения кристаллов формы "Н" и наоборот. Кристаллы Н-типа более стабильны по сравнению с кристаллами В-типа.
Yaowu Fenxi Zazhi 2001, 21, 342 обсуждает "S" форму натеглинида, которая отличается от формы "В" и формы "Н".
Раскрытие изобретения
Согласно первому аспекту изобретения предложен новый способ получения новой кристаллической формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина посредством реакции гидрохлорида метилового эфира D-фенилаланина с транс-4-изопропилциклогексанкарбоновой кислотой в присутствии ангидрида пропанфосфоновой кислоты или LiOH-Al2O3 в галогенированных углеводородных растворителях, таких как дихлорметан, дихлорэтан, при температуре между -10 и 90°С с последующим основным гидролизом.
Альтернативно продукт может быть получен посредством реакции транс-4-изопропилциклогексанкарбонилхлорида с гидрохлоридом метилового эфира D-фенилаланина в галогенированных углеводородных растворителях, таких как дихлорметан, дихлорэтан, в присутствии основания, такого как триэтиламин, пиридин, при температуре между -10 и 90°С с последующим основным гидролизом.
Согласно дальнейшему аспекту данного изобретения новая кристаллическая форма "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина, произведенная таким образом, имеет по меньшей мере одно, а предпочтительно все из следующих свойств:
(a) температура плавления в диапазоне от 126 до 132°С;.
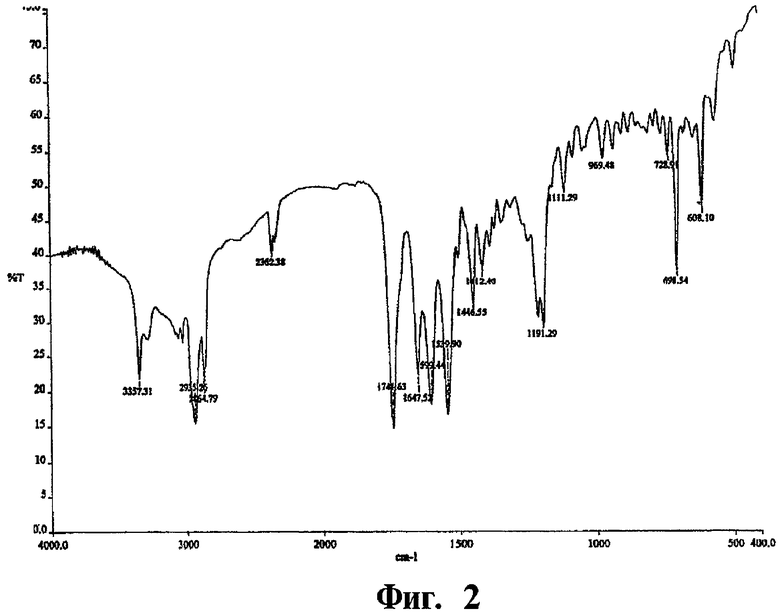
(b) порошковая дифракционная рентгенограмма, включающая в себя характеристические пики при 14,0, 17,8, 19,0, 20,2 и 21,2±0,2 градусах, измеренная под углом отражения 2θ;
(c) инфракрасный спектр поглощения, включающий в себя полосы поглощения в области 1742, 1648, 1599, 1540 и 1191±2 см-1.
Другой аспект изобретения включает применение формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина в приготовлении лекарственных средств для лечения сахарного диабета типа 2.
Данное изобретение также включает фармацевтическую композицию, содержащую терапевтически эффективное количество кристаллов формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Следующий аспект изобретения касается способа лечения пациентов, страдающих от сахарного диабета типа 2, посредством введения терапевтически эффективного количества фармацевтической композиции формы "С" N-(транс-4-изопропилциклогексилкарбонил)D-фенилаланина.
Краткое описание чертежей
На фиг.1 показана порошковая дифракционная рентгенограмма кристаллов формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина;
На фиг.2 показаны инфракрасные спектры поглощения кристаллов формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Осуществление изобретения
Предлагаемый способ получения формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина включает в себя:
(a) суспендирование метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина в воде или в смешивающемся с водой растворителе;
(b) обработку суспензии основанием;
(c) добавление воды с последующим доведением рН до 1,0-4,0 с использованием минеральной кислоты;
(d) экстракцию с использованием этилацетата;
(e) концентрирование этилацетатного экстракта;
(f) добавление петролейного эфира к этилацетатному концентрату и
(g) фильтрацию и высушивание полученного осадка с получением формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Смешивающийся с водой растворитель на стадии (а) выбирают из метанола, этанола, изопропанола или их смеси (предпочтительно метанол). Основание на стадии (b) выбирается из карбоната калия, карбоната натрия, гидроксида натрия, гидроксида калия, гидроксида лития или их смеси (предпочтительно карбонат калия).
Осадок, полученный на стадии (д), суспендируется в воде перед фильтрацией и высушиванием для получения формы "С" N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Метиловый эфир N-(транс-4-изопропилциклогексилкарбонил)-D-фенил-аланина приготавливается путем:
- реакции гидрохлорида метилового эфира D-фенилаланина с транс-4-изопропилциклогексанкарбоновой кислотой в галогенированных углеводородных растворителях;
- фильтрации реакционной смеси;
- концентрирования с получением метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Первая стадия вышеуказанного способа приготовления метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина проводится в присутствии ангидрида пропанфосфоновой кислоты, LiOH, адсорбированного на оксиде алюминия, или триэтиламина.
Альтернативный способ получения метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина включает стадии:
- реакции гидрохлорида метилового эфира D-фенилаланина с транс-4-изопропилциклогексанкарбонилхлоридом в галогенированных углеводородных растворителях и в присутствии основания;
- фильтрации реакционной смеси;
- концентрирования с получением метилового эфира)N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
Галогенированные углеводородные растворители выбраны из дихлорметана или дихлорэтана.
Основание выбрано из триэтиламина или пиридина. Реакционная температура равна от -10 до 90°С.
Варианты осуществления изобретения иллюстрируются посредством следующих примеров, не рассматриваемых как ограничения.
ПРИМЕР 1
Метиловый эфир N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина:
Гидрохлорид метилового эфира D-фенилаланина (10 г, 0,046 моль) был суспендирован в растворе триэтиламина (33 мл) в дихлорметане (50 мл); смесь охлаждена до 0-5°С, после чего к ней добавлена транс-4-изопропилциклогексанкарбоновая кислота (7,9 г, 0,046 моль). Раствор ангидрида пропанфосфоновой кислоты (46,4 мл, 0,046 моль) в этилацетате добавлялся по каплям в течение 30 минут, выдерживая температуру 0-5°С, и после этого смесь перемешивалась в течение 14 часов при температуре окружающей среды. Затем реакционная смесь была промыта 1,5 н. HCl, 5% раствором бикарбоната натрия и соляным раствором. Органический слой был сконцентрирован, давая на выходе 12,5 г метилового эфира)N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
ПРИМЕР 2
Метиловый эфир N-(транс-4-изопропилциклогексилкарбонил)-D-фенил-аланина:
Гидрохлорид метилового эфира D-фенилаланина (20 г, 0,092 моль) был суспендирован в растворе триэтиламина (66 мл) в дихлорэтане (100 мл) и смесь перемешивалась в течение 1 часа при комнатной температуре. Органический слой был отделен после промывки водой и высушен над обезвоженным сульфатом натрия. Транс-4-изопропилциклогексанкарбоновая кислота (15,8 г, 0,092 моль) была добавлена к органическому слою, далее LiOH-Al2О3 (5,5 г LiOH адсорбированного на 40,5 г оксида алюминия) и смесь нагревалась под дефлегматором в течение 24 часов. Реакционная смесь была отфильтрована через целитовый фильтр и промыта 1,5 н. HCl, 5% раствором бикарбоната натрия и соляным раствором. Органический слой был сконцентрирован, давая на выходе 15,5 г метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
ПРИМЕР 3
Метиловый эфир N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина:
Гидрохлорид метилового эфира D-фенилаланина (26 г, 0,12 моль) был суспендирован в растворе триэтиламина (85 мл) в дихлорметане (125 мл); смесь была охлаждена до 0-5°С. Раствор транс-4-изопропилциклогексанкарбонилхлорида (25 г, 0,13 моль) в дихлорметане (75 мл) добавлялся по каплям в течение 10 минут, выдерживая температуру 0-5°С, и после этого смесь перемешивалась в течение 12 часов при температуре окружающей среды. Затем реакционная смесь была промыта 1,5 н. HCl, 5% раствором бикарбоната натрия и соляным раствором. Органический слой был сконцентрирован, давая на выходе 38 г метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
ПРИМЕР 4
N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланин:
К суспензии метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина (38 г, 0,11 моль) в метаноле (600 мл) был добавлен раствор карбоната калия (80 г, 0,57 моль) в воде (400 мл) и реакционная смесь перемешивалась в течение 12 часов при температуре окружающей среды. Затем была добавлена вода (1500 мл) и посредством добавления 6 н. HCl рН была доведена до 2,0. Смесь была проэкстрагирована этилацетатом (3 × 400 мл) и объединенный экстракт был промыт соляным раствором. Органический слой был сконцентрирован до примерно 150 мл и затем смешан с петролейным эфиром (300 мл). Продукт был отфильтрован, суспендирован в воде (600 мл) и перемешивался в течение 12 часов при температуре окружающей среды. Пульпа была отфильтрована и высушена, давая на выходе 35 г титульного соединения. Это соединение показало точную температуру плавления 128-129°С. Были записаны дифракционная рентгенограмма и инфракрасный спектр поглощения конечного соединения, идентифицированного как кристаллическая форма С N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения продукта присоединения дипептидного производного и аминокислоты | 1978 |
|
SU910117A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ФЕНИЛАЛАНИНА С ХИНАЗОЛИНДИОНОВЫМ СКЕЛЕТОМ И ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ, ПРИМЕНЯЕМЫХ ПРИ ПОЛУЧЕНИИ ТАКИХ ПРОИЗВОДНЫХ | 2007 |
|
RU2469028C2 |
| ИММУНОФИЛИН-СПЕЦИФИЧЕСКИЕ ЛИГАНДЫ В КАЧЕСТВЕ АНТИАСТМАТИЧЕСКИХ И ИММУНОДЕПРЕССАНТНЫХ АГЕНТОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИ ГОТОВАЯ ФОРМА, ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1997 |
|
RU2172743C2 |
| КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИНГИБИТОРЫ СКВАЛЕН-СИНТЕТАЗЫ | 1994 |
|
RU2129547C1 |
| Способ получения гидрохлорида сложного метилового эфира @ -L-аспартил-L-фенилаланина | 1990 |
|
SU1834892A3 |
| ПРОИЗВОДНЫЕ 4,1-БЕНЗОКСАЗЕПИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ СКВАЛЕНСИНТЕТАЗЫ У МЛЕКОПИТАЮЩИХ, СПОСОБ ИНГИБИРОВАНИЯ РОСТА ГРИБКОВ У МЛЕКОПИТАЮЩИХ | 1993 |
|
RU2145603C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО 7Н-ПИРРОЛО[2,3-D] ПИРИМИДИНА И ЕГО ИНТЕРМЕДИАТА | 2016 |
|
RU2755618C2 |
| (2S,5R)-5-[(бензилокси)амино]пиперидин-2-карбоксамид | 2012 |
|
RU2610091C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ВКЛЮЧАЯ ТРАНС-7-ОКСО-6-(СУЛЬФОКСИ)-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-2-КАРБОКСАМИД И ЕГО СОЛИ | 2012 |
|
RU2769076C2 |
| СОЛИ ГЕТЕРОЦИКЛИЛАМИДЗАМЕЩЕННЫХ ИМИДАЗОЛОВ С СУЛЬФОНОВОЙ КИСЛОТОЙ | 2012 |
|
RU2606639C2 |
Получена новая кристаллическая форма С соединения N-(транс-4-изопропилцикло-гексилкарбонил)-D-фенилаланина (натеглинида), обладающая инфракрасным спектром и дифракционной рентгенограммой, отличающимися от имеющихся у известных форм В и Н данного соединения. Получение заявленной кристаллической формы С натеглинида осуществляется путем суспендирования метилового эфира N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина в воде или в смешивающемся с водой растворителе, затем полученную суспензию обрабатывают основанием, добавляют воду с последующим доведением рН до 1,0-4,0 с использованием минеральной кислоты; экстрагируют с использованием этилацетата, далее фильтруют и высушивают полученный осадок. Целью настоящего изобретения является получение кристаллической формы С соединения N-(транс-4-изопропилциклогексилкарбонил)-D-фенилаланина для применения в качестве средства для лечения сахарного диабета типа 2. 4 н. и 12 з.п. ф-лы, 2 ил.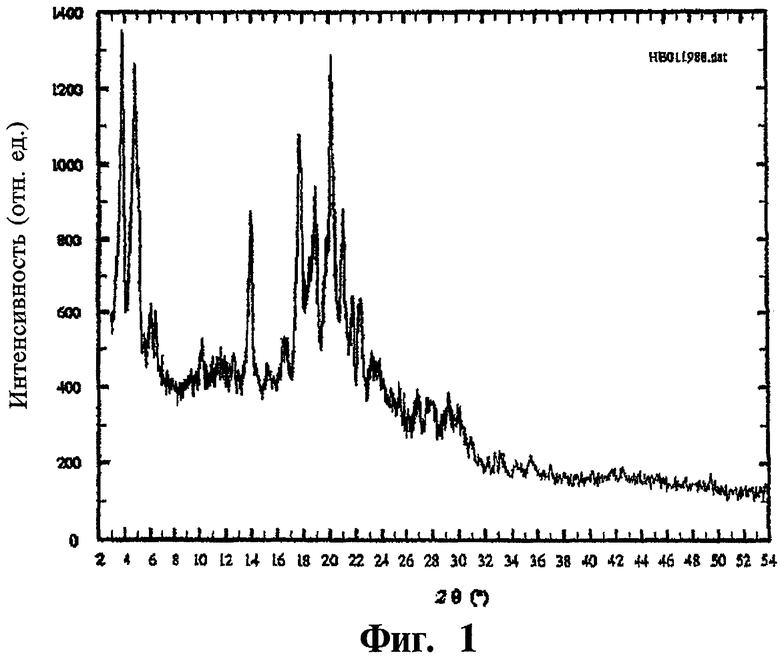
порошковая дифракционная рентгенограмма, измеренная под углом отражения 2θ, содержит характеристические пики при 14,0, 17,8, 19,0, 20,2 и 21,2±0,2°;
инфракрасный спектр поглощения содержит полосы поглощения в области 1742, 1648, 1599, 1540 и 1191±2 см-1.
| US 5463116 А, 31.10.1995 | |||
| ЕР 0526171 А2, 03.02.1993 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ N-АЦИЛ-α-АМИНОКИСЛОТ | 1995 |
|
RU2140903C1 |
| US 4816484 А, 28.03.1989. | |||
Авторы
Даты
2008-05-20—Публикация
2002-04-29—Подача