Недавно было показано, что ряд цеолитных систем возникает в результате конденсации слоистых предшественников при прокаливании. Примерами этого являются некоторые ферриеритные системы (см. L.Schreyeck et al., J.Chem.Soc, Chem. Commun., (1995), 2187) и материалы MWW, такие как МСМ-22 (см. S.L.Lawton et al., J.Phys.Chem. (1966) 100, 3788-3798). В настоящем изобретении раскрывается синтез трех новых слоистых алюмосиликатов: UZM-13, UZM-17 и UZM-19, которые при прокаливании превращаются в новый микропористый цеолит UZM-25. UZM-13 может быть получен с использованием, например, диэтилдиметиламмониевой (DEDMA) матрицы, UZM-17 может быть получен с использованием в качестве матрицы, например, этилтриметиламмония (ЕТМА), в то время как UZM-19 может быть получен с использованием в качестве матрицы, например, ди-четвертично-аммониевого катиона: тетраметилен(бис-1,4-триметиламмония) (Diquat-4).
UZM-13, UZM-17 и UZM-19 имеют составы свежесинтезированной формы, выражаемые следующей эмпирической формулой (в расчете на безводное состояние):
Mm n+Rr p+HwAlxEySiOz,
где М обозначает, по меньшей мере, один способный к обмену катион, который выбирается из группы, состоящей из щелочных металлов, щелочно-земельных металлов и их смесей, а «m» обозначает мольное отношение М к Si, которое варьирует от 0,01 до 0,35. Конкретные примеры М-катионов включают (но не ограничиваются ими) натрий, калий, литий, цезий, кальций, стронций, барий и их смеси. R представляет собой органический катион и выбирается из группы, состоящей из протонированных аминов, протонированных диаминов, четвертичных аммониевых ионов, дичетвертичных аммониевых ионов, протонированных алканоламинов и кватернизированных алкноламмониевых ионов. Значение «r», которое обозначает мольное отношение R к Si, варьирует от 0,05 до 1,0. Значение «n», которое обозначает среднюю валентность М, варьирует от 1 до 2. Значение «р», которое обозначает среднюю валентность R, варьирует от 1 до 2. Значение «w», которое обозначает мольное отношение гидроксильных протонов к Si, варьирует от 0 до 1,0. Значение «х», которое обозначает мольное отношение Al к Si, варьирует от 0 до 0,25. Е обозначает элемент, который обладает тетраэдрической координацией, присутствует в каркасе и выбирается из группы, состоящей из галлия, железа, хрома, индия, бора и их смесей. Значение «у», которое обозначает мольное отношение Е к Si, варьирует от 0 до 0,25, где x+y меньше или равно 0,25, a «z» является мольным отношением O к Si и определяется уравнением
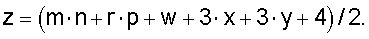
Когда М обозначает только один металл, то средняя валентность является валентностью этого одного металла, т.е.+1 или+2. Однако, когда присутствуют более одного металла М, общее количество
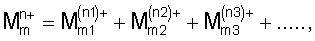
а средняя валентность «n» определяется уравнением
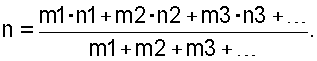
Когда присутствует только один органический катион R, средняя валентность является валентностью одного катиона R, т.е. +1 или +2. Когда же присутствуют более одного катиона R, общее количество R определяется уравнением
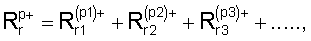
а средняя валентность «p» определяется уравнением
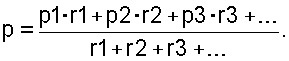
Эти алюмосиликатные композиции получают гидротермальной кристаллизацией реакционной смеси, приготовленной комбинированием в водных средах реакционно-способных источников R, М, алюминия, кремния и, возможно, Е. Соответствующим образом, в число источников алюминия входят (но не ограничивают этим изобретения) алкоксиды алюминия, осажденный оксид алюминия, гидроксид алюминия, соли алюминия и металлический алюминий. В число конкретных примеров алкоксидов алюминия входят (но не ограничивают этим изобретения) орто-втор-бутоксид алюминия и орто-изопропоксид алюминия. Источники оксида кремния включают (но не ограничивают этим изобретения) тетраэтилортосиликат, высокодисперсный диоксид кремния, осажденный диоксид кремния и коллоидный диоксид кремния. Источники металлов М включают (но не ограничивают этим изобретения) галогенидные соли, нитратные соли, ацетатные соли и гидроксиды соответствующих щелочных или щелочно-земельных металлов. Источники элементов Е включают (но не ограничивают этим изобретения) бораты щелочных металлов, борную кислоту, осажденный оксигидроксид галлия, сульфат галлия, сульфат железа (III), хлорид железа (III), хлорид хрома, нитрат хрома, хлорид индия и нитрат индия. Когда R представляет собой четвертичный аммониевый катион, источники включают (без ограничения) гидроксид и галогенидные соединения. В число конкретных примеров входят (без ограничения) гидроксид этилтриметиламмония, гидроксид диэтилдиметиламмония, дигидроксид тетраметилен(бис-1,4-триметиламмония), дигидроксид триметилен(бис-1,3-триметиламмония), дигидроксид диметилен(бис-1,2-триметиламмония), гидроксид триметилпропиламмония, гидроксид триметилбутиламмония и гидроксид триметилпентиламмония. Источниками R могут быть также нейтральные амины, диамины и алканоламины, которые в реакционной среде частично протонированы. Конкретными примерами являются триэтаноламин, триэтиламин и N,N,N',N'-тетраметил-1,6-диаминогексан.
Реакционная смесь, содержащая реакционно-способные источники желаемых компонентов может быть описана в виде мольных отношений оксидов с помощью формулы
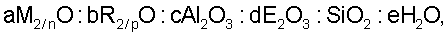
где «а» обозначает мольное отношение оксида М к Si и имеет значение от 0,01 до 0,35, «b» обозначает мольное отношение оксида R к Si и имеет значение от 0,05 до 0,75, «с» обозначает мольное отношение оксида алюминия к Si и имеет значение от 0 до 0,175, «d» обозначает мольное отношение оксида Е к Si и варьирует от 0 до 0,175, где c+d меньше или равно 0,175 и «е» обозначает мольное отношение воды к Si и имеет значение от 8 до 150.
В одном из предпочтительных способов получения композиций настоящего изобретения в качестве исходного раствора используется гомогенный алюмосиликатный раствор, который содержит источники Si, A1 и гидроксидную форму матрицы (или одной из матриц, если используется более чем одна матрица). В результате этого в конечной реакционной смеси возникает уникальная система, которая может быть дополнена добавлением инициирующих кристаллизацию источников М до прохождения реакции в реакционной смеси. Другое воплощение этого предпочтительного способа включает образование реакционной смеси с использованием двух таких гомогенных алюмосиликатных растворов с разным отношением Si/Al с последующим смешением их между собой до достижения заданного отношения Si/Al. Эти растворы должны содержать реакционно-способные источники алюминия, кремния, R и, возможно, Е. Если в качестве источника алюминия и кремния используются алкоксиды, то в этом случае первый раствор нагревают до температуры от 25 до 100°С в течение времени, достаточного для отгонки по крайней мере части спирта, образующегося в качестве побочного продукта реакции гидролиза. Альтернативным образом спирт может удаляться с помощью вакуума или путем продолжительной гомогенизации в открытой емкости.
После отгонки или удаления спирта первый раствор может быть в некоторых случаях выдержан при температуре от 25 до 100°С в течение времени от 0 до 96 час. Когда первый раствор приготовляют из источников алюминия и кремния, отличных от алкоксидов, т.е. из золя диоксида кремния, высокодисперсного диоксида кремния, осажденного оксида кремния и оксида алюминия, то, чтобы обеспечить образование гомогенного раствора, исходную смесь предпочтительно нагревают при температуре от 50 до 100°С в течение времени от 8 до 240 часов.
Чтобы получить конечную реакционную смесь для кристаллизации, к этим гомогенным алюмосиликатным растворам примешивают раствор, включающий дополнительный источник R, если это будет необходимо, и источник М. R может быть либо тем же самым, что и R в алюмосиликатном растворе, либо он может быть отличным от него.
Вне зависимости от того, используется ли несколько растворов или же все реакционно-способные источники смешиваются вместе с образованием реакционной смеси, реакцию в реакционной смеси проводят в условиях реакции, включающих температуру от 100 до 200°С, преимущественно от 135 до 175°С, в течение от 12 час до 21 суток, преимущественно в течение времени от 5 до 16 суток, в закрытом реакционном сосуде при аутогенном давлении. После завершения кристаллизации твердый продукт выделяют из гетерогенной смеси с помощью фильтрации или центрифугирования, после чего промывают деионизованной водой и сушат на воздухе при температуре от комнатной до 100°С.
Полученные в описанном выше процессе кристаллические композиции характеризуются слоистой структурой и уникальной рентгенограммой. Полученные в описанном выше процессе композиции получили обозначения UZM-13, UZM-17 и UZM-19. Эти особые вещества характеризуются тем, что они обладают по меньшей мере d - расстояниями и относительными интенсивностями, приведенным в таблицах А, В и С, соответственно.
Свежесинтезированные цеолиты должны содержать в своих порах некоторые способные к обмену или балансирующие заряд катионы. Эти способные к обмену катионы могут быть обменены на другие катионы или, в случае органических катионов, они могут быть удалены при нагревании в контролируемых условиях. Ионный обмен включает контактирование цеолитов с раствором, содержащим желаемый катион (в молярном избытке) в условиях обмена. Условия обмена включают температуру от 15 до 100°С и время от 20 мин до 50 час. В число катионов, которые могут быть обменены, входят (без ограничения) щелочные или щелочно-земельные металлы, редкоземельные металлы, такие как лантан, или их смеси. Условия прокаливания включают температуру от 300 до 600°С в течение времени от 2 до 24 час. Было обнаружено, что при прокаливании какого-либо из UZM-13, UZM-17 или UZM-19 образуется микропористый цеолит, имеющий трехмерный каркас из по меньшей мере тетраэдрических ячеек AlO2 и SiO2. Это цеолит характеризуется эмпирической формулой прокаленной формы (в расчете на безводное состояние):
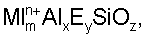
где Е, «m», «n», «x» и «y» определены выше, M1 обозначает способный к обмену катион, выбираемый из группы, состоящей из иона водорода, щелочных металлов, щелочно-земельных металлов и их смесей, и z=(m·n+3·х+3·у+4)/2. Этот прокаленный цеолит получил название UZM-25 и характеризуется рентгенограммой, имеющей по меньшей мере d-расстояния и относительные интенсивности, указанные в приведенной ниже в таблице D
Цеолит UZM-25 настоящего изобретения способен разделять смеси молекулярных частиц по размеру молекул (кинетическому диаметру) или по степени полярности молекулярных частиц. Когда разделение молекулярных частиц основано на размере молекул, разделение осуществляется за счет того, что молекулярные частицы меньшего размера входят во внутрикристаллические пустоты, в то время как частицы большего размера туда не проходят. Кинетические диаметры различных молекул, таких как кислород, азот, диоксид углерода и оксид углерода, даются в D.W.Breck, Zeolite Molecular Sieves (Цеолитные молекулярные сита), John Wiley and Sons (1974), стр.636.
UZM-25 настоящего изобретения может быть использован в качестве катализатора или носителя катализатора в процессах конверсии углеводородов. Процессы конверсии углеводородов хорошо известны в технике и включают крекинг, гидрокрекинг, алкилирование ароматических соединений и изопарафинов, изомеризацию, полимеризацию, реформинг, депарафиницацию, гидрогенизацию, дегидрогенизацию, трансалкилирование, деалкилирование, гидратацию, дегидратацию, гидрообработку, гидроденитрогенацию, гидродесульфуризацию, метанирование и процесс преобразования синтез-газа. Специфические условия реакции и типы сырья, которые могут быть использованы в этих процессах, приводятся в US 4310440 и US 4440871, которые введены в настоящую заявку в качестве ссылочного материала. Преимущественными процессами конверсии углеводородов являются алкилирование ароматических соединений и изомеризация ксилолов.
Представленные в следующих примерах (и приведенных выше таблицах) рентгенограммы были получены с использованием стандартных методов дифракции рентгеновских лучей на порошке. Источником излучения была рентгеновская трубка высокой интенсивности, работающая при 45 кВ и 35 мА. Рентгенограмму на основе медного К-альфа-излучения получали с использованием соответствующих компьютерных методов. Плоскоспрессованные порошковые образцы непрерывно сканировали со скоростью 2°(2Θ)/мин от 2 до 70°(2Θ). Межплоскостные расстояния (d) в ангстремах получали на основании положения дифракционных пиков, выраженных в 2Θ, где Θ есть угол Брэгга, наблюдаемых при оцифровывании данных. Интенсивности определяли по интегрированной площади дифракционных пиков после вычитания фона. I0 обозначает интенсивность самой сильной линии, или пика, а I - интенсивность каждого из всех остальных пиков.
Как хорошо известно специалистам, определение параметра 2Θ сопровождается как человеческой, так и механической ошибками, которые в сочетании могут привести к недостоверности ±0,4 для каждого приводимого значения 2Θ и до ±0,5 для приводимых значений нанокристаллических материалов. Эта недостоверность, разумеется, проявляется также и в приводимых значениях d-расстояний, которые рассчитываются на основании значений Θ. Такая неточность является общей для всей данной области техники и не является достаточной для того, чтобы помешать отличать обсуждаемые кристаллические материалы один от другого и от композиций предшествующего уровня техники. В приводимых рентгенограммах относительные интенсивности d-расстояний охарактеризованы пометками vs, s, m и w, которые означают очень сильный, сильный, средний и слабый, соответственно. В терминах 100×I/I0 эти обозначения ограничивают следующим образом: w=0-15, m=15-60, s=60-80 и vs=80-100. В некоторых случаях чистота синтезированного продукта может быть оценена на основании диаграммы дифракции рентгеновских лучей на порошке. Так, например, если утверждается, что образец является чистым, это означает лишь то, что на рентгенограмме образца отсутствуют линии, которые приписывают кристаллическим загрязнениям, но не потому, что присутствуют аморфные материалы.
С целью полнее проиллюстрировать изобретение ниже приводятся примеры. Следует иметь в виду, что эти примеры является лишь иллюстрацией и не предназначены для ограничения широкого объема изобретения, изложенного в прилагаемой формуле изобретения.
ПРИМЕР 1 (UZM-13)
Алюмосиликатный раствор приготавливают растворением 6,44 г три-втор-бутоксида алюминия в 151,18 г 20%-ного водного гидроксида диэтилдиметиламмония (DEDMAOH). Добавляют при перемешивании 80,62 г деионизованной воды, затем 161,76 г тетраэтилортосиликата (TEOS, 98%), после чего образовавшуюся реакционную смесь гомогенизуют в течение дополнительных 1,5 часа. Реакционную смесь переносят в круглодонную колбу и удаляют перегонкой избыток этанола. Последующий химический анализ раствора указал на состав с 8,66% Si и 0,27% Al.
Помещают в стакан 25,77 г полученного выше алюмосиликатного раствора, после чего добавляют 14,3 г DEDMAOH (20%) и гомогенизируют образовавшийся раствор. В отдельном стакане растворяют 1,21 г NaCl в 3,73 г деионизованной Н2O и добавляют этот раствор к полученной выше смеси при перемешивании. Образовавшуюся реакционную смесь перемешивают еще 20 мин и переносят в два 45-мл автоклава с тефлоновой футеровкой. Автоклавы нагревают в печи при 150°С и извлекают из печи через 168 и 264 часа. Твердые продукты собирают центрифугированием, промывают их деионизованной водой и сушат при 95°С. Анализ с помощью дифракции рентгеновских лучей на порошке показал, что оба продукта имеют характеристические линии материала, который был обозначен как UZM-13. Дифракционные линии продукта, полученного через 168 час, приведены в таблице 1. Элементный анализ показал, что UZM-13 содержит элементы в мольных отношениях: Si/Al=48,9, Na/Al=1,51, N/Al=6,42 и C/N=6,08. Высокие отношения Na/Al и N/Al указывают на слоистость материала.
ПРИМЕР 2 (UZM-13)
Алюмосиликатный раствор приготавливают растворением 3,26 г три-втор-бутоксида алюминия в 145,6 г гидроксида диэтилдиметиламмония (20%) (DEDMAOH). Добавляют при перемешивании 87,44 г деионизованной H2O, затем 163,84 г тетраэтилортосиликата (TEOS, 98%), после чего образовавшуюся реакционную смесь гомогенизуют в течение дополнительных 1,5 часа. Реакционную смесь переносят затем в круглодонную колбу и удаляют перегонкой избыток этанола. Элементный анализ показал, что раствор содержит 8,12% Si и 0,13% Al.
Помещают в стакан 26,48 г полученного выше алюмосиликатного раствора, после чего добавляют 13,54 г DEDMAOH (20%) и образовавшийся раствор хорошо перемешивают.В отдельном стакане растворяют 1,19 г Nacl в 3,79 г деионизованной H2O, добавляют после этого раствор NaCl к алюмосиликатному раствору и образовавшуюся реакционную смесь перемешивают еще 20 мин. Часть реакционной смеси переносят затем в 45 мл автоклав с тефлоновой футеровкой и выпаривают реакционную смесь при 150°С и аутогенном давлении. Через 168 час извлекают автоклав из печи, собирают твердый продукт центрифугированием, промывают его деионизованной водой и сушат при 95°С. Анализ с помощью дифракции рентгеновских лучей на порошке показал, что оба продукта имеют характеристические линии материала, обозначенного UZM-13. В таблице 2 показаны характеристические дифракционные линии этого продукта. Элементный анализ показал, что выделенное твердое вещество содержит элементы в мольных отношениях: Si/Al=87,23, Na/Al=0,93, N/Al=9,49 и C/N=6,06. Высокое отношение Na/Al указывает на слоистость материала.
ПРИМЕР 3 (UZM-13)
Алюмосиликатный раствор приготавливают растворением 11,40 г Al(O-secBu)3 (97%) в 508,19 г DEDMAOH (20%), после чего добавляют при перемешивании 387,83 г коллоидного кремнезема (Ludox AS-40, 40% SiO2), проводя все операции при интенсивном перемешивании. После перемешивания в течение 20 мин смесь помещают в тефлоновую колбу и выпаривают ее в течение 10 суток при 95°С, после чего смесь представляет собой прозрачный раствор. Элементный анализ показал, что раствор содержит 7,53% Si и 0,15% Al.
К 816,62 г полученного выше алюмосиликатного раствора добавляют при интенсивном перемешивании 294,93 г DEDMAOH (20%). Отдельно приготавливают раствор хлорида натрия растворением 39,13 г NaCl в 129,32 г деионизованной воды. При интенсивном перемешивании добавляют раствор хлорида натрия к алюмосиликатному раствору, и после завершения добавления перемешивают в течение еще одного часа. Реакционную смесь помещают в 2 л статический реактор Парра и выпаривают в течение 8 суток при 150°С и аутогенном давлении. Продукт выделяют центрифугированием, промывают деионизованной водой и сушат при 95°С. Анализ с помощью дифракции рентгеновских лучей на порошке показал, что продуктом является UZM-13. Характеристические для образца дифракционные линии приведены в таблице 3. Элементный анализ твердого вещества дал следующие в мольные отношения элементов: Si/Al=19,26, Na/Al=1,52, N/Al=3,43 и C/N=5,97.
ПРИМЕР 4 (UZM-17)
Алюмосиликатный раствор приготавливают как в примерах 1-3, за исключением того, что используют матрицу ЕТМА, используя ЕТМАОН (12,8%). Приготавливают раствор со следующей стехиометрией: Si/Al=23,7, ETMAOH/Si=0,542, H2O/Si=23,7. К 809 мкл алюмосиликатного раствора добавляют при перемешивании 291 мкл ЕТМАОН (12,8%). После этого добавляют 100 мкл 24,47%-ного водного раствора NaCl с последующим интенсивным перемешиванием в течение 30 мин. Реакционный сосуд герметизируют и упаривают его содержимое при 150°С в течение 336 час при аутогенном давлении. Твердые продукты выделяют центрифугированием, промывают деионизованной водой и сушат при 75°С. Анализ с помощью дифракции рентгеновских лучей на порошке указал на продукт, который был идентифицирован как UZM-17. Характеристические для UZM-17 дифракционные линии приведены в таблице 4.
ПРИМЕР 5 (UZM-17)
Алюмосиликатный раствор приготавливают как в примере 4 при следующей стехиометрии: Si/Al=48,42, ETMAOH/Si=0,521, H2O/Si=23,31. К 809 мкл алюмосиликатного раствора добавляют при перемешивании 292 мкл ЕТМАОН (12,8%). После этого добавляют 99 мкл 24,47%-ного водного раствора NaCl с последующим интенсивным перемешиванием в течение 30 мин. Реакционный сосуд герметизируют и упаривают его содержимое при 150°С в течение 168 час при аутогенном давлении. Твердые продукты выделяют центрифугированием, промывают деионизованной водой и сушат при 75°С. Анализ с помощью дифракции рентгеновских лучей на порошке указал на продукт, который был идентифицирован как UZM-17. Характеристические для UZM-17 дифракционные линии приведены в таблице 5.
ПРИМЕР 6
Приготавливают реакционную смесь добавлением при интенсивном перемешивании 62,25 г Diquat-4-дигидроксида (16,5%) к 29,57 г коллоидного кремнезема (Ludox AS-40, 40% SiO2). Далее, к реакционной смеси добавляют 9,41 г 24,47%-ного водного раствора Nacl с последующей дополнительной гомогенизацией. Часть реакционной смеси помещают в автоклав с тефлоновой футеровкой и упаривают в течение 168 час при 165°С и аутогенном давлении. Продукт выделяют фильтрацией, промывают деионизованной водой и сушат при 95°С. Анализ с помощью дифракции рентгеновских лучей на порошке указал на продукт, который был идентифицирован как UZM-19. Характеристические для UZM-19 дифракционные линии приведены в таблице 6. Элементный анализ показал, что продукт состоит из элементов в следующих соотношениях: Si/Al=127,1, Na/Al=0,67, N/Al=14,1 и C/N=4,6. Содержащийся в материале алюминий представляет собой примесь из источника оксида кремния Ludox AS-40.
ПРИМЕР 7 (UZM-25)
Каждый из слоистых алюмосиликатов UZM-13 (пример 1) и UZM-19 (пример 6) был прокален с образованием микропористого кристаллического цеолита, который был идентифицирован как UZM-25. UZM-13 прокаливали при 550°С на воздухе в течение 12 час, a UZM-19 прокаливали на воздухе при 520°С в течение 4 час с образованием UZM-25. Характеристические дифракционные линии, полученные для материалов UZM-25 помощью дифракции рентгеновских лучей на порошке, приведены в таблице 7.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ АЛЮМОСИЛИКАТНАЯ ЦЕОЛИТНАЯ КОМПОЗИЦИЯ UZM-15 | 2004 |
|
RU2340555C2 |
| UZM-16: КРИСТАЛЛИЧЕСКИЙ АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТНЫЙ МАТЕРИАЛ | 2004 |
|
RU2340552C2 |
| ВЫСОКОКРЕМНИСТЫЕ ЦЕОЛИТЫ UZM-5HS | 2004 |
|
RU2340553C2 |
| КРИСТАЛЛИЧЕСКАЯ АЛЮМОСИЛИКАТНАЯ ЦЕОЛИТНАЯ КОМПОЗИЦИЯ: UZM-9 | 2003 |
|
RU2304082C2 |
| UZM-12 И UZM-12HS: МИКРОПОРИСТЫЕ, КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТНЫЕ КОМПОЗИЦИИ И СПОСОБ КОНВЕРСИИ УГЛЕВОДОРОДА | 2005 |
|
RU2377181C2 |
| UZM-5, UZM-5P И UZM-6: КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТЫ И ПРОЦЕССЫ, ИСПОЛЬЗУЮЩИЕ ИХ | 2001 |
|
RU2273602C2 |
| КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТНЫЕ КОМПОЗИЦИИ UZM-8 И UZM-8HS И ПРОЦЕССЫ, В КОТОРЫХ ИСПОЛЬЗУЮТСЯ ЭТИ КОМПОЗИЦИИ | 2004 |
|
RU2340554C2 |
| КРИСТАЛЛИЧЕСКИЙ АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТ UZM-4M, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПРЕВРАЩЕНИЯ УГЛЕВОДОРОДОВ | 2003 |
|
RU2322392C2 |
| АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТ UZM-7, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2011 |
|
RU2528259C2 |
| АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТ UZM-35, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2009 |
|
RU2500619C2 |
Изобретение относится к получению цеолитных структур. Приготовлен ряд кристаллических алюмосиликатных композиций. Эти композиции имеют слоистую структуру, идентифицируются как UZM-13, UZM-17 и UZM-19 и характеризуются соответствующими рентгенограммами. При прокаливании при температуре от 400 до 600°С эти композиции образуют микропористый кристаллический цеолит с трехмерным каркасом, который был идентифицирован как UZM-25. Раскрыт способ приготовления этих композиций и способы применения UZM-25 для конверсии углеводородов. Изобретение обеспечивает получение новых каталитически активных продуктов. 2 н. 2 з. п. ф-лы, 11 табл.
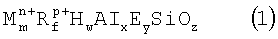
и эмпирический состав прокаленной формы (в расчете на безводное состояние), выражаемый эмпирической формулой:
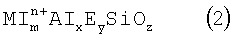
где в формуле (1) М обозначает по меньшей мере один способный к обмену катион, выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов и их смесей, «m» обозначает мольное отношение М к Si и варьирует от 0,01 до 0,35, R представляет собой органический катион, выбираемый из группы, состоящей из протонированных аминов, протонированных диаминов, четвертичных аммониевых ионов, дичетвертичных аммониевых ионов, протонированных алканоламинов и кватернизированных алканоламмониевых ионов, «r» обозначает мольное отношение R к Si и варьирует от 0,05 до 1,0, «n» обозначает среднюю валентность М и варьирует от 1 до 2, «р» обозначает среднюю валентность R и варьирует от 1 до 2, Н обозначает гидроксильный протон, «w» обозначает мольное отношение Н к Si и варьирует от 0 до 1,0, «х» обозначает мольное отношение А1 к Si и варьирует от 0 до 0,25, Е обозначает элемент, который обладает тетраэдрической координацией, присутствует в каркасе и выбирается из группы, состоящей из галлия, железа, хрома, индия, бора и их смесей, «у» обозначает мольное отношение Е к Si и варьирует от 0 до 0,25, где х+у меньше или равно 0,25, a «z» является мольным отношением О к Si и определяется уравнением:
z=(m·n+r·p+w+3·х+3·y+4)/2,
где в формуле (2) M1 обозначает, по крайней мере, один способный к обмену катион, выбираемый из группы, состоящей из протонов, щелочных металлов, щелочноземельных металлов и их смесей, «m» обозначает мольное отношение M1 к Si и варьирует от 0,01 до 0,35, «n» обозначает среднюю валентность M1 и варьирует от 1 до 2, «х» обозначает мольное отношение А1 к Si и варьирует от 0 до 0,25, Е обозначает элемент, который обладает тетраэдрической координацией, присутствует в каркасе и выбирается из группы, состоящей из галлия, железа, хрома, индия, бора и их смесей, «y» обозначает мольное отношение Е к Si и варьирует от 0 до 0,25 и где x+y меньше или равно 0,25, a «z» является мольным отношением О к Si и определяется уравнением:
z=(m·n+3·х+3·y+4)/2,
причем композиция формулы (1) отличается тем, что она имеет рентгенограмму, содержащую по меньшей мере d-расстояния и относительные интенсивности, приведенные в таблицах А, В или С
и где композиция формулы (2) отличается тем, что она имеет рентгенограмму, содержащую по меньшей мере d-расстояния и относительные интенсивности, приведенные в таблице D
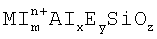
где М обозначает по меньшей мере один способный к обмену катион, выбираемый из группы, состоящей из иона водорода, щелочных металлов, щелочноземельных металлов и их смесей, «m» обозначает мольное отношение М к Si и варьирует от 0,01 до 0,35, «n» обозначает среднюю валентность М и варьирует от 1 до 2, «х» обозначает мольное отношение А1 к Si и варьирует от 0 до 0,25, Е обозначает элемент, который обладает тетраэдрической координацией, присутствует в каркасе и выбирается из группы, состоящей из галлия, железа, хрома, индия, бора и их смесей, «у» обозначает мольное отношение Е к Si и варьирует от 0 до 0,25, и где x+y меньше или равно 0,25, a «z» является мольным отношением О к Si и определяется уравнением:
z=(m·n+3·x+3·y+4)/2,
причем цеолит отличается тем, что он имеет рентгенограмму, содержащую по меньшей мере d-расстояния и относительные интенсивности, приведенные в таблице D.
| US 6419895 В1 16.07.2002 | |||
| US 6613302 А 02.09.2003. |
Авторы
Даты
2008-06-10—Публикация
2004-09-20—Подача