Уровень техники
Настоящее изобретение относится к алюмосиликатному цеолитному материалу, идентифицированному как UZM-16. Этот материал может быть деалюминирован с образованием UZM-16HS, что позволяет получать материалы с различной кислотностью, пористостью и ионообменными свойствами. UZM-16 и UZM-16HS могут применяться в процессах конверсии углеводородов.
Цеолиты представляют собой алюмосиликатные композиции, которые являются микропористыми и которые образованы из имеющих общие углы тетраэдров AlO2 и SiO2. Многочисленные цеолиты как природного происхождения, так и полученные синтетическим путем, применяют в различных промышленных процессах. Синтетические цеолиты получают с помощью гидротермального синтеза с использованием подходящих источников Si, Al, а также структурирующих агентов, таких как щелочные металлы, щелочноземельные металлы, амины или органозамещенные аммониевые катионы. Структурирующие агенты находятся в порах цеолита и в значительной степени ответственны за образующуюся в конечном итоге конкретную структуру. Эти агенты компенсируют обусловленный алюминием заряд решетки и могут также выполнять роль пространственных заполнителей. Цеолиты характеризуются равномерными размерами перовых отверстий, обладая значительной обменной емкостью и способностью обратимо десорбировать адсорбированную фазу, которая диспергирована по внутренним пустотам кристалла без значительного смещения каких-либо атомов, составляющих постоянную структуру цеолитного кристалла. Цеолиты могут быть использованы в качестве катализаторов для конверсии углеводородов, которая осуществляется как на внешних поверхностях, так и на внутренних поверхностях внутри поры.
Синтетический цеолит, называемый цеолитом Т, был получен в Na, К-системе и раскрыт Breck and Acara в US-A-2950952. Последующее кристаллографическое исследование с использованием дифракции электронов (J.M.Bennett and J.A.Gard, Nature, 214, 1005 (1967)) позволило выявить различия и установить уникальность решеток оффретита и эрионита, классифицируя цеолит Т как срастание двух структур. Синтетический цеолит со структурой оффретита, не содержащей сращенного эрионита, был получен в системах Na, К, ТМА и К, ТМА (R.Aiello and R.Barrer, J. Chem. Soc. (A), 1470, (1970)). Rubin и Rosinsky смогли получить материал, родственный эриониту в системе бензилтриметиламмоний (BzTMA), Na, K (US-A-3699139). В той же системе был приготовлен образец оффретита, не имеющий рентгенодифракционных линий, относящихся к эриониту (M.L.Occelli, R.A.Innes, S.S.Pollack, and J.V.Sanders, Zeolites, 7, 265 (1987)). Электронно-дифракционное исследование оффретита, эрионита и оффретит-эрионитных структур, полученных синтезом, включающим шесть органических матричных систем, в том числе BzTMA, характеризуют множество типов дефектов, возникающих в этой системе (J.V.Sanders, M.L.Occelli, R.A.Innes, S.S.Pollack, Studies in Surface Sciences and Catalysis, Ed. Y.Murakami, A.Iijima, and J.W.Ward, Elsevier, New York, 28, 429 (1986)).
В настоящей работе заявителями получен цеолит, обозначенный UZM-16, который имеет некоторое сходство с оффретитом, но имеет и существенные отличия, что делает его уникальной новой структурой. UZM-16 может быть получен в системе бензилтриметиламмония (BzTMA) с небольшим количеством добавленного калия. Рентгенограмма похожа на рентгенограмму оффретита, не имея при этом линий, ассоциируемых с эрионитом, но которая содержит широкую линию в спектре с центром при d=21,5 Å, которая включает неразрешенные пики, расположенные между d=18 до 27 Å. Эта особенность наблюдается в диаграммах дифракции электронов кристаллов и в виде интерференционных полос в изображениях решеток высокого разрешения. Кроме того, в диаграммах дифракции электронов (электронограммах) UZM-16 наблюдается уникальная периодичность, наблюдаемая в плоскости a-b, которая не известна для оффретита и эрионита. UZM-16 имеет более мезопористый характер, чем оффретит.
Краткое описание чертежей
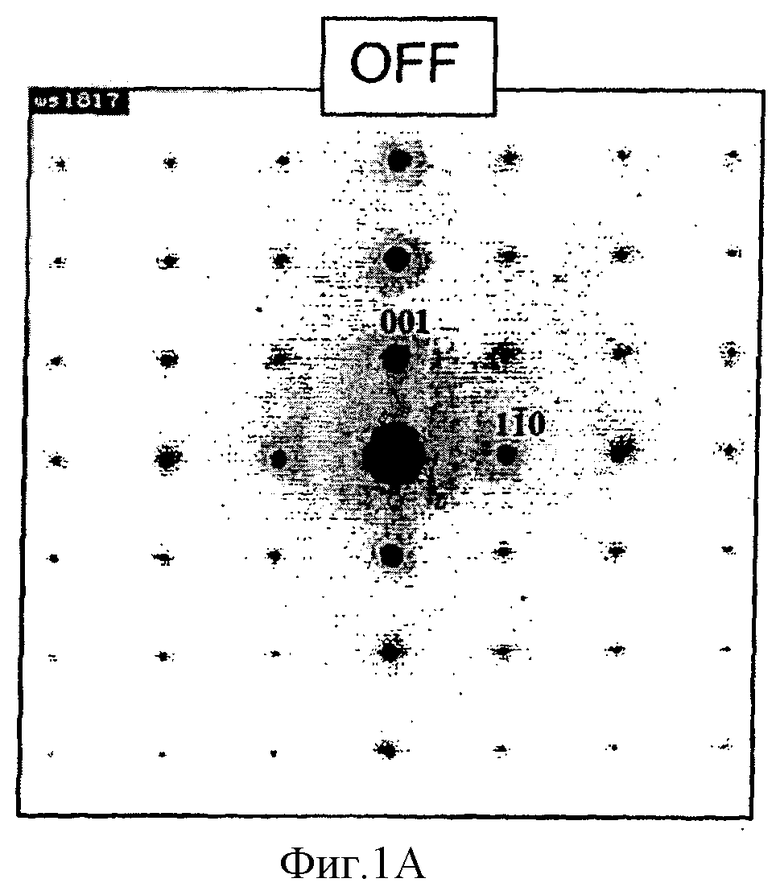
Фиг.1 представляет электронограммы оффретита (фиг.1А) и UZM-16 (фиг.1В) из примера 1, каждая из которых взята вдоль плоскости [110].
Фиг.2 представляет изображение решетки, полученной с помощью электронной микроскопии высокого разрешения для UZM-16 из примера 1.
Осуществление изобретения
Заявителями синтезировано новое семейство цеолитов, обозначенное UZM-16. В своей свежесинтезированной форме цеолит UZM-16 имеет состав, представленный формулой на основе безводной формы:
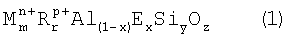
где М обозначает способный обмениваться катион, выбираемый из группы, состоящей из щелочных и щелочноземельных металлов. В число конкретных примеров катионов М входят (но не ограничиваются этим) литий, натрий, калий, цезий, стронций, кальций, магний, барий и их смеси, но калий и натрий являются предпочтительными. Значение «m», который представляет мольное отношение М к (Al+Е), варьирует 0 до 0,75. R обозначает катион бензилтриметиламмония (BzTMA) или комбинацию BzTMA с, по меньшей мере, одним органозамещенным катионом из группы, состоящей из четвертичных аммониевых катионов, протонированных аминов, протонированных диаминов, протонированных алканоламинов, дичетвертичных аммониевых катионов, кватернизованных алканоламмониевых катионов и их смесей. Значение «r», который представляет мольное отношение R к (Al+Е), варьирует от 0,25 до 5,0. Значение «n», который представляет средневзвешенную валентность М, варьирует от +1 до +2. Значение «p», который представляет средневзвешенную валентность органического катиона, имеет значение от +1 до +2. Е обозначает элемент, который присутствует в решетке и выбирается из группы, состоящей из галлия, железа, бора, хрома, индия и их смесей. Значение «x», который представляет мольную долю Е, варьирует от 0 до 1,0. Отношение кремния к (Al+Е) представляется символом «у», который варьирует от 3 до 25, в то время как мольное отношение О к (Al+Е) представляется символом «z» и имеет значение, которое дается уравнением:
z=(m·n+r·p+3+4·y)/2
Когда М представляет только один металл, средневзвешенная валентность является валентностью этого одного металла, т.е. +1 или +2. Однако когда присутствует более одного металла М, общее количество:
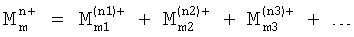
и средневзвешенная валентность «n» дается уравнением:
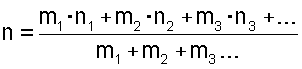
Аналогичным образом, когда присутствует только один органический катион R, средневзвешенная валентность является валентностью этого одного катиона R, т.е. +1 или +2. Когда присутствует более одного катиона R, общее количество R дается уравнением:
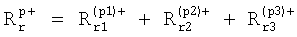
а средневзвешенная валентность «р» дается уравнением:
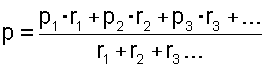
Эти алюмосиликатные цеолиты получают гидротермальной кристаллизацией реакционной смеси, приготовленной соединением источников R, алюминия, возможно Е и/или М и кремния в водных средах. Соответственным образом, источники алюминия включают (но не ограничиваются этим) алкоксиды алюминия, осажденный оксид алюминия, гидроксид алюминия, соли алюминия и металлический алюминий. Конкретные примеры алкоксидов алюминия включают (но не ограничиваются этим) орто-втор-бутоксид алюминия и орто-изопропоксид алюминия. Источники оксида кремния включают (но не ограничиваются этим) тетраэтилортосиликат, тонкий высокопористый порошок оксида кремния, осажденный кремнезем и коллоидный кремнезем. Предпочтительным источником оксида кремния является Ultrasil VN SP (89% SiO2). Источники металла М включают (но не ограничиваются этим) галогенидные соли, нитратные соли, ацетатные соли и гидроксиды соответствующих щелочных и щелочноземельных металлов. В частности, металлы М могут появляться в примесях в некоторых источниках гидроксидов органозамещенного аммония, а также в некоторых источниках оксида кремния. Например, коллоидный кремнезем Ludox AS-40 может содержать порядка 0,05% Na, в то время как гидроксид бензилтриметиламмония фирмы Aldrich Chemical Company имеет в качестве примеси 0,5% К. Источники элементов Е включают (но не ограничиваются этим) бораты щелочных металлов, борную кислоту, осажденный оксигидроксид галлия, сульфат галлия, сульфат железа(III), хлорид железа(III), хлорид хрома, нитрат хрома, хлорид индия и нитрат индия. Как указывалось, когда R является бензилтриметиламмонием, источники содержат (но не ограничиваются этим) гидроксидные, хлоридные, бромидные, йодидные и фторидные соединения. R может быть также комбинацией бензилтриметиламмония и, по меньшей мере, одного какого-либо другого органозамещенного аммониевого соединения. В том случае, когда R является четвертичным аммониевым катионом или кватернизованным алканоламмониевым катионом, источниками могут быть гидроксидные, хлоридные, бромидные, йодидные и фторидные соединения. К числу конкретных примеров принадлежат (не ограничиваясь этим) гидроксид диэтилдиметиламмония, гидроксид тетраэтиламмония, бромид гексаметония, хлорид тетраметиламмония и гидроксид метилтриэтиламмония. Источником R могут быть также нейтральные амины, диамины и алканоламины. Конкретными примерами являются триэтаноламин, триэтиламин и N,N,N',N′-тетраметил-1,6-диаминогексан. В отдельных случаях может быть использован реагент в форме раствора алюмосиликатного сырья. Эти растворы состоят из одного или более гидроксидов органозамещенного аммония и источников кремния и алюминия и их подвергают обработке с образованием прозрачного гомогенного раствора, который обычно хранят и используют в качестве реагента. Этот реагент содержит молекулы алюмосиликата, которые, как правило, не обнаруживаются в цеолитных реакционных смесях, получаемых из отдельных источников кремния и алюминия. Реагент обычно не содержит щелочи или содержит щелочь на уровне примесей, поступающих из источников кремния, алюминия и гидроксида органозамещенного аммония. В синтезе цеолита могут быть использованы один или более таких растворов. В случае замены Al на Е в синтезе может быть также использован силикат соответствующего металла.
Реакционную смесь, содержащую реакционноспособные источники желаемых компонентов, можно описать с помощью формулы, в которой даются молярные коэффициенты оксидов:
aM2/nO:bR2/pO:(1-c)Al2O3:cE2O3:dSiO2:eH2O
где «а» обозначает молярный коэффициент оксида М и имеет значение от 0 до 5, «b» обозначает молярный коэффициент оксида R и имеет значение от 1 до 120, «d» обозначает молярный коэффициент оксида кремния и имеет значение от 5 до 100, «с» обозначает молярный коэффициент оксида Е и имеет значение от 0 до 1,0 и «е» обозначает молярный коэффициент воды и имеет значение от 50 до 15000. В настоящем исследовании реакционную смесь выдерживают в условиях реакции, включающих температуру от 80 до 160°С, преимущественно от 95 до 125°С, в течение времени от 2 до 30 суток, преимущественно в течение времени от 5 до 15 суток, в герметичной реакционной емкости при самопроизвольном давлении. После завершения кристаллизации твердый продукт выделяют из гетерогенной смеси с помощью, например, фильтрации или центрифугирования, промывают деионизованной водой и сушат на воздухе при температуре от комнатной до 100°С.
Кристаллические цеолиты характеризуются трехмерной скелетной структурой, образованной, по меньшей мере, тетраэдрическими ячейками SiO2 и Al2О3. Кроме того, эти цеолиты характеризуются своей рентгенограммой. Рентгенограмма имеет, по меньшей мере, дифракционные линии с d-расстояниями и относительными интенсивностями, приведенными в таблице А.
Свежесинтезированный цеолит содержит в своих порах некоторые способные обмениваться или компенсирующие заряд катионы. Эти способные обмениваться катионы могут быть заменены другими катионами или в случае органических катионов они могут удаляться при нагревании в контролируемых условиях. Ионный обмен включает контактирование цеолитов с раствором, содержащим желаемый катион (в молярном избытке) в условиях обмена. Условия обмена включают температуру от 15 до 100°С и время от 20 мин до 50 час. Условия прокаливания включают температуру от 300 до 600°С и время от 2 до 24 час.
Специальной обработкой для удаления органических катионов, которая приводит к аммониевой форме цеолита, является аммиачное прокаливание. Прокаливание в атмосфере аммиака может разрушать органические катионы предположительно до протонной формы, которая может нейтрализоваться аммиаком с образованием аммониевого катиона. Полученная аммониевая форма цеолита может быть затем подвергнута ионному обмену с целью получения какой-либо другой желаемой формы. Условия аммиачного прокаливания включают обработку в аммиачной атмосфере при температуре от 250 до 600°С и более предпочтительно от 250 до 450°С в течение времени от 10 мин до 5 час. При необходимости обработку можно выполнять в несколько стадий, осуществляемых в том же температурном интервале, так чтобы общее время пребывания в аммиачной атмосфере не превышало 5 час. При температурах выше 500°С обработка должна быть кратковременной - менее получаса и более предпочтительно в течение времени порядка 5-10 мин. Продолжительное прокаливание при температуре выше 500°С может привести наряду с целевым ионным обменом на аммоний к нежелательному деалюминированию и протекает в жестких условиях, так как бóльшая часть органозамещенного аммония разлагается при более низких температурах.
Форма UZM-16 после ионного обмена может быть описана эмпирической формулой:
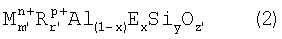
где R, х, y и Е описаны выше и m′ имеет значение от 0 до 5,75, М' обозначает катион, выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов, редкоземельных металлов, иона водорода, иона аммония и их смесей, n′ обозначает средневзвешенную валентность М′ и варьирует от 1 до 3, r′ имеет значение от 0 до 5,75, r′+m′>0 и p обозначает средневзвешенную валентность R и варьирует от +1 до +2. Значение z′ дается формулой:
z′=(m′·n′+r′·p+3+4·y)/2
Цеолиты UZM-16, представленные уравнением (2), могут быть далее обработаны с целью удаления алюминия и возможного введения кремния, в результате чего повышается отношение Si/Al и соответственно изменяются кислотность и ионообменные свойства цеолитов. Такие операции включают: а)осуществление контакта с фторсиликатным раствором или суспензией; b) прокаливание или пропарку с последующей кислотной экстракцией или ионным обменом; с) кислотную экстракцию или d) любое сочетание этих операций в произвольном порядке.
Фторсиликатная обработка известна в уровне техники и описана в US-A-6200463 В1, в котором цитируется US-A-4711770, где описан способ обработки цеолита фторсиликатной солью. Обычные условия такой обработки состоят в осуществлении контакта цеолита с раствором, содержащим фторсиликатную соль, такую как фторсиликат аммония (AFS) при температуре от 20 до 90°С.
Кислоты, которые можно использовать при проведении кислотной экстракции, включают (не ограничиваясь этим) минеральные кислоты, карбоксильные кислоты и их смеси. Примеры этих кислот включают серную кислоту, азотную кислоту, этилендиаминтетрауксусную кислоту (EDTA), лимонную кислоту, щавелевую кислоту и т.д. Концентрация кислоты, которая может быть использована, не является критичной, но удобно работать при концентрации от 1 до 80 мас.% и предпочтительно от 5 до 40 мас.%. Условия кислотной экстракции включают температуру от 10 до 100°С в течение времени от 10 мин до 24 час. После кислотной обработки цеолит UZM-16 выделяют, например, фильтрацией, промывают деионизованной водой и сушат при температуре от комнатной до 100°С. Цеолиты UZM-16, подвергнутые одной или более обработкам, посредством чего удаляется алюминий и, возможно, в скелет вводится кремний, далее будут называться UZM-16HS.
Достигаемая в результате кислотной экстракции степень деалюминирования зависит от формы катиона исходного UZM-16, а также от концентрации кислоты, времени и температуры, при которых проводится экстракция. Например, если в исходном UZM-16 содержатся органические катионы, степень деалюминирования будет невелика по сравнению с UZM-16, из которого органические катионы были удалены. Это может стать преимуществом, если цепью является деалюминирование только на поверхности UZM-16. Как отмечалось выше, удобные способы удаления органических катионов включают прокаливание, аммиачное прокаливание, пропарку и ионный обмен. Условия прокаливания, аммиачного прокаливания и ионного обмена определены выше. Условия пропарки включают температуру от 400 до 850°С с 1-100%-ным паром в течение времени от 10 мин до 48 час и предпочтительно при температуре от 500 до 600°С, концентрации пара от 5 до 50% и времени от 1 до 2 час.
Следует подчеркнуть, что операции прокаливания и пропарки не только удаляют органические катионы, но и могут также деалюминировать цеолит. Таким образом, альтернативные воплощения для деалюминирования включают: операцию прокаливания с последующей кислотной экстракцией и пропарку с последующей кислотной экстракцией. Еще одно воплощение для деалюминирования включает прокаливание или пропарку исходного цеолита UZM-16 с последующей ионообменной обработкой. Само собой разумеется, кислотную экстракцию можно проводить одновременно, до или после ионного обмена.
Условия ионного обмена являются теми же самыми, что и определены выше, а именно температура от 15 до 100°С и время от 20 мин до 50 час. Ионный обмен может проводиться с раствором, включающим катион (М1'), выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов, редкоземельных металлов, иона водорода, иона аммония и их смесей. При проведении этого ионного обмена катион M1 обменивается на вторичный или отличный от него катион М1'. В одном из предпочтительных воплощений композицию UZM-16HS после стадий пропарки или прокаливания вводят в контакт с ионообменным раствором, содержащим аммониевую соль. В число примеров входят (но не ограничиваются этим) нитрат аммония, хлорид аммония, бромид аммония и ацетат аммония. Раствор, содержащий аммониевый ион, может в некоторых случаях содержать минеральную кислоту, такую как (не ограничиваясь этим) азотная, хлористоводородная, серная или их смеси. Концентрация минеральной кислоты такова, что ее количество обеспечивает отношение Н+ к NH4 + от 0 до 1. Этот обмен на ион аммония способствует удалению возможных загрязнений, остающихся в порах после операций пропарки и/или прокаливания.
Из сказанного выше ясно, что с точки зрения эффективности условий процесса желательно, чтобы во время всего процесса деалюминирования в значительной степени сохранялась целостность структуры цеолитного кристалла и чтобы цеолит сохранял не менее 50%, предпочтительно не менее 70% и более предпочтительно не менее 90% своей первоначальной кристалличности. Удобный способ оценки кристалличности продуктов в сравнении с кристалличностью исходного материала состоит в сравнении относительных интенсивностей d-расстояний в соответствующих порошковых рентгенограммах. В качестве стандарта используют сумму интенсивностей (в произвольных единицах) пиков исходного материала над фоном, которую сравнивают с соответствующими интенсивностями пиков продуктов. Когда, например, численная сумма высот пиков молекулярно-ситового продукта составляет 85% от значения суммы интенсивностей пиков исходного цеолита, это означает сохранение 85% кристалличности. На практике принято использовать для этой цели только часть пиков, например пять или шесть из наиболее сильных пиков. Другими индикаторами сохранения кристалличности являются площадь поверхности и адсорбционная емкость. Эти тесты могут стать предпочтительными, когда замещенный металл значительно меняет, например усиливает, поглощение рентгеновских лучей образцом или когда пики подвергаются значительным сдвигам, как, например, в процессе деалюминирования.
После какой-либо из описанных выше операций деалюминирования UZM-16HS обычно сушат и он может быть использован в различных процессах, как описано ниже. Заявителями обнаружено, что свойства UZM-16HS могут быть подвергнуты дальнейшему модифицированию с помощью одной или более дополнительных операций. К этим операциям относятся пропарка, прокаливание или ионный обмен, которые могут осуществляться отдельно или в любых комбинациях. К числу таких операций относятся (но не ограничиваются этим):
пропарка→прокаливание→ионный обмен
прокаливание→пропарка→ионный обмен
ионный обмен→прокаливание→пропарка
ионный обмен→пропарка→прокаливание
пропарка→прокаливание
Чтобы образовать цеолиты изобретения, хотя и не обязательно с одним и тем же результатом, описанная выше операция деалюминирования может быть скомбинирована в любом порядке. Следует подчеркнуть, что определенная последовательность операций, например обработка фторсиликатом аммония, кислотная экстракция, пропарка, прокаливание и т.д., могут повторяться столько раз, сколько необходимо для получения желаемых свойств. Само собой разумеется, повторяться может и одна из операций без повторения других, например повторение обработки фторсиликатом аммония два или более раз перед проведением пропарки или прокаливания и т.п. Наконец, последовательность и/или повторение операций будет определять свойства конечной композиции UZM-16HS.
Полученный выше UZM-16HS описывается эмпирической формулой (для безводной формы):
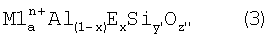
где M1 обозначает, по меньшей мере, один способный обмениваться катион, выбираемый из группы, состоящей из щелочных, щелочноземельных металлов, редкоземельных металлов, иона аммония, иона водорода и их смесей, а представляет мольное отношение M1 к (Al+Е) и варьирует от 0,01 до 50, n обозначает средневзвешенную валентность M1 и имеет значение от +1 до +3, Е обозначает элемент, выбираемый из группы, состоящей из галлия, железа, бора, хрома, индия и их смесей, x обозначает мольную долю Е и варьирует от 0 до 1,0, y′ обозначает мольное отношение Si к (Al+Е) и варьирует от более чем 3,0 до практически чистого оксида кремния и z′′ обозначает мольное отношение О к (Al+Е) и имеет значение, которое определяется уравнением:
z′′=(a·n+3+4·y')/2;
причем цеолит отличается тем, что он обладает рентгенограммой, имеющей, по меньшей мере, d-расстояния и относительные интенсивности, приведенные в таблице В.
Под практически чистым оксидом кремния подразумевается такой оксид кремния, из решетки которого удален практически весь алюминий и/или металлы Е. Хорошо известно, что практически невозможно удалить весь алюминий и/или металл Е. В численном выражении цеолит является практически чистым оксидом кремния тогда, когда y′ имеет значение, по меньшей мере, 3000, предпочтительно 10000 и наиболее предпочтительно 20000. Таким образом, пределы для y′ составляют от 3 до 3000, предпочтительно от более чем 10 до 3000; от 3 до 10000, предпочтительно более чем от 10 до 10000 и от 3 до 20000, предпочтительно более чем от 10 до 20000.
При указании здесь пропорций исходного материала для цеолита или адсорбционных свойств цеолитного продукта и т.п., если не оговорено особо, будет предполагаться «безводное состояние» цеолита. Выражение «безводное состояние» применяется здесь по отношению к цеолиту, в значительной степени не содержащему как физически адсорбированной, так и от химически адсорбированной воды.
Цеолиты настоящего изобретения (как UZM-16, так и UZM-16HS) способны разделять смеси молекулярных частиц по размеру молекул (кинетическому диаметру) или по степени полярности молекулярных частиц. Когда разделение молекулярных частиц основано на размере молекул, разделение производится за счет того, что меньшие молекулярные частицы входят в внутрикристаллическое пустое пространство, в которое не могут попасть более крупные частицы. Кинетические диаметры различных молекул, таких как кислород, азот, диоксид углерода, оксид углерода, приведены в D.W.Breck, Zeolite Molecular Sieves (цеолитные молекулярные сита), John Wiley and Sons (1974), p.636.
Кристаллические микропористые композиции настоящего изобретения (как UZM-16, так и UZM-16HS), свежесинтезированные, после прокаливания или после любой из указанных выше обработок, могут быть использованы в качестве катализаторов или носителей катализаторов в процессах конверсии углеводородов. Процессы конверсии углеводородов хорошо известны в технике и включают реакции с раскрытием кольца, крекинг, гидрокрекинг, алкилирование как ароматических соединений, так и изопарафинов, изомеризацию, полимеризацию, реформинг, депарафинизацию, гидрогенизацию, дегидрогенизацию, трансалкилирование, дезалкилирование, гидратацию, дегидратацию, гидроочистку, гидродеазотирование, гидродесульфуризацию, метанирование и процесс конверсии синтез-газа. Конкретные условия реакции и типы сырья, которые могут быть использованы в этих процессах, приведены в US-A-4310440 и US-A-4440871. Предпочтительным процессом конверсии углеводородов является процесс с раскрытием кольца, в котором циклические углеводороды превращаются в нециклические углеводороды, т.е. линейные или разветвленные углеводороды.
Эти кристаллические микропористые композиции могут катализировать и другие реакции, в том числе катализируемое основаниями алкилирование боковых цепей алкилароматических соединений, реакции альдольной конденсации, изомеризацию двойной связи олефинов и изомеризацию ацетиленов, дегидрогенизацию спиртов и димеризацию олефинов, олигомеризацию и превращение спиртов в олефины. Формы этих материалов с обмененными ионами могут с успехом катализировать восстановление NOx до N2 в автомобильных и промышленных выхлопах. Некоторые из условий реакции и типов сырья, которые могут быть использованы в этих процессах, приведены в US-A-5015796 и в Н.Pines, THE CHEMISTRY OF CATALYTIC HYDROCARBON CONVERSIONS (Химия каталитической конверсии углеводородов). Academic Press (1981), pp.123-124 и содержащихся там ссылках.
Приведенные в следующих ниже примерах (и, кроме того, в таблицах) рентгенограммы получены с помощью методов порошкового рентгеноструктурного анализа. Источником излучения была рентгеновская трубка высокой интенсивности, работающая при 45 кВ и 35 мА. Дифракционная картина от К-α-излучения меди получена с помощью соответствующих компьютерных методов. Плоские спрессованные порошковые образцы непрерывно сканировались со скоростью 2°(2θ) в минуту от 2° до 70° (2θ). Межплоскостные расстояния (d) в ангстремах получены на основании положения дифракционных пиков, выраженных в 2θ, где θ означает угол Брэгга, каким он представляется из оцифрованных данных. Интенсивности определяли на основании интегрированной площади дифракционных пиков после вычитания фона, где «Io» является интенсивностью наиболее сильной линии, или пика, а «I» является интенсивностью каждого из остальных пиков.
Как известно специалистам в данной области, определение параметра 2θ сопряжено с человеческими и механическими ошибками, которые в сумме могут привести к погрешности ±0,4 для каждого приводимого значения 2θ и до ±0,5 для приводимых значений нанокристаллических материалов. Эта погрешность проявляется естественно и в приводимых значениях d-расстояний, которые рассчитывают из значений θ. Эта погрешность является общей для всей данной области и поэтому не мешает отличать кристаллические материалы настоящего изобретения один от другого и от композиций предшествующего уровня техники. В некоторых приведенных рентгенограммах относительные интенсивности d-расстояний указаны с помощью обозначений vs, s, m и w, которые означают «очень сильный», «сильный», «средний» и «слабый» соответственно. Выраженные в единицах величины 100×I/Io указанные выше обозначения оцениваются как: w=0-15, m=15-60, s=60-80 и vs=80-100. В некоторых случаях чистота синтезированного продукта может быть оценена на основании порошковой рентгенограммы. Так, например, если считается, что образец чистый, то при этом лишь предполагается, что в рентгенограмме образца отсутствуют линии, приписываемые кристаллическим примесям, но при этом речь не идет об отсутствии аморфных материалов.
Для более полного иллюстрирования изобретения приводятся следующие примеры. Следует иметь в виду, что эти примеры являются только иллюстрацией и не предназначены для неуместного в данном случае ограничения широкого объема изобретения, которое дается в прилагаемой формуле изобретения.
ПРИМЕР 1
Алюмосиликатную реакционную смесь получают добавлением 2,33 г Al(O-sec-Bu)3 (95+%) к 63,35 г BzTMAOH (40%) при интенсивном перемешивании, после чего добавляют 28 г коллоидного кремнезема (LUDOX™ AS-40, 40% SiO2). Далее, к алюмосиликатной реакционной смеси при непрерывном перемешивании медленно прибавляют 6 г воды. Смесь гомогенизуют в течение еще 30 мин с помощью высокоскоростной мешалки и размещают по трем футерованным тефлоном автоклавам, которые помещают в печь при 125°С и автоклавируют там смеси в течение 3, 6 и 10 суток при самопроизвольном давлении. Твердые продукты выделяют фильтрацией, промывают деионизованной водой и сушат при 95°С.
Продукты трех реакций показали рентгенограмму, характерную для цеолита, обозначаемого UZM-16. Репрезентативные дифракционные линии 3-дневого образца показаны в приведенной ниже таблице 1. Площадь поверхности БЕТ прокаленного материала, определенная по адсорбции N2, составила 523 м2/г, а объем микропор 0,26 см3/г.
Отличие UZM-16 от структуры оффретита выявляется также с помощью дифракции электронов. Фиг.1 показывает сравнение электронограмм UZM-16 (фиг.1В) и оффретита (Фиг.1А), взятых вдоль плоскости [110] и показанных в указанной плоскости в направлениях (001) и  . Ясно, что периодичность в направлениях
. Ясно, что периодичность в направлениях  у UZM-16 отличается от той же периодичности у оффретита и что межплоскостное расстояние больше в три раза. Представленная здесь электронограмма соответствует электронограммам, приводимым в литературе для той же самой ориентации (J.V.Sanders, M.L.Ocelli, R.A.Innes, S.S.Pollack, Studies in Surface Sciences and Catalysis, Ed. Y.Murakami, A.Iijima, and J.W.Ward, Elsevier, New York, 28, 429 (1986)).
у UZM-16 отличается от той же периодичности у оффретита и что межплоскостное расстояние больше в три раза. Представленная здесь электронограмма соответствует электронограммам, приводимым в литературе для той же самой ориентации (J.V.Sanders, M.L.Ocelli, R.A.Innes, S.S.Pollack, Studies in Surface Sciences and Catalysis, Ed. Y.Murakami, A.Iijima, and J.W.Ward, Elsevier, New York, 28, 429 (1986)).
Бóльшее межплоскостное расстояние можно легко наблюдать на изображениях решетки UZM-16. Фиг.2 показывает изображение решетки, взятое вдоль [110]. Края решетки в вертикальном направлении на изображении соответствуют 19,3 Å, указанным с помощью отражения при 1/3  на фиг.1b. Это расстояние втрое больше
на фиг.1b. Это расстояние втрое больше 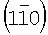 расстояния, которое можно ожидать у оффретита и которое было бы равным 6,65 Å.
расстояния, которое можно ожидать у оффретита и которое было бы равным 6,65 Å.
ПРИМЕР 2
Этот пример демонстрирует получение UZM-16, его модифицирование прокаливанием, ионный обмен и пропарку с образованием UZM-16HS с последующим дополнительным модифицированием с помощью кислотной экстракции, в результате чего образуется еще один вариант UZM-16HS. Алюмосиликатную реакционную смесь приготовляют добавлением 35,21 г Al(O-sec-Bu)3 (95+%) к 927,47 г BzTMAOH (40%) при интенсивном перемешивании. После растворения алюминиевого реагента добавляют 416,45 г коллоидного кремнезема (LUDOX™ AS-40, 40% SiO2) и гомогенизуют образовавшуюся смесь в течение 30 мин с помощью высокоскоростной мешалки. Смесь кристаллизуют при 125°С в течение 6 суток в перемешиваемом 2-л реакторе PARR™ при самопроизвольном давлении. Твердые продукты выделяют фильтрацией, промывают деионизованной водой и сушат при 95°С. С помощью порошкового рентгеноструктурного анализа идентифицируют продукт как UZM-16. Характеристические для рентгенограммы дифракционные линии представлены в приведенной ниже таблице 2. Элементный анализ показал, что этот родственный UZM-16 материал характеризуется отношением Si/Al, равным 5,83. Порцию 62,5 г UZM-16 вначале прокаливают в токе азота, постепенно повышая температуру до 250°С со скоростью 1°С/мин с выдержкой при 250°С в течение 2 час, после чего температуру постепенно повышают до 500°С со скоростью 1°С/мин, выдерживают 3 часа при 500°С, заменяют атмосферу на ток воздуха и выдерживают при 500°С еще 3 часа. Площадь поверхности БЕТ прокаленного материала составила 676 м2/г, а объем микропор 0,33 см3/г. Порцию 51 г прокаленного материала подвергают обмену на аммоний, суспендируя ее в растворе, содержащем 52 г NH4NO3, растворенного в 500 г деионизованной воды. Взвесь нагревают в течение 7 час до 85°С и затем выделяют фильтрацией и тщательно промывают деионизованной водой. Ионный обмен повторяют еще два раза, но в течение только 2,5 час при 85°С.
Порцию 40 г подвергнутого обмену на аммоний прокаленного UZM-16 пропаривают 2 часа при 600°С 50%-ным паром, используя горизонтальный пропариватель. Продукт идентифицируют как UZM-16HS с помощью порошкового рентгеноструктурного анализа. Характеристические дифракционные линии этого продукта показаны в приведенной ниже таблице 2. Измерения адсорбции азота дали для пропаренного подвергнутого обмену на аммоний материала UZM-16HS площадь поверхности БЕТ 424 м2/г и объем микропор 0,20 см3/г.
Порцию 20 г полученного пропаркой UZM-16HS дополнительно обрабатывают кислотой. Кислотный раствор приготовляют растворением 19,7 г HNO3 (69%) в 350 г деионизованной воды. Перед добавлением пропаренного UZM-16 раствор нагревают до 90°С. Образовавшуюся взвесь перемешивают 1 час при 90°С. Продукт выделяют фильтрацией, промывают деионизованной водой и сушат при 98°С. Модифицированный продукт определяется как UZM-16HS с помощью порошкового рентгеноструктурного анализа. Характеристические дифракционные линии показаны в приведенной ниже таблице 2. Элементные анализы пропаренного, промытого кислотой продукта дали значение Si/Al, равное 14,76.
ПРИМЕР 3
Алюмосиликатную реакционную смесь получают добавлением 35,21 г Al(O-sec-Bu)3 (95+%) к 927,47 г BzTMAOH (40%) при интенсивном перемешивании. После растворения алюминиевого реагента добавляют 416,45 г коллоидного кремнезема (LUDOX™ AS-40, 40% SiO2) и гомогенизуют образовавшуюся смесь в течение 30 мин с помощью высокоскоростной мешалки. Смесь кристаллизуют при 105°С в течение 12 суток в 2-л перемешиваемом реакторе PARR™ при самопроизвольном давлении. Твердый продукт выделяют фильтрацией, промывают деионизованной водой и сушат при 95°С. С помощью порошкового рентгеноструктурного анализа идентифицируют продукт как UZM-16. Характеристические для рентгенограммы дифракционные линии представлены в приведенной ниже таблице 3. Элементный анализ показал, что эта родственная UZM-16 композиция характеризуется отношением Si/Al, равным 5,7. Продукт вначале прокаливают в атмосфере азота, постепенно повышая температуру до 350°С со скоростью 1°С/мин с выдержкой при 350°С в течение 1 часа, после чего температуру постепенно повышают до 500°С со скоростью 1°С/мин, выдерживают 6 час при 500°С, заменяют атмосферу на воздух и выдерживают при 500°С еще 6 час. Площадь поверхности БЕТ прокаленного материала составила 574 м2/г, а объем микропор 0,24 см3/г. Порцию 98 г прокаленного материала подвергают обмену на аммоний, суспендируя ее в растворе, содержащем 100 г NH4NO3, растворенного в 1000 г деионизованной воды. Взвесь нагревают в течение 5 час до 80°С, продукт выделяют фильтрацией и тщательно промывают деионизованной водой. Ионный обмен повторяют еще 3 раза.
Порцию 18 г подвергнутого обмену на аммоний прокаленного UZM-16 пропаривают 2 часа при 600°С 50%-ным паром, используя горизонтальный пропариватель. 12 г этого пропаренного материала дополнительно экстрагируют кислотой. Кислотный раствор приготовляют разбавлением 10 г HNO3 (69%) в 300 г деионизованной воды. Перед добавлением пропаренного, подвергнутого обмену на аммоний UZM-16 раствор нагревают до 90°С. Продукт выделяют фильтрацией, промывают деионизованной водой и сушат при 98°С. Модифицированный продукт определяется как UZM-16HS с помощью порошкового рентгеноструктурного анализа. Характеристические дифракционные линии продукта показаны в таблице 3. Элементные анализы показали, что деалюминированный продукт характеризуется отношением Si/Al, равным 11,56. Измерения адсорбции азота показали, что площадь поверхности БЕТ составляет 466 м2/г, а объем микропор 0,19 см3/г.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ АЛЮМОСИЛИКАТНАЯ ЦЕОЛИТНАЯ КОМПОЗИЦИЯ UZM-15 | 2004 |
|
RU2340555C2 |
| ВЫСОКОКРЕМНИСТЫЕ ЦЕОЛИТЫ UZM-5HS | 2004 |
|
RU2340553C2 |
| КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТНЫЕ КОМПОЗИЦИИ UZM-8 И UZM-8HS И ПРОЦЕССЫ, В КОТОРЫХ ИСПОЛЬЗУЮТСЯ ЭТИ КОМПОЗИЦИИ | 2004 |
|
RU2340554C2 |
| КРИСТАЛЛИЧЕСКИЙ АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТ UZM-4M, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПРЕВРАЩЕНИЯ УГЛЕВОДОРОДОВ | 2003 |
|
RU2322392C2 |
| КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТЫ: UZM-13, UZM-17, UZM-19 И UZM-25 | 2004 |
|
RU2326050C2 |
| КРИСТАЛЛИЧЕСКАЯ АЛЮМОСИЛИКАТНАЯ ЦЕОЛИТНАЯ КОМПОЗИЦИЯ: UZM-9 | 2003 |
|
RU2304082C2 |
| МИКРОПОРИСТЫЕ UZM-5 ЦЕОЛИТНЫЕ НЕОРГАНИЧЕСКИЕ МЕМБРАНЫ ДЛЯ РАЗДЕЛЕНИЯ ГАЗОВ ПАРОВ И ЖИДКОСТЕЙ | 2012 |
|
RU2544667C9 |
| АЛЮМОСИЛИКАТНЫЙ ЦЕОЛИТ UZM-7, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2011 |
|
RU2528259C2 |
| UZM-5, UZM-5P И UZM-6: КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТЫ И ПРОЦЕССЫ, ИСПОЛЬЗУЮЩИЕ ИХ | 2001 |
|
RU2273602C2 |
| UZM-12 И UZM-12HS: МИКРОПОРИСТЫЕ, КРИСТАЛЛИЧЕСКИЕ АЛЮМОСИЛИКАТНЫЕ ЦЕОЛИТНЫЕ КОМПОЗИЦИИ И СПОСОБ КОНВЕРСИИ УГЛЕВОДОРОДА | 2005 |
|
RU2377181C2 |


Синтезированы микропористый кристаллический цеолит и его замещенный вариант, обозначаемые UZM-16. Эти цеолиты получают с помощью бензилтриметиламмониевого катиона (BzTMA) или сочетания BzTMA с, по меньшей мере, одним другим четвертичным аммониевым катионом. Эти цеолиты имеют структуру, родственную структуре оффретита, но проявляют структурные и другие отличия. Цеолиты UZM-16 могут быть деалюминированы с образованием цеолитов UZM-16HS, которые имеют другую кислотность, пористость и ионообменные свойства. Полученные продукты, как UZM-16, так и UZM-16HS, могут быть эффективными в различных процессах конверсии углеводородов. 5 н. и 4 з.п. ф-лы, 2 ил., 5 табл.
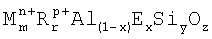 ,
,
где М обозначает, по меньшей мере, один способный обмениваться катион, выбираемый из группы, состоящей из щелочных и щелочноземельных металлов; m представляет мольное отношение М к (А1+Е) и варьирует от 0 до 0,75; R обозначает катион бензилтриметиламмония (BzTMA) или комбинацию BzTMA с, по меньшей мере, одним органозамещенным катионом из группы, состоящей из четвертичных аммониевых катионов, протонированных аминов, протонированных диаминов, протонированных алканоламинов, дичетвертичных аммониевых катионов, кватернизованных алканоламмониевых катионов и их смесей; r представляет мольное отношение R к (Al+Е) и имеет значение от 0,25 до 5,0; Е обозначает элемент, выбираемый из группы, состоящей из Ga, Fe, In, Cr, В и их смесей; х представляет мольную фракцию Е и варьирует от 0 до 1,0; n представляет средневзвешенную валентность М и имеет значение от +1 до +2; р представляет средневзвешенную валентность R и имеет значение от +1 до +2; у представляет мольное отношение Si к (Al+Е) и варьирует от более чем 3 до 25 и z представляет мольное отношение O к (А1+Е) и имеет значение, которое определяется уравнением
z=(m·n+r·p+3+4·y)/2;
при этом цеолит отличается тем, что он обладает рентгенограммой, имеющей, по меньшей мере, d-расстояния и относительные интенсивности, приведенные в таблице А:
 ,
,
где а имеет значение от 0 до 5,0, b имеет значение от 1 до 120, с имеет значение от 0 до 1,0, d имеет значение от 5 до 100 и е имеет значение от 50 до 15000.
 ,
,
где Ml обозначает, по меньшей мере, один способный обмениваться катион, выбираемый из группы, состоящей из щелочных металлов, щелочноземельных металлов, редкоземельных металлов, иона аммония, иона водорода и их смесей, а представляет мольное отношение Ml к (Al+Е) и варьирует от 0,01 до 50, Е обозначает элемент, выбираемый из группы, состоящей из галлия, железа, бора, хрома, индия и их смесей, х обозначает мольную долю Е и варьирует от 0 до 1,0, n представляет средневзвешенную валентность Ml и имеет значение от +1 до +3, y′ обозначает мольное отношение Si к (Al+Е) и имеет значение больше 3,0 и z′′ обозначает мольное отношение О к (Al+Е) и имеет значение, которое определяется уравнением
z′′=(a·n+3+4·y′)/2,
при этом цеолит отличается тем, что он обладает рентгенограммой, имеющей, по меньшей мере, d-расстояния и относительные интенсивности, приведенные в таблице В:
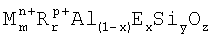 ,
,
где М′ обозначает способный обмениваться катион, выбираемый из группы, состоящей из иона аммония, иона водорода, щелочных металлов, щелочноземельных металлов, редкоземельных металлов и их смесей, n обозначает средневзвешенную валентность М′ и варьирует от 1 до 3, m′ обозначает мольное отношение М′ к (Al+Е) и варьирует от 0 до 5,75, R обозначает катион бензилтриметиламмония (BzTMA) или комбинацию BzTMA с по меньшей мере одним органозамещенным катионом из группы, состоящей из протонированных аминов, протонированных диаминов, протонированных алканоламинов, дичетвертичных аммониевых ионов, кватернизованных алканоламмониевых ионов и их смесей; р представляет средневзвешенную валентность органического катиона и варьирует от +1 до +2; r′ представляет мольное отношение R к (Al+Е) и варьирует от 0 до 5,75; r′+m′>0; y′представляет отношение Si к (Al+Е) и варьирует от 3 до 25; и z′ представляет мольное отношение О к (Al+Е) и имеет значение, которое определяется уравнением
z′=(m′·n+r′·p+3+4·y′)/2,
при этом исходный цеолит обладает рентгенограммой, имеющей, по меньшей мере, d-расстояния и относительные интенсивности, приведенные в таблице А.
| US 3699139 А, 17.10.1972 | |||
| US 4687653 А, 18.08.1987 | |||
| US 4834961 А, 30.05.1989 | |||
| US 5133951 А, 18.08.1987. |
Авторы
Даты
2008-12-10—Публикация
2004-04-20—Подача