Изобретение относится к сорбционным материалам для удаления ионов тяжелых металлов из грунтовых вод, поверхностных водных систем и может найти применение также на предприятиях химической и металлургической промышленности, использующих травильные и гальванические технологии.
Известен сорбент (патент РФ №2051112, МПК 6 C02F 1/28, опубл. 27.12.1995 г.), который представляет собой слой цеолита, обработанный раствором щавелевой кислоты с концентрацией 0,05-0,1 моль/л в присутствии минеральной кислоты до рН 1-2. При пропускании через слой такого сорбента сточных вод, содержащих ионы тяжелых металлов, достигается следующая степень очистки воды от ионов: Cr (III) и Cr (VI) до 100%, Cu (II) до 98,2%, Fe (II, III) до 99,2%, Zn (II) до 98,1%.
Однако у этого сорбента есть существенный недостаток: сорбент не очищает воду от ионов мышьяка, который присутствует практически во всех грунтовых и поверхностных водах и который является сильнейшим ядом для живых организмов.
Очистить эти воды от ионов мышьяка, причем от ионов мышьяка с разной валентностью, позволяет использование наиболее близкого по технической сущности и достигаемому эффекту к предложенному другой известный сорбент (патент US №6921732, МПК B01J 20/06, опубл. 26.07.2005 г.). Он представляет собой цеолит, покрытый нанофазными оксидами железа и марганца, причем сорбент содержит 0,25-10% оксида железа с молярным соотношением Mn/(Mn+Fe), равным 0,10. Сорбент получают путем добавления цеолита к железо-марганцевому раствору, приготовленному смешением раствора оксида железа с марганецсодержащим соединением. Эту смесь фильтруют, и из отфильтрованного продукта методом сушки получают сорбент в виде цеолита, покрытого нанофазными гидрооксидами железа и марганца.
Сорбент-прототип имеет следующие недостатки. Он позволяет удалять из воды только ионы мышьяка и не применяется для очистки воды от ионов других тяжелых металлов. При этом наибольшая концентрация загрязнения воды, при которой достигается высокая степень очистки, сравнительно мала: 1,57 мг/л (ppm). Кроме того, в процессе очистки от As (III), широко распространенного в природных условиях, высвобождаются ионы марганца Mn (II), которые также являются загрязнителями воды.
Основным техническим результатом предложенного сорбента является расширение списка ионов тяжелых металлов, улавливаемых до высокой степени очистки. Причем это не только анионы мышьяка (III), мышьяка (V) и хрома (VI), но и катионы кадмия, меди, свинца. Наибольшая концентрация загрязнения эффективно очищаемой воды составляет 5 мг/л, т.е. выше, чем у сорбента прототипа в 3,2 раза. Кроме того, при использовании предложенного сорбента не происходит высвобождение ионов марганца, а идет только процесс поглощения ионов мышьяка.
Указанные технические результаты достигаются тем, что сорбент для очистки воды от ионов тяжелых металлов, состоящий из измельченного цеолита и нанофазного материала, который включает в себя гидрооксид железа, согласно предложенному решению, дополнительно содержит нанофазный бемит при следующем соотношении компонентов, мас.%:
Пример конкретного выполнения 1.
Для получения заявленного сорбента взяли навеску 3 г цеолита Холинского месторождения РФ, имеющего согласно ТУ 2163-002-12763074-97 химический состав, %: SiO2 - 64,79, Н2O - 12,85, Al2O3 - 12,75, CaO - 1,89, MgO - 1,50, Fe2O3 - 1,40, К2О - 1,26, Na2O - 0,44, CaF2 - 0,03, TiO2 - 0,02, и в среднем содержащего 60% клиноптилолита. Навеску цеолита смешали с 0,53 г нанофазного бемита и 0,62 г нанофазного гидроксида железа. Полученную смесь перетерли в агатовой ступке в течение 5 мин, а затем сушили в течение 6 час в сушильном шкафу при температуре 190°С.
Нанофазный бемит получили взаимодействием порошка алюминия с водой в слабощелочной среде. Для этого взяли навеску 0,181 г алюминиевого порошка, представляющего собой согласно ГОСТ 5494-95 особо тонкоизмельченные частицы алюминия пластинчатой формы. Навеску алюминиевого порошка поместили в 125 мл дистиллированной воды и добавили 2 мл концентрированного раствора NH4OH для создания щелочной среды. Полученную смесь подогрели до 50°С и оставили до полного окончания реакции алюминиевого порошка с водой. Затем полученный осадок отфильтровали на воронке Бюхнера с помощью водоструйного насоса, промыли до нейтральной рН. Осадок сушили 2 часа в сушильном шкафу при 50-75°С, а затем при 160°С в течение 6 часов. Изучение рентгенофазового состава образца полученного осадка проводили на рентгеновском дифрактометре ДРОН-2 (НПО "Буревестник", РФ) с использованием R-излучения меди с длиной волны 1,54178Å и никелевым бета-фильтром. Дифрактометрические характеристики образца показали, что в качестве кристаллической фазы образец представляет собой бемит (табл.1). Примесей других кристаллических фаз не обнаружено.
Исследования полученного образца, проведенные на электронном микроскопе JEM 100 CXII (JEOL Ltd., Япония) в просвечивающем режиме, показали, что образец бемита состоит из игольчатых наночастиц толщиной 2-5 нм и длиной до 200 нм.
Нанофазный гидроксид железа Fe(ОН)3 получили в виде свежеосажденного геля путем взаимодействия растворов хлорида железа и NH4OH по методике, описанной в руководстве по лабораторному приготовлению неорганических препаратов (Ю.В.Карякин. Чистые химические реактивы. - М.-Л.: ГНТИ хим. лит. - 1947. - с.135). Электронно-микроскопические исследования образца показали, что он состоит из аморфных частиц размером 50-200 нм.
Пример конкретного выполнения 2.
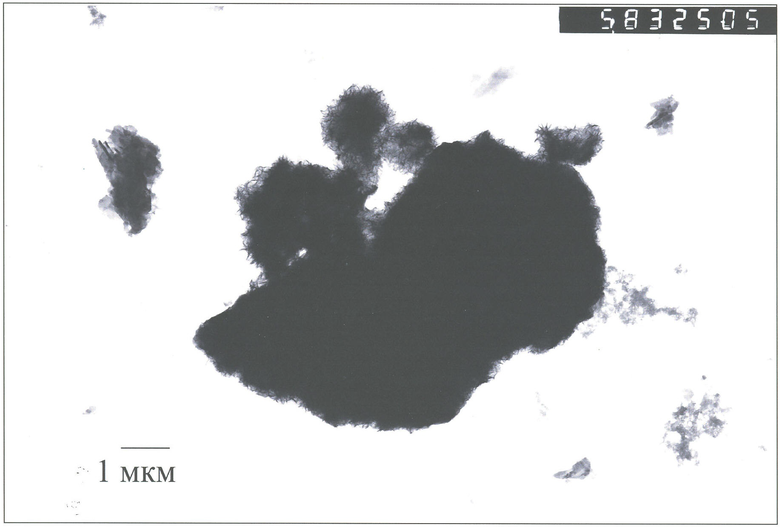
Для получения заявленного сорбента навеску 3 г цеолита Холинского месторождения, измельченного в течение 5 мин в агатовой ступке, поместили в 125 мл дистиллированной воды. Затем добавили 0,238 г алюминиевого порошка (ГОСТ 5494-95) и 2 мл концентрированного раствора NH4OH для создания щелочной среды. Полученную смесь подогрели до 50°С и оставили до полного окончания реакции алюминиевого порошка с водой. В полученную смесь, подкисленную до рН 4 соляной кислотой, добавили при перемешивании 53,04 мл раствора FeCl·6Н2О (концентрация 29,59 г/л), затем при перемешивании 5,1 мл концентрированного NH4OH. После охлаждения полученную смесь отфильтровали на воронке Бюхнера с помощью водоструйного насоса, промыли до нейтральной рН. Осадок сорбента сушили в сушильном шкафу сначала 2 часа при 50-75°С, а затем при 190°С в течение 6 часов. Таким образом получили сорбент, состоящий из измельченного цеолита и нанофазного материала, включающего в себя гидроксид железа и бемит. Полученный сорбент исследовали на электронном микроскопе. На электронной фотографии видно, что частицы цеолита, размер которых 1-8 мкм, покрыты нанофазными частицами бемита игольчатой формы и аморфными частицами гидроксида железа. Таким образом, полученный образец состоит из относительно крупных частиц цеолита, покрытых нанофазным материалом, и практически не содержит свободных наночастиц. Это обеспечивает меньшее забивание фильтрующих материалов и более низкую потерю напора воды при дальнейшем использовании сорбента.
Испытания полученных образцов сорбента на адсорбционную способность по отношению к ионам тяжелых металлов проводили следующим образом. Исследование поглощения ионов As (III) проводили из модельного раствора с концентрацией 2,5 мг/л, который готовили с использованием государственного стандартного образца с концентрацией 100 мг/л. Навеску 200 мг сорбента помещали в 20 мл модельного раствора (рН 6) и перемешивали на магнитной мешалке в течение 30 мин. Затем раствор отстаивали в течение 10-15 мин и анализировали методом инверсионной вольтамперометрии на остаточное содержание ионов AsO3 3-. Для этого аликвоту раствора (0,2-0,5 мл) помещали в ячейку с фоновым электролитом, проверенным на чистоту. В качестве рабочего электрода использовали золотой пленочный электрод на графитовой подложке, фон - 0,3 М соляная кислота. Удаления кислорода не требовалось, т.к. пик анодного окисления мышьяка наблюдался раньше потенциала восстановления кислорода. Накопление мышьяка на электроде в форме интерметаллида с золотом проводили в течение 60 секунд при Е=-1,0 В. Вольтамперные кривые снимали в постояннотоковом режиме на анализаторе СТА (изготовитель фирма ИТМ, г.Томск, РФ), совмещенном с компьютером. Анализатор имеет 3 электрохимических ячейки для параллельных опытов и ртутно-кварцевую лампу для УФ-облучения при необходимости. Одновременно проводили анализ трех аликвотных частей одного модельного раствора. Остаточная концентрация ионов есть среднее значение из 3-х параллельных опытов. Оценку концентрации проводили методом добавок стандартного раствора AsO3 3- с концентрацией 2,5 мг/л (в количестве 0,1 мл). Минимально определяемая концентрация составляла 0,001 мг/л. Процент сорбции был вычислен при принятии за 100% исходной концентрации AsO3 3-. Данные по сорбционной способности заявляемого сорбента с разным содержанием нанофазного бемита и гидроксида железа приведены в табл.2.
Как видно из табл.2, лучшими сорбционными характеристиками по отношению к ионам AsO3 3- обладает сорбент, содержащий нанофазный бемит и гидроксид железа при следующем соотношении компонентов, мас.%: нанофазный гидроксид железа - 12-18, нанофазный бемит - 5-13, цеолит - остальное. При содержании в сорбенте нанофазного гидроксида железа более и менее 12% и нанофазного бемита более 13 и менее 5% наблюдается ухудшение адсорбционных свойств.
Аналогичные результаты были получены при использовании цеолита Чугуевского месторождения РФ.
Для образца №2, содержащего 5% нанофазного бемита и 15% нанофазного гидроксида железа, аналогичным образом проводили испытания при более высокой концентрации ионов AsO3 3- - 5 мг/л. После проведения сорбции ионов AsO3 3- не обнаружено.
Аналогичным образом проводили испытания образцов сорбента на адсорбцию ионов других тяжелых металлов при концентрациях, многократно превышающих предельно допустимые концентрации: Cd2+ - 0,1 мг/л, Cu2+ - 2,5 мг/л, Pb2+ - 0,3 мг/л, AsO4 3- - 2,5 мг/л, CrO4 2- - 1,0 мг/л. Катионы определяли на ртутном пленочном электроде с серебряной подложкой, хромат-анионы - на рабочем графитовом электроде, анионы мышьяка (V) - на золотографитовом электроде. Данные, подтверждающие высокую сорбционную способность предложенного сорбента по отношению к ионам различных тяжелых металлов, приведены в табл.3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ ТЯЖЕЛЫХ МЕТАЛЛОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2592525C2 |
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ МЫШЬЯКА | 2014 |
|
RU2610612C2 |
| ПОЛИМЕРНЫЙ СОРБЦИОННЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ ОЧИСТКИ ВОДЫ ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2734712C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ДЛЯ ОЧИСТКИ РАСТВОРОВ ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2014 |
|
RU2561117C1 |
| СПОСОБ ДЕТОКСИКАЦИИ СТОЧНЫХ ВОД, ЗАГРЯЗНЕННЫХ СОЛЯМИ МЫШЬЯКА | 2013 |
|
RU2562495C2 |
| СОРБЦИОННЫЙ МАТЕРИАЛ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ ТЯЖЁЛЫХ МЕТАЛЛОВ | 2023 |
|
RU2838228C1 |
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ МЫШЬЯКА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2520473C2 |
| Сорбент для очистки водных сред от ионов мышьяка и способ его получения | 2015 |
|
RU2628396C2 |
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ ФТОРА | 2024 |
|
RU2838080C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ДЛЯ ОЧИСТКИ ВОДЫ ОТ МЫШЬЯКА | 2017 |
|
RU2638959C1 |
Изобретение касается удаления ионов тяжелых металлов из грунтовых и поверхностных вод и при очистке стоков. Сорбент для очистки воды от ионов тяжелых металлов состоит из измельченного цеолита, нанофазного гидроксида железа и нанофазного бемита при следующем соотношении компонентов, мас.%: нанофазный гидроксид железа 12-18 нанофазный бемит 5-13 цеолит - остальное. Сорбент позволяет улавливать ионы мышьяка разной валентности, кадмия, меди, свинца и хрома. 1 ил., 3 табл.
Сорбент для очистки воды от ионов тяжелых металлов, состоящий из измельченного цеолита и нанофазного материала, который включает в себя гидроксид железа, отличающийся тем, что сорбент дополнительно содержит нанофазный бемит при следующем соотношении компонентов, мас.%:
| US 6921732 А, 26.07.2005 | |||
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2242276C1 |
| СПОСОБ ЭЛЕКТРОКАТАЛИТИЧЕСКОЙ ОЧИСТКИ ПИТЬЕВЫХ И СТОЧНЫХ ВОД | 2003 |
|
RU2286950C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФИЛЬТРУЮЩЕГО МАТЕРИАЛА ДЛЯ УДАЛЕНИЯ ИОНОВ МАРГАНЦА ИЗ ВОДЫ | 1995 |
|
RU2091158C1 |
Авторы
Даты
2008-07-10—Публикация
2007-01-09—Подача