Изобретение относится к области обработки воды, в частности к способам получения фильтрующего материала, и может быть использовано для деманганации питьевых и сточных вод.
Известен способ получения марганцевого фильтрующего материала [1] состоящий в осаждении MnO2 на поддерживающий слой (силикатный песок, цеолит и так далее) сначала термическим разложением Mn(NO3)2, а затем электролитическим разложением соли марганца. Смесь поддерживающего материала с раствором Mn(NO3)2•6H2O нагревают при 180-280oC для осаждения MnO2 на подложке. 0,5-1,5 мг/л раствора соли марганца (сульфаты, хлориды и так далее) подвергают электролизу при плотности тока 9,3-5 А/дм2 и температуре 80-95oC с применением в качестве анода подложки (песок, цеолит) с осажденной MnO2. Полученный марганцевый материал обладает высокой каталитической активностью и стойкостью, и применяется для удаления из воды ионов железа (II) и марганца (II). Из технической сущности способа следует, что его реализация требует повышенных энерго- и теплозатрат, сложного аппаратурного оформления, что ограничивает широкое использование данной технологии. Кроме того, возможности способа ограничены и его малой производительностью.
Известен способ получения материала для удаления железа и марганца фильтрованием [2] Материал для контактного окислительного фильтрования готовят путем добавки 2%-ного водного раствора KMnO4 к раствору MnCl2 для образования пленки MnO2•H2O на поверхности носителя, например, кремнезема, цеолита. Для повышения прочности сцепления пленки MnO2 с поверхностью носителя добавляют связующий реагент - силикат натрия, нейтрализованный серной кислотой и превращенный в водонерастворимый ангидрид SiO2.
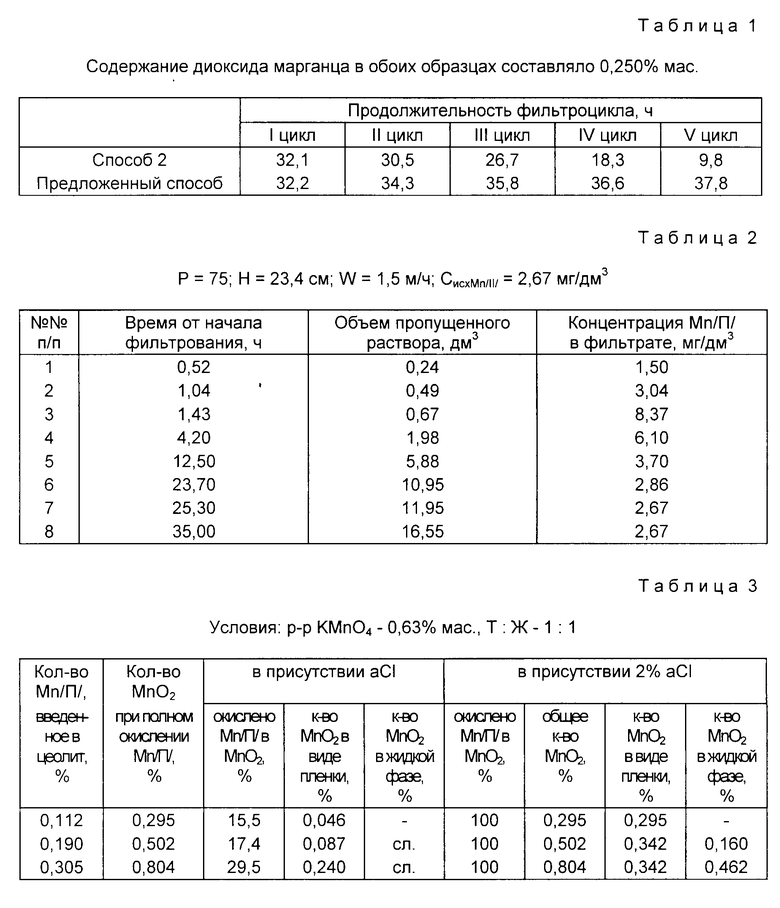
Согласно известной технологии была нанесена пленка MnO2 на поверхность природного цеолита-клиноптилолита Сокирницкого месторождения, с размером частиц 1-3 мм. Через слой загрузки P=75 г и высотой 2,34 дм (диаметр колонки 0,2 дм) пропускали модельную воду с содержанием марганца, равным 2,67 мг/дм3, жесткость и щелочность составляли 2,5 мг-экв/дм3(каждая), pH среды 6,9-7,1. Скорость фильтрования 1,5 м/ч. Фильтрование проводили до содержания в фильтрате 0,1 мг/дм3 марганца (II). На одном образце было проведено 5 циклов фильтрования-регенерации. Данные представлены в табл. 1.
Как следует из представленных в табл. 1 данных, в полученном по способу [2] марганецсодержащем фильтрующем материале пленка MnO2 связана с поверхностью носителя только адгезионными силами, в связи с чем происходит довольно быстрое ее смывание потоком очищаемой воды. Следствием этого является уменьшение продолжительности фильтроцикла в каждом последующем цикле фильтрования-регенерации.
Кроме того, из-за малой дисперсности адгезированных кластеров MnO2 коэффициент использования катализатора невысок, что требует частой регенерации.
Наиболее близким к изобретению по технической сущности является способ получения марганецсодержащего цеолита для удаления ионов железа из воды [R. Aiello, A. Nastro, C. Calella, Effluent and roater treatment Journal, 1978, v. 18, p. 611-617] [3]
В качестве исходных природных цеолитов использовали шабазитсодержащие и клиноптилолитсодержащие туфы зернением 35-50 (0,5-0,3 мм). Для введения марганца в цеолит 5г образца помещали в стеклянные колонки диаметром 20 мм, снабженные пористой перегородкой. Через предварительно промытую загрузку высотой 25 мм пропускали 0,7 дм3 1М раствора MnCl2 (12,6 мас.) со скоростью 0,4 м/ч в течение 5,6 ч (Т:Ж=1:140), и после промывки фильтровали 0,7 дм3 0,5% -ного раствора KMnO4 со скоростью 0,4 м/ч. Содержание катиона Mn(II) в образцах в результате их обработки раствором MnCl2 составило 0,63-0,80 мас. (определено методом атомно-адсорбционной спектроскопии AAS).
Для исследования селективности поглощения ионов железа через марганецсодержащий цеолит в той же колонке пропускали раствор сульфата железа с концентрацией Fe(II) от 1 до 5 мг/дм3 со скоростью 0,8-1,6 м/ч. Время контакта составляло 55-110 с. Жидкость в колонке поддерживалась над загрузкой на высоте 30 мм и не контактировала с кислородом воздуха.
Показано, что полученные материалы способны действовать как Mn-цеолиты - эффективно удаляют ионы железа (II). Однако в материалах [3] отсутствуют данные о возможности использования полученного марганецсодержащего цеолита для удаления из воды ионов марганца. Для определения эффективности Mn-цеолитов в процессе удаления из воды ионов марганца, нами были осуществлены опыты по введению марганца в клиноптилолит согласно известной технологии [3]
В качестве исходного фильтрующего материала использовали природный клиноптилолит Сокирницкого месторождения размером зерен 1-3 мм. В колонку диаметром 0,2 дм загружали 75 г клиноптилолита. Через слой загрузки высотой 2,34 дм (объем клиноптилолита Vкл=7,35•10-2 дм3) пропускали 10,5 дм3 1М раствора MnCl2 (Т:Ж=1:140) со скоростью 6 м/ч в течение 5,6 ч. Затем обработанный солью марганца клиноптилолит отмывали десятью колоночными объемами воды Vпр=0,735 дм3 со скоростью 2,6 м/ч в течение 0,9 ч от избытка соли марганца. Количество Mn(II), введенное обменным путем в образец клиноптилолита, составило 0,63 мас. (472 мг Mn(II) на количество цеолита в колонке). Отмытый клиноптилолит подвергали обработке 10,5 дм3 раствора перманганата калия концентрацией 5 г/дм3 со скоростью 6 м/ч в течение 5,6 ч.
Перманганат калия окисляет Mn(II) до оксида Mn(IV) по реакции: 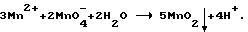 После обработки перманганатом калия визуально наблюдалось почернение зерен клиноптилолита вследствие образования на его поверхности пленки диоксида марганца ("черный" клиноптилолит).
После обработки перманганатом калия визуально наблюдалось почернение зерен клиноптилолита вследствие образования на его поверхности пленки диоксида марганца ("черный" клиноптилолит).
В описании известной технологии [3] не отражена операция отмывки обработанного перманганатом калия образца цеолита. Однако промывка необходима, так как нами показано, что после промывки "черного" клиноптилолита промывные воды содержали большое количество дисперсного осадка MnO2, не связанного с поверхностью клиноптилолита. Это свидетельствует о том, что содержание Mn(II) в образце значительно выше, чем необходимо для образования прочно удерживаемой пленки MnO2 на поверхности зерен клиноптилолита. Промывку вели пятью объемами колонки Vпр=0,368 дм3 со скоростью 2,5 м/ч в течение 0,45 ч, что обеспечивало удаление избытка перманганата калия и свободной двуокиси марганца. Затем отмытый марганецсодержащий клиноптилолит использовали для очистки воды от ионов Mn(II). Опыты проводились в динамических условиях в той же колонке. Массовая концентрация ионов Mn(II) в модельной воде, поступающей на фильтр, была равна 2,67 мг/дм3, жесткость и щелочность составляли 2,5 мг-экв/дм3 (каждая), pH среды 6,9-7,1 (по составу модельная вода аналогична артезианской воде). Воду фильтровали со скоростью 1,5 м/ч. Данные представлены в табл. 2.
Как следует из табл. 2, полученный марганецсодержащий фильтрующий материал не представляется возможным использовать для удаления марганца (II) из воды: концентрация Mn(II) в первой порции составляет 1,5 мг/дм3 и, пройдя через максимум 8,37 мг/дм3, снижается до исходной (2,67 мг/дм3). Позиции 1-8. Это можно объяснить следующим образом. Известный способ обеспечивает получение фильтрующего материала, содержащего пленку диоксида марганца. Однако реализуемые условия обработки цеолита марганецсодержащими реагентами приводят к тому, что введенное в ионообменные позиции минерала количество двухвалентного марганца значительно превышает то количество, которое необходимо для образования прочно удерживаемой пленки диоксида марганца на поверхности цеолита, и при этом остается неокисленным в процессе приготовления. В процессе фильтрования модельной воды, содержащей Mn(II), полученный Mn-цеолит ведет себя как ионообменник, т.е. неокисленный Mn(II), находящийся в обменном комплексе, замещается на ионы Na, Ca, содержащиеся в модельной воде, и вытесняется из Mn-цеолита в фильтрат, что и обуславливает нарастание содержания Mn2+ до 8,37 мг/дм3 за первые 1,5 ч фильтрования. Понижение содержания Mn(II) в фильтрате при последующем фильтровании до исходного содержания Mn(II) в очищаемой воде обусловлено отработкой цеолита как ионообменника при заданных условиях эксперимента (содержание Ca2+ и Na+ ионов, скорость фильтрования).
Таким образом, марганецсодержащий фильтрующий материал, полученный по известному способу [3] не представляется возможным использовать для удаления ионов Mn(II) из воды; при этом способ характеризуется значительными расходами реагентов и промывной воды и большой продолжительностью получения материала.
В основу изобретения поставлена задача усовершенствовать способ получения марганецсодержащего фильтрующего материала путем изменения параметров и условий обработки цеолита марганецсодержащими реагентами, что обеспечило бы формирование каталитически активной пленки диоксида марганца, эффективно удаляющей ионы марганца из воды, а следовательно, привело бы к достижению большой продолжительности фильтроцикла; а также обеспечило бы значительное уменьшение расходов реагентов и промывной воды, сокращение длительности получения пленки диоксида марганца.
Для решения поставленной задачи предложен способ получения фильтрующего материала для удаления ионов марганца из воды, состоящий в обработке природного цеолита последовательно раствором соли двухвалентного марганца до введения в обменный комплекс цеолита 0,090-0,130 мас. марганца (II) от массы цеолита и раствором перманганата калия в присутствии соли щелочного металла. Причем используют 1,0-2,0 мас.-ный раствор соли щелочного металла.
Отличительными признаками предложенного способа являются обработка цеолита раствором соли двухвалентного марганца до введения в обменный комплекс цеолита 0,090-0,130 мас. марганца (II) от массы цеолита и обработка раствором перманганата калия в присутствии соли щелочного металла с использованием 1,0-2,0 мас. раствора соли.
В результате детального исследования процесса получения марганецсодержащего цеолита установлено:
при окислении введенного любого избыточного количества Mn(II) в обменный комплекс цеолита максимальное количество прочно связанной с цеолитом хемосорбированной пленки MnO2 составляет 0,342 мас.
оптимальное количество хемосорбированной пленки MnO2, которое обеспечивает эффективную работу марганецсодержащего цеолита в процессе удаления ионов Mn(II) из воды, составляет 0,250-0,342 мас.
заявляемое количество введенного в обменный комплекс цеолита Mn(II) - 0,090-0,130 мас. и обеспечивает, при условии полного окисления, образование 0,250-0,342 мас. хемосорбированной пленки MnO2;
полное окисление введенного в обменный комплекс цеолита Mn(II) при значительном избытке перманганата калия, обеспечивается только в присутствии соли щелочного металла.
В табл. 3 представлены сопоставительные данные, полученные при окислении Mn(II), введенного в цеолит, в диоксид марганца в присутствии хлорида натрия и в отсутствии указанной соли.
Как следует из табл. 3, полнота окисления Mn(II) в диоксид марганца зависит от участия в процессе окисления соли щелочного металла хлорида натрия. В отсутствии хлорида натрия (условия известного способа 3) только незначительная часть Mn(II) окисляется до MnO2. Неокисленный Mn(II), находящийся в обменном комплексе цеолита, как следует из данных табл. 2, вытесняется в фильтрат при пропускании через марганецсодержащий цеолит воды, содержащей ионы Mn(II) и соли жесткости. При проведении процесса окисления Mn(II) в присутствии хлорида натрия создаются условия, обеспечивающие полное вытеснение марганца (II) из обменного комплекса цеолита и его полное окисление в избытке KMnO4 с образованием хемосорбированной пленки MnO2 и диоксида марганца, не связанного с цеолитом и переходящего в жидкую фазу (условия предложенного способа).
Таким образом, отличительные признаки предложенного способа получения марганецсодержащего фильтрующего материала 0,090-0,130 мас. Mn(II), введенного в обменный комплекс цеолита и окисление Mn(II) в присутствии соли щелочного металла обеспечивает достижение технического результата: получение хемосорбированной каталитически активной пленки MnO2 на цеолите при минимальных затратах реагентов и промывочной воды. Следует отметить, что достигаемая продолжительность фильтроцикла при пропускании марганецсодержащей воды через Mn-цеолит находится на уровне известного способа [2] Однако продолжительность фильтроцикла в известном способе [2] резко уменьшается от цикла к циклу, а в предложенном остается на уровне и даже растет от цикла к циклу (см. табл. 2). Это свидетельствует о получении эффективного фильтрующего материала для удаления Mn(II) из воды.
Способ реализуется следующим образом. Для получения марганецсодержащего фильтрующего материала используют природный цеолит закарпатскую клиноптилолитовую породу Сокирницкого месторождения с содержанием цеолита 60-70 мас. (ТУ 21 УССР 485-90 "Щебень и песок дробленные из цеолитов"). Исходный цеолит фракции 1-3 мкм загружают в колонку и обрабатывают раствором соли двухвалентного марганца массовой концентрации 0,400-0,870 мас. в пересчете на Mn(II) при времени контакта 1,0-1,5 ч и отношении Т:Ж=1:0,7, что соответствует такому объему жидкой фазы, который достаточен для заполнения межзернового пространства загрузки и полного ее покрытия раствором реагента. В качестве соли марганца используют MnCl2 (ГОСТ 612-75), Mn(NO3)2 (ГОСТ 6203-67). Обработанный солью марганца цеолит промывают от избытка соли. Такие условия обработки обеспечивают введение в обменный комплекс цеолита 0,090-0,130 мас. марганца (II) от массы цеолита. Затем загрузку цеолита обрабатывают раствором перманганата калия (ГОСТ 4527-65) с массовой долей 0,3-0,4% содержащего 1-2 мас. соли щелочного металла, при Т:Ж=1:0,7 и времени контакта 1,5-2,0 ч. В качестве солей щелочного металла используют NaCl (ГОСТ 4233-77), KCl (ГОСТ 4234-69).
В результате окисления Mn(II) на поверхности цеолита образуется 0,250-0,342 мас. диоксида марганца. Заключительным этапом является отмывка цеолита, содержащего хемосорбированную пленку диоксида марганца, от избытка перманганата калия.
Методики определения
1. Определение введенного в обменный комплекс клиноптилолита Mn(II)
Навеску воздушно-сухого (сушка при 60oC) клиноптилолита после обработки раствором соли двухвалентного марганца и отмывки водой обрабатывают 3-4 раза раствором хлористого аммония с массовой долей 5% при отношении твердой и жидкой фаз Т: Ж= 1:10 и времени контакта 1,5-2,0 ч. Затем навеску отмывают дистиллированной водой до отрицательной реакции на хлорид-ионы. Собирают вместе маточный раствор и отмывочную воду и доводят до определенного объемного V1. Отбирают аликвотную часть исследуемого раствора V2 и анализ на содержание Mn(II) проводят по ГОСТ 4974-72 "Вода питьевая. Методы определения содержания марганца".
Массовая доля Mn(II), введенного в цеолит определяется по следующей формуле: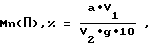
где g навеска анализируемого материала (Mn-цеолита), г;
a массовое количество Mn(II), определенное по стандартной шкале или калибровочному графику, мг;
V1 общий объем раствора, полученный после обработки цеолита NH4Cl и промывки, см3;
V2 объем пробы, взятой для анализа, см3.
2. Определение количества диоксида марганца в модифицированном клиноптилолите
Навеску воздушно-сухого (сушка при 60oC) клиноптилолита (1-2 г), содержащего диоксид марганца, обрабатывают 20 см3 серной кислоты (1:1) с добавлением 2-3 см3 3%-ного раствора перекиси водорода для восстановления Mn(IV) до Mn(II). Если на зернах клиноптилолита остались темные пятна, обработку необходимо повторить. Затем цеолит промывается водой. Маточный раствор и промывные воды собирают в одну емкость. Получают раствор объемом V1. Отбирают от объема V1 пробу объемом V2 для анализа на содержание Mn9II). Анализ проводят по ГОСТ 4974-72 "Вода питьевая. Методы определения содержания марганца".
Массовая доля MnO2 в модифицированном цеолите определяется по следующей формуле: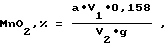
где a массовое количество Mn, найденное по стандартной шкале или калибровочному графику, мг;
g навеска анализируемого цеолита, г;
V1 общий объем раствора, полученный после обработки цеолита H2SO4 и его промывки, см3;
V2 объем пробы, взятой для анализа, см3.
Пример реализации способа
В колонну диаметром 0,2 дм загружают природный цеолит закарпатскую клиноптилолитовую породу Сокирницкого месторождения фракции 1-3 мкм в количестве 75 г. Высота слоя загрузки составляет 2,34 дм, объем клиноптилолита 0,0735 дм3. Загрузку обрабатывают 0,053 дм3 раствора азотнокислого марганца концентрации 0,870 мас. в пересчете на Mn(II) при Т:Ж=1:0,7 и времени контакта 1,5 ч. Обработанный солью марганца клиноптилолит промывают тремя колоночными объемами воды (Vпр=0,220 дм3) со скоростью 1 м/ч в течение 0,27 ч. Согласно анализу, в обменный комплекс клиноптилолита введено 0,130 мас. Mn(II). После промывки загрузку обрабатывают 0,053 дм3 раствора перманганата калия концентрации 0,4 мас. содержащего 2 мас. хлорида натрия. Время контакта 2 ч, Т: Ж= 1: 0,7. Визуально наблюдается почернение клиноптилолита вследствие образования пленки диоксида марганца.
Затем загрузку промывают одним колоночным объемом воды Vпр=0,074 дм3 (что является достаточным для промывки от избытка перманганата калия и хлорида натрия) условия аналогичны промывке от соли Mn(II)).
Анализ полученного марганецсодержащего фильтрующего материала (клиноптилолита) показывает, что он содержит 0,342 мас. MnO2, который находится на поверхности клиноптилолита в виде хемосорбированной пленки.
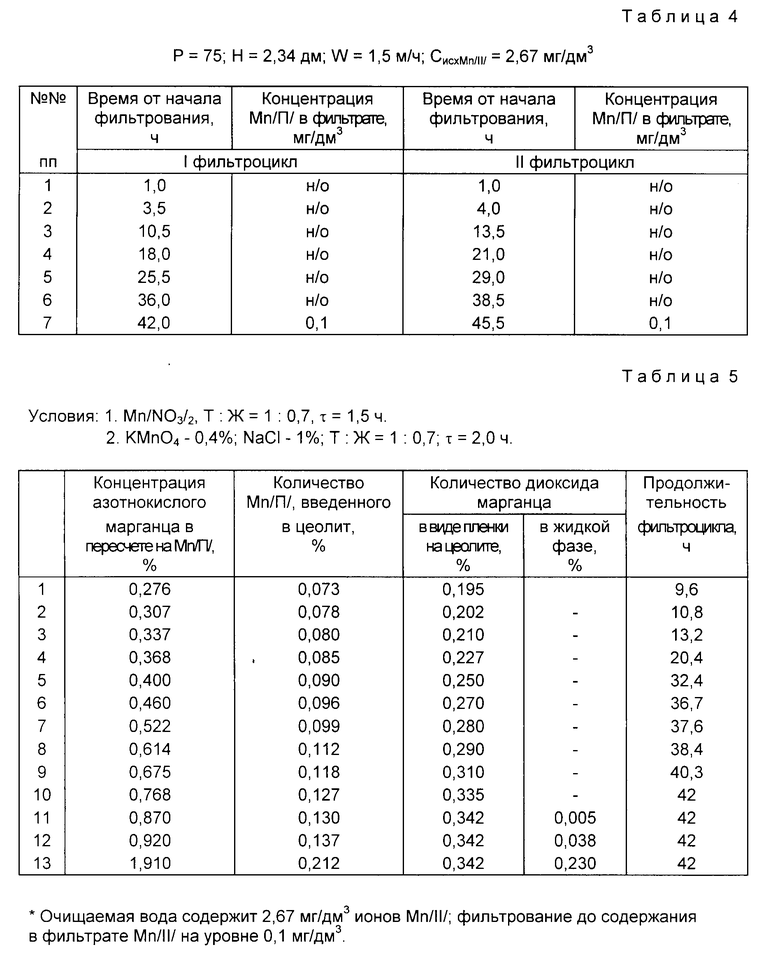
Для определения эффективности полученного модифицированного клиноптилолита через ту же колонку пропускали модельную воду, содержащую 2,67 мг/дм3 ионов Mn(II) при жесткости и щелочности, равных 2,5 мг-экв/дм3, со скоростью 1,5 м/ч. Данные представлены в табл. 4.
Данные табл. 4 показывают, что полученный согласно предложенному способу марганецсодержащий клиноптилолит может быть успешно использован для глубокой очистки воды от марганца (II). При этом продолжительность фильтрования в двух циклах фильтрация регенерация составляет 42,0 и 45,5 ч.
Существенным моментом является количество введенного в обменный комплекс цеолита двухвалентного марганца. Установлено, что заявляемое количество Mn(II) 0,090 0,130 мас. выбрано из условий, обеспечивающих образование в процессе окисления оптимального количества хемосорбированной, каталитически активной пленки диоксида марганца и, следовательно, получение фильтрующего материала, характеризующегося достаточно большой продолжительностью фильтроцикла в процессе очистки воды от ионов марганца (II), составляющей 32,4-42 ч. Это подтверждается данными табл. 5 (примеры 5-11).
При введении в обменный комплекс цеолита двухвалентного марганца в количестве ниже заявляемого предела, например 0,085% хемосорбированная пленка диоксида марганца образуется, но ее количество недостаточно для эффективной работы фильтрующего материала (пример 4).
Вводить двухвалентный марганец в количестве выше заявляемого, например 0,137% и 0,212% является экономически нецелесообразным: количество диоксида марганца, образованное из избыточного количества Mn(II) переходит в жидкую фазу (примеры 12, 13).
В табл. 5 также отражена оптимальная концентрация соли двухвалентного марганца, на примере Mn(NO3)2, обеспечивающая в условиях эксперимента введение заявляемого количества марганца (II) в обменный комплекс клиноптилолита, которая составляет 0,400-0,870 мас. в пересчете на Mn(II).
Необходимым условием полного окисления Mn(II), введенного в обменный комплекс клиноптилолита в заявляемом количестве, при достаточном избыточном окислителя (перманганата калия) является проведение процесса окисления в присутствии соли щелочного металла.
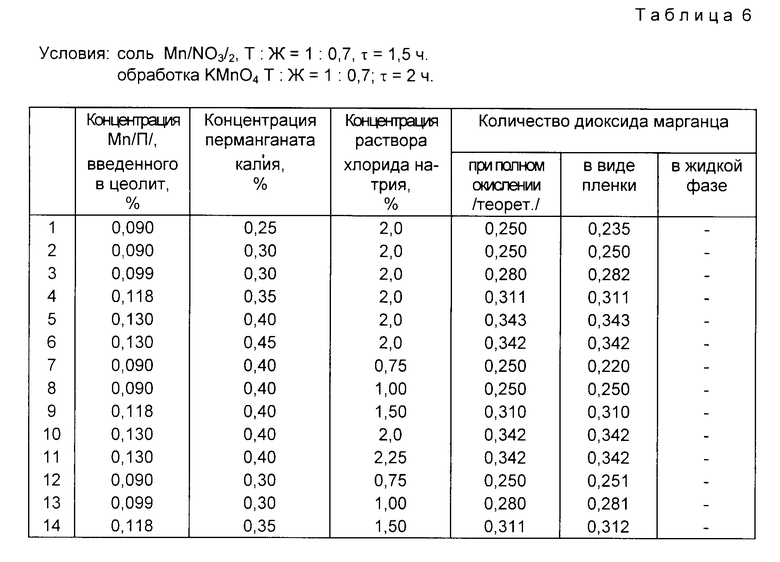
В табл. 6 отражена зависимость степени окисления двухвалентного марганца от концентрации перманганата калия в присутствии различного количества соли щелочного металла. Время контакта 2 ч, Т:Ж=1:0,7.
Как следует из представленных в табл. 6 данных, полнота окисления 0,090-0,130 мас. марганца (II) в диоксид марганца достигается при использовании раствора перманганата калия концентрации 0,30-0,40 мас. (примеры 2-5). При этом концентрация хлорида натрия обеспечивает полное вытеснение Mn(II) из обменного комплекса клиноптилолита и делает доступным его для полного окисления.
При запредельном снижении концентрации перманганата калия, например до 0,25 мас. его количество для окисления всего введенного марганца (II) оказывается недостаточным. В этих условиях пленка диоксида марганца образуется, но в количестве не обеспечивающем эффективную работу фильтрующего материала (пример 1). Верхний предел концентрации перманганата калия ограничен тем, что увеличение концентрации является экономически нецелесообразным, так как приводит к увеличению расхода без получения дополнительного результата (пример 6).
Заявляемая концентрация раствора соли щелочного металла (на примере NaCl) выбрана из условий, обеспечивающих количественное вытеснение 0,090-0,130 мас. двухвалентного марганца из обменного комплекса клиноптилолита в процессе обработки последнего перманганатом калия. В таких условиях происходит образование диоксида марганца в виде хемосорбированной пленки на поверхности клиноптилолита (примеры 8-10, 12-14).
Недостаток соли щелочного металла в процессе окисления, наблюдаемый при запредельном снижении концентрации соли приводит к тому, что часть марганца (II) остается в обменном комплексе и количество образованной пленки диоксида марганца находится за пределами оптимального значения (пример 7). Кроме того, нами показано, что неокисленный марганец переходит в фильтрат в процессе очистки исходной воды.
Запредельное повышение концентрации соли щелочного металла приводит лишь к перерасходу соли при достижении того же результата (пример 11).
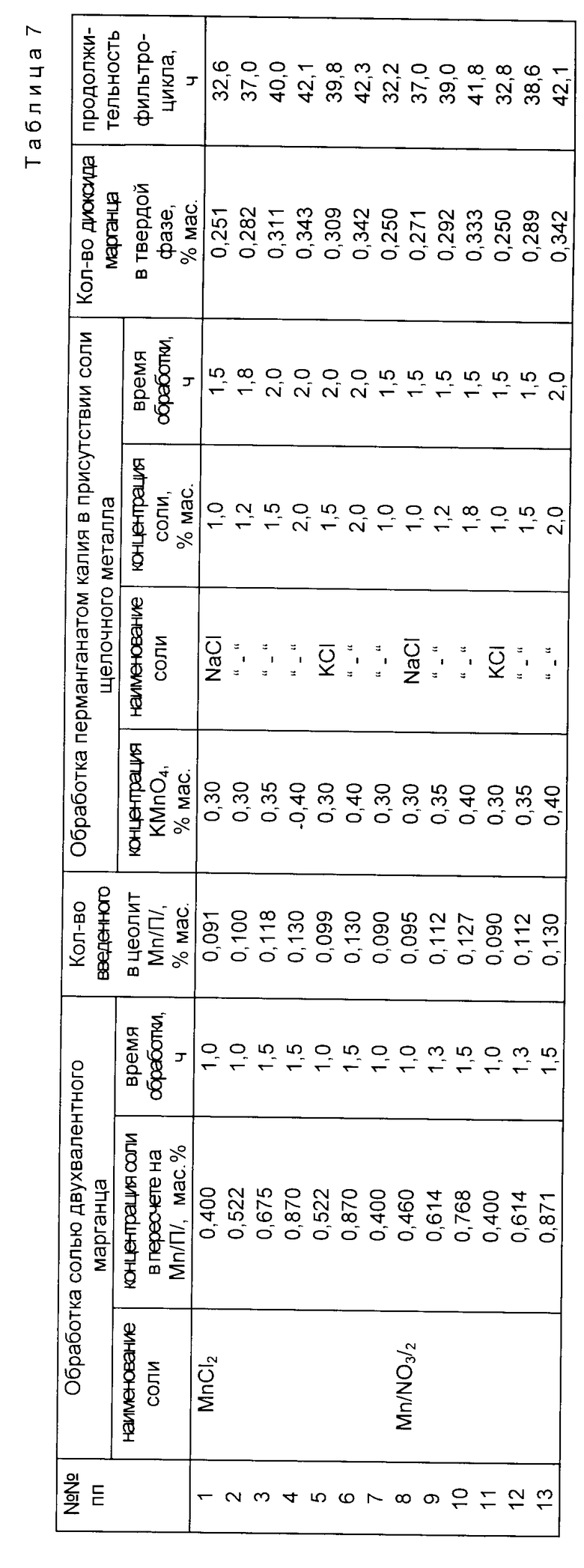
В табл. 7 представлены оптимальные параметры процесса получения марганецсодержащего клиноптилолита предложенным способом, обеспечивающие высокую эффективность фильтрующему материалу в процессе очистки воды от ионов марганца (II), что характеризуется достаточно большей продолжительностью фильтроцикла.
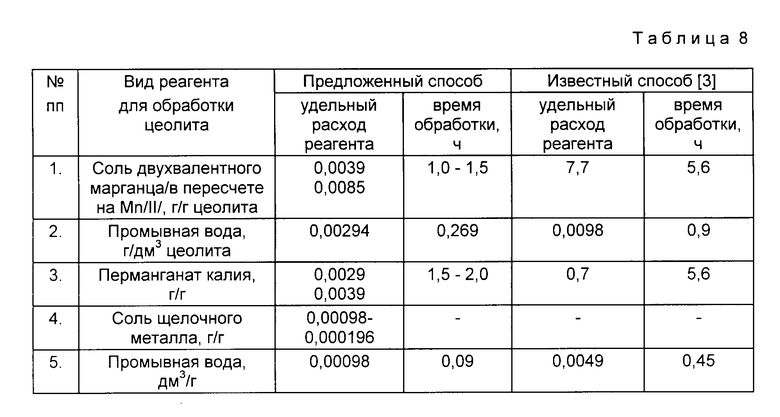
Сравнительные результаты по удельному расходу реагентов в процессе обработки цеолита и промывной воды, а также затраты времени при получении марганецсодержащего фильтрующего материала предложенным и известным способом [3] представлены в табл. 8.
Данные табл. 8 показывают, что предложенный способ получения фильтрующего материала, модифицированного диоксидом марганца, приводит к резкому уменьшению расхода реагентов (в 180-2000 раз) и промывных вод (в 4,5 раза). Следует также отметить, что время получения фильтрующего материала уменьшается в 3 раза.
Преимущества предложенного способа получения марганецсодержащего фильтрующего материала по сравнению с известным состоят в следующем.
Предложенный способ обеспечивает получение фильтрующего материала, модифицированного диоксидом марганца, при использовании которого достигается эффективная очистка воды от марганца (II) при длительности фильтроцикла 32,6-42,3 ч. Как указывалось ранее, фильтрующий материал, полученный по способу [3] невозможно использовать для очистки воды от ионов марганца (II).
Получение эффективного фильтрующего материала предложенным способом обеспечивается значительно меньшим количеством реагентов и промывной воды, чем это требуется в способе [3] удельный расход соли марганца (в пересчете на Mn(II)) уменьшается в 900-2000 раз; перманганата калия в 180-240 раз; промывной воды в 4,5 раза. Длительность процесса получения материала сокращается в 3 раза.
Достоинством фильтрующего материала, полученного предложенным способом, является возможность его использования и для очистки воды от железа (II).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ЖЕЛЕЗО-СЕРЕБРО | 1995 |
|
RU2083331C1 |
| СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДЫ ОТ ОРГАНИЧЕСКИХ ПРИМЕСЕЙ | 1992 |
|
RU2038843C1 |
| СПОСОБ ОЧИСТКИ ВОДЫ ОТ ОРГАНИЧЕСКИХ ВЕЩЕСТВ | 1992 |
|
RU2040481C1 |
| КОМПОЗИЦИЯ ДЛЯ ПОЛУЧЕНИЯ ПОКРЫТИЙ АНОДНЫМ ЭЛЕКТРООСАЖДЕНИЕМ | 1996 |
|
RU2115775C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНЫХ ПОРОШКОВ ЖЕЛЕЗА И ЕГО СПЛАВОВ | 1991 |
|
RU2022060C1 |
| СПОСОБ КОНДИЦИОНИРОВАНИЯ ВОДЫ | 1999 |
|
RU2163892C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФОСФОРА В ВОДЕ | 1991 |
|
RU2024866C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАГНИТНОГО ПОРОШКА МЕТАЛЛОВ И СПЛАВОВ ГРУППЫ ЖЕЛЕЗА | 1992 |
|
RU2041296C1 |
| МАССА ДЛЯ ПОЛУЧЕНИЯ ПОРИСТОГО КЕРАМИЧЕСКОГО МАТЕРИАЛА | 1991 |
|
RU2016877C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНОГО МАГНИТНОГО ПОРОШКА | 1997 |
|
RU2118923C1 |
Изобретение относится к области обработки воды, в частности к способам получения сорбентов, и может быть использовано для деманганации питьевых и сточных вод. Сущность изобретения: способ получения фильтрующего материала состоит в обработке цеолита последовательно раствором соли двухвалентного марганца до введения в обменный комплекс цеолита 0,090-0,130 мас.% марганца (II) от массы цеолита и раствором перманганата калия в присутствии соли щелочного металла концентрации 1-2 мас.%. Полученный фильтрующий материал эффективно очищает воду от марганца (II). Расход реагентов на получение материала уменьшается в 180-2000 раз. 1 з.п. ф-лы, 8 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Патент Японии N 5130387, кл | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент Японии N 4930938, кл | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| R.Aikllo, A.Nastro, C.Calella, Effluent and roater treatment Journal, 1978, v.18, p.611-617. | |||
Авторы
Даты
1997-09-27—Публикация
1995-10-06—Подача