ТЕХНИЧЕСКАЯ ОБЛАСТЬ ИЗОБРЕТЕНИЯ
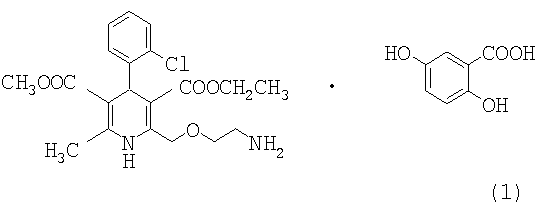
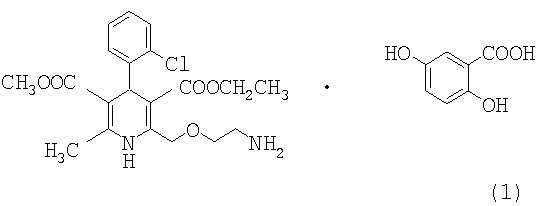
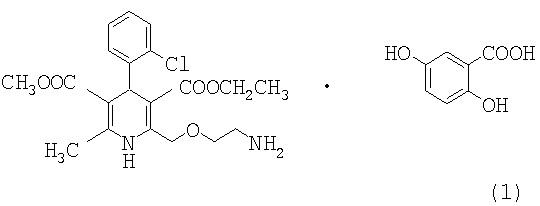
Настоящее изобретение относится к кислотной соли амлодипина гентизату и способу ее получения. Более конкретно настоящее изобретение относится к кристаллической кислотной соли амлодипина гентизату формулы 1, которая полезна для лечения сердечно-сосудистых заболеваний. Амлодипина гентизат, который получают взаимодействием амлодипина и гентизиновой кислоты, обладает преимуществами, заключающимися в низкой токсичности, отличной стабильности, улучшенной фармацевтической эффективности и сохраняющейся на протяжении длительного периода времени концентрации в крови.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Амлодипин представляет собой 3-этил-5-метил-2-(2-аминоэтокси-метил)-4-(2-хлорофенил)-6-метил-1,4-дигидро-3,5-пиридин дикарбоксилат и использовался в лечении ишемических и гипертензивных сердечных заболеваний в качестве блокатора кальциевых каналов. К тому же хорошо известно, что амлодипин представляет собой эффективный и полезный агент вследствие его пролонгированной активности.
Амлодипин впервые был раскрыт как новое соединение 1,4-дигидропиридинов в публикации европейского патента №89167. Этот патент поясняет, что фармацевтически приемлемые соли амлодипина могут быть получены из нетоксичных кислот с фармацевтически приемлемыми анионами, такими как хлорид, бромид, сульфат, фосфат, ацетат, малеат, фумарат, лактат, тартрат, цитрат, глюконат и более предпочтительно малеат.
Свободная форма амлодипина является также фармацевтически приемлемой, но по причине ее низкой стабильности его вводили в форме соли фармацевтически приемлемой кислоты.
Корейский патент №90479 раскрывает четыре физико-химических свойства, которые необходимы для формирования фармацевтически приемлемых солей: (1) высокая растворимость в воде; (2) отличная стабильность; (3) негигроскопичность и (4) технологичность производства препарата в виде таблеток. Однако очень трудно удовлетворить всем четырем требованиям в отношении физико-химических свойств, перечисленным выше, и есть данные, что даже малеатная соль, которая в настоящее время является наиболее предпочтительной фармацевтической формой, распадается в растворе в течение нескольких недель.
Корейский патент №91020 раскрывает, что амлодипина безилат превосходит обычные соли амлодипина и обладает отличной технологичностью в плане приготовления фармацевтического препарата. Однако он был отклонен по соображениям безопасности, так как в процессе производства амлодипина безилата используется бензолсульфоновая кислота, которая является коррозийной и токсичной.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения провели интенсивные и всесторонние исследования для преодоления вышеупомянутых проблем с успешным, в конечном итоге, получением новой кристаллической кислотной соли амлодипина гентизата путем взаимодействия амлодипина с гентизиновой кислотой, относительно менее токсичной органической кислотой по сравнению с бензолсульфоновой кислотой. Амлодипина гентизат обладает низкой токсичностью, превосходной стабильностью в разнообразных условиях, таких как изменения температуры и наличие воды и света, а также превосходным фармацевтическим действием с пролонгированной активностью, удовлетворяя, таким образом, всем требованиям в качестве фармацевтически приемлемой соли.
Таким образом, задачей настоящего изобретения является создание фармацевтически приемлемой кислотной соли амлодипина с отличными физико-химическими свойствами и низкой токсичностью.
В задачу настоящего изобретения также входит предложение способа получения кислотной соли амлодипина гентизата, удовлетворяющей всем требованиям в отношении физико-химических свойств как терапевтически приемлемая соль.
В задачу настоящего изобретения также входит предложение фармацевтической композиции, содержащей кислотную соль амлодипина гентизат в качестве терапевтически активного ингредиента, эффективного в лечении сердечно-сосудистых заболеваний.
ПОДРОБНОЕ ОПИСАНИЕ ВОПЛОЩЕНИЙ
Настоящее изобретение относится к кислотной соли амлодипина гентизату формулы 1, полезной для лечения сердечно-сосудистых заболеваний, которая обладает преимуществами, заключающимися в низкой токсичности, отличной стабильности, улучшенной фармацевтической эффективности и сохраняющейся на протяжении длительного периода времени концентрации в крови.
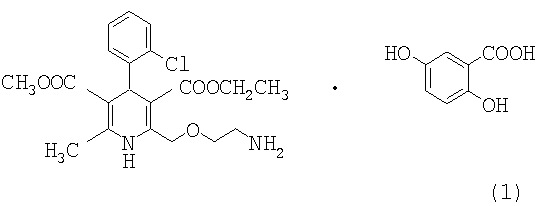
Кислотная соль амлодипина гентизат формулы 1 по настоящему изобретению включает все изомеры амлодипина и их смеси.
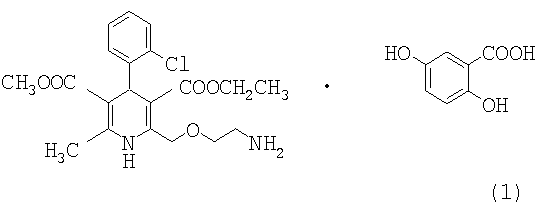
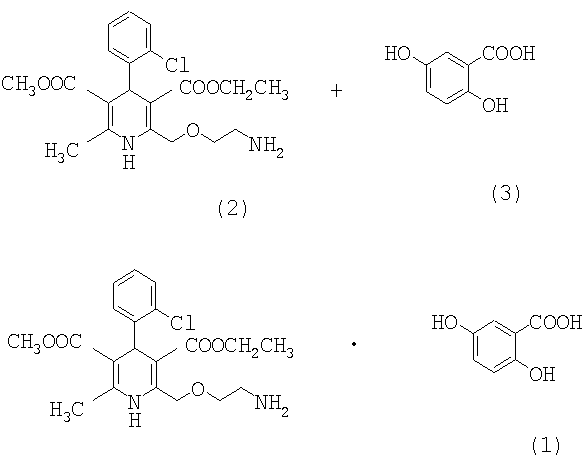
В другом аспекте настоящее изобретение относится к способу получения соли амлодипина гентизата вышеприведенной формулы (1). Соль амлодипина гентизат получают путем взаимодействия амлодипина формулы (2) с гентизиновой кислотой формулы (3) как показано на реакционной схеме 1 ниже.
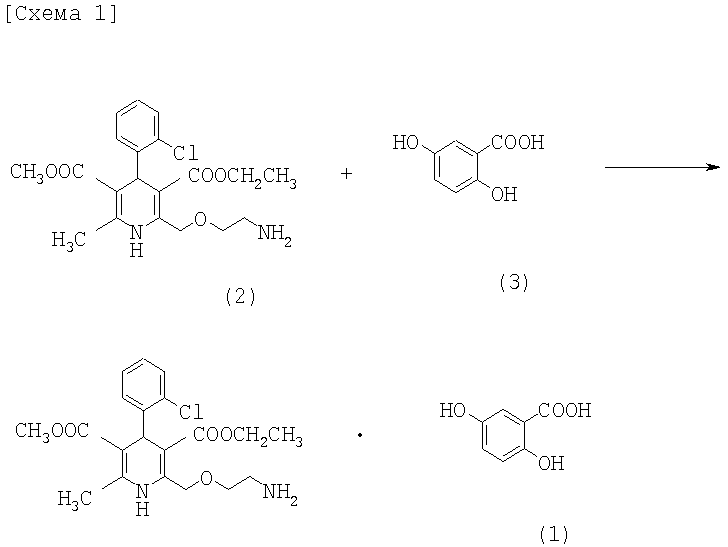
Вышеприведенная реакционная схема получения кислотной соли амлодипина включает следующие стадии:
(1) растворение или суспендирование амлодипина;
(2) растворение гентизиновой кислоты и добавление ее к вышеуказанному раствору амлодипина с получением смеси; и
(3) перемешивание вышеуказанной реакционной смеси и затем фильтрование, промывка и сушка полученных твердых веществ с получением кристаллической кислотной соли амлодипина гентизата.
Как указано выше, кристаллическую кислотную соль амлодипина гентизат по настоящему изобретению получают добавлением гентизиновой кислоты в раствор, содержащий амлодипин вышеуказанной формулы 2. Конкретные детали представлены ниже.
На стадии 1 для эффективного ускорения кристаллизации важна концентрация амлодипина в реакционном растворе, и предпочтительны ее значения в диапазоне от примерно 3 мас.% до примерно 60 мас.%. Может быть использован любой изомер, R-амлодипин или S-амлодипин, или смесь этих изомеров, но более предпочтителен S-амлодипин ввиду его высокой фармацевтической активности.
На стадии 2 предпочтительно использовать соответствующее количество гентизиновой кислоты в диапазоне от примерно 0,1 до примерно 5,0 эквивалентов относительно амлодипина. На стадиях 1 и 2 в качестве реакционного растворителя могут быть использованы вода или любой обычный органический растворитель. Более предпочтительно реакционный растворитель может быть одним из группы, состоящей из воды, метанола, этанола, изопропанола и ацетонитрила, или смесью.
На стадии 3 реакцию образования кристаллической кислотной соли амлодипина гентизата проводят при температуре в интервале от примерно -10 до примерно 60°С.
Известно, что амлодипина гентизат имеет относительно низкую токсичность по сравнению с амлодипина безилатом и обладает всеми физико-химическими свойствами, необходимыми для фармацевтически приемлемой соли (Экспериментальные Примеры 1 и 2). Поэтому настоящее изобретение включает фармацевтическую композицию, которая содержит изомер или смесь изомеров амлодипина гентизата вышеуказанной формулы 1 в качестве активного ингредиента для лечения сердечно-сосудистых заболеваний.
Фармацевтическая композиция по настоящему изобретению может быть изготовлена в виде пероральной или парентеральной лекарственной формы или в виде общеизвестных фармацевтически приемлемых лекарственных форм. В препарате в виде пероральной или парентеральной лекарственных форм могут быть объединены фармацевтически приемлемый наполнитель, разбавитель, связующее вещество, увлажняющий агент, разрыхлитель, поверхностно-активное вещество или эксципиент. Примеры твердых лекарственных форм для перорального введения включают таблетки, гранулы, порошки, капсулы и тому подобное. Такие твердые лекарственные формы могут содержать по меньшей мере один эксципиент, такой как крахмал, сахароза, лактоза и желатин. Дополнительно может быть включено смазывающее вещество, такое как стеарат магния и тальк.
Примеры жидких препаратов для перорального введения включают суспензии, растворы, эмульсии, сиропы и тому подобное, и такие жидкие формы могут содержать разбавитель, такой как вода и водный парафин, и эксципиент, такой как увлажняющий агент, подсластитель, корригент, консервант и другие подобные. Примеры препаратов для парентерального введения включают стерильный водный раствор, неводный раствор, суспензии, эмульсии, лиофилизированный препарат и суппозитории. Для неводных растворов и суспензий могут быть использованы пригодные для инъекций сложные эфиры, такие как этилолеат, и растительное масло, такое как пропиленгликоль, полиэтиленгликоль и оливковое масло. Суппозиторные препараты могут быть получены с использованием основы, такой как витепсол, макрогол, Tween 61, масло какао, лауриновое масло, глицерин-желатин и т.п.
Количество фактически вводимой фармацевтической композиции будет определено в свете сопутствующих обстоятельств, включающих возраст пациента, массу, пол, выбранный путь введения, состояние, подвергаемое лечению, тяжесть симптомов пациента и т.п. Согласно врачебной и фармацевтической практике соединение может быть введено в виде однократной суточной дозы или в виде многократных доз в течение суток. Подходящие дозы амлодипина гентизата составляют 1,0-10,0 мг в сутки в пересчете на амлодипин - основание.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
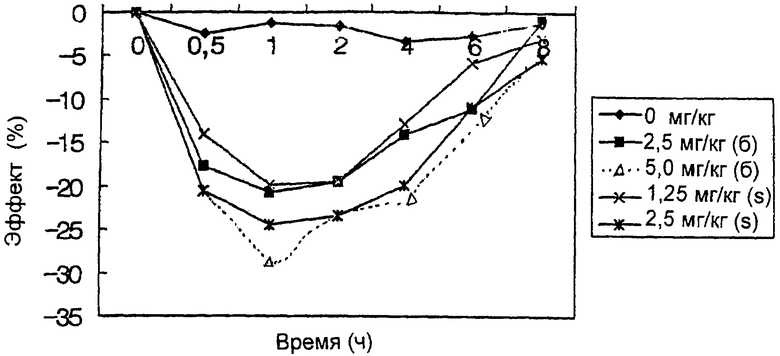
На чертеже показан антигипертензивный эффект соли (±)-амлодипина безилата и S-(-)-амлодипина гентизата.
Примеры
Лучшее понимание настоящего изобретения может быть достигнуто в свете следующих примеров, которые представлены, чтобы служить иллюстрациями, но не должны быть истолкованы как ограничения настоящего изобретения.
Пример 1: Получение соли (R,S)-(±)-амлодипина гентизат
5 г (12,2 ммоль) соли (R,S)-(±)-амлодипина гентизата растворяли в 30 мл этанола и смесь охлаждали до 5°С. Затем 1,88 г (12,2 ммоль) гентизиновой кислоты растворяли в 20 мл этанола и медленно добавляли к вышеуказанному раствору амлодипина. Реакционный раствор перемешивали при комнатной температуре в течение 2 ч. После промывания в 20 мл холодной воды полученное твердое вещество отфильтровывали и подвергали вакуумной сушке при 50°С с получением 6,62 г целевого ярко-желтого кристаллического соединения (выход 96,2%).
Т.пл. 156-159°С; 1Н-ЯМР (300 МГц, ДМСО-d6) δ (м.д.) 7,35-7,12 (m, 5H, ArH), 6,61 (d.d., 1Н), 6,47 (d, 1Н), 5,31 (s, 1Н), 4,74-4,55 (d.d., 2H), 3,99-3,94 (m, 2Н), 3,68 (brt, 2H), 3,50 (s, 3Н), 3,09 (brt, 2H), 2,30 (s, 3Н), 1,10 (t, 3Н).
Пример 2: Получение соли (S)-(-)-амлодипина гентизат
5 г (12,2 ммоль) соли (S)-(-)-амлодипина гектизата суспендировали в 7,5 мл этанола и перемешивали. Затем 1,9 г (12,3 ммоль) гентизиновой кислоты растворяли в 50 мл воды и медленно добавляли к вышеуказанному раствору амлодипина. Реакционный раствор перемешивали при комнатной температуре в течение 2 ч. После промывания в 20 мл холодной воды полученное твердое вещество отфильтровывали и подвергали вакуумной сушке при 50°С с получением 6,61 г целевого ярко-желтого кристаллического соединения (выход 96%).
Т.пл. 162-165°С; 1H-ЯМР (300 МГц, ДМСО-d6) δ (м.д.) 7,35-7,11 (m, 5H, ArH), 6,62 (d.d., 1H), 6,48 (d, 1H), 5,30 (s, 1H), 4,74-4,55 (d.d., 2H), 3,99-3,95 (m, 2H), 3,68 (brt, 2H), 3,50 (s, 3Н), 3,10 (brt, 2H), 2,30 (s, 3Н), 1,10 (t, 3Н); эмпирические значения элементного анализа для С6Н31N2О9Cl: С 57,40%, Н 5,60%, N 4,80%. Расчетное значение: С 57,60%, Н 5,55%, N 4,98%. Хиральная ВЭЖХ (высокоэффективная жидкостная хроматография): 99,9% э.и. (энантиомерный избыток).
Пример 3: Приготовление таблеток, содержащих соль амлодипина гентизат
315 г безводного гидрофосфата кальция и 525 г микрокристаллической целлюлозы (90 мкм) перемешивали и затем переносили в барабан. Далее 70 г соли амлодипина гентизата и 187,5 г микрокристаллической целлюлозы (50 мкм) перемешивали и затем пропускали через сито в вышеупомянутый барабан. Вышеупомянутое сито промывали 525 г микроцеллюлозы (90 мкм). Смесь, полученную после добавления 315 г безводного гидрофосфата кальция к вышеупомянутой смеси, перемешивали в течение 10 мин и затем добавляли к ней 40 г натрия крахмала гликолята и далее перемешивали еще в течение 6 мин. В заключение добавляли 20 г стеарата магния, получившийся продукт перемешивали в течение 3 мин и эту порошковую смесь прессовали обычным способом с формированием таблетки.
Пример 4: Приготовление капсул, содержащих соль амлодипина гентизат
Готовили премикс 525 г микрокристаллической целлюлозы (90 мкм) и сухого кукурузного крахмала. 70 г соли амлодипина гентизата смешивали с частью вышеупомянутого премикса и затем просеивали. Оставшийся премикс перемешивали в течение 10 мин, просеивали и потом перемешивали в течение еще 5 мин. В заключение полученной смесью заполняли капсулы, имеющие размер, подходящий для препарата в виде капсул.
Пример 5: Приготовление инъекционных растворов, содержащих соль амлодипина гентизат
Хлорид натрия растворяли в стерильной воде для инъекций и смешивали с пропиленгликолем. К этой смеси затем добавляли соль амлодипина гентизат с ее растворением и после этого добавляли стерильную воду для доведения раствора до целевой концентрации. В заключение раствор фильтровали через стерильный фильтр и потом заполняли им ампулы для инъекционных препаратов.
Экспериментальный Пример 1: Тест на пероральную токсичность
В таблице 1 представлено сравнение пероральной токсичности бензолсульфоновой кислоты, которая образует кристаллическую кислотную соль амлодипина безилат, и гентизиновой кислоты, которая образует кристаллическую кислотную соль амлодипина гентизат. Данные по бензолсульфоновой кислоте заимствованы из Регистра токсических эффектов химических веществ (Registry of Toxic Effects of Chemical Substances, RTECS).
95, 1962
Исходя из таблицы 1, следует отметить, что сама бензолсульфоновая кислота, которая обычно используется для получения кристаллической кислотной соли амлодипина, демонстрирует более высокую токсичность, тогда как гентизиновая кислота, используемая для получения кристаллической кислотной соли амлодипина в настоящем изобретении, демонстрирует относительно более низкую токсичность по сравнению с токсичностью бензолсульфоновой кислоты.
Экспериментальный Пример 2: Тест на стабильность
Этот эксперимент разработан для подтверждения стабильности соли амлодипина. Достаточно высокая стабильность лекарственного средства важна для возможности изготовления его в той или иной специфической препаративной форме. В частности, для изготовления лекарственного средства в виде таблеток или капсул особенно важно, чтобы оно было стабильно в атмосферных условиях, в то время как стабильность в водной среде более существенна тогда, когда лекарственное средство изготавливают в виде препарата для инъекций.
В следующей ниже таблице 2 представлены результаты мониторинга содержания активных ингредиентов относительно их начальных значений после хранения (±)-амлодипина безилата и (S)-(-)-амлодипина гентизата соответственно при 40°С с относительной влажностью 75% в течение периодов времени 2, 4 и 8 недель, полученные с помощью ВЭЖХ анализа. В следующей ниже таблице 3 представлены результаты такого же мониторинга в условиях 60°С с относительной влажностью 75%.
В Таблице 4 представлены данные по световой стабильности солей амлодипина гентизата по настоящему изобретению в сравнении со световой стабильностью амлодипина безилата; общая доза ультрафиолетового света (УФ) составляла 200 Вт·ч/м2.
Как видно из таблиц 2-4, соль (S)-(-)-амлодипина гентизат обладает лучшей световой стабильностью как в УФ, так и в видимом свете по сравнению со стабильностью обычных солей амлодипина безилата.
Экспериментальный Пример 3: Анализ концентрации активных ингредиентов в крови после перорального введения
Крысам Sprague Dowry, имеющим массу тела 250-270 г, перорально вводили (S)-(-)-амлодипина гентизат и (±)-амлодипина безилат из расчета 10 мг/кг (свободное основание) и брали у них образцы крови, используя обработанную гепарином пипетку, через 0,5, 1, 2, 4, 6 и 8 ч после введения. Образцы крови центрифугировали в течение 2 мин при 14000 об/мин с получением плазмы крови. 80 мкл этой плазмы крови смешивали с 240 мкл метанола, встряхивали на вортексе в течение 10 с и снова центрифугировали в течение 2 мин при 14000 об/мин. Супернатант до анализа хранили при -80°С, а подвижную фазу (35% ацетонитрил/20 мМ KH2PO4) заливали в колонку с обращенной фазой С-18 Capcell-pak, которая соединена с предохранительной колонкой С-18, со скоростью 1,0 мл/мин.
В таблице 5 представлены концентрации активного материала (амлодипина), обнаруженного в крови с течением времени.
Как видно из таблицы 5, (S)-(-)-амлодипина гентизат обнаруживается в наивысшей концентрации в крови после введения крысам в течение физиологически полезного периода времени 4-6 ч после введения, и это значение превышает соответствующее значение для (±)-амлодипина безилата, составляя от него примерно 120%.
Экспериментальный Пример 4: Сравнение фармацевтических эффективностей оптически активного (S)-(-)-амлодипина гентизата и (±)-амлодипина безилата
Этот эксперимент разработан с целью сравнения антигипертензивных активностей солей (S)-(-)-амлодипина гентизата и (±)-амлодипина безилата. Крыс с врожденной гипертензией (SHR, самцы, возраст 13-14 недель) закупали у Charles River Co. (Япония). Крыс оставляли в стабильном состоянии в чистой камере для содержания подопытных животных, в которой поддерживали постоянную температуру 22,5±1°С и влажность 55±5% при автоматическом регулировании освещения каждые 12 ч, и после этого вводили в эксперимент. Использовали таких SHR, которые имели систолическое кровяное давление 170 мм рт.ст. или выше, и каждая экспериментальная группа состояла из 8 крыс. Кровяное давление измеряли косвенным методом ("tail-cuff"), используя Multichannel 8000 (TSE Co., Германия). Для облегчения измерений крыс помещали в контейнер, выдерживали при 37°С в течение 10 мин и вводили им перорально 5 мг/кг тестируемого вещества после растворения его в дистиллированной воде (1,0 мл/100 г массы крысы). Измерения кровяного давления проводили соответственно через 2, 4, 6, 8, 10 и 24 ч после введения. Результаты измерений указаны в СКО (средняя квадратичная ошибка). Статистический анализ измерений проводили с использованием программы Sigma Stat (Jandel Co., США) в отношении непарного t-теста и однофакторного дисперсионного анализа (ANOVA), а вторую оценку проводили с помощью теста множественных сравнений Дунетта. Результаты измерений антигипертензивных активностей солей (S)-(-)-амлодипина гентизата и (±)-амлодипина безилата у крыс с врожденной гипертензией представлены на чертеже и в таблицах 6 и 7.
В обеих группах крыс, которым перорально вводили соли (±)-амлодипина безилат (таблица 6) и (S)-(-)-амлодипина гентизат (таблица 7), имел место дозозависимый антигипертензивный эффект, и очень сходные тенденции к снижению кровяного давления также проявлялись во всех экспериментальных группах. Оба тестируемых вещества начинали демонстрировать значительный уровень снижения кровяного давления через 30 мин после введения, и уровень снижения достигал пика через 1 ч после введения. Значительный антигипертензивный эффект сохранялся вплоть до 6 ч после введения. В частности, соли оптически активного (S)-(-)-амлодипина гентизата продемонстрировали уровень антигипертензивного действия, сходный с этим показателем у солей (±)-амлодипина безилата, при их использовании всего лишь в половинной дозе. Так, максимальный антигипертензивный эффект солей (±)-амлодипина безилата составил 20,8±7,3% при дозировке 2,5 мг/кг, в то время как максимальный антигипертензивный эффект солей оптически активного (S)-(-)-амлодипина гентизата составил 19,8±5,5% при дозировке 1,25 мг/кг, что составляет только половину дозировки солей (±)-амлодипина безилата. Более того, при дозировке 5 мг/кг максимальный антигипертензивный эффект солей (±)-амлодипина безилата составил 28,6±7,5%, при этом максимальный антигипертензивный эффект солей оптически активного (S)-(-)-амлодипина гентизата составил 24,5±7,9% при дозировке 2,5 мг/кг.
Следовательно, было показано, что соли как (±)-амлодипина безилата, так и (S)-(-)-амлодипина гентизата демонстрируют дозозависимый антигипертензивный эффект. Более того, из того результата, что соли оптически активного (S)-(-)-амлодипина гентизата могут проявлять сходный уровень антигипергензивного действия при их использовании в дозировке, составляющей половину от количества солей (±)-амлодипина безилата, можно заключить, что антигипертензивный эффект солей оптически активного (S)-(-)-амлодипина гентизата в два раза превосходит эффект солей (±)-амлодипина безилата.
Как установлено выше, амлодипина гентизат по настоящему изобретению представляет собой кристаллическую кислотную соль амлодипина, пригодную для фармацевтических препаратов, при этом в нем используется менее токсичное вещество - гентизиновая кислота, в отличие от типичных солей амлодипина безилата с высокотоксичным веществом - бензолсульфоновой кислотой, и тем не менее удовлетворяет всем физико-химическим требованиям, которые по меньшей мере эквивалентны таковым амлодипина безилата, и в связи с этим является полезным в качестве фармацевтического вещества для лечения сердечно-сосудистых заболеваний.
Данное изобретение описано в деталях относительно его предпочтительных воплощений. Однако авторы будут признательны специалистам в данной области, которые по рассмотрению данного раскрытия, могут внести изменения и улучшения в рамках и в духе настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| (S)-(-)-АМЛОДИПИНА КАМЗИЛАТ ИЛИ ЕГО ГИДРАТ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИХ | 2007 |
|
RU2403241C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОГО ГЕНТИЗАТА АМЛОДИПИНА | 2006 |
|
RU2393150C2 |
| КАМЗИЛАТ АМЛОДИПИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2002 |
|
RU2241701C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ГИПЕРТЕНЗИИ | 2011 |
|
RU2571284C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ИНГИБИТОР РЕНИНА, БЛОКАТОР КАЛЬЦИЕВЫХ КАНАЛОВ И ДИУРЕТИК | 2003 |
|
RU2316318C2 |
| СОЛЬ АЛИСКИРЕНА И СЕРНОЙ КИСЛОТЫ | 2007 |
|
RU2439054C2 |
| СОЛЬ АЛИСКИРЕНА И ОРОТОВОЙ КИСЛОТЫ | 2007 |
|
RU2456267C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГИПЕРТЕНЗИИ ИЛИ ПОВЫШЕННОГО КРОВЯНОГО ДАВЛЕНИЯ | 2010 |
|
RU2539382C2 |
| КОМБИНИРОВАННЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ НА ОСНОВЕ ТЕОРИИ ХРОНОТЕРАПИИ | 2007 |
|
RU2464014C2 |
| КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ АМЛОДИПИН И ЛОЗАРТАН, ИМЕЮЩАЯ УЛУЧШЕННУЮ СТАБИЛЬНОСТЬ | 2013 |
|
RU2628538C2 |
Изобретение относится к кислотной соли амлодипина гентизату формулы 1
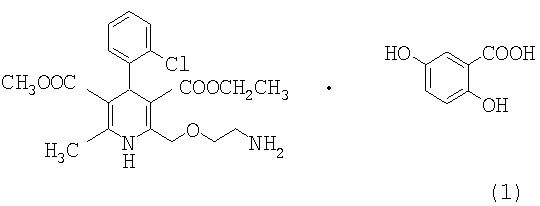
Изобретение также относится к способу получения амлодипина гентизата формулы 1 и к фармацевтической композиции. Технический результат - получение кислотной соли амлодипина гентизата формулы 1, полезной для лечения сердечно-сосудистых заболеваний. 3 н. и 8 з.п. ф-лы, 7 табл.
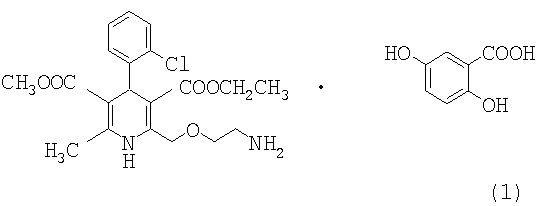
| Самовсасывающий центробежный насос | 1950 |
|
SU89167A1 |
| РАБОЧИЙ ОРГАН РОТОРНОГО ЭКСКАВАТОРА | 0 |
|
SU244944A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| RU 99121192 А, 27.09.2001. | |||
Авторы
Даты
2008-08-10—Публикация
2004-12-15—Подача