Область техники
Настоящее изобретение относится к новым веществам, а именно к оптическим изомерам (+)- и (-)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индола, способам их получения и использования на основе выявленной терапевтической активности ноотропного и седативного действия.
Предшествующий уровень техники
Известны производные гексагидро-гамма-карболина 8-алкил-2-[гамма-(р-фторбензоил)-пропил]-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индолы и их фармацевтически приемлемые соли (US 3983239, В1), проявляющие свойства депрессантов центральной нервной системы, способные ослаблять стереотипию, вызванную амфетамином, и являющиеся нейролептиками.
Известен 3,6-диметил-1,2,3,4,4а,9а-гексагидро-γ-карболина дигидрохлорид, имеющий фармакологическую активность, и препарат на его основе, получивший международное непатентуемое название «дикарбин» (US 3657254, В2). Описано психотропное действие препарата «дикарбин» и его выраженные нейролептические, антидепрессивные и активизирующие эффекты, которые проявляются только в зависимости от синдромов расстройств и состояния пациента, и терапевтический эффект зависит от дозы и продолжительности введения препарата.
Известен способ получения дикарбина (US 3657254, В1), включающий восстановление 3,6-диметил-1,2,3,4,4а,9а-гексагидро-γ-карболина гидрохлорида в водной кислой среде при температуре до 100°С, последующее подщелачивание реакционной смеси и выделение полученного основания 3,6-диметил-1,2,3,4,4а,9а-гексагидро-γ-карболина, обработку его соляной кислотой и выделение целевого продукта, в котором в качестве восстановителя предпочтительно используют амальгамированный цинк или олово. Согласно этому способу получают цис-изомер дикарбина, в котором атомы водорода 4а и 9b присоединены к атомам углерода в цис-положении.
Известно, что 2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол, получивший фармакологическое наименование «дикарбин», проявляет активность депрессанта центральной нервной системы и одновременно двухфазную активность по отношению к эффектам амфетамина и антагонизм по отношению к стереотипии, вызванной амфетамином (Psychopharmacologia, Vol.21, 1971, pages 82-88).
Известны фармакологические свойства, в частности антиаритмическая активность и антиоксидантные свойства, пиридоиндола «Стобадин», представляющего собой оптический изомер цис-дикарбина (L.Horakova and S.Stole. Antioxidant Pharmacodynamic Effects of Pyridoindole Stobadine. General Pharm., V.30, Issue 5, pages 627-638).
Известен способ селективного синтеза рацемического цис-дикарбина путем каталитического гидрирования соответствующего γ-карболина (L.Benes, S.Stole. Drugs of the Future. 1989, Vol.14, №2, p.135-137). При этом рацемический цис-дикарбин был разделен на оптические изомеры кристаллизацией его солей с (+)- и (-)-дибензоилвинными кислотами.
Известен рацемический транс-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол гидрохлорид, имеющий атомы водорода 4а и 9b в транс-положении и используемый в качестве анальгетика и седативного препарата. Он также используется в качестве большого транквилизатора, обладающего антипсихотическим действием, или малого транквилизатора, обладающего анксиолитическим действием, релаксанта, гипотензивного средства (US 3991199, B2).
Известен способ получения 2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола (2,8-диметил-γ-карболина) (Яхонтов Л.Н., Глушков Р.Г. Синтетические лекарственные средства. Медицина. 1983, с.234-237) восстановлением 2,8-диметил-γ-карболина цинковой пылью. С помощью этого способа синтеза получали смеси рацематов цис- и транс-изомеров дикарбина с преобладанием цис-изомера.
Известен способ селективного получения рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола гидроборированием 2,8-диметил-γ-карболина комплексом BF3·Et2O (Y.Nagai et al. Journal of Medicinal Chemistry. 1979, Vol.22, №6, 677-683).
Однако указанные выше активные вещества являются рацемическими смесями оптических изомеров, терапевтическая активность которых может быть различна, что при применении рацемических смесей может приводить к возникновению побочных эффектов, в частности при использовании комбинированной терапии ноотропными и седативными препаратами, использование которых должно быть строго дозировано.
Известные способы получения указанных активных веществ не позволяют выделить индивидуальные оптические изомеры из рацемата транс-изомера и в полной мере проявиться уникальным фармакологическим свойствам оптических (+)- и (-)-изомеров транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индола, которые могут заключаться в различном сочетании их терапевтического эффекта.
Раскрытие изобретения
Целью создания изобретения было получение из известной рацемической смеси индивидуального вещества, обладающего индивидуальной терапевтической эффективностью.
При создании изобретения была поставлена задача разделения изомера транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, используемого в терапии в качестве анальгетика и седативного препарата и имеющего атомы водорода 4а и 9b в транс-положении, на его оптические изомеры с получением индивидуальных оптических изомеров (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Кроме того, была поставлена задача определения индивидуальной терапевтической эффективности каждого из указанных оптических изомеров и возможностей их применения в терапии.
Поставленная задача была решена разработкой способа получения индивидуальных оптических изомеров (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола согласно изобретению, в котором осуществляют взаимодействие 2,8-диметил-гамма-карболина с боргидридом натрия и с эфиратом трехфтористого бора, обработку соляной кислотой, затем подщелачивают реакционную смесь, выделяют свободное основание рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, проводят кристаллизацию его солей с (+)-дибензоилвинной кислотой из этанола с получением индивидуальных солей (+)-транс-изомера, выделяют из полученных индивидуальных солей свободное индивидуальное основание (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, затем остаток переводят в свободное основание рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, проводят кристаллизацию его солей с (-)-дибензоилвинной кислотой из этанола с получением индивидуальной соли (-)-транс-изомера и выделяют свободное индивидуальное основание (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Поставленная задача была решена выделением нового вещества, представляющего собой оптический изомер (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол с положительным оптическим вращением, в котором атомы водорода в положениях 4а и 9b находятся в транс-положении, имеющий структурную формулу:
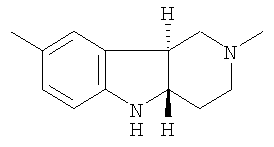
Поставленная задача была также решена выделением нового вещества, представляющего собой оптический изомер (-)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индол с отрицательным оптическим вращением, в котором атомы водорода в положениях 4а и 9b находятся в транс-положении, имеющий структурную формулу:
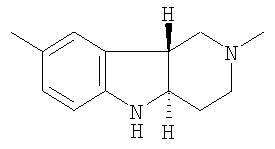
Поставленная задача была также решена созданием фармацевтической композиции ноотропного и седативного действия, содержащей в качестве активного ингредиента оптический изомер (+)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индол и/или его фармакологически приемлемую соль в эффективном количестве.
Поставленная задача была также решена созданием фармацевтической композиции ноотропного и седативного действия, содержащей в качестве активного ингредиента оптический изомер (-)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индол и/или его фармакологически приемлемую соль в эффективном количестве.
Изобретение в дальнейшем иллюстрируется примерами его осуществления, которые, однако, не ограничивают возможные варианты его осуществления.
Лучший вариант осуществления изобретения
А. Получение оптических изомеров (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Получение осуществляли способом согласно изобретению в две стадии следующим образом.
1. Получение рацемического изомера транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Известно, что рацемический транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол представляет собой смесь двух оптических изомеров, в которых атомы водорода в положениях 4а и 9b находятся в транс-положении, а углы вращения противоположны: положительное вращение для (+)-транс-изомера и отрицательное вращение для (-)-транс-изомера:
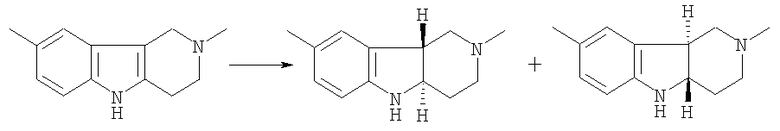
К охлаждаемому льдом раствору 2,8-диметил-γ-карболина (20 г, 0.1 моль) в ТГФ (300 мл) добавили тонко измельченный порошок боргидрида натрия (7.6 г, 0.2 моль) и затем при хорошем перемешивании и в атмосфере инертного газа постепенно, в течение часа, добавили раствор эфирата трехфтористого бора (48% BF3) (38 г, 0.27 моль) в тетрагидрофуране (ТГФ). После добавления всего количества BF3 реакционную массу перемешивали в течение 30 минут при комнатной температуре, а затем кипятили 4 часа.
После охлаждения к реакционной массе добавляли 6N-раствор HCl (150 мл) и упаривали ТГФ под вакуумом. К полученному раствору добавили диоксан (150 мл), кипятили 1 ч, затем упаривали. Остаток подщелачивали раствором щелочи NaOH и экстрагировали CHCl3.
По данным ТСХ, полученное вещество представляет собой свободное основание транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, содержащее небольшую, менее 10%, примесь цис-изомера, которая была отделена при кристаллизации. Для отделения цис-изомера полученная смесь была превращена в смесь дигидрохлоридов цис- и транс-изомеров действием спиртового раствора HCl, а последующая кристаллизация дигидрохлорида транс-изомера из этанола позволила освободиться от примеси дигидрохлорида цис-изомера. Подщелачивание дигидрохлорида рацемического транс-изомера и последующая экстракция привели к получению индивидуального основания рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Полученный продукт был исследован методами ТСХ и ЯМР. Аналитическую ТСХ проводили на пластинках Kieselgel 60 F254 (Merck).
По результатам исследований полученных веществ:
- для рацемического транс-изомера Rf=0,33 (система петролейный эфир-этилацетат-триэтиламин, 3:1:0.1);
- для цис-изомера (дикарбина) Rf=0,39 (в той же системе).
При этом по данным ТСХ и ЯМР полученный цис-изомер был идентичен известному образцу цис-изомера, полученному описанным в литературе методом (Яхонтов Л.Н., Глушков Р.Г. Синтетические лекарственные средства. Медицина, 1983, стр.234-237).
Общий выход основания транс-изомера составил около 70%, и его использовали для получения индивидуальных оптических изомеров.
Для полученных продуктов:
a) температуры плавления, измеренные на приборе Buchi SMP-20 и не исправленные:
- температура плавления Тпл дигидрохлорида рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола составляет 258-260°С;
- температура плавления Тпл свободного основания транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола составляет 83-87°С.
b) хроматографическая подвижность (Аналитическую ТСХ проводили на пластинках Kieselgel 60 F254 (Merck)):
- для транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола Rf=0.43 (система хлороформ-метанол-триэтиламин, 10:1:0.1);
- для цис-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола (дикарбина) в этой же системе Rf=0.35.
2. Разделение рацемического изомера транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола на оптические изомеры (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
К раствору 10 г рацемического транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола основания в 150 мл этанола добавляли эквимолярное количество (+)-дибензоилвинной кислоты (18.61 г). Через некоторое время выпадал кристаллический осадок соли, обогащенной (+)-транс-изомером.
Далее этот осадок несколько раз перекристаллизовывали из этанола, пока не добились конечного угла вращения, измеренного с помощью поляриметра Perkin-Elmer 241: для свободного основания [α]D 20+58° (Cl, CHCl3), для дигидрохлорида [α]20 D +7° (Cl, Н2О). Свободное основание (+)-транс-изомера получали подщелачиванием раствора соли с помощью раствора NaOH с последующей экстракцией эфиром и упариванием.
Затем маточный раствор после выделения соли (+)-изомера подщелачивали добавлением раствора щелочи, свободное основание выделяли экстракцией эфиром и после упаривания в вакууме получали вещество, представляющее собой смесь оснований, обогащенную (-)-изомером транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола. К этой смеси в 150 мл этанола добавляли эквимолярное количество (-)-дибензоилвинной кислоты. Через некоторое время выпадал кристаллический осадок соли, обогащенный (-)-транс-изомером.
Далее этот осадок несколько раз перекристаллизовывали из этанола, пока не добились конечного угла вращения, измеренного с помощью поляриметра Perkin-Elmer 241: для свободного основания [α]D 20-58° (Cl, CHCl3), для дигидрохлорида [α]20 D-10° (Cl, Н2O).
Спектры ЯМР для оптических изомеров регистрировали на приборе Varian-400 VXR, с рабочей частотой 400 МГц (1Н ЯМР) и 100,6 МГц (13С ЯМР). Химические сдвиги были измерены с использованием остаточных растворителей в качестве внутренних стандартов.
Полученный (+)- транс-изомер и его соль дигидрохлорид характеризуются:
- свободное основание: брутто формула C13H17N2; угол вращения [α]20 D+58° (Cl, CHCl3);
- дигидрохлорид: брутто формула C13H18N2·2HCl; угол вращения [α]20 D+7° (Cl, Н2O).
Молекулярный вес 276,1.
Полученный (-)-транс-изомер и его соль дигидрохлорид характеризуются:
- свободное основание: брутто формула C13H17N2; угол вращения [α]20 D-58° (Cl, CHCl3);
- дигидрохлорид: брутто формула C13H18N2·2HCl; угол вращения [α]20 D-10°(Cl, Н2O).
Молекуляный вес 276,1.
Для исследуемых веществ (+)- и (-)-транс -изомеров ЯМР-спектры совпадают:
1Н ЯМР-спектр (CDCl3): 1,92 (мультиплет, 2Н); 2.08 (мультиплет, 2Н); 2.19 (синглет, 3Н); 2,34 (синглет, 3Н); 2.80 (дублет триплетов, 1Н); 2.94 (мультиплет, 2Н); 3.37 (дублет дублетов, 1Н); 3.89 (широкий синглет, 1Н); 6.58 (дублет дублетов, 1Н); 6.78 (синглет, 1Н); 6.79 (дублет, 1Н) м.д.;
13С ЯМР-спектр: 20.76; 30.98; 45.83; 47.35; 54.27; 57.02; 67.98; 110.25; 122.77; 127.36; 128.63; 131.07; 149.10 м.д.
В. Исследование биологической активности индивидуальных оптических изомеров (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола.
Были исследованы предполагаемые фармакологические свойства веществ, являющихся оптическими (+)- и (-)-изомерами транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, при их индивидуальном применении.
Доклиническую оценку ноотропной и седативной активности указанных веществ осуществляли на мышах по тесту спонтанной ориентации (поведения патрулирования) в крестообразном лабиринте, который позволяет одновременно выявлять ноотропное, транквилизирующее, седативное и психостимулирующее действие веществ.
Для оценки исследовательского поведения животных использовали закрытый крестообразный лабиринт (Салимов P.M. Оценка упорядоченности пути в процессе исследовательского поведения у мышей. Журнал высшей нервной деятельности, 1988. Т.38. №3, с.569-571).
Мышь помещали в центральный отсек лабиринта и в полуавтоматическом режиме регистрировали последовательность ее переходов из одного рукава в другой.
Тест заканчивался, когда происходило 12 таких переходов (Салимов P.M. Оценка упорядоченности пути в процессе исследовательского поведения у мышей. Журнал высшей нервной деятельности, 1988, Т. 38, №3, с.569-571; Salimov R.M., McBride W.J., Sinclair J.D., Lumeng L., Li T.-K. Performance in the cross-maze и slip funnel tests of four pairs of rat lines selectively bred for divergent alcohol drinking behavior. Addict. Biol. 1996a, 1:273-280; Salimov R.M., McBride W.J., McKenzie D.L., Lumeng L. и Li T.-K. Ethanol consumption by adolescent alcohol-preferring P rats on subsequent behavioral performance in the cross-maze и slip funnel tests. Alcohol. 1996b, 13: с.297-300).
Последующий компьютерный анализ записи позволял выделить ряд показателей поведения. Наиболее информативными из них были следующие:
1) общее время, проведенное мышью в центральном отсеке лабиринта, - показатель T_ChTm, и общее время, проведенное мышью в боковых отсеках лабиринта, - показатель T_GlTm.
Эти показатели отражают уровень двигательной активности животного, а также характеризуют интенсивность обследования ими новой среды и могут быть использованы для оценки стимулирующего/тимолептического или, наоборот, седативного эффекта веществ (Salimov R.M., McBride W.J., McKenzie D.L., Lumeng L. и Li T.-K. Ethanol consumption by adolescent alcohol-preferring P rats on subsequent behavioral performance in the cross-maze и slip funnel tests. Alcohol. 1996b, 13:297-300); Salimov R.M.; Salimova N.B.; Shvets L.N.; Maisky A.I. Haloperidol administered subchronically reduces the alcohol-deprivation effect in mice. Alcohol. 20:61-68; 2000; Markina N.V., Salimov P.M., Poletaeva I.I. Exploratory behaviour of F2 crosses of mouse lines having selected for different brain weight: A multivariate analysis. Prog. Neuro-Psychopharmacol. Biol. Psychiat. 2004, 28(3):583-589);
2) латентный период - показатель F_ChTm, и продолжительность первого визита в боковой отсек - показатель F_GlTm.
Эти показатели отражают уровень тревожности животного в новой обстановке и могут быть использованы для оценки транквилизирующего (анксиолитического) эффекта веществ (Salimov R.M. Different behavioral patterns related to alcohol use in rodents: A factor analysis. Alcohol. 1999, 17:157-162).
Эти показатели отрицательно коррелируют с продолжительностью пребывания животного в открытых рукавах в общеизвестном тесте открытого приподнятого крестообразного лабиринта, что позволяет использовать избирательное изменение этих показателей в качестве индикатора тревожности и, следовательно, применять их для оценки транквилизирующего действия веществ (Салимов P.M., Маркина Н.В., Перепелкина О.В., Майский A.M., Полетаева И.И. Быстрая толерантность к этанолу и добровольное потребление больших доз алкоголя у мышей, селектированных по весу мозга. Журн. высшей нервной деятельности. 2003, т.53, №1, с.100-106; Salimov R.; Salimova N.; Shvets L.; Shvets N. Effect of chronic piracetam on age-related changes of cross-maze exploration in mice. Pharmacol. Biochem. Behav. 1995, 52:637-640; Salimov R.M., McBride W.J., Sinclair J.D., Lumeng L., Li T.-K. Performance in the cross-maze и slip funnel tests of four pairs of rat lines selectively bred for divergent alcohol drinking behavior. Addict. Biol. 1996a, 1:273-280; Salimov R.M., McBride W.J., McKenzie D.L., Lumeng L. и Li T.-K. Ethanol consumption by adolescent alcohol-preferring P rats on subsequent behavioral performance in the cross-maze и slip funnel tests. Alcohol. 1996b, 13:297-300; Salimov R.M. Different behavioral patterns related to alcohol use in rodents: A factor analysis. Alcohol. 1999, 17:157-162; Маркина Н.В., Попова Н.В., Салимов P.M., Салимова Н.Б., Савчук Н.Б., Полетаева И.И. Сравнение уровня тревожности и стресс-реактивности мышей, селектированных на большой и малый вес мозга // Журнал высшей нервной деятельности. 1999. Т.49. №5. С.789-798);
3) "длина" первого цикла патрулирования - показатель F_PtrN, и длина второго цикла патрулирования - показатель S_PtrN.
Эти показатели исчисляют числом заходов животного в отсеки лабиринта, совершенных им для обследования обстановки до момента, когда животное побывает во всех четырех отсеках лабиринта, хотя бы один раз (Салимов P.M. Оценка упорядоченности пути в процессе исследовательского поведения у мышей. Журн. высш. нервн. деят. 1988. Т.38. №3. С.569-571; Salimov R.M., McBride W.J., Sinclair J.D., Lumeng L., Li T.-K. Performance in the cross-maze и slip funnel tests of four pairs of rat lines selectively bred for divergent alcohol drinking behavior. Addict. Biol. 1996a, 1:273-280; Salimov P.M., McBride W.J., McKenzie D.L., Lumeng L. и Li T.-K. Ethanol consumption by adolescent alcohol-preferring P rats on subsequent behavioral performance in the cross-maze и slip funnel tests. Alcohol. 1996b, 13:297-300; Markina N.V., Salimov R.M., Poletaeva I.I. Exploratory behavior of F2 crosses of mouse lines having selected for different brain weight: A multivariate analysis. Prog. Neuro-Psychopharmacol. Biol. Psychiat. 2004, 28(3):583-589). При этом, чем большее число заходов требуется мыши, чтобы посетить все 4 боковые рукава, то есть совершить один цикл патрулирования, тем менее "систематично" и менее эффективно исследование лабиринта;
4) число циклов патрулирования - показатель PatrlN, совершенных за время эксперимента, как еще один показатель эффективности исследовательского поведения. Чем больше циклов патрулирования, тем более "систематично" и более эффективно исследование лабиринта животным.
Показатели групп 3 и 4 могут использоваться для оценки ноотропного действия веществ.
Поведение патрулирования, оцениваемое по показателям групп 3 и 4, избирательно нарушается при действии таких повреждающих мозг факторов, как ионизирующая радиация (Григорьев А.Ю., Салимов P.M. Поведенческие критерии для прогноза исхода церебральной формы лучевого поражения у крыс. Радиобиология. 1988, т.28, №2, с.270-272), алкогольная интоксикация (Салимов P.M., Маркина Н.В., Перепелкина О.В., Майский А.И., Полетаева И.И. Быстрая толерантность к этанолу и добровольное потребление больших доз алкоголя у мышей, селектированных по весу мозга. Журн. высш. нервн. деят. 2003, т.53, №1, с.100-106), экспериментальное нейротоксическое повреждение мозга (Salimov R.M., Salimova N.B. L-glutamate abolishes differential responses to alcohol deprivation in mice. Alcohol. 1993, 10:251-257) и старение (Salimov R.; Salimova N., Shvets L.; Shvets N. Effect of chronic piracetam on age-related changes of cross-maze exploration in mice. Pharmacol. Biochem. Behav. 1995, 52:637-640), и улучшается при действии ноотропных средств, например, после введения пирацетама и меклофеноксата (Салимов P.M. Оценка упорядоченности пути в процессе исследовательского поведения у мышей. Журн. высш. нервн. деят. 1988. Т.38. №3. С.569-571; Salimov R.; Salimova N.; Shvets L.; Shvets N. Effect of chronic piracetam on age-related changes of cross-maze exploration in mice. Pharmacol. Biochem. Behav. 1995, 52:637-640; Salimov R.M., Kovalev G.I. Effects of N-cholinergic drugs on behavior in the explorative cross-maze in mice: comparison with cognitive enhancers. Eur. Neuropsychopharmacology, 2005, v.15, Suppl. 2, S.230);
5) число поворотов направо - показатель R_TrnN, и число поворотов налево - показатель L_TrnN, совершаемых животными при переходе из одного тупика в другой тупик лабиринта, и индекс асимметрии - показатель rl_Ind - этих поворотов:
rl_Ind=R_TrnN·(R_TrnN+L_TrnN)-1;
6) спонтанное стереотипное поведение - показатель S_VisN, характеризующее посещение животным поочередно двух отсеков лабиринта более двух раз подряд.
Уменьшение спонтанной стереотипии характерно для действия некоторых седативных средств, например для галоперидола, а также для некоторых седативных средств, например, для галоперидола, а также для некоторых ноотропных средств, например для пирацетама.
В работе использовали взрослых самцов мышей линии C57BL/6. Мышей содержали в виварии при естественном освещении и на стандартном пищевом рационе в стандартных клетках по 3-5 особей в каждой. В начале экспериментов их возраст составлял 3-4 месяца.
Животным контрольной группы вводили физиологический раствор.
Животным исследуемых групп в количестве животных в группе вводили исследуемые вещества изомеры (+)- или (-)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индол в физиологическом растворе или, для сравнения, только известные препараты пирацетам или меклофеносат в физиологическом растворе, и через 1 час оценивали поведение животных. Исследуемые вещества вводили в крахмальном растворе внутрь желудка с помощью нетравмирующего зонда.
Эксперименты проводили в первой половине дня в период от 10:00 до 15:00 в изолированном лабораторном помещении с использованием "белого шума" интенсивностью 70 дБ над порогом слышимости человека.
Результаты обрабатывали с помощью пакета программ STATISTICA. Использовали анализ дисперсий со встроенной функцией сравнения средних по критерию Стьюдента.
Пример 1. Исследование седативного действия галоперидола.
Исследуемым животным вводили однократно нейролептик галоперидол в дозе 0,5 мг/кг, результаты испытаний животных по тесту исследовательского поведения мышей в крестообразном лабиринте приведены в таблице 1.
Однократное введение мышам внутрь желудка нейролептика галоперидола в дозе 0,5 мг/кг оказывало седативное действие, которое выражалось в статистически значимом замедлении передвижения животных в лабиринте, то есть в увеличении времени пребывания в центре и боковых рукавах лабиринта, - показателей T_ChTm, T_GlTm, а также в уменьшении спонтанной стереотипии (показатель S_VisN). Это соответствует ранее опубликованным результатам с использованием данного теста [Салимов, 1988; Salimov et al., 2000].
Пример 2. Исследование ноотропного действия пирацетама и меклофеноксата.
Исследуемым животным вводили однократно известные ноотропные препараты: пирацетам в дозе 300 мг/кг или меклофеноксат в дозе 100 мг/кг, результаты испытаний животных по тесту исследовательского поведения мышей в крестообразном лабиринте приведены в таблицах 2а и 2б.
Однократное введение мышам внутрь желудка известных ноотропных препаратов - пирацетам в дозе 300 мг/кг и меклофеноксат в дозе 100 мг/кг - оказывало ноотропное действие, которое выражалось в статистически значимом укорочении первого и второго патрулирования лабиринта - уменьшение значений показателей F_PtrN и S_PtrN, и увеличении общего числа патрулирований - увеличение показателя PatrlN. Эти результаты соответствуют ранее опубликованным данным с использованием этого теста [Салимов, 1988; Salimov et al., 1995; Salimov, Kovalev, 2005].
Пример 3. Исследование седативного и ноотропного действия оптического изомера (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола согласно изобретению.
Для исследований был использован индивидуальный оптический изомер (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол, полученный способом согласно изобретению.
Исследуемым животным однократно вводили внутрь желудка (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол в дозах 2,5 и 5,0 мг/кг, результаты испытаний животных по тесту исследовательского поведения мышей в крестообразном лабиринте приведены в таблице 3.
+ - статистически значимое отличие от контроля по критерию Фишера, дисперсионный анализ (р<0,05).
Из результатов испытаний следует, что однократное введение мышам внутрь желудка оптического изомера (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола в дозах 2,5 и 5,0 мг/кг оказывало седативное действие, которое выражалось в статистически значимом замедлении передвижения животных в лабиринте - увеличении времени пребывания в центре и боковых рукавах лабиринта - показателей T_ChTm, T_GlTm. Эти эффекты (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола сходны с седативными эффектами галоперидола, приведенными в примере 1 (табл.1).
Кроме того, оптический изомер (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол в дозах 2,5 и 5,0 мг/кг оказывал ноотропное действие, которое выражалось в статистически значимом улучшении поведения патрулирования лабиринта - уменьшении показателя S_PtrN (табл.3). Это действие изомера (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол сходно с ноотропными эффектами препаратов пирацетам и меклофеноксат, представленными в примере 2 (табл.2а и 2б).
Пример 4. Исследование седативного и ноотропного действия оптического изомера (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола согласно изобретению.
Для исследований были использованы индивидуальные изомеры (-)транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b] индола, полученные способом согласно изобретению.
Исследуемым животным однократно вводили внутрь желудка (+) или (-) изомеры транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола в дозах 2,5 и 5,0 мг/кг, результаты испытаний животных по тесту исследовательского поведения мышей в крестообразном лабиринте приведены в таблице 4.
Из результатов испытаний следует, что однократное введение мышам внутрь желудка оптического изомера (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола в дозах 2,5 и 5,0 мг/кг оказывало седативное действие, которое выражалось в статистически значимом замедлении передвижения животных в лабиринте - увеличении времени пребывания в центре и боковых рукавах лабиринта - показателей T_ChTm, T_GlTm. Помимо этого (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол вызывал уменьшение спонтанной стереотипии (показатель S_VisN). Эти эффекты (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо [4,3-b] индола сходны с седативными эффектами галоперидола, приведенными в примере 1 (табл.1).
+ - статистически значимое отличие от контроля по критерию Фишера, дисперсионный анализ (р<0,05).
Кроме того, оптический изомер (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол в дозах 2,5 и 5,0 мг/кг оказывал ноотропное действие, которое выражалось в статистически значимом улучшении поведения патрулирования лабиринта - уменьшении показателя S_PtrN (табл.3). Это действие изомера (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол сходно с ноотропными эффектами препаратов пирацетам и меклофеноксат, представленными в примере 2 (табл.2а и 2б).
Из результатов испытаний следует, что однократное введение мышам внутрь желудка (+) и (-) изомеров транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола в дозах 2,5 и 5,0 мг/кг оказывало седативное действие, которое выражалось в статистически значимом замедлении передвижения животных в лабиринте - увеличении времени пребывания в центре и боковых рукавах лабиринта - показателей T_ChTm, T_GlTm. Этот эффект изомеров (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол сходен с седативным эффектом галоперидола, приведенным в примере 1 (табл.1).
Кроме того, (+) и (-) изомеры транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола в дозе 2,5 и 5,0 мг/кг оказывали ноотропное действие, которое выражалось в статистически значимом улучшении поведения патрулирования лабиринта - уменьшении показателя S_PtrN (табл.3). Это действие (+) и (-) изомеров транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола сходно с ноотропными эффектами препаратов пирацетам и меклофеноксат, представленными в примере 2 (табл.2а и 2б).
При этом замечено различие фармакологических свойств оптических изомеров (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, которое состоит в том, что (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол изомер обладает более выраженной седативной активностью по сравнению с (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индолом. В то же время (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индол, в отличие от (+)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола, обладал способностью снижать спонтанную стереотипию.
Таким образом, при разделении рацемического изомера транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола способом согласно изобретению были получены оптические изомеры (+)- и (-)-транс-2,8-диметил-2,3,4,4а,5,9b-гексагидро-1Н-пиридо[4,3-b]индола согласно изобретению, являющиеся оптическими антиподами друг другу и обладающие различной биологической активностью и, следовательно, различием в терапевтическом применении, что позволяет более эффективно их использовать для лечения индивидуальных состояний пациентов. Полученные соединения могут быть успешно использованы в различных фармацевтических композициях с различным содержанием активного ингредиента, в сочетании с различными наполнителями.
Промышленная применимость
Оптические изомеры согласно изобретению, полученные способом согласно изобретению, в котором использованы технологически приемлемые приемы, могут успешно применяться, например, в фармацевтических композициях согласно изобретению, получение которых может быть осуществлено с помощью известных технологий.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2007 |
|
RU2338533C1 |
| ЛИГАНДЫ АЛЬФА-АДРЕНОЦЕПТОРОВ, ДОПАМИНОВЫХ, ГИСТАМИНОВЫХ, ИМИДАЗОЛИНОВЫХ И СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2407744C2 |
| СРЕДСТВО ДЛЯ УЛУЧШЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ И ПАМЯТИ НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО (4,3-b) ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2334514C1 |
| ГЕРОПРОТЕКТОР НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b) ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2003 |
|
RU2283108C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРЫХ И ХРОНИЧЕСКИХ НАРУШЕНИЙ МОЗГОВОГО КРОВООБРАЩЕНИЯ, В ТОМ ЧИСЛЕ ИНСУЛЬТА, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО[4,3-b]ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2340342C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ НА ОСНОВЕ ГИДРИРОВАННОГО ПИРИДО(4,3-b)ИНДОЛА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕЕ ОСНОВЕ | 2009 |
|
RU2428185C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 1995 |
|
RU2106864C1 |
| Способ получения пиридоиндолов | 1974 |
|
SU592359A3 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ШИЗОФРЕНИИ НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2006 |
|
RU2338537C2 |
| ПРОИЗВОДНЫЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-B)ИНДОЛОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2140417C1 |
Настоящее изобретение представляет новые оптические изомеры (+)- и (-)-транс-2,3,4,4а,5,9b-гексагидро-2,8-диметил-1Н-пиридо[4,3-b]индола и способ их получения. Оптические изомеры, являющиеся оптическими антиподами друг другу, обладают индивидуальной биологической активностью и могут быть использованы в качестве активного ингредиента в фармацевтических композициях ноотропного и седативного действия для лечения различных индивидуальных состояний пациентов. 5 н.п. ф-лы, 5 табл.
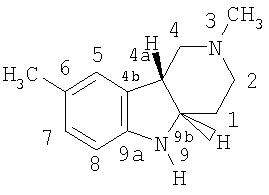
в котором атомы водорода в положениях 4а и 9b находятся в трансположении.
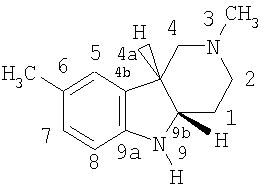
в котором атомы водорода в положениях 4а и 9b находятся в трансположении.
| US 3991199 А, 09.11.1976 | |||
| ПРОИЗВОДНЫЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-B)ИНДОЛОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2140417C1 |
| Загоревский B.A | |||
| и др | |||
| Журнал Всесоюзного Общества им | |||
| Д.И.Менделеева, Химия, 1982, т.XXVII, №1, с.102-104 | |||
| Guintdinov R.R | |||
| et al | |||
| NEUROPHARMACOLOGY, 1991, vol.30, no.11, рр.1251-1254. | |||
Авторы
Даты
2008-08-10—Публикация
2005-09-12—Подача