Изобретение относится к фосфорорганической химии, а именно к длинноцепным алкилфосфоновым кислотам общей формулы (Ia, б), обладающим антикоррозионной активностью и полученных на основе α-олефинов промышленных фракций C16-C18 и С20-С26
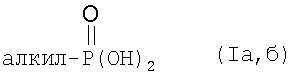
где алкил = CnH2n+1, n=16, 18 (a),
n=20, 22, 24, 26 (б).
Изобретение может быть использовано в различных отраслях промышленности, в частности, для защиты трубопроводов, резервуаров, строительных металлических конструкций, оборудования для добычи, транспорта и переработки нефти и газа, при металлообработке.
Низшие аналоги предлагаемых длинноцепных алкилфосфоновых кислот, полученные из олефинов С6-С10, используются в качестве смачивателей, детергентов, мягчителей, связывающих агентов, присадок к смазочным маслам (Пудовик А.Н., Гурьянова И.В., Ишмаева Э.А. Реакции присоединения фосфорсодержащих соединений с подвижным атомом водорода. // Реакции и методы исследования органических соединений / Под ред. Б.А.Казанского, И.Л.Кнунянца, М.М.Шемякина, Н.Н.Мельникова, кн. 19. / Химия. - М., 1968. - 848 с.)
Известны низшие алкилфосфоновые кислоты, полученные взаимодействием фосфористой кислоты с индивидуальными моноолефинами (гексеном-1, циклогексеном, октеном-1, деценом-1) в присутствии пероксида бензоила при температуре кипения олефинов (Griffin C.E., Wells H.J. // J. Org. Chem. 1959. V.24. P.2049; Griffin C.E. // J. Org. Chem. 1960. V.25, N3. - P.665-666). Однако выходы целевых алкилфосфоновых кислот низкие (18-23%), что связано с образованием теломеров в качестве побочных продуктов в результате вторичного присоединения первичных алкилфосфоновых кислот по кратной связи С=С олефинов. Таким образом, путь к алкилфосфоновым кислотам при прямом фосфорилировании олефинов фосфористой кислотой затруднителен.
Известно получение O,O-диалкиловых эфиров алкилфосфоновых кислот реакцией радикального присоединения O,O-диалкилфосфористых кислот к олефинам (Пудовик А.Н., Коновалова И.В. // ЖОХ. 1959. Т.29. №10. С.3342-3346; Stiles A.R., Vaughan W.E., Rust F.F. // J. Am. Chem. Soc. 1958. V.80. N3. P.714-716; патент GB 694772, опубл. 29.071953), (патент GB 660918, опубл. 14.11.1951, патент US 4108889, опубл. 19.11.1976). O,O-Диалкиловые эфиры алкилфосфоновых кислот используют для получения соответствующих алкилфосфоновых кислот путем их гидролиза соляной кислотой (патент GB 660918, опубл. 14.11.1951) или обработкой таких эфиров безводными хлористым или бромистым водородом с последующим гидролизом образующихся хлор- или броман-гидридов алкилфосфоновых кислот (патент US 4108889, опубл. 19.11.1976).
Однако в литературе не обнаружено сведений о получении длинноцепных алкилфосфоновых кислот на основе фосфорилирования α-олефинов промышленных фракций C16-C18 и С20-С26 и их применении в качестве ингибиторов коррозии стали. Проблема разработки эффективного способа переработки в практически полезные продукты промышленных высших α-олефинов, получаемых из фракций углеводородного сырья при переработке нефти, в настоящее время в нашей стране является актуальной в связи с накоплением огромного количества этих α-олефинов, отличающихся низкой реакционной способностью и не находящих к настоящему времени рационального применения для создания коммерческой продукции.
Технический результат - возможность переработки промышленных фракций α-олефинов C16-C18 и С20-С26 в алкилфосфоные кислоты.
Технический результат достигается предлагаемым способом получения смесей длинноцепных алкилфосфоновых кислот общей формулы (1а,б) на основе а-олефинов промышленных фракций C16-C18 или С20-С26
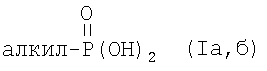
алкил = CnH2n+1, n=16, 18 (a), n=20, 22, 24, 26 (б).
Сущность изобретения заключается в том, что α-олефины промышленных фракций С16-С18 или С20-С26 (ТУ 2411-067-05766801-97 и ТУ 2411-068-05766801-97 производства ОАО "Нижнекамскнефтехим") подвергают взаимодействию с O,O-диметилфосфористой кислотой в молярном соотношении 1:(1.0-2.0) в присутствии пероксида бензоила в количестве 1.0-5.0% от веса O,O-диметилфосфористой кислоты при 110-150°С в течение 10-12 ч при перемешивании в отсутствие растворителя с последующим гидролизом промежуточных высших O,O-диметил(алкил) фосфонатов соляной кислотой при 100-110°С в течение 6-9 часов при перемешивании с последующим упариванием реакционной смеси до получения твердого продукта, содержащего смесь длинноцепных алкилфосфоновых кислот C16Н33Р(O)(OH)2 и C18H37P(O)(OH)2 или смесь С20Н41Р(О)(ОН)2, С22Н45Р(O)(ОН)2, С24Н49Р(O)(ОН)2 и С26Н53Р(O)(ОН)2 соответственно. Для синтеза целевых продуктов промежуточные O,O-диметил(алкил)фосфонаты можно не очищать, что повышает технологичность предлагаемого способа получения длинноцепных алкилфосфоновых кислот (I), которые были испытаны на антикоррозионную активность без очистки.
Проведенный газовый хроматографический анализ состава исходных олефинов промышленной фракции C16-C18 показывает, что эта фракция содержит только углеводороды с четным числом атомов углерода, причем суммарное содержание олефинов рядов С16 и C18 составляет 98%. Во фракции C16-C18 имеются 2 буша пиков с временами удерживания 9.67-10.40 мин состава C16 с массовым числом 222 и 12.01-12.68 мин состава C18 с массовым числом 252. При этом соотношение пиков олефинов с массами C16 и C18 составляет 3:2. По данным хроматограмм и масс-спектров установлено, что общее содержание α-олефинов во фракции C16-C18 составляет 80%. По данным спектров ЯМР 1H общее содержание α-олефинов во фракции C16-C18 составляет не менее 82%. Остальное приходится на олефины с внутренней связью С=С.
Массовое распределение в газовых хроматограммах фракции C20-С26 показывает, что в этой фракции содержатся, в основном, олефины рядов C20, С22, С24 и С26 в соотношении 48.6:21.0:14.6:8.6%. Остальное приходится на олефины рядов C18 и C28. По данным спектров ЯМР 1Н общее содержание α-олефинов во фракции C20-С26 составляет не менее 85%. Таким образом, значительное содержание α-олефинов во фракциях C16-C18 и С20-С26 обусловливает высокий выход целевых продуктов.
Изобретение иллюстрируется следующими примерами.
Пример 1. Длинноцепные алкилфосфоновые кислоты (1а) на основе реакции α-олефинов фракции C16-C18 с O,O-диметилфосфористой кислотой в соотношении 1:1.
Смесь 33.5 г (140.0 ммоль) олефинов промышленной фракции C16-C18, 15.5 г (140.9 ммоль) O,O-диметилфосфористой кислоты и 0.4 г (1.7 ммоль, 2.6% от веса O,O-диметилфосфористой кислоты) пероксида бензоила нагревают 10-12 ч при 130-140°С при перемешивании. Смесь отмывают водой, органический слой отделяют и выпаривают в вакууме. Не вступившие в реакцию олефины отгоняют из остатка в вакууме. В остатке получают 33.6 г твердого вещества, который разбавляют 70 мл концентрированной соляной кислоты и нагревают 6-8 ч при перемешивании при 100-110°С. Раствор выпаривают в вакууме. В остатке получают 27.3 г (81%) твердых алкилфосфоновых кислот (Ia) с т.пл. 60°С, кислотное число 139. ИК спектр (KBr, ν, см-1): 2921 с, 2852 с ν (СН3 as, s; CH2 as, s); 2750 ср. ш, 2738 ср. ш ν (O-Н); 2298 ср. о. ш 2γ (ОН); 1720 ср. о. ш, 1640 ср. о. ш δ (ОН); 1129 о. с. ш ν (Р=O); 1000 о. с ν [Р-О(Н)]. Спектр ЯМР 1Н (600 МГц, CDCl3, смесь гомологов и изомеров, δ, м.д., J, Гц): 0.85 (т, 3Н, СН3С, 3JHH 7.1); 1.28 [м, 28Н, С(СН2)14СР; 32Н, C(СН2)15СР]; 1.39-1.76 (м, 2Н, С-CH2Р); 9.21 [уш. м; 2Н, Р(ОН)2]. Спектр ЯМР 31Р (С6Н6, δP, м.д.): 37.1. Масс-спектр (ЭУ), m/z (Iотн, %): 306.3 [М]+ (13) и 334.3 [М]+ (5).
Найдено, %: С 64.71; Н 11.61; Р 9.37. C16H35О3P и С18Н39O3Р.
Вычислено, %: С 62.60 и 64.60; Н 11.54 и 11.78; Р 10.11 и 9.26. М 306.3 и 334.4.
Пример 2. Длинноцепные алкилфосфоновые кислоты (Iа) на основе реакции α-олефинов фракции C16-C18 с O,O-диметилфосфористой кислотой в соотношении 1:2.
Смесь 100.0 г (419.5 ммоль) олефинов промышленной фракции C16-C18, 87.3 г (793.6 ммоль) O,O-диметилфосфористой кислоты и 0.9 г (6.2 ммоль, 1.0% от веса O,O-диметилфосфористой кислоты) пероксида бензоила нагревают 12 ч при 110-120°С при перемешивании. Смесь отмывают водой, органический слой отделяют и выпаривают в вакууме. В остатке получают 120.5 г твердого вещества, который разбавляют 250 мл концентрированной соляной кислоты и нагревают 8 ч при перемешивании при 100-110°С. Раствор выпаривают в вакууме. В остатке получают 110.5 г (87%) твердых алкилфосфоновых кислот (Ia) с т.пл. 59-61°С. Данные ИК, ЯМР 1H, 31P и масс-спектров соответствуют спектрам образца соединения (Ia), полученного в примере 1.
Найдено, %: С 63.55; Н 11.56; Р 9.77. С16H35О3Р и С18H39О3Р.
Вычислено, %: С 62.60 и 64.60; Н 11.54 и 11.78; Р 10.11 и 9.26. М 306.3 и 334.4.
Пример 3. Длинноцепные алкилфосфоновые кислоты (Iб) на основе реакции α-олефинов фракции C20-С26 с O,O-диметилфосфористой кислотой в соотношении 1:1.
Смесь 146.5 г (454.3 ммоль) олефинов промышленной фракции C20-С26, 50.0 г (454.5 ммоль) O,O-диметилфосфористой кислоты и 5.5 г (22.7 ммоль, 5.0% от веса O,O-диметилфосфористой кислоты) пероксида бензоила нагревают 10 ч при 140-150°С при перемешивании. Смесь отмывают водой, органический слой отделяют и выпаривают в вакууме. Не вступившие в реакцию олефины отгоняют из остатка в вакууме. Остаток разбавляют 240 мл концентрированной соляной кислоты и нагревают 9 ч при перемешивании при 100-110°С. Раствор выпаривают в вакууме. В остатке получают 136.8 г (75%) твердых алкилфосфоновых кислот (Iб) в виде пасты. ИК-спектр (KBr, ν, см-1): 2923 с, 2854 с ν (СН3 as, s; СН3 as, s); 2744 ср. ш, 2735 ср. ш ν (O-Н); 2356 ср. о. ш 2γ (ОН); 1723 ср. ш, 1695 ср. ш δ (ОН); 1378 ср δ (СН3 s); 1128 с. ш ν (Р=O); 1005 о. с ν [Р-О(Н)]. Спектр ЯМР 1H (400 МГц, D2О, смесь гомологов и изомеров, δ, м.д., J, Гц): 0.90 (т, 3Н, СН3С, 3JHH 7.3); 1.29 (м, ССНС); 1.93 (м, 2Н, ССН2Р); 8.10 [м; 2Н, Р(ОН)2]. Спектр ЯМР 31P (С6Н6, δP, м.д.): 33.1, 33.8 и 36.2 в соотношении 1:143: 1.
Найдено, %: С 68.37; Н 12.41; Р 6.97. С22Н47O3Р, С20Н43О3Р, С24Н51O3Р и С26Н55O3Р.
Вычислено, %: С 66.23, 67.62, 68.82 и 69.87; Н 11.98, 12.16, 12.31 и 12.44; Р 8.55, 7.93, 7.40 и 6.94.
Полученные образцы длинноцепных алкилфосфоновых кислот прошли испытания в качестве ингибиторов углекислотной коррозии мягкой стали с использованием электрохимической ячейки с барботажем углекислого газа в присутствии ПАВ (неонол) или в его отсутствие (рабочие электроды MS-R-101S Pattern 44B, электрод сравнения Ag/AgCl, pH-электрод, датчик температуры, капилляр Луггина, отверстия для ввода углекислого газа и выхода газа, состав агрессивной среды основан на стандартном растворе ASTM D1144, который включает 24.5 г/л NaCl (98.8%), 0.66 г/л KCl (98.3%), 0.2 г/л NaHCO3 (98.0%), 5.2 г/л MgCl2 (98.5%), 1.16 г/л CaCl2 (98.3%) и 4.09 г/л Na2SO4 (98.3%), в соответствии со стандартными методиками (Griffith Р. // J. Petroleum Tech. - 1984. - Vol.36, No.3. - P.361-367; Brill J.P. // J. Petroleum Tech. - 1987. - Vol.39, No.1. - P.15-21). Образцы соединений вносились в стандартный раствор при использовании однофазной системы, либо в слой керосина, либо в слой стандартного раствора при использовании двухфазной системы органический/неорганический слои в соотношении 1:9. Установлено, что в концентрации 10 мг/л соединения (Ia) ингибируют коррозию мягкой стали на 99.5% через 6 ч после внесения ингибитора в отсутствие неонола (см. таблицу). В среде пластовых попутно добываемых вод, отобранных из скважины №1010 Зюзеевского месторождения Республики Татарстан, ингибирующая активность соединений (Ia) составляет 94.6% по отношению к мягкой стали.
Таким образом, длинноцепные алкилфосфоновые кислоты, полученные на основе высших промышленных α-олефинов, являются эффективным ингибитором коррозии и заявляемый способ их получения решает проблему утилизации отходов производства в практически полезные продукты.
Р - ингибирующая активность, %;
γ - коэффициент ингибирования.
aВвод ингибитора в слой стандартного раствора;
бВвод ингибитора в слой керосина.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЛИННОЦЕПНЫХ S-АЛКИЛОВЫХ ЭФИРОВ О, О-ДИАЛКИЛДИТИОФОСФОРНЫХ КИСЛОТ, ОБЛАДАЮЩИХ АНТИКОРРОЗИОННОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2337913C1 |
| ГИДРОФОБИЗАТОР СТРОИТЕЛЬНЫХ МАТЕРИАЛОВ НА ОСНОВЕ ДЛИННОЦЕПНЫХ ОЛЕФИНОВ | 2009 |
|
RU2400456C1 |
| ФОСФОРСЕРООРГАНИЧЕСКИЙ ИНГИБИТОР КОРРОЗИИ СТАЛИ НА ОСНОВЕ АЛЬФА-ОЛЕФИНОВ ПРОМЫШЛЕННОЙ ФРАКЦИИ C, C | 2011 |
|
RU2449056C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ПОЛИЭФИРОВ АРИЛДИТИОФОСФОНОВЫХ КИСЛОТ И ИХ АММОНИЕВЫХ СОЛЕЙ ИЗ ГИПЕРРАЗВЕТВЛЕННЫХ ПОЛИЭФИРПОЛИОЛОВ, КОМПОЗИЦИИ ПОЛИЭФИРОВ АРИЛДИТИОФОСФОНОВЫХ КИСЛОТ И ИХ АММОНИЕВЫЕ СОЛИ, ОБЛАДАЮЩИЕ АНТИКОРРОЗИОННОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2427584C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНИРОВАННЫХ ПАРАФИНОВ НА ОСНОВЕ ВЫСШИХ АЛЬФА-ОЛЕФИНОВ | 2005 |
|
RU2288908C1 |
| N-[АЛКИЛФЕНОКСИПОЛИ(ЭТИЛЕНОКСИ)КАРБОНИЛМЕТИЛ]МОРФОЛИНИЙ ХЛОРИДЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ИНГИБИТОРОВ АСФАЛЬТОСМОЛОПАРАФИНОВЫХ ОТЛОЖЕНИЙ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2322435C1 |
| 1,2,3-ТРИС[(АММОНИО)МЕТИЛКАРБОНИЛОКСИПОЛИ(АЛКИЛЕНОКСИ)]ПРОПАН ТРИХЛОРИДЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ЭМУЛЬГАТОРОВ ВОДОМАЗУТНЫХ ЭМУЛЬСИЙ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2284988C1 |
| N, N-ДИЭТИЛ-N-[ИЗОАЛКОКСИКАРБОНИЛМЕТИЛ]- N-[АЛКИЛФЕНОКСИПОЛИ(ЭТИЛЕНОКСИ)КАРБОНИЛЭТИЛ]АММОНИЙ 2-ГИДРОКСИПРОПИОНАТЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ИНГИБИТОРОВ КОРРОЗИИ СТАЛИ | 2008 |
|
RU2379280C1 |
| ТРИС[(АММОНИО)МЕТИЛКАРБОНИЛОКСИПОЛИ(2-МЕТИЛЭТИЛЕНОКСИ)]ПРОПАН ТРИХЛОРИДЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ЭМУЛЬГАТОРОВ ВОДОБИТУМНЫХ ЭМУЛЬСИЙ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2294337C1 |
| [(ГЕТЕРИЛОНИО)МЕТИЛКАРБОНИЛОКСИПОЛИ(АЛКИЛЕНОКСИ)]-[(АММОНИО)МЕТИЛКАРБОНИЛОКСИПОЛИ(АЛКИЛЕНОКСИ)]ПРОПАН ТРИХЛОРИДЫ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ ЭМУЛЬГАТОРОВ ВОДОБИТУМНЫХ И ВОДОМАЗУТНЫХ ЭМУЛЬСИЙ, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2005 |
|
RU2286990C1 |
Изобретение относится к фосфорорганической химии, а именно к способу получения длинноцепных алкилфосфоновых кислот, обладающих антикоррозионной активностью, на основе α-олефинов промышленной фракции C16-C18 и С20-С26. Изобретение может быть использовано для защиты трубопроводов, резервуаров, строительных металлических конструкций, оборудования для добычи, транспорта и переработки нефти и газа при металлообработке. Длинноцепные алкилфосфоновые кислоты получают взаимодействием α-олефинов промышленных фракций C16-C18 и С20-С26 с O,O-диметилфосфористой кислотой в молярном соотношении 1:(1.0-2.0) в присутствии пероксида бензоила в количестве 1.0-5.0% от веса O,O-диме-тилфосфористой кислоты при 110-150°С в течение 10-12 ч в отсутствие растворителя с последующим гидролизом промежуточных высших O,O-диметил(алкил)фосфонатов соляной кислотой при нагревании с получением целевого продукта, представляющего собой смесь длинноцепных алкилфосфоновых кислот. Технический результат - разработка нового способа получения смесей алкилфосфоновых кислот и ингибитора коррозии мягкой стали. 2 н.п. ф-лы, 1 табл.
| Способ получения диалкиловых эфиров алкилфосфоновых кислот | 1970 |
|
SU511013A3 |
| WO 2007112312 (Innovative properties company) 04.10.2007 | |||
| US 6433359 (Innovative properties CO) 13.08.2002 | |||
| US 4108889 (The Procter and Gamble company) 22.08.1978 | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| M.GABOYARD ET ALL, Phosphorus, Sulfur and Silicon, 2002, v.177, 877-891 | |||
| STEPHEN MANN ET ALL, J.C.S | |||
| Chem | |||
| Coram, | |||
Авторы
Даты
2008-11-10—Публикация
2007-06-04—Подача