Настоящее изобретение относится к оригинальному материалу, который может быть использован в медицинской или ветеринарной области, в частности, но не исключительно, для выполнения внутрикостных имплантатов, в частности зубных имплантатов, или для выполнения костных протезов. Настоящее изобретение касается также способа получения этого материала, а также его использования.
Многие типы металлических материалов или пластмасс используют в медицинской или ветеринарной области для замены биологических структур (в частности, кости) или для закрепления функциональных органов (зубные или другие имплантаты).
Выбор материала осуществляют в зависимости от присущих ему структурных характеристик, а также в зависимости от его биосовместимости в плане толерантности или, что еще лучше, в плане биологического вживления.
В документе FR-A-2722694 описан полученный путем литья материал для выполнения внутрикостных имплантатов или костных протезов, представляющий собой термопластический полимер (в частности, поли(эфирэфиркетон), называемый также PEEK), содержащий гидроксиапатит кальция, трехкальциевый фосфат, ортофосфорную кислоту и цеолит типа TiO2.
Несмотря на обнадеживающие результаты, полученные при использовании этого типа материала, оказалось, что результаты в плане биологической интеграции являются не совсем удовлетворительными.
Настоящим изобретением предлагается новый материал, являющийся производным от материала, описанного в вышеуказанном документе FR-A-2722694, который сочетает в себе хорошие общие механические качества и очень хорошую биосовместимость в плане биологического вживления и который может эффективно использоваться как в медицинской, так и в ветеринарной областях.
Соответствующий материал представляет собой полученную путем литья деталь, состоящую из биосовместимого связующего вещества, содержащего одно или несколько соединений, обеспечивающих добавление кальция и фосфора, при этом упомянутую деталь подвергают операции поверхностной очистки.
Эта очистка способствует выведению на поверхность и, следовательно, поверхностный доступ для элементов, добавляемых к связующему веществу, в частности для кальция и фосфора; это обеспечивает или, по меньшей мере, способствует образованию ионных связей между добавленными элементами и химическими, минеральными или органическими окружающими элементами после биологической имплантации детали из материала. В случае присутствия рассасывающихся добавленных элементов, сразу же после исчезновения этих элементов, ткани, биологические клетки или окружающие химические элементы получают пространство для интеграции в материал.
Этот отличительный признак позволяет улучшить сцепление и колонизацию клеток с целью обеспечения хорошего биологического вживления типа трансплантации и хорошей биосовместимости имплантата.
Биосовместимое связующее вещество выбирают в зависимости от получаемых физических характеристик после формовки, в частности, при помощи операции литья под давлением. Например, можно использовать термопластический полимер типа поли(эфирэфиркетона), полиэфиркетон, блок-полиэфирамид, полисульфон, политетрафторэтилен или полиимид; можно также использовать природный полимер, в частности, типа целлюлозы. Этот полимер может быть рассасывающимся или нерассасывающимся.
Предпочтительно используют поли(эфирэфиркетон) (РЕЕК), учитывая его высокий модуль Юнга и его хорошие структурные характеристики. PEEK является полукристаллическим полимером, образованным одной ароматической линейной цепочкой, основанной на повторении следующих блоков:
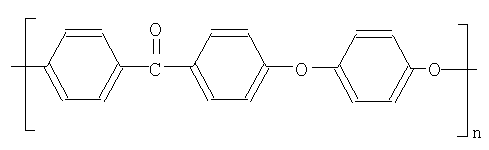
Характеристики этого полимера раскрыты в коммерческой брошюре, выпущенной в 1992 году компанией ICI MATERIALS "Vitrex PEEK, the high temperature engineering thermoplastic-properties and processing".
Добавления кальция и фосфора предпочтительно осуществляют при помощи фосфатов кальция, получаемых, например, из трехкальциевого фосфата (Са3(PO4)2); двухкальциевого фосфата или монетита (CaHPO4), гидроксиапатита кальция ((Са5(PO4)3ОН) или (Са10(PO4)6Р2O), со стехиометрическим составом или без него, или из содержащих их веществ.
Присутствие фосфатов кальция позволяет материалу приблизиться к природному составу кости для усиления биосовместимости. Предпочтительно используют вещества, содержащие, по меньшей мере, частично рассасывающиеся фосфаты кальция.
В частности, гидроксиапатит кальция является веществом, которое присутствует в кости. Предпочтительно его можно использовать в нестехиометрическом виде, так как по этой причине он слегка рассасывается, что представляет интерес для тканной интеграции.
Двухкальциевый или трехкальциевый фосфат представляет интерес, так как он является недорогим и является одним из базовых компонентов для образования гидроксиапатита кальция; с другой стороны, он является рассасывающимся, а также выполняет функцию зарубцевания.
Можно также использовать эти различные добавки фосфатов кальция в смеси.
Кроме добавок фосфатов кальция полученный путем литья материал в соответствии с настоящим изобретением может содержать ортофосфорную кислоту (Н3(PO4)). Ортофосфорную кислоту в природном виде предписывают в качестве фиксатора кальция и в качестве подкисляющего вещества; кроме того, речь идет об основном компоненте нуклеотидов, являющихся базовыми единицами нуклеиновых кислот, участвующих в образовании ядра живых клеток.
Кроме того, в материал в соответствии с настоящим изобретением предпочтительно добавляют наполнитель из одного или двух соединений, позволяющих создавать или способствующих образованию электростатических связей с окружающей средой. Этот наполнитель или эти наполнители можно выбирать из цеолитов и/или некоторых оксидов; в частности, можно предусмотреть использование керамик типа диоксида титана (TiO2), диоксида циркония (ZrO2), оксида алюминия (Al2О3) или диоксида кремния (SiO2).
Данные наполнители являются электростатическими соединениями, обеспечивающими функцию ионного сцепления; кроме того, они имеют повышенную молекулярную массу и способствуют улучшению непроницаемости материала для рентгеновских лучей.
Материал в соответствии с настоящим изобретением формуют при помощи литья под давлением или прессования выдавливанием. Оборудование и условия формования соответствуют данной смеси и, в частности, природе используемого связующего.
Для сохранения достаточной прочности и долговечности формуемого материала содержание связующего должно составлять, по меньшей мере, 65%, предпочтительно от 65% до 90% по весу конечного материала.
С другой стороны, для добавления достаточного количества химических элементов, предназначенных для улучшения биологической интеграции, содержание дополнительных компонентов (трехкальциевого фосфата и/или двухкальциевого фосфата, и/или гидроксиапатита кальция, в случае необходимости, соединенного(ых), по меньшей мере, с одним соединением, например, типа цеолита или оксида, предназначенным для улучшения электростатичности и непроницаемости для рентгеновских лучей, и с ортофосфорной кислотой) должно составлять от 10 до 35% по весу конечного материала.
Хорошим соотношением, в частности, в плане механических характеристик является 80% по весу связующего полимера и 20% по весу дополнительного(ых) соединения(ий).
Настоящее изобретение относится также к способу получения этого материала. Соответствующий способ заключается в следующем: тщательно, до получения однородной смеси, смешивают предназначенное для формования биосовместимое связующее с одним или несколькими соединениями, обеспечивающими добавление кальция и фосфата; полученную смесь подвергают операции формования; осуществляют одну или несколько операций поверхностной очистки и деконтаминации сформованной детали; упомянутую деконтаминированную деталь помещают в асептическую упаковку.
Операцию поверхностной очистки предпочтительно осуществляют при помощи, по меньшей мере, одной ванны в растворе, в частности, очистителя с одновременной обработкой ультразвуком.
Предпочтительно операции поверхностной очистки и деконтаминации осуществляют путем последовательного погружения сформованной детали в ванны из хлористоводородной или серной кислоты, ацетона, пероксида водорода, гипохлорида натрия или дезинфицирующего(-их) вещества, обрабатываемые ультразвуком, между которыми осуществляют операции промывки водой или погружения в водяные ванны, обрабатываемые ультразвуком.
Пример 1
Базовые смеси готовят на основе поли(эфирэфиркетона)(РЕЕК), трехкальциевого фосфата (Са3(PO4)2) и диоксида титана (TiO2).
PEEK используют в виде порошка или в гранулированном виде (размер: примерно 100 микрон), выпускаемых компанией "Vitrex Europa GmbH", Hauptstr. 11 D-65719 HOFHEIM - Германия.
Трехкальциевый фосфат доступен в порошкообразном виде (зерна размером около 200 микрон); он выпускается, например, компанией «S.A. Cooperation Pharmaceutique Française", 77020 MELUN - Франция.
Оксид титана также выпускается в виде порошка компанией «S.A.Cooperation Pharmaceutique Française", 77020 MELUN - Франция.
а) Состав
Ниже приведено несколько примеров возможного состава:
б) Смешивание
Компоненты каждой смеси смешивали в смесителе с турбинной мешалкой до получения идеальной однородности.
в) Сушка
Каждую полученную однородную смесь сушили в сушильном шкафу с воздушной циркуляцией в течение 3 часов при 150°С.
г) Формование
Операцию формования осуществляли на прессе для выдавливания типа KRAUSS-MAFFEI, модель 90-340-32, компания KRAUSS MAFFEI FRANCE, 92632 GENNEVILLIERS - Франция.
Условия подготовки оборудования и условия формования смеси соответствуют описанию из вышеупомянутой коммерческой брошюры «ICI MATERIALS».
Поскольку PEEK является полукристаллическим термопластиком, то форму необходимо нагревать до температуры, по меньшей мере, превышающей температуру его перехода в стеклообразное состояние (140°С). В противном случае качество поверхности готовых деталей будет плохим. Действительно, поверхностный слой будет в аморфной фазе, а сердцевина - в кристаллической; если форма была слишком холодной, то деталь может быть полностью аморфной, и механические характеристики существенно снизятся.
Терморегулирование формы обеспечивают при помощи масляного нагревателя, позволяющего поддерживать ее при температуре порядка 160°С. Изоляционные средства ограничивают рассеивание тепла и предохраняют периферические органы пресса для выдавливания. Эти средства могут быть выполнены в виде изоляционных пластин из комплексного стекловолоконного материала.
Для осуществления последовательных операций литья под давлением на питательном бункере устанавливают вибратор для обеспечения вытекания смеси.
Как правило, формование осуществляют при температуре порядка 340-400°С и под давлением примерно от 70 до 140 МПа.
Форму выполняют соответственно детали, которую необходимо изготовить, например, для изготовления костного протеза, в частности, для ортопедических целей. Можно также выполнять блок из материала, который затем режут или механически обрабатывают в соответствии с необходимой формой костного заполнителя или имплантата, например, типа зубного имплантата.
д) Поверхностная очистка - деконтаминация
После получения сформованного материала его подвергают операциям поверхностной очистки и деконтаминации перед асептической упаковкой.
Предпочтительно на первом этапе эти операции осуществляют путем погружения сформованного материала в разные ванны, обрабатываемые ультразвуком; каждое используемое вещество может выполнять функцию очистителя поверхности или дезинфицирующего средства, или одновременно обе функции.
В любом случае вещество или вещества, обеспечивающие функцию поверхностной очистки, получают таким образом, чтобы в сочетании с воздействием ультразвуком выводить на поверхность, в частности, фосфор и кальций (в виде фосфата кальция) и диоксид титана. Доступность на поверхности фосфата кальция способствует обмену с окружающей средой и электростатическому сцеплению некоторых элементов, присутствующих в биологической среде, с материалом после имплантации; этот обмен и/или это электростатическое сцепление приводят к проникновению клеток в имплантированный материал. Одновременно присутствие на поверхности диоксида титана способствует этому обмену и появлению электростатических связей.
Кроме того, поскольку фосфат кальция является, по меньшей мере, частично рассасывающимся, его исчезновение после имплантации материала приводит к появлению полостей или сети полостей, также способствующих проникновению клеток из окружающих тканей.
В качестве средств для осуществления операций поверхностной очистки и деконтаминации можно использовать хлористоводородную кислоту (например, 30%-ный раствор HCl) или серную кислоту (например, 30%-ный раствор H2SO4), ацетон (С3Н6О), пероксид водорода (Н2О2, например, 110 объем. частей или 30%) и/или гипохлорид натрия (NaClO), предпочтительно применяемые в комбинации. Предпочтительно используют дополнительные ванны с чисто дезинфицирующими средствами типа Gigasept (зарегистрированный знак) или Lysetol (зарегистрированный знак).
Соответствующий порядок осуществления операций поверхностной очистки и деконтаминации состоит в погружении имплантата в ряд последовательных различных ванн, обрабатываемых ультразвуком:
- HCl 30%: 20 мин
- Н2О: 10 мин (или промывка)
- ацетон: 20 мин
- H2O: 10 мин (или промывка)
- H2O2 30%: 20 мин
- NaClO: 20 мин
- Н2O: 10 мин (или промывка)
- Gigasept 12%: 60 мин
- Н2O Ppi: 20 мин (или промывка)
Имплантат помещают в стерилизационную оболочку для пропускания через автоклав; после этого он проходит через цикл стерилизации при температуре порядка 135°С в течение 10 минут под давлением порядка 2150 мбар. Эта операция стерилизации в автоклаве дополняет функцию поверхностной очистки; она может быть осуществлена в сочетании с обработкой оксидом этилена или гамма-лучами.
е) Результаты
Исследование при помощи электронного сканирующего микроскопа (ЭСМ) показывает, что операции поверхностной очистки/деконтаминации и стерилизации способствуют выведению фосфата кальция на поверхность. Эти фосфаты кальция выходят через микропоры и кристаллизуются.
После имплантации анализ поверхности показывает наличие отверстий и полостей в поверхности материала, а также присутствие углерода, кислорода и азота, в то время как кальций и фосфор присутствуют в малых количествах по отношении к первоначально добавленным количествам.
Это свидетельствует о частичном исчезновении частиц фосфата кальция с поверхности и о колонизации отверстий и полостей окружающими биологическими материалами, что является признаком биологического вживления типа трансплантации.
Клинический анализ установленных имплантатов показывает, что при контакте с рассматриваемым материалом развивается кортикальный костный слой, что является следствием физических и атомных характеристик материала.
В данном случае речь идет о настоящем принципе трансплантации; эти результаты свидетельствуют о клинической реальности интеграции материала в окружающую ткань.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИТНАЯ ДЕТАЛЬ ДЛЯ ВНУТРИКОСТНОЙ ИМПЛАНТАЦИИ И СПОСОБ ИЗГОТОВЛЕНИЯ ТАКОЙ ДЕТАЛИ | 2011 |
|
RU2609870C2 |
| Высокопрочный антифрикционный композит на основе полиэфирэфиркетона для медицины и способ его изготовления | 2020 |
|
RU2729653C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО МАТЕРИАЛА ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ С ИСПОЛЬЗОВАНИЕМ ГИДРОЛИТИЧЕСКОЙ КОНВЕРСИИ | 2015 |
|
RU2599022C1 |
| КОМПОЗИЦИЯ СТОМАТОЛОГИЧЕСКОГО ПЛОМБИРОВОЧНОГО МАТЕРИАЛА ИЛИ МАТЕРИАЛА ИМПЛАНТАТА И ПОРОШКООБРАЗНЫЙ МАТЕРИАЛ, ЖИДКОСТЬ ДЛЯ ГИДРАТАЦИИ, МАТЕРИАЛ ИМПЛАНТАТА И СПОСОБ ДОСТИЖЕНИЯ СВЯЗЫВАНИЯ | 2003 |
|
RU2332201C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОЙ БИОАКТИВНОЙ КЕРАМИКИ НА ОСНОВЕ ОКСИДА ЦИРКОНИЯ | 2015 |
|
RU2595703C1 |
| СПОСОБ НАНЕСЕНИЯ КАЛЬЦИЙ-ФОСФАТНОГО ПОКРЫТИЯ НА ИМПЛАНТАТЫ ИЗ ТИТАНА И ЕГО СПЛАВОВ | 2007 |
|
RU2348744C1 |
| Биомедицинский материал на основе гидроксиапатита и способ его получения | 2022 |
|
RU2782925C1 |
| СПОСОБ ПОДГОТОВКИ ШИХТЫ ДЛЯ ПОЛУЧЕНИЯ БИОКЕРАМИКИ | 2009 |
|
RU2431627C2 |
| КОМПОЗИЦИЯ МНОГОЦЕЛЕВОГО БИОМАТЕРИАЛА | 2005 |
|
RU2389495C2 |
| МЕДИЦИНСКИЙ КЛЕЙ-БИОИМПЛАНТАТ НОВОГО ПОКОЛЕНИЯ НА ОСНОВЕ БИОПОЛИМЕРНЫХ НАНОКОМПОЗИТОВ В ВИДЕ ПОЛУСИНТЕТИЧЕСКОЙ ПОЛИМЕРНОЙ МАТРИЦЫ С ПРИМЕНЕНИЕМ ЛАЗЕРНЫХ ТЕХНОЛОГИЙ | 2011 |
|
RU2477996C1 |
Изобретение относится к медицине. Описан материал, который используют в виде детали, выполненной путем формования литьем, и он представляет собой биосовместимое связующее, содержащее одно или несколько соединений, обеспечивающих добавление кальция или фосфора, отличающийся тем, что его подвергают операции поверхностной очистки, предназначенной для выведения на поверхность и, следовательно, для обеспечения доступности на поверхности добавляемых к связующему элементов, в частности кальция и фосфора. Этот материал предпочтительно используют для изготовления внутрикостных имплантатов или костных протезов. 4 н. и 16 з.п. ф-лы.
| Способ получения N-((гидроксиамино)-оксоалкил)-2-(хиназолин-4-иламино)-бензамидов | 2019 |
|
RU2722694C1 |
| DE 10055465 A1, 23.05.2002 | |||
| ПОКРОВНЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), И ИМПЛАНТАТ ДЛЯ БИОМЕДИЦИНСКОГО ИСПОЛЬЗОВАНИЯ (ВАРИАНТЫ) | 1993 |
|
RU2124329C1 |
Авторы
Даты
2008-11-20—Публикация
2003-12-23—Подача