Изобретение относится к детали, предназначенной для имплантации в костную ткань, такой как зубной имплантат, протез или заполнитель костной полости, в медицинских или ветеринарных целях, при этом указанная деталь выполнена из материала, который в сочетании со специальным способом изготовления позволяет ускорить ее остеоинтеграцию в принимающую (рецепторную) ткань.
Известны различные имплантаты, выполненные из биосовместимого полимера, способ изготовления которых обеспечивает создание поверхностной структуры, содержащей микропоры, способствующие клеточной колонизации со стороны рецепторной ткани и ускорению остеоинтеграции указанного имплантата.
Эти известные имплантаты показывают очень удовлетворительные результаты, однако толщина слоя остеоинтеграции, получаемого при помощи этого механизма, которая соответствует глубине поверхностных микропор, составляет примерно 1000 нанометров (1 мкм). Вместе с тем, общеизвестно, что более предпочтительной является толщина взаимопроникновения ткани и имплантата, составляющая по крайней мере от 1 мкм до 10 мкм, тем более, когда характеристики упругости имплантата и рецепторной ткани являются разными. Такое улучшенное взаимопроникновение особенно желательно, если имплантат усилен, в частности, волокнами, особенно в начале процесса остеоинтеграции, когда формирующееся корковое вещество пока не имеет модуля упругости, сравнимого с модулем упругости имплантата.
Кроме того, такие микропористые поверхностные структуры трудно и даже невозможно получить при помощи экономичных способов изготовления имплантата, таких как формование литьем под давлением.
Изобретение призвано восполнить недочеты известных технических решений и предложить имплантат и экономичный способ его получения, позволяющие увеличить глубину взаимопроникновения между имплантатом и принимающей костной тканью.
В связи с этим объектом изобретения является деталь, предназначенная для внутрикостной имплантации in vivo, выполненная из материала, содержащего:
- термопластическое органическое связующее; и
- волоконный наполнитель,
при этом волокна в основном отслоены от связующего на части их длины в поверхностном слое указанной детали.
Под волокнами следует понимать микроволокна, нановолокна или нанотрубки, отношение длины которых к толщине превышает 10. Микроволокна являются волокнами, толщина которых имеет значение порядка микрометра или микрона, то есть толщина которых по существу составляет от 10-6 до 10-5 метров. Нановолокна и нанотрубки являются волокнами, толщина которых имеет значение порядка нанометра, то есть по существу составляет от 10-9 до 10-8 метров.
Расслоение волокон в поверхностном слое позволяет создать промежутки, которые действуют наподобие каналов и за счет свойства капиллярности в толщине этого слоя переносят в нем органические жидкости, ускоряя, таким образом, клеточную колонизацию этого слоя. Природа волокон тоже способствует и ускоряет, за счет абсорбции, перемещение этих органических жидкостей.
Изобретение можно применять в соответствии с описанными ниже предпочтительными вариантами выполнения, которые можно рассматривать индивидуально или в любой технически возможной комбинации.
Предпочтительно термопластическое связующее выполнено из полиэфирэфиркетона (ПЭЭК), известного своими свойствами биосовместимости.
Предпочтительно волоконный наполнитель содержит волокна, выполненные из полимера семейства ароматических полиамидов, которые тоже обладают отличными свойствами биосовместимости в сочетании с повышенными механическими характеристиками. В частности, волокна поли(амида-имида), температура стеклования которых близка к температуре литья" под давлением ПЭЭК, обеспечивают, за счет свойства легкой деформации во время литья, равномерное распределение волокон в имплантате, даже если они являются относительно длинными.
Эффект проводимости расслоенных волокон в поверхностном слое позволяет получить толщину указанного слоя не менее 2 мкм, то есть значительно превышающую ту, которую можно получить при имплантатах, изготавливаемых посредством пластического литья под давлением, содержащих микропоры на поверхности без эффекта расслоения.
Предпочтительно материал имплантата в дополнение к волокнам содержит наполнитель из соединений на основе кальция и фосфора. Эти ресорбируемые соединения способствуют остеоинтеграции и заживлению.
Предпочтительно наполнитель из соединения на основе кальция выполнен из трехкальциевого фосфата Ca3(PO4)2 с гексагональной β-структурой. Во время операции формования литьем под давлением эти соединения трехкальциевого фосфата трансформируются в кристаллы не стехиометрического ресорбируемого апатита кальция.
Предпочтительно материал имплантируемой детали может также содержать наполнитель из цеолитов. Цеолиты способствуют электростатическим связям со средой имплантации и ионному сцеплению с этой средой. Кроме того, такой наполнитель помогает сделать материал рентгеноконтрастным.
Предпочтительно волоконный наполнитель содержит волокна, сделанные из силикатов кальция (Ca2SiO4). Присутствие этих волокон на поверхности детали ускоряет абсорбцию интерстициальных жидкостей в среде имплантации и, следовательно, клеточную колонизацию поверхности детали.
Объектом изобретения является также способ изготовления такого имплантата, при этом указанный способ содержит следующие этапы, на которых:
a) посредством экструзии и грануляции смешивают термопластический полимер и волоконный наполнитель;
b) формуют деталь посредством литья под давлением в пресс-форме, содержащей полость соответствующей формы, из гранулята, полученного на этапе а);
c) заготовку, полученную на этапе b), подвергают обработке в травильных ваннах под действием ультразвука в течение времени, необходимого для расслоения волокон в поверхностном слое.
Способ пластического литья под давлением позволяет экономично получать готовый имплантат этого типа сразу после операции формования и в большом количестве. Кроме того, он позволяет ориентировать волокна при помощи потока материала, поступающего в пресс-форму, и получать, таким образом, оптимальный эффект усиления даже для имплантатов сложной формы. Физико-химическая обработка, сочетающая в себе химическое воздействие ванн и механическое воздействие ультразвуков, позволяет одновременно протравливать/очищать поверхность имплантата, чтобы удалять с него любое загрязнение, связанное со способом формования литьем под давлением, и производить в поверхностном слое расслоение волокон, которые могут создавать искомый эффект проводимости.
Чтобы получить деталь, содержащую, кроме волокон, соединения на основе кальция и фосфатов, изобретением предлагается также способ получения гранулята или компаунда, содержащий этапы, на которых:
- изготавливают первый гранулят или компаунд, смешивая посредством экструзии и грануляции полимерное связующее с соединениями, вводимыми в виде порошков; и
- этот первый гранулят смешивают с волокнами во время второй операции экструзии и грануляции таким образом, чтобы получить гранулят, используемый для операции формования литьем под давлением.
Предпочтительно во время изготовления первого гранулята можно также вводить наполнитель из цеолитов.
Предпочтительно волоконный наполнитель составляет от 5 мас.% до 15 мас.% смеси. Эта доля одновременно обеспечивает значительный эффект усиления конечной детали, позволяет получать ее при помощи способа литья под давлением и смешивать волокна с полимерным связующим посредством экструзии и грануляции или "compounding", независимо от того, был или не был предварительно введен наполнитель из соединений, содержащих кальций и/или цеолиты.
Объектом изобретения является также гранулят или компаунд для изготовления посредством пластического литья под давлением имплантата, усиленного волокнами, при этом указанный гранулят содержит:
- полимерное связующее из полиэфирэфиркетона (ПЭЭК);
- 10-20 мас.% наполнителя из соединений, содержащих кальций и цеолиты;
- 5-15 мас.% волоконного наполнителя.
Гранулят этого типа можно использовать напрямую для пластического литья под давлением на этапе b) заявленного способа.
Согласно первому варианту получения заявленного гранулята, волоконный наполнитель содержит волокна из поли(амида-имида), температура стеклования которого равна или ниже температуры литья под давлением ПЭЭК.
Согласно второму варианту получения заявленного гранулята, волоконный наполнитель содержит волокна из силиката кальция (Ca2SiO4).
После формования деталь подвергают травлению в последовательном ряду ванн под действием ультразвука для придания ей способности к имплантации in vivo и для формирования в ней поверхностного слоя, способствующего остеоинтеграции в принимающей среде.
Предпочтительно травление осуществляют в последовательном ряду ванн в следующем порядке:
- погружение в ванну при воздействии ультразвука для уменьшения количества частиц, содержащих железо;
- погружение в растворитель связующего при воздействии ультразвука, который инертен по отношению к волокнам.
Первая ванна позволяет удалить поверхностное загрязнение металлическими частицами литейного пресса и пресс-формы. Вторая ванна, в которой растворяется только связующее, позволяет с одновременным действием ультразвуков получать расцепление или расслоение между частицами и матрицей в поверхностном слое. Порядок прохождения через ванны имеет значение, поскольку кислота может также оказывать восстанавливающее воздействие по отношению к волокнам и/или к наполнителю из соединений, содержащих кальций и цеолиты и присутствующих на поверхности. При первоочередном осуществлении травления кислотой последующее действие растворителя позволяет опять получить на поверхности эти соединения.
Согласно предпочтительному варианту выполнения, в частности, соответствующему варианту, в котором материал имплантата содержит волокна и наполнитель из цеолитов и соединений, содержащих кальций в матрице ПЭЭК, операция травления включает в себя погружение в следующие ванны, содержащие:
- соляную кислоту
- ацетон
- пероксид водорода,
между которыми производят промывку в водяной ванне тоже под действием ультразвука. В частности, если заявленная имплантируемая деталь содержит волокна из силикатов кальция, последняя ванна пероксида водорода позволяет создавать на поверхности этих волокон, находящихся на поверхности детали, слой диоксида кремния (SiO2). Этот слой диоксида кремния абсорбирует влагу и способствует прохождению органических жидкостей в поверхностном слое имплантата.
Далее следует описание предпочтительных, но не ограничительных вариантов выполнения изобретения, со ссылками на фиг.1-4, на которых:
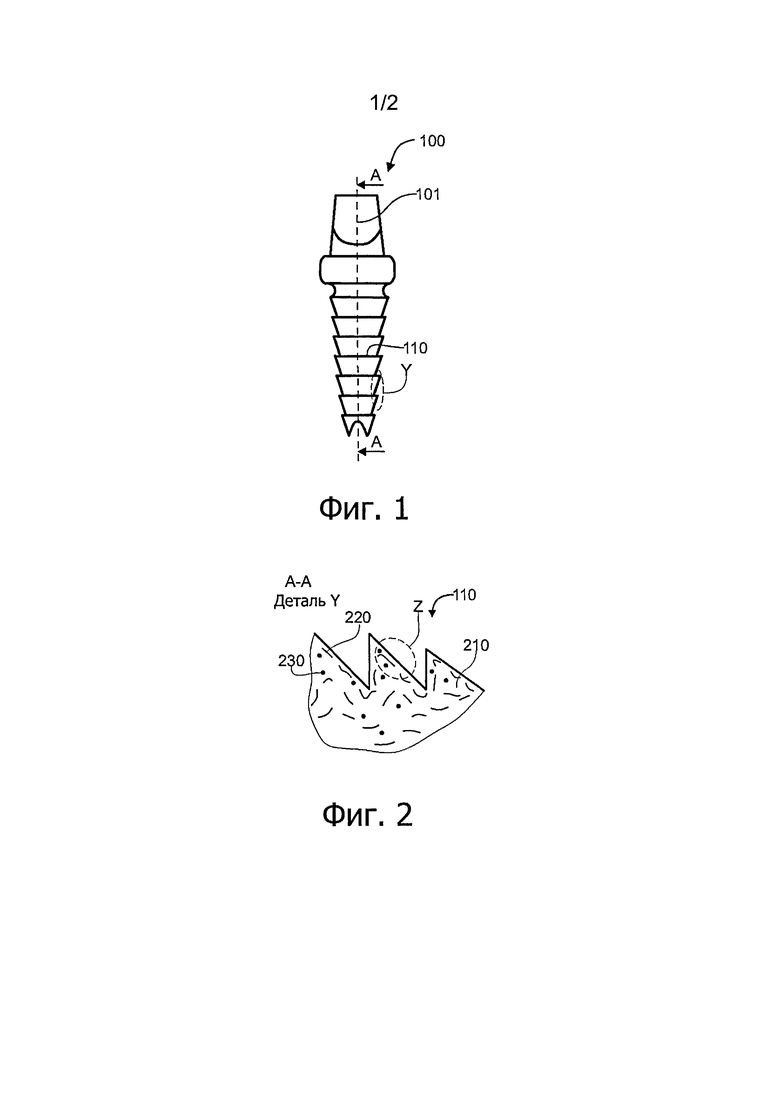
Фиг.1 - вид спереди внутрикостного зубного имплантата согласно примеру выполнения изобретения.
Фиг.2 - деталь Y фиг.1 в разрезе по линии АА фиг.1.
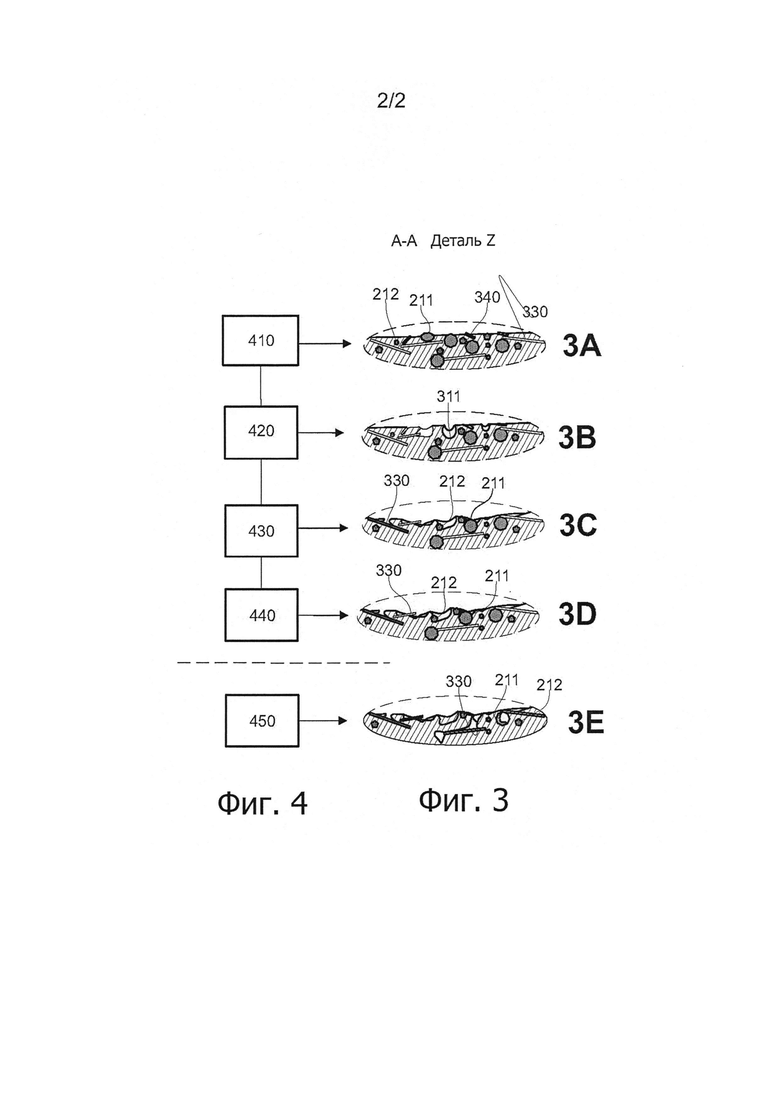
Фиг.3 - вид детали Z фиг.2 в разрезе по линии АА в поверхности имплантата согласно примеру выполнения изобретения в ходе фаз реализации и внутрикостной имплантации указанного имплантата, представленных на фиг.3А-3Е.
Фиг.4 - блок-схема различных фаз реализации и применения заявленного имплантата.
На фиг.1 показан пример имплантата (100), имеющего сложную форму, который можно экономично получить при помощи способа формования путем пластического литья под давлением. Этот пример выполнения, который не носит ограничительного характера, иллюстрирует применение изобретения для изготовления зубного имплантата. Указанный зубной имплантат содержит верхнюю часть (101), предназначенную для размещения на ней надстроек, таких как абатмент, и так называемую нижнюю часть (110), предназначенную для имплантации в костную часть. Нижняя часть (110) может, при желании, содержать рельефные элементы, такие как бороздки, способствующие ее первичному механическому закреплению в гнезде, таком как отверстие, выполненное в приемной костной ткани. Эти скрепляющие бороздки или рельефные элементы могут иметь размер порядка одного миллиметра. Указанный имплантат в основном выполнен из термопластического полимера, имеющего хорошие свойства биосовместимости, который можно применять для технологий формования литьем под давлением. Например, но, не ограничиваясь указанным, указанный полимер может представлять собой полиэфирэфиркетон или ПЭЭК, выпускаемый в продажу компанией VICTREX® под названием VICTREX® PEEK 150G®. Предпочтительно связующее может представлять собой материал, содержащий кальций и цеолиты, такой как материал, описанный во французском патенте FR 2722694 или в американском патенте US 5872159.
На фиг.2 детально в разрезе показан материал имплантата, содержащий матрицу (210) или связующее из ПЭЭК, частицы (230) соединений, содержащих кальций, диаметром порядка 1 мкм (10-6 метра), и усилительные волокна (220). Согласно этому примеру выполнения, усилительные волокна (220) выполнены из поли(амида-имида), например, представляют собой волокна, выпускаемые в продажу под названием KERMEL® ТЕСН компанией KERMEL®, 20 рю Ампер, Ф-68027 Кольмар, Франция. Согласно примеру выполнения с использованием микроволокон, последние имеют диаметр около 7 мкм при длине около 700 мкм (0,7 мм). Поскольку имплантат получают при помощи способа пластического литья под давлением, температура литья ПЭЭК равна или превышает температуру стеклования этого полимера, чтобы волокна могли легко деформироваться при температуре литья под давлением и чтобы они могли по существу следовать за потоком материала.
Согласно предпочтительному варианту выполнения, волоконный наполнитель может также или исключительно содержать волокна силиката кальция (Ca2SiO4) (на фиг.2 не показаны). Этот материал является жестким при температуре литья под давлением и, следовательно, при этой температуре не деформируется. Поэтому волокна силиката кальция предпочтительно имеют меньший размер, порядка 1 мкм в диаметре при длине от 10 до 50 мкм. Во избежание любого явления скапливания во время литья под давлением общее количество смешиваемых волокон любого типа не должно превышать 15 мас.%.
Предпочтительно наполнитель (230) из соединений, содержащих кальций, сделан из трехкальциевого фосфата Ca3(PO4)2 в фазе β. Фаза β трехкальциевого фосфата является кристаллической фазой с гексагональной структурой, стабильной при низкой температуре.
При одновременном воздействии совокупной влаги, содержащейся в порошках трехкальциевого фосфата, ПЭЭК и, возможно, цеолитов, это соединение претерпевает трансформацию во время операции формования литьем под давлением в соответствии со следующей реакцией:
4 Ca3(PO4)2+4(H2O)=>3((Са3(PO4)2)(ОН)2Ca+2HPO4+½O2
3((Са3(PO4)2)(ОН)2Са соответствует гидроксиапатиту. Этот апатит является полностью не стехиометрическим, и, благодаря этому, ресорбируемым, что придает материалу имплантируемой детали в соответствии с изобретением свойства интеграции в костную ткань, как при трансплантации.
Для этого порошки, применяемые во время литья под давлением, не обезвоживают. Предпочтительно они могут быть повторно гидратированы, или в них можно добавить ортофосфорную кислоту (H3PO4), чтобы способствовать этой реакции.
Показанное на фиг.3 наблюдение поверхности в еще более увеличенном виде позволяет анализировать морфологию этой поверхности в зависимости от этапов осуществления способа и от применения заявленной имплантируемой детали, при этом этапы способа представлены на фиг.4.
Согласно примеру выполнения, имплантат получают посредством осуществления первого этапа, целью которого является получение гранулята, в котором смешаны:
- 80 мас.% ПЭЭК
- 10 мас.% трехкальциевого фосфата (Ca3PO4)
- 10 мас.% диоксида титана (TiO2)
Смесь получают посредством экструзии при температуре в пределах от 340°C до 400°C.
При грануляции этого экструдата получают первый гранулят, который смешивают с 10 мас.% волокон поли(амида-имида) типа KERMEL® ТЕСН и волокон силиката кальция согласно тому же принципу экструзии-грануляции.
Полученный второй гранулят используют для формования (410) имплантата путем пластического литья под давлением. Формование происходит при температуре от 340°C до 400°C под давлением от 70 до 140 МПа, при этом пресс-форму нагревают до температуры, превышающей температуру стеклования ПЭЭК, то есть до температуры предварительного нагрева пресс-формы около 160°C.
Поскольку температура перехода в стеклообразное состояние волокон типа KERMEL® равна 340°C, они могут деформироваться при температуре литья под давлением, что позволяет им следовать за потоком материала и равномерно распределяться в грануляте во время операции экструзии-грануляции, и в детали во время операции формования литьем под давлением.
После операции формования (410), как показано на фиг.3А, поверхность имплантата является по существу гладкой и содержит несколько слегка выступающих над поверхностью частиц (211) соединений, содержащих кальций и цеолиты (212). Волокна (330), в данном случае волокна силиката кальция, тоже присутствуют вблизи поверхности и могут слегка выступать из этой поверхности. Поверхность имплантата содержит также металлические включения (340), появившиеся в результате контакта с пресс-формой и с винтами литейного пресса.
После операции формования имплантат подвергают обработке посредством пропускания через ряд ванн химического травления под действием ультразвука. Например, следующий протокол дает хорошие практические результаты, при этом ультразвук применяют с частотой 42 кГц:
- HCl 30%: 35 минут
- H2O: 10 минут (промывка)
- C3H6O (ацетон): 35 минут при температуре кипения ацетона
- Сушка имплантата с испарением ацетона
- H2O2 30%: 35 минут
- H2O: 10 минут (промывка).
После этого имплантат погружают, тоже под действием ультразвука, в стерилизующие вещества:
- GIGASEPT® 12%: 35 минут
- H2O ppi: 35 минут
При этом ванна в растворе GIGASEPT® является необязательной.
На первом этапе (420) имплантат подвергают кислотному травлению в соляной кислоте. Целью этого травления в основном является удаление металлических включений. По завершении этого травления поверхность имплантата, показанная на фиг.3 В, не содержит включений, а также частиц, содержащих кальций, которые выступали из поверхности, и на их месте остались соответствующие впадины (311).
После промывки на следующем этапе (430) имплантат погружают в ванну ацетона, тоже при воздействии ультразвука. Как показано на фиг.3С, после этого этапа (430) определенная толщина ПЭЭК растворилась, в результате чего проявились ранее находившиеся под поверхностью частицы (211, 212) соединений, содержащих кальций и цеолиты. Действие ультразвука способствует также расслоению между волокнами (330), появляющимися на поверхности, и их имплантации в матрицу.
После промывки на следующем этапе (440) имплантат подвергают обработке в ванне пероксида водорода, тоже при воздействии ультразвука. Как показано на фиг.3D, эта ванна существенно не меняет морфологию поверхности. С другой стороны, она оказывает воздействие на поверхность волокон силиката кальция, способствуя окислению и образованию на их поверхности диоксида кремния (SiO2).
Предпочтительно после этого имплантат помещают в стерилизационную оболочку для пропускания через автоклав. При этом он проходит цикл стерилизации при температуре порядка 135°C в течение 10 минут по давлением порядка 2150 гПа. Эта операция стерилизации в автоклаве способствует функции поверхностного травления; ее можно объединить с обработкой окисью этилена или гамма-лучами. Кроме того, она способствует кристаллизации частиц кальциевых соединений на поверхности. После этой стерилизации имплантат упаковывают в стерильную упаковку, и он готов для имплантации в костную ткань.
Во время имплантации (450) указанного имплантата в ткань, органические жидкости, такие как кровь, за счет капиллярности следуют по расслоениям между волокнами и матрицей, как в случае волокон KERMEL, так и в случае волокон из силиката кальция, см. фиг.3Е. В случае волокон из силиката кальция диоксид кремния, присутствующий на поверхности этих волокон, абсорбирует эти жидкости и способствует их перемещению под поверхностью. На поверхности и, - за счет проводимости через волокна, - под этой поверхностью соединения на основе кальция (211) входят в контакт с этими органическими жидкостями. Ресорбирующая способность этих соединений способствует клеточной колонизации, что приводит к вживлению поверхности имплантата в костную ткань.
Применение этой поверхностной обработки к известному имплантату, содержащему только соединения фосфата кальция и диоксид титана в матрице из ПЭЭК, позволяет получить толщину активного поверхностного слоя примерно в 1 мкм. Эта же обработка в отношении имплантата идентичной формы, но выполненного из материала, содержащего дополнительно 10 мас.% волокон поли(амида-имида) или волокон силиката кальция, позволяет получить толщину активного поверхностного слоя в 3,6 мкм.
Представленное описание наглядно показывает, что, благодаря своим различным отличительным признакам и их преимуществам, настоящее изобретение позволяет получить искомый технический результат. В частности, оно позволяет получить усиленный имплантат, выполненный посредством формования литьем под давлением, содержащий поверхностный слой остеоинтеграции толщиной, по меньшей мере, в три раза превышающей толщину, получаемую без усиления.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАТЕРИАЛ ДЛЯ МЕДИЦИНСКИХ ИЛИ ВЕТЕРИНАРНЫХ НУЖД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЕ | 2003 |
|
RU2338557C2 |
| Высокопрочный антифрикционный композит на основе полиэфирэфиркетона для медицины и способ его изготовления | 2020 |
|
RU2729653C1 |
| Модифицированное кальций-фосфатное покрытие на титановом имплантате с внедренным в него фармакологическим препаратом и способ его получения | 2024 |
|
RU2833928C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОМИКРОБНЫХ ИМПЛАНТАТОВ ИЗ ПОЛИЭФИРЭФИРКЕТОНА | 2010 |
|
RU2526168C2 |
| КОМПОЗИЦИЯ СТОМАТОЛОГИЧЕСКОГО ПЛОМБИРОВОЧНОГО МАТЕРИАЛА ИЛИ МАТЕРИАЛА ИМПЛАНТАТА И ПОРОШКООБРАЗНЫЙ МАТЕРИАЛ, ЖИДКОСТЬ ДЛЯ ГИДРАТАЦИИ, МАТЕРИАЛ ИМПЛАНТАТА И СПОСОБ ДОСТИЖЕНИЯ СВЯЗЫВАНИЯ | 2003 |
|
RU2332201C2 |
| БИОАКТИВНОЕ ПОКРЫТИЕ НА ИМПЛАНТАТЕ ИЗ ТИТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2385740C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО МАТЕРИАЛА ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ С ИСПОЛЬЗОВАНИЕМ ГИДРОЛИТИЧЕСКОЙ КОНВЕРСИИ | 2015 |
|
RU2599022C1 |
| ИМПЛАНТИРУЕМОЕ МЕДИЦИНСКОЕ УСТРОЙСТВО | 2010 |
|
RU2545823C2 |
| КОМПОЗИТНЫЙ ВНУТРЕННИЙ ФИКСАТОР | 2009 |
|
RU2545424C2 |
| Способ получения модифицированного биопокрытия с микрочастицами трикальцийфосфата и/или волластонита на имплантате из магниевого сплава | 2021 |
|
RU2763091C1 |
Изобретение относится к медицине и представляет собой имплантат для внутрикостной имплантации, выполненный из материала, содержащего: термопластическое органическое связующее, представляющее собой полиэфирэфиркетон; волоконный наполнитель, волокна которого выполнены из поли(амида-имида); наполнитель из соединения на основе кальция, представляющего собой трехкальциевый фосфат Са3(PO4)2 с гексагональной β-структурой. Волокна, локализованные на поверхностном слое имплантата, в основном отслоены от связующего на всей длине или на части их длины. Изобретение относится также к способу изготовления имплантата. Технический результат заключается в равномерном распределении волокон, усиленном импланте с увеличенной глубиной взаимопроникновения между имплантатом и костной тканью. 2 н. и 5 з.п. ф-лы, 4 ил.
1. Имплантат, предназначенный для внутрикостной имплантации in vivo, отличающийся тем, что выполнен из материала, содержащего:
- термопластическое органическое связующее, представляющее собой полиэфирэфиркетон, и
- волоконный наполнитель, волокна которого выполнены из поли(амида-имида),
- наполнитель из соединения на основе кальция, представляющего собой трехкальциевый фосфат Са3(PO4)2 с гексагональной β-структурой,
при этом волокна, локализованные на поверхностном слое имплантата, в основном отслоены от связующего на всей длине или на части их длины.
2. Имплантат по п. 1, отличающийся тем, что он содержит волокна, выполненные из силиката кальция (Ca2SiO4).
3. Имплантат по п. 1, отличающийся тем, что толщина поверхностного слоя превышает или равна 2000 нанометров.
4. Имплантат по п. 1, отличающийся тем, что дополнительно содержит наполнитель из цеолитов.
5. Способ изготовления имплантата по любому из пп. 1-4, отличающийся тем, что содержит этапы, на которых:
a) посредством экструзии и грануляции смешивают полиэфирэфиркетон и волоконный наполнитель из поли(амида-имида); и
b) формуют имплантат посредством литья под давлением в пресс-форме, содержащей полость соответствующей формы, из гранулята, полученного на этапе а); и
c) заготовку, полученную на этапе b), подвергают обработке в ваннах травления при воздействии ультразвука в течение времени, необходимого для расслоения волокон в поверхностном слое.
6. Способ по п. 5, отличающийся тем, что волоконный наполнитель составляет от 5 мас.% до 15 мас.% смеси.
7. Способ по п. 5, отличающийся тем, что этап с) способа включает следующие операции:
- пропускание через ванну соляной кислоты при воздействии ультразвука для уменьшения количества частиц, содержащих железо; и
- пропускание через ванну ацетона при воздействии ультразвука;
- пропускание через ванну пероксида водорода,
между которыми производят промывку в водяной ванне тоже при воздействии ультразвука.
| US 6193516 B1, 27.02.2001 | |||
| WO 2009039438 A2, 26.03.2009 | |||
| US 20110039974 A1, 17.02.2011 | |||
| US 2005020894 A1, 22.09.2005 | |||
| Сепаратор для отделения примесей от жидкости | 1982 |
|
SU1064972A1 |
| МАТЕРИАЛ ДЛЯ МЕДИЦИНСКИХ ИЛИ ВЕТЕРИНАРНЫХ НУЖД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЕ | 2003 |
|
RU2338557C2 |
| US 5476880 A, 19.12.1995 | |||
| WO 2010009567 A2, 28.01.2010 | |||
| С.И | |||
| ОЖЕГОВ, Словарь русского языка, 24-е издание, Москва, "ОНИКС 21 век" "Мир и Образование", 2004, стр | |||
| Гидравлический способ добычи торфа | 1916 |
|
SU206A1 |
Авторы
Даты
2017-02-06—Публикация
2011-07-13—Подача