Предпосылки настоящего изобретения
Область применения настоящего изобретения
Настоящее изобретение касается фармацевтических составов, пригодных для лечения и/или профилактики заболеваний сердца. Более конкретно, настоящее изобретение касается использования талипорфина или его производных в качестве активных ингредиентов для лечения и/или профилактики заболеваний сердца.
Описание родственных способов
За последние годы во всем мире произошел рост населения старшего возраста. В основном это обусловлено развитием медицины и улучшением образа жизни. Однако часто увеличение возраста сопровождается ростом сердечно-сосудистых заболеваний. К примерам таких заболеваний относятся стенокардия, острый инфаркт миокарда, а также атеросклероз коронарной артерии, которые сочетаются с систолией и окклюзией (закупоркой) кровеносных сосудов. Помимо этого, окклюзия кровеносных сосудов часто приводит к гипертрофии сердца, вызывая сердечную недостаточность и аритмию. Аналогичным образом сердечная аритмия часто связана с имешией миокарды. Обычно считается, что злокачественная желудочковая (вентрикулярная) аритмия, вызывающая коллапс (острую сердечную недостаточность), является тем основным механизмом, который ответственен за внезапную смерть. С аритмией связана также реперфузия, возникающая после высвобождения закупоренной коронарной артерии. Такая аритмия может увеличить смертность и болезненность при проведении тромболитической терапии и коронарной ангиопластики. Было предложено несколько причин возникновения реперфузионной аритмии. Среди них в качестве основной причины считается продуцирование свободных кислородных радикалов, а также последующее перокисление ими липидных мембран.
К лекарственным средствам, используемым для лечения пациентов с сердечной недостаточностью, относятся диуретики, дигиталис, ингибиторы трансферазы вазопрессина, активаторы симпатической нервной системы или ингибиторы фосфодиэстеразы. Значительно усилить систолию способны дигиталис, активаторы симпатической нервной системы или ингибиторы трансферазы вазопрессина, однако эти лекарственные средства могут вызвать аритмию или тахикардию. Поэтому при длительном применении указанных лекарственных средств не происходит повышения выживаемости пациентов. Недавно подтвержден положительный эффект на выживаемость пациентов с сердечной недостаточностью, выявленный путем введения им блокатора рецептора вазопрессина, блокатора рецептора вазоэндотелиозина, а также каведилола, обладающих блокирующим действием симпатических α- и β-адреноцепторов соответственно (Ye TL et al., J. Pharmacol. Exp. Ther., 1992, 263:92-98; Bristow MR et al., Circulation, 1996, 94:2807-2816; Colucci WS et al., Circulation, 1996, 94:2800-2806).
Из-за тесной взаимосвязи закупорки коронарной артерии с сердечной недостаточностью и с аритмией для лечения сердечной недостаточности используют стандартное лекарственное средство - строфантин, который может увеличить систолию, но обычно он вызывает аритмию. Таким образом, указанное лекарственное средство не способствует увеличению выживаемости пациентов. Следовательно, сохраняется необходимость в разработке эффективных средств для подавления аритмии, инфаркта, а также развития сердечной недостаточности, возникающих в результате острой коронарной атаки.
Имеются сообщения о том, что некоторые соединения способны увеличить систолию, это такие соединения, как синтетический 2-фенил-4-оксигидрохинолин (Su MJ et al., Brit. J.Pharmacol, 1993, 110:310-316), талипорфин из Lauraceae и Rutaceae (Su MJ et al., Eur.J. Pharmacol., 1994, 254:141-150), лириоденин из Fissistigma glaucescens (Chang GJ et al., Brit. J. Pharmacol., 1996, 118:503-512), (-)-кариахин из Cryptocarya chinensis (Wu MH et al., Brit.J. Pharmacol., 1995, 116:3211-3218), а также производные берберина; причем было подтверждено, что лириоденин, (-)-карахин и производные берберина обладают антиаритмической способностью. Обычно антиаритмическую способность оценивают в модели на изолированном сердце крысы, это делают, вызывая сердечную аритмию путем перевязки на 30 мин сосудов и последующей реперфузии. Однако внешний ток K+, выявляемый у других животных, слегка отличен от тока в случае крысы. Поэтому в таких испытаниях для того, чтобы продемонстрировать указанную разницу во внешнем токе K+, были использованы также морские свинки. Помимо этого, исследованиями Su et al. было показано, что талипорфин обладает способностью увеличивать систолию, а также внутренние токи Са2+. Из-за усиления систолии лекарственные средства, имеющие такие функции, непригодны при ишемическом некрозе миокарды и теоретически они бесполезны в лечении инфаркта миокарды и аритмии. Однако настоящее изобретение показывает, что талипорфин и его производные, в особенности в малых дозах, полезны для лечения и/или профилактики заболеваний сердца.
Краткое содержание настоящего изобретения
Один аспект настоящего изобретения содержит в себе как отличительный элемент фармацевтический состав для лечения и/или профилактики заболеваний сердца у млекопитающих, содержащий эффективное количество соединения формулы I:
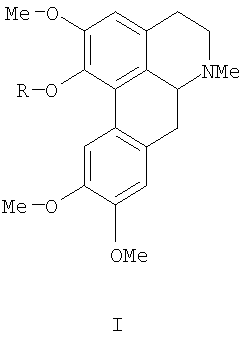
или их сложноэфирные производные, в которых R представляет собой водород, ацетил, пропионил, бутирил или трет-бутоксикарбонил, или их фармацевтически приемлемые соли; а также фармацевтически приемлемый носитель или наполнитель.
Другой аспект настоящего изобретения характеризует соединение формулы I:

в которой R представляет собой пропионил, бутирил или трет-бутоксикарбонил, или их фармацевтически приемлемые соли.
Другой аспект настоящего изобретения характеризует соединение формулы II, а также фармацевтический состав, содержащий тот же активный ингредиент, как для лечения и/или профилактики заболеваний сердца у млекопитающих. Указанный фармацевтический состав содержит эффективное количество соединения формулы II:
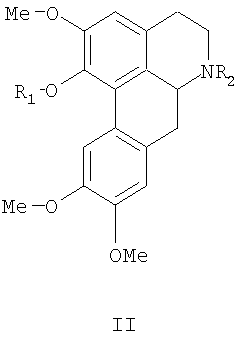
или его сложноэфирные производные, в которых R1 представляет собой водород, ацетил, пропионил, бутирил или трет-бутоксикарбонил, a R2 представляет собой этил, аллил, пропил, бутил, изобутил или циклопропилметил, или их фармацевтически приемлемые соли; а также фармацевтически приемлемый носитель или наполнитель.
Еще один аспект настоящего изобретения характеризует соединение формулы III, а также фармацевтический состав, содержащий тот же самый активный ингредиент, как для лечения и/или профилактики заболеваний сердца у млекопитающих. Указанный фармацевтический состав содержит эффективное количество соединения формулы III:
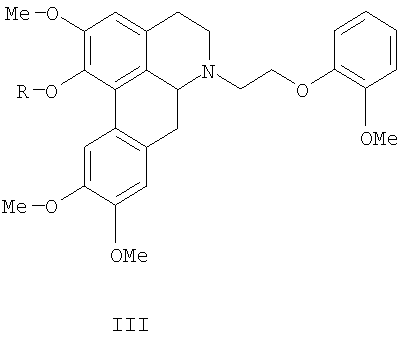
или его сложноэфирные производные, в которых R представляет собой водород, ацетил, пропионил, бутирил или трет-бутоксикарбонил, или их фармацевтически приемлемые соли; а также фармацевтически приемлемый носитель или наполнитель.
Последний аспект настоящего изобретения характеризует способ лечения и/или предотвращения заболеваний сердца у млекопитающих, включающий введение указанному млекопитающему эффективного количества соединения формулы I, или II, или III, или их производных, или их фармацевтически приемлемых солей.
Краткое описание чертежей
Настоящее изобретение будут более полно понято, а его преимущества станут очевидными при ссылке на приведенное далее описание настоящего изобретения и на сопровождающие его чертежи. На этих чертежах показано следующее.
Фиг.1 представляет собой исходную запись, показывающую влияние 10 мкл хинидина на проводимость узла AV. А - предсердная деполяризация; Н - деполяризация узла His; S - артефакт стимуляции; V - желудочковая деполяризация.
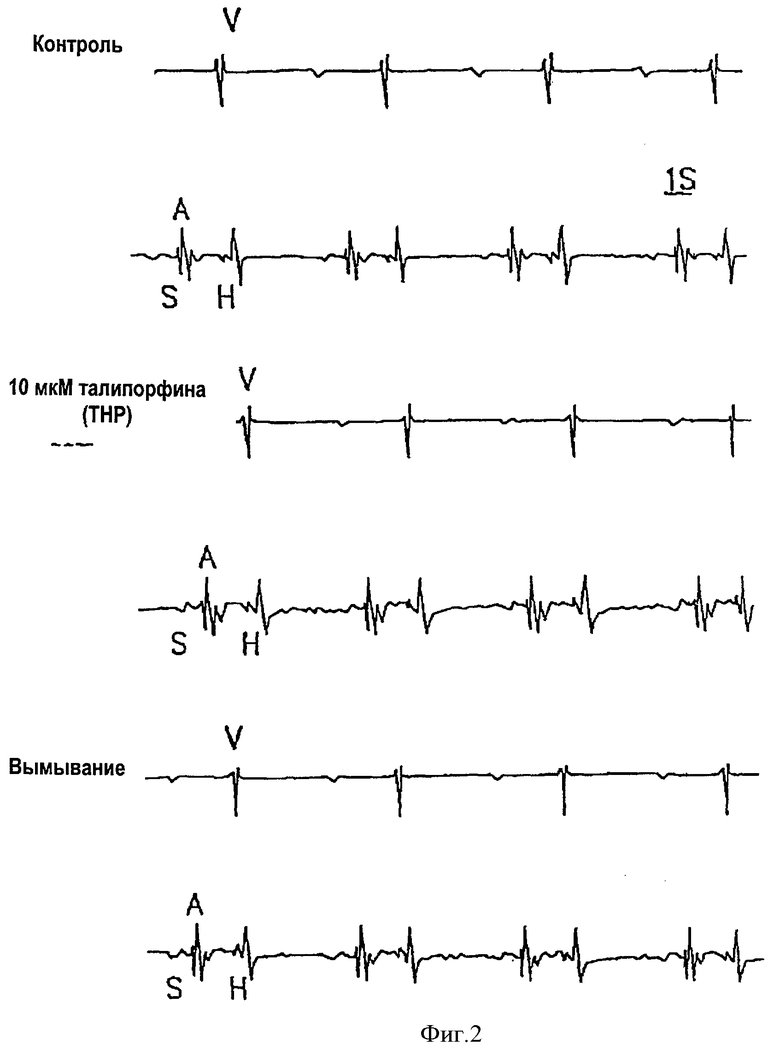
Фиг.2 представляет собой исходную запись, показывающую влияние 10 мкл талипорфина на проводимость узла AV. А - предсердная деполяризация; Н - деполяризация узла His; S - артефакт стимуляции; V - желудочковая деполяризация.
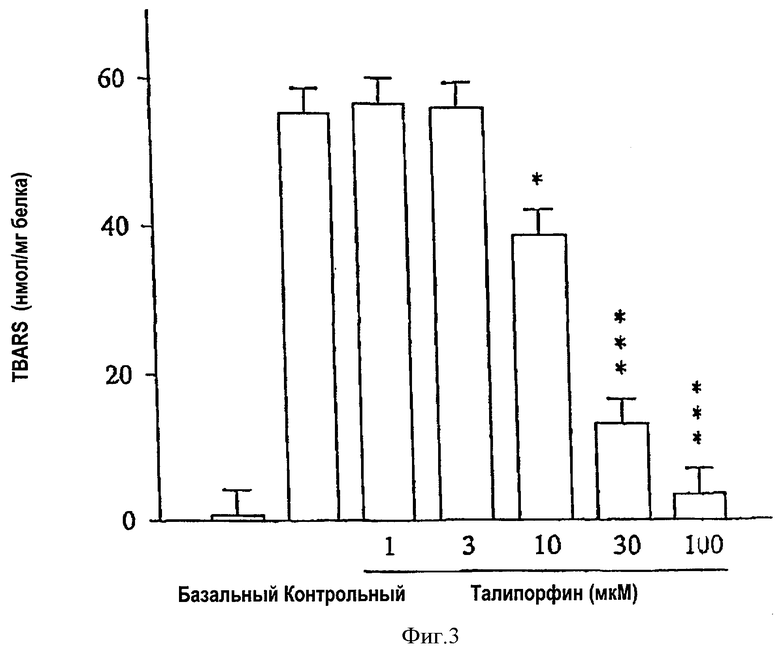
На фиг.3 приведена диаграмма эффектов подавления талипорфином вызванного медью липидного перокисления липопротеинов человека низкой плотности. Данные приведены как среднее арифметическое ± среднеквадратичная ошибка (n=4). *р<0,05, **р<0,01, ***р<0,001 по сравнению с контролем.
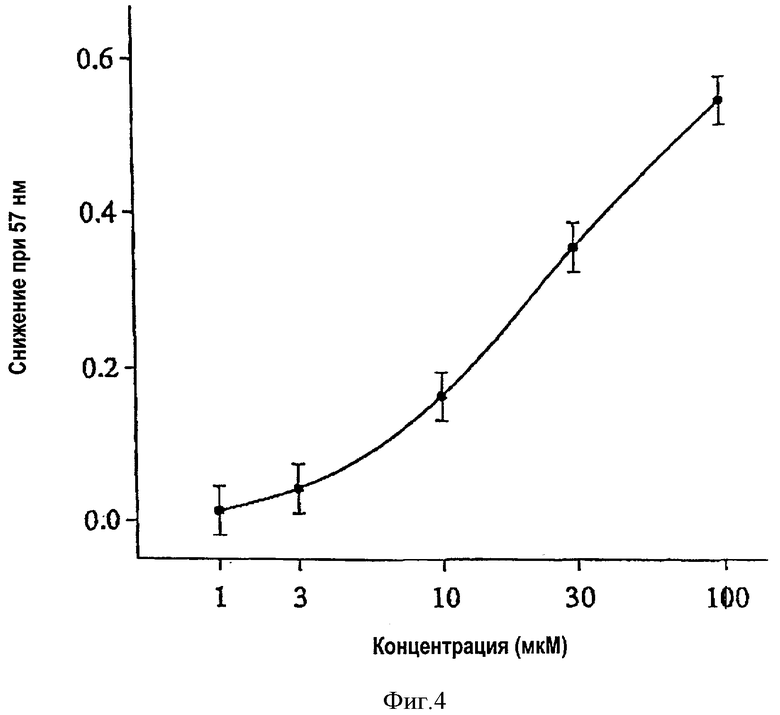
На фиг.4 приведена кривая зависимости захвата радикалов 1,1-дифенил-2-пикрилгидразила (DPPH) от дозы талипорфина. Данные приведены как среднее арифметическое ± среднеквадратичная ошибка (n=4).
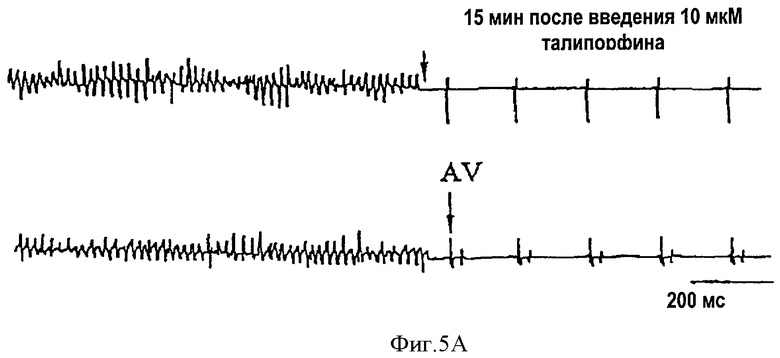
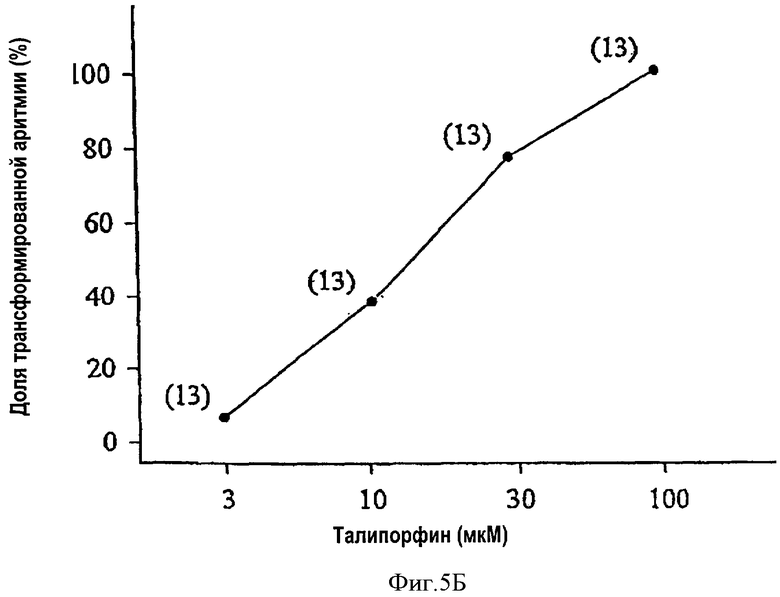
На фиг.5 приведена диаграмма, показывающая а) превращение полиморфной желудочковой тахикардии, вызванной ишемической реперфузией, в нормальный синусовый ритм с помощью 10 мкМ талипорфина; отмечены предсердная (А) и желудочковая (V) деполяризации; б) антиаритмическая эффективность талипорфина.
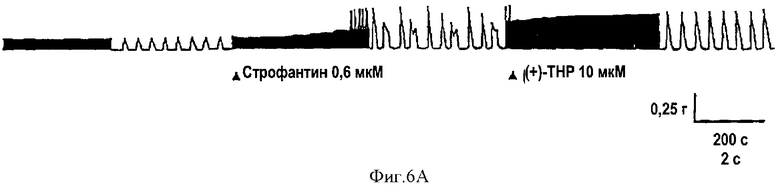
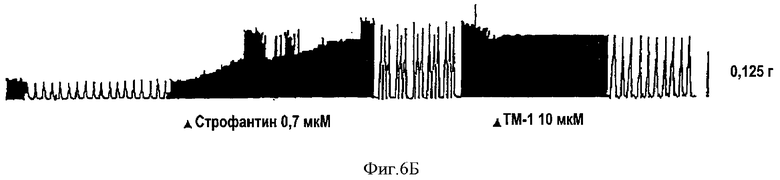
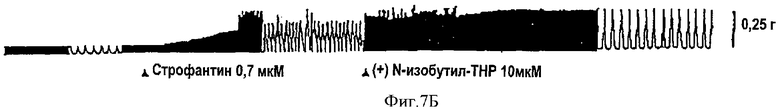
На фиг.6-7 показаны диаграммы аритмии, вызванной с помощью строфантина на полосках правых желудочков морских свинок.
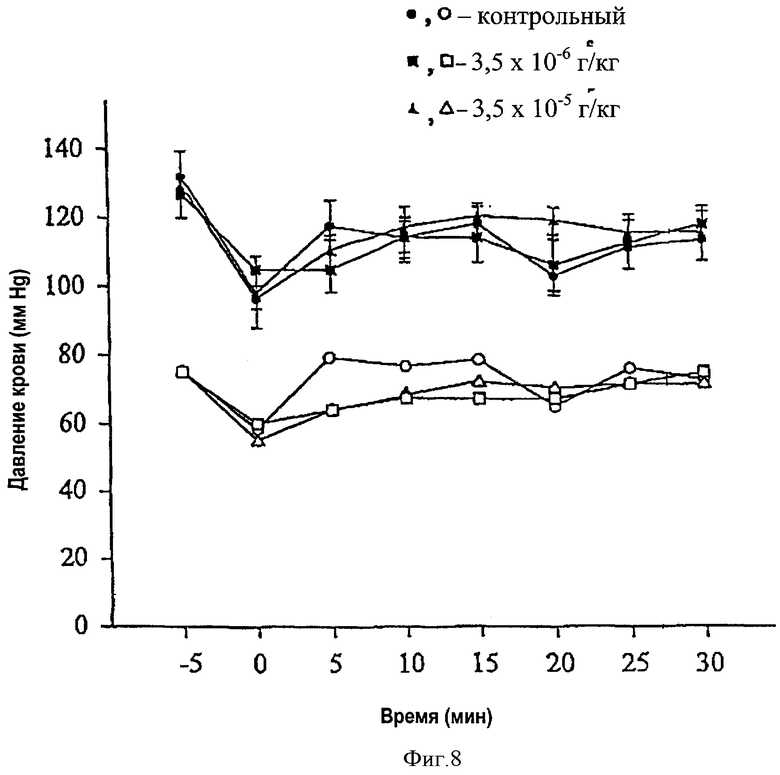
Фиг.8 представляет собой диаграмму систолического и диастолического кровяного давления крыс, коронарные сосуды которых были лигированы на 30 мин; диаграмма представлена для животных из контрольной группы и группы, получавшей талипорфин. Разница между контролем и двумя концентрациями талипорфина была статистически несущественна.
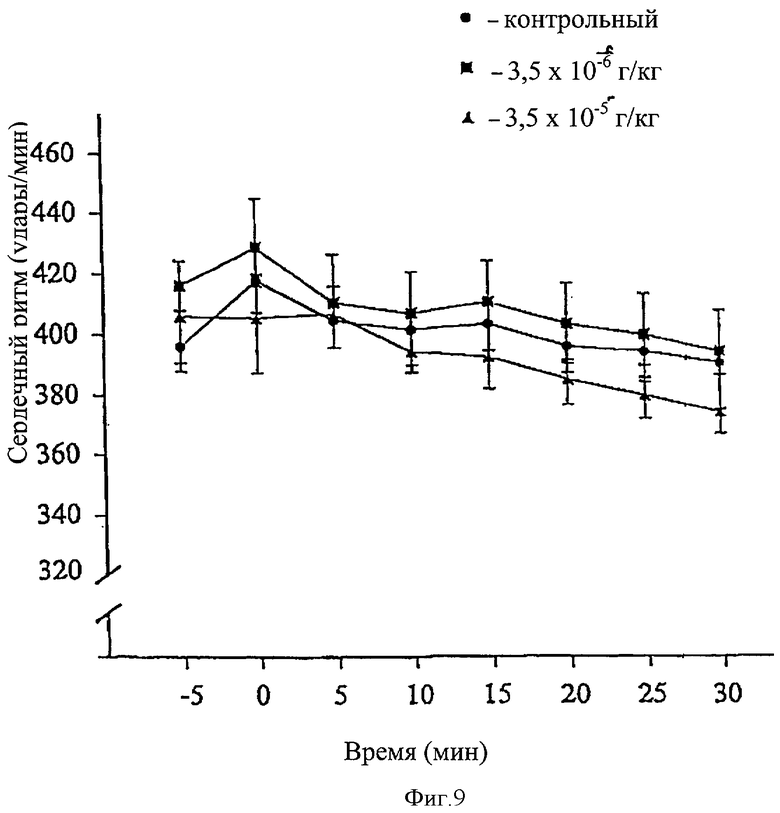
Фиг.9 представляет собой диаграмму сердечного ритма крыс, коронарные сосуды которых были лигированы на 30 мин; диаграмма представлена для животных из контрольной группы и группы, получавшей талипорфин. Разница между контролем и двумя концентрациями талипорфина была статистически несущественна.
Подробное описание настоящего изобретения
Талипорфин (далее для его обозначения используют аббревиатуру ТНР) представляет собой природное соединение фенольного алкалоида апорфина, выделяемого из растений нескольких семейств, типа Lauraceae. Предыдущими исследованиями выявлено, что ТНР является частичным агонистом кальциевого (Са+2) канала и обладает сильными блокирующими активностями Na+ и K+ каналов. Несмотря на то, что при кардиальной ишемии или ишемической реперфузии блокирующие активности ТНР Na+ и K+ каналов способны уменьшить частоту и тяжесть аритмии, однако активирование указанным средством кальциевого канала может увеличить перегрузку и вызвать аритмию в процессе ишемии или ишемической реперфузии.
В вариантах настоящего изобретения влияние ТНР или его производных на аритмию при глобальной ишемической реперфузии изучалось на изолированных сердцах морских свинок; полученные результаты сравнивали с традиционной моделью на крысах для случая лигированной реперфузии.
В другом варианте настоящего изобретения в модели на морских свинках использовали 0,6-0,8 мкМ строфантина для подавления Na+/K+ насоса в целях усиления сердечных сокращений и индуцирования аритмии при последующем введении ТНР или его производных; эти исследования проводили для оценки влияния строфантина на индуцированную аритмию.
В альтернативном варианте настоящего изобретения для того, чтобы наблюдать за выживаемостью, степенью аритмии и ее тяжестью in vivo при сердечной ишемии или ишемической реперфузии, а также диапазоном некроза миокарды при сердечной ишемии, проводилось внутривенное введение ТНР.
Помимо этого, было проведено сравнение ТНР с современными антиаритмическими лекарственными средствами; сравнение проводили по электрофизиологическому воздействию на крыс и морских свинок, для этого оценивали захват свободных радикалов с помощью ТНР или его производных и выявляли изменения концентрации лактатдегидрогеназы в крови животных. Увеличение концентрации лактатдегидрогеназы может служить индикатором повреждения миокарды. Кроме того, в настоящем изобретении оценивается также влияние ТНР или его производных на продуцирование оксида азота (NO) в крови животных в процессе кардиальной ишемии или ишемической реперфузии.
Согласно одному аспекту настоящего изобретения фармацевтический состав, содержащий ТНР или его производные, или их сложные эфиры, или их фармацевтически приемлемые соли, вводился нуждающемуся в этом пациенту перорально или инъекционно. Дополнительно указанный фармацевтический состав, предназначенный для перорального или инъекционного введения нуждающемуся в этом пациенту, может также содержать фармацевтически приемлемый носитель или наполнитель. Рецептура таких фармацевтических составов хорошо известна людям, квалифицированным в данной области знаний.
Используемые здесь фармацевтически приемлемые соли включают соли неорганических кислот, такие как гидрохлориды, гидробромиды, сульфаты и фосфаты; соли органических кислот, такие как ацетат, малеат, тартрат, метансульфонат; а также соли аминокислот, такие как соли аргинина, аспартамовой и глутаминовой кислоты. Пригодные фармацевтические формы включают стерильные водные растворы или дисперсии, стерильные порошки, таблетки, пилюли, капсулы и им подобные. Помимо этого, активнодействующие соединения могут входить в препараты и составы с отсроченным высвобождением. Фармацевтически приемлемые носители включают любой и все растворители, расщепляющие средства, связующие, наполнители, скользящие вещества, замедляющие абсорбцию средства и т.п. Поскольку соединение по настоящему изобретению может также представлять собой сложный эфир, то безусловно, что такие сложные эфиры также входят в границы настоящего изобретения.
Ниже настоящее изобретение будет проиллюстрировано примерами, назначением которых не является никакая степень его ограничения.
Пример 1: получение талипорфина
1. Получение норглауцина
Для получения экстракта, богатого (+)-лауролитсином, стебли Phoebe formosana Hayata экстрагировали 2% уксусной кислотой (60°С, трижды). К 50 г неочищенного (+)-лауролитсина в 500 мл реакционную колбу добавили 250 мл N,N-диметилформамида (ДМФ) и 40 мл этилформиата. Полученную смесь перемешивали в течение 60 ч при 90°С, а затем провели перекристаллизацию метанолом. В результате получили 7,5 г N-формиллауролитсина. Физические характеристики были следующими: т.пл.: 275-277°С; 1Н ЯМР (CD3OD, 400 MHz) δ 8.61, 8.44 (1Н, s, N-CHO), 8.45, 8.40 (1Н, s, H-11), 7.21, 7.16 (1Н, s, H-8), 6.63 (1Н, s, H-3), 3.89 (3Н, s, 10-ОМе), 3.58 (3Н, s, 1-OMe); EIWS (70 eV) m/z (rel. int. %) 341(90), 296(40), 283(100), 240(30), 58(70).
В реакционную колбу поместили N-формиллауролитсин (10,3 г; 29,4 ммол), метанол (100 мл), карбонат калия (12,3 г) и йодометан (13 мл). Получившуюся смесь дегазировали в течение 2 мин при пониженном давлении, а затем реакционную колбу герметично закрыли. Смесь перемешивали в течение 24 ч при 60°С, после этого провели ее выпаривание при пониженном давлении и распределение между хлороформом (300 мл) и водой (150 мл × 2). Органическую фазу высушили над Na2CO3, отфильтровали и выпаривали при пониженном давлении. Остаток перекристаллизовали из метанола, при этом получили N-формилнорглауцин (9,5 г; 87%) в виде игольчатых кристаллов. Физические характеристики были следующими: т.пл.: 151-152°С; 1H ЯМР (CDCl3, 400 MHz) δ 8.37, 8.23 (1Н, s, N-CHO), 8.12, 8.11 (1Н, s, H-11), 6.78, 6.74 (1Н, s, H-8), 6.63, 6.60 (1Н, s, H-3), 4.46 (dd, J=14.4, 4.3 Hz), 4.89 (1Н, dd, J=13.9, 4.2 Hz, H-6a), 3.90 (9Н, s, 3 х ОМе), 3.65 (3Н, s, 1-OMe); EIMS (70 eV m/z (rel. int %) [M]+ 365(5), 355(100), 340(40).
В 100 мл реакционную колбу поместили N-формилнорглауцин (2,00 г; 5,42 ммол), гидроксид калия (2,30 г; 41,5 ммол) и этанол (50 мл). Смесь нагревали в колбе с обратным холодильником в течение 3 ч (Chastanet J. Et al., Heterocycles, 1992, 34:1565-1572), упаривали при пониженном давлении и провели ее распределение между водой (100 мл) и хлороформом (300 мл × 3). Получившуюся органическую фазу высушили над Na2SO4 и отфильтровали. Затем провели выпаривание при пониженном давлении с получением твердого вещества, очистка которого колоночной хроматографией (силикагель, 0,2% метанол/хлороформ в качестве элюанта) привела к (+)-норглауцину (1,75 г; 95%). Физические характеристики были следующими: аморфное твердое вещество; [α]D 24 + 77.1° (с=0.35, CHCl3); 1H ЯМР (CDCl3, 400 MHz) δ 8.09 (1Н, s, H-11), 6.73 (1Н, s, H-8), 6.58 (1Н, s, H-3), 3.90 (3Н, s, 9-ОМе), 3.88 (3Н, s, 10-ОМе), 3.86 (3Н, s, 2-OMe), 3.65 (3Н, s, 1-OMe), 3.81 (1Н, dd, J=13.9, 4.2 Hz, H-6a); HR LC/MS m/z [M+H]+ 342.1682 (вычислено для C20H24NO4 342.1705).
2. Получение (+)-талипорфина (ТНР)
В 250 мл реакционную колбу последовательно загрузили норглауцин (1,90 г; 5,2 ммол), метанол (50 мл) и 35,5% формальдегид (6,0 мл). К этой смеси при перемешивании порциями при комнатной температуре добавляли NaBH4 (суммарное количество 2,0 г; 52 ммол). Получившуюся смесь оставили для взаимодействия на 6 ч, выпарили при пониженном давлении, а затем провели распределение между водой (150 мл) и хлороформом (150 мл × 3). Органическую фазу промыли солевым раствором, высушили над Na2SO4, отфильтровали и выпарили при пониженном давлении. Полученное твердое вещество очистили колоночной хроматографией (силикагель, хлороформ в качестве элюанта), получив в результате глауцин (1,78 г; 90%) в виде твердого вещества. Физические характеристики были следующими: т. пл.: 112-114°С (диэтиловый эфир); [α]D 24 + 120.0° (с - 0.30, МеОН); 1H ЯМР (CDCl3, 400 MHz) δ 8.06 (1Н, s, H-11), 6.75 (1Н, s, H-8), 6.56 (1Н, s, H-3), 3.91 (3Н, s, 9-OMe), 3.88 (3Н, s, 10-ОМе), 3.86 (3Н, s, 2-OMe), 3.64 [3Н, s, 1-OMe), 2.54 (3Н, s, N-Me).
В 100 мл реакционную колбу, содержащую глауцин (3,02 г; 8,45 ммол), добавили 6,0 мл 90% серной кислоты в среде водяной бани (Castedo L. et al., Heterocycles, 1980, 14:1135-1138). Получившуюся смесь вакуумировали при пониженном давлении в течение 2 мин, а затем реакционную колбу герметично закрыли. После перемешивания в течение 13 суток в темноте при комнатной температуре реакционную смесь при перемешивании вылили в сосуд, содержащий 100 мл ледяной воды. Смесь оттитровали водным раствором аммиака (25%) до рН 8,0, а затем провели экстрагирование хлороформом (80 мл × 3). Органическую фазу высушили над Na2SO4, отфильтровали и выпарили при пониженном давлении. Полученный осадок (3,48 г) очистили методом колоночной хроматографии (силикагель, 1-3% метанол/хлороформ в качестве элюанта), получив в результате талипорфин (1,82 г; выход 62%). Физические характеристики были следующими: т.пл.: 185-187°С (МеОН); [α]D 24 + 66.7° (с=0.31, МеОН); 1Н ЯМР (CDCl3, 400 MHz) δ 8.03 (1Н, s, H-11), 6-76 (1Н, s, H-8), 6.52 (1H, s, H-3), 3.90 (6Н, s, 2-Ome and 9-ОМе), 3.88 (3Н, s, 10-ОМе), 2.53 (3Н, s, N-Me); EIMS (70 eV) m/z (rel. int. %) [M]+ 341(100), 326(34), 298(24), 267(28).
Пример 2: получение (+)-N-пропилнорталипорфина
1. Получение (+)-N-пропилнорглауцина
Согласно способу получения N-формиллауролитсина, описанному в примере 1, 30 г неочищенного лауролитсина растворили в смеси диметилформамида (75 мл) и пропионового ангидрида (6 мл). Смесь оставили для взаимодействия на 24 ч при комнатной температуре, а затем провели перекристаллизацию из ментола, получив в результате 8,02 г N-пропиониллауролитсина. Физические характеристики были следующими: т.пл.: 185-189°С; 1H ЯМР (CD3OD, 400 MHz) δ 8.06 (1Н, s, H-11), 3.71 (1Н, s, H-8), 6.61 (1Н, s, H-3), 3.88 (3Н, s, 10-ОМе), 3.59 (3Н, s, 1-OMe), 2.52 (2Н, q, J=7.2 Hz, NCOCH2CH3), 1.16 (3Н, t, J=7.2 Hz, NCOCH2CH3); EIMS (70 eV) m/z (rel. int. %) [M]+ 369(100), 296(87), 283(85), 269(44), 240(16), 57(34).
К смеси N-пропиониллауролитсина (2,50 г; 6,78 ммол), метанола (125 мл) и карбоната калия (2,60 г) добавили йодометан (3,5 мл; 56,2 ммол). При соблюдении аналогичных условий реакции и следуя способу, описанному в примере 1, был получен N-пропионилнорглауцин (2,21 г; 82,4%). Физические характеристики были следующими: т.пл.: 150-152°С (МеОН); 1H ЯМР (CDCl3, 400 MHz) δ 8.13 (1H, s, H-11), 6.76 (1H, s, H-8), 6.60 (1H, s, H-3), 3.89 (3Н, s, 9-OMe), 3.87 (6H, s, 2-Ome or 10-OMe), 3.59 (3Н, s, 1-OMe), 2.45 (2H, q, J=7.2 Hz, NCOCH2CH3), 1.18 (3Н, t, J=7.2 Hz, NCOCH2CH3); EIMS (7C eV) m/z (rel. int. %) [M]+ 397(79), 324(58), 311(100), 265(16), 57(20).
В сухую реакционную колбу последовательно добавили безводный тетрагидрофуран (15 мл) и LiAlH4 (380 мг; 10 ммол), смесь перемешивали в течение 10 мин. К полученной взвеси каплями добавляли раствор N-пропионилнорглауцина (4,01 г; 10,1 ммол) в безводном тетрагидрофуране (5 мл). Получившуюся смесь нагревали при перегонке в колбе с обратным холодильником в течение 2 ч. Для того чтобы разрушить избыток LiAlH4, к указанной смеси на ледяной бане добавили Na2SO4·10Н2О. После этого смесь отфильтровали через целитную подкладку, а остаток промыли хлороформом. Объединили фильтрат и промывные воды, выпарили их и перекристаллизовали с диэтиловым эфиром, в результате был получен N-пропилнорглауцин (3,36 г; 86%). Физические характеристики были следующими: т.пл.: 95-97°С; [α]D 24 + 106.7° (с=0.33, МеОН); 1H ЯМР (CDCl3, 400 MHz) δ 8.03 (1Н, s, H-11), 6.75 (1Н, s, H-8), 6.54 (1Н, s, H-3), 3.86 (3Н, s, 9-OMe), 3.83 (6Н, s, 2-Ome or 10-OMe), 3.60 (3H, s, 1-OMe), 2.88 and 2.43 (2H, m, N-CH2C2H5), 1.50 (2H, m, N-CH2CH2CH3), 0.93 (3H, t, J=7.2 Hz, N-С2Н4СН3); EIMS (70 eV) m/z (rel. int. %) [M]+ 383(100), 368(82), 354(45), 352(36), 281(19).
2. Получение (+)-пропилнорталипорфина
Провели взаимодействие N-пропилнорглауцина (1,20 г; 10,3 ммол) с 90% серной кислотой (3 мл), реакцию осуществляли в соответствии со способом получения (+)-ТНР, описанным в примере 1. В результате был получен (+)-пропилнорталипорфин (346 мг; выход 30%). Физические характеристики были следующими: т.пл.: 66-70°С (МеОН); [α]D 24 + 60.2° (с=0.33, МеОН); 1Н ЯМР (CDCl3, 400 MHz) δ 8.00 (1Н, s, H-11), 6.75 (1Н, s, H-8), 6.51 (1Н, s, H-3), 3.90 (6Н, s, 2-Ome or 9-OMe), 3.89 (3H, s, 10-OMe), 2.60 (1Н, m) and 2.43 (1Н, m) (N-CH2CH3), 1.57 (2H, m, N-CH2СН2СН3), 0.95 (3H, t, J=7.2 Hz, N-С2Н4СН3); EIMS (70 eV) m/z (rel. int. %) [M]+ 369(100), 354(22), 340(36), 298(20).
Пример 3: электрофизиологическое воздействие ТНР на крыс и морских свинок
Профиль электрограмм
Исследования проводили в соответствии с «Руководством по уходу за лабораторными животными и использованию их», опубликованным Национальным Институтом здравоохранения США (публикация Национального Института здравоохранения США, №85-23, пересмотренная в 1996 г.). После гепаринизации и анестезии взрослых особей крыс и морских свинок с помощью уретана (1,25 г/кг) их умерщвляли. После выделения сердца проводили перфузию аорты, используя для этого 10 мкМ гуанидина и ТНР соответственно. В целях регистрации электрограммы пучка Гиса на верхушку треугольника Коха поместили пару биполярных электродов, соединенных серебряной проволочкой. Помимо этого, для записи Т-волны другую пару биполярных электродов, соединенных серебряной проволочкой, поместили на поверхность правого желудочка. Электростимуляция правого предсердия в области верхней полой вены проводилась циклом продолжительностью 300 мс. С помощью электрокардиографа были записаны интервал QT, время проводимости по синусо-предсердному участку (интервал SA), предсердно-желудочковому узлу (интервал АН), системе Гиса-Пуркинье (интервал HV). Аналогичным образом были записаны кривая восстановления системы Гиса-Пуркинье (а именно, соотношение H2V2 и V1H2), а также предсердный и желудочковый рефракторный период и рефракторный период узла AV. Полученные результаты приведены на фиг.1 и фиг.2.
Пример 4: антиоксидантная активность и активность в отношении захвата свободных радикалов ТНР или его производных
Было проведено предварительное инкубирование липопротеинов человека низкой плотности (LDL, 100 мкг/мл) с диметилсульфоксидом (0,1%, базальный и контрольный) или с различными концентрациями ТНР. Процесс проводили в течение 10 мин при 37°С, затем добавили CuSO4 (кроме базальной). Для того чтобы определить влияние ТНР на перокисление липидов, инкубирование продолжили в течение дополнительных 12 ч. Полученные результаты приведены на фиг.3.
После инкубирования различных концентраций ТНР с 1,1-дифенил-2-пикрилгидразилом (DPPH, 100 мкМ) в течение 30 мин при комнатной температуре (25°С) измерили снижение абсорбции DPPH. Измерения проводили при 517 нм. В результате была построена кривая зависимости дозы ТНР на захват радикалов DPPH. Полученные результаты приведены на фиг.4.
Пример 5: антиаритмическое действие ТНР или его производных
1. Аритмия у крыс, вызванная лигированием-реперфузией
Для индуцирования ишемии миокарды на изолированном сердце крысы было проведено лигирование путем временного затягивания шелковой лигатуры вокруг главной левой коронарной артерии. Реперфузия достигалась при высвобождении напряжения на лигатуре, используемого для индуцирования аритмии. После этого ввели 10 мкМ ТНР и зарегистрировали желудочковую и предсердную электрограммы. Полученные результаты приведены на фиг.5.
2. Аритмия у морских свинок, вызванная глобальной ишемией-реперфузией
Изолированное сердце морских свинок лигировали при глобальной ишемии. Реперфузия достигалась при высвобождении напряжения, приложенного к лигатуре. После этого были введены различные концентрации ТНР, а затем регистрировали желудочковую фибрилляцию (VF). Полученные результаты приведены в таблице 1.
Влияние ТНР на вызванную реперфузией желудочковую фибрилляцию изолированного сердца морских свинок при глобальной ишемии
3. Аритмия у морских свинок, вызванная строфантином
После того, как 0,6-0,8 мкМ строфантина ввели в желудочки морских свинок, наблюдалось усиление сокращений. Спустя 10 мин была индуцирована аритмия. Для аннулирования аритмии, вызванной строфантином, ввели 10-20 мкМ ТНР или его производных. Полученные результаты приведены на фиг.6-7.
4. Клинические использования ТНР для крыс
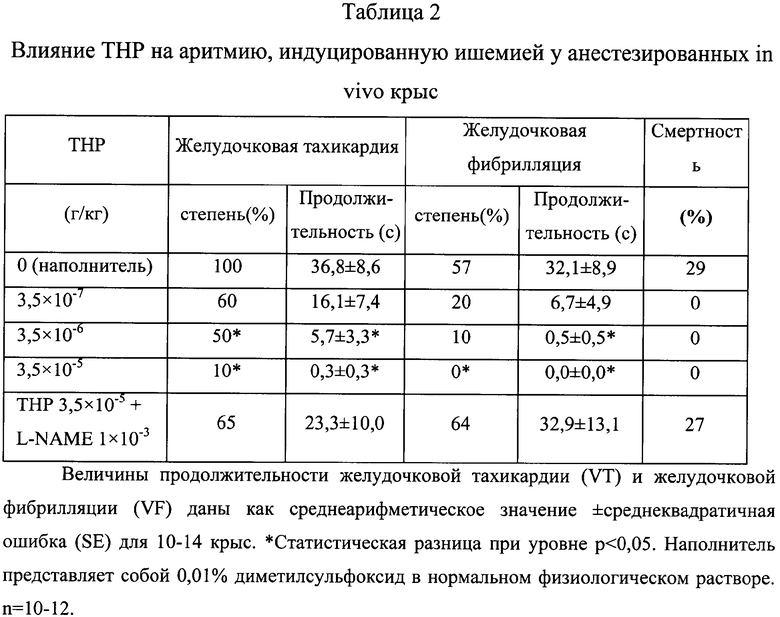
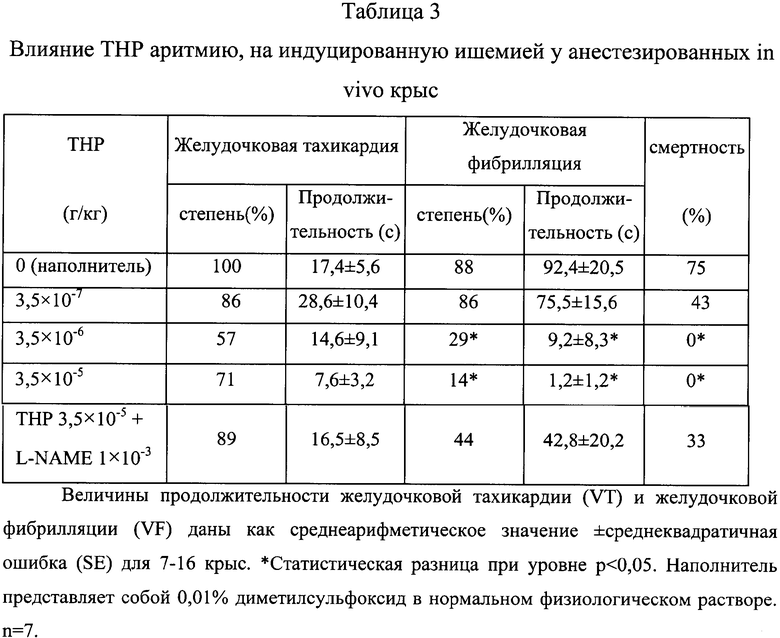
Для того чтобы вызвать ишемию миокарды, провели лигирование путем временного затягивания шелковой лигатуры вокруг главной левой коронарной артерии. Реперфузия достигалась при высвобождении напряжения на лигатуре, используемого для индуцирования аритмии (группы, подвергнутые операции). Мнимо оперированные животные прошли все хирургические манипуляции, за исключением того факта, что шелк, прошедший вокруг левой коронарной артерии, не был завязан (мнимо оперированные группы). За 15 мин до наступления коронарной окклюзии животным через яремную вену провели инфузию болюсом ТНР (3,5×10-7, 3,5×10-6, 3,5×10-5 г/кг), L-NAME (метиловый эфир Nω-нитро-L-аргинина; 1×10-3 г/кг) или наполнителя (диметилсульфоксид / NaCl 0,9%, 1:103; объем/объем). Окклюзия коронарной артерии продолжалась в течение 30 мин или 5 мин, после этого наступала 30 мин реперфузия. Затем животных случайным образом разделили на следующие группы: (1) мнимо оперированные + наполнитель; (2) мнимо оперированные + ТНР (3,5×10-5 г/кг); (3) оперированные + наполнитель; (4) оперированные + ТНР (3,5×10-7 г/кг); (5) оперированные + ТНР (3,5×10-6 г/кг); (6) оперированные + ТНР (3,5×10-5 г/кг); (7) оперированные + L-NAME (1×10-3 г/кг) + ТНР (3,5×10-5 г/кг). До наступления ишемии или периода реперфузии, а также во время этих процессов проводилась регистрация сердечного ритма (HR), кровяного давления (ВР), а также изменений на электрокардиограмме (ЭКГ). Эктопическую активность желудочка оценивали по диагностическому критерию, поддержанному Лэмбетской конвенцией. У оставшихся в живых животных фиксировали степень и продолжительность желудочковой аритмии, включая желудочковую тахикардию (VT) и желудочковую фибрилляцию (VF). Для того чтобы проанализировать различие по продолжительности VT и VF среди групп животных, получавших лекарственные средства и наполнитель, был использован тест Манна-Уитни. При изучении аритмии изменения кровяного давления и сердечного ритма у крыс, получавших лекарственные средства, и у крыс, получавших наполнитель, анализ проводили сначала с помощью теста ANOVA (анализ вариантов), а затем по тесту Бонферрони. Процентное различие случаев желудочковой тахикардии, желудочковой фибрилляции и коэффициента смертности анализировали методом хи-квадрат. Полученные результаты приведены в таблицах 2-3.
Объем инфаркта определяли по методике окрашивания синим хлоридом тетразолия. После окклюзии в течение 4 ч левой нисходящей коронарной артерии животные были умерщвлены. Объем инфарктной ткани выражен как процент от общего объема желудочка или зоны окклюзии. Статистический анализ разницы в оценке объема инфаркта проводился по критерию Стьюдента. Полученные результаты приведены в таблице 4.
Зона риска и объем инфаркта желудочка крыс, получавших обработку ТНР после 4-часового коронарного лигирования
L-NAME 1×10-3
Повреждение клеток оценивали по измерениям лактатдегидрогеназы в плазме. Образцы артериальной крови отбирали по окончании ишемии или ишемической реперфузии из катетера сонной артерии, затем их поместили в гепаринизированные пробирки. Кровь сохраняли при 4°С вплоть до ее центрифугирования, проводимого при 2000 g в течение 15 мин. Плазму восстановили, а ее аликвоты были использованы для определения активности лактатдегидрогеназы, которое проводили с помощью стандартного набора фирмы Sigma. Образцы депротеинизированной плазмы заморозили и выдерживали до анализа. Определение NO проводили по хемилюминесцентной методике NO/озон, описанной в работе Yanu F. et al., (1997) Clin.Chem. 43:657-662. Различие в содержании NO и лактатдегидрогеназы в плазме оценивали статистически по методу Стьюдента. Полученные результаты приведены в таблицах 5-6.
Влияние ТНР на высвобождение лактатдегидрогеназы (мкмол/л)
Влияние ТНР на высвобождение NO (мкмол/л)
Если сердце обрабатывали хинидином, то синусо-предсердный интервал (SA), предсердно-желудочковый интервал (АН), интервал Гиса-Пуркинье (HV), а также Т волны были более протяженными (фиг.1). При использовании ТНР интервал SA остался таким же, а интервал HV стал слегка более протяженным, чем в случае с хинидином; этот факт указывает на то, что хинидин обладает слабой селективностью. Помимо этого, 3,10 и 30 мкМ ТНР способны пролонгировать эффективный предсердный рефракторный период (AERP) с 60 мс до 90, 100 и 120 мс соответственно; пролонгировать эффективный желудочковый рефракторный период (VERP) со 160 мс до 160, 170 и 190 мс соответственно; а эффективный рефракторный предсердно-желудочковый период (AVNERP) со 170 мс до 170, 200 и 240 мс соответственно. При аналогичном сравнении 3, 10 и 30 мкМ хинидина способны пролонгировать период AERP с 40 мс до 60, 80 и 130 мс соответственно; период VERP со 180 мс до 170, 180 и 190 мс; период AVNERP со 130 мс до 150, 200 и 245 мс соответственно. Кроме того, 3, 10 и 30 мкМ ТНР могут изменить продолжительность цикла Венкебаха (WCL) с 200 мс до 210, 230 и 280 мс соответственно; в то время как 3, 10 и 30 мкМ хинидина способны изменить продолжительность указанного цикла со 150 мс до 170, 210 и 300 мс соответственно. Как ТНР, так и хинидин пролонгируют периоды AERP, VERP и AVNERP, однако только хинидин подавляет проводимость узла AV (удлиненный интервал АН). Напротив, даже если концентрация ТНР поднимается до 10 мкМ, то при этом проводимость в узле AV не подавляется.
Более того, 3-10 мкМ ТНР пролонгирует продолжительность потенциала действия предсердий и желудочков как у крыс, так и у морских свинок. Помимо этого, ТНР способен значительно подавлять транзиторный внешний ток калия у крыс, а также запаздывающий внешний ток калия у морских свинок. Было обнаружено также, что ТНР может подавлять внутренний ток натрия, но усиливает внутренний ток кальция (Su MJ et al., Eur. J. Pharmacol., 1994, 254:141-150). Таким образом, ТНР обладает способностью пролонгировать потенциал действия, усиливать сокращения сердца, а также снижать сердечный ритм.
Влияние ТНР на перокисление липидов оценивалось также по его действию на образование химически активной тиобарбитуровой кислоты (TBARS) из липопротеинов низкой плотности (LDL). Действие CuSO4 на липопротеины низкой плотности в течение 12 ч приводит к их перокислению, на что указывает увеличение концентрации TBARS (фиг.3). Дополнительное введение ТНР подавляет образование TBARS, этот процесс зависит от концентрации ТНР (IC50, 15,7 мкмол/л). Помимо антиокисления LDL, ТНР способен к захвату аниона пероксида, продуцируемого системой ксантин/ксантиноксидаза, этот процесс зависит от концентрации (ЕС50 составляет 12,6 мкМ).
В системе 1,1-дифенил-2-пикрилгидразила (DPPH) активность ТНР по захвату свободных радикалов оценивается как IC0,200. После улавливания неспаренных электронов DPPH путем введения ТНР проводили мониторинг снижения оптического поглощения, процесс осуществляли при 517 нм. На фиг.4 изображена картина захвата DPPH с помощью ТНР, указанный процесс зависит от концентрации, IC0,200 составляет 12,4 мкмол/л.
ТНР в дозе 3-30 мкМ может быть эффективен для снятия аритмии, возникшей на изолированном сердце крысы в результате 30 мин лигирования и последующей реперфузии при IC50, составляющей 15,7 мкмол/л. Аналогичным образом, 10 мкМ ТНР могут быть эффективны для подавления аритмии, возникшей на изолированном сердце морской свинки в результате глобальной ишемии с последующей реперфузией (таблица 1). Строения коронарных артерий крыс и морских свинок различаются, однако ТНР способен быть эффективным при подавлении аритмии, индуцированной на изолированных сердцах обоих этих животных в результате ишемической реперфузии.
Обратимся к фиг.6, 7. После введения 0,6-0,8 мкМ строфантина в желудочек морских свинок наблюдалось усиление сердечных сокращений. Спустя 5-10 мин индуцировалась аритмия. Для подавления аритмии может быть эффективным введение 10-20 мкМ ТНР или его производных, такая же концентрация хинидина не выявляет аналогичной эффективности (данные не приведены).
Внутривенное введение ТНР крысам, перенесшим ишемию миокарды, не приводило к изменению диастолического и систолического кровяного давления, а также сердечного ритма (HR) (фиг.8, 9). Существенной разницы между группами, получавшими наполнитель, и группами, получавшими лекарственные средства (3,5×10-6 или 3,5×10-5 г/кг ТНР), не отмечалось.
В группе, получавшей наполнитель в условиях ишемии, тяжелая желудочковая аритмия возникала спустя 6-7 мин после окклюзии коронарной артерии, она достигала пика спустя 8-12 мин и ослабевала спустя приблизительно 15 мин после начала. Было вычислено, что продолжительность желудочковой фибрилляции составила 32,1±8,9 с, а продолжительность желудочковой тахикардии - 36,8±8,6 с. У находящихся в группе из 14 крыс, получавших наполнитель, желудочковая фибрилляция наблюдалась у 57% животных, в то время как желудочковая тахикардия - у 100% животных. Введение ТНР в дозе 3,5×10-5 г/кг вызвало снижение степени желудочковой тахикардии и желудочковой фибрилляции до 10% и 0% соответственно (р<0,05). Продолжительность желудочковой тахикардии и желудочковой фибрилляции значительно снизилась, эти величины составили 0,3±0,3 и 0,0±0,0 с соответственно (р<0,05). Особенно важной чертой является очень эффективное снижение смертности, происходящее даже при очень низких дозах ТНР - 3,5×10-7 г/кг. Помимо этого, в группе, получавшей L-NAME+THP, степень и продолжительность желудочковой тахикардии и желудочковой фибрилляции, а также смертность не отличались от измерений, сделанных в контрольной группе (оперированные-наполнитель); это свидетельствует, что L-NAME (1×10-3 г/кг) полностью уничтожает антиаритмическое действие ТНР, а также его эффективное снижение смертности (таблица 2).
Тяжесть аритмии, вызванной реперфузией, в существенной степени зависит от продолжительности периода, предшествующего ишемии. Поэтому для того чтобы получить наивысшую степень нарушения ритма, был выбран протокол с 5 мин периодом ишемии при последующем 30 мин периоде реперфузии. В таблице 3 показано, что в группе, получавшей наполнитель, в период реперфузии приблизительно у 88% животных наблюдалась желудочковая фибрилляция, а 75% из них умерли, преимущественно от желудочковой фибрилляции. Напротив, у животных, предварительно получавших ТНР (3,5×10-6 и 3,5×10-5 г/кг), было выявлено интенсивное снижение степени желудочковой фибрилляции с 88% до 29% и 13% (р<0,05), а также снижение продолжительности желудочковой фибрилляции с 92,4±20,5 с до 9,2±8,3 и 1,2±1,2 с (р<0,05). При использовании ТНР в дозе 3,5×10-6 г/кг процент смертности также снизился с 75% до 0% (р<0,05). Однако совместное введение L-NAME с талипорфином (3,5×10-5 г/кг) только частично препятствует его антиаритмическому действию, а также его действию по предотвращению смертности.
Была сделана оценка зоны ишемии и объема инфаркта спустя 4 ч после ишемии, исследования проводились по методике окрашивания. Для каждой из экспериментальных групп зоны риска существенно не различались (таблица 4); это указывает на тот факт, что при окклюзии левой коронарной артерии в каждой группе риску подвержен одинаковый объем тканей. В группе, получавшей наполнитель, зона некроза выражается или как процент от зоны риска (45,2±1,0%), или как процент от общего объема желудочка (19,8±2,2%), определяя тот объем ткани сердца, который в случае риска становится некротическим. Введение ТНР снижает распространение некроза миокарды, причем это снижение зависит от вводимой дозы. Указанное снижение наблюдается или в виде соотношения зона некроза/зона риска (38,1±5,0%; 29,0±2,5% и 10,7±8%) для доз ТНР, составляющих 3,5×10-7, 3,5×10-6, 3,5×10-5 г/кг соответственно; или в виде соотношения зона некроза/общий объем желудочка (17,9±2,3%; 13,4±2% и 10,7±8%) для доз ТНР, составляющих 3,5×10-7; 3,5×10-6; 3,5×10-5 г/кг соответственно. Однако в группе, получавшей L-NAME+THP, объем инфаркта не отличался от величины, наблюдаемой для контрольной группы (оперированные-наполнитель), это означает, что действие L-NAME (1 мг/кг) полностью уничтожает воздействие ТНР (3,5×10-5 г/кг), угнетающее инфаркт.
Биохимические показатели повреждения клеток (высвобождение лактатдегидрогеназы, LDH) определяли в период ишемии, а также в период реперфузии. Низкую активность лактатдегидрогеназы можно было наблюдать в контрольной группе перед окклюзией (123,6±20,6 мкмол/л). В плазме крыс из группы оперированные-наполнитель наблюдалось значительное увеличение указанного фермента (500,5±81,4 мкмол/л и 273,7±29,2 мкмол/л соответственно) после окклюзии или после окклюзии-реперфузии. Однако введение ТНР во время ишемии или ишемической реперфузии ослабляет высвобождение лактатдегидрогеназы, причем это ослабление зависит от дозы препарата (таблица 5).
Высвобождение оксида азота (NO) определяют по наличию в плазме животных нитрита (NO2 -) и нитрата (NO3 -), анализ проводят для животных с 30 мин ишемией или спустя 5 мин после 30 мин реперфузии. Согласно измерениям оказалось, что в группе мнимо оперированных животных для животных, обработанных заранее ТНР, и для необработанных животных содержание NO составило 9,6±2,3 и 7,6±0,9 мкм/л соответственно. ТНР создает у оперированных животных очень резкое увеличение NO в плазме; при дозе в 3,5×10-6 г/кг наблюдалось 2- и 3,5-кратное увеличение по сравнению с необработанными (наполнитель) животными или с животными с ишемической реперфузией соответственно (таблица 6).
И наконец, настоящее изобретение демонстрирует, что ТНР и его производные не только подавляют тяжесть желудочковой аритмии, вызванной ишемией, или реперфузии, но эти соединения также снижают объем инфаркта после продолжительной коронарной окклюзии. Одновременно ТНР и его производные повышают концентрацию NO и снижают концентрацию лактатдегидрогеназы в крови крыс после локальной ишемии или реперфузии. Как отмечалось выше, оказалось, что многие традиционные антиаритмические лекарственные средства могут вызывать побочные действия, а также они менее эффективны при аритмии, вызванной реперфузией. Успешное полифакторное действие ТНР и его производных по настоящему изобретению дает возможность применения их в качестве эффективных антиаритмических и кардиопротекторных средств.
Несмотря на то, что частные случаи настоящего изобретения были показаны и описаны со ссылкой на его предпочтительные варианты, однако квалифицированным в данной области знаний людям должно быть понятно, что без отступления от сущности и границ настоящего изобретения возможны изменения, различные по форме и деталям.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ПРОТИВОФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2136667C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМ ДЕЙСТВИЕМ | 2019 |
|
RU2700263C1 |
| ПРИМЕНЕНИЕ КАУРАНОВЫХ СОЕДИНЕНИЙ В ПРОИЗВОДСТВЕ МЕДИКАМЕНТОВ | 2004 |
|
RU2345761C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИИШЕМИЧЕСКОЙ, ГИПОТЕНЗИВНОЙ, ПРОТИВОАРИТМИЧЕСКОЙ И НООТРОПНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2216322C1 |
| СРЕДСТВО, УВЕЛИЧИВАЮЩЕЕ УСТОЙЧИВОСТЬ СЕРДЦА К АРИТМОГЕННОМУ ДЕЙСТВИЮ ИШЕМИИ И РЕПЕРФУЗИИ | 2014 |
|
RU2587783C1 |
| КАРДИОПРОТЕКТОРНОЕ И АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 2022 |
|
RU2783444C1 |
| АНТИАРИТМИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2664668C1 |
| СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ, ВОВЛЕКАЮЩИХ МОДУЛЯЦИЮ РЕЦЕПТОРОВ РИАНОДИНА | 2013 |
|
RU2644350C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМ, АНТИФИБРИЛЛЯТОРНЫМ, ПРОТИВОИШЕМИЧЕСКИМ ДЕЙСТВИЕМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2477130C1 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАРИТМИЧЕСКУЮ АКТИВНОСТЬ | 2014 |
|
RU2565404C1 |


Изобретение относится к медицине, а именно к кардиологии, и касается лечения таких заболеваний сердца как сердечная аритмия, ишемия и инфаркт миокарда. Для этого вводят талипорфин в эффективных дозах. Способ обеспечивает эффективное лечение указанной патологии за счет антиаритмического действия талипорфина, а также его способности уменьшать зону ишемии миокарда и увеличивать синтез NO. 6 табл., 9 ил.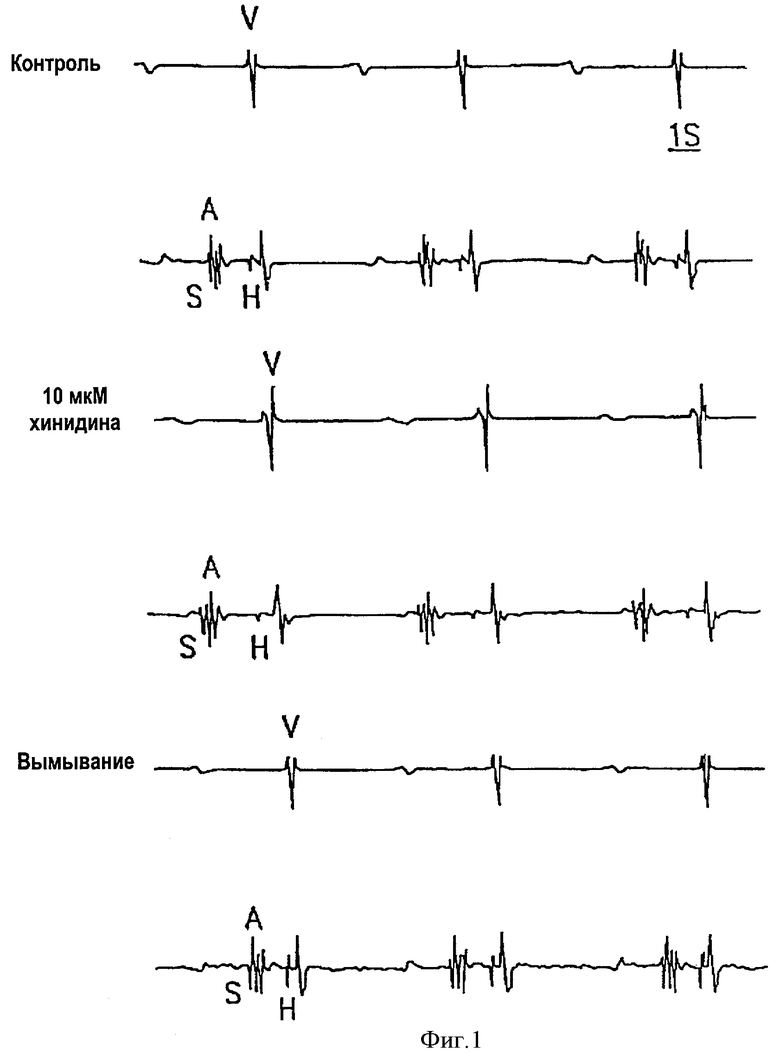
Способ лечения и/или предотвращения заболевания сердца млекопитающих, выбранного из группы, включающей сердечную аритмию, ишемию миокарда или инфаркт миокарда, внезапную смерть, вызванную острым инфарктом миокарда, путем введения указанному млекопитающему эффективного количества талипорфина.
| СУМАРОКОВ А.В | |||
| и др | |||
| Клиническая кардиология | |||
| - М.: Медицина, 1986, с.58-63 | |||
| US 4202980 13.05.1980 | |||
| US 4461895 24.07.1984 | |||
| TENG CM et al | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| SU MJ et al | |||
| "Thaliporohine, a positive inotropic agent with a | |||
Авторы
Даты
2009-03-27—Публикация
2001-02-28—Подача