Изобретение относится к способу получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она (I), который используют в качестве промежуточного продукта для получения биологически активных веществ
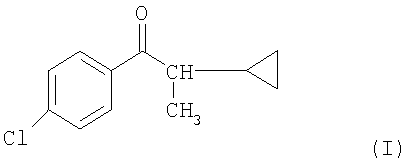
Известен способ получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она (I), заключающийся в том, что:
а) 4-хлорбензальдегид вступает во взаимодействие с реактивом Гриньяра, приготовленным из магния и хлористого кротила, которое приводит к образованию 1-(4-хлорфенил)-2-метил-3-бутен-1-ола;
б) полученный продукт подвергают взаимодействию с дибромметаном, цинковой пылью и однохлористой медью с использованием ультразвука для активации процесса;
в) полученный в результате реакции 1-(4-хлорфенил)-2-циклопропилпропан-1-ол окисляют смесью оксалилхлорида с диметилсульфоксидом в растворе сухого хлористого метилена при температуре -78°С. Получают 1-(4-хлорфенил)-2-циклопропилпропан-1-он (I) (патент СССР №1718722, опубл. 07.03.1992).
Общая схема реакций:
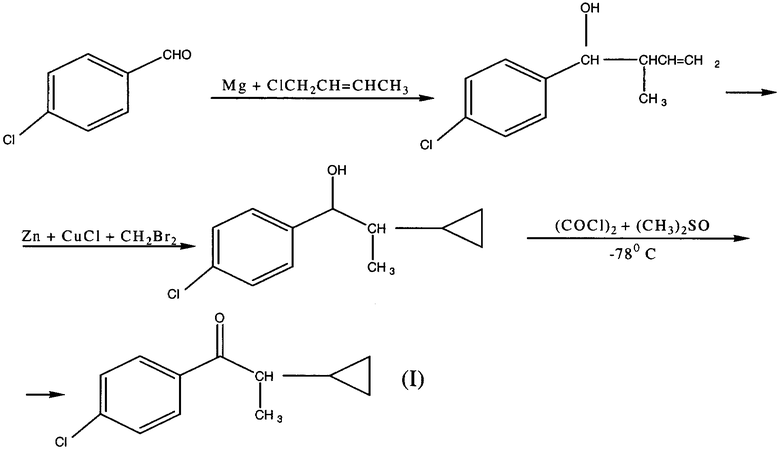
Количество стадий 3, общий выход, считая на исходный 4-хлорбензальдегид, 48-50%.
Основным недостатком способа является необходимость использования токсичного оксалилхлорида и низких температур (-78°С) на последней стадии процесса, а также выделение продуктов реакции на каждой стадии процесса при помощи колоночной хроматографии на SiO2, что создает немалые трудности при реализации процесса в промышленных условиях.
Настоящее изобретение позволяет исключить стадию окисления и в значительной степени упростить и удешевить процесс получения кетона (I). Суть изобретения состоит в том, что 1-(4-хлорфенил)-2-циклопропилпропан-1-он получают циклопропанированием соответствующего непредельного кетона, 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II), который, в свою очередь, получают из 4-хлорбензонитрила и хлористого кротила при действии на него
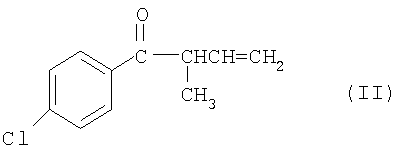
цинка (реакция Барбье) в органическом растворителе в присутствии хлористого алюминия или без него.
Последовательность реакций может быть представлена следующей схемой:
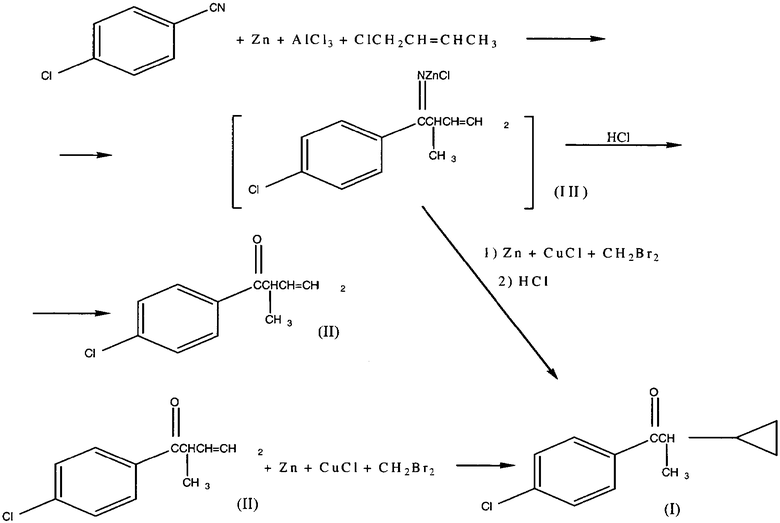
Известен способ получения аллилкетонов путем взаимодействия нитрилов и аллилбромидов с цинком в присутствии хлористого алюминия (Tetrahedron Letters 41, 2000, 8803-8806). Получение 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II), так же как и сам кетон (II), в этой работе не описано.
Известен способ циклопропанирования алкенов при действии на них дибромметана, цинковой пыли и хлорида одновалентной меди в эфире с использованием хлористого ацетила в качестве катализатора (J. Org. Chem., 1990, 55, 2491-2494). Получение 1-(4-хлорфенил)-2-циклопропилпропан-1-она (I) в этой работе также не описано.
Известен также способ получения 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II), заключающийся во взаимодействии 2-бутенилтитантрис (диэтиламида) с имидазолидидом 4-хлорбензойной кислоты в тетрагидрофуране при сильном охлаждении (от -78°С до -25°С). Продолжительность процесса более 12 часов. После завершения реакции реакционную смесь гидролизуют соляной кислотой. Целевой продукт извлекают экстракцией эфиром и очищают перегонкой в высоком вакууме (Chemische Berichte, 118, 348-353, 1985). Этот способ можно использовать в лабораторных условиях, однако трудно реализовать в промышленном масштабе. Других способов получения 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II) в информационных источниках обнаружено не было.
Таким образом, объектом настоящего изобретения является новый способ получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она (I), в котором 4-хлорбензонитрил подвергают взаимодействию с хлористым или бромистым кротилом и цинком и, не обязательно, в присутствии хлористого алюминия в органическом растворителе с получением 1-(4-хлорфенил)-2-метил-3-бутен-1-она. Полученный 1-(4-хлорфенил)-2-метил-3-бутен-1-он вводят в реакцию с дибромметаном, цинком и однохлористой медью в органическом растворителе, в ультразвуковой бане или в присутствии катализатора.
В качестве растворителя на первой стадии можно использовать тетрагидрофуран, диэтиловый эфир, диоксан или их смеси. На второй стадии можно использовать также хлористый метилен, бензол, смесь толуола и диметилового эфира этиленгликоля в соотношении 2:1, а также другие растворители.
В качестве катализаторов на второй стадии используют либо хлористый ацетил, либо триметилхлорсилан, а также натрийборгидрид или натрий-бис-(2-метоксиэтокси)-дигидроалюминат.
В связи с тем, что 1-(4-хлорфенил)-2-метил-3-бутен-1-он разлагается при перегонке в вакууме, была опробована возможность проведения второй стадии, стадии циклопропанирования, с использованием отделенной от осадка реакционной смеси, образовавшейся после завершения реакции 4-хлорбензонитрила, цинка и хлористого кротила и содержащей негидролизованную промежуточную цинковую соль (III) (Ю.К.Юрьев «Практические работы по органической химии. Выпуск I и II»., Издательство Московского Университета, 1964., 274). То есть без выделения 1-(4-хлорфенил)-2-метил-3-бутен-1-она в чистом виде. Оказалось, что таким образом можно получить целевой продукт с выходом 86%, считая на исходный 4-хлорбензонитрил и чистотой по ГЖХ до 84%.
Другим объектом изобретения является способ получения 1-(4-хлорфенил)-2-метил-3-бутен-1-она, заключающийся в том, что 4-хлорбензонитрил подвергают взаимодействию с бромистым или хлористым кротилом и цинковой пылью в растворе тетрагидрофурана в присутствии хлористого алюминия или без него, при температуре от 10°С до 35-40°С. Процесс получения включает стадию выделения и очистки, заключающуюся в том, что после добавления к образовавшейся реакционной смеси не смешивающегося с водой органического растворителя, например гексана, ее обрабатывают 2М соляной кислотой, после чего целевой продукт выделяют из органического слоя известным способом. По сравнению с известным способом (Chemische Berichte, 118, 348-353, 1985) заявляемый способ значительно проще и дешевле.
Далее следуют примеры, иллюстрирующие, но не ограничивающие изобретение.
Пример 1. Получение 1-(4-хлорфенил)-2-метил-3-бутен-1-она.
К раствору 6,78 г (0,05 моль) 4-хлорбензонитрила в 45 мл ТГФ добавляют 13,0 г (0,2 моль) цинковой пыли и охлаждают до 10°С. Затем к реакционной массе добавляют 2,67 г (0,02 моль) хлористого алюминия, температура повышается до 15°С. К полученной суспензии добавляют по каплям раствор 10,12 г (0,075 моль) бромистого кротила в 50 мл ТГФ за 1 час 30 минут. По окончании прибавления реакционную массу перемешивают 3,5 часа при температуре 35-40°С. Затем к реакционной массе добавляют 60 мл гексана и охлаждают ее до 0°С. При этой температуре медленно прибавляют 36 мл 2М соляной кислоты и перемешивают 10 минут. Слои разделяют, органический слой промывают 2М соляной кислотой (2 раза по 35 мл), 5%-ным раствором углекислого натрия (2 раза по 35 мл) и насыщенным раствором хлорида натрия (3 раза по 35 мл). Сушат над сульфатом натрия. Растворитель удаляют. Остаток перегоняют в вакууме. Получают 5,84 г 1-(4-хлорфенил)-2-метил-3-бутен-1-она. Выход 60%, Ткип 100-103°С/0,83 мм Hg. Чистота по ГЖХ 82%. В спектре ПМР, снятом в d-ДМСО наряду с сигналами ароматических протонов, наблюдаемых в области 7,45-7,95 м.д., присутствовал дублет протонов метильной группы в области 1,25 м.д. (d, 3Н), в области 4,15 м.д. (t, 1H) наблюдался триплет винильного протона, в области 5,05-5,20 м.д. (d.d., 2H) присутствовал дублет дублетов метиленовых протонов, а в области 5,80-5,95 м.д. (m, 1H) наблюдался мультиплет метинового протона.
Пример 2. В условиях примера 1, без добавления хлористого алюминия. Получили 5,94 г 1-(4-хлорфенил)-2-метил-3-бутен-1-она. Выход 61%. Чистота по ГЖХ 81,5%.
Пример 3. Получение 1-(4-хлорфенил)-2-метил-3-бутен-1-она.
К раствору 27,5 г (0,2 моль) 4-хлорбензонитрила в 180 мл ТГФ, добавляют 52,0 г (0,8 моль) цинковой пыли и охлаждают реакционную массу до 10°С. Затем к реакционной массе добавляют 10,68 г (0,08 моль) хлористого алюминия, температура реакционной смеси поднимается до 25°С. К полученной суспензии добавляют по каплям 27,15 г (0,3 моль) хлористого кротила в 135 мл ТГФ за 1 час 30 минут. Температура реакционной смеси поднимается до 30°С. Поддерживая температуру реакционной массы 35-40°С, ее перемешивают 4 часа. Затем к реакционной смеси добавляют 210 мл гексана, охлаждают до 0°С и медленно добавляют 160 мл 2М соляной кислоты. Слои разделяют, органический слой промывают 2М соляной кислотой (2 раза по 100 мл), 5%-ным раствором углекислого натрия (2 раза по 120 мл) и насыщенным раствором хлористого натрия (3 раза по 100 мл). Сушат над безводным сульфатом натрия. Растворитель удаляют, а остаток перегоняют в вакууме. Получают 33,84 г 1-(4-хлорфенил)-2-метил-3-бутен-1-она. Выход 87%, чистота по ГЖХ 76,7%.
Пример 4. Получение 1-(4-хлорфенил)-2-циклопропилпропан-1-она.
К суспензии 7,8 г (0,12 моль) цинковой пыли и 1,19 г (0,012 моль) однохлористой меди в 40 мл дихлорметана добавляют 5,22 г (0,03 моль) дибромметана, а потом 0,19 г (0,0024 моль) хлористого ацетила и перемешивают 10 минут. Затем к реакционной смеси за 15 минут добавляют 5,74 г (0,03 моль) 1-(4-хлорфенил)-2-метил-3-бутен-1-она в 15 мл дихлорметана. После этого к реакционной массе за 15 минут добавляют по каплям 10,44 г (0,06 моль) дибромметана в 5 мл дихлорметана. Реакционную массу нагревают до 40°С и перемешивают при температуре 40-45°С 5 часов. Затем реакционную массу остужают, добавляют 40 мл гексана и охлаждают до 0°С. После чего добавляют 30 мл 2М соляной кислоты. Слои разделяют, органический слой промывают 2М соляной кислотой, 5%-ным раствором соды и насыщенным раствором хлористого натрия. Сушат над безводным сульфатом натрия, растворитель удаляют в вакууме. Получают 5,37 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 86%, чистота по ГЖХ 81%. Общий выход, считая на 4-хлорбензонитрил, составляет 70,4%.
Пример 5. Получение 1-(4-хлорфенил)-2-циклопропилпропан-1-она.
К раствору 6,87 г (0,05 моль) 4-хлорбензонитрила в 60 мл смеси растворителей, эфира и ТГФ (в соотношении 85:15), прибавляют 13 г (0,2 моль) цинковой пыли и 2,67 г (0,02 моль) хлорида алюминия. Затем при комнатной температуре за 1 час прибавляют 6,79 г (0,075 моль) хлористого кротила в 10 мл смеси растворителей. Реакционную массу перемешивают 3 часа при 34°С. Потом реакционную массу фильтруют, фильтрат помещают в другую колбу и добавляют к нему 14,3 г (0,22 моль) цинковой пыли, 4,35 г (0,044 моль) однохлористой меди и 26,1 г (0,15 моль) дибромметана. Реакционную массу перемешивают на ультразвуковой бане 5 часов при температуре 36-42°С. Затем охлаждают до 0°С и осторожно добавляют 50 мл 2М соляной кислоты, перемешивают 10 минут и переносят в делительную воронку. Слои разделяют, водный слой экстрагируют эфиром (2 раза по 30 мл). Объединенные органические фракции промывают 2М соляной кислотой (2 раза по 30 мл) и водой (3 раза по 50 мл). Растворитель удаляют в вакууме. Получают 8,93 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 85,7%, чистота по ГЖХ 84%.
Пример 6. Получение 1-(4-хлорфенил)-2-циклопропилпропан-1-она.
К раствору 20,61 г (0,15 моль) 4-хлорбензонитрила в 120 мл смеси растворителей, эфир с ТГФ (в соотношении 85:15), прибавляют 39 г (0,6 моль) цинковой пыли и 8,01 г (0,06 моль) хлорида алюминия. Затем при комнатной температуре за 1 час добавляют 20,37 г (0,225 моль) хлористого кротила в 60 мл смеси растворителей. Реакционную массу перемешивают 3 часа при 34°С. Затем реакционную массу фильтруют и фильтрат переносят в капельную воронку.
В колбу помещают 39 г (0,6 моль) цинковой пыли, 5,94 г (0,06 моль) однохлористой меди, 26,1 г (0,15 моль) дибромметана в 90 мл эфира. Затем в колбу добавляют 0,92 г (0,012 моль) хлористого ацетила. Колбу нагревают на водяной бане, температура 35°С, 5 минут. Реакционная масса из светло-серой становится темно-серого цвета. Затем за 10 минут добавляют реакционную массу с предыдущей стадии. После чего прикапывают 52,2 г (0,3 моль) дибромметана в 30 мл эфира. Реакционная масса начинает кипеть, дибромметан прикапывают с такой скоростью, чтобы поддерживать равномерное кипение. После добавления дибромметана смесь перемешивают 5 часов при 45-50°С. Затем реакционную массу охлаждают до 0°С и медленно прибавляют 150 мл 2М соляной кислоты. Перемешивают 10 минут и переносят в делительную воронку. Слои разделяют, водный слой промывают эфиром (2 раза по 50 мл). Органические фракции объединяют и промывают 2М соляной кислотой (2 раза по 50 мл) и водой (3 раза по 70 мл). Сушат над безводным сульфатом натрия. Растворитель удаляют, получают 27,01 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 86%, чистота по ГЖХ 78%.
Пример 7. Получение 1-(4-хлоррфенил)-2-циклопропилпропан-1-она.
К суспензии 26 г (0,4 моль) цинковой пыли в 50 мл смеси диоксана с ТГФ (в соотношении 80:20) добавляют 5,34 г (0,04 моль) хлорида алюминия. Затем в колбу прикапывают за 15 минут смесь 13,7 г (0,1 моль) 4-хлорбензонитрила и 25 мл (0,15 моль) хлористого кротила в 100 мл смеси растворителей. Реакционную массу перемешивают 4 часа при 30-40°С. Реакционную смесь фильтруют и фильтрат переносят в капельную воронку.
В колбу помещают 26 г (0,4 моль) цинковой пыли, 60 мл бензола, 8 мл (0,1 моль) дибромметана, 4 г (0,04 моль) однохлористой меди и несколько капель триметилхлорсилана. Нагревают до 40°С и перемешивают 5 минут. Затем в течение 30 минут добавляют фильтрат с первой стадии. По окончании добавления фильтрата по каплям вводят 16 мл (0,2 моль) дибромметана за 30 минут. Реакционную массу перемешивают 5 часов при 40-45°С. Затем охлаждают до 0°С и осторожно прибавляют 250 мл 2М соляной кислоты, перемешивают 5 минут. Переносят в делительную воронку и разделяют слои. Органическую фазу промывают 250 мл 3%-ным раствором гидрокарбоната натрия и 250 мл насыщенного раствора хлорида натрия. Сушат над безводным сульфатом натрия. Растворитель удаляют. Получают 18 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 86%. Чистота по ГЖХ 77%.
Пример 8. Получение 1-(4-хлоррфенил)-2-циклопропилпропан-1-она.
К раствору 6,87 г (0,05 моль) 4-хлорбензонитрила в 40 мл ТГФ добавляют 13,0 г (0,2 моль) цинковой пыли и 2,67 г (0,02 моль) хлористого алюминия. Затем при комнатной температуре за 40 минут прибавляют 6,79 г (0,075 моль) хлористого кротила в 40 мл ТГФ. Реакционную массу перемешивают 3,5 часа при температуре 34-37°С. Затем ТГФ удаляют в вакууме, а остаток растворяют в 40 мл хлористого метилена.
Суспензию 13,0 г (0,2 моль) цинковой пыли и 0,12 г (0,001 моль) однохлористой меди в 55 мл хлористого метилена нагревают до 35°С и при этой температуре добавляют 3,0 мл (0,0015 моль) 0,5М раствора натрийборгидрида в диглиме и перемешивают 15 минут при этой температуре. Затем быстро добавляют раствор с предыдущей стадии. После этого за 45 минут прикапывают раствор 26,1 г (0,15 моль) дибромметана в 10 мл хлористого метилена при температуре 35-37°С. По окончании прибавления дибромметана в реакционную массу добавляют 0,074 г (0,0007 моль) однохлористой меди и перемешивают реакционную массу при 40-45°С в течение 5-ти часов.
Затем реакционную массу охлаждают до 0°С и добавляют 50 мл 2М соляной кислоты. Слои разделяют, объединенные органические слои промывают 2М раствором соляной кислоты (2 раза по 50 мл), насыщенным раствором хлористого натрия (2 раза по 50 мл) и водой (3 раза по 50 мл) и сушат над безводным сульфатом натрия. Растворитель удаляют. Получают 8,64 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 83%. Чистота по ГЖХ 78%.
Пример 9. Получение 1-(4-хлоррфенил)-2-циклопропилпропан-1-она.
К раствору 6,87 г (0,05 моль) 4-хлорбензонитрила в 40 мл ТГФ добавляют 13,0 г (0,2 моль) цинковой пыли и 2,67 г (0,02 моль) хлористого алюминия. Затем при комнатной температуре за 40 минут прибавляют 6,79 г (0,075 моль) хлористого кротила в 40 мл ТГФ. Реакционную массу перемешивают 3,5 часа при температуре 34-37°С. Затем ТГФ удаляют в вакууме, а остаток растворяют в 40 мл хлористого метилена.
Суспензию 13,0 г (0,2 моль) цинковой пыли и 0,12 г (0,001 моль) однохлористой меди в 55 мл хлористого метилена нагревают до 35°С и при этой температуре добавляют 0,43 г (0,0015 моль) 70%-ного раствора натрий-бис-(2-метоксиэтокси)-дигидроалюмината в толуоле, и перемешивают 15 минут при этой температуре. Затем быстро добавляют раствор с предыдущей стадии. После этого за 45 минут прикапывают раствор 26,1 г (0,15 моль) дибромметана в 10 мл хлористого метилена при температуре 35-37°С. По окончании прибавления дибромметана в реакционную массу добавляют 0,074 г (0,0007 моль) однохлористой меди и перемешивают реакционную массу при 40-45°С в течение 5-ти часов.
Затем реакционную массу охлаждают до 0°С и добавляют 50 мл 2М соляной кислоты. Слои разделяют, объединенные органические слои промывают 2М раствором соляной кислоты (2 раза по 50 мл), насыщенным раствором хлористого натрия (2 раза по 50 мл) и водой (3 раза по 50 мл) и сушат над безводным сульфатом натрия. Растворитель удаляют. Получают 8,34 г 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Выход 80%. Чистота по ГЖХ 76%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,1,2-ТРИФТОР-1-БУТЕН-4-ОЛА | 1995 |
|
RU2078072C1 |
| Способ получения производных 1-оксо-5-инданилоксиуксусной кислоты | 1974 |
|
SU738509A3 |
| СПОСОБ ПОЛУЧЕНИЯ (Z)-1-[4-(2-ДИМЕТИЛАМИНОЭТОКСИ) ФЕНИЛ]-1,2-ДИФЕНИЛБУТ-1-ЕНА | 1989 |
|
SU1617890A1 |
| Способ получения N-замещенных галоидпирролидинонов-2 | 1976 |
|
SU942590A3 |
| Способ получения 2,5-диметил-4-фенил-4-пропионилоксипиперидина | 1983 |
|
SU1165679A1 |
| Композиция для получения окрашенных изделий | 1982 |
|
SU1516014A3 |
| Способ получения транс, транс-8, 10-додекадиенола-1 | 1980 |
|
SU963226A1 |
| ПРОИЗВОДНЫЕ 2-ЦИАНО-1,3-ДИОНА, ИЛИ ИХ ЭНОЛЬНЫЕ ТАУТОМЕРНЫЕ ФОРМЫ, ИЛИ СЕЛЬСКОХОЗЯЙСТВЕННО ПРИЕМЛЕМЫЕ СОЛИ ЭНОЛЬНОЙ ТАУТОМЕРНОЙ ФОРМЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С РОСТОМ СОРНЯКОВ | 1992 |
|
RU2051148C1 |
| Способ получения 1-арил-2/1-имидазолил/алкильных эфиров,тиоэфиров или их солей | 1976 |
|
SU622405A3 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТАНОВ, СОДЕРЖАЩИХ ФРАГМЕНТЫ ПРОСТРАНСТВЕННО ЗАТРУДНЕННОГО ФЕНОЛА | 2000 |
|
RU2184727C2 |
Изобретение относится к способу получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она (I), который является промежуточным продуктом для получения биологически активных веществ, а также к способу получения 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II) - промежуточного продукта для получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она. Способ получения 1-(4-хлорфенил)-2-циклопропилпропан-1-она заключается в том, что 4-хлорбензонитрил подвергают взаимодействию с хлористым или бромистым кротилом и цинком в органическом растворителе и, не обязательно, в присутствии хлористого алюминия с получением после гидролиза реакционной смеси 2М соляной кислотой, выделения и очистки 1-(4-хлорфенил)-2-метил-3-бутен-1-она, который подвергают взаимодействию с дибромметаном, цинком и однохлористой медью в органическом растворителе в присутствии катализатора или в ультразвуковой бане с последующим выделением целевого продукта известным способом. Изобретение позволяет простыми и более дешевыми способами получать целевые продукты. 2 н. и 2 з.п. ф-лы.

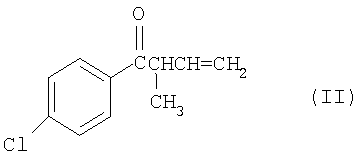
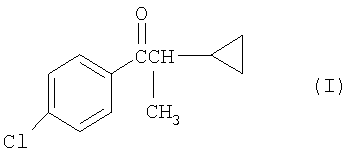
заключающийся в том, что
а) 4-хлорбензонитрил подвергают взаимодействию с хлористым или бромистым кротилом и цинком в органическом растворителе и, не обязательно, в присутствии хлористого алюминия, с получением после гидролиза реакционной смеси 2М соляной кислотой, выделения и очистки 1-(4-хлорфенил)-2-метил-3-бутен-1-она (II)
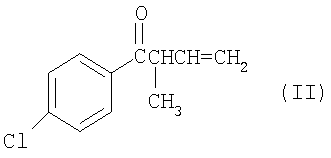
б) полученный 1-(4-хлорфенил)-2-метил-3-бутен-1-он (II) подвергают взаимодействию с дибромметаном, цинком и однохлористой медью в органическом растворителе в присутствии катализатора или в ультразвуковой бане с последующим выделением целевого продукта известным способом.
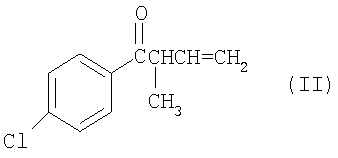
заключающийся в том, что 4-хлорбензонитрил подвергают взаимодействию с хлористым или бромистым кротилом и цинковой пылью в растворе терагидрофурана, не обязательно в присутствии хлористого алюминия, при температуре 10-40°С, при этом процесс получения включает стадию выделения и очистки, на которой реакционную массу после добавления к ней не смешивающегося с водой органического растворителя обрабатывают 2М раствором соляной кислоты и выделяют целевой продукт из органического растворителя известным способом.
| Способ получения производных циклопропана | 1988 |
|
SU1718722A3 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Reetz M.T., Wenderoth В., Urz R | |||
| Syntheses von β,γ- und α,β-ungesättigten Ketonen mittels Allyltitan-Agenzien | |||
| Chemische Berichte, 1985, Bd.118, №1, s.348-353 | |||
| Lee A.S.-Y | |||
| et al | |||
| Synthesis of allyl ketone via Lewis acid promoted Barbiertype reaction | |||
| Tetrahedron Letters, 2000, vol.41, №45, pp.8803-8806. | |||
Авторы
Даты
2009-03-27—Публикация
2007-08-02—Подача