Изобретение относится к химической технологии неорганических веществ, конкретно к процессу получения пероксида водорода окислением изопропанола кислородсодержащим газом.
Пероксид водорода в больших количествах используют в целлюлозно-бумажной и текстильной промышленности в качестве отбеливателя. Различные карбонатные, боратные и другие соединения пероксида водорода входят в составы отбеливающих, дезинфицирующих и моющих средств промышленного, медицинского и бытового назначения.
Технология производства пероксида водорода окислением изопропанола подробно описана в книге [Химия и технология перекиси водорода. / Под ред. Г.А.Серышева. - Л.: Химия, 1984. - 1984. - 200 с].
При окислении изопропанола молекулярным кислородом протекают цепные реакции, которые описываются брутто уравнением
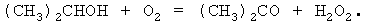
При недостатке кислорода протекают побочные реакции
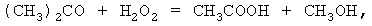
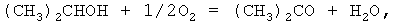
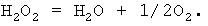
Для подавления побочных реакций отношение концентрации кислорода в окисляющем газе к концентрации пероксида водорода в оксидате [O2]газ/[H2O2]окс. должно быть больше 2,0 при давлении 1 МПа и 1,0 при давлении 3 МПа. При увеличении концентрации пероксида водорода скорость его накопления в реакционной массе возрастает, однако при достижении критической концентрации, зависящей от давления и других параметров, начинают интенсивно протекать деструктивные процессы.
Промышленный процесс ведут под давлением 1-1,5 МПа и температуре 110-140°С в многосекционном противоточном реакторе. Из оксидата, содержащего 9-10% пероксида водорода, под вакуумом отгоняют ацетон, азеотропную смесь изопропанол - вода, и получают товарный пероксид водорода. Основным недостатком данной технологии является малая удельная производительность, которая составляет всего 4-5 кг Н2O2/(м3·ч).
Возможность многократной интенсификации процесса получения пероксида водорода путем использования чистого кислорода рассмотрена в работе специалистов ГИПХ [Рылеев Г.И., Яцук А.Г. Интенсификация процесса получения перекиси водорода изопропиловым методом. // Интенсификация процессов тепло- и массообмена в химических аппаратах. Л., 1985. - с.25-29]. Однако промышленная реализация такого способа ограничивается высокой пожарной опасностью процесса.
Известен способ получения пероксида водорода окислением вторичного спирта молекулярным кислородом азотокислородной смеси в реакторе секционного типа (прототип) [патент 2109679 RU, МПК7 С01В 15/023, опубл. 1998.04.27]. Отличительной особенностью способа является поддержание отношения массовых концентраций
[O2]газ:[Н2О2]окс и [Н2O2]Oокс:[СН3СООН]окс, на уровнях, не менее, как 2:1 и 66:1 соответственно.
Согласно примерам из описания, окисляющий газ содержал 35 об.% кислорода. В двухсекционном реакторе поддерживали давление 1 МПа, температуру верхней секции 125°С, нижней секции - 140°С. В этих условиях съем пероксида водорода составлял 12-19 кг Н2O2/(м3·ч).
Недостатком данного способа является низкое содержание в оксидате пероксида водорода, которое составляло 10%. Для выделения 1 т 50% пероксида водорода необходимо переработать около 5 т такого оксидата, что требует значительных энергозатрат.
Целью изобретения является повышение содержания пероксида водорода в оксидате, что дает возможность уменьшить энергозатраты на выделение товарного пероксида водорода.
Поставленная цель достигается тем, что из оксидата, полученного окислением изопропанола кислородсодержащим газом, содержащего ацетон, изопропанол, воду, пероксид водорода, стабилизатор и органические примеси, вначале отделяют ацетон, полученный кубовый поток делят на циркуляционную и целевую части в соотношении (0,2-2,0):1, а затем циркуляционную часть возвращают на стадию окисления изопропанола, а из целевой части выделяют 30-60% водной раствор пероксида водорода.
Для окисления изопропанола используют очищенный атмосферный воздух, технический кислород в смеси с воздухом или кислород с флегматизатором, в качестве которого используют частично или полностью отработанную парогазовую смесь из реактора окисления.
На фиг.1 представлена общая блок-схема получения пероксида водорода окислением изопропанола кислородсодержащим газом, особенностью которой является возврат в реактор окисления циркуляционного потока оксидата после отделения ацетона.
На фиг.2. показана схема подачи в реактор окисления окисляющего газа при использовании одновременно воздуха и кислорода, причем в нижнюю часть реактора подают смешанный поток, содержащий 40-70% кислорода, а в среднюю часть - атмосферный воздух.
На фиг.3 показана схема работы реактора окисления только на кислороде, который для обеспечения безопасности смешивают с циркулирующим потоком частично или полностью отработанного окисляющего газа, содержащего органические пары и инертные газы, например азот.
В таблице приведены данные о количестве материальных потоков в расчете на 1 т 100% пероксида водорода и их составы по примеру 1.
Установка для получения пероксида водорода, фиг.1, включает секционированный реактор окисления 1, ректификационную колонну отделения из оксидата ацетона 2, ректификационную колонну выделения товарного пероксида водорода 3, узел гидрогенизации ацетона в изопропанол 4, абсорбер очистки отработанных газов 5.
В верхнюю часть реактора 1 подают изопропанол из узла 4 (поток 6) и азеотропную смесь изопропанол - вода (поток 7) из колонны 3, а также стабилизатор (поток 8). В реактор возвращают циркуляционную часть кубового продукта колонны 2 (поток 9). Этот поток вводят в одну или несколько точек по высоте реактора 1, обеспечивая адиабатический режим в отдельных секциях реактора. В нижнюю часть реактора вводят кислородсодержащий газ (поток 10). Процесс ведут при давлении 1-3 МПа и температуре 110-155°С. Отработанный газ, содержащий 3-7% кислорода, (поток 11), направляют в абсорбер 5. Оксидат, содержащий ацетон, изопропанол, воду, пероксид водорода, органические примеси и стабилизатор, (поток 12), направляют через дроссель в колонну 2.
В ректификационной колонне 2 при давлении, близком к атмосферному, из оксидата дистиллятом отделяют ацетон, который направляют на гидрогенизацию (поток 13). Кубовый поток делят на циркуляционную и целевую части в соотношении (0,2-2,0):1, а затем циркуляционную часть (поток 9) возвращают на стадию окисления изопропанола, а целевую часть (поток 14) направляют через дроссель в колонну 3.
В ректификационной колонне 3 при остаточном давлении 20-50 кПа дистиллятом выделяют азеотроп изопропанол - вода, который возвращают на окисление в реактор 1 (поток 7). Кубовым продуктом получают 30-60% товарный пероксид водорода (поток 15).
В узле гидрогенизации 4 из ацетона (поток 13) и водорода (поток 16) на катализаторе при повышенном давлении получают изопропанол, который после очистки подают на окисление (поток 6).
В абсорбер 5 для очистки отработанных газов от паров ацетона и изопропанола (поток 11) подают деминерализованную воду (поток 17). Полученный раствор направляют в колонну 3 (поток 18). Энергию избыточного давления очищенного газа утилизируют в детандере, а затем газ сбрасывают в атмосферу (поток 19).
При использовании в качестве окислителя одновременно воздуха и кислорода в реактор 1 окислитель целесообразно подавать двумя потоками, фиг.2. В нижнюю часть реактора подают воздушно-кислородную смесь с максимально допустимым содержанием кислорода (поток 10), который получают путем смешения кислорода (поток 20) и очищенного атмосферного воздуха (поток 21). В секцию реактора, в которой содержание кислорода в окисляющем газе снижается примерно до 21 об.%, подают очищенный атмосферный воздух (поток 22).
При использовании в качестве окислителя кислорода безопасность процесса обеспечивают путем организации циркуляции частично или полностью отработанного окисляющего газа, фиг.3. Для этого кислород (поток 20) смешивают с парогазовой смесью (поток 23), которую выводят из реактора 1. Полученную смесь (поток 10) подают в реактор 1.
Возврат в реактор 1 из колонны 2 циркуляционного потока 9 без ацетона обеспечивает снижение в реакторе концентрации ацетона, уменьшение скорости побочной реакции образования уксусной кислоты. Это дает возможность при использовании в качестве окисляющего газа очищенного атмосферного воздуха получать оксидат, содержащий до 15% пероксида водорода. При использовании для окисления изопропанола частично или полностью кислорода по схемам, представленным на фиг.2 и фиг.3, в нижней секции реактора концентрация кислорода в газе превышает 40 об.%. Это дает возможность получать, исходя из ограничения [O2]газ/[Н2О2]окс≥2, оксидат с концентрацией пероксида водорода до 20%. В результате расход энергетики на выделение из оксидата 50% пероксида водорода по сравнению с прототипом существенно снижается.
Циркуляционный поток позволяет также использовать тепловой эффект основной реакции окисления для выделения ацетона в колонне 2 и осуществлять процесс окисления в условиях, близких к адиабатическому.
Ниже представлены примеры осуществления данного способа, полученные расчетным путем с использованием моделирующей программы ChemCAD в расчете на 1 т 100% пероксида водорода.
Пример 1. Процесс ведут по схеме, приведенной на фиг.1. В реактор 1 на окисление подают 6162 кг смеси, содержащей 88,5 мас.%, изопропанола, 2289 кг газовой смеси, содержащей 40 об.% кислорода и 4332 кг циркуляционного потока. Окисление ведут при давлении 1,2 МПа и температуре 140°С в адиабатическом режиме. Получают оксидат с 16,2 мас.%, пероксида водорода, в котором на 1 моль пероксида водорода приходится 0,56 моля ацетона. Оксидат дросселируют до атмосферного давления и из полученной парожидкостной смеси в колонне 2 при температуре куба 92°С выделяют ацетон. Кубовый продукт разделяют на циркуляционную и основную части в соотношении 0,85:1. Из основной части (поток 14) в колонне 3 при остаточном давлении 30 кПа, температуре куба 88°С отгоняют азеотропную смесь изопропанол-вода и получают 1933 кг водного раствора, содержащего 51,74 мас.%, пероксида водорода. Расход тепловой энергии на выделение пероксида водорода из оксидата (поток 12) составляет 9,2 ГДж, в том числе 5,1 ГДж в кипятильнике колонны 3.
Пример 2 (сопоставительный). Процесс проводят по аналогии с примером 1, но при отсутствии циркуляционного потока 9. Получают оксидат с 10,4 мас.%, пероксида водорода, в котором на 1 моль пероксида водорода приходится 1,03 моля ацетона. Расход тепловой энергии на выделение пероксида водорода из оксидата составляет 11,1 ГДж, в том числе 7,5 ГДж в кипятильнике колонны 3.
Пример 3. Процесс проводят по аналогии с примером 1, но в качестве окисляющего газа используют атмосферный воздух. Получают оксидат с 12,4 мас.%, пероксида водорода, в котором на 1 моль пероксида водорода приходится 0,84 моля ацетона. Кубовый продукт разделяют на циркуляционную и основную части в соотношении 0,27:1. Расход тепловой энергии на выделение пероксида водорода из оксидата составляет 10,3 ГДж, в том числе 6,3 ГДж в кипятильнике колонны 3.
Пример 4. Процесс проводят по аналогии с примером 1, но в качестве окисляющего газа используют 95 об.% технический кислород, который флегматизируют парогазовым потоком по схеме, представленной на фиг.3. Окисление проводят при температуре 160°С и получают оксидат, содержащий 18,8 мас.%, пероксида водорода, который на 1 моль пероксида водорода содержит 0,41 моль ацетона. Кубовый продукт колонны 2, содержащий 22,0 мас.%, пероксида водорода, разделяют на циркуляционную и основную части в соотношении 1,5:1. В колонне 3 получают 55,6% пероксид водорода. Расход тепловой энергии на выделение пероксида водорода из оксидата составляет 9,1 ГДж, в том числе 4,6 ГДж в кипятильнике колонны 3.
Из представленных примеров следует, что разделение кубового продукта колонны отгонки ацетона на циркуляционную и основную части в соотношении (0,2-2,0):1 с возвратом циркуляционной части на стадию окисления обеспечивает снижение расхода энергетики по сравнению с прототипом на 10-20%. При этом обеспечивается работа реактора окисления в режиме, близком к адиабатическому, что упрощает конструкцию реактора.
Расход на 1 т 100% пероксида водорода и мольный состав материальных потоков по примеру 1
| название | год | авторы | номер документа |
|---|---|---|---|
| ДВУХСТАДИЙНЫЙ СПОСОБ ВЫДЕЛЕНИЯ 40-60% ВОДНОГО РАСТВОРА ПЕРОКСИДА ВОДОРОДА | 2007 |
|
RU2353575C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 2017 |
|
RU2648887C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОПИЛЕНОКСИДА ИЗ ПРОПИЛЕНА И ПЕРОКСИДА ВОДОРОДА | 2008 |
|
RU2372343C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛЭТИЛКЕТОНА | 2020 |
|
RU2731903C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРЕКИСИ КУМОЛА И/ИЛИ ГИДРОПЕРЕКИСИ ВТОРБУТИЛБЕНЗОЛА | 2002 |
|
RU2222527C1 |
| СПОСОБ РЕКУПЕРАЦИИ АНИЛИНА | 2006 |
|
RU2327683C2 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ С - С ОЛЕФИНОВ | 1996 |
|
RU2168504C2 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА | 1996 |
|
RU2162466C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОГЕКСАНОНА | 2021 |
|
RU2760548C1 |
| Способ получения водного раствора пероксида водорода | 1989 |
|
SU1685865A1 |
Изобретение относится к химической технологии неорганических веществ, а именно к получению пероксида водорода. Сущность изобретения: пероксид водорода получают окислением изопропанола кислородсодержащим газом и последующим выделением из оксидата, содержащего ацетон, изопропанол, воду, пероксид водорода, стабилизатор и органические примеси. Из оксидата в ректификационной колонне отделяют ацетон, полученный кубовый продукт делят на циркуляционную и целевые части в соотношении (0,2-2,0):1,0, затем циркуляционную часть возвращают на стадию окисления изопропанола, а из целевой части выделяют 30-60% водный раствор пероксида водорода. Технический результат: повышение содержания пероксида водорода и снижение энергетических затрат на выделение товарного пероксида водорода. 3 ил., 1 табл.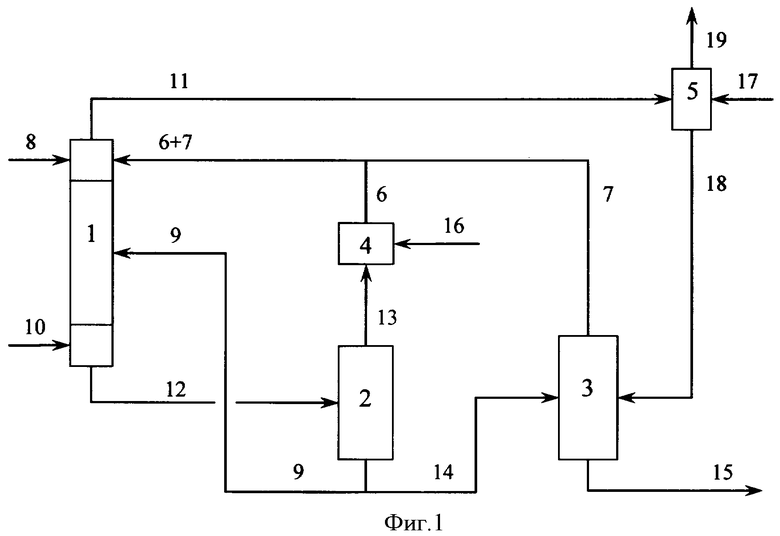
Способ получения пероксида водорода окислением изопропанола кислородсодержащим газом и последующим выделением из оксидата, содержащего ацетон, изопропанол, воду, пероксид водорода, стабилизатор и органические примеси, 30-60%-ного водного раствора пероксида водорода методом ректификации, отличающийся тем, что из оксидата вначале отделяют ацетон, полученный кубовый остаток делят на циркуляционную и целевую части в соотношении (0,2-2,0):1,0, а затем циркуляционную часть возвращают на стадию окисления изопропанола, а из целевой части выделяют 30-60%-ный водный раствор пероксида водорода.
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ВОДОРОДА | 1993 |
|
RU2109679C1 |
| Устройство для лужения печатных плат | 1978 |
|
SU778966A1 |
| Способ получения водного раствора пероксида водорода | 1989 |
|
SU1685865A1 |
Авторы
Даты
2009-05-27—Публикация
2008-01-14—Подача