Изобретение относится к области разработки высокоэффективных методов синтеза полициклического нитрамина 2,4,6,8,10,12-гексанитро-2,4,6,8,10,12-гексаазоизовюрцитана (гексанитрогексаазоизовюрцитан, ГАВ). На настоящий момент ГАВ, также известный, как CL-20, считается наиболее мощным стабильным взрывчатым веществом. Испытание взрывчатых составов на основе этого нитрамина показало, что их мощность в среднем на 14% процентов превышает мощность аналогичных составов с октогеном [Наир У.Р., Сиваблан Р., Гор Г.М., Гиза М., Астина Ш.Н., Сингх X. Физика горения и взрыва. 2005, №3, с.3-17]. Однако применение ГАВ сдерживается из-за высокой стоимости синтеза нитрамина [С.В.Сысолятин, А.А.Лобанова, Ю.Т.Черникова, Г.В.Сакович. Успехи химии, 2005, №7, с.815-821].
Традиционно синтез ГАВ осуществляется с помощью трехстадийной методики (см. схему), включающей в себя стадию сборки полициклического каркаса 2,4,6,8,10,12-гексабензил-2,4,6,8,10,12-гексаазаизовюрцитана (гексабензилгексаазаизовюрцитан, ГБ), замену бензильных групп при атомах азота на ацетильные и формильные группы (синтез предшественника ГАВ - 2,6,8,12-тетраацетил-4,10-диформил-2,4,6,8,10,12-гексаазаизовюрцитана (тетраацетилдиформилгексаазаизовюрцитан, ТАДФ)) и последующее нитрование полученного предшественника, приводящее к образованию целевого продукта [US 5739325, B01J23/44, С06 В25/34, С07 В61/00, 14.04.1998].
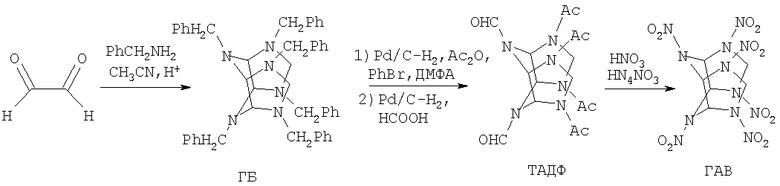
Каталитическая реакция замещения бензильных групп при атомах азота на ацетильные и формильные группы (реакция гидродебензилирования-ацилирования ГБ) является ценоопределяющей для всего метода синтеза CL-20. В то же время стадии синтеза полициклического каркаса ГБ и нитрования ТАДФ (см. схему) изучены достаточно хорошо, и их применение не представляет затруднений.
Недостатком известного способа проведения реакции гидродебензилирования-ацилирования является низкая устойчивость катализатора реакции к процессам дезактивации. В ходе проведения реакции гидродебензилирования-ацилирования ГБ происходит быстрая и необратимая дезактивация дорогостоящего палладиевого катализатора [US 5739325, B01J 23/44, С06 В25/34, С07В 61/00, 14.04.1998].
Одним из возможных способов снижения стоимости полициклического нитрамина ГАВ является разработка катализатора реакции гидродебензилирования-ацилирования, более устойчивого к процессам дезактивации, чем известные катализаторы.
В предшествующих работах авторов было обнаружено, что основными причинами дезактивации палладиевых катализаторов реакции гидродебензилирования-ацилирования является агломерация частиц палладия на поверхности углеродного носителя. Было показано, что стоимость регенерации палладиевого катализатора в этом случае достаточно велика, и поэтому экономически более выгодно сжигать отработанный палладиевый катализатор с целью выделения благородного металла (метод деструктивной регенерации палладиевого катализатора) [Коскин А.П., Симакова И.Л. Сборник докладов I Всероссийской научно-технической конференции молодых ученых «Перспективы создания и применения конденсированных энергетических материалов», 27-29 сентября 2006 года, г.Бийск, с.42-52].
Изобретение решает задачу повышения стабильности катализатора гидродебензилирования-ацилирования, используемого в процессе синтеза предшественника ГАВ-ТАДФ.
Технический результат - повышение производительности синтеза ТАДФ в реакции гидродебензилирования-ацилирования.
Задача решается составом катализатора получения 2,6,8,12-тетраацетил-4,10-диформил-2,4,6,8,10,12-гексаазаизовюрцитана (далее ТАДФ) по реакции гидродебензилирования-ацилирования 2,4,6,8,10,12-гексабензил-2,4,6,8,10,12-гексаазаизовюрцитана (далее ГБ) на основе палладия, углеродного носителя и стабилизирующих добавок.
Катализатор содержит палладий в количестве не ниже 6.0 мас.%.
В качестве металла-стабилизатора можно использовать иридий, платину, либо смесь этих металлов. Предпочтительным является использование иридия с содержанием 3 мас.%.
В качестве подложки для благородных металлов можно использовать мезопористый углеродный носитель.
Задача также решается способом приготовления катализатора гидродебензилирования-ацилирования, по которому на стадии осаждения предшественников металлических активных компонентов используют водный раствор, содержащий смесь ионов металлов. В качестве источника ионов палладия и металла-стабилизатора можно использовать любые водно-растворимые соли или комплексы соответствующих металлов, например водные растворы комплексных кислот H2[PdCl4], Н2[IrCl6] и Н2[PtCl6]. Оптимальным оказалось использование палладий-иридиевого биметаллического катализатора с содержанием 6 мас.% палладия и 3 мас.% иридия.
Задача решается также способом проведения реакции гидродебензилирования-ацилирования при температуре 20-30°С и давлении водорода 4-5 бар в присутствии биметаллического палладийсодержащего катализатора, где в качестве катализатора используют катализатор, описанный выше. Повышение температуры выше 30°С или давления водорода выше 5 бар приводит к существенному снижению выхода целевого продукта (ТАДФ).
Сущность изобретения иллюстрируется следующими примерами.
Пример 1 (сравнительный по прототипу).
Катализатор для процесса гидродебензилирования-ацилирования, состоящий из палладия, нанесенного на углеродный носитель Сибунит (удельная поверхность по БЭТ - 320 м2/г), в количестве 6 мас.%, готовят методом осаждения соли палладия на углеродном носителе с последующим восстановлением ионов палладия до металла. Для этого в стеклянном реакторе (100 мл) готовят суспензию углеродного носителя Сибунит (10 г) в дистиллированной воде (25 мл) и при интенсивном перемешивании добавляют 1М водный раствор H2[PdCl4] (5.92 мл). Полученную смесь выдерживают при перемешивании в течение 1 ч, затем по каплям добавляют 1М водный раствор Na2CO3 до значения pH раствора = 8-9 и проводят восстановление формиатом натрия при температуре 90-100°С. После этого полученный катализатор отделяют от жидкой фазы на фильтре, тщательно промывают дистиллированной водой для удаления ионов хлора и сушат в токе воздуха.
Процесс гидродебензилирования-ацилирования ГБ в присутствии описанного выше катализатора проводят в термостатированном автоклаве из нержавеющей стали (объем 150 мл), снабженном электромагнитной мешалкой, системой подачи газообразного водорода и насосом для подачи жидких реагентов. В автоклав загружают 3.4 г ГБ и 0.34 г катализатора и продувают водородом, после чего подают 10% раствор бромбензола в ДМФА (0.6 мл) и уксусный ангидрид (5.1 мл), устанавливают температуру 25°С, давление водорода 4 бар и включают перемешивание. После 10 ч процесс прерывают, смесь промежуточного продукта и катализатора отделяют в атмосфере азота от реакционной смеси, промывают на фильтре этиловым спиртом и сушат до постоянного веса. Затем эту смесь переносят обратно в автоклав, добавляют муравьиную кислоту из расчета 5 мл НСООН на 1 г смеси. После этого подготавливают автоклав и продолжают процесс гидродебензилирования-ацилирования в тех же реакционных условиях (температура 25°С, давление водорода 4 бар). Через 6 ч катализатор отделяют от реакционной смеси фильтрованием и собирают остатки продуктов реакции, промывая Pd/C муравьиной кислотой. Полученный фильтрат концентрируют на ротационном вакуумном испарителе. Выход целевого продукта (ТАДФ) составляет 69%.
Активность отработанного палладиевого катализатора реакции тестируют, проводя на нем рецикл реакции гидродебензилирования-ацилирования. Для этого катализатор предварительно очищают от компонентов реакционной смеси, последовательно промывая его муравьиной кислотой, 1% водным раствором Na2CO3 и дистиллированной водой и сушат в вакууме. Выход ТАДФ при проведении рецикла реакции гидродебензилирования-ацилирования, проведенного по стандартной методике реакции, описанной выше, составляет 0%.
Пример 2 (сравнительный по прототипу).
Испытание каталитической активности проводят аналогично примеру 1, с тем отличием, что вместо приготовленного катализатора 6 мас.% Pd/Сибунит используют коммерчески доступный катализатор Pd/C (E101 NE/W, Degussa, 10 мас.% Pd). Выход ТАДФ на свежем катализаторе составляет 75%, а при проведении рецикла реакции гидродебензилирования-ацилирования ГБ - 0%
Пример 3.
Аналогичен примеру 1, с тем отличием, что вместо приготовленного катализатора, содержащего 6 мас.% Pd/Сибунит в реакции гидродебензилирования-ацилирования ГБ используют катализатор, содержащий 6 мас.% палладия и 3 мас.% иридия, приготовленный методом осаждения из смеси водных растворов комплексных кислот H2[PdCl4] и Н2[IrCl6] (5.92 мл и 1.64 мл соответственно).
Выход ТАДФ на свежем биметаллическом палладий-иридиевом катализаторе составляет 76%, при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 70%, второго - 59%.
Пример 4.
Аналогичен примеру 1, с тем отличием, что для ускорения реакции гидродебензилирования-ацилирования используют палладий-платиновый катализатор с содержанием палладия 6 мас.% и платины 3 мас.%. Катализатор готовят аналогично примеру 3, с тем отличием, что для нанесения металла стабилизатора вместо 1М водного раствора Н2[IrCl6] используют 1М водный раствор Н2[PtCl6].
Выход ТАДФ на свежем катализаторе составляет 72%, при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 73%, второго - 0%.
Пример 5.
Аналогичен примеру 1, с тем отличием, что для ускорения реакции гидродебензилирования-ацилирования используют триметаллический палладий-платино-иридиевый катализатор с содержанием палладия 6 мас.%, платины 1.5 мас.% и иридия 1.5 мас.%. Катализатор приготовлен аналогично примеру 3, с тем отличием, что для нанесения металла стабилизатора вместо смеси 1М водных растворов H2[PdCl4] и Н2[IrCl6] используют смесь 1М водных растворов H2[PdCl4], Н2[IrCl6] и H2[PtCl6] в соотношении (2:1:1 по массе металлов).
Выход ТАДФ на свежем триметаллическом катализаторе составляет 60%, при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 51%, второго - 22%.
Пример 6.
Аналогичен примеру 3, с тем отличием, что вместо биметаллического палладий-иридиевого катализатора с содержанием палладия 6 мас.% и иридия 3 мас.% используют катализатор 4%Pd-3%Ir/C.
Выход ТАДФ составляет 0%.
Пример 7.
Аналогичен примеру 3, с тем отличием, что для ускорения реакции гидродебензилирования-ацилирования используют катализатор 6%Pd-l%Ir/C.
Выход ТАДФ составляет 73%, а при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 0%.
Пример 8.
Аналогичен примеру 3, с тем отличием, что для ускорения реакции гидродебензилирования-ацилирования используют катализатор 6%Pd-4%Ir/C.
Выход ТАДФ на свежем катализаторе составляет 72%, при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 67%, второго - 55%.
Пример 9.
Аналогичен примеру 3, с тем отличием, что вместо биметаллического палладий-иридиевого катализатора используют смесь катализаторов 6 мас.% Pd/C и 6 мас.% Ir/С в соотношении 2:1 по массе.
Выход ТАДФ составляет 69%, а при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 0%.
Пример 10.
Аналогичен примеру 3, с тем отличием, что для ускорения реакции гидродебензилирования-ацилирования используют катализатор, в котором в качестве подложки металлов вместо углеродного материала Сибунит используют каталитический волокнистый углерод (КВУ, удельная поверхность по БЭТ - 150 м2/г).
Выход ТАДФ на свежем катализаторе составляет 70%, при проведении первого рецикла реакции гидродебензилирования-ацилирования ГБ - 66%, второго - 50%.
Пример 11.
Аналогичен примеру 3, с тем отличием, что реакцию гидродебензилирования-ацилирования ГБ проводят при температуре 50°С. Выход ТАДФ составляет 0%.
Пример 12.
Аналогичен примеру 3, с тем отличием, что реакцию гидродебензилирования-ацилирования ГБ проводят при давлении водорода 6 бар. Выход ТАДФ составляет 0%.
Как видно из приведенных примеров и таблицы, использование предлагаемого биметаллического палладий-иридиевого катализатора в реакции гидродебензилирования-ацилирования ГБ позволяет увеличить производительность катализатора по целевому продукту (ТАДФ) за счет повышения устойчивости катализатора к процессам дезактивации. Необходимым оказалось использование катализаторов с содержанием палладия выше 6 мас.% и металла-стабилизатора (металл VIIIb группы) не ниже 1.5 мас.% и проведение реакции гидродебензилирования-ацилирования при температуре 25-30°С и давлении водорода 4-5 бар. Оптимальным является применение катализатора, содержащего 6 мас.% Pd, 3 мас.% Ir на углеродном носителе, а увеличение содержания металла-стабилизатора до 4 мас.% не приводит к повышению стабильности катализатора.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЕБЕНЗИЛИРОВАНИЯ 2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАИЗОВЮРЦИТАНА | 2010 |
|
RU2448110C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ГЕКСААЗАИЗОВЮРЦИТАНОВ | 2010 |
|
RU2451020C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,03,11 ,05,9]ДОДЕКАНА | 2015 |
|
RU2610695C2 |
| Способ получения катализатора и способ его применения для многократного использования в промышленном процессе двухстадийного гидрогенолиза при производстве 2,4,6,8,10,12-гексанитро-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,0,0]додекана | 2016 |
|
RU2641694C1 |
| Способ получения 4,10-диформил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,0,0]додекана | 2021 |
|
RU2772755C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4,6,8,10,12-ГЕКСАНИТРО-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАНА | 2008 |
|
RU2360916C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4,6,8,10,12-ГЕКСАНИТРО-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО [5,5,0,0,0]ДОДЕКАНА | 2006 |
|
RU2355693C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИМЕТАЛЛИЧЕСКОГО КАТАЛИЗАТОРА (ВАРИАНТЫ) И ЕГО ПРИМЕНЕНИЕ ДЛЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2010 |
|
RU2428769C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРААЦЕТИЛДИФОРМИЛГЕКСААЗАИЗОВЮРЦИТАНА | 2003 |
|
RU2266907C9 |
| Циано-полинитро-2,4,6,8,10,12-гексаазаизовюрцитаны и способы их получения | 2024 |
|
RU2828547C1 |
Изобретение относится к области разработки высокоэффективного метода синтеза гексанитрогексаазоизовюрцитана (ГАВ), в частности разработки метода проведения реакции гидродебензилирования-ацилирования с использованием биметаллического палладийсодержащего катализатора. Описан катализатор получения тетраацетилдиформилгексаазаизовюрцитана по реакции гидродебензилирования-ацилирования гексабензилгексаазаизовюрцитана на основе палладия, одного или двух металлов VIIIb и углеродного носителя, содержащие не ниже 6 мас.% палладия и не ниже 1.5 мас.% металла VIIIb группы. Описан способ приготовления катализаторов и способ получения тетраацетилдиформилгексаазаизовюрцитана. Технический результат - повышение устойчивости катализаторов к процессам их дезактивации. 3 н. и 3 з.п. ф-лы, 1 табл.
1. Катализатор получения 2,6,8,12-тетраацетил-4,10-диформил-2,4,6,8,10,12-гексаазаизовюрцитана по реакции гидродебензилирования-ацилирования 2,4,6,8,10,12-гексабензил-2,4,6,8,10,12-гексаазаизовюрцитана на основе палладия и углеродного носителя, отличающийся тем, что он дополнительно содержит в качестве стабилизирующих добавок один или несколько благородных металлов VIIIb группы.
2. Катализатор по п.1, отличающийся тем, что он содержит палладий в количестве не ниже 6,0 мас.%.
3. Катализатор по п.1, отличающийся тем, что он содержит один или несколько благородных металлов VIIIb группы в количестве не ниже 1,5 мас.%.
4. Способ приготовления катализатора получения 2,6,8,12-тетраацетил-4,10-диформил-2,4,6,8,10,12-гексаазаизовюрцитана по реакции гидродебензилирования-ацилирования 2,4,6,8,10,12-гексабензил-2,4,6,8,10,12-гексаазаизовюрцитана нанесением палладия на углеродный носитель, отличающийся тем, что его готовят осаждением ионов металлов из их смеси в водном растворе на поверхность углеродного носителя, после чего восстанавивают ионы палладия и одного или нескольких благородных металлов VIIIb группы до металлического состояния.
5. Способ получения 2,6,8,12-тетраацетил-4,10-диформил-2,4,6,8,10,12-гексаазаизовюрцитана по реакции гидродебензилирования-ацилирования 2,4,6,8,10,12-гексабензил-2,4,6,8,10,12-гексаазаизовюрцитана, отличающийся тем, что в качестве катализатора используют катализатор по пп.1-3 или приготовленный по п.4.
6. Способ по п.5, отличающийся тем, что реакцию гидродебензилирования-ацилирования проводят при температуре 20-30°С и давлении водорода 4-5 бар.
| US 5739325, 14.04.1998 | |||
| ВЗРЫВЧАТЫЙ СОСТАВ | 2003 |
|
RU2252925C1 |
| МАЛОЧУВСТВИТЕЛЬНЫЕ ВЗРЫВЧАТЫЕ СОСТАВЫ НА ОСНОВЕ ГЕКСАНИТРОГЕКСААЗАИЗОВЮРЦИТАНА И ВЗРЫВЧАТЫЕ СОСТАВЫ НА ИХ ОСНОВЕ | 1998 |
|
RU2199512C2 |
| US 5529649 A, 25.06.1996. | |||
Авторы
Даты
2009-06-27—Публикация
2008-02-14—Подача