Изобретение относится к органической химии, а именно к способу получения промежуточного продукта 4,10-диформил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазагетрацикло[5,5,0,03,11,05,9]додекана(ТАГАВ), используемого для получения высокоэффективного взрывчатого вещества 2,4,6,8,10,12-гексанитро-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,03,11,05,9]додекана (ГАВ).
Важной стацией в синтезе ГАВ является получение промежуточного продукта ТАГАВ. Из уровня техники известен способ получения ТАГАВ по патенту США № 5739325, 14.04.1998, опубл. Chem. Abstr. 127: 110983 (1998), включающий гидрогенолиз 4,10-дибензил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,03,11,05,9] додекана (ДБ) в среде муравьиной кислоты и удаление летучих компонентов из реакционной массы.
Существенным недостатком данного способа является использование пленочного выпарного аппарата под давлением, что увеличивает многотоннажность и энергозатраты на производство и приводит к снижению технологичности процесса. При реализации указанного способа получают смоловидный продукт с выходом 86% в расчете на ДБ, который не кристаллизуют, а если провести стадию кристаллизации, то выход будет недостаточно высоким.
Также известен способ по патенту РФ № 2146676 (Бюллетень № 8, 2000 г., опубл. 20.03.2000 г.), принятый за прототип, в котором ТАГАВ получают с применением по меньшей мере двух реакционных растворителей, где первым растворителем является муравьиная кислота, а второй растворитель выбирают из органических растворителей, содержащих эфирную группу (гликолевые эфиры) или амидную группу и имеющих температуру кипения выше температуры кипения муравьиной кислоты.
Недостатком описанного способа, препятствующего его широкому применению, является использование труднолетучего и высококипящего растворителя эфира, который удаляется не полностью, и его остатки содержатся в полученном продукте, что существенно снижает безопасность проведения нитрования ТАГАВ при получении ГАВ. К недостаткам способа по прототипу также относятся: необходимость добавления в реакционную массу свежего растворителя, т.к при отгонке часть его "уходит" вместе с отгоняемыми компонентами, кроме того, растворитель после дистилляции требуется регенерировать, т.е. появляется промежуточный этап. Способ по прототипу требует сложного аппаратурного оформления (используют роторный испаритель, снабженный вакуумным насосом, работающим под давлением) и имеет высокую насыщенность технологическими операциями, что нецелесообразно при его использовании в промышленном масштабе.
Задачей заявляемого изобретения является получение с высоким выходом целевого продукта (ТАГАВ) без использования труднолетучих и высококипящих реагентов при одновременном повышении технологичности процесса.
Поставленная задача решается предложенным способом получения ТАГАВ, включающим гидрогенолиз ДБ в среде муравьиной кислоты и воды с получением толуола в качестве побочного продукта, последующее удаление муравьиной кислоты, воды и толуола из реакционной массы отгонкой с использованием органического инертного растворителя и кристаллизацию. Особенность заключается в том, что в качестве органического инертного растворителя используют бензол или толуол, который добавляют к реакционной массе после завершения гидрогенолиза, удаление муравьиной кислоты, воды и толуола из реакционной массы ведут азеотропной отгонкой при температуре ниже температуры кипения муравьиной кислоты, образованный азеотроп охлаждают, бензол или толуол возвращают в процесс, а полученный продукт кристаллизуют в среде двух последовательно добавляемых органических растворителей.
При этом в качестве двух последовательно добавляемых органических растворителей используют этанол и этилацетат или этанол и изопропанол, или ацетон и этилацетат, или ацетон и изопропанол, или метанол и изопропанол.
Процесс заместительного гидрогенолиза иллюстрируется следующей формулой:
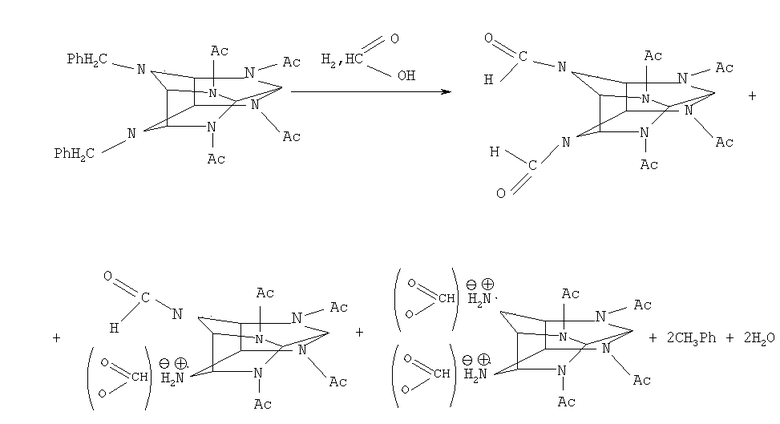
В результате гидрогенолиза ДБ в среде муравьиной кислоты и воды реакционная масса содержит смесь компонентов, состав которой представлен в Таблице 1.
Было установлено, что в концентрированной муравьиной кислоте образуется ТАГАВ. С понижением концентрации кроме основного продукта образуются формиатные соли (соли ТАГАВ) - моноформиат 4-формил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,03,11,05,9]додекан (МФАТ) и диформиат 2,6,8,12-тетраацетил-2,6,8,10,12-гаксаазатетрацикло[5,5,0,03,11,05,9]додекан (ДФАТ). В процессе азеотропной отгонки (бензол-вода, бензол-муравьиная кислота или толуол-вода, толуол-муравьиная кислота) за счет дегидратации происходит переход вышеуказанных солей в ТАГАВ.

Таким образом упрощается кристаллизация ТАГАВ в среде двух последовательно добавляемых органических растворителей - этанола и этилацетата или этанола и изопропанола, или ацетона и этилацетата, или ацетона и изопропанола, или метанола и изопропанола. Добавление первого органического растворителя каждой пары приводит к гомогенизации реакционной массы, улучшению качества процесса кристаллизации, а второй растворитель каждой пары способствует полноте осаждения и увеличению выхода ТАГАВ.
Предлагаемый способ отличается от прототипа использованием иного органического инертного растворителя, а именно ароматического углеводорода - бензол или толуол (в прототипе - растворитель, содержащий эфирную или амидную группу), имеющего качественно иное соотношение между его точкой кипения и точкой кипения муравьиной кислоты, а именно ниже точки кипения последней; иной последовательностью введения его в процесс - после гидрогенолиза (в прототипе гидрогенолиз ведется в присутствии органического инертного растворителя);
иным процессом отгонки - азеотропная отгонка при постоянной температуре реакционной массы (в прототипе отгонку ведут путем изменения температуры реакционной массы); полным возвратом в процесс органического инертного растворителя без его регенерации (в прототипе существует необходимость добавления свежего растворителя и регенерации уже используемого), что позволяет считать предложенный способ соответствующим критерию "новизна".
Сравнение заявляемого способа с прототипом и другими способами получения ТАГАВ показало, что неизвестно техническое решение поставленной задачи, в котором имело место предложенное сочетание признаков.
Только предлагаемая совокупность отличительных от прототипа признаков с остальными существенными признаками заявляемого способа позволяет не только улучшить качество получаемого продукта, исключив использование труднолетучих и высококипящих реагентов, но и, в целом, существенно повысить технологичность процесса получения качественного ТАГАВ с высоким выходом, а именно это дает основание считать предлагаемое техническое решение, имеющим изобретательский уровень.
При этом для получения высокого выхода целевого продукта в качестве двух последовательно добавляемых органических растворителей используют этанол и этилацетат или этанол и изопропанол, или ацетон и этилацетат, или ацетон и изопропанол, или метанол и изопропанол.
Сведения, подтверждающие возможность осуществления способа.
Пример 1. В автоклав помещают 14, 70г ДБ, 1,43 г шестипроцентного палладиевого катализатора и 46,0 мл (54,4 г) 77% раствора муравьиной кислоты, содержащего 12,5 г воды. Реакционную массу перемешивают в атмосфере водорода в течение 24 часов при температуре 25-30°С. По окончании выдержки палладиевый катализатор отделяют от реакционной массы фильтрованием и промывают 15 мл муравьиной кислоты. Затем в трехгорлую колбу, снабженную мешалкой, термометром, холодильником и насадкой для азеотропной отгонки, помещают реакционную массу после гидрогенолиза, состоящую из муравьиной кислоты, воды, толуола и смеси продуктов, содержащей 10,5 г ТАГАВ и 1,5 г смеси солей. К этому раствору добавляют бензол (модуль 0,5-1,5 по объему). При температуре 74-76°С и перемешивании проводят азеотропную отгонку с бензолом сначала воды, затем смеси муравьиной кислоты и толуола. Отгоняемую азеотропную смесь охлаждают при помощи холодильника, конденсируя пары в насадке для азеотропной отгонки. Т.о. отгоняют 63-65 мл муравьиной кислоты и бензол (80-90% от добавленного). Слой бензола отделяют от слоя муравьиной кислоты и возвращают в колбу, а отгоняемый компонент (смесь муравьиной кислоты и воды) сливают из насадки. После завершения всего процесса азеотропной отгонки бензол также отгоняют и его можно использовать для следующего цикла получения ТАГАВ. Добавлением в колбу этанола (4,5-5 мл на 1 г продукта) реакционную массу гомогенизируют, а затем образовавшийся ТАГАВ осаждают этилацетатом (4,0-5,0 мл на 1 г продукта).
Закристаллизовавшийся продукт отфильтровывают, получая 11,87 г ТАГАВ (98,9%).
Тпл ТАГАВ 290-293°С.
ИК-спектр (в пластинке KBr), см-1:
3020, 3000, 2910 (СН); 1710-1650 (NC=O); 1420-1355 (C=O); 1285, 1205, 1165, 1080, 1050, 1030, 965, 930, 905, 720, 675, 620, 580.
ПМР-спектр в CDCl3, мд:
2,09-2,17 мультиплет(12Н, СН3СO); 6,0 дуплет (0,2H, СН); 6,12 синглет (0,45Н, СН); 6,23-6,25 дуплет (1,5Н, СН); 6.46 синглет (1,7 Н, СН); 6,67 дуплет (1,5Н, СН); 6,7-6,8 мультиплет(0,65H, СН).
Пример 2. В автоклав помещают 14,70г ДБ, 1,43 г шестипроцентного палладиевого катализатора и 46,0 мл (54,4 г) 77% раствора муравьиной кислоты, содержащего 12,5 г воды. Реакционную массу перемешивают в атмосфере водорода в течение 24 часов при температуре 25-30°С. По окончании выдержки палладиевый катализатор отделяют от реакционной массы фильтрованием и промывают 15 мл муравьиной кислоты. Затем в трехгорлую колбу, снабженную мешалкой, термометром, холодильником и насадкой для азеотропной отгонки, помешают реакционную массу после гидрогенолиза, состоящую из муравьиной кислоты, воды, толуола и смеси продуктов, содержащей 10,5 г ТАГАВ и 1,5 г смеси солей. К этому раствору добавляют толуол (модуль 0,5-1,5 по объему). При температуре 110-112°С и перемешивании проводят азеотропную отгонку с толуолом сначала воды, затем смеси муравьиной кислоты и толуола. Отгоняемую азеотропную смесь охлаждают при помощи холодильника, конденсируя пары в насадке для азеотропной отгонки. Т.о. отгоняют 63-65 мл муравьиной кислоты и толуол (80-90% от добавленного). Толуол отделяют от муравьиной кислоты и возвращают в колбу, а отгоняемый компонент (смесь муравьиной кислоты и воды) сливают из насадки. После завершения всего процесса азеотропной отгонки толуол также отгоняют и его можно использовать для следующего цикла получения ТАГАВ. Добавлением в колбу этанола (4,5-5 мл на 1 г продукта) реакционную массу гомогенизируют, а затем образовавшийся ТАГАВ осаждают этилацетатом (4,0-5,0 мл на 1 г продукта).
Закристаллизировавшийся продукт отфильтровывают, получая 11,87 г ТАГАВ (98,9%).
Тпл ТАГАВ 290-293°С.
ИК-спектр (в пластинке KBr), см-1:
3020, 3000, 2910 (СН); 1710-1650 (NC=О); 1420-1355 (С=О); 1285, 1205, 1165, 1080, 1050, 1030, 965, 930, 905, 720, 675, 620, 580.
ПМР-спектр в CDCl3, мд:
2,09-2,17 мультаплет (12H, СН3СО); 6,0 дуплет (0,2Н, СН); 6.12 синглет (0,45H, СН); 6,23-6,25 дуплет (1,5H, СН); 6,46 синглет (1,7Н, СН); 6,67 дуплет (1,5Н, СН); 6,7-6,8 мультиплет (0,65H, СН).
В качестве двух последовательно добавляемых органических растворителей могут быть использованы и другие пары растворителей, а не только этанол и этилацетат. Но именно эта пара обусловливает наиболее высокий выход ТАГАВ после кристаллизации (Таблица 2). Пара растворителей для кристаллизации ТАГАВ подбирается так: первый из них (этанол, метанол, ацетон) хорошо растворяет смолы и примеси, частично растворяет диформильное производное, делая реакционную массу более гомогенной, что способствует получению продукта более высокого качества. Второй растворитель (этилацетат, изопропанол) - осадитель, в нем ТАГАВ не растворим и при добавлении его к реакционной массе выпадает в осадок, что способствует увеличению выхода диформильного производного.
Экспериментальным путем были установлены оптимальные соотношения пары растворителей в расчете на диформильное производное (Таблица 2).
Технологическое оформление заявляемого способа значительно проще, чем у ближайшего аналога, и существенно повышена безопасность при дальнейшем использовании целевого продукта в коммерческих масштабах с высоким выходом. Повышена экономичность способа.
Реализация данного способа позволяет удовлетворить давно существующую потребность в получении с высоким выходом целевого продукта без использования труднолетучих и высококипящих реагентов, снижающих его качество, при одновременном повышении технологичности процесса; использовать стандартное оборудование и доступные реактивы, следовательно, предложенное техническое решение соответствует критерию промышленной применимости.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,4,6,8,10,12-ГЕКСАНИТРО-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАНА | 2008 |
|
RU2360916C1 |
| Способ получения 4,10-диформил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,0,0]додекана | 2021 |
|
RU2772755C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4,6,8,10,12-ГЕКСАНИТРО-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО [5,5,0,0,0]ДОДЕКАНА | 2006 |
|
RU2355693C2 |
| ОДНОРЕАКТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ 4,10-ДИ(2-ЭТОКСИАЦЕТИЛ)-2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАНА | 2023 |
|
RU2834298C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,03,11 ,05,9]ДОДЕКАНА | 2015 |
|
RU2610695C2 |
| 4-(3,4-ДИБРОМТИОФЕНКАРБОНИЛ)-10-ИЗОНИКОТИНИЛ-2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАН В КАЧЕСТВЕ АНАЛЬГЕТИЧЕСКОГО СРЕДСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2022 |
|
RU2799639C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2, 4, 6, 8, 10, 12-ГЕКСАНИТРО-2, 4, 6, 8, 10, 12-ГЕКСААЗАТЕТРАЦИКЛО [5, 5, 0, 0, 0]ДОДЕКАНА | 2001 |
|
RU2199540C2 |
| 4-(3,4-ДИБРОМТИОФЕНКАРБОНИЛ)-2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАН В КАЧЕСТВЕ АНАЛЬГЕТИЧЕСКОГО СРЕДСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2565766C1 |
| ПРОИЗВОДНЫЕ 4-(3,4-ДИБРОМТИОФЕНКАРБОНИЛ)-2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,03,11,05,9]ДОДЕКАНА С САЛИЦИЛОВЫМИ КИСЛОТАМИ В КАЧЕСТВЕ АНАЛЬГЕТИЧЕСКИХ СРЕДСТВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2022 |
|
RU2802003C1 |
| 4,10-БИС((±)-5-БЕНЗОИЛ-2,3-ДИГИДРО-1Н-ПИРРОЛО[1,2-А]ПИРРОЛ-1-КАРБОНИЛ)-2,6,8,12-ТЕТРААЦЕТИЛ-2,4,6,8,10,12-ГЕКСААЗАТЕТРАЦИКЛО[5,5,0,0,0]ДОДЕКАН В КАЧЕСТВЕ АНАЛЬГЕТИЧЕСКОГО СРЕДСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2558148C1 |
Изобретение относится к органической химии, а именно к способу получения промежуточного продукта тетраацетилдиформилгексаазаизовюрцитана (ТАГАВ), используемого для получения высокоэффективного взрывчатого вещества 2,4,6,8,10,12-гексанитро-2,4,6,8,10,12-гексаазатетрацикло [5,5,0,03,11, 05,9]додекана (ГАВ). Описывается способ получения 4,10-диформил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,03,11,05,9]додекана путем гидрогенолиза 4,10-дибензил-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,03,11,05,9]додекана в среде муравьиной кислоты и воды с получением толуола в качестве побочного продукта, последующего удаления муравьиной кислоты, воды и толуола из реакционной массы с использованием азеотропной отгонки с бензолом или толуолом при температуре ниже температуры кипения муравьиной кислоты, образованный азеотроп охлаждают, при этом бензол или толуол возвращают в процесс, а полученный продукт кристаллизуют в среде двух последовательно добавляемых органических растворителей, один из которых гомогенезирует реакционную массу, а другой осаждает полученный продукт, например этанол и этилацетат или этанол и изопропанол, или ацетон и этилацетат, или ацетон и изопропанол, или метанол и изопропанол. 1 з.п. ф-лы, 2 табл.
| СПОСОБ ВЫДЕЛЕНИЯ ПРОИЗВОДНОГО ГЕКСААЗАИЗОВЮРТЦИТАНА, СОДЕРЖАЩЕГО АЦИЛЬНУЮ ГРУППУ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ ТЕТРААЦИЛБИС(АРИЛМЕТИЛ)ГЕКСААЗАИЗОВЮРТЦИТАНА И СПОСОБ ПОЛУЧЕНИЯ ТЕТРААЦИЛГЕКСААЗАИЗОВЮРТЦИТАНА | 1997 |
|
RU2146676C1 |
| ПРОИЗВОДНОЕ ГЕКСААЗАИЗОВАРТЗИТАНА, СОДЕРЖАЩЕЕ АЦИЛЬНУЮ ГРУППУ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2125572C1 |
| WO 9919328 A1 22.04.1999 | |||
| US 6472525 B1 29.10.2002 | |||
| JP 10291989 A2 04.11.1998 | |||
| СПОСОБ АЦИЛИРОВАНИЯ ГЕКСАКИС(ФЕНИЛМЕТИЛ)ГЕКСААЗАИЗОВЮРЦИТАНА | 1998 |
|
RU2182151C2 |
Авторы
Даты
2005-12-27—Публикация
2003-08-25—Подача