Изобретение относится к ветеринарной микробиологии, а именно к технологии получения специфического иммуномодулирующего средства, иммуномодулятор может быть использован для коррекции иммунного статуса животных и повышения эффективности иммунной защиты.
В настоящее время проблема регуляции и восстановления защитных функций организма при заболеваниях и воздействии дестабилизирующих факторов окружающей среды является одной из актуальных проблем ветеринарной медицины.
Иммунокоррекция предполагает использование фармакологических средств для изменения функциональной активности иммунной системы. Основным обоснованием для назначения иммунологических средств является клиническая картина, характеризующаяся наличием хронических, вялотекущих и трудноподдающихся лечению инфекционных процессов. Нарушение функции иммунной системы рассматривается как один из патогенетических механизмов любого патологического процесса (Ю.Н.Федоров. Иммунодефициты крупного рогатого скота / Ветеринария. - 2006. - №1. - С.3-6).
Иммуномодуляторы, разрешенные к применению, могут быть разного происхождения: микробного, растительного и животного, синтетические, полученные на основе иммуноглобулинов и цитокинов. Вакцина БЦЖ, применяемая в настоящее время с целью профилактики туберкулеза, стимулирует одновременно естественную резистентность организма, а также используется для специфической патогенетической терапии больных туберкулезом легких. Стимулирующие свойства вакцины БЦЖ послужили основанием для приготовления из отдельных фракций разрушенной культуры БЦЖ иммуномодулирующих средств (патент РФ RU №2112543, A61K 39/04, A61K 47/48, 1998).
Известно иммуномодулирующее средство, восстанавливающее иммунный статус организма и обеспечивающее эффективную перестройку организма человека в отношении опухолевых клеток, возбудителей инфекционных заболеваний (патент РФ RU №2034542, кл. A61K 31/305, 1995).
Предложенное иммуномодулирующее средство в качестве активного начала содержит формальдегид, а в качестве целевых добавок NaCl и дистиллированную воду. Известно, что формальдегид является естественным продуктом метаболизма клеток. Применение препарата включает механизм естественной саморегуляции, который на первом этапе характеризуется увеличением или понижением отдельных показателей иммунного статуса организма, а в дальнейшем их нормализацией. Однако отсутствие в составе иммуномодулятора специфического составляющего ограничивает сферу применения препарата и, в частности, с целью повышения противотуберкулезной резистентности.
Наиболее близким техническим решением к заявленному является способ получения вакцины против туберкулеза (патент РФ RU №2217164, кл. A61K 39/04). Способ предусматривает получение нового типа неживой бесклеточной (молекулярной) вакцины. Способ включает культивирование микобактерий из штамма БЦЖ, выделение двух фракций. Фракцию клеточных оболочек конъюгируют на целлюлозной матрице при соотношении 1:10 (по массе) в присутствии треххлористого хрома, затем добавляют цитоплазматическую фракцию до содержания белка 1,5-2 мг/мл.
Однако приготовление суспензии целлюлозы из хлопковой ваты в качестве матрицы предусматривает применение сильнодействующих химических соединений (раствор аммиака, сернокислая медь, щелочной раствор, концентрированная серная кислота и другие), что является небезопасным для работающих, затратным при изготовлении, препарат используется только для реиммунизации крупного рогатого скота, ранее привитого вакциной БЦЖ, при этом у препарата низкая способность восстанавливать у животных утраченную иммунологическую реактивность.
Задачей изобретения является получение специфического иммуномодулятора, способного восстанавливать утраченную иммунологическую реактивность, устранять вторичные иммунодефициты, усиливать протективные свойства вакцины БЦЖ.
Задача достигается путем культивирования микобактерий из штамма БЦЖ с последующим разрушением их ультразвуком. Разрушенную суспензию микобактерий центрифугируют при 15000 об/мин в течение 30 минут и надосадочную жидкость сливают, добавляют 37-40%-ный формальдегид (формалин) при 0,6-0,7%-ном содержании формалина в растворе. Приготовленную смесь инкубируют в термостате при 37°С в течение 5-9 дней. Затем измеряют содержание белка. Реакционную смесь конъюгируют с поливинилпирролидоном (ПВП) при соотношении 1 мг/мл белка 600 мг ПВП.
Предложенный способ отличается тем, что выделенный антигенный комплекс из разрушенной культуры БЦЖ центрифугируют при 15000 об/мин, смешивают с формалином до конечной его концентрации 0,6-0,7%, реакционную смесь инкубируют в термостате при температуре 37°С в течение 5-9 дней и затем добавляют ПВП, концентрацию которого доводят на 1 мг/мл белка 600 мг ПВП (1:600), ставят на магнитную мешалку при комнатной температуре до получения эффекта, измеряют содержание белка и вводят подкожно.
По мнению А.А.Евглевского реакция формальдегид - белок (пептид) состоит из двух стадий. В течение первой стадии, быстрой и необратимой, происходит взаимодействие формальдегида с аминогруппами белка и особенно лизина с образованием метилоламинной группы. На втором этапе в реакции участвуют активные радикалы циклических аминокислот, содержащие фенольные, гуанидиновые и индольные группы. Наибольшее значение имеет соединение через формальдегид свободных аминогрупп лизина с СН-группами ядер тирозина и гистидина, которые характеризуются большой стойкостью. В результате блокирования свободных аминогрупп происходит увеличение отрицательных зарядов аллергенов, что снижает аллергическое действие препаратов (патент SU №1825630, кл. A61K 39/35, 1993).
Сущность изобретения поясняется на конкретных примерах выполнения способа.
Пример 1. Получение антигенного комплекса из вакцинного штамма БЦЖ.
Проводят посев вакцинного штамма БЦЖ на жидкую синтетическую среду Сотона. Вакцинный штамм культивируют в конических колбах емкостью 0,5-1,0 л при температуре 37°С в течение 2-3-х недель. Выросшую бактериальную массу собирают и трижды отмывают стерильным физиологическим раствором, центрифугируют в течение 20 минут при 3 тыс.об/мин. Отмытую бактериальную массу ресуспендируют в стерильном физиологическом растворе из расчета 1:5 (1,0 г бактериальной массы и 5 мл физиологического раствора). Флаконы с суспензией бактериальных клеток помещают на 24 часа на шуттель-аппарат при комнатной температуре.
Суспензию бактериальных клеток подвергают ультразвуковой дезинтеграции на аппарате УЗДН-1 (22-35 кГц, 60-70 Вт/см2 в течение 30 мин), полученную взвесь центрифугируют 30 мин при 15000 об/мин (этот параметр является оптимальным для получения комплекса антигенов цитоплазматической фракции и клеточных оболочек БЦЖ). Надосадочную жидкость сливают.
Количество белка в надосадочной жидкости определяют на фотоэлектроколориметре с использованием красителя бромфенолового синего (БФС). На кружок фильтровальной бумаги диаметром 2 см, помещенный на пористый фильтр, вставленный в колбу с отсосом (водоструйный насос), наносят пробу фракции. Осадок, образовавшийся на фильтровальной бумаге, промывают 4 мл 10%-ной трихлоруксусной кислоты, затем тремя порциями дистиллированной воды. Фильтр с осадком помещают для окрашивания в 0,05%-ный раствор БФС в 2%-ной уксусной кислоте, инкубируют 30 мин, затем в течение 30 мин 3-кратно отмывают от несвязавшегося красителя 2%-ной уксусной кислотой. Отмытый фильтр переносят в пробирку, содержащую 5 мл 0,025 н. раствора NaOH, инкубируют 30 мин и колориметрируют синий элюат при 590 нм. Количество белка в пробе определяют по калибровочной кривой. Для построения калибровочной кривой на фильтр наносят по 25 мкл растворов, содержащих известные количества белка (от 10 до 150 мкг в пробе). Фильтраты высушивают на воздухе, инкубируют 30 мин в 10%-ной трихлоруксусной кислоте, отмывают 3-кратно дистиллированной водой, помещают для окрашивания на 30 мин в 0,05%-ный раствор БФС, отмывают 30 мин 2%-ной уксусной кислотой, элюируют краситель в 5 мл 0,025 н. раствора NaOH в течение 30 мин и колориметрируют элюаты при 590 нм.
В объем антигенного комплекса (99,3 мл) добавляют 37%-ного медицинского формальдегида 0,7 мл или 40%-ного - 0,6 мл. Реакционную смесь инкубируют в термостате при 37°С в течение 5-9 дней, конъюгируют с поливинилпирролидоном молекулярной массой 12600±2700 (синтетический неприродный полиэлектролит, модулирующий иммуногенез, обладает митогенными свойствами, стимулирует миграцию стволовых клеток), концентрацию которого доводят на 1 мг/мл белка 600 мг ПВП (1:600). В качестве эксперимента брали разные соотношения ПВП к белку (1:400, 1:600 и 1:800 мг), в результате чего установили, что оптимальной концентрацией является соотношение 1:600, так как удается получить гомогенную слегка вязкую жидкость, которая легко вводится через инъекционную иглу и обеспечивает необходимую дозу ПВП на 1 кг массы животного. При соотношении 1:400 легко растворяется в жидкости и не обеспечивает достаточного количества ПВП для дозы. При соотношении 1:800 получается сильновязкая жидкость, которую невозможно ввести через инъекционную иглу. В 100 мг/мл белка после инкубирования постепенно частями добавляют ПВП, размешивая на магнитной мешалке при комнатной температуре до получения эффекта, вновь измеряют содержание белка, доводят дозу по содержанию белка на кг массы животного, при необходимости: добавляют в одном случае надосадочную жидкость разрушенной БЦЖ с известным содержанием белка; во втором - стерильный физиологический раствор. Стимулирующий эффект ПВП с молекулярной массой 12600 наиболее выражен в дозе 10-20 мг/кг массы (Р.В.Петров, P.M.Хаитов, Р.И.Атауллаханов. Иммуногенетика и искусственные антигены / АМН СССР. - М.: Медицина, 1983. - 256 с.). Реакционную смесь разливают во флаконы и стерилизуют на установке АСИС при 80°С в течение 30 мин и в стерильном боксе закрывают пробками. В результате получают комплексный иммуномодулятор микробного происхождения (КИМ-М).
Испытание иммуномодулирующих свойств препаратов на морских свинках.
Из 40 морских свинок формируют 4 группы по 10 животных в каждой: 10-ти морским свинкам ввели подкожно комплекс антигенов БЦЖ (КАГ-БЦЖ) в дозе 500 мкг белка в 0,7 мл физиологического раствора (1-я группа); 10-ти животным ввели подкожно КАГ-БЦЖ, инкубированный в растворе формалина (КАГ-БЦЖ-Ф), в дозе 500 мкг белка в 0,7 мл физиологического раствора (2-я группа); 10-ти морским свинкам ввели подкожно ППД-туберкулин, инкубированный в растворе формалина (ППД-Ф) в дозе 1,3 мл (3-я группа); 10 морских свинок используют в качестве контроля (4-я группа). Через 14 дней после введения препаратов по 5 животных каждой группы были привиты вакциной БЦЖ внутрикожно в дозе 100 мкг в 0,1 мл физиологического раствора. Через месяц после вакцинации морских свинок всех групп исследуют ППД-туберкулином для млекопитающих и инфицируют вирулентной культурой М. bovis штамм 14 подкожно в дозе 0,0001 мг. Через 30 дней всех морских свинок исследуют ППД-туберкулином и убивают для проведения патологоанатомических исследований. В результате исследований оценивают степень пораженности туберкулезом внутренних органов животных и индекс защиты по схеме Г.И.Гельберга и Е.А.Финкеля (Гельберг С.И. К методике экспериментального изучения иммуногенных свойств противотуберкулезных вакцин и эффективность методов их применения / С.И.Гельберг, Е.А.Финкель // Пробл. туберкулеза. - 1959. - №2. - С.80-84): сначала определяют в количественных показателях интенсивность распространения поражения туберкулезного характера у морских свинок каждой опытной и контрольной групп. Показатель поражений оценивают от 0 до 9.
Затем устанавливают средний показатель поражения для каждой опытной группы животных путем вычисления средних арифметических величин из индивидуальных показателей по формуле:
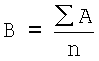 ,
,
где В - показатель интенсивности поражений группы животных;
А - показатель поражения каждой морской свинки в группе;
n - количество животных в группе.
Для оценки напряженности иммунитета применяют индекс защиты, предложенный А.И.Тогуновой (1948). Из среднего показателя интенсивности поражения контрольной группы вычитают такой же показатель, установленный для опытной группы. Затем полученный остаток, взятый в процентах, делят на средний показатель интенсивности поражения контрольной группы по формуле:
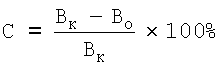 ,
,
где С - индекс защиты;
ВК - показатель интенсивности поражений в контрольной группе;
ВО - показатель интенсивности поражений в опытной группе.
Результаты исследований препаратов на их способность формировать у животных противотуберкулезную защиту показаны в таблице 1.
Способность формировать противотуберкулезную защиту у морских свинок установлена при введении комплекса антигенов БЦЖ, инкубированного с формалином (2-я группа): степень пораженности составила 4,0±0,00, индекс защиты 41%. Способность названного препарата усиливать протективные свойства вакцины БЦЖ также выше, чем у животных других групп: степень пораженности - 0,60±0,60, индекс защиты 91%.
Испытание препаратов на их способность восстанавливать у морских свинок утраченную иммунологическую реактивность.
Ранее установлено, что предварительное подкожное введение взрослым морским свинкам туберкулопротеида влечет за собой снижение выраженности туберкулиновых реакций (иммунологическая толерантность) после вакцинации животных БЦЖ (М.М.Авербах. Иммунология и иммунопатология туберкулеза. - М.: Медицина, 1976. - С.78-79).
16 морским свинкам вводят ППД-туберкулин для млекопитающих, инкубированный с формалином, подкожно в дозе 1,3 мл и делят животных по 4 в каждой: через 5 дней после индукции толерантности 4-м морским свинкам вводят комплекс антигенов БЦЖ (КАГ-БЦЖ) подкожно в дозе 500 мкг белка (1-я группа); 4-м - вводят комплекс антигенов БЦЖ, инкубированный с формалином (КАГ-БЦЖ-Ф) подкожно в дозе 500 мкг белка (2-я группа); 4-м животным вводят комплекс антигенов БЦЖ, инкубированный с формалином и конъюгированный с поливинилпирролидоном (КАГ-БЦЖ-Ф-ПВП) подкожно в дозе 500 мкг белка (3-я группа); 4-м - вводят иммуномодулирующее средство (Ласкавый, Рыбин. Патент РФ RU №2034542, кл. A61K 31/305, 1995) подкожно в дозе 1,3 мл (4-я группа). 4 здоровые морские свинки служат в качестве контроля (5-я группа).
Морские свинки первых 4-х групп через 7 дней после введения изучаемых препаратов прививают вакциной БЦЖ внутрикожно в дозе 100 мкг в 0,1 мл и через 30 дней после иммунизации морских свинок всех групп заражают вирулентной культурой М.bovis штамм 14 подкожно в дозе 0,0001 мг/мл и через 30 дней убивают для проведения патологоанатомических исследований.
Результаты исследований показаны в таблице 2.
Наиболее высокая способность восстанавливать утраченную иммунологическую реактивность у морских свинок установлена у препарата, изготовленного из комплекса антигенов БЦЖ, инкубированного с формалином и конъюгированного с ПВП (3-я группа): степень пораженности органов - 1,75±0,75 баллов; индекс защиты - 80%, тогда как у комплекса антигенов БЦЖ (1-я группа), соответственно: 4,0±0,00; 53,8%. Несколько выше эта способность у известного иммуномодулирующего средства (Ласкавый, Рыбин), соответственно: 3,66±0,66; 57,7% (4-я группа). Способность восстанавливать утраченную иммунологическую реактивность у препарата, изготовленного из комплекса антигенов БЦЖ, инкубированного с формалином выше, соответственно: 2,66±0,66; 69,3% (2-я группа).
Испытание препарата на молодняке крупного рогатого скота
В опыт берут 60 телят в возрасте от 10 до 20 дней и делят их на 3 группы: 20-ти телятам вводят изучаемый препарат подкожно в дозе 20 мкг белка на кг массы животного (0,8-1,0 мг белка на животное) в 1,0 мл (1-я группа). Через 30 дней этих животных прививают вакциной БЦЖ в дозе 1 мг в 0,2 мл. Других 20 телят аналогичного возраста прививают также вакциной БЦЖ (2-я группа) и 20 телят используют в качестве контроля (3-я группа). Через 4 месяца у животных всех групп отбирают венозную кровь, в которой определяют концентрацию нейтрофилов, Т-лимфоцитов (Е-рок), Т-киллеров (ЕА), Т-лимфоцитов, распознающих антигены микобактерий туберкулеза (ЕТ), В-лимфоцитов (ЕАС), иммунологические параметры анализируют с помощью дискретно-динамического анализа, составляют дифференциально-прогностические таблицы, определяют состояние иммунитета (патент РФ RU №2257913, кл. A61K 39/00, G01N 33/53).
Содержание всех иммунокомпетентных клеток у телят, привитых вакциной БЦЖ, после введения препарата достоверно выше, чем у контрольных животных, особенно выше содержание Т-лимфоцитов и Т-киллеров (Р<0,001). Повышенное количество клеток-киллеров, В-лимфоцитов, Т-лимфоцитов, распознающих антиген, установлено также у телят, привитых только вакциной БЦЖ (таблица 3).
Средние показатели иммунологических параметров, тыс/мкл
Р
<0,001
<0,001
<0,01
<0,001
<0,01
Р
>0,05
<0,001
<0,01
<0,001
<0,05
Результаты оценки иммунитета у телят опытных групп показаны в таблице 4, 5, 6. Наибольший процент иммунных животных, у привитых вакциной БЦЖ после введения препарата (90%), у привитых только вакциной БЦЖ - 75% и у интактных - 40%. Повышенная противотуберкулезная устойчивость у части интактного молодняка крупного рогатого скота связана, вероятно, с генетическими факторами.
Разработана и предлагается технология изготовления комплексного иммуномодулятора микробного происхождения (КИМ-М) из составляющих: комплекс антигенов разрушенной культуры БЦЖ, инкубированной в растворе формалина, и конъюгированный с поливинилпирролидоном. Препарат обладает протективными свойствами, способностью восстанавливать нарушенную иммунологическую реактивность, усиливать протективные свойства вакцины БЦЖ.
Результаты исследований препаратов на их способность формировать у животных противотуберкулезную защиту
Результаты оценки иммуномодулирующих свойств препаратов на их способность восстанавливать иммунологическую реактивность у морских свинок
Дифференциально-прогностическая таблица для оценки иммунитета у молодняка крупного рогатого скота, привитого вакциной БЦЖ, после введения препарата, тыс/мкл
Дифференциально-прогностическая таблица для оценки иммунитета у молодняка крупного рогатого скота, привитого вакциной БЦЖ, тыс/мкл
Дифференциально-прогностическая таблица для оценки иммунитета у интактного молодняка крупного рогатого скота, тыс/мкл
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СПЕЦИФИЧЕСКОГО ИММУНОМОДУЛЯТОРА | 2011 |
|
RU2478399C2 |
| СПОСОБ ОЦЕНКИ ИММУНОМОДУЛИРУЮЩИХ ПРЕПАРАТОВ | 2007 |
|
RU2354401C1 |
| Способ получения специфического иммуномодулятора | 2021 |
|
RU2764467C1 |
| СПОСОБ СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ТУБЕРКУЛЕЗА | 2013 |
|
RU2562550C2 |
| ИММУНОМОДУЛИРУЮЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1996 |
|
RU2112543C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТУБЕРКУЛЕЗА | 2004 |
|
RU2266753C1 |
| ВАКЦИНА ПРОТИВ ТУБЕРКУЛЕЗА | 1999 |
|
RU2153354C1 |
| РЕКОМБИНАНТНЫЕ ШТАММЫ ВИРУСА ГРИППА, ЭКСПРЕССИРУЮЩИЕ МИКОБАКТЕРИАЛЬНЫЙ ПРОТЕКТИВНЫЙ АНТИГЕН ESAT-6, И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2005 |
|
RU2318872C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТУБЕРКУЛЕЗНОГО АНАТОКСИНА | 2008 |
|
RU2360697C1 |
| ПРОТИВОТУБЕРКУЛЕЗНАЯ ВАКЦИНА | 2007 |
|
RU2443773C2 |
Изобретение относится к технологии получения иммуномодулирующего средства. Штамм БЦЖ культивируют с последующим разрушением полученной культуры ультразвуком. Далее из разрушенной культуры выделяют антигенный комплекс, представляющий собой цитоплазматические и клеточные оболочки, при 15000 об/мин полученную надосадочную жидкость (антигенный комплекс) смешивают с формалином, реакционную смесь инкубируют при температуре 37°C в термостате, определяют содержание белка, коньюгируют на поливинилпирролидоне (ПВП) при соотношении 1 мг/мл белка - 600 мг ПВП (1:600) по массе на магнитной мешалке при комнатной температуре до получения гомогенной жидкости. Полученный специфический иммуномодулятор способен восстанавливать утраченную иммунологическую реактивность, устранять вторичные иммунодефициты, усиливать протективные свойства вакцины БЦЖ. 6 табл.
Способ получения специфического иммуномодулятора, включающий культивирование вакцинного штамма БЦЖ с последующим разрушением культуры ультразвуком, выделением антигенного комплекса (цитоплазматического и клеточных оболочек) при 15000 об/мин, отличающийся тем, что надосадочную жидкость (антигенный комплекс) смешивают с формалином, реакционную смесь инкубируют при температуре 37°С, определяют содержание белка, конъюгируют на поливинилпирролидоне (ПВП) при соотношении 1 мг/мл белка - 600 мг ПВП (1:600) по массе на магнитной мешалке при комнатной температуре до получения гомогенной жидкости.
| СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ПРОТИВ ТУБЕРКУЛЕЗА | 2001 |
|
RU2217164C2 |
| JP 2007291006 А, 08.11.2007 | |||
| US 2007207954 А1, 06.09.2007 | |||
| Аппарат для регистрации работы | 1931 |
|
SU26124A1 |
Авторы
Даты
2009-09-10—Публикация
2007-10-25—Подача