Изобретение относится к области биотехнологии и иммунологии и может быть использовано в технологии изготовления панелей сывороток, содержащих антитела опасных вирусных инфекций.
Тест-системы для анализа антител к антигенам вируса гепатита В в сыворотке или плазме крови и в образцах крови, подготовленной для переливания, появились в России в 90-е годы. Однако до сих пор нет никаких стандартных препаратов для контроля правильности и чувствительности анализов на выявление анти-ВГВ антител.
Антитела к вирусу гепатита В появляются в крови инфицированных через 5-6 месяцев. Однако спектр антител на каждом этапе развития инфекции помогает клиницистам оценить эффективность выбранного курса лечения, а аналитикам подтвердить результаты анализа [1].
Anti-HBs у больных начинают выявляться в крови только в отдаленном периоде, спустя длительное время после исчезновения HBsAg. Титры анти-HBs редко бывают высокими и со временем снижаются до необнаруживаемых концентраций. В диагностическом плане выявление анти-HBs может служить лишь критерием ретроспективного подтверждения ранее перенесенного гепатита В (ГВ). Динамический контроль за системой HBsAg-anti-HBs имеет важное клиническое значение для оценки течения инфекционного процесса и его исхода. Обнаружение анти-HBs, особенно в сочетании с anti-HBe, рассматривается как надежный критерий развития постинфекционного протективного иммунитета. Накопление анти-HBs в крови является наиболее информативным тест-контролем вакцинации против HBV- инфекции.
В сыворотке крови больных острым ГВ очень рано начинают появляться анти-НВс класса М, индикация которых имеет важное диагностическое значение. Они появляются уже в начале острой фазы болезни еще до пика повышения АлАТ, до появления желтухи, подтверждая альтернативную репликацию вируса. Выявление анти-НВс IgM является важным критерием диагностики ГВ при уже отрицательной индикации HBsAg. В фазу «окна» после исчезновения HBsAg и до появления anti-HBs суммарные анти-НВс становятся единственными ИФА - маркерами HBV.
Anti-HBe появляются при остром гепатите В через 2-3 недели желтушного периода. Наступление сероконверсии HBeAg-anti-HBe знаменует резкое снижение инфекционного процесса» [2].
На основе проведенного анализа литературы следует, что постоянный ИФА контроль спектра и количества антител ВГВ является необходимым условием успешного лечения болезни.
Детекция антител к каждому из HBV-антигенов имеет самостоятельное диагностическое значение. Так, например, известно, что анти-НВе и анти-НВс IgM антитела выявляются на самых ранних этапах сероконверсии, анти-HBs, как правило, появляются позднее.
Было показано, что наличие в сыворотке анти-HBCore IgM является достаточно надежным маркером вирусной репликации [3].
Задачей изобретения является разработка способа получения панели сывороток, содержащих антитела к вирусу гепатита В.
Поставленная задача решается изготовлением стандартной панели сывороток, содержащих все виды антител и образцы сывороток, не содержащих антител, для контроля специфичности тест-систем.
Для формирования панели используют образцы плазмы, собранные в различных регионах России. Образцы заготавливают в соответствии с этическими нормами и санитарными правилами. Каждый образец получают методом плазмафереза в гемаконе и замораживают.
Разработка панели антител к ВГВ - сложнейшая задача, т.к. наряду с аттестацией спектра антител в образцах панели необходимо тестировать зависимость чувствительности тест-систем на антитела к различным субтипам антигенов HBV. К сожалению, эта задача не может быть решена количественно ввиду отсутствия международных стандартов на отдельные антитела. Поэтому в настоящем изобретении в качестве меры концентрации определенного антитела использованы титры антител в сертифицированных тест-системах [4].
Нативные сыворотки разводят неиммунной сывороткой здоровых доноров с добавлением стабилизаторов. Это позволяет сохранить концентрацию биохимических компонентов сыворотки практически неизменной.
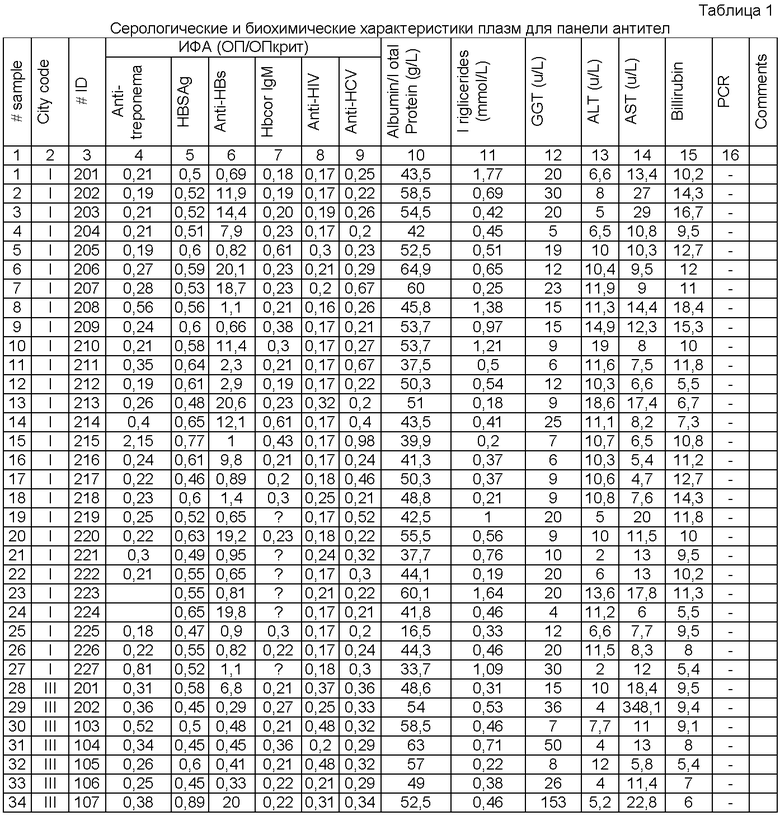
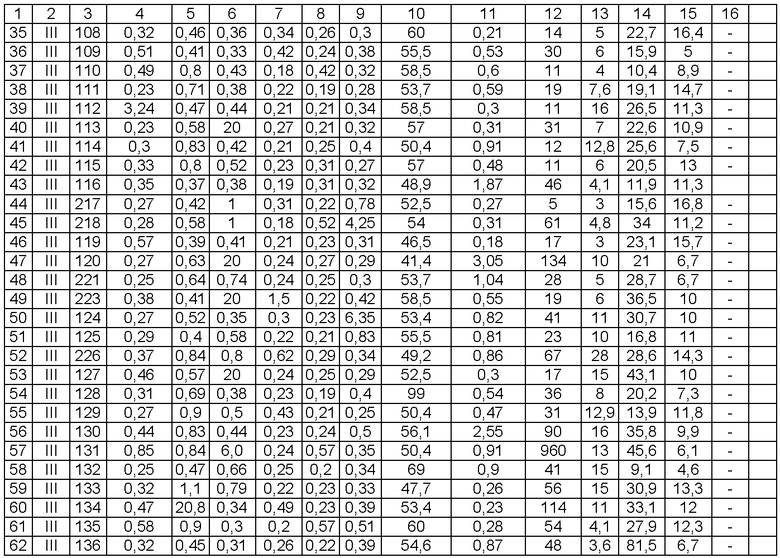
Характеристика индивидуальных образцов плазмы. Все образцы плазмы прошли всестороннюю аттестацию по иммунобиологическим маркерам: HBsAg, anti-HBs, anti-HBc IgM, anti-HBe, anti-HIV, anti-HCV and HBV DNA и биохимическим свойствам: общий белок, ALT, AST, GGT, bilirobin. Результаты представлены в табл.1.
Содержание HBsAg в исследуемых сыворотках определяют с помощью коммерческих тест-систем: «Рекоматгеп В» (ВФС 42-3170-98, ДЭУП «Вектор-БиАльгам», Кольцово, Новосибирская обл.), «Вектогеп В-HBs-антиген» и «Вектогеп В-HBs-антиген (Комплектация 2)» (ФСП 42-0117-0761-01, ЗАО «Вектор-Бест», Кольцово, Новосибирская обл.), "MonoLisa Ag HBs II" (Sanofi Pasteur, Франция).
Содержание анти-HBs антител определяют с помощью тест-системы «BeктоHBsAg-антитела-стрип» (ФСП 42-0117-0495-00, ЗАО «Вектор-Бест»).
Содержание анти-НВс IgM определяют с помощью тест-систем «Векто НВс-IgM стрип» (ЗАО «МБС», Новосибирск).
Содержание анти-НВс IgG определяют с помощью тест-систем «Векто НВс-IgG стрип» (ЗАО «МБС», Новосибирск).
Содержание анти-НВе IgG определяют с помощью тест-систем «Векто НВе-IgG стрип» (ЗАО «МБС», Новосибирск).
Содержание анти-ВИЧ и анти-ВГС антител определяют с помощью тест-систем «Рекомат-ВИЧ-1/2 ДС/М» (ФС 42-3345-96) и «ВГС-ДСМ» (ВФС 42-3114-98) (ЗАО «МБС», Новосибирск).
По результатам первичной аттестации отбирают кандидатов, содержащих анти-HBs и НВс IgM антитела, анти-НВс IgG и анти-НВе антитела. Из этих кандидатов готовят пулы одноименных антител.
Одновременно формируют выборку кандидатов, отрицательных на HBV DNA, HBsAg и не содержащих специфических антител. Из этой выборки готовят 6 пулов отрицательных образцов панели.
Кандидатов с антителами титруют в одноименных тест-системах, перечисленных ранее. Серийные 3-кратные разведения приготавливают, начиная с разведения 1:10. В качестве титра Т образца принимается (обратная) величина разведения нативной плазмы до значения ОП=ОПкрит.
Значения титров индивидуальных образцов плазмы используют для подбора коэффициентов разведения (КР) перед пулированием. Каждый образец плазмы должен быть представлен в кандидатском пуле в равном количестве. КР соответствует разведению образца в среднем до минимального титра.
Для формирования панели антител готовят около 20 пулов положительных по разным антителам сывороток и 8 пулов сывороток отрицательных. Следует иметь в виду, что большинство сывороток anti-HBs и anti-HBcAg - антитела не содержат HBsAg. Сыворотки anti-НВе и ant-HBc IgM являются, большей частью, положительными на HBV DNA and HBsAg. Поэтому панель антител к ВГВ содержит, в общем случае, и антигены, и антитела. Все пулы кандидатов, разведенных до рабочей концентрации, тестируют в нескольких диагностикумах российского и зарубежного производства (например, ЗАО МБС, Вектор Бест, BioRad и т.д.) для расчета аттестованной (паспортной) величины (табл.2). Из этих пулов отбирают 24 образца для панели антител.
Титры антител в кандидатских пулах в НЧС
Для испытаний стабильности формируют выборки положительных и отрицательных образцов панели - всего 5. Каждый пул делят на 5 частей - для испытаний при температурах 4°С, 37°С и 45°С, и при температуре - 20°С, выбранной в качестве референс-температуры.
Активность термостатированных образцов определялась относительно активности образцов, хранившихся при референс-температуре.
Оценки активности препаратов, хранившихся при повышенных температурах, далее используют для предсказания стабильности их при длительном хранении при различных температурах с использованием метода формальной кинетики Аррениуса [5].
Дополнительно выполняют испытания стабильности кандидатов - пулов в циклах замораживания-оттаивания.
Сыворотки стабилизированы добавлением мертиолята и гентамицина в количестве 0,02%.
В соответствии с требованиями экспертов ВОЗ по биологической стандартизации в процессе испытания сыворотки подвергают 5 циклам замораживания-оттаивания по 1 разу в сутки. Замораживание производят при температуре - 24°С в течение ночи. Оттаивание сывороток проводят при температуре 37°С на водяной бане.
ИФА проводят на системе «Вектогеп HBsAg-антитела-стрип», производитель «Вектор Бест».
По результатам испытаний установлено, что кандидаты в образцы панели антител выдерживают 4 цикла замораживания-оттаивания.
Панели сывороток, содержащих различные виды анти-HBV антител необходимы для разработки новых диагностических тест-систем и для выполнения внешнего контроля качества выполнения анализов в клинических диагностических лабораториях [6].
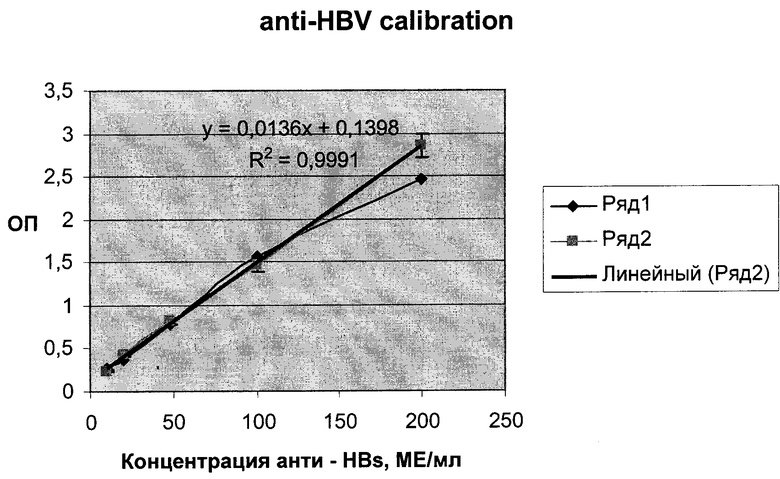
На чертеже дана кривая калибровки референс-препарата anti-HBs антител ОСО иммуноглоб человека против вируса гепатита В.
Далее следует пример выполнения способа.
Поступление сывороток здоровых доноров
Плазма доноров поступает на производство в гемаконах CPDA емкостью 250 мл, герметично укупоренные.
Каждая донорская плазма (сыворотка), поступающая на производство для изготовления панели антител, должна иметь паспорт с характеристиками - ИН (индивидуальный номер) донора, объем сыворотки, дата забора крови, предприятие - изготовитель, а также отвечать следующим требованиям: не иметь признаков гемолиза и гиперлипидемии, прозрачная, цвет - янтарный или светло-желтый, посторонние механические примеси, взвесь, осадок отсутствуют.
Инактивация сывороток здоровых доноров
Флаконы с донорской сывороткой помещают в термостат при температуре 56°С. Фиксируют время начала инактивации. Инкубирование сыворотки проводят 3 ч. После истечения этого времени сыворотку достают из термостата, фиксируют время окончания инактивации.
Измерение объема сывороток здоровых доноров
Измеряют объем каждой плазмы с помощью стерильного стеклянного мерного цилиндра.
Приготовление сыворотки из плазмы: гемаконы с плазмой прогревают до 37°С, с помощью шприца в гемакон вводят 2,7% раствор CaCl2 из расчета на 9 частей плазмы добавляют 1 часть CaCl2, тщательно перемешивают и помещают гемаконы на 1 ч в термостат при температуре 37°С для образования сгустка фибрина. Затем проводят 3-4 цикла замораживания-оттаивания плазмы для сжатия сгустка фибрина, полученную сыворотку фильтруют через каскад фильтров: 1,2 мкм, 0,8 мкм, 0,45 мкм.
Добавление к сыворотке раствора консерванта
В каждый флакон с донорской сывороткой добавляют мертиолят, сыворотку тщательно перемешивают. Конечная концентрация мертиолята в сыворотке составляет 0,015%.
Фасовка сывороток здоровых доноров
От каждого образца сыворотки в стерильном боксе в ламинаре автоматической пипеткой отбирают 5 аликвот по (1±0,05) мл сыворотки в пластиковые пробирки «Эппендорф» емкостью 1,5 мл для контроля по биохимическим показателям и для исследования вирусных маркеров в ИФА и методом ПЦР. Пробирки закрывают, на каждой пробирке маркером пишут кодовый номер образца сыворотки.
Оставшийся объем сыворотки фасуют в стерильные пластиковые флаконы емкостью 25-30 мл для длительного хранения. На каждом флаконе маркером пишут номер сыворотки.
Хранение сыворотки здоровых доноров
Донорскую сыворотку помещают на хранение в морозильные камеры при температуре от минус 30°С до минус 35°С. Сыворотку до переработки хранят при этих условиях в течение до 5-х лет. Допускается однократное замораживание и оттаивание сывороток.
Контроль биохимических показателей сывороток здоровых доноров
По одной аликвоте каждой донорской сыворотки передают в биохимическую лабораторию облЦСПИД для контроля биохимических показателей (уровень ферментов, общее содержание белка, pH). Содержание белка определяют микрометодом Лоури.
Сыворотки, не соответствующие требованиям по биохимическим показателям, отбраковывают и утилизируют.
Контроль аликвот сывороток здоровых доноров методом ИФА
По одной аликвоте каждой донорской сыворотки передают в ИФА лабораторию облЦСПИД для исследования сывороток на содержание HBs антигена, антител к ВГС, ВИЧ-1,2 типов и анти-HBs, анти-НВс, анти-НВе антител. ИФА анализ проводят на аттестованных ГИСК им.Л.А.Тарасевича, иммуноферментных тест-системах: «BeктoHBsAg-антитела», «ВектоНВс-IgM», «BeктоHBсAg-антитела» и «ВектоНВе-IgG» производства ЗАО МБС и других фирм.
Сыворотки, не соответствующие требованиям, предъявляемым к качеству сывороток здоровых доноров (т.е. содержащие HBs антиген, антитела к ВИЧ-1,2), отбраковывают и помещают в банк сывороток для выполнения исследовательских работ.
Изготовление положительных кандидатов панели антител
Для приготовления панели сывороток с различными типами антител отбирают в процессе первичного скрининга (методами ИФА и ПЦР) 60 иммуноспецифических сывороток крови HBV-инфицированных лиц с положительным ПЦР.
Отобранные после первичного скрининга иммуноспецифические сыворотки титруют в тест-системах "РекомбиБест анти-HBs" (ЗАО "ВекторБест", г.Новосибирск). Причем сыворотки титруют в 3-х параллельных определениях на двух планшетах.
В качестве иммуноспецифических образцов для приготовления панели отбирают те сыворотки, которым в процессе титрования соответствует закономерное уменьшение величин ОП в ИФА.
На основании анализа результатов ИФА и ПЦР устанавливают, что используемые для приготовления панели иммуноспецифические сыворотки содержат антитела к HBs, HBc и к НВе антигенам. Определяют спектр антител во всех 60-ти иммуноспецифических сыворотках. В сумме отобранные сыворотки имеют антитела ко всем антигенам HBV. По результатам титрования на основе статистической обработки строят усредненные кривые титрования для каждой иммуноспецифической сыворотки.
Для определения кратности разведения выделяют участок прямо пропорциональной зависимости значений ОП от степени разведения и калибруют его относительно референс-препарата ОСО иммуноглобулинов человека против вируса гепатита В 42-28-320-00 (см. чертеж). На этих участках для каждой сыворотки выбирают значения титра (Т) в соответствии с требуемой концентрацией специфических антител. По кривым титрования определяют необходимую степень разведения для каждого номера пула от №1 до №19.
Для изготовления каждого положительного кандидата используют пул 3-4 сывороток, разведенных каждая до титра 1:5. Кратность разведения подбирают таким образом, чтобы значения оптических плотностей при выполнении ИФА лежали в диапазоне от значений ОП Крит для выбранной тест-системы "РекомбиБест анти-HBs" (ЗАО "ВекторБест", г.Новосибирск) до значений ОП, равных 1,4 о.е.
На этапе разведения иммунные сыворотки каждого номера смешивают в равных долях с одинаковым титром. В состав каждого кандидата добавляют стабилизатор
[10].
Смешивание пула для каждого кандидата осуществляют в течение 5-7 мин в колбе объемом 1500 см3, установленной на магнитной мешалке. Всего приготовлено 6 иммуноспецифических кандидатов с титром в диапазоне от 100 до 200 и 2 иммуноспецифических кандидата с титром 50, 2 с титром 20 и 9 образцов с титрм от 2-х до 10-ти. При этом №1-8 содержат анти-HBs, №9-12 содержат HBc IgM антитела, №13-16 содержат анти-НВс IgG антитела и №17-19 содержат НВе IgG антитела.
Дополнительно готовят 8 кандидатов - отрицательных образцов панели №20-27, которые получают смешиванием 3-4 образцов отрицательных сывороток в колбах объемом 1000 мл на магнитной мешалке при добавлении стабилизатора. Все кандидаты №1-27 разливают по 600 мкл во флаконы R2 и замораживают в кассетах по 60 флаконов.
Режим лиофилизации на установке "TG-50" (ФРГ) подбирают по результатам предварительного физико-химического анализа фазовых превращений в разводящей донорской сыворотке со стабилизатором при замораживании. Подготовленные сыворотки панели замораживают со скоростью (0,5-1,0)°С/мин до температуры - 60°С и выдерживают при этой температуре в течение 10 ч. Затем кассеты с кандидатами быстро загружают в предварительно охлажденную камеру лиофильной установки и включают вакуумный насос. На этапе сублимации льда температуру материала поддерживают ниже температуры его стеклования (-30°С).
Средняя скорость нагревания материала на этапе досушивания составляет 6°С/мин, время выдерживания при 27°С составляет 8 ч.
Лиофильно высушенные сыворотки панели имеют остаточное содержание воды около 1,0 мас.%. Флаконы с сыворотками укупоривают под вакуумом.
Установлено, что в процессе лиофилизации специфическая активность сывороток не изменяется.
Сыворотки панели инактивированы, но с ними необходимо обращаться как с потенциально инфекционным материалом.
Испытания стабильности
Стабильность сывороток в различных условиях хранения в темноте во флаконах определяют по результатам теста термодеградации.
Объединенная выборка лиофилизованных кандидатов анти-ВГВ панели была исследована в тесте ускоренной термодеградации. Образцы термостатировали в условиях контролируемой температуры при температурах: -20°С, +4°С, +37°С и 45°С, извлекали через определенные промежутки времени, растворяли в бидистиллированной воде и анализировали в дублях в тест-системах «анти-HBs» (МБС) и "HBcore IgM" (ВекторБест). В эксперименте не отмечены экспериментально значимые потери активности для определенного типа антител. Средние величины рассчитанных % потерь активности за месяц и за год приведены в табл.3. Образцы продемонстрировали высокую стабильность. Предсказываемая потеря активности за год при +4°С составляет около 0.3% для кандидатов. Предсказанная потеря активности за месяц составляет примерно 4% при 37°С, давая возможность кратковременному хранению при повышенных температурах, например, при транспортировке образцов.
Следовательно, имеются определенные основания предполагать, что оба кандидата анти-HBs и "HBcore IgM" в составе панели имеют достаточный уровень стабильности.
Предсказание активности образцов панели антител на основе ускоренных испытаний
Рекомендуется использовать растворенные образцы панели антител при хранении при 4°С в течение месяца.
Стабильность жидких образцов панели испытывают в тесте замораживание - оттаивание. Результаты испытаний показывают, что специфические свойства кандидатов не изменяются в течение 4-х циклов замораживания - оттаивания.
По результатам теста установлено, что сыворотки панели должны при температуре (2-6)°С сохранить неизменной специфическую активность в течение не менее трех лет.
Список использованной научно-технической и патентной литературы
1. Fields H.A., David C.I., Bradley D.W. and Maynard J.E. Experimental conditions affecting the sensitivity of enzyme-linked immunosorbent assay (ELISA) for detection of hepatitis В surface antigen (HBsAg). // Bulletin of the World Health Organization, 1983, v.61, 1, p.135-142.
2. Канев А.Н., Воробьева М.С., Шалунова Н.В. и др. Конструирование и производство референс-панелей сывороток для контроля качества тест-систем в России. // Вестник АМН, 1998, №3.
3. Development of Control Serum for Microbial Antibody Tests // Biologicals (2001) 29, 39-43.
4. Ferguson-M; Holmes H., Sands E.D. National Institute for Biological Standards and control / UK Blood Transfusion Service working standards for: HbsAg, anti-HCV and anti-HIV-1. // Vox-Sang. 2001; 80: 205-210.
5. Контроль качества клинических диагностических лабораторных исследований. Принципы и методы. Под ред проф. Меньшикова В.В. Москва, 1994, 154 стр.
6. Carrett A.J., Seagroatt V., Supran E.M. at all. - «Бюллетень ВОЗ», 1988, т.66, №1, стр.44-60.
7. Патент РФ №2136313. "СТАБИЛИЗИРУЮЩИЙ СОСТАВ ДЛЯ ПОЛУЧЕНИЯ РЕФЕРЕНС-СЫВОРОТОК, СОДЕРЖАЩИХ IGM-АНТИТЕЛА".
8. Информационный бюллетень фирмы Boston Biomedica, Inc (USA), 1994, p.12.
9. Dawson GJ., Lesniewski RR., Stewart JL., Boardway KM., Gutierrez RA., Pendy L., Johnson RG., Alcalde X., Rote KV., Devare SG., et al. - Detection of antibodies to hepatitis С virus in U.S. blood donors. - "J-Clin-Microbiol." 1991, Mar, v.29, N3, p.551-6.
10. Патент РФ №2011202 "Стабилизирующий состав для контрольных сывороток положительных на антитела к вирусным и микробным антигенам".
11. Kirkwood TBL, Tydeman MS. Design and analysis of accelerated degradation tests for the stability of biological standards II. A flexible computer program for data analysis Journal of Biological Standardization Volume, 1984, 12, 207-214.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ РАБОЧЕГО СТАНДАРТА СЫВОРОТОК, СОДЕРЖАЩИХ АНТИТЕЛА К ВИРУСУ ГЕПАТИТА С | 2008 |
|
RU2380711C2 |
| СПОСОБ ПОЛУЧЕНИЯ РЕФЕРЕНС-ПАНЕЛИ СЫВОРОТОК ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ И ИММУНОБЛОТОВ, ИСПОЛЬЗУЕМЫХ ДЛЯ СЕРОЛОГИЧЕСКОЙ ДИАГНОСТИКИ МАРКЕРОВ ВИЧ-1 | 2015 |
|
RU2603483C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПАНЕЛИ СЫВОРОТОК РАЗЛИЧНЫХ СУБТИПОВ И ГЕНОТИПОВ ВИРУСА ГЕПАТИТА В ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА В | 2006 |
|
RU2346282C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ НИЗКОТИТРАЖНОЙ ПАНЕЛИ СЫВОРОТОК ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ И ИММУНОБЛОТОВ, ИСПОЛЬЗУЕМЫХ ДЛЯ ДИАГНОСТИКИ АНТИТЕЛ К РАЗНЫМ СУБТИПАМ ВГС | 2009 |
|
RU2408024C1 |
| ПАНЕЛЬ СЫВОРОТОК, СОДЕРЖАЩИХ АНТИТЕЛА К АНТИГЕНАМ HCV РАЗНЫХ СУБТИПОВ | 2010 |
|
RU2456617C2 |
| МАСТЕР ПАНЕЛИ СЫВОРОТОК, СОДЕРЖАЩИХ И НЕ СОДЕРЖАЩИХ HBsAg, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2005 |
|
RU2314540C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПАНЕЛИ СЫВОРОТОК С HBsAg AD- И AY-СУБТИПОВ ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА В | 2011 |
|
RU2463610C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕФЕРЕНС-ПАНЕЛИ ОБРАЗЦОВ СЫВОРОТОК, ПРЕДНАЗНАЧЕННОЙ ДЛЯ ОЦЕНКИ СПЕЦИФИЧНОСТИ РЕЗУЛЬТАТОВ СЕРОЛОГИЧЕСКОЙ ДИАГНОСТИКИ СОЦИАЛЬНО ЗНАЧИМЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2521232C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕФЕРЕНС-ПАНЕЛИ ДЛЯ КОНТРОЛЯ КАЧЕСТВА ТЕСТ-СИСТЕМ И ВАКЦИН ПРОТИВ ГЕПАТИТА В | 1999 |
|
RU2181893C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАБОЧИХ СТАНДАРТОВ СЫВОРОТОК, СОДЕРЖАЩИХ AY И AD СУБТИПЫ HBsAg | 2004 |
|
RU2271011C1 |
Изобретение относится к биотехнологии и иммунологии, а именно к иммунологической диагностике. Предложена технология изготовления панелей сывороток, содержащих антитела опасных вирусных инфекций. Для приготовления панели сывороток с различными типами антител отбирают в процессе первичного скрининга (методами ИФА и ПЦР) 60 иммуноспецифических сывороток крови HBV-инфицированных лиц с положительным ПЦР и 25 донорских сывороток. На основании анализа результатов ИФА и ПЦР устанавливают, что используемые для приготовления панели иммуноспецифические сыворотки содержат антитела к HBs, НВс и к НВе антигенам. Одновременно формируют выборку кандидатов, отрицательных на HBV DNA, и не содержащих антител к антигенам HBV. Из этой выборки готовят 6 пулов отрицательных образцов панели. Панель содержит весь спектр антител к ВГВ и позволяет контролировать эффективность применяемого способа лечения гепатита B. 1 з.п. ф-лы, 3 табл., 1 ил.
1. Способ изготовления панели сывороток для определения антител к вирусу гепатита В, отличающийся тем, что образцы плазмы аттестуют по иммунобиологическим маркерам: HBsAg, anti-HBs, anti-HBc JgM, anti-HBe, anti-HIV, anti-HCV and HBV DNA, и биохимическим свойствам: общий белок, ALT, AST, GGT, билирубин; в качестве иммуноспецифических образцов для приготовления панели отбирают те сыворотки, которым в процессе титрования соответствует закономерное уменьшение величин ОП в ИФА и содержат антитела к HBs, НВс и к НВе антигенам, для отрицательных образцов панели отбирают сыворотки, отрицательные в ПЦР, и не содержащие HBV антигены и антитела к ним, а также антитела к ВГС, ВИЧ-1,2 типов; для изготовления каждого положительного кандидата используют пул 3-4 сывороток, разведенных каждая до титра 1:5.
2. Способ по п.1, отличающийся тем, что лиофильно высушенные сыворотки панели имеют остаточное содержание воды около 1,0 мас.%.
| СПОСОБ ИЗГОТОВЛЕНИЯ КОНТРОЛЬНОЙ ПАНЕЛИ СЫВОРОТОК AY ЭНД AD СУБТИПОВ HBsAg ДЛЯ КОНТРОЛЯ КАЧЕСТВА ДИАГНОСТИКИ ГЕПАТИТА B | 2003 |
|
RU2265028C2 |
| ТАО J | |||
| at al | |||
| Influence factors of serum fibrosis markers in liver fibrosis | |||
| World J Gastroenterol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| LARIZZA D | |||
| at al | |||
| Serum liver enzymes in Turner syndrome | |||
| Eur J Pediatr | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| HATZAKIS A | |||
| at al | |||
| HBV virological assessment | |||
| J Hepatol | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Review. | |||
Авторы
Даты
2009-09-20—Публикация
2007-05-29—Подача