Изобретение относится к биохимии, а именно к способам проведения иммуноферментного и ДНК-гибридизационного анализа.
Известны конъюгат и способ одновременного выявления обоих компонентов связывающейся пары [заявка №2002104927/15, МПК G01N 33/48, опубл. 2005.04.27], где описывается твердофазный иммунологический микроанализ с использованием в качестве меток флуоресцентных красителей и регистрацией сигналов методом проточной цитометрии.
Недостаток способа заключается в том, что в нем для одновременного выявления 2-х компонентов используется флуоресцентный анализ. Недостатками которого, в свою очередь, являются токсичность используемых красителей, высокий фон флуоресцентного сигнала, который снижает его чувствительность, и ограниченная область применения (только для иммунного анализа).
Известен коньюгат для иммуноферментного анализа и способ иммуноферментного анализа [патент РФ №2014610, МПК G01N 33/535, опубл. 1994.06.15, (прототип)], где конъюгат получается путем химической сшивки биоспецифической молекулы с ферментами с последующей хроматографической очисткой. Для проведения анализа способ использует две фазы: твердую фазу для иммобилизации формируемого биоспецифического комплекса и жидкую, для внесения растворов реагирующих веществ и промежуточных промывок, а для обнаружения наличия аналита и его количества использует конъюгаты биоспецифической молекулы с репотерным ферментом.
Недостаток конъюгата заключаются в том, что в качестве фермента используют природную лаккозу, получение которой достаточно затратный и трудоемкий процесс.
Недостатки способа заключаются в том, что он пригоден только для иммуноферментного анализа и при его осуществлении на твердой фазе иммобилизуется только один биоспецифический комплекс и соответственно одна процедура дает ответ о содержании только одного аналита. Измерение проводят колориметрическим методом, обладающим недостаточной чувствительностью и узким линейным диапазоном.
Техническим результатом изобретения является разработка экспрессного, более точного, универсального и технологичного биолюминесцентного способа молекулярного микроанализа.
Технический результат достигается тем, что в конъюгате для биолюминесцентного молекулярного микроанализа, полученном из фермента, соединенного с биоспецифическим реагентом, с последующей очисткой конъюгата на хроматографической колонке, новым является то, что в качестве фермента используют рекомбинантный Ca2+ зависимый фотопротеин обелин с измененным спектром биолюминесценции: рекомбинантный обелин W92F; H22E или рекомбинантный обелин Y138F.
Технический результат достигается также и тем, что в способе одновременного определения двух аналитов биолюминесцентным молекулярным микроанализом, включающем обработку твердой фазы биоспецифическими реагентами, отделение непрореагировавшей жидкой фазы, обработку твердой фазы ферментосодержащим конъюгатом, разделение жидкой и твердой фаз и анализ твердой фазы, новым является то, что в качестве биоспецифического реагента для первой обработки твердой фазы используют два разных иммуноглобулина, или один иммуноглобулин с двойной специфичностью, или два разных олигонуклеотида, а конечную обработку твердой фазы проводят одновременно двумя коньюгатами, состоящими соответственно из рекомбинантных Ca2+ зависимых фотопротеинов обелинов с разными спектрами биолюминесценции и молекул с разной биоспецифичностью, где в качестве рекомбинантных обелинов используют W92F; H22E и рекомбинантный обелин Y138F, с последующим анализом на двухканальном биолюминометрес широкополостными светофильтрами.
Перечисленные выше отличительные от прототипа признаки позволяют сделать вывод о соответствии заявляемых технических решений критерию «новизна».
Признаки, отличающие заявляемые технические решения от прототипа, не выявлены в других технических решениях и, следовательно, обеспечивают заявляемому решению соответствие критерию «изобретательский уровень».
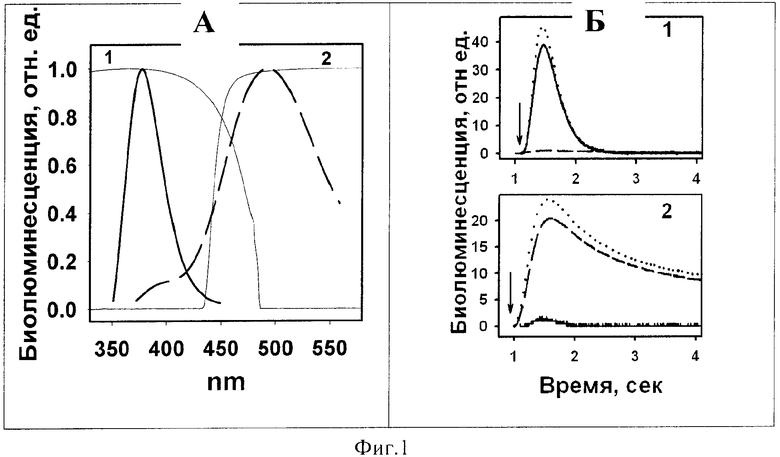
На фиг.1А представлены спектры биолюминесценции рекомбинантных обелинов W92F; H22E (-) и Y138F(- -) и спектры пропускания использованных для разделения сигналов широкополостных фотофильтров и ФС6 (1) и ЖС 16 (2). На фиг.1Б показано прохождение сигналов от «цветных» обелинов через фотофильтры, установленные в каналах биолюминометра 1 и 2. Стрелками указан момент впрыска раствора CaCl2. Точечными линиями показаны пропускание каждого канала соответствующих сигналов без светофильтра.
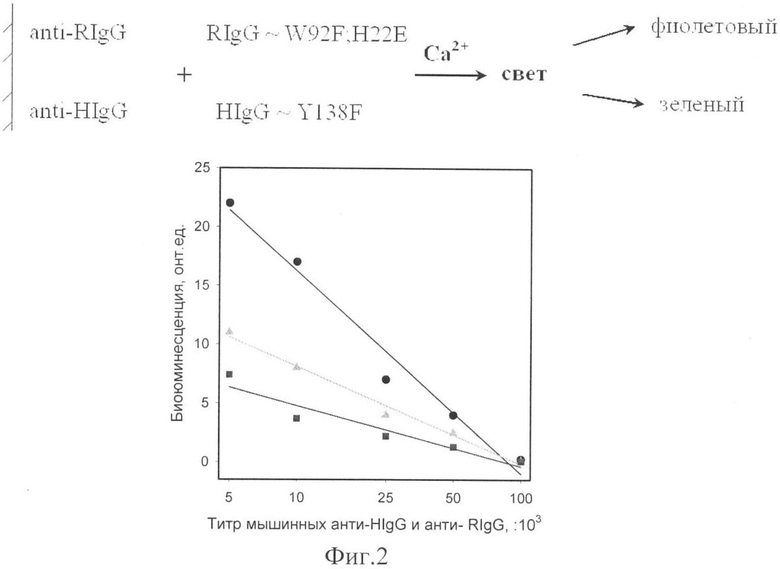
На фиг.2 (вверху) дана схема одновременного анализа двух разных иммуноглобулинов - кролика (RIgG) и человека (HIgG). На фиг.2 (внизу) результаты определения мышиных анти-RigG (■) и анти-HigG (▲) антител, полученные разделением сигналов с помощью светофильтров. Общий сигнал меток без разделения показан (●).
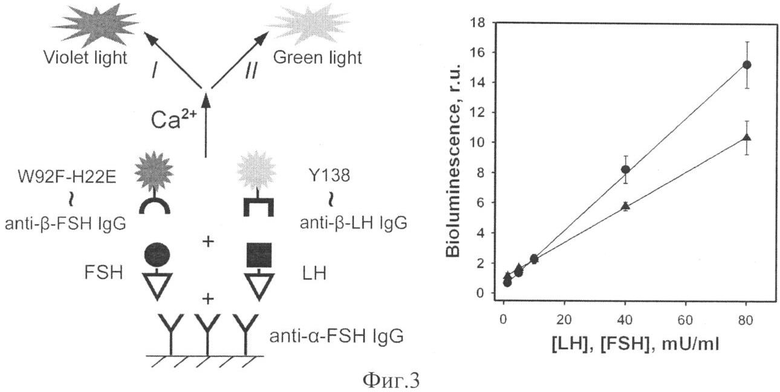
На фиг.3 (слева) показана схема проведения одновременного твердофазного иммуноанализа гонадотропных гормонов (лютеинизирующего - LH и фолликулстимулирующего - FSH) в стандартных сыворотках человека; справа приведены полученные калибровочные кривые при одновременном двухцветном определении LH (▲) и FSH (●).
При реализации способа рекомбинантные формы Ca2+-активирумого фотопротеина обелина с измененными спектрами биолюминесценции химически коньюгируют с гаптенами (например, биотином или олигонуклеотидами) или другими белками (например, стрептавидином или иммуноглобулинами) и полученные производные используют в качестве специфических меток для связывания с соответствующими анализируемыми молекулами в образце (например, сыворотки крови, ампликонами после ПЦР-процедуры). На твердой фазе (например, поверхность пластиковых пробирок или микрочастиц) иммобилизуются специфические комплексы (например, антигены-антитела или нуклеотидные гибриды), состав которых зависит от наличия анализируемого вещества в образце. После обработки твердой фазы смесью специфических меток и необходимых промывок сигнал от каждого аналита регистрируется сразу после внесении в пробирку раствора CaCl2, с помощью двухканального биолюминометра. В каждый канал встраивается фотофильтр, обеспечивающий прохождение светового сигнала только одного цвета. Таким образом, каждый канал регистрирует сигнал только одной метки (фиг.1Б).
Пример 1. Получение химических конъюгатов мутантных форм обелина с иммуноглобулинами
Тионилирование мутантных форм обелина проводили в 50 мМ BICINE, pH 8,5, 250 мМ NaCl, 5 мМ ЭДТА, используя 10-кратный молярный избыток 2-иминотиолана в течение 30 мин при комнатной температуре. Избыток реагента отделяли гель-фильтрацией на колонке, уравновешенной 20 мМ PIPES, pH 7,5, 250 мМ NaCl, 5 мМ ЭДТА. Sulfo-SMCC (сульфо-сукцинимидный эфир 4-(N-малеимидометил-) циклогексановой кислоты)-активацию иммуноглобулинов, проводили в 20 мМ PIPES, pH 7,5, 250 мМ NaCl, 5 мМ ЭДТА используя 50-кратный молярный избыток Sulfo-SMCC в течение двух часов при комнатной температуре. Избыток реагента отделяли гель-фильтрацией на колонке, уравновешенной 20 мМ PIPES, pH 7,5, 250 мМ NaCl, 5 мМ ЭДТА. Конъюгирование проводили инкубированием тионилированных мутантов обелина с SMCC-активированными иммуноглобулинами в молярном соотношении 1:5 при 4°С в течение ночи. Полученные конъюгаты мутантных белков с иммуноглобулинами выделяли гель-фильтрацией на колонке, заполненной биогелем Р-150, уравновешенной 0,1М фосфатным буфером pH 7,0, содержащим 0,15М NaCl и 5 мМ ЭДТА, или на колонке Superose 6, уравновешенной буфером, содержащем 0,02 М Трис-HCl pH 7,0, 0,1 М NaCl и 5 мМ ЭДТА.
Пример 2. Получение коньюгатов мутантных форм обелина с олигонуклеотидами
Тионилирование мутантных форм обелина проводили в 50 мМ фосфатном буфере pH 7.5, 5, 0,15 М NaCl (PBS), 5 мМ ЭДТА, используя 10-кратный молярный избыток 2-иминотиолана в течение 30 мин при комнатной температуре. Избыток реагента отделяли гель-фильтрацией на колонке, уравновешенной тем же буфером. SMCC-активацию олигонуклеотидов NH2-dT(30) и NH2-dA(30) проводили в 0.1 М NaHCO3, используя 100-кратный молярный избыток SMCC в течение 30 мин при комнатной температуре. Избыток реагента отделяли гель-фильтрацией на колонке, уравновешенной 50 ммоль/L NaH2PO4 pH 7.5, 5 ммоль/L EDTA. Конъюгирование проводили инкубированием тионилированных мутантов обелина с SMCC-олигонуклеотидами в молярном соотношении 3:1 при 4°С в течение ночи. Полученные конъюгаты мутантных белков с олигонуклеотидами выделяли анионообменной хроматографией на колонке MonoQ, уравновешенной 20 мМ Tris-HCl pH 7.0, 5 мМ ЭДТА в градиенте раствора NaCl (0-47%) в том же буфере.
Пример 3. Одновременный биолюминесцентный анализ античеловеческих и антикроличьих иммуноглобулинов мыши
В пробирки вносили по 200 мкл смеси моноклональных мышиных античеловечеких и антикроличьих IgG с конечным титром по каждому 5000, 10000, 25000, 50000 и 100000, сорбцию проводили в течение ночи при 4°С. После промывки (трижды, PBS, 0,1% Tween 20, 5 мМ ЭДТА) блокировали не занятые места на поверхности 1% бычьим сывороточным альбумином в PBS буфере (1 час при 37°С). После промывки в пробирки вносили по 200 мкл раствора конъюгатов RIgG~W92F; H22E и HIgG~Y138F. Реакцию проводили 1 ч при комнатной температуре. После чего содержимое лунок отбрасывали, лунки промывали. Биолюминесцентный сигнал обелина измеряли сразу после впрыска 200 мкл 0,1 М раствора CaCl2 в 0,1 М ТрисHCl pH 8,8. Разделение сигналов производили с помощью широкополостных оптических фильтров, вмонтированных в каналы биолюминометра.
Пример 4. Одновременный биолюминесцентный анализ LH и FSH
В пробирки, активированные анти-αFSH (10 мкг/мл), вносили смесь стандартных сывороток с концентрациями 1,25; 5; 10; 40; 80 мМЕ/мл и смесь контрольных сывороток. После инкубации (при перемешивании 1 час при 37°С) и промывки (трижды, PBS, 0,1% Tween20, 5 мМ ЭДТА) вносили смесь меток в соотношении 1:1 (анти-βFSH~W92F; H22E (7,8 мкг/мл) и анти-βLH~Y138F (1 мкг/мл)). Реакцию проводили 40 мин при комнатной температуре при перемешивании. Снова промывали. Биолюминесцентный сигнал сорбированных меток измеряли сразу после впрыска 0,1 М раствора CaCl2 в 0,1 М ТрисHCl pH 8,8. Разделение сигналов производили с помощью широкополостных оптических фильтров, вмонтированных в каналы биолюминометра.
В заявляемом способе в качестве ферментов используются рекомбинантные фотопротеины, выделенные из рекомбинантных штаммов бактерий E coli, обладающих высокой продуктивностью, что существенно упрощает и удешевляет их получение.
Биолюминесценция фотопротеинов происходит с высоким квантовым выходом и характеризуется отсутствием фонового сигнала, что обеспечивает высокую чувствительность анализа.
Реакция фотопротеинов крайне проста - биолюминесценция инициируется добавлением раствора CaCl2 и имеет характер яркой вспышки, в нашем случае фиолетового и зеленого цвета (биолюминесценция обелина дикого типа имеет голубой цвет).
Биолюминесцентный сигнал фотопротеинов имеет практически не ограниченный линейный диапазон.
Заявляемый способ обеспечивает возможность одновременного определения двух аналитов.
Измерения проводят биолюминесцентным способом, который обеспечивает высокую чувствительность, сравнимую только с радиоизотопным (до 1 аттомоль).
Способ предназначен для проведения как иммуноанализа, так и ДНК-гибридизационного анализа.
Изобретение относиться к области биохимии, а именно к способам проведения иммуноферментного и ДНК-гибридизационного анализа. Предлагается конъюгат для биолюминесцентного молекулярного микроанализа, полученный из фермента, соединенного с биоспецифическим реагентом, где в качестве фермента используют Са2+ зависимый фотопротеин обелин с измененным спектром биолюминесценции: рекомбинантный обелин W92F; H22E или рекомбинантный обелин Y138F. Способ одновременного определения двух аналитов биолюминесцентным молекулярным микроанализом включает в себя обработку твердой фазы биоспецифическими реагентами, отделение непрореагировавшей жидкой фазы, обработку твердой фазы ферментсодержащим конъюгатом, разделение жидкой и твердой фаз и анализ твердой фазы. При этом в качестве биоспецифического реагента для первой обработки твердой фазы используют два иммуноглобулина или один иммуноглобулин с двойной специфичностью или два разных олигонуклеотида. Конечную обработку твердой фазы проводят одновременно двумя коньюгатами, состоящими, соответственно, из рекомбинантных обелинов с разными спектрами биолюминесценции и молекул с разной биоспецифичностью, где в качестве рекомбинантных обелинов используют W92F; H22E и рекомбинантный обелин Y138F с последующим анализом на двухканальном биолюминометре с широкополосными светофильтрами. Использование данного способа позволяет более точно, быстро, универсально и технологично проводить биолюминесцентный способ молекулярного микроанализа 2 н.п. ф-лы, 3 ил.
1. Конъюгат для биолюминесцентного молекулярного микроанализа, полученный из фермента, соединенного с биоспецифическим реагентом, с последующей очисткой конъюгата на хроматографической колонке, отличающийся тем, что в качестве фермента используют рекомбинантный Са2+ зависимый фотопротеин обелин с измененным спектром биолюминесценции: рекомбинантный обелин W92F; H22E или рекомбинантный обелин Y138F.
2. Способ одновременного определения двух аналитов биолюминесцентным молекулярным микроанализом, включающий обработку твердой фазы биоспецифическими реагентами, отделение непрореагировавшей жидкой фазы, обработку твердой фазы ферментосодержащим конъюгатом, разделение жидкой и твердой фаз и анализ твердой фазы, отличающийся тем, что в качестве биоспецифического реагента для первой обработки твердой фазы используют два разных иммуноглобулина или один иммуноглобулин с двойной специфичностью или два разных олигонуклеотида, а конечную обработку твердой фазы проводят одновременно двумя коньюгатами, состоящими, соответственно, из рекомбинантных Ca2+ зависимых фотопротеинов обелинов с разными спектрами биолюминесценции и молекул с разной биоспецифичностью, где в качестве рекомбинантных обелинов используют W92F; H22E и рекомбинантный обелин - Y138F, с последующим анализом на двухканальном биолюминометре с широкополосными светофильтрами.
| ФРАНК Л.А | |||
| и др | |||
| Использование Ca-активируемого фотопротеина обелина как метки в иммуноферментном анализе | |||
| Иммунология, 1997, №1, с.55-57 | |||
| US 6649414 B1, 18.11.2003 | |||
| US 5648218 A, 15.07.1997 | |||
| US 7241864 A1, 10.07.2007 | |||
| US 20050214776 A1, 29.09.2005 | |||
| VISOTSKI E.S | |||
| et al | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
Авторы
Даты
2009-11-20—Публикация
2008-06-04—Подача