Родственные заявки
Данная патентная заявка претендует на приоритет временной заявки №60/552778, поданной 12 марта 2004 г. и временной заявки №60/553059, поданной 15 марта 2004 г., которые целиком включены сюда в качестве ссылок.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область техники
Настоящее изобретение относится к обнаружению и оценке свежести, или степени деградации, или порчи продукта на белковой основе, как показателя уровня качества продукта на белковой основе.
Описание известного уровня техники
Традиционные способы оценки свежести или степени порчи рыбы включают сенсорную оценку (внешний вид, проба на ощупь и запах). Этот способ является субъективным и спорным.
Патент США №5744321 раскрывает колориметрический способ быстрой оценки степени бактериальной деградации рыбы, такой как треска, полосатая зубатка и зимняя камбала, путем смешивания рыбного мяса с питательным бактериальным бульоном и проведения реакции экстракта с водорастворимым хромогеном, таким как ионизированная соль тетразолиевого красителя, который вступает в восстановительную реакцию с бактериями рыбы с образованием водонерастворимого формазанового красителя или окрашенного продукта реакции. Затем прибавляют поверхностно-активный агент для облегчения солюбилизации образовавшегося формазанового красителя, проводят лизис, и останавливают реакции, и прибавляют растворитель типа алифатического спирта для растворения образовавшегося формазанового красителя или окрашенного продукта реакции и предотвращения дальнейшего разрушения и потемнения со временем. Растворенный продукт реакции имеет окраску, интенсивность которой зависит от бактериальной популяции образца рыбы, и которая может быть оценена колориметрически путем визуального сравнения со стандартной цветовой шкалой, указывающей низкую, среднюю и высокую бактериальную обсемененность. Этот способ является усложненным, потому что включает использование ряда стадий и реагентов.
Таким образом, существует потребность в создании точного, удобного и объективного способа оценки свежести рыбных продуктов для поставщиков рыбы, ресторанов, компаний, оказывающих представительские услуги, и продовольственных предприятий и т.д.
Суть изобретения
Настоящее изобретение предусматривает способ оценки свежести рыбного продукта, включающий:
вырезание небольшого количества образца из рыбного продукта;
прибавление к образцу эффективного количества окрашивающего реагента, включающего, по меньшей мере, один из проникающего в клетку красителя и не проникающего в клетку флуоресцентного красителя;
инкубирование образца с добавленным окрашивающим реагентом в течение предварительно определенного периода времени;
определение свежести рыбного продукта на основании, по меньшей мере, одного из следующих параметров: интенсивность первой флуоресценции, эмитируемой инкубируемым образцом, интенсивность второй флуоресценции, эмитируемой инкубируемым образцом, первое расстояние от верхнего конца образца до самой дальней точки образца, в которой детектируется первая флуоресценция, и второе расстояние от верхнего конца образца до самой дальней точки образца, в которой детектируется вторая флуоресценция.
В присутствии внутриклеточной эстеразной активности проникающий в клетку краситель превращается в соединение, эмитирующее первую флуоресценцию. Не проникающий в клетку флуоресцентный краситель не проникает через интактные мембраны живых клеток, но может проникать в нарушенные мембраны клеток и эмитировать вторую флуоресценцию. Если окрашивающий реагент включает как проникающий в клетку краситель, так и не проникающий в клетку краситель, то первая флуоресценция должна отличаться от второй флуоресценции, т.е. они должны эмитировать разные цвета флуоресценции. Примеры проникающих в клетку красителей включают кальцеин AM и С12-резазурин. Примеры не проникающих в клетку красителей включают гомодимер EthD-1, краситель Sytox® Green и краситель YoYo-1.
Кроме того, проникающий в клетку краситель, такой как кальцеин AM и С12-резазурин, может быть использован в комбинации с красителем трипановым синим. Окрашивание красителем трипановым синим зависит от потери целостности мембранами мертвых клеток. Краситель трипановый синий нормально не проходит через интактные клеточные мембраны. В общем, мертвые клетки становятся проницаемыми для красителя трипанового синего. Таким образом, краситель трипановый синий может гасить флуоресценцию мертвых клеток в сочетании с проникающим в клетку красителем. Снижение флуоресценции после прибавления трипанового синего может быть мерой числа мертвых клеток.
В соответствии с одним вариантом исполнения настоящего изобретения стадия определения может быть проведена путем сравнения, по меньшей мере, одного параметра с предварительно установленной корреляционной зависимостью между свежестью и, по меньшей мере, одним параметром.
Интенсивности первой флуоресценции и второй флуоресценции могут быть количественно определены с помощью цифрового устройства, и предварительно установленная корреляция может быть определена на основании количественно определенной интенсивности первой флуоресценции и второй флуоресценции.
В соответствии с другим вариантом исполнения настоящего изобретения первая флуоресценция и вторая флуоресценция могут быть зарегистрированы в виде изображения с помощью оптического устройства, и предварительно установленная корреляция между свежестью и интенсивностью, по меньшей мере, одной из первой флуоресценции и второй флуоресценции может быть представлена в виде стандартной цветовой шкалы.
Предпочтительно, окрашивающий реагент включает эффективное количество кальцеина AM и эффективное количество гомодимера EthD-1. Свежесть первого продукта может быть затем определена на основании красной (гомодимер EthD-1) флуоресценции и зеленой (кальцеин) флуоресценции, эмитируемой образецом.
В соответствии с еще одним вариантом исполнения настоящего изобретения не проникающий в клетку флуоресцентный краситель, входящий в состав окрашивающего реагента, является красителем трипановым синим. Свежесть первого продукта может быть затем определена на основании синей окраски, появляющейся в образце. Предпочтительно, свежесть определяют по величине расстояния, на которое краситель трипановый синий проникает в образец, причем более свежая рыба соответствует меньшей глубине проникания.
Другие цели и признаки настоящего изобретения будут понятны из приведенного далее детального описания, рассматриваемого в сочетании с прилагаемыми чертежами.
Следует понимать однако, что чертежи предназначены только для иллюстрации, а не для установления объема изобретения, который определяется прилагаемой формулой изобретения. Следует также понимать, что чертежи не обязательно выполнены в масштабе и что, если не указано иное, они предназначены только для концептуальной иллюстрации описанных тут конструкций и процедур.
Краткое описание чертежей
На чертежах:
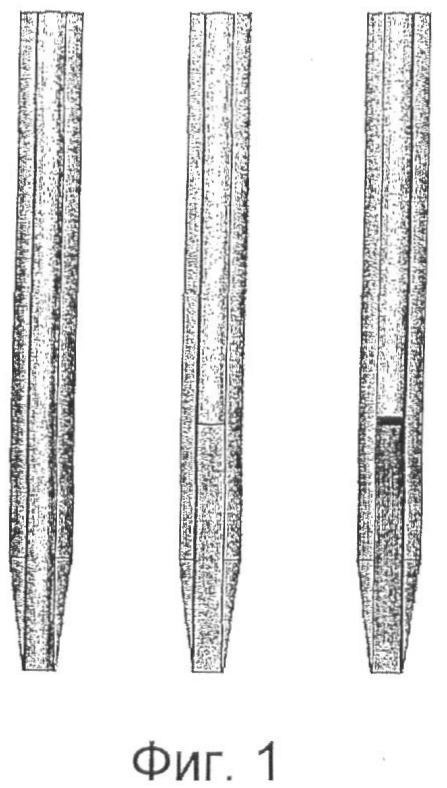
Фиг.1 отображает трубку, используемую в примере.
Фиг.2 показывает флуоресцентные изображения образцов лосося, хранящихся при 1°С и отобранных в разные дни хранения, полученные с помощью флуоресцентного анализа Live/Dead (живые/мертвые).
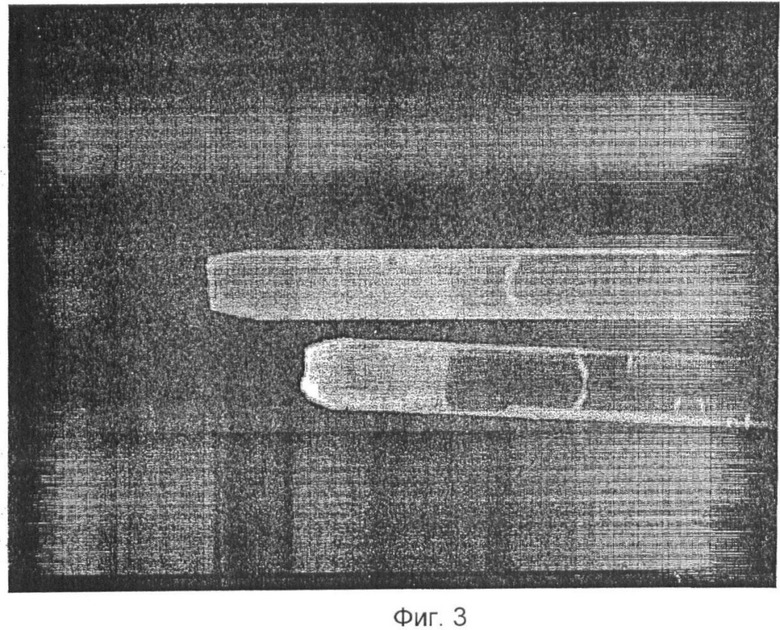
Фиг.3 показывает флуоресцентные изображения образцов лосося, хранящихся при 1°С и отобранных в дни хранения 1 и 8 с помощью флуоресцентного анализа Live/Dead.
Фиг.4 показывает корреляцию свежести образцов лосося и соотношения расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается зеленая флуоресценция, и расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается красная флуоресценция.
Фиг.5 показывает флуоресцентные изображения образца, взятого у живой радужной форели.
Фиг.6 показывает флуоресцентные изображения образца, взятого у рыбного продукта на основе радужной форели, хранящегося при 4°С в течение семи дней.
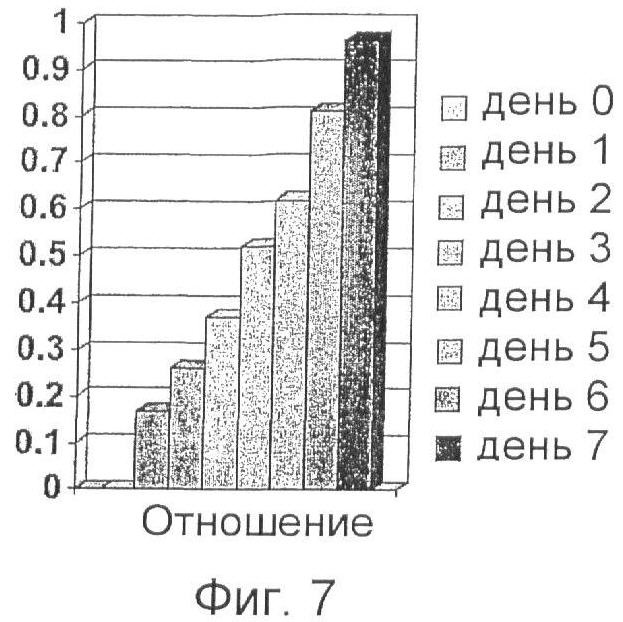
Фиг.7 иллюстрирует корреляцию между свежестью образца радужной форели и соотношением расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается зеленая флуоресценция, и расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается красная флуоресценция.
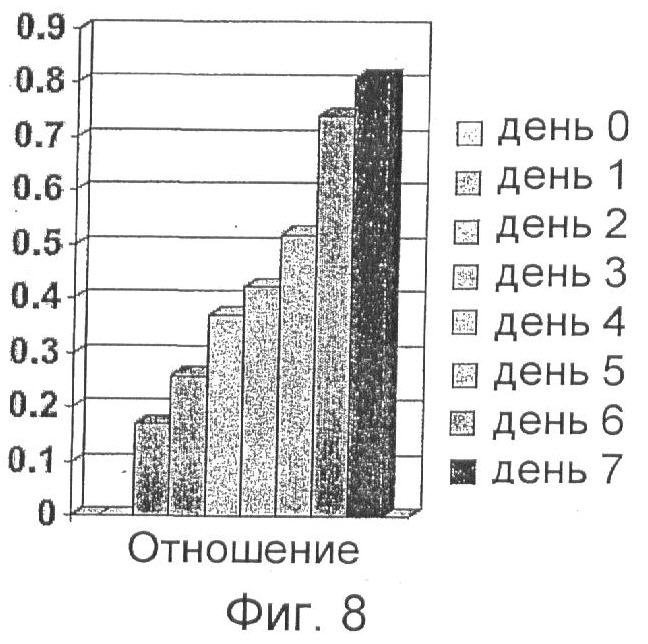
Фиг.8 отображает корреляцию между свежестью образца дуврской камбалы и соотношением расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается зеленая флуоресценция, и расстояния от верхнего конца образца до самой дальней точки образца, в которой наблюдается красная флуоресценция.
Фиг.9 показывает изображения, полученные через определенные промежутки времени на протяжении 16 минут после прибавления красителей, для образца дуврской камбалы, хранящегося при 1°С в течение пяти дней, с помощью флуоресцентного анализа Live/Dead.
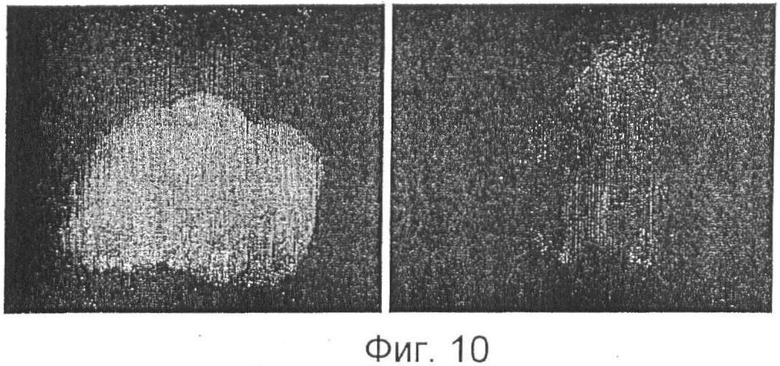
Фиг.10 показывает флуоресцентные изображения образцов лосося, хранящихся при 1°С и отобранных в дни хранения 1 и 5.
Фиг.11 иллюстрирует глубину проникновения окрашивающего красителя трипанового синего в образцы лосося, хранящиеся при 1°С и отбираемые в дни хранения 1, 4 и 7, с помощью анализа с трипановым синим.
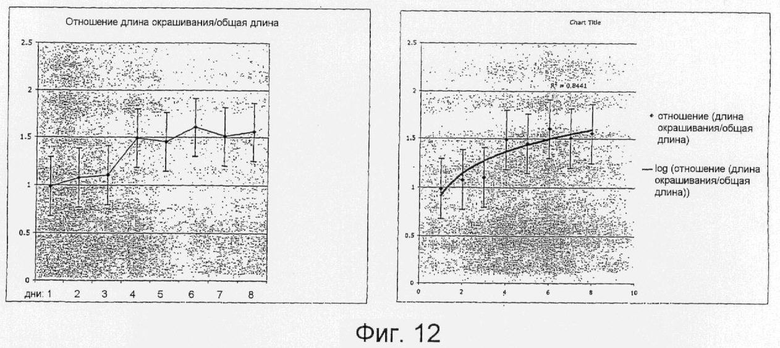
Фиг.12 иллюстрирует расстояние, на которое краситель трипановый синий проникает в образцы лосося, хранящиеся при температуре 1°С, взятые в дни хранения с 1 по 8.
Детальное описание предпочтительных в настоящее время вариантов исполнения
Экспериментальные материалы и процедуры
Филе лосося
Две упаковки замороженного филе лосося в хорошем состоянии разделяли на 8 порций. Каждая порция составляет примерно 60 грамм в замороженном состоянии. Четыре порции помещают в холодильную камеру с постоянной температурой 1°С (±0,5°С), а другие четыре порции помещают в стандартный лабораторный холодильник, поддерживающий температуру 4°С. Все эти порции хранят в повторно запечатываемом пакете для предотвращения окисления и обезвоживания в периоды между отбором проб.
Способы отбора проб
Образцы филе лосося отбирают ежедневно и наблюдают изменения. Для точных измерений важно обеспечить постоянство размеров образцов. Был изготовлен инструмент для отбора проб, предназначенный для высверливания образца из рыбы. Инструмент, используемый в экспериментах, представлял собой прозрачную трубку из материала Lexan® (поликарбонатная смола), имеющую наружный диаметр 4,8 мм, внутренний диаметр 2,1 мм и длину 90 мм. Один конец трубки был срезан на конус для образования режущей поверхности (см. Фиг.1). При введении в мякоть рыбного продукта часть мяса вдавливается в донное отверстие трубки. Затем путем осторожного поворачивания и вытягивания вынимается образец, который остается в трубке. Аппликатор с наружным диаметром 2 мм может быть использован для осторожного уплотнения образца и удаления воздушных зазоров. Трубка предпочтительно выполнена безвредной для пищевых продуктов и является оптически прозрачной. Могут быть пригодными также другие акриловые или поликарбонатные материалы. Полученный таким способом с помощью такого инструмента образец имеет размер примерно 2,1 мм ×~5-25 мм.
Такой способ отбора проб имеет несколько преимуществ, включая:
- малый, воспроизводимый размер образца;
- стандартный размер образца;
- четкая маркировка контейнера;
- недорогой, одноразовый, нетоксичный инструмент;
- небьющийся;
- образец виден через трубку.
Окрашивание, инкубирование
Небольшой объем окрашивающего раствора может быть введен в верхнее отверстие трубки для инкубирования в течение требуемого периода времени, например примерно 10 минут. Типично, объем окрашивающего раствора может изменяться от 1 мкл до 1 мл. Время инкубирования может меняться от 1 минуты до 1 часа.
Окрашивающий раствор может быть раствором, содержащим кальцеин AM и гомодимер этидия, например раствором, приготовленным из набора LIVE/DEAD для определения жизнеспособности/цитотоксичности фирмы Molecular Probes (L3224). Набор L3224 включает две пробы: кальцеин AM и гомодимер этидия-1. Кальцеин AM представляет собой флуорогенный субстрат эстеразы, который гидролизуется до продукта с зеленой флуоресценцией (кальцеин). Таким образом, зеленая флуоресценция является индикатором клеток, обладающих эстеразной активностью, а также имеющих интактную мембрану для удерживания эстеразных продуктов. Зеленая флуоресценция означает, что они являются живыми на основании некоторого уровня эстеразной активности. Гомодимер этидия-1 представляет собой высокоаффинный краситель для нуклеиновых кислот с красной флуоресценцией, который может проходить только через нарушенные мембраны мертвых клеток. Если клетки красные, это означает, что они "мертвые". Концентрация кальцеина AM может составлять от 0,1 до 50 мкМ.
Концентрация гомодимера EthD-1 составляет от 0,1 до 100 мкМ.
Использование набора для анализа на определение жизнеспособности/цитотоксичности LIVE/DEAD обеспечивает несколько преимуществ:
- Простота. Реагенты одновременно прибавляются к образцу, который затем инкубируют в течение 3-10 минут во время оттаивания или сразу же после оттаивания. Стадии промывки перед анализом не требуются.
- Специфичность и надежность. Клетки с зеленой флуоресценцией являются живыми; клетки с красной флуоресценцией являются мертвыми.
- Универсальность. Анализ на определение жизнеспособности/цитотоксичности LIVE/DEAD является применимым для прилипающих клеток, таких как астроциты, неприлипающих клеток и определенных тканей. Результаты могут быть проанализированы методом флуоресцентной микроскопии с использованием стандартных наборов флуоресцеиновых барьерных фильтров (longpass filter), а также методами поточной цитометрии или флуорометрии. Флуоресцентная эмиссия двух зондов легко разделяется и различается. Одно- или многочастотные светодиоды (LED) могут быть использованы для получения света возбуждения в интервале длин волн 360-520 нм. Другие источники освещения включают: флуоресцентные лампы, лампы с газовой смесью, переносные источники УФ-излучения, проекционные лампы и лазеры.
- Простота количественных определений. Измерения индивидуальных клеток дают только две популяции; клетки с двойной окраской встречаются редко. Ткани могут иметь смешанные популяции с "промежуточными" стадиями окрашивания.
Окрашивающий раствор может также быть раствором трипанового синего. Трипановый синий используется как краситель для колориметрического метода определения жизнеспособности клеток. Концентрация раствора трипанового синего может составлять от 0,1 до 10 мМ. В биологических экспериментах с клетками трипановый синий является самым распространенным красителем, используемым для различения жизнеспособных клеток от нежизнеспособных. Только нежизнеспособные клетки поглощают краситель, приобретают синюю окраску и могут также иметь асимметричный вид. Наоборот, живые, здоровые клетки выглядят круглыми и преломляющими, не поглощая окрашенный в синий цвет краситель. Использование этого красителя, однако, требует учета фактора времени. Жизнеспособные клетки со временем поглощают трипановый синий, что может повлиять и на результаты подсчета и определения жизнеспособности. Для предотвращения поглощения красителя жизнеспособными клетками, которые после этого выглядят как нежизнеспособные, образец, окрашенный трипановым синим, может быть разбавлен. Например, окрашенные трипановым синим образцы могут быть зафиксированы погружением в 2% глутаральдегид в 0,1 М фосфатном буфере (рН 7,4) и сохранены для дальнейших наблюдений. Для того чтобы уменьшить нежизнеспособную окраску, отбор проб предпочтительно проводят в течение 5-30 минут. Кроме того, трипановый синий имеет большее сродство к белкам сыворотки, чем к клеточным белкам. Для клеток в среде с высоким содержанием сыворотки фон может оказаться слишком темным. В этом случае клетки предпочтительно выделяют из ткани.
Визуализация и запись изображений
Могут быть получены изображения отраженной флуоресценции для документирования каких-либо изменений характера окрашивания в зависимости от времени хранения и температуры.
Для количественных определений и/или автоматизации процесса могут быть использованы формирователи изображения, имеющие функции захвата, хранения и/или анализа изображения, такие как устройства с ПЗС (CCD) или на КМОП-структурах (CMOS).
Такие устройства включают систему UVP BioDoclt с цифровой камерой; цифровую камеру Nikon CoolPix 995 с телеобъективом; фотомикроскоп Nikon Eclipse E800, оснащенный светлым полем, системой DIC (независимые от устройства цвета), фазовой и флуоресцентной оптикой; синие и зеленые излучающие светодиоды (LED) и систему детектирования на ПЗС (CCD).
В данных исследованиях образцы наблюдали с использованием 4× 0,13 объектива Plan Fluor с цифровой апертурой (n.a.). Цифровые изображения получали с помощью цветной ПЗС-камеры CoolCam с жидкостным охлаждением на трех микросхемах (three-chip) (Cool Camera Company, Decatur, GA 30033) и сохраняли на персональном компьютере Pentium IV 3,0 GHz с помощью прикладной программы Image Pro Plus version 4.5 (Media Cybernetics, Silver Springs, MD 20910). Цифровые изображения сохраняли для дальнейшей распечатки и анализа с использованием программ ImageJ или ImagePro Plus. Для воспроизведения использовались прикладные программы Adobe PhotoShop и Microsoft PowerPoint.
Цифровые изображения получали таким образом, чтобы для сравнения цвета окрашенных образцов как функции жизнеспособности или "свежести" клеток могли быть использованы количественные способы. Цвет окрашенных образцов и глубина проникновения краски в образец являются важными критериями оценки свежести образца.
Результаты
Флуоресцентный анализ Live/Dead
Окрашивающий раствор содержит 5,0 мкМ кальцеина AM и 10,0 мкМ гомодимера EthD-1. Он был приготовлен из реагентов набора для определения жизнеспособности/цитотоксичности LIVE/DEAD фирмы Molecular Probes (L3224). Примерно 10-30 мкл окрашивающего раствора помещали сверху на образцы (2,1 мм ×~2-10 мм). Свежесть образца может быть определена на основании соотношения изменений красной и зеленой флуоресцентной эмиссии после инкубации в течение примерно 5-10 минут. Флуоресцентное изображение получают путем возбуждения образца на длине волны 490±40 нм и регистрации на 525±20 нм.
Фиг.2 и 3 отображают результаты анализа образцов лосося, хранившихся в течение разного числа дней при одинаковой температуре (1°С). Изображение, представленное на Фиг.2, было получено через 5 минут после прибавления красителя. Зеленый цвет указывает на эстеразную активность (свежий образец). Красный цвет указывает на ядра клеток с нарушенными мембранами. Расстояние, которое краситель проходит от верхней части образца вглубь, зависит от числа дней хранения. Изображение, показанное на Фиг.3, было получено через 30 минут после окрашивания образцов.
В таблице ниже приведены сводные данные флуоресцентного метода определения свежести Live/Dead (5,0 мкМ кальцеина AM и 10,0 мкМ гомодимера-1 EthD-1) замороженного образца лосося, хранящегося при 1°С, при отборе проб с 24-часовыми интервалами. Фиг.4 отображает корреляцию между свежестью рыбного продукта и соотношением расстояний, пройденных зеленой и красной флуоресценцией.
Сводные данные флуоресцентнго анализа Live/Dead
Фиг.5-8 отображают результаты флуоресцентного анализа для других видов рыбы, хранившихся различное число дней при одинаковой температуре. Фиг.5 показывает результаты флуоресценции для свежего образца радужной форели (Oncorhynchus mykiss). Фиг.6 показывает результаты флуоресценции для образца радужной форели, хранящегося при 4°С в течение семи дней. На Фиг.6 верхнее изображение показывает информацию о зеленой и красной окраске образцов; среднее изображение показывает полутоновое изображение информации о зеленой окраске; нижнее изображение представляет собой полутоновое изображение информации о красной окраске. Оба изображения на Фиг.5 и 6 были получены через 30 минут после прибавления красителя к образцу радужной форели. Краситель добавляли в верхнее отверстие трубки (левая сторона изображения).
Представленный на Фиг.7 график построен на основании результатов анализа образцов радужной форели, взятых от 3 рыб (всего 12 образцов), отбираемых ежедневно из рыбы, хранившейся 7 дней при 4°С. Образцы визуализировали через 30 минут после прибавления красителя. Этот график показывает среднее отношение расстояний, пройденных зеленой и красной флуоресценцией, для образцов, взятых в один день.
Фиг.8 отображает корреляцию свежести дуврской камбалы {Microstomus pacificus) и соотношения расстояний, пройденных зеленой и красной флуоресценцией. Процедура, использованная для Фиг.8, была такой же, как и для Фиг.7, за исключением того, что вместо образцов радужной форели в соответствии с Фиг.7 была взята дуврская камбала (Microstomus pacificus).
Изображения, полученные через определенные промежутки времени, как показано на Фиг.9, демонстрируют, что поглощение красителя изменяется со временем. Используемый образец представляет собой образец дуврской камбалы (Microstomus pacificus), хранившийся в течение 5 дней при 1°С.
Фиг.10 показывает флуоресцентные изображения образцов лосося, помещенных на чашки.
Измерения с трипановым синим
Примерно 10-30 мкл окрашивающего реагента трипанового синего (0,5 мас.%/об.) прибавляют сверху на образцы (2,1 мм ×2-10 мм). Измеряют глубину проникновения красителя трипанового синего в образец. Время инкубации составляет 10 минут. Образцы хранятся при 1°С и метятся при комнатной температуре. Для наблюдения образцов используется проходящий/отраженный свет.
Фиг.11 и 12 показывают корреляцию свежести образцов лосося с расстоянием, на которое краситель трипановый синий проникает в образец. Как показано на Фиг.12, соотношение глубины проникновения красителя к общей длине образца для Дня 1 является уникальным, значения для Дня 2, и Дня 3, и с Дня 4 по День 8 являются близкими. День 1 значительно отличается от остальных и День 2, и День 3 значительно отличаются от Дней 4-8.
В таблице ниже приведены сводные данные результатов анализа с трипановым синим.
Сводные данные результатов анализа с трипановым синим
Изобретение не ограничено описанными выше вариантами исполнения, представленными только в виде примеров, но может быть модифицировано различными способами в пределах объема защиты, определяемого прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ экспресс-детекции жизнеспособных микроорганизмов в мясе и мясных продуктах | 2020 |
|
RU2755766C1 |
| БИОПОЛИМЕРНЫЙ МАТРИКС ДЛЯ ПРОЛИФЕРАЦИИ КЛЕТОК И РЕГЕНЕРАЦИИ НЕРВНЫХ ТКАНЕЙ | 2011 |
|
RU2478398C1 |
| СПОСОБЫ ДЕТЕКЦИИ АНТИЦИТОМЕГАЛОВИРУСНЫХ НЕЙТРАЛИЗУЮЩИХ АНТИТЕЛ | 2013 |
|
RU2660712C2 |
| КОМПОЗИЦИИ И СПОСОБЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ОЦЕНКИ ЦИТОТОКСИЧНОСТИ ОТДЕЛЬНЫХ КЛЕТОК | 2009 |
|
RU2532228C2 |
| СПОСОБ ОЦЕНКИ ЖИЗНЕСПОСОБНОСТИ КЛЕТОК В МИКРОБИОРЕАКТОРЕ С ПОМОЩЬЮ ОПТИЧЕСКОГО СВЕТОВОДА | 2012 |
|
RU2532839C2 |
| СПОСОБ АКТИВАЦИИ ЦИТОТОКСИЧЕСКИХ ЛИМФОЦИТОВ ЧЕЛОВЕКА | 2015 |
|
RU2603079C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ТЕРАПЕВТИЧЕСКОЙ КЛЕТОЧНОЙ КОМПОЗИЦИИ | 2018 |
|
RU2775967C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ УНИЧТОЖЕНИЯ КЛЕТОК | 2008 |
|
RU2471349C2 |
| Способ долгосрочного культивирования и экспансии NK-клеток с высокой жизнеспособностью и функциональной активностью | 2021 |
|
RU2794770C1 |
| КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ ГЛАЗ, СВЯЗАННОЙ С НУКЛЕИНОВЫМИ КИСЛОТАМИ | 2012 |
|
RU2642609C2 |





Изобретение относится к пищевой промышленности и может быть использовано для определения качества рыбопродуктов. Способ включает вырезание небольшого количества образца из рыбного продукта. Затем к образцу прибавляют окрашивающий реагент, включающий проникающий в клетку краситель и не проникающий в клетку флуоресцентный краситель. Проникающий в клетку краситель превращается в соединение, эмитирующее первую флуоресценцию в присутствии внутриклеточной эстеразной активности. Не проникающий флуоресцентный краситель может проникать в клетку через нарушенные клеточные мембраны и эмитировать вторую флуоресценцию. Первая и вторая флуоресценция отличаются друг от друга. Определяют свежесть рыбного продукта на основании, по меньшей мере, одного параметра, выбранного из группы, состоящей из интенсивности первой флуоресценции, эмитируемой инкубируемым образцом, интенсивности второй флуоресценции, эмитируемой инкубируемым образцом, первого расстояния от верхнего конца образца до самой дальней точки образца, в которой детектируется первая флуоресценция; второго расстояния от верхнего конца образца до самой дальней точки образца, в которой детектируется вторая флуоресценция. Изобретение позволяет точно и объективно оценить свежесть рыбных продуктов. 3 н. и 26 з.п. ф-лы, 2 табл., 12 ил.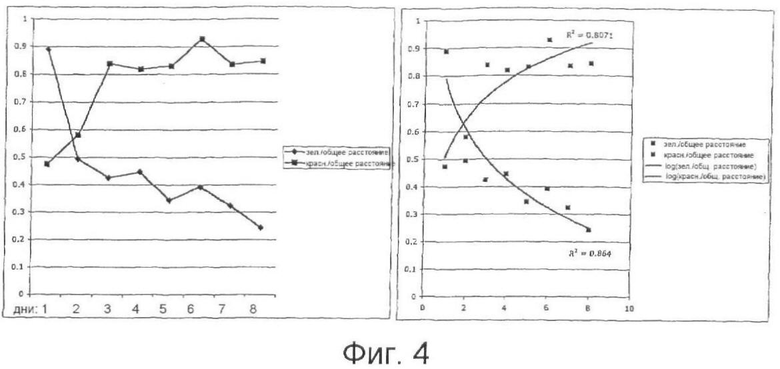
1. Способ оценки свежести рыбного продукта, включающий: вырезание небольшого количества образца из рыбного продукта; прибавление к образцу эффективного количества окрашивающего реагента, включающего по меньшей мере один из проникающего в клетку красителя и непроникающего в клетку флуоресцентного красителя, где проникающий в клетку краситель превращается в соединение, эмитирующее первую флуоресценцию в присутствии внутриклеточной эстеразной активности; непроникающий флуоресцентный краситель может проникать в клетку через нарушенные клеточные мембраны и эмитировать вторую флуоресценцию; и первая флуоресценция и вторая флуоресценция отличаются друг от друга, если индикаторный реагент включает как проникающий в клетку краситель, так и непроникающий в клетку краситель; инкубирование образца с добавленным окрашивающим реагентом в течение предварительно определенного периода времени и определение свежести рыбного продукта на основании по меньшей мере одного параметра, выбранного из группы, состоящей из интенсивности первой флуоресценции, эмитируемой инкубируемым образцом, интенсивности второй флуоресценции, эмитируемой инкубируемым образцом, первого расстояния от верхнего конца образца до самой дальней точки образца, в которой детектируется первая флуоресценция; второго расстояния от верхнего конца образца до самой дальней точки образца, в которой детектируется вторая флуоресценция.
2. Способ по п.1, в котором стадию определения проводят путем сравнения по меньшей мере одного параметра с предварительно установленной корреляционной зависимостью между свежестью и по меньшей мере одним параметром.
3. Способ по п.1, в котором интенсивности первой флуоресценции и второй флуоресценции количественно определяют с помощью цифрового устройства, и предварительно установленную корреляционную зависимость устанавливают на основании количественно определенных интенсивностей первой флуоресценции и второй флуоресценции.
4. Способ по п.3, в котором интенсивности первой флуоресценции и второй флуоресценции регистрируют в виде изображения оптическим устройством, и предварительно установленная корреляционная зависимость между свежестью и интенсивностью по меньшей мере одной из первой флуоресценции и второй флуоресценции представлена в виде стандартной цветовой шкалы.
5. Способ по п.1, в котором окрашивающий реагент включает как проникающий в клетку краситель, так и непроникающий в клетку краситель.
6. Способ по п.5, в котором определение свежести рыбного продукта осуществляется на основании соотношения интенсивностей первой флуоресценции и второй флуоресценции.
7. Способ по п.5, в котором определение свежести рыбного продукта осуществляется на основании соотношения первого расстояния и второго расстояния.
8. Способ по п.5, в котором проникающий в клетку краситель является кальцеином AM, а непроникающий в клетку краситель является гомодимером EthD-1, причем первая флуоресценция является зеленой, а вторая флуоресценция является красной.
9. Способ по п.5, в котором проникающий в клетку краситель является С12-резазурином, а непроникающий в клетку краситель является красителем Sytox® Green, причем первая флуоресценция является красной, а вторая флуоресценция является зеленой.
10. Способ по п.1, в котором проникающий в клетку краситель выбирают из группы, состоящей из кальцеина AM и С12-резазурина, а непроникающий в клетку краситель выбирают из группы, состоящей из гомодимера EthD-1, красителей YoYo-1 и Sytox® Green.
11. Способ по п.1, в котором окрашивающий реагент дополнительно включает краситель трипановый синий, если окрашивающий реагент включает проникающий в клетку краситель.
12. Способ оценки свежести рыбного продукта, включающий: вырезание небольшого количества образца из рыбного продукта; прибавление к образцу окрашивающего реагента, включающего эффективное количество кальцеина AM и эффективное количество гомодимера EthD-1; инкубирование образца с добавленным окрашивающим реагентом в течение предварительно определенного периода времени; определение свежести рыбного продукта на основании по меньшей мере одного параметра из интенсивности зеленой флуоресценции и первого расстояния от верхнего края инкубируемого образца до самой дальней точки инкубируемого образца, в которой детектируется зеленая флуоресценция, и по меньшей мере одного параметра из интенсивности красной флуоресценции и второго расстояния от верхнего края инкубируемого образца до самой дальней точки инкубируемого образца, в которой наблюдается красная флуоресценция.
13. Способ по п.12, в котором определение свежести осуществляют на основании соотношения интенсивностей зеленой флуоресценции и красной флуоресценции.
14. Способ по п.12, в котором определение свежести осуществляют на основании соотношения первого расстояния и второго расстояния.
15. Способ по п.12, в котором определение свежести проводят путем сравнения интенсивности зеленой флуоресценции и красной флуоресценции с предварительно установленной корреляционной зависимостью между свежестью и интенсивностью зеленой флуоресценции и красной флуоресценции.
16. Способ по п.15, в котором интенсивности зеленой флуоресценции и красной флуоресценции количественно определяют с помощью цифрового устройства, и предварительно установленную корреляционную зависимость определяют на основании количественно определенной интенсивности зеленой флуоресценции и красной флуоресценции.
17. Способ по п.15, в котором интенсивности зеленой флуоресценции и красной флуоресценции регистрируют в виде изображения с помощью оптического устройства, и предварительно установленная корреляционная зависимость между свежестью и интенсивностью зеленой флуоресценции и красной флуоресценции представлена в виде стандартной цветовой шкалы.
18. Способ по п.12, в котором окрашивающий реагент включает 0,1-50 мкМ кальцеина AM.
19. Способ по п.12, в котором окрашивающий реагент включает 0,1-100 мкМ гомодимера EthD-1.
20. Способ по п.12, в котором количество окрашивающего реагента составляет от примерно 1 мкл до 1 мл.
21. Способ по п.12, в котором предварительно определенная продолжительность стадии инкубирования составляет от примерно 1 до 45 мин.
22. Способ по п.12, в котором предварительно определенная продолжительность стадии инкубирования составляет от примерно 5 до 10 мин, и стадия инкубирования проводится при комнатной температуре.
23. Способ по п.12, в котором рыбный продукт выбирают из группы, состоящей из лосося, радужной форели, дуврской камбалы и палтуса.
24. Способ оценки свежести рыбного продукта, включающий: вырезание небольшого количества образца из рыбного продукта; прибавление к образцу окрашивающего реагента, включающего эффективное количество красителя трипанового синего; инкубирование образца с добавленным окрашивающим реагентом в течение предварительно определенного периода времени; определение свежести рыбного продукта на основании глубины проникания от верхнего края инкубируемого образца до самой дальней точки инкубируемого образца, в которой детектируется синяя флуоресценция.
25. Способ по п.24, в котором определение свежести проводят путем сравнения глубины проникания с предварительно установленной корреляционной зависимостью между свежестью и глубиной проникания.
26. Способ по п.24, в котором окрашивающий реагент включает 0,1-10 мМ красителя трипанового синего.
27. Способ по п.24, в котором количество окрашивающего агента составляет от 1 мкл до 1 мл.
28. Способ по п.24, в котором предварительно определенная продолжительность стадии инкубирования составляет от примерно 2 до 45 мин.
29. Способ по п.24, в котором предварительно определенная продолжительность стадии инкубирования составляет примерно 10-30 мин, и инкубирование проводится при комнатной температуре.
| WO 03048761, 12.06.2003 | |||
| US 4026666 A, 31.05.1977 | |||
| СПОСОБ КОНТРОЛЯ КАЧЕСТВА МЯСА | 1991 |
|
RU2015507C1 |
Авторы
Даты
2009-11-27—Публикация
2005-03-11—Подача