Изобретение относится к новым химическим соединениям, являющимся производными изоиндолов, а также к композициям, содержащим их, и их применению в качестве лекарственных средств.
Настоящее изобретение более предпочтительно относится к их фармацевтическому применению, в частности к их применению в качестве ингибиторов активности белка-шаперона Hsp90.
Такими производными по настоящему изобретению могут быть, в частности, производные 1-(бензимидазол-2-ил)-2,3,4,6-тетрагидро-2H-пиридо[2,1-a]изоиндола или 1-(азабензимидазол-2-ил)-2,3,4,6-тетрагидро-2H-пиридо[2,1-a]изоиндола, или 1-(бензимидазол-2-ил)-2,5-дигидро-3H-пирроло[2,1-a]изоиндола, или 1-(азабензимидазол-2-ил)-2,5-дигидро-3H-пирроло[2,1-a]изоиндола.
Более предпочтительно изобретение относится, согласно первому аспекту, к новым производным бензизоксазола.
Соединения по настоящему изобретению проявляют, в частности, противораковую активность, в особенности ингибирующую активность в отношении белка-шаперона Hsp90 и более особо активность путем ингибирования каталитической активности АТФ-азного типа белка-шаперона Hsp90.
Белки-шапероны
Молекулярные шапероны группы "Heat Schock Proteins" (HSP), классифицируемые в зависимости от их молекулярной массы (Hsp27, Hsp70, Hsp90 и т.д.), представляют собой ключевые элементы равновесия между синтезом и деградацией клеточных белков, ответственных за правильное сворачивание белков. Они играют жизненно важную роль в ответе на клеточный стресс. HSPs, в частности Hsp90, также вовлечены в регуляцию различных важных функций клетки путем их сочетания с различными белками-клиентами, вовлеченными в клеточную пролиферацию или апоптоз (Jolly C. et Morimoto R.I., J. N. Cancer Inst. (2000), 92, 1564-72; Smith D.F. et al., Pharmacological Rev. (1998), 50, 493-513; Smith D.F., Molecular Chaperones in the Cell, 165-178, Oxford University Press 2001).
Различные патологии человека являются следствием неправильного сворачивания ключевых белков, ведущего, в частности, к нейродегенеративным болезням вследствие агрегации некоторых белков, как в случае болезней Альцгеймера и Гентингтона или заболеваний, связанных с прионами (Tytell M. et Hooper P.L., Emerging Ther. Targets (2001), 5, 3788-3796). При таких патологиях могли бы быть эффективными подходы, нацеленные на прерывание или нарушение функционирования шаперонов.
Шаперон Hsp90
Шаперон Hsp90, который представляет собой от 1 до 2% белков, содержащихся в клетке, был недавно выявлен в качестве особенно многообещающей цели при противораковой терапии (см. Moloney A. et Workman P., Expert Opin. Biol. Ther. (2002), 2(1), 3-24; Choisis et al., Drug Discovery Today (2004), 9, 881-888). Такой интерес поддерживается, в частности, цитоплазматическими взаимодействиями Hsp90 с главными белками-клиентами Hsp90, белками, которые вовлечены в шесть механизмов прогрессирования опухоли, таких, как определенные Hanahan D. и Weinberg R.A. (Cell (2002), 100, 57-70), а именно:
- способность пролиферировать в отсутствие факторов роста: EGFR-R/HER2, Src, Akt, Raf, MEK, Bcr-Abl, Flt-3 и т.п.;
- способность избегать апоптоза: мутантная форма p53, Akт, cюрвивин и т.п.;
- нечувствительность к сигналам остановки пролиферации: Cdk4, Plk, Wee1 и т.п.;
- способность активизировать ангиогенез: VEGF-R, FAK, HIF-1, Akt и т.п.;
- способность пролиферировать без репликативного предела: hTert и т.п.;
- способность захватывать новые ткани и метастазировать: c-Met.
Среди других белков-клиентов Hsp90 значительный интерес в рамках противораковой терапии представляют также рецепторы стероидных гормонов, такие, как рецептор эстрогена или рецептор андрогена.
Недавно было показано, что альфа-форма Hsp90 играла также внеклеточную роль путем взаимодействия с металлопротеазой MMP-2, причастной к опухолевой инвазии (Eustace B.K. et al., Nature Cell Biology (2004), 6, 507-514).
Hsp90 состоит из двух N- и С-концевых доменов, разделенных областью с сильным зарядом. Динамическое взаимодействие между двумя такими доменами, координируемое фиксацией нуклеотидов и кошаперонов, определяет конфигурацию шаперона и состояние его активности. Ассоциация белков-клиентов зависит принципиально от природы кошаперонов Hsp70/Hsp40, Hop60 и т.п. и природы нуклеотида АДФ или АТФ, связанного с N-концевым доменом Hsp90. Таким образом, гидролиз АТФ до АДФ и фактор обмена АДФ/АТФ управляют совокупностью "механики" шаперона, и было показано, что достаточно предупреждать гидролиз АТФ до АДФ - АТФ-азную активность Hsp90 - для высвобождения в цитоплазму белков-клиентов, которые будут при этом разлагаться протеасомой (Neckers L. et Neckers K., Expert Opin. Emerging Drugs (2002), 7, 277-288; Neckers L., Current Medicinal Chemistry, (2003), 10, 733-739; Piper P.W., Current Opin. Invest. New Drugs (2001), 2, 1606-1610).
Ингибиторы Hsp90
Первыми известными ингибиторами Hsp90 являются соединения группы амсамицинов, в частности гелданамицин (1) и гербимицин A. Рентгенографическими исследованиями было доказано, что гелданамицин связывается с сайтом АТФ N-концевого домена Hsp90, где он ингибирует АТФ-азную активность шаперона (Prodromou C. et al., Cell (1997), 90, 65-75).
В настоящее время компании NIH и Kosan BioSciences заявляют о клинической проработке 17AAG (2), который представляет собой ингибитор Hsp90, производный гелданамицина (1), который блокирует АТФ-азную активность Hsp90, связываясь с сайтом распознавания N-концевого домена АТФ. Результаты клинических испытаний фазы I 17AAG (1) в настоящее время дают начало испытаний фазы II, но также направляют исследования к более растворимым производным, таким, как аналог 3 (17DMAG по номенклатуре Kosan BioSciences), носитель цепочки, содержащей диметиламиновую группу вместо метоксигруппы, и к оптимизированным композициям 17AAG (CNF1010 по номенклатуре Conforma Therapeutics):
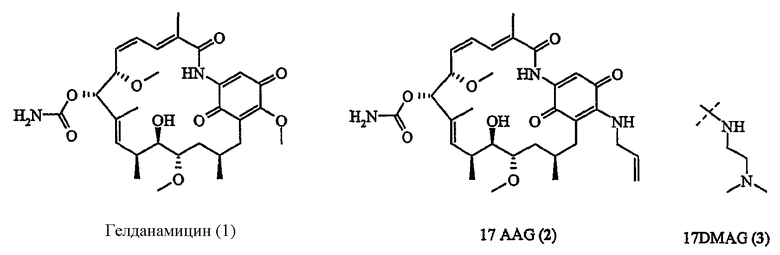
Радицикол (4) представляет собой также ингибитор Hsp90 натурального происхождения (Roe S.M. et al., J. Med Chem. (1999), 42, 260-66). Однако, если упомянутое соединение является в первом приближении лучшим ингибитором in vitro Hsp90, его метаболическая нестабильность относительно нуклеофильной серы делает его применение in vivo затрудненным. Производные оксимы, являющиеся более устойчивыми, такие, как KF 55823 (5) или KF 25706, были разработаны компанией Kyowa Hakko Kogyo (Soga et al., Cancer Research (1999), 59, 2931-2938).
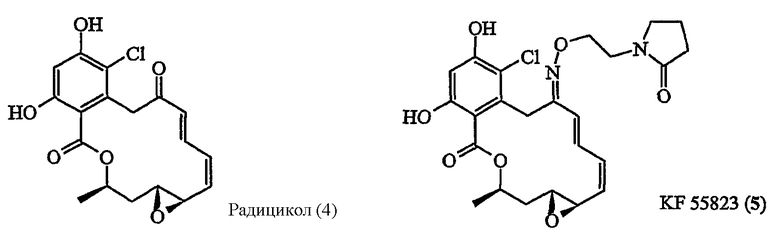
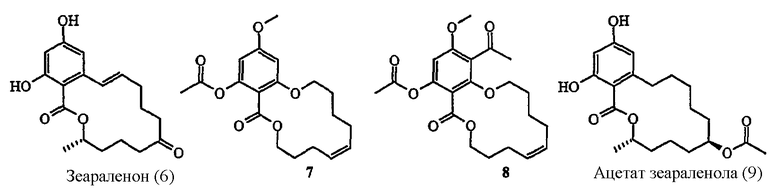
Структуры натурального происхождения, сходные с радициколом, были также недавно описаны, например, зеараленон (6), описанный компанией Conforma Therapeutics (WO 03041643), или соединения (7-9).
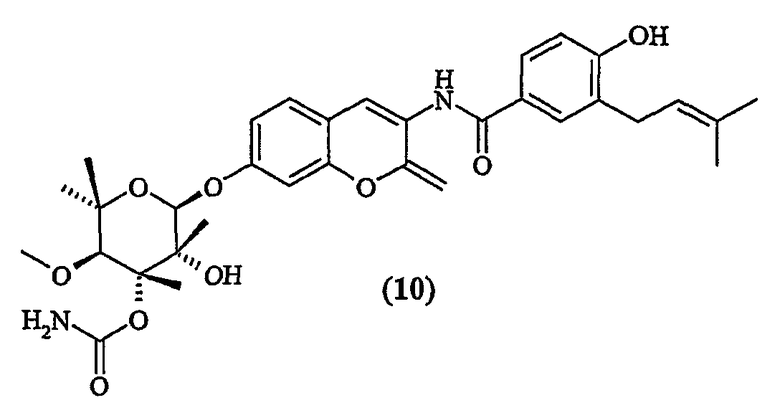
Ингибитор Hsp90 натурального происхождения, новобиоцин, (10) связывается с сайтом АТФ, расположенным в различных точках в C-концевом домене белка (Itoh H. et al., Biochem J. (1999), 343, 697-703).
Депсипептид под названием рипаламицин или ICI101 был недавно описан как неконкурентный ингибитор сайта АТФ Hsp90 (J. Pharmacol. Exp. Ther. (2004), 310, 1288-1295).
Пурины, такие, как соединения PU3 (11) (Chiosis et al., Chem. Biol. (2001), 8, 289-299) и PU24FCl (12) (Chiosis et al., Curr. Canc. Drug Targets (2003), 3, 371-376) были также описаны как ингибиторы Hsp90:
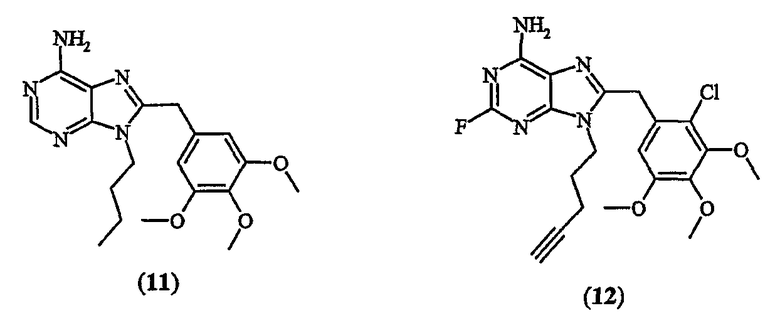
В заявке WO2004/072080 (Cellular Genomics) заявлена группа 8-гетероарил-6-фенил-имидазо[1,2-a]пиразинов в качестве модуляторов активности Hsp90.
В заявке WO2004/050087 (Ribotarget/Vernalis) заявлена группа пиразолов, дающих полезный эффект при лечении патологий, связанных с ингибированием "белков теплового шока", таких, как шаперон Hsp90.
В заявке WO2004/056782 (Vernalis) заявлена новая группа пиразолов, дающих полезный эффект при лечении патологий, связанных с ингибированием "белков теплового шока", таких, как шаперон Hsp90.
В заявке WO2004/07051 (Vernalis) заявлены производные арилизоксазолов, дающие полезный эффект при лечении патологий, связанных с ингибированием "белков теплового шока", таких, как шаперон Hsp90.
В заявке WO2004/096212 (Vernalis) заявлена третья группа пиразолов, дающих полезный эффект при лечении патологий, связанных с ингибированием "белков теплового шока", таких, как шаперон Hsp90.
В заявке WO2005/00300 (Vernalis) более общим образом заявлены 5-членные гетероциклы, содержащие в качестве заместителей арильные радикалы и дающие полезный эффект при лечении патологий, связанных с ингибированием "белков теплового шока", таких, как шаперон Hsp90.
Наконец, в заявке WO2005/00778 (Kyowa Hakko Kogyo) заявлена группа производных бензофенона в качестве ингибиторов Hsp90, дающих полезный эффект при лечении опухолей.
Таким образом, настоящее изобретение относится к продуктам формулы (I):
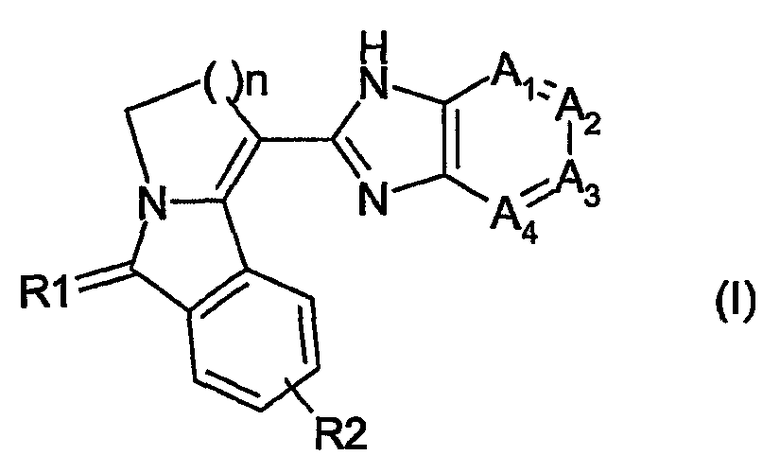
где:
A1, A2, A3 и A4, являющиеся одинаковыми или различными, представляют собой CRa или N;
n равно 1 или 2;
R1 представляет собой атом кислорода или серы, или радикал NRb;
R2 независимо выбран из группы, которую составляют H, галоген, CF3, нитро, циано, метил, этил, гидрокси, меркапто, амино, метокси, тиометокси, метиламино, диметиламино, ацетиламино, карбокси и карбоксамидо;
Ra выбран из группы, которую составляют H, галоген, CF3, гидрокси, меркапто, нитро, амино, OR3, SR3, NR3R4, NH-OH, NH-CO-H, NH-CO-OH, NH-CO-NH2, карбокси, циано, карбоксамидо, Y-(CH2)p-алкил, Y-(CH2)p-циклоалкил, Y-(CH2)p-гетероциклоалкил, Y-(CH2)p-арил или Y-(CH2)p-гетероарил, где Y=O, S, NH, O-C(O), C(O)-NH, NH-C(O), NH-S(O) или NH-S(O)2, где p=1, 2 или 3, и где арил содержит от 6 до 10 звеньев, циклоалкил содержит от 3 до 10 звеньев и гетероарил или гетероциклоалкил, в котором от 1 до 3 гетероатомов выбраны из O, N или S, содержит от 4 до 10 звеньев; причем все эти радикалы при необходимости могут быть замещенными;
R3 и R4 независимо выбраны из атома водорода или алкилов, алкенилов, алкинилов, арилов или гетероарилов, аралкилов или гетероаралкилов; причем все упомянутые алкилы, алкенилы, алкинилы, арилы, гетероарилы, аралкилы или гетероаралкилы при необходимости могут быть замещенными;
Rb выбран из группы, которую составляют H, (CH2)m-циклоалкил, (CH2)m-гетероциклоалкил, (CH2)m-арил или (CH2)m-гетероарил, где m=0, 1, 2, причем все эти радикалы при необходимости могут быть замещенными;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Относительно продуктов формулы (I) здесь и далее приведенные термины имеют следующие значения.
- Термин галоген означает атомы фтора, хлора, брома или иода и предпочтительно атомы хлора или брома.
- Термин алкил означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода, выбранный из метила, этила, пропила, изопропила, бутила, изобутила, втор-бутила, трет-бутила, пентила, изопентила, втор-пентила, трет-пентила, нео-пентила, гексила, изогексила, втор-гексила, трет-гексила и в равной мере из гептила, октила, нонила, децила, ундецила и додецила, а также их линейных или разветвленных изомеров. В качестве более предпочтительных можно упомянуть алкильные радикалы, содержащие не более 6 атомов углерода, и, в частности, метил, этил, пропил, изопропил, н-бутил, изобутил, трет-бутил, линейный или разветвленный пентил, линейный или разветвленный гексил.
- Термин алкенил означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода, предпочтительно 4 атома углерода, выбранный, например, из радикалов, имеющих следующие значения: этенил или винил, пропенил или аллил, 1-пропенил, н-бутенил, изобутенил, 3-метилбут-2-енил, н-пентенил, гексенил, гептенил, октенил, циклогексилбутенил и деценил, а также их линейные или разветвленные изомеры. Из алкенилов в качестве более предпочтительных можно упомянуть аллил или бутенил.
- Термин алкинил означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода, предпочтительно 4 атома углерода, выбранный, например, из радикалов, имеющих следующие значения: этинил, пропинил или пропаргил, бутинил, н-бутинил, изобутинил, 3-метилбут-2-инил, пентинил или гексинил, а также их линейные или разветвленные изомеры. Среди алкинилов в качестве более предпочтительного можно упомянуть пропаргил.
- Термин алкокси, который может представлять собой, например, OR3, означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода и предпочтительно 6 атомов углерода, выбранный, например, из радикалов метокси, этокси, пропокси, изопропокси, линейного, вторичного или третичного бутокси, пентокси, гексокси и гептокси, а также их линейных или разветвленных изомеров.
- Термин алкилтио или алкил-S-, который может представлять собой, например, SR3, означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода и представляющий собой, в частности, радикалы метилтио, этилтио, изопропилтио и гептилтио. В радикалах, содержащих атом серы, последняя может быть окислена до SO или SO2.
- Термин ацил или R-CO- означает линейный или разветвленный радикал, содержащий не более 12 атомов углерода, в котором радикал R представляет собой атом водорода, алкил, циклоалкил, циклоалкенил, циклоалкил, гетероциклоалкил или арил, причем данные радикалы имеют приведенные ранее значения и при необходимости могут быть замещенными соответственно указанному ранее: для примера можно упомянуть такие радикалы, как формил, ацетил, пропионил, бутирил или бензоил, или также валерил, гексаноил, акрилоил, кротоноил, карбамоил.
- Термин циклоалкил означает карбоциклический моноциклический или бициклический радикал, содержащий от 3 до 10 звеньев, и означает, в частности, циклопропил, циклобутил, циклопентил и циклогексил.
- Термин циклоалкилалкил означает радикал, в котором циклоалкил и алкил имеют значения, выбранные из приведенных ранее: данный радикал означает также, например, циклопропилметил, циклопентилметил, циклогексилметил и циклогептилметил.
- Под радикалом ацилокси понимают радикалы ацил-O-, в которых ацил имеет значения, приведенные ранее: для примера можно упомянуть радикалы ацетокси и пропионилокси.
- Под ациламиногруппой понимают радикалы ацил-N-, в которых ацил имеет значения, приведенные ранее.
- Термин арил означает ненасыщенные моноциклические или состоящие из конденсированных циклов карбоциклические радикалы. В качестве примера такого арильного радикала можно упомянуть фенил или нафтил; в качестве более предпочтительного радикала можно упомянуть фенил.
- Под арилалкилом понимают радикалы, являющиеся результатом комбинации упомянутых ранее замещенных при необходимости алкилов и также упомянутых ранее замещенных при необходимости арилов; для примера можно упомянуть бензил, фенилэтил, 2-фенетил, трифенилметил или нафтиленметил.
- Термин гетероцикл означает карбоциклический насыщенный (гетероциклоалкил) или ненасыщенный (гетероарил) радикал, содержащий не более 6 звеньев, перемежаемых одним или несколькими одинаковыми или различными гетероатомами, выбранными из атомов кислорода, азота или серы.
В качестве гетероциклоалкилов можно упомянуть, в частности, диоксолан, диоксан, дитиолан, тиооксолан, тиооксан, оксиранил, оксоланил, диоксоланил, пиперазинил, пиперидинил, пирролидинил, имидазолидинил, пиразолидинил, морфолинил или также тетрагидрофурил, тетрагидротиенил, хроманил, дигидробензофуранил, индолинил, пиперидинил, пергидропиранил, пириндолинил, тетрагидрохинолил, тетрагидроизохинолил или тиоазолидинил, причем все упомянутые радикалы при необходимости могут быть замещенными.
Среди гетероциклоалкилов можно упомянуть, в частности, замещенный при необходимости пиперазинил, замещенный при необходимости пиперидинил, замещенный при необходимости пирролидинил, имидазолидинил, пиразолидинил, морфолинил или тиоазолидинил.
- Под гетероциклоалкилалкилом понимают радикалы, в которых гетероциклоалкильный и алкильный остатки имеют приведенные ранее значения.
Среди гетероарилов с 5 звеньями можно упомянуть фурил, такой, как 2-фурил, тиенил, такой, как 2-тиенил и 3-тиенил, пирролил, диазолил, тиазолил, тиадиазолил, тиатриазолил, изотиазолил, оксазолил, оксадиазолил, 3- или 4-изоксазолил, имидазолил, пиразолил, изоксазолил.
Среди гетероарилов с 6 звеньями можно упомянуть, в частности, пиридил, такой, как 2-пиридил, 3-пиридил и 4-пиридил, пиримидил, пиримидинил, пиридазинил, пиразинил и тетразолил.
В качестве гетероарильных конденсированных радикалов, содержащих по меньшей мере один гетероатом, выбранный из серы, азота и кислорода, можно упомянуть, например, бензотиенил, такой, как 3-бензотиенил, бензофурил, бензофуранил, бензопирролил, бензимидазолил, бензоксазолил, тионафтил, индолил, пуринил, хинолил, изохинолил и нафтиридинил.
Среди гетероарильных конденсированных радикалов можно упомянуть в качестве более предпочтительных бензотиенил, бензофуранил, индолил или хинолил, бензимидазолил, бензотиазолил, фурил, имидазолил, индолизинил, изоксазолил, изохинолил, изотиазолил, оксадиазолил, пиразинил, пиридазинил, пиразолил, пиридил, пиримидинил, пирролил, хиназолил, 1,3,4-тиадиазолил, тиазолил, тиенил и триазолильные группы, причем все упомянутые радикалы при необходимости могут быть замещенными аналогично гетероарильным радикалам.
- Термин циклический амин, который может представлять собой, например, NR3R4, означает циклоалкил, содержащий от 3 до 8 звеньев, в котором один атом углерода замещен атомом азота, причем циклоалкил имеет приведенные ранее значения и может содержать также один или несколько других гетероатомов, выбранных из O, S, SO2, N или NR9, где R3 такой же, как определенный ранее, в качестве примеров таких циклических аминов можно упомянуть, например, пирролидинил, пиперидинил, морфолинил, пиперазинил, индолинил, пириндолинил или тетрагидрохинолил.
Термин "пациент" означает человека, а также других млекопитающих.
Термин "пролекарство" означает соединение, которое может быть трансформировано in vivo по метаболическому механизму (такому, как гидролиз) в соединение формулы (I). Например, эфир продукты формулы (I), содержащий гидроксильную группу, может быть превращен гидролизом in vivo в начальное соединение. Или также сложный эфир продукты формулы (I), содержащий карбоксигруппу, может быть превращен гидролизом in vivo в начальное соединение.
В качестве примеров сложных эфиров продуктов формулы (I), содержащих гидроксильную группу, можно упомянуть ацетаты, цитраты, лактаты, тартраты, малонаты, оксалаты, салицилаты, пропионаты, сукцинаты, фумараты, малеаты, метилен-бис-b-гидроксинафтоаты, гентизаты, изотионаты, ди-п-толилтартраты, метансульфонаты, этансульфонаты, бензолсульфонаты, п-толуолсульфонаты, циклогексилсульфаматы и хинаты.
Сложные эфиры продуктов формулы (I), в частности обладающих полезным действием, содержащих гидроксильную группу, могут быть получены, исходя из кислотных остатков, таких, как описанные Bundgaard et al., J. Med. Chem., 1989, 32, стр. 2503-2507; упомянутые сложные эфиры представляют собой, в частности, замещенные аминометилбензоаты, диалкиламинометилбензоаты, в которых обе алкильные группы могут быть связаны вместе или могут соединяться через атом кислорода или через атом азота, замещенный при необходимости, например, алкилированный атом азота, или также (морфолинометил)бензоаты, например, 3- или 4-(морфолинометил)бензоаты, и (4-алкилпиперазин-1-ил)бензоаты, например, 3- или 4-(4-алкилпиперазин-1-ил)бензоаты.
Одна или несколько карбоксильных групп продуктов формулы (I) могут быть переведены в солевую форму или этерифицированы различными группами, известными специалисту в данной области техники, среди которых в качестве не ограничительного примера можно упомянуть следующие соединения:
- соединения, применяемые для перевода в солевую форму: минеральные основания, такие, как, например, основания натрия, калия, лития, кальция, магния или аммония, или органические основания, такие, как, например, метиламин, пропиламин, триметиламин, диэтиламин, триэтиламин, N,N-диметилэтаноламин, трис(гидроксиметил)аминометан, этаноламин, пиридин, пиколин, дициклогексиламин, морфолин, бензиламин, прокаин, лизин, аргинин, гистидин, N-метилглюкамин;
- соединения, применяемые для этерификации: алкильные радикалы для образования алкоксикарбонильных групп, таких, как, например, метоксикарбонил, этоксикарбонил, трет-бутоксикарбонил или бензилоксикарбонил, упомянутые алкильные радикалы могут содержать в качестве заместителей радикалы, выбранные, например, из атомов галогенов, гидроксила, алкокси, ацила, ацилокси, алкилтио, амино или арила, как, например, хлорметил, гидроксипропил, метоксиметил, пропионилоксиметил, метилтиометил, диметиламиноэтил, бензил или фенетил.
Под этерифицированной карбоксигруппой понимают, например, радикалы, такие, как алкилоксикарбонил, например, метоксикарбонил, этоксикарбонил, пропоксикарбонил, бутил- или трет-бутилоксикарбонил, циклобутилоксикарбонил, циклопентилоксикарбонил или циклогексилоксикарбонил.
Также можно упомянуть радикалы, образуемые остатками легко расщепляемых сложных эфиров, такие, как метоксиметил, этоксиметил; ацилоксиалкилы, такие, как пивалоилоксиметил, пивалоилоксиэтил, ацетоксиметил или ацетоксиэтил; алкилоксикарбонилоксиалкилы, такие, как метоксикарбонилоксиметил или -этил, изопропилоксикарбонилоксиметил или -этил.
Перечень таких радикалов сложных эфиров можно найти, например, в европейском патенте EP 0034536.
Под карбоксамидной группой понимают, например, радикалы типа -CONR3R4, в которых R3 и R4 имеют значения, приведенные ранее.
Под алкиламиногруппой понимают радикалы, в которых алкил выбран из упомянутых ранее алкилов. Предпочтительными являются алкилы, содержащие не более 4 атомов углерода, для примера можно упомянуть метиламино-, этиламино-, пропиламино- или линейную или разветвленную бутиламиногруппу.
Под диалкиламиногруппой понимают радикалы, в которых алкилы, являющиеся одинаковыми или различными, выбраны из алкилов, упомянутых ранее. Как и в предыдущем случае, предпочтительными являются алкилы, содержащие не более 4 атомов углерода, для примера можно упомянуть диметиламино-, диэтиламино-, линейную или разветвленную метилэтиламиногруппу.
Радикалы NR3R4 могут также представлять собой гетероцикл, который содержит или не содержит дополнительный гетероатом. Можно упомянуть пирролил, имидазолил, индолил, пиперидинил, морфолинил и пиперазинил. Предпочтительными являются пиперидинил, морфолинил и пиперазинил.
Под карбоксигруппой в солевой форме понимают соли, образованные, например, с основаниями натрия, калия, лития, кальция, магния или аммония.
Можно также упомянуть соли, образованные с органическими основаниями, такими, как метиламин, пропиламин, триметиламин, диэтиламин, триэтиламин. Предпочтительными являются соли натрия.
Если продукты формулы (I) содержат аминогруппу, которая может образовывать с кислотой соль, то такие кислотные соли, разумеется, в равной мере составляют часть настоящего изобретения. Можно упомянуть соли, полученные, например, с соляной или метансульфоновой кислотой.
Аддитивными солями продуктов формулы (I) с минеральными или органическими кислотами могут быть, например, соли, образованные с соляной, бромоводородной, иодоводородной, азотной, серной, фосфорной, пропионовой, уксусной, трифторуксусной, муравьиной, бензойной, малеиновой, фумаровой, янтарной, винной, лимонной, щавелевой, глиоксиловой, аспарагиновой, аскорбиновой кислотами, алкилмоносульфоновыми кислотами, такими, как, например, метансульфоновая кислота, этансульфоновая кислота, пропансульфоновая кислота, алкилдисульфоновыми кислотами, такими, как, например, метандисульфоновая кислота, альфа, бета-этандисульфоновая кислота, арилмоносульфоновыми кислотами, такими, как бензолсульфоновая кислота, и арилдисульфоновыми кислотами.
Можно напомнить, что стереоизомерия может быть определена в широком смысле как изомерия соединений, имеющих совпадающую формулу, но разные группы которых расположены по-разному в пространстве, как, в частности, в монозамещенных циклогексанах, заместитель в которых может быть в аксиальном или экваториальном положении и в которых возможны различные вращательные конформации, как у производных этана. Однако, существует другой тип стереоизомерии, обусловленный различными пространственными положениями фиксированных заместителей как относительно двойной связи, так и относительно циклов, которую часто называют геометрической изомерией или цис-транс-изомерией. Термин стереоизомер употребляется в настоящей заявке в самом широком смысле и относится, таким образом, к совокупности соединений, упомянутых ранее.
В соединениях формулы (I), таких же, как определено ранее и далее, алкилы, алкенилы, алкинилы, циклоалкилы, гетероциклоалкилы, арилы, гетероарилы, аралкилы или гетероаралкилы могут при необходимости содержать в качестве заместителей один или несколько радикалов, являющихся одинаковыми или различными, выбранных из атомов галогенов; гидроксила; циклоалкила, содержащего более 6 звеньев; ацила, содержащего более 7 атомов углерода; циано; нитро; свободной, переведенной в солевую форму или этерифицированной карбоксигруппы; тетразолила; -NH2, -NH(алкила), -N(алкил)(алкила); SO2-NH-CO-NH-алкила; SO2-NH-CO-NH-фенила; -C(O)-NH2; -C(O)-NH(алкила); -C(O)-N(алкил)(алкила), -NH-C(O)-(алкила), -N(алкил)-C(O)-(алкила); тиенила; фенила, алкила, алкилтио-, алкокси- и феноксигрупп, содержащих в качестве заместителей один или несколько радикалов, являющихся одинаковыми или различными, выбранных из атомов галогенов, гидроксила, алкокси, алкила, -NH2, -NH(алкила) и -N(алкил)(алкила).
Более предпочтительно в соединениях формулы (I), таких же, как определено ранее и далее, алкилы, алкенилы, алкинилы, циклоалкилы, гетероциклоалкилы, арилы, гетероарилы, аралкилы или гетероаралкилы могут при необходимости содержать в качестве заместителей один или несколько радикалов, являющихся одинаковыми или различными, выбранных из атомов галогенов; гидроксила; свободной, переведенной в солевую форму или этерифицированной карбоксигруппы; -NH2, -NH(алкила), -N(алкил)(алкила); фенила, алкила и алкоксигруппы, содержащих в качестве заместителей один или несколько радикалов, являющихся одинаковыми или различными, выбранных из атомов галогенов, гидроксила, алкокси, алкила, -NH2, -NH(алкила) и -N(алкил)(алкила).
Еще более предпочтительно, в соединениях формулы (I), таких же, как определено ранее и далее, алкилы, алкенилы, алкинилы, циклоалкилы, гетероциклоалкилы, арилы, гетероарилы, аралкилы или гетероаралкилы могут при необходимости содержать в качестве заместителей один или несколько радикалов, являющихся одинаковыми или различными, выбранных из атомов галогенов, гидроксила и алкокси.
Настоящее изобретение относится также, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой:
A1, A2, A3 и A4, являющиеся одинаковыми или различными, являются такими, что A1 и A4, являющиеся одинаковыми или различными, представляют собой CRa, а A2 и A3 представляют собой N или CRa;
причем заместители n, Ra, R1 и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится также, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой:
A1, A2, A3 и A4, являющиеся одинаковыми или различными, являются такими, что A1 и A4, являющиеся одинаковыми или различными, представляют собой CRa, а A2 и A3 представляют собой N или CRa, где Ra представляет собой H или OH;
причем заместители n, R1 и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится также, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой:
A1, A2, A3 и A4 являются такими, что A1 и A4 представляют собой CH, а A2 и A3, являющиеся одинаковыми или различными, представляют собой N, CH или COH;
причем заместители n, R1 и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится также, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой:
R1 представляет собой атом кислорода или радикал NRb, где Rb представляет собой H или (CH2)m-гетероарил, где m=0, 1, 2;
причем A1, A2, A3, A4, n и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
В том случае, когда Rb представляет собой (CH2)m-гетероарил, настоящее изобретение относится, в частности, к значениям Rb, в котором m равно 1, а гетероарил представляет собой пиридил, замещенный при необходимости аминогруппой NR3R4, где R3 и R4 такие же, как определено ранее, причем другие заместители A1, A2, A3, A4, n и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится также, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой n равно 2;
причем A1, A2, A3, A4, R1 и R2 имеют значения, приведенные ранее;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится, в частности, к таким же, как определено ранее, соединениям формулы (I), в которой:
A1, A2 и A4 представляют собой CH, а A3 представляют собой N, CH или COH;
n равно 2;
R1 представляет собой атом кислорода;
R2 представляет собой H;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится наиболее предпочтительно к таким же, как определено ранее, следующим соединениям формулы (I):
- 1-{3-H-имидазо[4,5-c]пиридин-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он;
- 1-{1-H-6-гидроксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он;
причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Настоящее изобретение относится также к способам получения продуктов формулы (I) по настоящему изобретению.
Синтез ядра 2,3,4,6-тетрагидро-2H-пиридо[2,1-a]изоиндола мало описан в литературе.
Известны некоторые производные, замещенные в позиции 1 данного ядра, такие, как представленные далее:
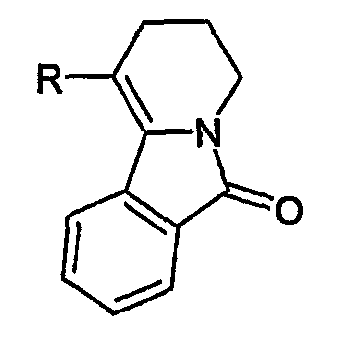
где R=H, CN, CO2Et, PO3Et2, Ph, Ph(замещенный), N(Me)Ph, SPh, Salk.
Gourves J.P. et al. (Eur. J. Org. Chem. 1999, 3489) описывают синтез, в котором используется межмолекулярная циклизация по реакции Хорнера-Вадсворта-Эммонса в качестве ключевой стадии:
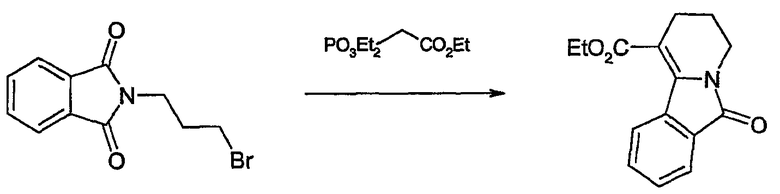
В патенте JP 49102699 описано получение 1-фенилтио- и 1-трет-бутилтио-6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола достаточно подобным образом, но с использованием стадии циклизации, индуцируемой фотохимическим облучением N-(4-фенил- или 4-трет-бутилтиобутил)фталимидов:

Deok-Chan et al. (Tetrahedron Lett. 1996, 37, 2577-80) описывают синтез ядра 6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола восстановительной циклизацией N-(4-иодбутилтиобутил)фталимида, индуцируемой иодидом самария:
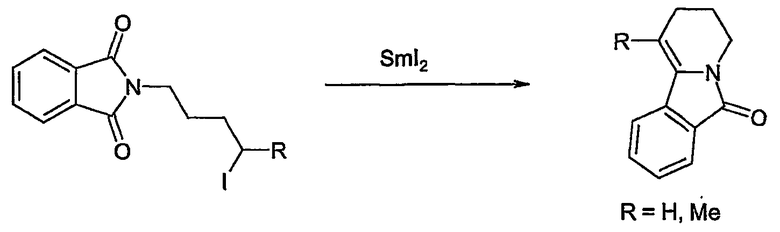
Earl R.A. и Volhardt P.C. (Heterocycles, 1982, 19, 265-71) описывают синтез ядра 6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола по ретро-реакции "ен-имино" Дильса-Aльдера:
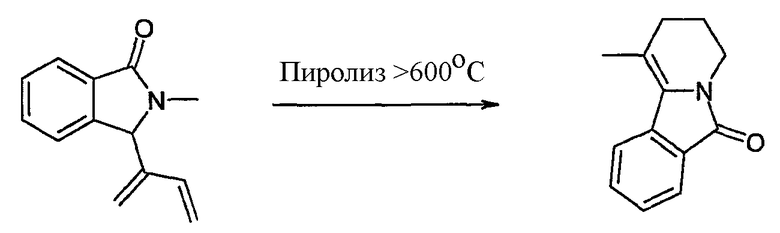
Mazzochi et al. (Tetrahedron Lett. 1983, 24, 143-46) описывают синтез ядра 6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола по межмолекулярной реакции Патерно-Бюхи:
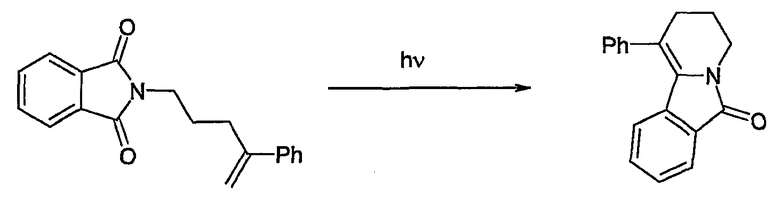
Наконец, Malacria M. et al. (Organic Lett. 2003, 5, 5095-97) описывают синтез ядра 6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола по реакции тандемной радикальной циклизации:
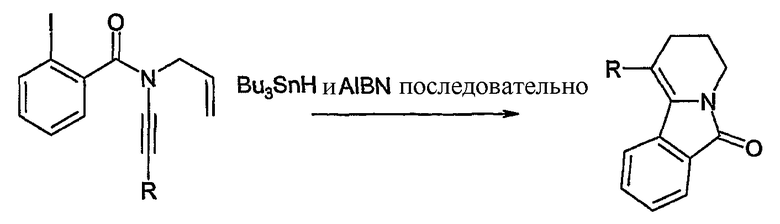
Скелет 2,3,4,6-тетрагидро-2H-пиридо[2,1-a]изоиндола также иногда обнаруживается в более сложных тетрациклических структурах, таких, как производные мероцианина, описанные в патенте IT671447, производные гемипорфиразина, описанные в патенте SU 178001, или в красителях, применяемых в качестве сополимеров при получении синтетических текстильных волокон, таких, как описанные в патентах DE 2128326, BE662237, US3221041 или NL 6504566.
Синтез ядра 2,5-дигидро-3H-пирроло[2,1-a]изоиндола мало описан в литературе.
Известны некоторые производные, замещенные в позиции 1 данного ядра, такие, как представленные далее:
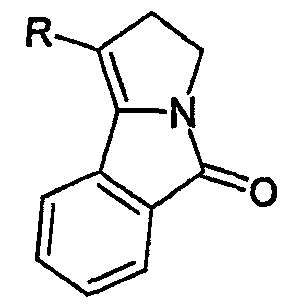
где R=H, CN, CO2Et, CO2Me, Ph, StBu.
Petter R.C. et al. (J. Org. Chem. 1990, 55, 3088-3097) описывают синтез, в котором используется межмолекулярная циклизация по реакции Хорнера-Вадсворта-Эммонса в качестве ключевой стадии:
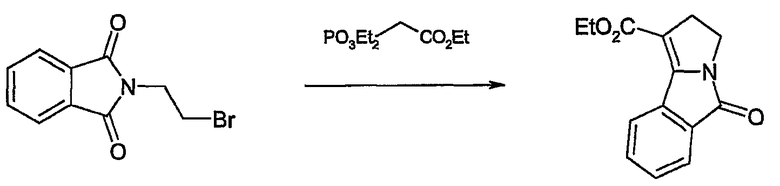
Muchovski et al. (Tetrahedron Lett. 1980, 21, 4585-88) описывают синтез раскрытия соли трифенилфосфония сложного циклопропанового эфира фталимидом:
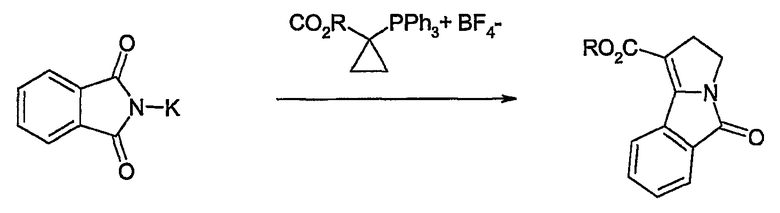
Deok-Chan et al. (Tetrahedron Lett. 1996, 37, 2577-80) описывают синтез восстановительной циклизацией N-(4-иодбутилтиобутил)фталимида, индуцируемой иодидом самария:
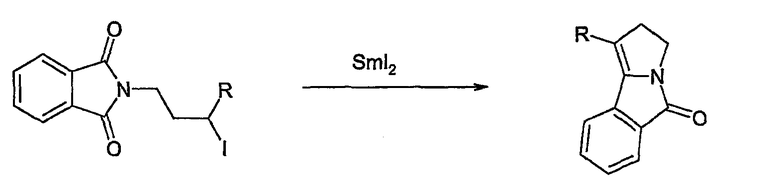 R=H, Me
R=H, Me
Yoon et al. (J. Amer. Chem. Soc. 1995, 117, 2698-2710) описывают синтез путем циклоприсоединения азометинилида с акрилатом с последующей дегидратацией аддукта в кислой среде:
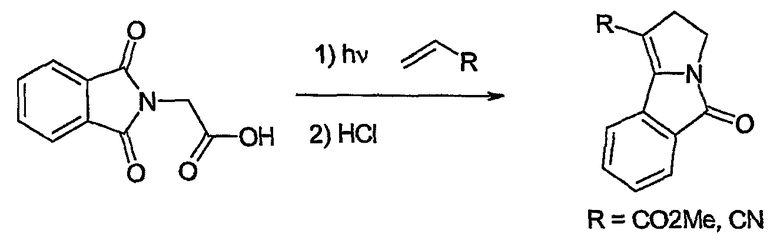
Sato et al. (Liebigs Ann. Chem. 1985, 1099-1108) описывают синтез с использованием стадии циклизации, индуцируемой фотохимическим облучением N-(4-фенил- или 4-трет-бутилтиобутил)фталимидов:
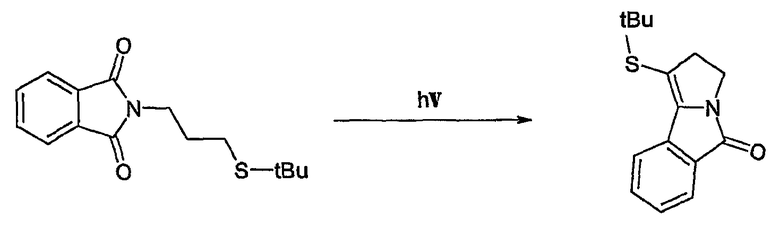
Более того, скелет 2,5-дигидро-3H-пирроло[2,1-a]изоиндола обнаруживается в многочисленных тетрациклических соединениях.
Общие способы синтеза
Первый разработанный оригинальный общий способ, описываемый общей схемой 1 и инспирированный упомянутыми ранее работами, оказался особенно эффективным в рамках настоящего изобретения, в частности для синтеза производных типа 6-оксо-2,3,4,6-тетрагидропиридо[2,1-a]изоиндола:
Схема 1

Замена группы =O радикалом =R1, таким, как определено в общей формуле (I), может быть осуществлена общими способами, известными специалисту в данной области техники, в частности способами, описанными в изданиях:
- Comprehensive Organic Chemistry, составители D. Barton et al. (Pergamon Press);
- Advanced Organic Chemistry, составитель J. Marsh (Wiley Interscience).
Второй общий способ синтеза был разработан на основе использования сложного метилового эфира 6-оксо-2,3,4,6-тетрагидро-1H-пиридо[2,1-a]изоиндол-1-карбоновой кислоты или сложного метилового эфира 6-оксо-2,5-дигидро-3H-пирроло[2,1-a]изоиндол-1-карбоновой кислоты для формирования ядра типа бензимидазола. Он оказался особенно эффективным в рамках настоящего изобретения для осуществления в две последовательные стадии согласно схеме 2:
Схема 2
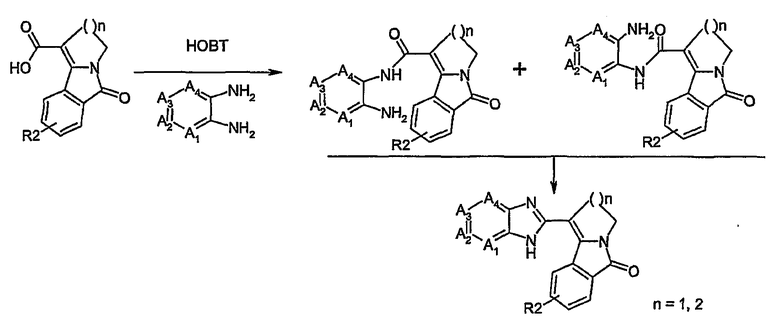
Соединения, являющиеся объектом настоящего изобретения, обладают интересными фармакологическими свойствами: было установлено, что они обладают, в частности, свойствами ингибиторов АТФ-азной активности белков-шаперонов. Среди таких белков можно упомянуть, в частности‚ Hsp90.
Таким образом, объектом настоящего изобретения в качестве лекарственных средств являются фармацевтически приемлемые соединения общей формулы (I).
Более предпочтительно объектом настоящего изобретения в качестве лекарственных средств являются следующие соединения:
- 1-{3-H-имидазо[4,5-c]пиридин-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он;
- 1-{1-H-6-гидроксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он;
а также их пролекарства, причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также фармацевтически приемлемые аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями.
Соединения могут вводиться парентерально, буккально, перлингвально, ректально или топически.
Настоящее изобретение относится также к фармацевтическим композициям, отличающимся тем, что в качестве действующего вещества они содержат по меньшей мере одно из лекарственных средств общей формулы (I).
Настоящее изобретение относится также к фармацевтическим композициям, таким, как определено ранее, отличающимся тем, что их применяют в качестве лекарственных средств, в частности для химиотерапии раковых заболеваний.
Настоящее изобретение относится также к фармацевтическим композициям, таким, как определено ранее, содержащим дополнительно действующие вещества других лекарственных средств для химиотерапии раковых заболеваний.
Упомянутые композиции могут представлять собой растворы или суспензии для инъекций, таблетки, таблетки, покрытые оболочкой, капсулы, сиропы, суппозитории, кремы, помады и лосьоны. Упомянутые лекарственные формы приготавливают общепринятыми способами. Действующее вещество может быть введено в традиционно применяемые в таких композициях эксципиенты, такие, как водные или неводные наполнители, тальк, гуммиарабик, лактоза, крахмал, стеарат магния, масло какао, твердые жиры животного или растительного происхождения, производные парафинов, гликоли, различные смачивающие агенты, диспергаторы или эмульгаторы, консерванты.
Обычная доза, варьируемая в зависимости от пациента и вида заболевания, может составлять, например, для человека при пероральном введении от 10 до 500 мг в день.
Соединения, соответствующие общей формуле (I), такие, как определено ранее, проявляют также значительную ингибирующую активность в отношении шаперона Hsp90.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), такой, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственного средства, предназначенного для профилактики или лечения заболевания, отличающегося нарушением активности белка Hsp90.
Настоящее изобретение относится также к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственных средств, предназначенных для ингибирования активности белка Hsp90.
Настоящее изобретение относится также к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I), при котором заболевание, подлежащее профилактике или лечению, представляет собой заболевание млекопитающего.
Результаты испытаний, приведенные далее в экспериментальной части, иллюстрируют ингибирующую активность соединений по настоящему изобретению в отношении таких белков.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственного средства, предназначенного для лечения раковых заболеваний.
Настоящее изобретение относится также к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I), при котором заболевание, подлежащее лечению, представляет собой рак в виде солидных или неоформленных опухолей.
Таким образом, свойства соединений общей формулы (I) по настоящему изобретению позволяют использовать их в качестве лекарственных средств, в частности для лечения злокачественных опухолей.
Среди раковых заболеваний настоящее изобретение особо предпочтительно относится к лечению солидных опухолей и лечению раковых заболеваний, резистентных к действию цитотоксических агентов.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I), при котором заболевание, подлежащее лечению, представляет собой рак, резистентный к действию цитотоксических агентов.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственного средства, предназначенного для лечения раковых заболеваний, среди которых рак легкого, молочной железы и яичника, глиобластомы, хронические миелоидные лейкозы, острые лимфобластические лейкозы, рак простаты, поджелудочной железы и толстой кишки, метастатические меланомы, опухоли щитовидной железы и почечные карциномы.
Также среди главных потенциальных показаний в отношении ингибиторов Hsp90 могут быть упомянуты не ограничительным образом:
"немелкоклеточный" рак легкого, рак молочной железы, рак яичника и глиобластомы, при которых происходит сверхэкспрессия EGF-R или HER2;
хронические миелоидные лейкозы, при которых происходит сверхэкспрессия Bcr-Abl;
острые лимфобластические лейкозы, при которых происходит сверхэкспрессия Flt-3;
рак молочной железы, простаты, легкого, поджелудочной железы, толстой кишки или яичника, при которых происходит сверхэкспрессия Akt;
метастатические меланомы и опухоли щитовидной железы, при которых происходит сверхэкспрессия мутантной формы белка B-Raf;
андрогензависимый и андрогеннезависимый рак простаты;
эстрогензависимый и эстрогеннезависимый рак молочной железы;
почечные карциномы, при которых происходит сверхэкспрессия HIF-1a или мутантного белка c-met и т.д.
Настоящее изобретение относится также к применению продуктов формулы (I), такой, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственного средства, предназначенного для химиотерапии раковых заболеваний.
В качестве лекарственных средств по настоящему изобретению, предназначенных для химиотерапии раковых заболеваний, продукты формулы (I) по настоящему изобретению могут быть использованы индивидуально или в сочетании с химиотерапией или радиотерапией или попеременно в сочетании с другими терапевтическими средствами.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственных средств, предназначенных для химиотерапии раковых заболеваний и применяемых индивидуально или в сочетании.
Настоящее изобретение относится также, в частности, к фармацевтическим композициям, таким, как определено ранее, содержащим дополнительно действующие вещества других лекарственных средств для химиотерапии раковых заболеваний.
Такими терапевтическими средствами могут быть противоопухолевые средства, применяемые в общем порядке.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I) для получения лекарственных средств, предназначенных для применения индивидуально или в сочетании с химиотерапией или радиотерапией или попеременно в сочетании с другими терапевтическими средствами.
Настоящее изобретение относится также в равной мере к применению продуктов формулы (I), таких, как определено ранее, или фармацевтически приемлемых солей упомянутых продуктов формулы (I), при котором терапевтическими средствами могут быть противоопухолевые средства, применяемые в общем порядке.
В качестве примеров известных ингибиторов протеинкиназы можно упомянуть, в частности, бутиролактон, флавопиридол, 2-(2-гидроксиэтиламино)-6-бензиламино-9-метилпурин, оломуцин, гливек, а также ирессу.
Соединения общей формулы (I) по настоящему изобретению также могут быть в равной мере эффективно использованы в комбинации с антипролиферативными средствами: в качестве примеров таких антипролиферативных средств, которые однако не ограничиваются данным перечнем, можно упомянуть ингибиторы ароматазы, антиэстрогены, ингибиторы топоизомеразы I, ингибиторы топоизомеразы II, средства, действующие на микроканалы, алкилирующие средства, ингибиторы гистондезацетилазы, ингибиторы фарнезилтрансферазы, ингибиторы COX-2, ингибиторы MMP, ингибиторы mTOR, антинеопластические антиметаболиты, соединения платины, соединения, уменьшающие активность протеинкиназ, и также антиангиогенные соединения, агонисты гонадорелина, антиандрогены, бенгамиды, бифофонаты и трастузумаб.
В качестве примеров можно упомянуть также антимикротубулярные средства, такие, как таксоиды, винкаалкалоиды, алкилирующие средства, такие, как циклофосфамид, ДНК-интеркаланты, такие, как цис-платинум, средства, интерактивные в отношении топоизомеразы, такие, как камптотецин и его производные, антрациклины, такие, как адриамицин, антиметаболиты, такие, как 5-фторурацил и его производные, и аналогичные средства.
Таким образом, настоящее изобретение относится к соединениям формулы (I) в качестве ингибиторов киназ, причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также фармацевтически приемлемые аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями, а также их пролекарства.
Настоящее изобретение относится предпочтительно к соединениям формулы (I), таким, как определено ранее, в качестве ингибиторов Hsp90, причем упомянутые продукты формулы (I) представляют собой все возможные изомерные формы рацематов, энантиомеров и диастереоизомеров, а также фармацевтически приемлемые аддитивные соли упомянутых продуктов формулы (I) с минеральными и органическими кислотами или с минеральными и органическими основаниями, а также их пролекарства.
Продукты формулы (I) по настоящему изобретению могут быть получены с применением или адаптацией известных способов и, в частности, способов, описанных в литературных источниках, например, способов, описанных R.C. Larock в издании Comprehensive Organic Transformations, VCH publishers, 1989.
Для проведения реакций, описанных далее, может оказаться необходимой защита активных функциональных групп, таких, как, например, гидрокси, амино, имино, тио или карбокси, в тех случаях, когда их наличие требуется в конечных соединениях, но их участие в реакциях синтеза продуктов формулы (I) является нежелательным. Можно использовать традиционные защитные группы в соответствии с принятыми стандартными методиками, как, например, описанные T.W. Greene и P.G.M. Wuts в издании "Protective Groups in Organic Chemistry", John Wiley and Sons, 1991.
Приведенные далее примеры синтезов иллюстрируют настоящее изобретение, не ограничивая его.
Примеры, иллюстрирующие изобретение
Пример 1: 1-{3-H-имидазо[4,5-c]пиридин-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он
В колбу вместимостью 250 мл вносят 4 г пиридин-3,4-диамина и 9,5 г 5-(1,3-диоксо-1,3-дигидроизоиндол-2-ил)пентановой кислоты, затем 45 г полифосфорной кислоты (PPA). Твердую смесь нагревают до 210°C на масляной бане. В ходе реакции отмечается переходное образование 2-{4-(3H-имидазо[4,5-c]пиридин-2-ил)бутил}изоиндол-1,3-диона. Через 16 часов нагревания реакция завершается. После охлаждения реакционную смесь растворяют в воде. Примеси удаляют экстракцией этилацетатом. Водный слой нейтрализуют (pH 7) 2н. раствором гидроксида натрия. Продукт извлекают 6 последовательными экстракциями смесью этилацетата и метанола (9/1 по объему). После очистки флеш-хроматографией на диоксиде кремния элюированием смесью дихлорметана и метанола (95/5 по объему) получают 1,46 г 1-{3-H-имидазо[4,5-c]пиридин-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-она в виде твердого вещества белого цвета со следующими характеристиками:
- спектр ЯМР 1H (400 МГц, ДМСО-d6): 2,08 (м, 2H); 2,88 (т, J=6,0 Гц, 2H); 3,81 (т, J=6,0 Гц, 2H), 7,54 (м, 2H); 7,60 (д, J=5,5 Гц, 1H); 7,78 (м, 1H); 7,95 (м уширенный, 1H); 8,34 (д, J=5,5 Гц, 1H); 8,97 (с, 1H); 12,95 (м очень растянутый, 1H);
- масс-спектр (E/I): m/z=302 (M+).
Пример 2: 1-{1-H-6-гидроксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он
Стадия 1. В трехгорлой колбе вместимостью 25 мл растворяют 942 мг сложного метилового эфира 3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он-1-карбоновой кислоты, который может быть получен согласно Eur. J. Org. Chem. 1999, 3489, в 10 мл диоксана и прибавляют 168 мг моногидрата гидроксида лития. После 6 часов перемешивания при комнатной температуре выпаривают диоксан и растворяют в 20 мл воды, затем доводят до pH 2 добавлением водного 1 M раствора соляной кислоты. Образовавшийся осадок отделяют, промывают водой, затем сушат в сушильном шкафу в вакууме при 50°C. Таким образом, получают 820 мг 3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он-1-карбоновой кислоты в виде белого порошка, используемого в таком виде на следующей стадии.
Стадия 2. В трехгорлой колбе вместимостью 25 мл растворяют 442,5 мг 3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-он-1-карбоновой кислоты в 20 мл дихлорметана, затем прибавляют 400 мг гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDCI) и 270 мг 1-гидроксибензотриазола и перемешивают при комнатной температуре в течение 1 часа. После концентрирования раствора при пониженном давлении прибавляют последовательно 10 мл тетрагидрофурана и 276 мг 4-метоксибензол-1,2-диамина и выдерживают при 70°C в течение 5 часов. Реакционную смесь упаривают и, таким образом, получают 680 мг смеси двух региоизомерных амидов, используемой в таком виде на следующей стадии.
Стадия 3. В трехгорлой колбе вместимостью 100 мл растворяют 118 мг смеси региоизомеров, полученной ранее, в 5 мл трифторуксусной кислоты и 0,5 мл трифторуксусного ангидрида и нагревают при 85°C в течение 2,5 часов. После концентрирования при пониженном давлении остаток очищают флеш-хроматографией на силикагеле, элюируя смесью диизопропилового эфира и метанола (95/5 по объему). Таким образом, получают 97 мг 1-{1-H-6-метоксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-она в виде порошка бежевого цвета со следующими характеристиками:
- масс-спектр (E/I): m/z=331 (M+).
Стадия 4. В трехгорлой колбе вместимостью 25 мл перемешивают в течение 20 часов при комнатной температуре раствор 61 мг 1-{1-H-6-метоксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-она в 2 мл уксусной кислоты и 3 мл 48%-ного водного раствора бромоводородной кислоты. Реакционную смесь выливают в 100 мл воды и нейтрализуют насыщенным раствором гидрокарбоната натрия в присутствии 25 мл дихлорметана. Водный слой экстрагируют 2 раза по 20 мл дихлорметана. Объединенные органические слои сушат над сульфатом магния и концентрируют при пониженном давлении. Загрязненный продукт очищают хроматографированием на силикагеле, элюируя смесями дихлорметана и метанола (сначала 95/5, затем 90/10 по объему), и получают, таким образом, 49 мг 1-{1-H-6-гидроксибензимидазол-2-ил}-3,4-дигидро-2H-пиридо[2,1-a]изоиндол-6-она в виде взбитой массы белого цвета со следующими характеристиками:
- масс-спектр (E/I): m/z=317 (M+);
- спектр ЯМР 1H (400 МГц, ДМСО-d6): 2,04 (м, 2H); 2,83 (т, J=6,0 Гц, 2H); 3,80 (т, J=6,0 Гц, 2H), 6,74 (д уширенный, J=8,5 Гц, 1H); 6,90 (м уширенный, 1H); 7,42 (м уширенный, 1H); 7,53 (м, 2H); 7,75 (м, 1H); 8,02 (м уширенный, 1H); 9,22 (м растянутый, 1H); 12,4 (м очень растянутый, 1H).
Пример 3: Фармацевтическая композиция
Изготавливают таблетки, соответствующие следующему составу:
соединение примера 1 0,2 г
эксципиент, дополняющий массу таблетки до 1 г
(ингредиенты эксципиента: лактоза, тальк, крахмал, стеарат магния)
Биологические испытания по определению биологических характеристик соединений по настоящему изобретению
Неорганический фосфат, высвобождающийся в ходе гидролиза АТФ вследствие АТФ-азной активности Hsp82, определяют количественно с малахитовым зеленым. В присутствии этого реактива образуется комплекс "неорганический фосфат-молибдат-малахитовый зеленый", который поглощает при длине волны 620 нм. Испытуемые соединения инкубируют в реакционном объеме 30 мкл в присутствии 1 мкM Hsp82 и 250 мкM субстрата (АТФ) в буфере, состоящем из 50 мM Hepes-NaOH (pH 7,5), 1 мM DTT, 5 мM MgCl2 и 50 мM KCl при 37°C в течение 60 минут. Параллельно готовят серию растворов неорганического фосфата в интервале от 1 до 40 мкM в таком же буфере. Затем определяют АТФ-азную активность прибавлением 60 мкл реактива biomol green (Tebu). Через 20 минут инкубирования при комнатной температуре измеряют абсорбцию в различных лунках посредством микропланшетного фотометра при длине волны 620 нм. После чего по эталонной кривой рассчитывают концентрацию неорганического фосфата в каждой пробе. АТФ-азную активность Hsp82 выражают через концентрацию неорганического фосфата, продуцируемого за 60 минут. Действие различных испытуемых соединений выражают в процентном отношении ингибирования АТФ-азной активности.
Образование АДФ, обусловленное АТФ-азной активностью Hsp82, было использовано для разработки другого способа оценки ферментативной активности данного фермента посредством применения системы ферментативного связывания, вводящей в действие пируваткиназу (PK) и лактатдегидрогеназу (LDH). В данном спектрофотометрическом способе кинетического типа PK катализирует образование АТФ и пирувата, исходя из фосфоэнолпирувата (PEP) и АДФ, продуцируемого HSP82. Образовавшийся пируват, субстрат для LDH, затем превращают в лактат в присутствии NADH. В данном случае уменьшение концентрации NADH, измеренное по уменьшению абсорбции при длине волны 340 нм, пропорционально концентрации АДФ, продуцируемого HSP82.
Испытуемые соединения инкубируют в реакционном объеме 100 мкл буфера, состоящего из 100 мM Hepes-NaOH (pH 7,5), 5 мM MgCl2, 1 мM DTT, 150 мM KCl, 0,3 мM NADH, 2,5 мM PEP и 250 мкM АТФ. Данную смесь предварительно инкубируют при 37°C в течение 30 минут перед прибавлением 3,77 единицы LDH и 3,77 единицы PK. Реакцию инициируют прибавлением испытуемого соединения в разных концентрациях и Hsp82 с концентрацией 1 мкM. После чего в непрерывном режиме осуществляют измерение ферментативной активности Hsp82 с помощью микропланшетного фотометра при 37°C и длине волны 340 нм. Начальную скорость реакции определяют измерением угла наклона касательной к записанной кривой в начале координат. Ферментативную активность выражают в мкM АДФ, образующегося в минуту. Действие различных испытуемых соединений выражают в процентном отношении ингибирования АТФ-азной активности согласно приведенной далее градации.
- A: IC50<1 мкM;
- B: 1 мкM<IC50<10 мкM;
- C: 10 мкM<IC50<100 мкM.
Таблица результатов
A000187458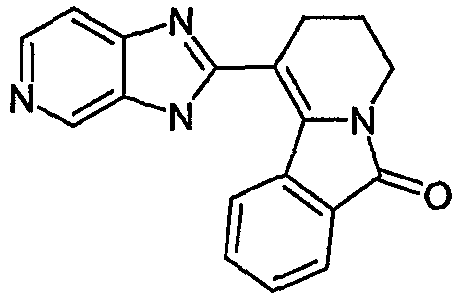
A003338065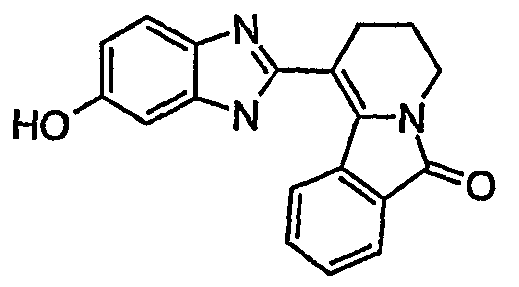
| название | год | авторы | номер документа |
|---|---|---|---|
| ТИЕНОПИРИДИНЫ | 2006 |
|
RU2415859C2 |
| ПРОИЗВОДНЫЕ ГИДРОКСИБЕНЗАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ Hsp90 | 2006 |
|
RU2458919C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ ПРОИЗВОДНЫЕ ПИРИДО [4,3-d]ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРА HSP90 И ИНГИБИТОРА HER2 | 2009 |
|
RU2532375C2 |
| МОДУЛЯТОРЫ ПРОТЕОЛИЗА НА ОСНОВЕ ИМИДОВ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2704807C2 |
| 2-КАРБОКСАМИД ЦИКЛОАМИНО ПРОИЗВОДНЫЕ МОЧЕВИНЫ В КОМБИНАЦИИ С ИНГИБИТОРАМИ Hsp90 ДЛЯ ЛЕЧЕНИЯ ПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2624493C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА | 2006 |
|
RU2416605C2 |
| ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833354C1 |
| [9,10-ДИМЕТОКСИ-3-(2-МЕТИЛПРОПИЛ)-1H,2H,3H,4H,6H,7H,11BH- ПИРИДО-[2,1-A]ИЗОХИНОЛИН-2-ИЛ]МЕТАНОЛ И СВЯЗАННЫЕ С НИМ СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ | 2016 |
|
RU2736509C2 |
| ИМИДНЫЕ МОДУЛЯТОРЫ ПРОТЕОЛИЗА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2738833C2 |
| КОМБИНАЦИИ ИНГИБИТОРА HSP90 | 2009 |
|
RU2519673C2 |
Описываются новые производные изоиндола общей формулы (I),
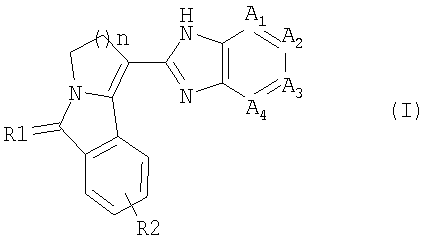
в которой А1, А2 и А4 обозначает СН, а A3 обозначает N или С-ОН; n равно 2; R1 представляет собой О; R2 обозначает Н; и фармацевтическая композиция, их содержащая. Новые соединения являются ингибиторами активности белка-шаперона Hsp90 и могут быть использованы при химиотерапии раковых заболеваний. 2 н. и 4 з.п. ф-лы.
1. Производные изоиндола общей формулы (I)
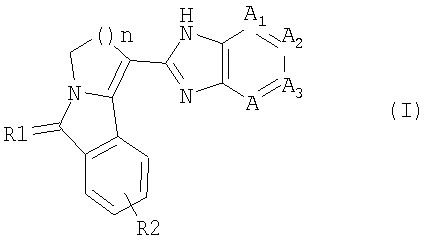
где А1, А2, и А4 обозначают СН, а A3 обозначает N или С-ОН;
n равно 2;
R1 обозначает атом кислорода;
R2 обозначает Н.
2. Соединения по п.1, а именно следующие:
1-{3-Н-имидазо[4,5-с]пиридин-2-ил}-3,4-дигидро-2Н-пиридо[2,1-а]изоиндол-6-он;
1-{1-Н-6-гидроксибензимидазол-2-ил}-3,4-дигидро-2Н-пиридо[2,1-а]изоиндол-6-он.
3. Соединения по п.1 в качестве лекарственных средств для химиотерапии раковых заболеваний, а также их пролекарства.
4. Соединения по п.2 в качестве лекарственных средств для химиотерапии раковых заболеваний, а также их пролекарства.
5. Фармацевтические композиции в качестве лекарственных средств для химиотерапии раковых заболеваний, содержащие в качестве активного ингредиента по меньшей мере одно из лекарственных средств по пп.3 и 4.
6. Производные изоиндола общей формулы (1) по п.1 или 2 в качестве ингибиторов Hsp90.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| RU 2003116061/04 A, 10.12.2004 | |||
| RU 2003116648/04 A, 10.02.2005 | |||
| ИМИДАЗОПИРИМИДИНЫ И ИМИДАЗОПИРИДИНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ НАРУШЕНИЙ | 1998 |
|
RU2201929C2 |
| ПИРРОЛОИНДОЛЫ, ПИРИДИНОИНДОЛЫ И АЗЕПИНОИНДОЛЫ В КАЧЕСТВЕ АГОНИСТОВ 5-НТ2С | 1999 |
|
RU2232162C2 |
Авторы
Даты
2009-12-10—Публикация
2006-04-05—Подача