Изобретение относится к органической химии, в частности к самоорганизующимся надмолекулярным ионным ассоциатам (ассоциаты) разноименно заряженных фталоцианинов и их использованию для окисления сульфида натрия. Изобретение может быть использовано в газо- и нефтеперерабатывающей, нефтяной, химической, кожевенной и других отраслях промышленности при обезвреживании сточных вод, содержащих сероводородные соединения.
Прототипом служит катализатор N-(4'-гидроксифенил)-N-(карбоксиметил)сульфамоил фталоцианин кобальта, обладающий активностью в гомогенном окислении сульфида натрия 50 моль (Na2S)/моль(катализатора)мин при комнатной температуре, на воздухе, концентрация Na2S равна 0,0234 М, время реакции 15 мин [S.A.Borisenkova, E.G.Girenko, B.G.Gherassimov at al. / J.Porphyrins Phthalocyanines, 1999, N3, p.210-215] [I].
Недостатком этого катализатора является низкая активность.
Задача настоящего изобретения состоит в изыскании более активных катализаторов гомогенного окисления сульфида натрия, работающих в тех же условиях: комнатная температура и в присутствии кислорода воздуха.
Задача решается тем, что разработан катализатор, являющийся производным фталоцианина, который представляет собой надмолекулярный ионный ассоциат разноименно заряженных фталоцианинов структурной формулы I и II
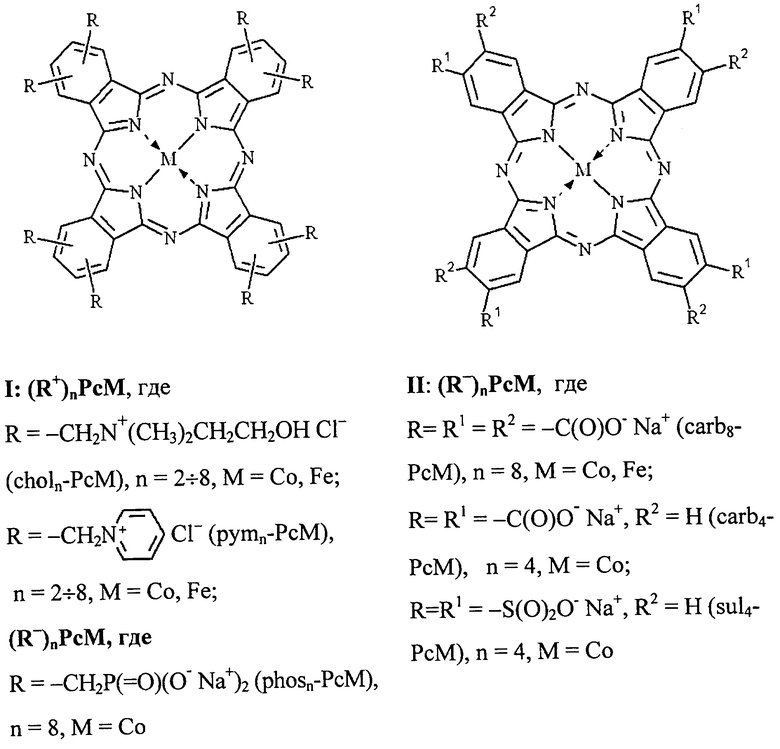
Поставленная задача также решается тем, что мольное соотношение компонентов в ассоциате 1:1÷2.
Известен способ окисления сульфида натрия [I] с использованием катализатора, представляющего собой N-(4'-гидроксифенил)-N-(карбоксиметил)сульфамоил фталоцианин кобальта, как описано выше. Он отличается невысокой активностью.
Задача настоящего изобретения состоит в разработке способа каталитического окисления сульфида натрия, который бы обеспечивал высокую конверсию.
Поставленная задача решается тем, что процесс окисления сульфида натрия проводят в водном растворе с использованием кислорода воздуха с указанным выше катализатором при комнатной температуре.
Около 20 лет назад на примере порфиринов, а затем смесей порфиринов и фталоцианинов было установлено, что при смешивании растворов комплексов с четырьмя противоположными по знаку заряда заместителями (R+ или R-) образуются прочные ассоциаты (в литературе используется и другие названия - супрамолекулярные агрегаты, комплексы, ионные пары с переносом заряда и проч.) строго определенного состава - димеры и триммеры [Т.Shimidzu and Т.Iyoda, Chem. Phys. Lett. 1981, p.853; H.Segawa, H.Nishino, Т.Kamikawa, К.Honda and Т.Shimidzu, Chem. Lett. 1989, p.1917; S.Gaspard, C.R., Acad. Sci. Paris. 1984, 298, p.379]. Использование нами термина «ассоциаты» обусловлено следующими причинами. Тетрапиррольные макроциклы в растворах склонны к взаимодействию друг с другом посредством нековалентного связывания. В результате образуются агрегаты, состоящие из нескольких одинаковых молекул. Для того чтобы отличать такие агрегаты от изучаемых нами, мы используем термин «ассоциаты», так как наши образования состоят из разных молекул. Использовать термин «комплексы» также неудобно, так как исходные молекулы являются фталоцианиновыми комплексами. Таким образом, выражение «надмолекулярный ионный ассоциат» обозначает систему, состоящую из нескольких молекул (надмолекулярный), различных по своим свойствам, связанных между собой преимущественно ионными связями, но не только.
Фталоцианины с катионными аммониометильными заместителями choln-PcM и pymn-PcM получали хлорметилированием фталоцианина кобальта или фталоцианина железа α,α'-дихлорметиловым эфиром и последующим взаимодействием хлорметилзамещенного производного с 2-(диметиламино)этанолом или пиридином, соответственно. Среднюю степень замещения регулировали, изменяя время реакции хлорметилирования.
Аналогично получали и анионный фосфонатометилзамещенный фталоцианин кобальта phosn-PcCo, однако при взаимодействии с хлорметилзамещенным производным использовали триметилфосфит или триэтилфосфит с последующим гидролизом диалкилфосфонатных групп.
Натриевую соль тетракарбоксифталоцианина кобальта carb4-PcCo получали нейтрализацией известного 2,9,16,23-тетракарбоксифталоцианина кобальта [С.А.Михаленко, Л.И.Соловьева, Е.А.Лукьянец // ЖОХ. 2004. Т.74. Вып.3. С.496-505].
Натриевую соль октакарбоксифталоцианина кобальта carb8-PcCo получали по способу, описанному в работе [Патент РФ 2304582, 2007, БИ №23].
Натриевую соль октакарбоксифталоцианина железа carb8-PcFe получали по методике, аналогичной carb8-PcCo.
Натриевую соль тетрасульфофталоцианина кобальта sul4-PcCo получают как в работе [Rollman L.D., Ivamoto R.T. J. Amer. Chem. Soc. 1968. V.90. №5. P.1455].
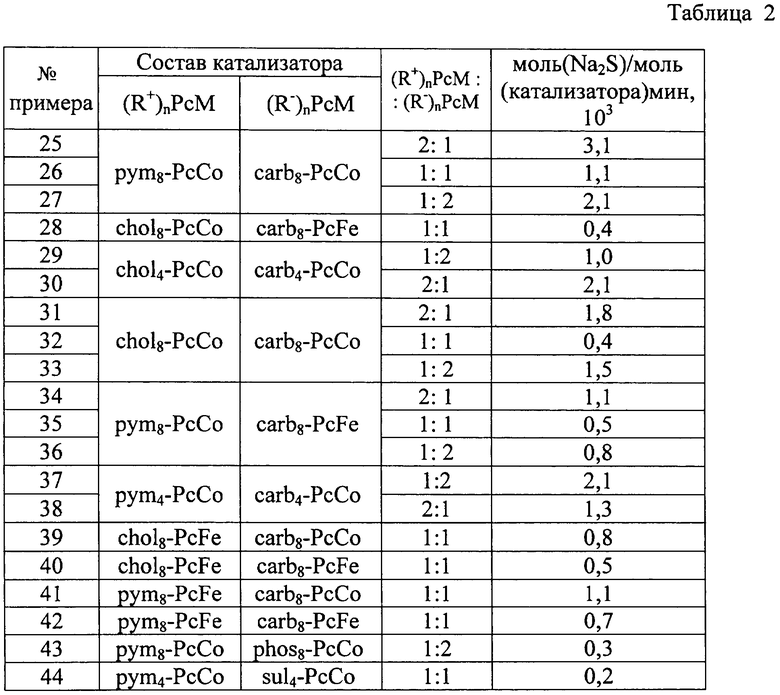
Ассоциаты получали путем смешивания водных растворов фталоцианинов с разноименно заряженными заместителями. Состав ассоциатов регулировали, изменяя стехиометрическое соотношение компонентов (R-)nPcM:(R+)nPcM. Состав катализаторов в соответствии с изобретением приведен в таблице 1.
Каталитическая активность катализаторов, выраженная в молях окисленного сульфида натрия на моль катализатора в минуту (моль(Na2S)ок/моль(катализатора)мин), приведена в таблице 2.
Как видно из таблицы 2, некоторые катализаторы показали каталитическую активность, на один - три порядка большую в сравнении с прототипом, в таких же условиях: при окислении кислородом воздуха при комнатной температуре.
Таким образом, получен активный катализатор, который позволяет эффективно проводить процесс окисления сульфида натрия при комнатной температуре в атмосфере воздуха.
Нижеприведенные примеры иллюстрируют предлагаемое изобретение.
Пример 1. Получение октакис(N-(2-гидроксиэтил)-N,N-диметиламмониометил)фталоцианина кобальта (chol8-PcCo).
К 11 г (0,082 моль) хлористого алюминия добавляют при перемешивании 3 мл триэтиламина. После охлаждения массы до температуры 70-80°С к смеси приливают 6 мл (0,0075 моль) α,α'-дихлорметилового эфира, а затем загружают 3 г (0,0052 моль) фталоцианина кобальта. Смесь нагревают в течение 3 часов при перемешивании и температуре 90-93°С, после чего выгружают на лед. Осадок отфильтровывают, промывают водой, метанолом и сушат. Выход октакис(хлорметил)фталоцианина кобальта 5,65 г (78,6%). Электронный спектр поглощения, λmax=673 нм (ДМФА). Найдено, %: Cl 29,11. Вычислено, %: Cl 29,56.
К 0,7 г (0,00073 моль) октакис(хлорметил)фталоцианина кобальта добавляют 5 мл диметилформамида и 1,5 мл 2-(диметиламино)этанола, после чего смесь нагревают при перемешивании на кипящей водяной бане в течение 2-х часов. Осадок отфильтровывают, промывают ацетоном, переосаждают из метанола с ацетоном и сушат. Выход 1,0 г (83,3%) комплекса (I). Электронный спектр поглощения, λmax=672 нм (H2O). Найдено, %: Cl 16,51; N 13,02. Вычислено для C80H134N18O10C18Co, %: Cl 16,95; N 13,4.
Пример 2. Получение октакис(пиридиниометил)фталоцианина кобальта октахлорид (pym8-PcCo).
К 0,49 г (0,00051 моль) октакис(хлорметил)фталоцианина кобальта (примеры 1-2) добавляют 5,0 мл пиридина, после чего смесь нагревают при перемешивании на кипящей водяной бане в течение 2-х часов. Осадок отфильтровывают, промывают ацетоном, переосаждают из метанола с ацетоном и сушат. Выход 0,43 г (83,3%) комплекса (II). Электронный спектр поглощения, λmax=672 нм (H2O). Найдено, %: Cl 16,51; N 13,02. Вычислено для C90H74N18C18Co, %: Cl 16,95; N 13,4.
Пример 3. Получение октакис(фосфонометил)фталоцианина кобальта (phos8-PcCo).
К 2,0 г (0,00208 моль) октакис(хлорметил)фталоцианина кобальта, полученного как в примере 1, добавляют 5 мл триэтилфосфита и смесь нагревают при 150°С в течение 2 ч. Избыток триэтилфосфита удаляют в вакууме, продукт переосаждают из бензола гексаном. Выход октакис[(диэтоксифосфонил)метил]фталоцианина кобальта 3,0 г (81,3%) комплекса (I). Электронный спектр поглощения, λmax=685 нм (H2O). Найдено, %: Р 13,31; Со 3,51. Вычислено для C72H104CoN8O24P8, %: P 13,98; Со 3,33.
Смесь 0,50 г (0,000282 моль) вышеполученного эфира и 1 мл концентрированной бромисто-водородной кислоты нагревают при 110°С в течение 2 ч. Избыток бромисто-водородной кислоты отгоняют в вакууме, остаток промывают водой, спиртом и сушат. Выход продукта 0,27 г (72,3%). Электронный спектр поглощения, λmax=684 нм (водный раствор NaOH, pH 10). Найдено, %: Р 18,1; Со 4,2. Вычислено для C40H40CoN8O24P8, %: P 18,72; Со 4,45.
Пример 4. Получение окта-4,5-карбоксифталоцианина железа (carb8-PcFe).
Данный фталоцианин железа получали взаимодействием пиромеллитового диангидрида с безводным бромидом железа (II) в присутствии мочевины, сульфата натрия и молибдата аммония (в молярном соотношении 4:1:10:10:0,1) при 205-210°С в течение трех часов с последующим омылением полученного технического тетраимида октакарбоксифталоцианина железа 25% раствором гидроокиси калия (кипячением в течение 25 часов) до калиевой соли октакарбоксифталоцианина железа. Затем подкисляли ее 10% водным раствором соляной кислоты до свободной кислоты с последующей обработкой последней водным раствором гидроокиси натрия. Выход натриевой соли технического октакарбонатного фталоцианина железа составил 35%. Полученную соль очищают от примесей, в том числе и от олигомерных продуктов, методом колоночной хроматографии на оксиде алюминия. Элюент - фосфатный буфер pH 8. Из фракции с Rf 0,9 (на пластинке silufol) выделяют с выходом 10% (в расчете на диангидрид пиромеллитовой кислоты) carb8-PcFe. Готовый продукт сушат при 105-110°С в вакууме над P2O5 до постоянной массы.
Найдено, %: С 42,98; Н 1,10; N 9,81. C40H8FeN8Na8O16. Вычислено, %: С 43,82; Н 0,74; N 10,22.
Пример 5. Получение катализатора - ассоциата pym8-PcCo: carb8-РсСо=2:1.
К 1 мл 3,30·10-5 М водного раствора carb8-PcCo прибавляют 1 мл 6,60·10-5 М водного раствора pym8-PcCo, перемешивают 15 мин. Концентрация раствора полученного ассоциата составляет 1,65·10-5 М.
Пример 6. Получение катализатора - ассоциата pym8-PcCo: carb8-РсСо=1:1.
К 1 мл 3,30·10-5 М водного раствора carb8-PcCo прибавляют 1 мл 3,30·10-5 М водного раствора pym8-PcCo и перемешивают 15 мин. Концентрация раствора полученного ассоциата составляет 1,65·10-5 М.
Пример 7. Получение катализатора, включающего ассоциат pym8-РсСо:carb8-PcCo=1:2.
К 1 мл 6,60·10-5 М водного раствора carb8-PcCo прибавляют 1 мл 3,30·10-5 М водного раствора pym8-PcCo и перемешивают 15 мин. Концентрация раствора полученного ассоциата составляет 1,65·10-5 М.
Примеры 8-24. Остальные катализаторы согласно таблице 1 получали аналогичным образом.
Пример 25. Каталитическое окисление сульфида натрия.
Смешивают в реакторе 10 мл (0,024 М) сульфида натрия и 0,37 мл водного раствора катализатора, содержащего (1,65·10-5 М) pym8PcCo:carb8PcCo=2:1 (пример 5). Конечная концентрация катализатора составила 5,0·10-7 М. Реакцию проводили при комнатной температуре в атмосфере воздуха при интенсивном перемешивании в течение 15 минут. Анализы на остаточный сульфид натрия после опыта проводили методом потенциометрического титрования на универсальном иономере И-500 по стандартной методике раствором азотнокислого аммиаката серебра. Измерительный электрод - сульфид-серебряный, электрод сравнения - хлор-серебряный.
По результатам анализа конверсия сульфида натрия составила 100% или 3,1·103 моль(Na2S)/моль(катализатора)мин.
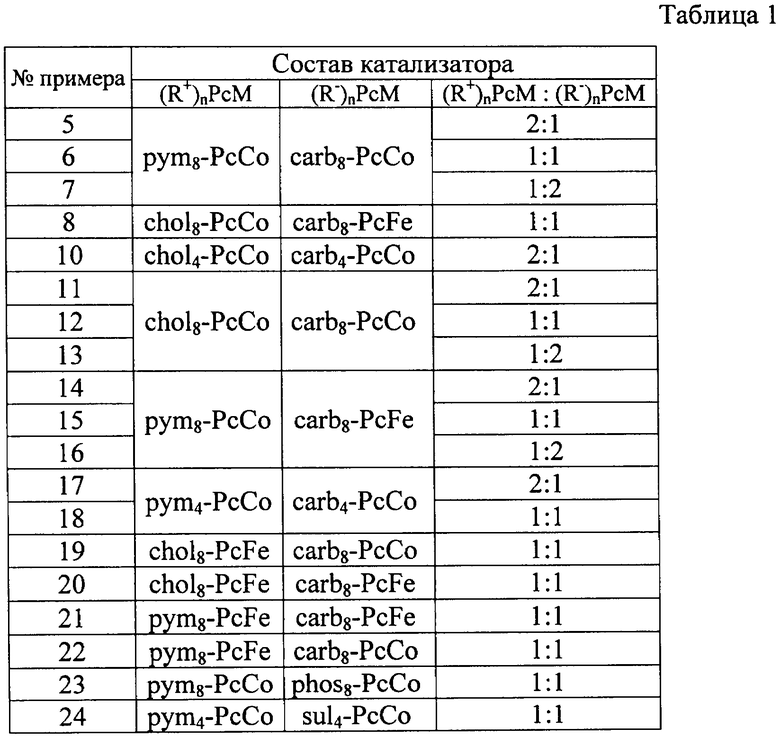
Примеры 26-44. Процесс проводили по примеру 25, но с использованием катализаторов по примерам 6-24. Результаты приведены в таблице 2.
Таким образом, как видно из таблицы 2, предложенный катализатор обладает активностью, большей, чем у прототипа, в 4 и более раз: самый активный катализатор показал активность в 62 раза выше, чем у прототипа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОМОДУЛЬНОГО ВОЛОКНА ИЗ СРЕДНЕПРОЧНЫХ УГЛЕРОДНЫХ ВОЛОКОН | 2008 |
|
RU2400577C2 |
| КАТАЛИЗАТОР И СПОСОБ ОКИСЛИТЕЛЬНОЙ ДЕМЕРКАПТАНИЗАЦИИ НЕФТИ И НЕФТЕПРОДУКТОВ | 2008 |
|
RU2381065C1 |
| КАТАЛИЗАТОР И СПОСОБ ГОМОГЕННОЙ ОКИСЛИТЕЛЬНОЙ ДЕМЕРКАПТАНИЗАЦИИ НЕФТИ И НЕФТЕПРОДУКТОВ | 2008 |
|
RU2381067C1 |
| ЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ ЖЕЛЕЗА И СПОСОБ ПОЛУЧЕНИЯ ХЛОРПРОИЗВОДНЫХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2007 |
|
RU2340589C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОНОМЕТИЛЗАМЕЩЕННЫХ ФТАЛОЦИАНИНОВ | 2011 |
|
RU2465908C1 |
| КВАТЕРНИЗОВАННЫЕ ФТАЛОЦИАНИНЫ И СПОСОБ ФОТООБЕЗЗАРАЖИВАНИЯ ВОДЫ | 2005 |
|
RU2281953C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-(ДИ-6,7-КАРБОКСИ) АНТРАХИНОНОПОРФИРАЗИНА | 2004 |
|
RU2268890C1 |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ СУЛЬФИДСОДЕРЖАЩИХ ЩЕЛОЧНЫХ РАСТВОРОВ | 2006 |
|
RU2319671C1 |
| Способ приготовления катализатора для окисления сернистых соединений | 1989 |
|
SU1685513A1 |
| ГОМОГЕННЫЕ КАТАЛИЗАТОРЫ ОКИСЛЕНИЯ ДИЭТИЛДИТИОКАРБАМАТА НАТРИЯ НА ОСНОВЕ ТЕТРА-4-(4'-КАРБОКСИФЕНИЛАМИНО)ФТАЛОЦИАНИНА КОБАЛЬТА(II), МОДИФИЦИРОВАННОГО НИТРОГРУППАМИ ИЛИ ФРАГМЕНТАМИ АМИНОБЕНЗОЙНОЙ КИСЛОТЫ | 2016 |
|
RU2623735C1 |
Изобретение относится к органической химии, в частности к самоорганизующимся надмолекулярным ионным ассоциатам разноименно заряженных фталоцианинов и их использованию для окисления сульфида натрия. Описан катализатор для окисления сульфида натрия, являющийся производным фталоцианина, отличающийся тем, что он представляет собой надмолекулярный ионный ассоциат противоположно заряженных фталоцианинов структурной формулы I и II

Описан также способ окисления сульфида натрия кислородом воздуха в присутствии вышеописанного катализатора. Технический результат - достигается конверсия субстрата до 100%, что соответствует активности 3,1·103 моль(Na2S)/моль(катализатора)мин. 2 н. и 1 з.п. ф-лы, 2 табл.
1. Катализатор для окисления сульфида натрия, являющийся производным фталоцианина, отличающийся тем, что он представляет собой надмолекулярный ионный ассоциат противоположно заряженных фталоцианинов структурной формулы I и II
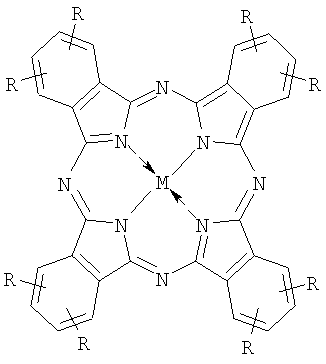
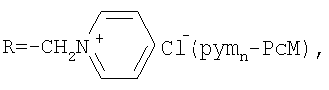

2. Катализатор по п.1, отличающийся тем, что мольное соотношение компонентов в ассоциате 1:1÷2.
3. Способ окисления сульфида натрия кислородом воздуха в присутствии катализатора, представляющего собой производное фталоцианина, отличающийся тем, что используют катализатор по п.1.
| Borisenkova S.A., Girenko E.G., Gherassimov B.G | |||
| at al | |||
| - J | |||
| Porphyrins Phthalocyanines, №3, p.210-215,1999 | |||
| Бромпроизводные, 3,6,3 ,6 ,3 ,6 ,3 ,6октаоксифталоцианина кобальта, проявляющие каталитическое свойство в реакции окисления сульфида натрия кислородом воздуха и способ их получения | 1977 |
|
SU740803A1 |
| СПОСОБ ОКИСЛЕНИЯ СЕРНИСТЫХ СОЕДИНЕНИЙ В РАСТВОРАХ | 1988 |
|
SU1623012A1 |
| CN 1200956 A, 09.12.1998 | |||
| US 4250022, 10.02.1981. | |||
Авторы
Даты
2010-02-10—Публикация
2008-10-21—Подача